| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
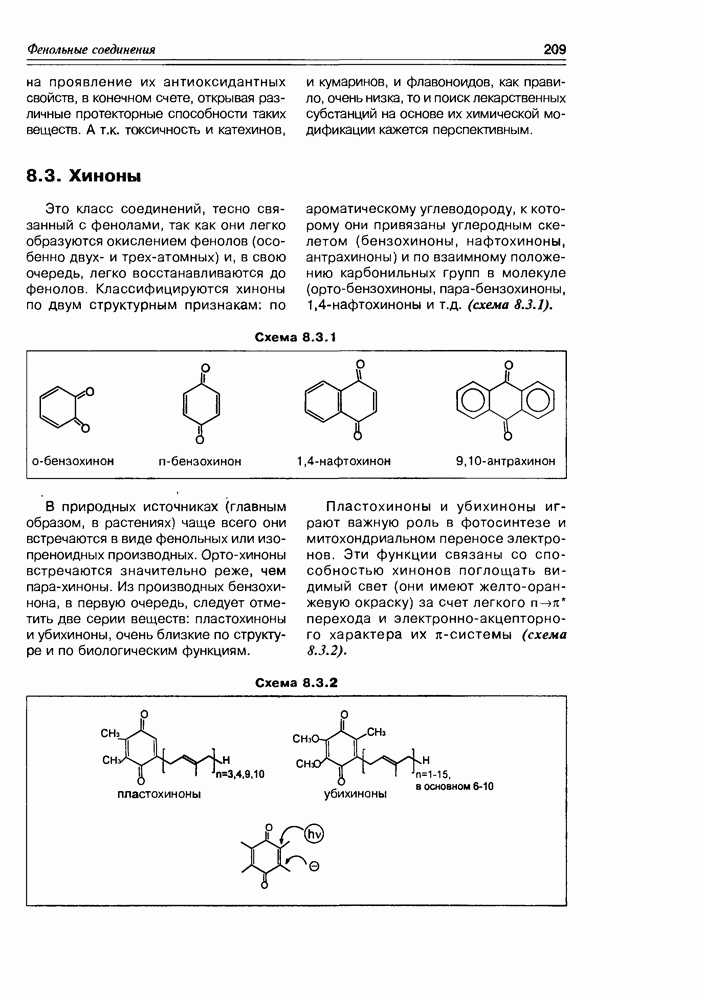
10.3. Коферменты
Здесь мы кратко отметим те низкомолекулярные соединения, которые постоянно синтезируются в организме животного и человека из достаточно широко распространенных простых соединений, таких как аминокислоты и нуклеотиды, некоторые поликетиды, изопреноиды, и участвуют в различных ферментативных реакциях.
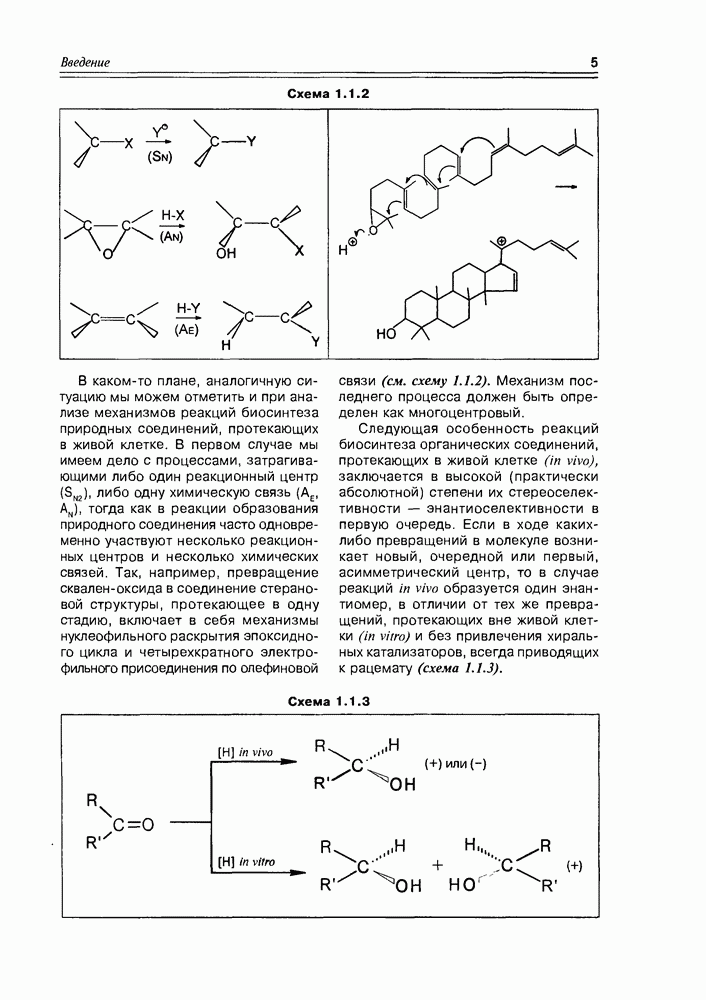
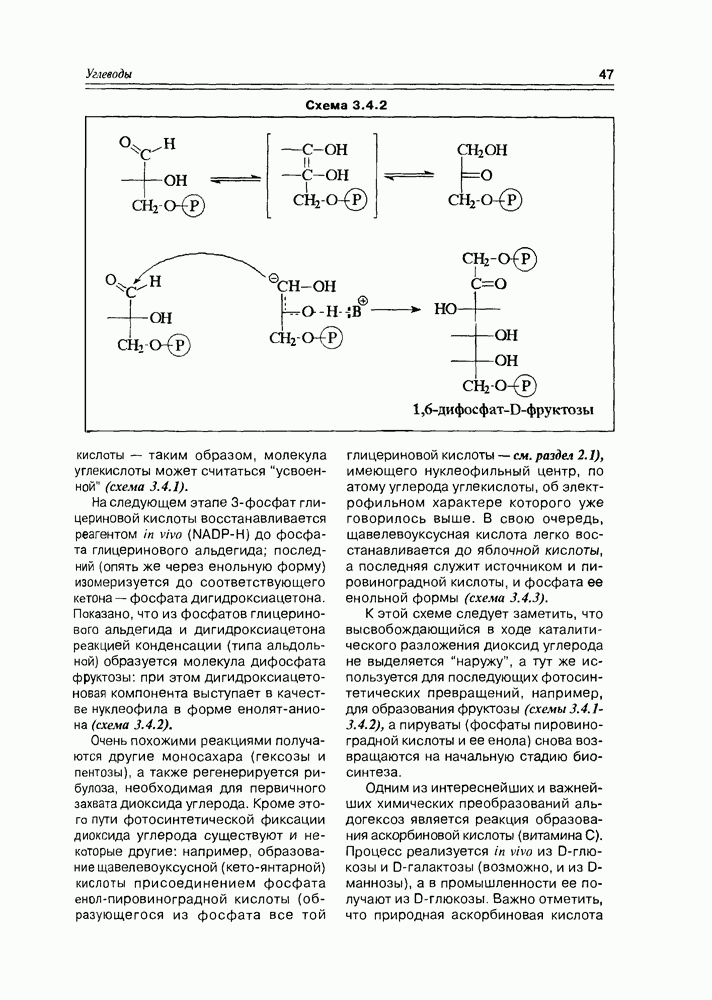
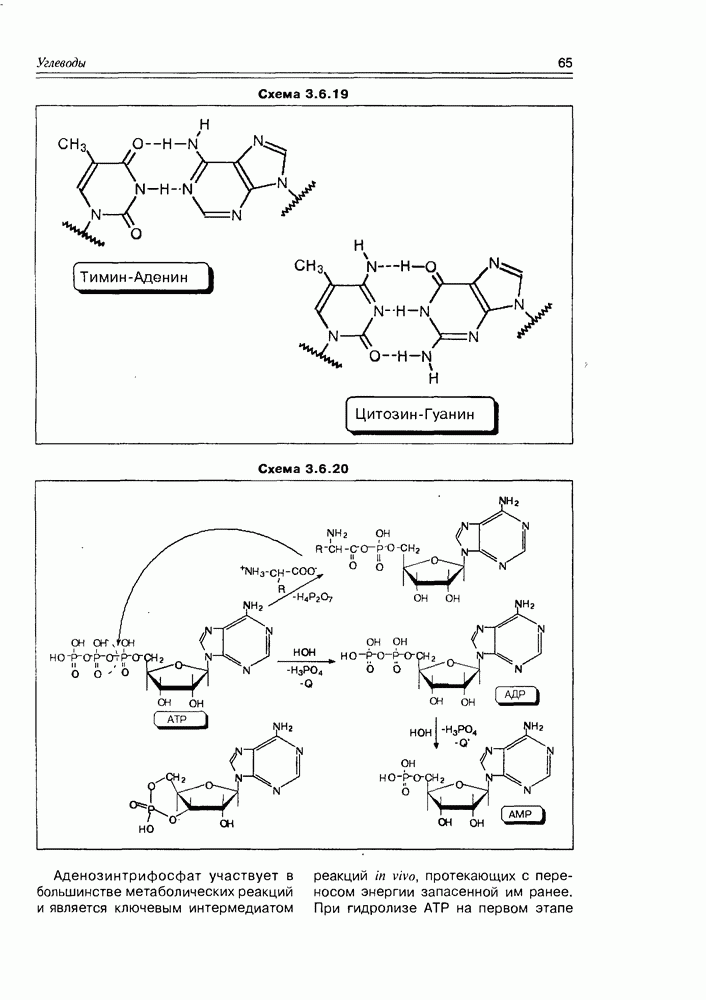
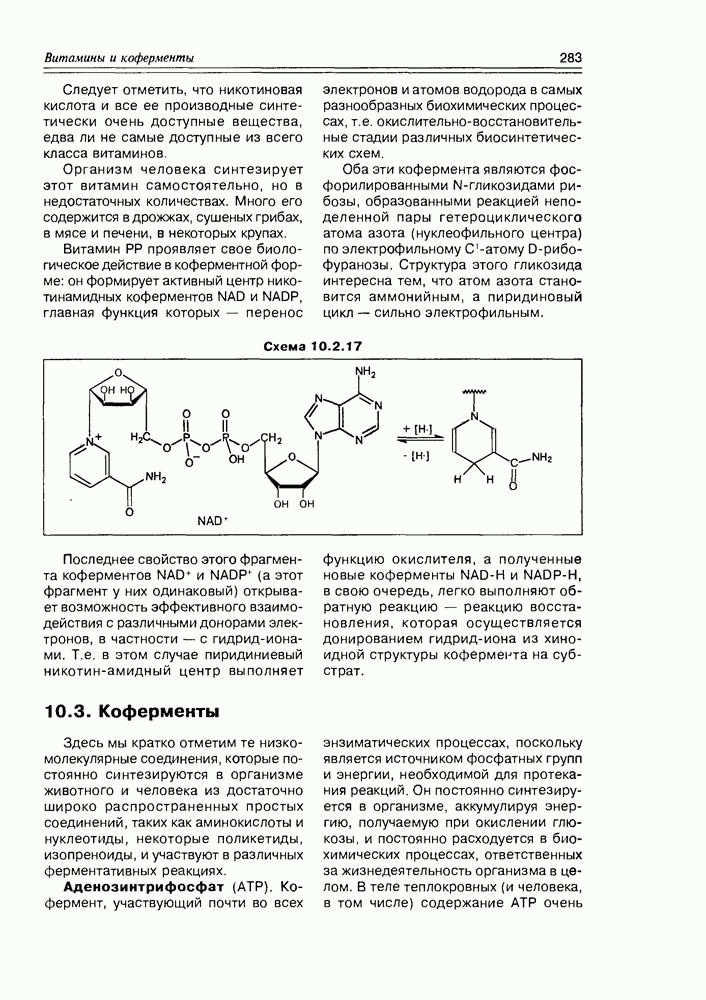
Аденозинтрифосфат (АТР). Кофермент, участвующий почти во всех функцию окислителя, а полученные новые коферменты NAD-H и NADP-H, в свою очередь, легко выполняют обратную реакцию — реакцию восстановления, которая осуществляется донированием гидрид-иона из хиноидной структуры кофермента на субстрат.
энзиматических процессах, поскольку является источником фосфатных групп и энергии, необходимой для протекания реакций. Он постоянно синтезируется в организме, аккумулируя энергию, получаемую при окислении глюкозы, и постоянно расходуется в биохимических процессах, ответственных за жизнедеятельность организма в целом. В теле теплокровных (и человека, в том числе) содержание АТР очень
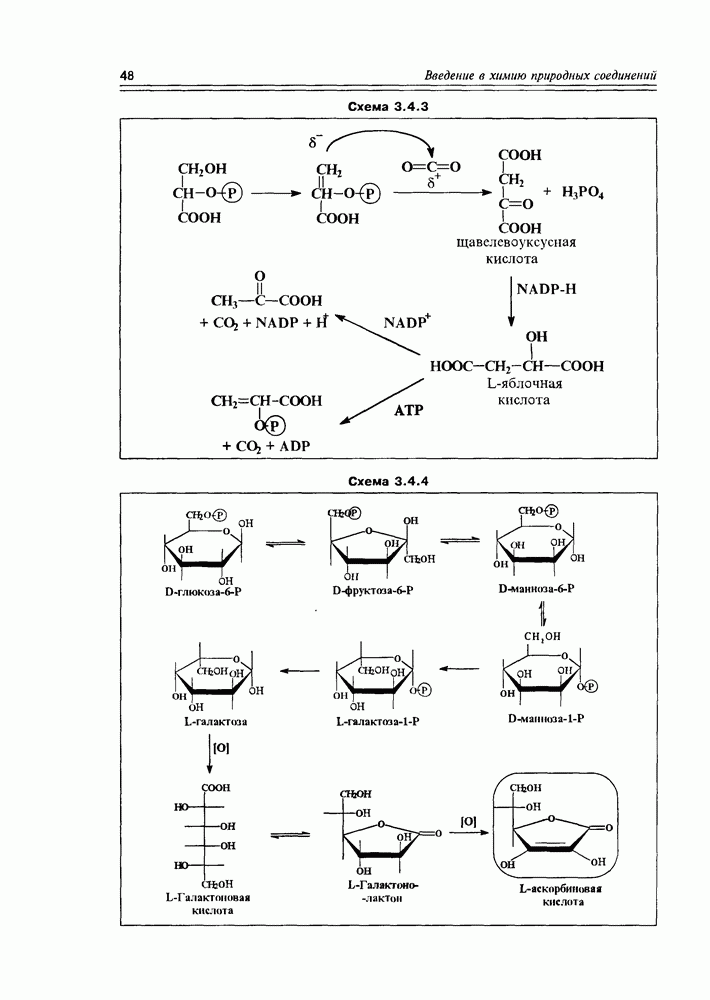
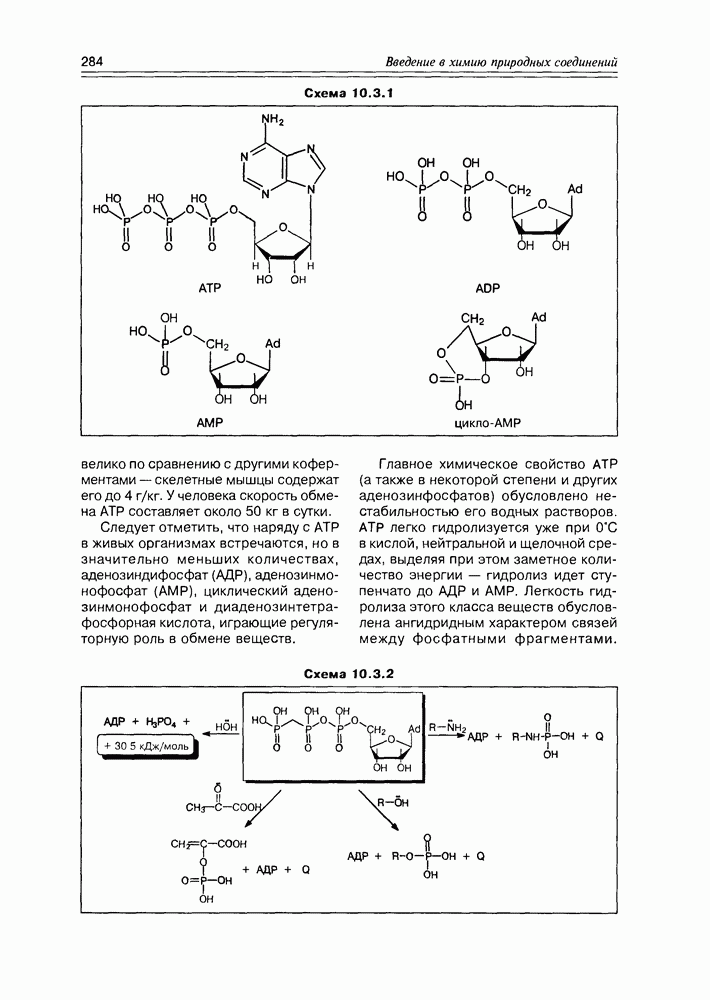
Схема 10.3.1

велико по сравнению с другими коферментами — скелетные мышцы содержат его до 4 г/кг. У человека скорость обмена АТР составляет около 50 кг в сутки.
Следует отметить, что наряду с АТР в живых организмах встречаются, но в значительно меньших количествах, аденозиндифосфат (АДР), аденозинмо-нофосфат (АМР), циклический адено-зинмонофосфат и диаденозинтетра-фосфорная кислота, играющие регуляторную роль в обмене веществ.
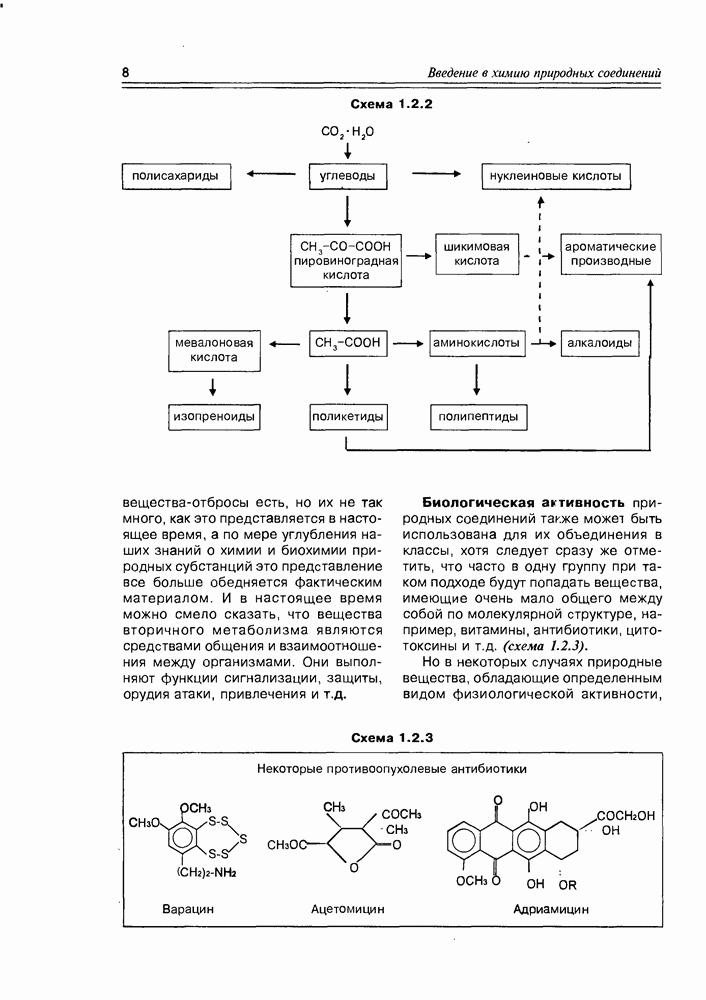
Главное химическое свойство АТР (а также в некоторой степени и других аденозинфосфатов) обусловлено нестабильностью его водных растворов. АТР легко гидролизуется уже при 0° С в кислой, нейтральной и щелочной средах, выделяя при этом заметное количество энергии — гидролиз идет ступенчато до АДР и АМР. Легкость гидролиза этого класса веществ обусловлена ангидридным характером связей между фосфатными фрагментами.
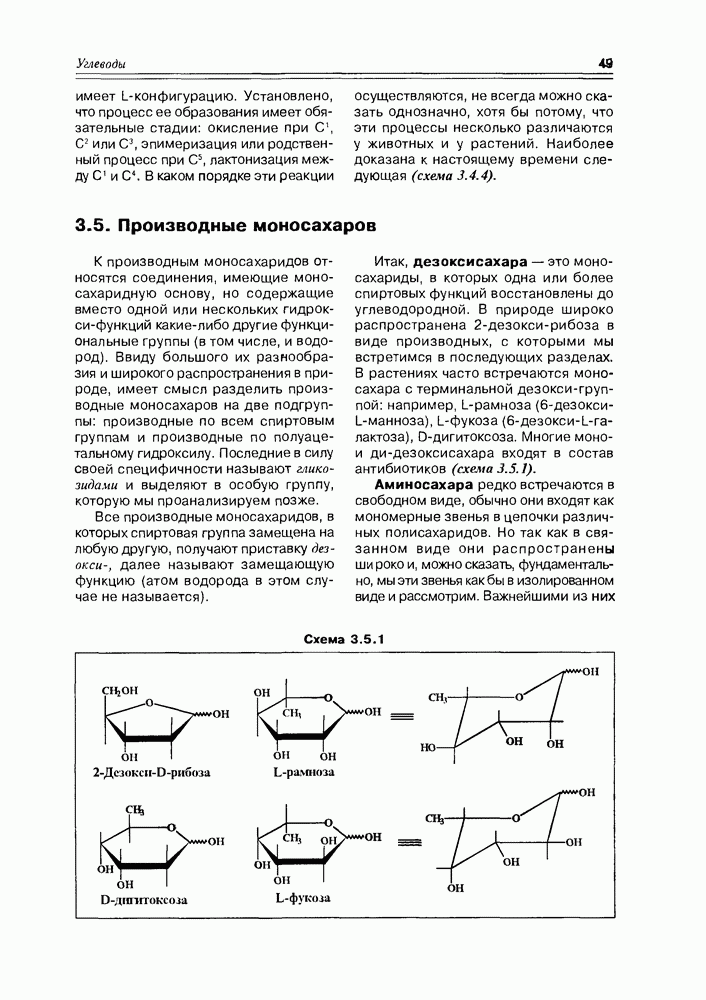
Схема 10.3.2

Ангидридные связи аденозинфосфатов также легко (с выделением энергии) разрываются при действии других типичных нуклеофилов (аминов, сульфидов, спиртов и т.д.), что используется в биосинтезе большинства природных соединений (схема 10.3.2).
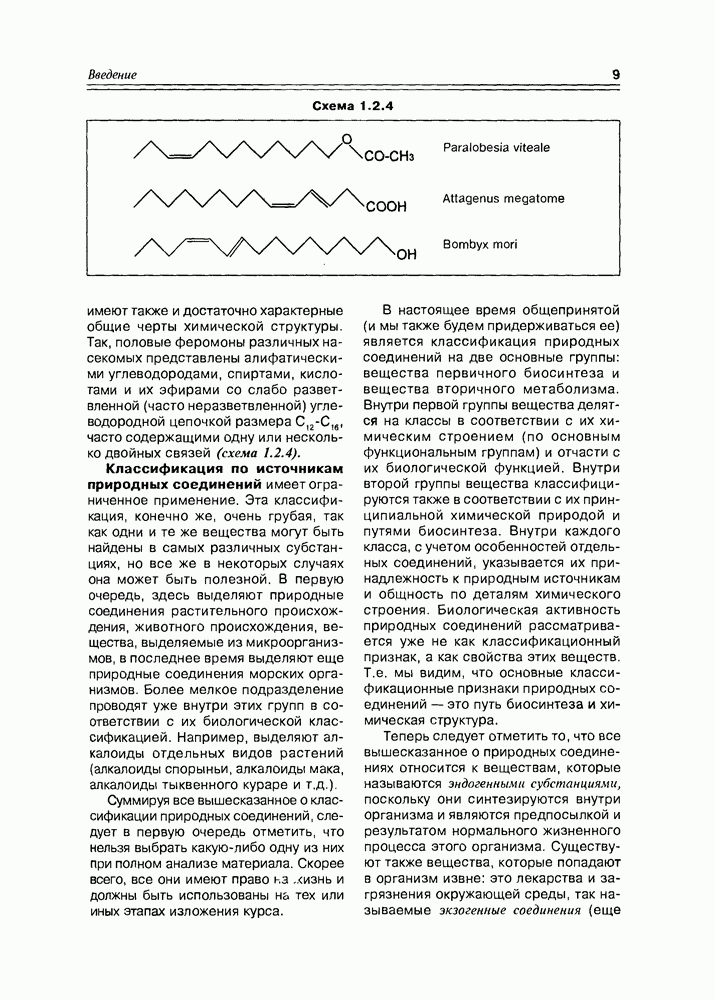
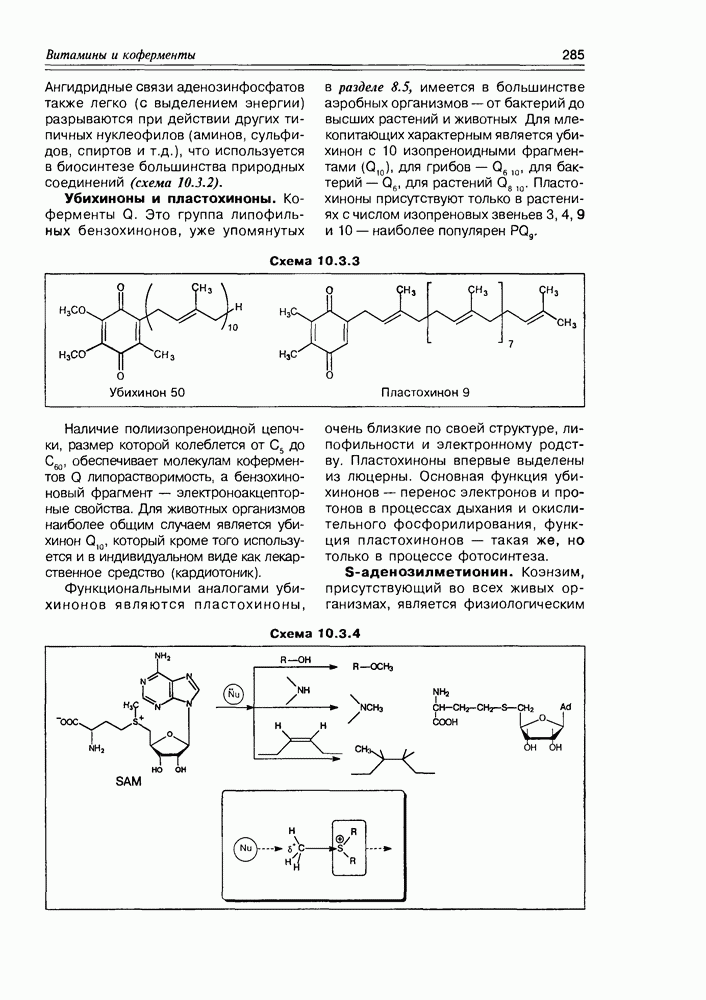
Убихиноны и пластохиноны. Коферменты Q. Это группа липофильных бензохинонов, уже упомянутых в разделе 8.5, имеется в большинстве аэробных организмов — от бактерий до высших растений и животных Для млекопитающих характерным является убихинон с 10 изопреноидными фрагментами  для грибов
для грибов  для бактерий
для бактерий  для растений
для растений  Пластохиноны присутствуют только в растениях с числом изопреновых звеньев 3, 4, 9 и 10 — наиболее популярен
Пластохиноны присутствуют только в растениях с числом изопреновых звеньев 3, 4, 9 и 10 — наиболее популярен 
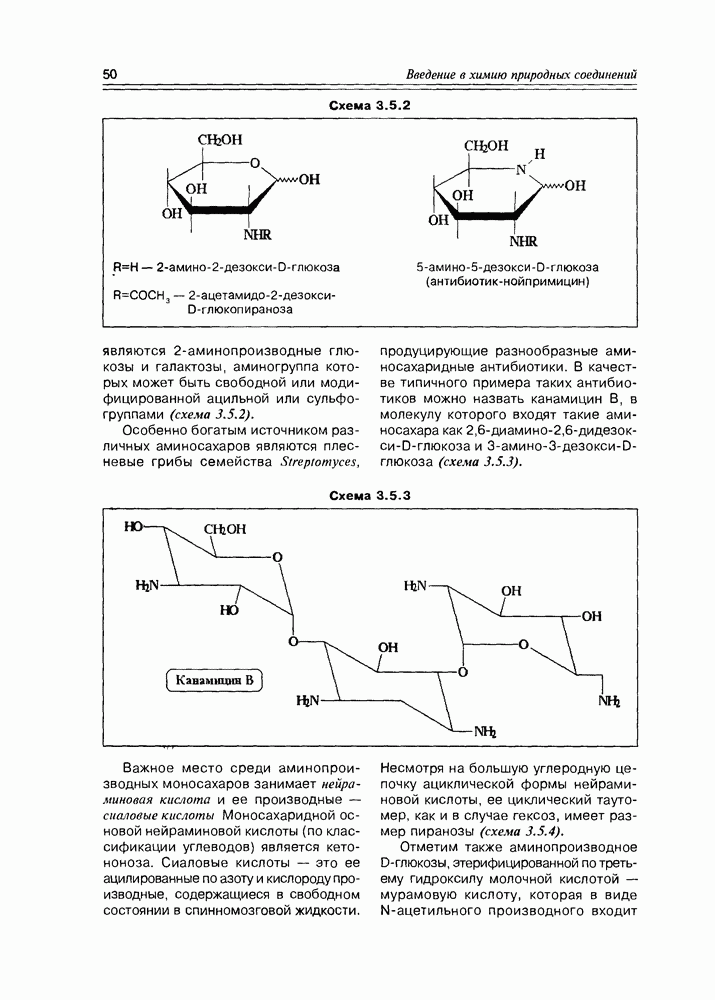
Схема 10.3.3

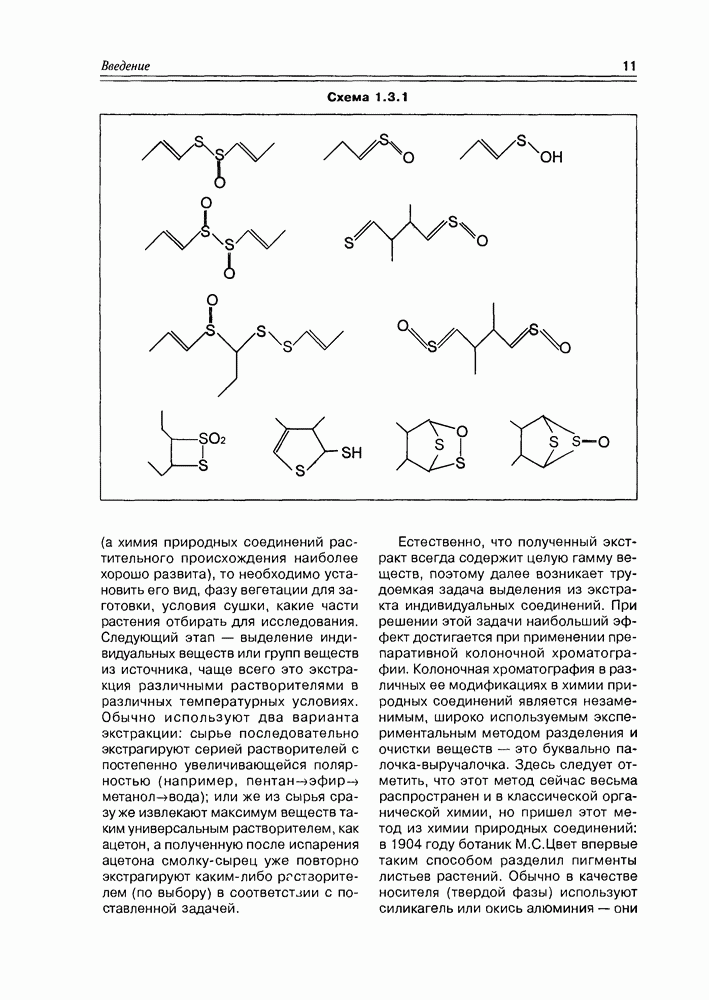
Наличие полиизопреноидной цепочки, размер которой колеблется от  до
до  обеспечивает молекулам коферментов Q липорастворимость, а бензохиноновый фрагмент — электроноакцепторные свойства. Для животных организмов наиболее общим случаем является уби-хинон
обеспечивает молекулам коферментов Q липорастворимость, а бензохиноновый фрагмент — электроноакцепторные свойства. Для животных организмов наиболее общим случаем является уби-хинон  , который кроме того используется и в индивидуальном виде как лекарственное средство (кардиотоник).
, который кроме того используется и в индивидуальном виде как лекарственное средство (кардиотоник).
Функциональными аналогами убихинонов являются пластохиноны, очень близкие по своей структуре, липофильности и электронному родству. Пластохиноны впервые выделены из люцерны. Основная функция убихинонов — перенос электронов и протонов в процессах дыхания и окислительного фосфорилирования, функция пластохинонов — такая же, но только в процессе фотосинтеза.
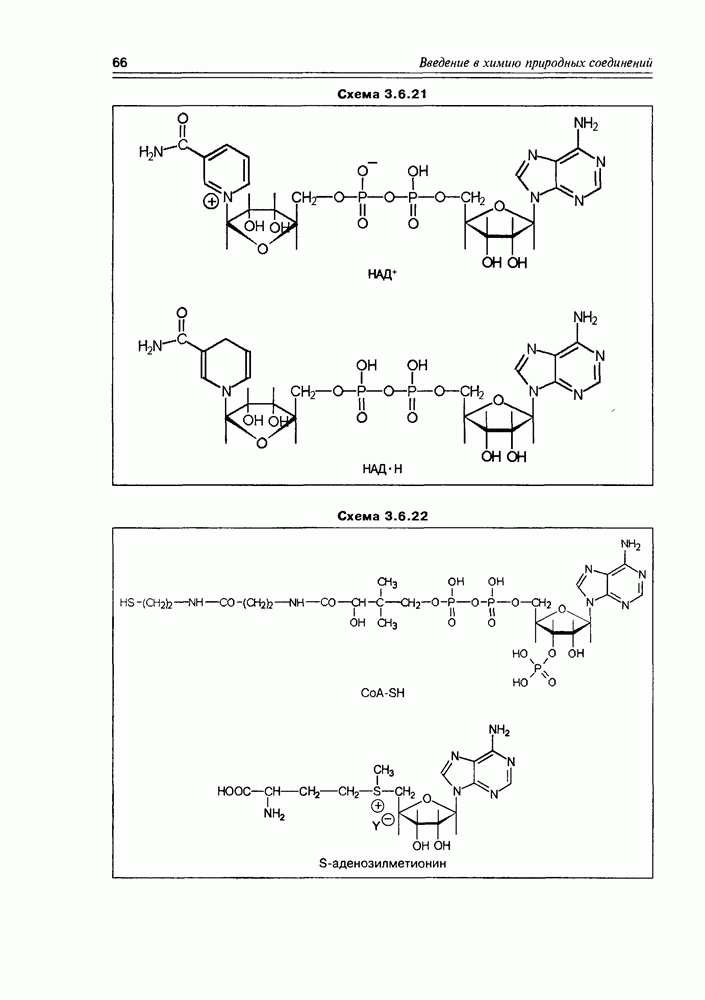
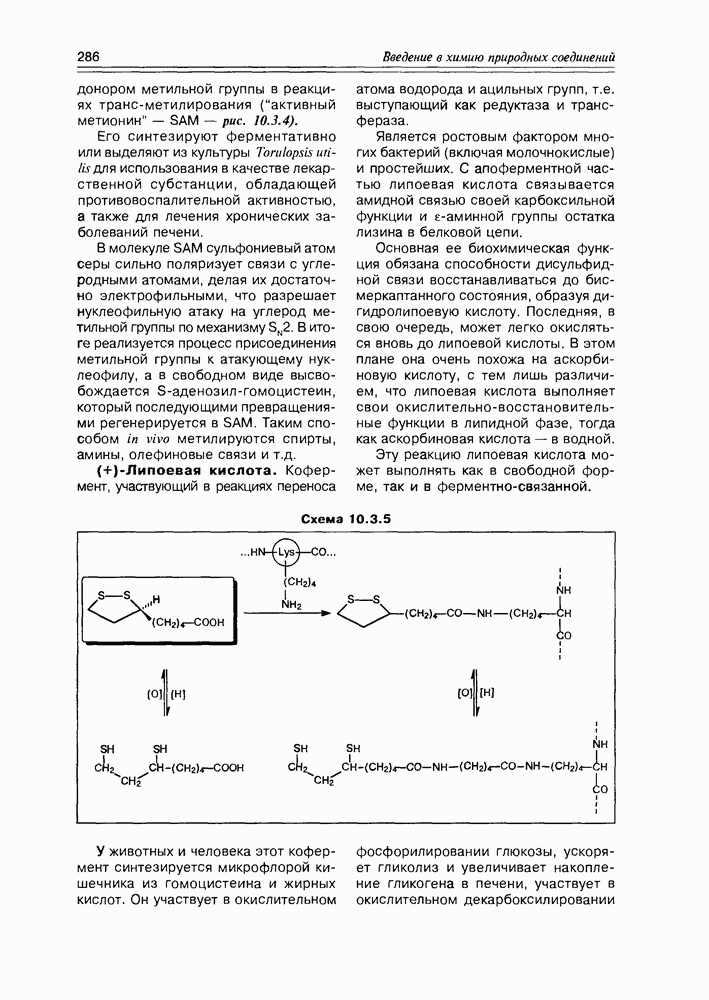
S-аденозилметионин. Коэнзим, присутствующий во всех живых организмах, является физиологическим
Схема 10.3.4

донором метильной группы в реакциях транс-метилирования (“активный метионин” — SAM — рис. 10.3.4).
Его синтезируют ферментативно или выделяют из культуры Torulopsis utilis для использования в качестве лекарственной субстанции, обладающей противовоспалительной активностью, а также для лечения хронических заболеваний печени.
В молекуле SAM сульфониевый атом серы сильно поляризует связи с углеродными атомами, делая их достаточно электрофильными, что разрешает нуклеофильную атаку на углерод метильной группы по механизму  В итоге реализуется процесс присоединения метильной группы к атакующему нуклеофилу, а в свободном виде высвобождается S-аденозил-гомоцистеин, который последующими превращениями регенерируется в SAM. Таким способом in vivo метилируются спирты, амины, олефиновые связи и т.д.
В итоге реализуется процесс присоединения метильной группы к атакующему нуклеофилу, а в свободном виде высвобождается S-аденозил-гомоцистеин, который последующими превращениями регенерируется в SAM. Таким способом in vivo метилируются спирты, амины, олефиновые связи и т.д.
(+)-Липоевая кислота. Кофермент, участвующий в реакциях переноса атома водорода и ацильных групп, т.е. выступающий как редуктаза и транс-фераза.
Является ростовым фактором многих бактерий (включая молочнокислые) и простейших. С апоферментной частью липоевая кислота связывается амидной связью своей карбоксильной функции и  -аминной группы остатка лизина в белковой цепи.
-аминной группы остатка лизина в белковой цепи.
Основная ее биохимическая функция обязана способности дисульфидной связи восстанавливаться до бисмеркаптанного состояния, образуя дигидролипоевую кислоту. Последняя, в свою очередь, может легко окисляться вновь до липоевой кислоты. В этом плане она очень похожа на аскорбиновую кислоту, с тем лишь различием, что липоевая кислота выполняет свои окислительно-восстановительные функции в липидной фазе, тогда как аскорбиновая кислота — в водной.
Эту реакцию липоевая кислота может выполнять как в свободной форме, так и в ферментно-связанной.
Схема 10.3.5

У животных и человека этот кофермент синтезируется микрофлорой кишечника из гомоцистеина и жирных кислот. Он участвует в окислительном фосфорилировании глюкозы, ускоряет гликолиз и увеличивает накопление гликогена в печени, участвует в окислительном декарбоксилировании
Схема 10.3.6

а-оксокислот совместно с тиаминдифосфатом. В медицине применяется при коронарном атеросклерозе, заболеваниях печени и диабетическом полиневрите.
Цитиколин. Коэнзим, являющийся холиновым производным нуклеотида цитидина, участвует в биосинтезе лецитина. Выделен из печени и дрожжей. Обладает церебральным сосудорасширяющим эффектом. Образует лецитин реакцией нуклеофильной спиртовой группы диацилглицерида по электроположительному атому фосфора пирофосфатного фрагмента, макроэргического по своей природе, как во всех ди- и трифосфатах (см. АТР).
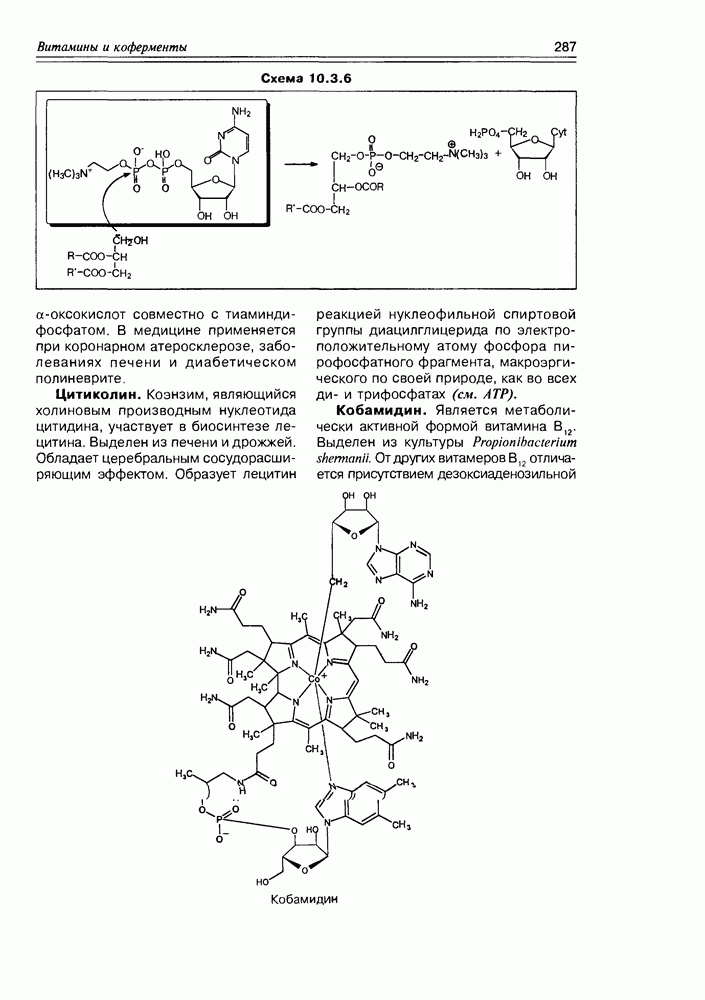
Кобамидин. Является метаболически активной формой витамина В12. Выделен из культуры Propionibcicterium shermanii. От других витамеров  отличается присутствием дезоксиаденозильной
отличается присутствием дезоксиаденозильной

группы вместо  групп, он имеет активированную связь углерод-кобальт, при диссоциации которой высвобождается карбанионный центр при
групп, он имеет активированную связь углерод-кобальт, при диссоциации которой высвобождается карбанионный центр при  рибозного фрагмента, участвует в катализе реакции изомеризации метилмалоновой кислоты в янтарную, в заключительном этапе процесса окисления некоторых липидов, боковой цепочки холестерола, алкильной группы протеиногенных кислот.
рибозного фрагмента, участвует в катализе реакции изомеризации метилмалоновой кислоты в янтарную, в заключительном этапе процесса окисления некоторых липидов, боковой цепочки холестерола, алкильной группы протеиногенных кислот.
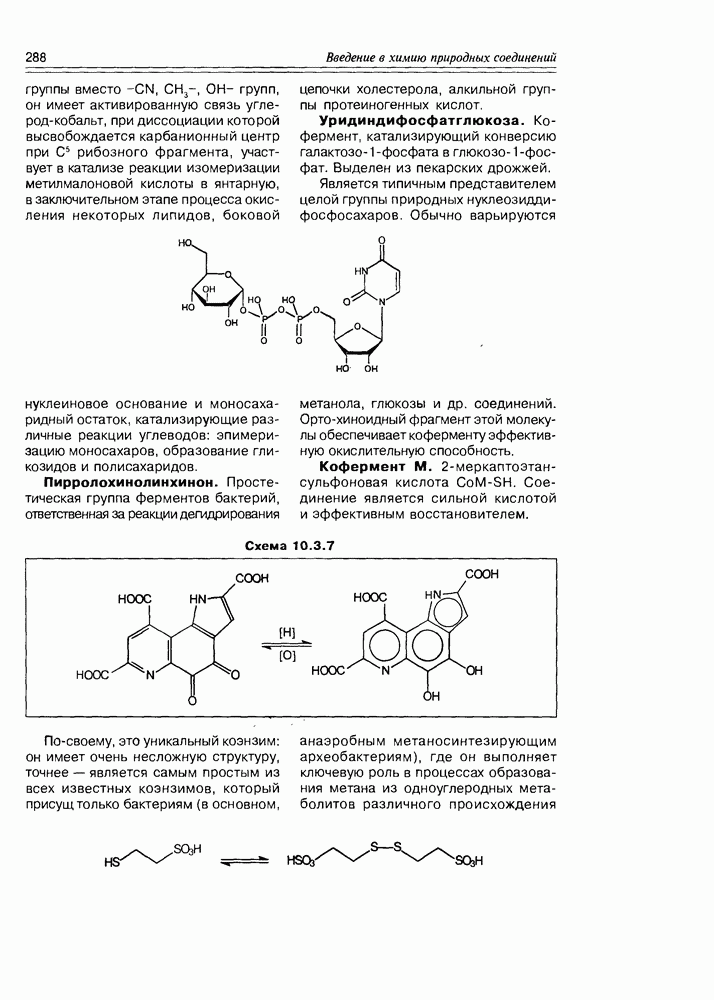
Уридиндифосфатглюкоза. Кофермент, катализирующий конверсию галактозо-1-фосфата в глюкозо-1-фосфат. Выделен из пекарских дрожжей.
Является типичным представителем целой группы природных нуклеозидди-фосфосахаров. Обычно варьируются нуклеиновое основание и моносахаридный остаток, катализирующие различные реакции углеводов: эпимеризацию моносахаров, образование гликозидов и полисахаридов.
Пирролохинолинхинон. Простетическая группа ферментов бактерий, ответственная за реакции дегидрирования метанола, глюкозы и др. соединений. Ортохиноидный фрагмент этой молекулы обеспечивает коферменту эффективную окислительную способность.
Кофермент М. 2-меркаптоэтан-сульфоновая кислота  . Соединение является сильной кислотой и эффективным восстановителем.
. Соединение является сильной кислотой и эффективным восстановителем.
Схема 10.3.7

По-своему, это уникальный коэнзим: он имеет очень несложную структуру, точнее — является самым простым из всех известных коэнзимов, который присущ только бактериям (в основном, анаэробным метаносинтезирующим археобактериям), где он выполняет ключевую роль в процессах образования метана из одноуглеродных метаболитов различного происхождения
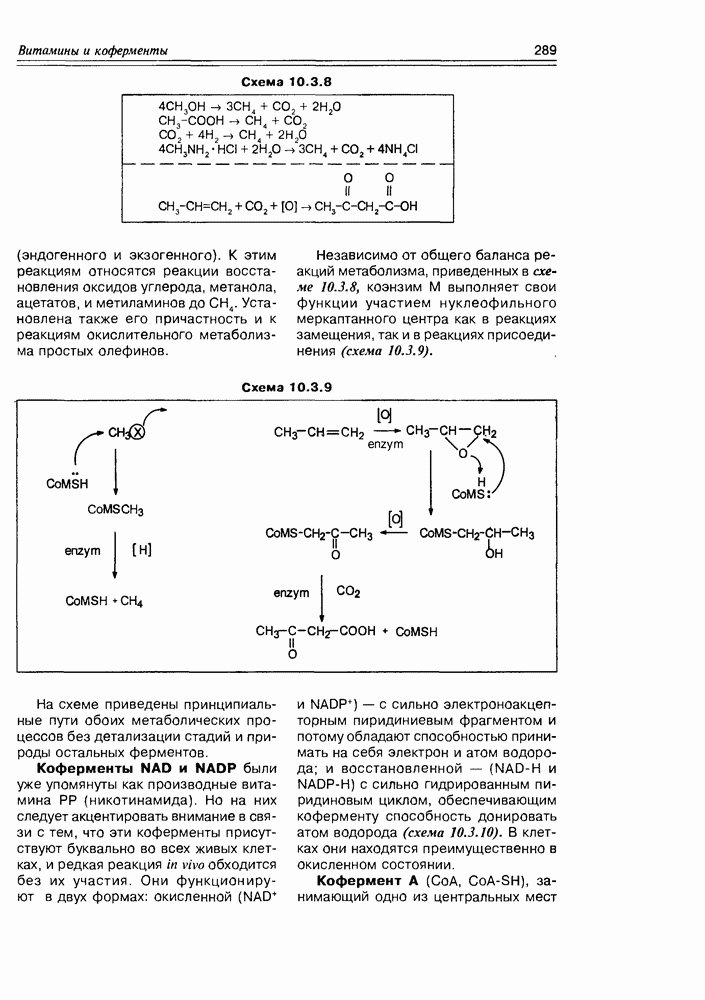
Схема 10.3.8

(эндогенного и экзогенного). К этим реакциям относятся реакции восстановления оксидов углерода, метанола, ацетатов, и метиламинов до  . Установлена также его причастность и к реакциям окислительного метаболизма простых олефинов.
. Установлена также его причастность и к реакциям окислительного метаболизма простых олефинов.
Независимо от общего баланса реакций метаболизма, приведенных в схеме 10.3.8, коэнзим М выполняет свои функции участием нуклеофильного меркаптанного центра как в реакциях замещения, так и в реакциях присоединения (схема 10.3.9).
Схема 10.3.9

На схеме приведены принципиальные пути обоих метаболических процессов без детализации стадий и природы остальных ферментов.
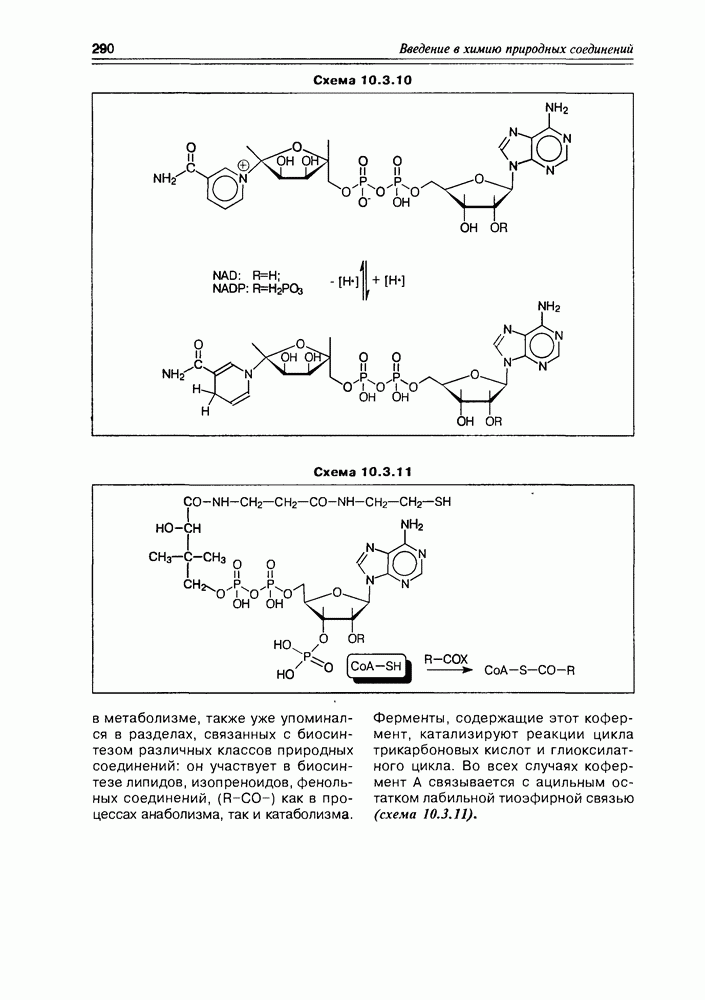
Коферменты NAD и NADP были уже упомянуты как производные витамина РР (никотинамида). Но на них следует акцентировать внимание в связи с тем, что эти коферменты присутствуют буквально во всех живых клетках, и редкая реакция in vivo обходится без их участия. Они функционируют в двух формах: окисленной (NAD+ и NADP+) - с сильно электроноакцепторным пиридиниевым фрагментом и потому обладают способностью принимать на себя электрон и атом водорода; и восстановленной — (NAD-H и NADP-H) с сильно гидрированным пиридиновым циклом, обеспечивающим коферменту способность донировать атом водорода (схема 10.3.10). В клетках они находятся преимущественно в окисленном состоянии.
Кофермент А (СоА, CoA-SH), занимающий одно из центральных мест
Схема 10.3.10

Схема 10.3.11

в метаболизме, также уже упоминался в разделах, связанных с биосинтезом различных классов природных соединений: он участвует в биосинтезе липидов, изопреноидов, фенольных соединений, (R-CO-) как в процессах анаболизма, так и катаболизма.
Ферменты, содержащие этот кофермент, катализируют реакции цикла трикарбоновых кислот и глиоксилатного цикла. Во всех случаях кофермент А связывается с ацильным остатком лабильной тиоэфирной связью (схема 10.3.11).
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ АВТОРА
- Глава 1. ВВЕДЕНИЕ
- 1.1. Предмет химии природных соединений
- 1.2. Классификация природных соединений
- 1.3. Методология химии природных соединений
- 1.4. Углерод и жизнь
- Глава 2. ПРОСТЕЙШИЕ БИФУНКЦИОНАЛЬНЫЕ ПРИРОДНЫЕ СОЕДИНЕНИЯ — МОСТИК К МАССИВУ ПРИРОДНЫХ СОЕДИНЕНИЙ
- 2.2. Оксокислоты
- 2.3. Аминоспирты
- Глава 3. УГЛЕВОДЫ
- 3.2. Свойства и структура моносахаридов
- 3.3. Химические свойства моносахаридов
- 3.4. Биосинтетические реакции углеводов
- 3.6. Гликозиды
- Глава 4. АМИНОКИСЛОТЫ, ПЕПТИДЫ, БЕЛКИ
- 4.2. Химические свойства а-аминокислот
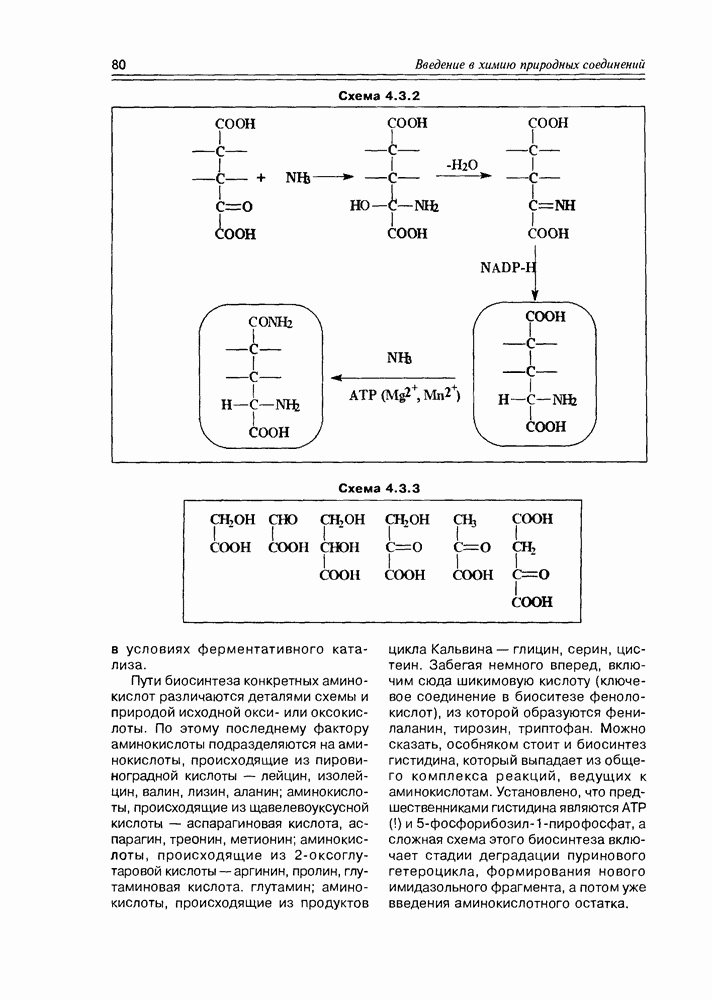
- 4.3. Биосинтез аминокислот
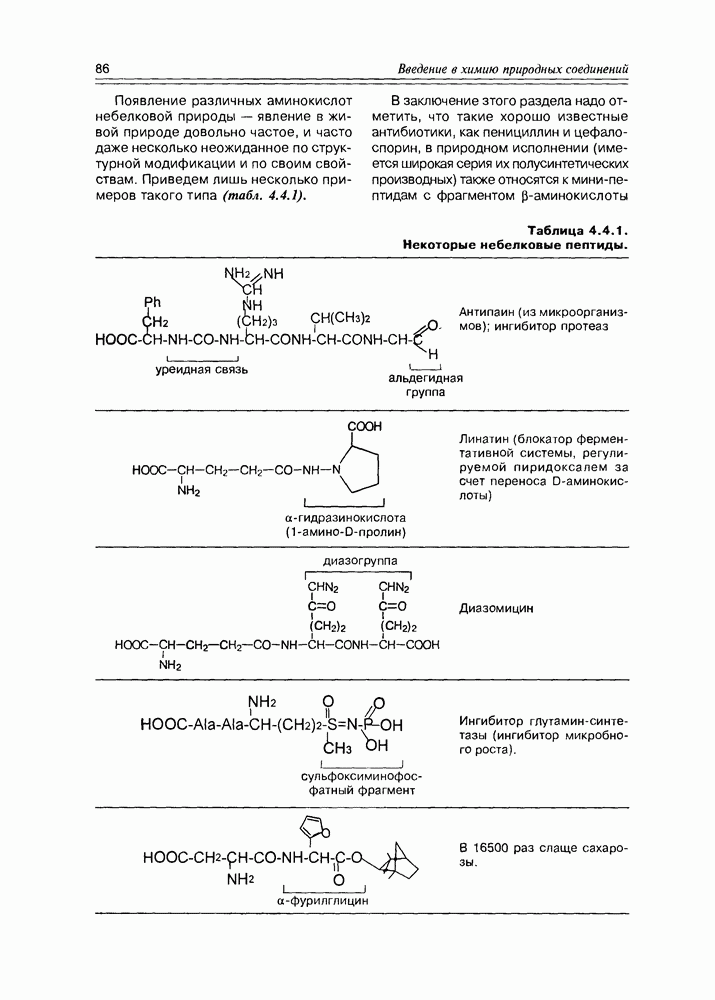
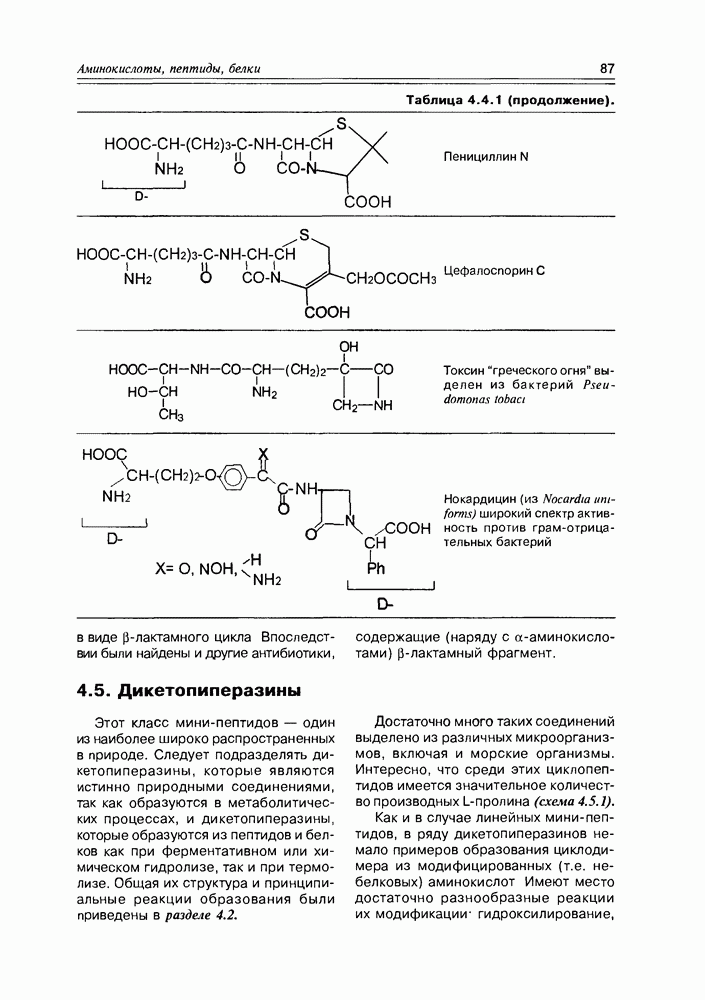
- 4.4. Полипептиды
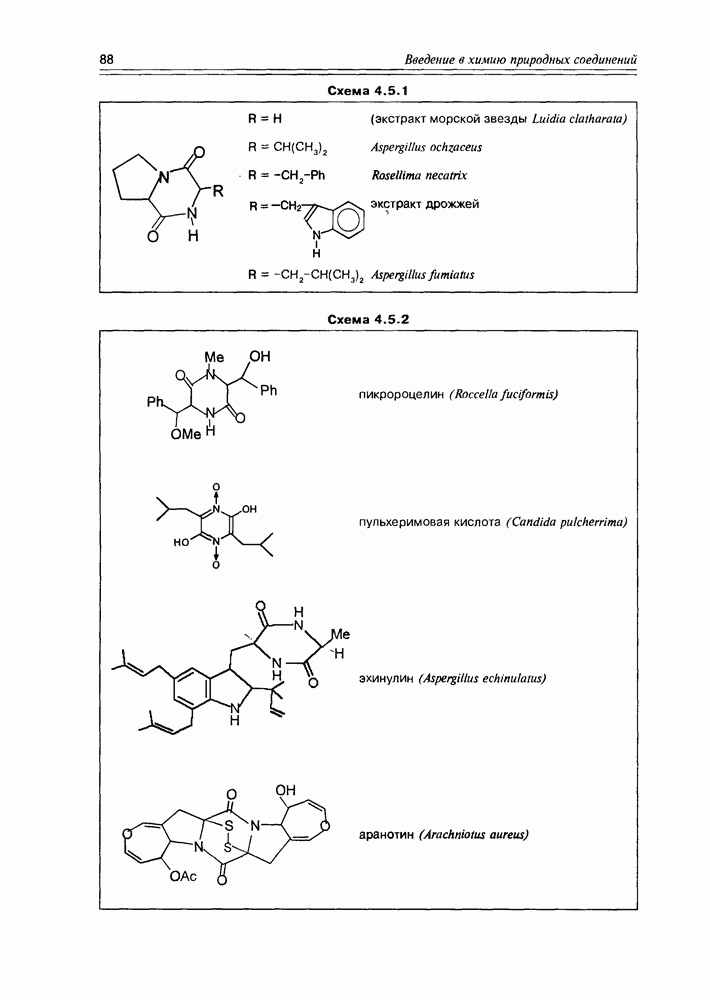
- 4.5. Дикетопиперазины
- 4.6. Циклопептиды
- 4.7. Депсипептиды
- 4.8. Белки
- Глава 5. ЛИПИДЫ: ЖИРНЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- 5.1.1. Химические свойства жирных кислот
- 5.2. Метаболиты жирных кислот
- 5.2.2. Карбоциклические оксилипины
- 5.3. Жиры и жироподобные производные жирных кислот
- 5.4. Биосинтез жирных кислот и их производных
- Глава 6. ИЗОПРЕНОИДЫ-1
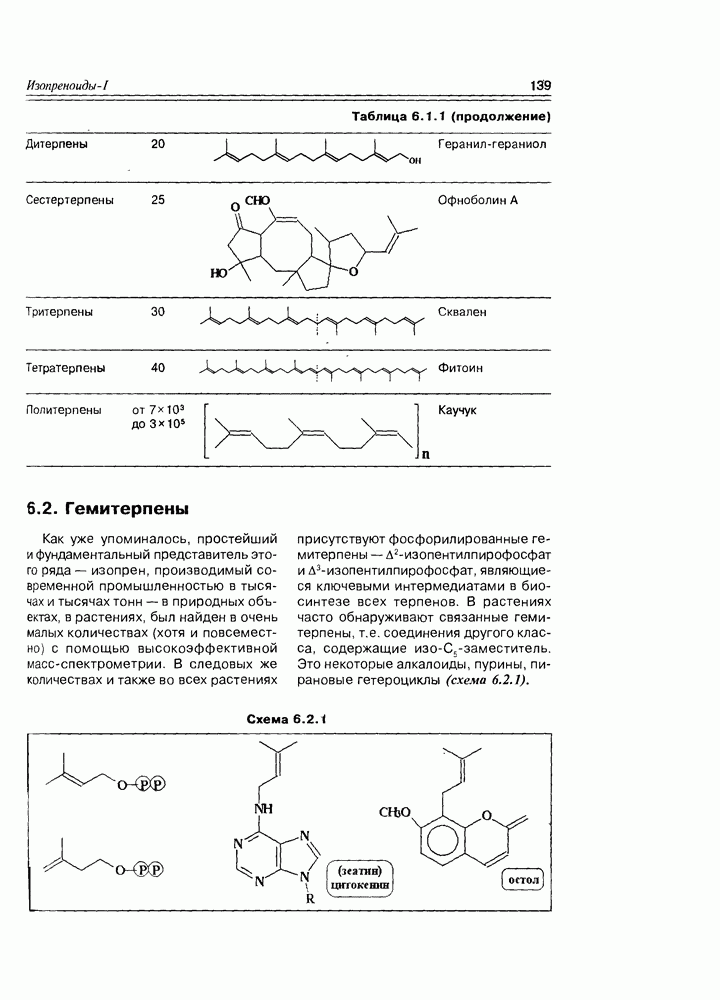
- 6.2. Гемитерпены
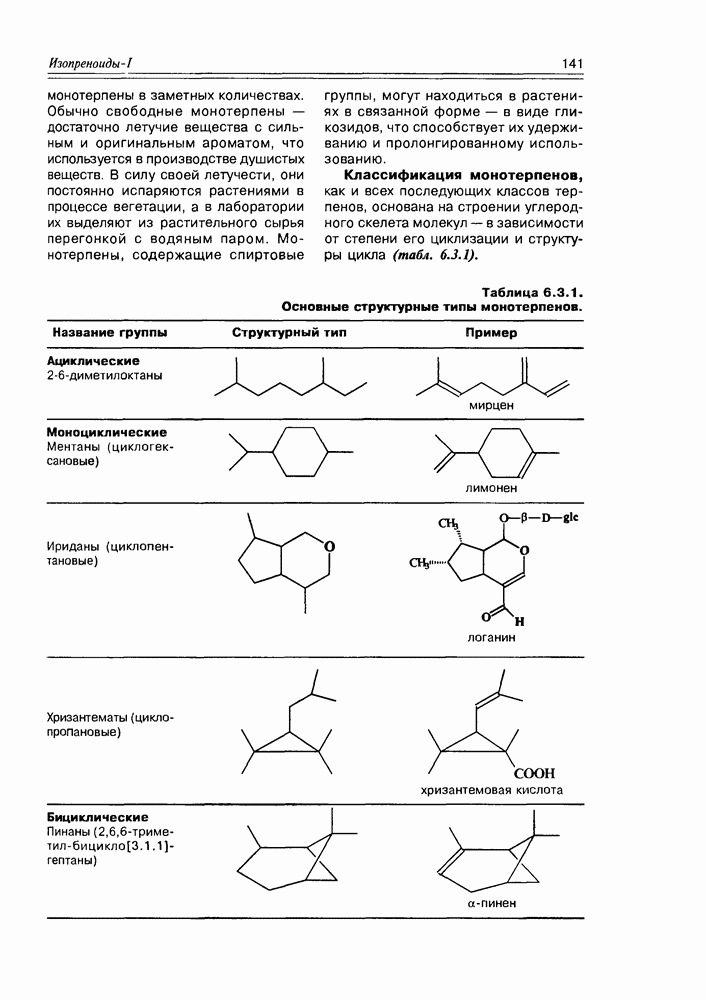
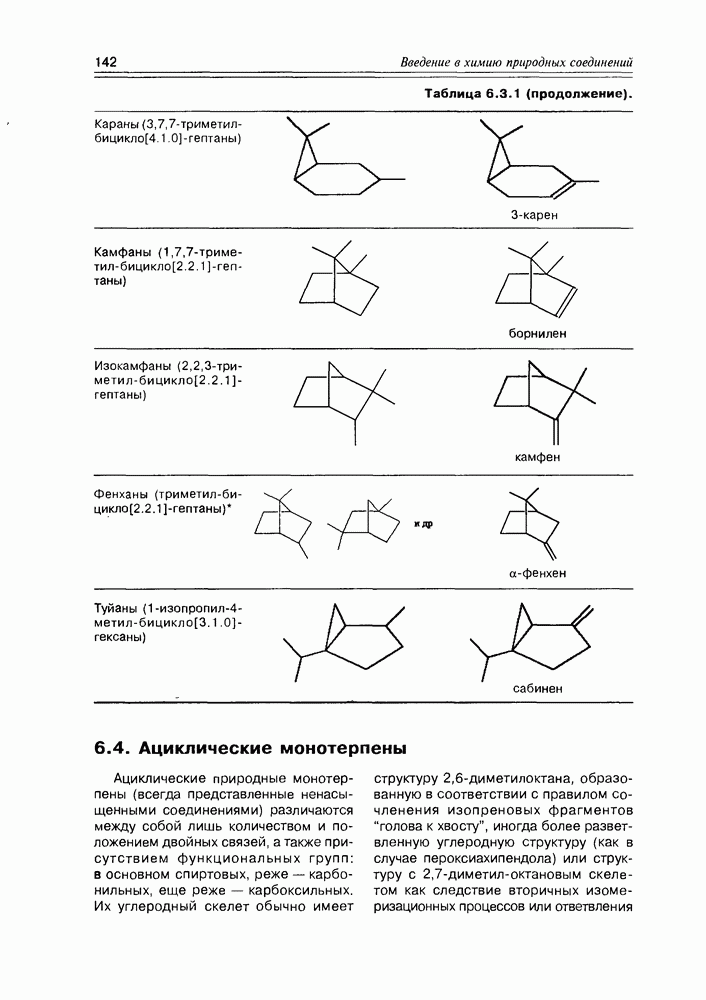
- 6.3. Монотерпены
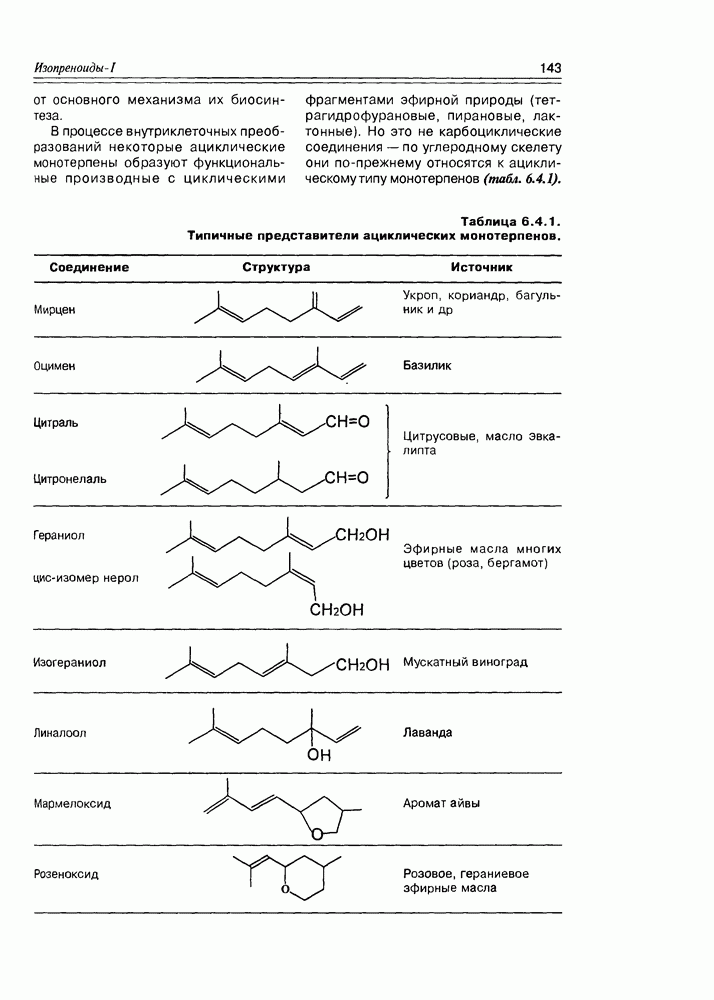
- 6.4. Ациклические монотерпены
- 6.5. Моноциклические терпены
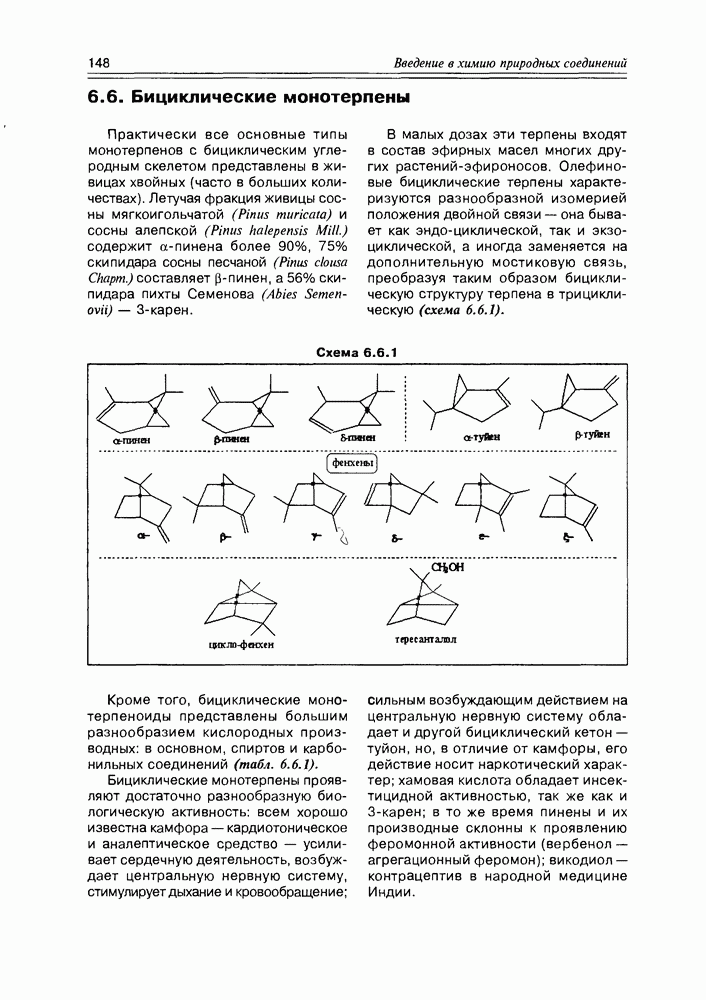
- 6.6. Бициклические монотерпены
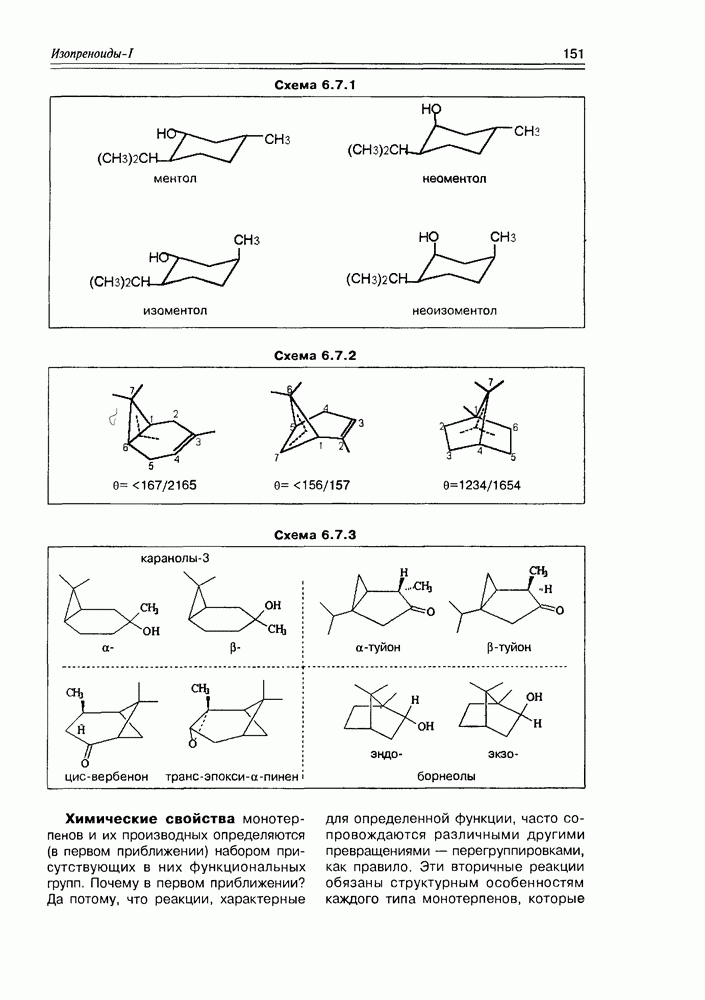
- 6.7. Строение и свойства монотерпенов
- 6.8. Биосинтез изопреноидов
- Глава 7. ИЗОПРЕНОИДЫ II. ОТ СЕСКВИТЕРПЕНОВ ДО ПОЛИТЕРПЕНОВ
- 7.2. Химические свойства сесквитерпенов
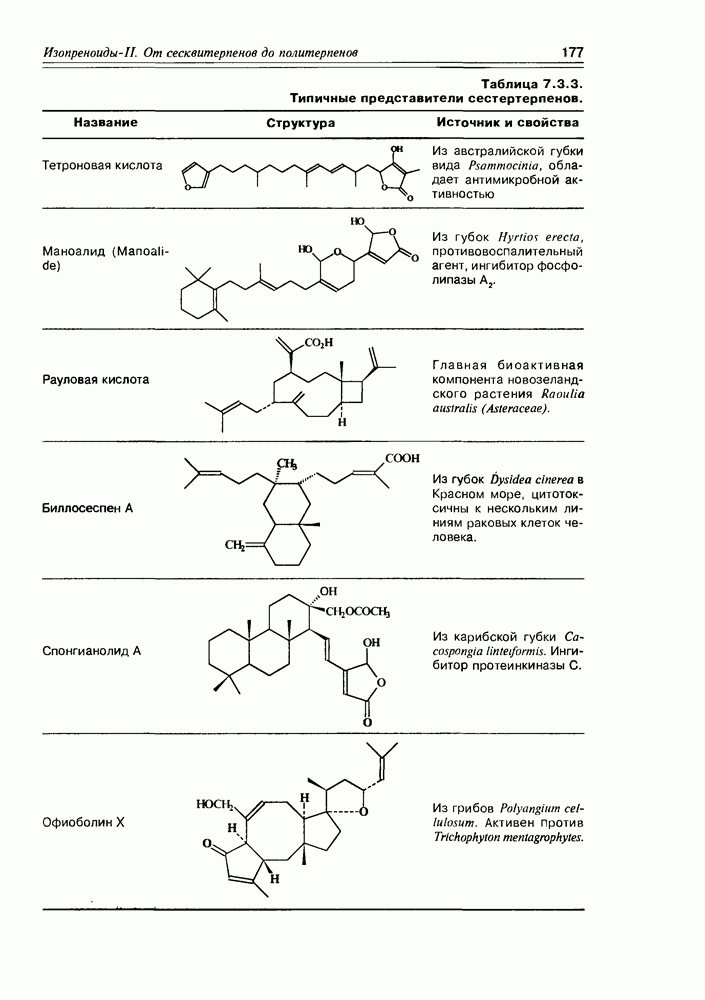
- 7.3. Дитерпены и сестертерпены
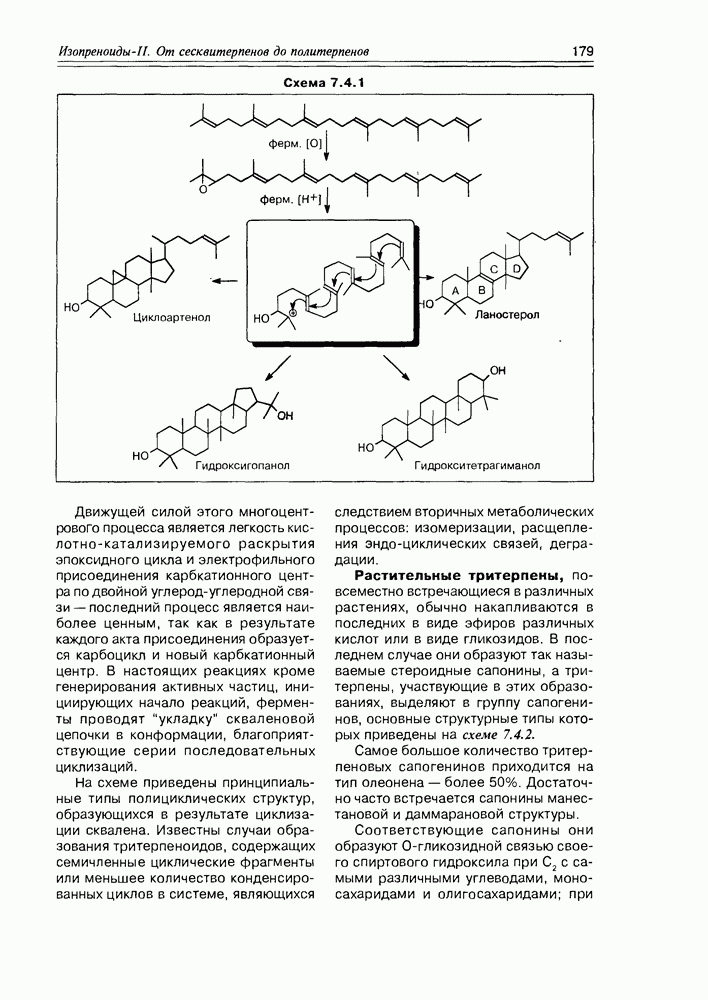
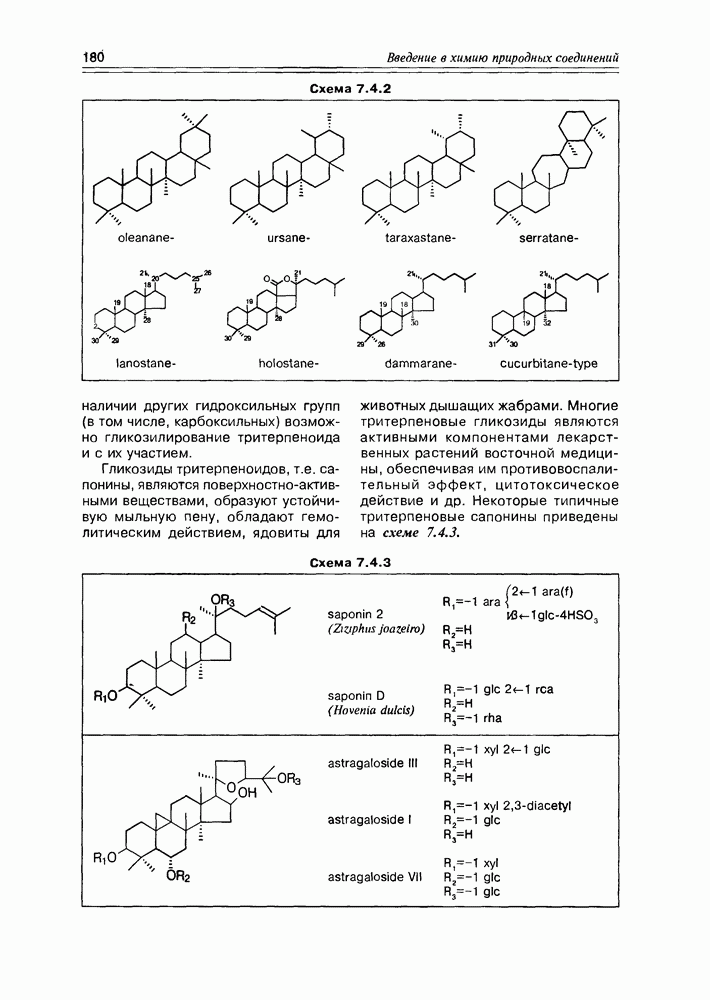
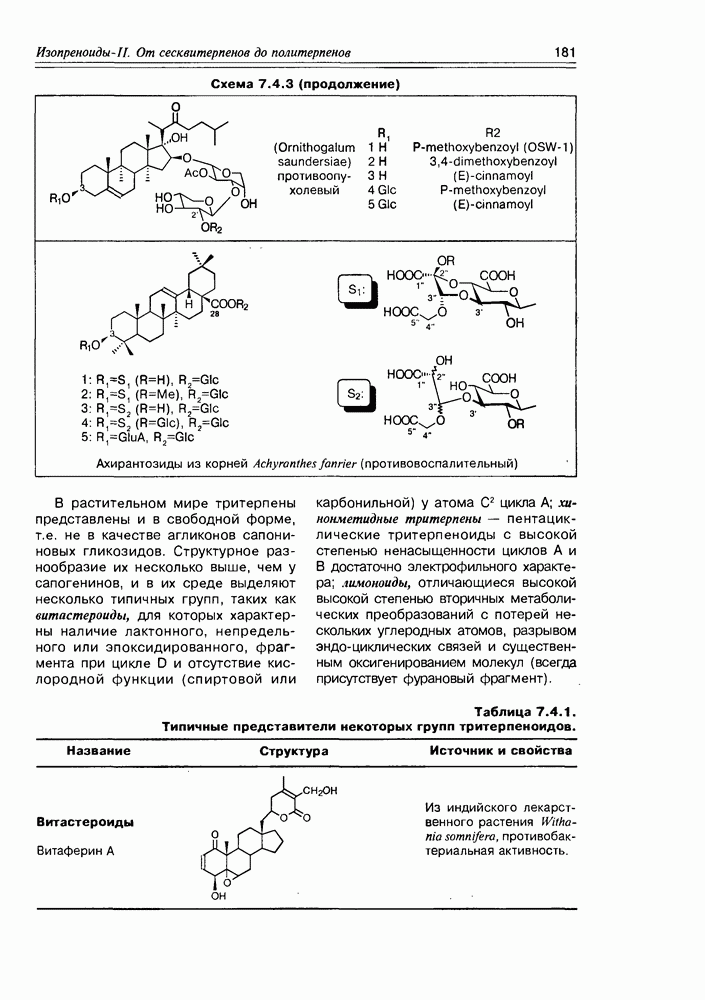
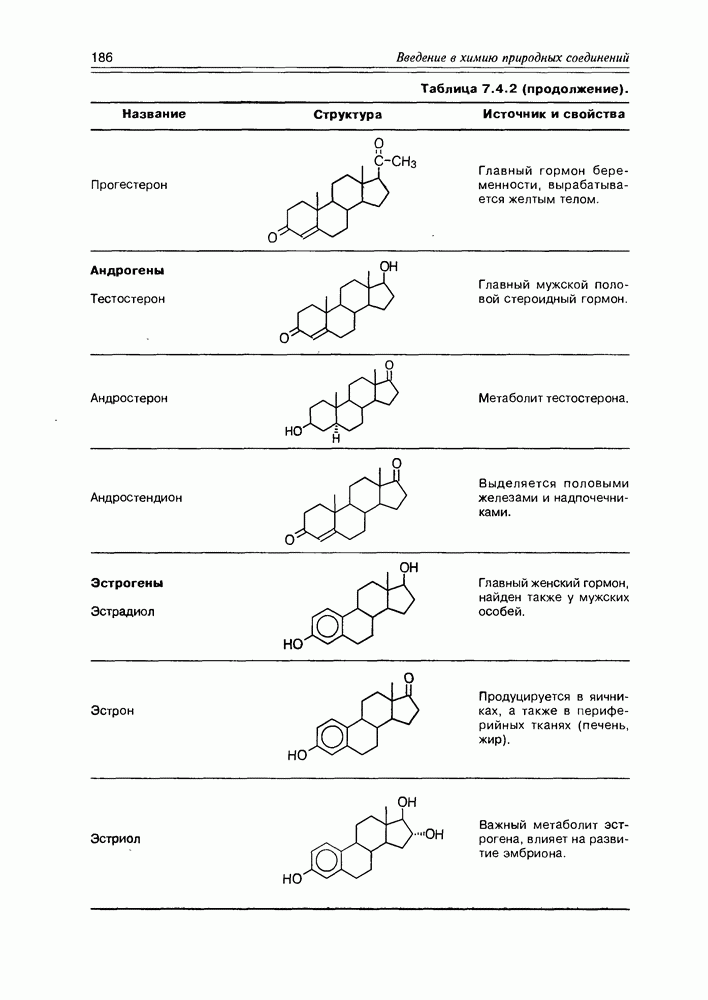
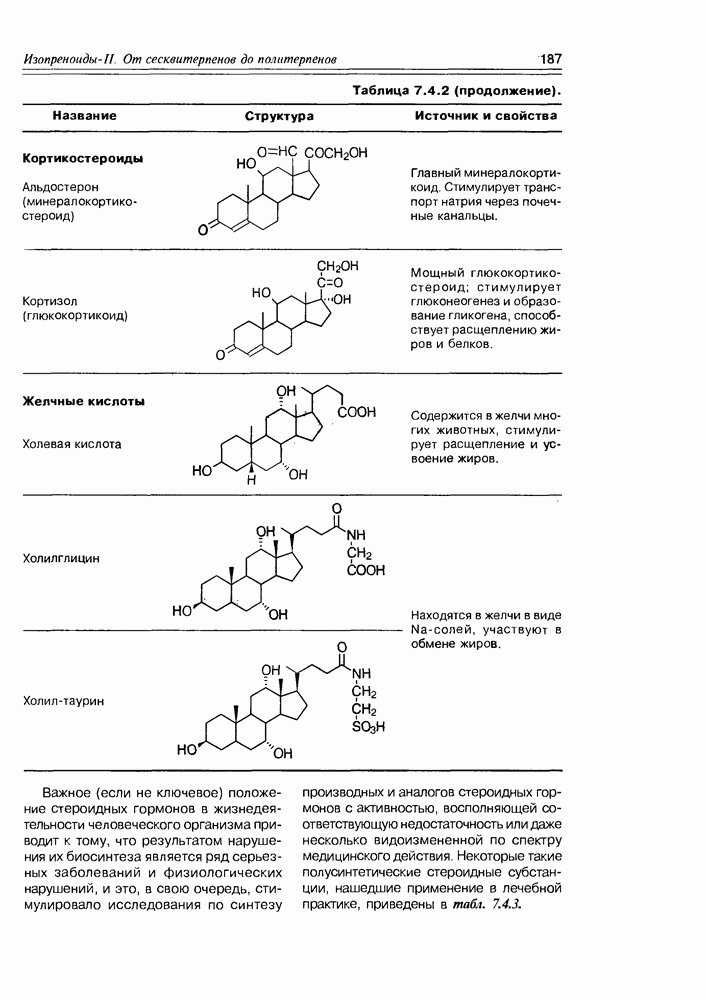
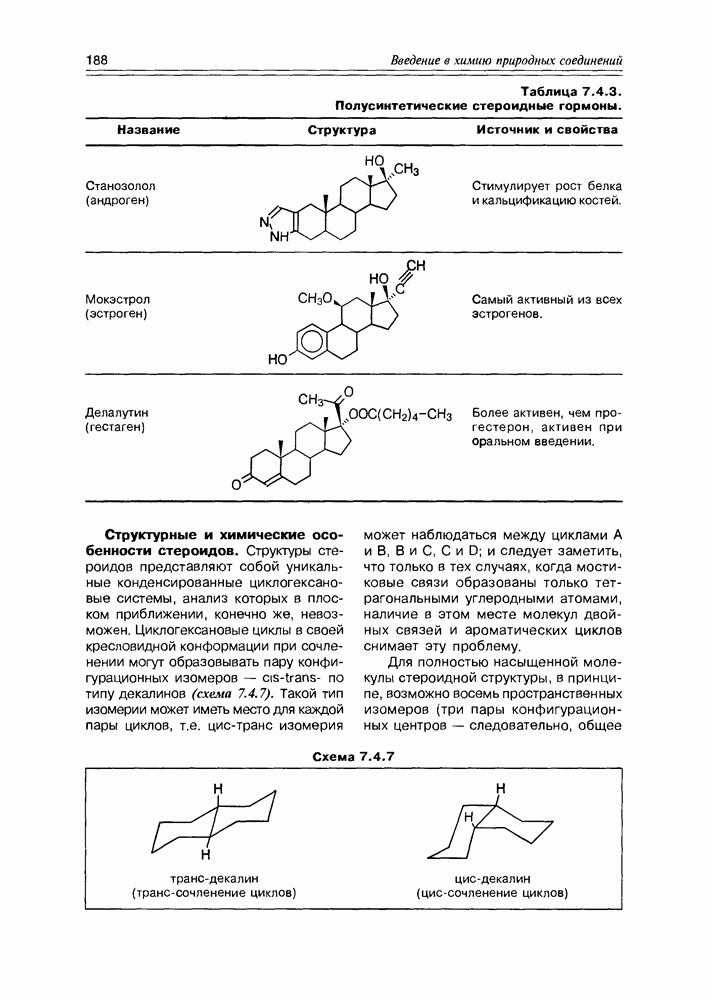
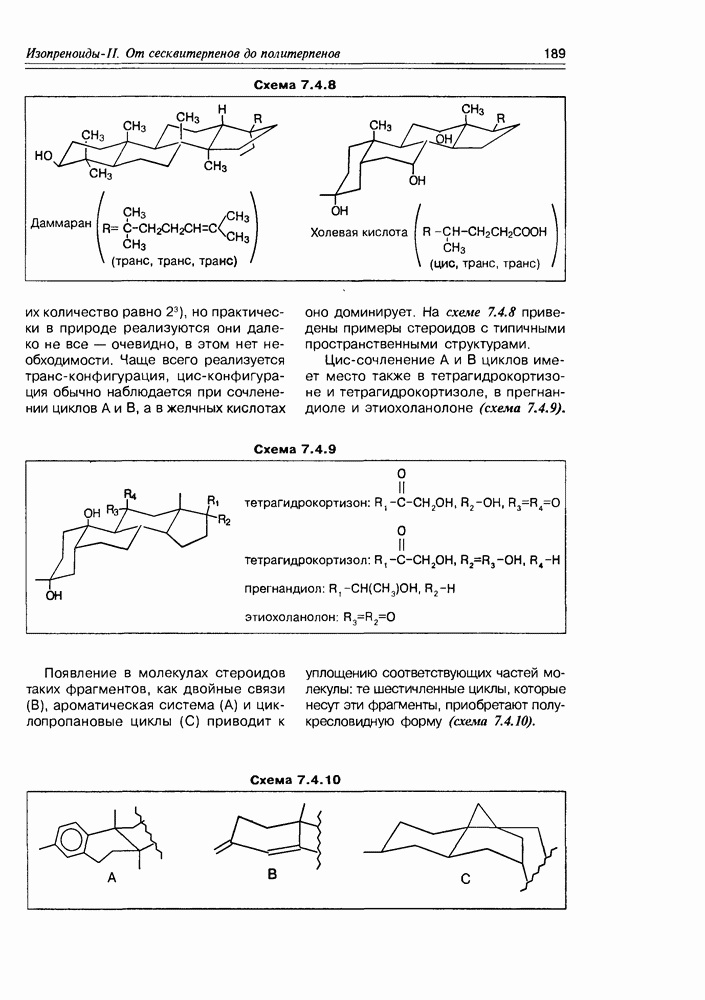
- 7.4. Тритерпеноиды и стероиды
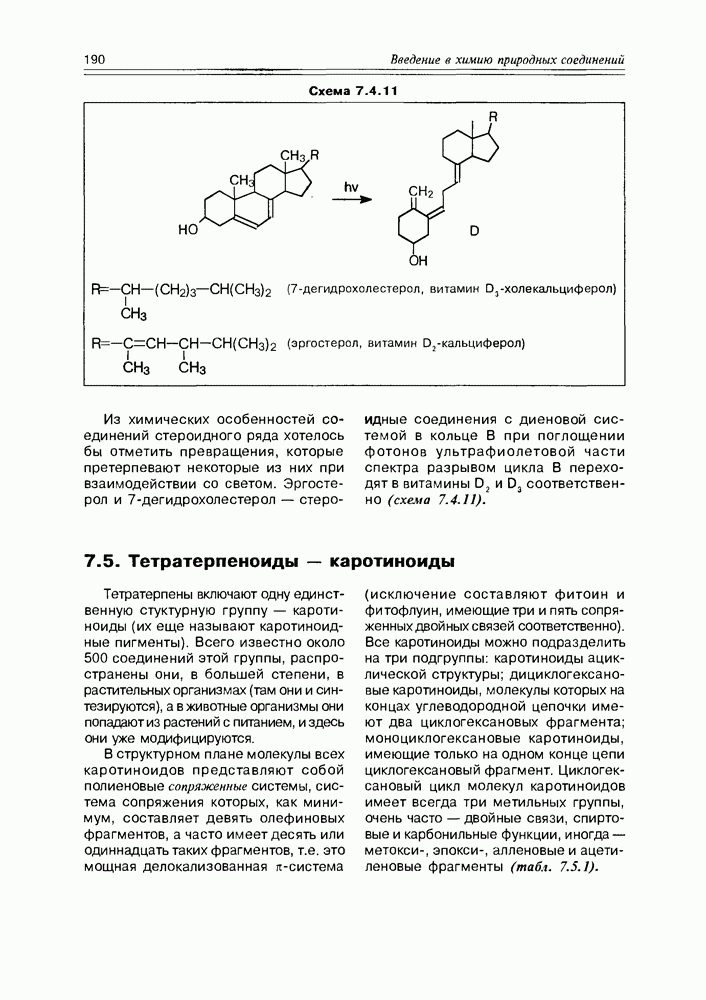
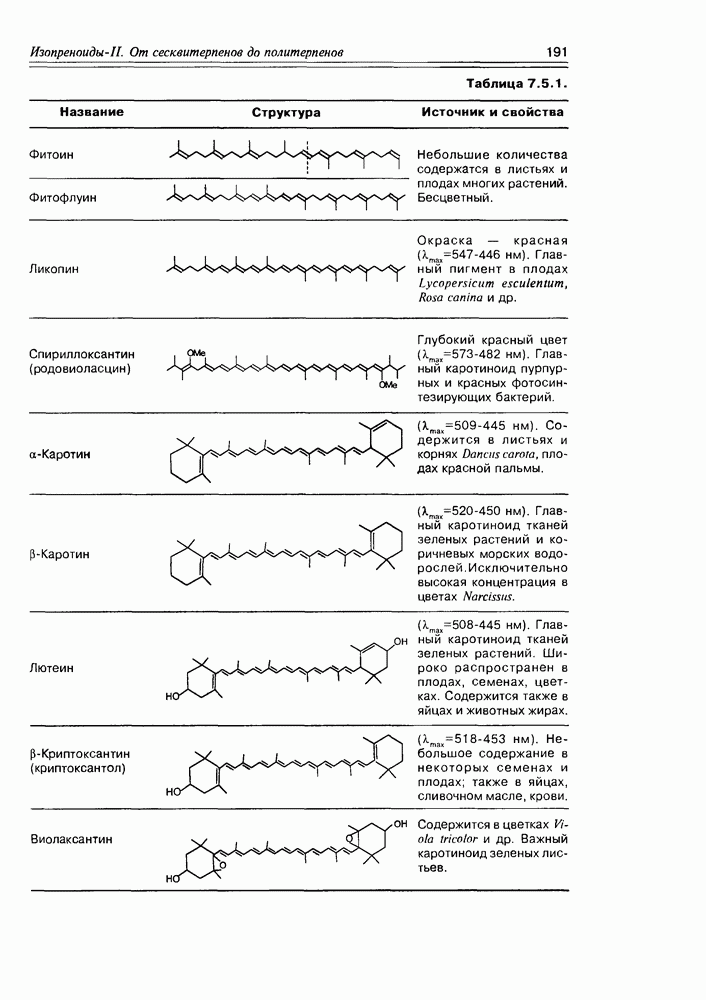
- 7.5. Тетратерпеноиды — каротиноиды
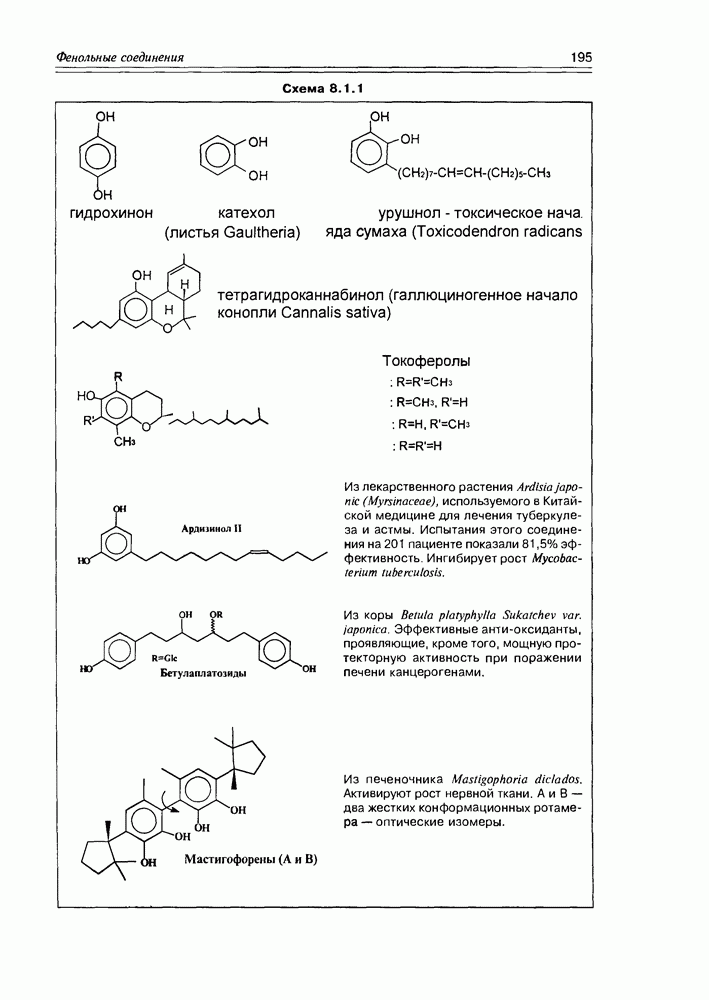
- Глава 8. ФЕНОЛЬНЫЕ СОЕДИНЕНИЯ
- 8.2. Пираны
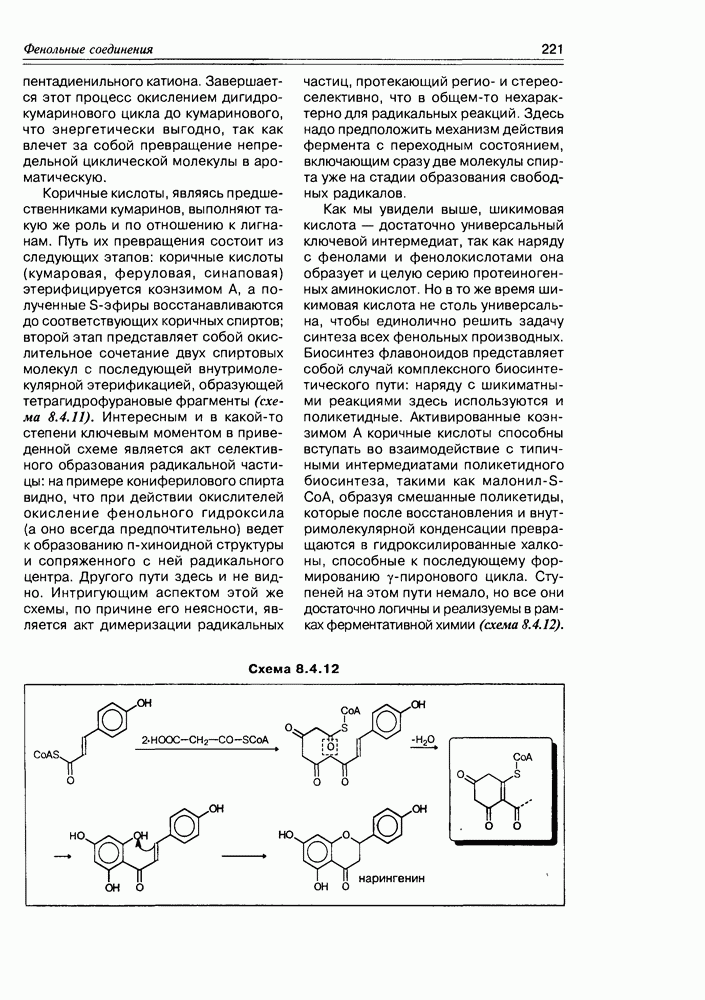
- 8.4. Биосинтез фенольных соединений
- Глава 9. АЛКАЛОИДЫ И ПОРФИРИНЫ
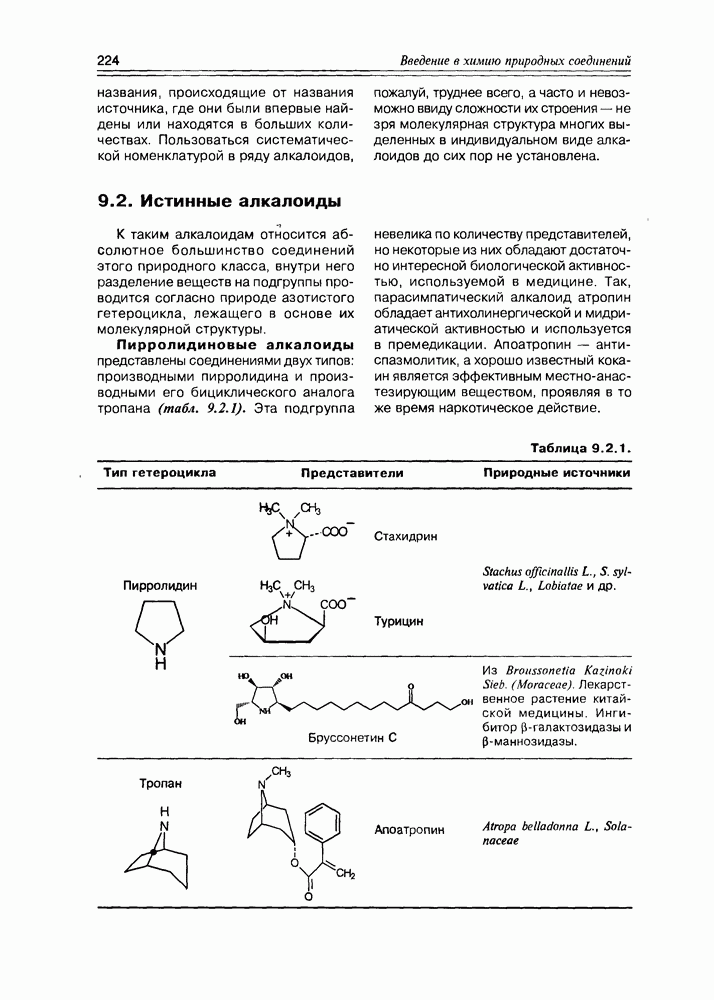
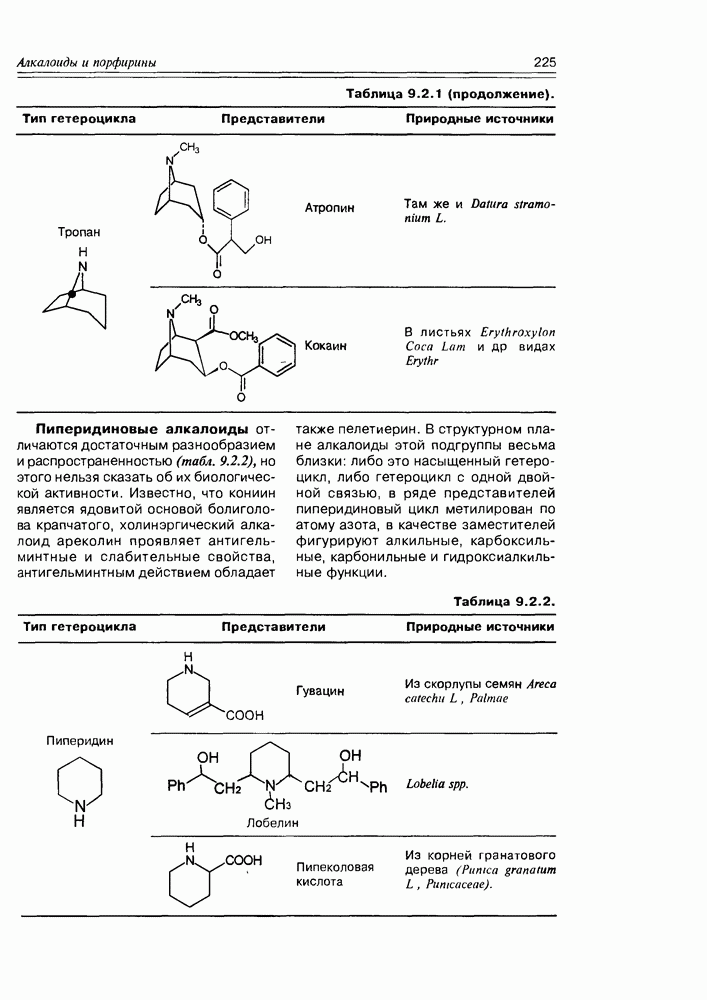
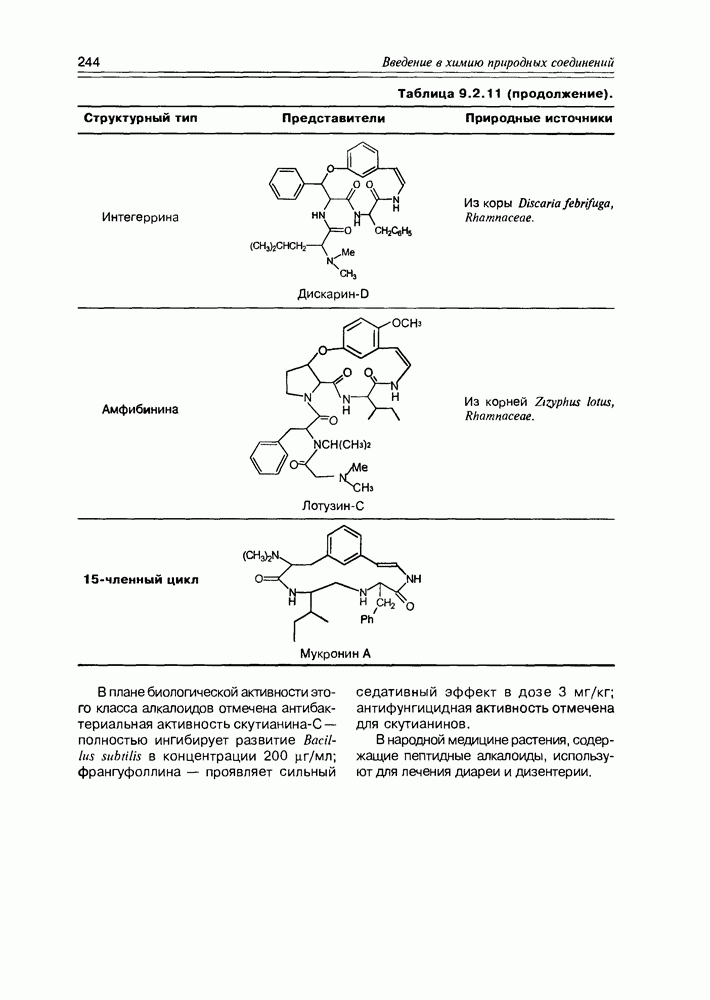
- 9.2. Истинные алкалоиды
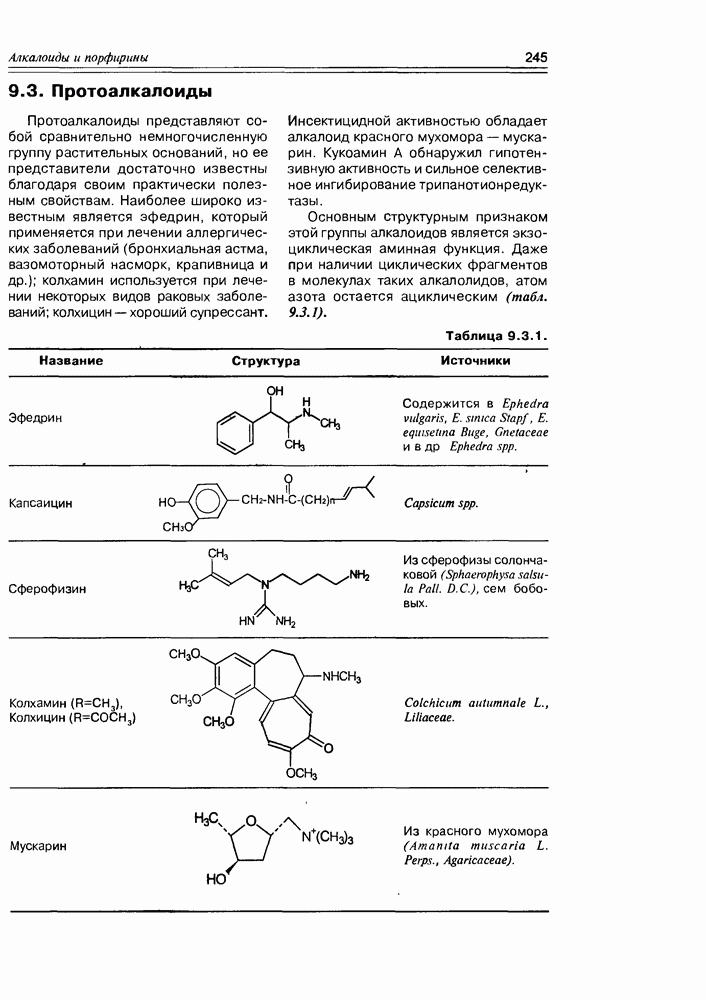
- 9.3. Протоалкалоиды
- 9.5. Химические свойства и химические модификации алкалоидов
- 9.6. Аминокислоты и биосинтез алкалоидов
- 9.7. Порфирины
- Глава 10. ВИТАМИНЫ И КОФЕРМЕНТЫ
- 10.1. Витамины — собственно
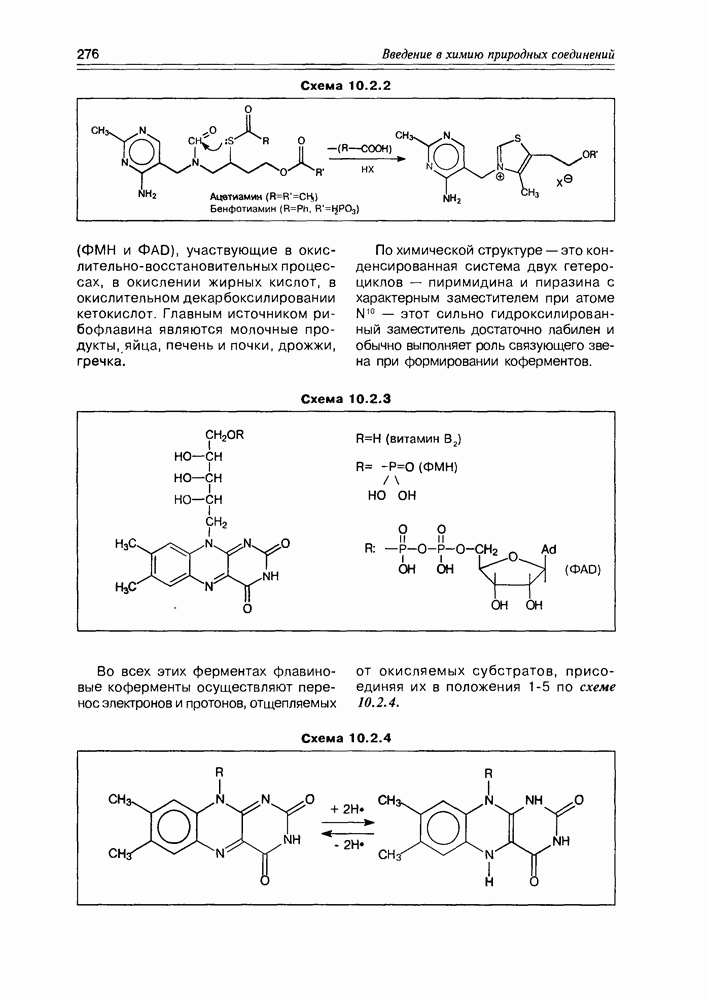
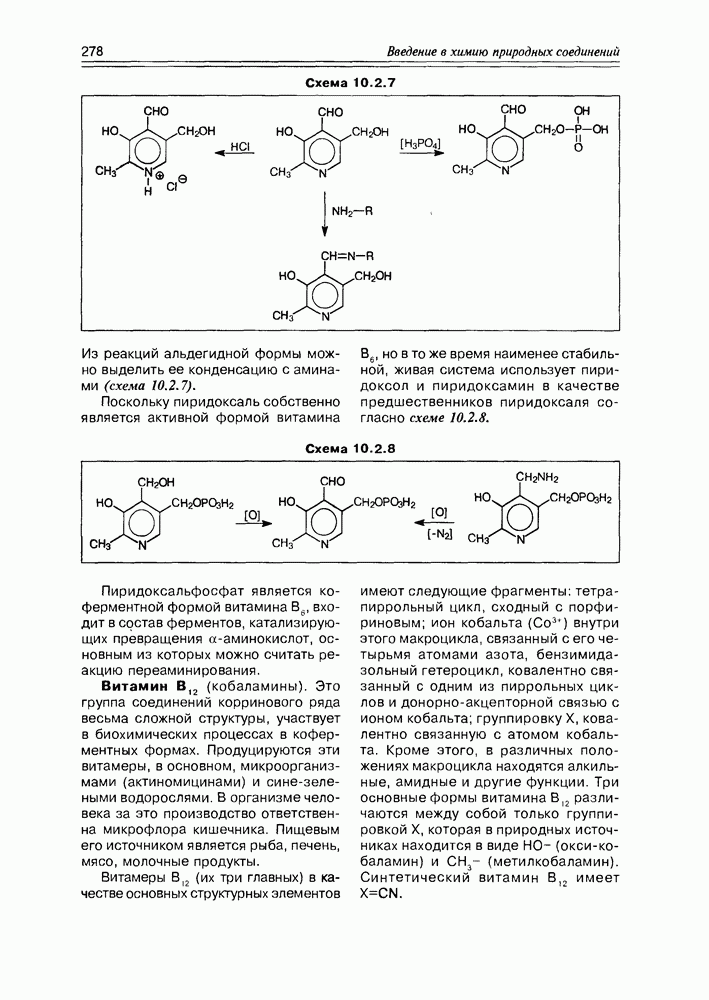
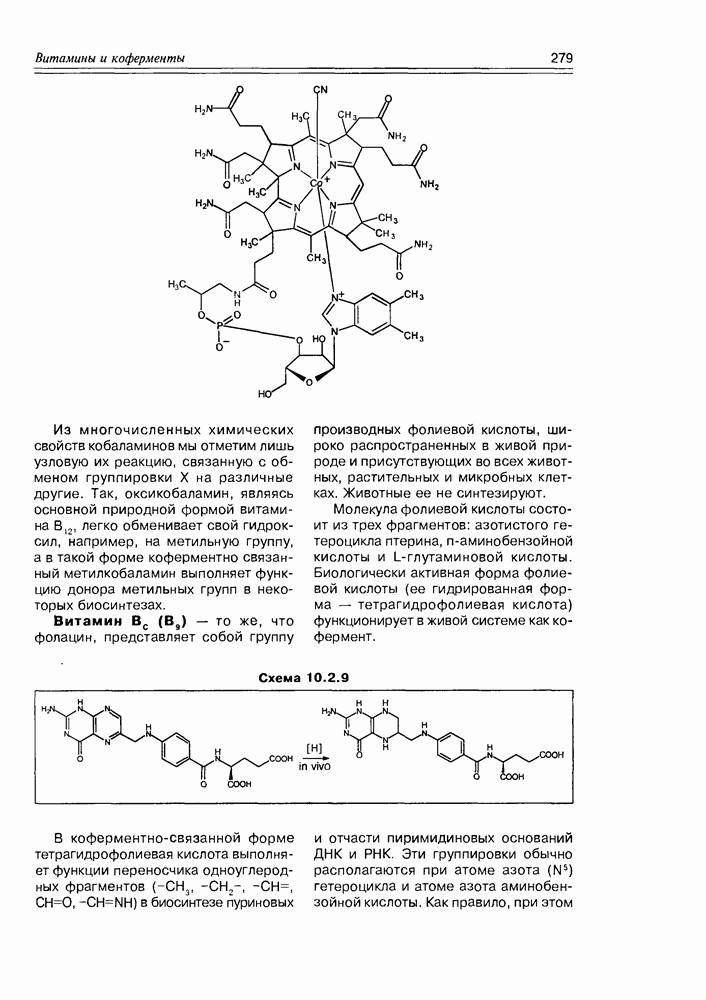
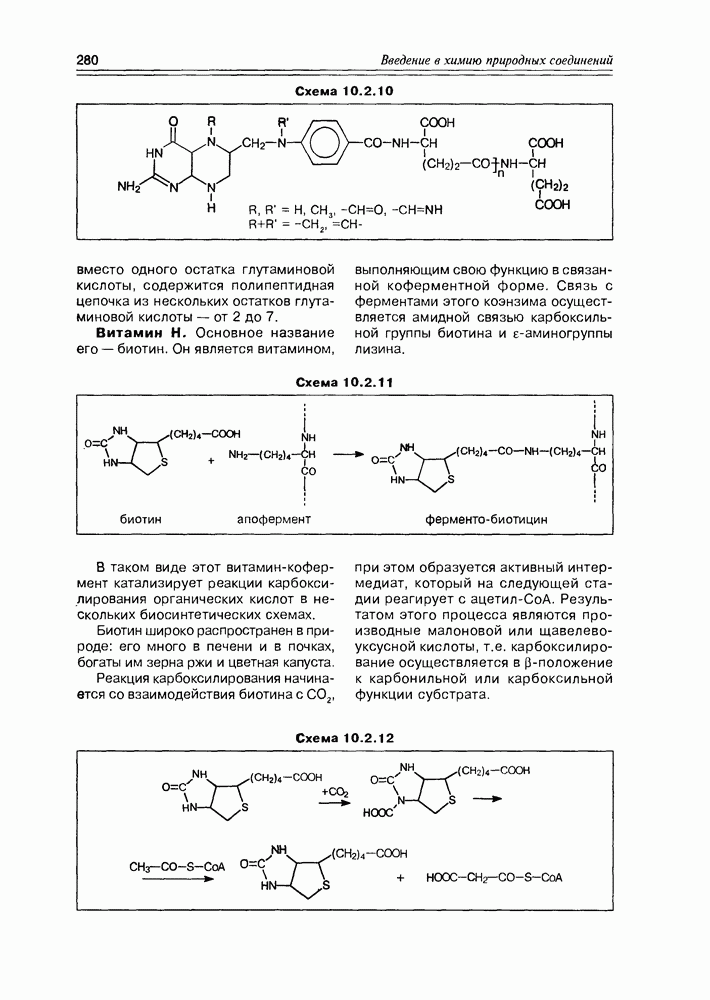
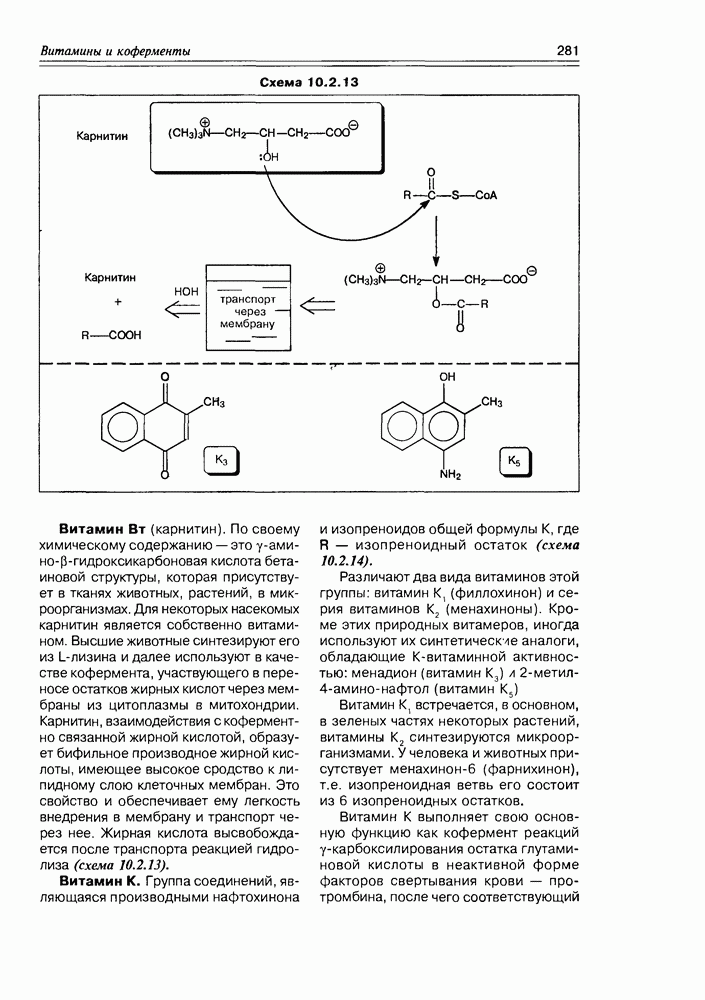
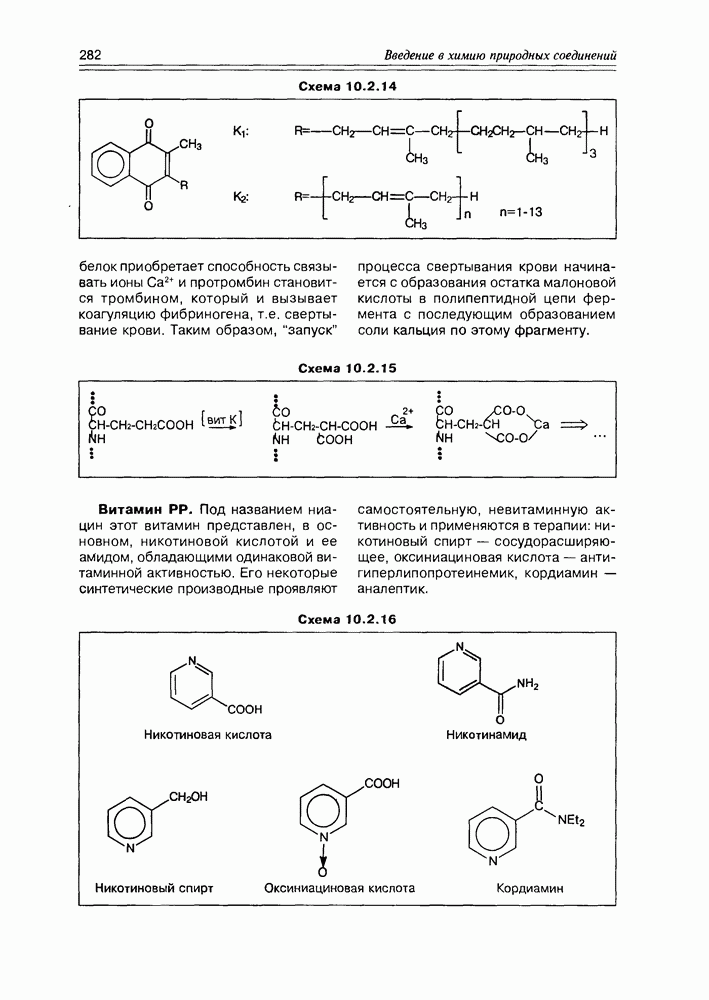
- 10.2. Витамины-коферменты
- 10.3. Коферменты
- Глава 11. АНТИБИОТИКИ
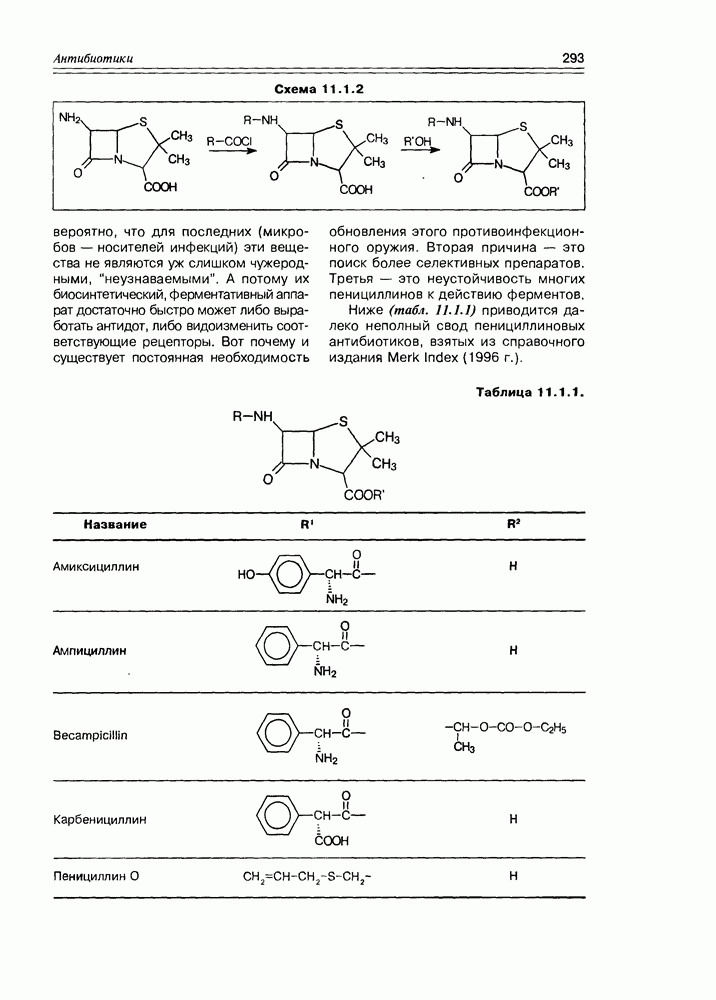
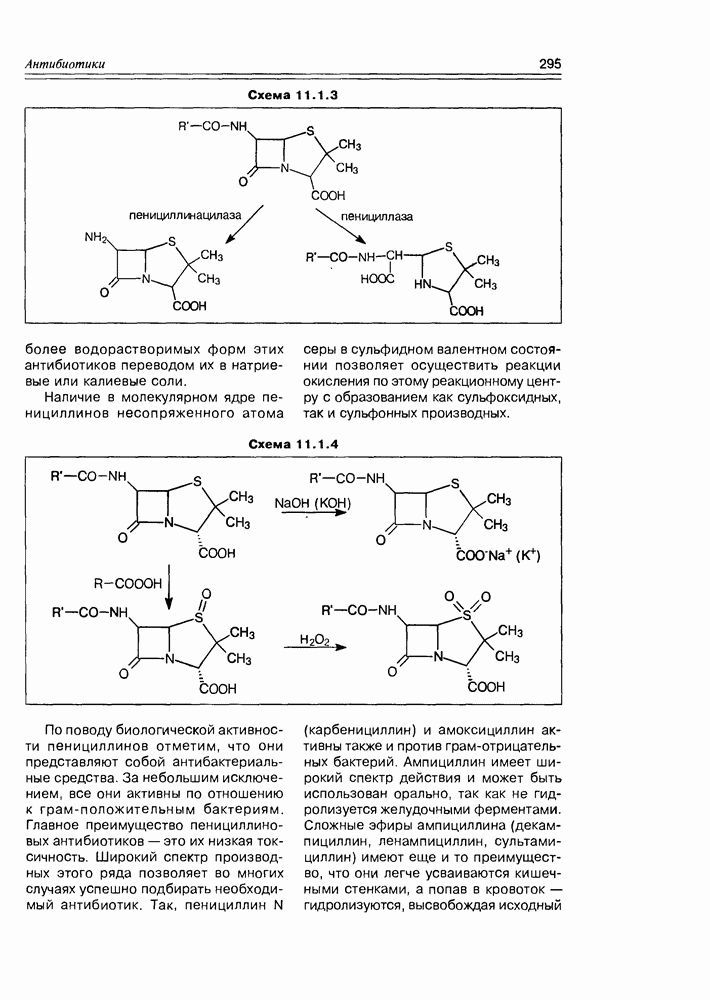
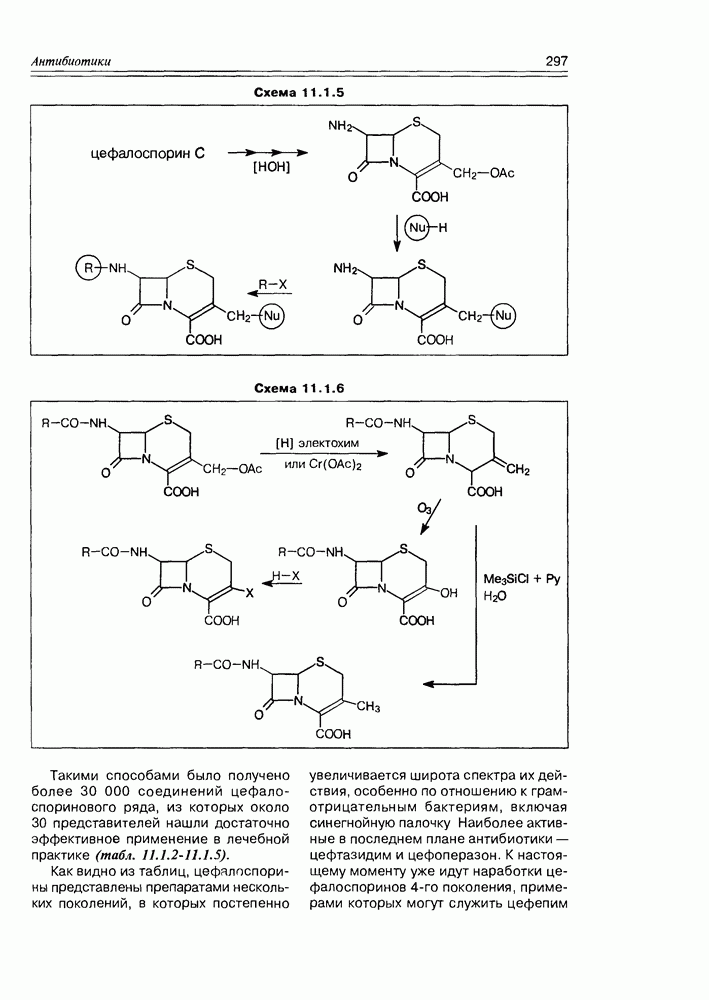
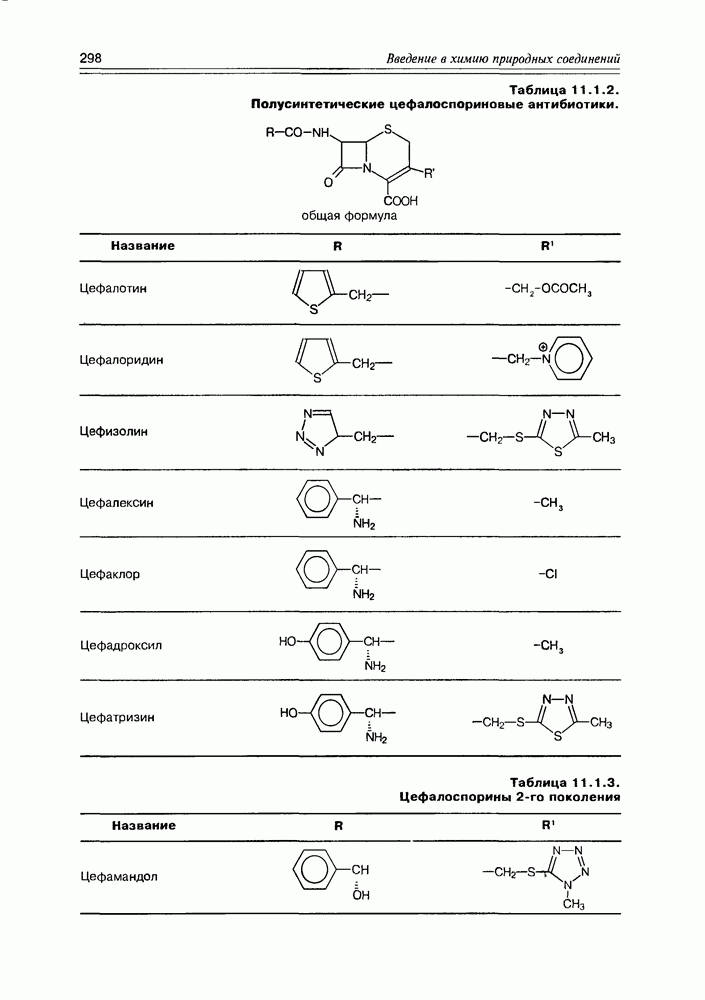
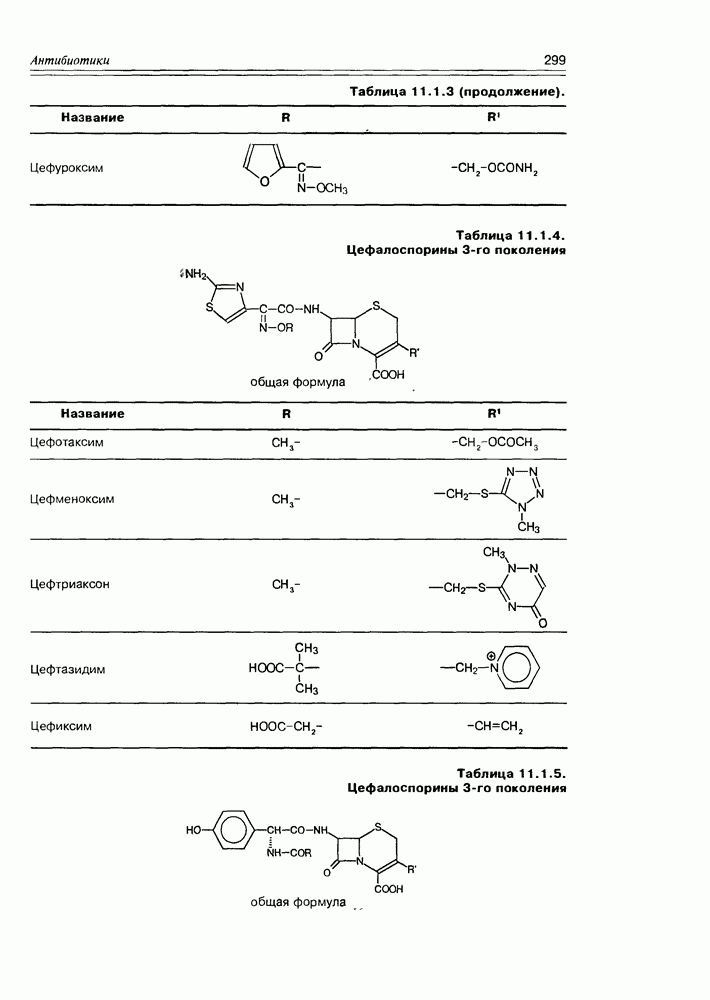
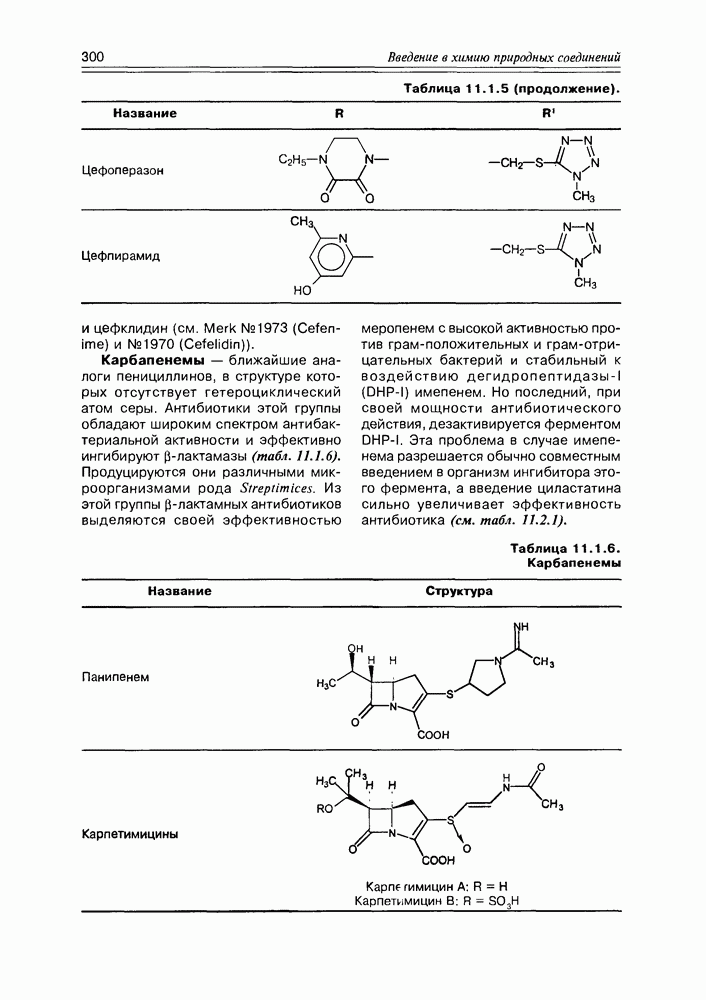
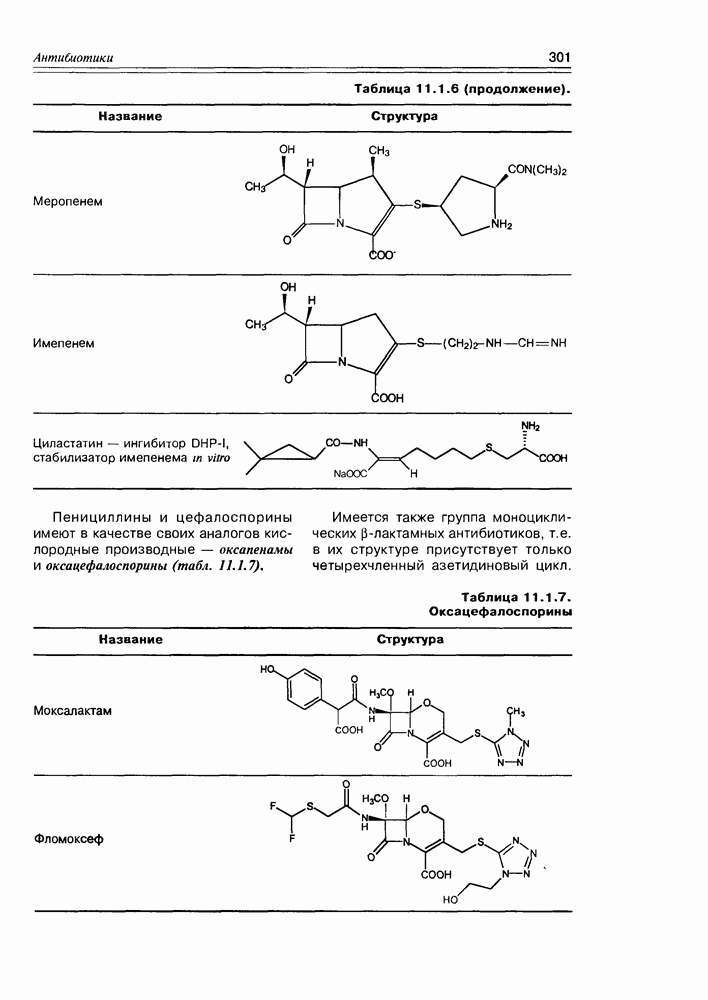
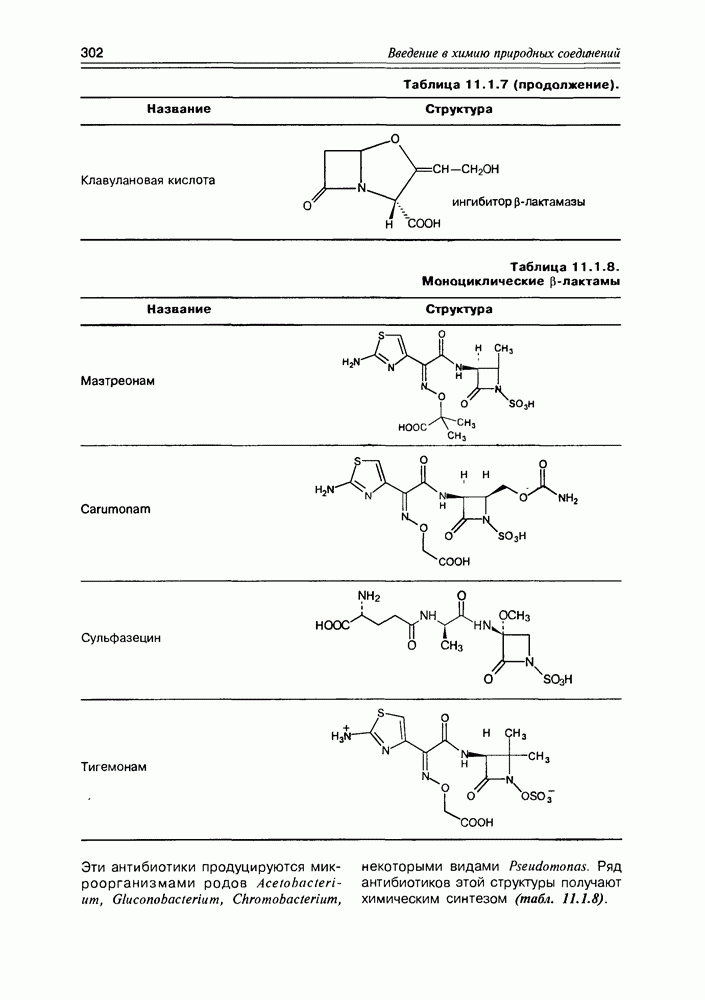
- 11.1. b-Лактамные антибиотики
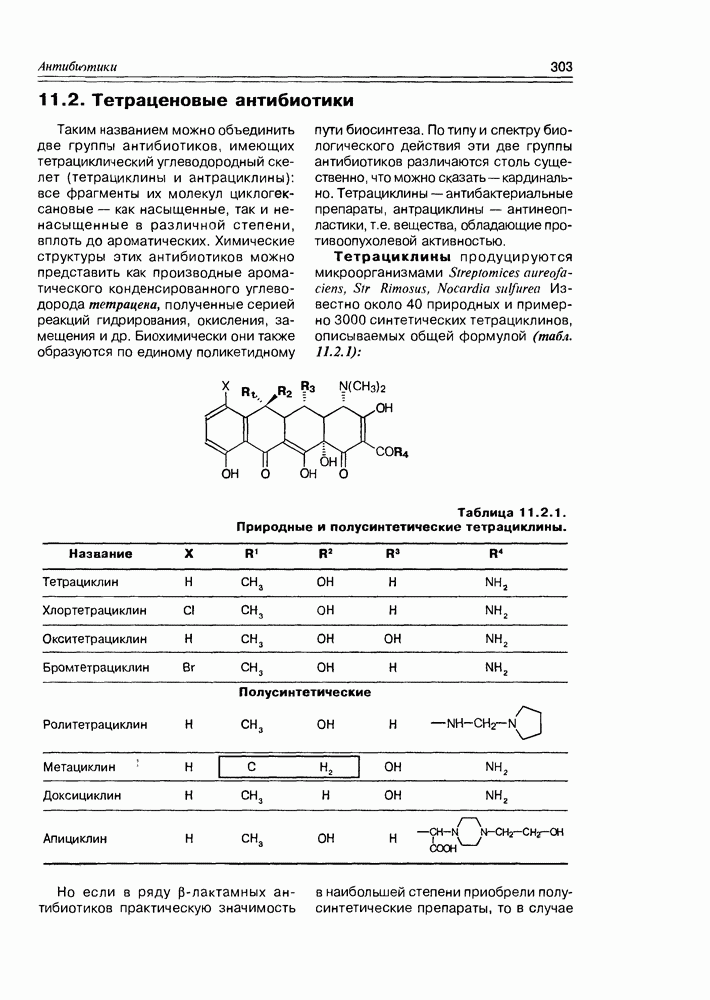
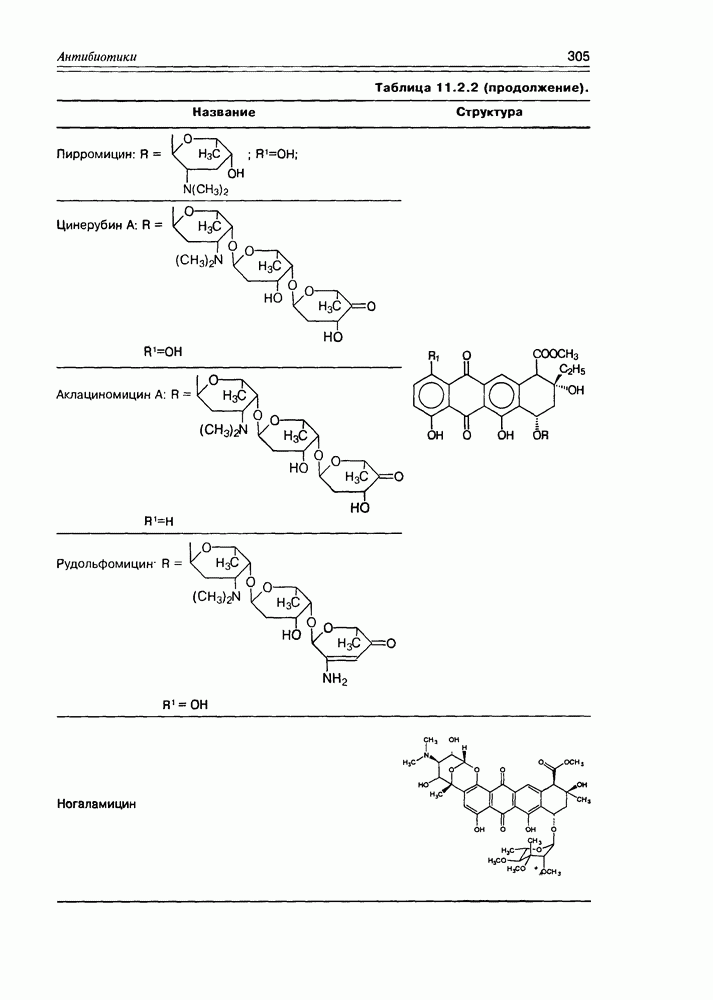
- 11.2. Тетраценовые антибиотики
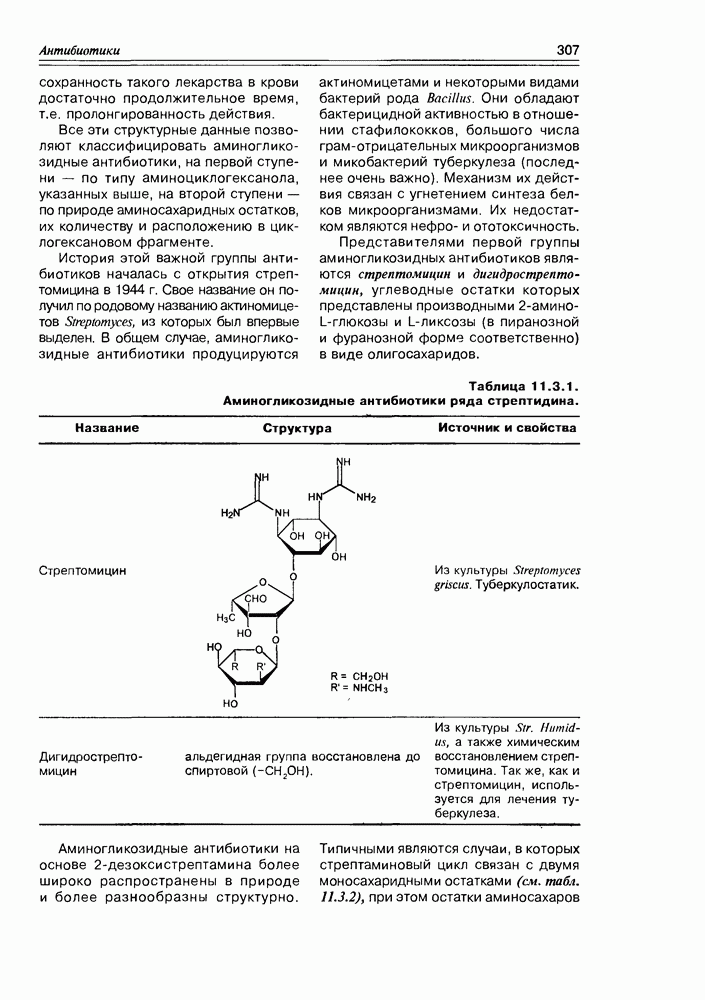
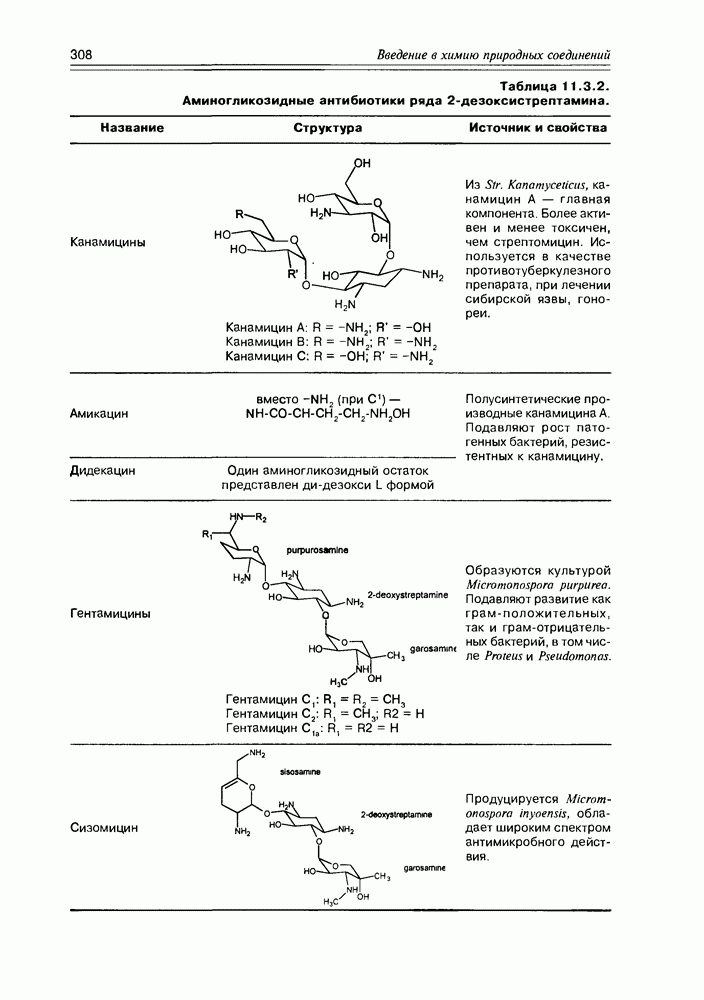
- 11.3. Аминогликозидные антибиотики
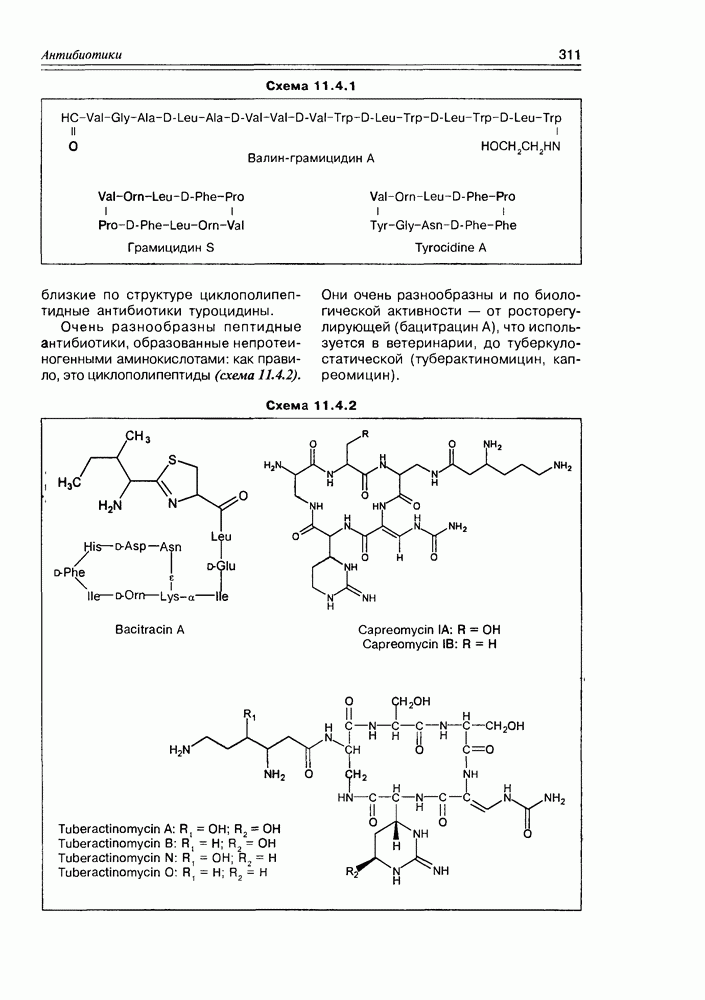
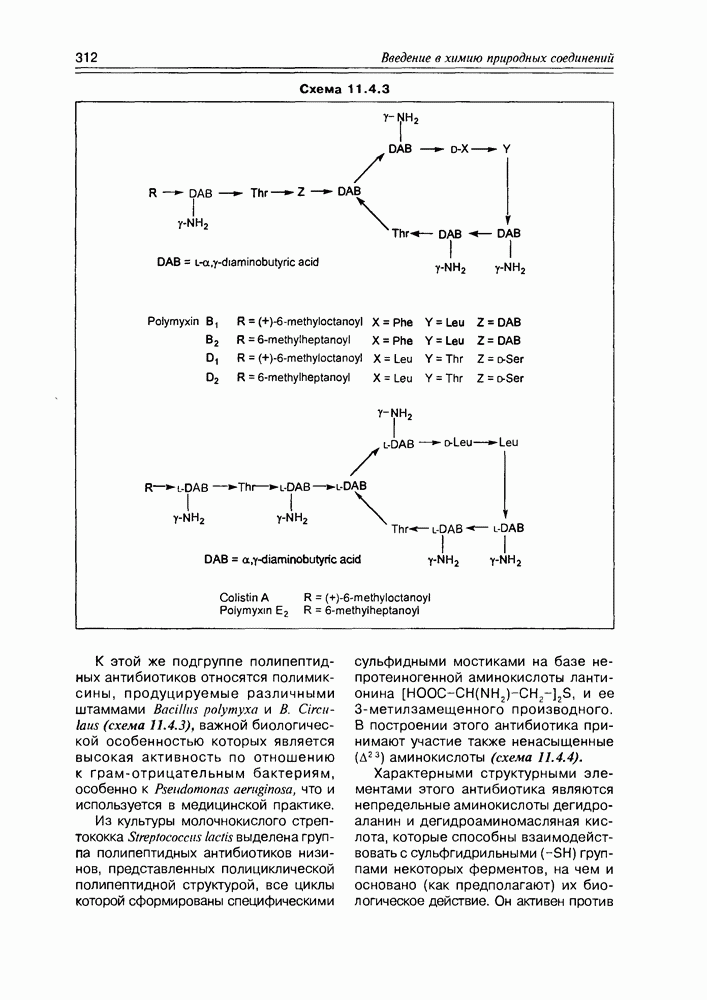
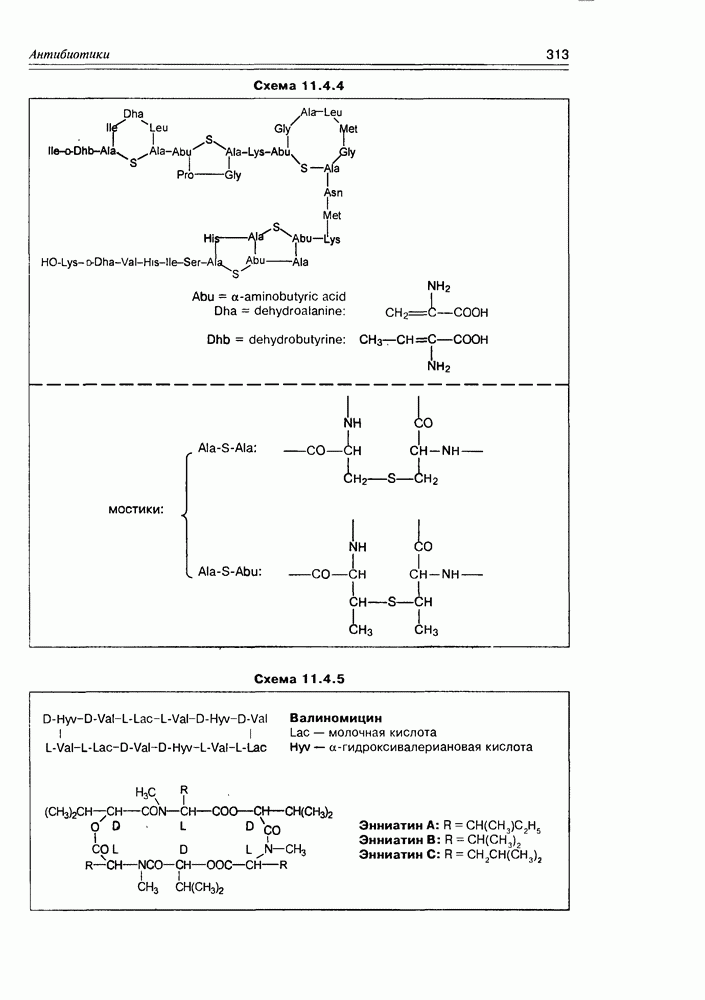
- 11.4. Пептидные антибиотики
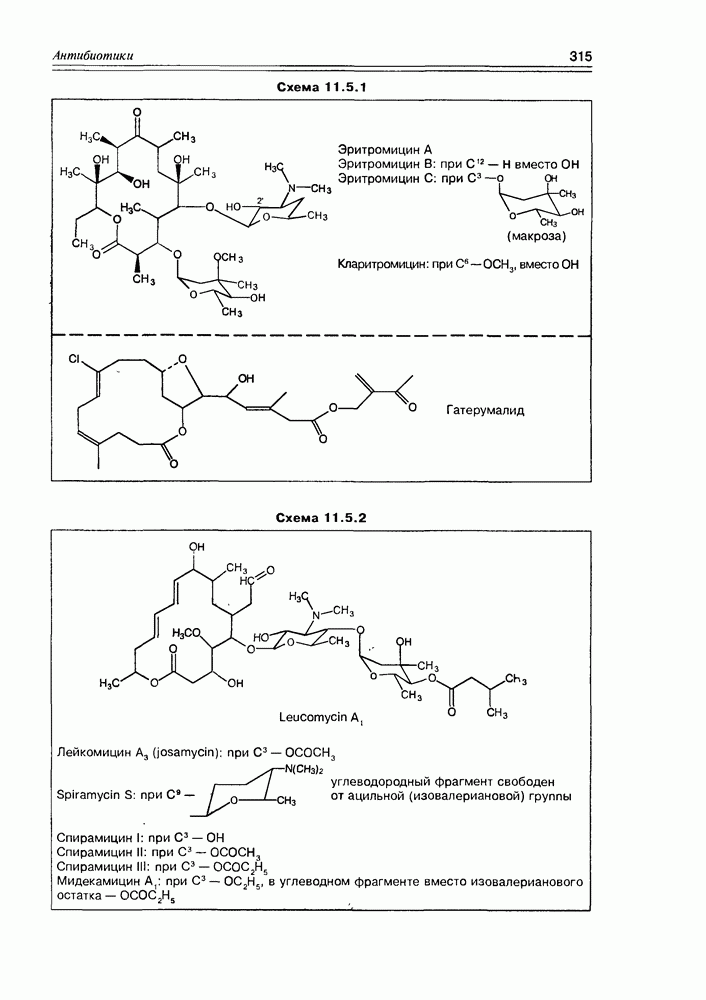
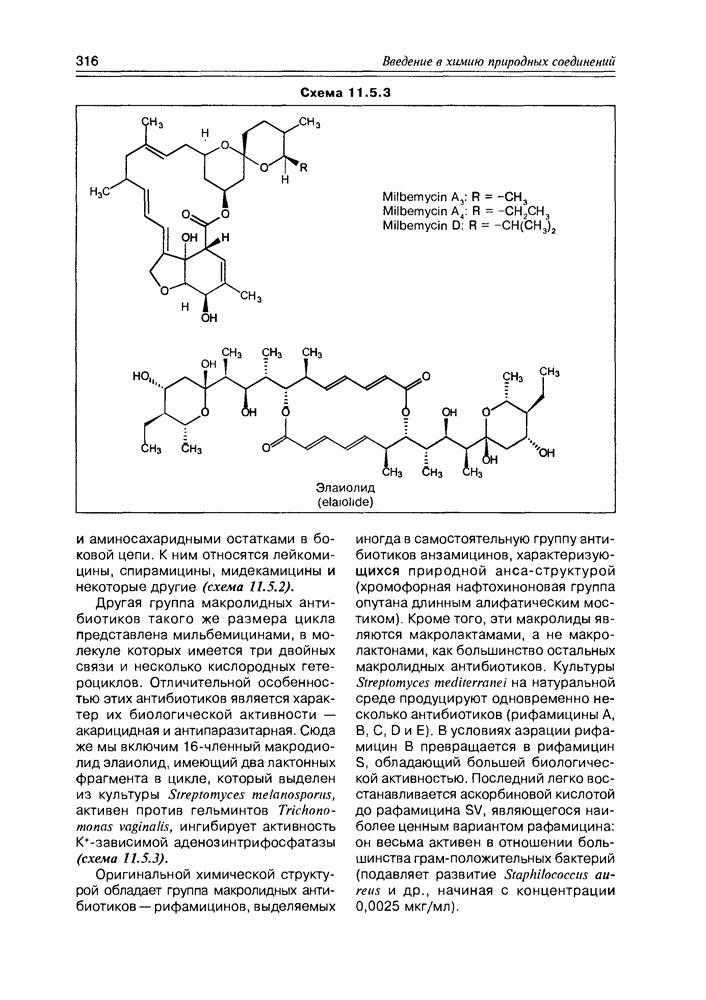
- 11.5. Макролидные антибиотики
- 11.6. Полиэфирные антибиотики
- 11.7. Антибиотики разные
- Глава 12. РАЗНЫЕ ГРУППЫ ПРИРОДНЫХ СОЕДИНЕНИЙ
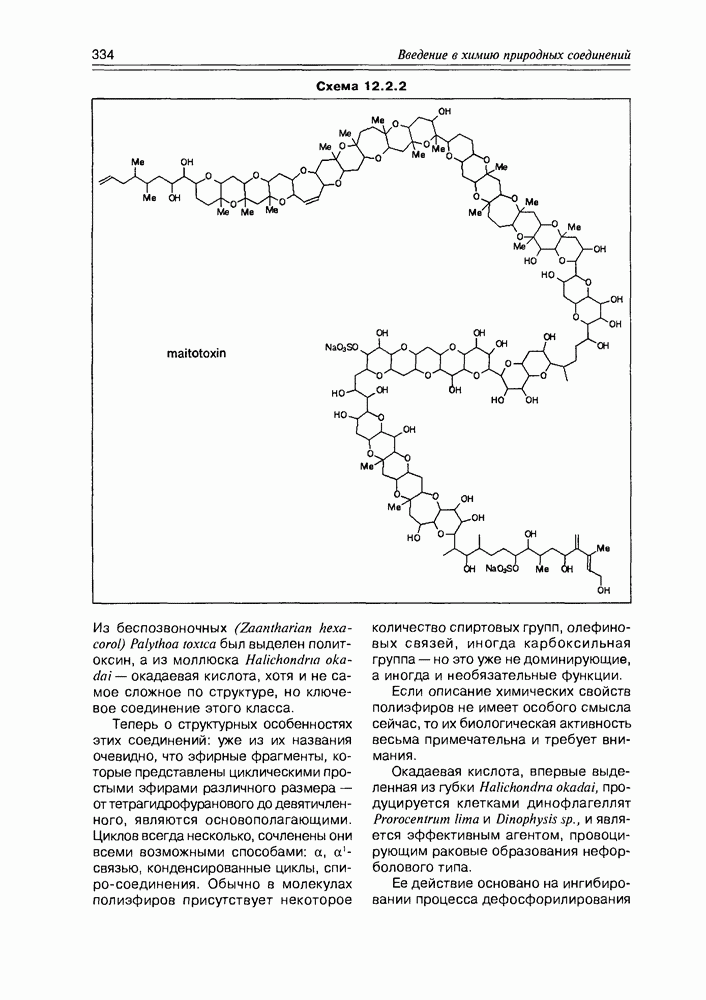
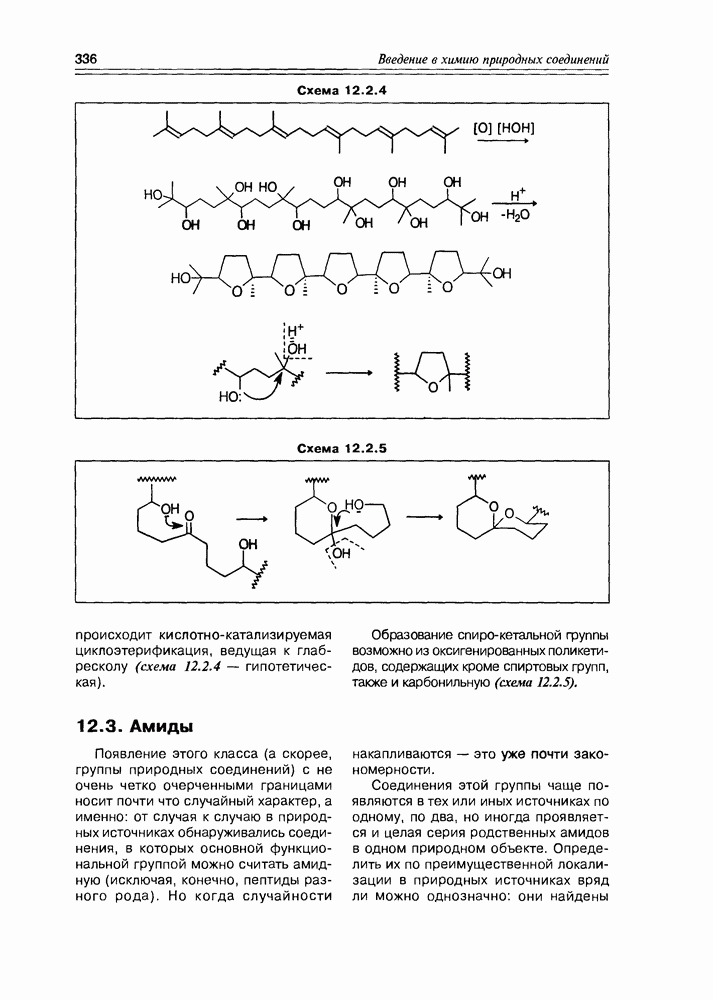
- 12.2. Полиэфиры
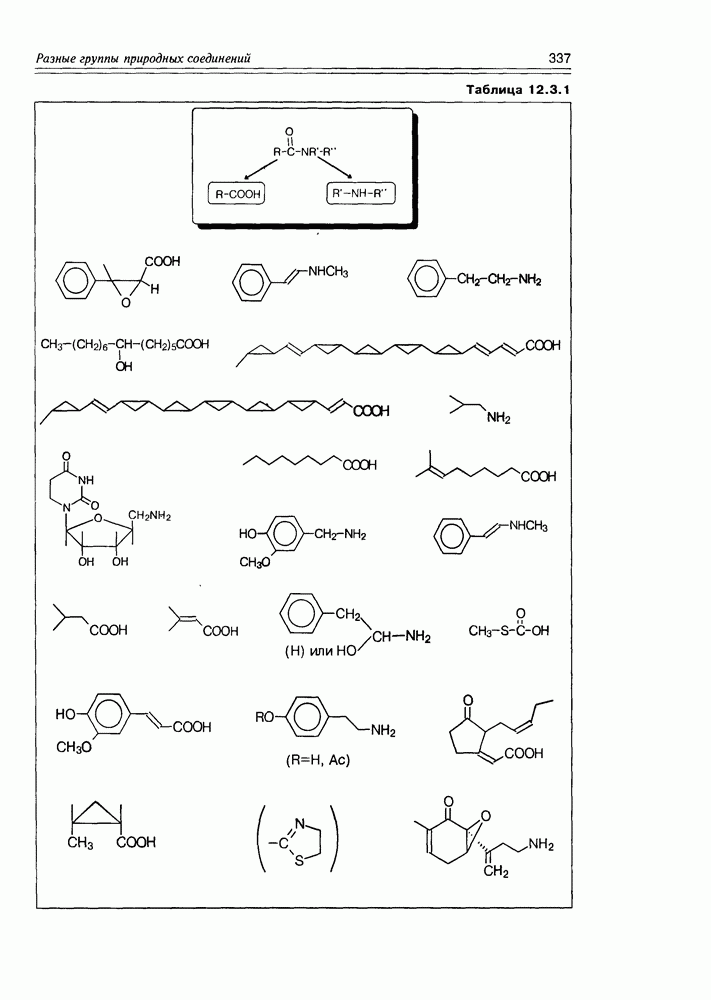
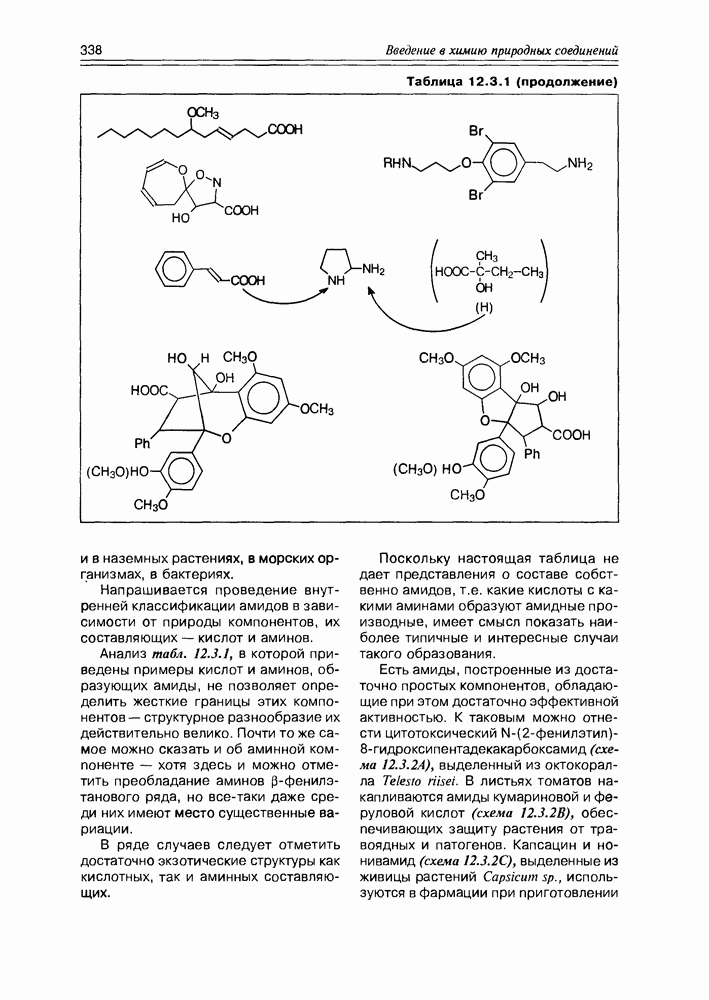
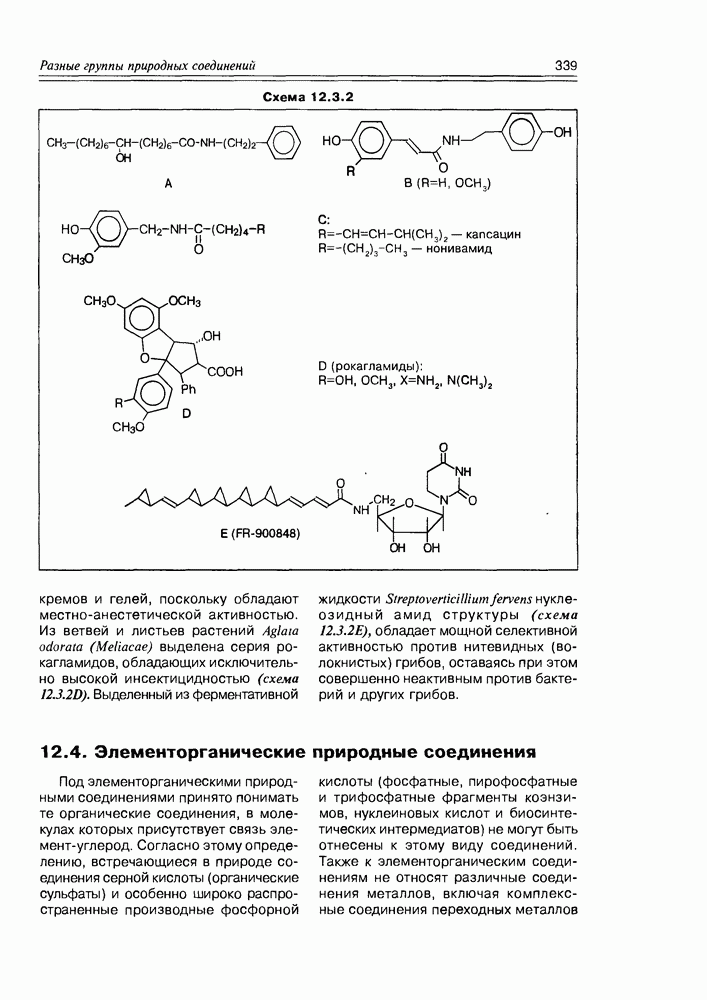
- 12.3. Амиды
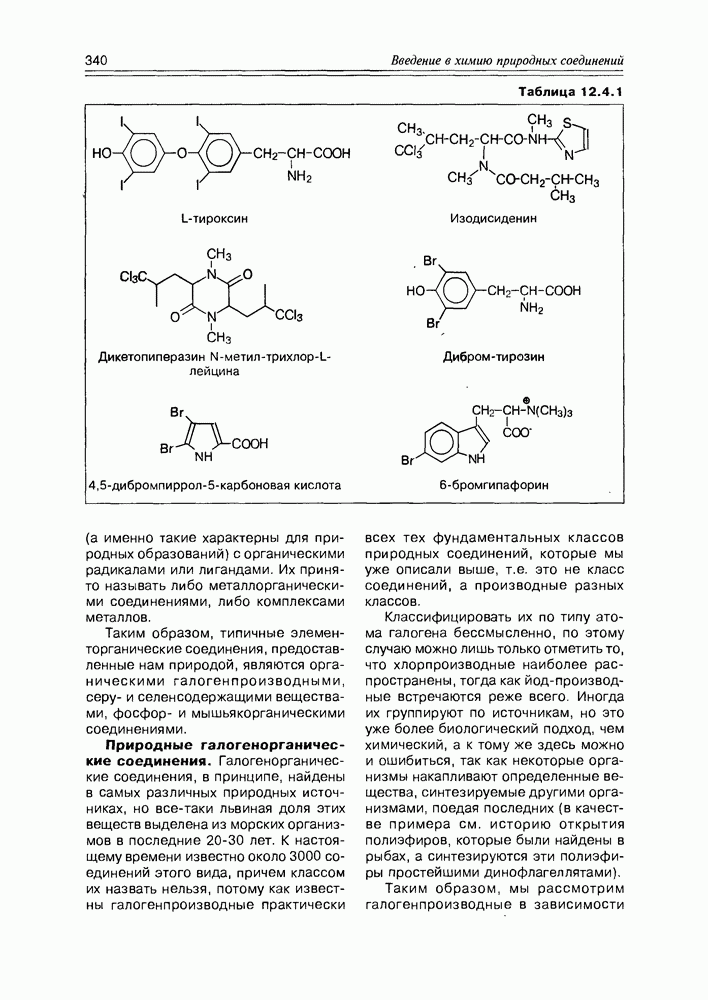
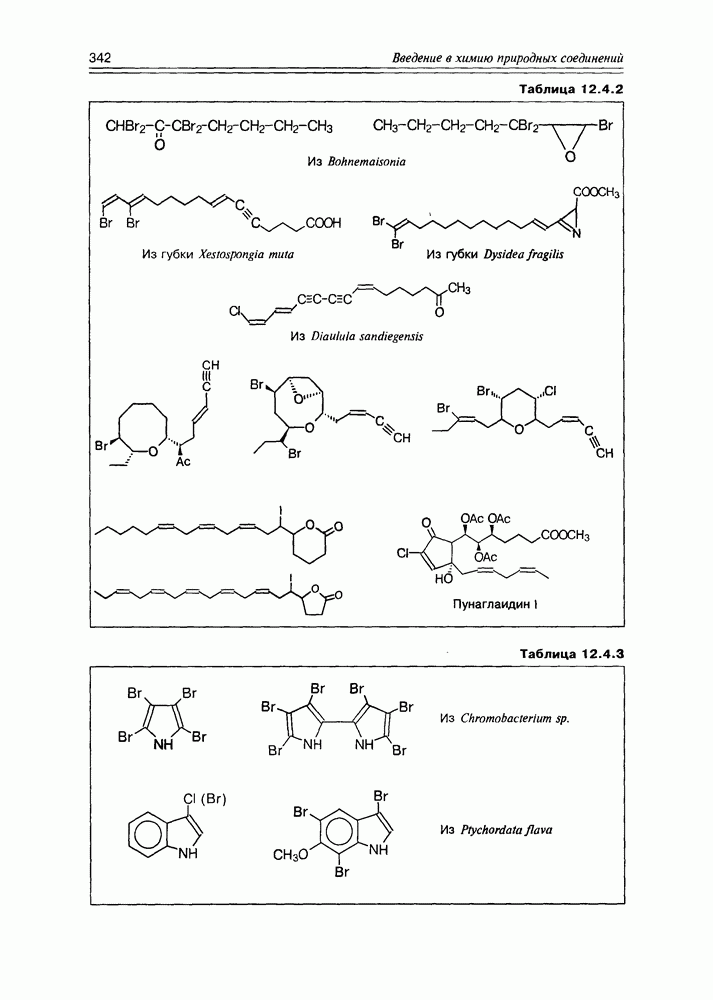
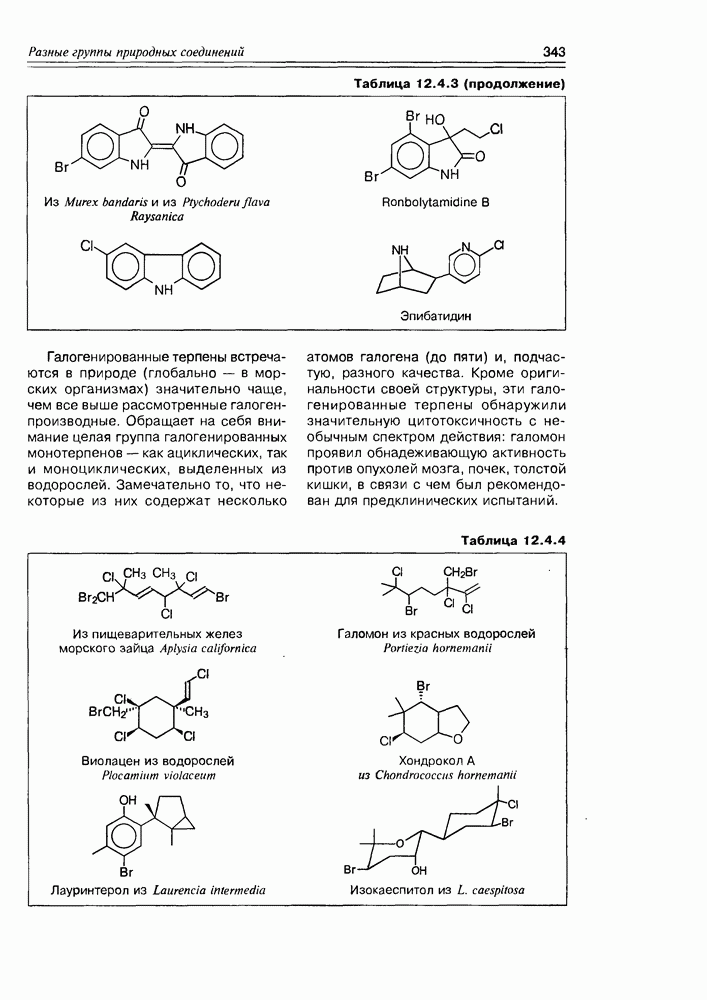
- 12.4. Элементорганические природные соединения
- Глава 13. МЕТАЛЛО-КОЭНЗИМЫ