| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
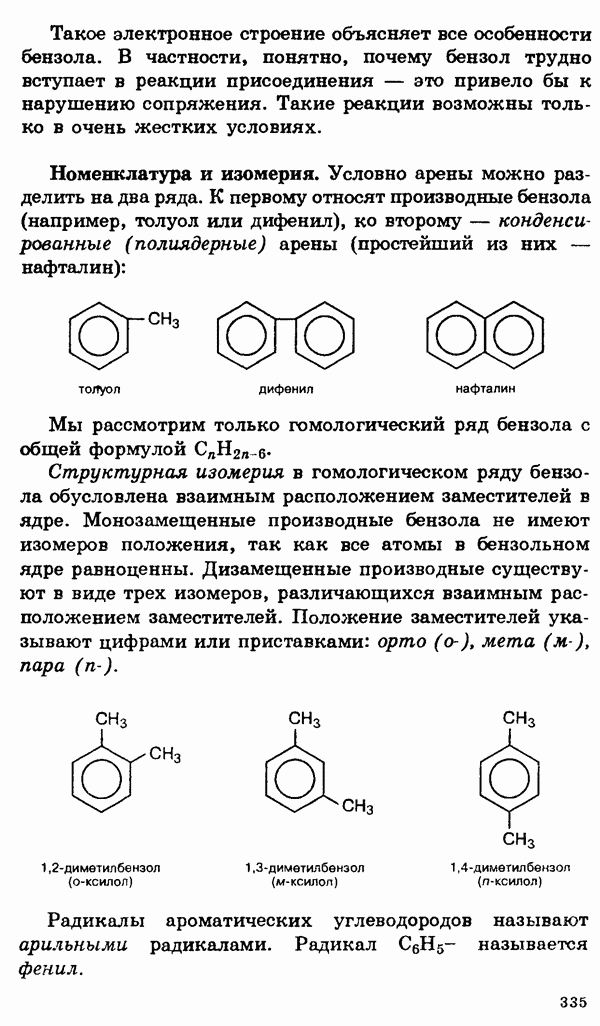
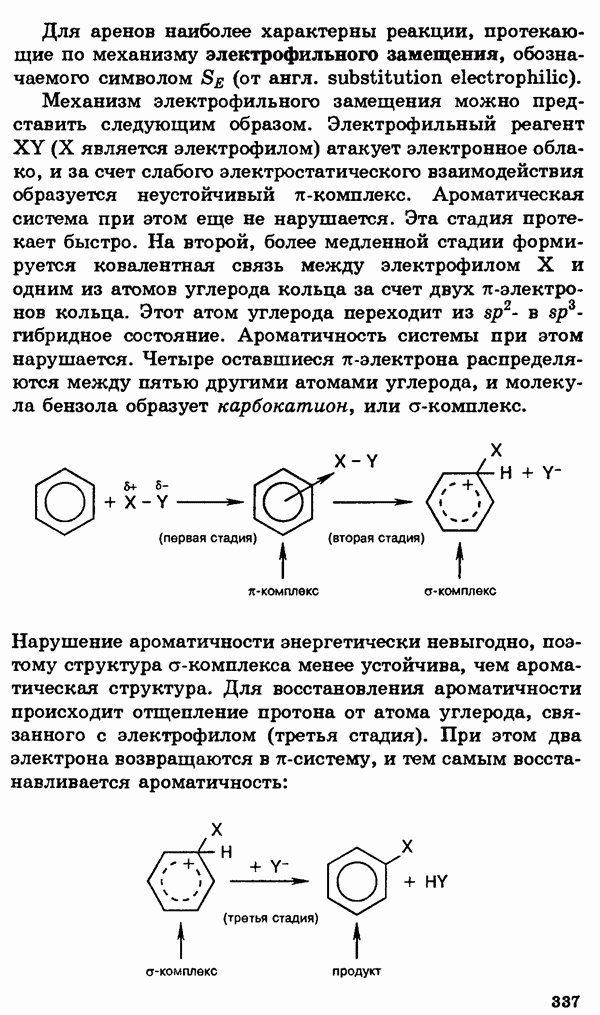
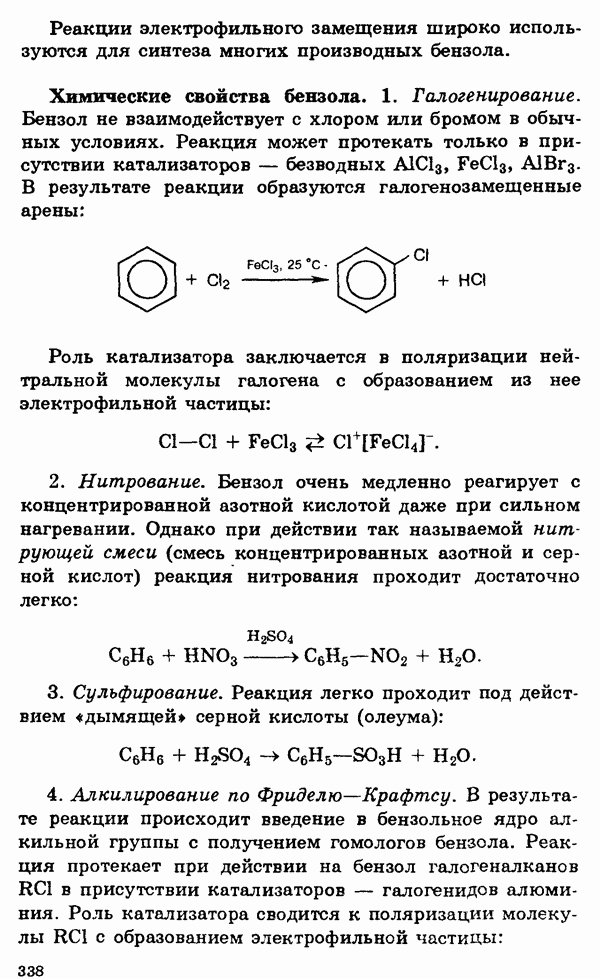
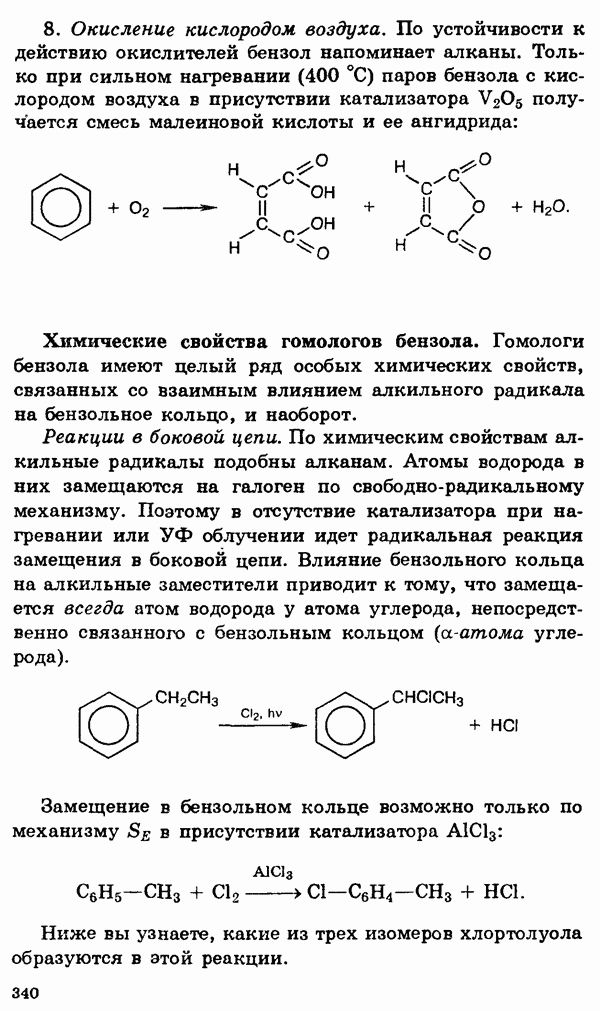
§ 13. Свойства s-элементов (щелочных и щелочноземельных металлов) и их соединений
Общее рассмотрение.
s-элементами называются элементы главных подгрупп I и II групп Периодической системы, а также гелий. Все они, кроме водорода и гелия, являются металлами. Металлы I группы называются щелочными, поскольку все они реагируют с водой, образуя щелочи. Металлы II группы, за исключением бериллия, принято называть щелочноземельными. Возникновение этого термина связано со старинным названием оксидов этих металлов — щелочные земли. Франций, завершающий I группу, и радий, завершающий II группу, являются радиоактивными элементами. Единственный природный изотоп  имеет малый период полураспада
имеет малый период полураспада  мин, поэтому о его химических свойствах известно не так уж много.
мин, поэтому о его химических свойствах известно не так уж много.
Все  -металлы имеют во внешней оболочке атомов по одному или два электрона. Эти металлы могут легко отдавать свои
-металлы имеют во внешней оболочке атомов по одному или два электрона. Эти металлы могут легко отдавать свои  -электроны, образуя ионы с устойчивыми электронными конфигурациями благородных газов.
-электроны, образуя ионы с устойчивыми электронными конфигурациями благородных газов.
Все s-металлы при обычных условиях находятся в твердом состоянии, ни один из них не образует аллотропных модификаций. Металлы I группы очень мягкие и имеют небольшую плотность по сравнению с другими металлами. Литий, натрий и калий легче воды и плавают на ее поверхности, реагируя с ней. Металлы II группы тверже, чем металлы I группы. Они имеют сравнительно более высокую плотность, хотя она гораздо меньше, чем у переходных металлов.
Химические свойства металлов.
Все  -металлы на свежем разрезе имеют блестящую поверхность, однако вступая в контакт с кислородом воздуха, они энергично окисляются и быстро тускнеют. Поэтому все s-металлы, за исключением бериллия и магния, приходится хранить под слоем керосина или жидкого парафина, чтобы воспрепятствовать их контакту с воздухом. Бериллий и магний образуют на поверхности защитный слой оксида и поэтому корродируют сравнительно медленно.
-металлы на свежем разрезе имеют блестящую поверхность, однако вступая в контакт с кислородом воздуха, они энергично окисляются и быстро тускнеют. Поэтому все s-металлы, за исключением бериллия и магния, приходится хранить под слоем керосина или жидкого парафина, чтобы воспрепятствовать их контакту с воздухом. Бериллий и магний образуют на поверхности защитный слой оксида и поэтому корродируют сравнительно медленно.
Все s-металлы горят в атмосфере воздуха, образуя оксиды одного или нескольких типов — нормальные оксиды состава  (I группа) и
(I группа) и  (II группа), пероксиды состава
(II группа), пероксиды состава  (I группа) и
(I группа) и  (II группа), супероксиды состава
(II группа), супероксиды состава  (I группа) и
(I группа) и  (II группа).
(II группа).
Например, только литий сгорает на воздухе с образованием оксида

а натрий образует смесь пероксида и супероксида

Оксиды натрия и калия могут быть получены только при соблюдении особых условий, например при нагревании смеси пероксида с избытком металла в отсутствие кислорода:

Все  -металлы I и II групп соединяются с водородом при нагревании, образуя гидриды, например:
-металлы I и II групп соединяются с водородом при нагревании, образуя гидриды, например:

Также все s-металлы при нагревании реагируют с галогенами, серой, азотом, фосфором и углеродом, образуя при этом галогениды

Все s-металлы I и II групп восстанавливают холодную воду до гидроксидов и водорода:

Их реакционная способность возрастает сверху вниз по группе. Так, литий реагирует с водой относительно медленно, тогда как калий реагирует с водой со взрывом, самопроизвольно загорается и горит фиолетовым пламенем на поверхности воды.
Активность металлов I и II групп по отношению к кислотам тоже возрастает сверху вниз по группе

Все щелочные металлы реагируют с кислотами со взрывом, поэтому в лабораториях такие реакции, как правило, не проводят.
Соединения s-металлов.
Выше было указано, что  -металлы образуют оксиды трех типов, которые обладают типичными основными свойствами. За исключением оксидов бериллия и магния, оксиды, пероксиды и супероксиды остальных элементов легко реагируют с водой, образуя сильно щелочные растворы, например:
-металлы образуют оксиды трех типов, которые обладают типичными основными свойствами. За исключением оксидов бериллия и магния, оксиды, пероксиды и супероксиды остальных элементов легко реагируют с водой, образуя сильно щелочные растворы, например:

Гидроксиды КОН и NaOH — важнейшие химические соединения щелочных металлов. В промышленности их получают электролизом растворов хлоридов.
При реакции щелочей с кислотами образуются соли:

Реакции такого типа называются реакциями нейтрализации.
Гидриды, нитриды, фосфиды и карбиды  -металлов реагируют с водой (см. § 9—12), например:
-металлов реагируют с водой (см. § 9—12), например:

а также с кислотами:

Обнаружение некоторых s-металлов по окрашиванию пламени.
Потенциалы (энергии) ионизации щелочных и щелочноземельных металлов очень малы, поэтому при внесении металла или его соединения в пламя горелки элемент легко ионизуется, окрашивая пламя в цвет, соответствующий его спектральной линии возбуждения. Желтый цвет пламени характерен для соединений натрия, фиолетовый — для соединений калия, кирпичнокрасный — для соединений кальция.
Рекомендуемая литература: [Кузьменко, 1977, гл. 17], [Третьяков, § 61—66], [Фримантл, т. 2, гл. 13], [Хомченко, 1993, гл. 13].
| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- Глава I. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ
- § 1. Предмет химии. Важнейшие понятия и законы химии
- Основные стехиометрические законы химии
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 2. Строение атома
- Электронные конфигурации атомов
- Ядро атома и радиоактивные превращения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 3. Строение молекул. Химическая связь. Валентность элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 4. Агрегатные состояния вещества
- Характерные свойства газов, жидкостей и твердых тел
- Газообразное состояние. Газовые законы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 5. Закономерности протекания химических реакций
- Химическая кинетика
- Химическое равновесие
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 6. Растворы. Электролитическая диссоциация. Гидролиз солей
- Электролиты и электролитическая диссоциация
- Гидролиз солей
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 7. Классификация химических реакций. Окислительно-восстановительные процессы. Электролиз
- Окислительно-восстановительные реакции
- Электролиз
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
- § 8. Номенклатура, классификация неорганических веществ. Свойства и способы получения
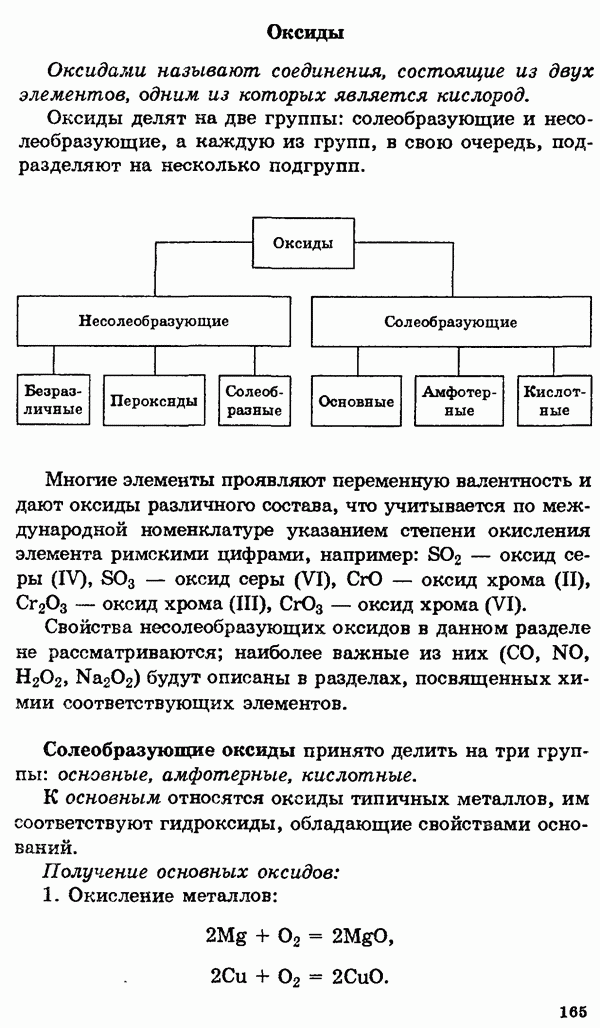
- Оксиды
- Основания (гидроксиды металлов)
- Кислоты
- Соли
- § 9. Водород. Галогены и их соединения
- Галогены и их соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 10. Подгруппа кислорода
- Сера и ее соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 11. Подгруппа азота
- Фосфор и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 12. Подгруппа углерода
- Углерод и его соединения
- Кремний и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 13. Свойства s-элементов (щелочных и щелочноземельных металлов) и их соединений
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 14. Алюминий — типичный р-металл
- Соединения алюминия и их свойства
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 15. Главные переходные металлы (d-элементы) и их соединения
- Химические свойства d-элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 16. Задачи для повторения по неорганической химии
- Глава III. ОРГАНИЧЕСКАЯ ХИМИЯ
- § 17. Основные понятия и закономерности в органической химии. Предмет органической химии
- Классификация и номенклатура органических соединений
- Изомерия органических соединений
- Взаимное влияние атомов в молекуле и реакционная способность органических соединений
- Общая характеристика органических реакций
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 18. Предельные (насыщенные) углеводороды
- Циклоалканы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 19. Алкены. Диеновые углеводороды
- Диеновые углеводороды (алкадиены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 20. Алкины
- ЗАДАЧИ И УПРАЖНЕНИЯ
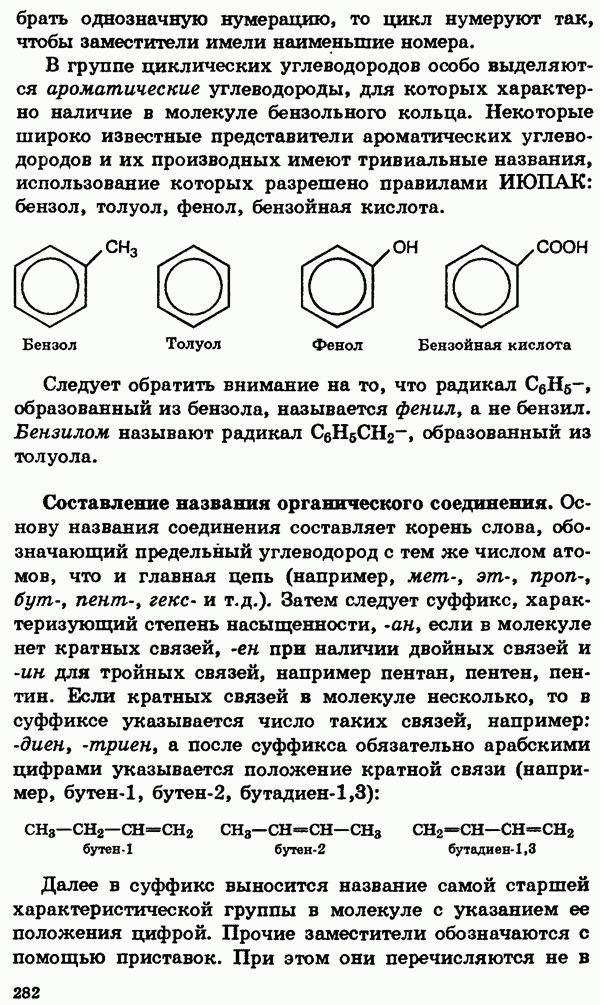
- § 21. Ароматические углеводороды (арены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 22. Спирты и фенолы
- Многоатомные спирты
- Фенолы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 23. Карбонильные соединения — альдегиды и кетоны
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 24. Карбоновые кислоты. Сложные эфиры. Жиры
- Сложные эфиры. Жиры
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава 4. ОСНОВНЫЕ ПРИЕМЫ РЕШЕНИЯ ЗАДАЧ
- Определение молекулярной формулы веществ
- Определение состава и разделение смесей
- Задачи на газовые законы
- Способы выражения концентрации растворов
- Ионные реакции в растворах
- Задачи на окислительно-восстановительные реакции
- Разные задачи
- ПРОГРАММА ПО ХИМИИ ДЛЯ ПОСТУПАЮЩИХ В УНИВЕРСИТЕТЫ
- ОТВЕТЫ
- Рекомендуемая литература