| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
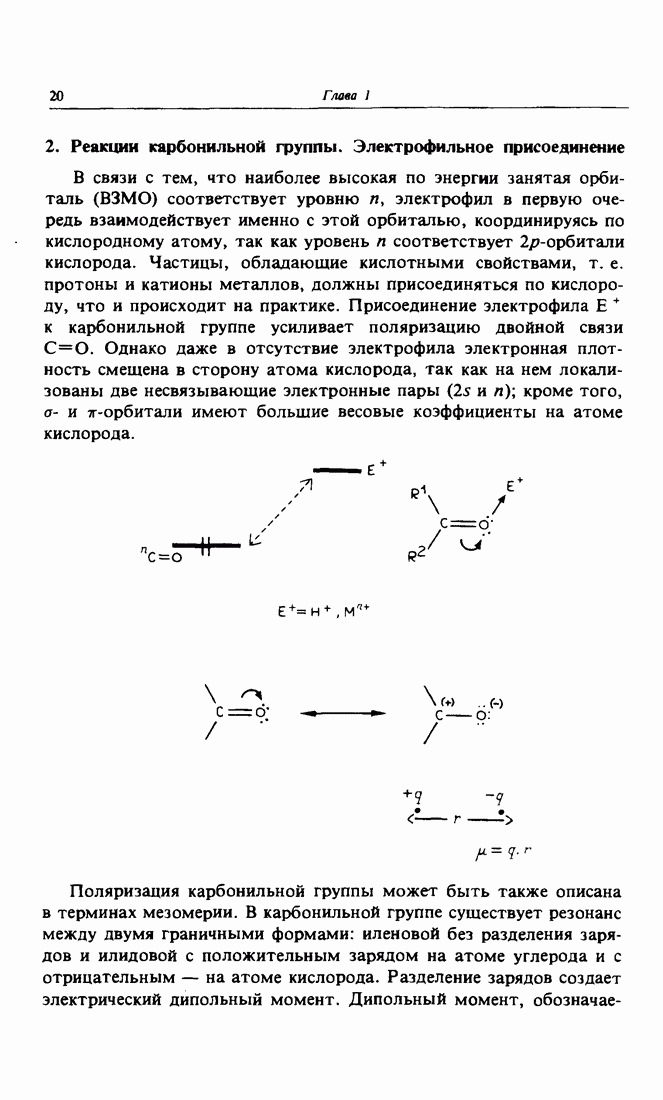
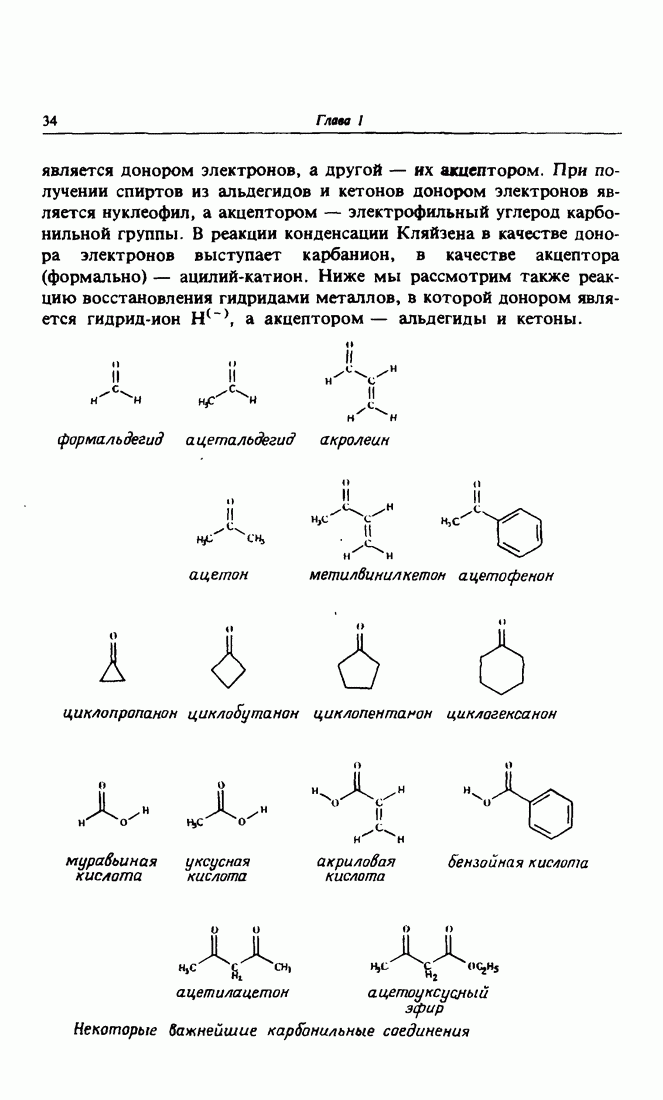
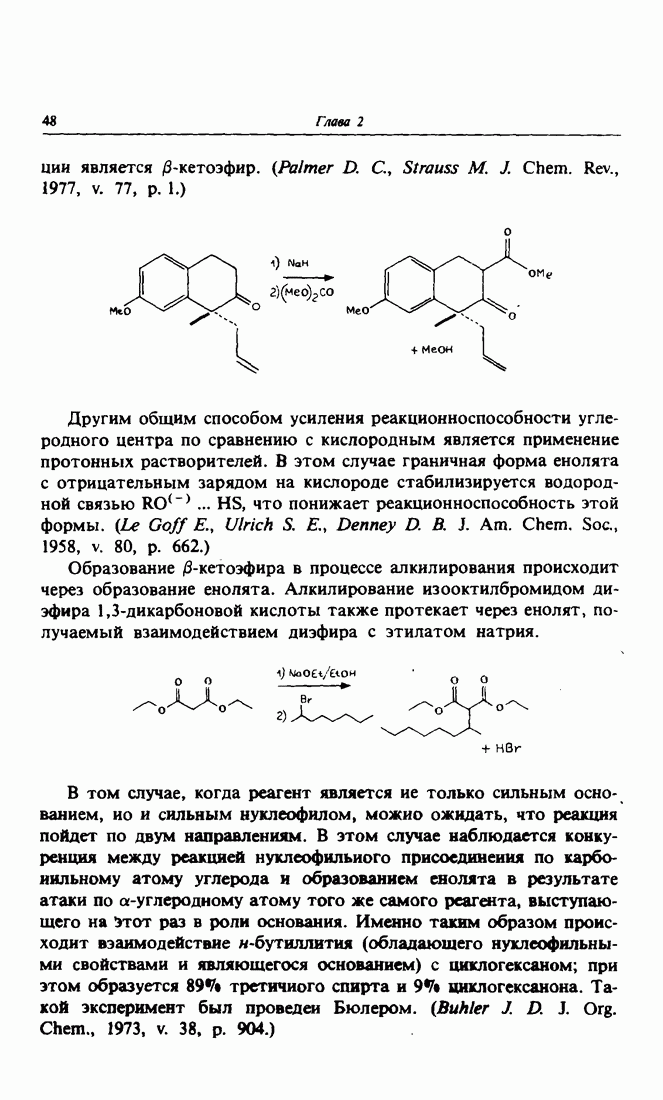
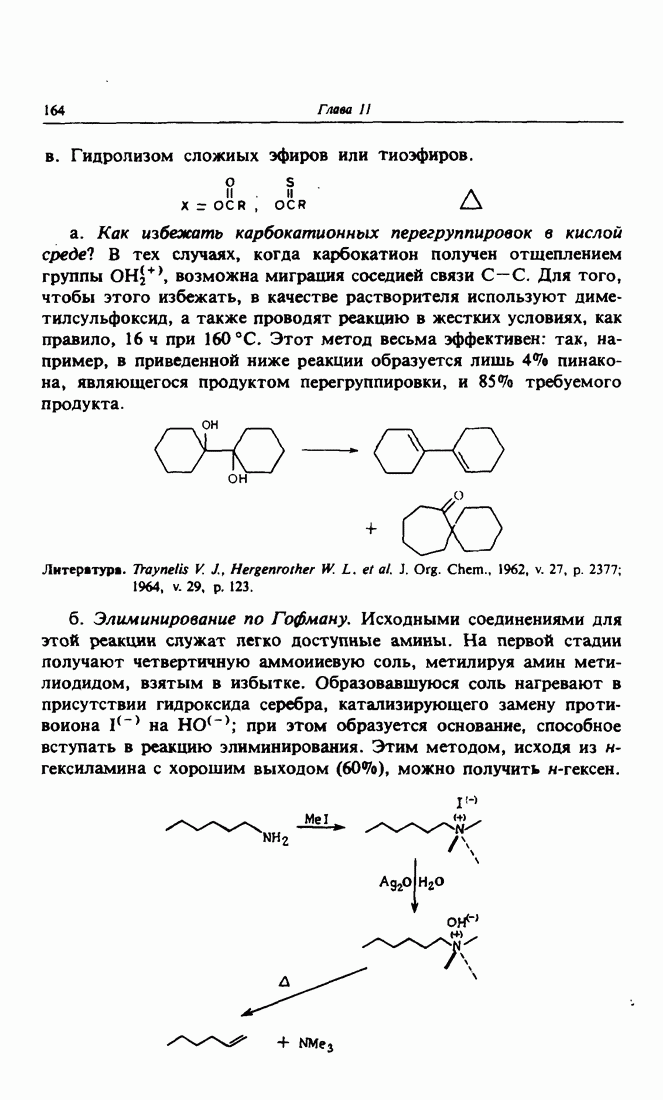
2. Реакции карбонильной группы. Электрофильное присоединение
В связи с тем, что наиболее высокая по энергии занятая орбиталь  соответствует уровню
соответствует уровню  электрофил в первую очередь взаимодействует именно с этой орбиталью, координируясь по кислородному атому, так как уровень
электрофил в первую очередь взаимодействует именно с этой орбиталью, координируясь по кислородному атому, так как уровень  соответствует
соответствует  -орбитали кислорода. Частицы, обладающие кислотными свойствами,
-орбитали кислорода. Частицы, обладающие кислотными свойствами,  протоны и катионы металлов, должны присоединяться по кислороду, что и происходит на практике. Присоединение электрофила
протоны и катионы металлов, должны присоединяться по кислороду, что и происходит на практике. Присоединение электрофила  к карбонильной группе усиливает поляризацию двойной связи
к карбонильной группе усиливает поляризацию двойной связи  Однако даже в отсутствие электрофила электронная плотность смещена в сторону атома кислорода, так как на нем локализованы две несвязывающие электронные пары
Однако даже в отсутствие электрофила электронная плотность смещена в сторону атома кислорода, так как на нем локализованы две несвязывающие электронные пары  ил); кроме того,
ил); кроме того,  и
и  -орбитали имеют большие весовые коэффициенты на атоме кислорода.
-орбитали имеют большие весовые коэффициенты на атоме кислорода.
(см. скан)
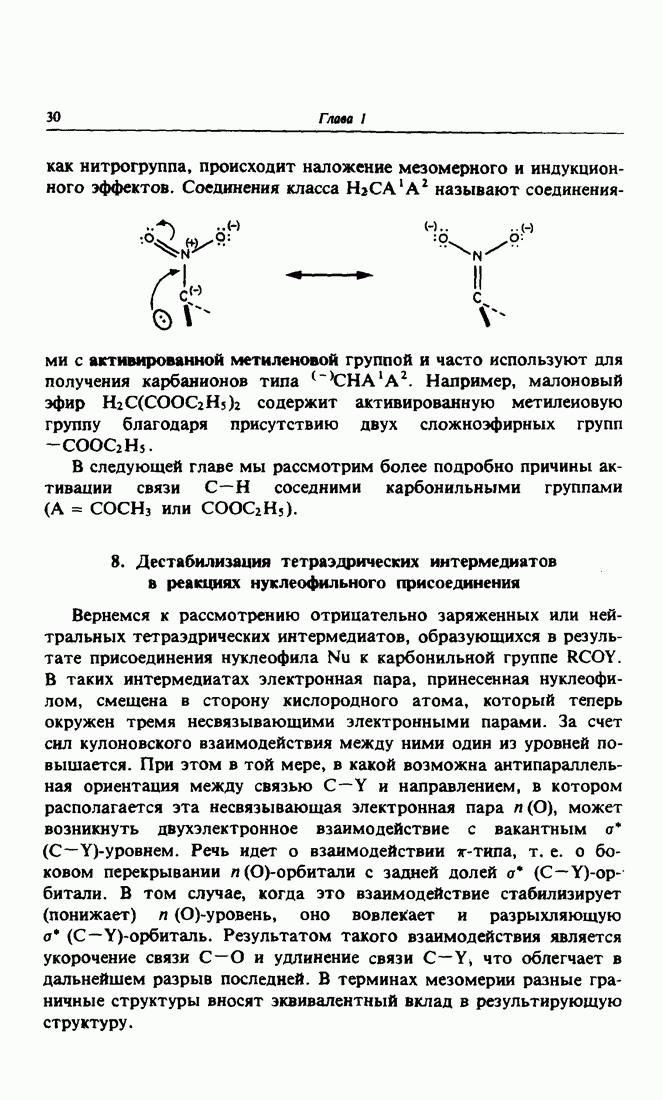
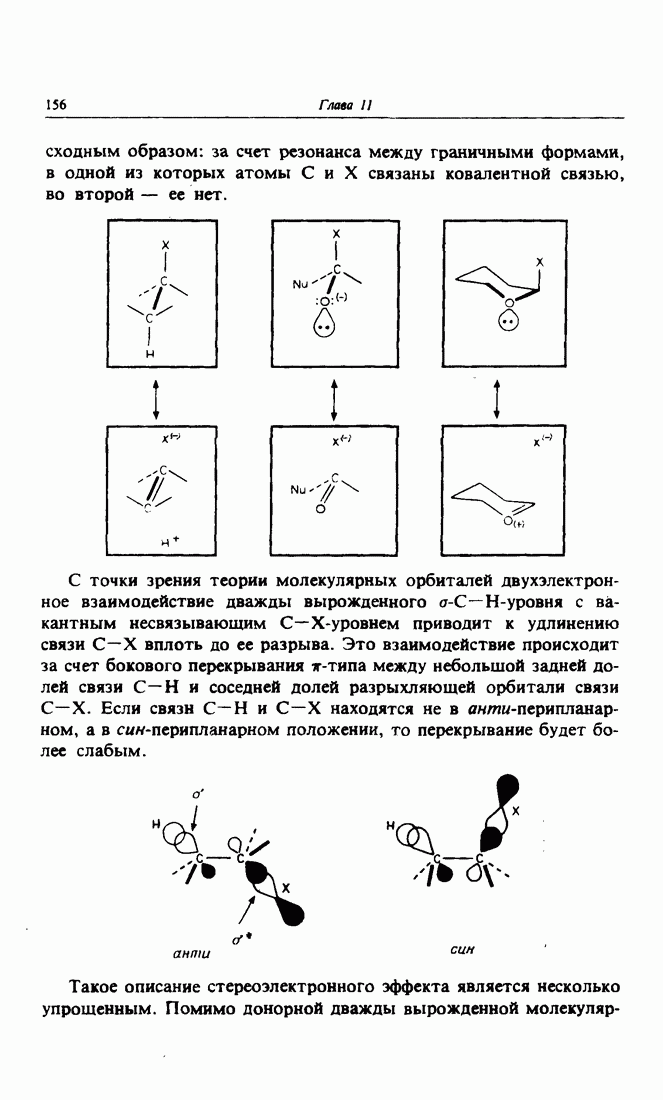
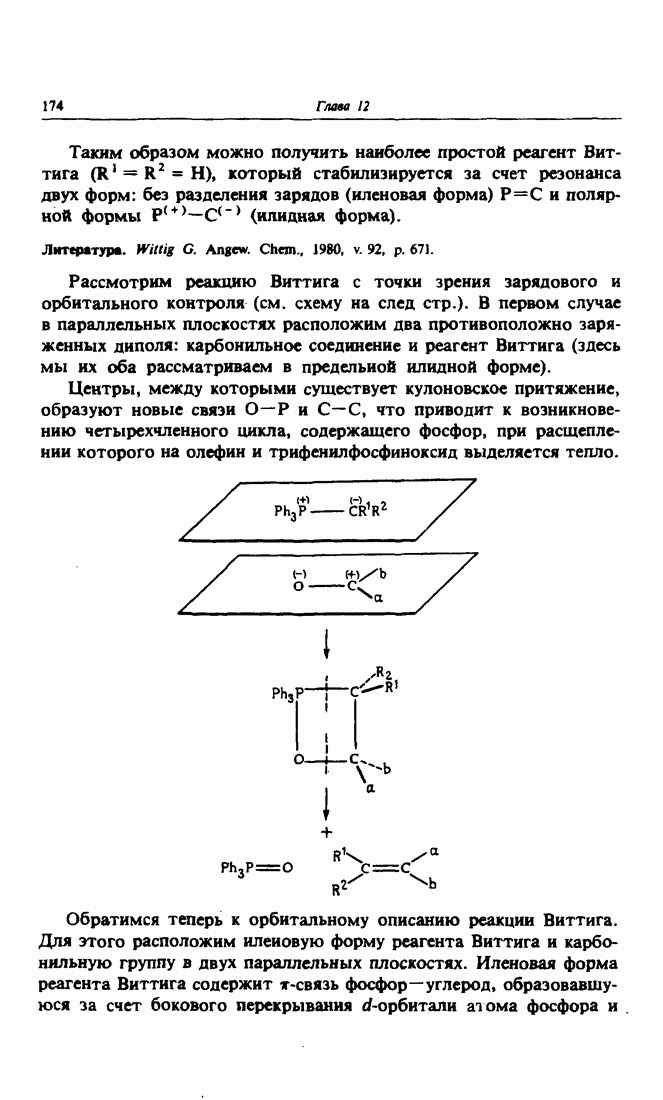
Поляризация карбонильной группы может быть также описана в терминах мезомерии. В карбонильной группе существует резонанс между двумя граничными формами: иленовой без разделения зарядов и илидовой с положительным зарядом на атоме углерода и с отрицательным — на атоме кислорода. Разделение зарядов создает электрический дипольный момент. Дипольный момент,
обозначаемый буквой  можно представить как произведение абсолютной величины зарядов
можно представить как произведение абсолютной величины зарядов  на расстояние
на расстояние  между ними. Для альдегидов и кетонов дипольный момент составляет приблизительно
между ними. Для альдегидов и кетонов дипольный момент составляет приблизительно  (Дебай), что соответствует
(Дебай), что соответствует  Поскольку длина связи
Поскольку длина связи  равна 1,20 А, величина заряда на каждом полюсе,
равна 1,20 А, величина заряда на каждом полюсе,  на атомах углерода: и кислорода, составляет от 1/3 до 3/4 заряда электрона, что представляет собой весьма значительную величину.
на атомах углерода: и кислорода, составляет от 1/3 до 3/4 заряда электрона, что представляет собой весьма значительную величину.
За счет диполь-дипольного взаимодействия в конденсированной фазе происходит взаимное притяжение молекул, содержащих карбонильную группу. В результате карбонильные соединения имеют более высокие температуры плавления и кипения по сравнению с углеводородами, содержащими такое же число углеродных атомов. При комнатной температуре эти вещества представляют собой жидкости, способные растворять другие полярные вещества, например некоторые соли. Так, ацетон  является одним из наиболее распространенных растворителей.
является одним из наиболее распространенных растворителей.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА
- ВВЕДЕНИЕ
- 1. Орбитальный и зарядовый контроль
- 2. Жесткие и мягкие кислоты и основания
- 3. Термохимические данные и их применение
- Глава 1. КАРБОНИЛЬНАЯ ГРУППА. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ПРИСОЕДИНЕНИЯ-ФРАГМЕНТАЦИИ
- 1. Карбонильная группа. Простое орбитальное описание
- 2. Реакции карбонильной группы. Электрофильное присоединение
- 3. Основность и нуклеофильность
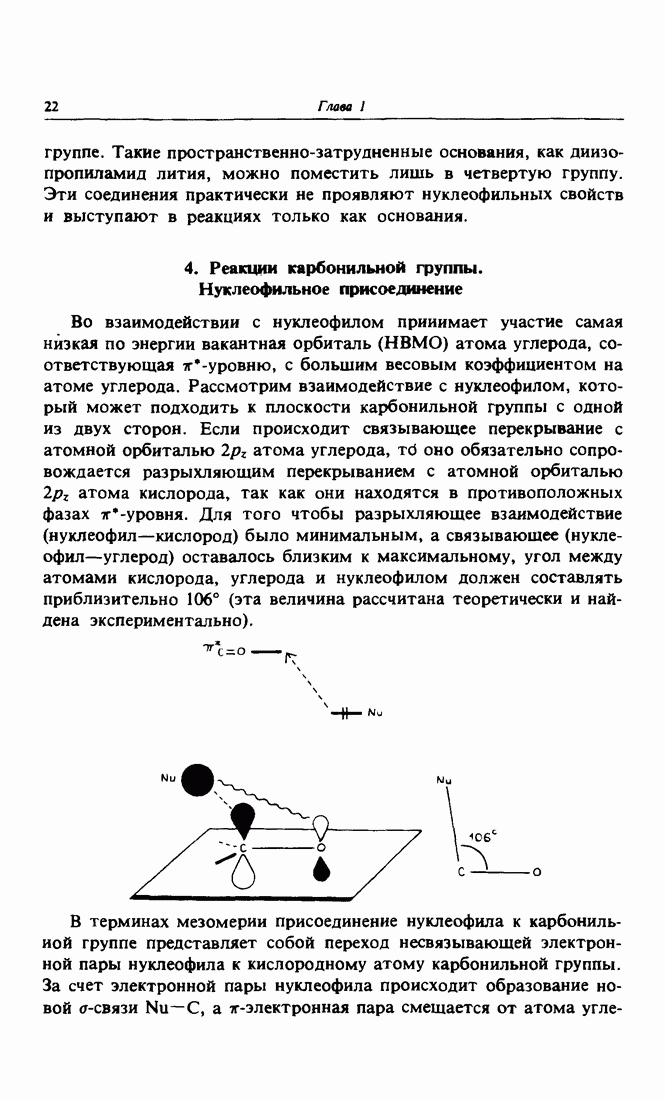
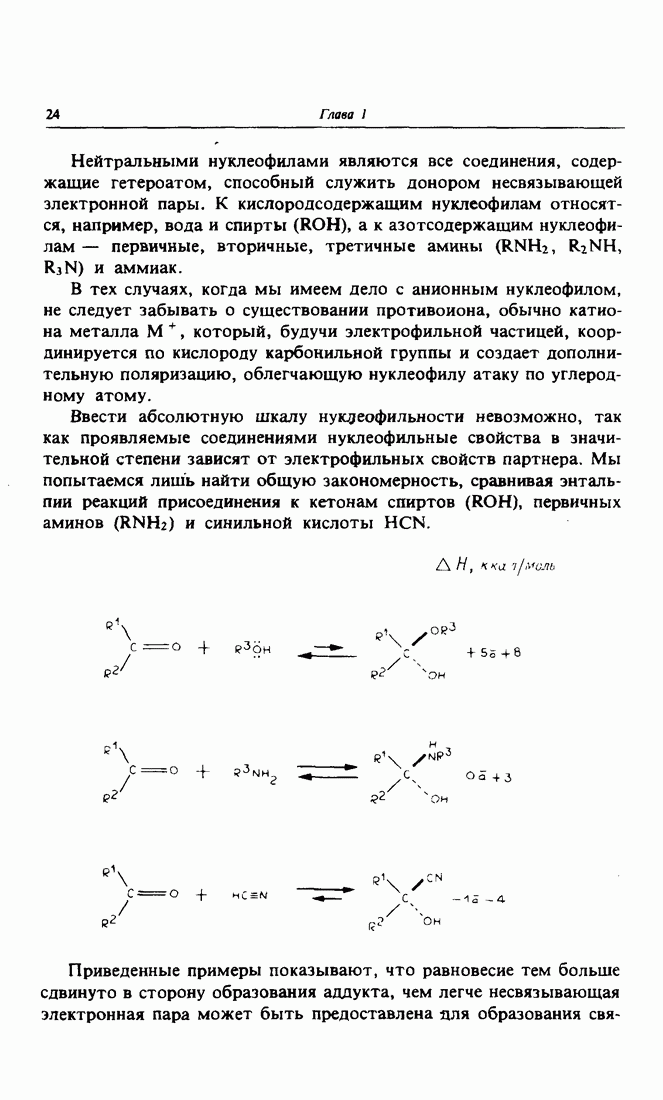
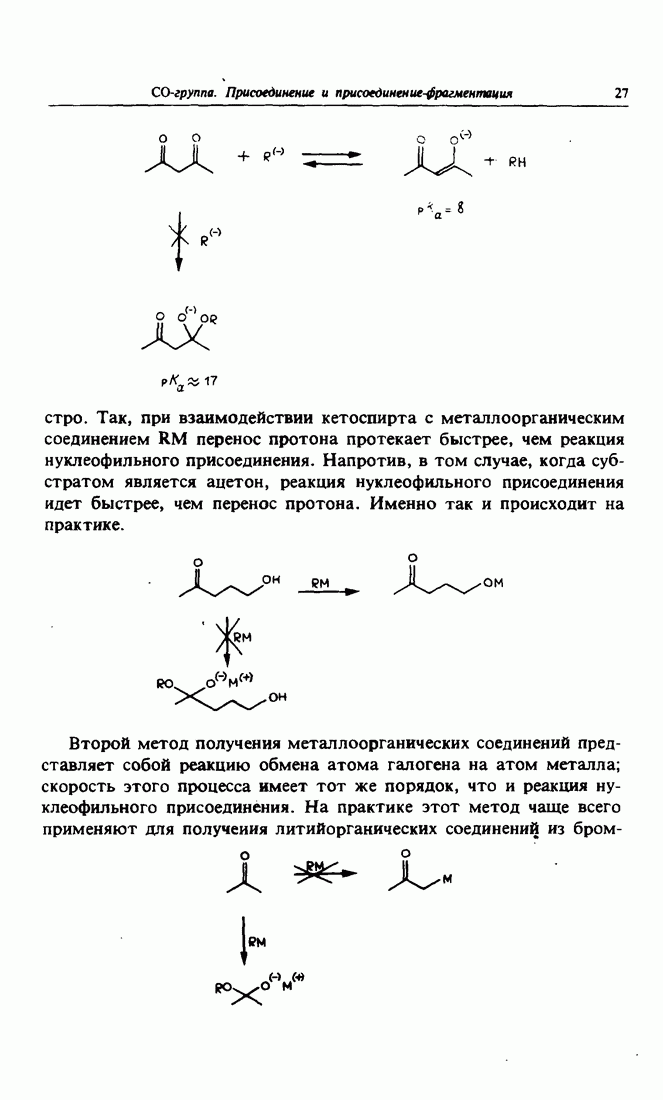
- 4 Реакции карбонильной группы. Нуклеофильное присоединение
- 5. Защита и регенерация
- 6. Получение различных металлоорганических производных
- 7. Активированная метиленовая группа
- 8. Дестабилизация тетраэдрических интермедиатов в реакциях нуклеофильного присоединения
- 9. Реакции присоединения-фрагментации
- 10. Восстановление гидридами металлов
- 11. Описание конфигурации асимметрического атома углерода
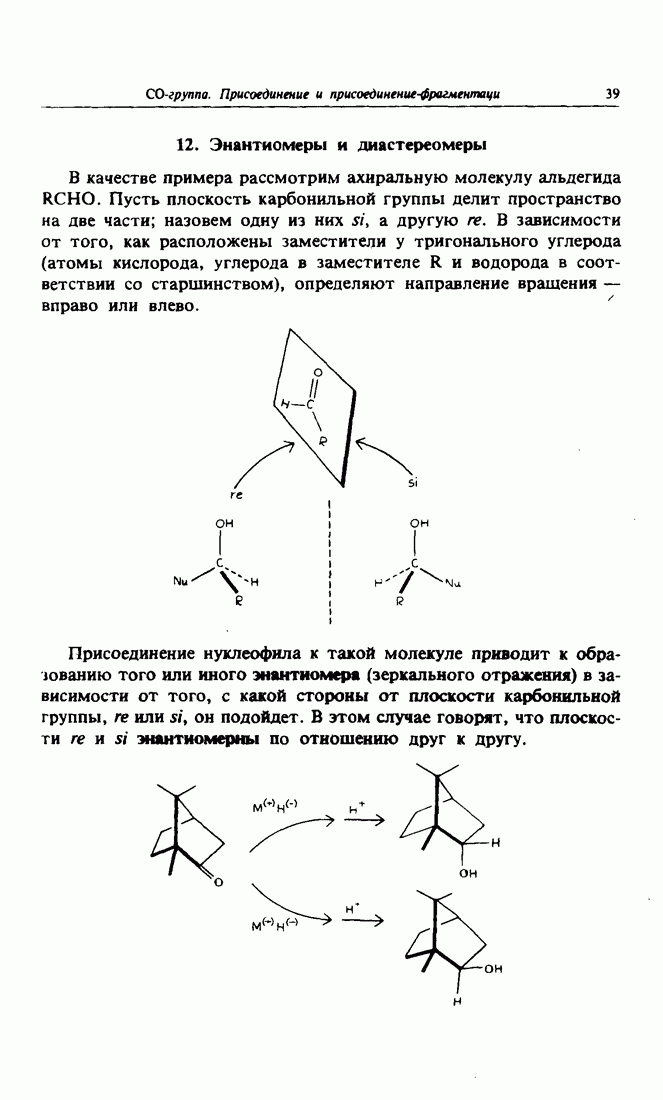
- 12. Энантиомеры и диастереомеры
- 13. Асимметрическая 1,2-индукция
- Глава 2. КАРБОНИЛЬНАЯ ГРУППА. ЕНОЛИЗАЦИЯ. КОНДЕНСАЦИЯ ПО МИХАЭЛЮ
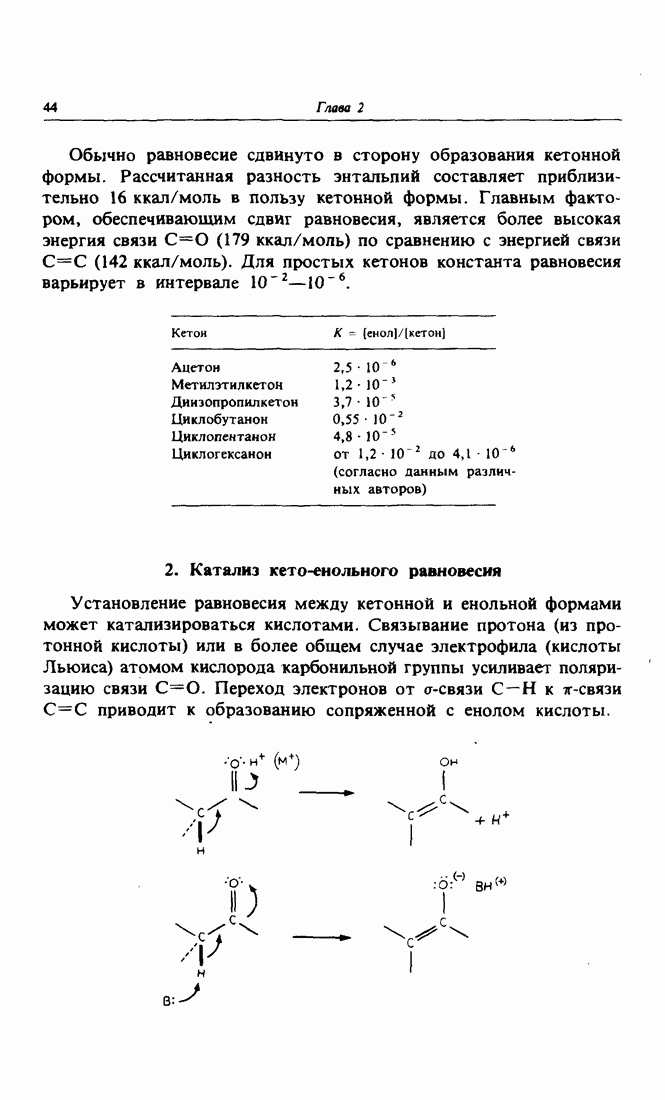
- 1. Кето-енольное равновесие
- 2. Катализ кето-енольного равновесия
- 3. Стереохимия и реакция енолнэации
- 4. Причины ослабления связи Ca-H в кетонах
- 5. Еноляты и их получение
- 6. Эфиры енолов
- 7. Конфигурация енолов и эфиров енолов
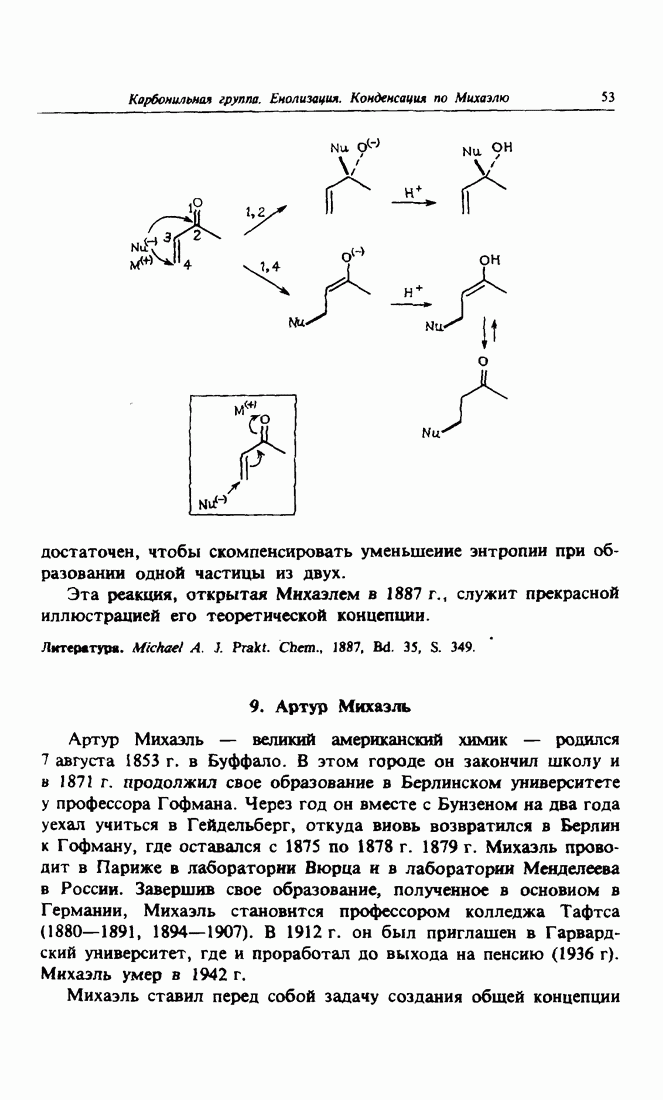
- 8. Реакция Михаэля
- 9. Артур Михаэль
- 10. Региоселективность в реакции Михаэля
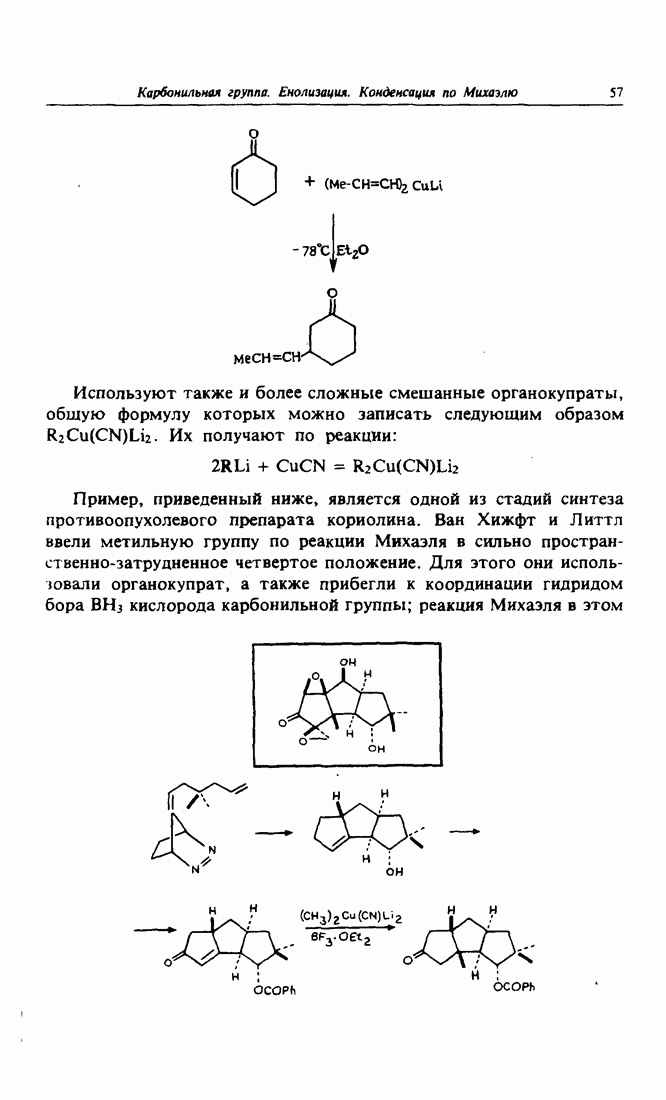
- 11. Применение органокулратов
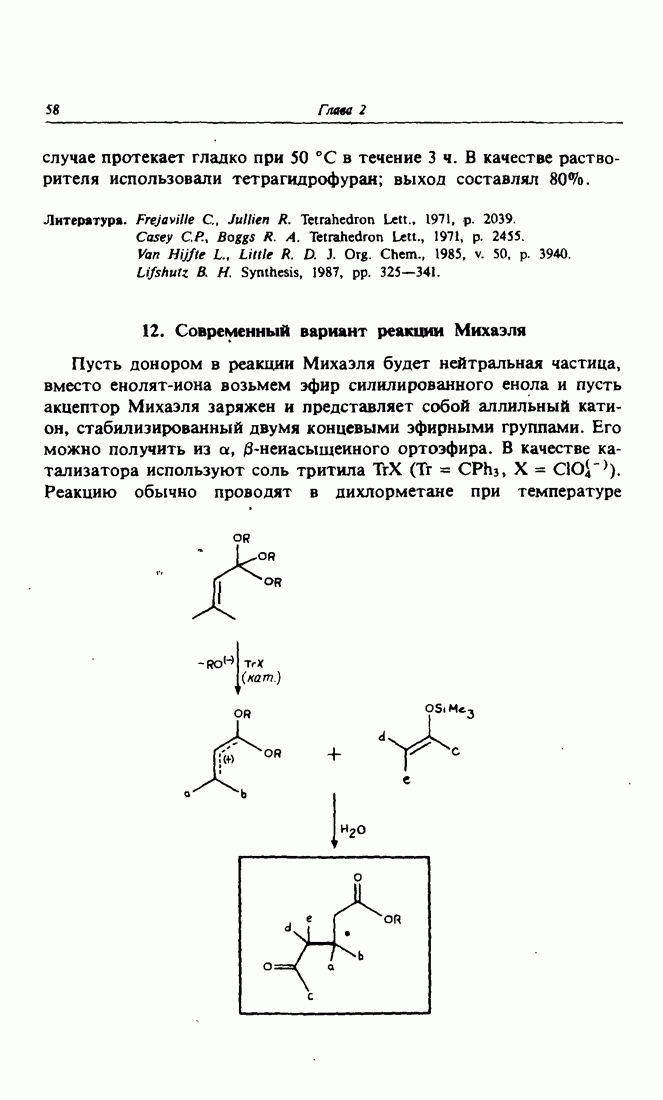
- 12. Современный вариант реакции Михаэля
- 13. Сопряжение или отсутствие сопряжения?
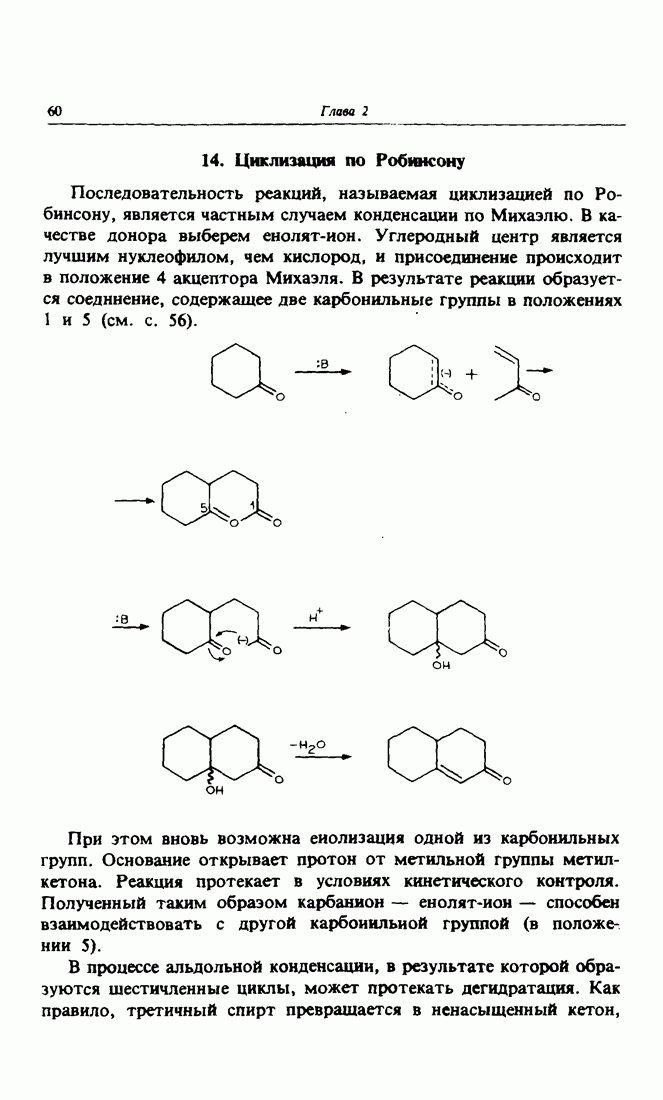
- 14. Циклизация по Робинсону
- 15. Сэр Роберт Робинсон
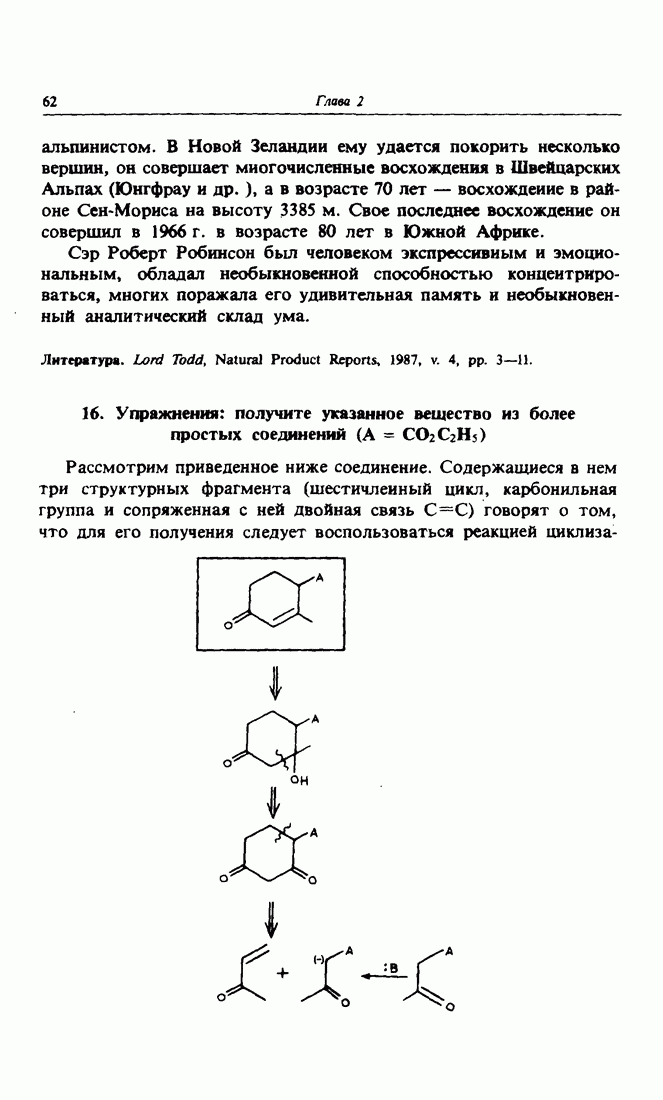
- 16. Упражнения: получите указанное вещество из более простых соединений (A=CO2C2H5)
- Глава 3. КАРБОНИЛЬНАЯ ГРУППА. АЛЬДОЛЬНАЯ КОНДЕНСАЦИЯ
- 2. Устойчивость продуктов альдольиой конденсации
- 3. Управление реакцией альдольной конденсации: доноры и акцепторы
- 4. Управление реакцией альдольной конденсации: син- и анти-диастереомеры
- 5. Стереоселективные реакции альдольной конденсации
- Глава 4. НЕКОТОРЫЕ РЕШЕНИЯ ПРОБЛЕМЫ СЕЛЕКТИВНОСТИ (ХИМИЧЕСКАЯ, РЕГИО- И СТЕРЕОСЕЛЕКТИВНОСТЬ)
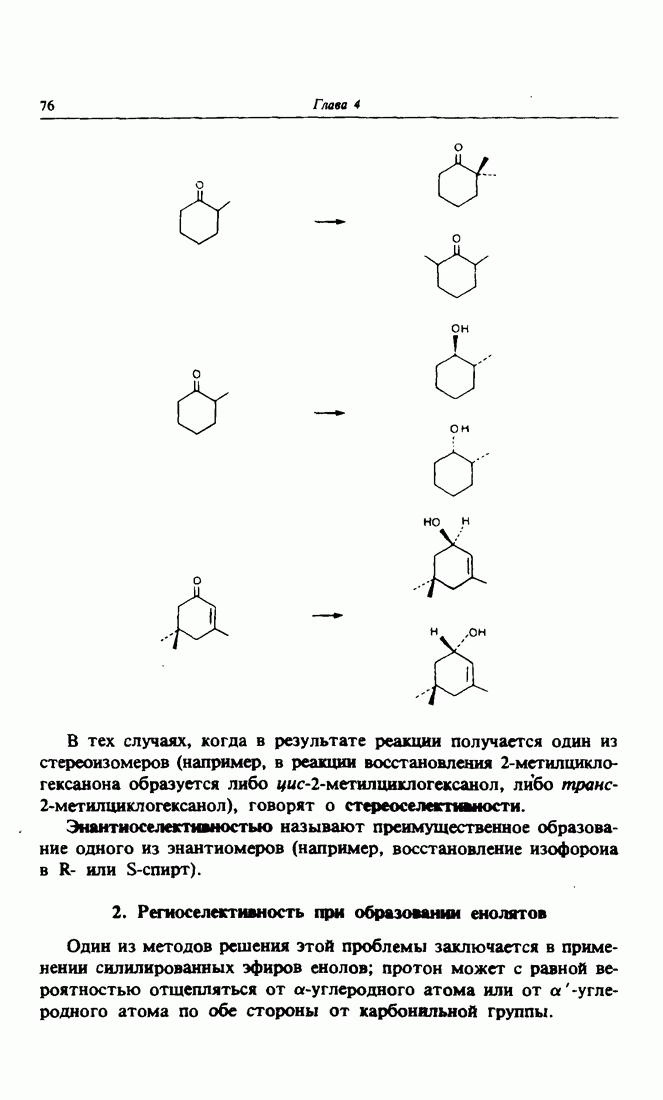
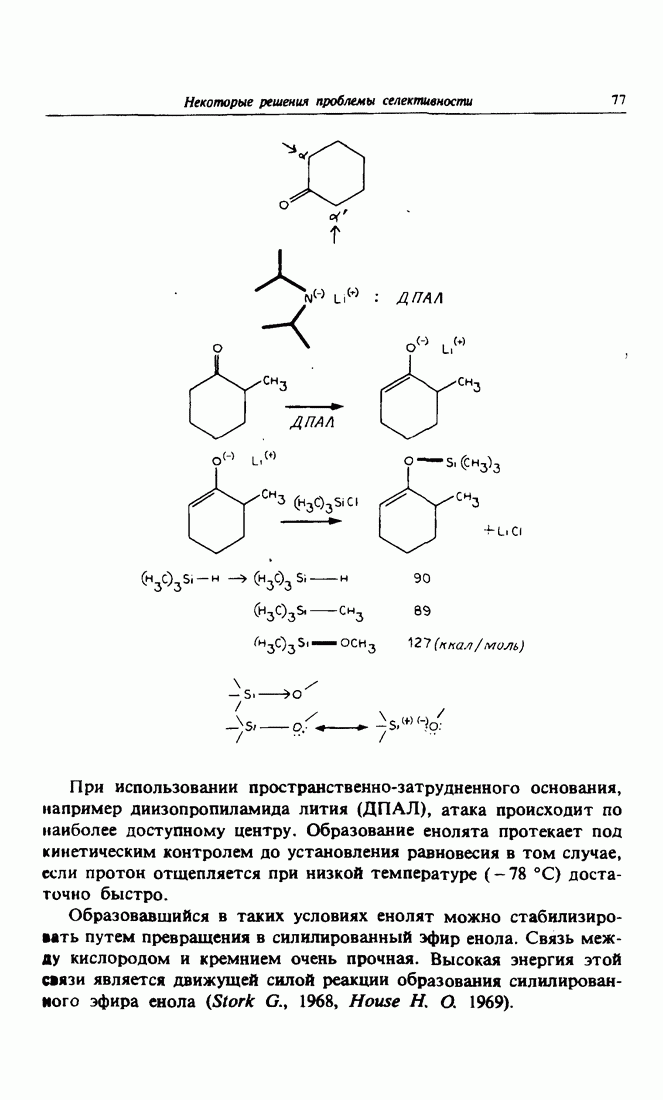
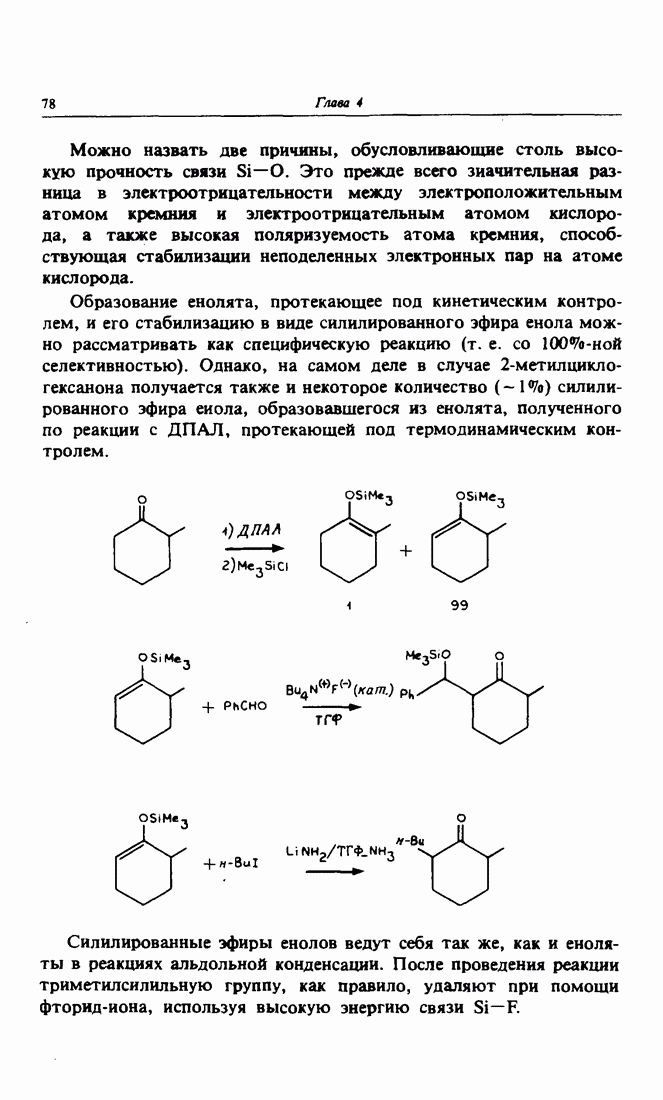
- 2. Региоселективность при образовании енолятов
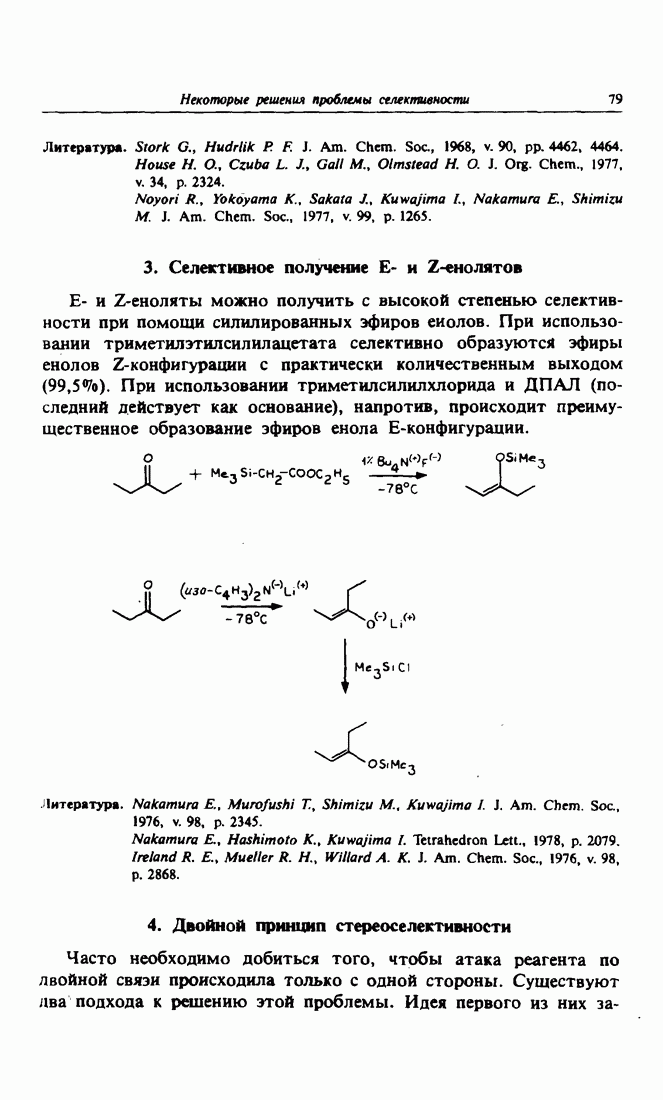
- 3. Селективное получение Е- и Z-енолятов
- 4. Двойной принцип стереоселективности
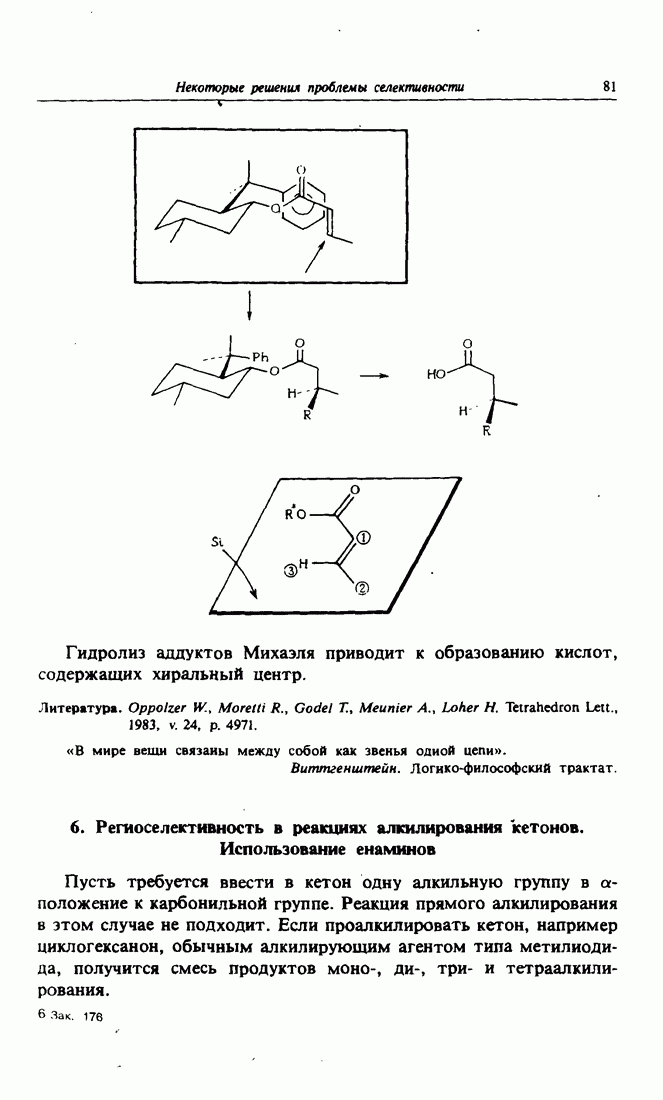
- 5. Энантиоселективная реакция Михаэля
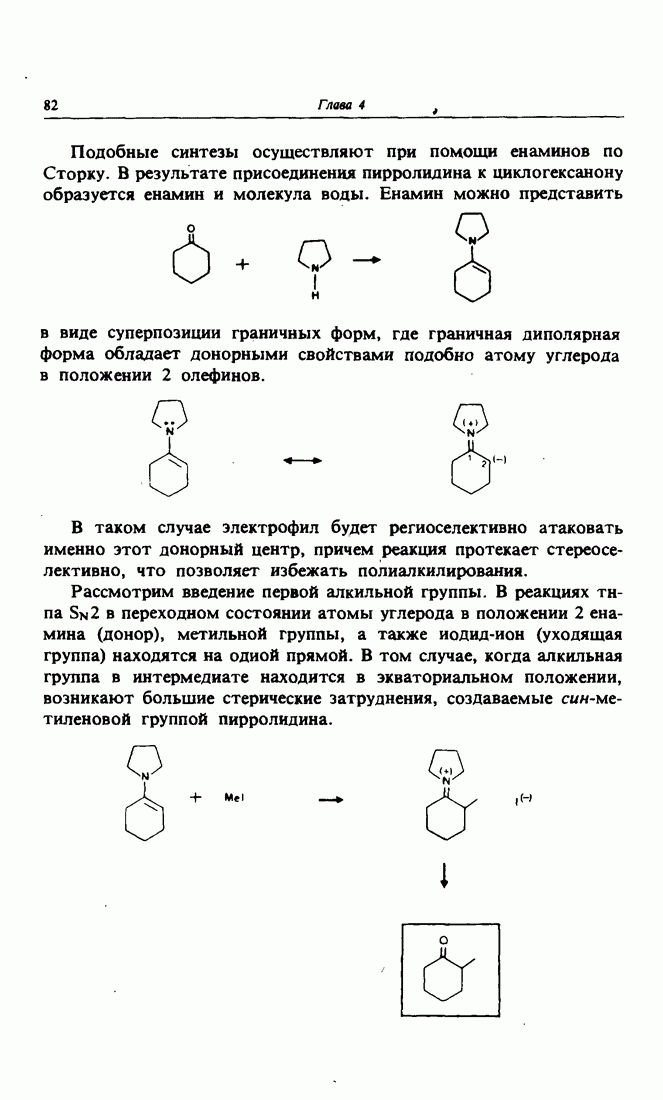
- 6. Региоселективность в реакциях алкилирования кетонов. Использование енаминов
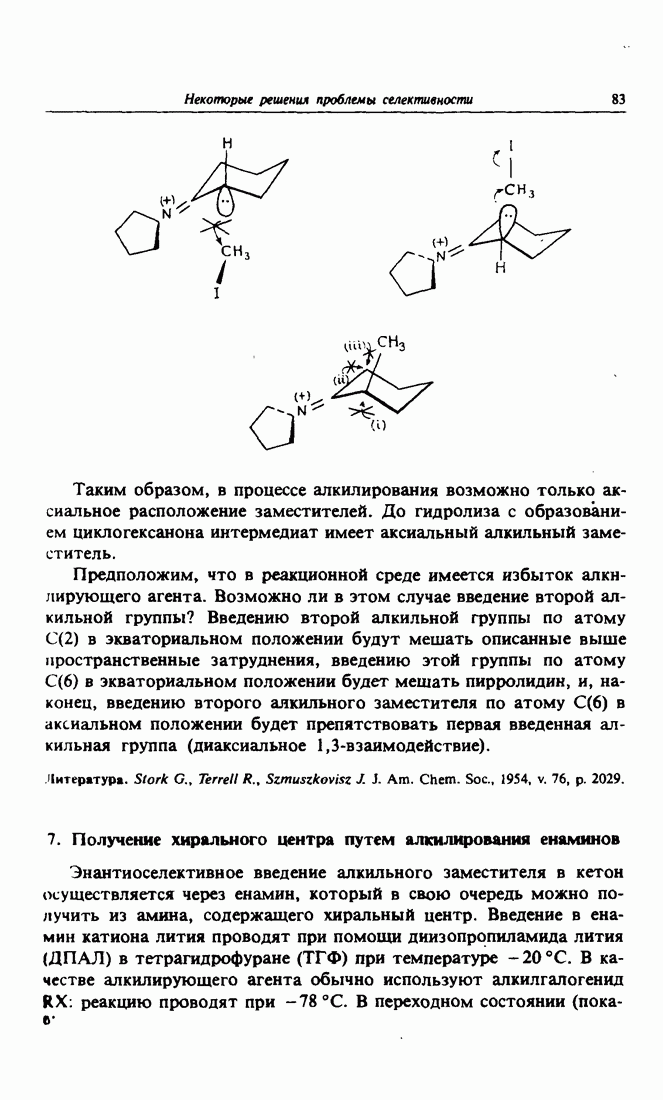
- 7. Получение хирального центра путем алкилирования енаминов
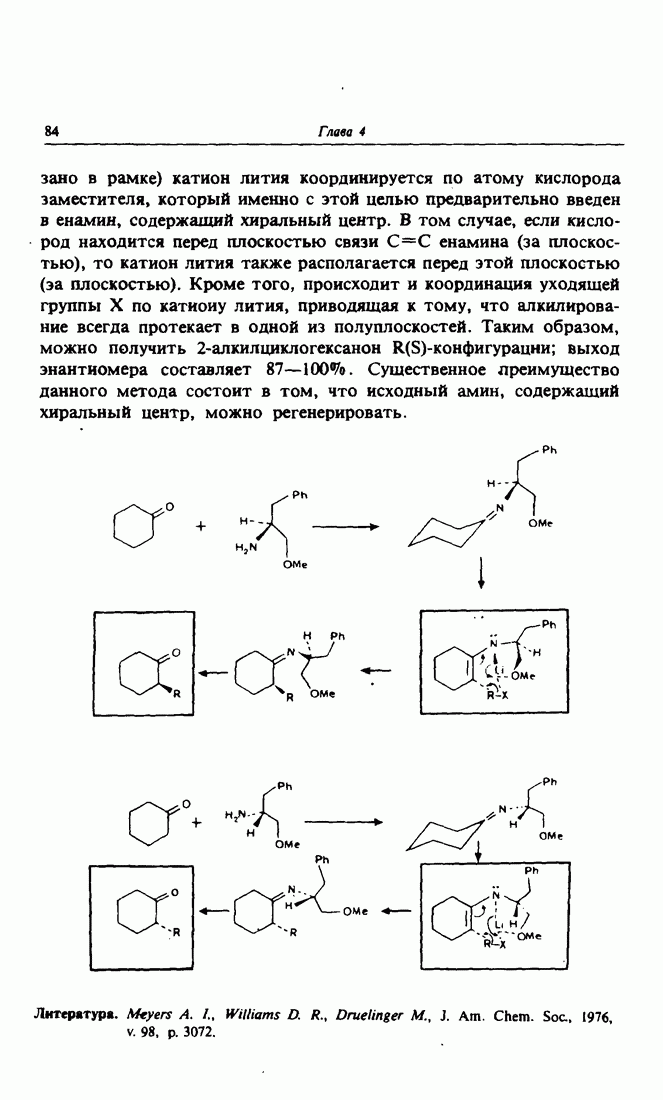
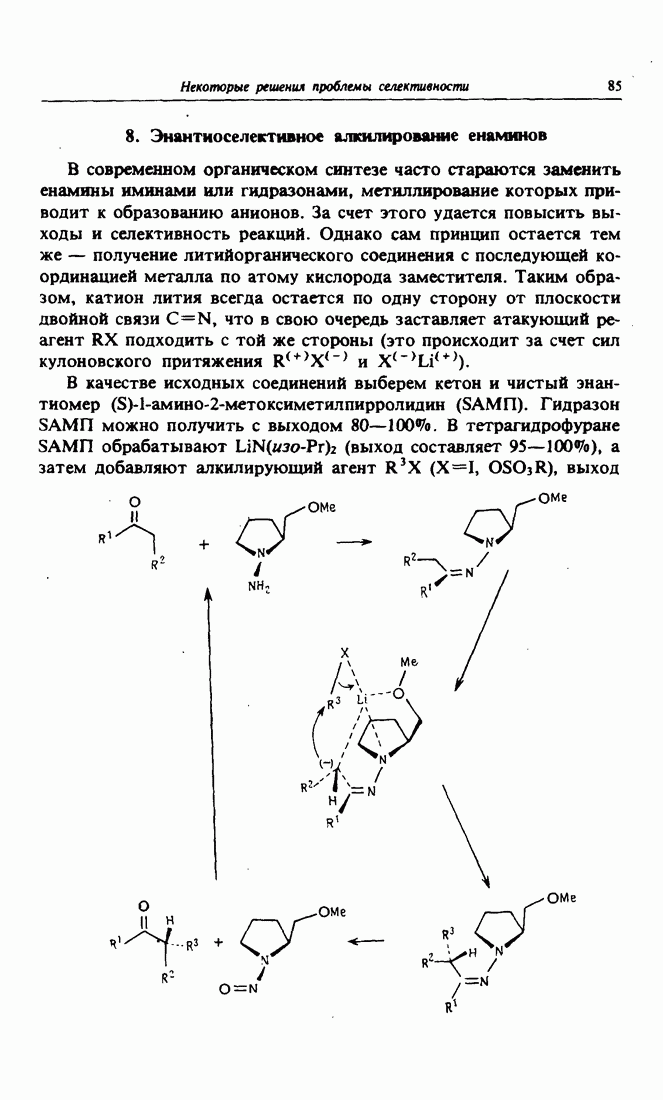
- 8. Энантиоселективное алкилирование енаминов
- 9. Перенос хиральности
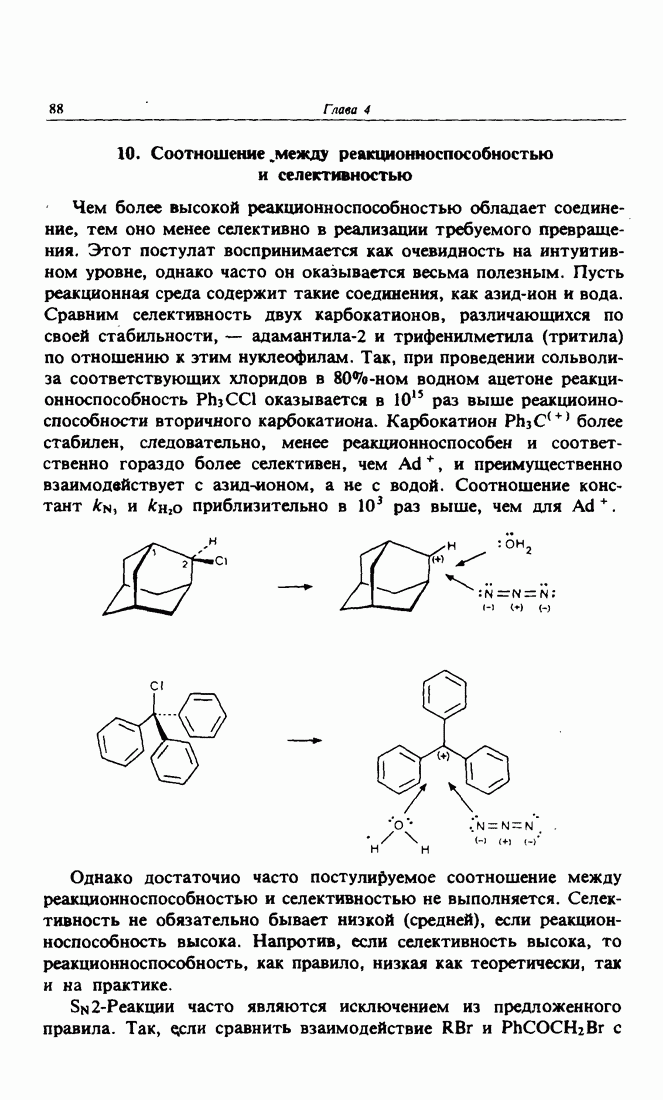
- 10. Соотношение между реакционноспособностью и селективностью
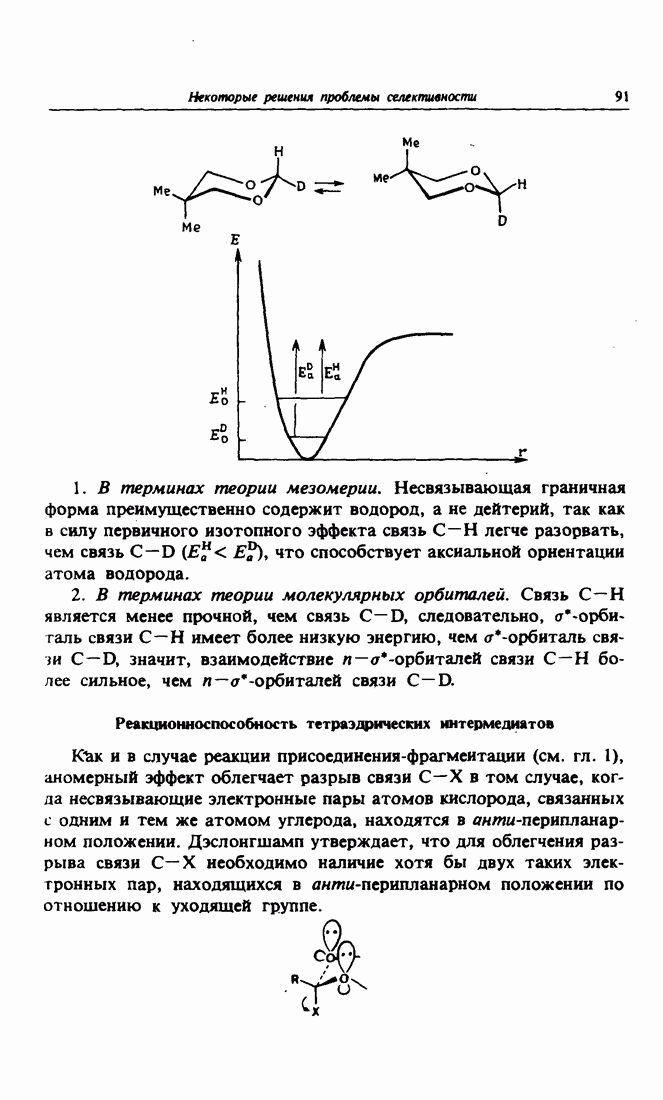
- 11. Стереоэлектронный эффект
- 12. Конформации переходного состояния «кресло» и «ванна»
- Глава 5. ЗАЩИТА И РЕГЕНЕРАЦИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП. СПИРТОВАЯ И КАРБОНИЛЬНАЯ ГРУППЫ. ОБРАЩЕНИЕ ПОЛЯРНОСТИ
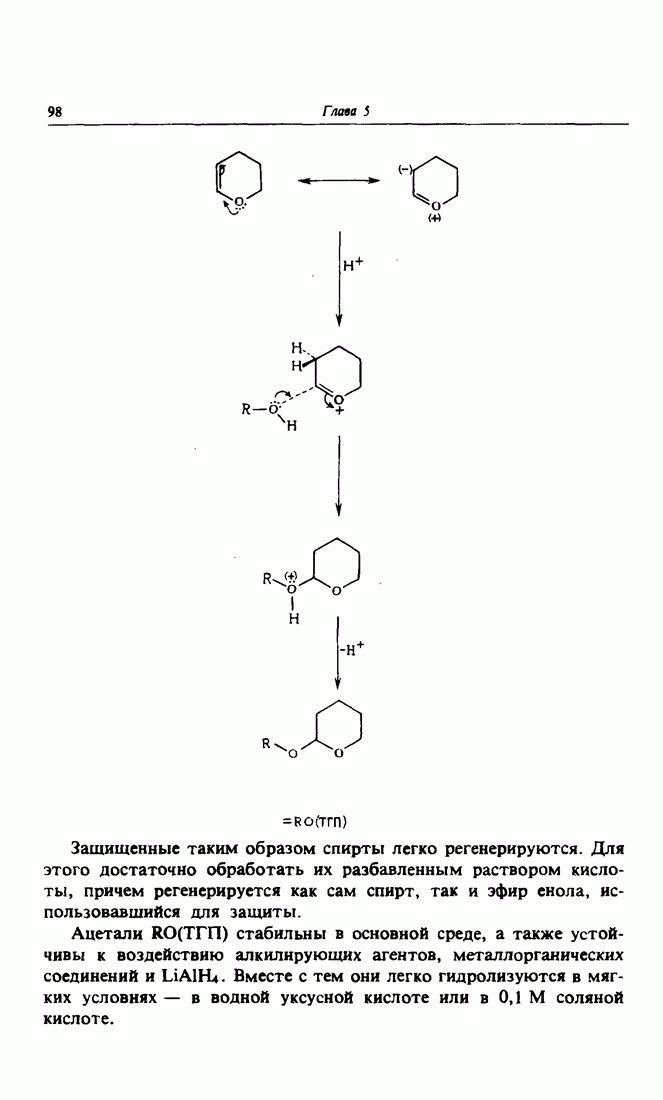
- 1. Защита карбонильной группы ацетальной
- 2. Защита спиртов. Диметил-трет-бутилсилиловые эфиры
- 3. Защита спиртовых групп при помощи эфиров енолов
- 4. Обращение полярности
- 5. Э. Дж. Кори
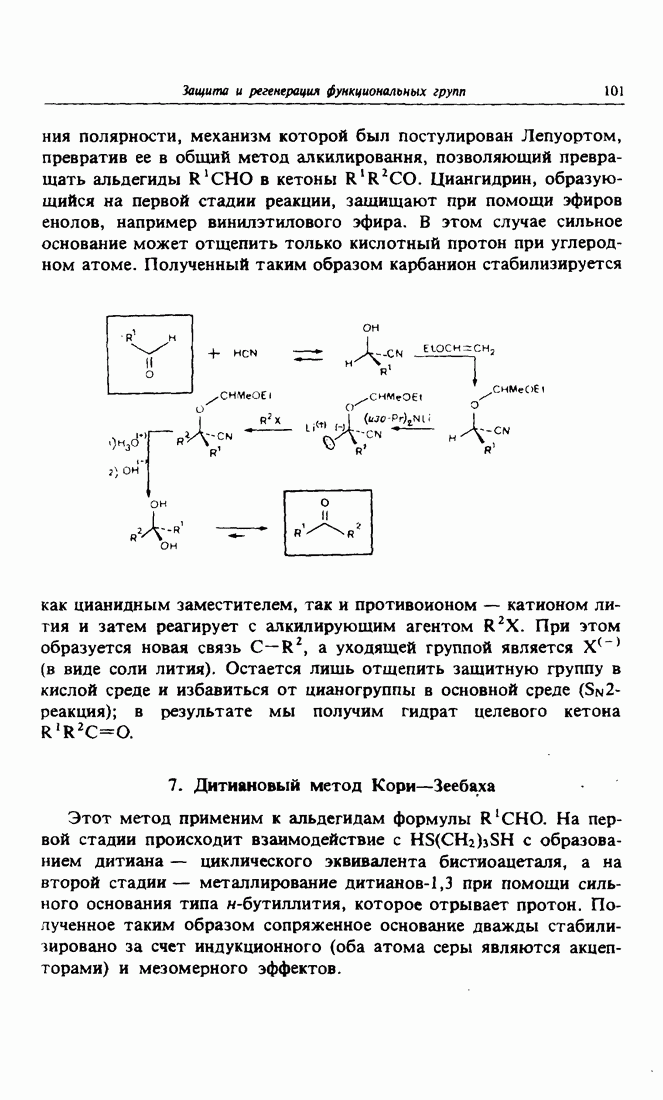
- 6. Инверсия полярности по методу Лепуорта — Шторка
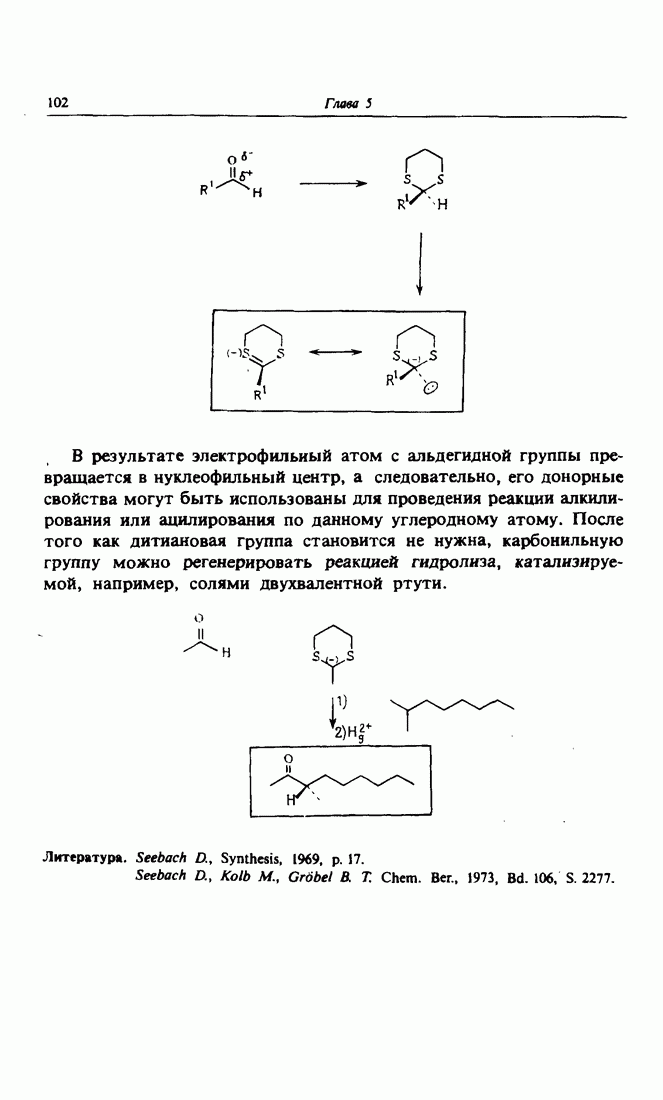
- 7. Дитиановый метод Кори-Зеебаха
- Главе 6. АКТИВАЦИЯ
- 2. Стабилизация конечного состояния
- 3. Дестабилизация начального состояния
- 4. Стабилизация переходного состояния
- Главв 7. ПОСТРОЕНИЕ ЦИКЛОВ
- 2. Региоселективность
- 3. Реакция Дильса — Альдера в условиях обращенного электронного соответствия
- 4. Стереоселективность в реакциях Дильса — Альдера
- 5. Напряжение в циклах
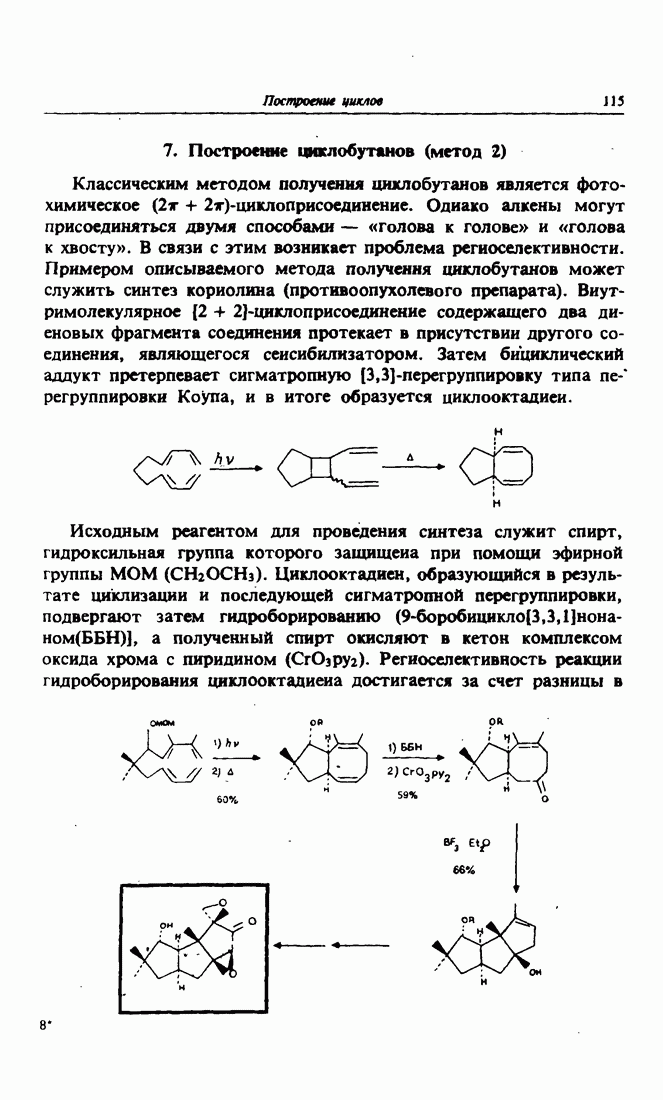
- 6. Построение циклобутанов (метод 1) Термическая димеризация
- 7. Построение циклобутанов (метод 2)
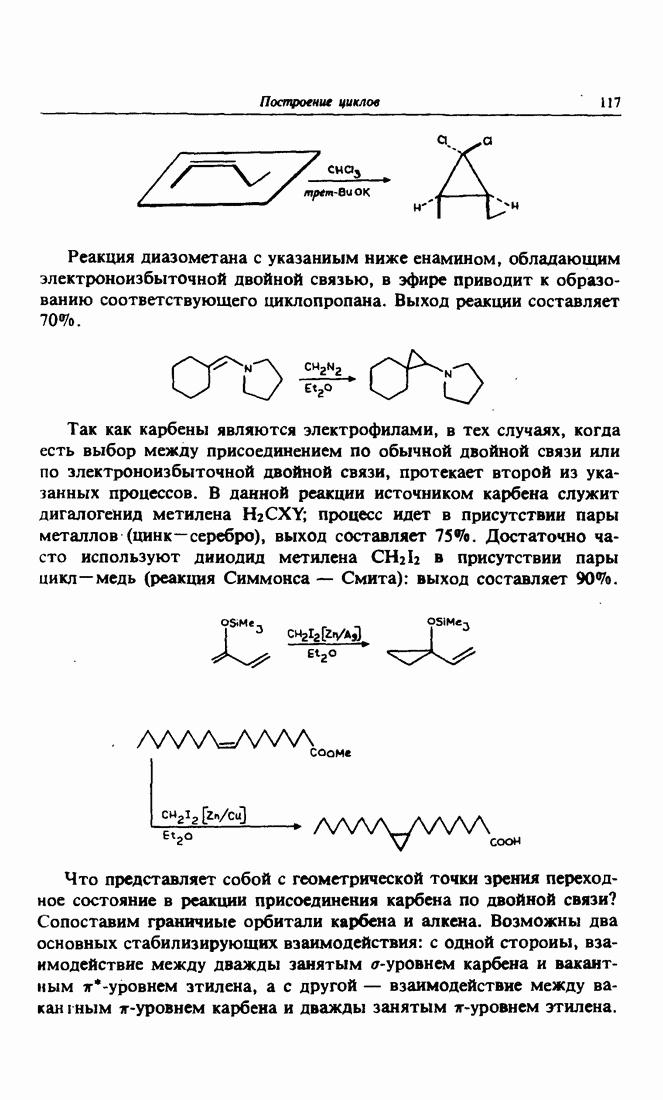
- 8. Синтез циклопропанов. Присоединение карбенов к алкенам
- Глааа 8. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ЗАМЕЩЕНИЯ
- 2. Соотношение структура — реакционноспособность
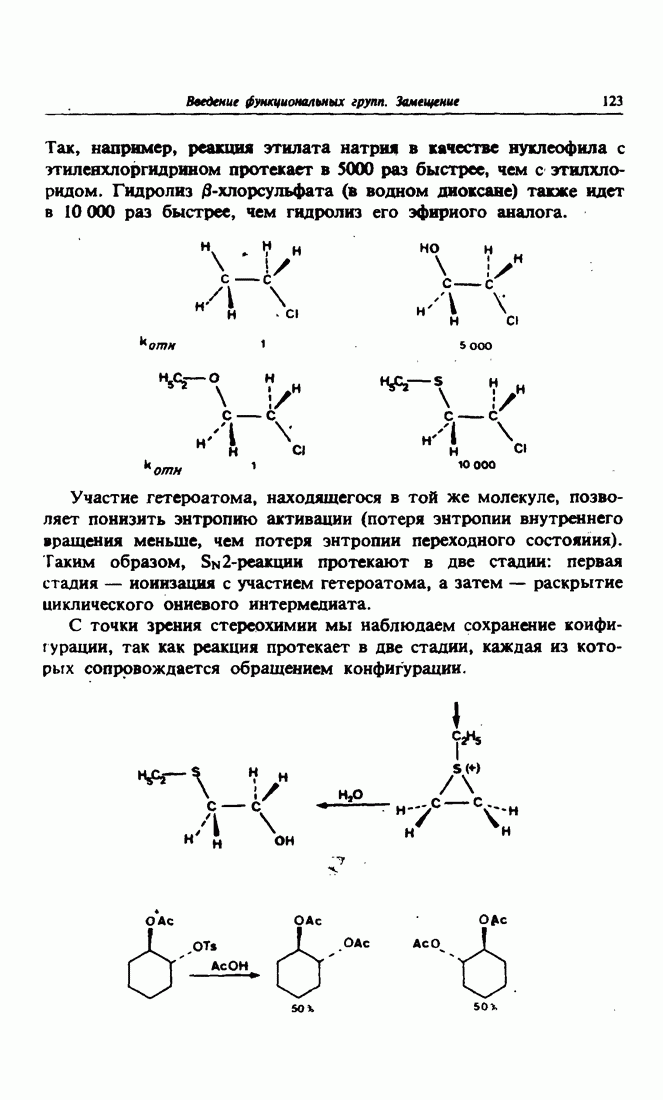
- 3. Участие соседней группы в Sn2-реакциях
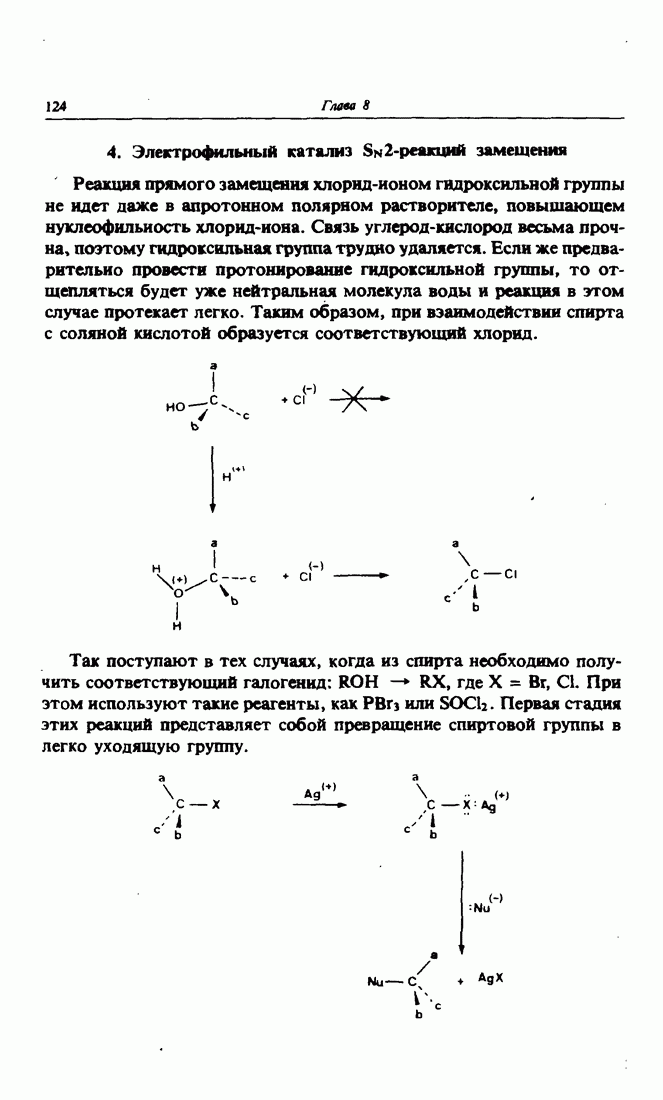
- 4. Электрофильный катализ Sn2-реакций замещения
- 5. Региоселеггивность в реакциях алкилирования
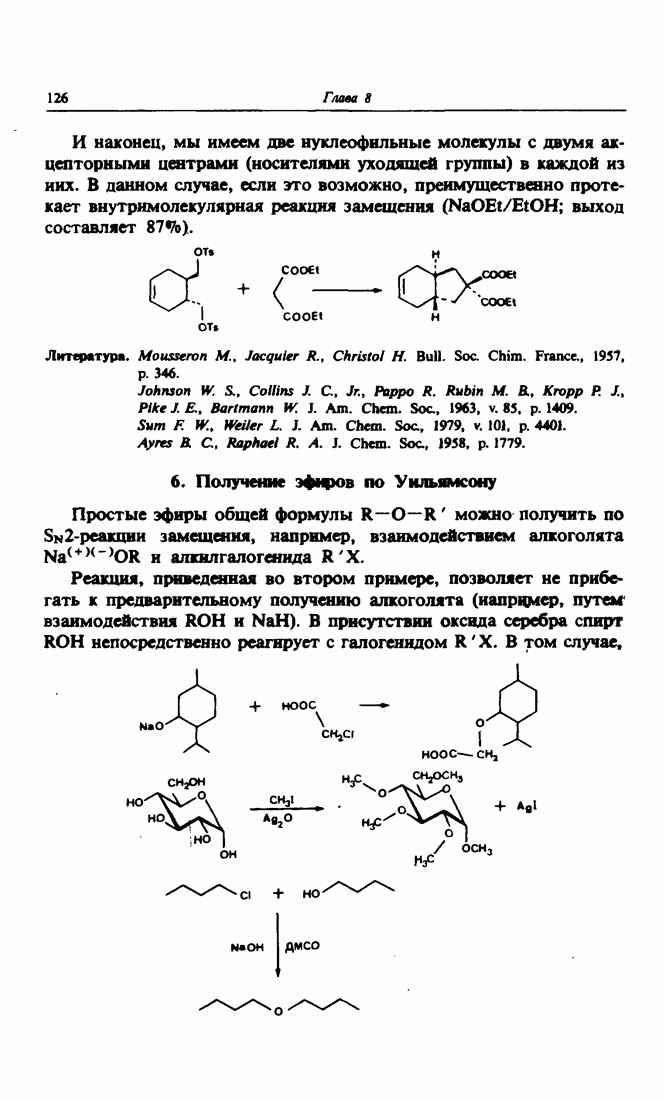
- 6. Получение эфиров по Уильямсону
- 7. К вопросу об обозначениях
- Глава 9. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ВОССТАНОВЛЕНИЯ
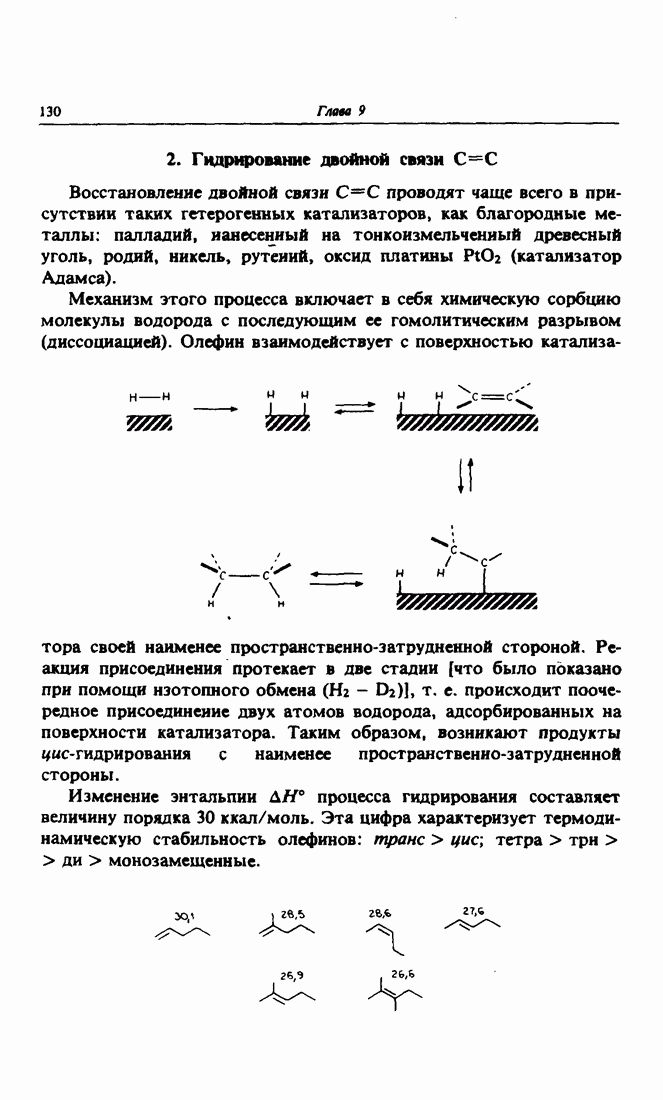
- 2. Гидрирование двойной связи С=С
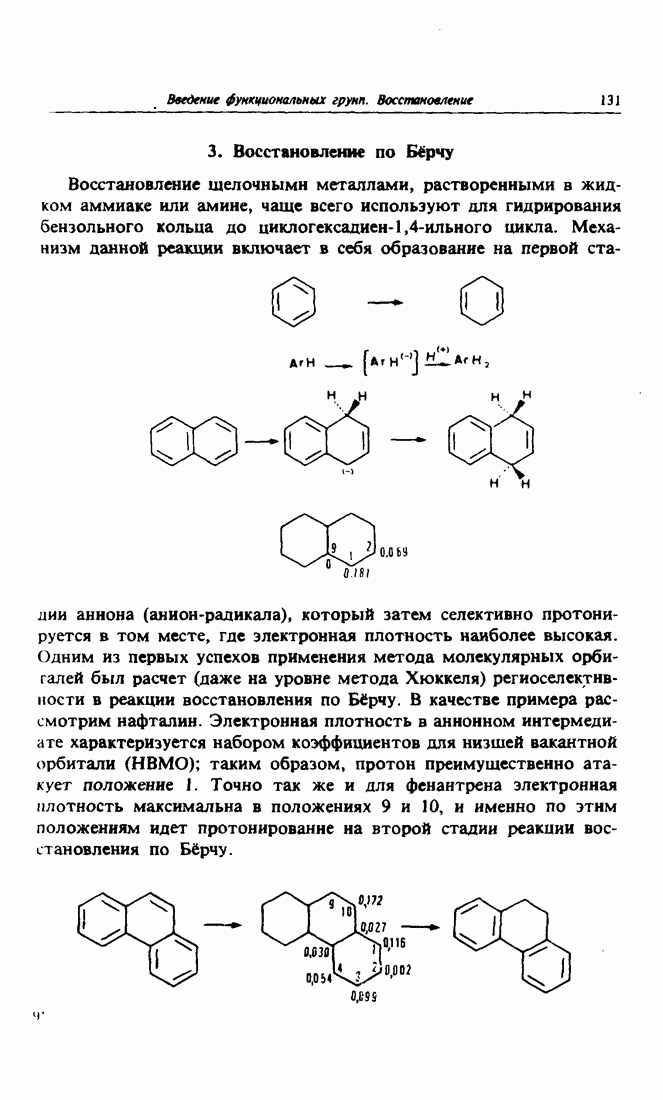
- 3. Восстановление по Бёрчу
- 4. Восстановление карбонильной группы
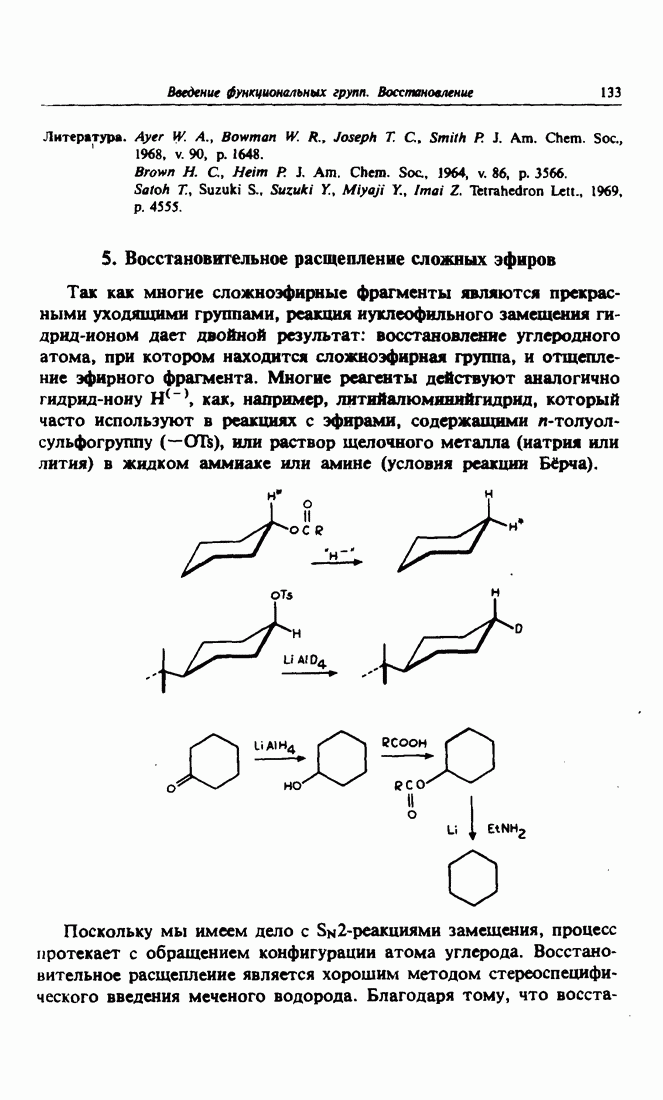
- 5. Восстановительное расщепление сложных эфиров
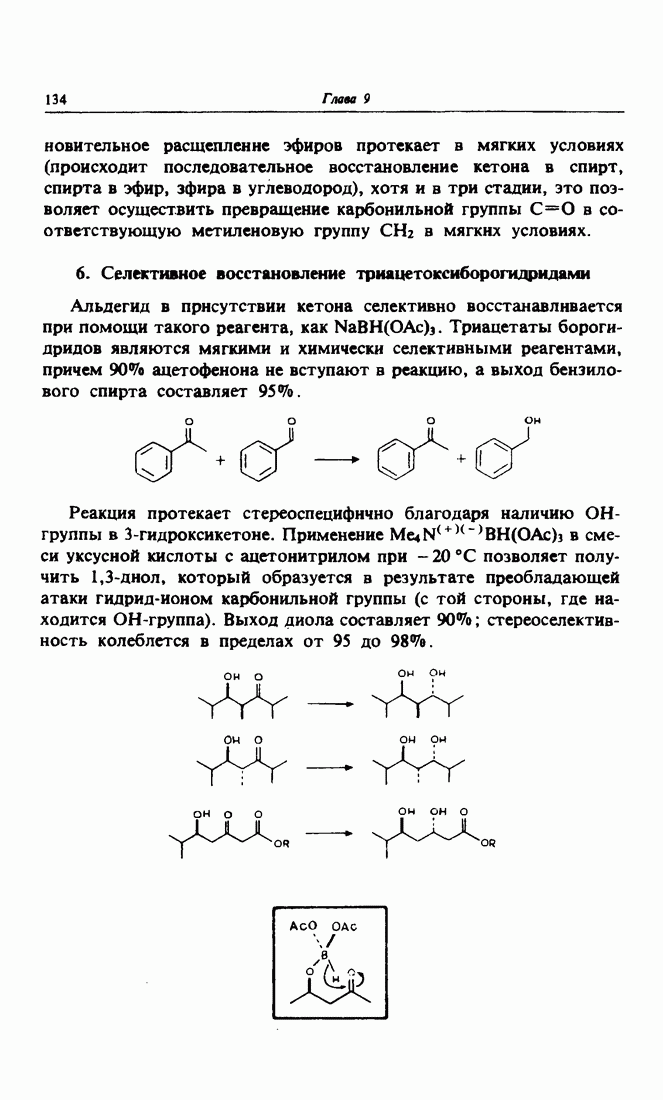
- 6. Селективное восстановление триацетоксиборогидридами
- Глава 10. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ОКИСЛЕНИЯ
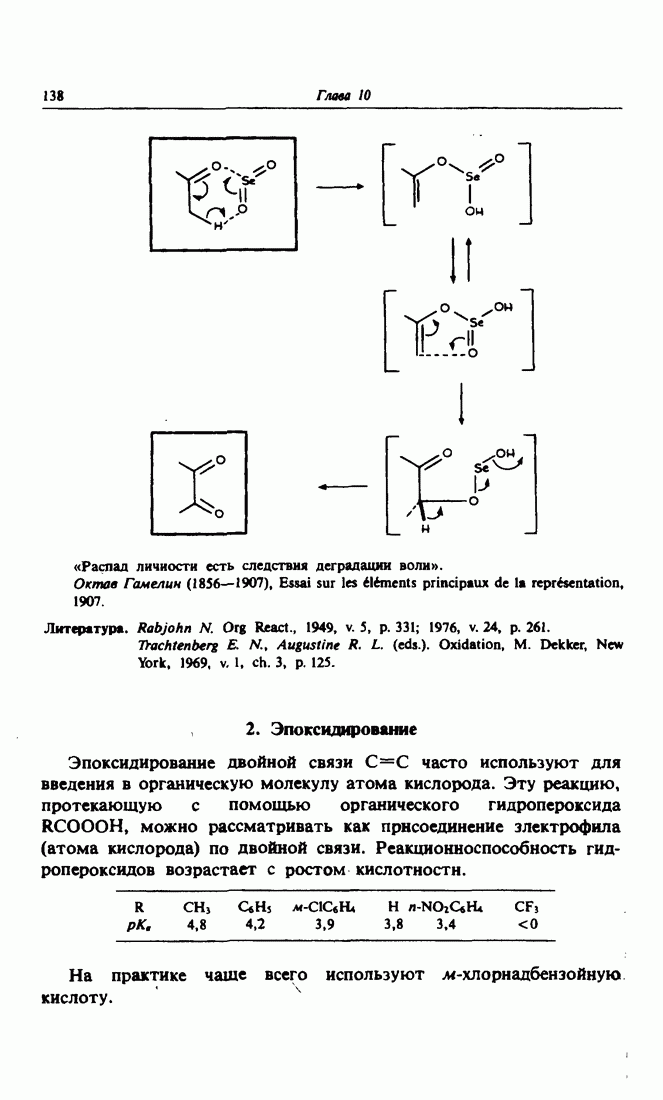
- 2. Эпоксидирование
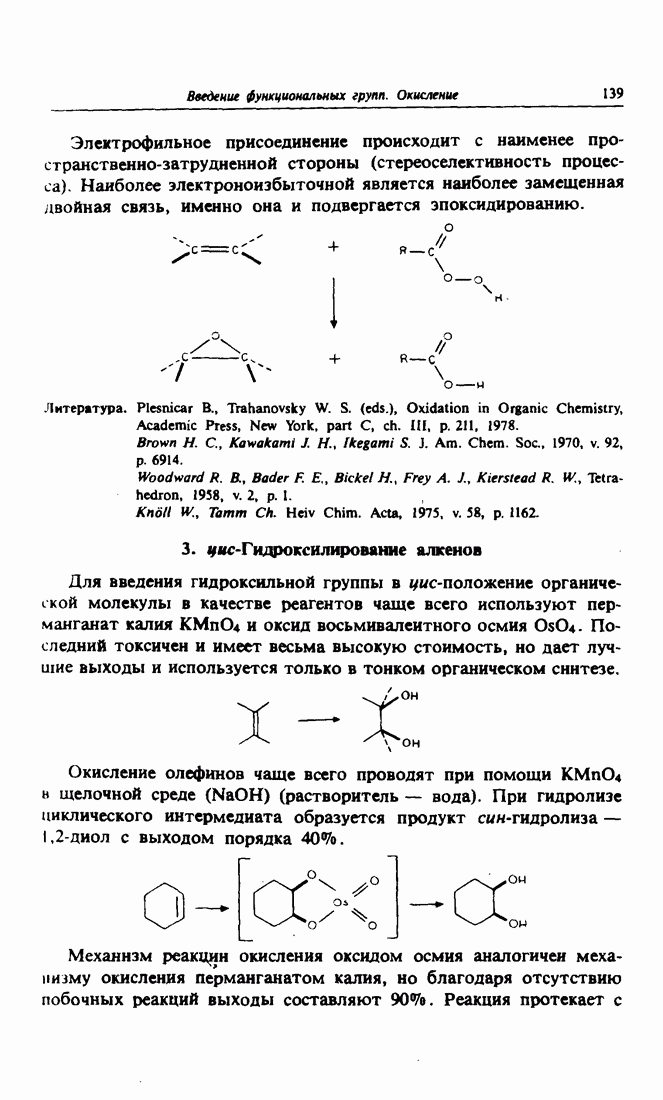
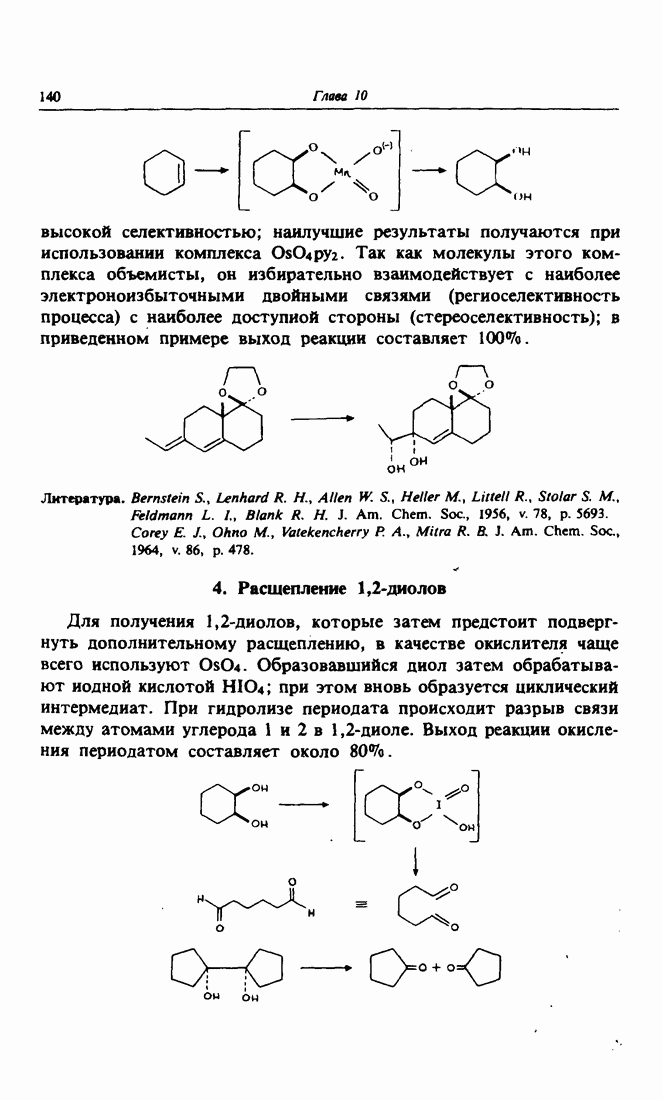
- 3. цис-Гидроксилирование алкенов
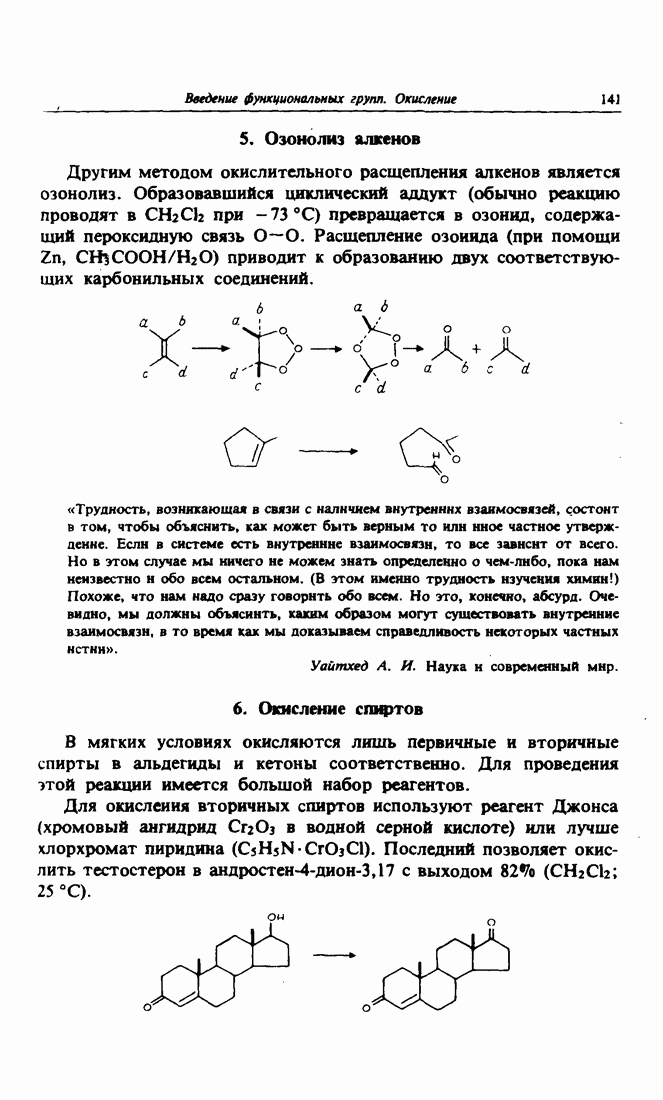
- 4. Расщепление 1,2-диолов
- 5. Озонолиз алкенов
- 6. Окисление спиртов
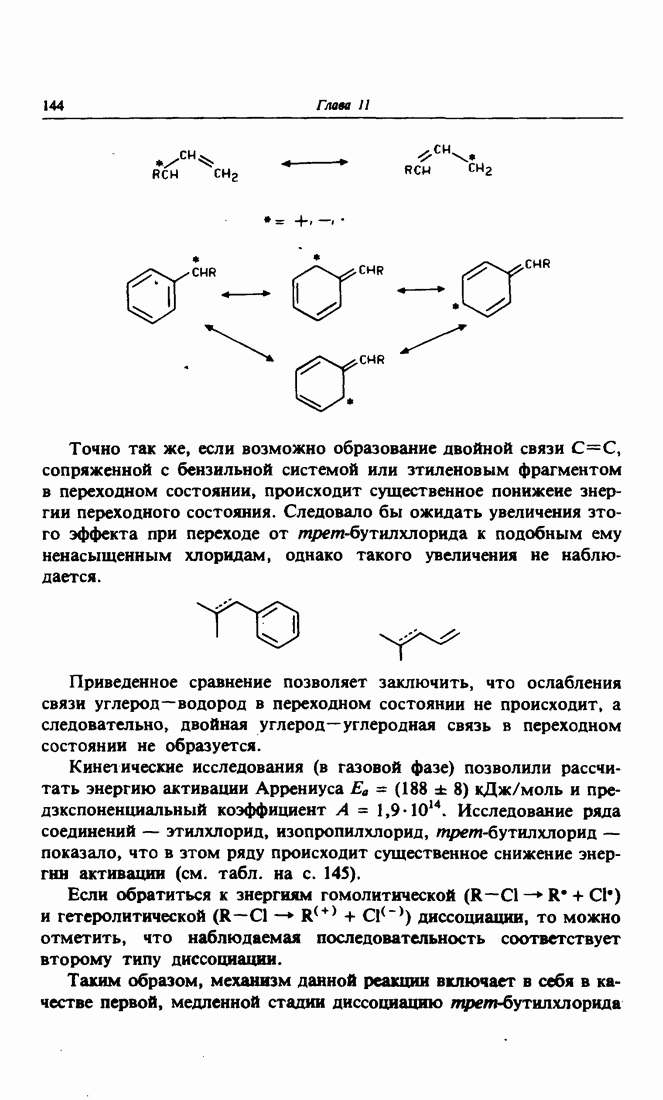
- Главе 11. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ЭЛИМИНИРОВАНИЯ
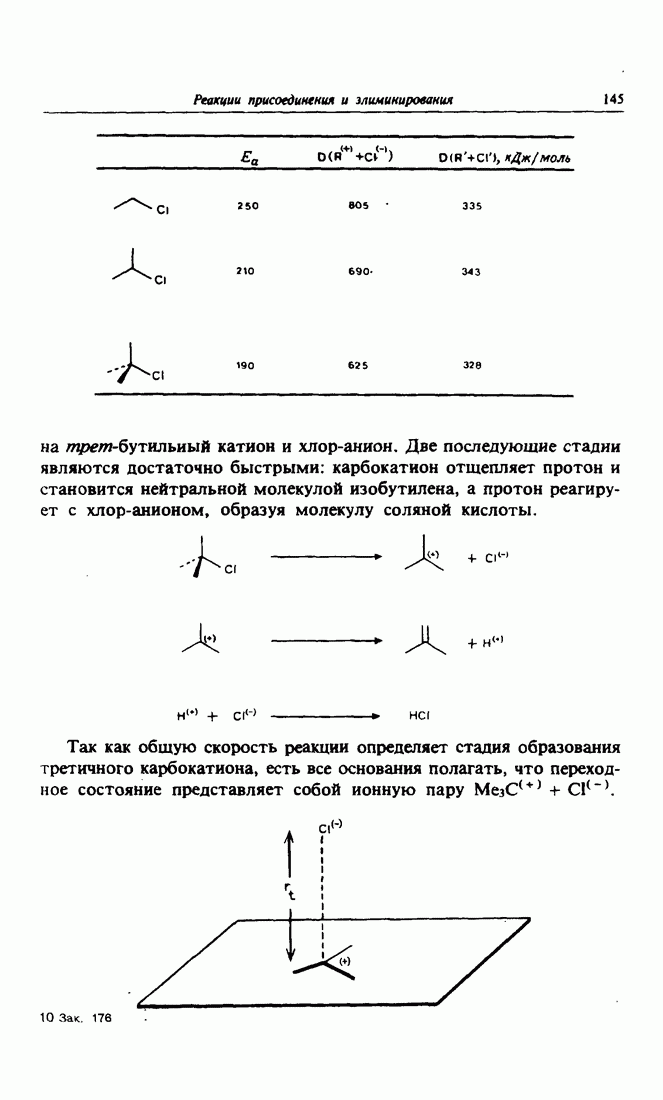
- 2. Классически механизм реакции электрофильного присоединения. Правило Марковникова
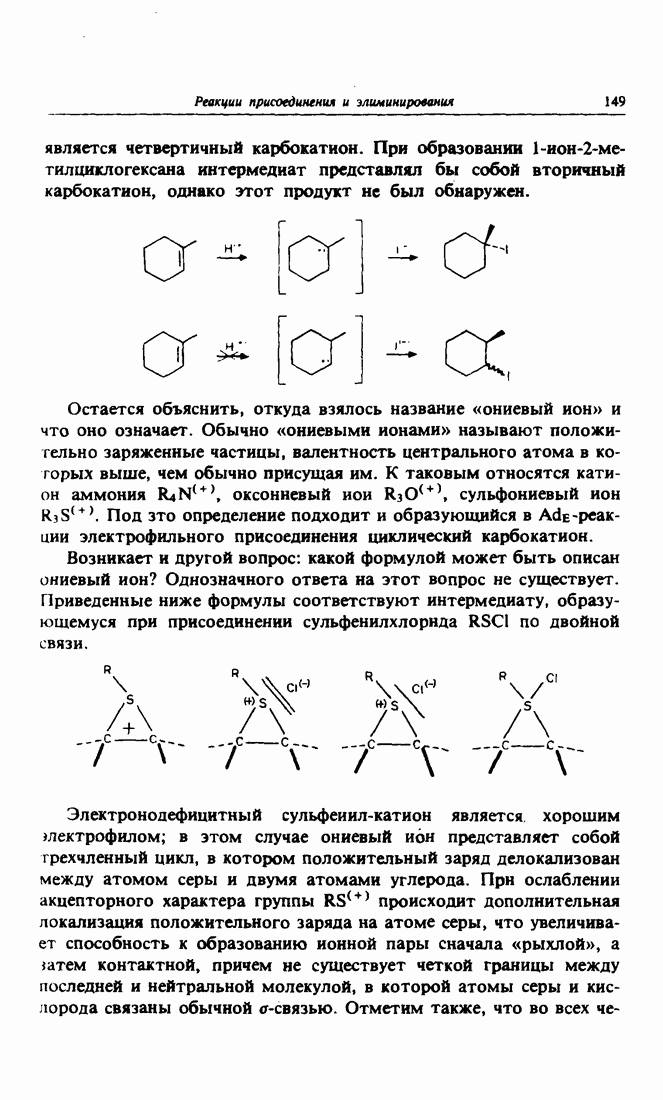
- 3. Основные электрофильные агенты
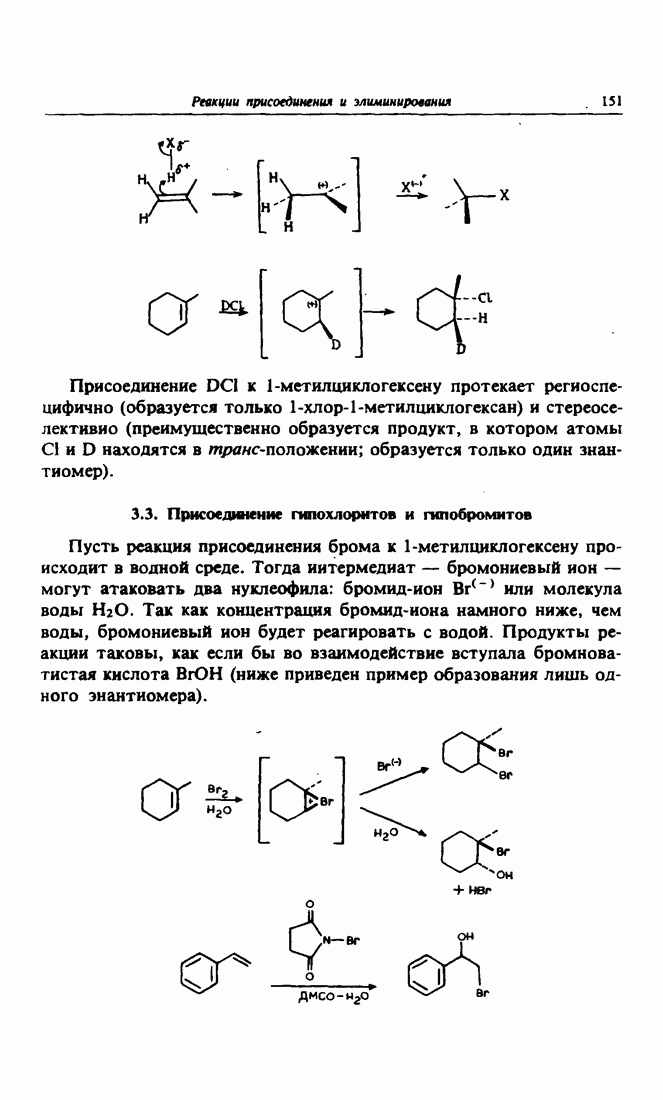
- 3.3. Присоединение гипохлоритов и гипобромитов
- 3.4. Оксимеркурирование
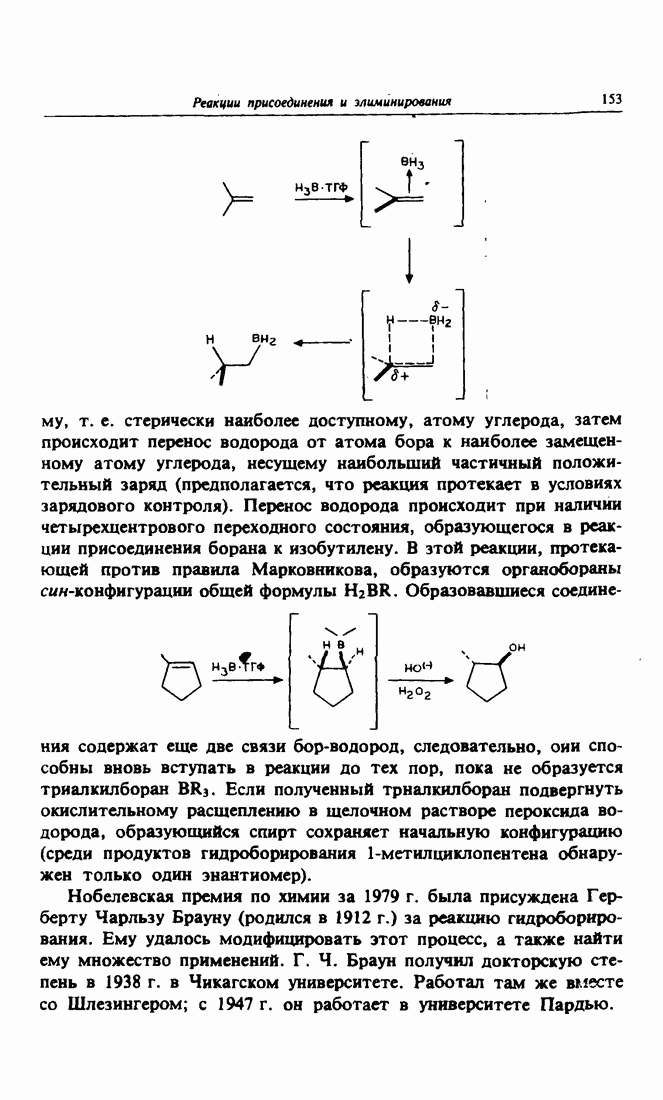
- 3.5. Гидроборирование
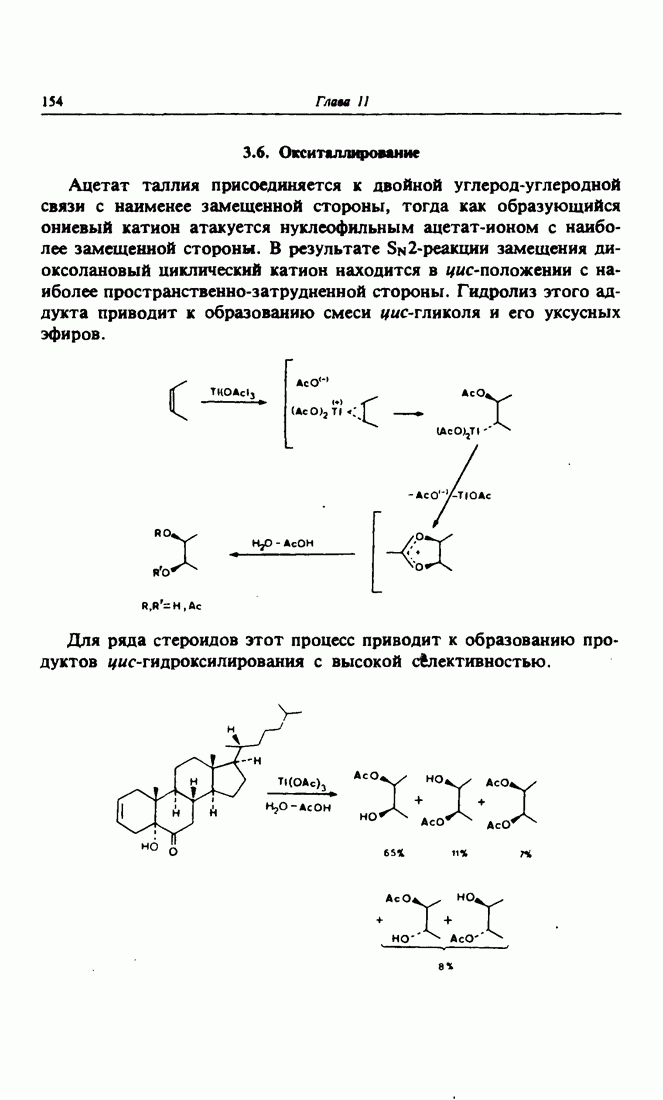
- 3.6. Окситаллирование
- 4. Стереохимия реакции присоединения по двойной связи С=С
- 5. Конкуренция нуклеофила и растворителя в реакции электрофильного присоединения
- 6. Присоединение к напряженным олефинам: цис-присоединение
- 7. Стереохимия реакций бимолекулярного элиминирования
- 8. Виды b-элиминирования
- Главв 12. ПЕРЕГРУППИРОВКИ ФУНКЦИОНАЛЬНЫХ ГРУПП. ПРЕВРАЩЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ В ОЛЕФИНЫ ПО РЕАКЦИИ ВИТТИГА
- 2. Реакция Дарзана
- 3. Дарзан — один из великих политехников
- 4. Обобщение и модернизация метода
- 5. Стереоселективность реакции Кори — Чайковского
- 6. Реакция Виттига
- 7. Георг Виттиг
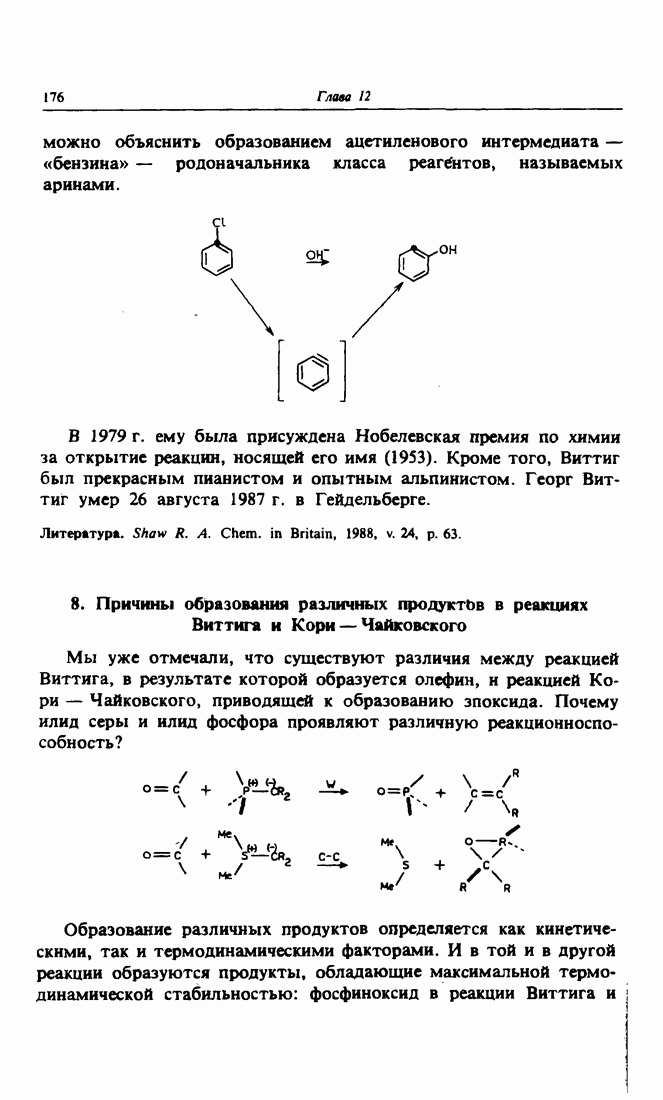
- 8. Причины образования различных продуктов в реакциях Виттига и Кори — Чайковского
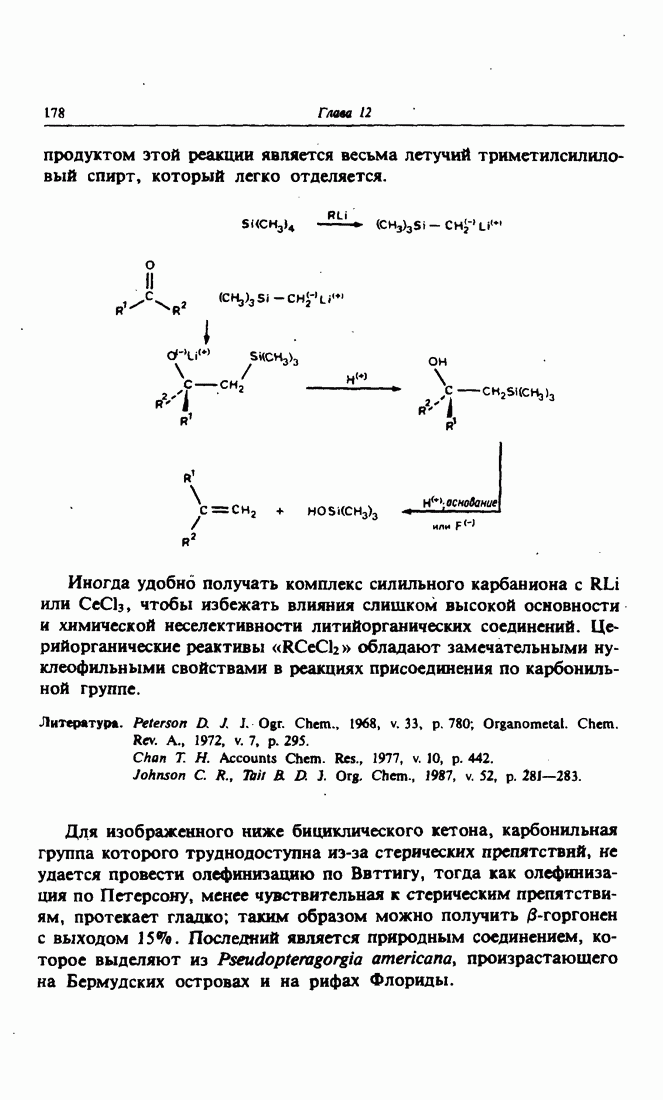
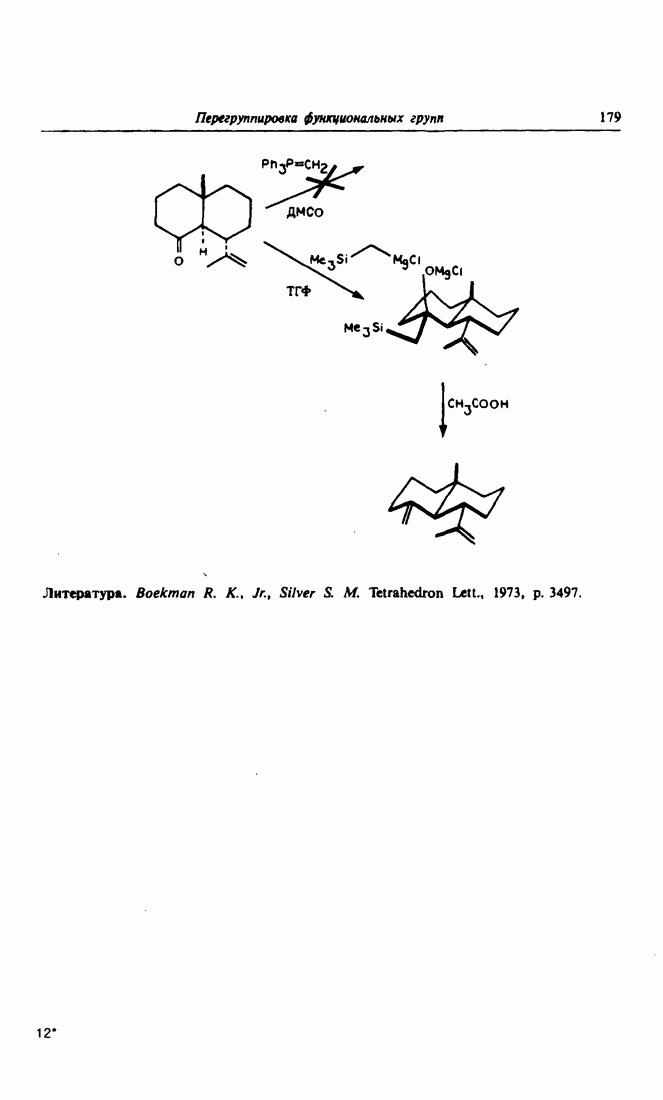
- 9. Разновидность реакции Виттига: олефинирование по Петерсону
- Главе 13. ПЕРЕГРУППИРОВКИ
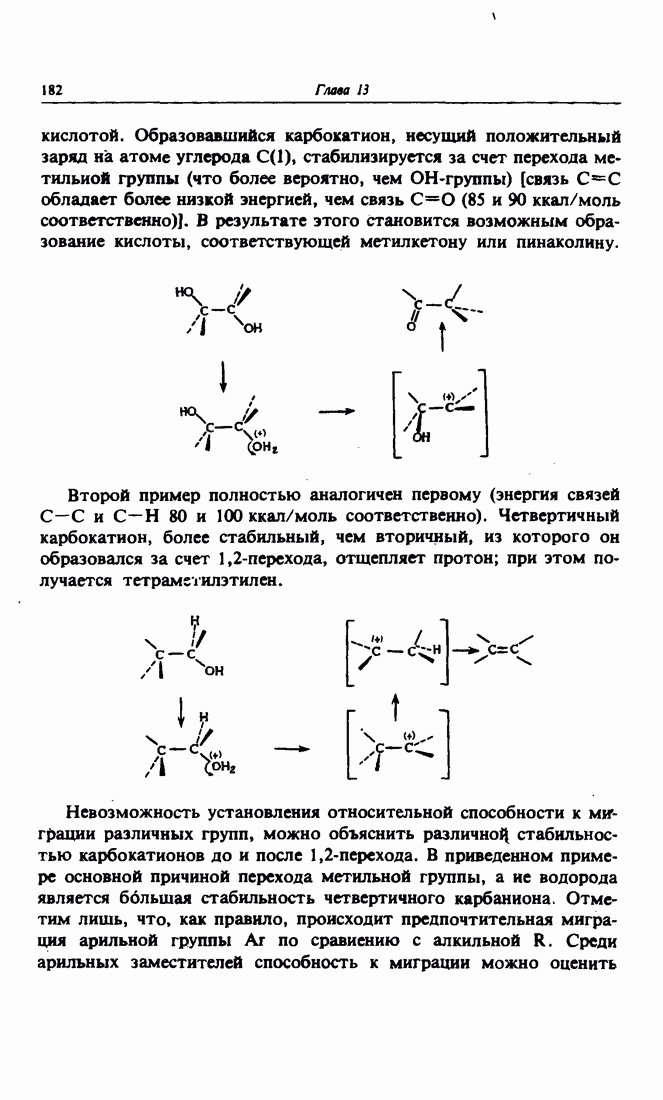
- 2. 1,2-Переход в карбокатионах
- 3. Перегруппировка Бекмана
- 4. Перегруппировка Курциуса
- 5. Перегруппировка Байера — Виллигера
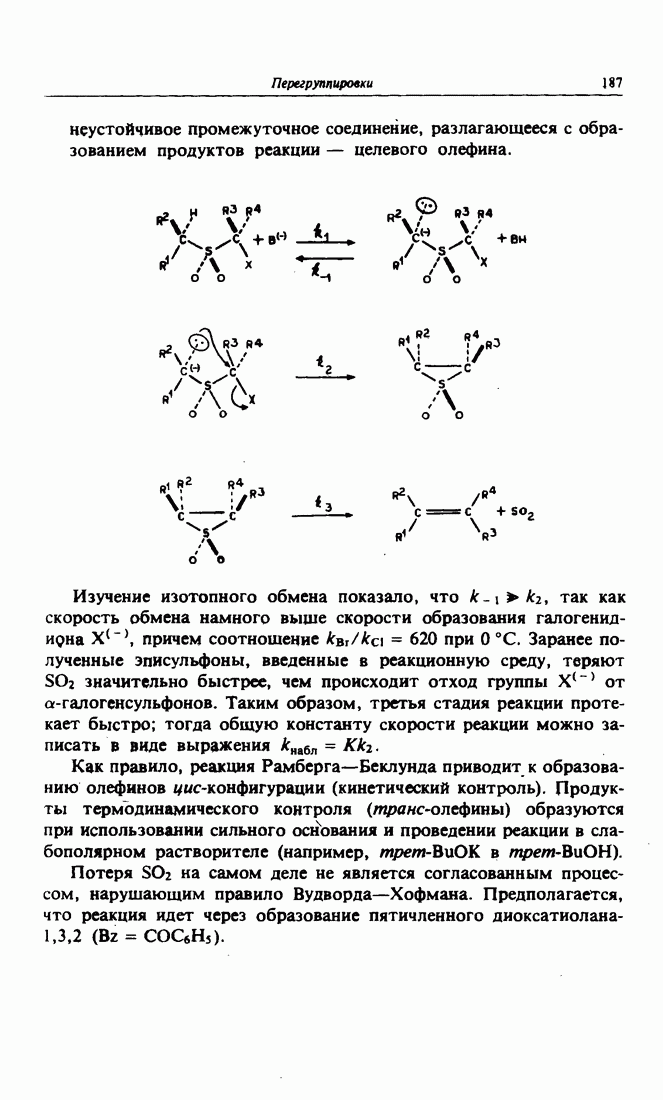
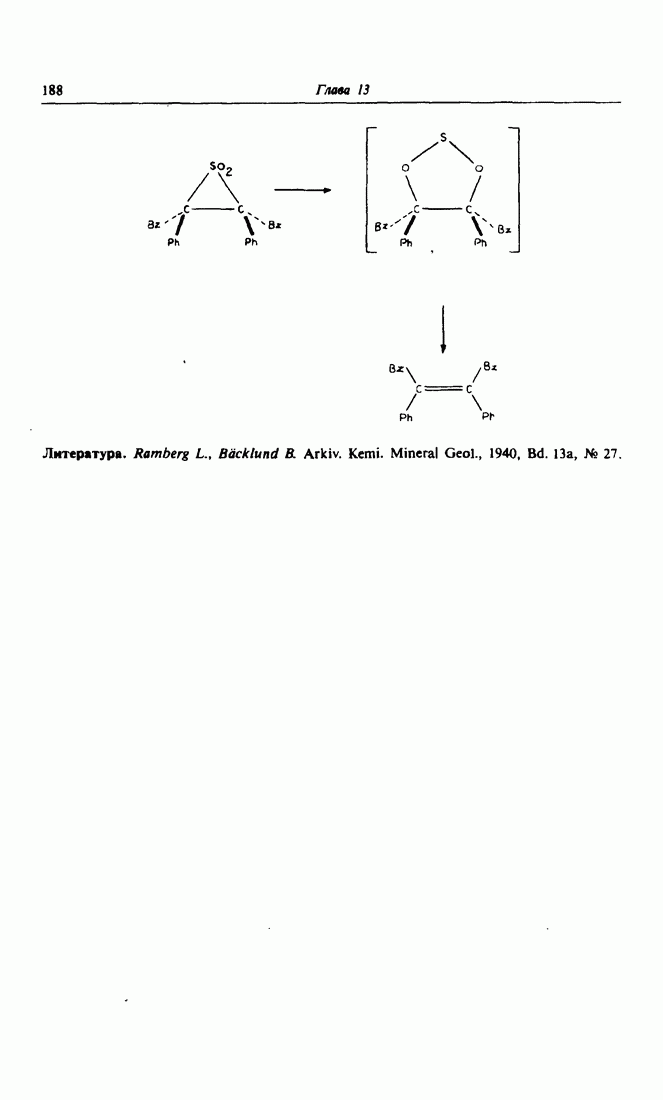
- 6. Реакция Рамберга-Беклунда
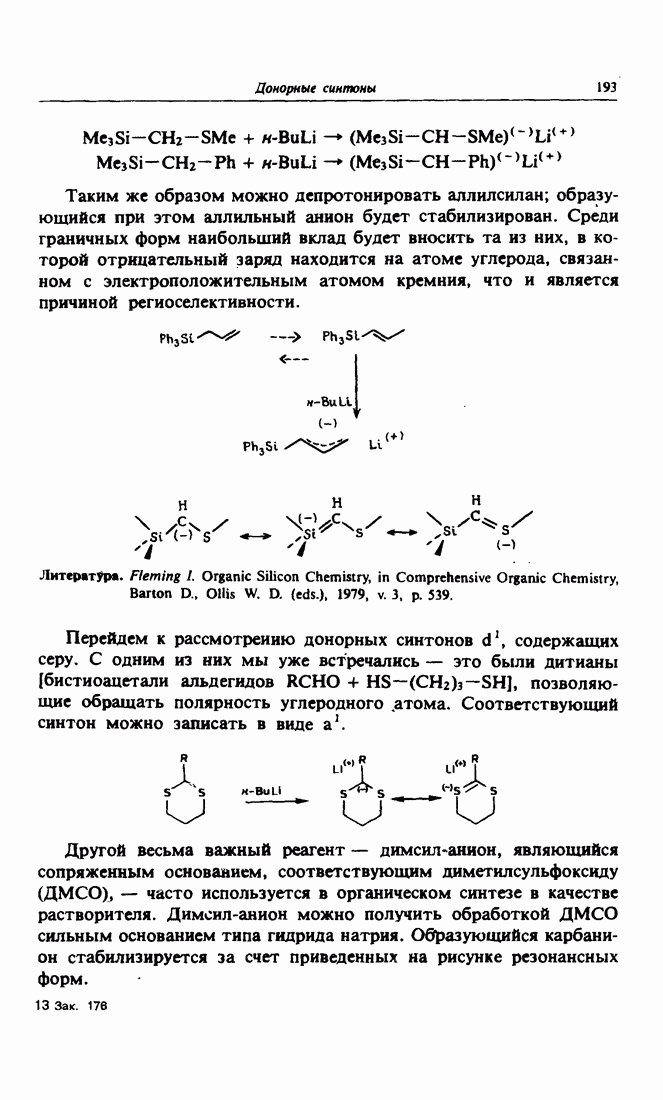
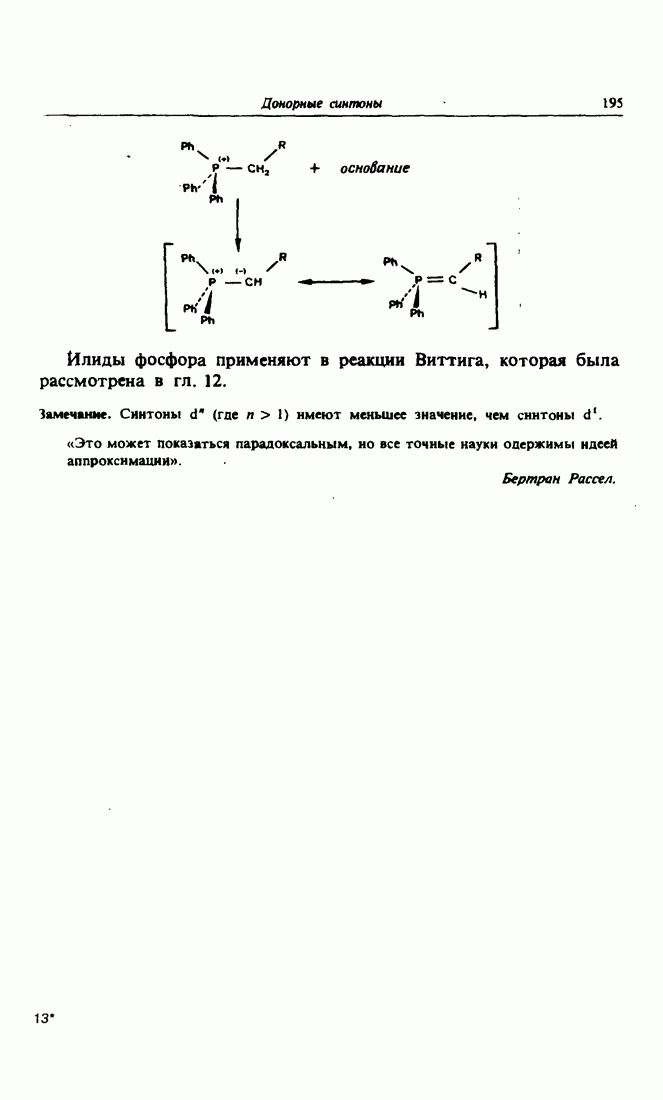
- Глава 14. ДОНОРНЫЕ СИНТОНЫ
- 2. Алкильные донорные синтоны
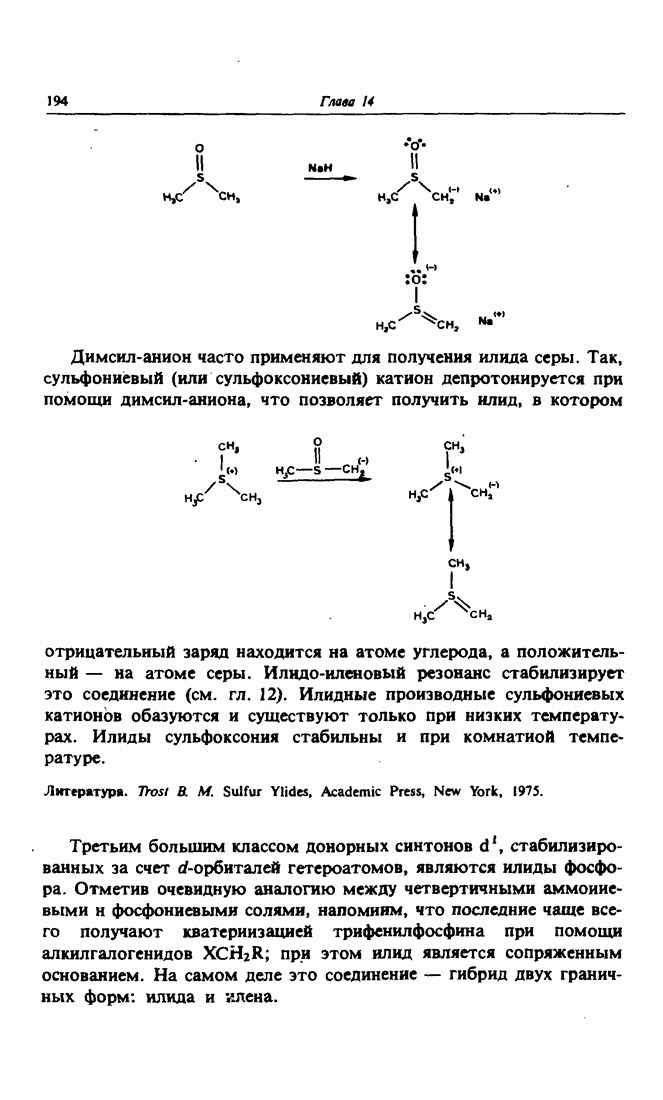
- 3. Донорные синтоны d1 с гетероатомами, обладающими d-орбиталью
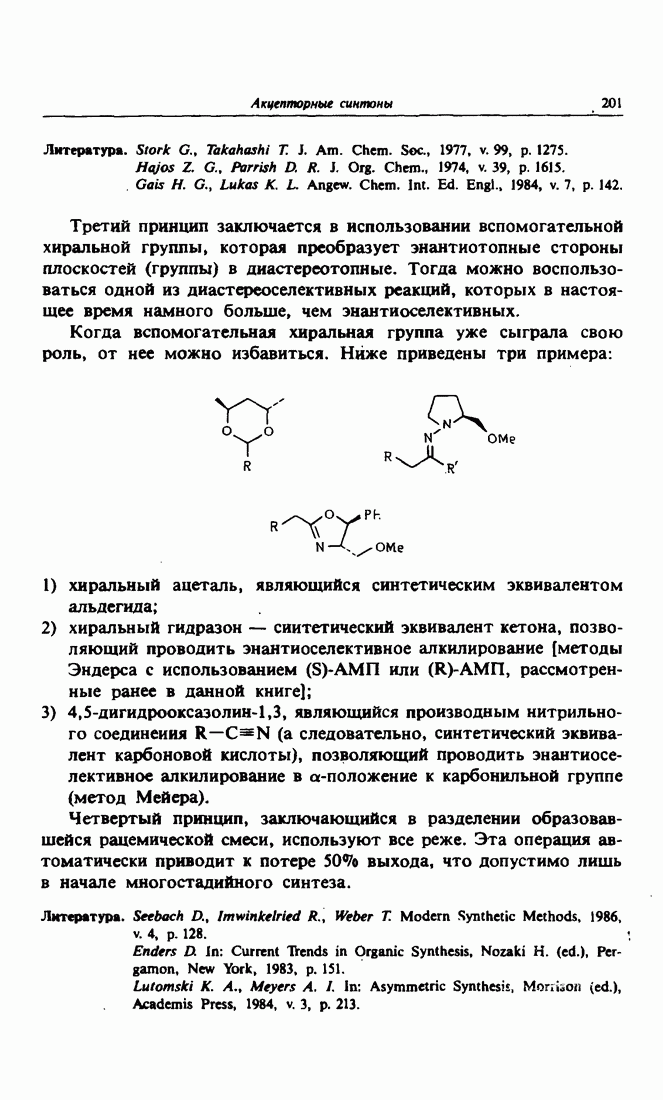
- Глава 15. АКЦЕПТОРНЫЕ СИНТОНЫ
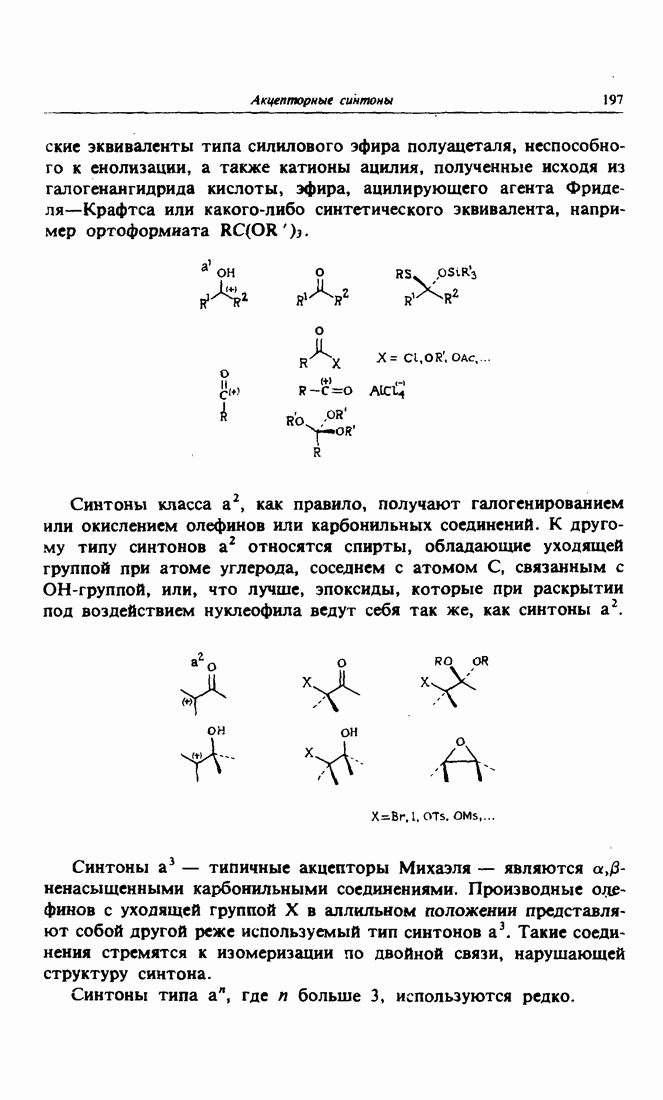
- 1. Синтоны-акцепторы
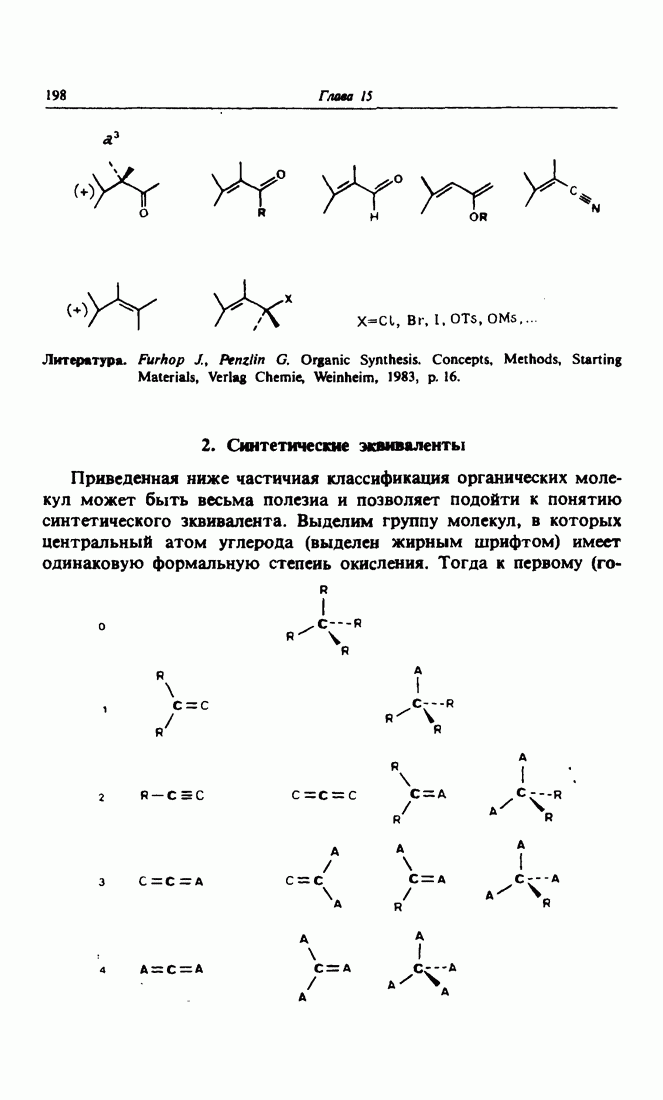
- 2. Синтетические эквиваленты
- 3. Контролируемое образование новых связей
- 4. Расчленение молекулы на фрагменты
- 5. Двойное расчленение молекулы
- 6. Изменение реакционноспособности в результате обращения полярности
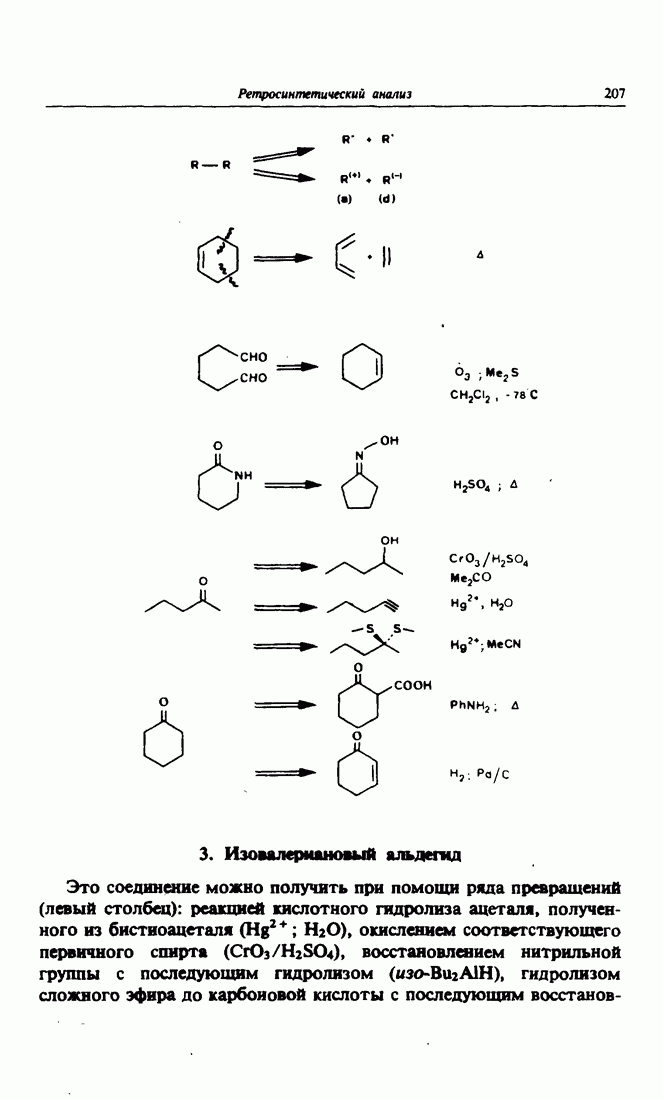
- Глава 16. РЕТРОСИНТЕТИЧЕСКИЙ АНАЛИЗ
- 2. Цепь превращений
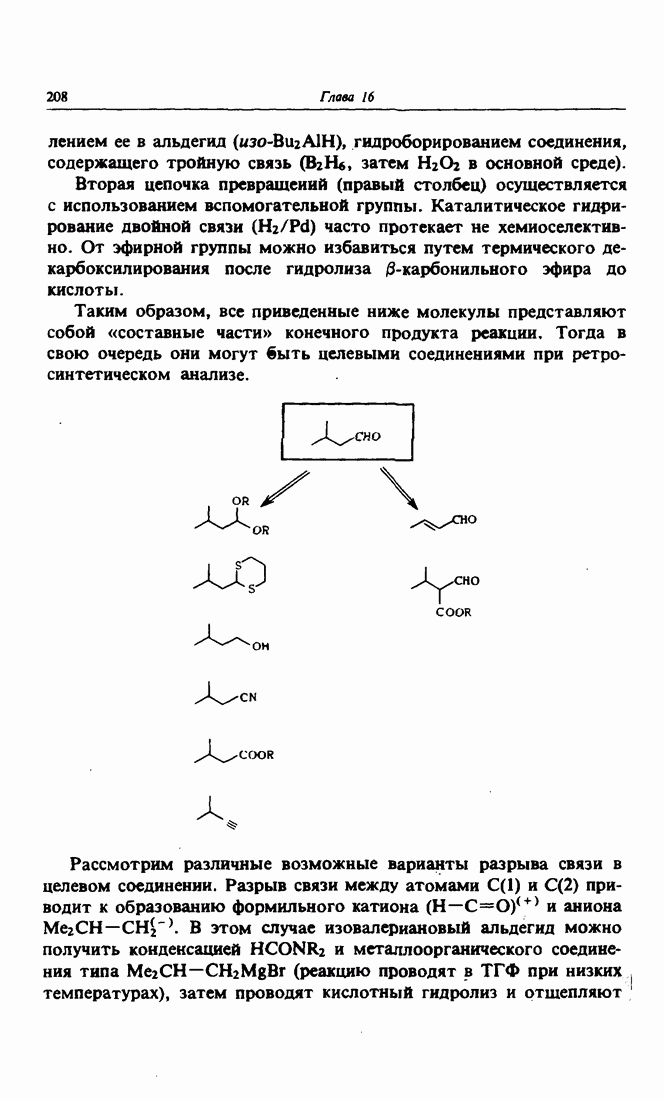
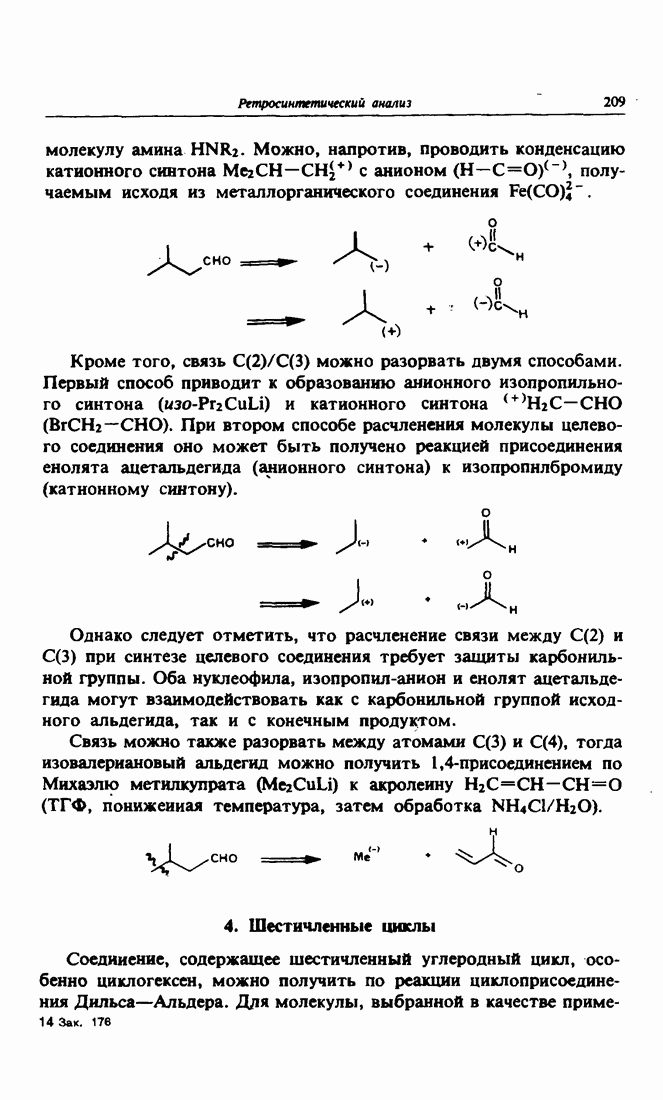
- 3. Изовалериановый альдегид
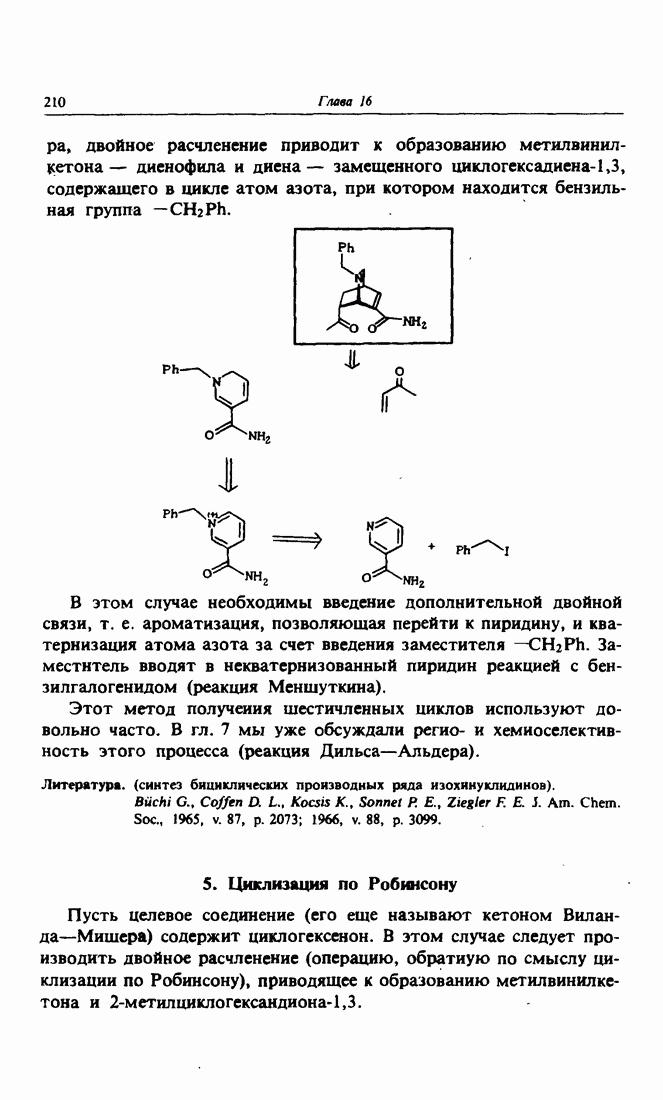
- 4. Шестичленные циклы
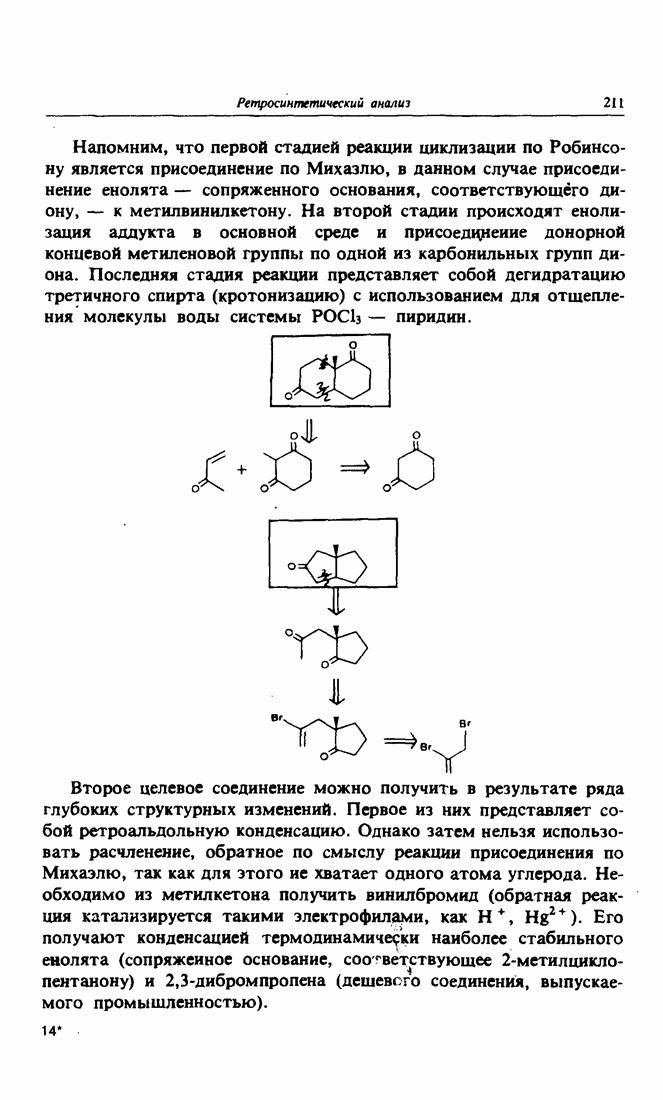
- 5. Циклизация по Робинсону
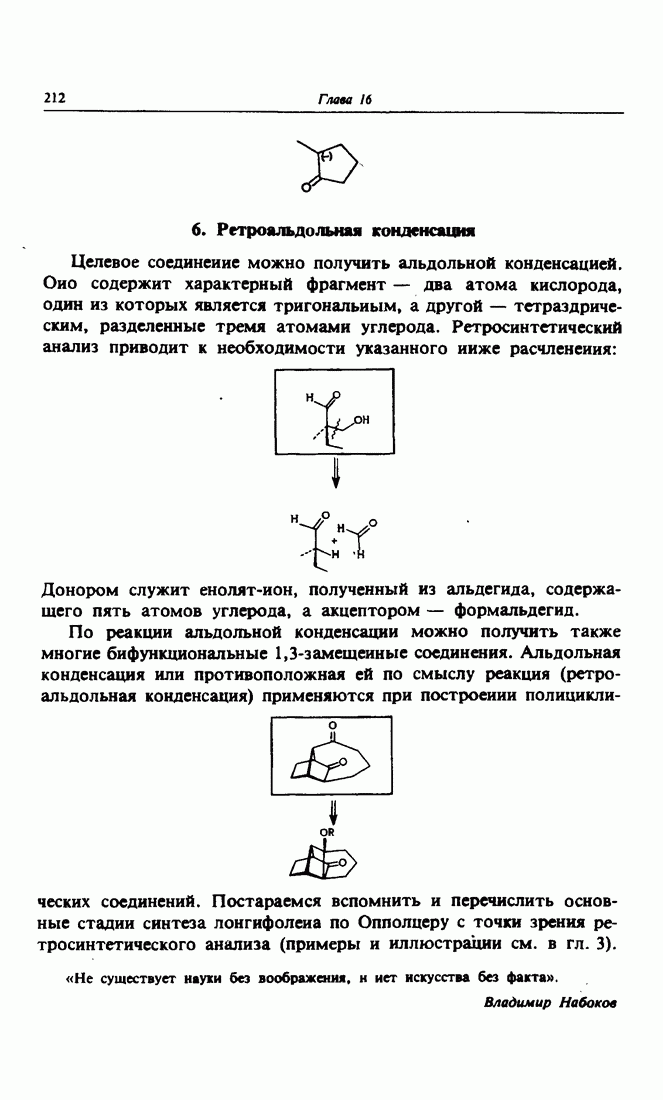
- 6. Ретроальдольная конденсация
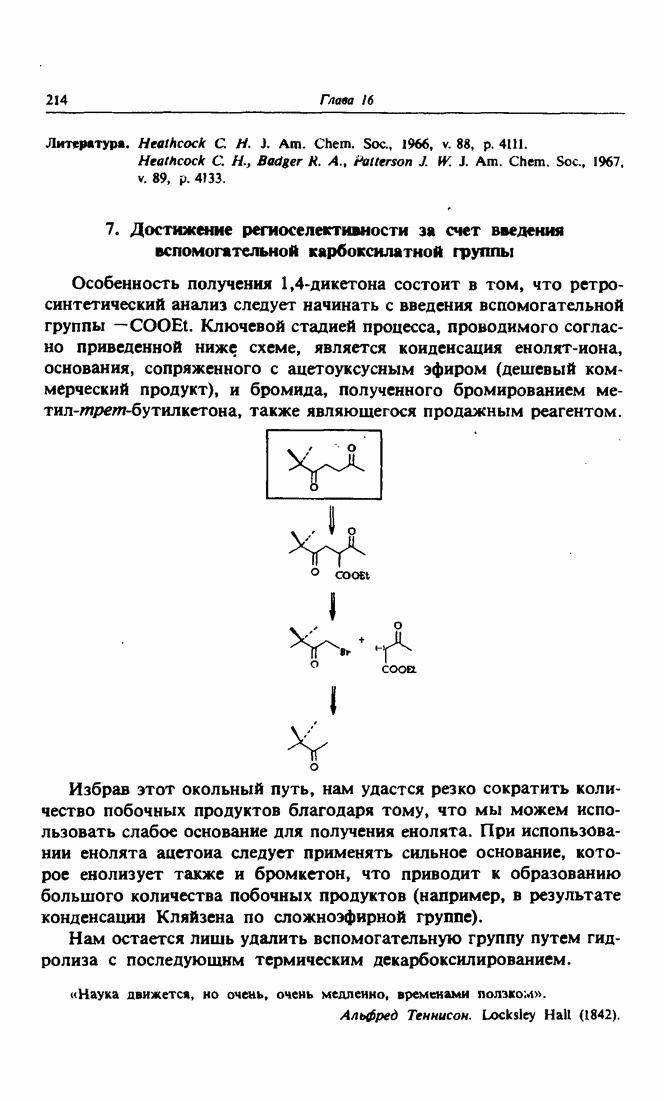
- 7. Достижение региоселективности за счет введения вспомогательной карбоксилатной группы
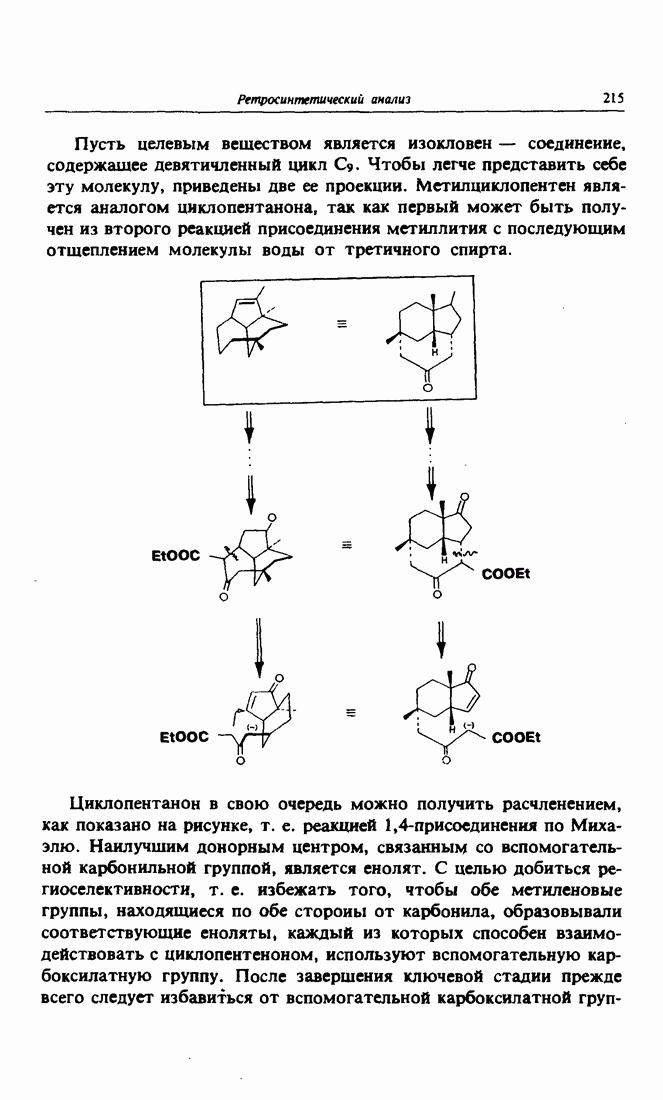
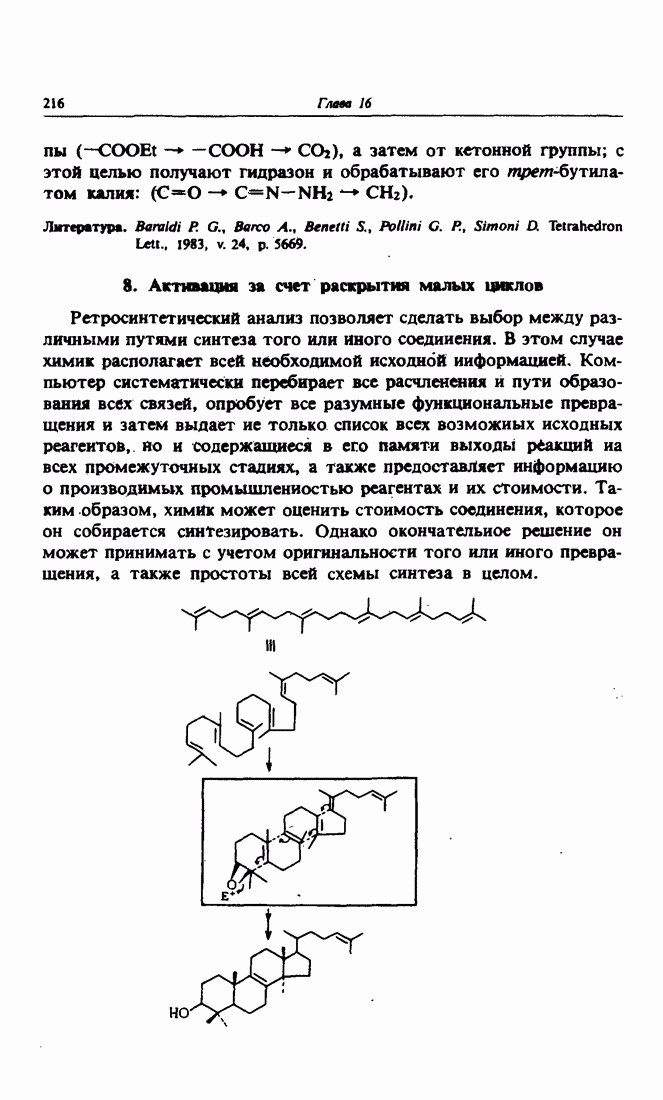
- 8. Активация за счет раскрытия малых циклов
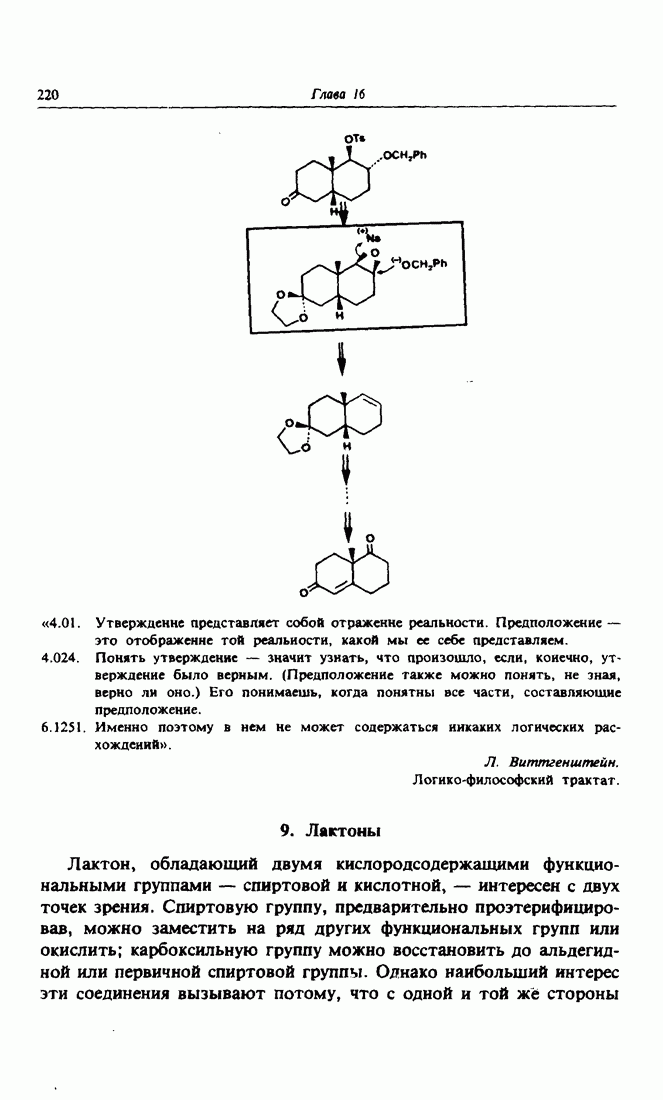
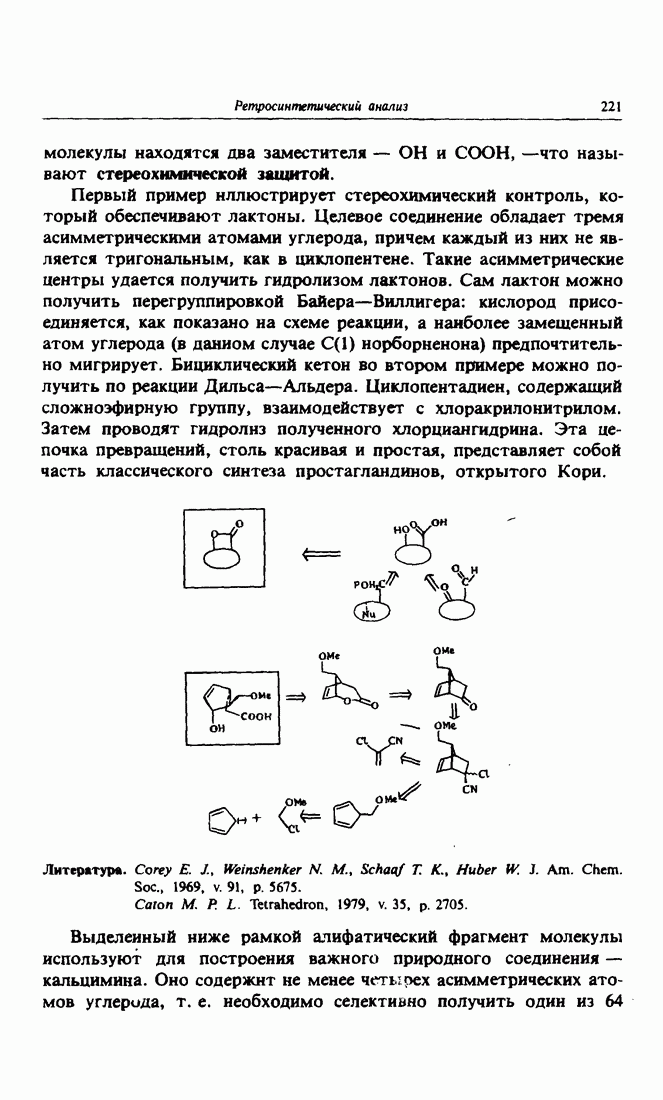
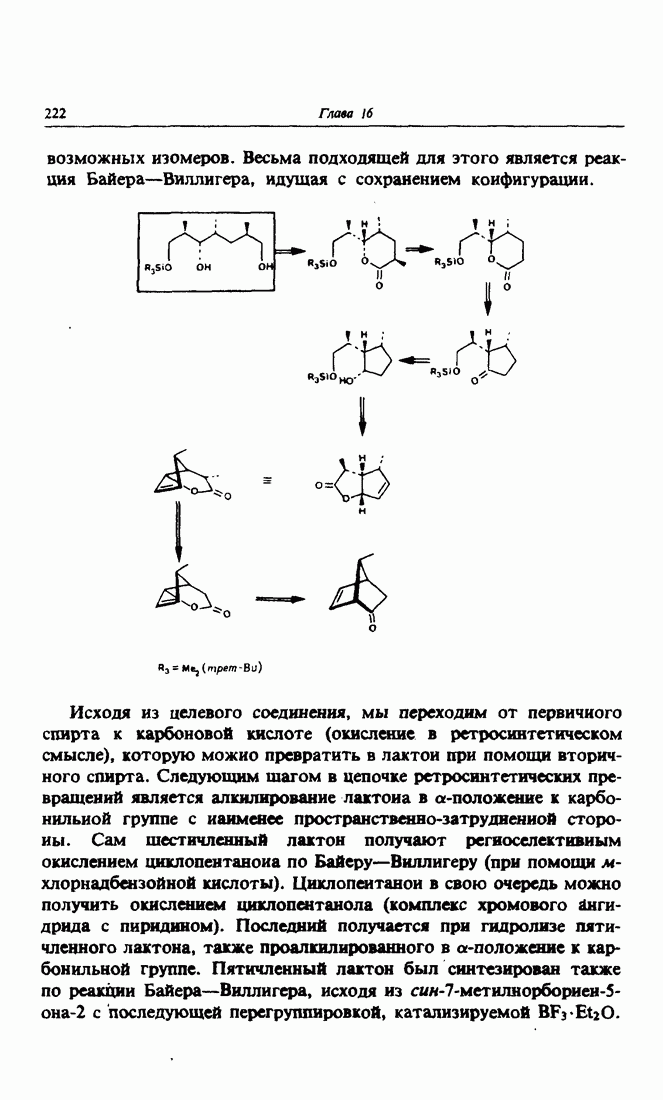
- 9. Лактоны
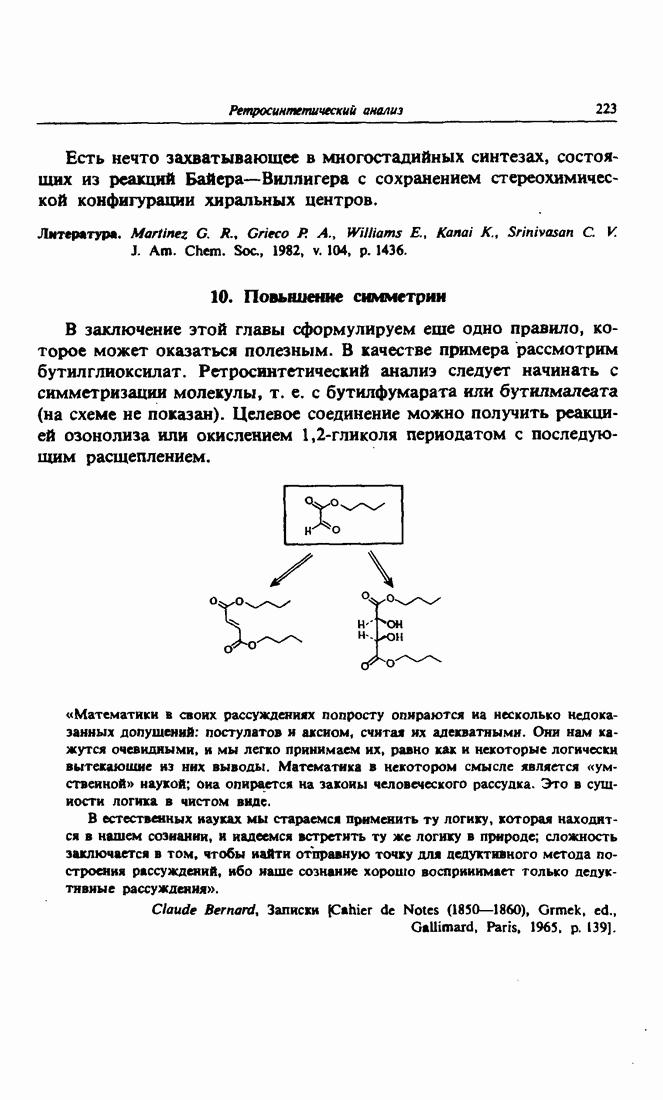
- 10. Повышение симметрии
- ПОСЛЕСЛОВИЕ