| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ПОДГРУППА МАРГАНЦА
В состав этой подгруппы входят элементы побочной подгруппы седьмой группы: марганец, технеций и рений. Отношение между ними и элементами главной подгруппы седьмой группы — галогенами — приблизительно такое же, как и между элементами главной и побочной подгрупп шестой группы. Имея в наружном электронном слое атома всего два электрона, марганец и его аналоги не способны присоединять электроны и, в отличие от галогенов, соединений с водородом не образуют. Однако высшие кислородные соединения этих элементов до некоторой степени сходны с соответствующими соединениями галогенов, так как в образовании связей с кислородом у них, как и у галогенов, могут участвовать семь электронов. Поэтому их высшая степень окисленности равна  .
.
Из элементов подгруппы марганца наибольшее практическое значение имеет сам марганец. Рений, открытый в 1925 г., — редкий элемент, однако, благодаря ряду ценных свойств, находит применение в технике. Технеций в земной коре не встречается. Он был получен в 1937 г. искусственно, бомбардировкой ядер атомов молибдена ядрами тяжелого изотопа водорода — дейтронами (см. § 37).
Технеций был первым элементом, полученным искусственным, «техническим» путем, что и послужило основанием для его названия.
231. Марганец (Manganum).
Марганец принадлежит к довольно распространенным элементам, составляя (масс.) земной коры. Из соединений, содержащих марганец, наиболее часто встречается минерал пиролюзит, представляющий собой диоксид марганца
(масс.) земной коры. Из соединений, содержащих марганец, наиболее часто встречается минерал пиролюзит, представляющий собой диоксид марганца  . Большое значение имеют также минералы гаусманит
. Большое значение имеют также минералы гаусманит  и браунит
и браунит  .
.
СССР располагает большими запасами марганца. По запасам  с высоким содержанием марганца СССР занимает первое место в мире.
с высоким содержанием марганца СССР занимает первое место в мире.
Марганец получают либо электролизом раствора  , либо восстановлением из его оксидов кремнием в электрических печах. Второй (силикотермический) метод более экономичен, но дает менее чистый продукт. При электролитическом методе руду восстанавливают до соединений марганца со степенью окисленности
, либо восстановлением из его оксидов кремнием в электрических печах. Второй (силикотермический) метод более экономичен, но дает менее чистый продукт. При электролитическом методе руду восстанавливают до соединений марганца со степенью окисленности  , а затем растворяют в смеси серной кислоты с сульфатом аммония. Получающийся раствор подвергают электролизу. Снятые с катодов осадки металла переплавляют в слитки.
, а затем растворяют в смеси серной кислоты с сульфатом аммония. Получающийся раствор подвергают электролизу. Снятые с катодов осадки металла переплавляют в слитки.
Марганец — серебристо-белый твердый хрупкий металл. Его плотность  , температура плавления
, температура плавления  . Известны четыре кристаллические модификации марганца, каждая из которых термодинамически устойчива в определенном интервале температур. Ниже
. Известны четыре кристаллические модификации марганца, каждая из которых термодинамически устойчива в определенном интервале температур. Ниже  устойчив а-марганец, имеющий сложную структуру — в его элементарную ячейку входят 58 атомов. Сложность структуры марганца при температурах ниже
устойчив а-марганец, имеющий сложную структуру — в его элементарную ячейку входят 58 атомов. Сложность структуры марганца при температурах ниже  обусловливает его хрупкость.
обусловливает его хрупкость.
В ряду напряжений марганец находится между алюминием и цинком: стандартный электродный потенциал системы  равен —1,18 В. На воздухе марганец покрывается тонкой оксидной пленкой, предохраняющей его от дальнейшего окисления даже при нагревании. Но в мелкораздробленном состоянии марганец окисляется довольно легко. Вода при комнатной температуре действует на марганец очень медленно, при нагревании — быстрее. Он растворяется в разбавленных соляной и азотной кислотах, а также в горячей концентрированной серной кислоте (в холодной
равен —1,18 В. На воздухе марганец покрывается тонкой оксидной пленкой, предохраняющей его от дальнейшего окисления даже при нагревании. Но в мелкораздробленном состоянии марганец окисляется довольно легко. Вода при комнатной температуре действует на марганец очень медленно, при нагревании — быстрее. Он растворяется в разбавленных соляной и азотной кислотах, а также в горячей концентрированной серной кислоте (в холодной  он практически нерастворим); при этом образуются катионы
он практически нерастворим); при этом образуются катионы  .
.
Марганец применяется главным образом в производстве легированных сталей. Марганцовистая сталь, содержащая до  , обладает высокими твердостью и прочностью. Из нее изготовляют рабочие части дробильных машин, шаровых мельниц, железнодорожные рельсы. Кроме того, марганец входит в состав ряда сплавов на основе магния; он повышает их стойкость против коррозии. Сплав меди с марганцем и никелем — манганин (см. §
, обладает высокими твердостью и прочностью. Из нее изготовляют рабочие части дробильных машин, шаровых мельниц, железнодорожные рельсы. Кроме того, марганец входит в состав ряда сплавов на основе магния; он повышает их стойкость против коррозии. Сплав меди с марганцем и никелем — манганин (см. §  дает низким температурным коэффициентом электрического сопротивления.
дает низким температурным коэффициентом электрического сопротивления.
В небольших количествах марганец вводится во многие сплавы алюминия.
Марганец образует четыре простых оксида  и
и  и смешанный оксид
и смешанный оксид  . Первые два оксида обладают основными свойствами, диоксид марганца
. Первые два оксида обладают основными свойствами, диоксид марганца  амфотерен, а высший оксид
амфотерен, а высший оксид  является ангидридом марганцовой кислоты
является ангидридом марганцовой кислоты  . Известны также производные марганца (IV), но соответствующий оксид
. Известны также производные марганца (IV), но соответствующий оксид  не получен.
не получен.
В практическом отношении наиболее важны соединения марганца (II), диоксид марганца и соли марганцовой кислоты—перманганаты, в которых марганец находится в степени окисленности  .
.
Соединения марганца (II). Соли марганца (II) получаются при растворении марганца в разбавленных кислотах или при действии кислот на различные природные соединения марганца. Так, из раствора, остающегося после получения хлора действием соляной кислоты на диоксид марганца, выкристаллизовывается хлорид марганца  в виде бледно-розовых кристаллов. В твердом виде соли марганца (II) обычно розового цвета, растворы же их почти бесцветны.
в виде бледно-розовых кристаллов. В твердом виде соли марганца (II) обычно розового цвета, растворы же их почти бесцветны.
При действии щелочей на растворы солей марганца (II) выпадает белый осадок — гидроксид  . Осадок легко растворяется в кислотах. На воздухе он быстро темнеет, окисляясь в бурый гидроксид
. Осадок легко растворяется в кислотах. На воздухе он быстро темнеет, окисляясь в бурый гидроксид  .
.
Оксид  , или закись марганца,
, или закись марганца,  получается в виде зеленого порошка при восстановлении других оксидов марганца водородом.
получается в виде зеленого порошка при восстановлении других оксидов марганца водородом.
Соединения марганца (IV). Наиболее стойким соединением марганца является темно-бурый диоксид марганца  он легко образуется как при окислении низших, так и при восстановлении высших соединений марганца. Как уже указывалось,
он легко образуется как при окислении низших, так и при восстановлении высших соединений марганца. Как уже указывалось,  — амфотерный оксид; однако и кислотные, и основные свойства выражены у него очень слабо.
— амфотерный оксид; однако и кислотные, и основные свойства выражены у него очень слабо.
В кислой среде диоксид марганца — довольно энергичный окислитель. В качестве окислителя его применяют при получении хлора из соляной кислоты и в сухих гальванических элементах. Соли марганца (IV), например  и
и  , весьма нестойки.
, весьма нестойки.
Соединения  и (VII). При сплавлении диоксида марганца с карбонатом и нитратом калия получается зеленый сплав, растворяющийся в воде с образованием красивого зеленого раствора. Из этого раствора можно выделить темно-зеленые кристаллы манганита калия
и (VII). При сплавлении диоксида марганца с карбонатом и нитратом калия получается зеленый сплав, растворяющийся в воде с образованием красивого зеленого раствора. Из этого раствора можно выделить темно-зеленые кристаллы манганита калия  соли марганцовистой кислоты
соли марганцовистой кислоты  , очень нестойкой даже в растворе.
, очень нестойкой даже в растворе.
Реакцию образования манганата калия можно выразить уравнением:

Если раствор манганата оставить стоять  воздухе, то окраска его постепенно изменяется, переходя из зеленой в малиновую, причем образуется темно-бурый осадок. Это объясняется тем, что в водном растворе манганаты самопроизвольно превращаются в соли марганцовой кислоты
воздухе, то окраска его постепенно изменяется, переходя из зеленой в малиновую, причем образуется темно-бурый осадок. Это объясняется тем, что в водном растворе манганаты самопроизвольно превращаются в соли марганцовой кислоты  (перманганаты) с одновременным образованием диоксида марганца. Реакция выражается уравнением
(перманганаты) с одновременным образованием диоксида марганца. Реакция выражается уравнением

или в ионно-молекулярной форме:

При этой реакции один  окисляет два других таких же иона в ионы
окисляет два других таких же иона в ионы  , а сам восстанавливается, образуя
, а сам восстанавливается, образуя  .
.
Процесс превращения манганата в перманганат обратим. Поэтому в присутствии избытка гидроксид-ионов зеленый раствор манганата долгое время может сохраняться без изменения. Если же прибавить кислоту, связывающую гидроксид-ионы, зеленая окраска почти мгновенно изменяется  малиновую.
малиновую.
При действии сильных окислителей (например, хлора) на раствор манганата последний полностью превращается в перманганат:

Перманганат калия  — наиболее широко применяемая соль марганцовой кислоты. Кристаллизуется он в виде красивых темно-фиолетовых, почти черных призм, умеренно растворимых в воде. Растворы
— наиболее широко применяемая соль марганцовой кислоты. Кристаллизуется он в виде красивых темно-фиолетовых, почти черных призм, умеренно растворимых в воде. Растворы  имеют темно-малиновый, а при больших концентрациях — фиолетовый цвет, свойственный ионам
имеют темно-малиновый, а при больших концентрациях — фиолетовый цвет, свойственный ионам  . Как и все соединения марганца (VII), перманганат калия — сильный окислитель. Он легко окисляет многие органические вещества, превращает соли
. Как и все соединения марганца (VII), перманганат калия — сильный окислитель. Он легко окисляет многие органические вещества, превращает соли  в соли железа (III), сернистую кислоту окисляет в серную, из соляной кислоты выделяет хлор и т. д.
в соли железа (III), сернистую кислоту окисляет в серную, из соляной кислоты выделяет хлор и т. д.
Вступая в окислительно-восстановительные реакции,  восстанавливаться в различной степени. В зависимости от
восстанавливаться в различной степени. В зависимости от  среды продукт восстановления может представлять собою
среды продукт восстановления может представлять собою  (в кислой среде),
(в кислой среде),  (в нейтральной или в слабощелочной среде) или
(в нейтральной или в слабощелочной среде) или  (в сильнощелочной среде).
(в сильнощелочной среде).
Проиллюстрируем эти три случая реакциями взаимодействия  с растворимыми сульфитами. Если к подкисленному серной кислотой фиолетовому раствору
с растворимыми сульфитами. Если к подкисленному серной кислотой фиолетовому раствору  прибавить сульфит калия
прибавить сульфит калия  , то жидкость становится почти бесцветной, так как образующаяся соль марганца (II) имеет бледно-розовую окраску. Реакция выражается уравнением
, то жидкость становится почти бесцветной, так как образующаяся соль марганца (II) имеет бледно-розовую окраску. Реакция выражается уравнением

или в ионно-молекулярной форме:

При действии сульфита калия на нейтральный раствор перманганата калия тоже происходит обесцвечивание раствора, но, кроме того, выпадает бурый осадок диоксида марганца и раствор приобретает щелочную реакцию

или в ионно-молекулярной форме:

При большой концентрации щелочи и малом количестве восстановителя образуются ионы манганата согласно уравнению:

Как энергичный окислитель перманганат калия широко применяют в химических лабораториях и производствах; он служит также прекрасным дезинфицирующим средством.
При нагревании в сухом виде перманганат калия уже при температуре около  разлагается согласно уравнению:
разлагается согласно уравнению:

Этой реакцией иногда пользуются в лаборатории для получения кислорода.
Соответствующая перманганатам свободная марганцовая кислота  в безводном состоянии не получена и известна только в растворе. Концентрацию ее раствора можно довести до
в безводном состоянии не получена и известна только в растворе. Концентрацию ее раствора можно довести до  . Это очень сильная кислота, в водном растворе полностью диссоциированная на ионы: ее кажущаяся степень диссоциации в
. Это очень сильная кислота, в водном растворе полностью диссоциированная на ионы: ее кажущаяся степень диссоциации в  растворе равна
растворе равна  .
.
Оксид марганца (VII), или марганцовый ангидрид,  может быть получен действием концентрированной серной кислоты на перманганат калия:
может быть получен действием концентрированной серной кислоты на перманганат калия:

Марганцовый ангидрид — зеленовато-бурая маслянистая жидкость. Он очень неустойчив: при нагревании или при соприкосновении с горючими веществами он со взрывом разлагается на диоксид марганца и кислород.
| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- Глава I. АТОМНО-МОЛЕКУЛЯРНОЕ УЧЕНИЕ
- 4. Закон сохранения массы.
- 5. Основное содержание атомно-молекулярного учения.
- 6. Простое вещество и химический элемент.
- 7. Закон постоянства состава.
- 8. Закон объемных отношений.
- 9. Атомные и молекулярные массы. Моль.
- 10. Определение молекулярных масс веществ, находящихся в газообразном состоянии.
- 11. Парциальное давление газа.
- 12. Эквивалент. Закон эквивалентов.
- 13. Определение атомных масс. Валентность.
- 14. Химическая символика.
- 15. Важнейшие классы и номенклатура неорганических веществ.
- 16. Химические расчеты.
- Глава II ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА
- 17. Периодический закон Д. И. Менделеева.
- 18. Периодическая система элементов.
- 19. Значение периодической системы.
- Глава III СТРОЕНИЕ АТОМА. РАЗВИТИЕ ПЕРИОДИЧЕСКОГО ЗАКОНА
- 20. Радиоктивность.
- 21. Ядерная модель атома.
- 22. Атомные спектры.
- 23. Квантовая теория света.
- 24. Строение электронной оболочки атома по Бору.
- 25. Исходные представления квантовой механики.
- 26. Волновая функция.
- 27. Энергетическое состояние электрона в атоме.
- 29. Орбитальное квантовое число. Формы электронных облаков.
- 30. Магнитное и спиновое квантовые числа.
- 31. Многоэлектронные атомы.
- 32. Принцип Паули. Электронная структура атомов и периодическая система элементов.
- 33. Размеры атомов и ионов.
- 34. Энергия ионизации и сродство к электрону.
- 35. Строение атомных ядер. Изотопы.
- 36. Радиоактивные элементы и их распад.
- 37. Искусственная радиоктивность. Ядерные реакции.
- Глава IV. ХИМИЧЕСКАЯ СВЯЗЬ И СТРОЕНИЕ МОЛЕКУЛ
- 38. Теория химического строения.
- 39. Ковалентная связь. Метод валентных связей.
- 40. Неполярная и полярная ковалентная связь.
- 41. Способы образования ковалентной связи.
- 42. Направленность ковалентной связи.
- 43. Гибридизация атомных электронных орбиталей.
- 44. Многоцентровые связи.
- 45. Метод молекулярных орбиталей.
- 46. Ионная связь.
- 47. Водородная связь.
- Глава V. СТРОЕНИЕ ТВЕРДОГО ТЕЛА И ЖИДКОСТИ
- 48. Межмолекулярное взаимодействие.
- 49. Кристаллическое состояние вещества.
- 50. Внутреннее строение кристаллов.
- 51. Реальные кристаллы.
- 52. Аморфное состояние вещества.
- 53. Жидкости.
- Глава VI. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ПРОТЕКАНИЯ ХИМИЧЕСКИХ РЕАКЦИЙ
- 54. Превращения энергии при химических реакциях.
- 55. Термохимия.
- 56. Термохимические расчеты.
- 57. Скорость химической реакции.
- 59. Зависимость скорости реакции от температуры и от природы реагирующих веществ.
- 60. Катализ.
- 61. Скорость реакции в гетерогенных системах.
- 62. Цепные реакции.
- 63. Необратимые и обратимые реакции. Химическое равновесие.
- 64. Смещение химического равновесия. Принцип Ле Шателье.
- 65. Факторы, определяющие направление протекания химических реакций.
- 66. Термодинамические величины. Внутренняя энергия и энтальпия.
- 67. Термодинамические величины. Энтропия и энергия Гиббса.
- 68. Стандартные термодинамические величины. Химико-термодинамические расчеты.
- Глава VII. ВОДА, РАСТВОРЫ
- 69. Вода в природе.
- 70. Физические свойства воды.
- 71. Диаграмма состояния воды.
- 72. Химические свойства воды.
- 73. Характеристика растворов. Процесс растворения.
- 74. Способы выражения состава растворов.
- 75. Гидраты и кристаллогидраты.
- 76. Растворимость.
- 77. Пересыщенные растворы.
- 78. Осмос.
- 79. Давление пара растворов.
- 80. Замерзание и кипение растворов.
- Глава VIII. РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- 81. Особенности растворов солей, кислот и оснований.
- 82. Теория электролитической диссоциации.
- 83. Процесс диссоциации.
- 84. Степень диссоциации. Сила электролитов.
- 85. Константа диссоциации.
- 86. Сильные электролиты.
- 87. Свойства кислот, оснований и солей с точки зрения теории электролитической диссоциации.
- 88. Ионно-молекулярные уравнения.
- 89. Произведение растворимости.
- 90. Диссоциация воды. Водородный показатель.
- 91. Смещение ионных равновесий.
- 92. Гидролиз солей.
- Глава IX. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ. ОСНОВЫ ЭЛЕКТРОХИМИИ
- 93. Окисленность элементов.
- 94. Окислительно-восстановительные реакции.
- 95. Составление уравнений окислительно-восстановительных реакций.
- 96. Важнейшие окислители и восстановители.
- 97. Окислительно-восстановительная двойственность.
- 98. Химические источники электрической энергии.
- 99. Электродные потенциалы.
- 100. Ряд напряжений металлов.
- 101. Электролиз.
- 102. Законы электролиза.
- 103. Электролиз в промышленности.
- 104. Электрохимическая поляризация.
- Глава X. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДЫ
- 105. Дисперсное состояние вещества.
- 106. Состояние вещества на границе раздела фаз.
- 107. Коллоиды и коллоидные растворы.
- 108. Дисперсионный анализ.
- 109. Сорбция и сорбционные процессы.
- 110. Ионообменная адсорбция.
- 111. Хроматография.
- 112. Электрокинетические явления.
- 113. Устойчивость и коагуляция дисперсных систем.
- 114. Структурообразование в дисперсных системах.
- Глава XI. ВОДОРОД
- 115. Водород в природе. Получение водорода.
- 116. Свойства и применение водорода.
- 117. Пероксид водорода
- Глава XII. ГАЛОГЕНЫ
- 118. Галогены в природе. Физические свойства галогенов.
- 119. Химические свойства галогенов.
- 120. Получение и применение галогенов.
- 121. Соединения галогенов с водородом.
- 122. Кислородсодержащие соединения галогенов.
- Глава XIII. ГЛАВНАЯ ПОДГРУППА ШЕСТОЙ ГРУППЫ
- 123. Кислород в природе. Воздух.
- 124. Получение и свойства кислорода.
- 125. Озон.
- 126. Сера в природе. Получение серы.
- 127. Свойства и применение серы.
- 128. Сероводород. Сульфиды.
- 129. Диоксид серы. Сернистая кислота.
- 130. Триоксид серы. Серная кислота.
- 131. Получение и применение серной кислоты.
- 132. Пероксодвусерная кислота.
- 133. Тиосерная кислота.
- 134. Соединения серы с галогенами.
- 135. Селен (Selenium). Теллур (Tellurium).
- Глава XIV. ГЛАВНАЯ ПОДГРУППА ПЯТОЙ ГРУППЫ
- 136. Азот в природе. Получение и свойства азота.
- 137. Аммиак. Соли аммония.
- 138. Фиксация атмосферного азота. Получение аммиака.
- 139. Гидразин. Гидроксиламин. Азидоводород.
- 140. Оксиды азота.
- 141. Азотистая кислота.
- 142. Азотная кислота.
- 143. Промышленное получение азотной кислоты.
- 144. Круговорот азота в природе.
- 145. Фосфор в природе. Получение и свойства фосфора.
- 146. Соединения фосфора с водородом и галогенами.
- 147. Оксиды и кислоты фосфора.
- 148. Минеральные удобрения.
- 149. Мышьяк (Arsenicum).
- 150. Сурьма (Stibium).
- 151. Висмут (Bismuthum).
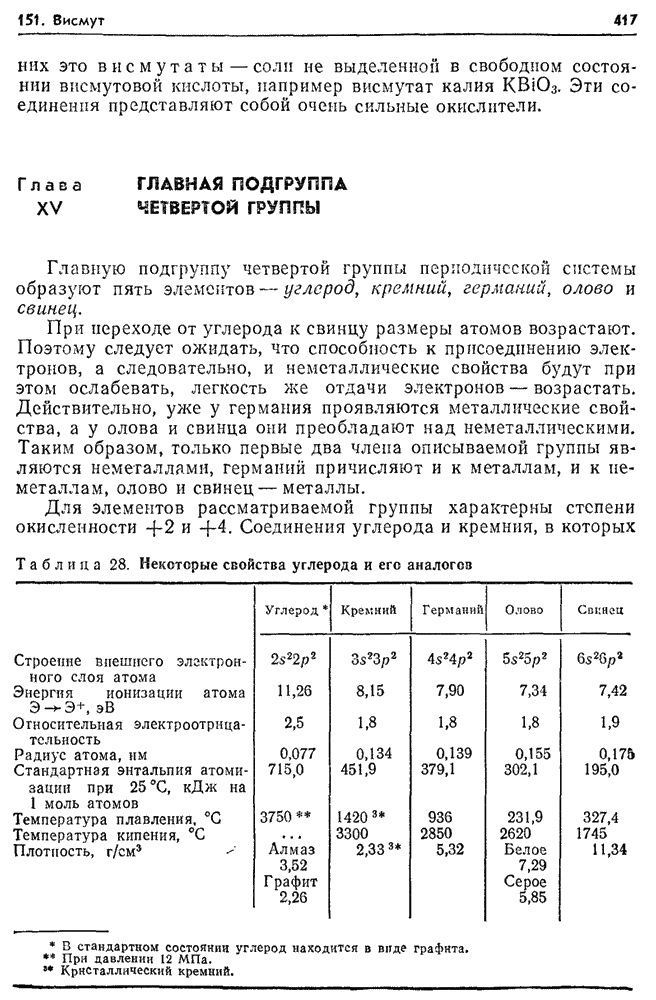
- Глава XV. ГЛАВНАЯ ПОДГРУППА ЧЕТВЕРТОЙ ГРУППЫ
- 152. Углерод в природе.
- 153. Аллотропия углерода.
- 154. Химические свойства углерода. Карбиды.
- 155. Диоксид углерода. Угольная кислота.
- 156. Оксид углерода (II).
- 157. Соединения углерода с серой и азотом.
- 158. Топливо и его виды.
- 159. Газообразное топливо.
- 160. Общая характеристика органических соединений.
- 161. Отличительные особенности органических соединений.
- 162. Теория химического строения органических соединений.
- 163. Классификация органических соединений.
- 164. Предельные (насыщенные) углеводороды.
- 165. Непредельные (ненасыщенные) углеводороды.
- 166. Предельные циклические углеводороды.
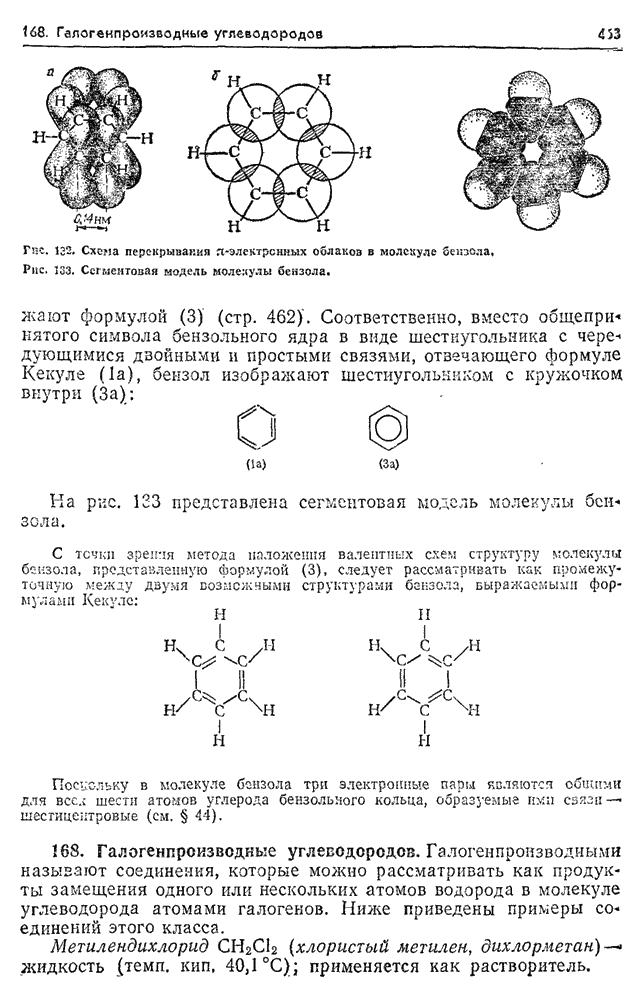
- 167. Ароматические углеводороды.
- 168. Галогенпроизводные углеводородов.
- 169. Спирты и фенолы.
- 170. Простые эфиры.
- 171. Альдегиды и кетоны.
- 172. Карбоновые кислоты.
- 173. Сложные эфиры карбоновых кислот. Жиры.
- 174. Углеводы.
- 175. Амины.
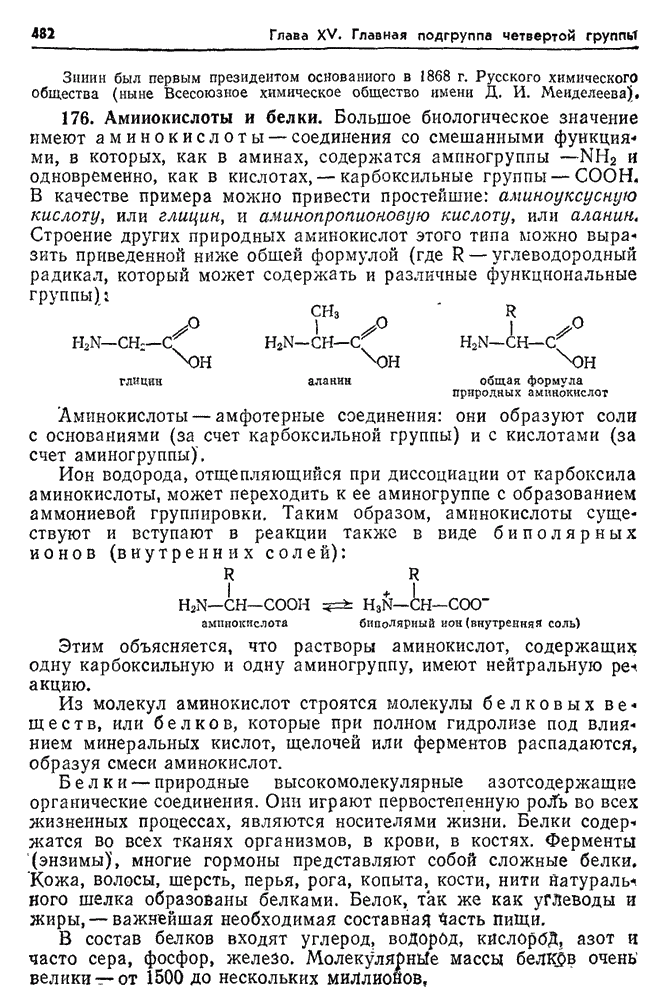
- 176. Аминокислоты и белки.
- 177. Природные и синтетические высокомолекулярные соединения (полимеры).
- 178. Кремний в природе. Получение и свойства кремния.
- 179. Соединения кремния с водородом и галогенами.
- 180. Диоксид кремния.
- 181. Кремниевые кислоты и их соли.
- 182. Стекло.
- 183. Керамика.
- 184. Цемент.
- 185. Кремнийорганические соединения.
- 186. Германий (Germanium).
- 187. Олово (Stannuin).
- 188. Свинец (Plumbum).
- 189. Свинцовый аккумулятор.
- Глава XVI. ОБЩИЕ СВОЙСТВА МЕТАЛЛОВ. СПЛАВЫ
- 190. Физические и химические свойства металлов. Электронное строение металлов, изоляторов и полупроводников.
- 191. Кристаллическое строение металлов.
- 192. Добывание металлов из руд.
- 193. Получение металлов высокой чистоты.
- 194. Сплавы.
- 195. Диаграммы состояния металлических систем.
- 196. Коррозия металлов.
- Глава XVII. ПЕРВАЯ ГРУППА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ
- 197. Щелочные металлы в природе.
- 198. Натрий (Natrium).
- 199. Калий (Kalium).
- ПОДГРУППА МЕДИ
- 200. Медь. (Cuprum).
- 201. Серебро (Argentum).
- 202. Золото (Aurum).
- Глава XVIII. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- 203. Основные положения координационной теории.
- 204. Основные типы и номенклатура комплексных соединений.
- 205. Пространственное строение и изомерия комплексных соединений.
- 206. Природа химической связи в комплексных соединениях.
- 207. Диссоциация комплексных соединений в растворах.
- 208. Влияние координации на свойства лигандов и центрального атома.
- Глава XIX. ВТОРАЯ ГРУППА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ
- 209. Бериллий (Beryllium).
- 210. Магний (Magnesium).
- 211. Кальций (Calcium).
- 212. Жесткость природных вод и ее устранение.
- 213. Стронций (Strontium). Барий (Barium).
- 214. Цинк (Zincum).
- 215. Кадмий (Cadmium).
- 216. Ртуть (Hydrargyrum).
- Глава XX. ТРЕТЬЯ ГРУППА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ
- 217. Бор (Borum).
- 218. Алюминий (Aluminium).
- 219. Галлий (Gallium). Иидий (Indium). Таллий (Thallium).
- ПОБОЧНАЯ ПОДГРУППА ТРЕТЬЕЙ ГРУППЫ. ЛАНТАНОИДЫ. АКТИНОИДЫ
- 220. Подгруппа скандия.
- 221. Лантаноиды.
- 222. Актиноиды.
- Глава XXI. ПОБОЧНЫЕ ПОДГРУППЫ ЧЕТВЕРТОЙ, ПЯТОЙ, ШЕСТОЙ И СЕДЬМОЙ ГРУПП
- ПОДГРУППА ТИТАНА
- 224. Титан (Titanium).
- 225. Цирконий (Zirconium). Гафний (Hafnium).
- ПОДГРУППА ВАНАДИЯ
- 226. Ванадий (Vanadium).
- 227. Ниобий (Niobium). Тантал (Tantalum).
- ПОДГРУППА ХРОМА
- 228. Хром (Chromium).
- 229. Молибден (Mollbdenium).
- 230. Вольфрам (Wolfram).
- ПОДГРУППА МАРГАНЦА
- 231. Марганец (Manganum).
- 232. Рений (Rhenium).
- Глава XXII. ВОСЬМАЯ ГРУППА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ
- 233. Общая характеристика благородных газов.
- 234. Гелий (Helium).
- 235. Неон. Аргон.
- ПОБОЧНАЯ ПОДГРУППА ВОСЬМОЙ ГРУППЫ
- 236. Железо (Ferrum).
- 237. Значение железа и его сплавов в технике. Развитие металлургии в СССР.
- 238. Физические свойства железа. Диаграмма состояния системы железо — углерод.
- 239. Производство чугуна и стали.
- 240. Термическая обработка стали.
- 241. Сплавы железа.
- 242. Химические свойства железа. Соединения железа.
- 243. Кобальт (Cobaltum).
- 244. Никель (Niccolum).
- 245. Общая характеристика платиновых металлов.
- 246. Платина (Platinum).
- 247. Палладий (Palladium). Иридий (Iridium).
- ПРИЛОЖЕНИЕ
- Некоторые единицы СИ
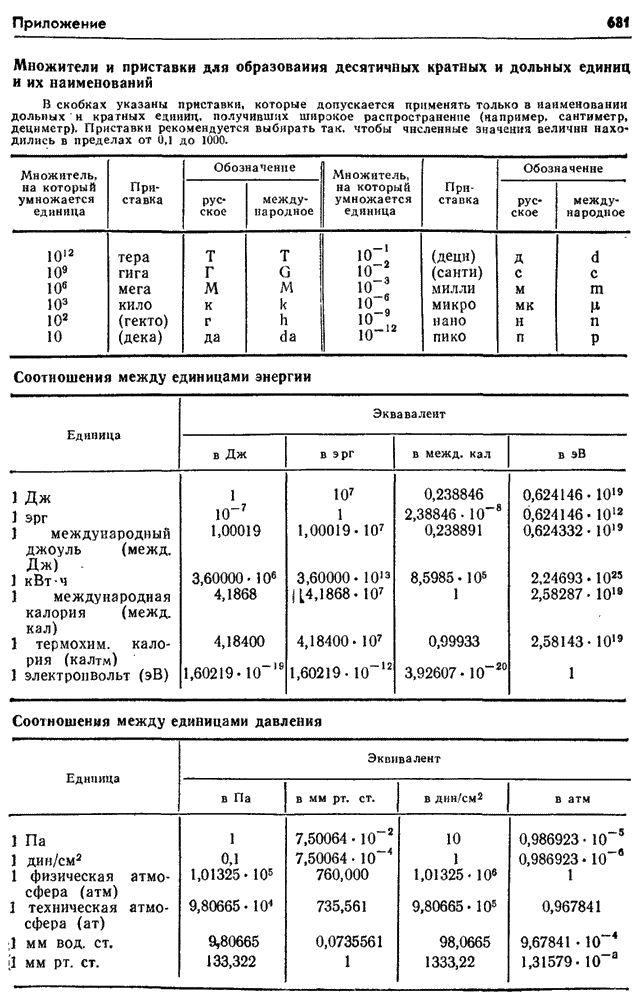
- Множители и приставки для образования десятичных кратных и дольных единиц и их наименований
- Соотношения между некоторыми внесистемными единицами и единицами СИ
- Литература для углубленного изучения общей и неорганической химии