| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
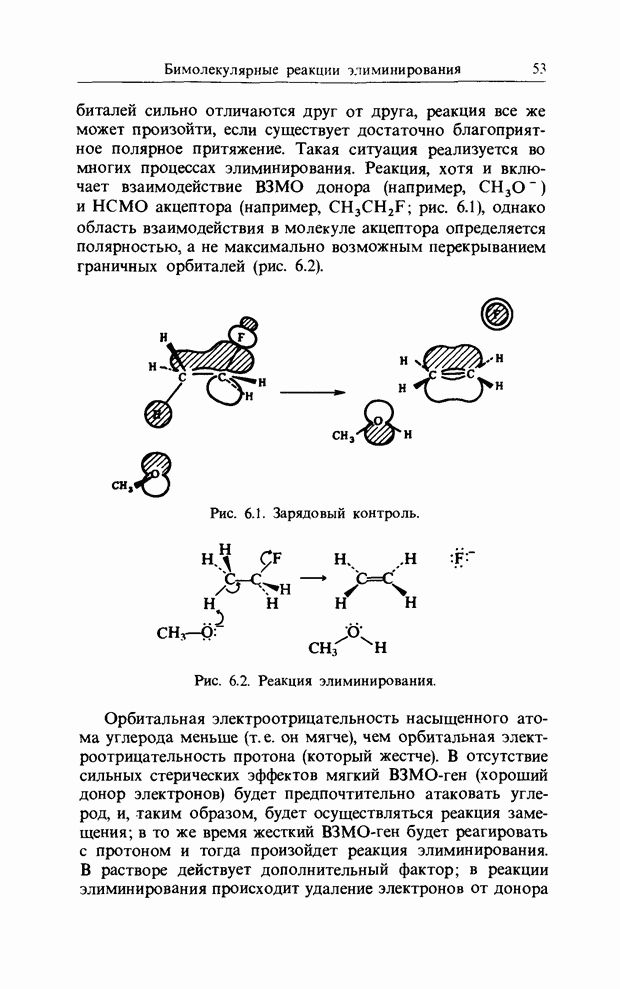
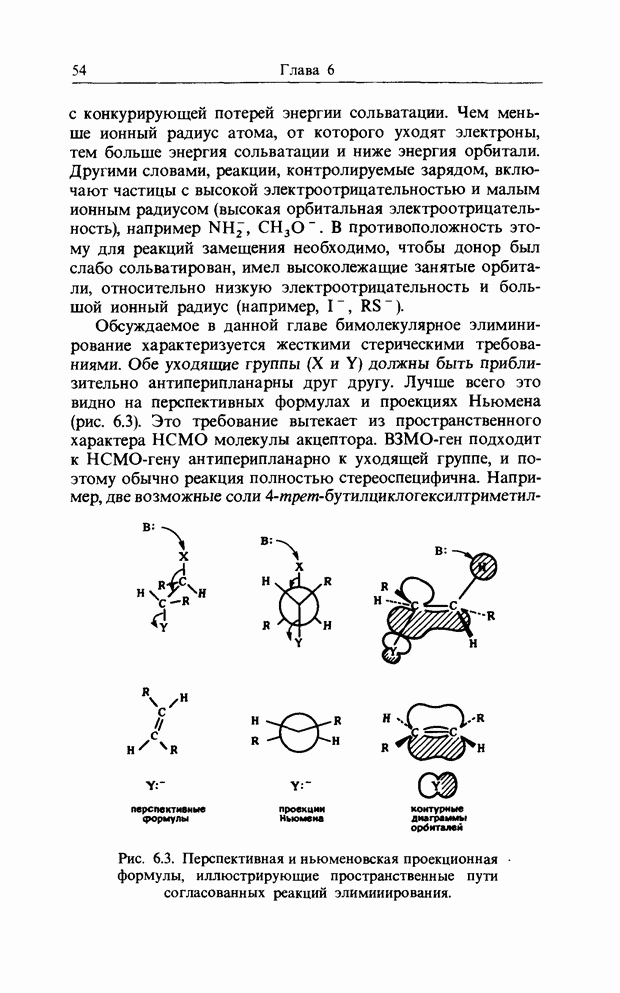
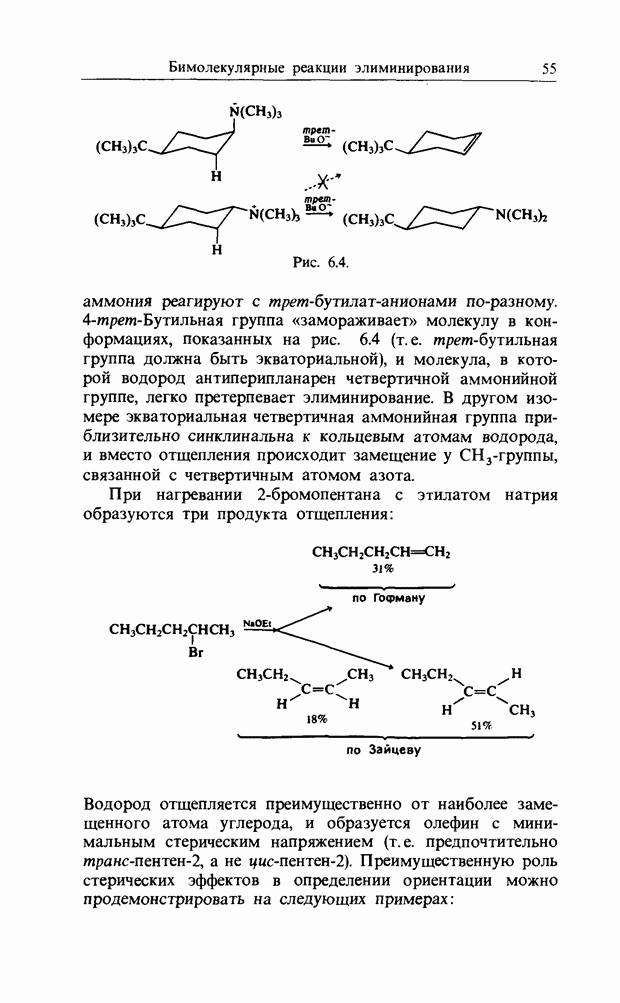
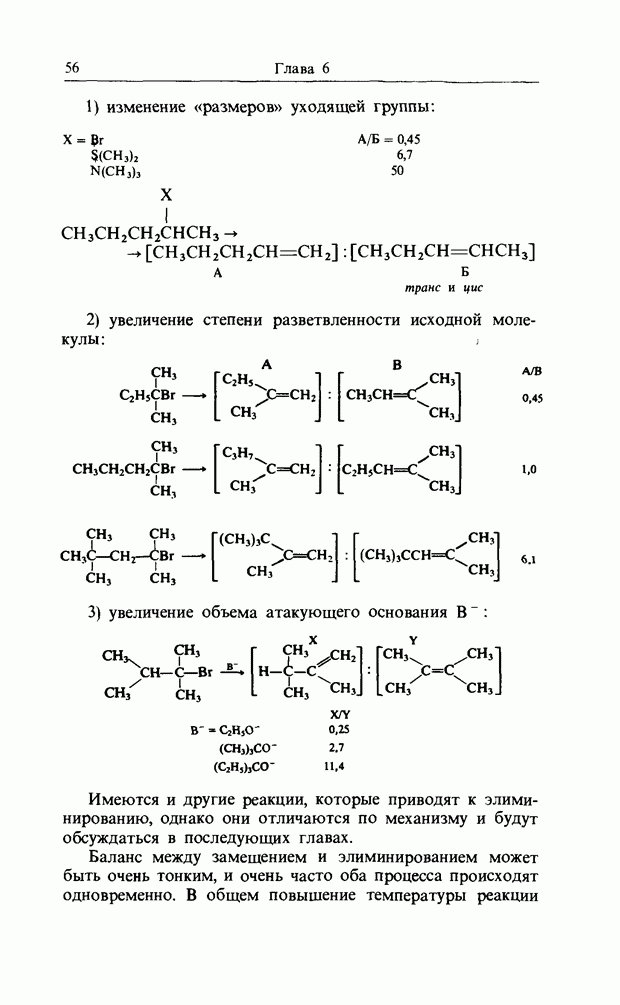
10. АЛЬТЕРНАНТНЫЕ УГЛЕВОДОРОДЫ И АРОМАТИЧНОСТЬ
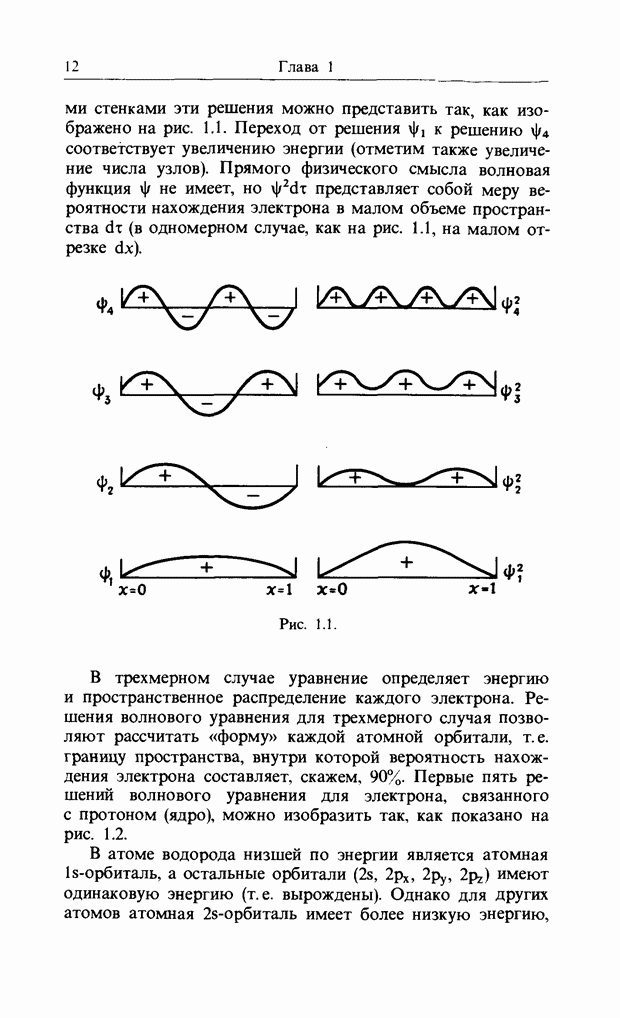
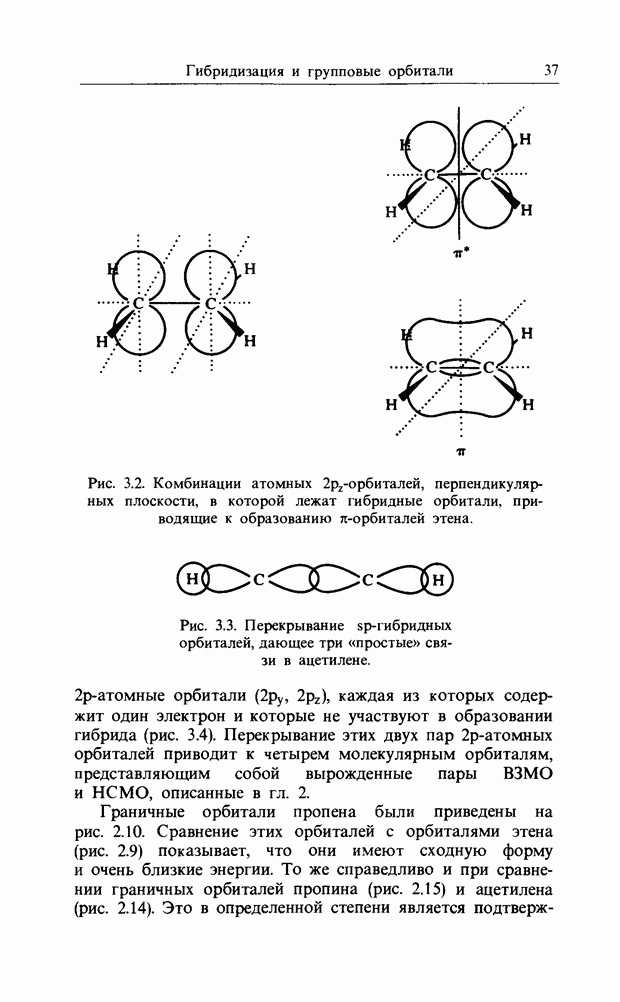
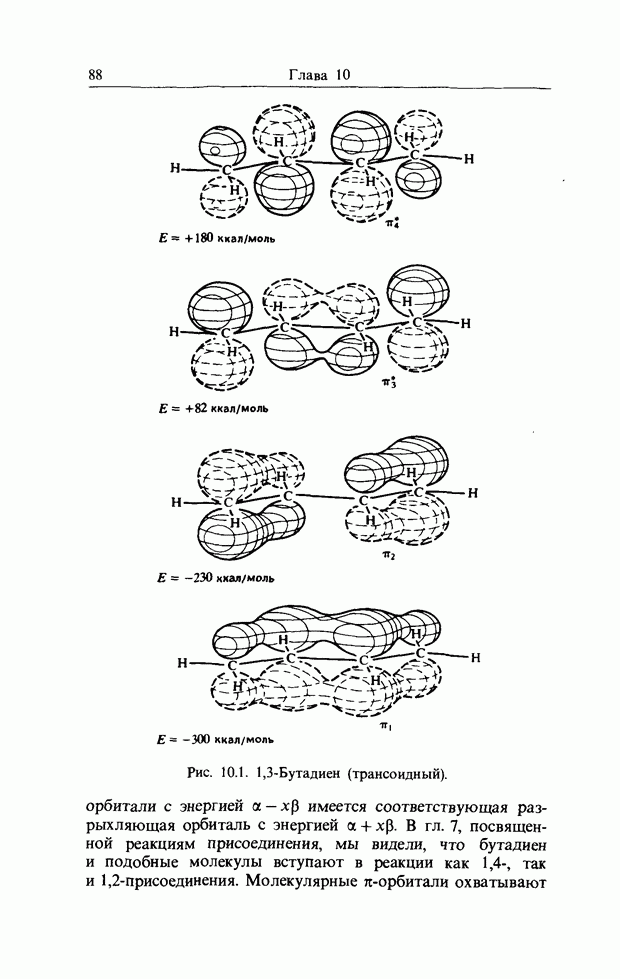
Молекулярные  -орбитали сопряженных молекул типа бутадиена (рис. 10.1) можно разбить на пары с энергиями
-орбитали сопряженных молекул типа бутадиена (рис. 10.1) можно разбить на пары с энергиями  , где
, где  и
и  - постоянные. Для каждой связывающей
- постоянные. Для каждой связывающей
(см. скан)
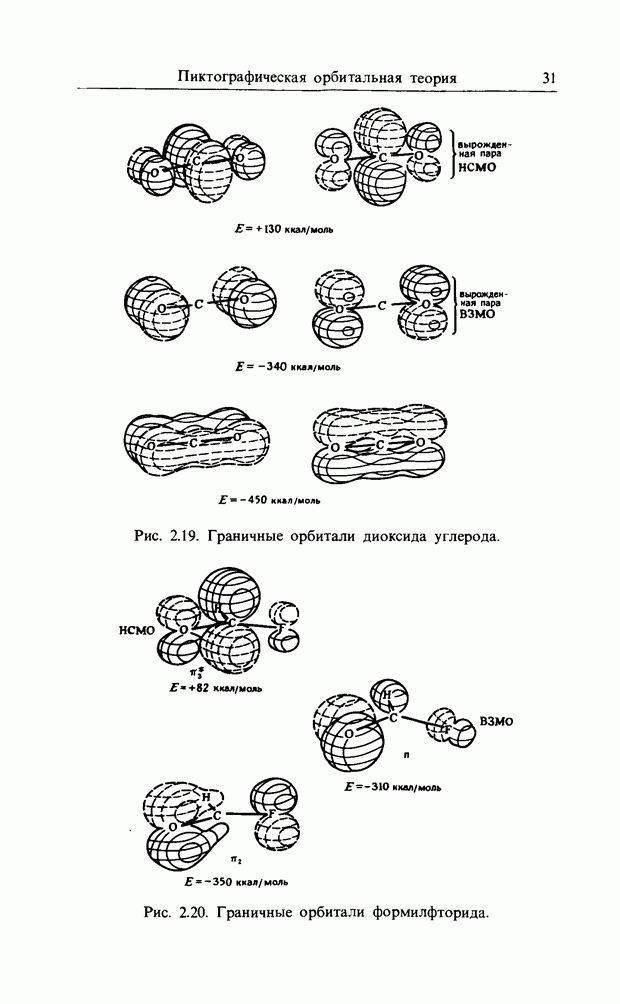
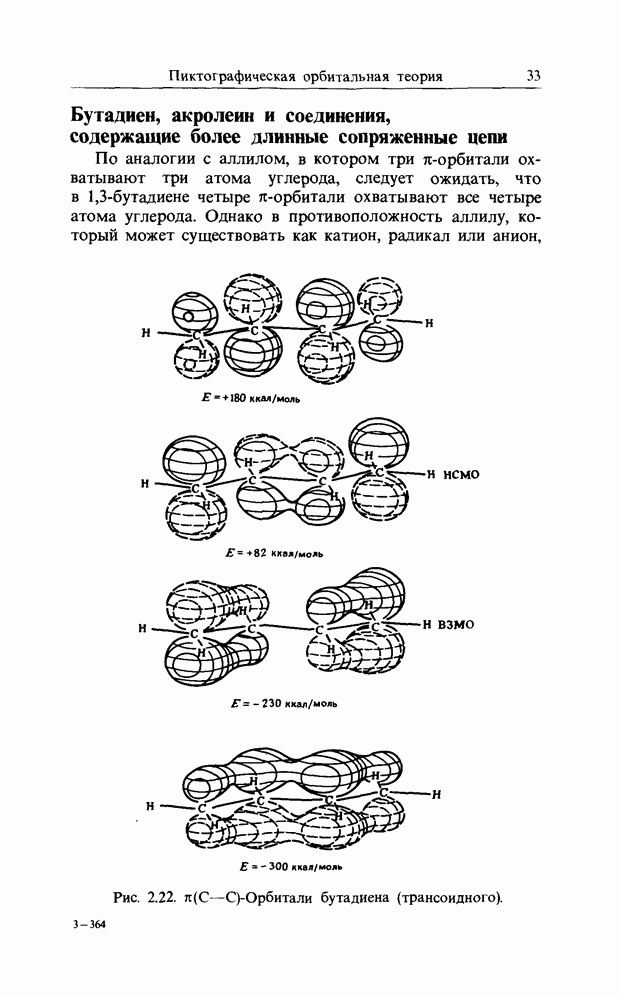
Рис. 10.1. 1,3-Бутадиен (трансоидный).
орбитали с энергией  имеется соответствующая разрыхляющая орбиталь с энергией
имеется соответствующая разрыхляющая орбиталь с энергией  . В гл. 7, посвященной реакциям присоединения, мы видели, что бутадиен и подобные молекулы вступают в реакции как 1,4-, так и 1,2-присоединения. Молекулярные
. В гл. 7, посвященной реакциям присоединения, мы видели, что бутадиен и подобные молекулы вступают в реакции как 1,4-, так и 1,2-присоединения. Молекулярные  -орбитали охватывают
-орбитали охватывают
всю молекулу целиком, и то же самое применимо к молекулярным  -орбиталям гексатриена и октатетраена. Обе эти молекулы могут вступать в реакцию сопряженного присоединения (т.е. 1,6- и 1,8-присоединение соответственно). В аллильном и пентадиенильном радикалах
-орбиталям гексатриена и октатетраена. Обе эти молекулы могут вступать в реакцию сопряженного присоединения (т.е. 1,6- и 1,8-присоединение соответственно). В аллильном и пентадиенильном радикалах

расположение я-орбиталей такое же (т.е. орбитали можно разбить на пары с энергиями  ), но, поскольку в этих радикалах число атомов углерода в цепи сопряжения нечетное, должна существовать несвязывающая орбиталь с х = 0 (т.е. с энергией а). Кроме того, вследствие парности свойств
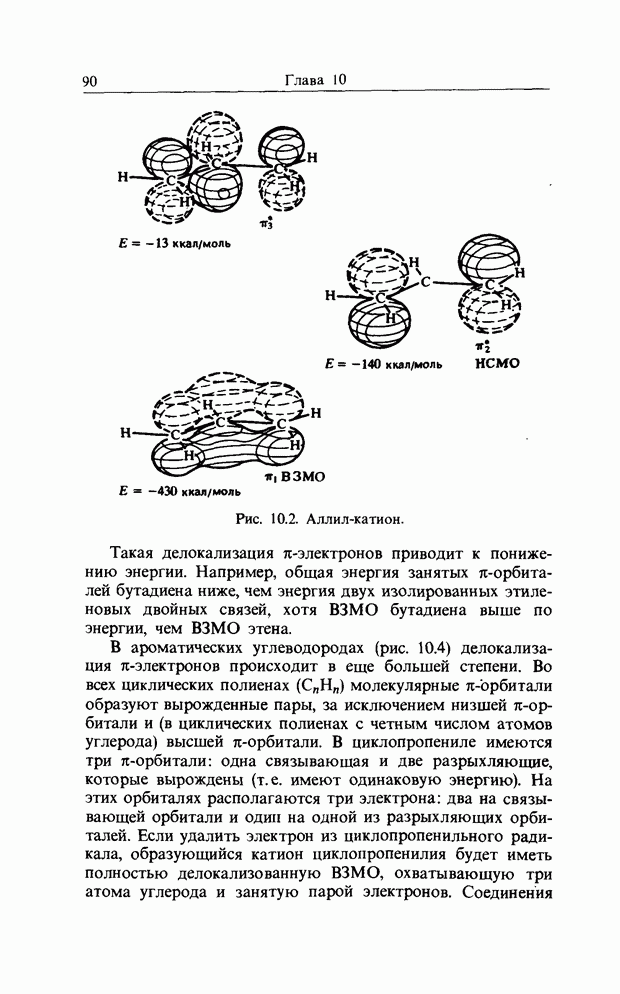
), но, поскольку в этих радикалах число атомов углерода в цепи сопряжения нечетное, должна существовать несвязывающая орбиталь с х = 0 (т.е. с энергией а). Кроме того, вследствие парности свойств  -молекулярных орбиталей сопряженных систем несвязывающая орбиталь будет иметь узел на каждом перемежающемся (через один) атоме углерода. Это имеет важные последствия для неспаренного электрона аллила (или пентадиенила), который и будет занимать эту несвязывающую орбиталь. Если к аллильному радикалу добавить электрон, то в образовавшемся аллил-анионе отрицательный заряд будет в равной степени распределен по концевым атомам углерода; аналогично если неспаренный электрон удалить из аллильного радикала, то в получившемся катионе (рис. 10.2) положительный заряд будет поровну распределен между концевыми атомами углерода.
-молекулярных орбиталей сопряженных систем несвязывающая орбиталь будет иметь узел на каждом перемежающемся (через один) атоме углерода. Это имеет важные последствия для неспаренного электрона аллила (или пентадиенила), который и будет занимать эту несвязывающую орбиталь. Если к аллильному радикалу добавить электрон, то в образовавшемся аллил-анионе отрицательный заряд будет в равной степени распределен по концевым атомам углерода; аналогично если неспаренный электрон удалить из аллильного радикала, то в получившемся катионе (рис. 10.2) положительный заряд будет поровну распределен между концевыми атомами углерода.
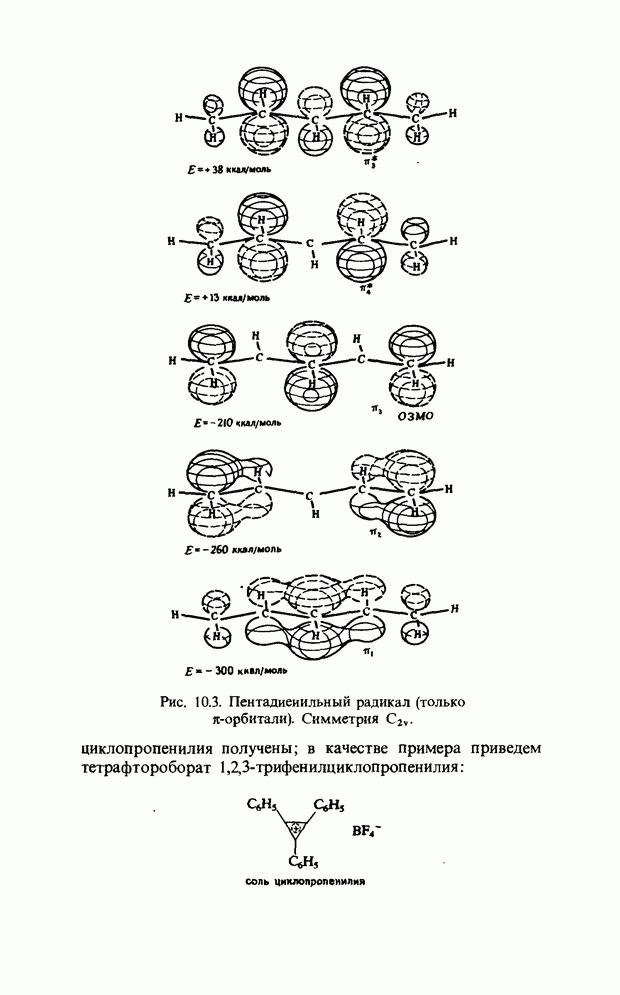
В пентадиенил-анионе отрицательный заряд будет центрирован на атомах углерода в положениях 1, 3 и 5, и, конечно, положительный заряд в пентадиенил-катионе будет в этих же положениях. Так же будет распределен неспаренный электрон в пентадиенильном радикале (рис. 10.3).
С точки зрения теории резонанса можно представить две или три канонические формы:

резонансные структуры аллильного катиона

резонансные структуры пентадненильного радикала

Рис. 10.2. Аллил-катион.
Такая делокализация  -электронов приводит к понижению энергии. Например, общая энергия занятых
-электронов приводит к понижению энергии. Например, общая энергия занятых  -орбиталей бутадиена ниже, чем энергия двух изолированных этиленовых двойных связей, хотя В3МО бутадиена выше по энергии, чем В3МО этена.
-орбиталей бутадиена ниже, чем энергия двух изолированных этиленовых двойных связей, хотя В3МО бутадиена выше по энергии, чем В3МО этена.
В ароматических углеводородах (рис. 10.4) делокализация  -электронов происходит в еще большей степени. Во всех циклических полиенах
-электронов происходит в еще большей степени. Во всех циклических полиенах  молекулярные
молекулярные  -орбитали образуют вырожденные пары, за исключением низшей
-орбитали образуют вырожденные пары, за исключением низшей  -орбитали и (в циклических полиенах с четным числом атомов углерода) высшей
-орбитали и (в циклических полиенах с четным числом атомов углерода) высшей  -орбитали. В циклопропениле имеются три
-орбитали. В циклопропениле имеются три  -орбитали: одна связывающая и две разрыхляющие, которые вырождены (т.е. имеют одинаковую энергию). На этих орбиталях располагаются три электрона: два на связывающей орбитали и один на одной из разрыхляющих орбиталей. Если удалить электрон из циклопропенильного радикала, образующийся катион циклопропенилия будет иметь полностью делокализованную В3МО, охватывающую три атома углерода и занятую парой электронов. Соединения
-орбитали: одна связывающая и две разрыхляющие, которые вырождены (т.е. имеют одинаковую энергию). На этих орбиталях располагаются три электрона: два на связывающей орбитали и один на одной из разрыхляющих орбиталей. Если удалить электрон из циклопропенильного радикала, образующийся катион циклопропенилия будет иметь полностью делокализованную В3МО, охватывающую три атома углерода и занятую парой электронов. Соединения
(см. скан)
Рис. 10.3. Пентадиеиильныи радикал (только  -орбитали). Симметрия
-орбитали). Симметрия  .
.
циклопропенилия получены; в качестве примера приведем тетрафтороборат 1,2,3-трифенилциклопропенилия:


Рис. 10.4. Энергетические уровни  -орбиталей циклических молекул
-орбиталей циклических молекул  (от
(от  до n = 8).
до n = 8).
Квадратный циклобутадиен  имеет четыре
имеет четыре  -орбигали: связывающую орбиталь, две вырожденные несвязывающие орбитали и разрыхляющую орбиталь. На этих четырех орбиталях необходимо разместить четыре электрона; два могли бы занять связывающую орбиталь и по одному с параллельными спинами - вырожденные несвязывающие орбитали (правило Гунда). Такое предположение эшибочно, потому что нет никаких причин ожидать, что щклобутадиен будет квадратным; на самом деле более низкой энергией, вероятно, должна обладать продолговатая
-орбигали: связывающую орбиталь, две вырожденные несвязывающие орбитали и разрыхляющую орбиталь. На этих четырех орбиталях необходимо разместить четыре электрона; два могли бы занять связывающую орбиталь и по одному с параллельными спинами - вырожденные несвязывающие орбитали (правило Гунда). Такое предположение эшибочно, потому что нет никаких причин ожидать, что щклобутадиен будет квадратным; на самом деле более низкой энергией, вероятно, должна обладать продолговатая  с четырьмя
с четырьмя  -электронами на двух изолированных «двойных связях» (теорема Яна-Теллера). Эксперимент юдтверждает, что циклобутадиен ведет себя как очень напряженный циклоолефин, а не как бирадикал.
-электронами на двух изолированных «двойных связях» (теорема Яна-Теллера). Эксперимент юдтверждает, что циклобутадиен ведет себя как очень напряженный циклоолефин, а не как бирадикал.
Циклопентадиен - относительно кислый углеводород, I анион (рис. 10.5), образующийся при обработке циклопен-гадиена сильным основанием, имеет три  -орбитали, соторые делокализованы по пяти атомам углерода. Высшие
-орбитали, соторые делокализованы по пяти атомам углерода. Высшие  -орбитали образуют вырожденную пару и являются
-орбитали образуют вырожденную пару и являются  Низшая
Низшая  -орбиталь имеет гораздо более низкую энергию, и между В3МО и низшей
-орбиталь имеет гораздо более низкую энергию, и между В3МО и низшей  -орбиталью расположены четыре
-орбиталью расположены четыре  -орбитали (не показаны),
-орбитали (не показаны),  вырожденные пары.
вырожденные пары.
Бензол является прототипом ароматических соединений. На рис. 10.6 показаны шесть  -молекулярных орбиталей:
-молекулярных орбиталей:

Рис. 10.5. Связывающие  -орбитали циклопентадиениланиона [вырожденные пары
-орбитали циклопентадиениланиона [вырожденные пары  -орбиталей с
-орбиталей с  ккал/моль
ккал/моль  ккал/моль, расположенные между верхними и нижним
ккал/моль, расположенные между верхними и нижним  -уровнями, не показаны].
-уровнями, не показаны].
три связывающие и три разрыхляющие. Очень важно отметить, что между показанными на рисунке двумя верхними вырожденными  -уровнями и нижним
-уровнями и нижним  -уровнем расположены четыре
-уровнем расположены четыре  -орбитали
-орбитали  и вырожденная пара
и вырожденная пара  не показанные на рисунке. Однако В3МО в основном состоянии бензола являются верхние связывающие
не показанные на рисунке. Однако В3МО в основном состоянии бензола являются верхние связывающие  -уровни.
-уровни.
Для химии бензола характерны реакции «присоединения с отщеплением», в которых в конечном продукте сохраняются шесть делокализованных  -электронов.
-электронов.

На первый взгляд пиридин (рис. 10.7) имеет очень во многом сходную картину делокализации электронов. Две высшие занятые  -орбитали близки по энергии, соответствуя вырожденной паре В3МО бензола. Их энергия значительно ниже, что соответствует наличию в ядре более
-орбитали близки по энергии, соответствуя вырожденной паре В3МО бензола. Их энергия значительно ниже, что соответствует наличию в ядре более

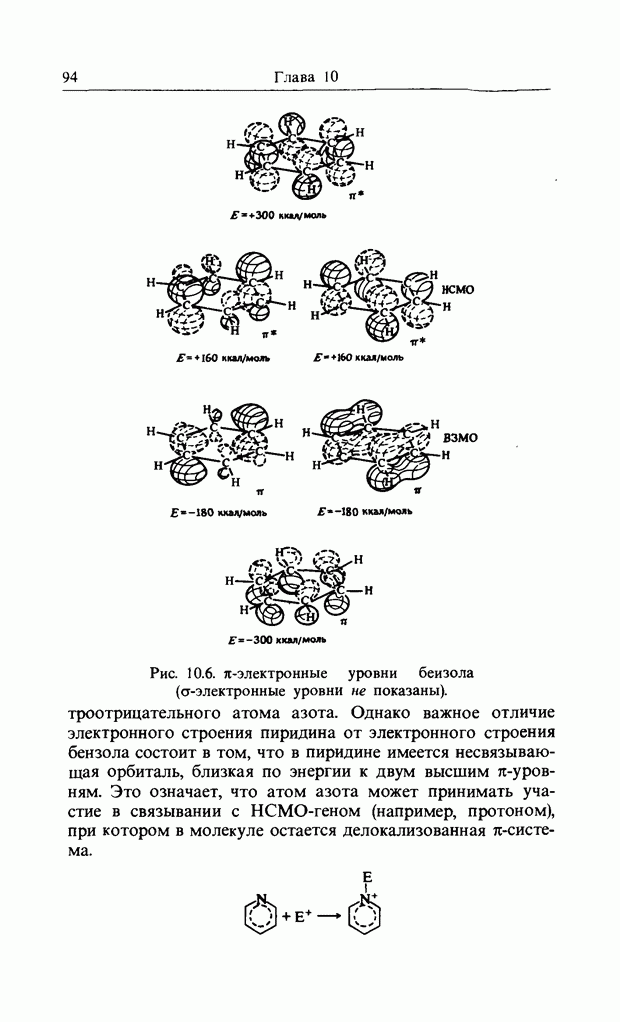
Рис. 10.6.  -электронные уровни бензола (ст-электронные уровни не показаны).
-электронные уровни бензола (ст-электронные уровни не показаны).
электроотрицательного атома азота. Однако важное отличие электронного строения пиридина от электронного строения бензола состоит в том, что в пиридине имеется несвязывающая орбиталь, близкая по энергии к двум высшим  -уровням. Это означает, что атом азота может принимать участие в связывании с НСМО-геном (например, протоном), при котором в молекуле остается делокализованная
-уровням. Это означает, что атом азота может принимать участие в связывании с НСМО-геном (например, протоном), при котором в молекуле остается делокализованная  -система.
-система.


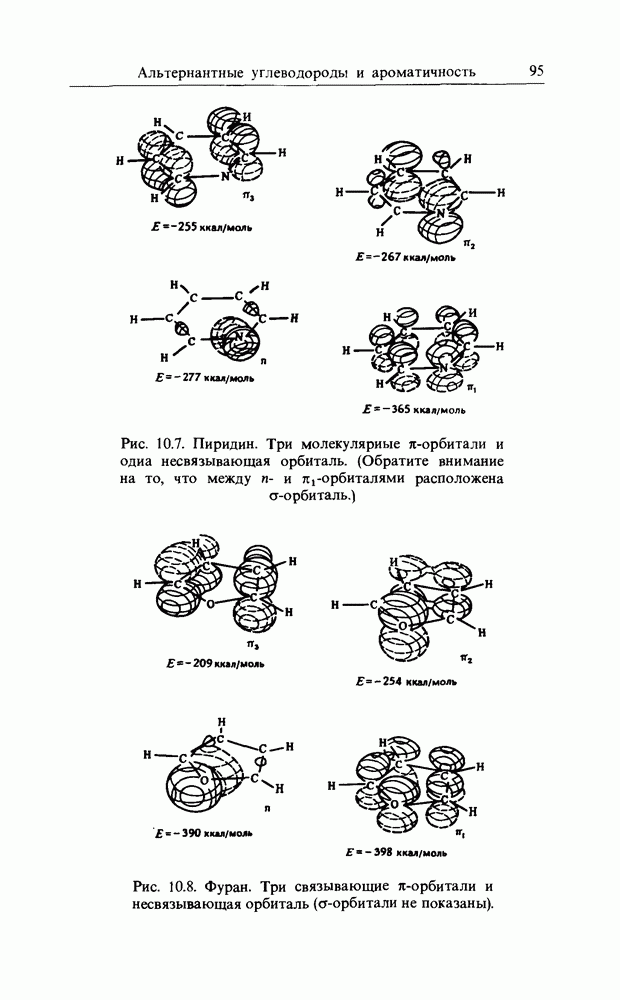
Рис. 10.7. Пиридин. Три молекулярные  -орбитали и одна несвязывающая орбиталь. (Обратите внимание на то, что между
-орбитали и одна несвязывающая орбиталь. (Обратите внимание на то, что между  и
и  -орбиталями расположена
-орбиталями расположена  -орбиталь.)
-орбиталь.)

Рис. 10.8. Фуран. Три связывающие  -орбитали и несвязывающая орбиталь (ст-орбитали не показаны).
-орбитали и несвязывающая орбиталь (ст-орбитали не показаны).

Рис. 10.9. Пиррол. Показаны только связывающие  -орбитали. (Обратите внимание на то, что между
-орбитали. (Обратите внимание на то, что между  и
и  -орбиталями имеются три
-орбиталями имеются три  -орбитали.)
-орбитали.)
Пятичленные гетероциклические соединения пиррол 1 фуран имеют три связывающие  -орбитали, аналогичные юдобным орбиталям бензола и пиридина, а фуран, подобно гаридину, имеет несвязывающую орбиталь, центрированию на гетероатоме. В пирроле энергии высшей связывающей пары орбиталей близки, чего не наблюдается в фуране. Кимия пиррола более похожа на химию бензола, чем химия бурана. Фуран (рис. 10.8) вступает в реакции циклоприсоединения (см. гл. 15) и в общем более склонен к реакциям трисоединения, чем пиррол (рис. 10.9). Электроны на
-орбитали, аналогичные юдобным орбиталям бензола и пиридина, а фуран, подобно гаридину, имеет несвязывающую орбиталь, центрированию на гетероатоме. В пирроле энергии высшей связывающей пары орбиталей близки, чего не наблюдается в фуране. Кимия пиррола более похожа на химию бензола, чем химия бурана. Фуран (рис. 10.8) вступает в реакции циклоприсоединения (см. гл. 15) и в общем более склонен к реакциям трисоединения, чем пиррол (рис. 10.9). Электроны на  орбитали фурана очень прочно связаны, и фуэан не является сильным основанием в противоположность тиридину, в котором энергетическая щель между высшими
орбитали фурана очень прочно связаны, и фуэан не является сильным основанием в противоположность тиридину, в котором энергетическая щель между высшими  -уровнями и несвязывающей орбиталью относительно мага. Пиридинсильное основание.
-уровнями и несвязывающей орбиталью относительно мага. Пиридинсильное основание.
ДОПОЛНИТЕЛЬНАЯ ЛИТЕРАТУРА
(см. скан)
(см. скан)
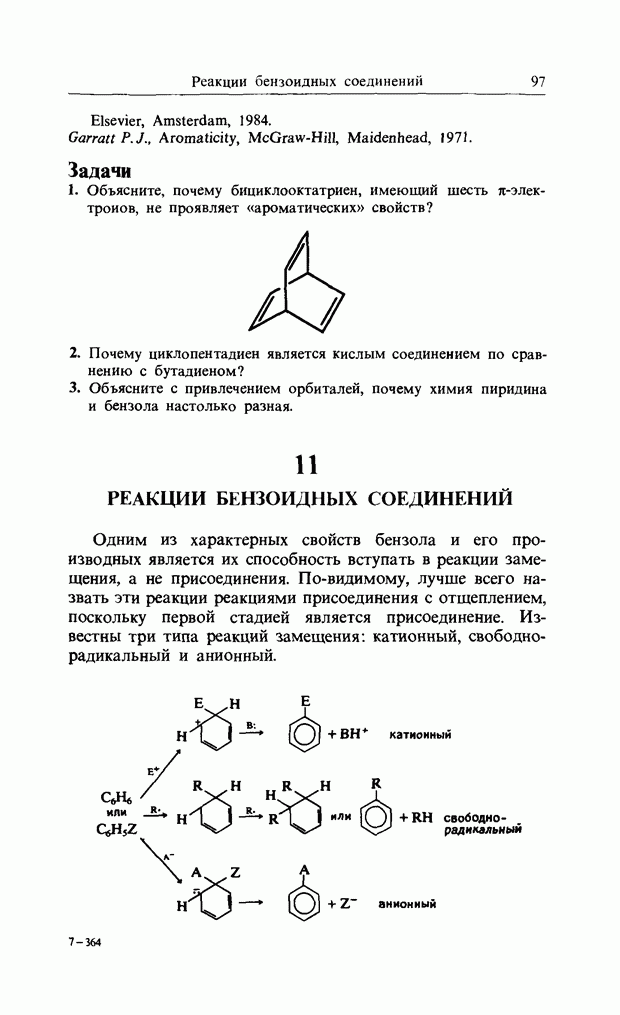
Задачи
1. Объясните, почему бициклооктатриен, имеющий шесть  -электронов, не проявляет «ароматических» свойств?
-электронов, не проявляет «ароматических» свойств?

2. Почему циклопентадиен является кислым соединением по сравнению с бутадиеном?
3. Объясните с привлечением орбиталей, почему химия пиридина и бензола настолько разная.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ ПЕРЕВОДЧИКА
- ПРЕДИСЛОВИЕ АВТОРОВ К РУССКОМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- НОМЕНКЛАТУРА
- 1. АТОМНЫЕ И МОЛЕКУЛЯРНЫЕ ОРБИТАЛИ
- 2. ПИКТОГРАФИЧЕСКАЯ ОРБИТАЛЬНАЯ ТЕОРИЯ
- 3. ГИБРИДИЗАЦИЯ И ОРБИТАЛИ ФУНКЦИОНАЛЬНЫХ ГРУПП
- 4. СВЯЗЬ УГЛЕРОД ВОДОРОД И РЕАКЦИИ ПЕРЕНОСА РАДИКАЛОВ
- 5. РЕАКЦИИ ЗАМЕЩЕНИЯ И СВЯЗЬ УГЛЕРОД ГАЛОГЕН
- 6. БИМОЛЕКУЛЯРНЫЕ РЕАКЦИИ ЭЛИМИНИРОВАНИЯ
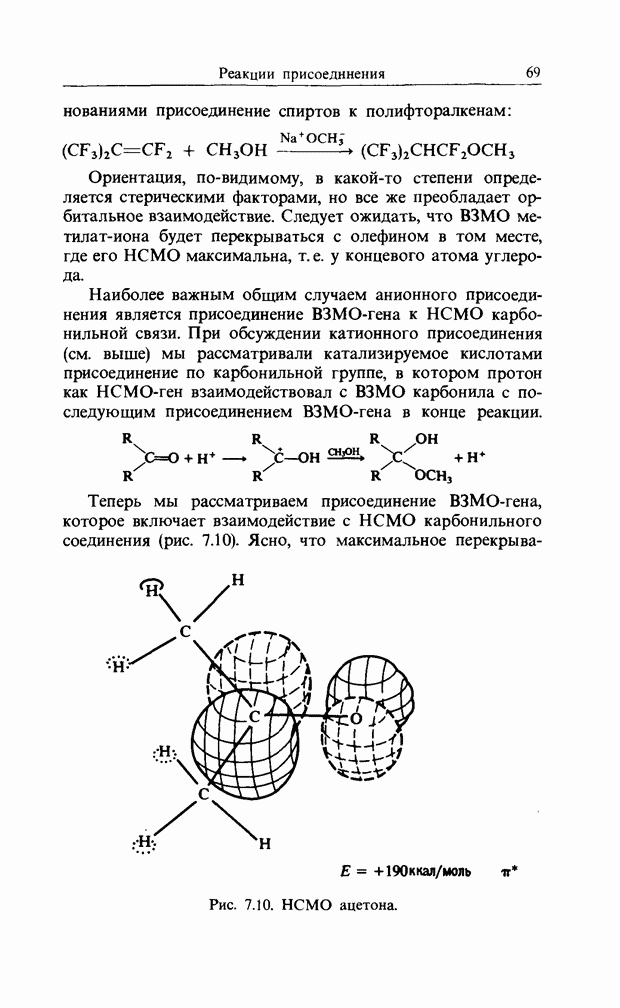
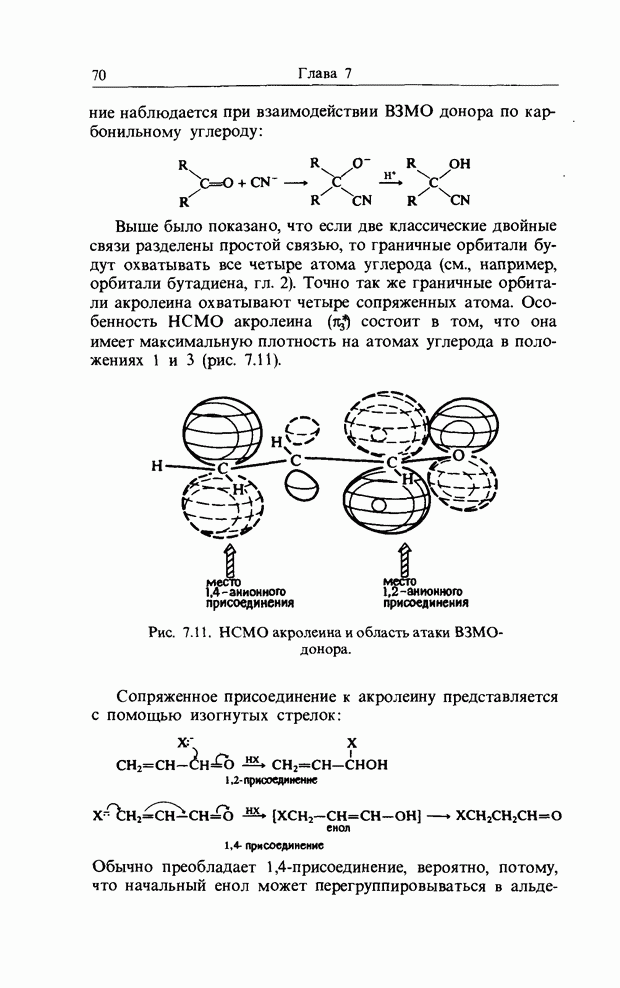
- 7. РЕАКЦИИ ПРИСОЕДИНЕНИЯ
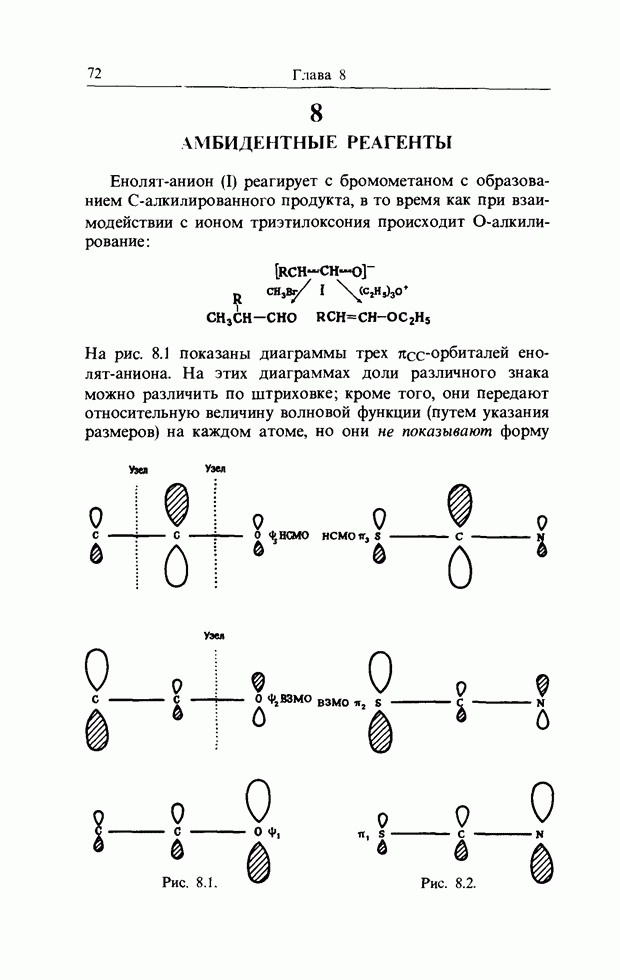
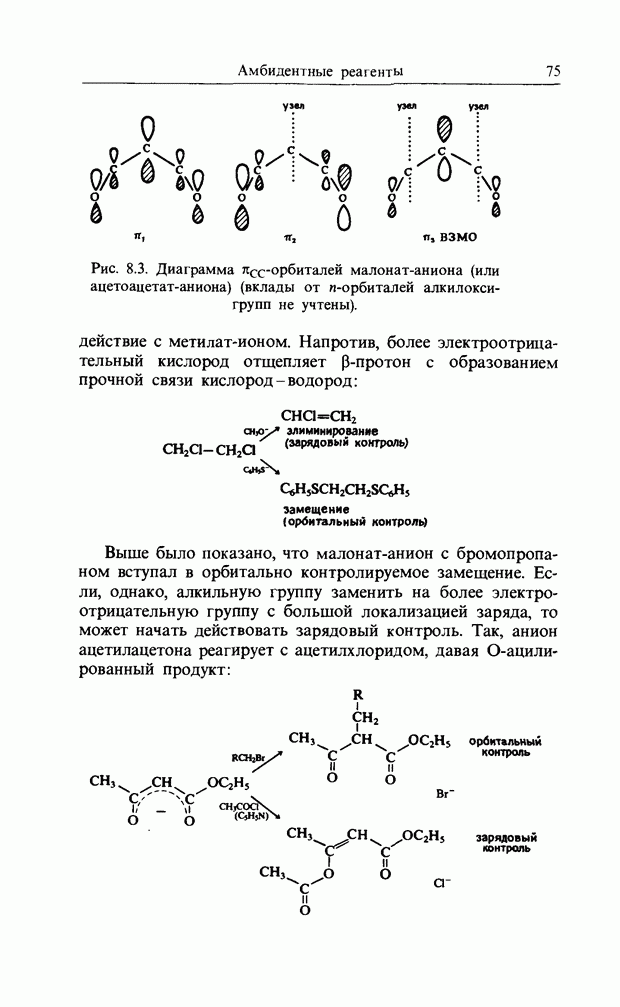
- 8. АМБИДЕНТНЫЕ РЕАГЕНТЫ
- 9. РЕАКЦИОННОСПОСОБНЫЕ ИНТЕРМЕДИАТЫ
- 10. АЛЬТЕРНАНТНЫЕ УГЛЕВОДОРОДЫ И АРОМАТИЧНОСТЬ
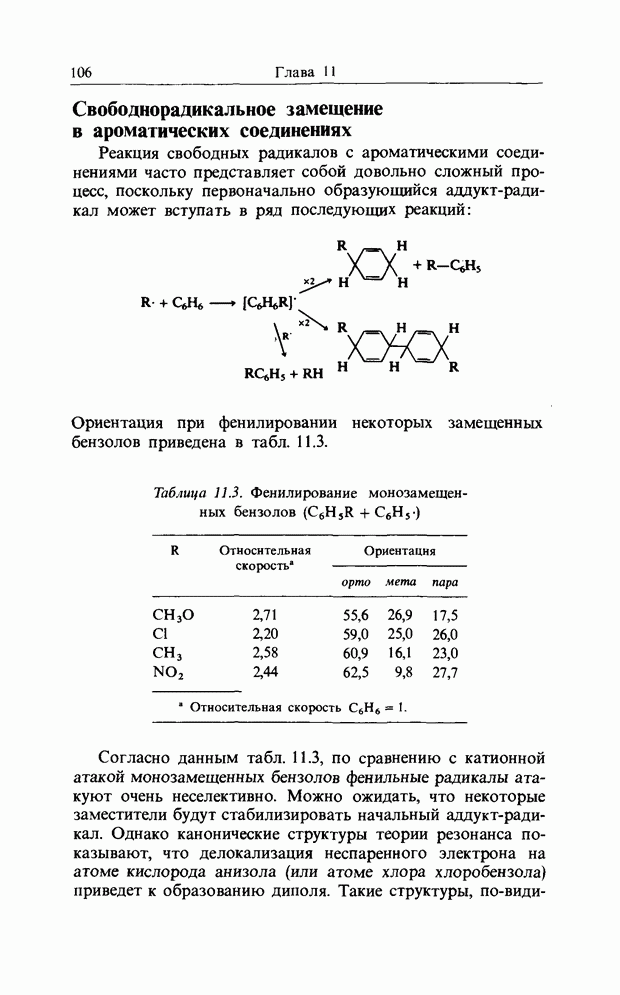
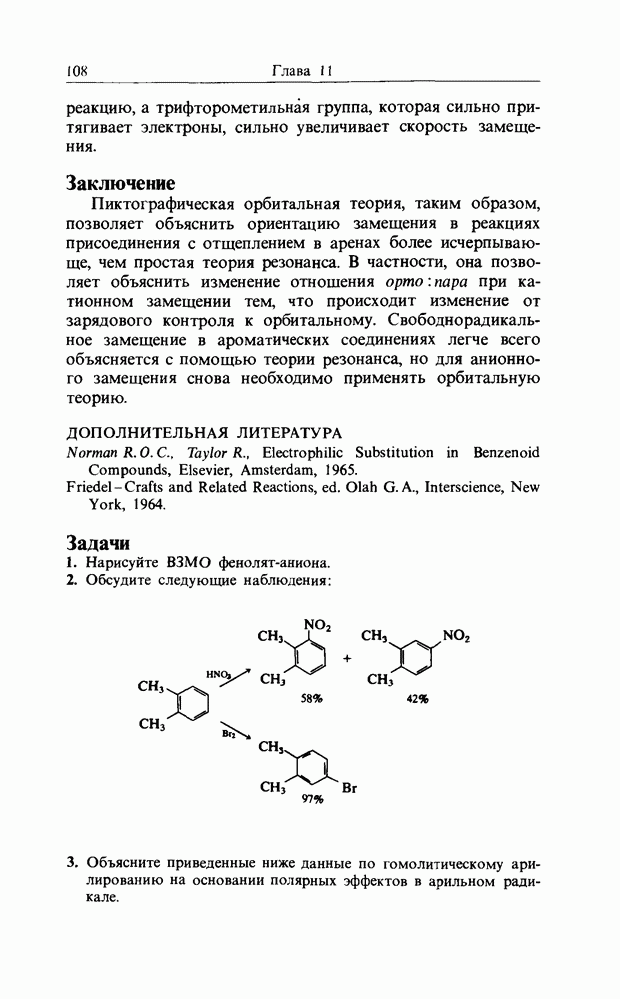
- 11. РЕАКЦИИ БЕНЗОИДНЫХ СОЕДИНЕНИЙ
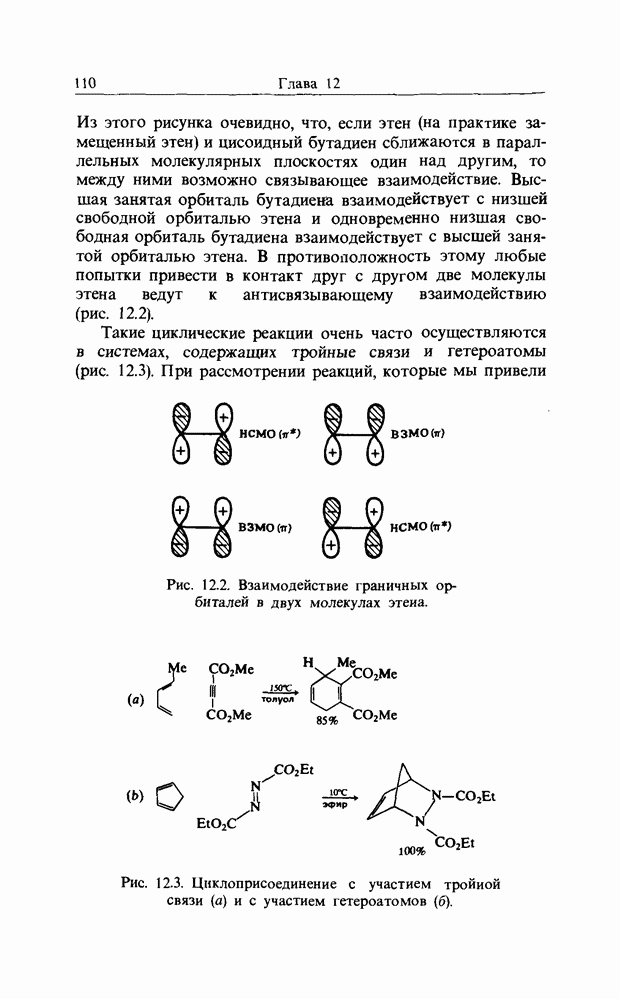
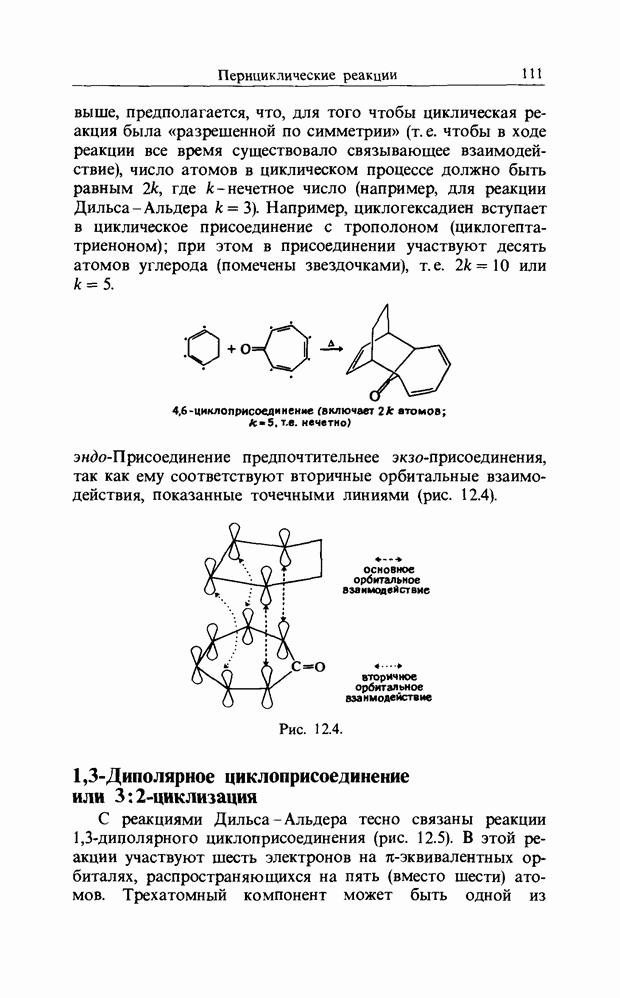
- 12. ПЕРИЦИКЛИЧЕСКИЕ РЕАКЦИИ