| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
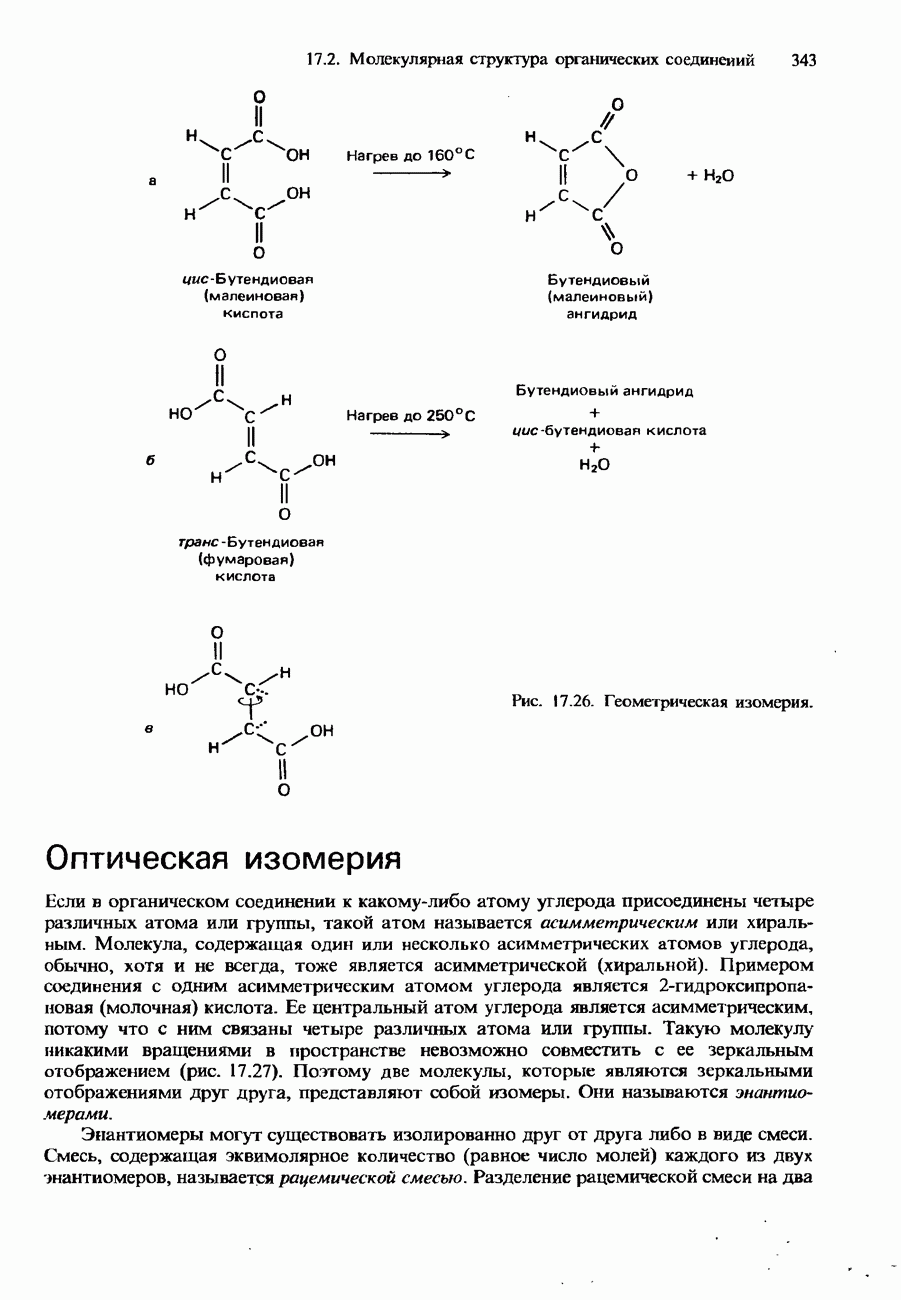
19.3. Карбонильная группа
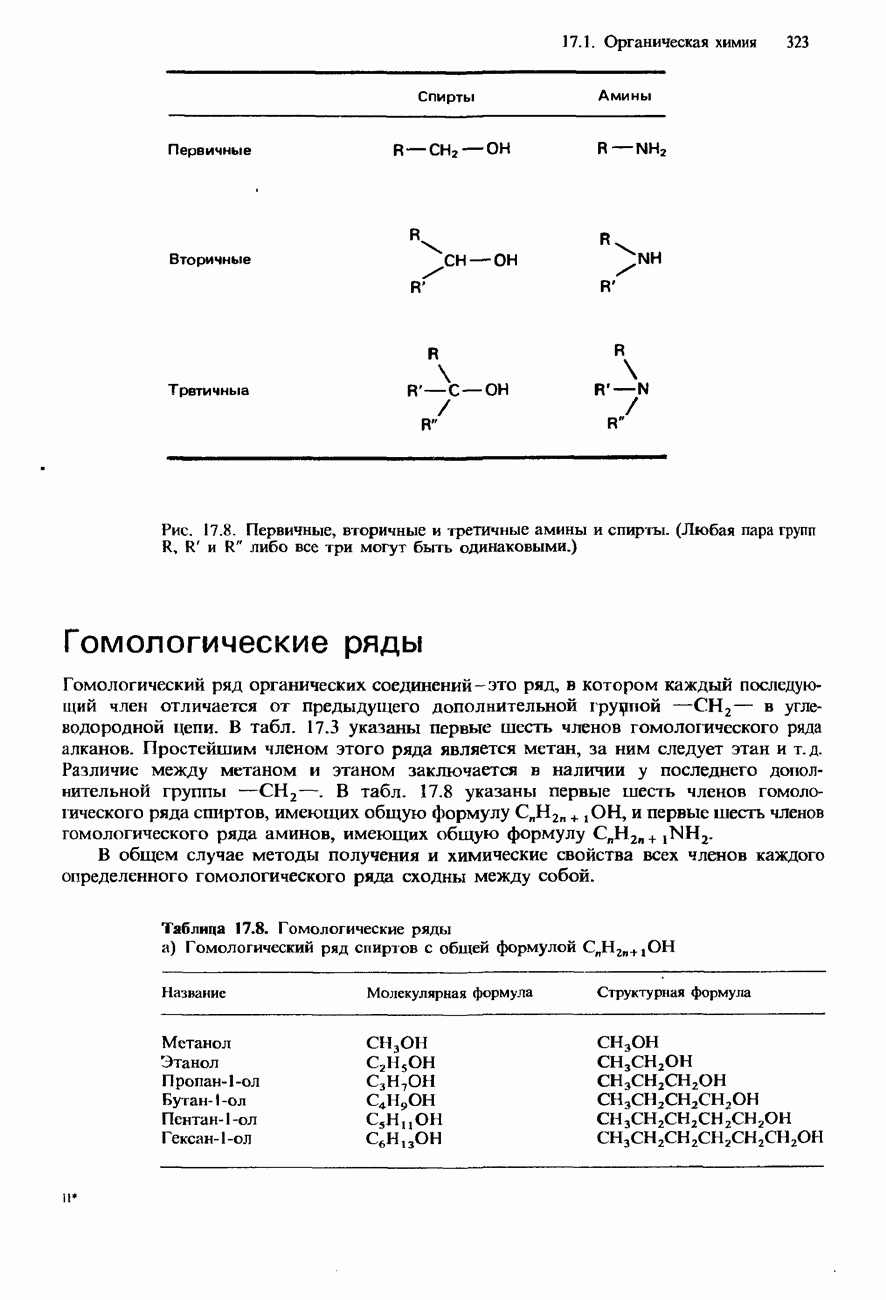
Карбонильная группа 
входит в состав альдегидов, кетонов, карбоновых кислот, хлорангидридов карбоновых кислот, их ангидридов и амидов. Атом углерода в этой группе  -гибридизован. Таким образом, карбонильная группа имеет плоскую структуру (см. рис. 2.7):
-гибридизован. Таким образом, карбонильная группа имеет плоскую структуру (см. рис. 2.7):

Атом углерода в карбоксильной группе связан с атомом кислорода  -связью и
-связью и  -связыо. Вследствие мезомерного эффекта карбонильная группа поляризована, и на более электроотрицательном атоме кислорода в ней сосредоточена большая электронная плотность:
-связыо. Вследствие мезомерного эффекта карбонильная группа поляризована, и на более электроотрицательном атоме кислорода в ней сосредоточена большая электронная плотность:

Небольшой положительный заряд на атоме углерода делает его восприимчивым к нуклеофильной атаке.
АЛЬДЕГИДЫ И КЕТОНЫ
Альдегиды и кетоны вместе называются карбонильными соединениями. У альдегидов к атому углерода карбонильной группы присоединена одна алкильная или арильная группа, а у кетонов - две такие группы:

Группы  могут быть алкильными либо арильными. Гомологические ряды альдегидов и кетонов имеют одинаковую общую формулу
могут быть алкильными либо арильными. Гомологические ряды альдегидов и кетонов имеют одинаковую общую формулу  . В табл. 19.9 указаны некоторые важнейшие представители альдегидов и кетонов.
. В табл. 19.9 указаны некоторые важнейшие представители альдегидов и кетонов.
Физические свойства
За исключением метаналя (формальдегида), который представляет собой газ, остальные члены гомологических рядов альдегидов и кетонов при нормальных условиях
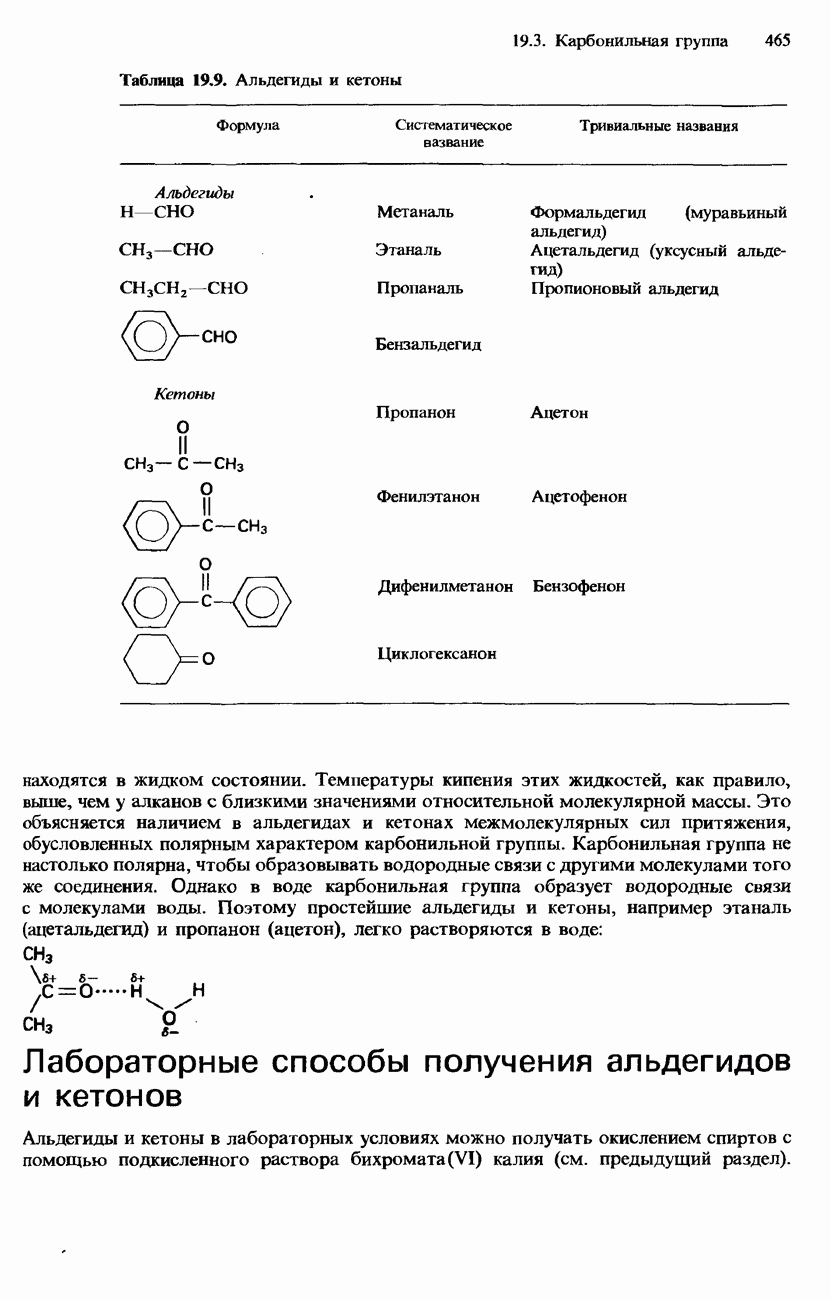
Таблица 19.9. Альдегиды и кетоны

находятся в жидком состоянии. Температуры кипения этих жидкостей, как правило, выше, чем у алканов с близкими значениями относительной молекулярной массы. Это объясняется наличием в альдегидах и кетонах межмолекулярных сил притяжения, обусловленных полярным характером карбонильной группы. Карбонильная группа не настолько полярна, чтобы образовывать водородные связи с другими молекулами того же соединения. Однако в воде карбонильная группа образует водородные связи с молекулами воды. Поэтому простейшие альдегиды и кетоны, например этаналь (ацетальдегид) и пропанон (ацетон), легко растворяются в воде:

Лабораторные способы получения альдегидов и кетонов
Альдегиды и кетоны в лабораторных условиях можно получать окислением спиртов с помощью подкисленного раствора бихромата (VI) калия (см. предыдущий раздел).
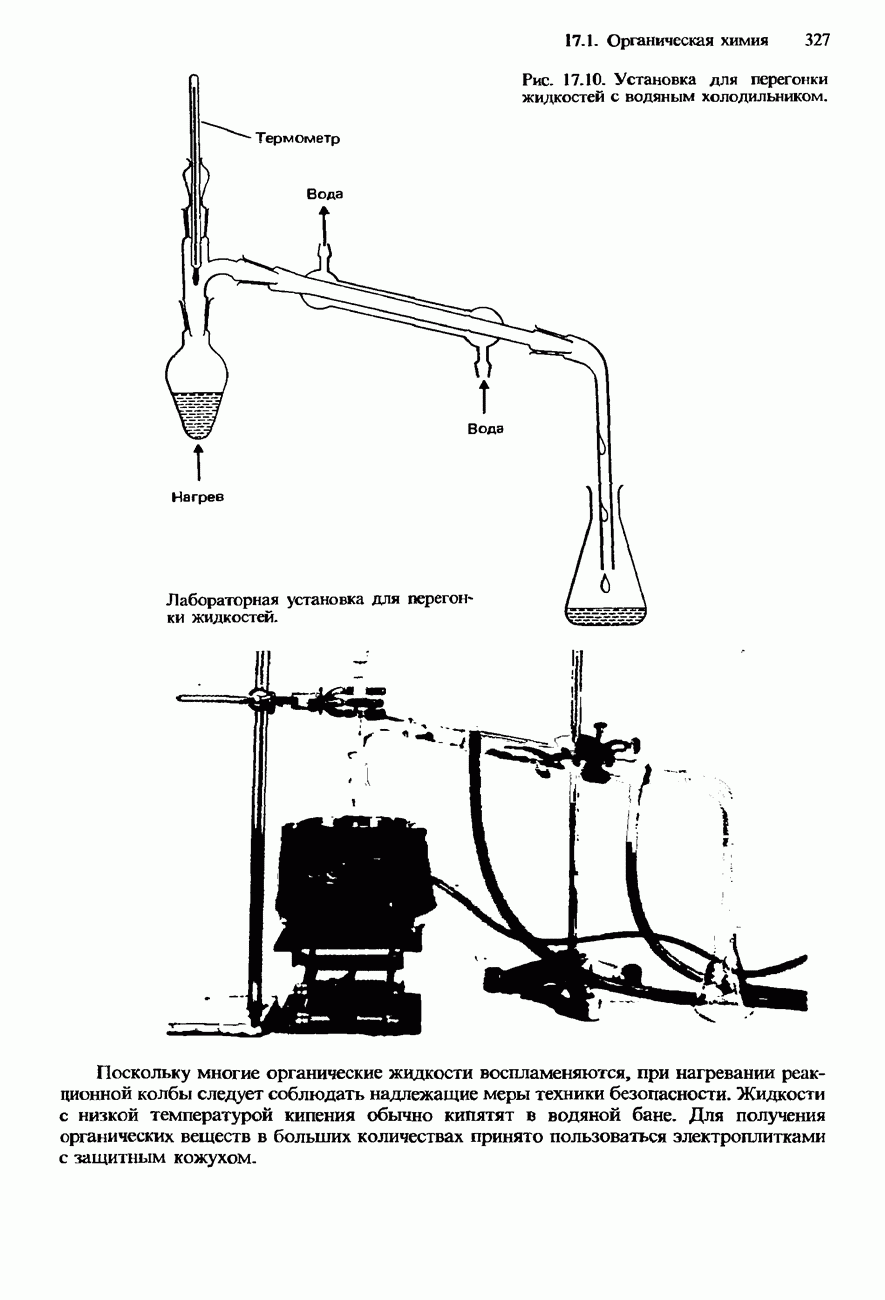
(см. скан)
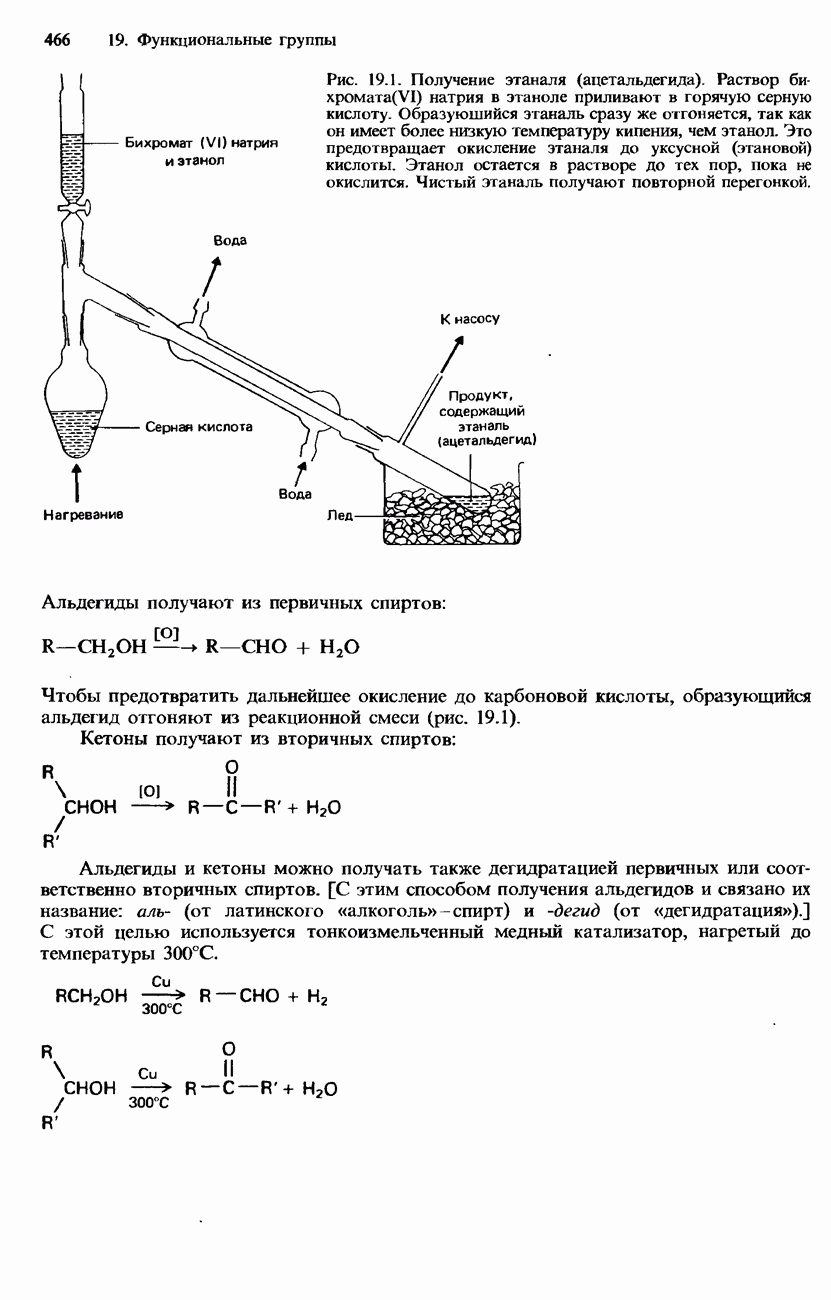
Рис. 19.1. Получение этаналя (ацетальдегида). Раствор бихромата!) натрия в этаноле приливают в горячую серную кислоту. Образующийся этаналь сразу же отгоняется, так как он имеет более низкую температуру кипения, чем этанол. Это предотвращает окисление этаналя до уксусной (этановой) кислоты. Этанол остается в растворе до тех пор, пока не окислится. Чистый этаналь получают повторной перегонкой.
Альдегиды получают из первичных спиртов:

Чтобы предотвратить дальнейшее окисление до карбоновой кислоты, образующийся альдегид отгоняют из реакционной смеси (рис. 19.1).
Кетоны получают из вторичных спиртов:

Альдегиды и кетоны можно получать также дегидратацией первичных или соответственно вторичных спиртов. [С этим способом получения альдегидов и связано их название: аль- (от латинского  -спирт) и -дегид (от «дегидратация»).] С этой целью используется тонкоизмельченный медный катализатор, нагретый до температуры 300°С.
-спирт) и -дегид (от «дегидратация»).] С этой целью используется тонкоизмельченный медный катализатор, нагретый до температуры 300°С.

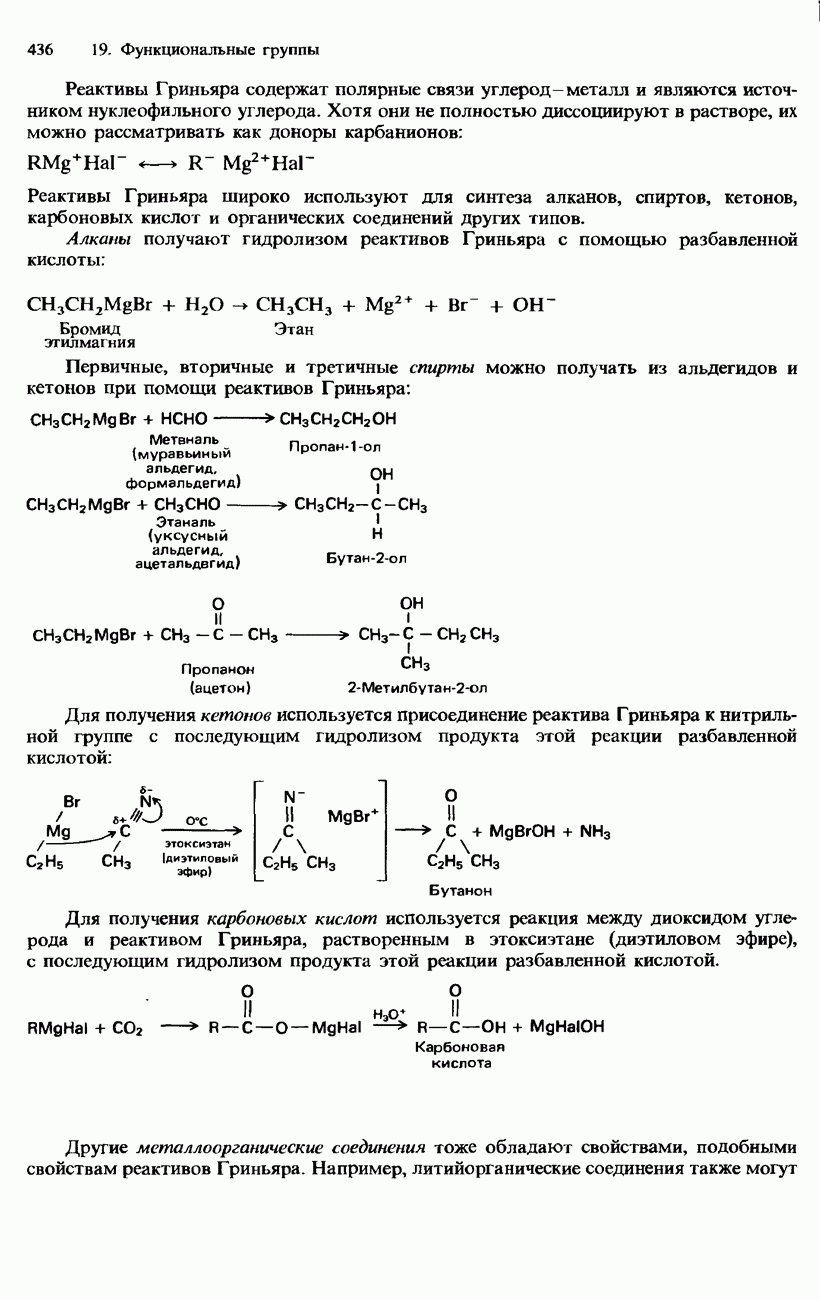
Кроме того, альдегиды и кетоны можно получать с помощью реактивов Гриньяра (см. разд. 19.1).
Химические свойства альдегидов и кетонов
Реакции присоединения. Альдегиды и кетоны вступают в реакции нуклеофильного присоединения. Общий механизм нуклеофильного присоединения к карбонильной группе описан в разд. 17.3.
Кетоны, как правило, обладают меньшей реакционной способностью по отношению к нуклеофильным агентам, чем альдегиды. Это объясняется электроно-донорными свойствами алкильных групп. Поскольку кетоны содержат две такие группы, положительный заряд на карбонильном атоме углерода у них меньше, чем у альдегидов.
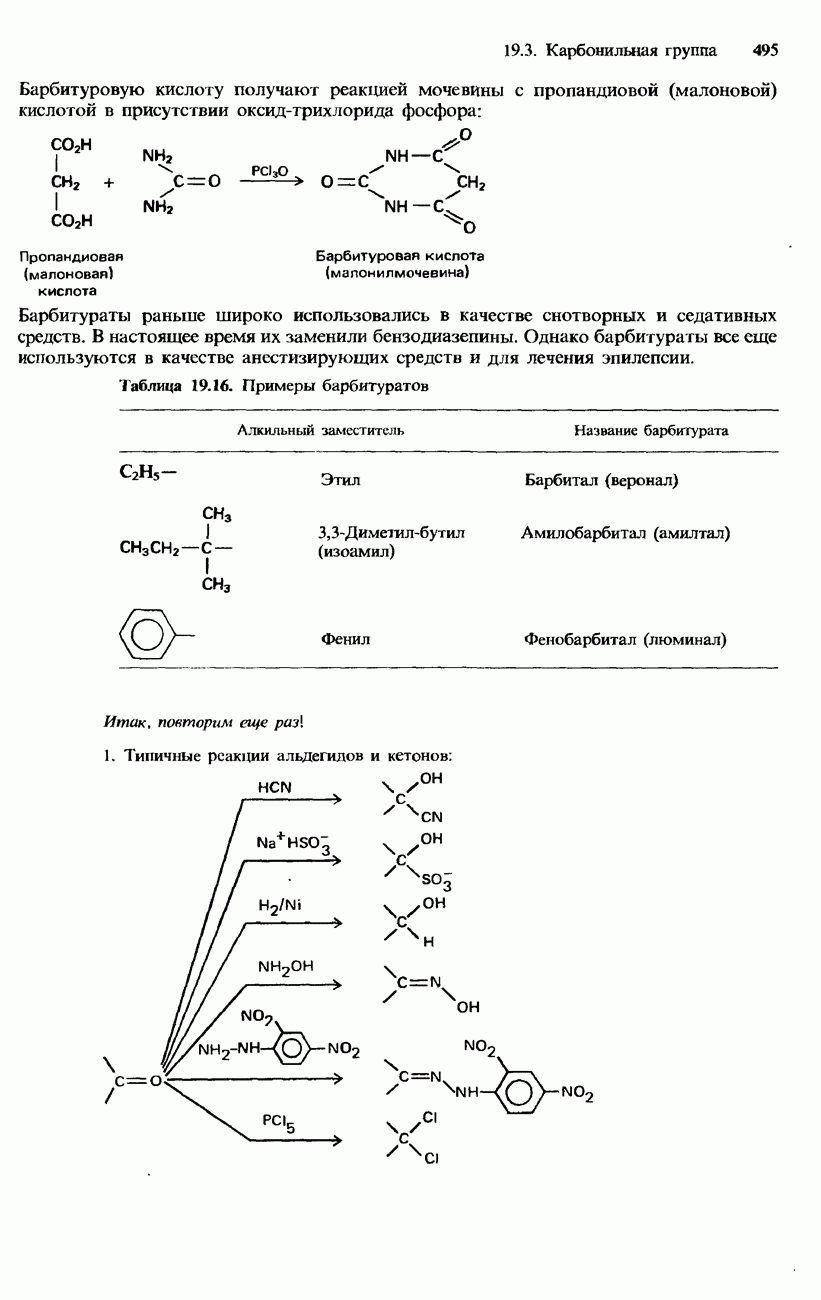
Присоединение циановодорода. И альдегиды, и кетоны вступают в реакцию нуклеофильного присоединения с циановодородом, образуя 2-гидроксинитрилы (циан-гидрины). Например, при обработке этаналя (ацетальдегида) цианидом натрия, а затем избытком минеральной кислоты протекает следующая реакция:

Механизм этого нуклеофильного присоединения описан в разд. 17.3.
Присоединение гидросульфита. Альдегиды и метилкетоны, обрабатываемые при комнатной температуре насыщенным водным раствором гидросульфита натрия  вступают с ним в реакцию нуклеофильного присоединения, образуя кристаллические ионные соединения. Нуклеофильным агентом в данном случае является гидросульфит-ион
вступают с ним в реакцию нуклеофильного присоединения, образуя кристаллические ионные соединения. Нуклеофильным агентом в данном случае является гидросульфит-ион  :
:

Этаналь (ацетальдегид) вступает в эту реакцию легче, чем пропанон (ацетон).
Присоединение водорода. Альдегиды и кетоны способны присоединять водород по карбонильной группе, образуя соответственно первичные и вторичные спирты. В этой реакции используется платиновый либо никелевый катализатор:

Вместо водорода в качестве восстановителя может использоваться  лития
лития  либо
либо  натрия
натрия  натрия). При использовании литийалюминийгидрида в качестве растворителя применяется безводный этоксиэтан (диэтиловый эфир) либо тетрагидрофуран. Тетрагидридоалюминат-ионы являются источниками нуклеофильных гидридных ионов:
натрия). При использовании литийалюминийгидрида в качестве растворителя применяется безводный этоксиэтан (диэтиловый эфир) либо тетрагидрофуран. Тетрагидридоалюминат-ионы являются источниками нуклеофильных гидридных ионов:

Для завершения реакции к реакционной смеси добавляют воду, которая гидролизует продукт:

Кроме того, вода разрушает избыточное количество  Восстановление альдегидов и кетонов с помощью борогидрида натрия протекает менее интенсивно. В этом случае в качестве растворителя используется вода либо водный раствор метанола или этанола.
Восстановление альдегидов и кетонов с помощью борогидрида натрия протекает менее интенсивно. В этом случае в качестве растворителя используется вода либо водный раствор метанола или этанола.
Присоединение реактивов Гриньяра. Метаналь (формальдегид) и другие альдегиды, а также кетоны реагируют с реактивами Гриньяра в безводном этоксиэтане (диэти-ловом эфире), образуя соответственно первичные, вторичные и третичные спирты (см. разд. 19.1).
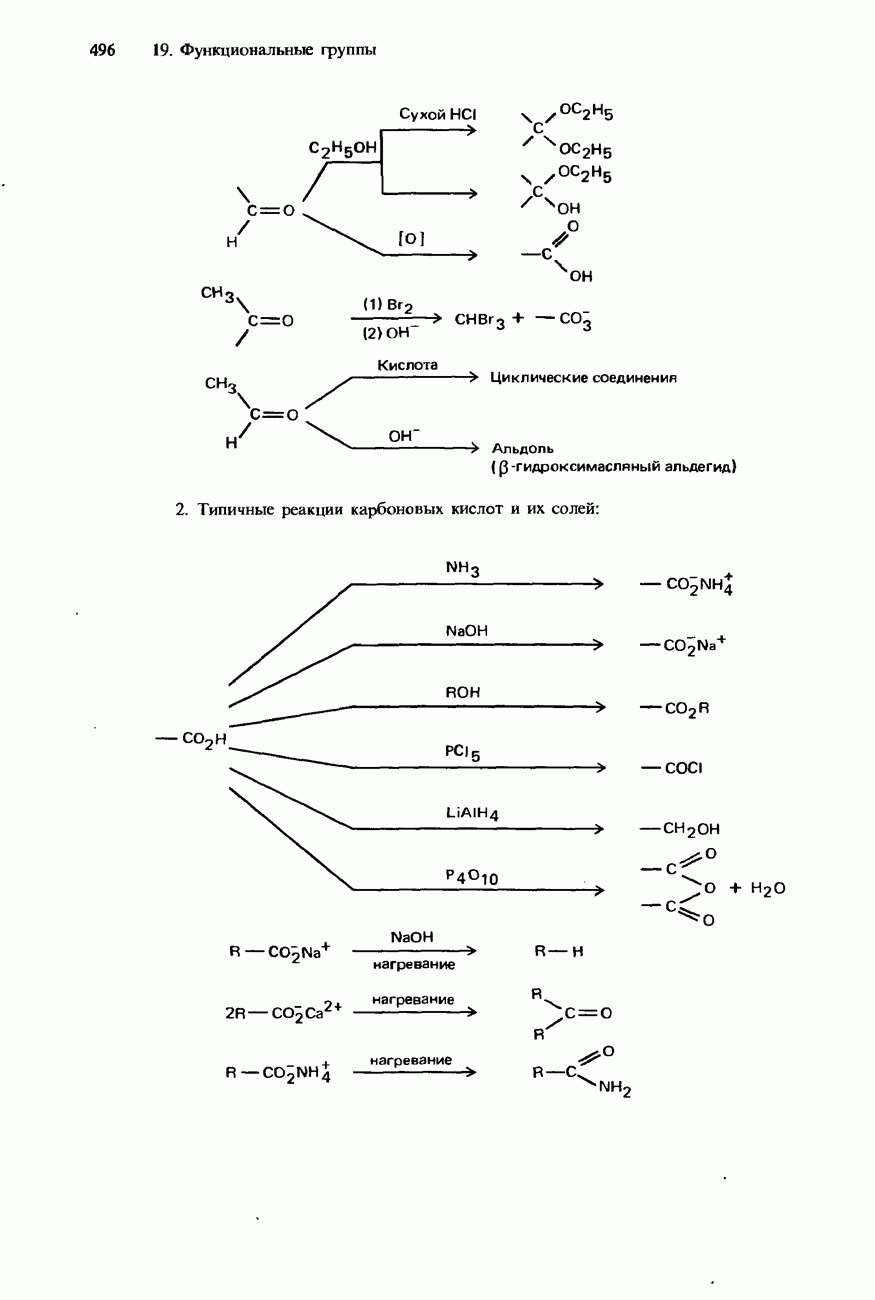
Присоединение спиртов. Альдегиды, но не кетоны, в присутствии хлороводорода соединяются со спиртами, образуя ацетали. Хлороводород в этой реакции выступает в роли катализатора:

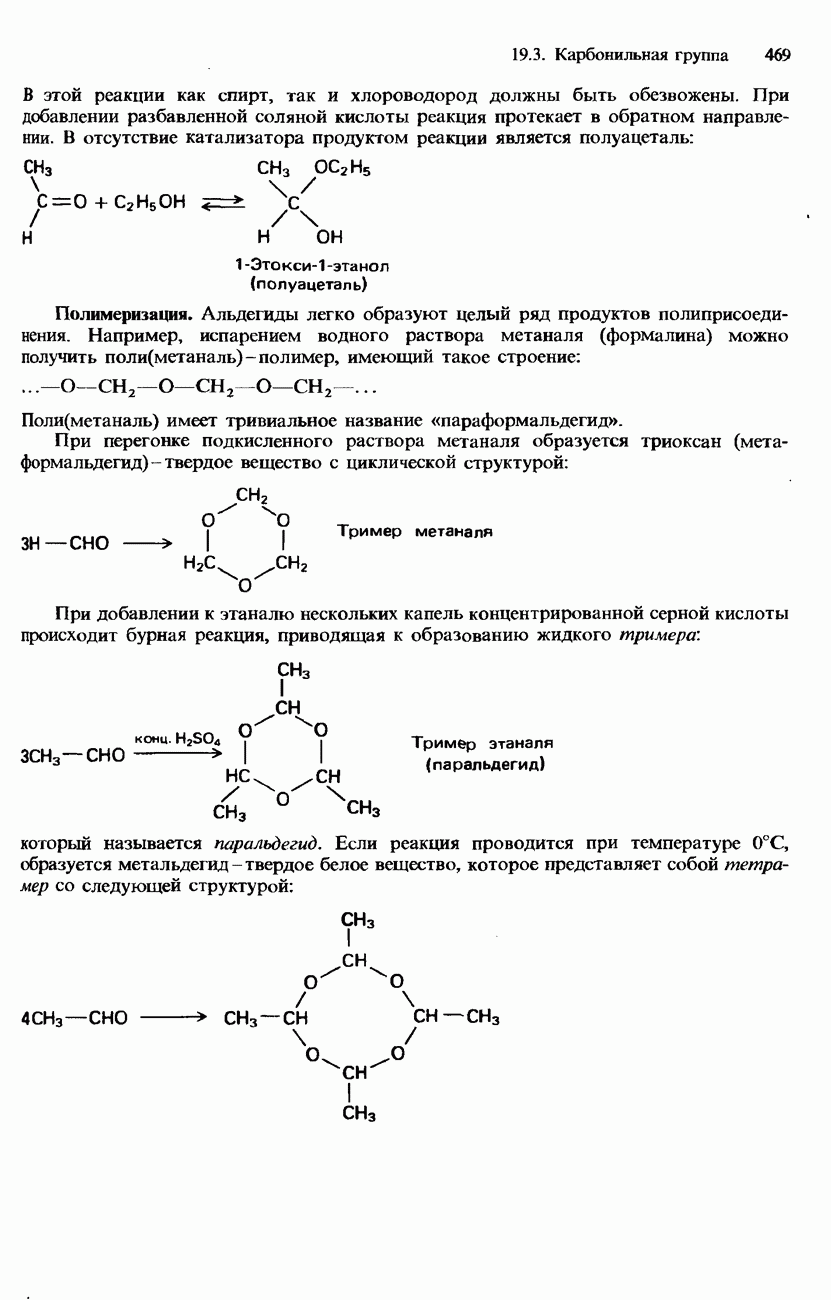
В этой реакции как спирт, так и хлороводород должны быть обезвожены. При добавлении разбавленной соляной кислоты реакция протекает в обратном направлении. В отсутствие катализатора продуктом реакции является полуацеталь:

Полимеризация. Альдегиды легко образуют целый ряд продуктов полиприсоединения. Например, испарением водного раствора метаналя (формалина) можно получить  -полимер, имеющий такое строение:
-полимер, имеющий такое строение:

Поли(метаналь) имеет тривиальное название «параформальдегид».
При перегонке подкисленного раствора метаналя образуется триоксан ( -твердое вещество с циклической структурой:
-твердое вещество с циклической структурой:

При добавлении к этаналю нескольких капель концентрированной серной кислоты происходит бурная реакция, приводящая к образованию жидкого тримера:

который называется паральдегид. Если реакция проводится при температуре 0°С, образуется метальдегид - твердое белое вещество, которое представляет собой тетрамер со следующей структурой:

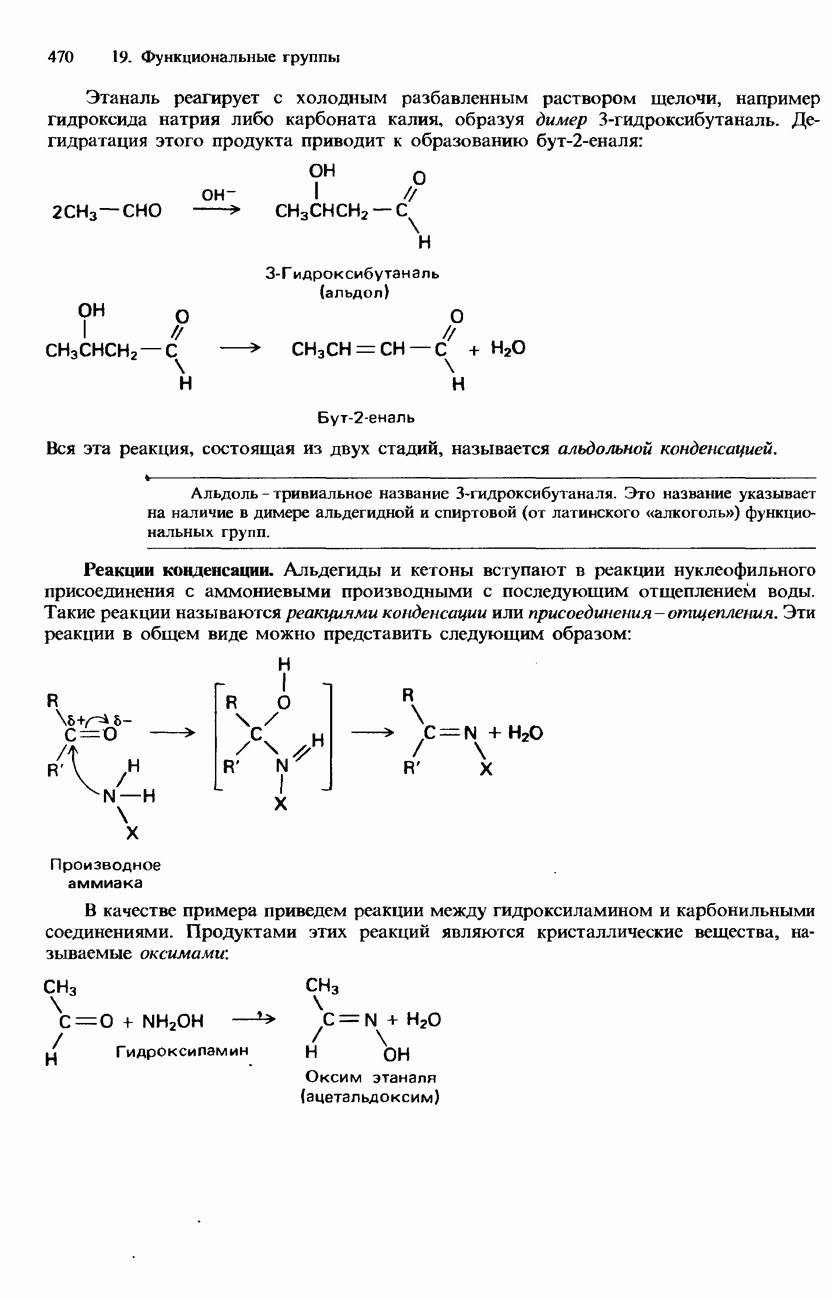
Этаналь реагирует с холодным разбавленным раствором щелочи, например гидроксида натрия либо карбоната калия, образуя димер 3-гидроксибутаналь. Дегидратация этого продукта приводит к образованию бут-2-еналя:

Вся эта реакция, состоящая из двух стадий, называется алъдольной конденсацией.
Альдоль - тривиальное название 3-гидроксибутаналя. Это название указывает на наличие в димере альдегидной и спиртовой (от латинского «алкоголь») функциональных групп.
Реакции конденсации. Альдегиды и кетоны вступают в реакции нуклеофильного присоединения с аммониевыми производными с последующим отщеплением воды. Такие реакции называются реакциями конденсации или присоединения - отщепления. Эти реакции в общем виде можно представить следующим образом:

В качестве примера приведем реакции между гидроксиламином и карбонильными соединениями. Продуктами этих реакций являются кристаллические вещества, называемые оксимами:


Альдегиды и кетоны вступают в реакции конденсации с 2,4-динитрофенилгидразинами, образуя 2,4-динитрофенилгидразоны, кристаллические вещества желтого или оранжевого цвета с четко выраженной температурой плавления:

Окисление карбонильных соединений. Альдегиды легко окисляются до карбоновых кислот под действием таких окислителей, как подкисленный раствор  -ионов либо перманганат-ионов:
-ионов либо перманганат-ионов:

Для окисления альдегидов может использоваться также реактив Толлена. Он представляет собой водно-аммиачный раствор нитрата серебра. Этот раствор содержит комплексные катионы  Альдегиды восстанавливают этот ион до металлического серебра, которое осаждается на внутренних стенках пробирки, образуя на них серебряное зеркало:
Альдегиды восстанавливают этот ион до металлического серебра, которое осаждается на внутренних стенках пробирки, образуя на них серебряное зеркало:

Алифатические альдегиды восстанавливают также ионы  в реактиве Фелинга. Так называется щелочный раствор сульфата
в реактиве Фелинга. Так называется щелочный раствор сульфата  и калиево-натриевой соли 2,3-дигидроксибутандиоата (тартрат калия-натрия, или соль Рошеля). В результате реакции образуется красноватый осадок оксида
и калиево-натриевой соли 2,3-дигидроксибутандиоата (тартрат калия-натрия, или соль Рошеля). В результате реакции образуется красноватый осадок оксида 

Ароматические альдегиды, например бензальдегид, не вступают в такую реакцию. Кетоны не вступают в реакцию ни с реактивом Толлена, ни с реактивом Фелинга. Кетоны окисляются только под действием таких сильных окислителей, как горячая азотная кислота и хромовая кислота:

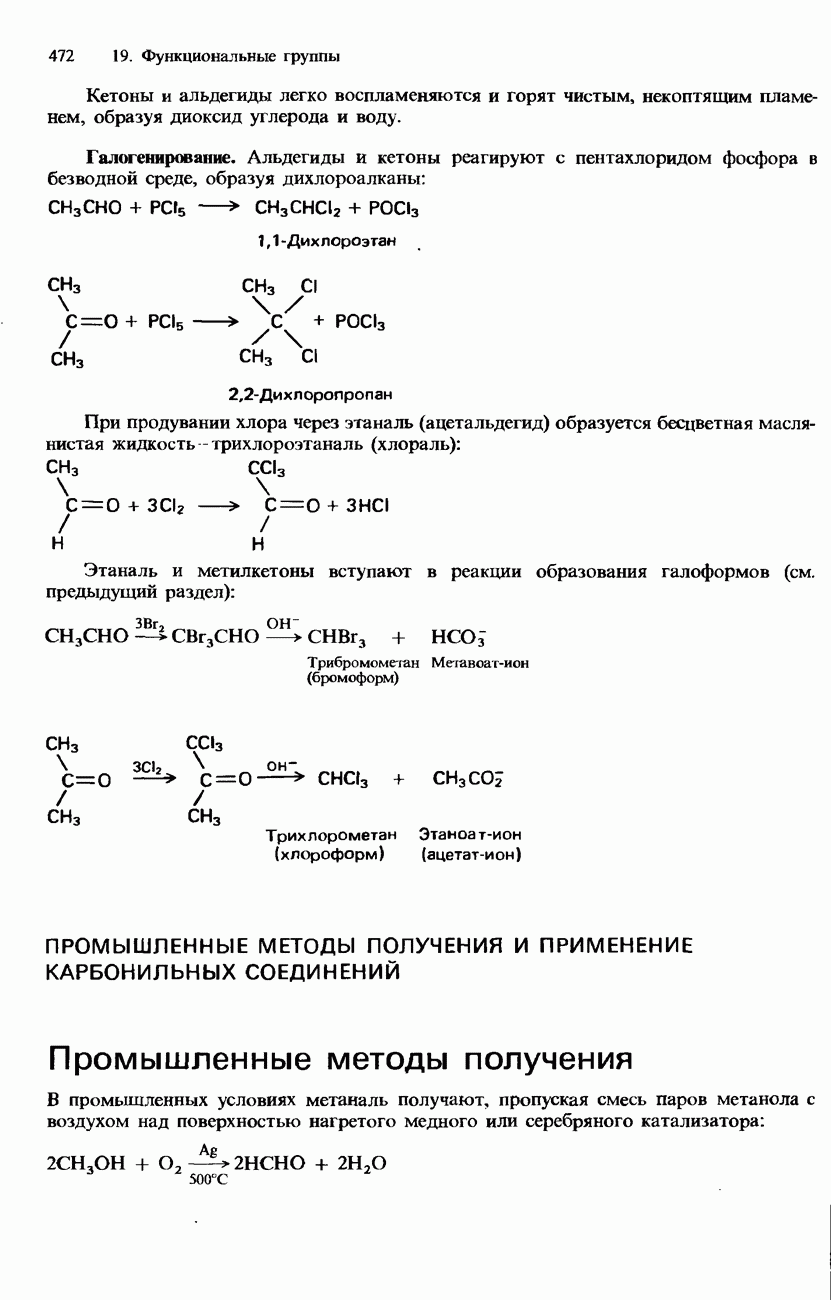
Кетоны и альдегиды легко воспламеняются и горят чистым, некоптящим пламенем, образуя диоксид углерода и воду.
Галогенирование. Альдегиды и кетоны реагируют с пентахлоридом фосфора в безводной среде, образуя дихлороалканы:

При продувании хлора через этаналь (ацетальдегид) образуется бесцветная маслянистая жидкость - трихлороэтаналь (хлораль):

Этаналь и метилкетоны вступают в реакции образования галоформов (см. предыдущий раздел):

Трихлорометан Этаноат-ион (хлороформ) (ацетат-ион)
| << Предыдущий параграф | Следующий параграф >> |
- 11. ПЕРИОДИЧЕСКИЙ ЗАКОН
- 11.1 Периодичность
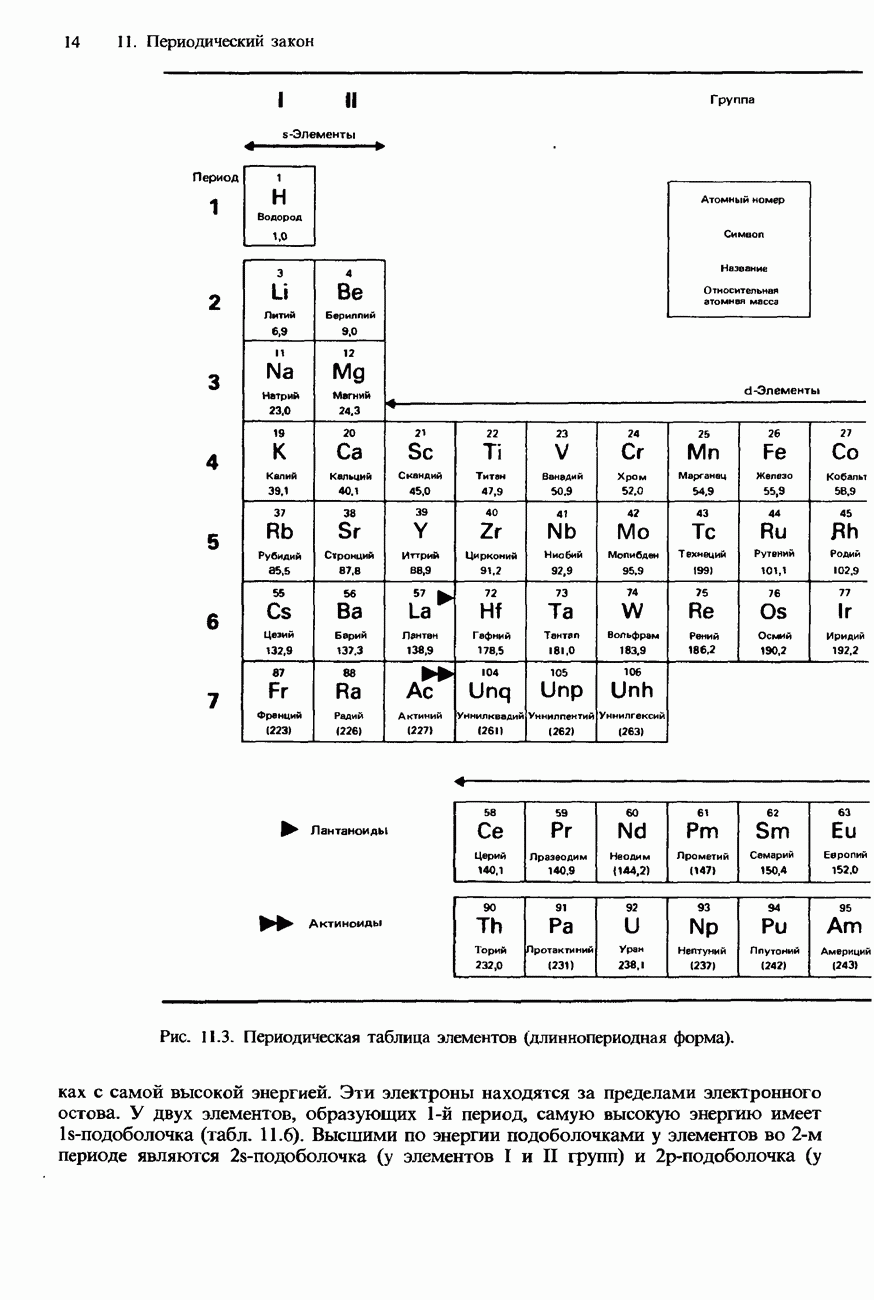
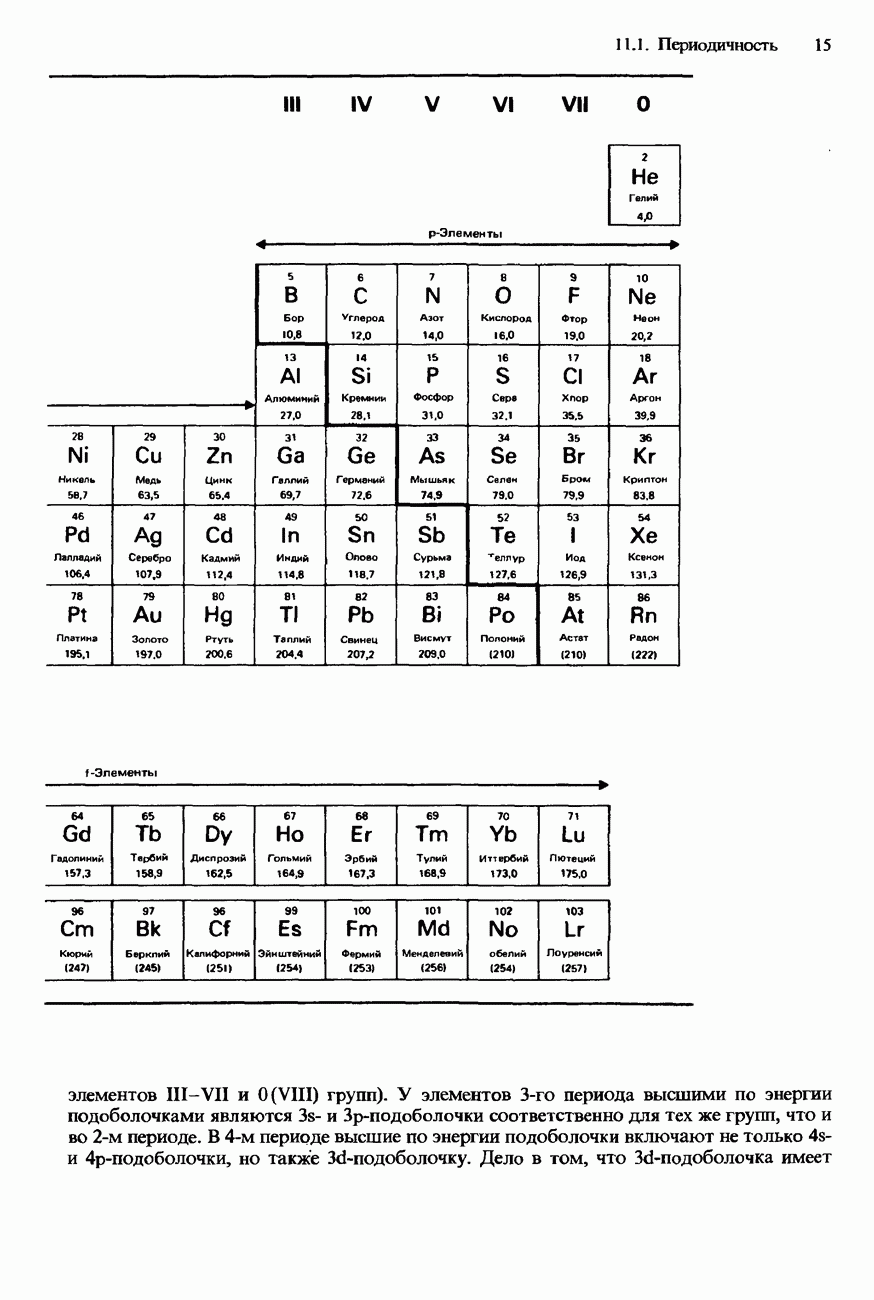
- СОВРЕМЕННАЯ ФОРМА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ
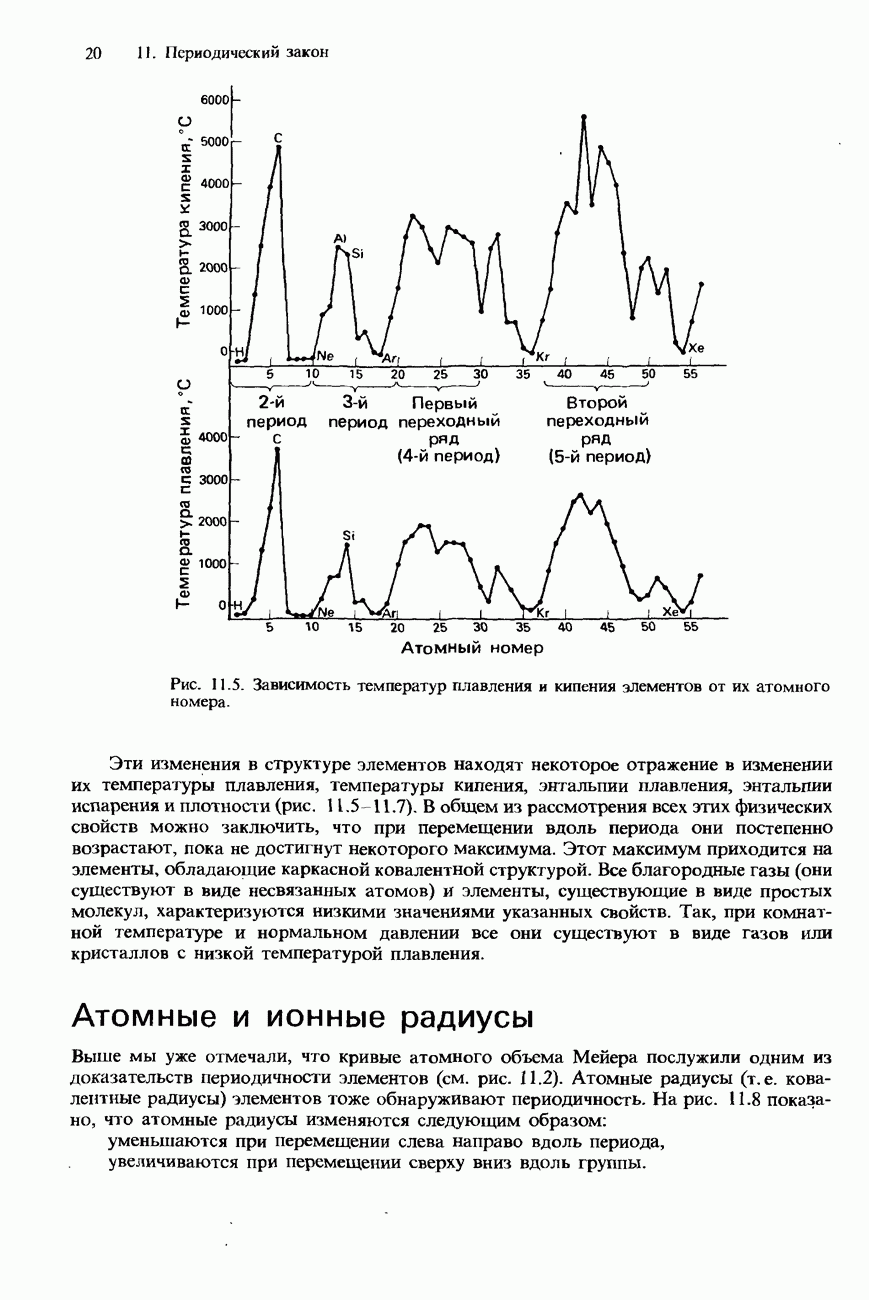
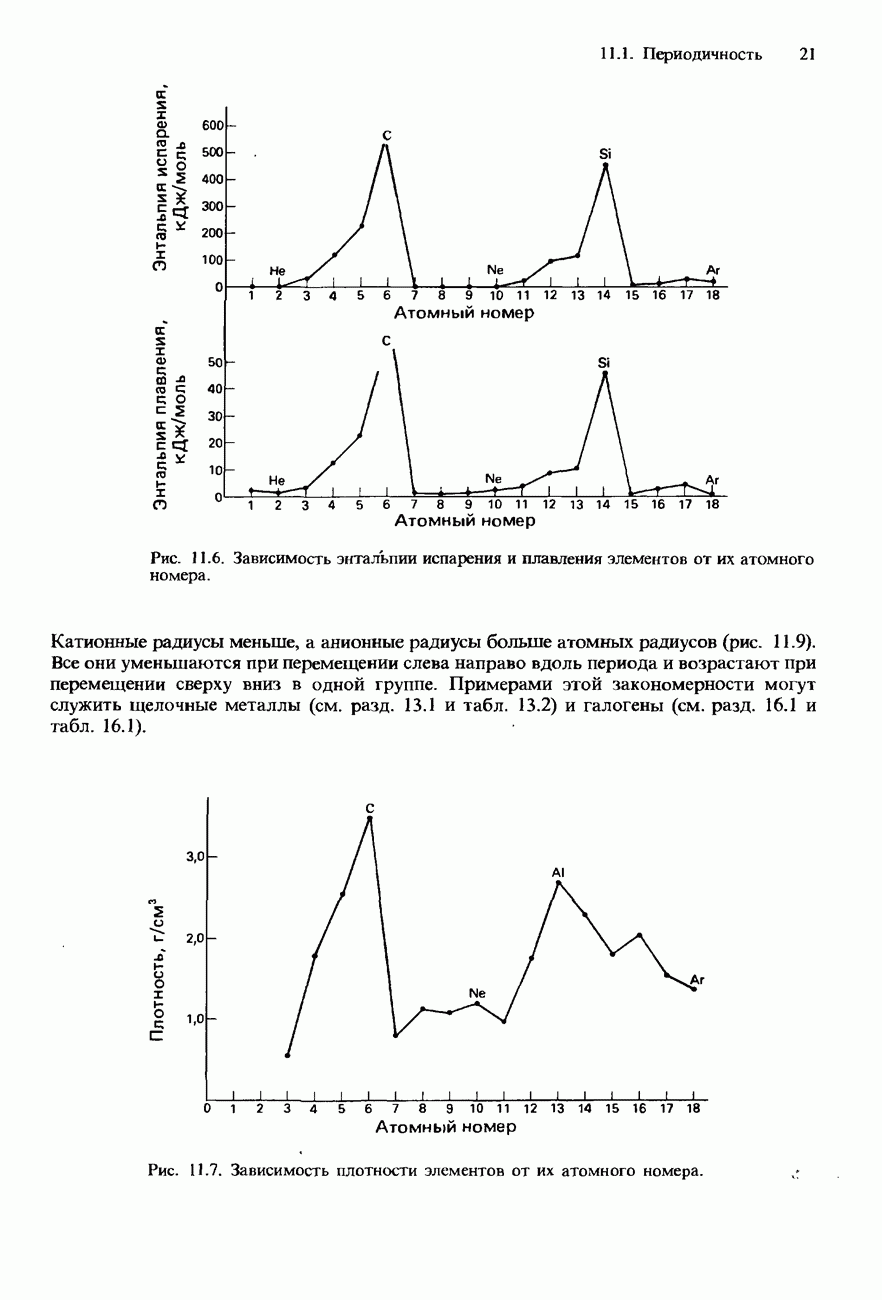
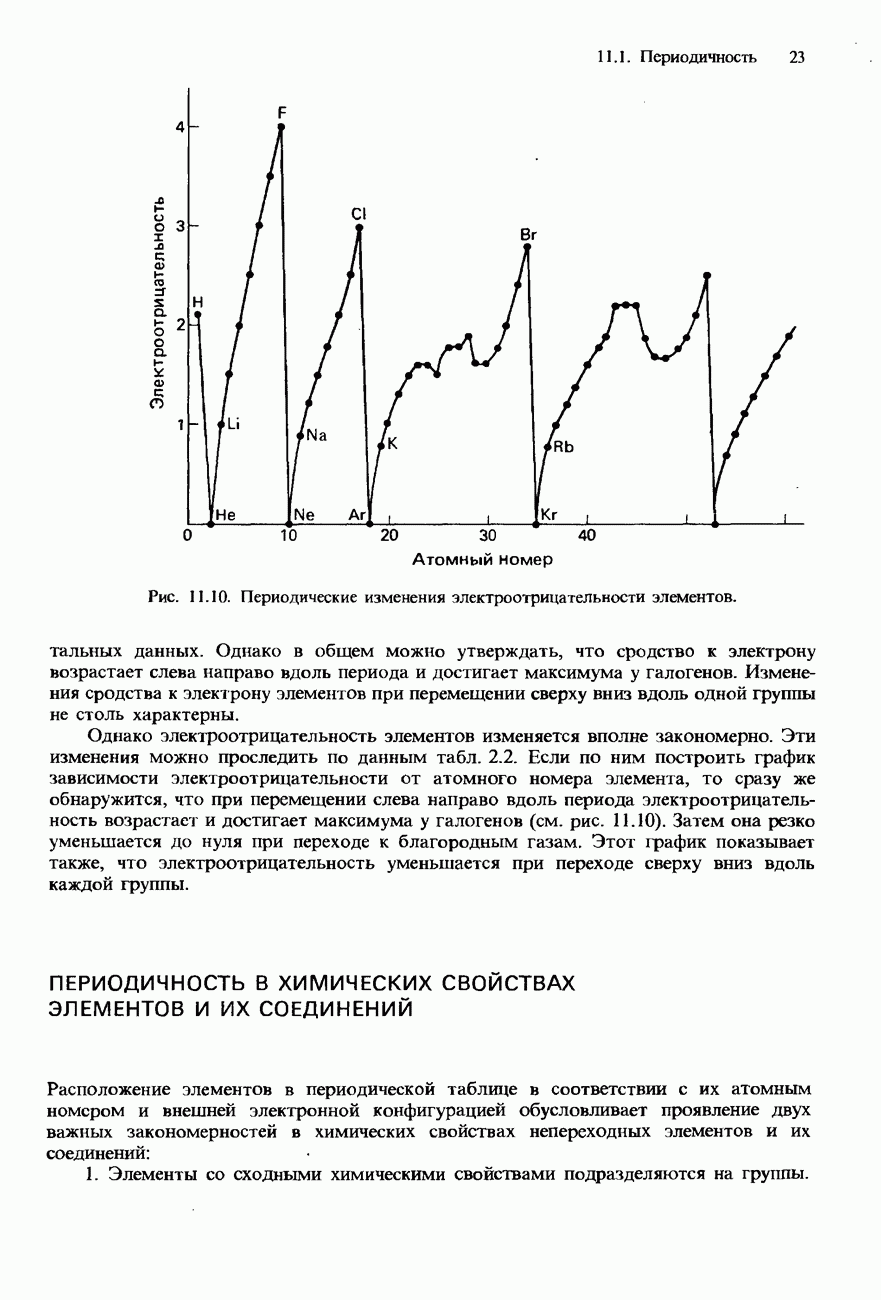
- ПЕРИОДИЧНОСТЬ
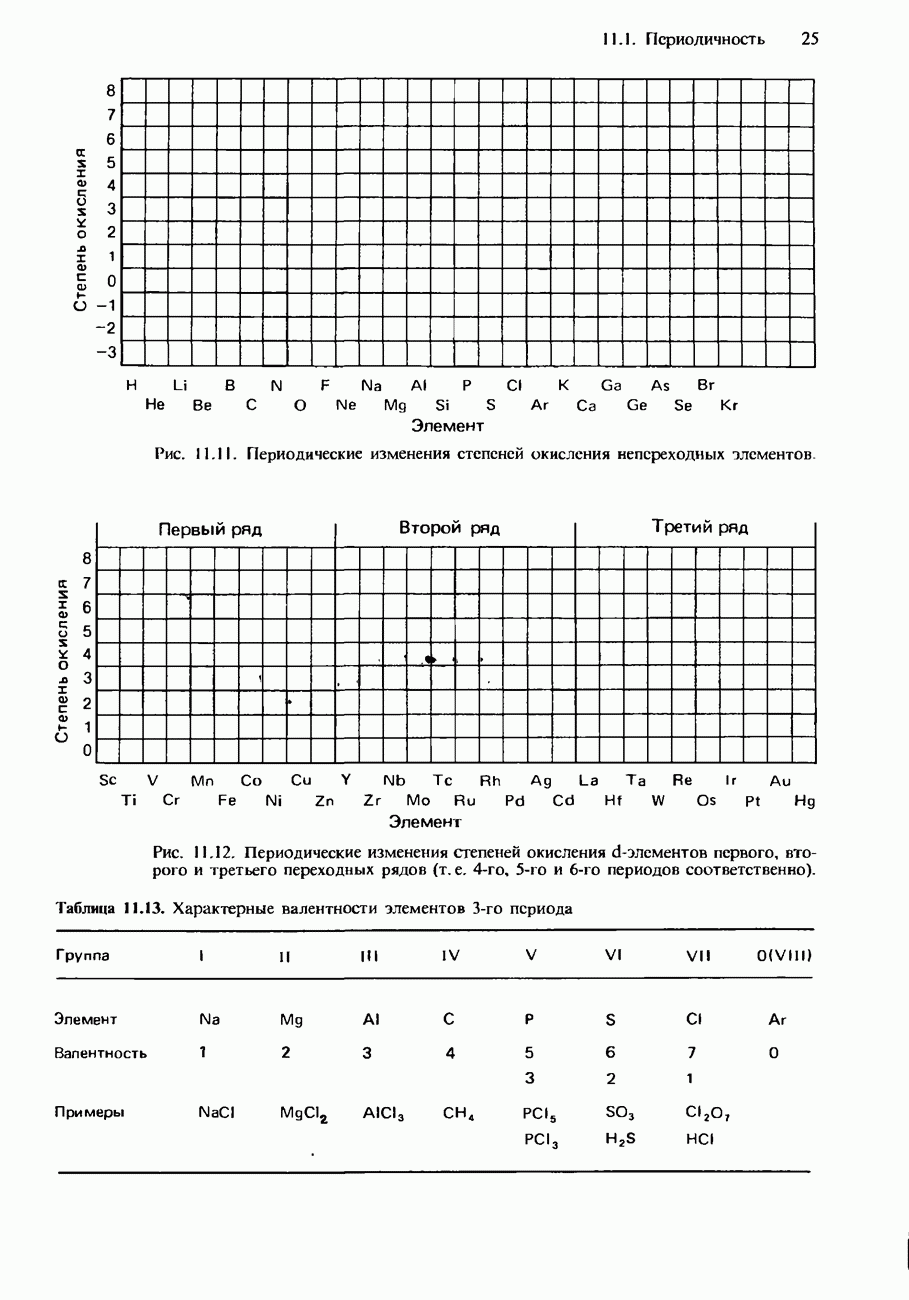
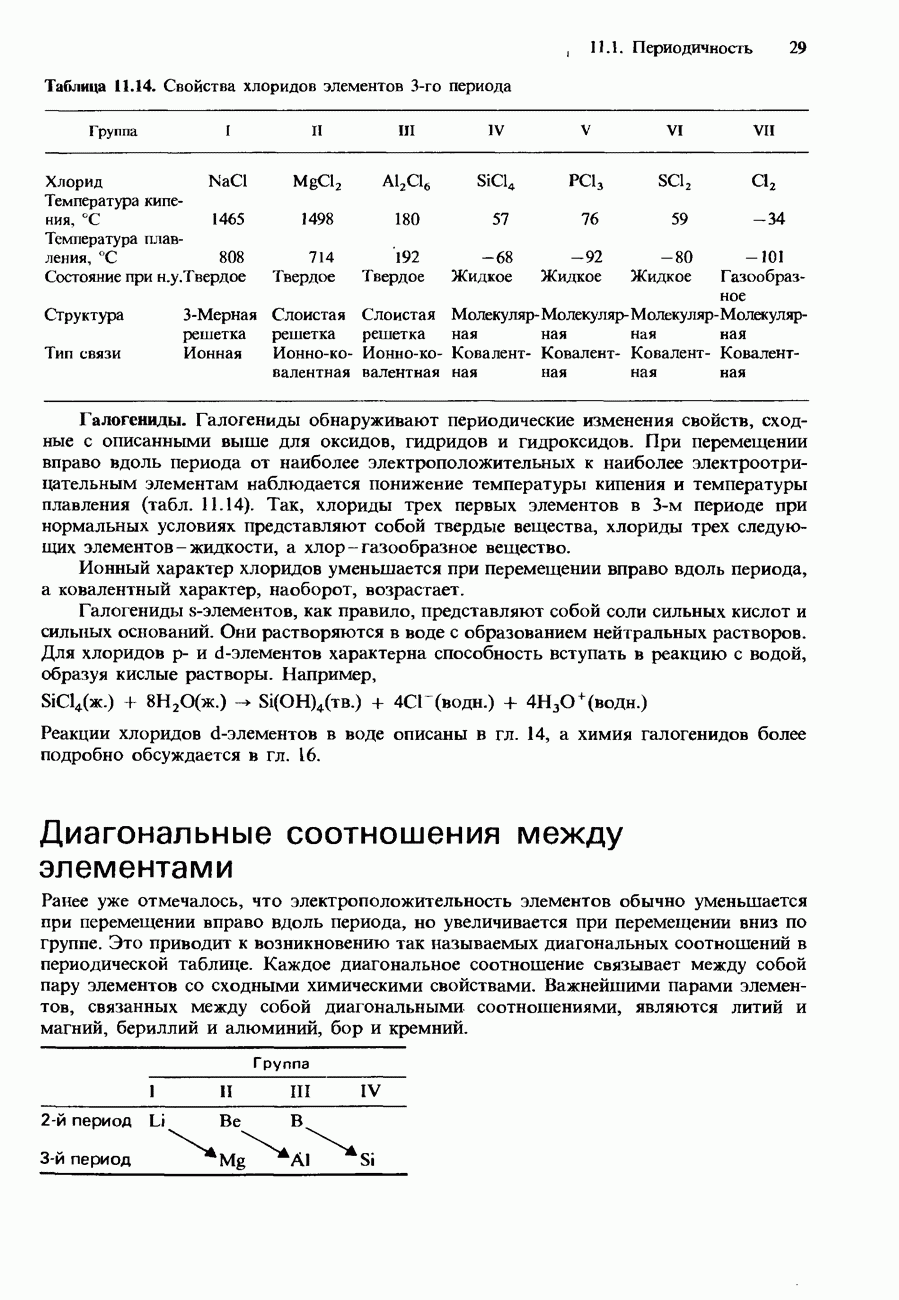
- ПЕРИОДИЧНОСТЬ В ХИМИЧЕСКИХ СВОЙСТВАХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 12. ВОДОРОД И ВОДА
- 12.1. ВОДОРОД
- ПОЛУЧЕНИЕ ВОДОРОДА В ЛАБОРАТОРНЫХ УСЛОВИЯХ
- РАЗЛИЧНЫЕ ФОРМЫ ВОДОРОДА
- ФИЗИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ХИМИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ТИПЫ СОЕДИНЕНИЙ ВОДОРОДА
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПОЛУЧЕНИЕ И ИСПОЛЬЗОВАНИЕ ВОДОРОДА
- 12.2 Вода
- ХИМИЧЕСКИЕ РЕАКЦИИ С УЧАСТИЕМ ВОДЫ
- ИСТОЧНИКИ ПРЕСНОЙ ВОДЫ И ЕЕ ИСПОЛЬЗОВАНИЕ
- КАЧЕСТВО ВОДЫ
- ЗАГРЯЗНЕНИЕ ВОДЫ
- ОЧИСТКА И ПОДГОТОВКА ВОДЫ
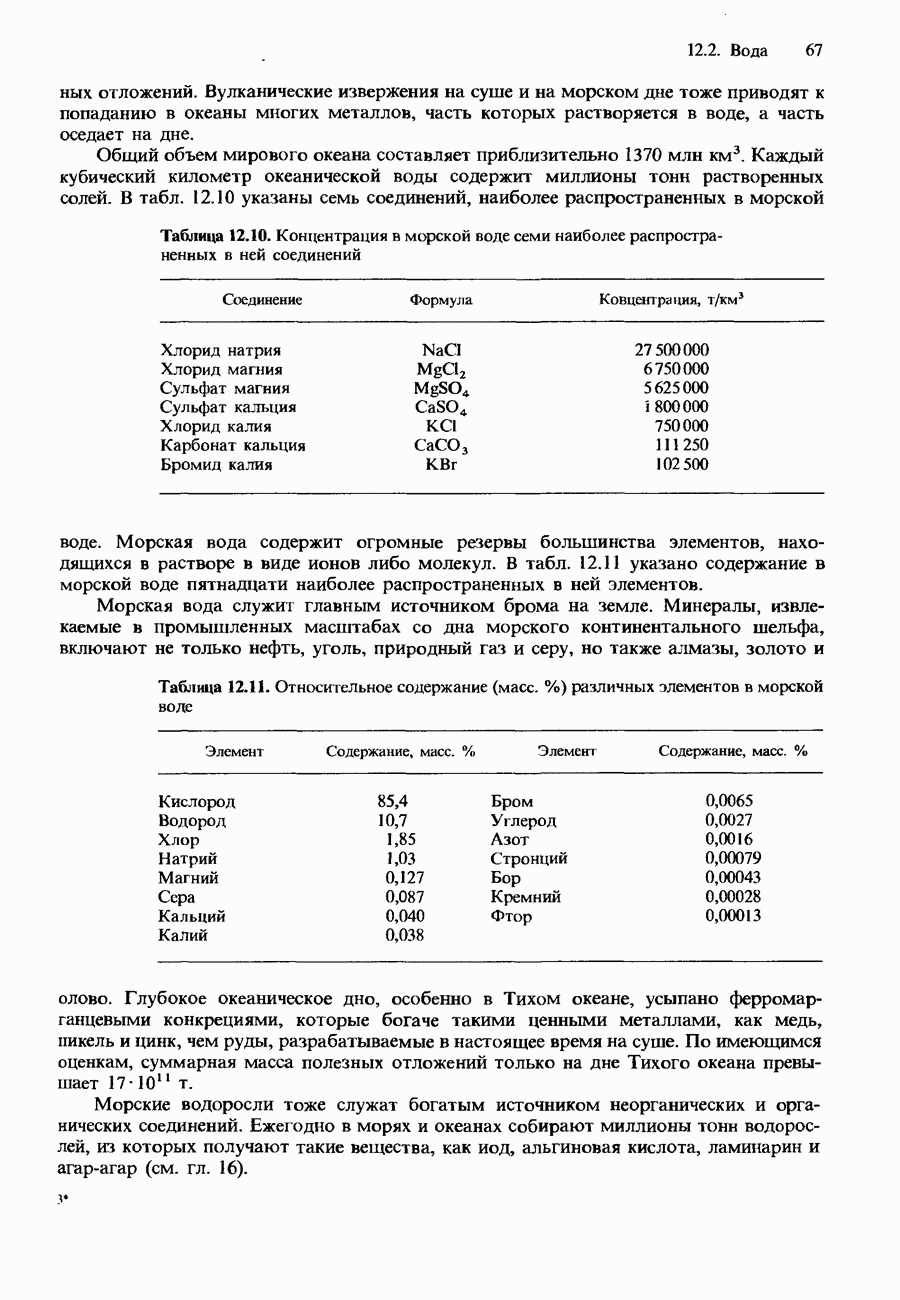
- ОКЕАНЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 13. s-Металлы
- 13.1 Структура и свойства s-металлов
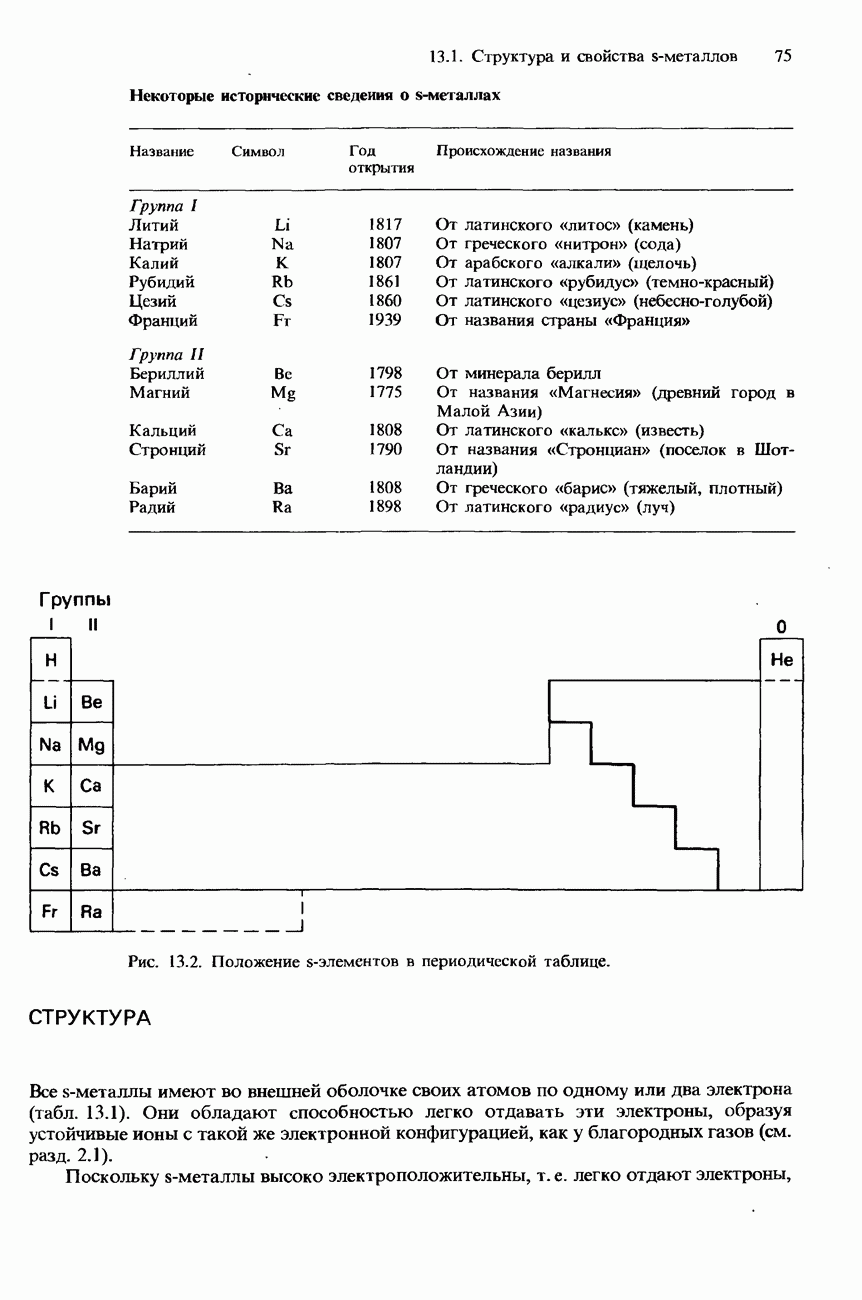
- СТРУКТУРА
- ФИЗИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ S-МЕТАЛЛОВ
- 13.2 Соединения, образуемые s-металлами
- ДРУГИЕ БИНАРНЫЕ СОЕДИНЕНИЯ
- ГИДРОКСИДЫ
- КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- ТЕРМИЧЕСКАЯ УСТОЙЧИВОСТЬ ОКСОСОЕДИНЕНИЙ S-МЕТАЛЛОВ
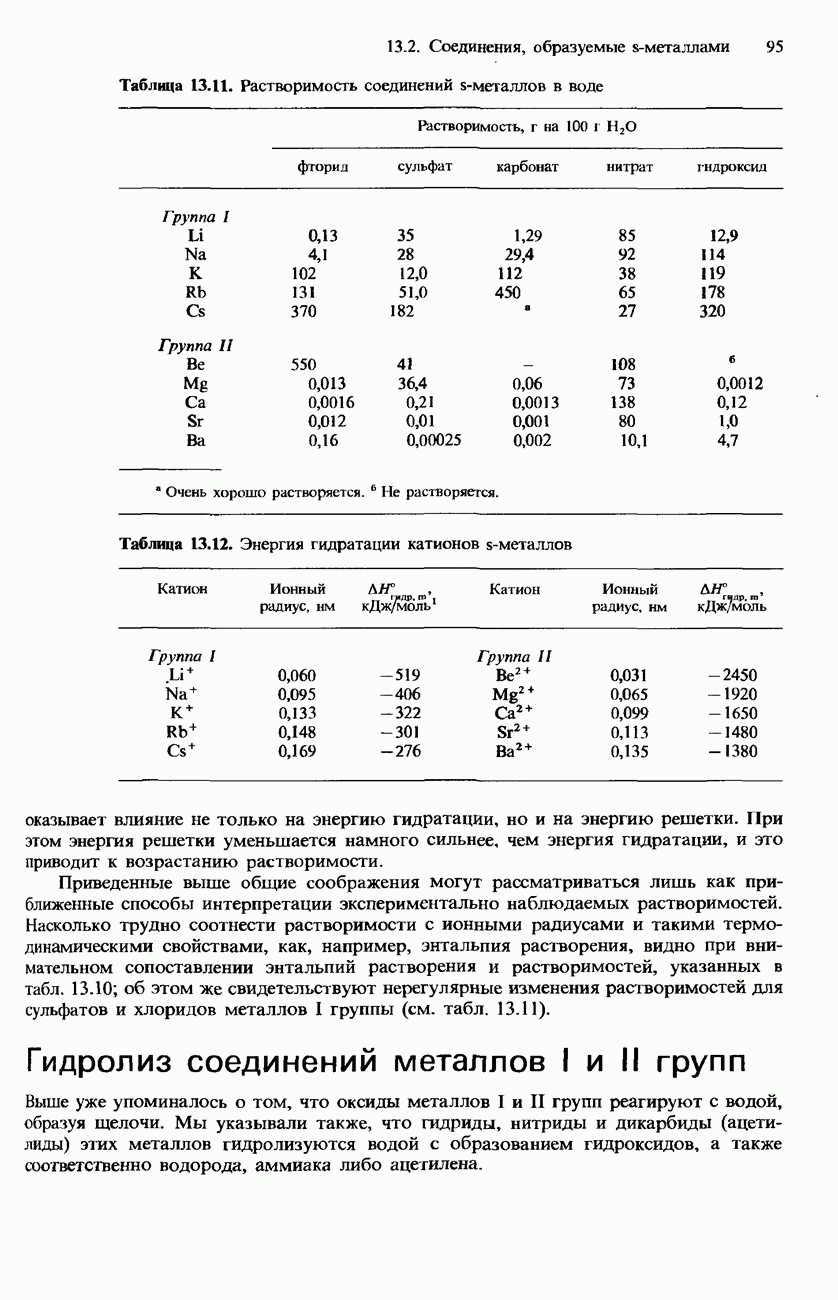
- РАСТВОРИМОСТЬ СОЛЕЙ И ГИДРОКСИДОВ МЕТАЛЛОВ I И II ГРУПП В ВОДЕ
- АНОМАЛЬНЫЕ СВОЙСТВА ЛИТИЯ И БЕРИЛЛИЯ, А ТАКЖЕ ИХ СОЕДИНЕНИЙ
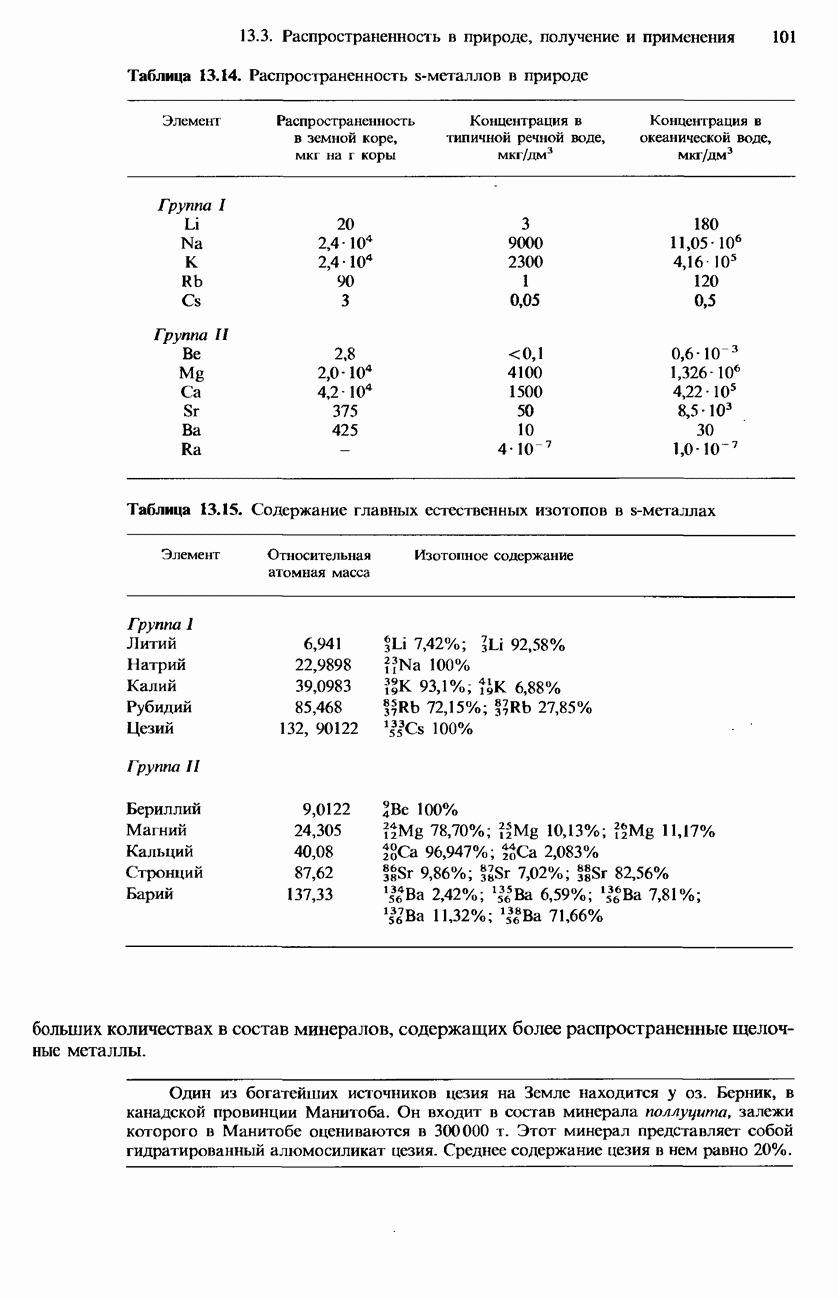
- 13.3. Распространенность в природе, получение и применение
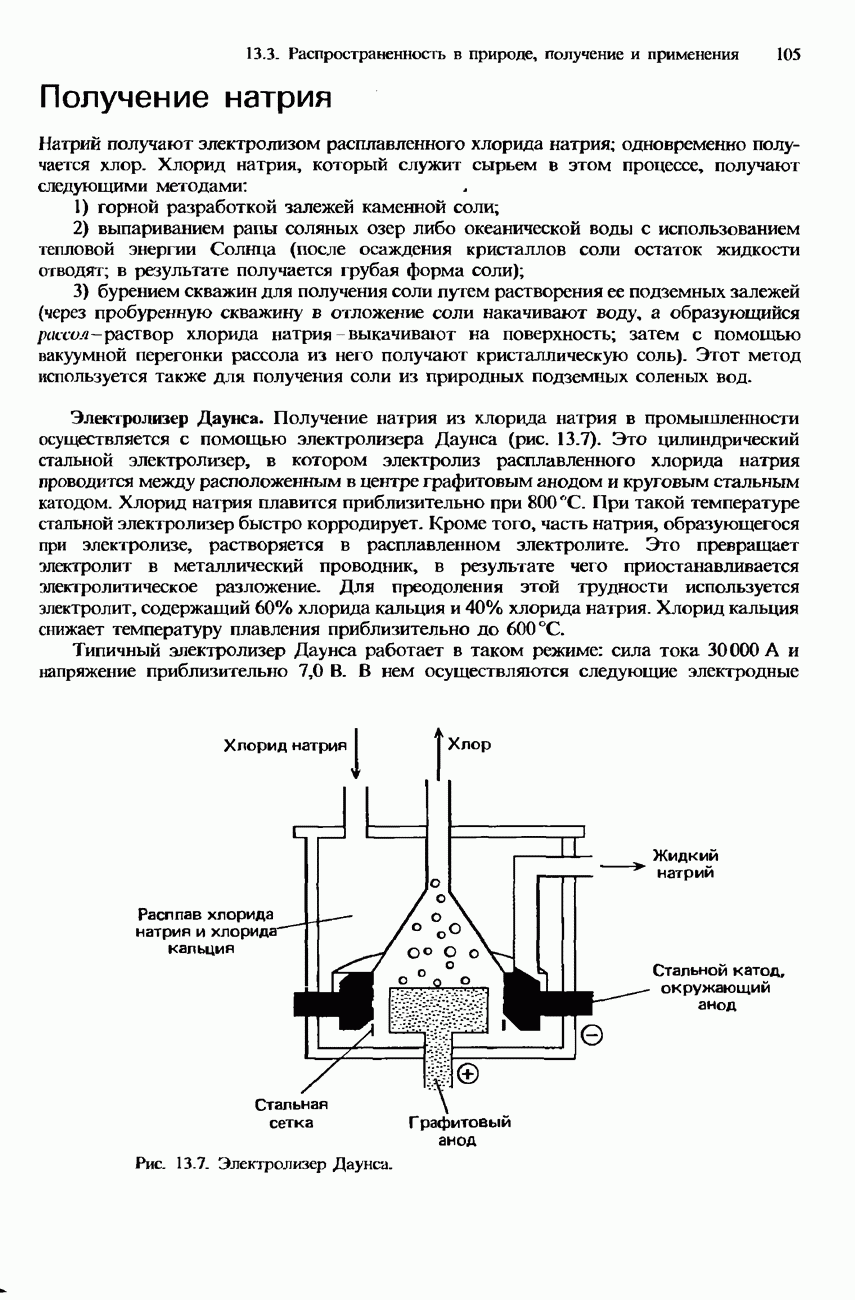
- ПОЛУЧЕНИЕ S-МЕТАЛЛОВ
- ПОЛУЧЕНИЕ СОЕДИНЕНИЙ S-МЕТАЛЛОВ
- ПРИМЕНЕНИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 14. d-ЭЛЕМЕНТЫ
- 14.1. Структура и свойства d-элементов
- d-ЭЛЕМЕНТЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА
- ХИМИЧЕСКИЕ СВОЙСТВА
- 14.2 Химия семи d-элементов
- МАРГАНЕЦ
- ЖЕЛЕЗО
- КОБАЛЬТ
- НИКЕЛЬ
- МЕДЬ
- ЦИНК
- 14.3. Распространенность в природе, получение и применения
- ПРОИЗВОДСТВО ЖЕЛЕЗА И СТАЛИ
- ПОЛУЧЕНИЕ ДРУГИХ МЕТАЛЛОВ ПЕРВОГО ПЕРЕХОДНОГО РЯДА
- ПРИМЕНЕНИЯ d-ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 15. ЭЛЕМЕНТЫ III-VI ГРУПП
- 15.1. Алюминий и другие элементы III группы
- БОР
- ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ АЛЮМИНИЯ
- ПРИМЕНЕНИЯ АЛЮМИНИЯ И ЕГО СОЕДИНЕНИЙ
- 15.2. IV группа периодической системы
- СОЕДИНЕНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ ИЗ РУД
- ПРИМЕНЕНИЯ УГЛЕРОДА
- ПРИМЕНЕНИЯ КРЕМНИЯ
- ПРИМЕНЕНИЯ ГЕРМАНИЯ, ОЛОВА И СВИНЦА
- 15.3. Элементы V группы
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ. ПОЛУЧЕНИЕ И ПРИМЕНЕНИЯ АЗОТА И ФОСФОРА
- СОЕДИНЕНИЯ АЗОТА
- СОЕДИНЕНИЯ ФОСФОРА
- 15.4. Элементы VI группы. Кислород и сера
- КИСЛОРОД
- СОЕДИНЕНИЯ КИСЛОРОДА
- СЕРА
- СОЕДИНЕНИЯ СЕРЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 16. ГАЛОГЕНЫ И БЛАГОРОДНЫЕ ГАЗЫ
- 16.1. Галогены
- ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ ГАЛОГЕНОВ
- ЛАБОРАТОРНЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ГАЛОГЕНОВ
- ФИЗИЧЕСКИЕ И БИОЛОГИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ ГАЛОГЕНОВ
- 16.2. Соединения галогенов
- ГАЛОГЕНОВОДОРОДЫ
- КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ ГАЛОГЕНОВ
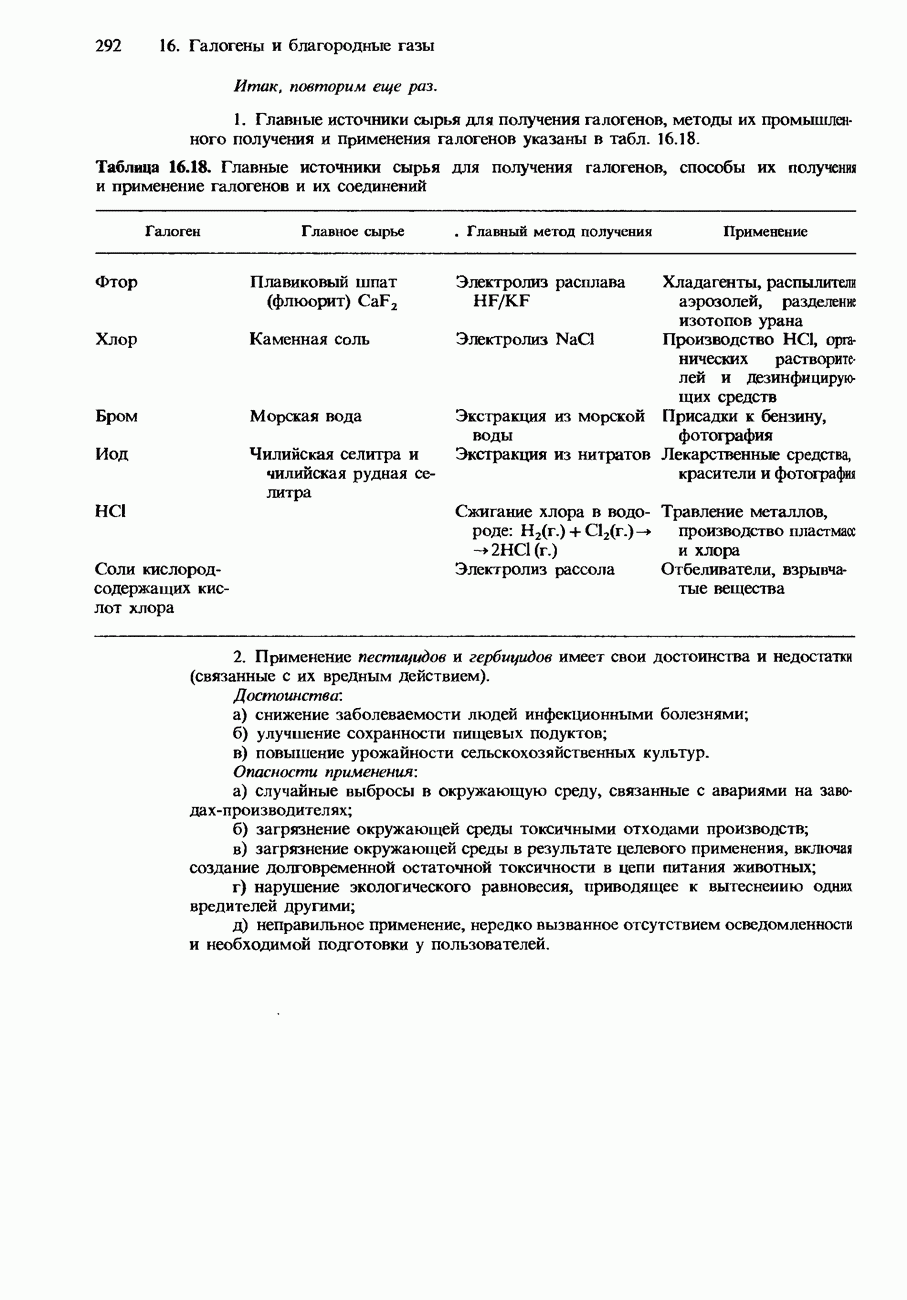
- 16.3. Распространенность, получение и применение галогенов и их соединений
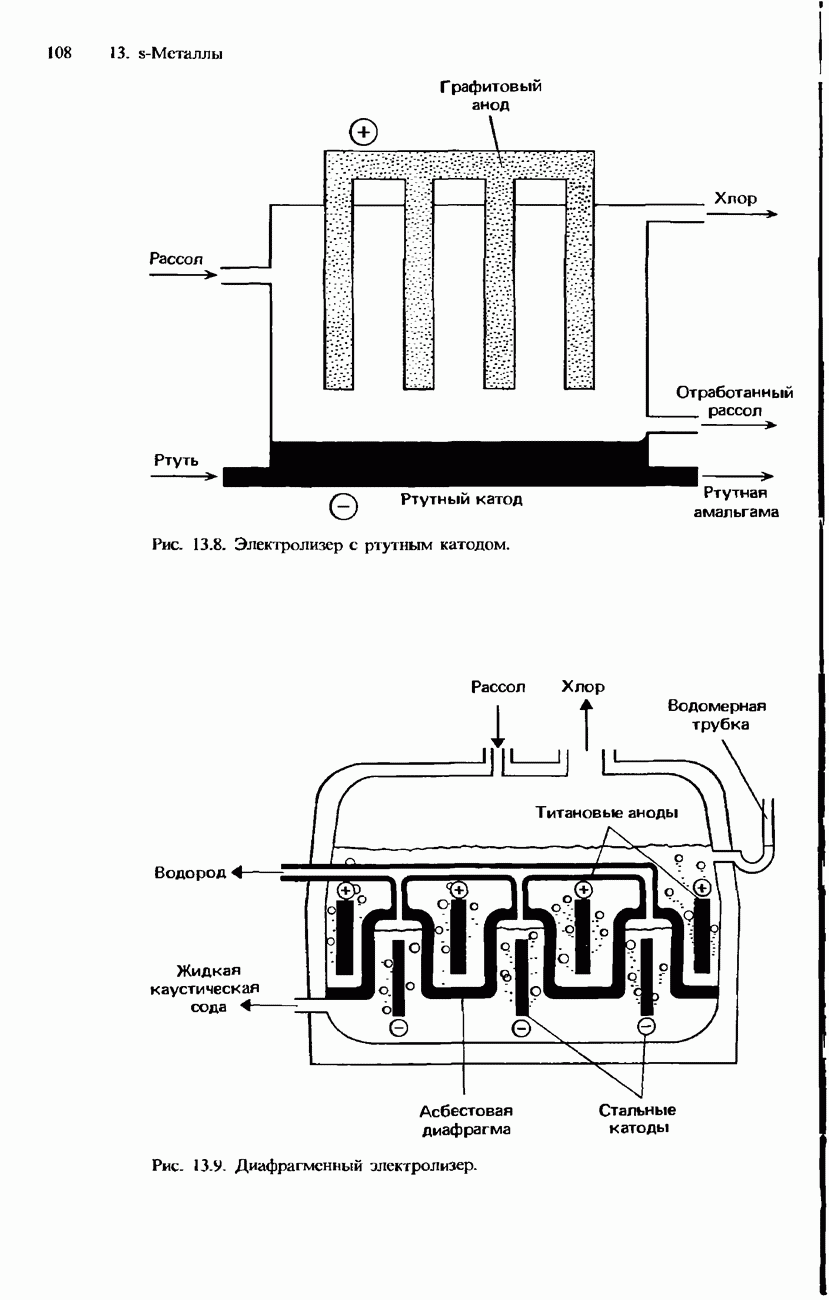
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ХЛОРА
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ДРУГИХ ГАЛОГЕНОВ
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СОЕДИНЕНИЙ ХЛОРА
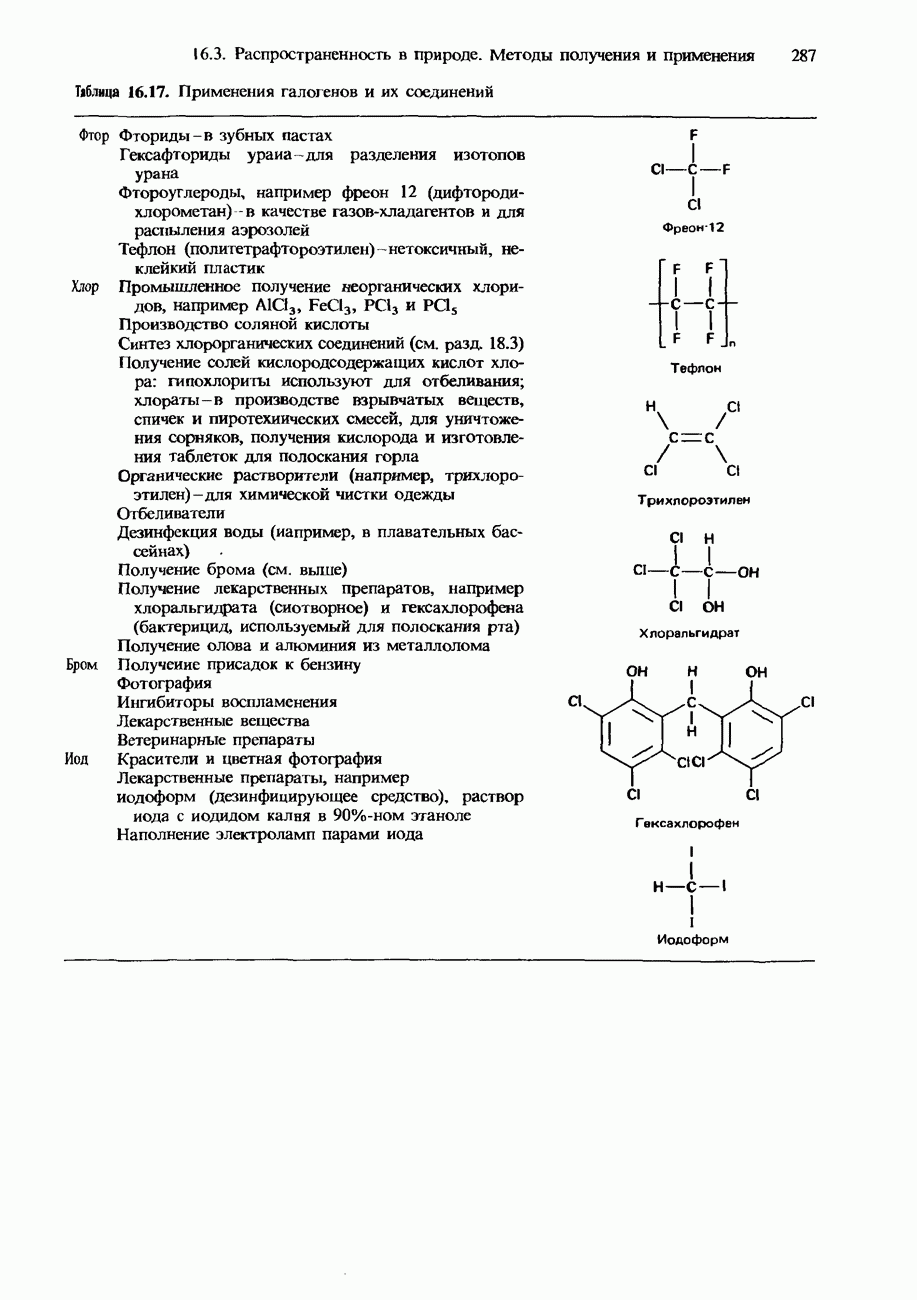
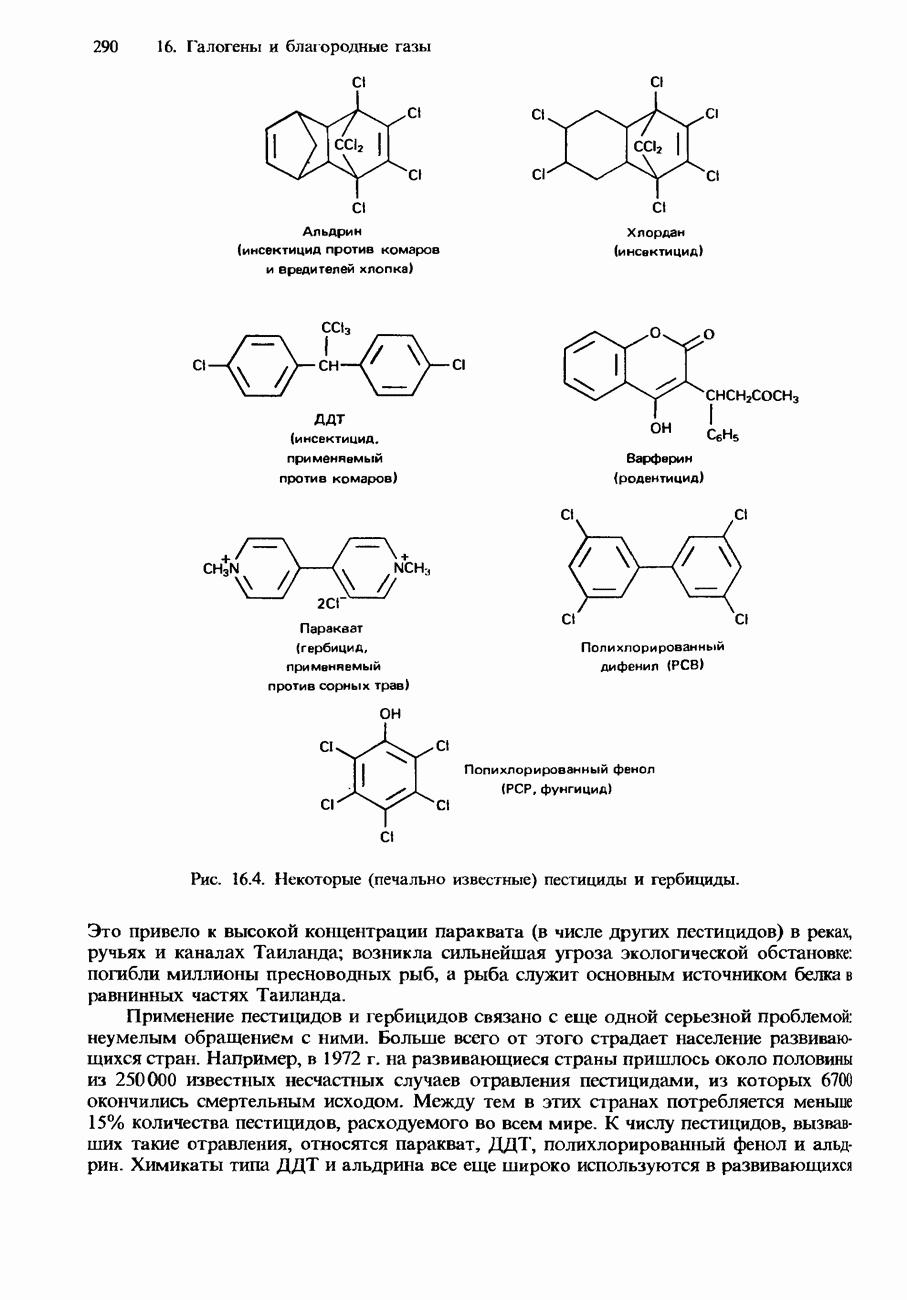
- ПРИМЕНЕНИЯ ГАЛОГЕНОВ И ИХ СОЕДИНЕНИЙ
- ТОКСИЧНОСТЬ ХЛОРСОДЕРЖАЩИХ ПРОДУКТОВ
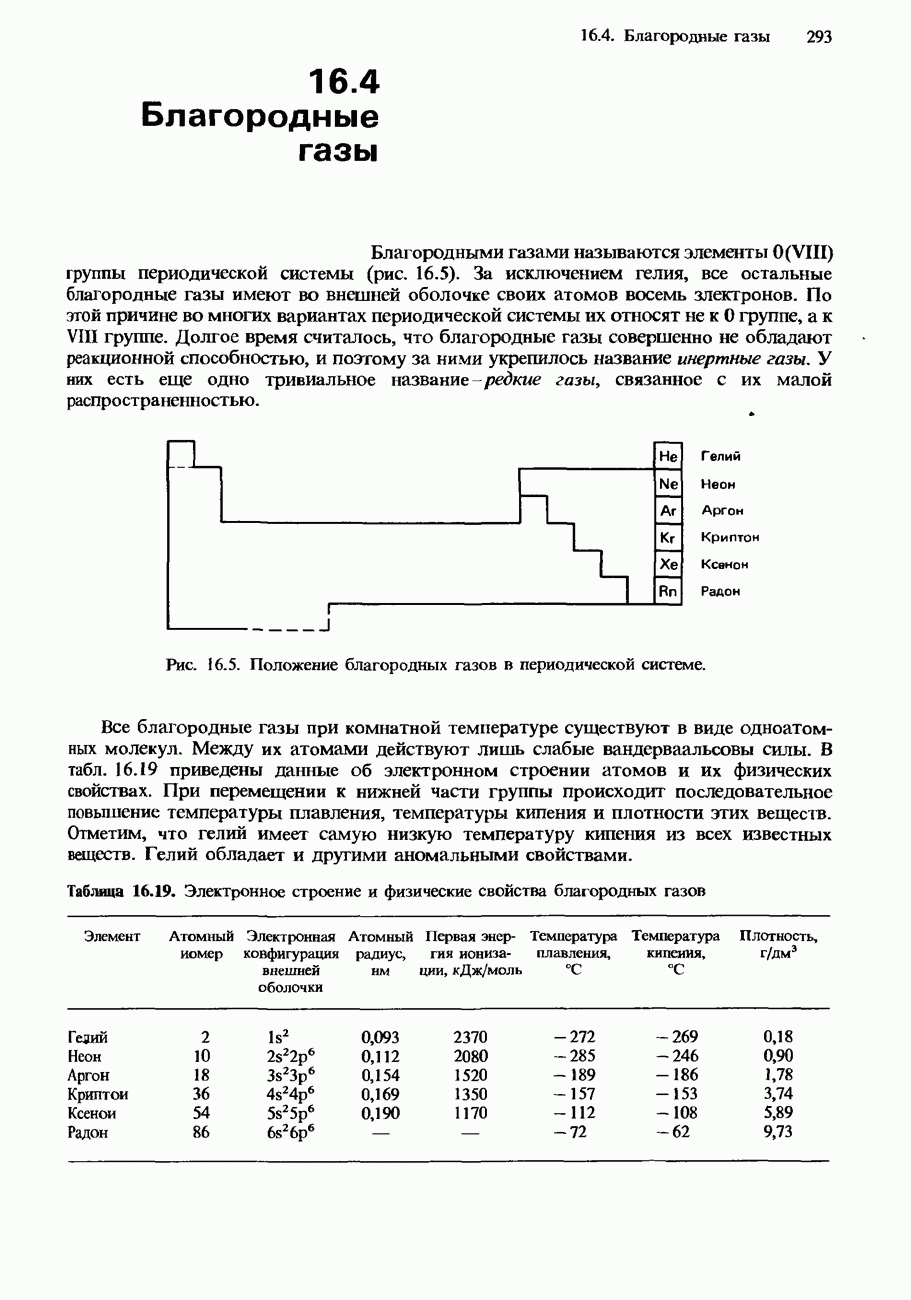
- 16.4. Благородные газы
- СОЕДИНЕНИЯ БЛАГОРОДНЫХ ГАЗОВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 17. ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ
- 7.1. Органическая химия
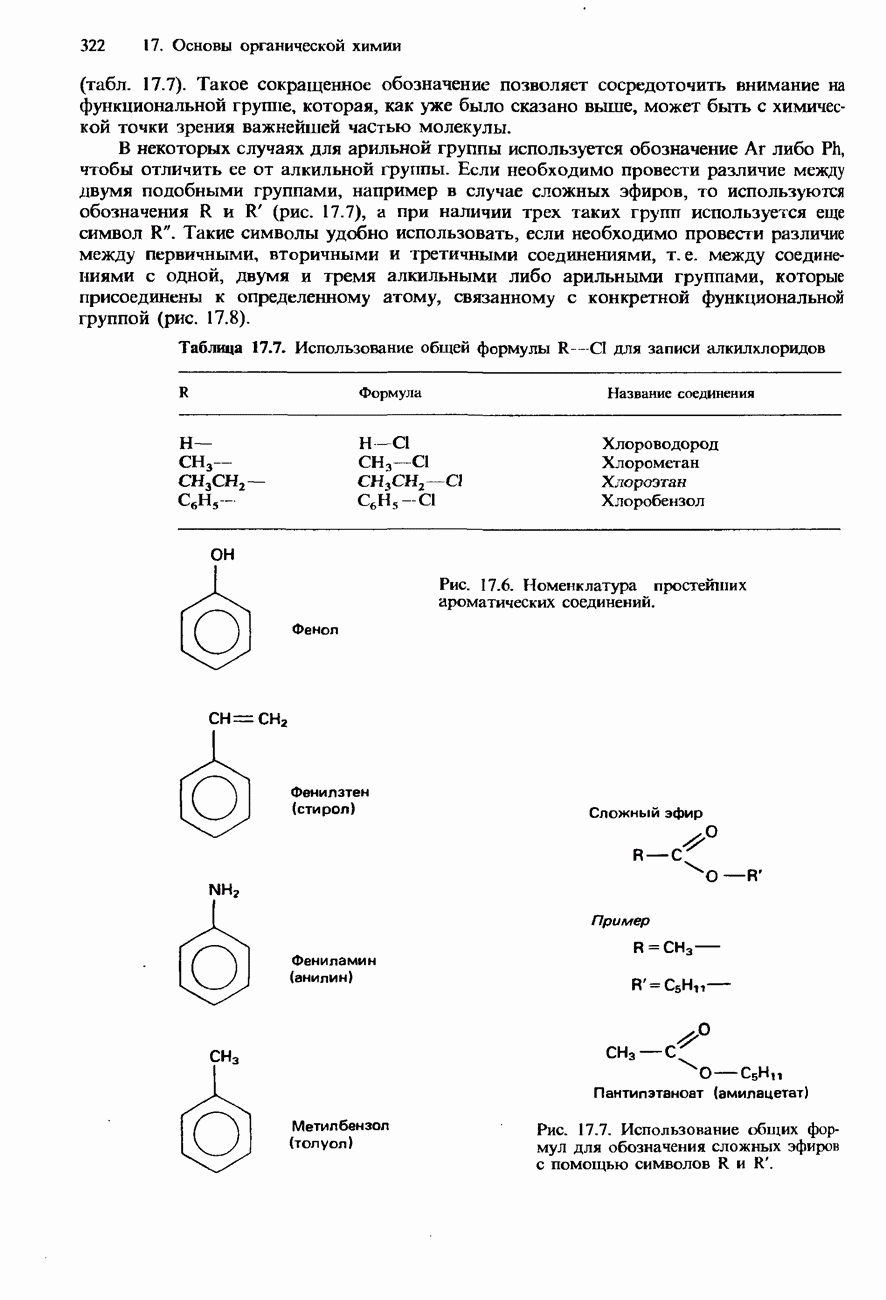
- НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
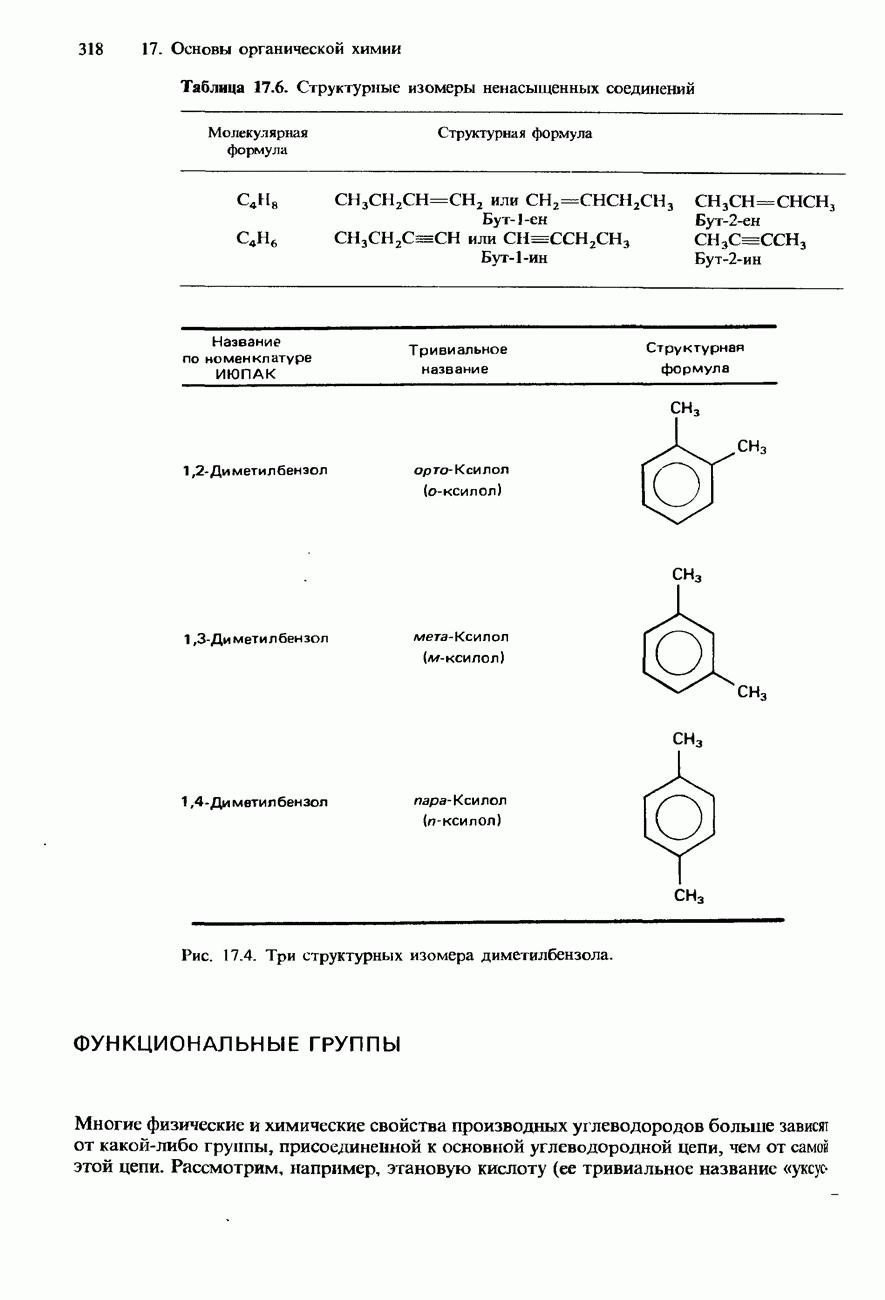
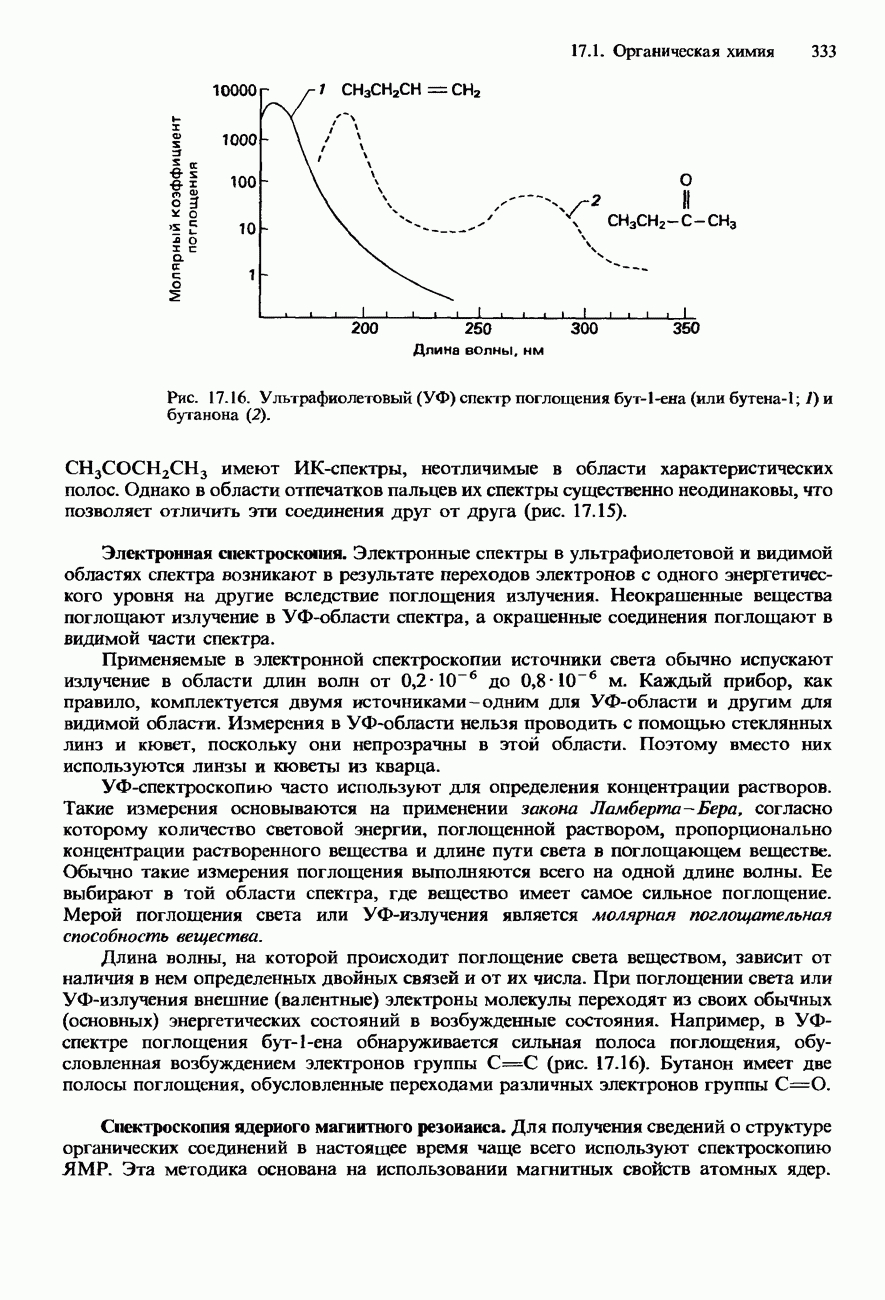
- УГЛЕВОДОРОДЫ
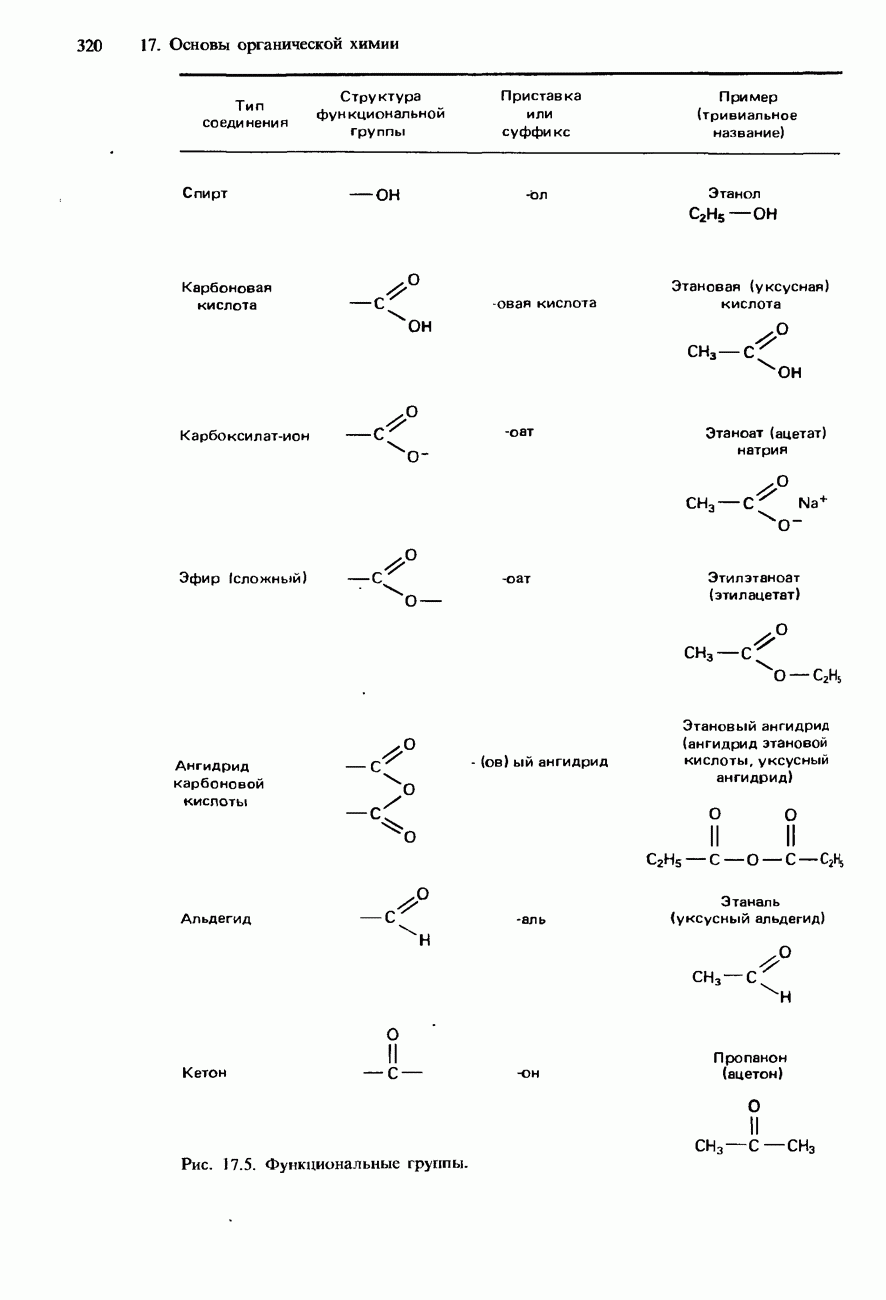
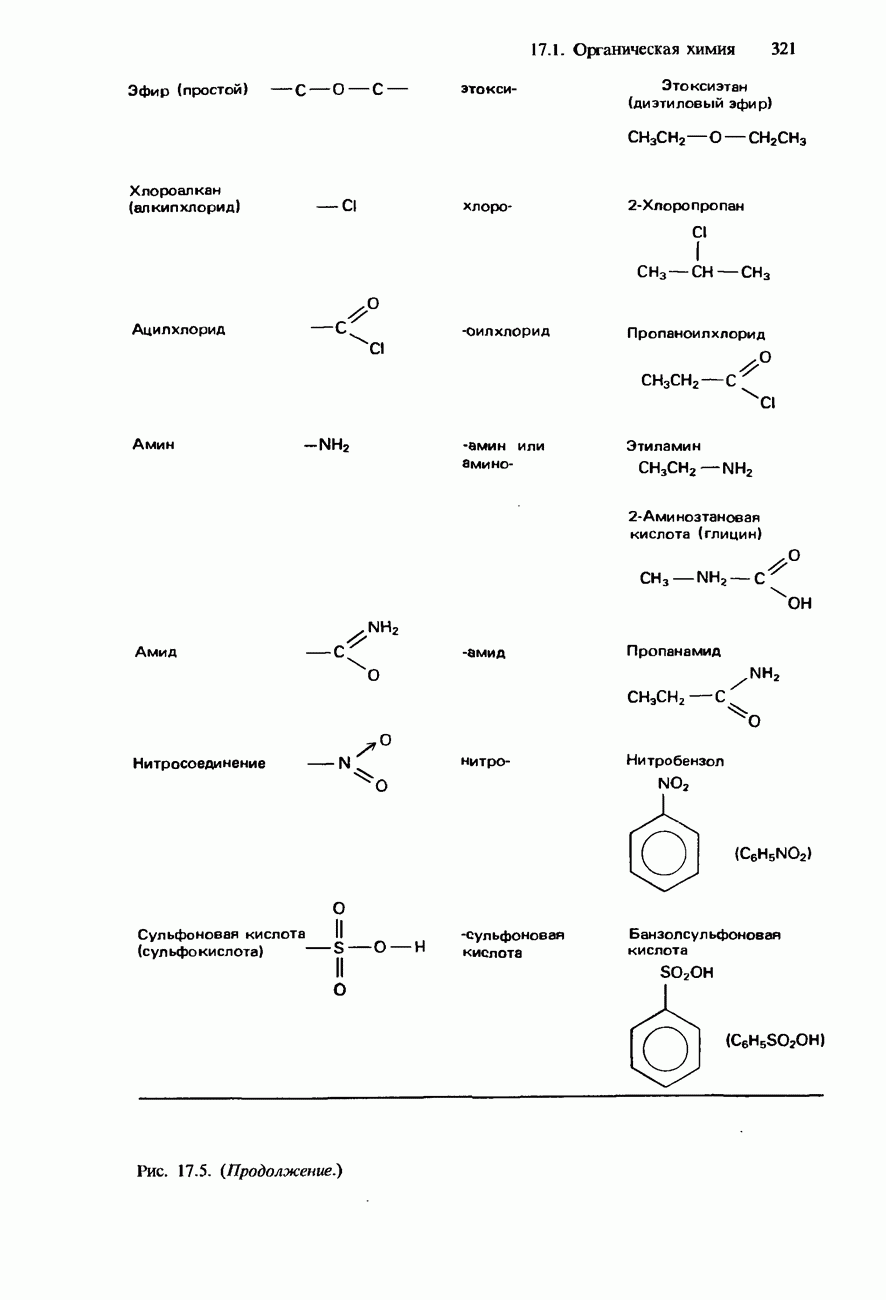
- ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ПОЛУЧЕНИЕ И ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 17.2. Молекулярная структура органических соединений
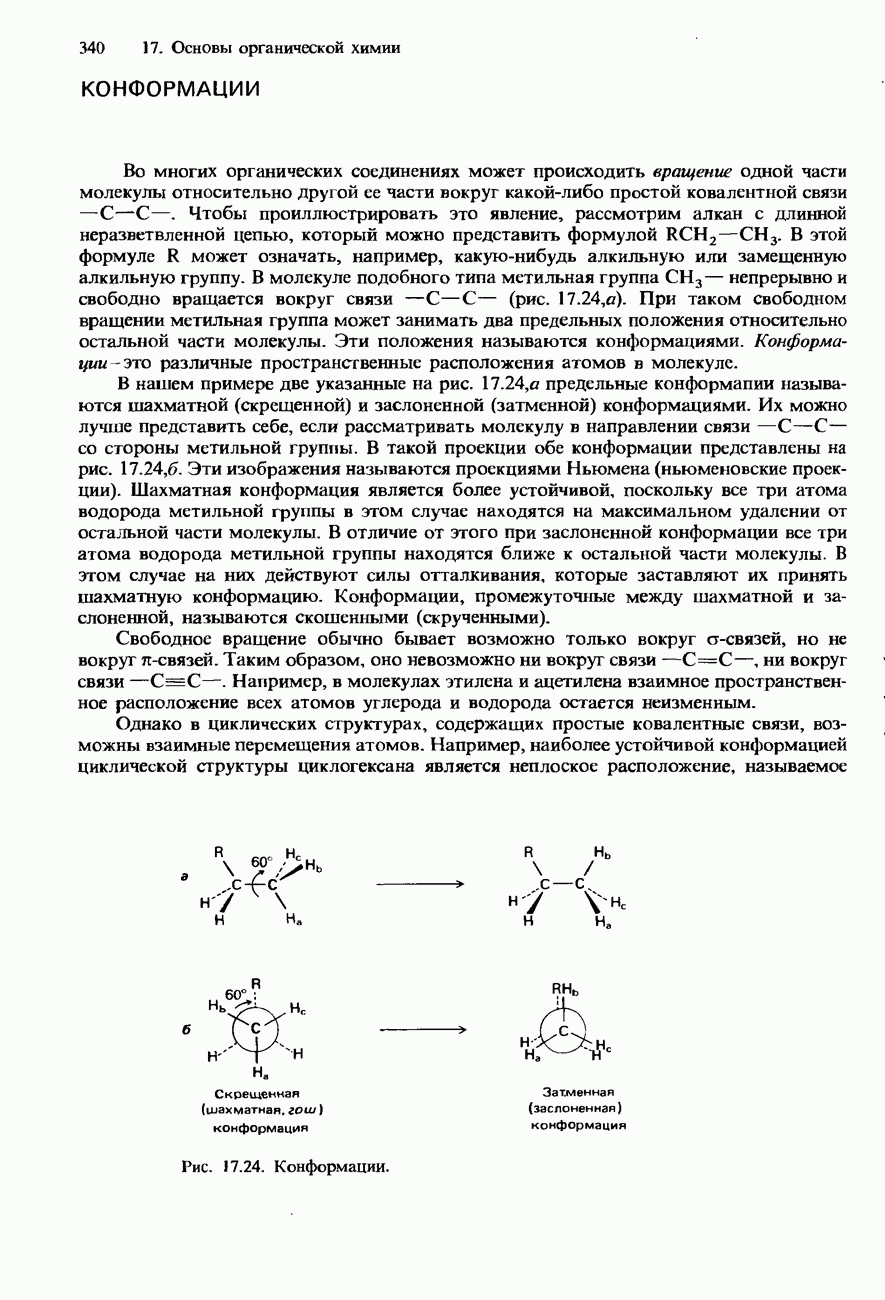
- КОНФОРМАЦИИ
- СТЕРЕОИЗОМЕРИЯ
- 17.3. Механизмы органических реакций
- ФАКТОРЫ, ВЛИЯЮЩИЕ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- НУКЛЕОФИЛЫ И ЭЛЕКТРОФИЛЫ
- ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 18. УГЛЕВОДОРОДЫ
- 18.1. Алифатические углеводороды
- АЛКАНЫ
- АЛКЕНЫ
- АЛКИНЫ
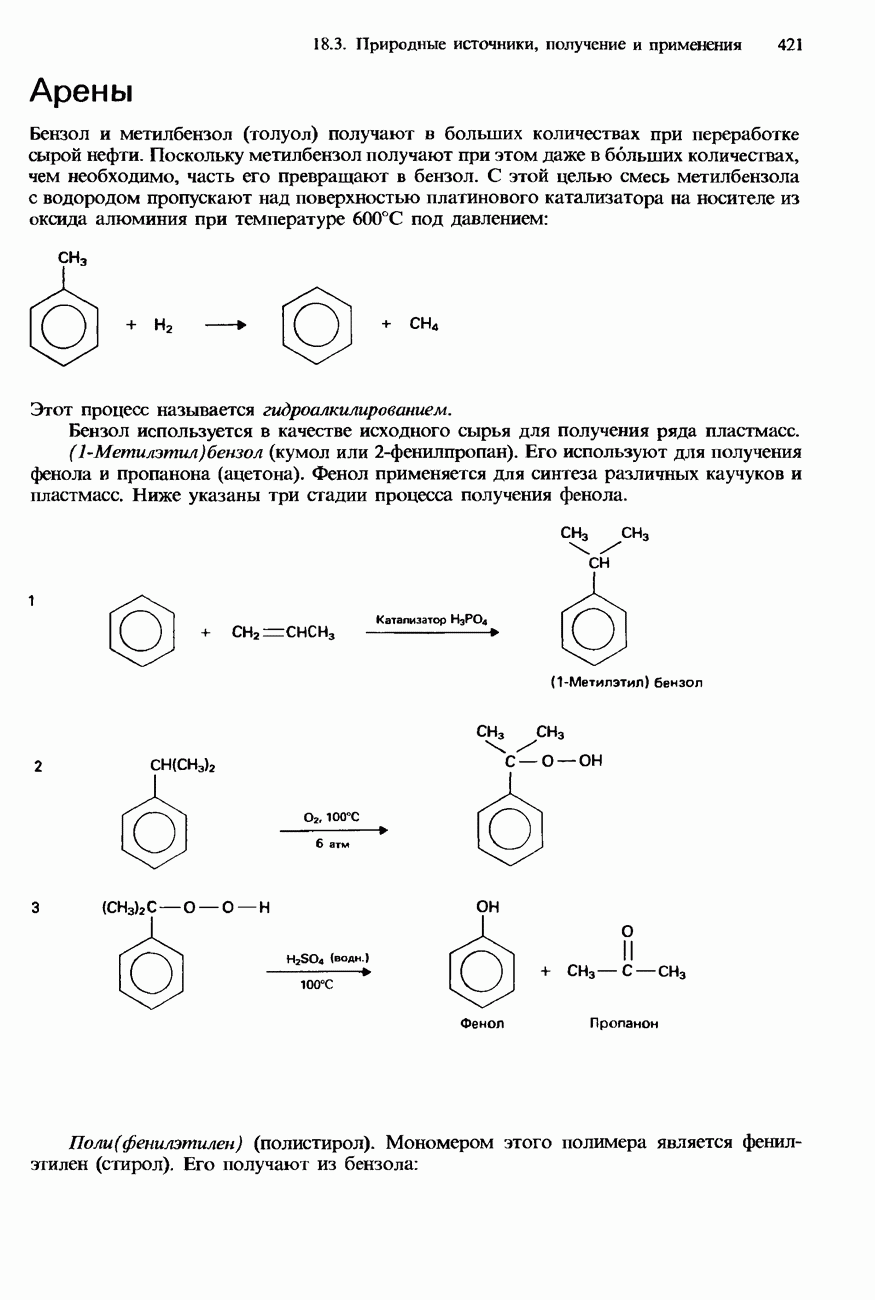
- 18.2. Арены
- БЕНЗОЛ
- МЕТИЛБЕНЗОЛ
- 18.3. Природные источники, получение и применения
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ УГЛЕВОДОРОДОВ
- ПЕРЕРАБОТКА НЕФТИ
- ПРИМЕНЕНИЯ УГЛЕВОДОРОДОВ
- ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ НЕФТЬЮ И ПРОДУКТАМИ ЕЕ СГОРАНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 19. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
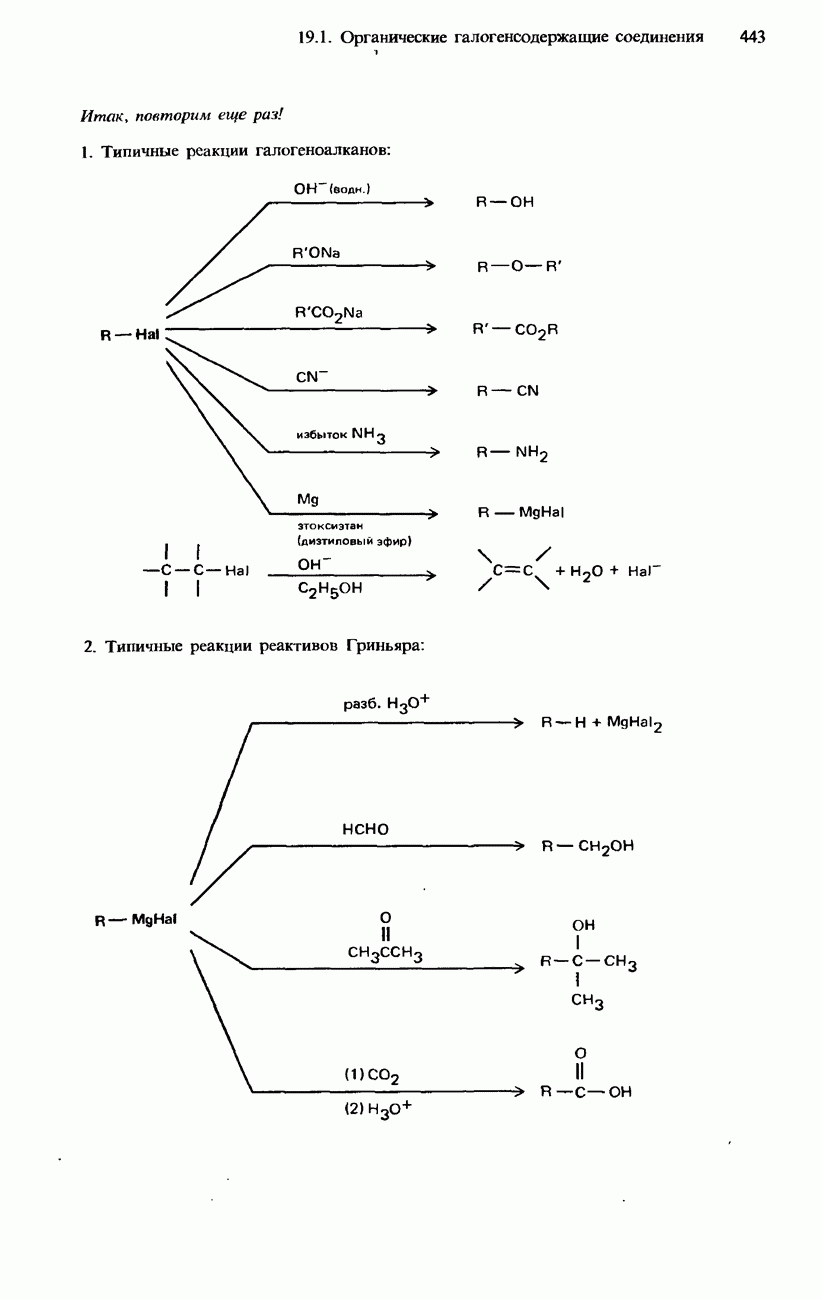
- 19.1. Органические галогенсодержащие соединения
- ГАЛОГЕНОАЛКЕНЫ
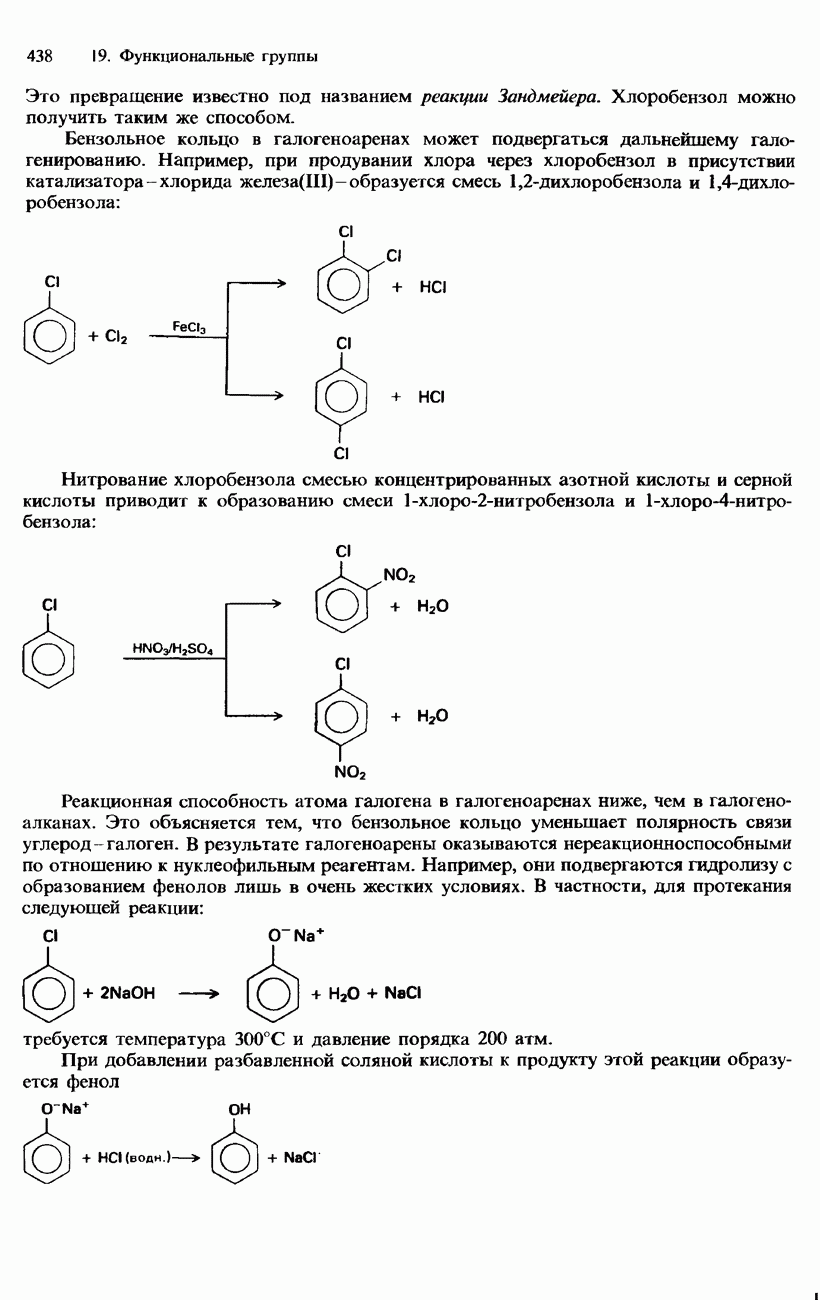
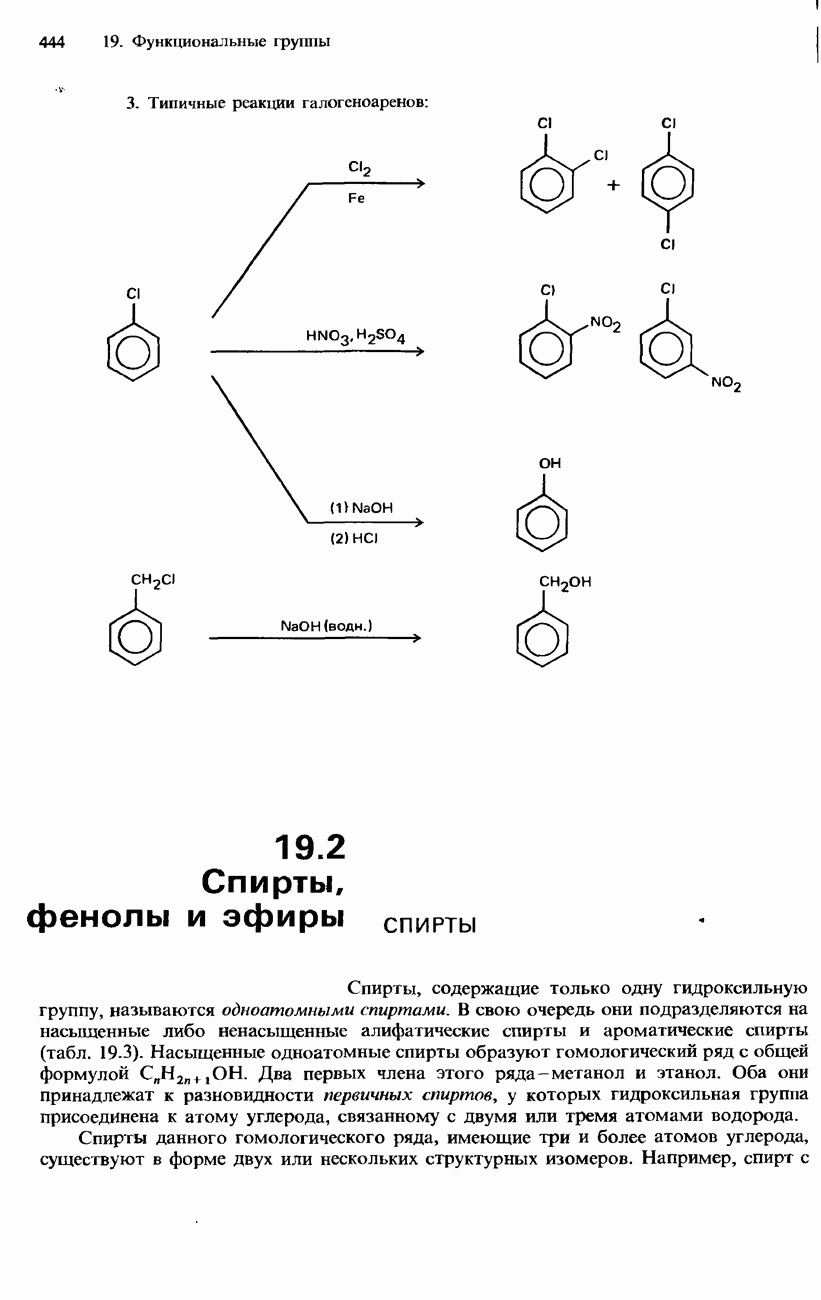
- ГАЛОГЕНОАРЕНЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ОРГАНИЧЕСКИХ ГАЛОГЕНСОДЕРЖАЩИХ СОЕДИНЕНИЙ
- 19.2. Спирты, фенолы и эфиры
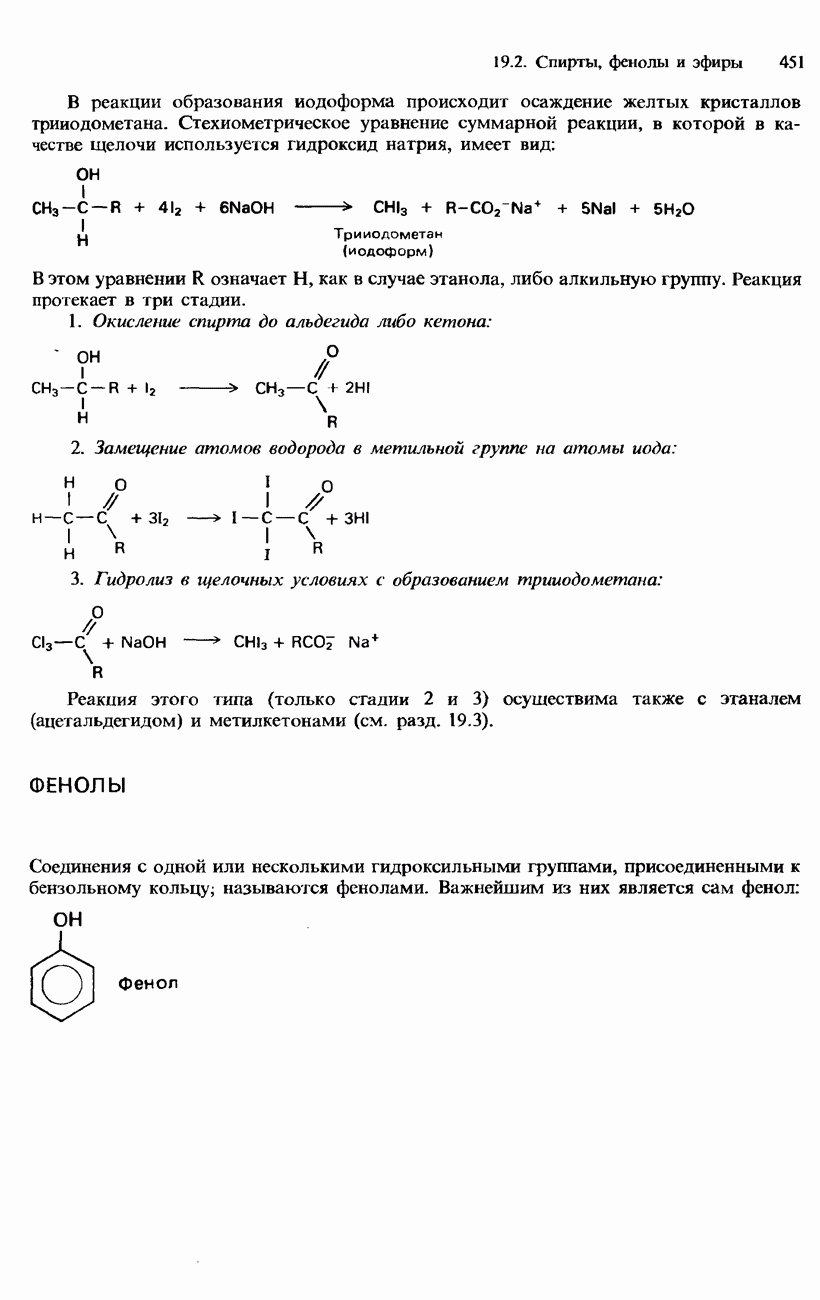
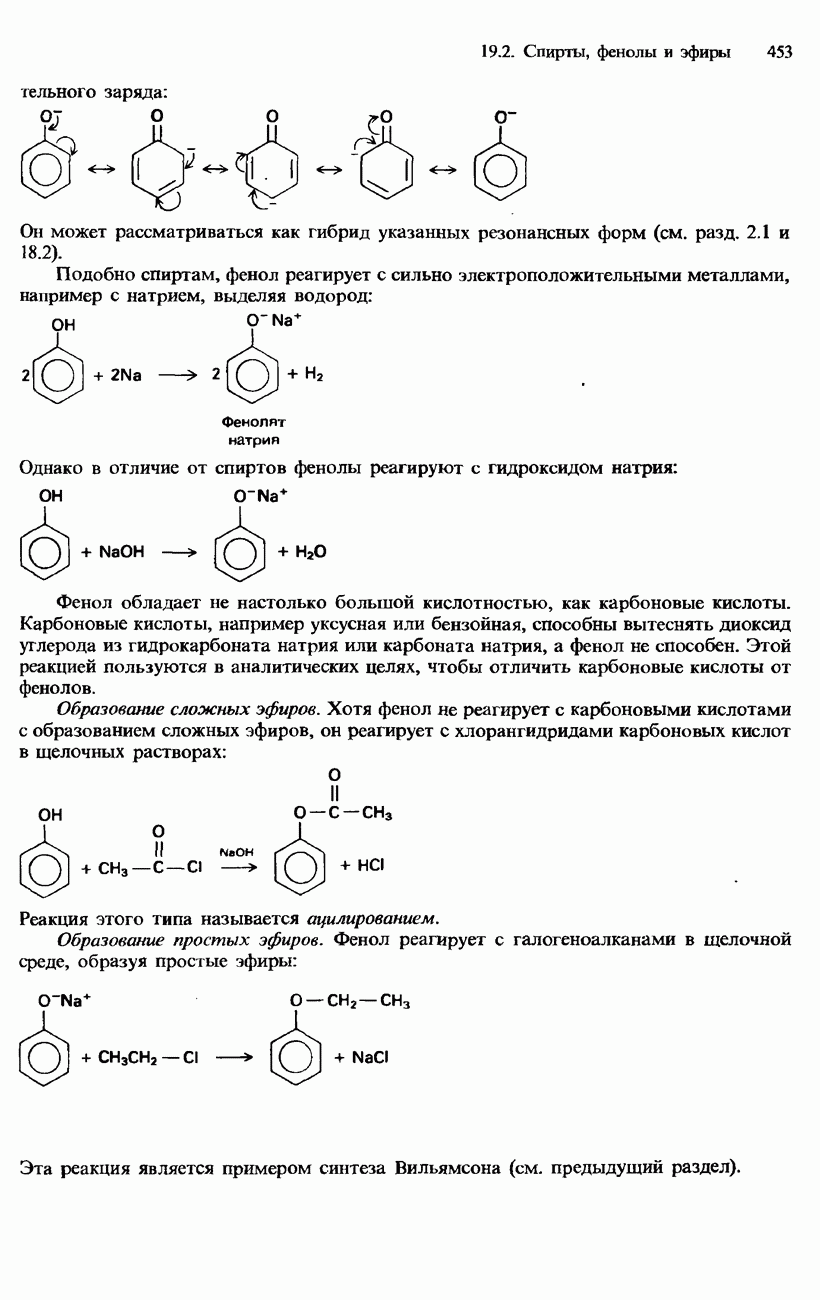
- ФЕНОЛЫ
- ПРОСТЫЕ ЭФИРЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ СПИРТОВ, ФЕНОЛОВ И ПРОСТЫХ ЭФИРОВ
- 19.3. Карбонильная группа
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
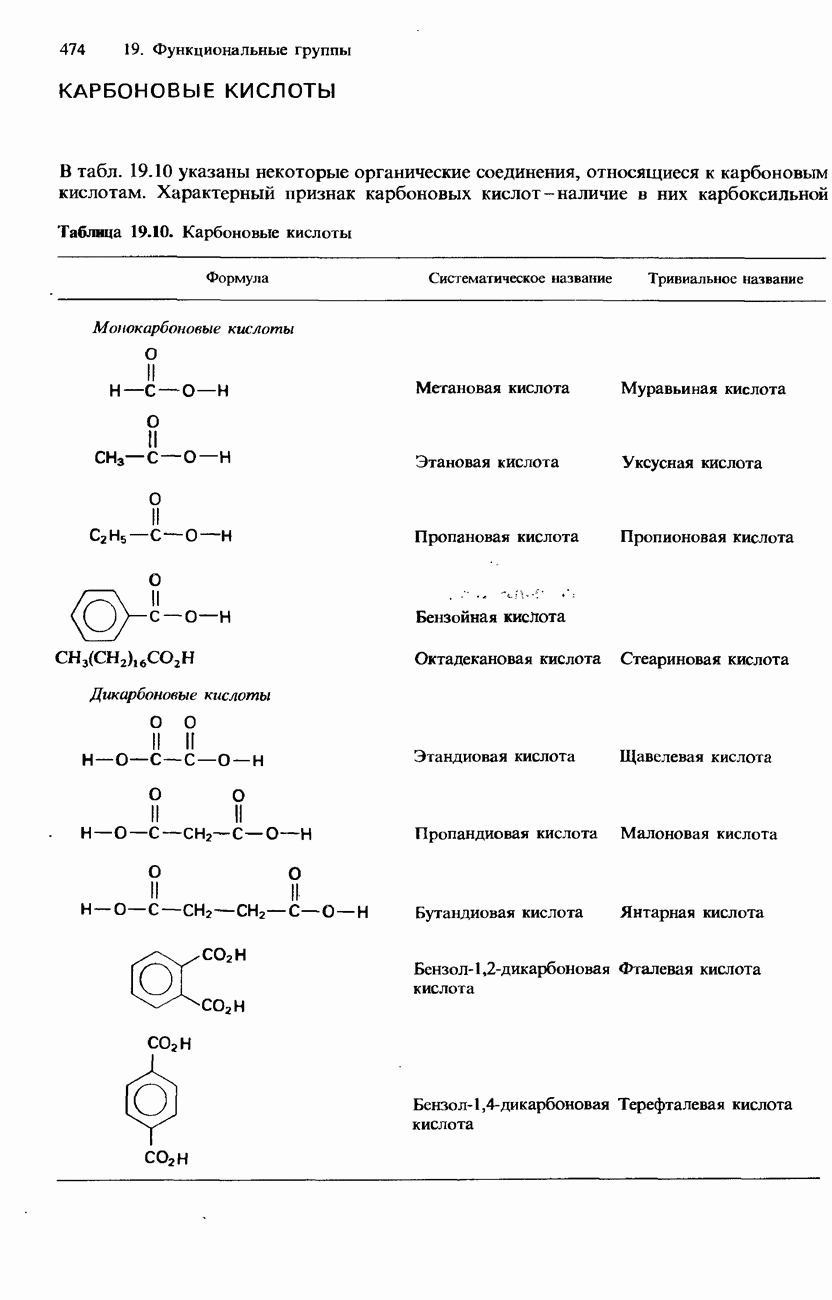
- КАРБОНОВЫЕ КИСЛОТЫ
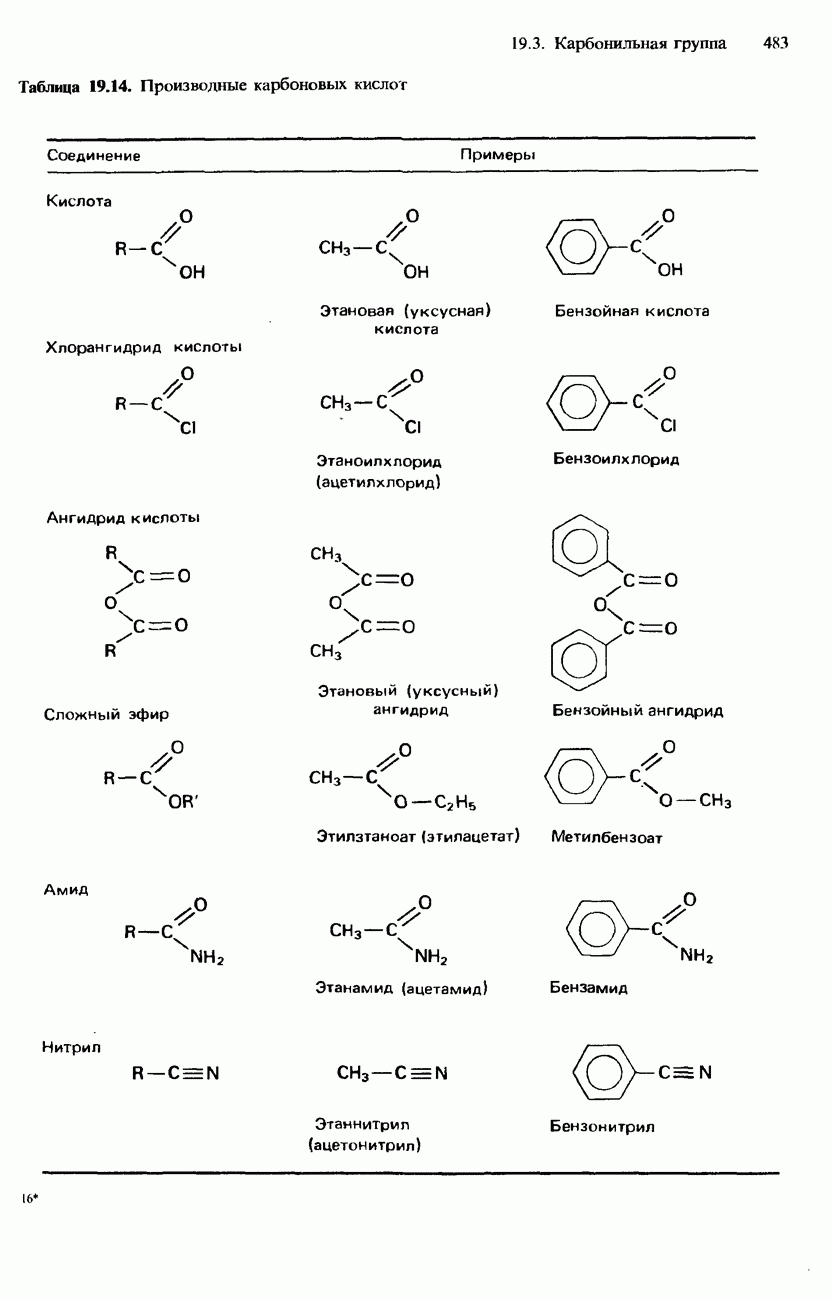
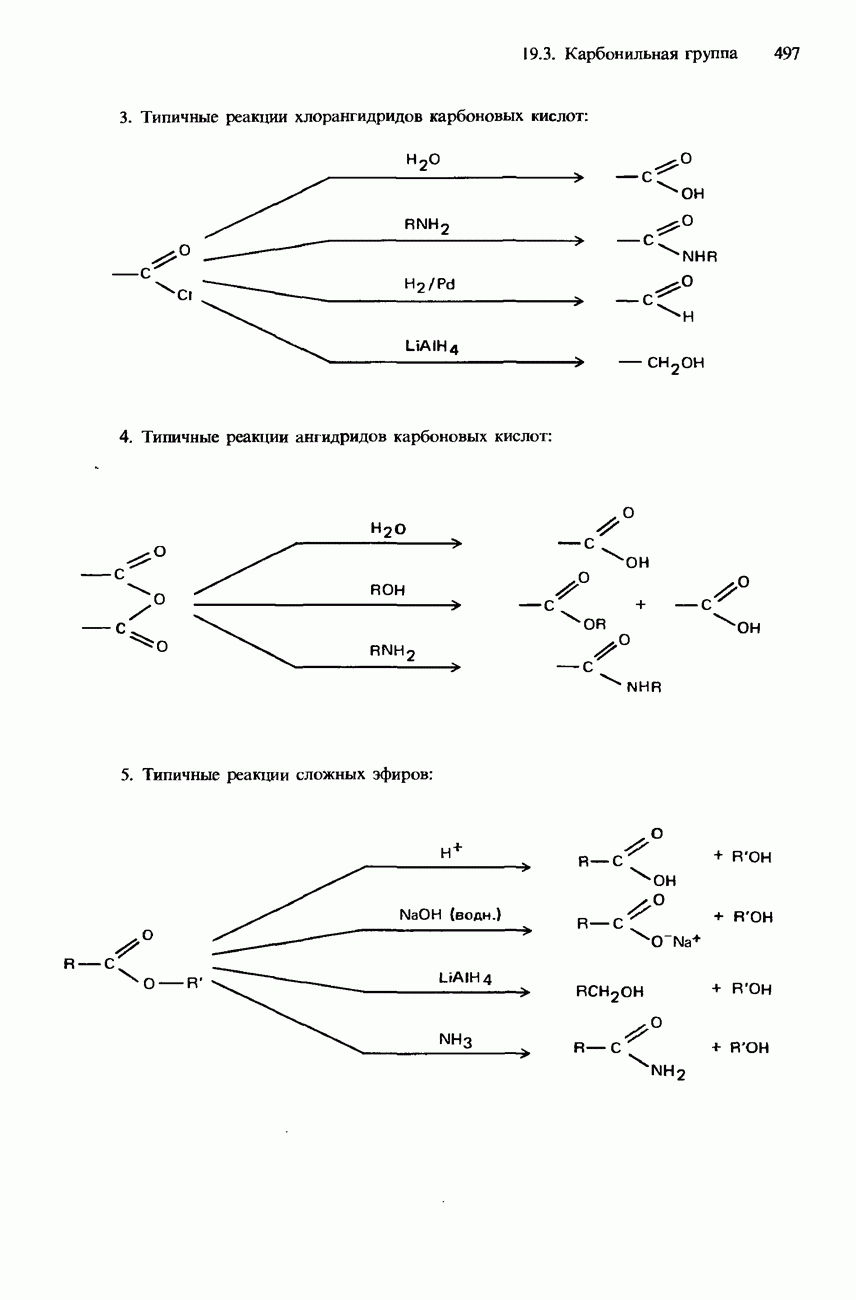
- ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
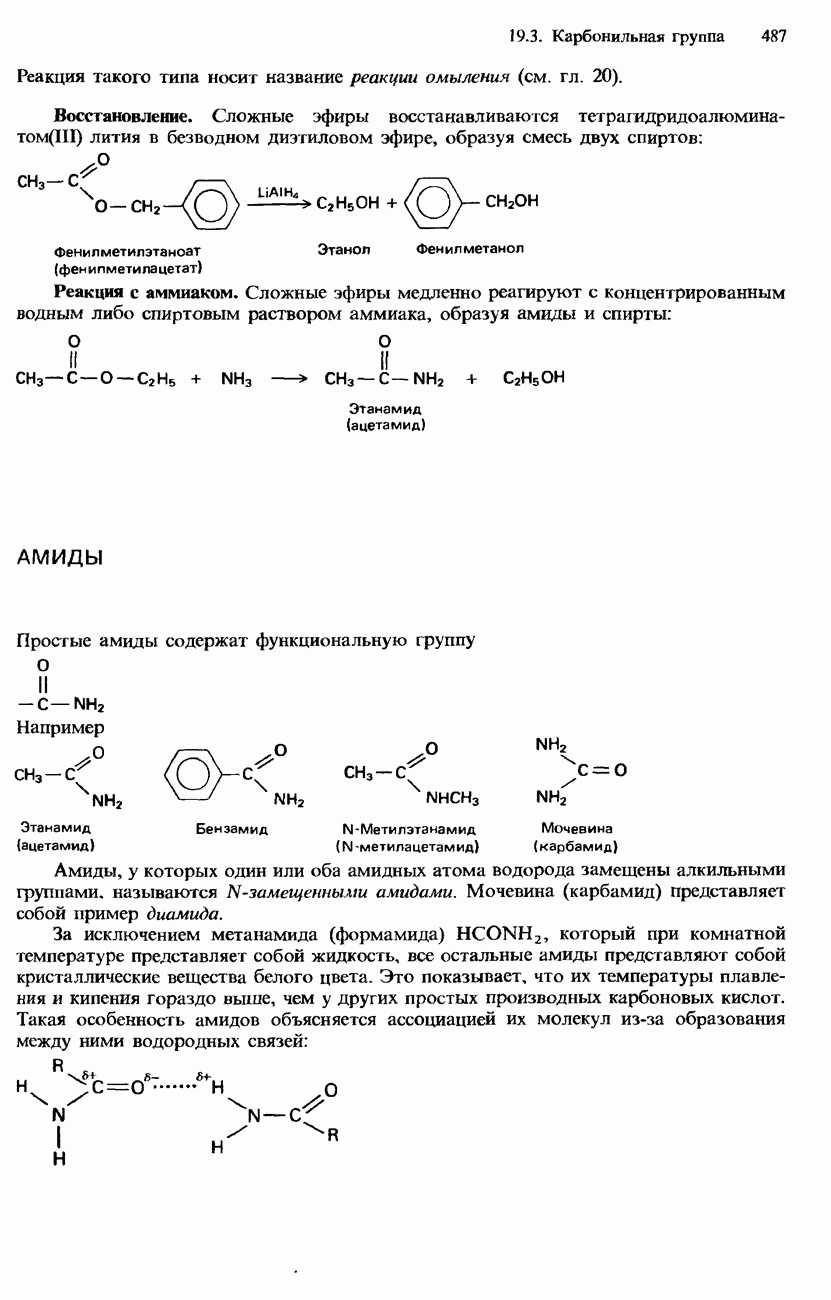
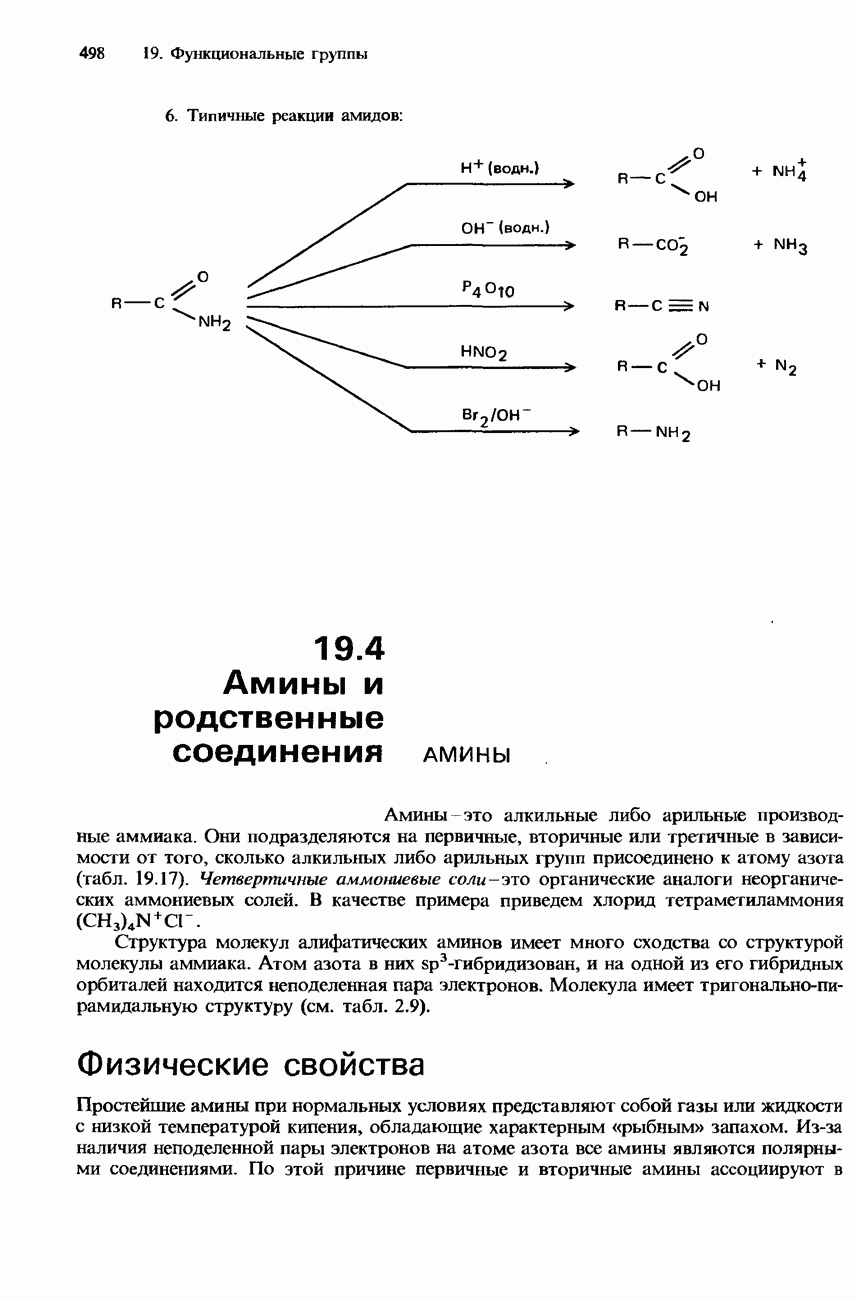
- АМИДЫ
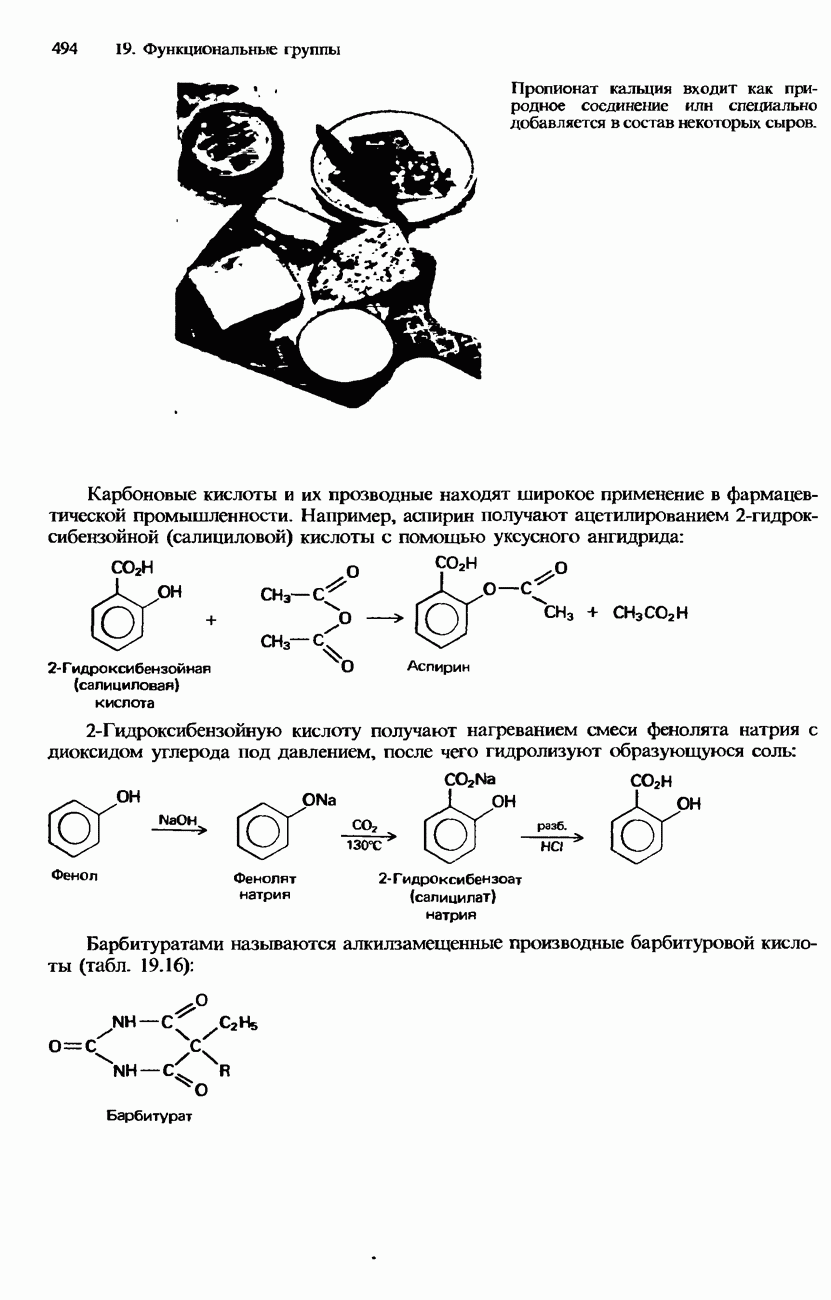
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ И ИХ ПРОИЗВОДНЫХ
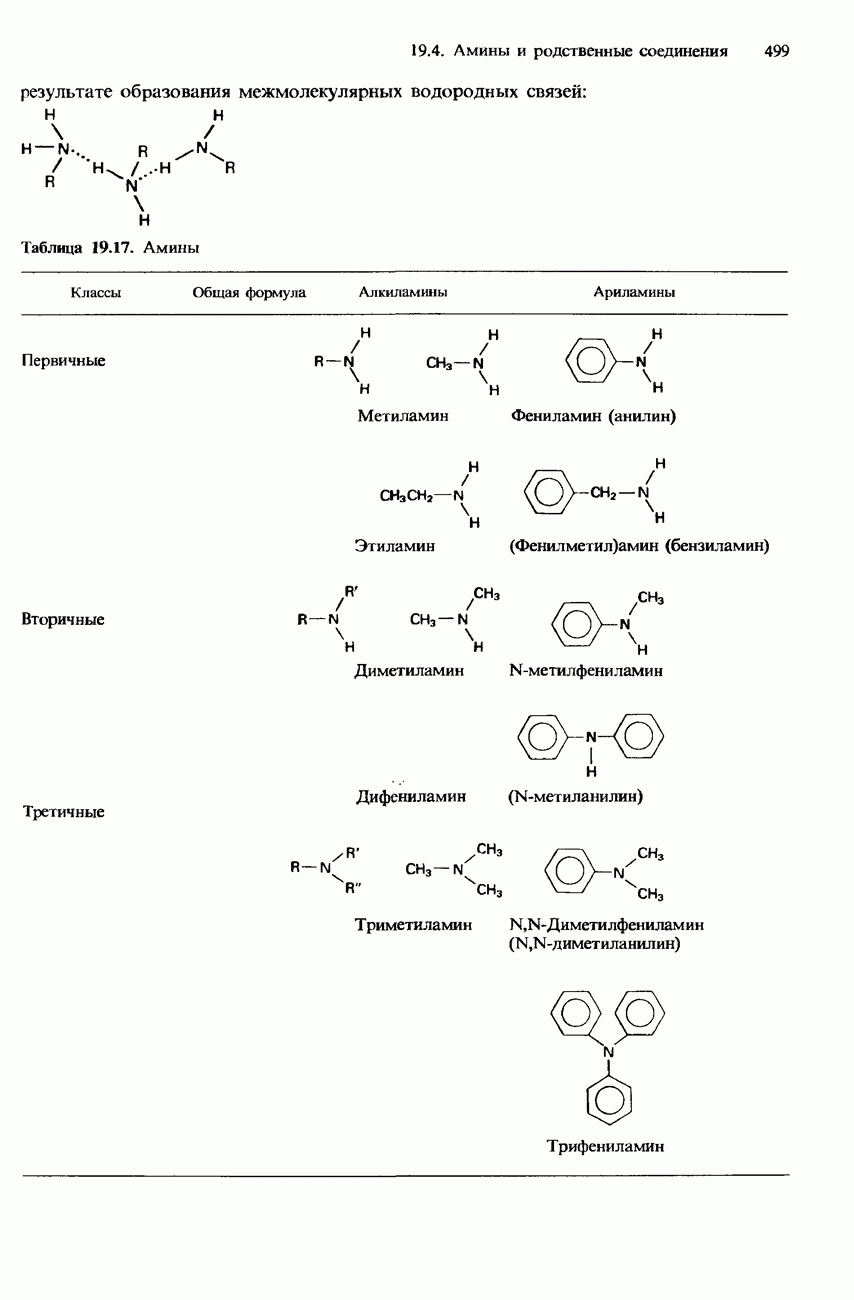
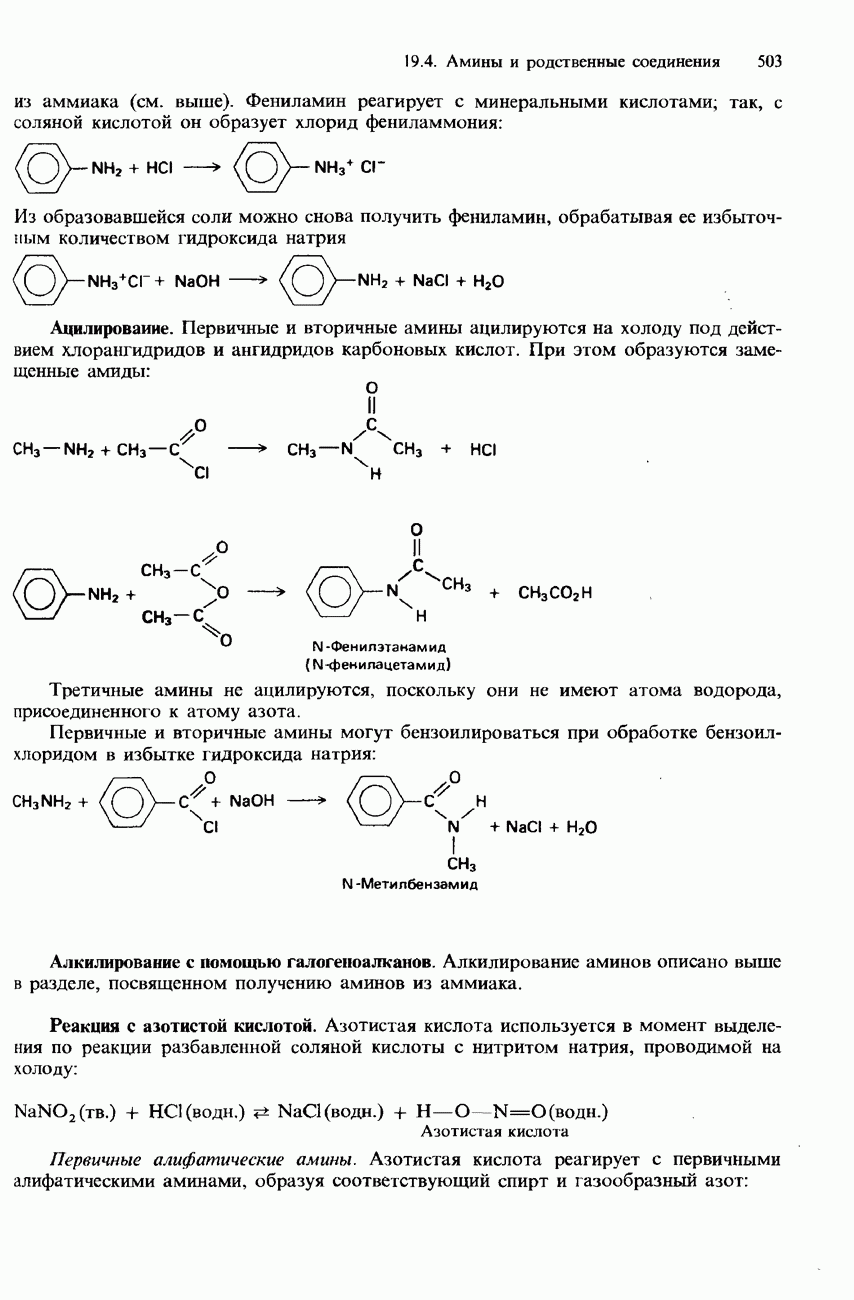
- 19.4 Амины и родственные соединения
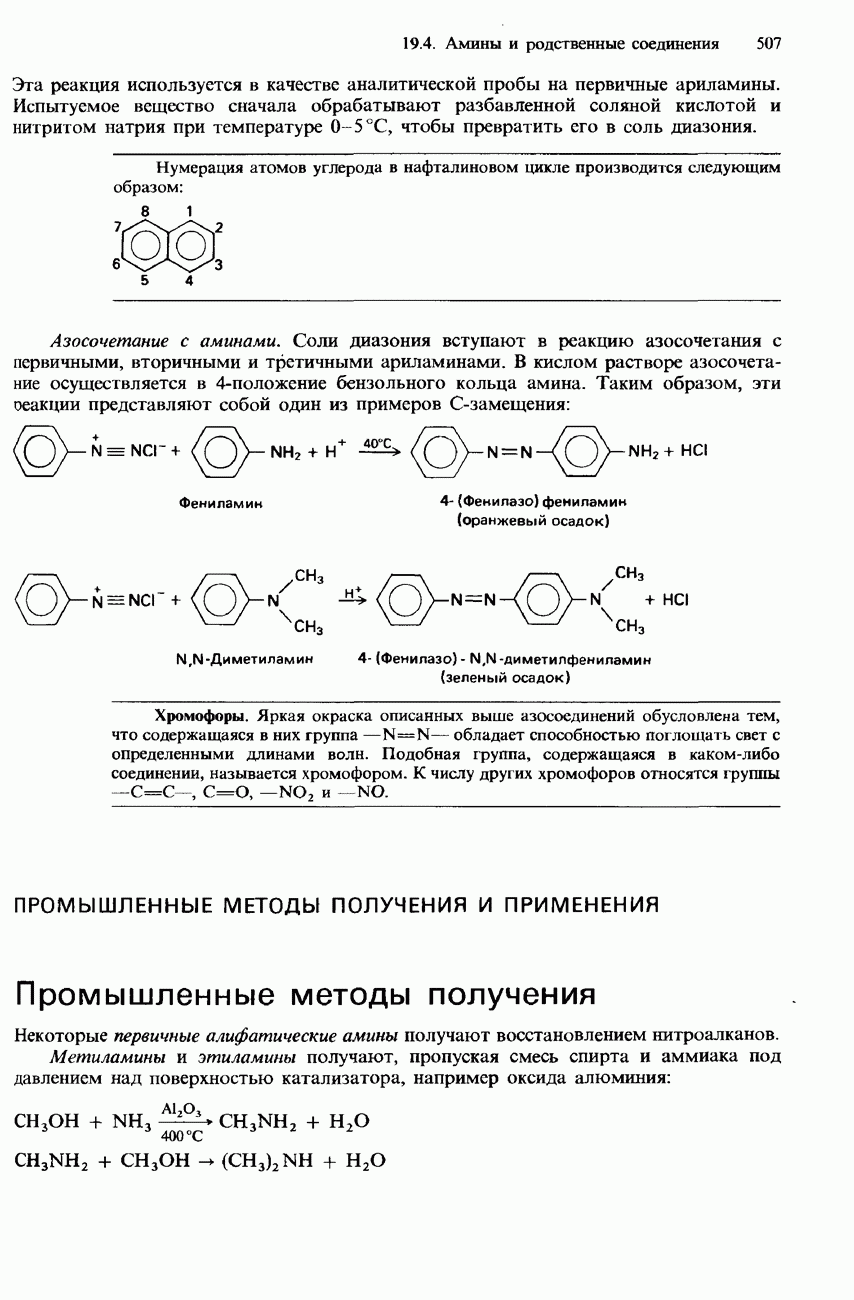
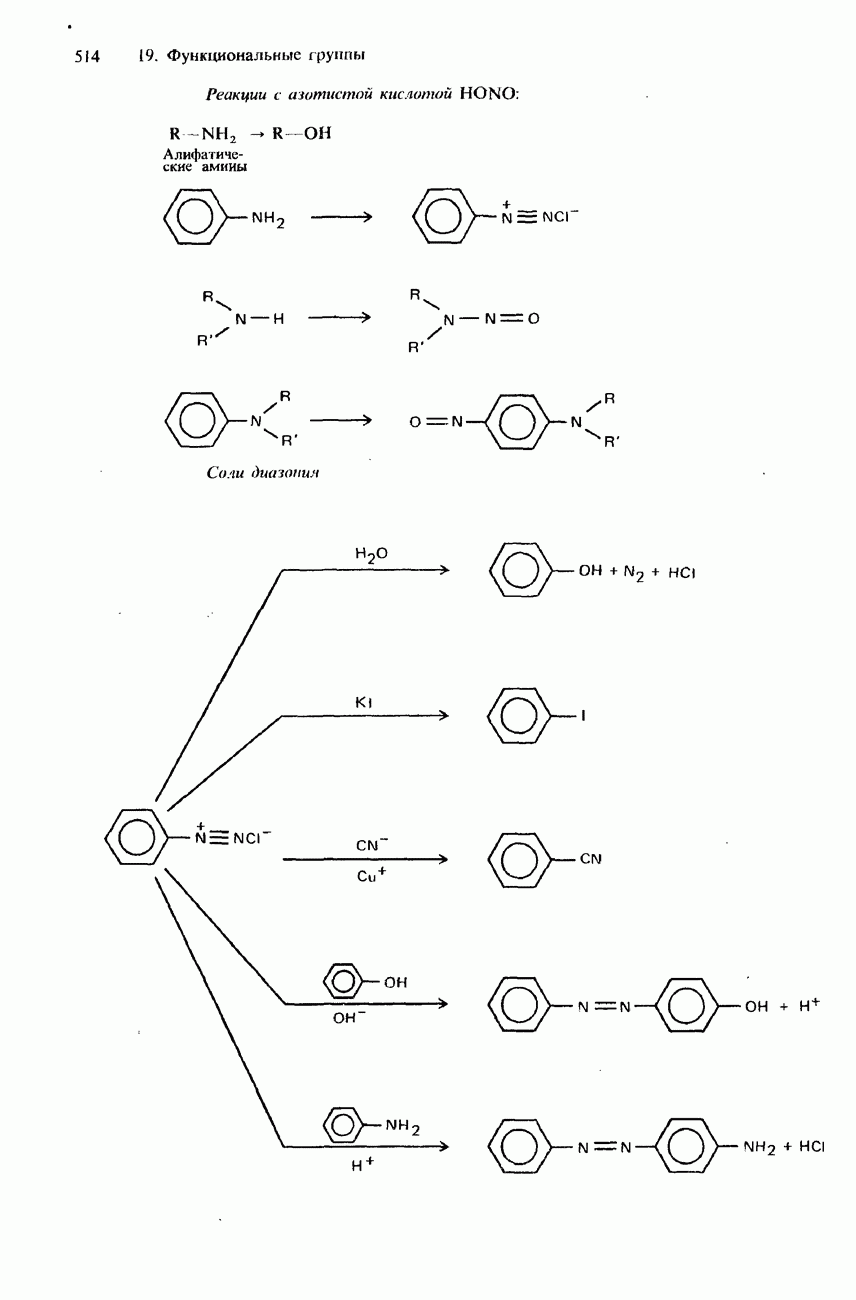
- СОЛИ ДИАЗОНИЯ
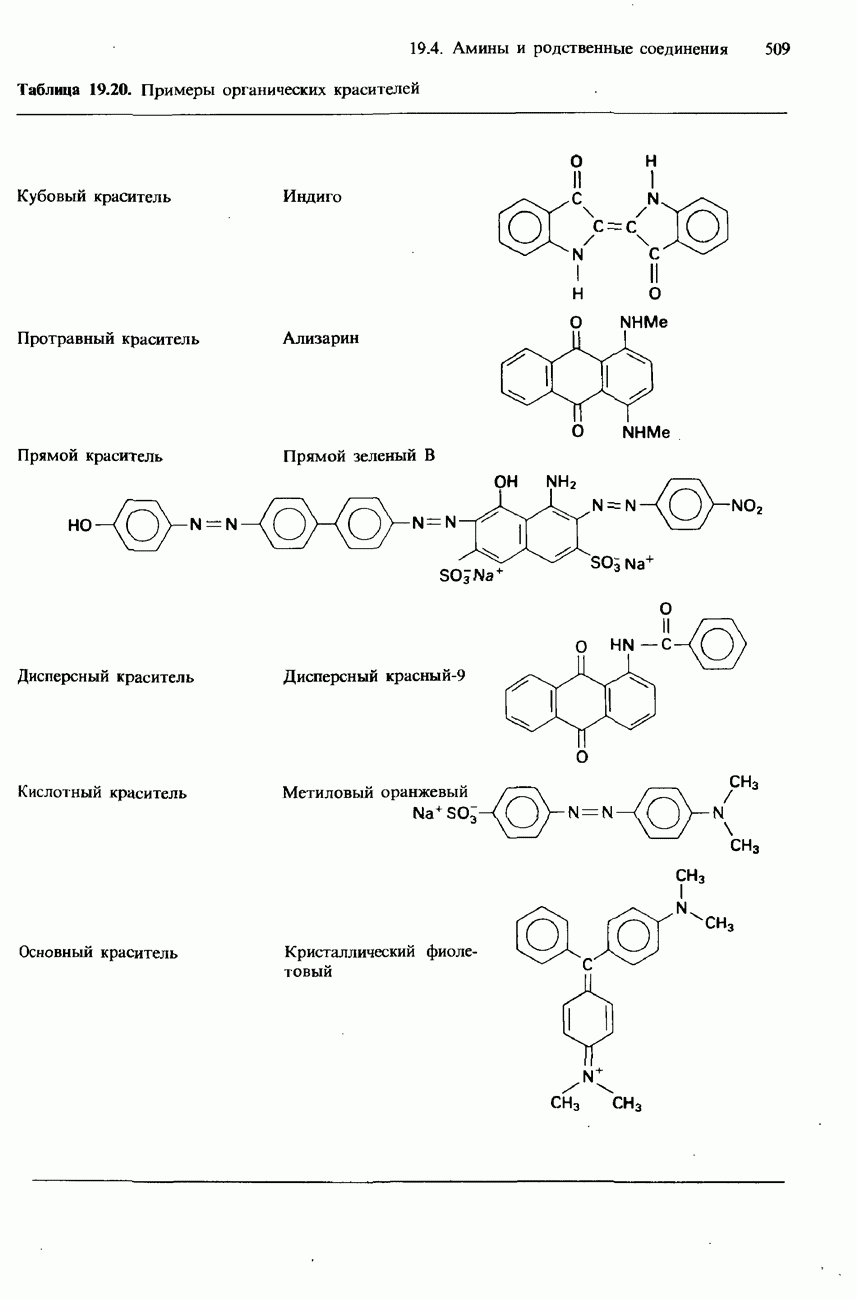
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 20. ПРИРОДНЫЕ СОЕДИНЕНИЯ И ПОЛИМЕРЫ
- 20.1. Аминокислоты, пептиды и белки
- АМИНОКИСЛОТЫ
- ПЕПТИДЫ
- БЕЛКИ
- 20.2. Углеводы и нуклеиновые кислоты
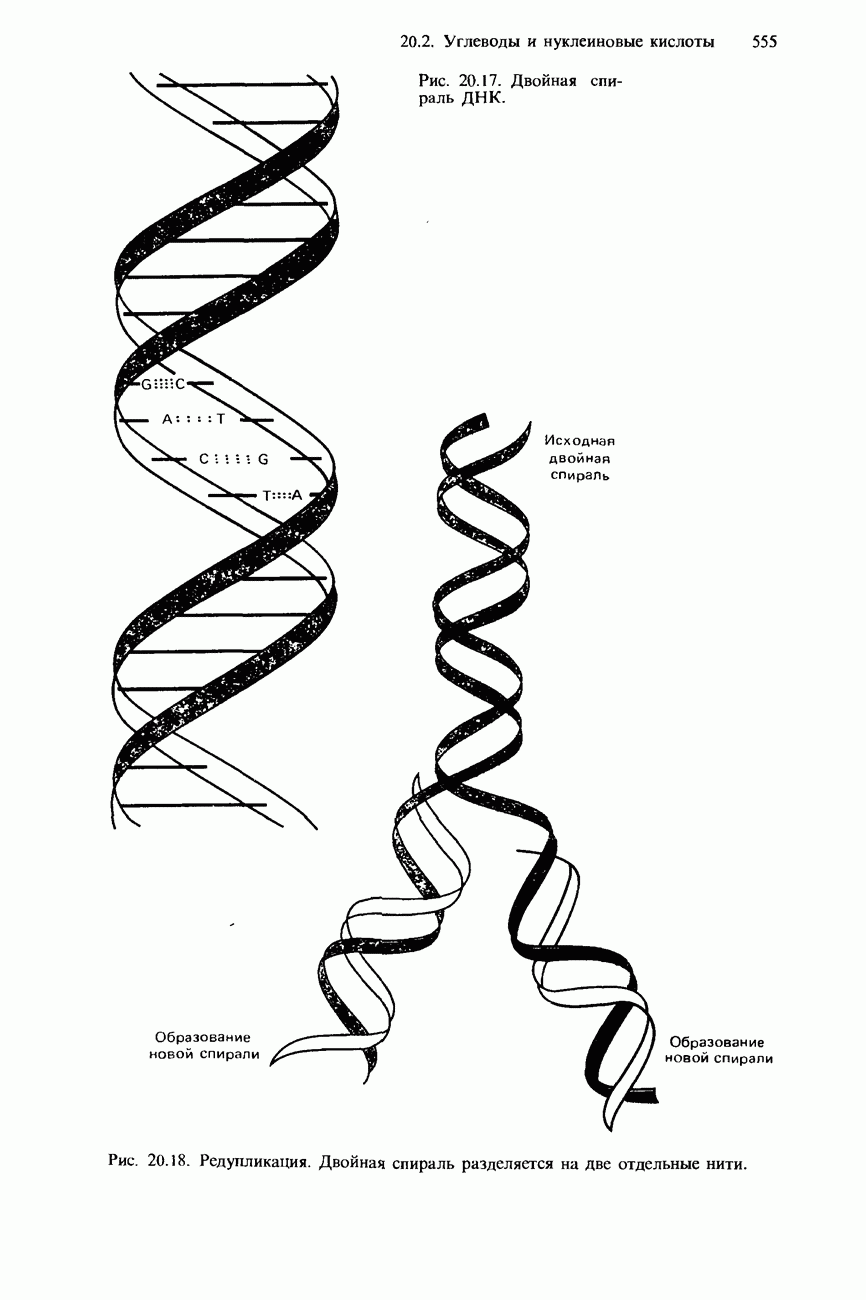
- НУКЛЕИНОВЫЕ КИСЛОТЫ
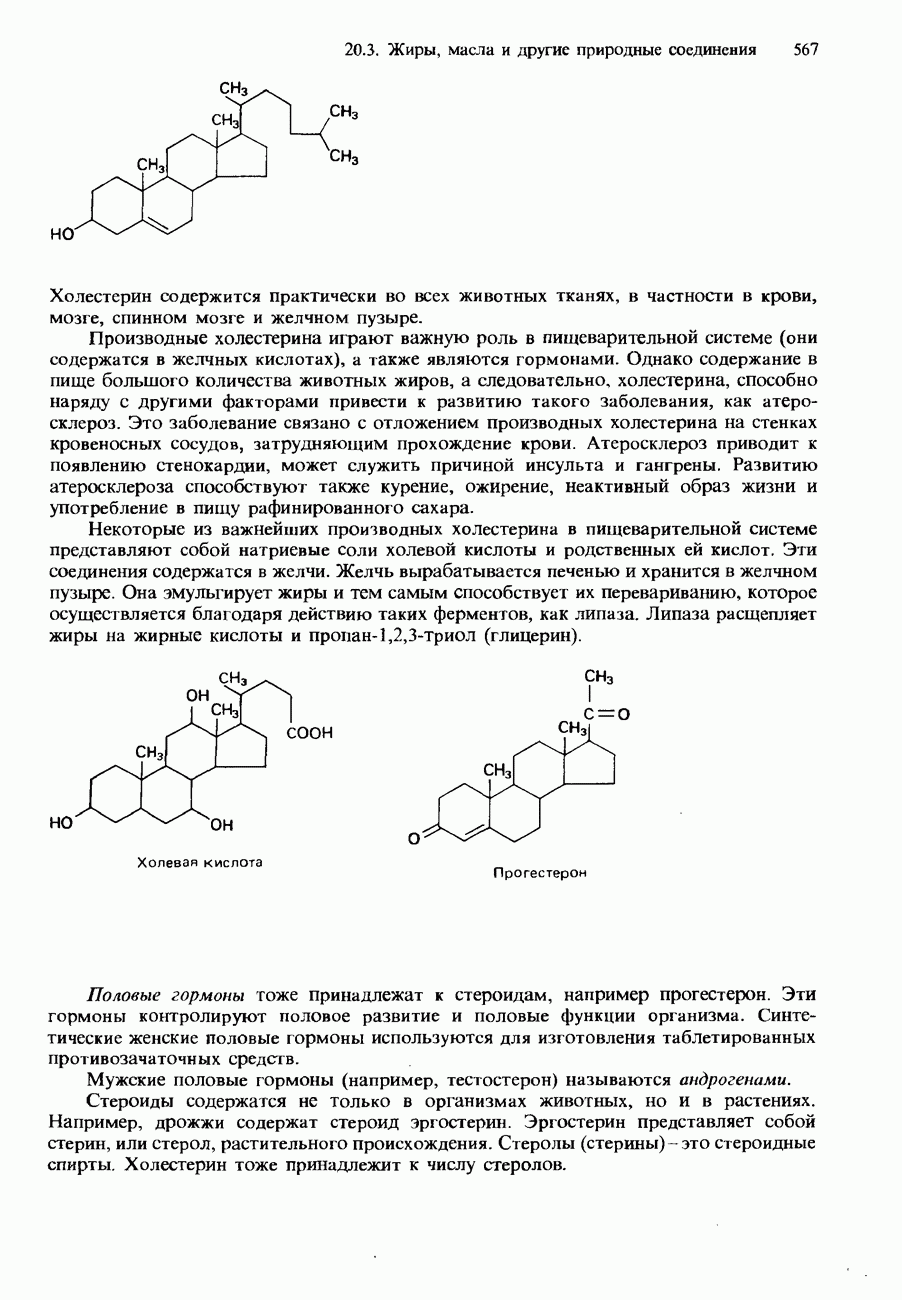
- 20.3. Жиры, масла и другие природные соединения
- ЖИРНЫЕ КИСЛОТЫ И ТРИГЛИЦЕРИДЫ
- ВОСКИ
- ФОСФОЛИПИДЫ И ГЛИКОЛИПИДЫ
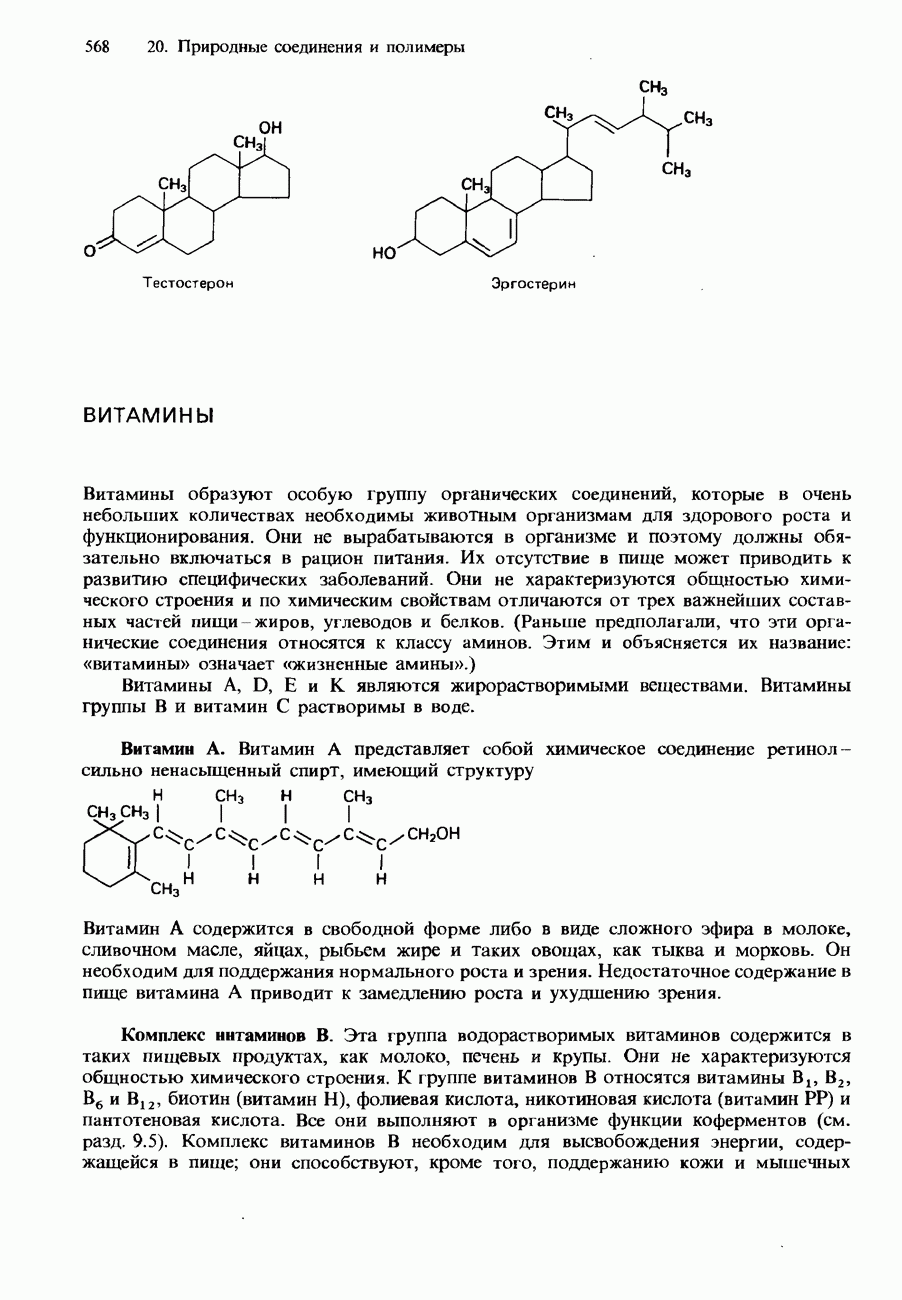
- ВИТАМИНЫ
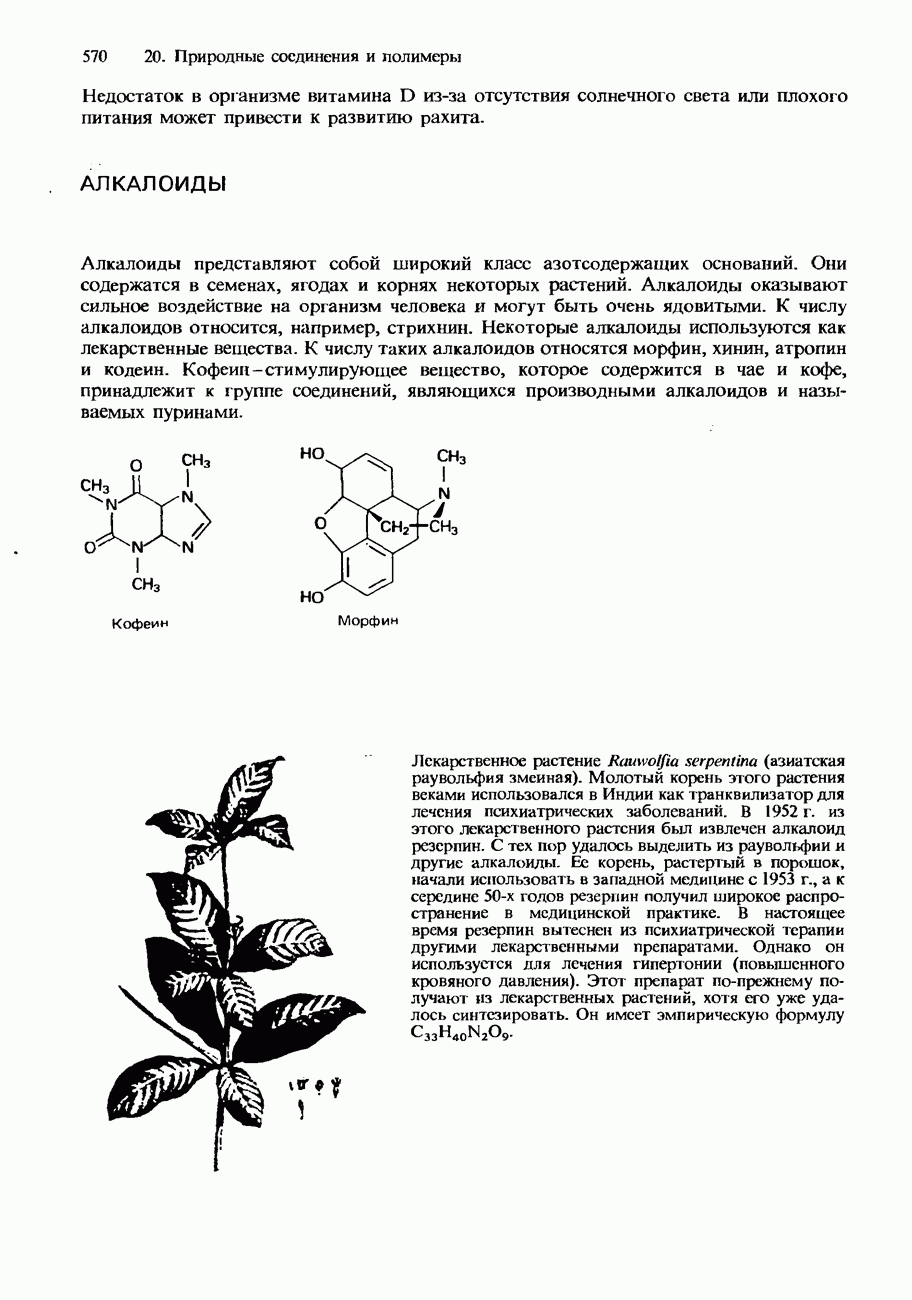
- АЛКАЛОИДЫ
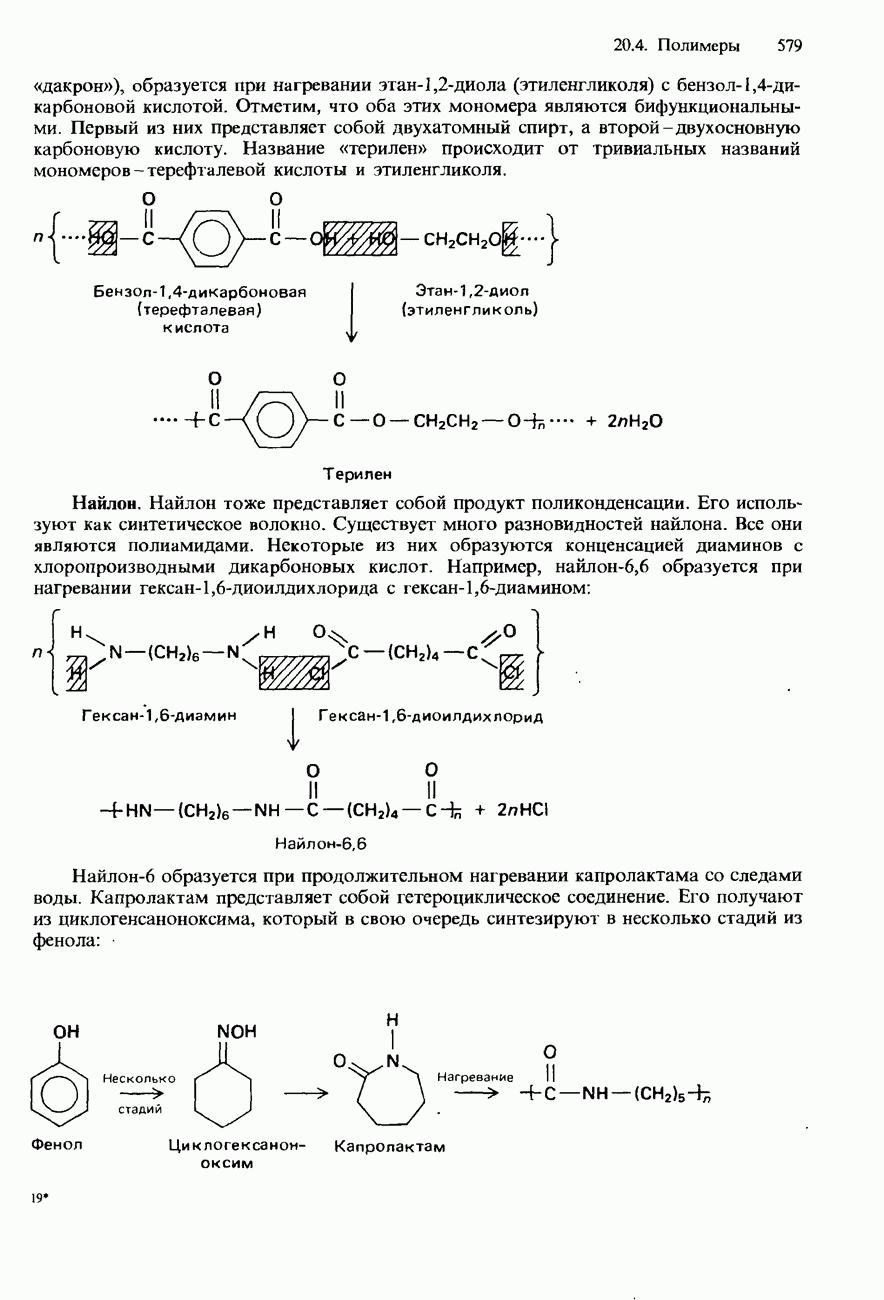
- 20.4. Полимеры
- ПОЛИМЕРИЗАЦИЯ
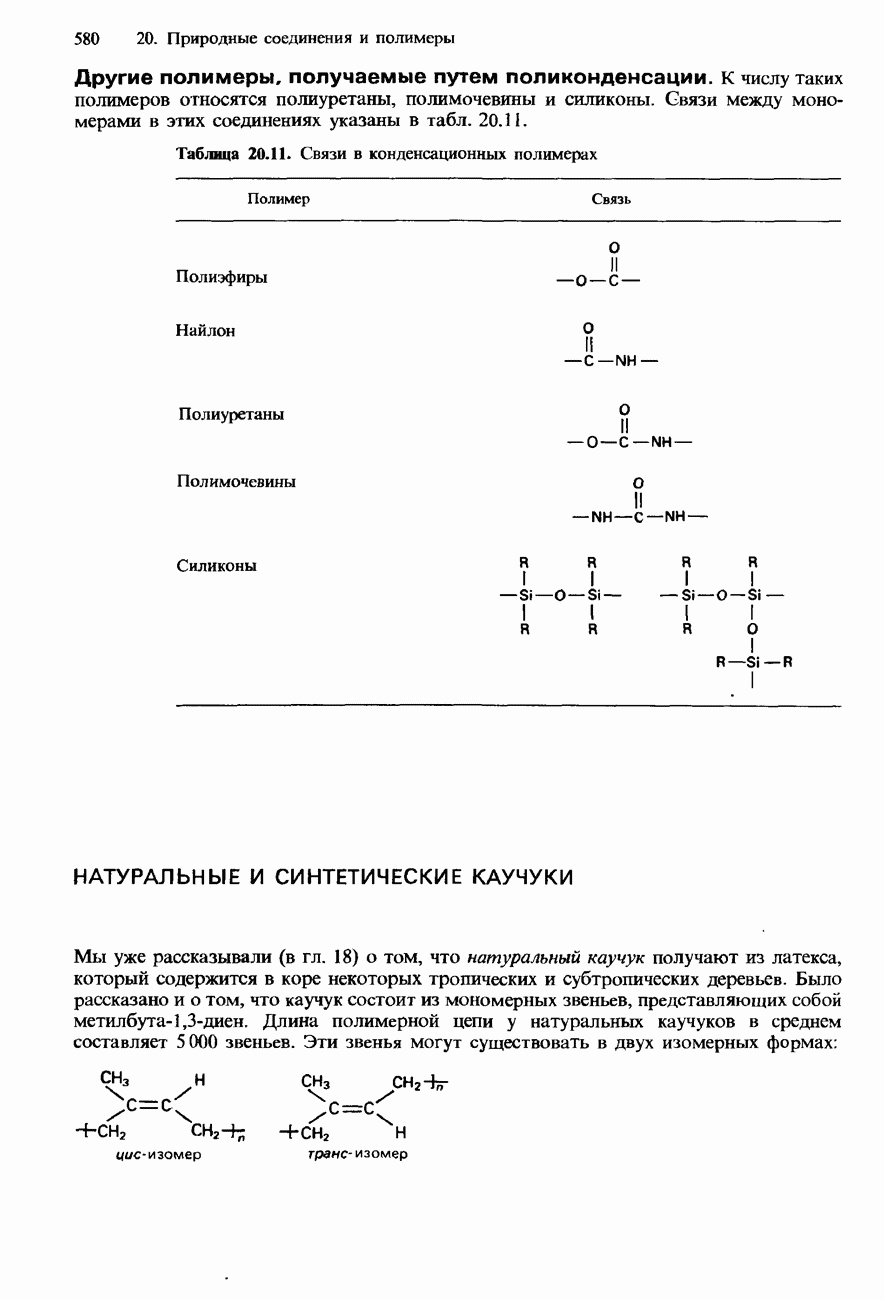
- НАТУРАЛЬНЫЕ И СИНТЕТИЧЕСКИЕ КАУЧУКИ
- ЦЕЛЛЮЛОЗНОЕ ВОЛОКНО
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- ПРИЛОЖЕНИЯ