| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ВОПРОСЫ ДЛЯ ПРОВЕРКИ
1. а) Кратко опишите химические свойства водорода и объясните, почему эти свойства делают водород в некоторых отношениях уникальным среди других элементов.
б) Обсудите свойства гидридов трех элементов, каждый из которых является типичным представителем  р- и d-элементов.
р- и d-элементов.
в) Как объяснить, что масс-спектр  полученного в результате реакции между
полученного в результате реакции между  содержит только один основной пик (с массовым числом 35), тогда как масс-спектр образца HDO, полученного взаимодействием
содержит только один основной пик (с массовым числом 35), тогда как масс-спектр образца HDO, полученного взаимодействием  содержит три основных пика (с массовыми числами 18, 19 и 20).
содержит три основных пика (с массовыми числами 18, 19 и 20).
2. а) Каким изменением энтальпии сопровождается образование 1 моля твердого гидрида натрия из входящих в него элементов в их стандартном состоянии?
б) Энтальпия образования твердого гидрида натрия равна  а гидрида кальция
а гидрида кальция  Чем объяснить столь большое различие между этими величинами?
Чем объяснить столь большое различие между этими величинами?
в) Образование хлороводорода из составляющих его элементов и последующее растворение  в воде демонстрируют два разных типа химической связи, в которых может принимать участие водород.
в воде демонстрируют два разных типа химической связи, в которых может принимать участие водород.
Опишите эти два типа связи и объясните следующие свойства хлороводорода и его водного раствора: 1) значение  и 2) электропроводность.
и 2) электропроводность.
г) Тетрагидридоалюминат(НГ) лития широко используется в органической химии.
1) Составьте полное уравнение реакции, используемой для получения этого соединения.
2) Нарисуйте структурную формулу этого соединения.
3) Запишите две реакции, в которых оно проявляет восстановительные свойства.
3. а) Энергия ионизации атомов водорода равна  а сродство к электрону атомов хлора равно
а сродство к электрону атомов хлора равно 
1) Запишите уравнения этих двух процессов, используя следующие дополнительные данные:

2) Вычислите стандартное изменение энтальпии для процесса

б) В приведенной ниже таблице указаны энтальпии гидратации некоторых ионов.

1) Используя результат, полученный при ответе на вопрос (а), определите энтальпию гидратации протона.
2) Сопоставьте это значение с приведенными выше для других ионов и кратко объясните, почему протон имеет такую энтальпию гидратации.
4. Этот вопрос касается гидридов различных элементов.
а) В каждом из следующих пунктов укажите название гидрида и составьте уравнение описываемой реакции.
1) Гидрид, который быстро и полностью гидролизуется в холодной воде.
2) Гидрид, который самопроизвольно возгорается на воздухе.
3) Гидрид, при электролизе которого в расплавленном состоянии на аноде выделяется водород.
4) Гидрид, водный раствор которого представляет собой двухосновную кислоту.
5) Гидрид, водный раствор которого представляет собой слабую щелочь.
б) Гидрид, который может быть лигандом для ионов переходных  -металлов.
-металлов.
б) Укажите названия двух гидридов, которые могут соединяться друг с другом по реакции присоединения, и запишите уравнение этой реакции.
в) Объясните, на чем основана способность углерода образовывать длинноцепочечные углеводороды.
г) Судя по энтальпии сгорания метана, эта реакция очень экзотермична. Чем же объяснить устойчивость метана на воздухе?
д) Как объяснить большое различие в температурах кипения метана и воды?
5. На приведенной ниже схеме указаны некоторые реакции водорода:

Пользуясь этой схемой, дайте ответы на следующие вопросы:
а) К какому типу принадлежит химическая реакция получения этана?
б) Назовите два продукта, которые обладают основными свойствами.
в) В какой из указанных выше реакций водород выступает в роли окислителя? Запишите пару ион - электронных уравнений для этой реакции.
г) Объясните, почему во фтороводороде имеются сильные водородные связи, а в водороде вообще отсутствует такой тип связи.
д) 1) Составьте полное уравнение образования метанола.
2) Исходя из предположения, что эта реакция протекает до полного завершения, вычислите, какую массу метанола можно получить из  водорода (объем газа указан при нормальных условиях).
водорода (объем газа указан при нормальных условиях).
е) Какую роль в образовании хлороводорода играет свет?
ж) Промышленное получение аммиака на некоторых заводах осуществляется под давлением, превышающим 200 атм. Укажите одно соображение в пользу дальнейшего повышения давления и одно соображение против него.
з) Схематически изобразите форму молекулы сероводорода.
и) Сгорание водорода представляет собой экзотермическую реакцию. Почему же для зажигания водорода надо затратить энергию?
6. а) Опишите один из методов промышленного получения водорода, указав при этом, как производится его отделение от других продуктов проводимой для этого реакции.
б) Как можно получить в лабораторных условиях и собрать образец водорода, из которого удалены главные примеси? (Обратите внимание на то обстоятельство, что концентрированная серная кислота не пригодна для осушения чистого водорода, так как она обладает способностью образовывать  в этом случае необходимо пользоваться каким-либо другим осушителем.)
в этом случае необходимо пользоваться каким-либо другим осушителем.)
в) Опишите, какую структуру и какой тип химической связи имеют гидриды следующих элементов: 1) натрия, 2) азота (один гидрид по вашему выбору),
3) иода. Какие реакции происходят между этими гидридами и водой?
7. а) Опишите, каковы структура и тип химической связи в молекуле воды.
б) Опишите, что должно наблюдаться при опускании безводного сульфата  в достаточно большой объем воды. Объясните результаты этих наблюдений с учетом особенностей строения и типа химической связи для тех частиц, содержащих медь, которые присутствуют в полученном растворе.
в достаточно большой объем воды. Объясните результаты этих наблюдений с учетом особенностей строения и типа химической связи для тех частиц, содержащих медь, которые присутствуют в полученном растворе.
в) Опишите, какие реакции ионов каждого из названных ниже металлов в растворах сульфатов  произойдут с избыточным количеством следующих веществ: 1) водного раствора гидроксида калия и 2) водного раствора аммиака.
произойдут с избыточным количеством следующих веществ: 1) водного раствора гидроксида калия и 2) водного раствора аммиака.
8. а) Объясните значение термина гидролиз.
б) После полного гидролиза хлорида  весь хлор в этом соединении оказывается прореагировавшим. Запишите уравнение гидролиза хлорида алюминия.
весь хлор в этом соединении оказывается прореагировавшим. Запишите уравнение гидролиза хлорида алюминия.
в) После полного гидролиза хлорида  лишь половина всего хлора, содержащегося в этом соединении, оказывается прореагировавшей. Запишите уравнение гидролиза хлорида магния.
лишь половина всего хлора, содержащегося в этом соединении, оказывается прореагировавшей. Запишите уравнение гидролиза хлорида магния.
г) Натрий, магний и алюминий имеют атомные номера II, 12 и 13 соответственно. Эти элементы принадлежат к одному периоду периодической таблицы. Хлорид натрия вообще не подвержен гидролизу.
1) Что представляет собой атомный номер элемента?
2) Почему указанные элементы принадлежат к одному периоду периодической таблицы?
3) Почему три указанных хлорида отличаются друг от друга по степени гидролиза?
д) Углерод и кремний принадлежат к одной группе периодической таблицы; кремний имеет больший атомный номер. Тетрахлорометан (тетрахлорид углерода) не подвержен гидролизу, а тетрахлорид кремния гидролизуется полностью.
1) Объясните, почему эти два элемента принадлежат к одной группе периодической таблицы.
2) Как объяснить различия в степени гидролиза двух указанных хлоридов?
е) Расплавленное бинарное соединение А подвергнуто электролизу при определенных условиях. На катоде образовался пар, который удалось сконденсировать в твердое вещество серого цвета; на свежем разрезе это вещество имеет блестящую поверхность, которая быстро тускнеет во влажном воздухе. На аноде выделился газ, который при сгорании в атмосфере хлора образует «влажный» дым.
1) Запишите название продукта, выделяющегося на катоде.
2) Запишите название продукта, выделяющегося на аноде.
3) Запишите ионную формулу бинарного соединения А.
4) Для выделения двух указанных продуктов в данном эксперименте необходимо соблюдать два практических условия. Укажите их.
ж) Если соединение А, обсуждаемое в п. (е), опустить в воду, то произойдет выделение такого же газа, что и на аноде при описанном выше электролизе, а образующийся после завершения реакции раствор при добавлении в него фенолфталеина приобретает розовую окраску.
1) Запишите уравнение реакции гидролиза вещества А.
2) С учетом реакции, упомянутой в п. (1), укажите, в роли какого химического агента может использоваться вещество А.
3) Укажите простой практический метод получения вещества А.
9. При определенных химических условиях вода может выступать в роли а) брен-стедовской кислоты, б) бренстедовского основания, в) лиганда, г) нуклеофила, д) окислителя.
Укажите по два вещества из приведенного ниже перечня, которые иллюстрируют каждую из указанных способностей воды:  Там, где необходимо, запишите уравнение реакции, название продуктов и кратко перечислите физические условия, при которых осуществляется реакция.
Там, где необходимо, запишите уравнение реакции, название продуктов и кратко перечислите физические условия, при которых осуществляется реакция.
| << Предыдущий параграф | Следующий параграф >> |
- 11. ПЕРИОДИЧЕСКИЙ ЗАКОН
- 11.1 Периодичность
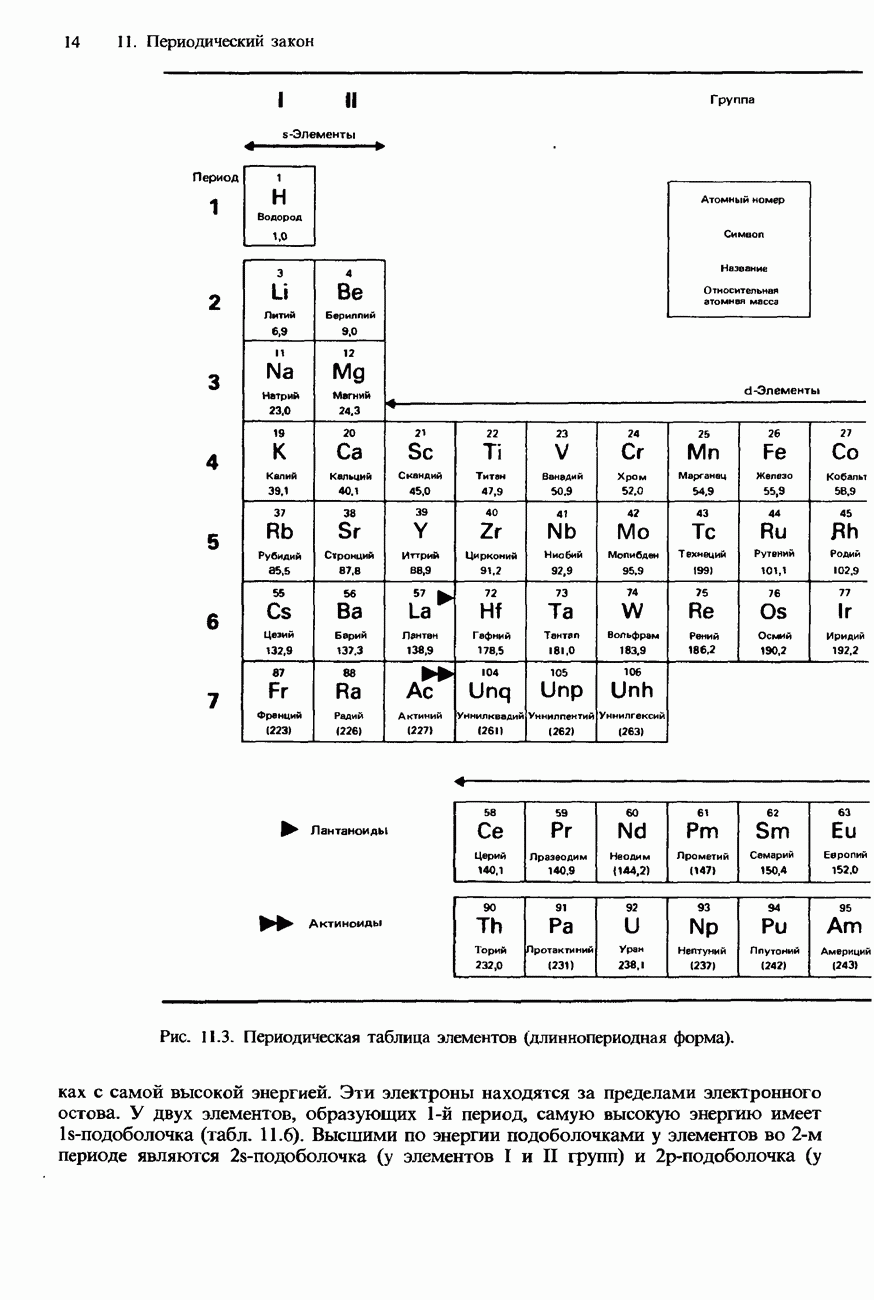
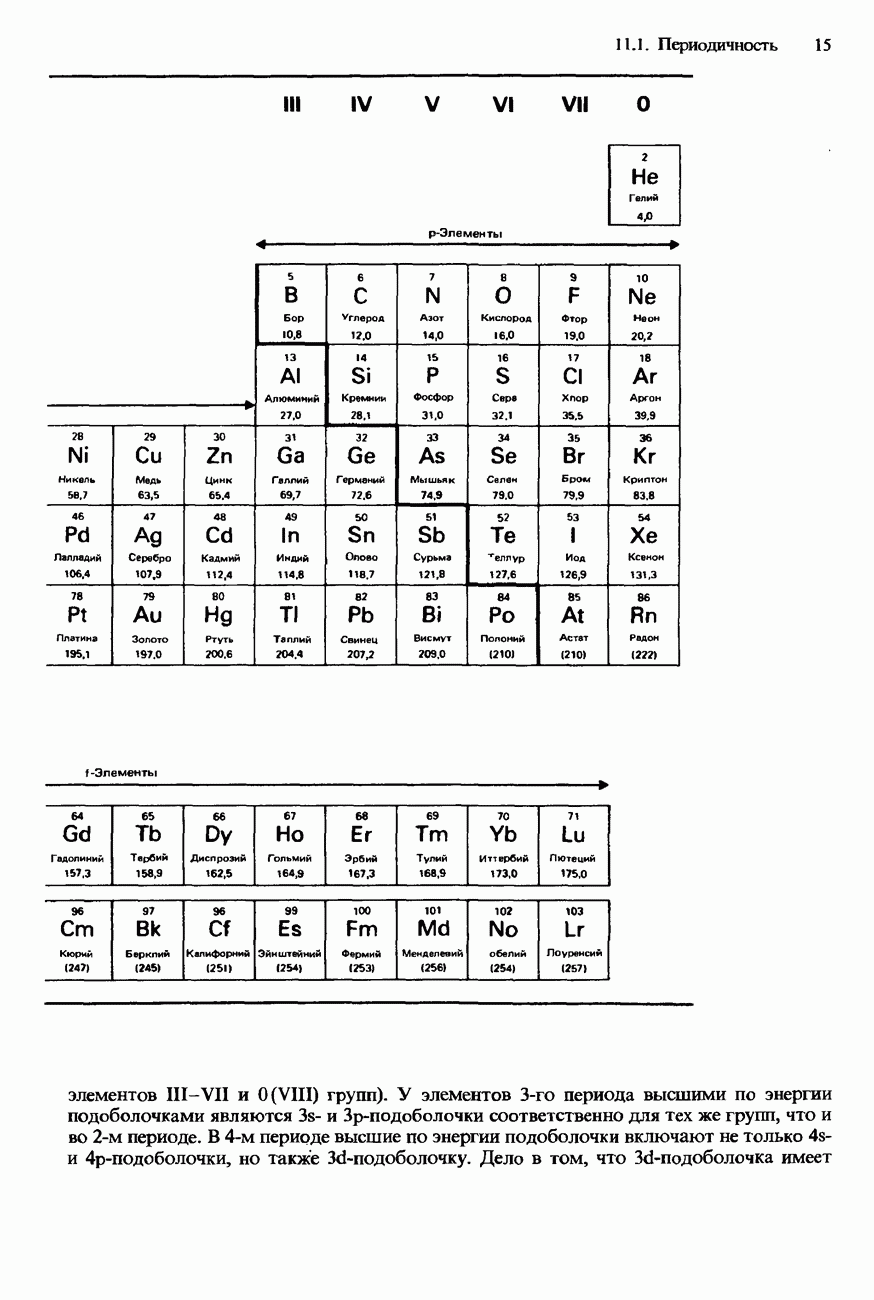
- СОВРЕМЕННАЯ ФОРМА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ
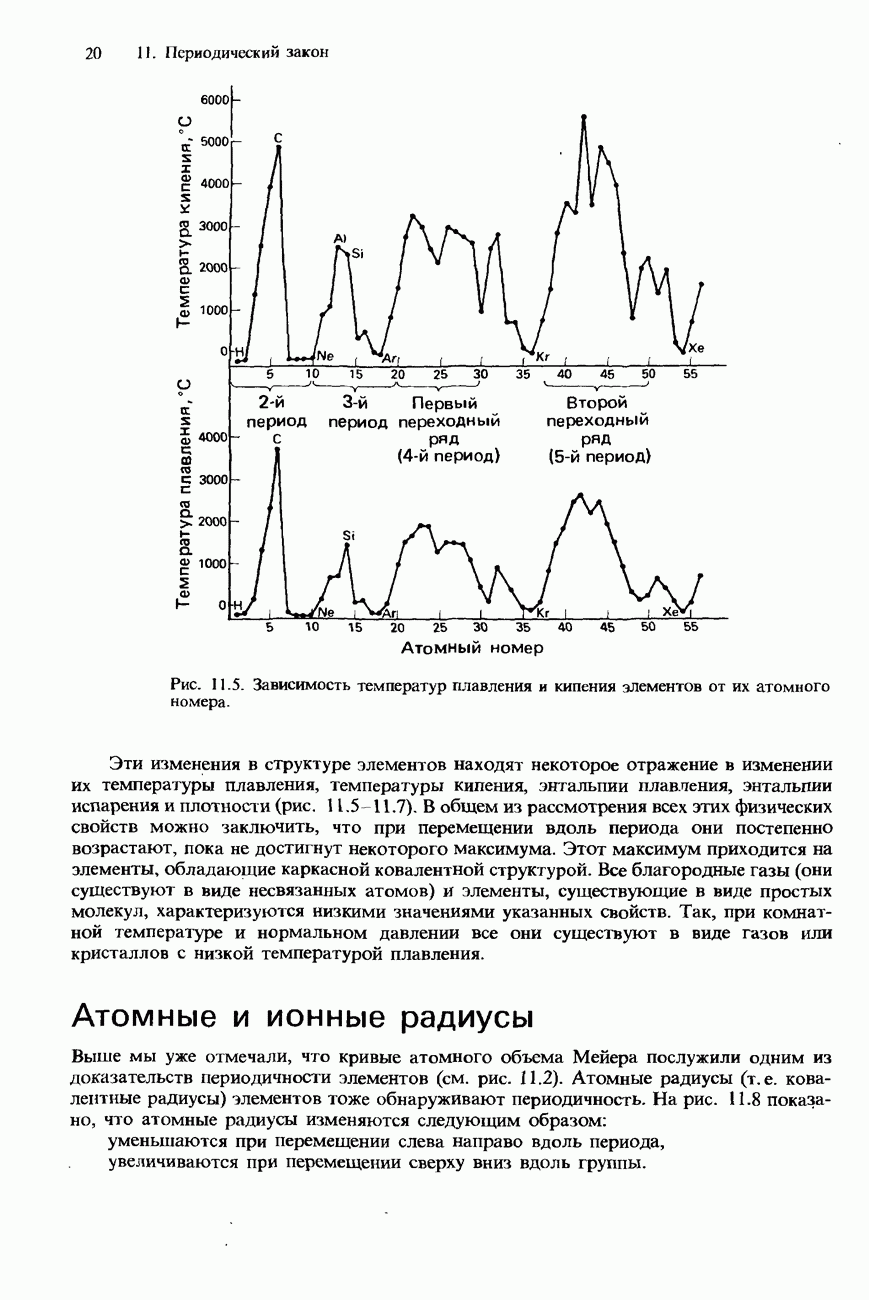
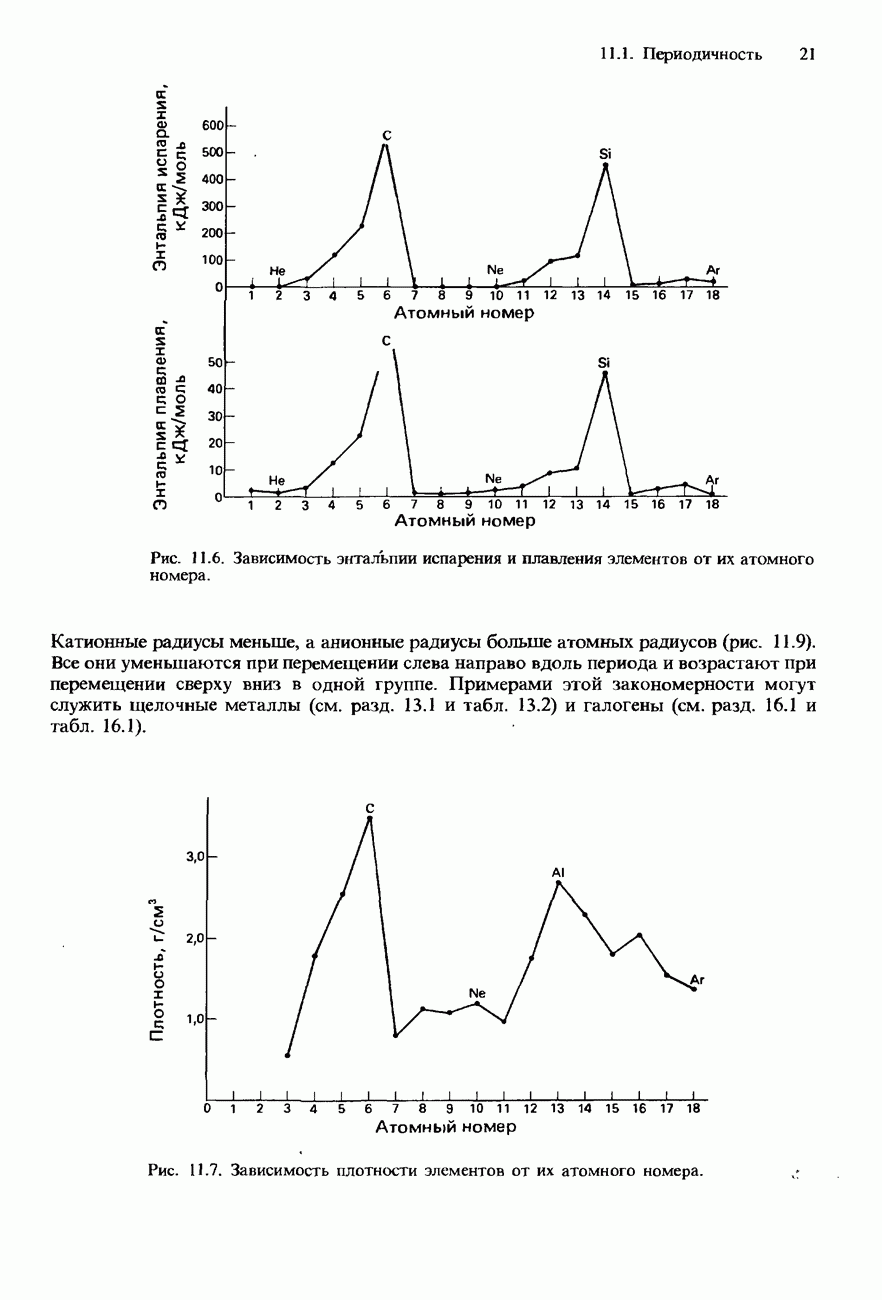
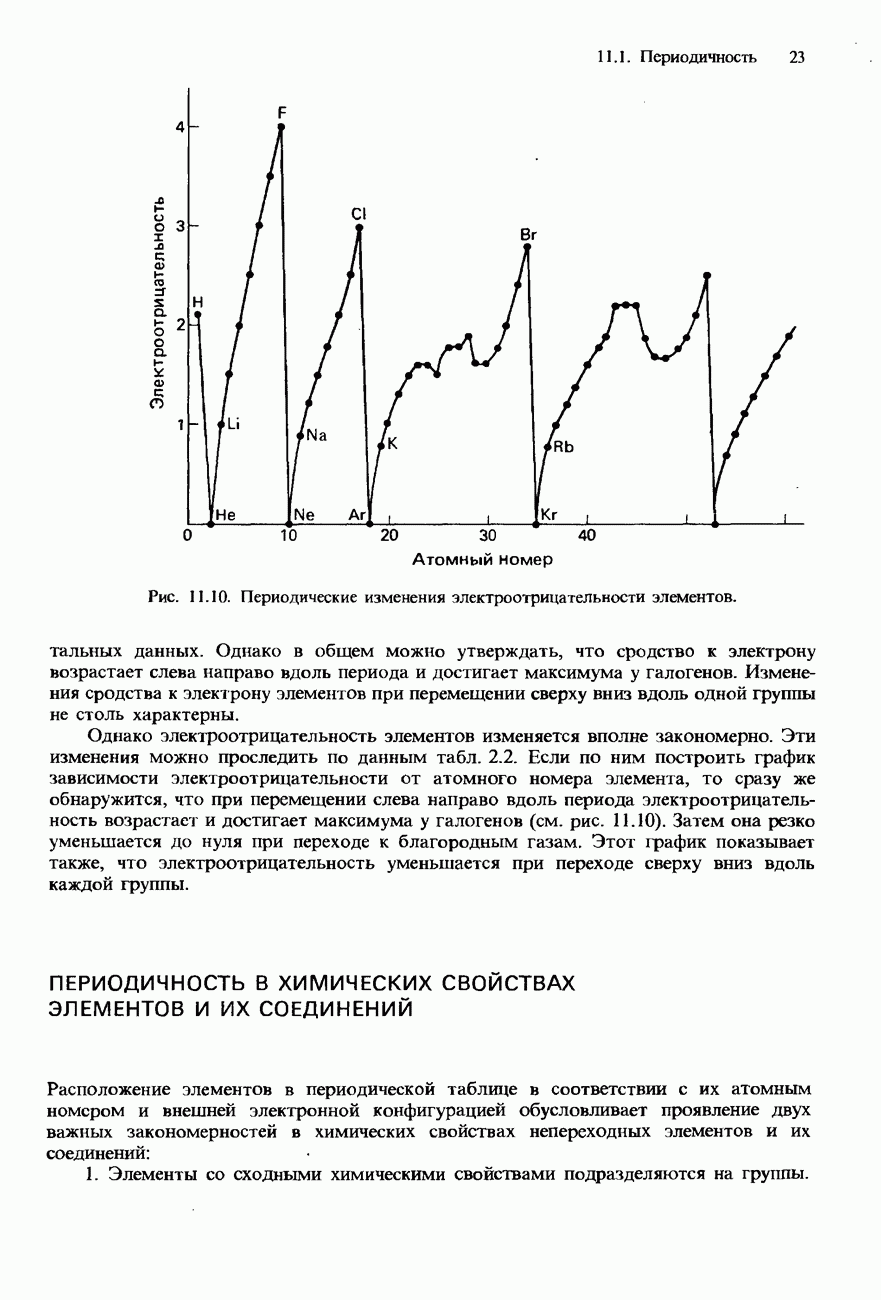
- ПЕРИОДИЧНОСТЬ
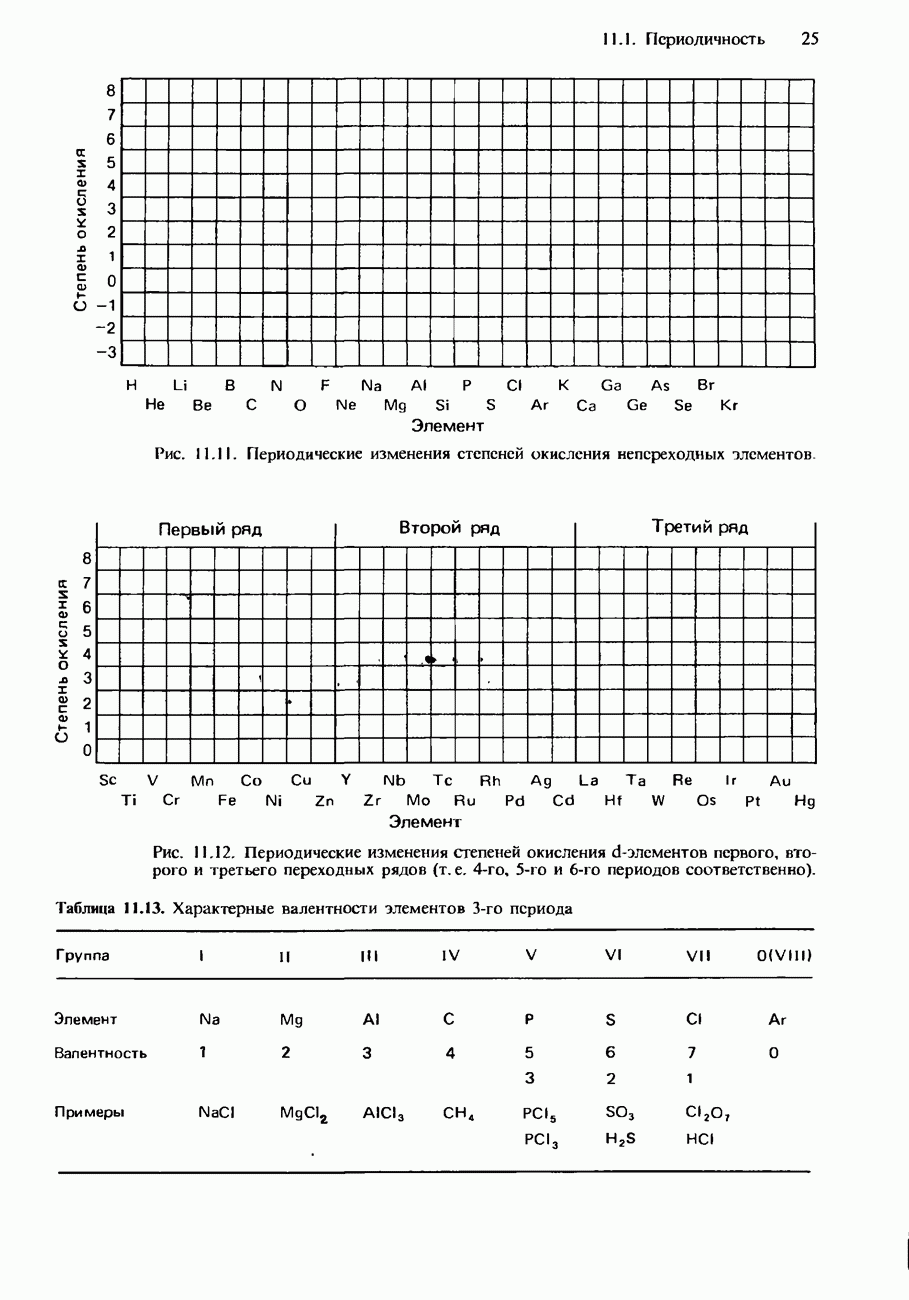
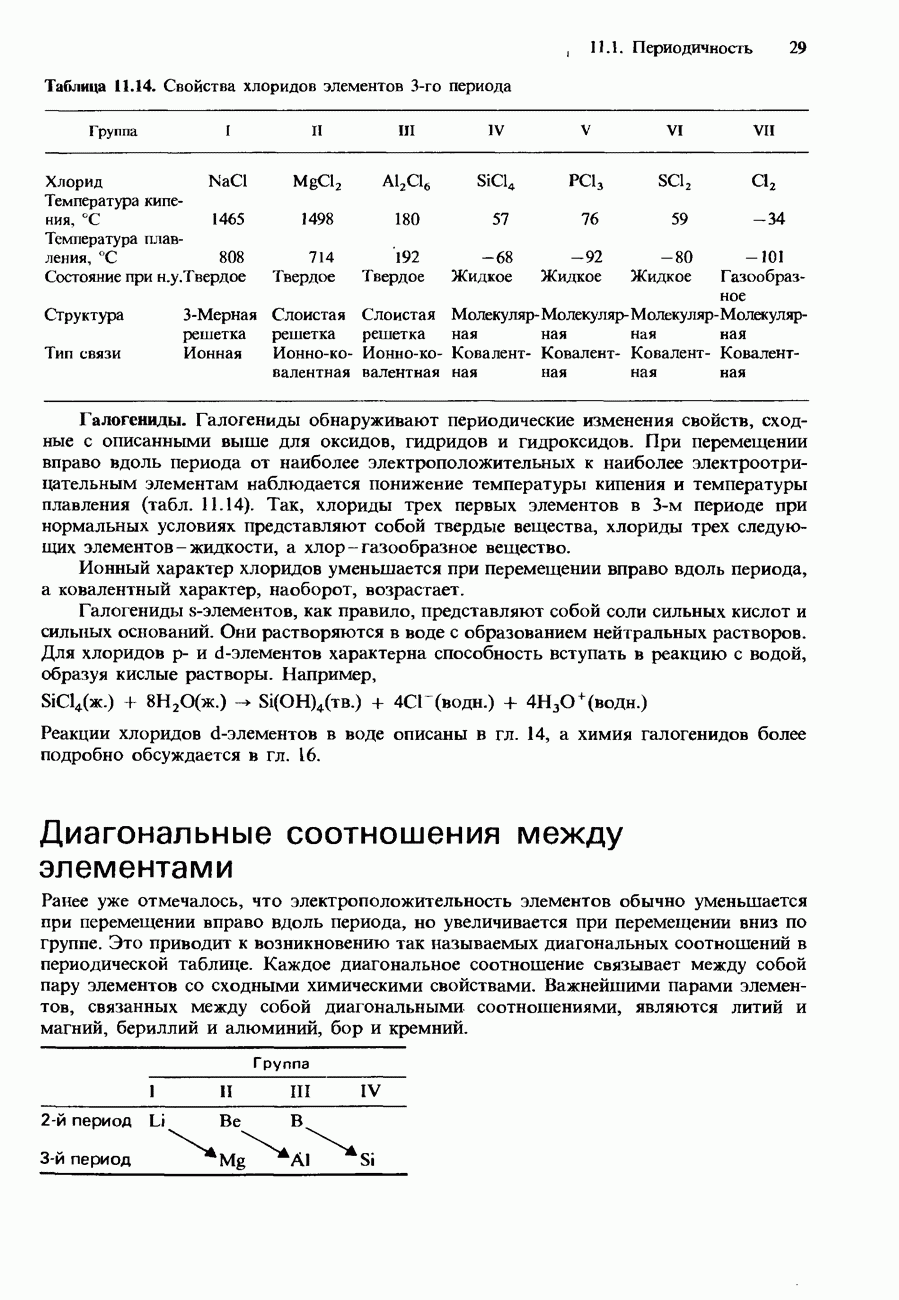
- ПЕРИОДИЧНОСТЬ В ХИМИЧЕСКИХ СВОЙСТВАХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 12. ВОДОРОД И ВОДА
- 12.1. ВОДОРОД
- ПОЛУЧЕНИЕ ВОДОРОДА В ЛАБОРАТОРНЫХ УСЛОВИЯХ
- РАЗЛИЧНЫЕ ФОРМЫ ВОДОРОДА
- ФИЗИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ХИМИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ТИПЫ СОЕДИНЕНИЙ ВОДОРОДА
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПОЛУЧЕНИЕ И ИСПОЛЬЗОВАНИЕ ВОДОРОДА
- 12.2 Вода
- ХИМИЧЕСКИЕ РЕАКЦИИ С УЧАСТИЕМ ВОДЫ
- ИСТОЧНИКИ ПРЕСНОЙ ВОДЫ И ЕЕ ИСПОЛЬЗОВАНИЕ
- КАЧЕСТВО ВОДЫ
- ЗАГРЯЗНЕНИЕ ВОДЫ
- ОЧИСТКА И ПОДГОТОВКА ВОДЫ
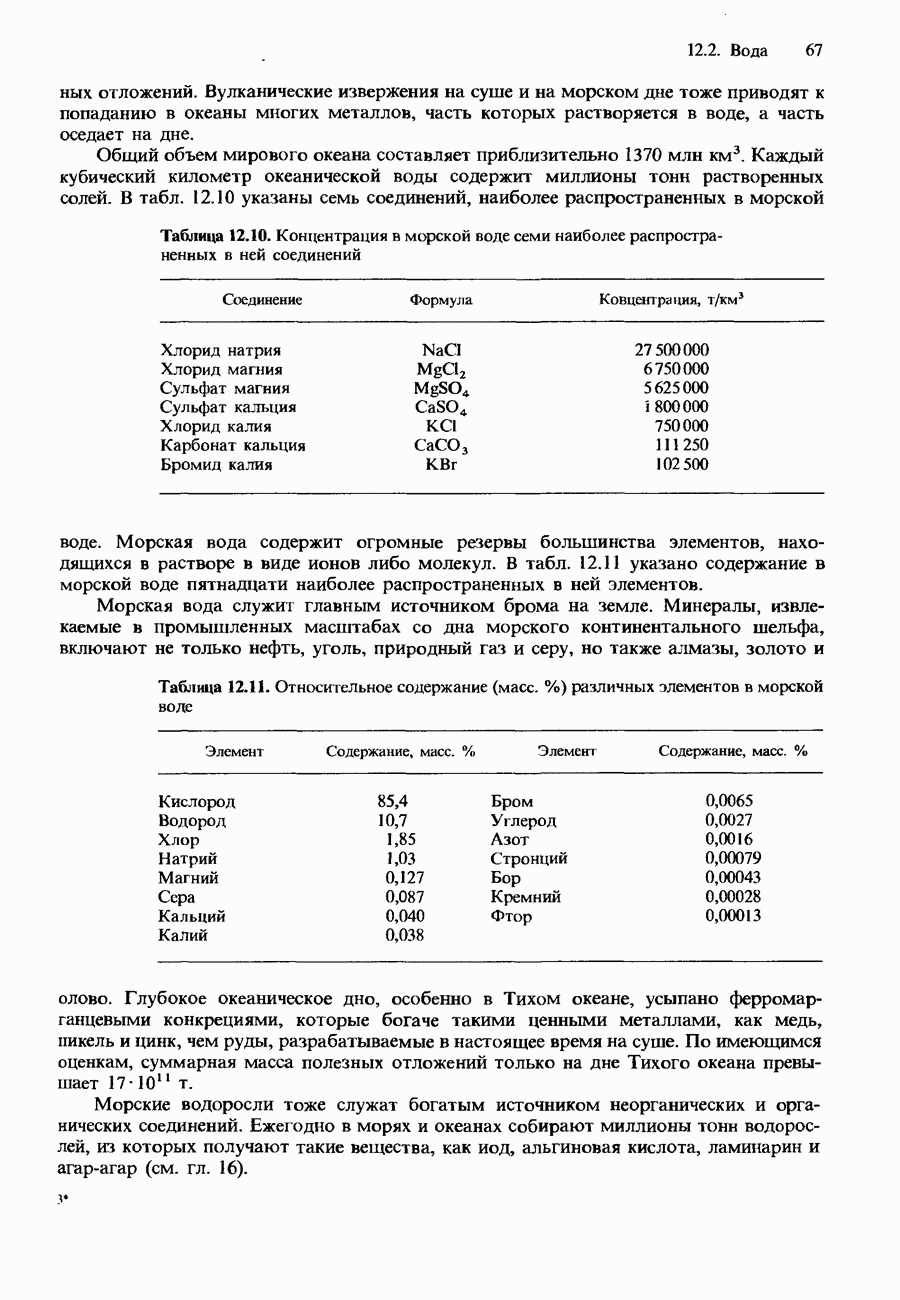
- ОКЕАНЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 13. s-Металлы
- 13.1 Структура и свойства s-металлов
- СТРУКТУРА
- ФИЗИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ S-МЕТАЛЛОВ
- 13.2 Соединения, образуемые s-металлами
- ДРУГИЕ БИНАРНЫЕ СОЕДИНЕНИЯ
- ГИДРОКСИДЫ
- КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- ТЕРМИЧЕСКАЯ УСТОЙЧИВОСТЬ ОКСОСОЕДИНЕНИЙ S-МЕТАЛЛОВ
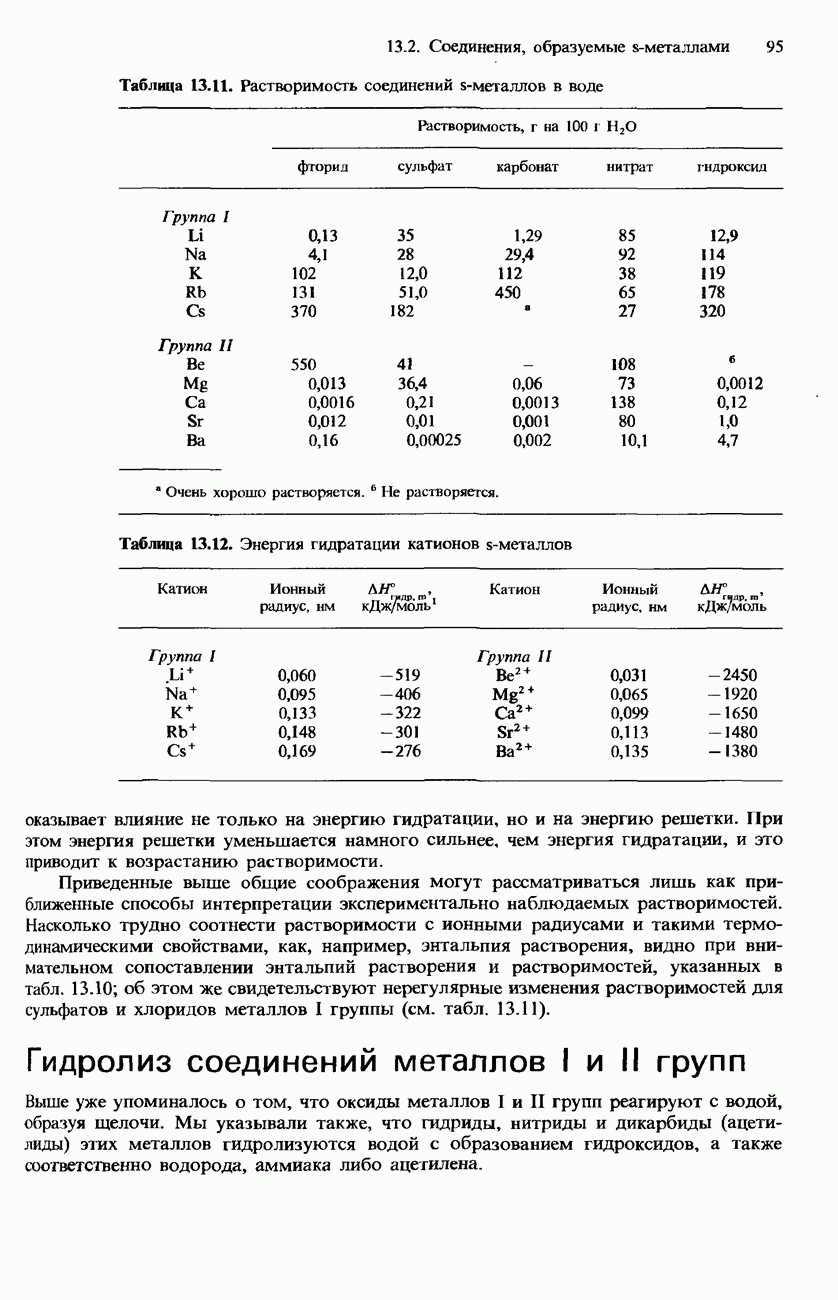
- РАСТВОРИМОСТЬ СОЛЕЙ И ГИДРОКСИДОВ МЕТАЛЛОВ I И II ГРУПП В ВОДЕ
- АНОМАЛЬНЫЕ СВОЙСТВА ЛИТИЯ И БЕРИЛЛИЯ, А ТАКЖЕ ИХ СОЕДИНЕНИЙ
- 13.3. Распространенность в природе, получение и применение
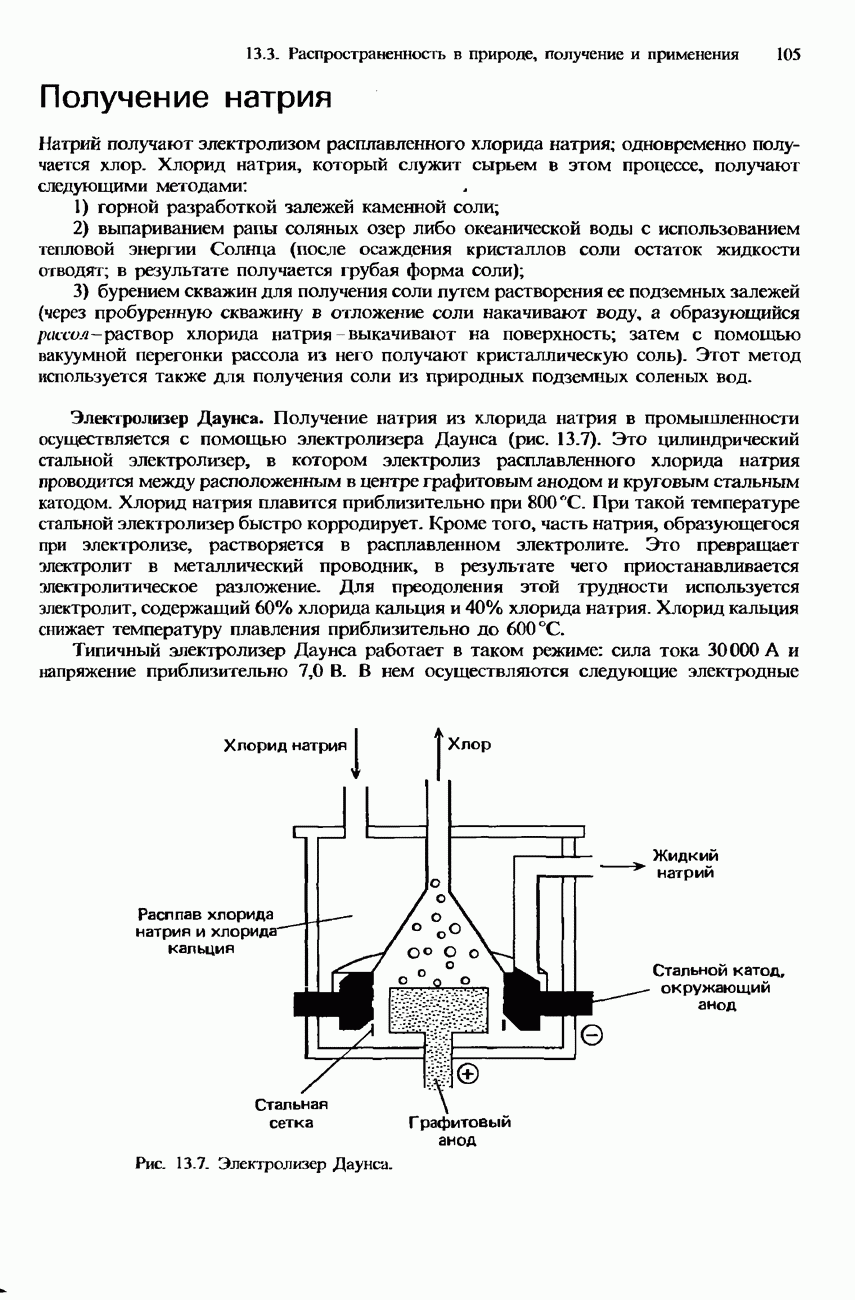
- ПОЛУЧЕНИЕ S-МЕТАЛЛОВ
- ПОЛУЧЕНИЕ СОЕДИНЕНИЙ S-МЕТАЛЛОВ
- ПРИМЕНЕНИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 14. d-ЭЛЕМЕНТЫ
- 14.1. Структура и свойства d-элементов
- d-ЭЛЕМЕНТЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА
- ХИМИЧЕСКИЕ СВОЙСТВА
- 14.2 Химия семи d-элементов
- МАРГАНЕЦ
- ЖЕЛЕЗО
- КОБАЛЬТ
- НИКЕЛЬ
- МЕДЬ
- ЦИНК
- 14.3. Распространенность в природе, получение и применения
- ПРОИЗВОДСТВО ЖЕЛЕЗА И СТАЛИ
- ПОЛУЧЕНИЕ ДРУГИХ МЕТАЛЛОВ ПЕРВОГО ПЕРЕХОДНОГО РЯДА
- ПРИМЕНЕНИЯ d-ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 15. ЭЛЕМЕНТЫ III-VI ГРУПП
- 15.1. Алюминий и другие элементы III группы
- БОР
- ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
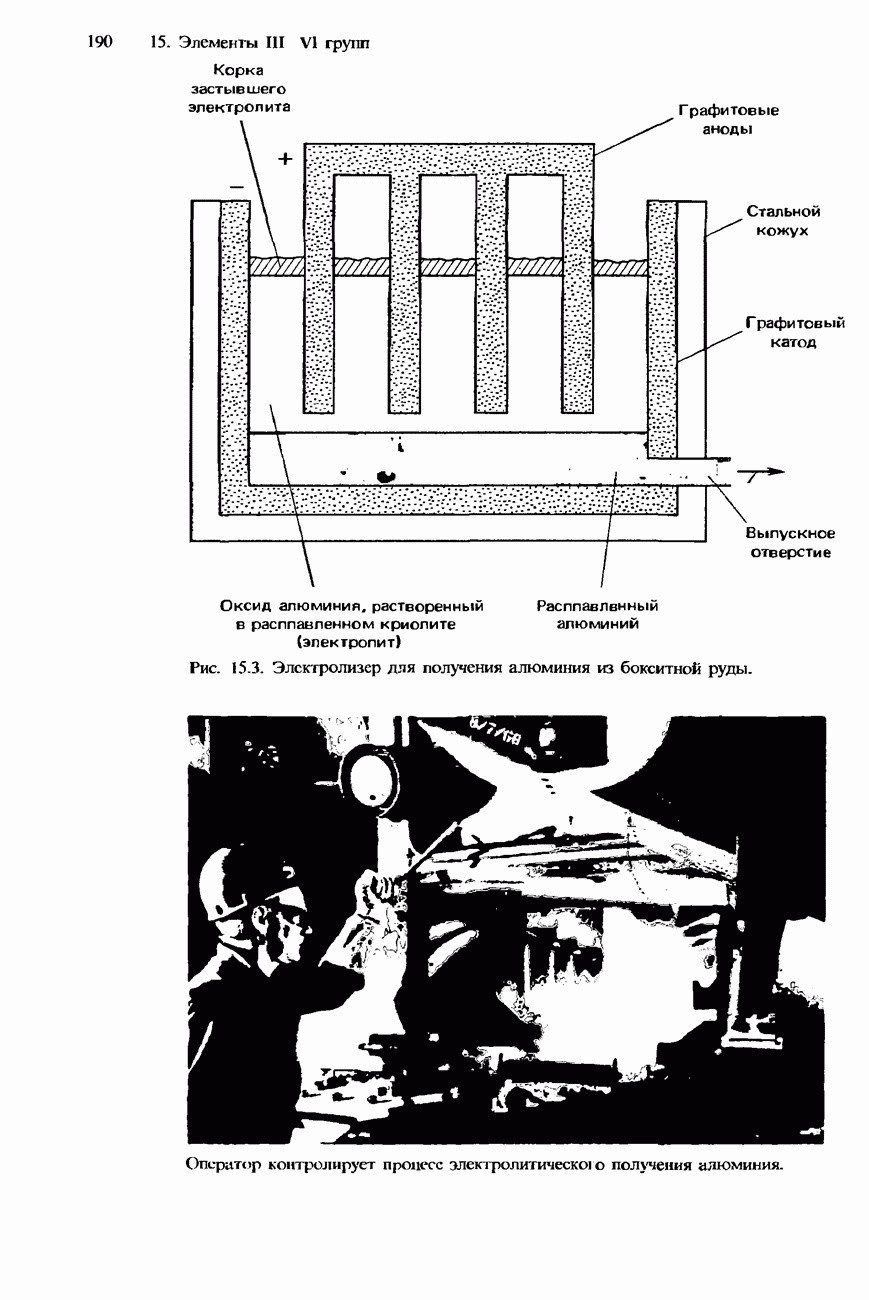
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ АЛЮМИНИЯ
- ПРИМЕНЕНИЯ АЛЮМИНИЯ И ЕГО СОЕДИНЕНИЙ
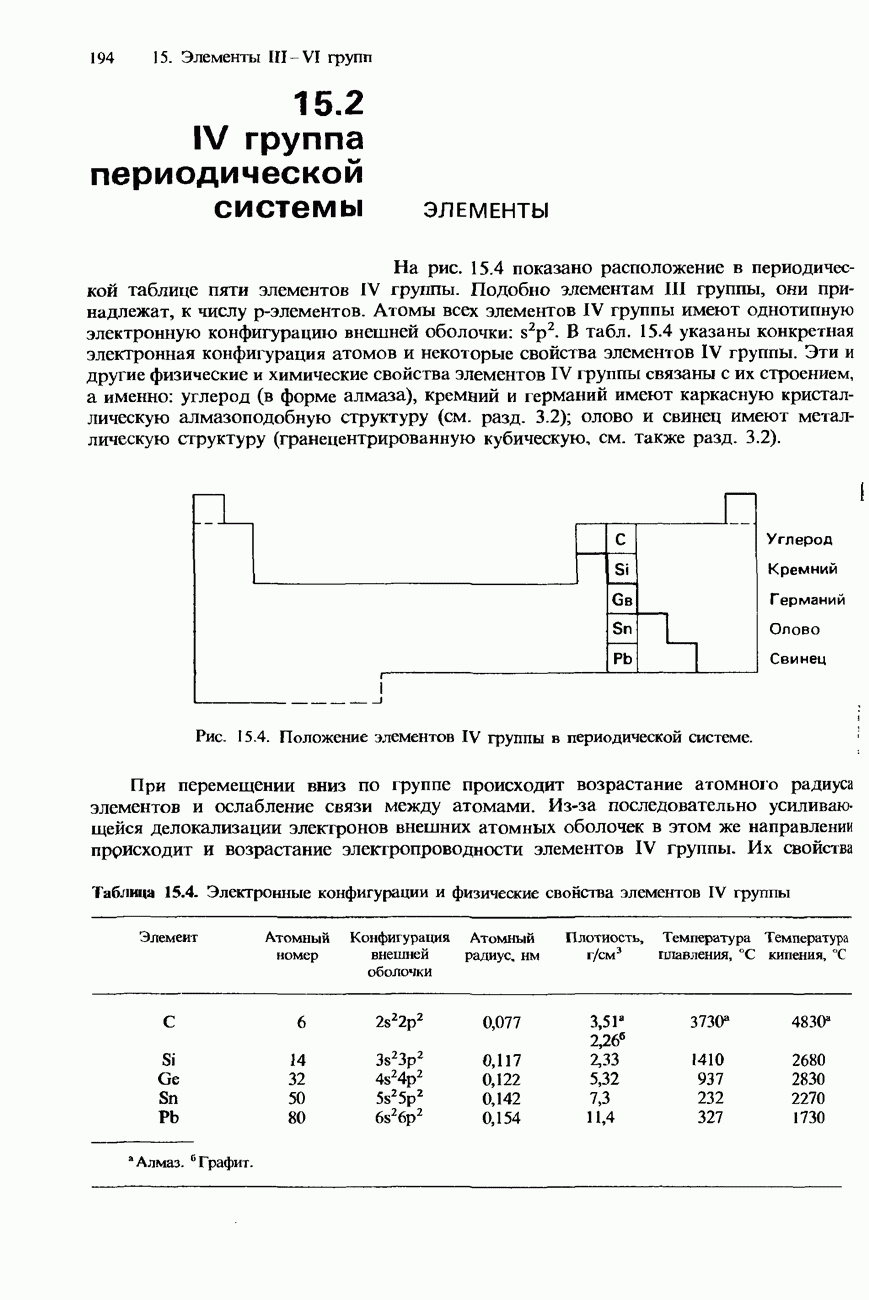
- 15.2. IV группа периодической системы
- СОЕДИНЕНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ ИЗ РУД
- ПРИМЕНЕНИЯ УГЛЕРОДА
- ПРИМЕНЕНИЯ КРЕМНИЯ
- ПРИМЕНЕНИЯ ГЕРМАНИЯ, ОЛОВА И СВИНЦА
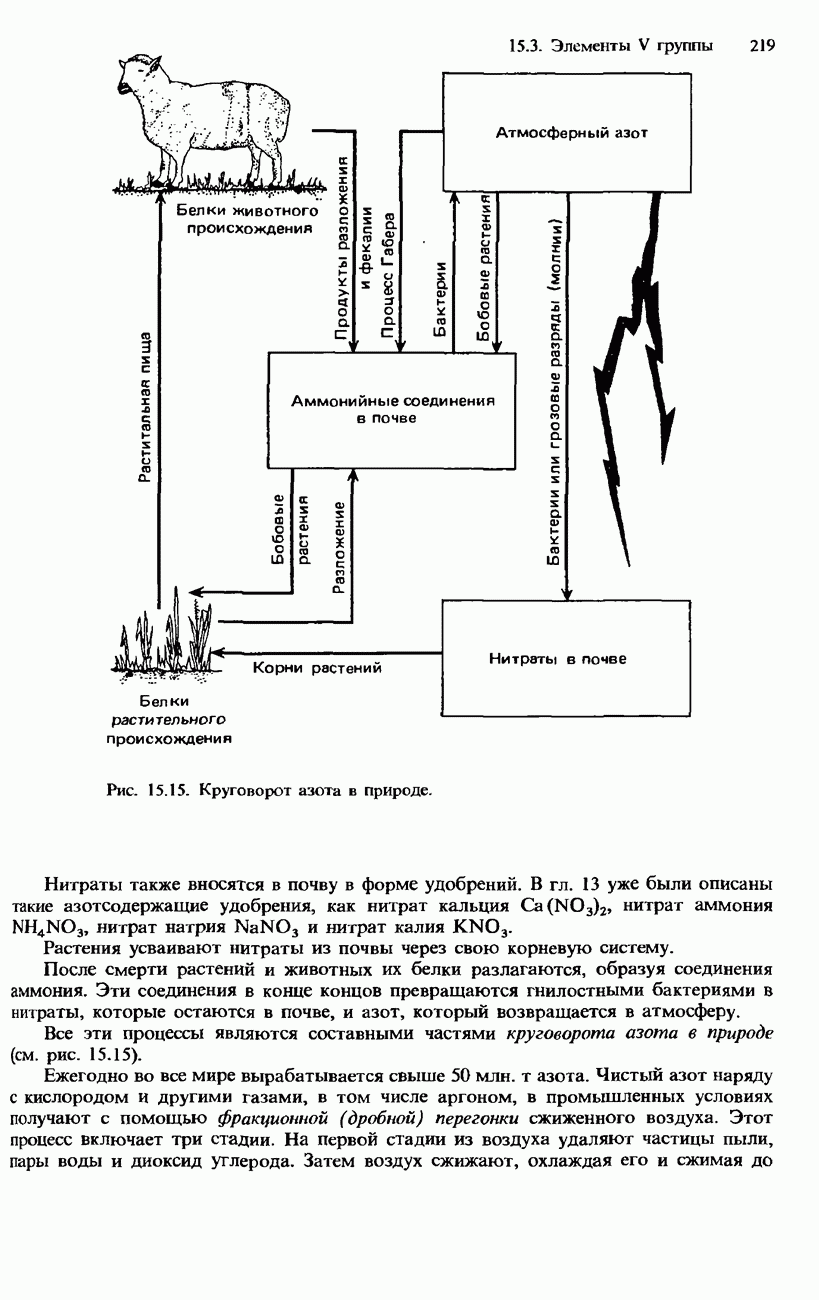
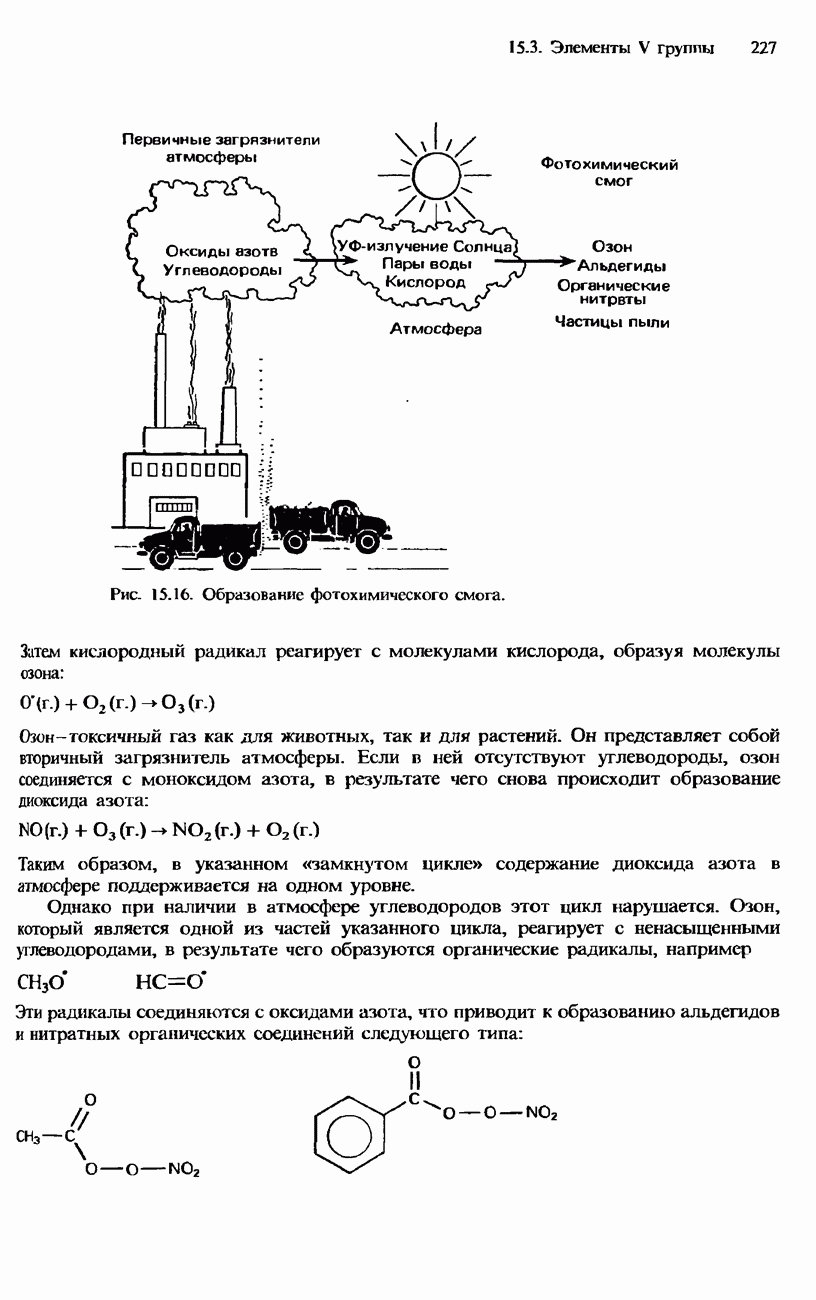
- 15.3. Элементы V группы
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ. ПОЛУЧЕНИЕ И ПРИМЕНЕНИЯ АЗОТА И ФОСФОРА
- СОЕДИНЕНИЯ АЗОТА
- СОЕДИНЕНИЯ ФОСФОРА
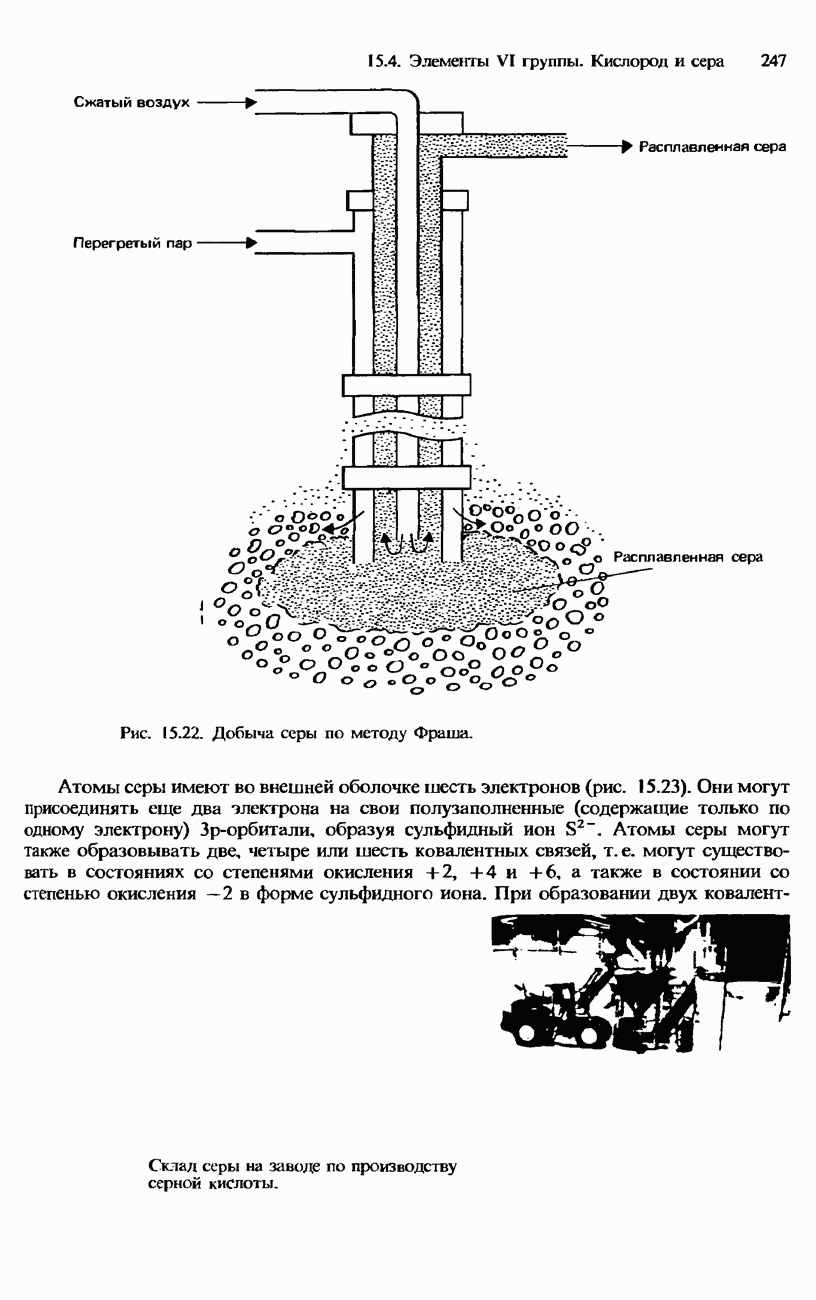
- 15.4. Элементы VI группы. Кислород и сера
- КИСЛОРОД
- СОЕДИНЕНИЯ КИСЛОРОДА
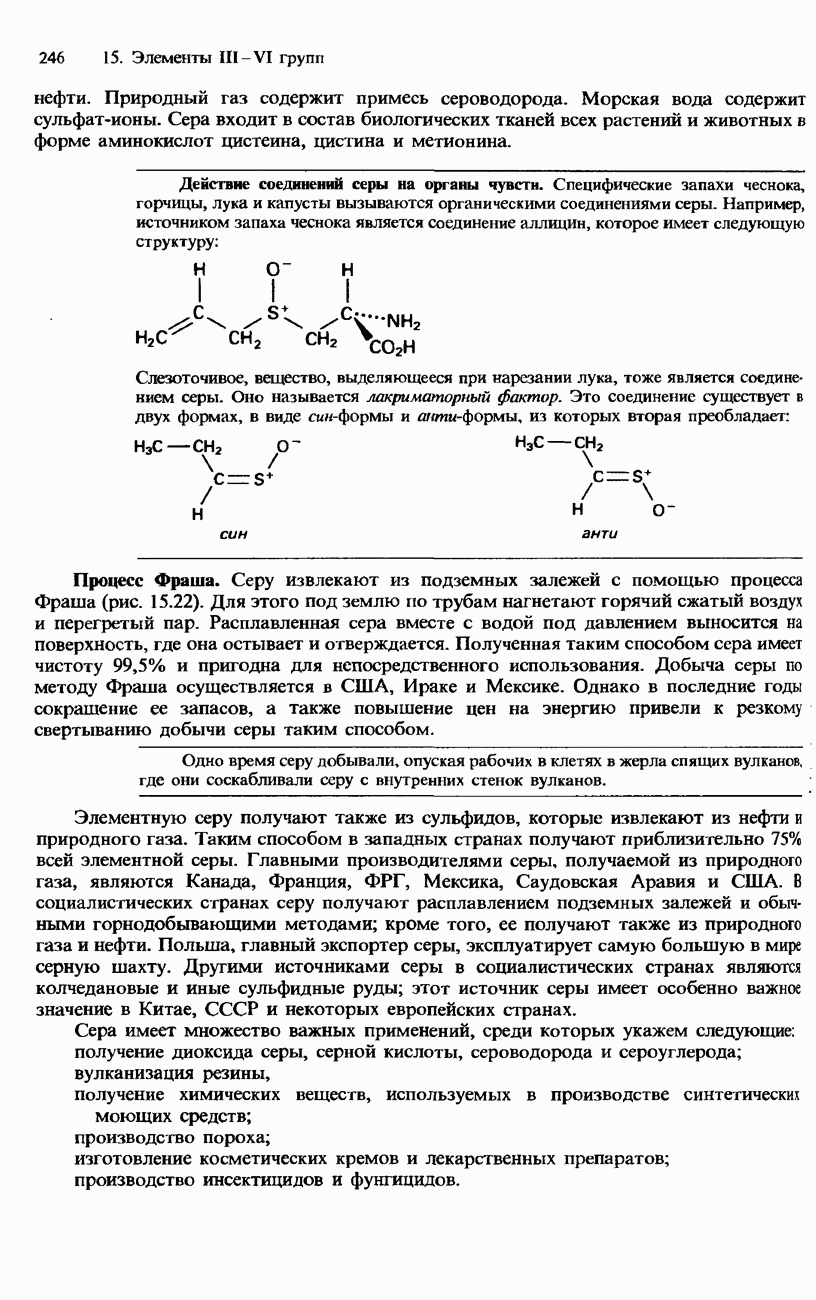
- СЕРА
- СОЕДИНЕНИЯ СЕРЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 16. ГАЛОГЕНЫ И БЛАГОРОДНЫЕ ГАЗЫ
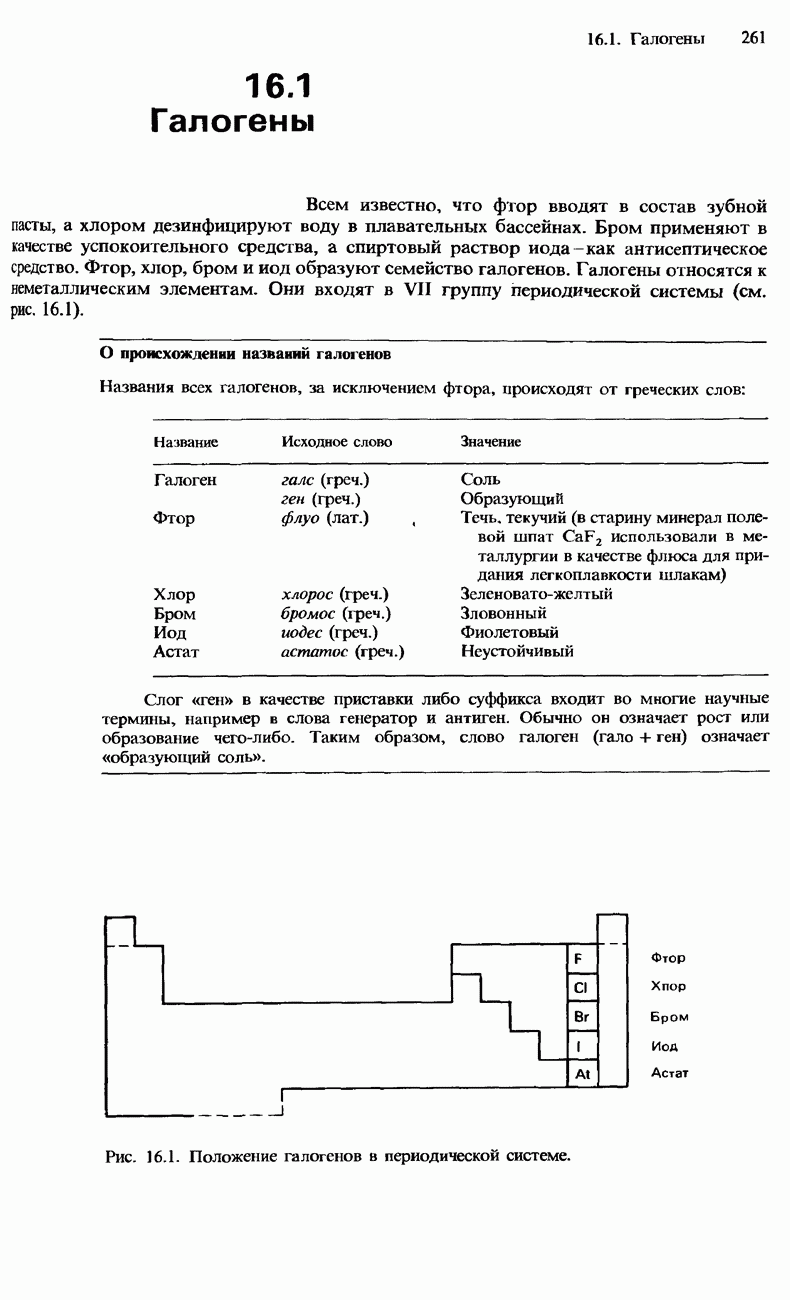
- 16.1. Галогены
- ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ ГАЛОГЕНОВ
- ЛАБОРАТОРНЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ГАЛОГЕНОВ
- ФИЗИЧЕСКИЕ И БИОЛОГИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ ГАЛОГЕНОВ
- 16.2. Соединения галогенов
- ГАЛОГЕНОВОДОРОДЫ
- КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ ГАЛОГЕНОВ
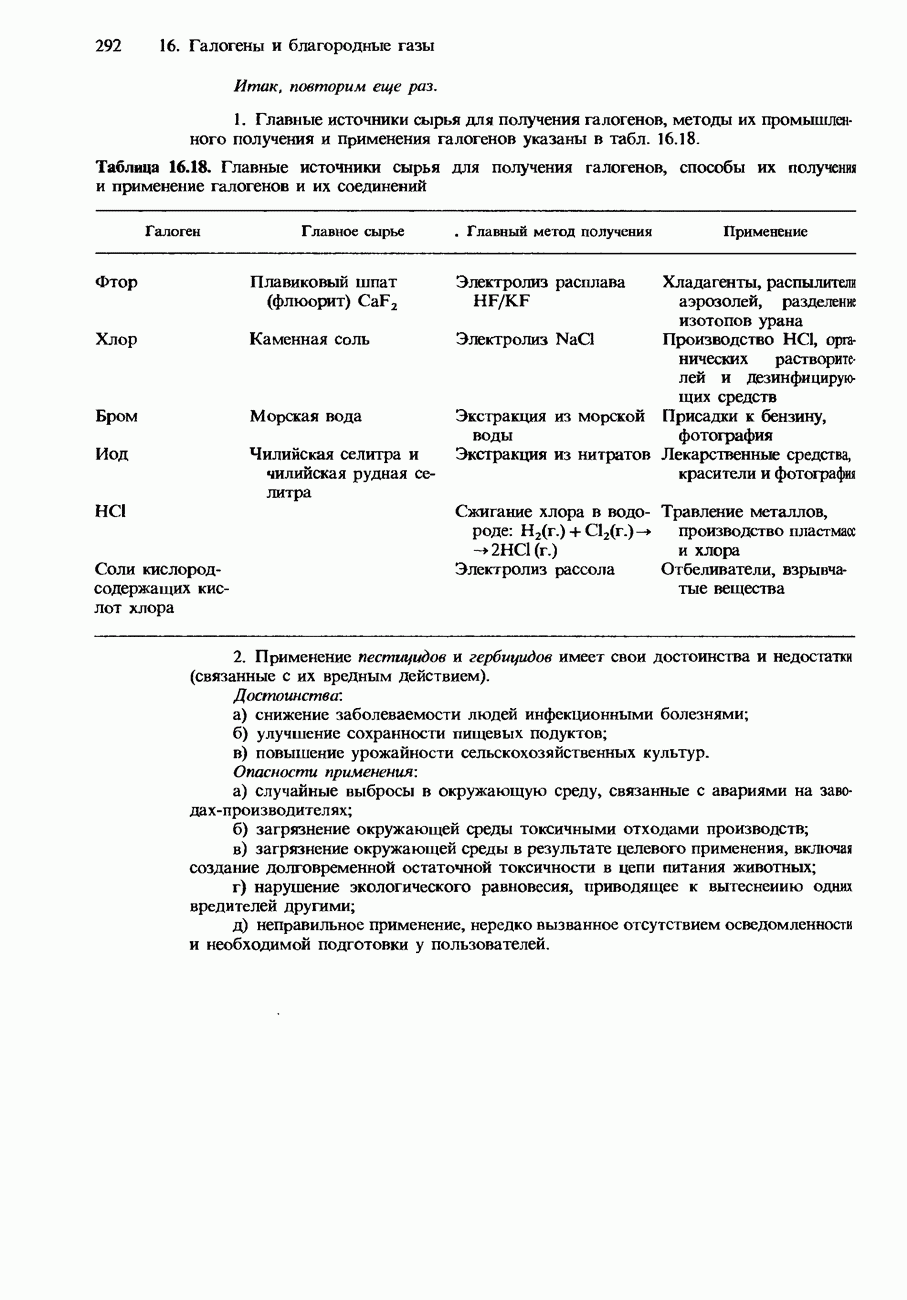
- 16.3. Распространенность, получение и применение галогенов и их соединений
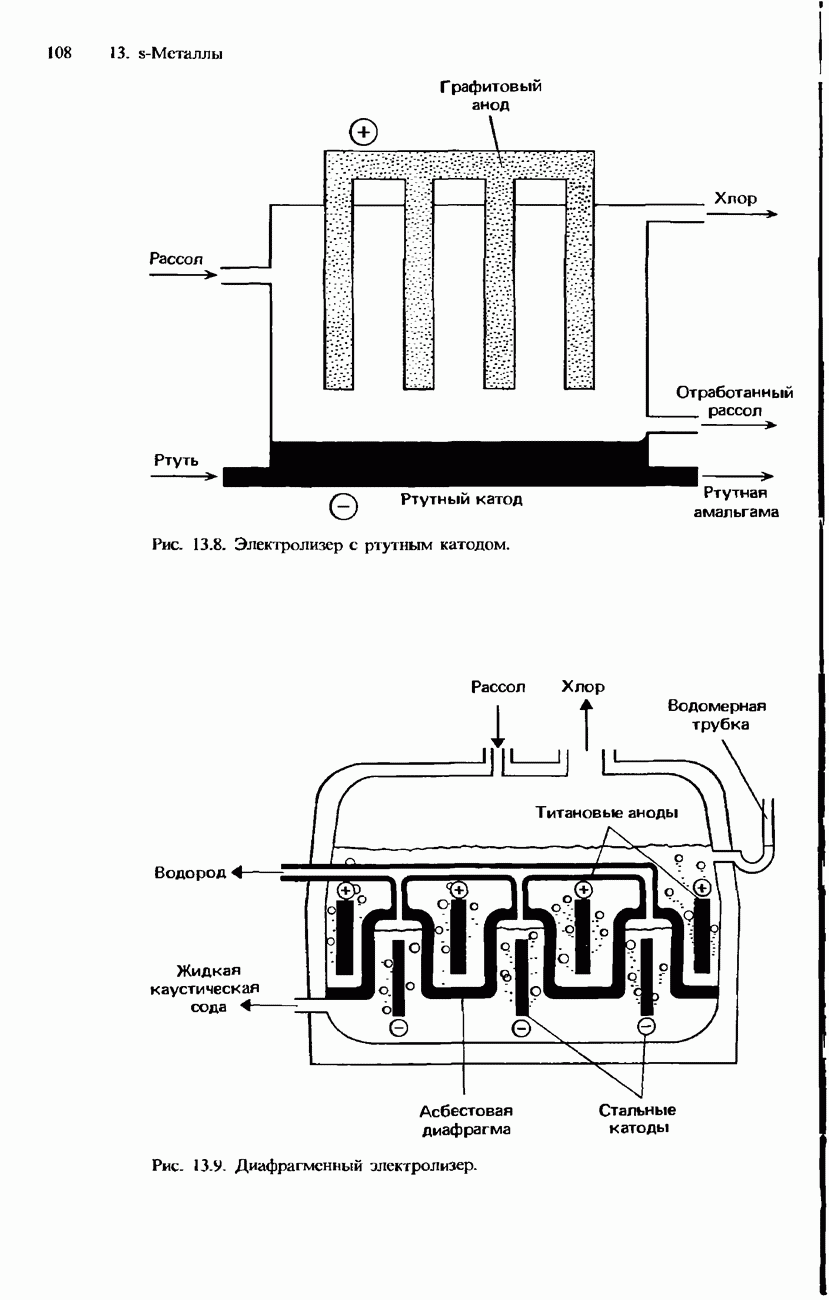
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ХЛОРА
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ДРУГИХ ГАЛОГЕНОВ
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СОЕДИНЕНИЙ ХЛОРА
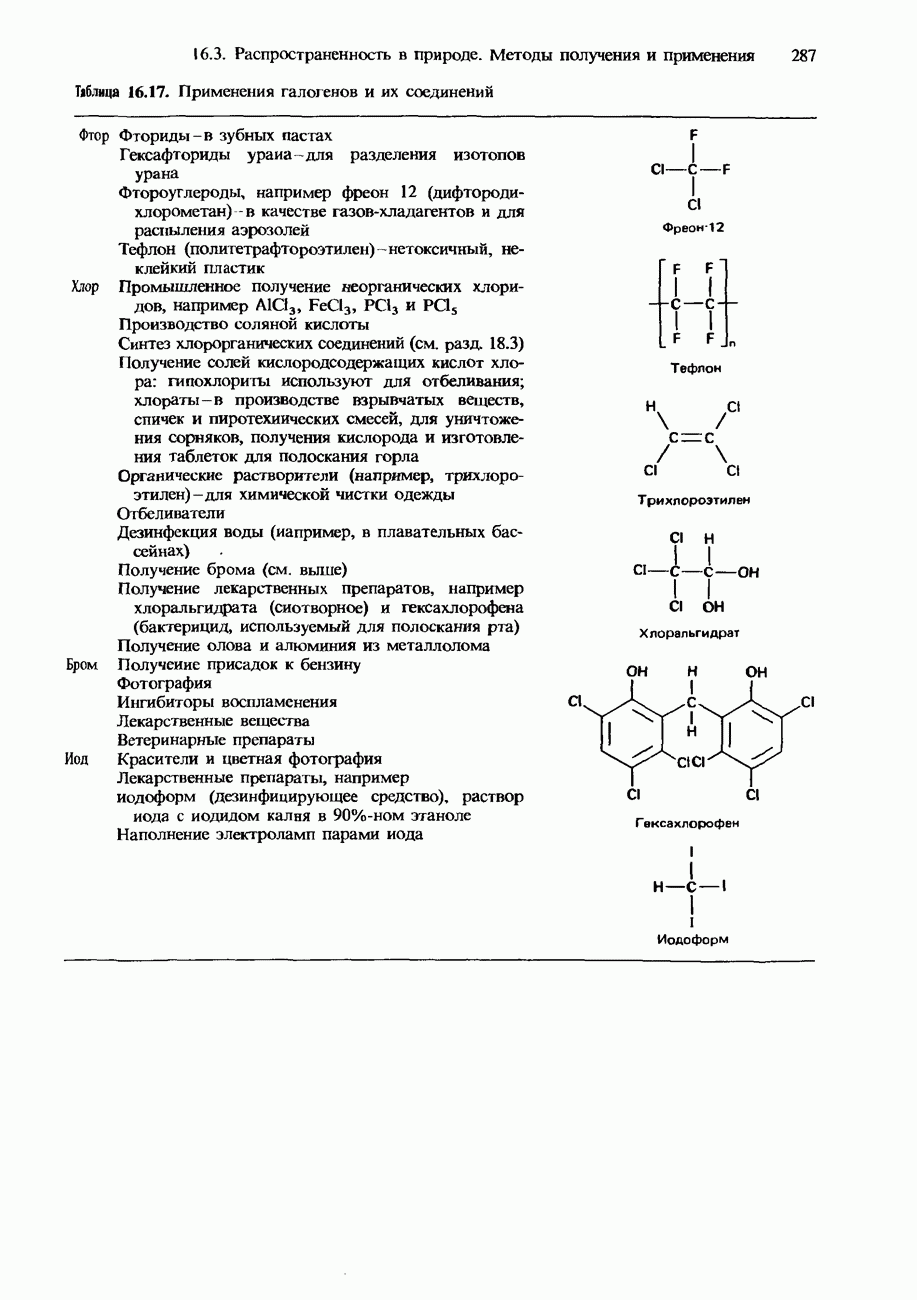
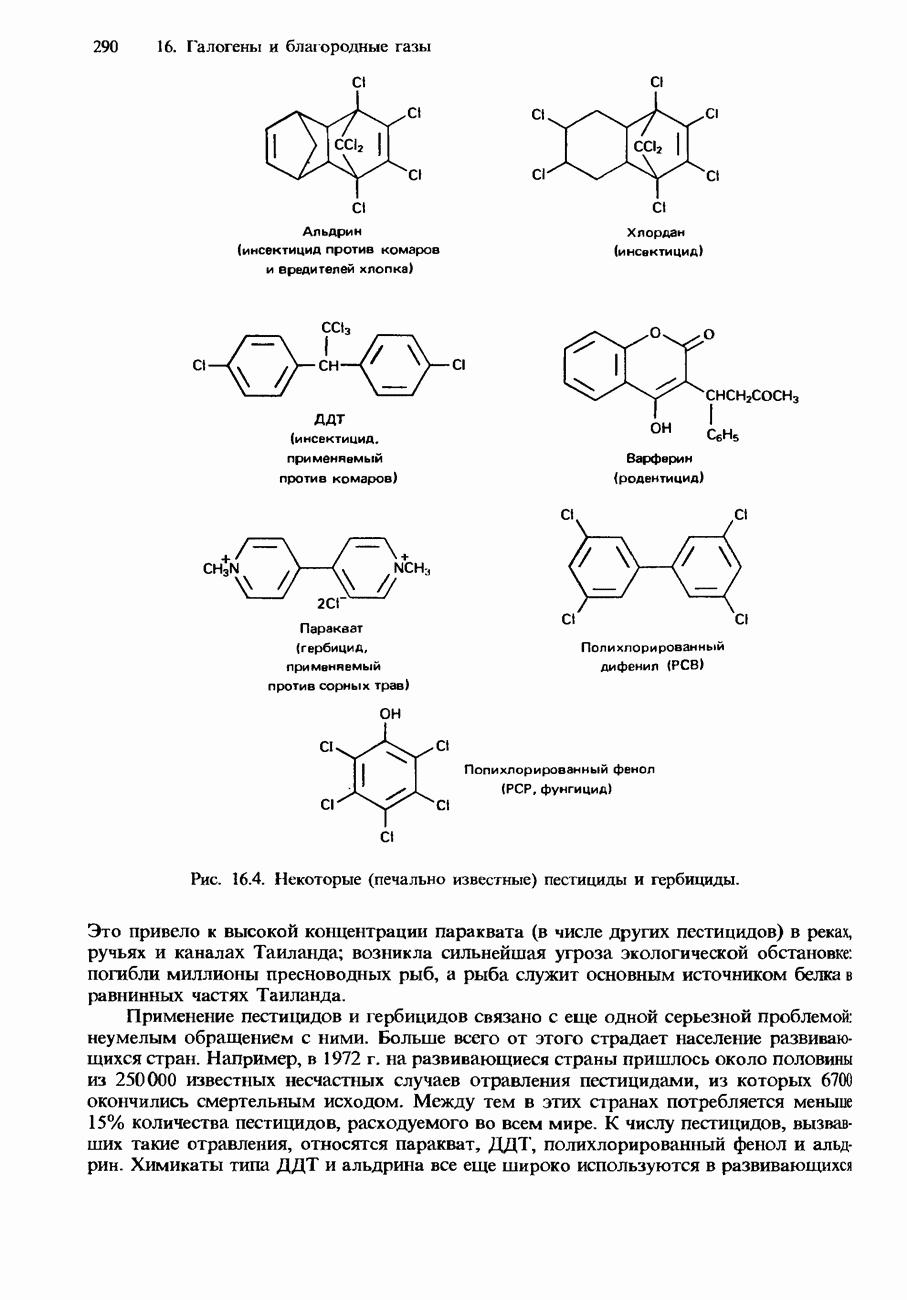
- ПРИМЕНЕНИЯ ГАЛОГЕНОВ И ИХ СОЕДИНЕНИЙ
- ТОКСИЧНОСТЬ ХЛОРСОДЕРЖАЩИХ ПРОДУКТОВ
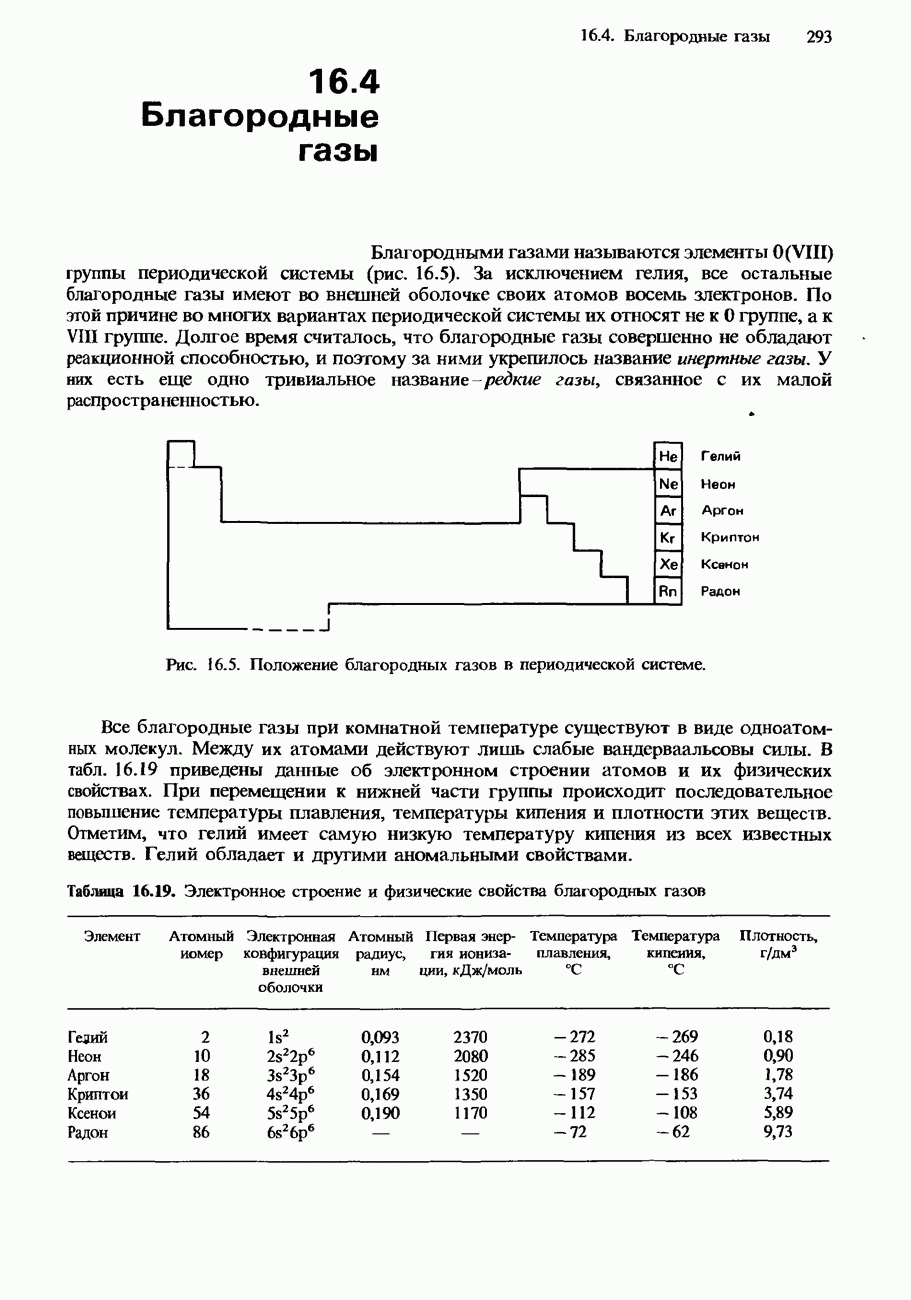
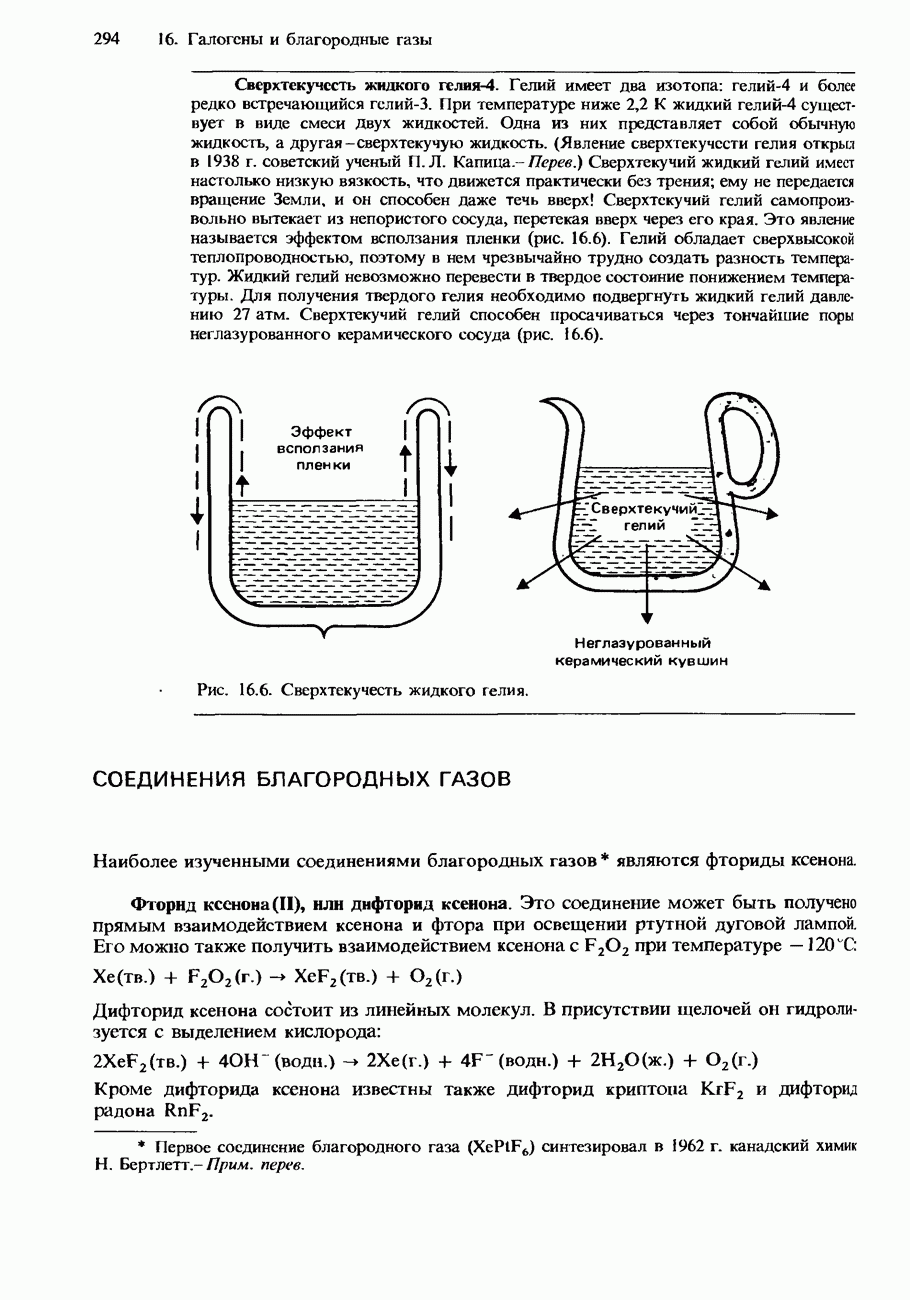
- 16.4. Благородные газы
- СОЕДИНЕНИЯ БЛАГОРОДНЫХ ГАЗОВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
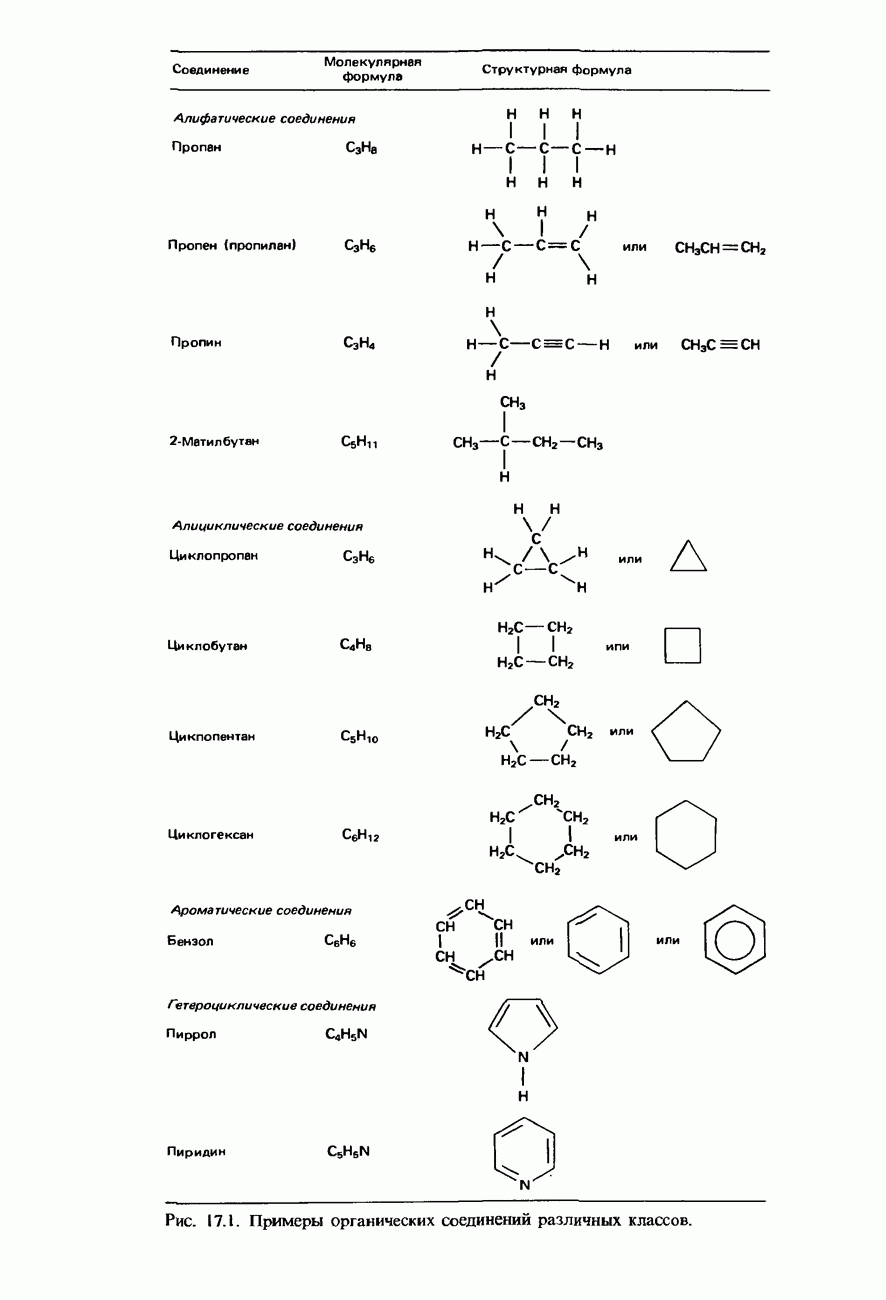
- 17. ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ
- 7.1. Органическая химия
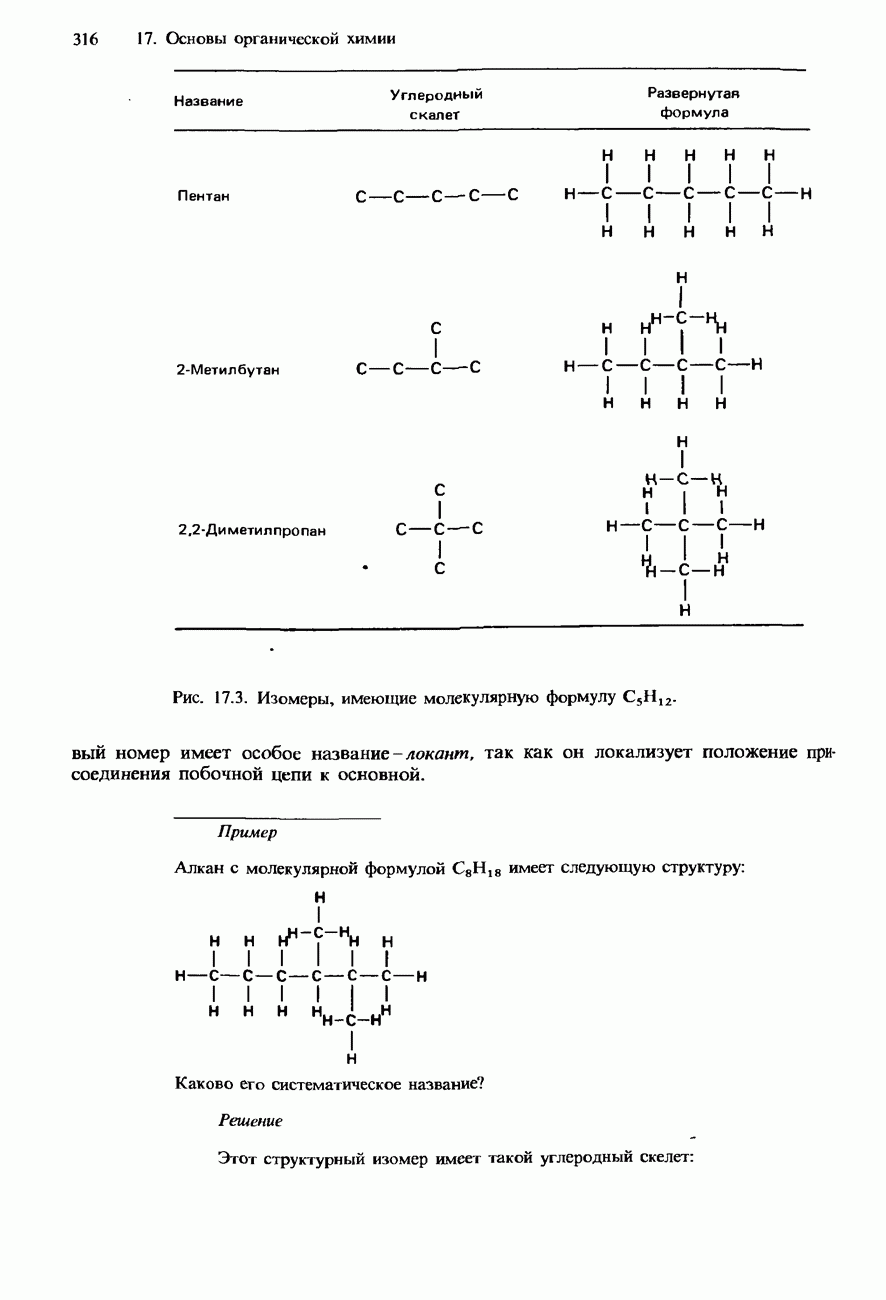
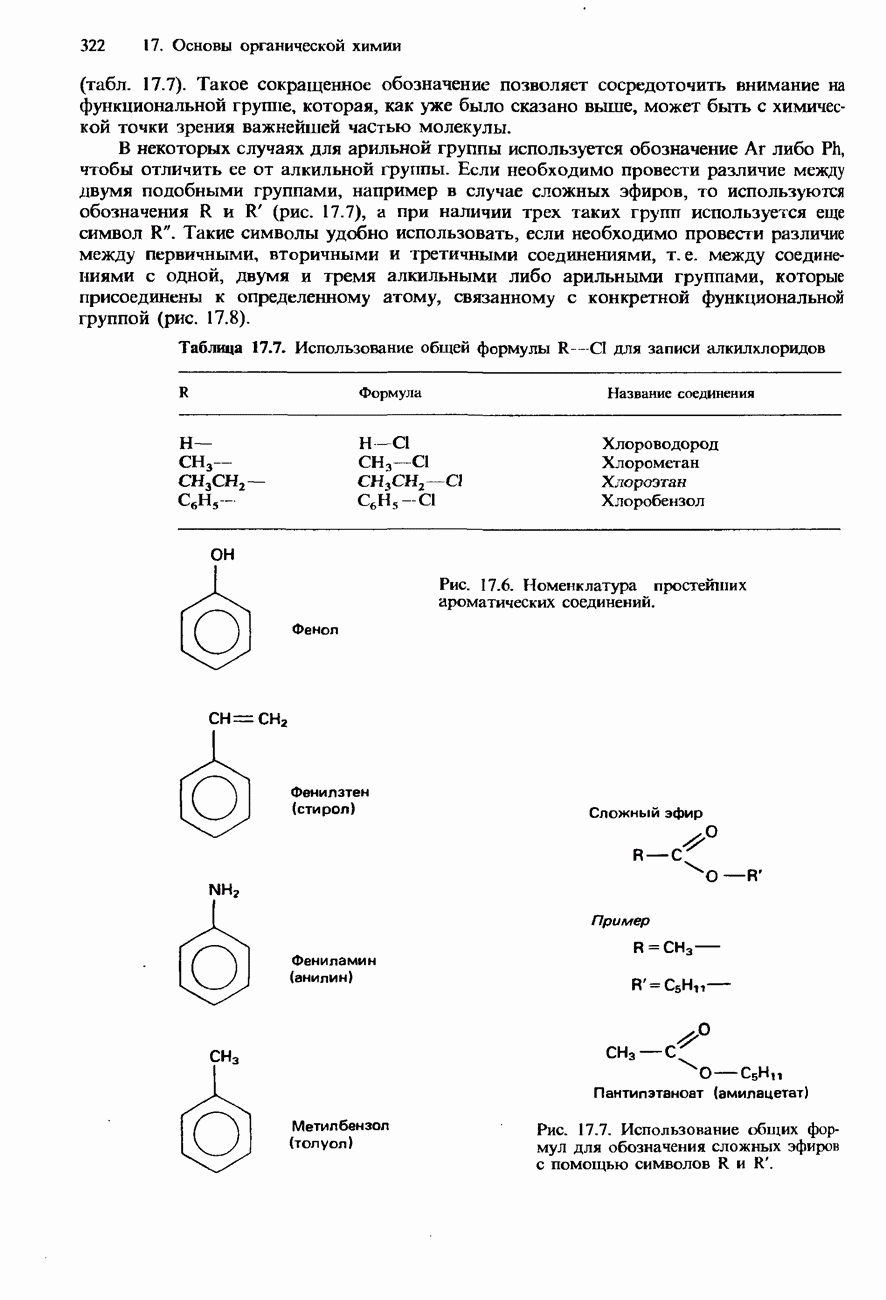
- НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
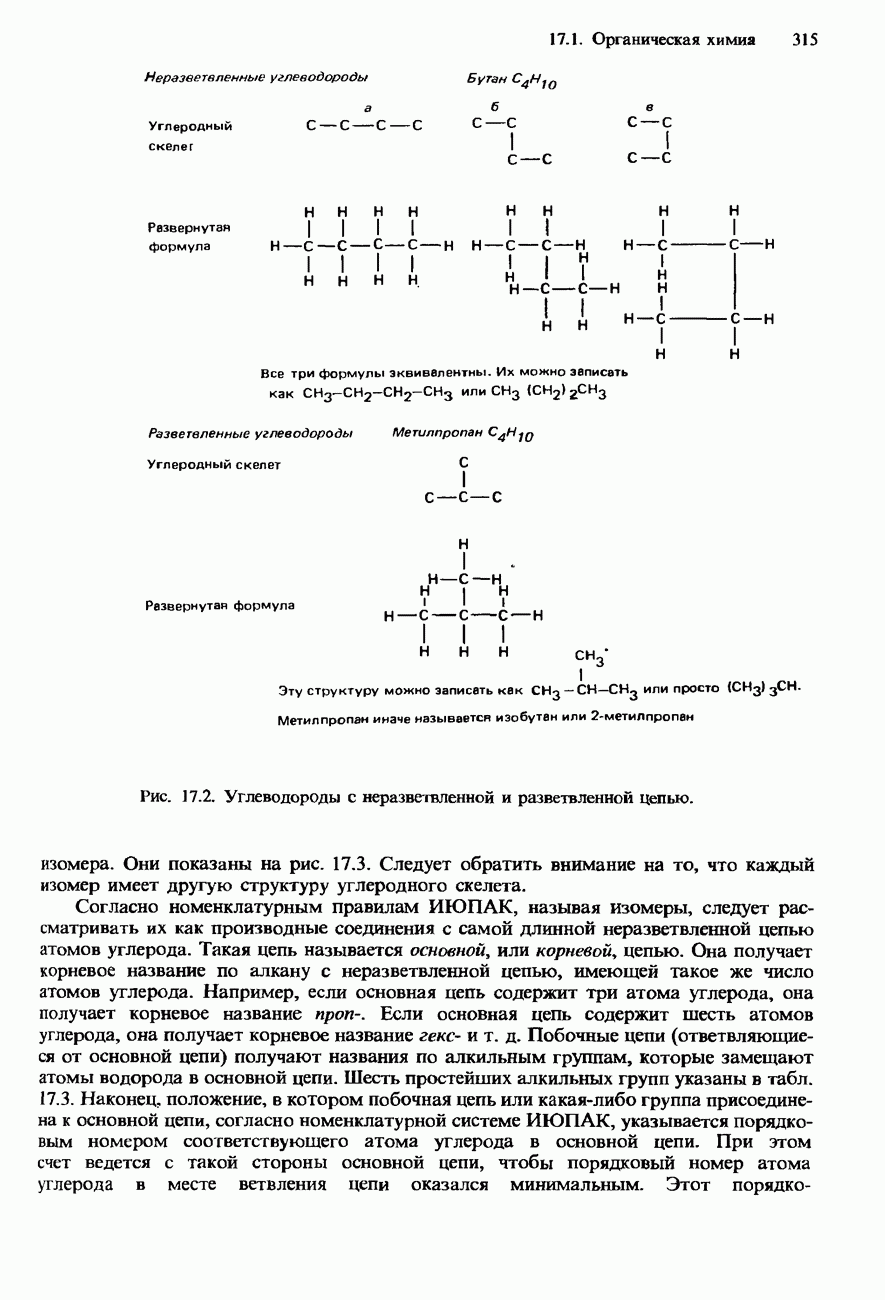
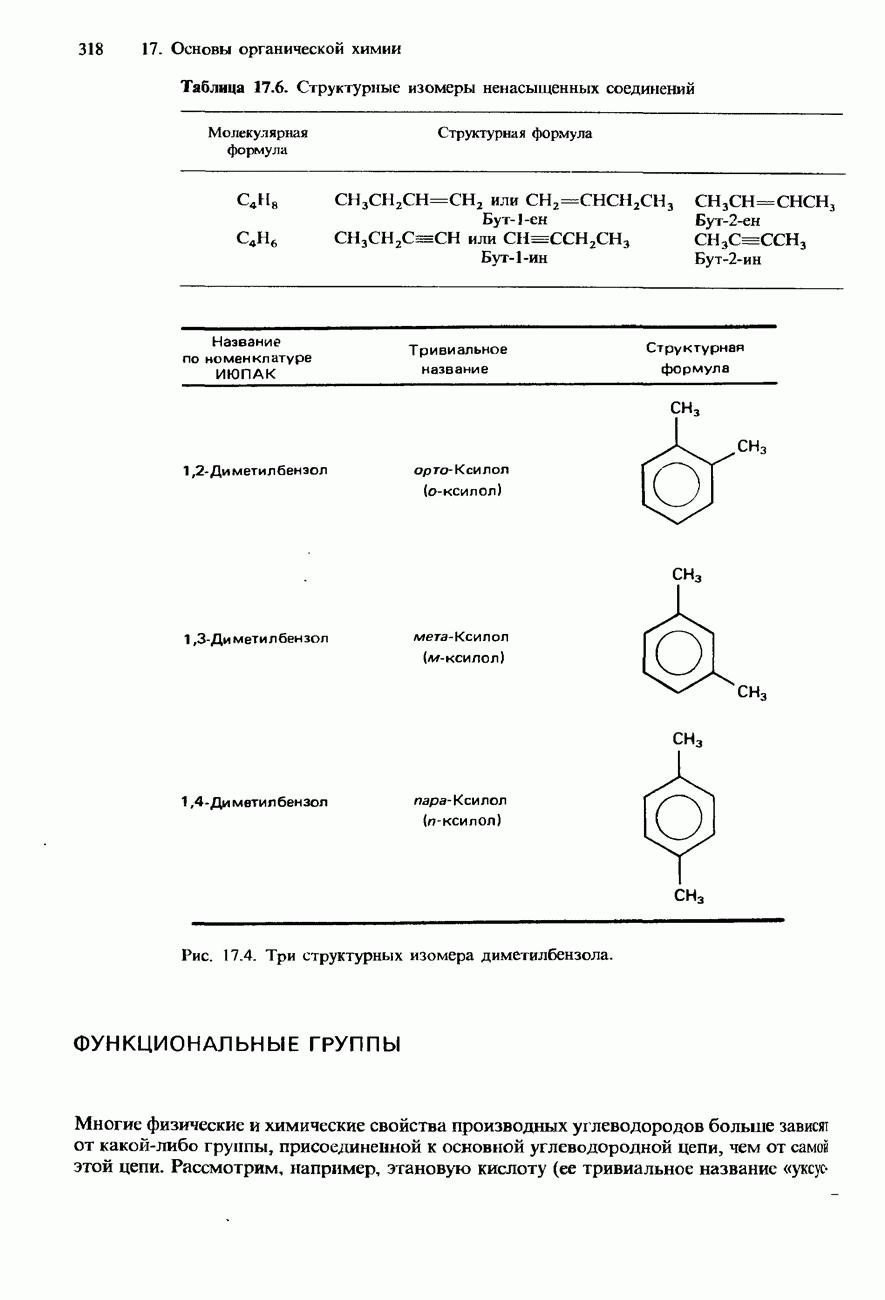
- УГЛЕВОДОРОДЫ
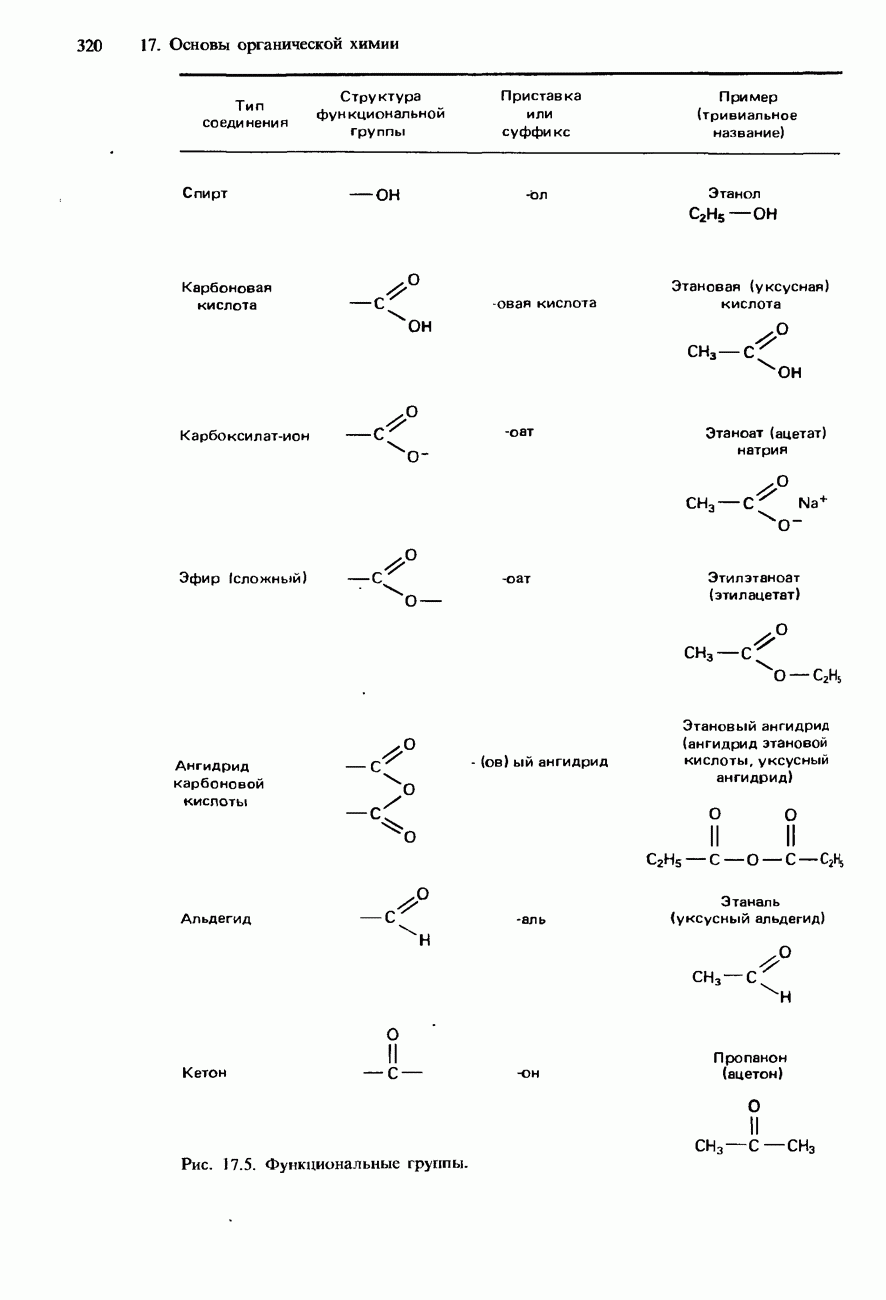
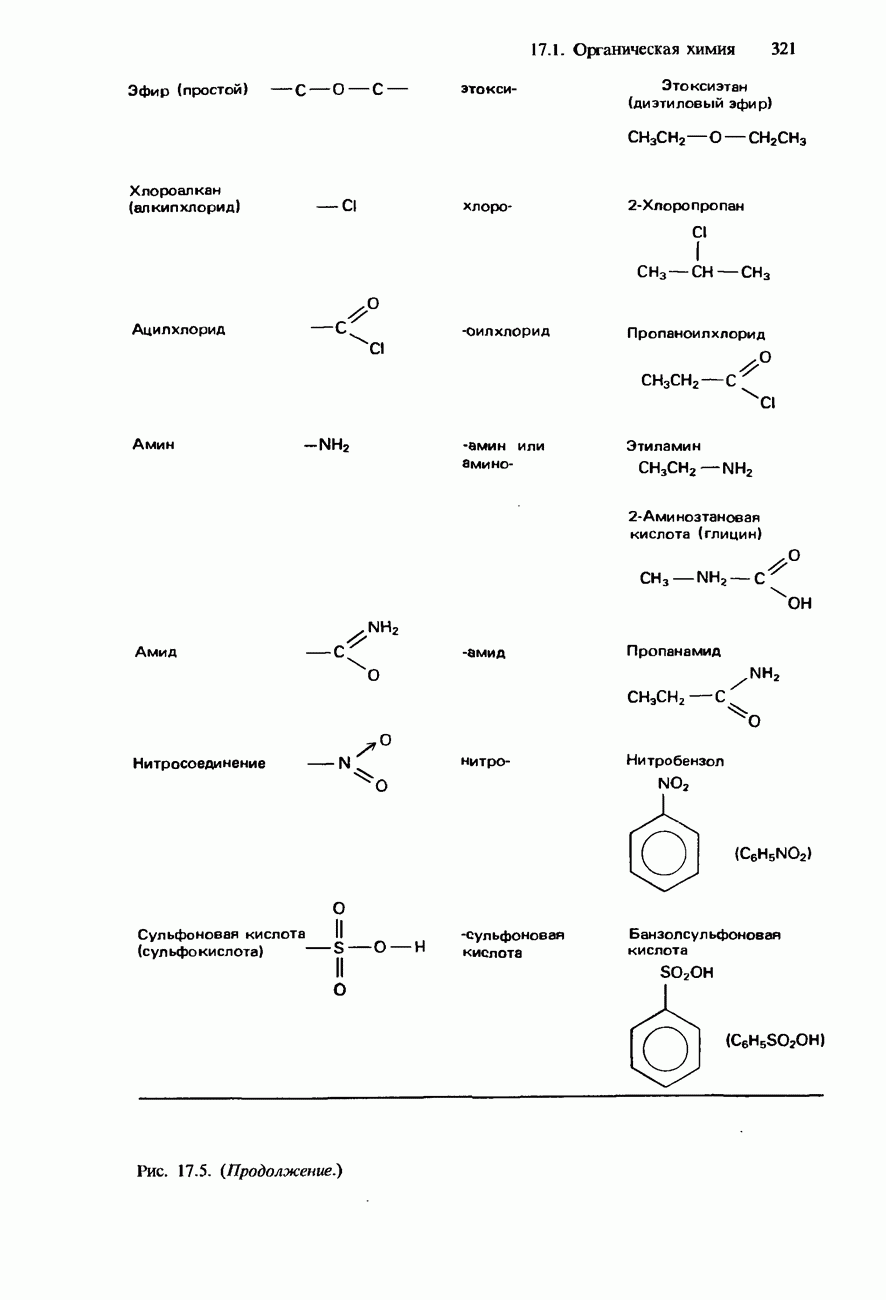
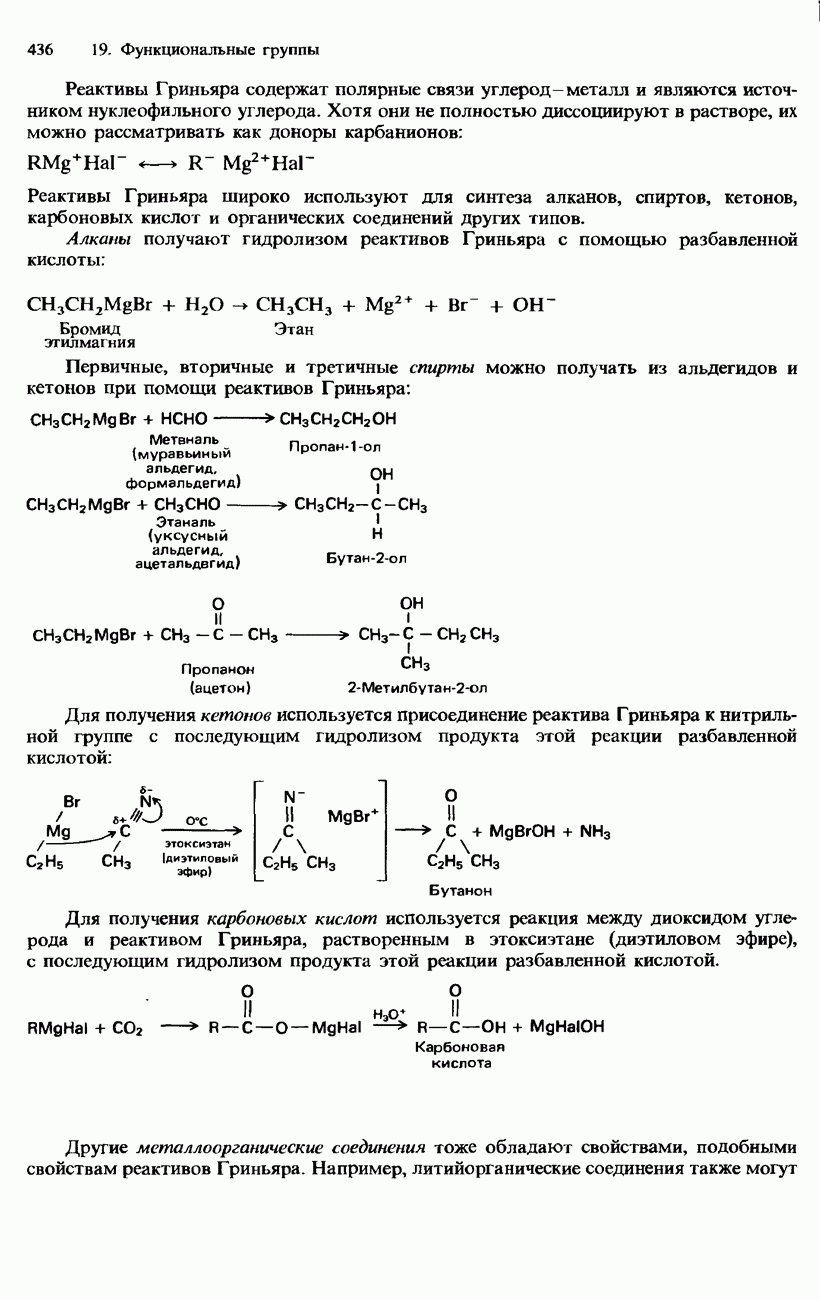
- ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ПОЛУЧЕНИЕ И ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 17.2. Молекулярная структура органических соединений
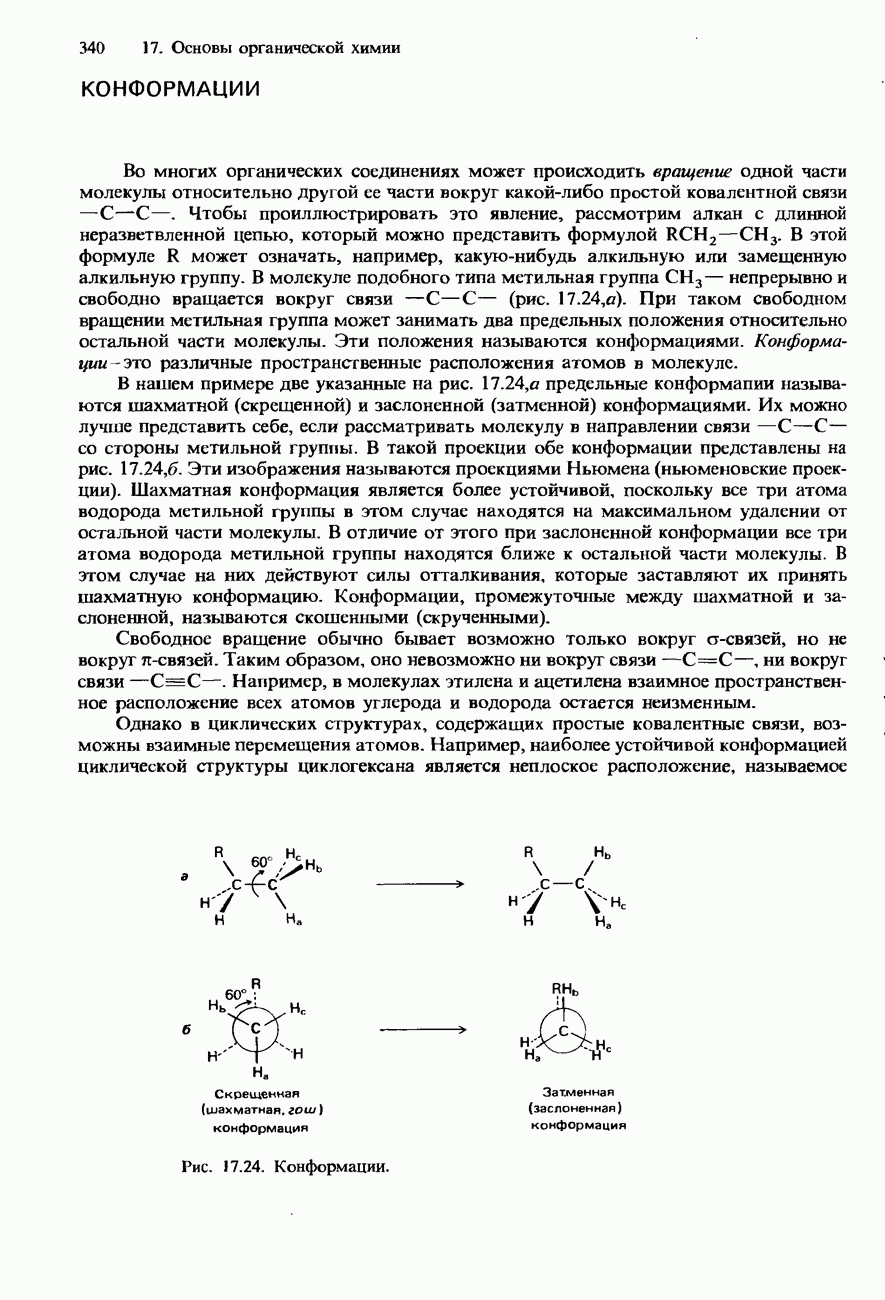
- КОНФОРМАЦИИ
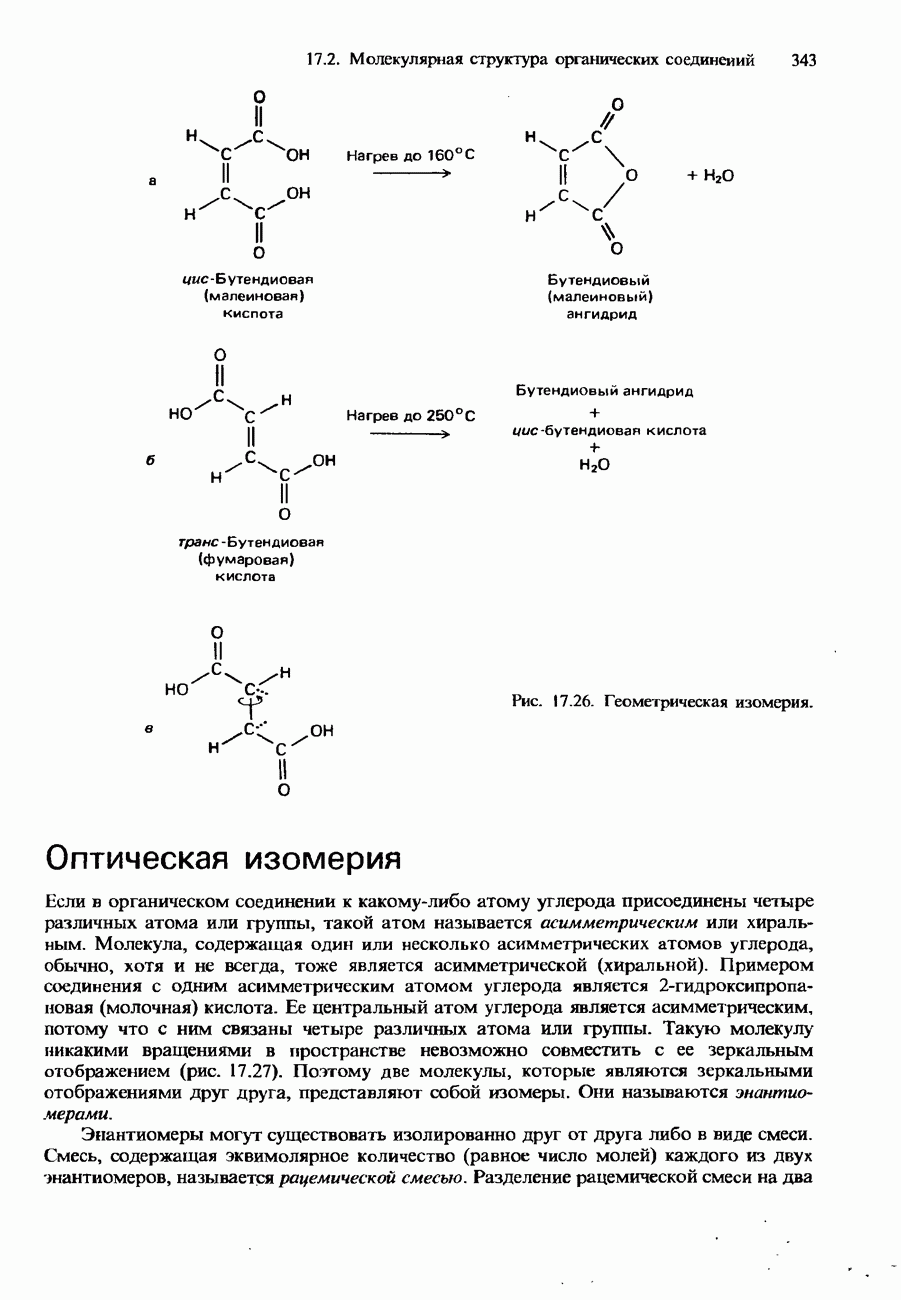
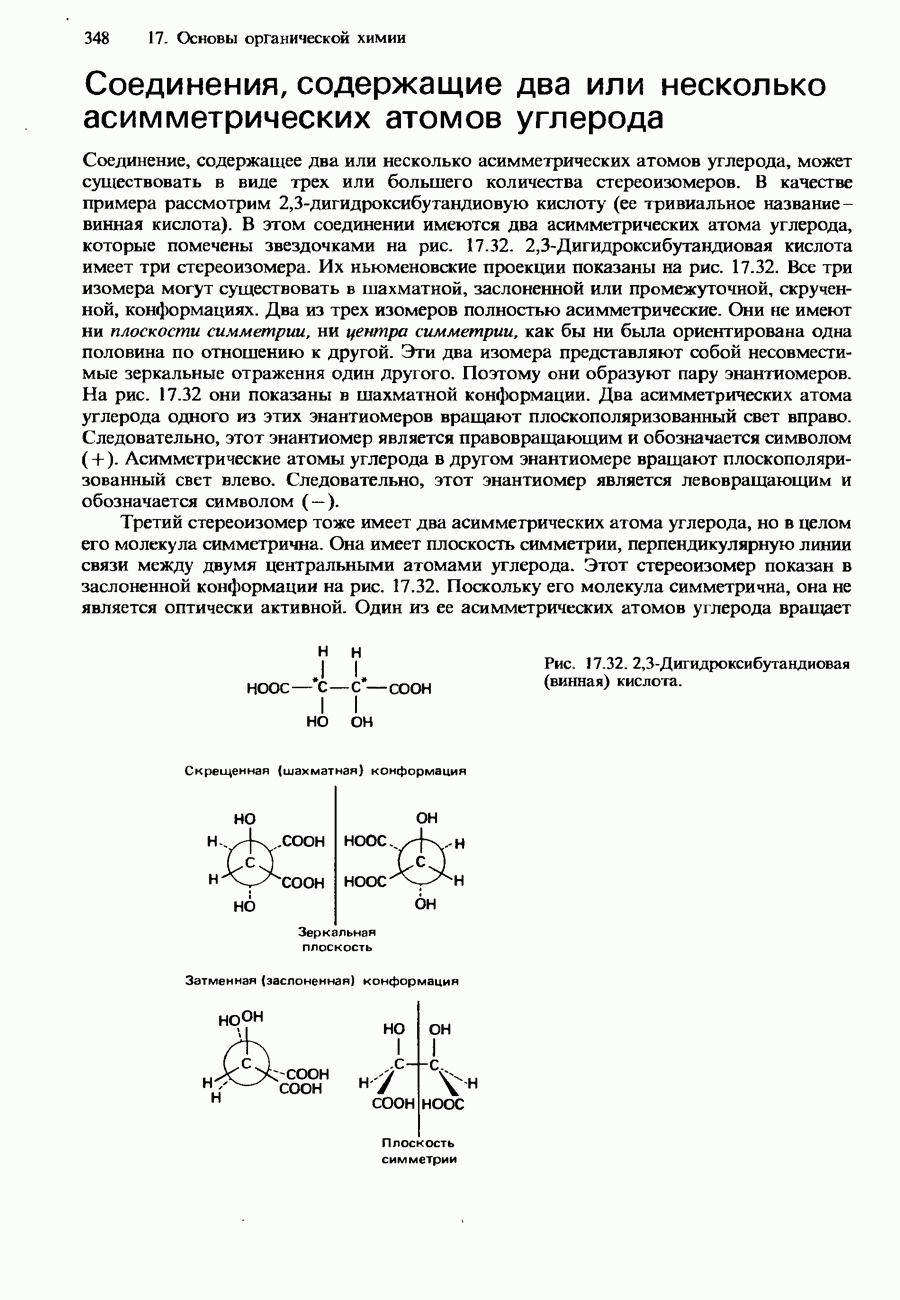
- СТЕРЕОИЗОМЕРИЯ
- 17.3. Механизмы органических реакций
- ФАКТОРЫ, ВЛИЯЮЩИЕ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- НУКЛЕОФИЛЫ И ЭЛЕКТРОФИЛЫ
- ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 18. УГЛЕВОДОРОДЫ
- 18.1. Алифатические углеводороды
- АЛКАНЫ
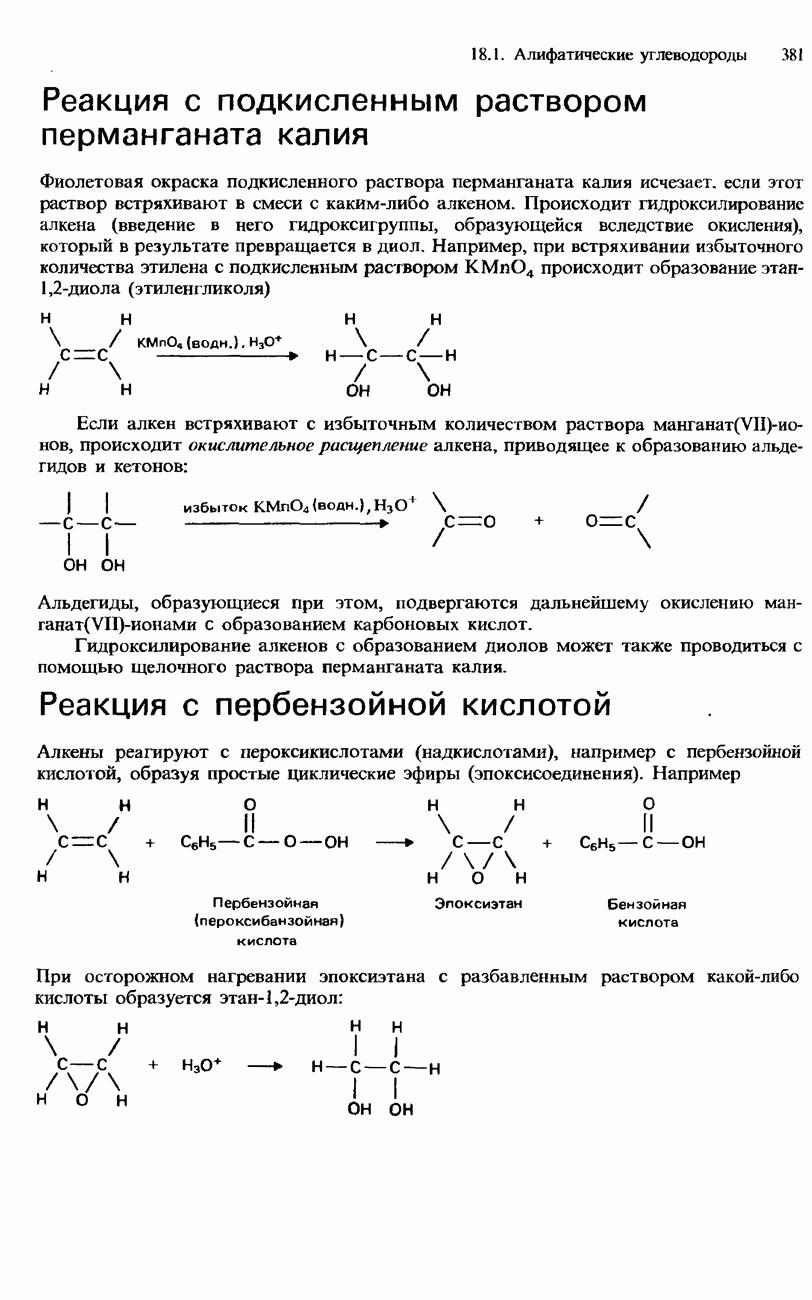
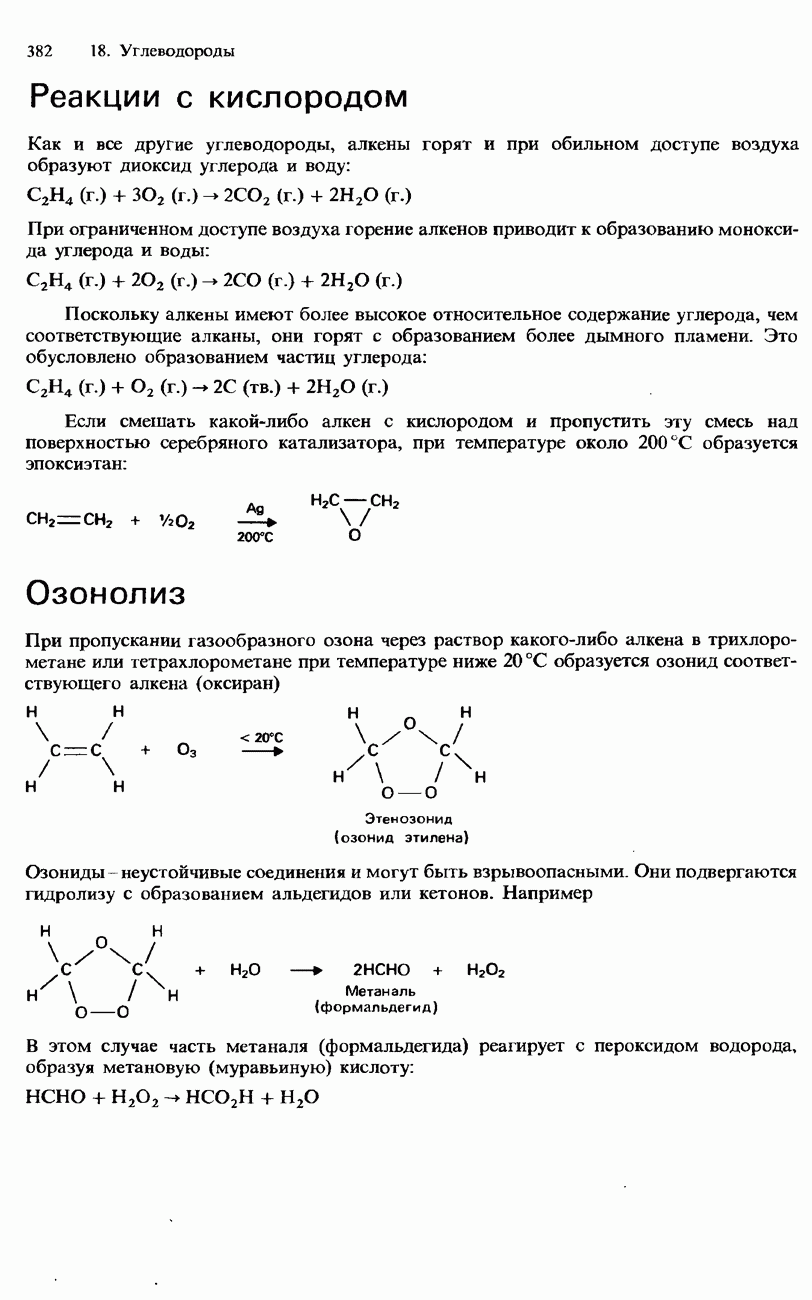
- АЛКЕНЫ
- АЛКИНЫ
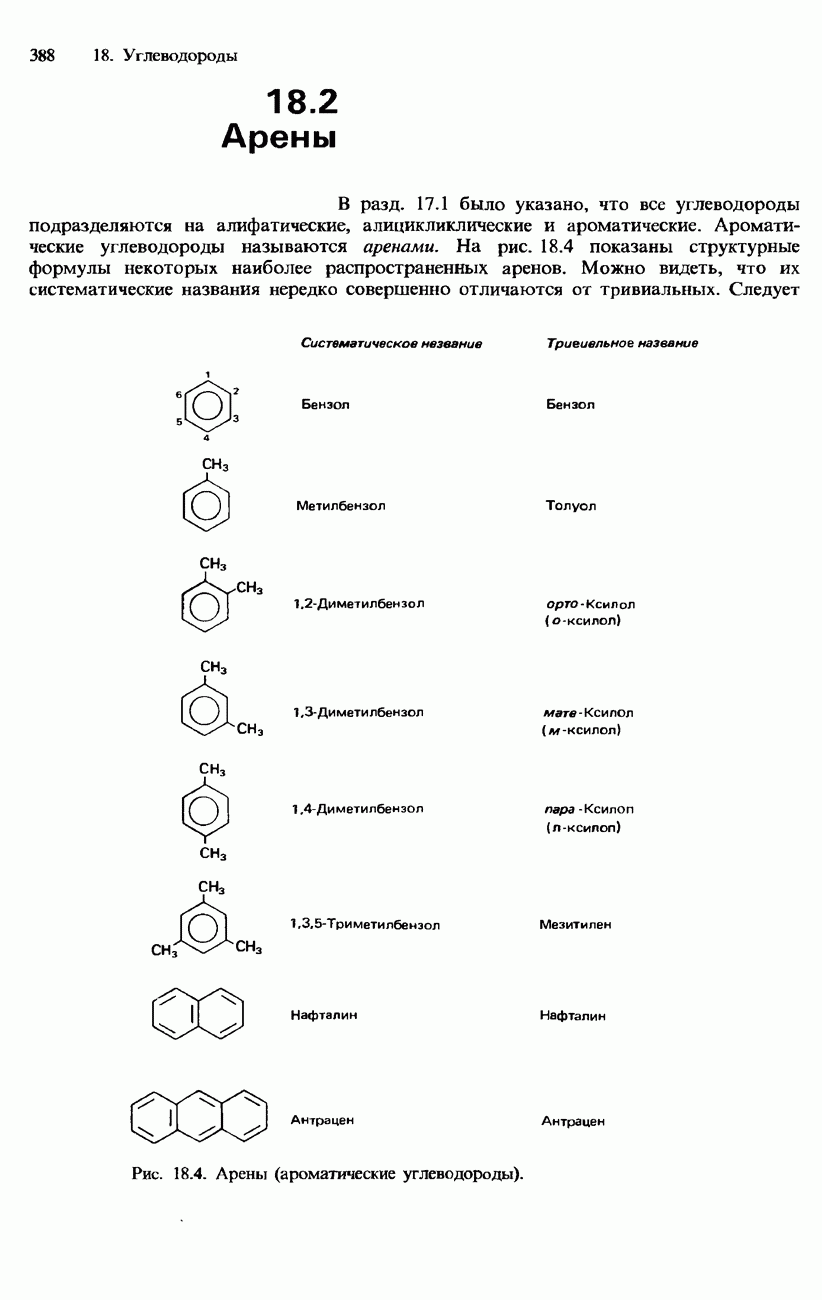
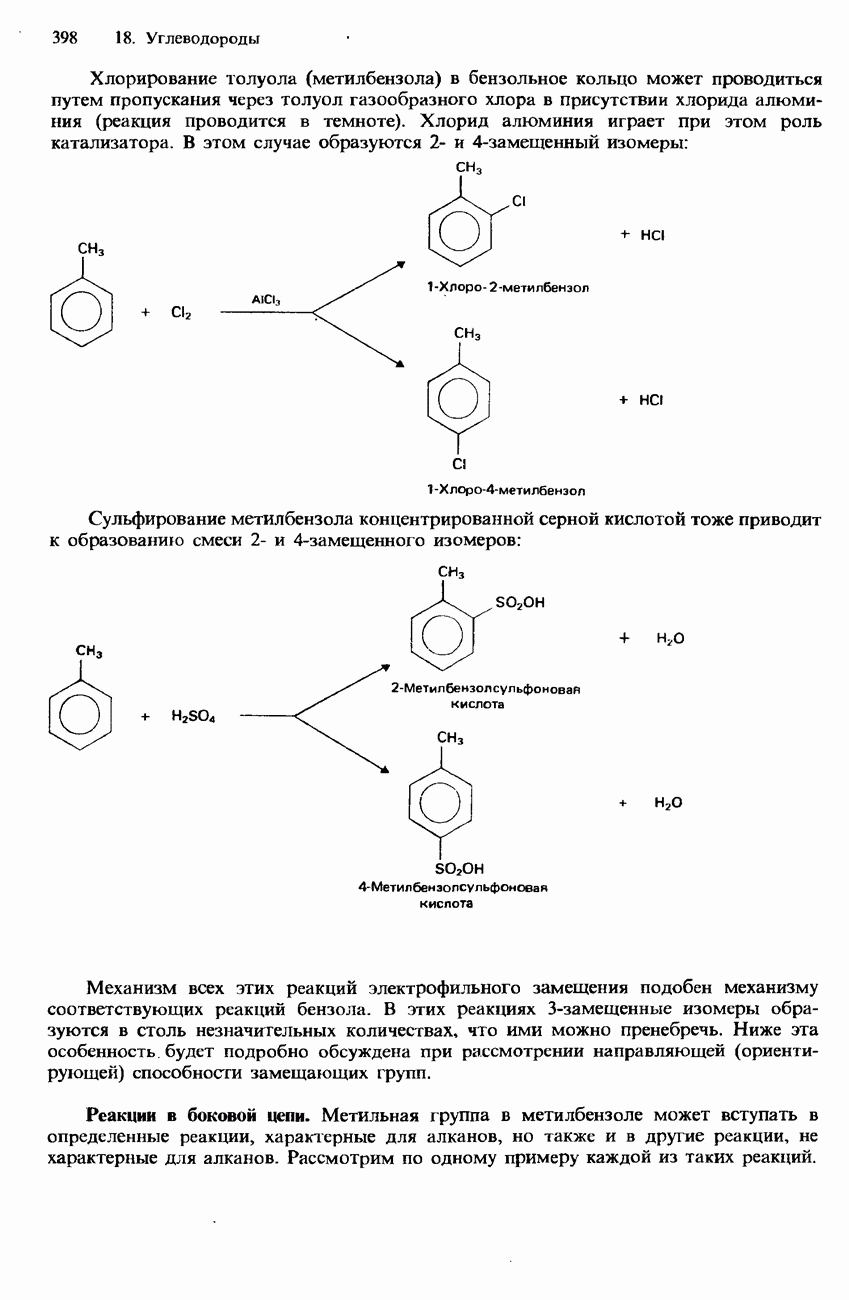
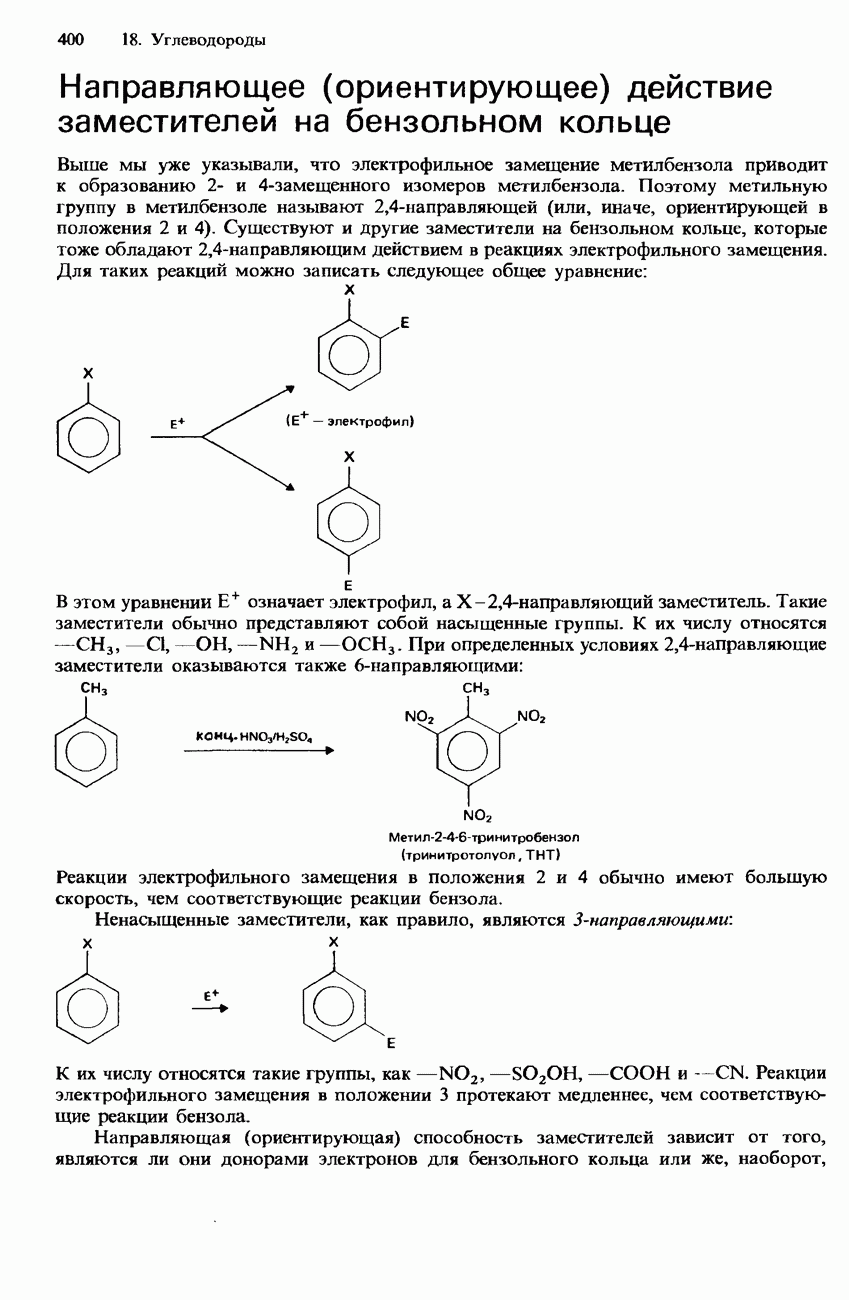
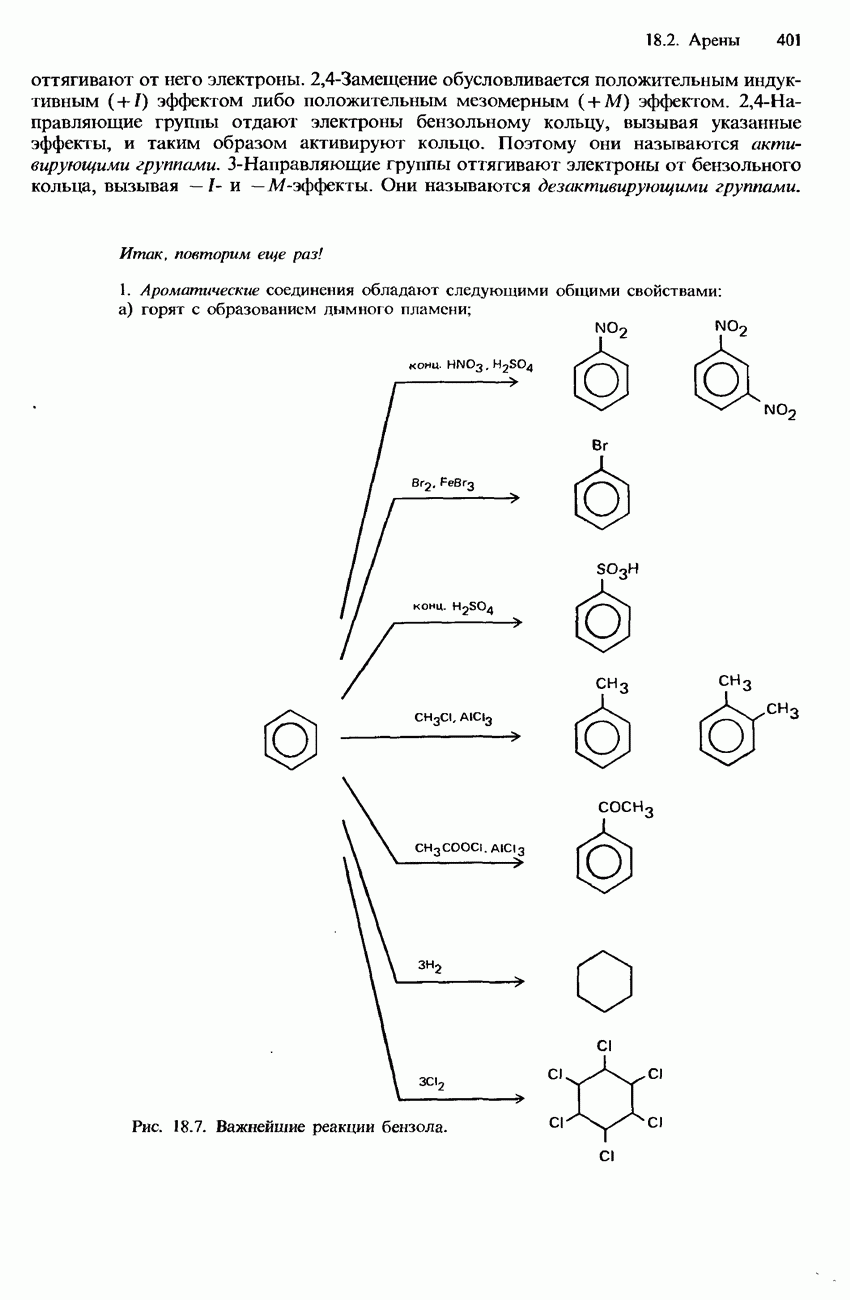
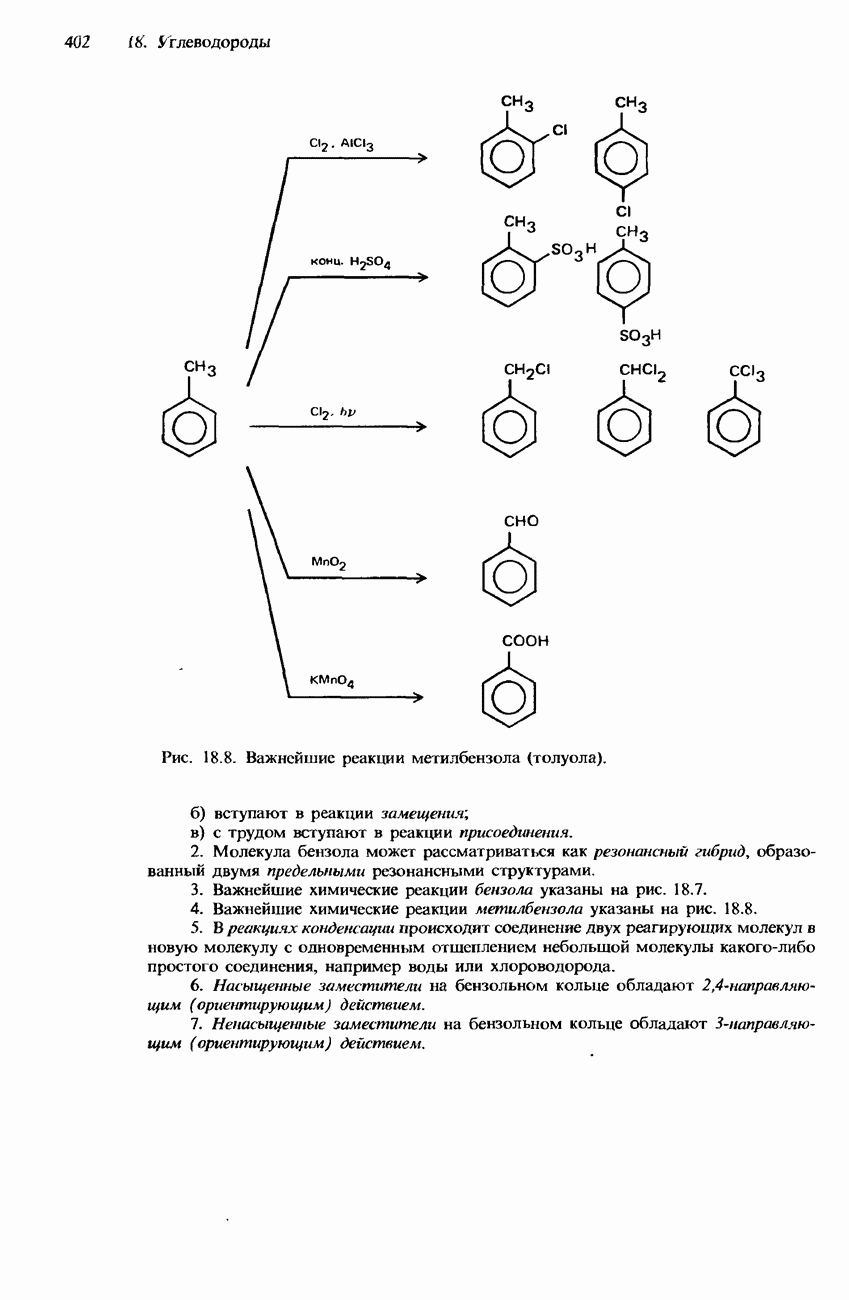
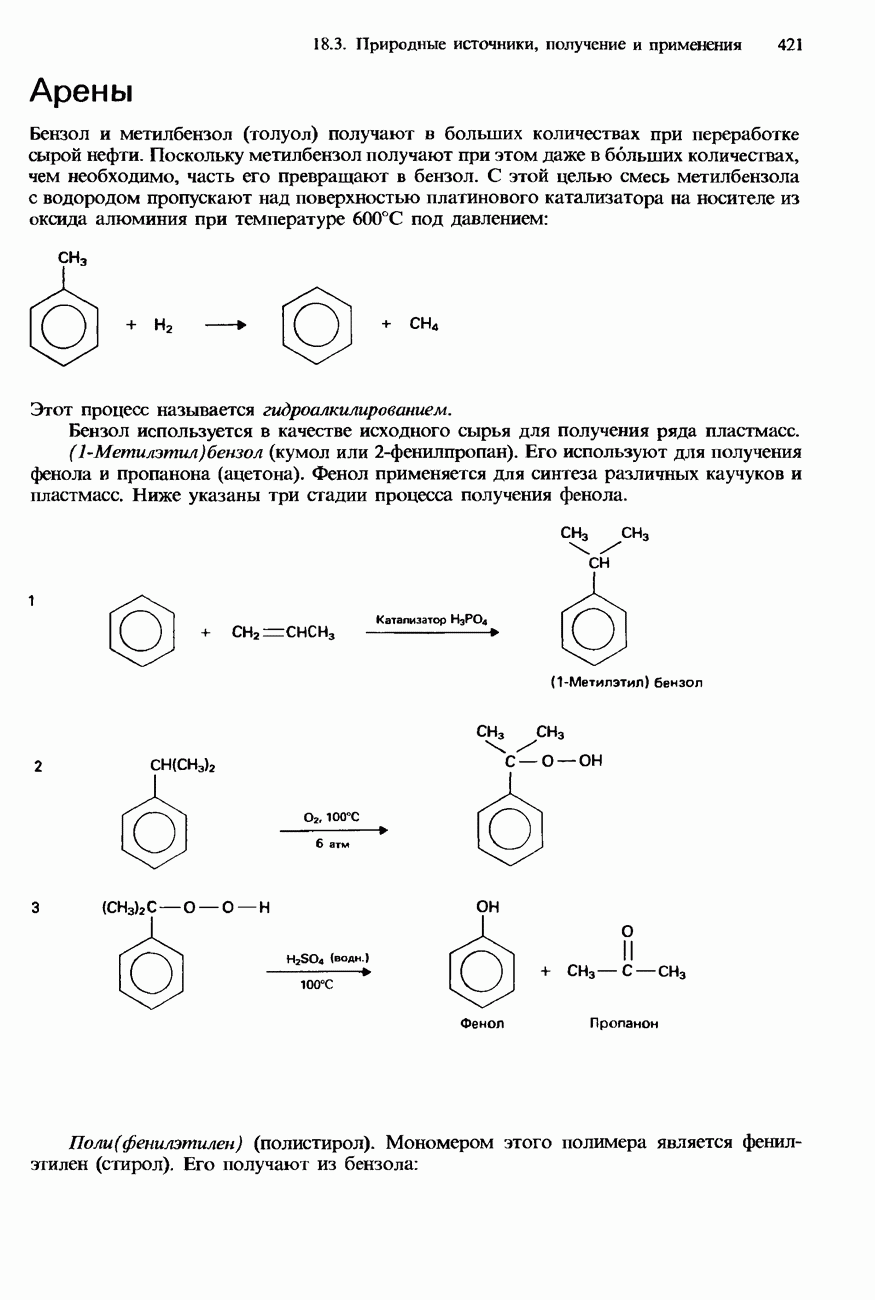
- 18.2. Арены
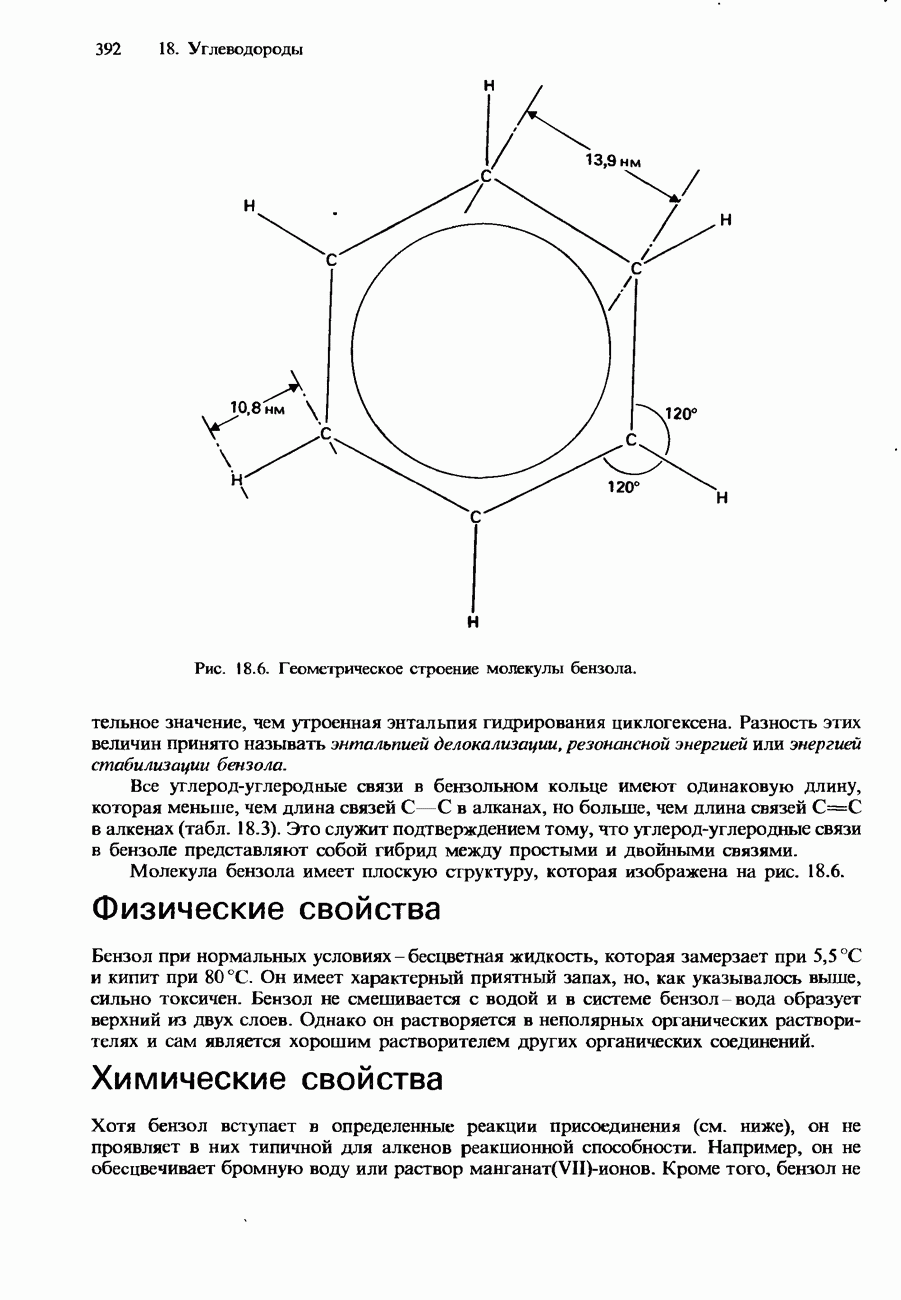
- БЕНЗОЛ
- МЕТИЛБЕНЗОЛ
- 18.3. Природные источники, получение и применения
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ УГЛЕВОДОРОДОВ
- ПЕРЕРАБОТКА НЕФТИ
- ПРИМЕНЕНИЯ УГЛЕВОДОРОДОВ
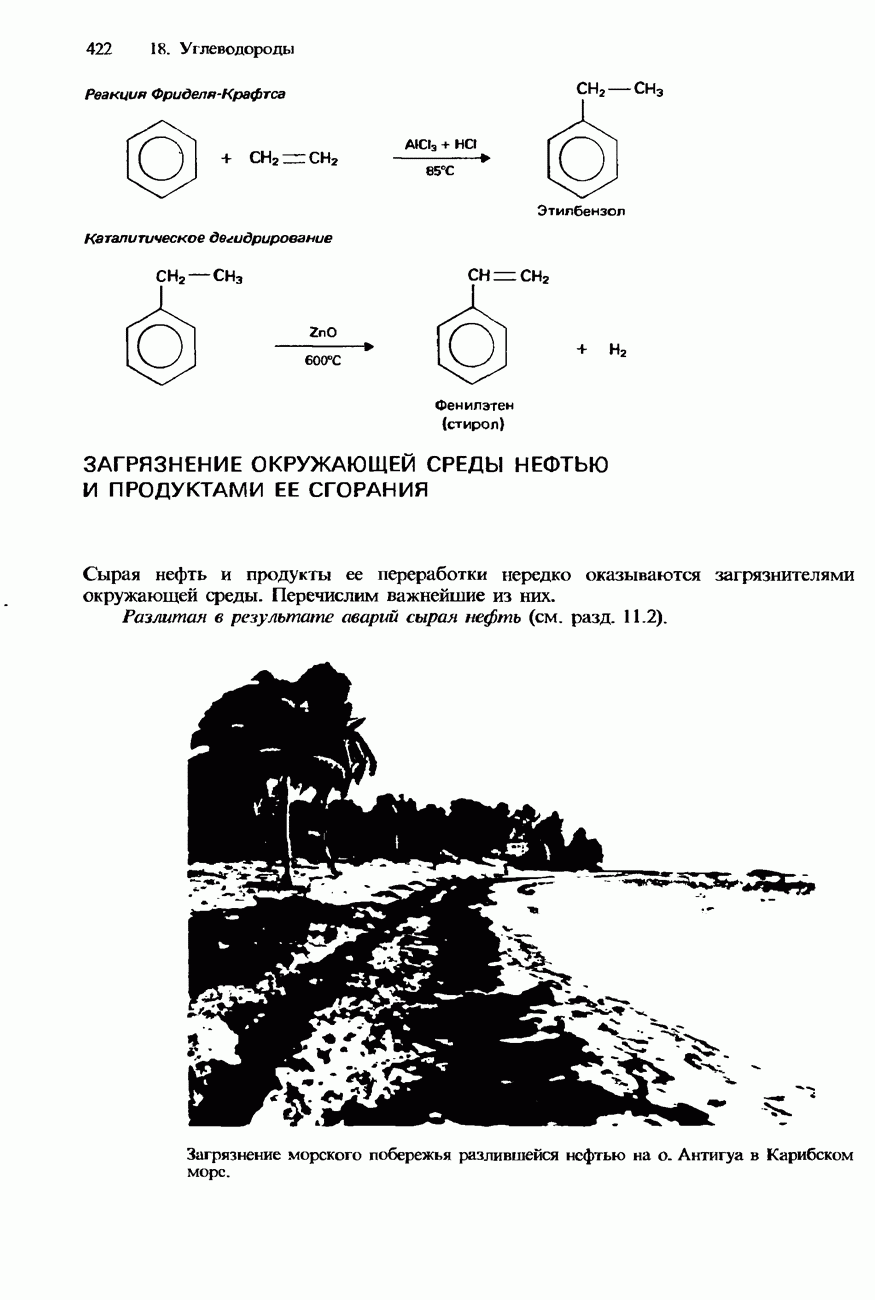
- ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ НЕФТЬЮ И ПРОДУКТАМИ ЕЕ СГОРАНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 19. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
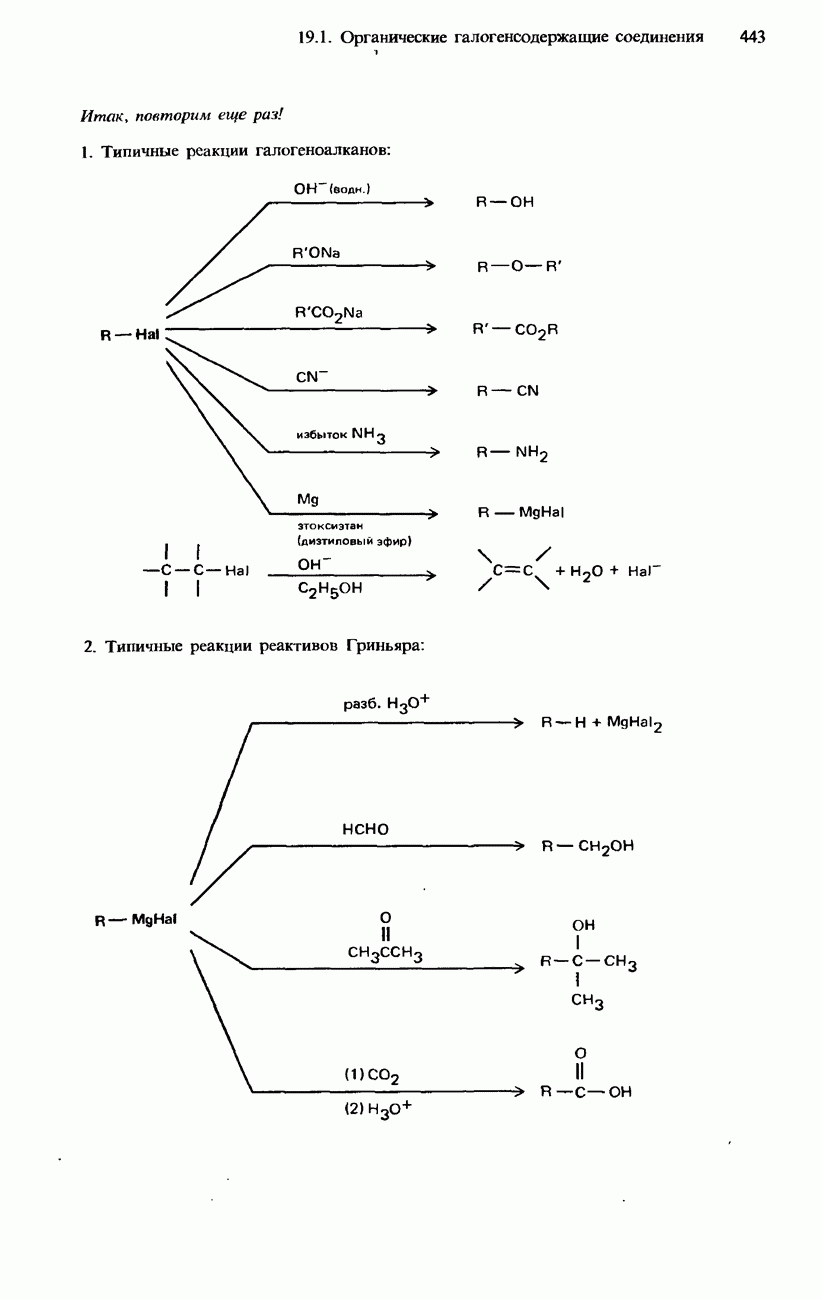
- 19.1. Органические галогенсодержащие соединения
- ГАЛОГЕНОАЛКЕНЫ
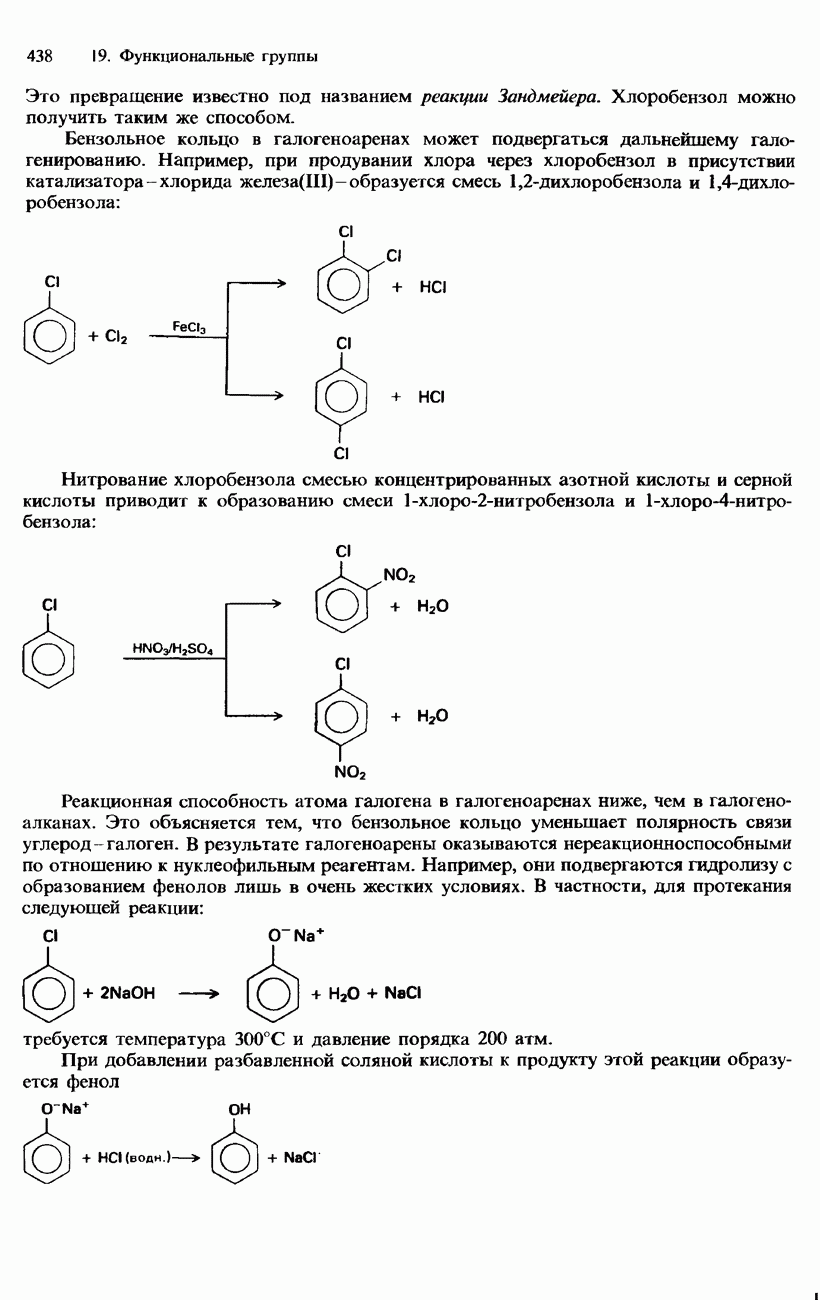
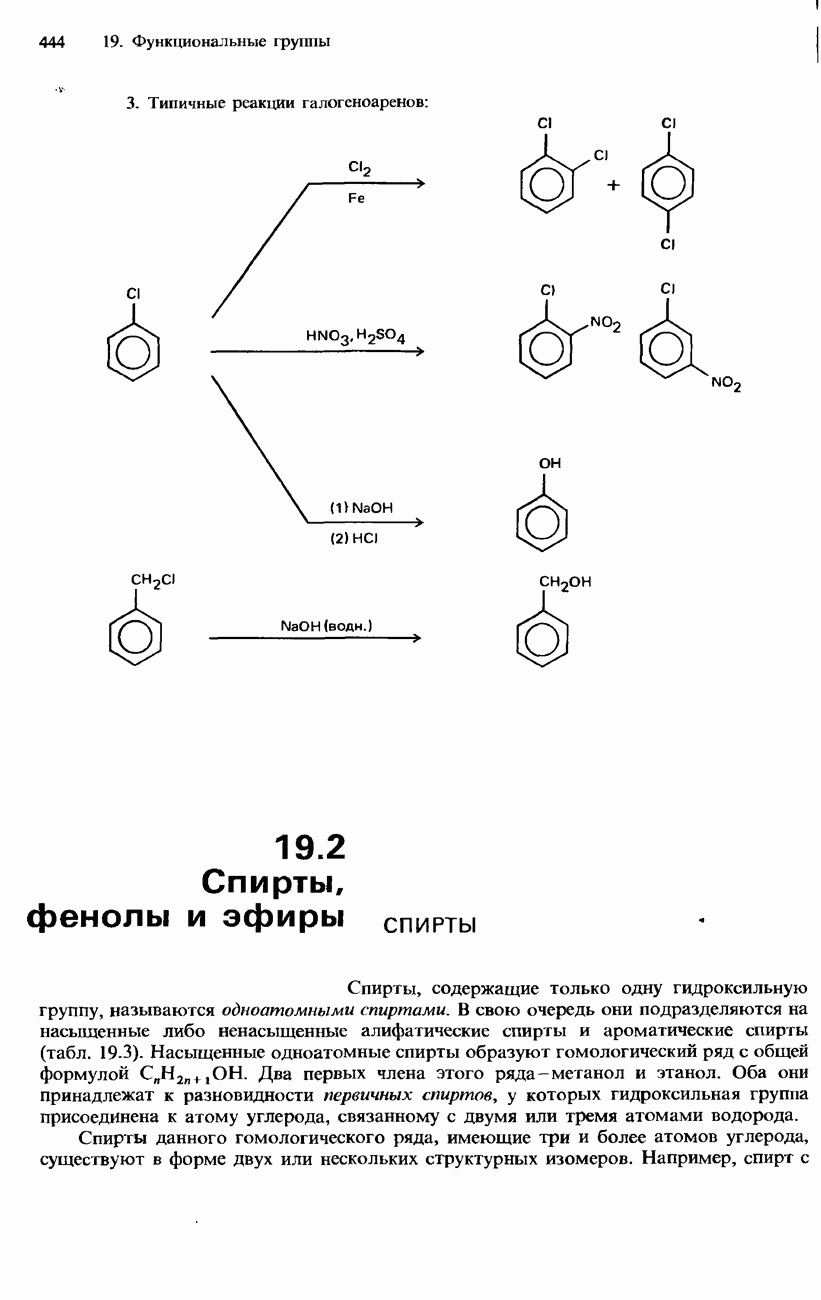
- ГАЛОГЕНОАРЕНЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ОРГАНИЧЕСКИХ ГАЛОГЕНСОДЕРЖАЩИХ СОЕДИНЕНИЙ
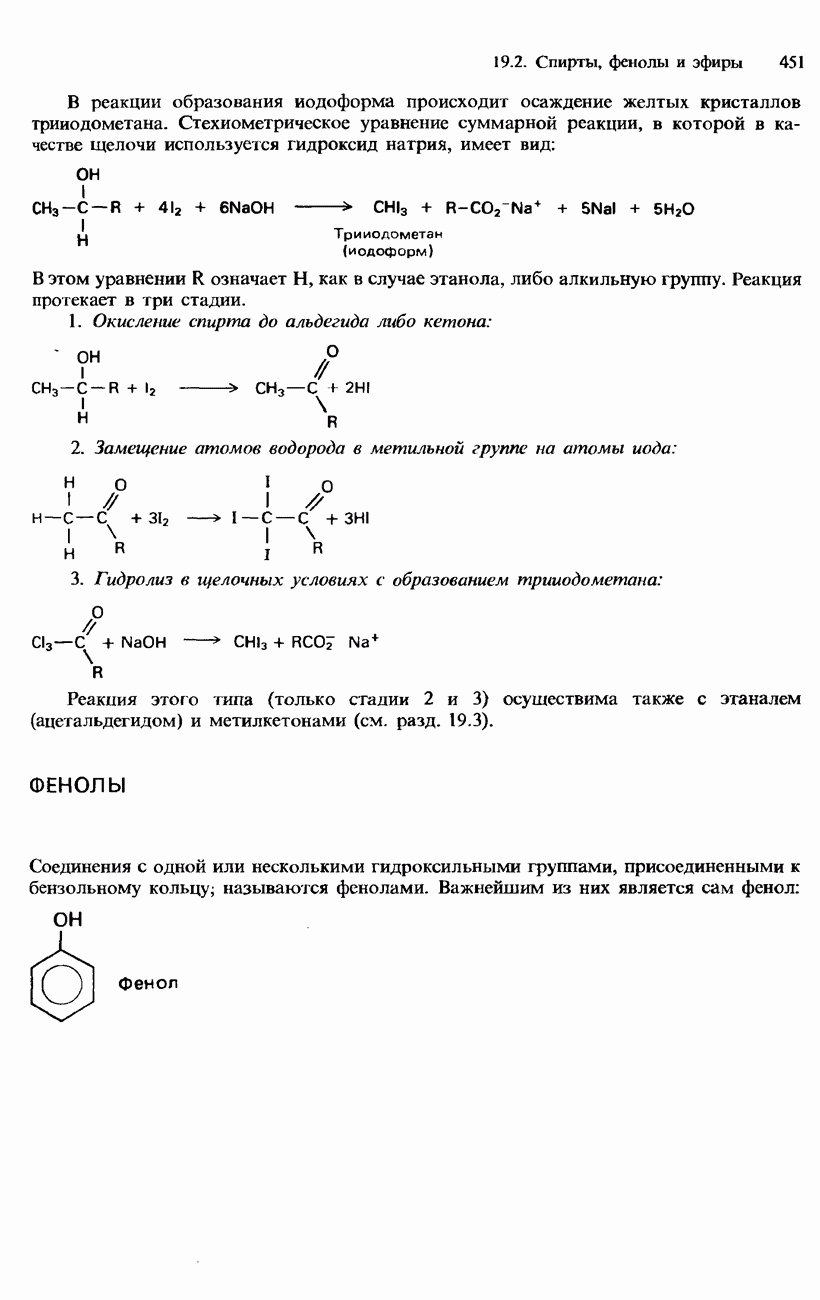
- 19.2. Спирты, фенолы и эфиры
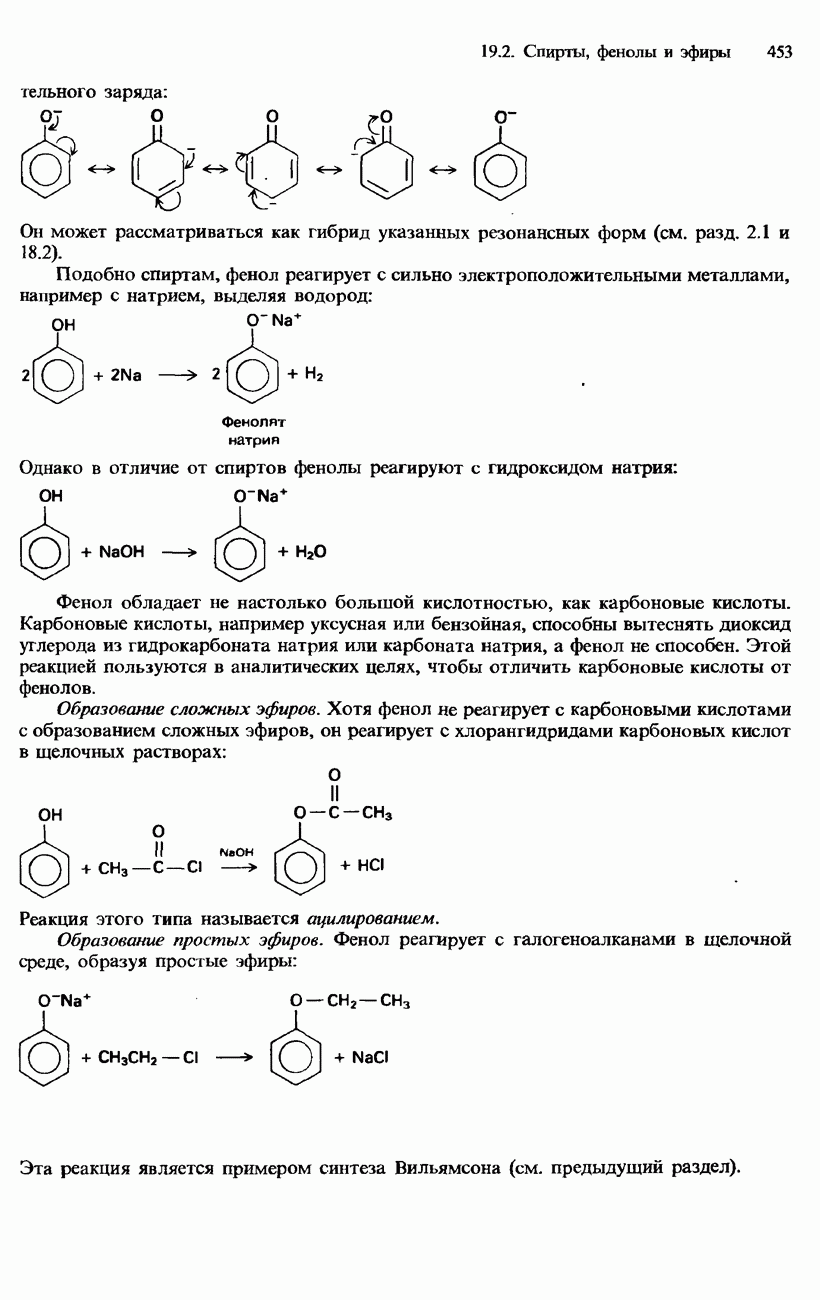
- ФЕНОЛЫ
- ПРОСТЫЕ ЭФИРЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ СПИРТОВ, ФЕНОЛОВ И ПРОСТЫХ ЭФИРОВ
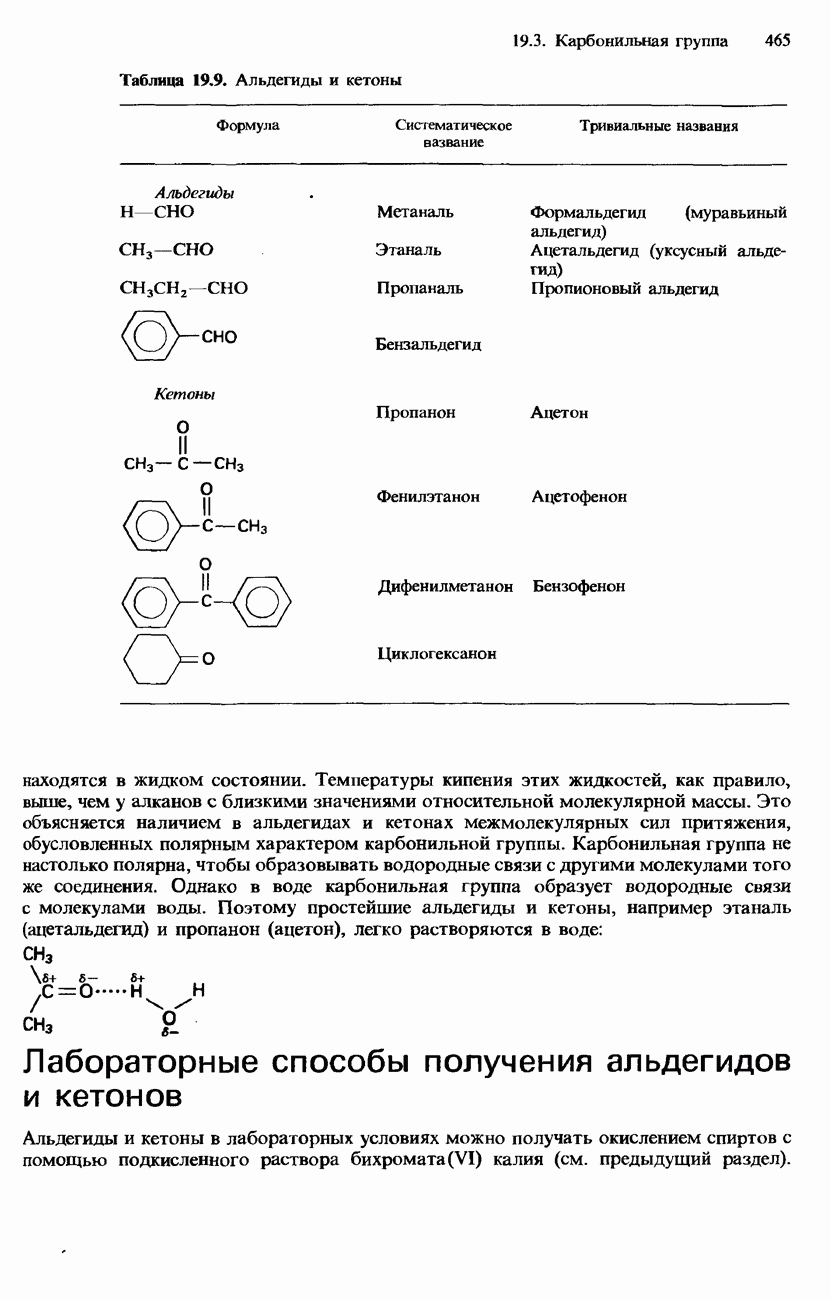
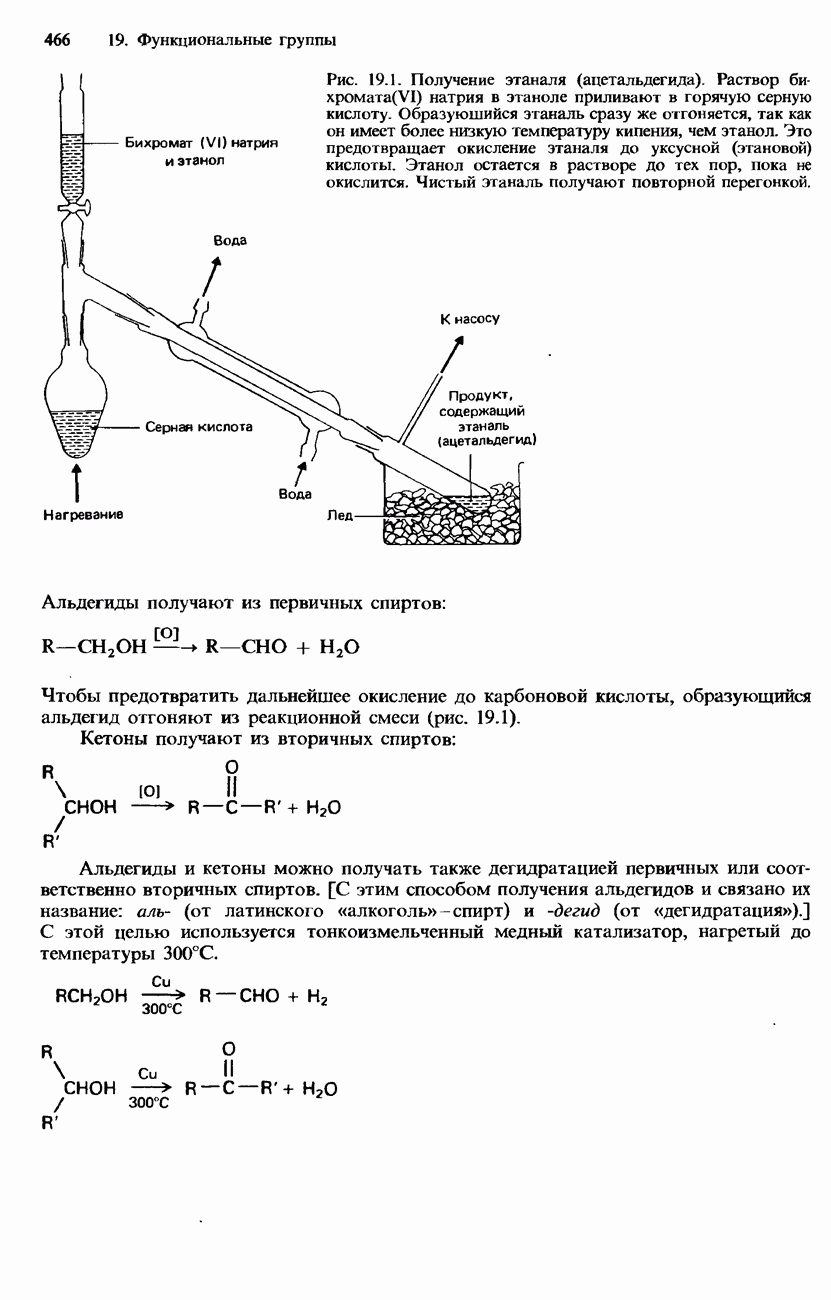
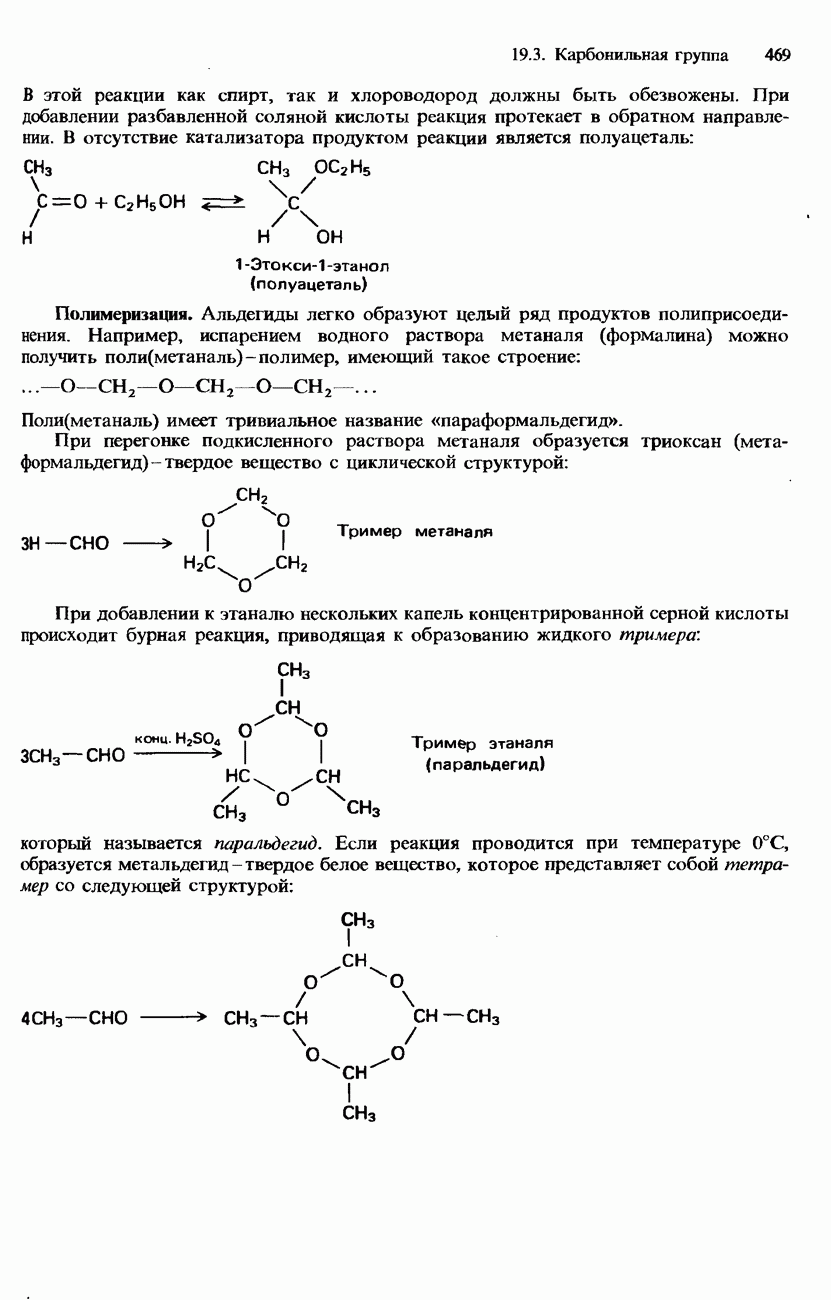
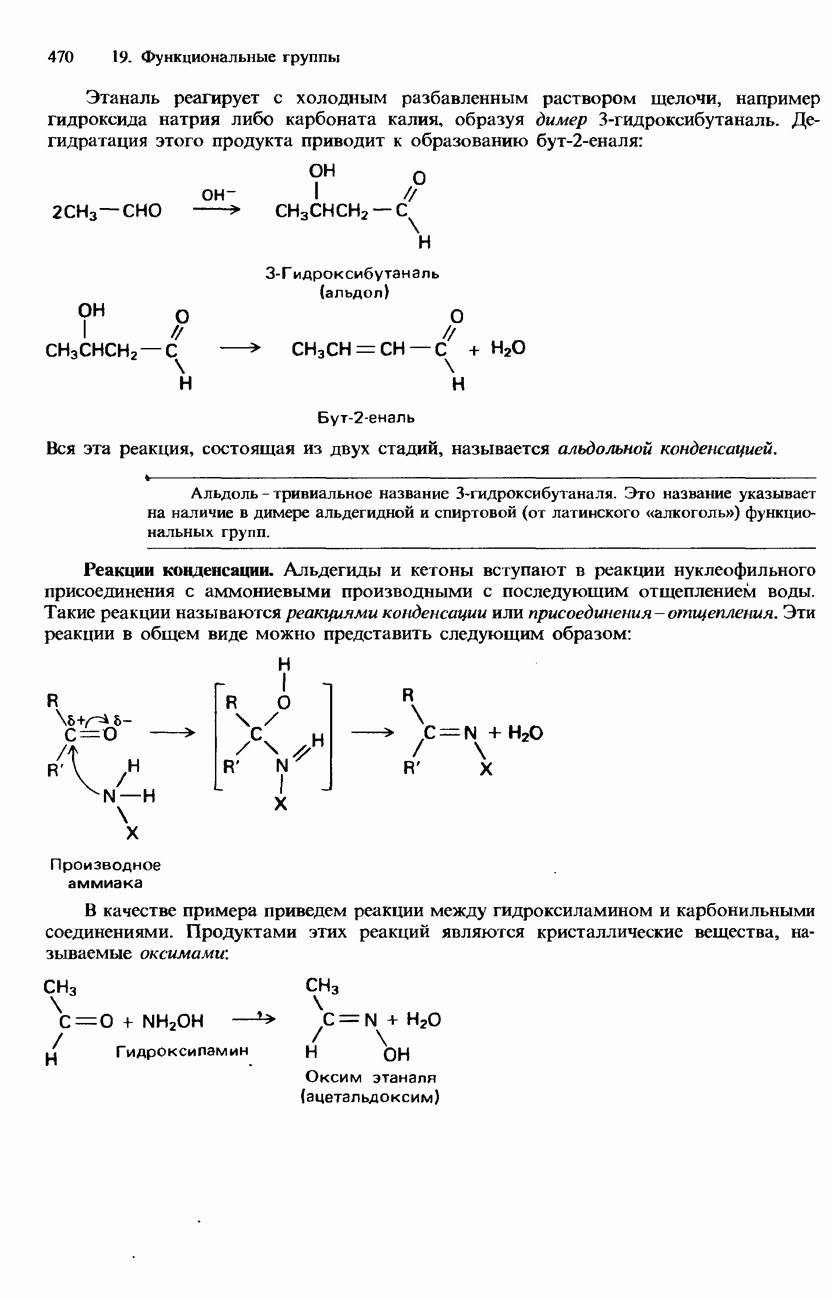
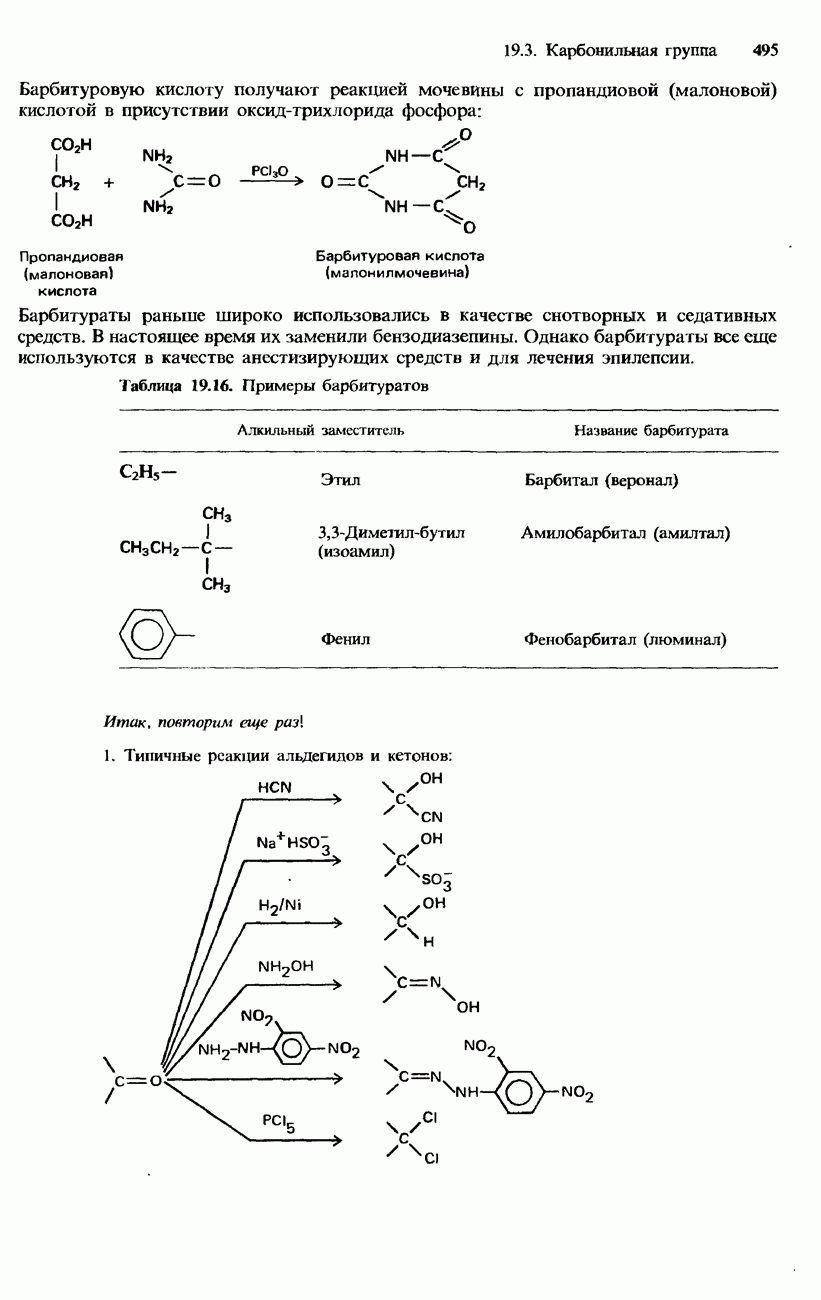
- 19.3. Карбонильная группа
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
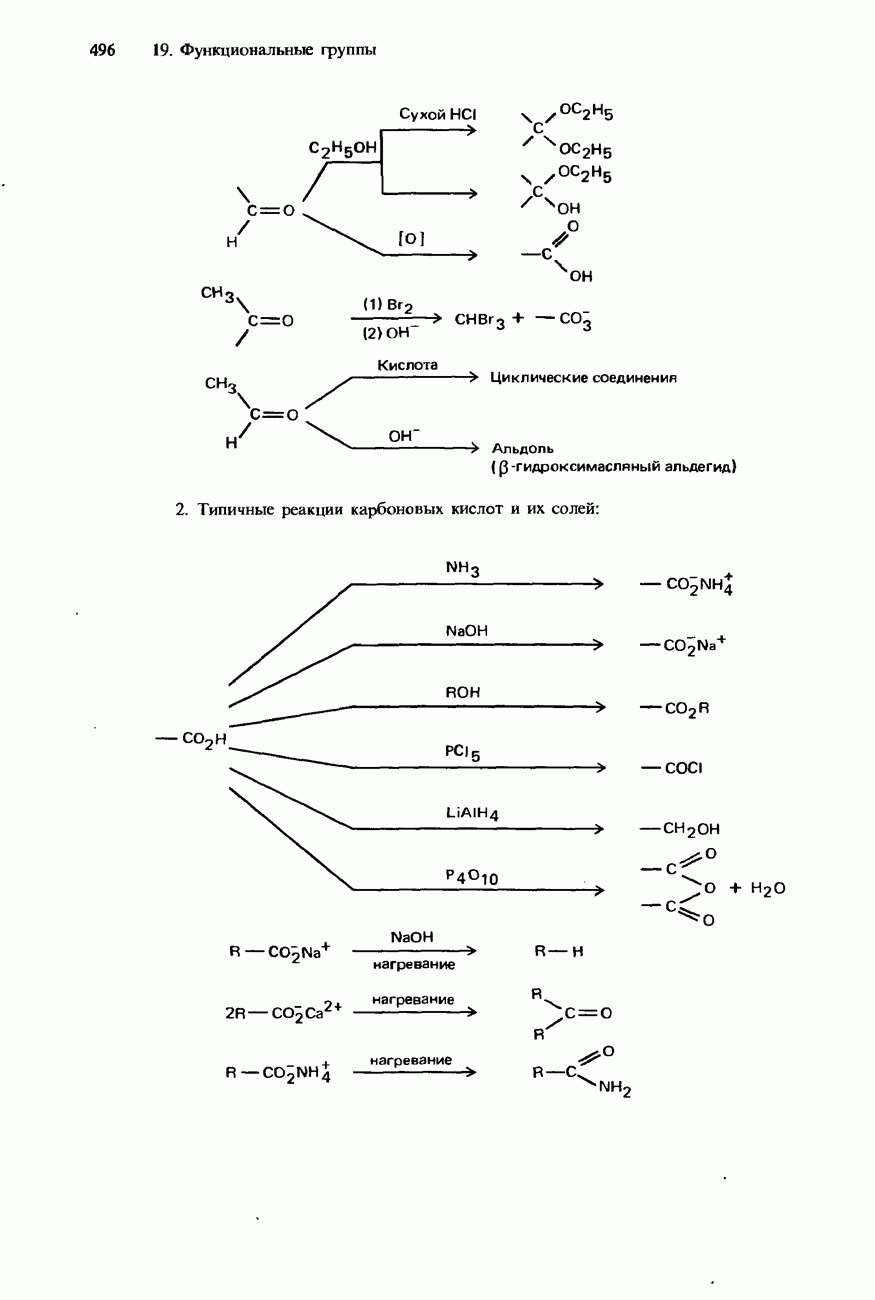
- КАРБОНОВЫЕ КИСЛОТЫ
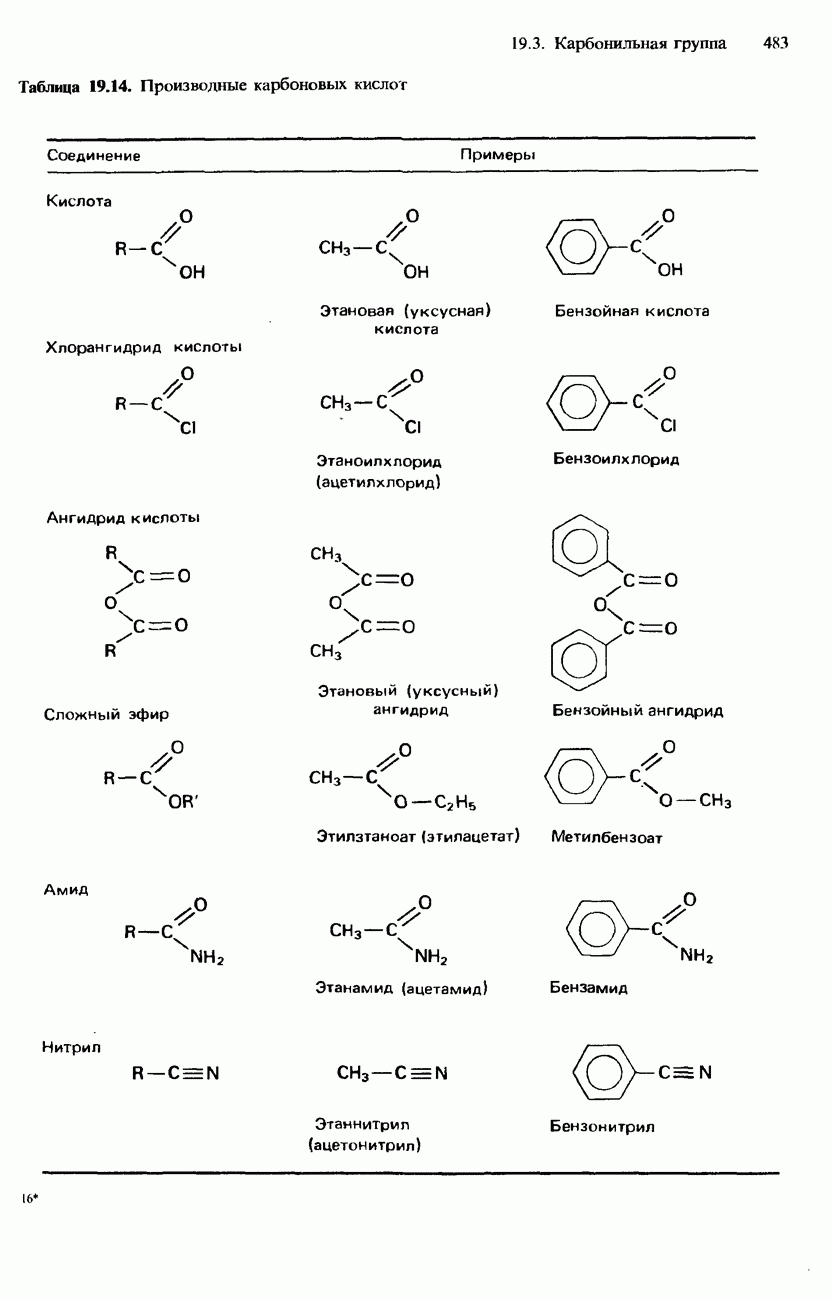
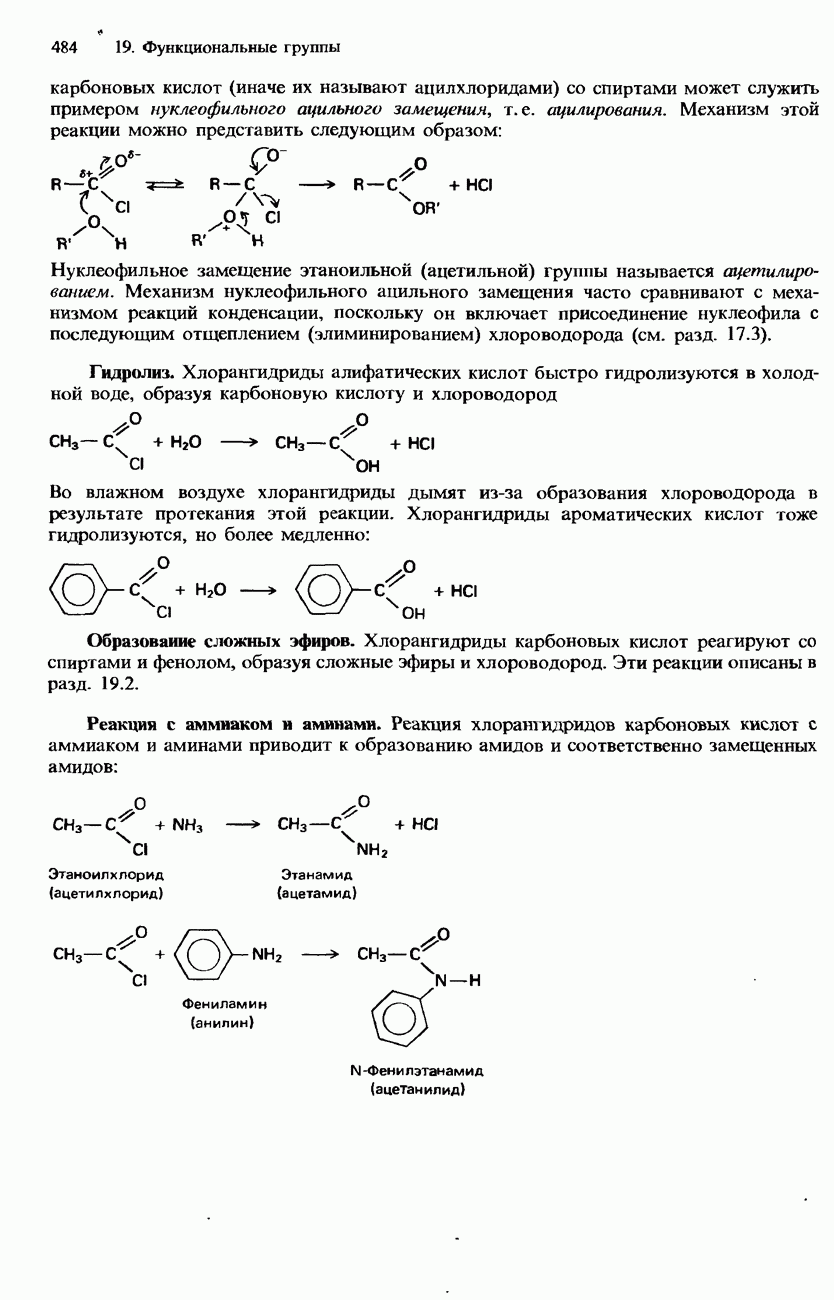
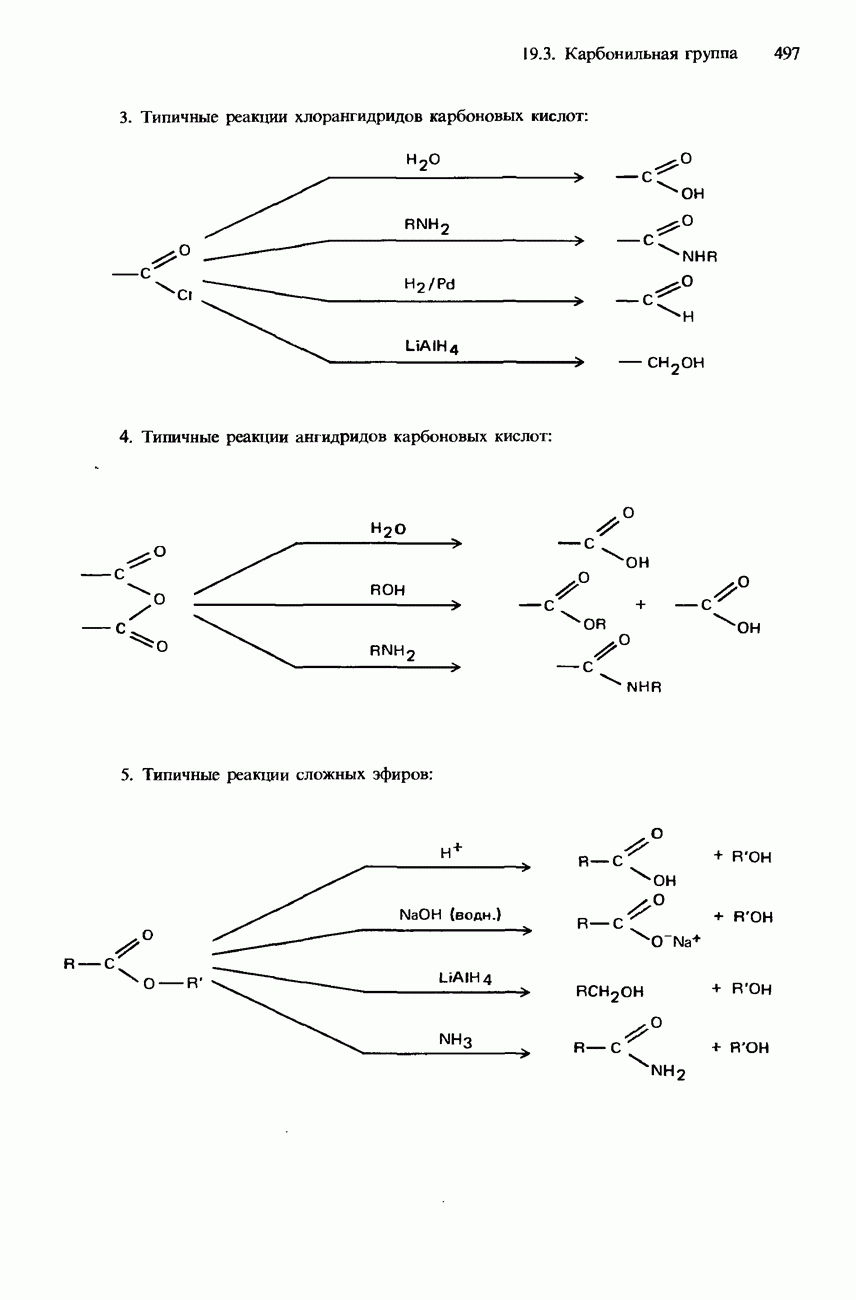
- ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
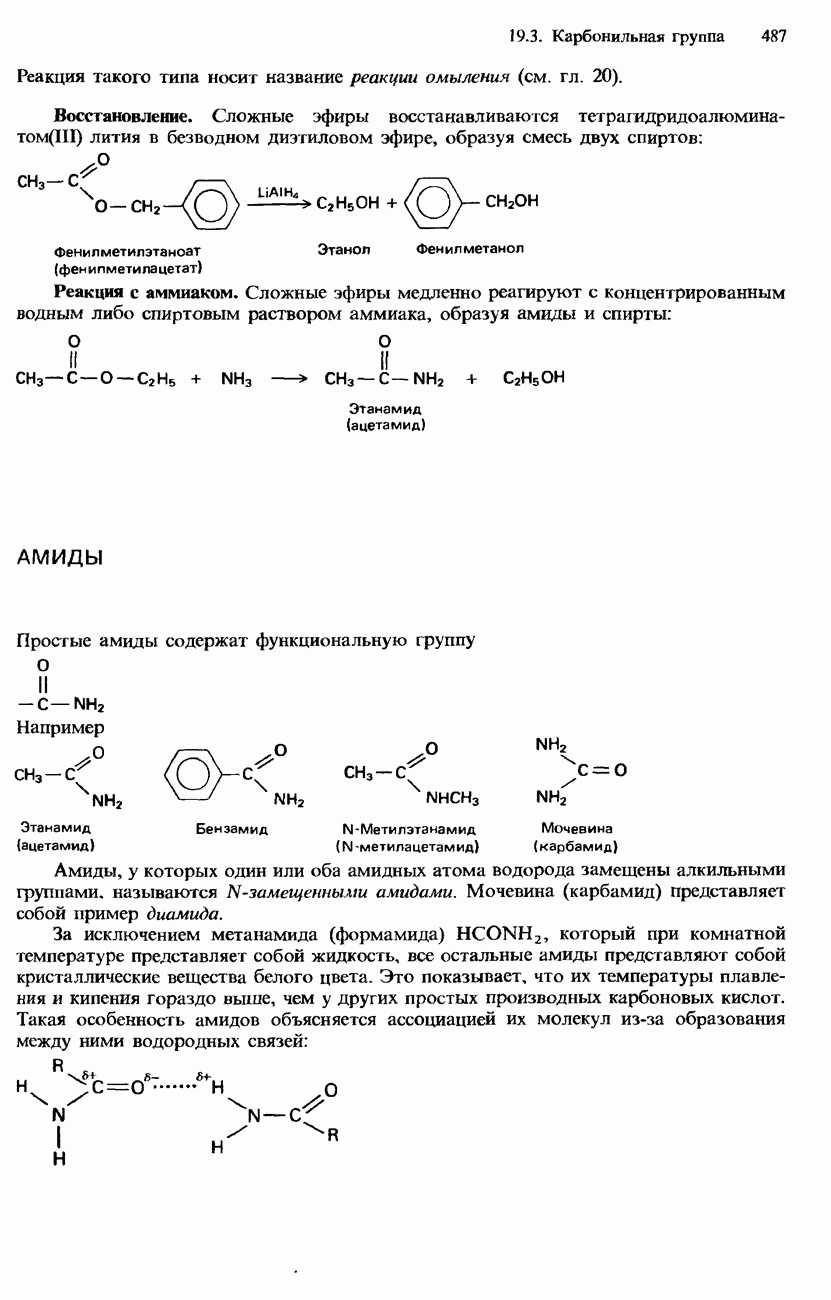
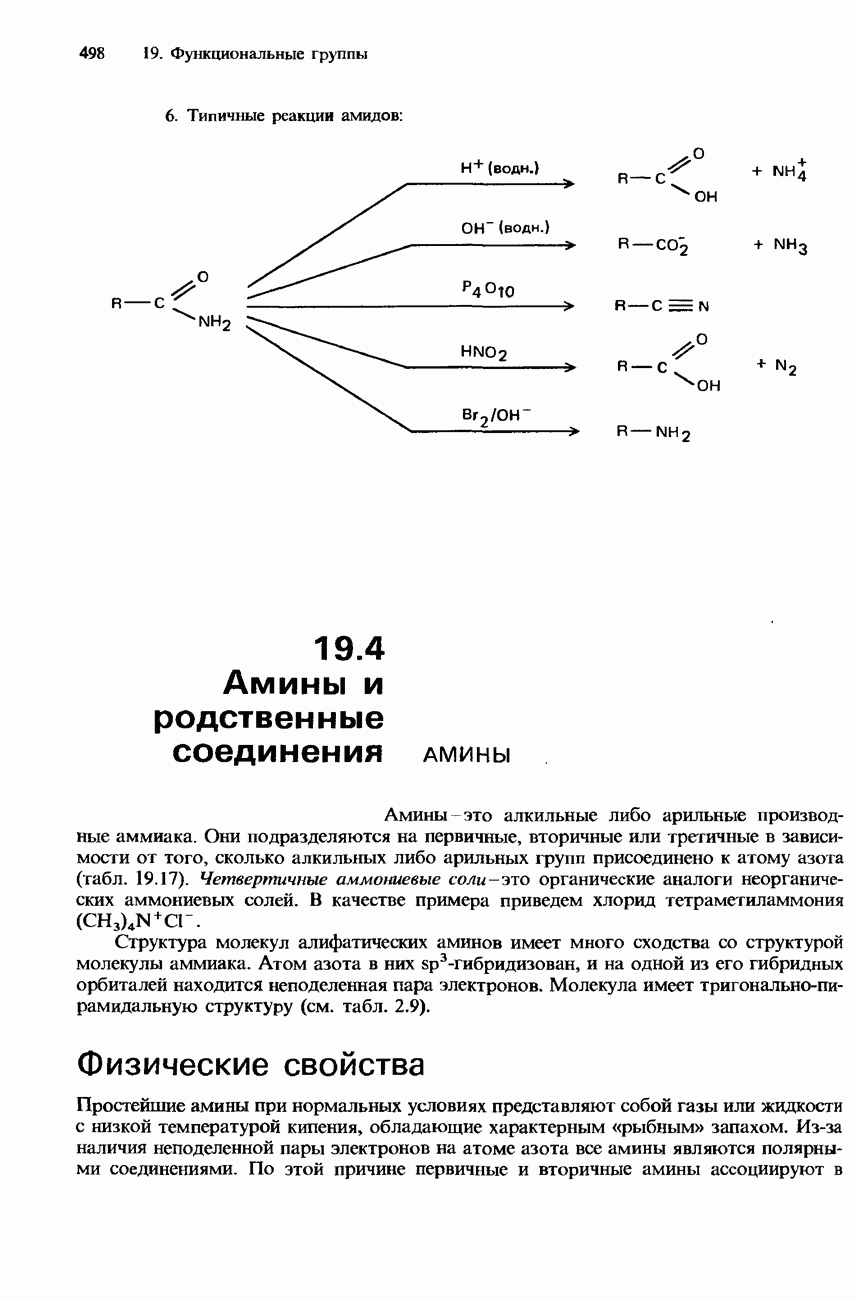
- АМИДЫ
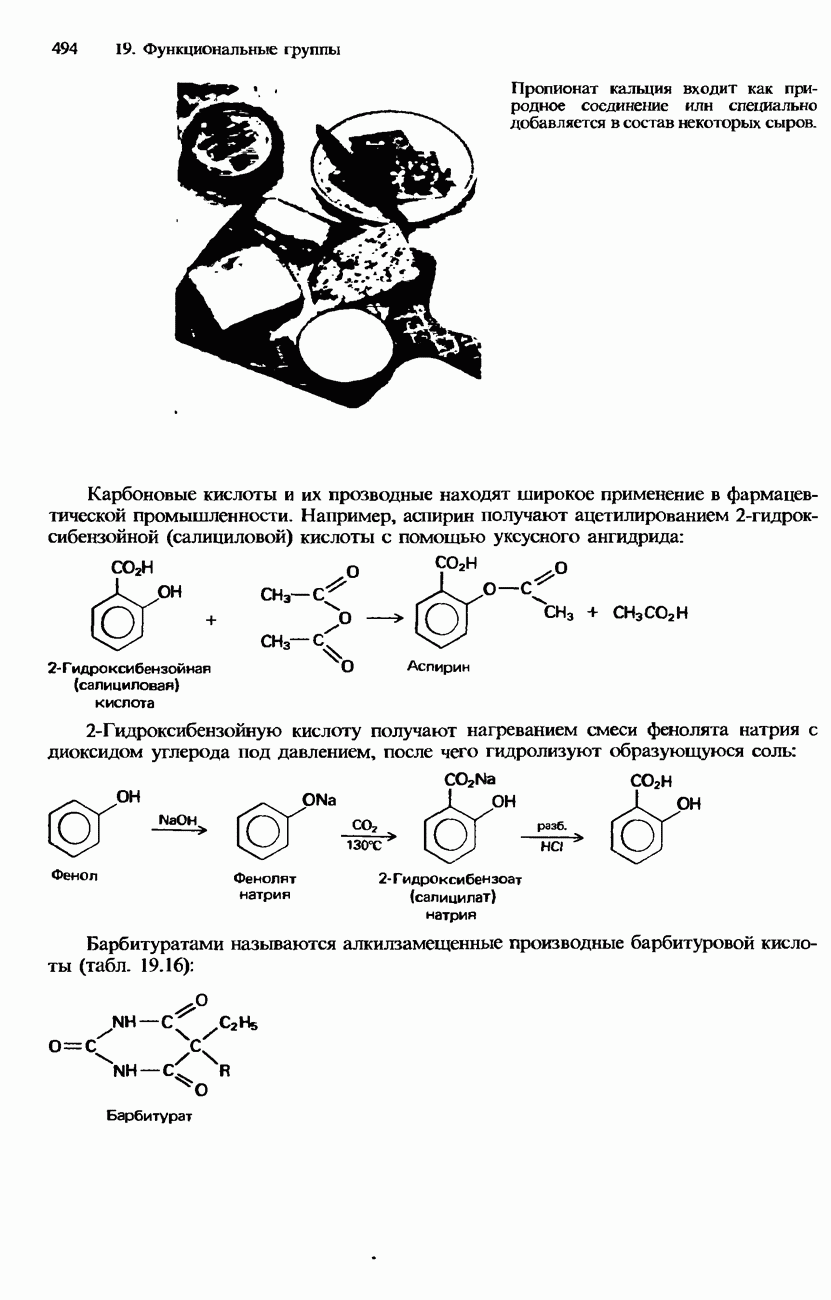
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ И ИХ ПРОИЗВОДНЫХ
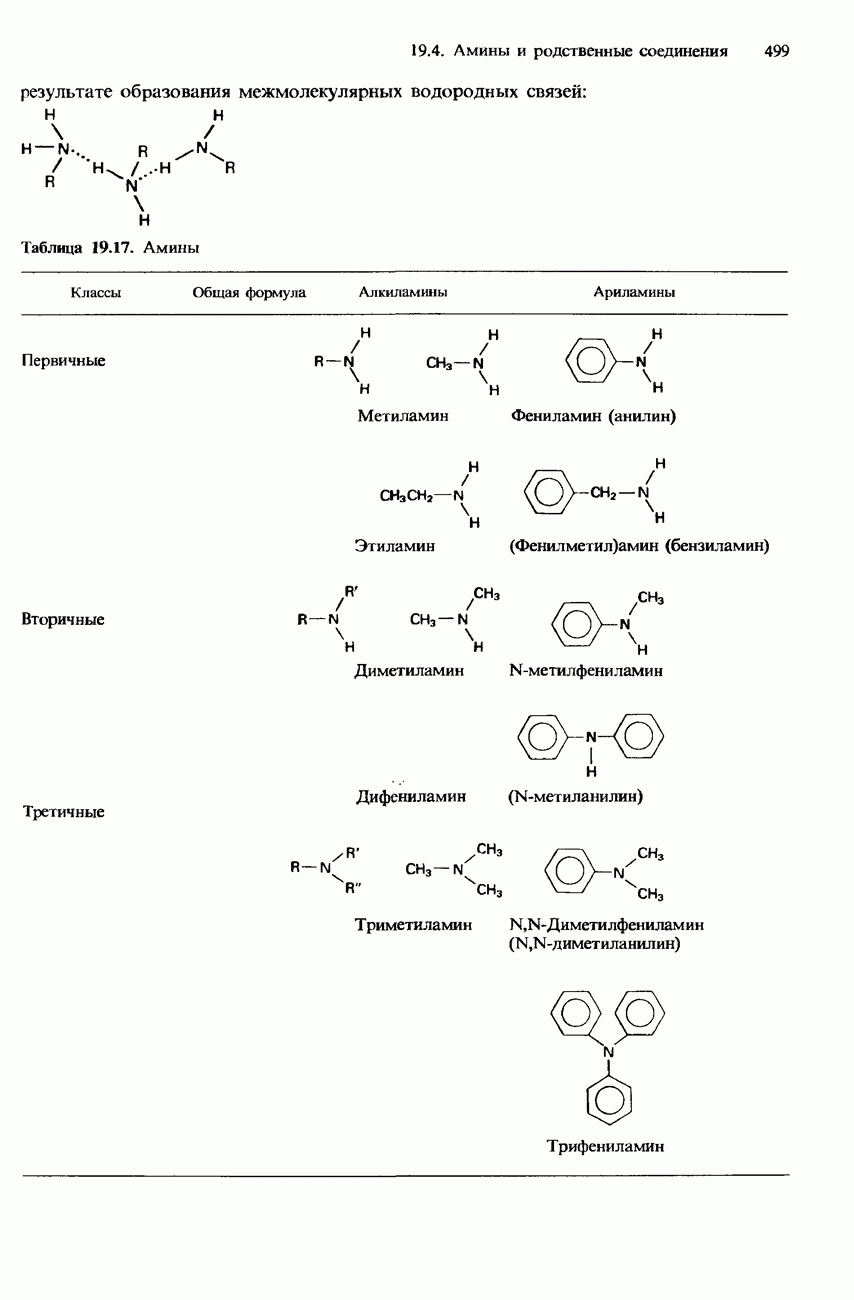
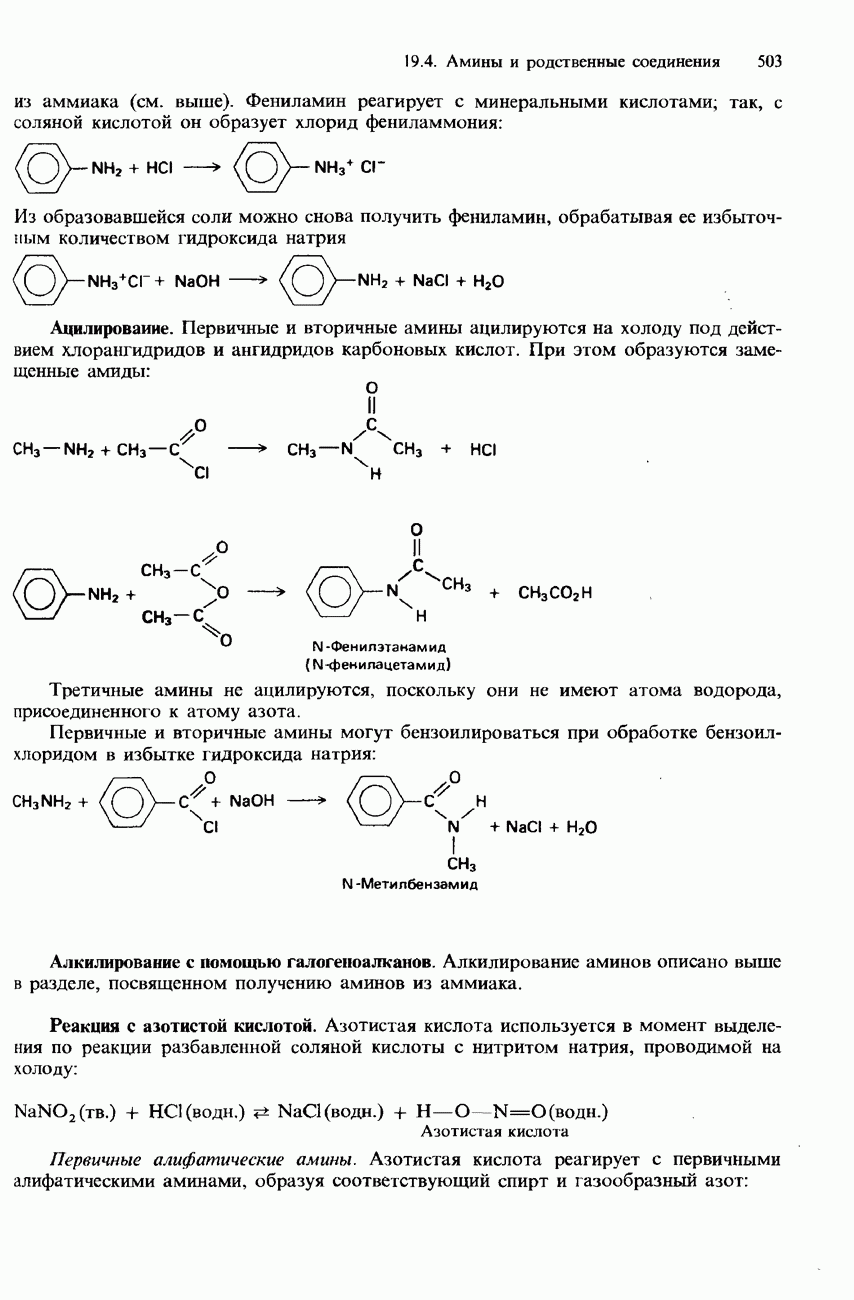
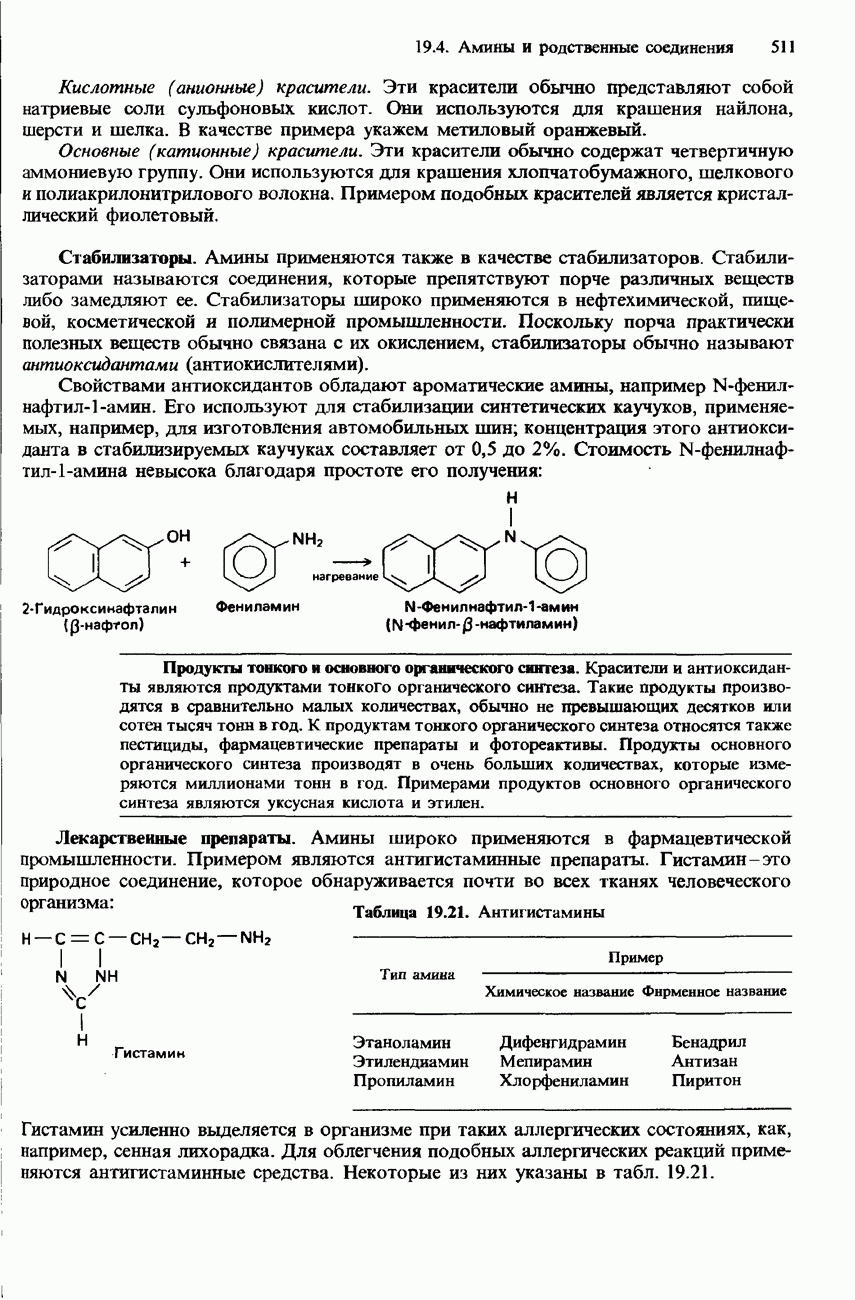
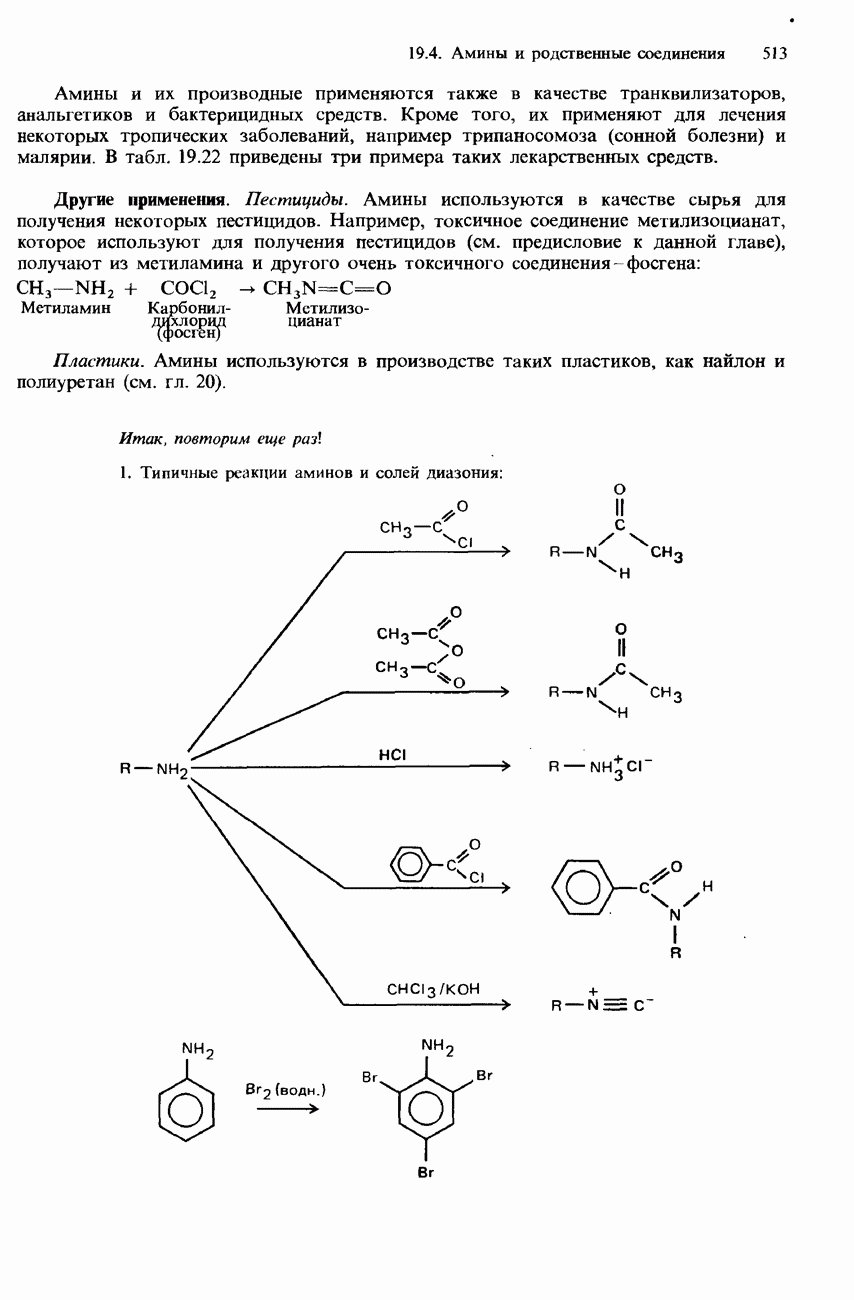
- 19.4 Амины и родственные соединения
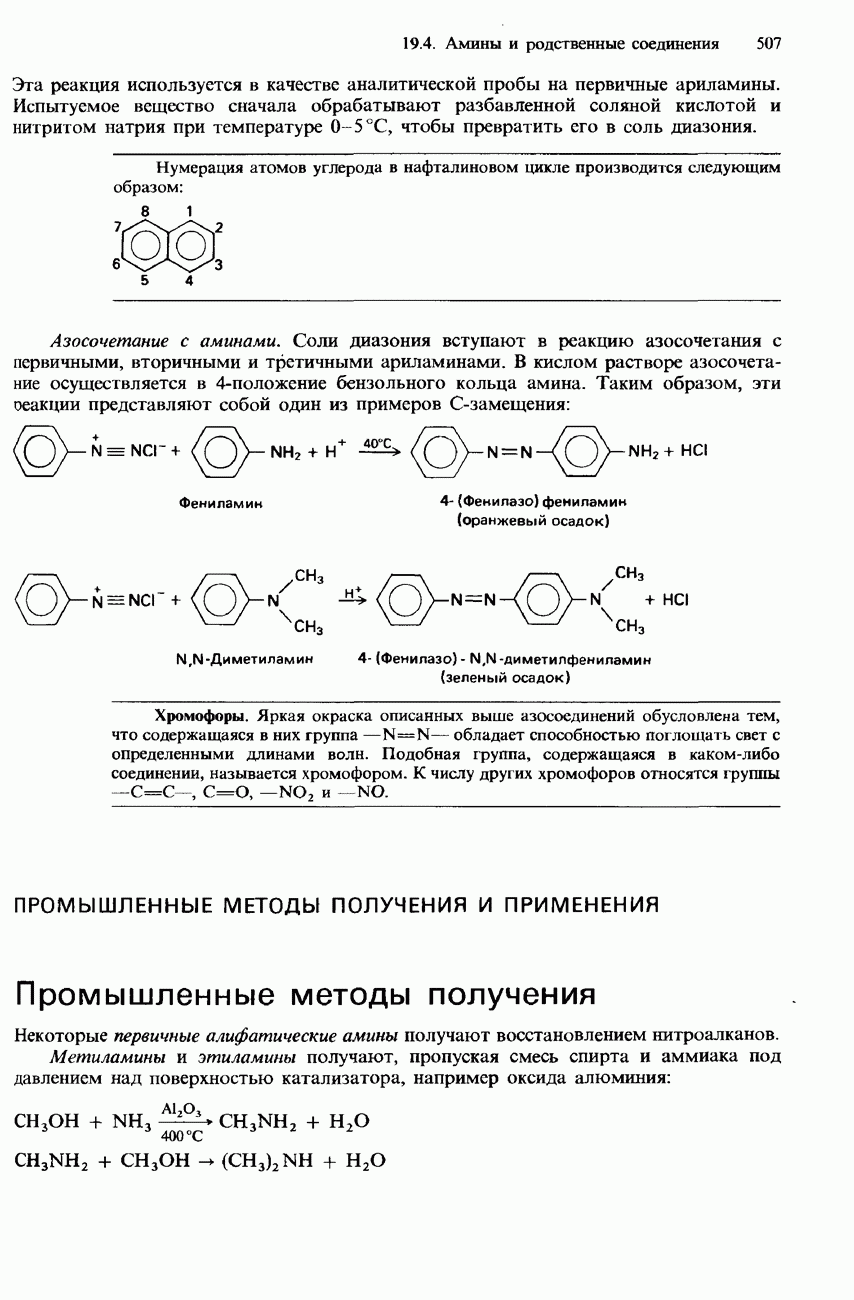
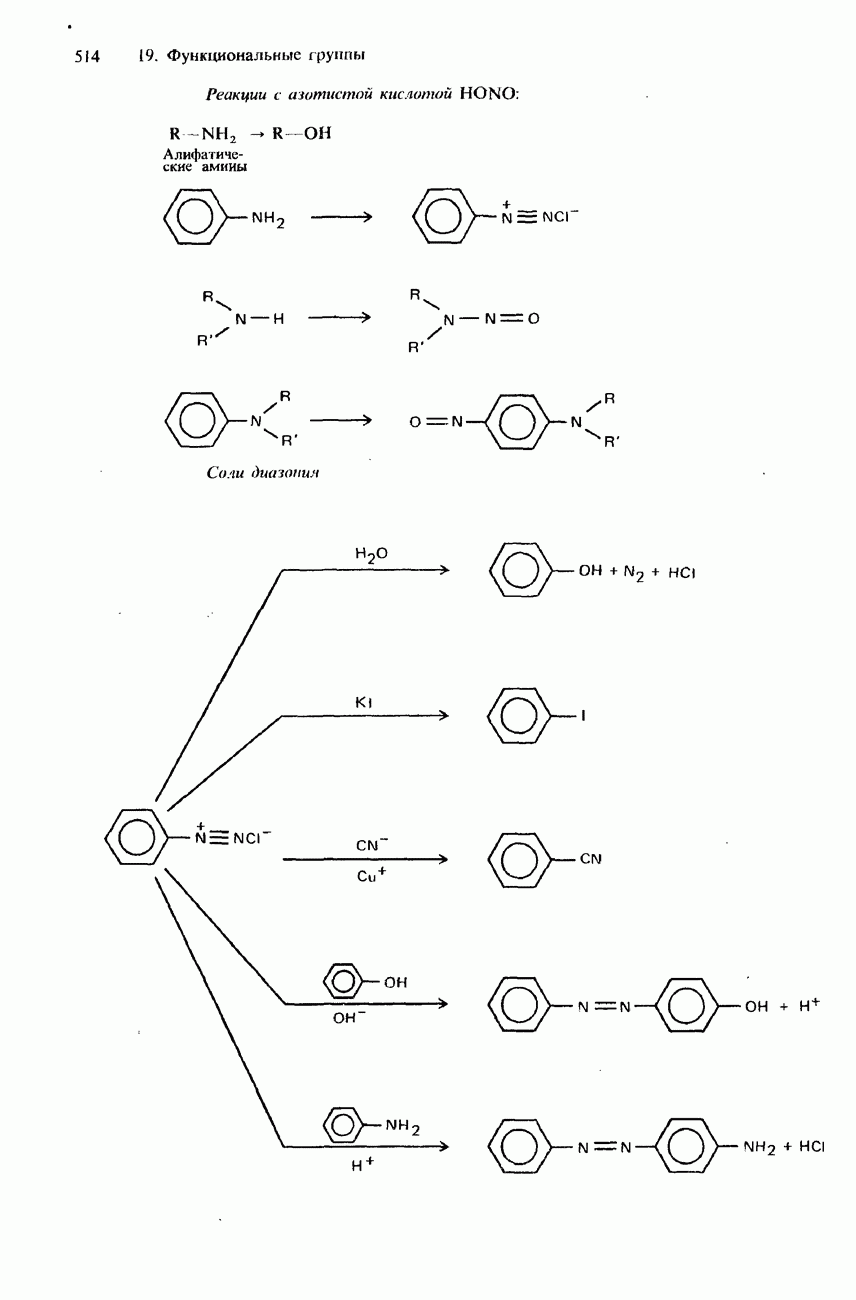
- СОЛИ ДИАЗОНИЯ
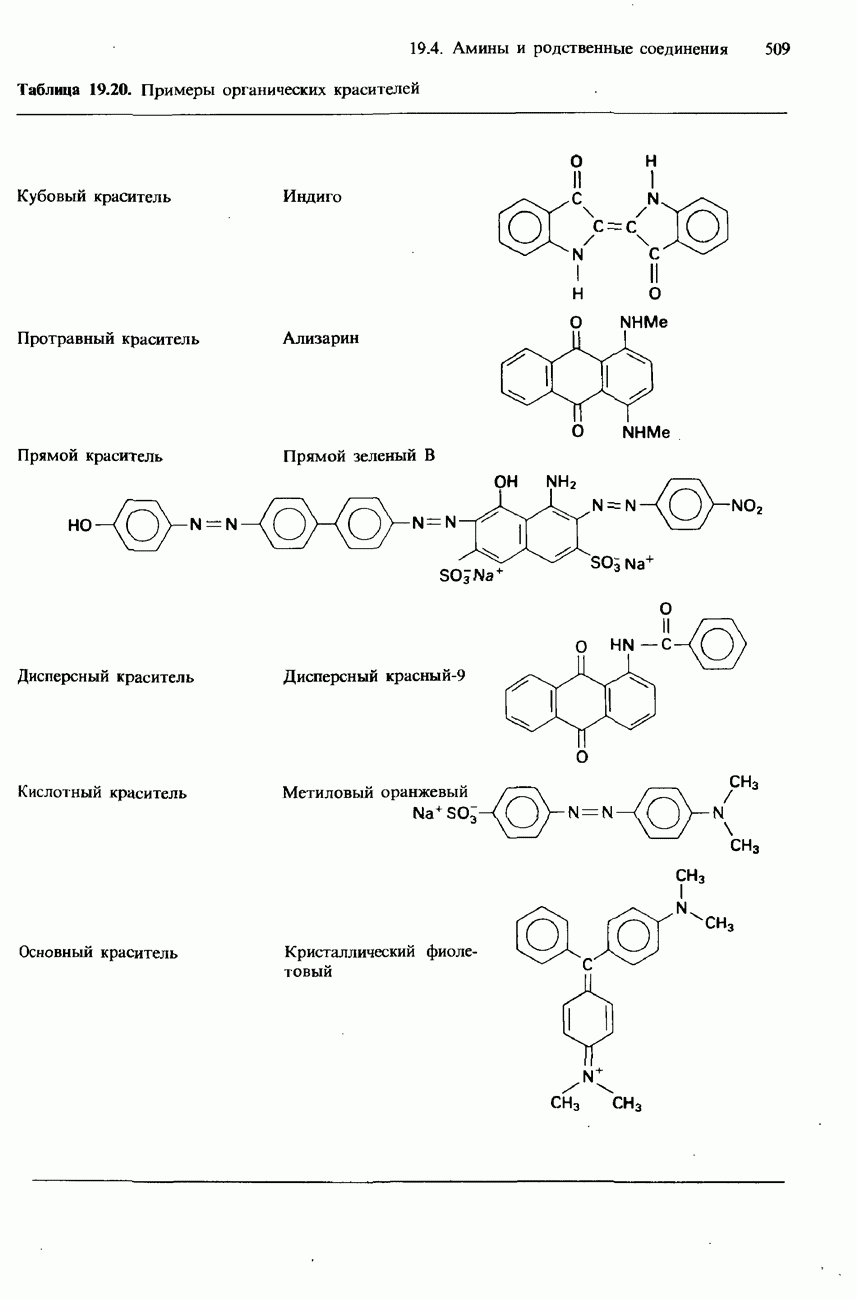
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 20. ПРИРОДНЫЕ СОЕДИНЕНИЯ И ПОЛИМЕРЫ
- 20.1. Аминокислоты, пептиды и белки
- АМИНОКИСЛОТЫ
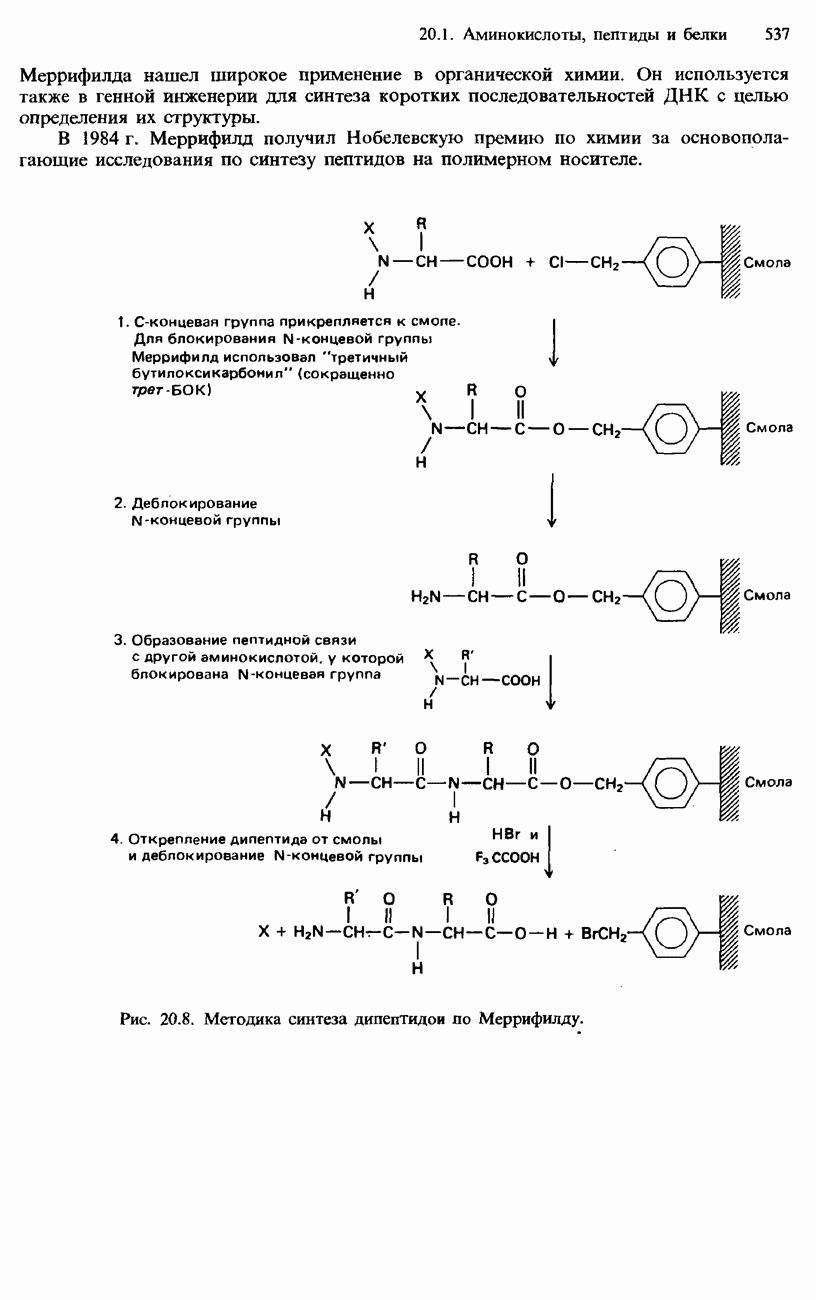
- ПЕПТИДЫ
- БЕЛКИ
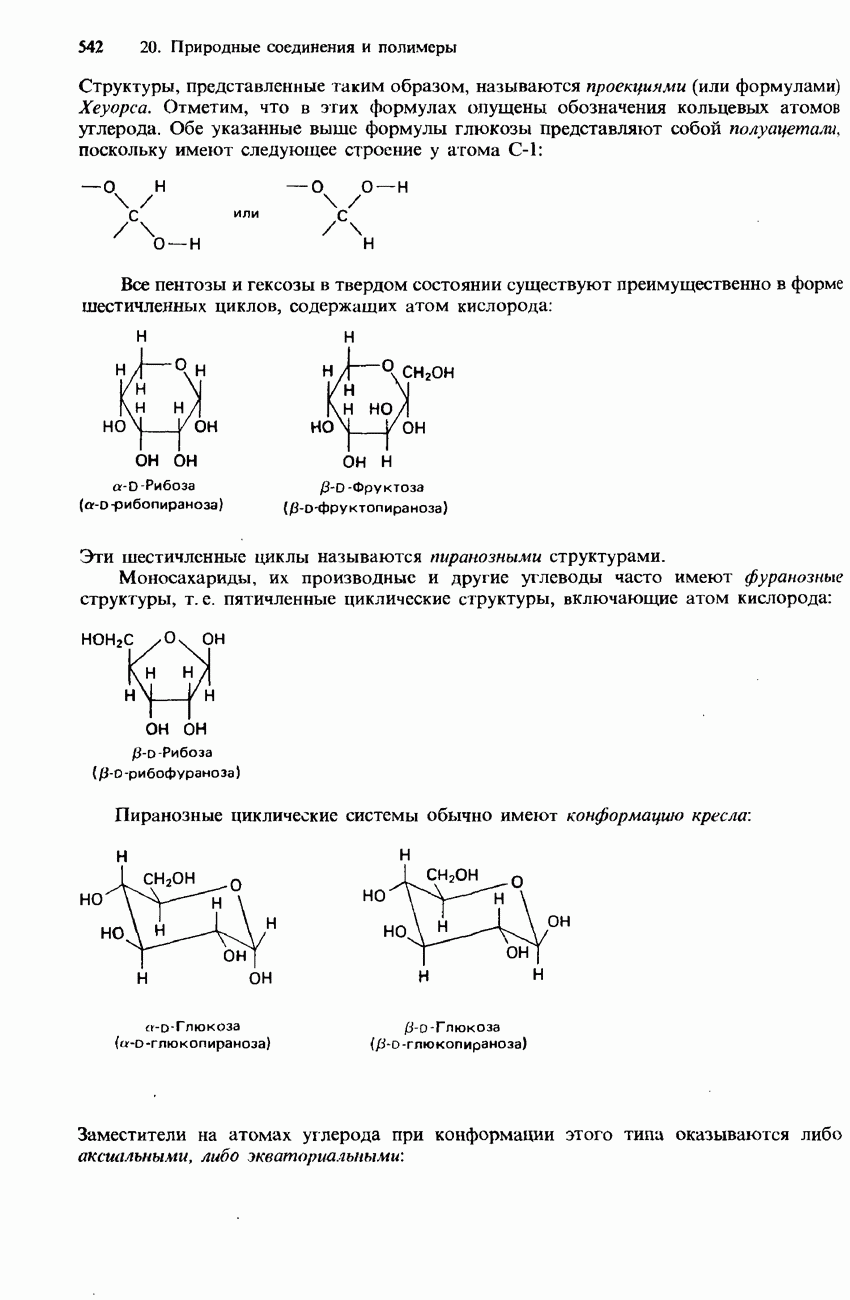
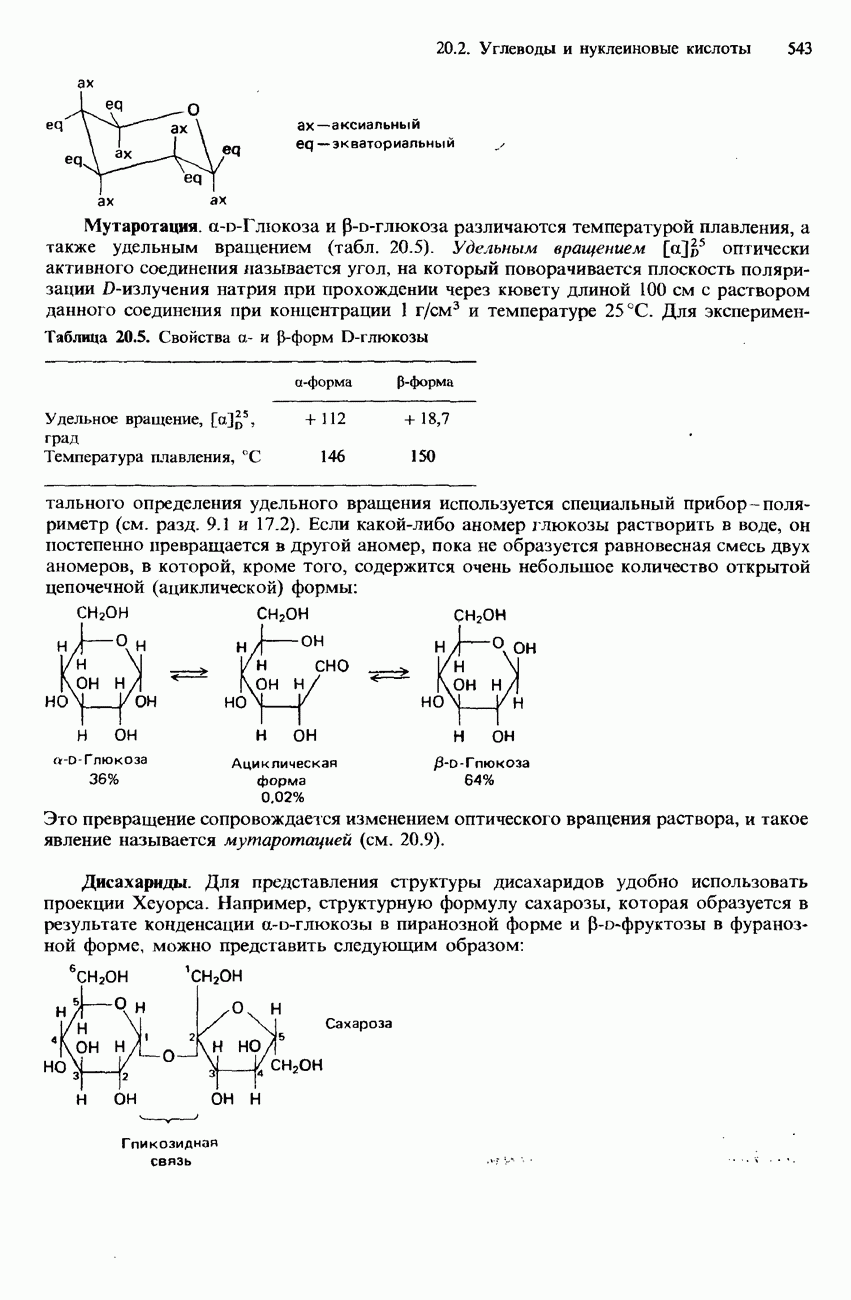
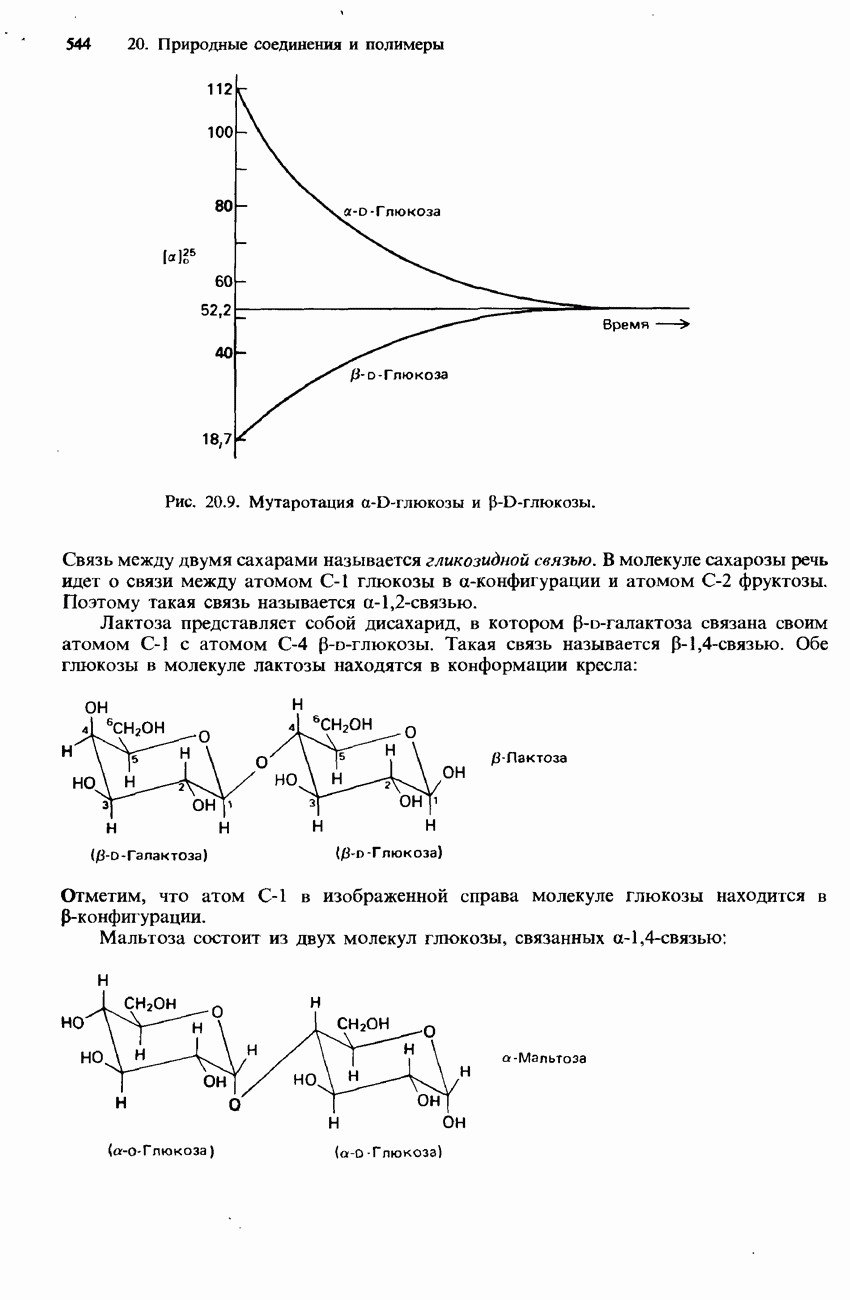
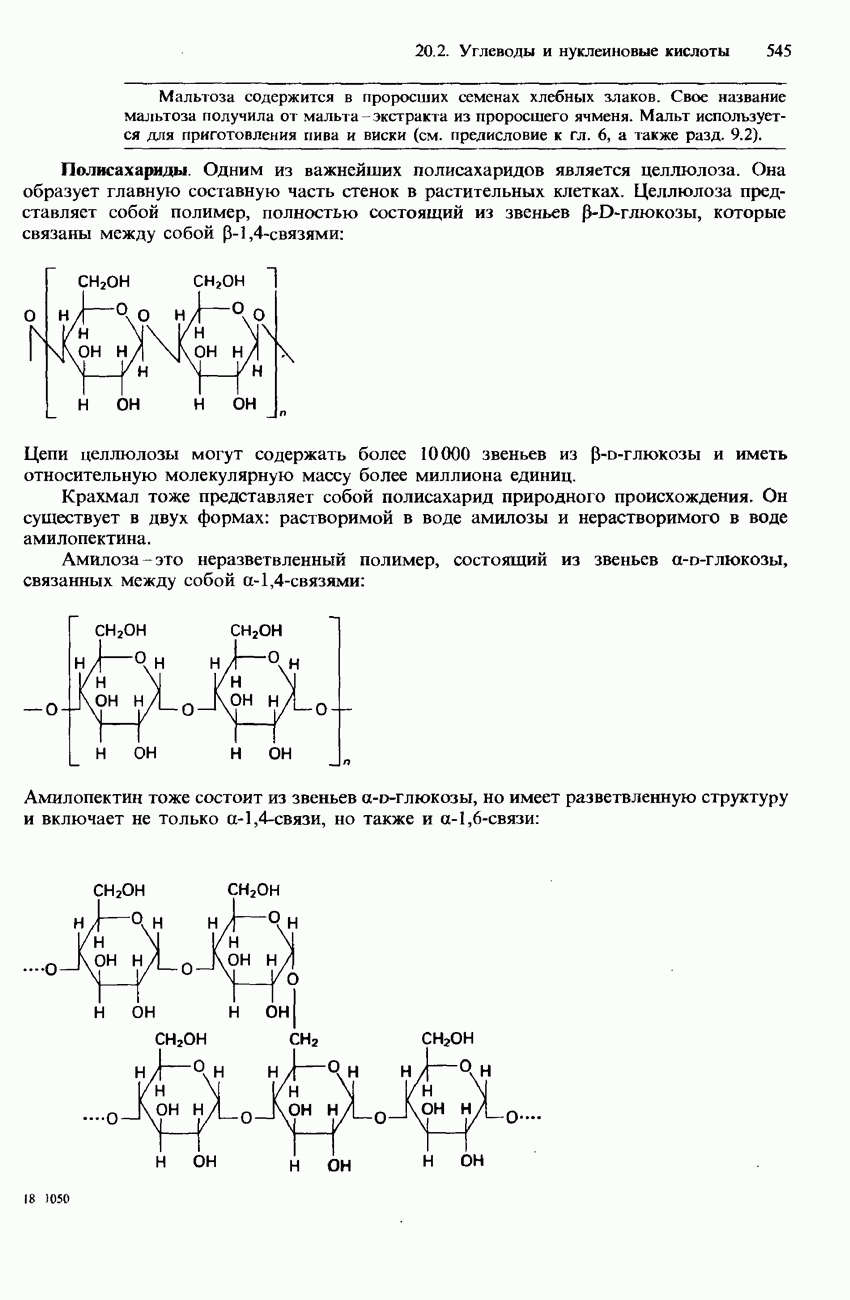
- 20.2. Углеводы и нуклеиновые кислоты
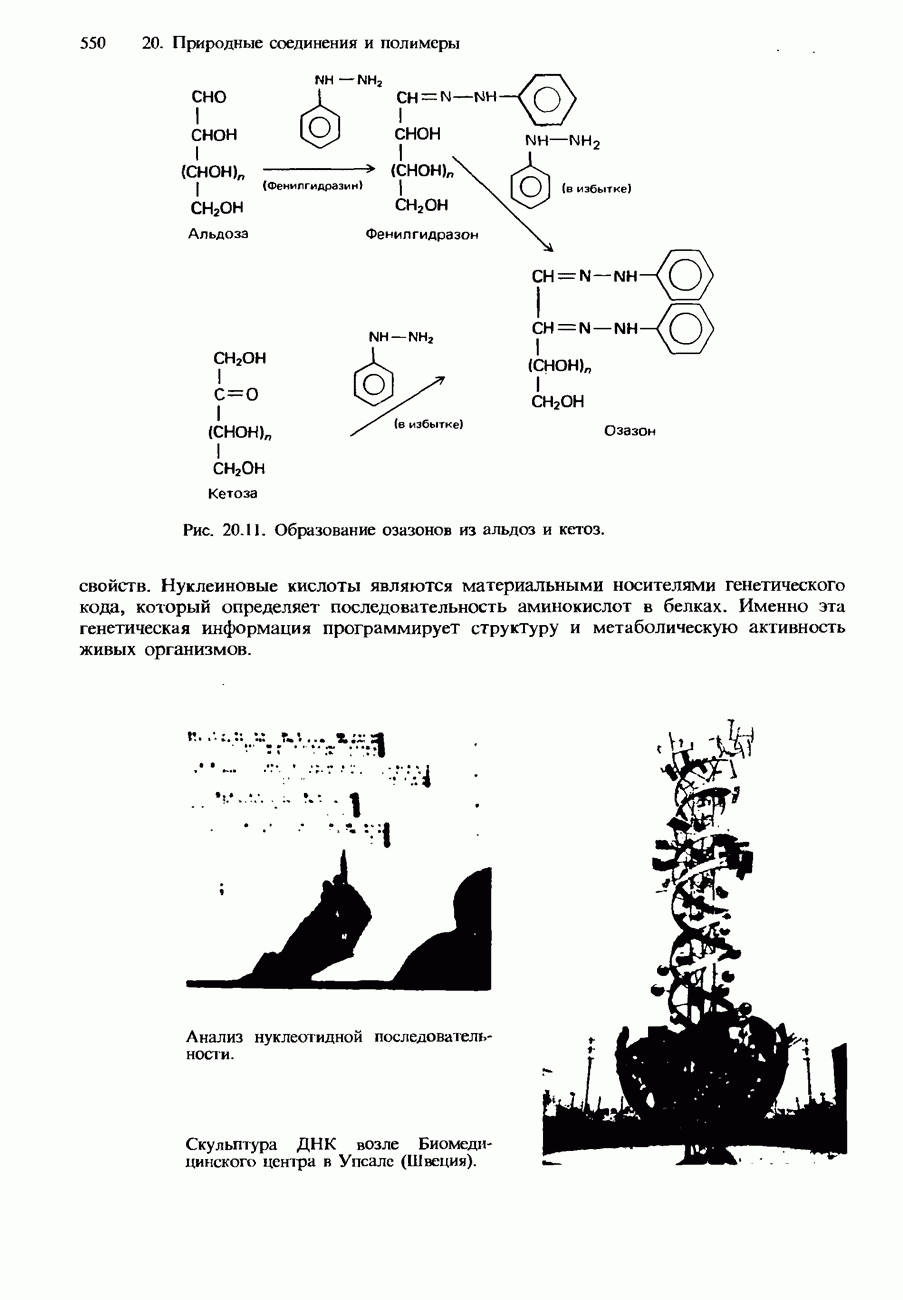
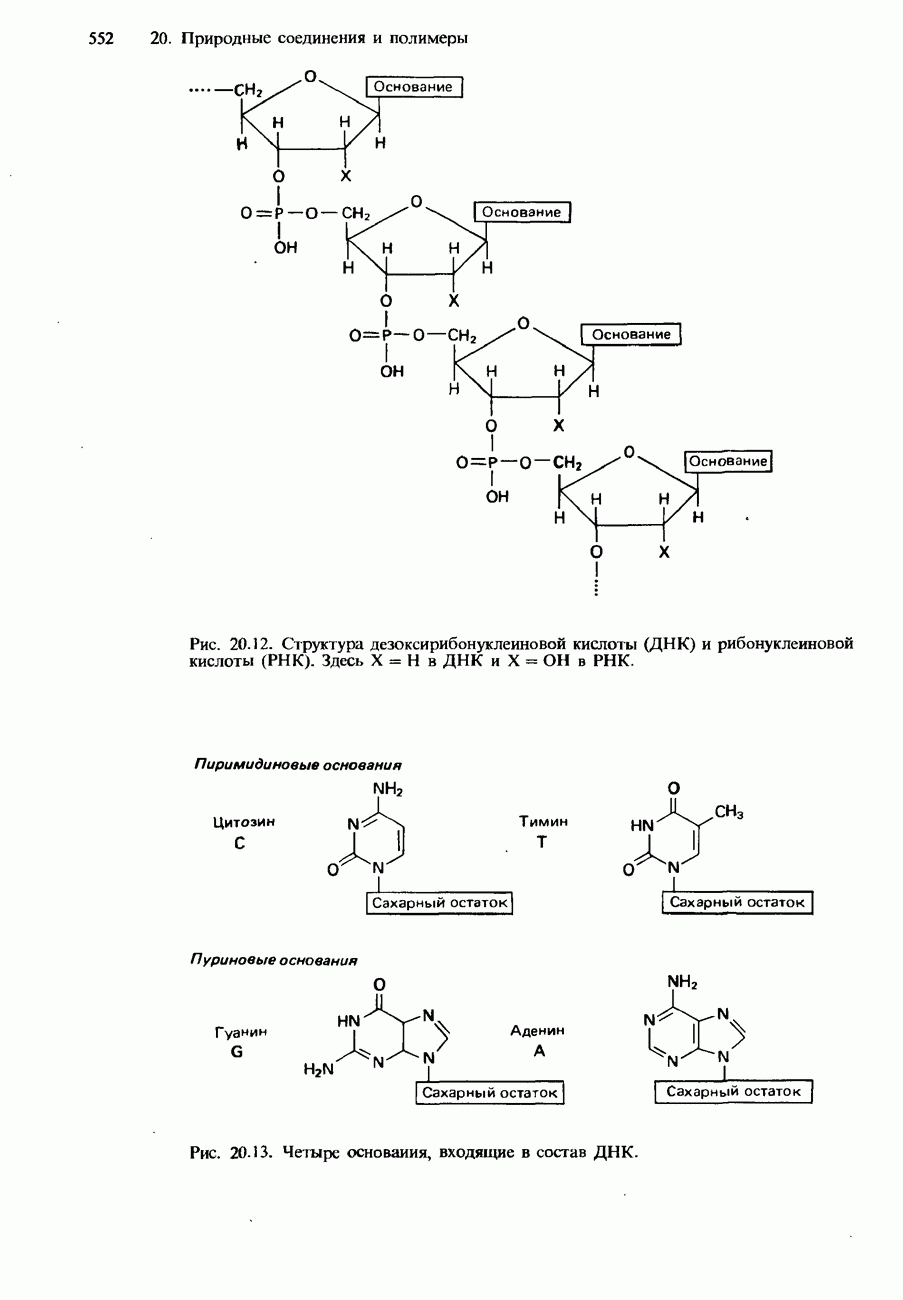
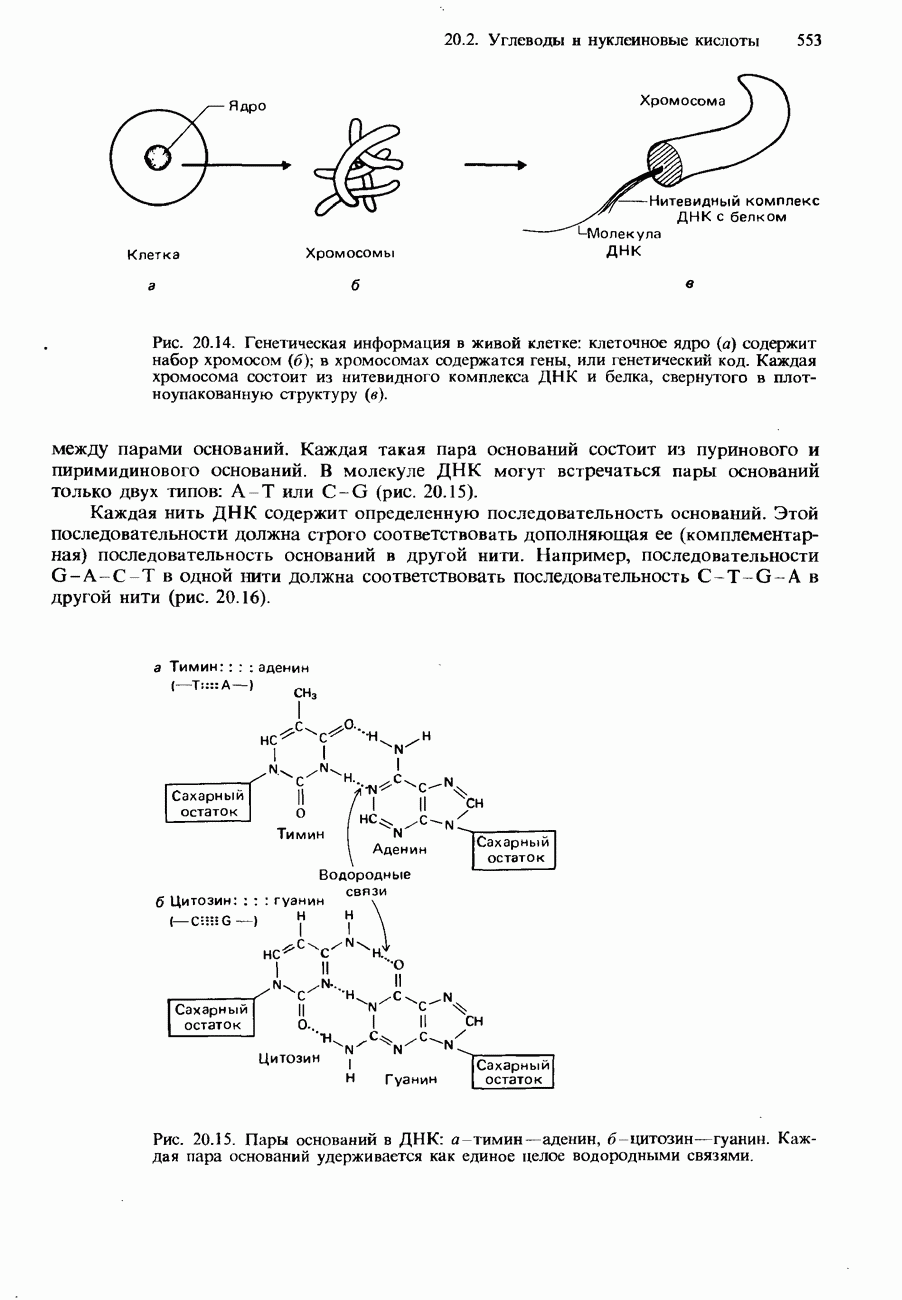
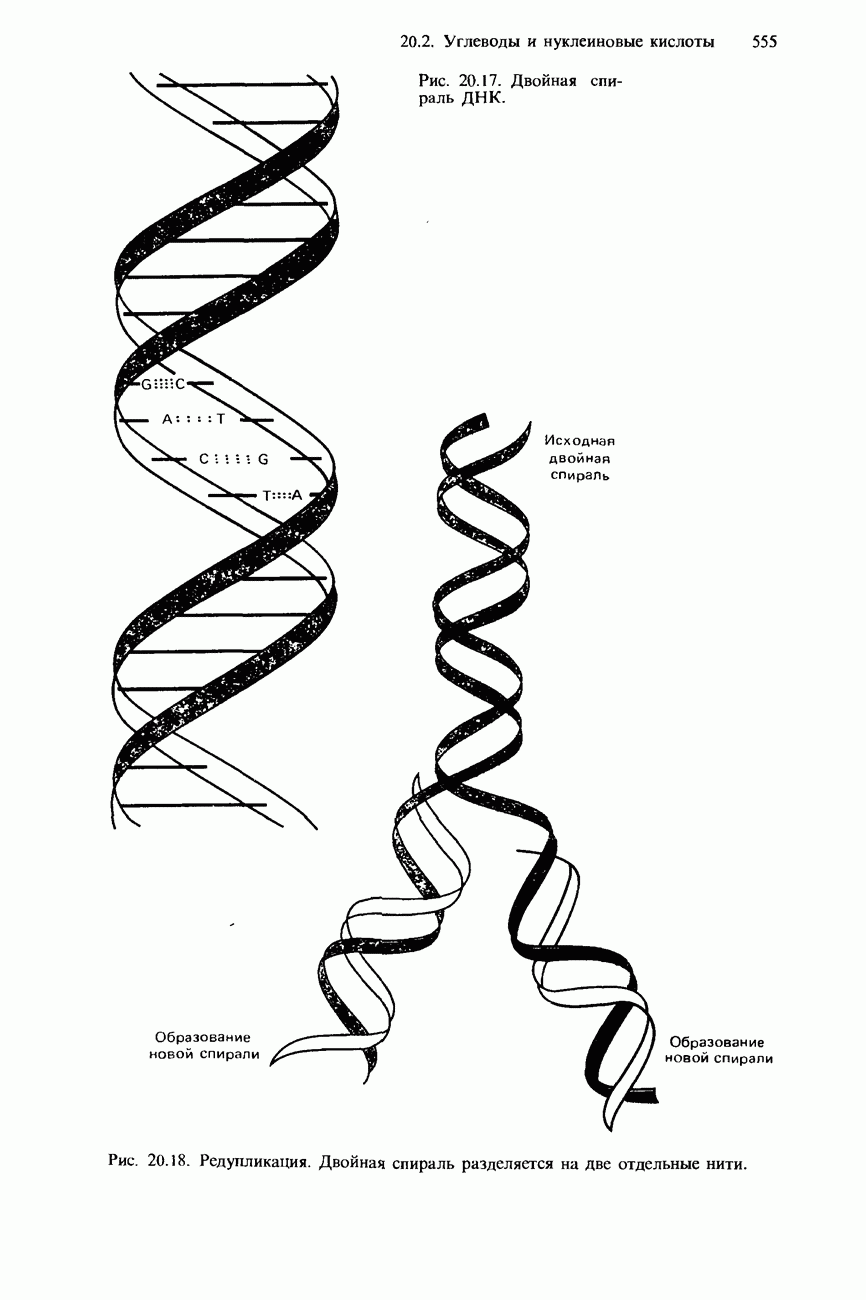
- НУКЛЕИНОВЫЕ КИСЛОТЫ
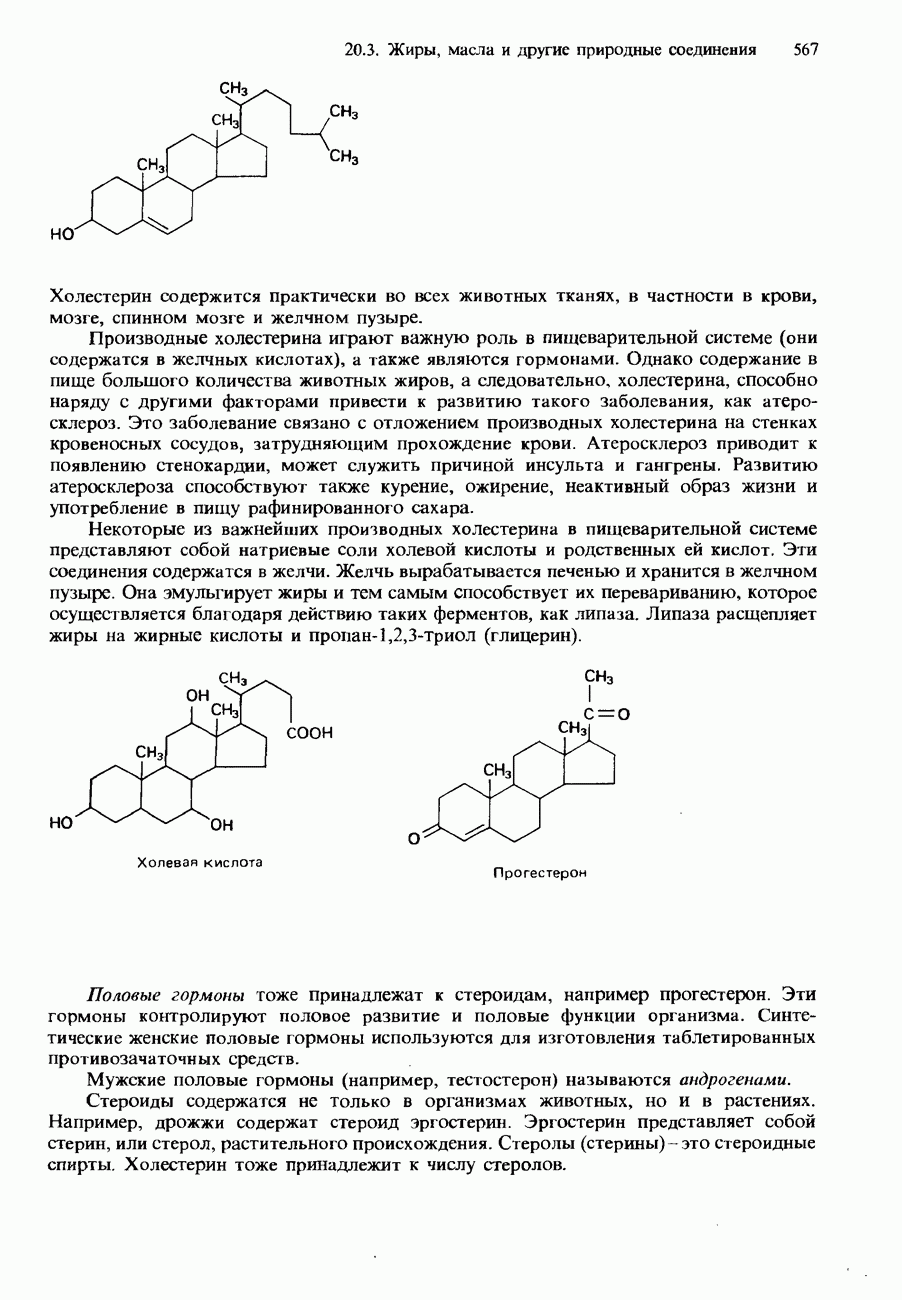
- 20.3. Жиры, масла и другие природные соединения
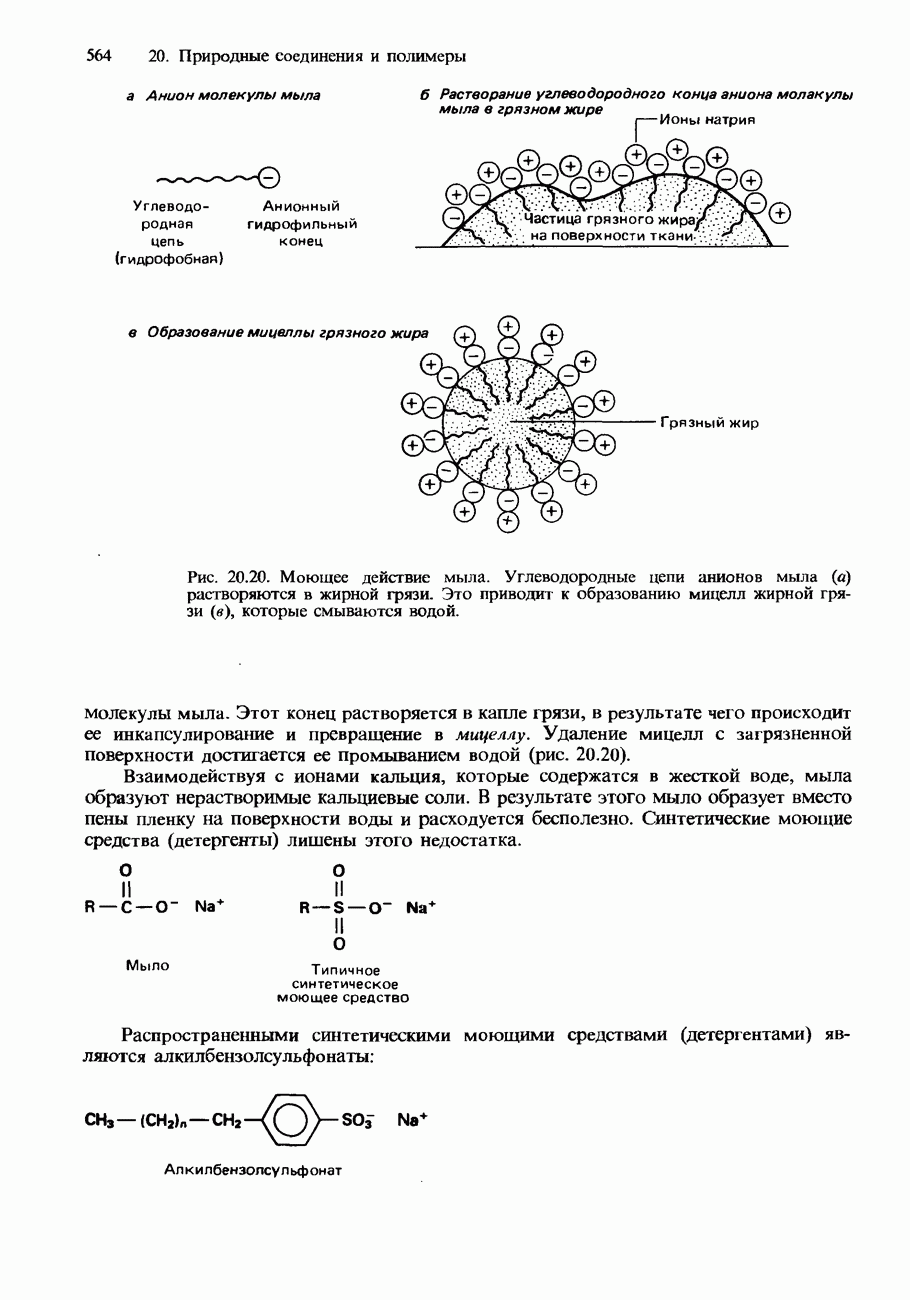
- ЖИРНЫЕ КИСЛОТЫ И ТРИГЛИЦЕРИДЫ
- ВОСКИ
- ФОСФОЛИПИДЫ И ГЛИКОЛИПИДЫ
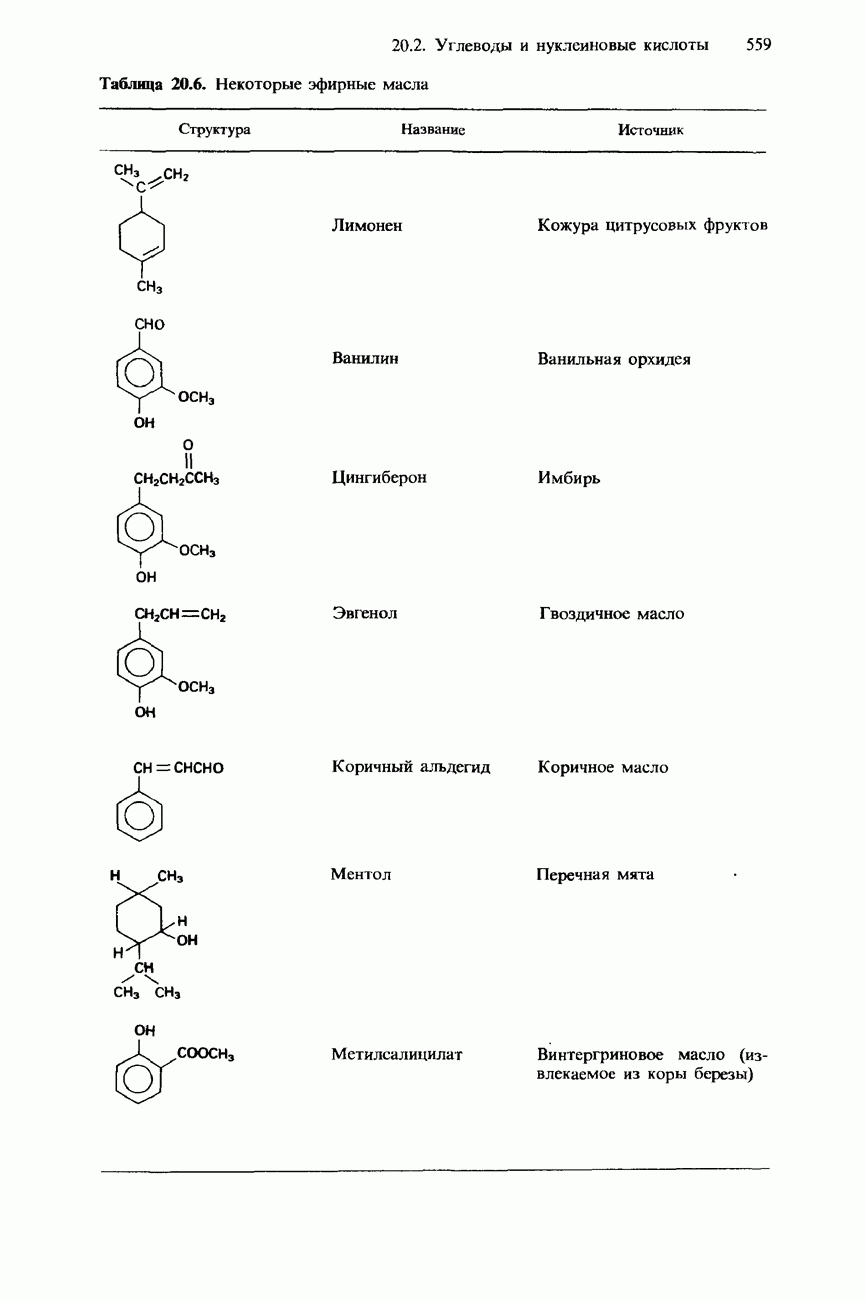
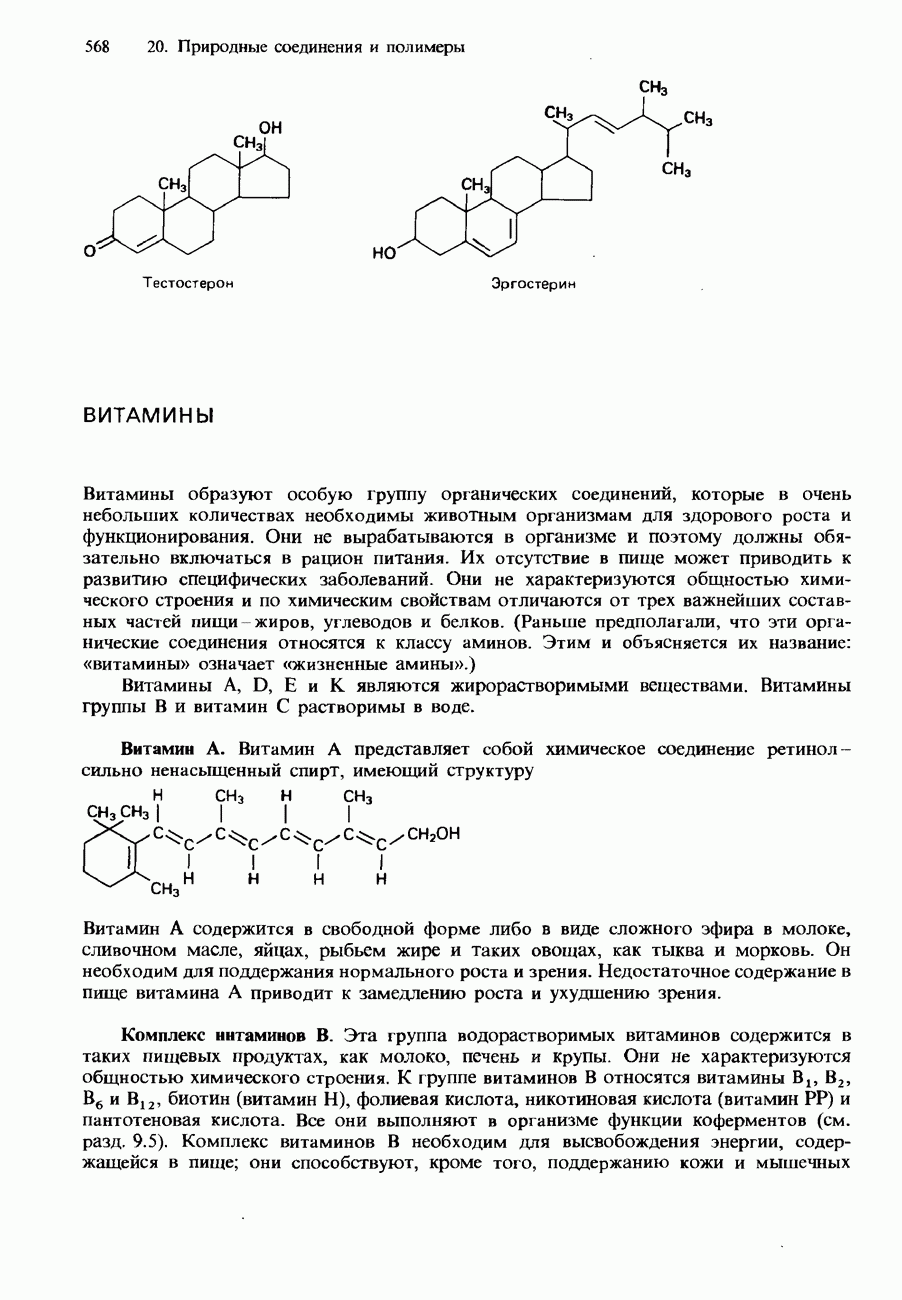
- ВИТАМИНЫ
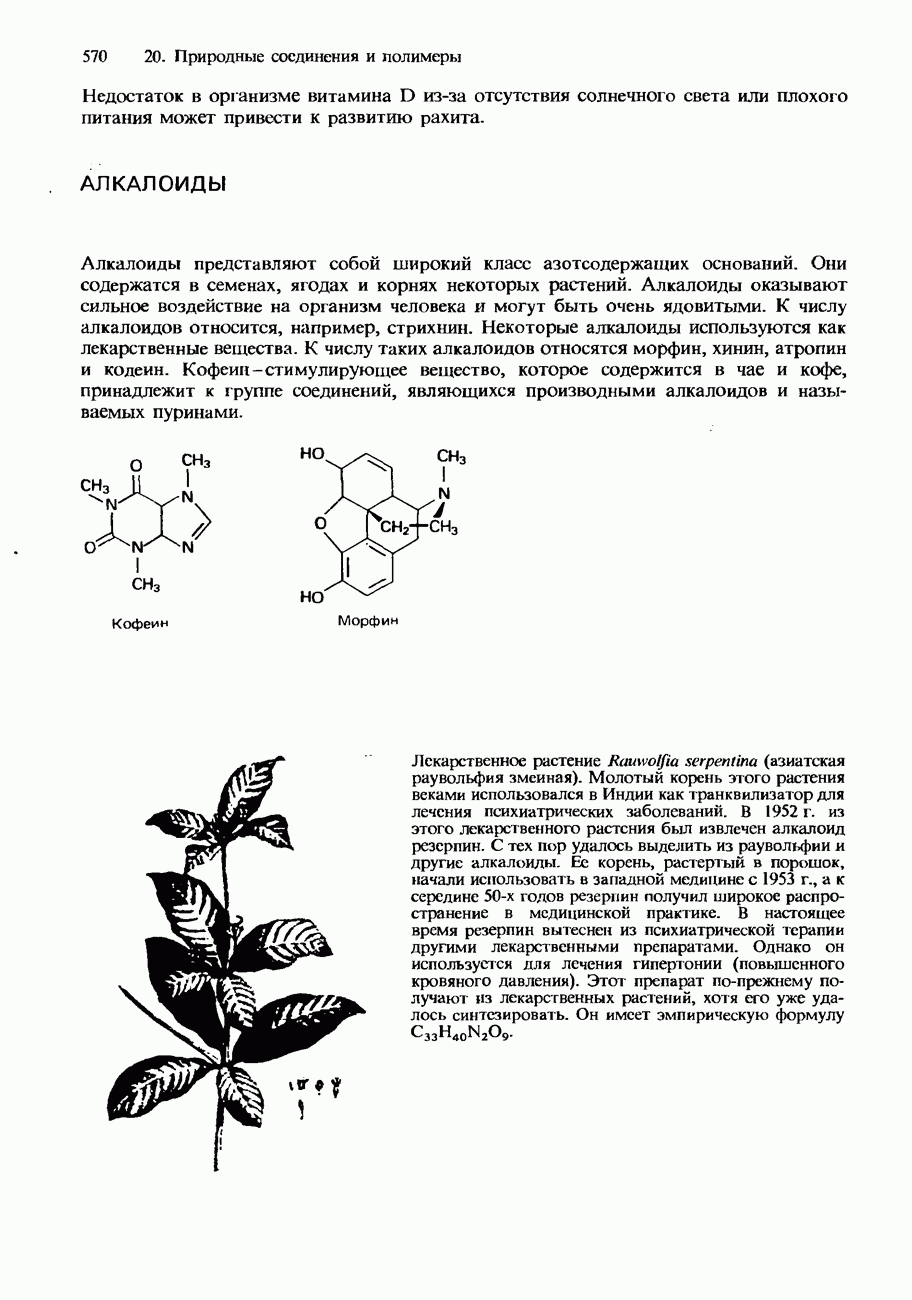
- АЛКАЛОИДЫ
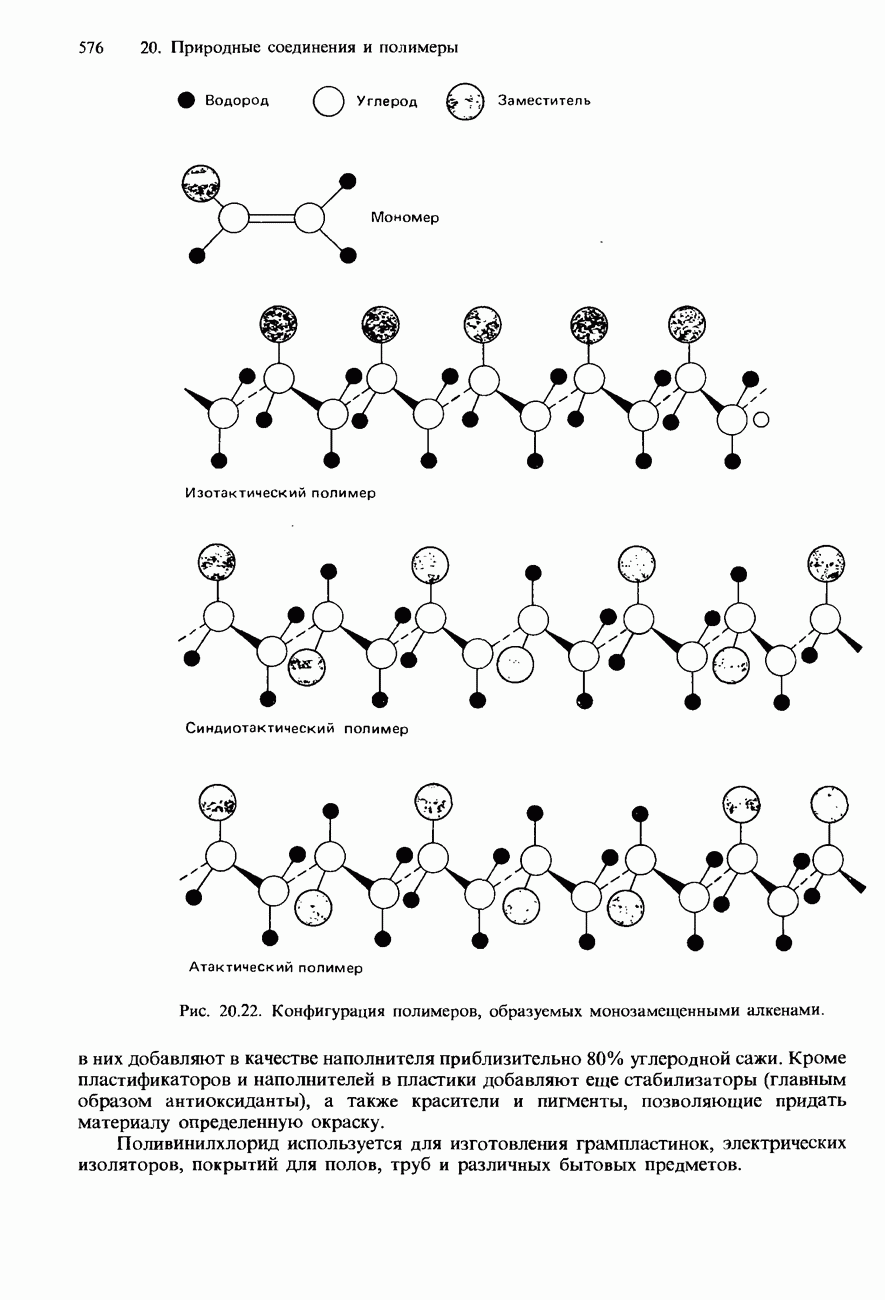
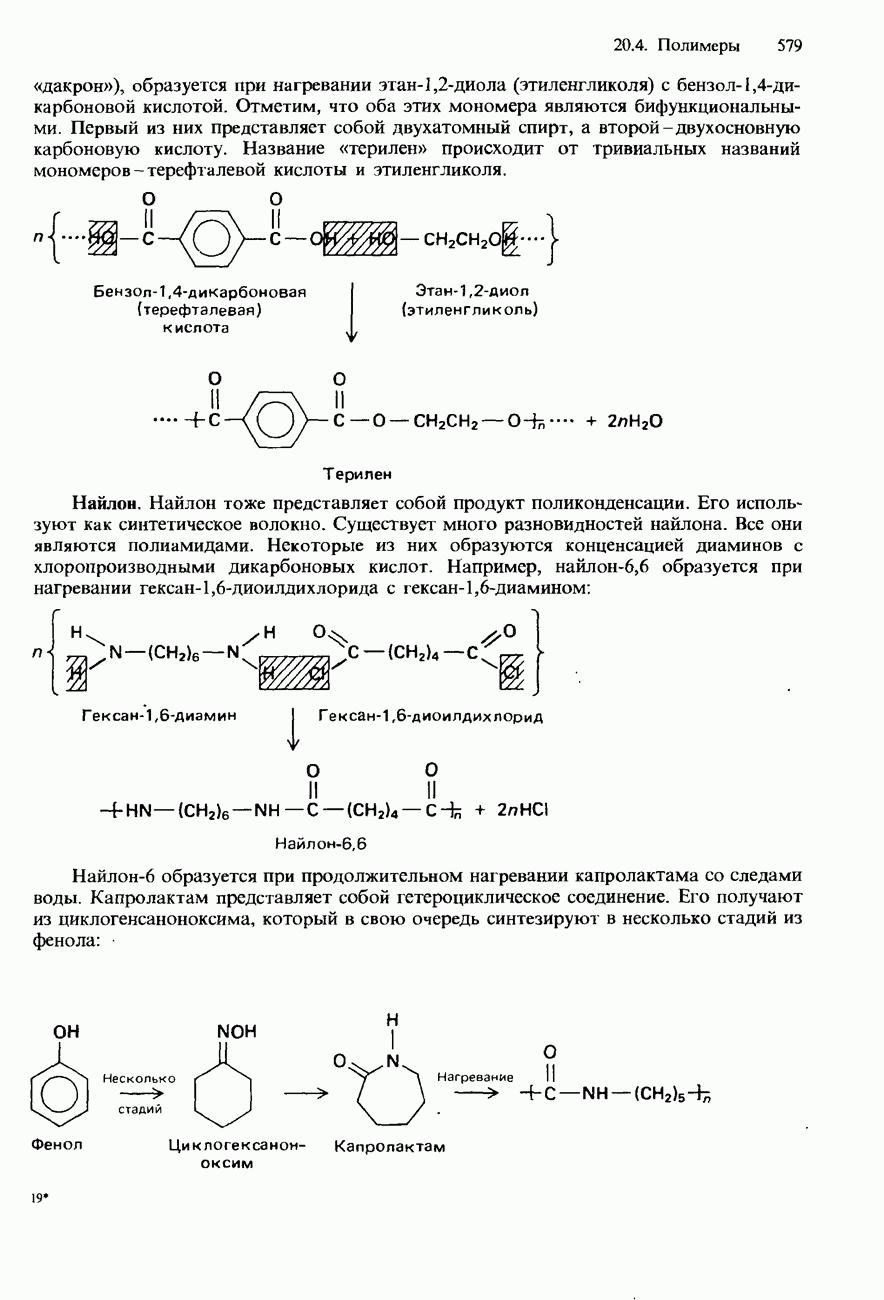
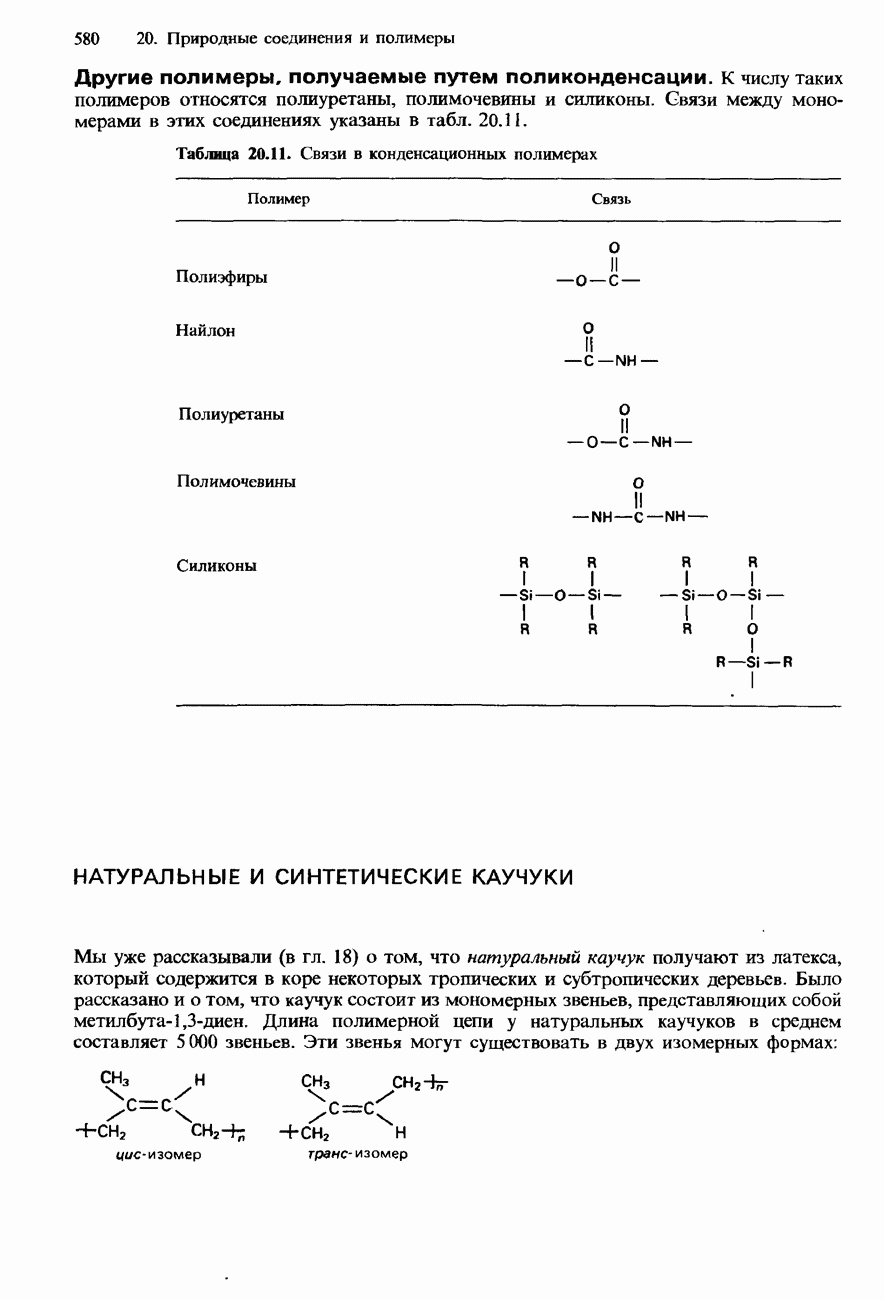
- 20.4. Полимеры
- ПОЛИМЕРИЗАЦИЯ
- НАТУРАЛЬНЫЕ И СИНТЕТИЧЕСКИЕ КАУЧУКИ
- ЦЕЛЛЮЛОЗНОЕ ВОЛОКНО
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- ПРИЛОЖЕНИЯ