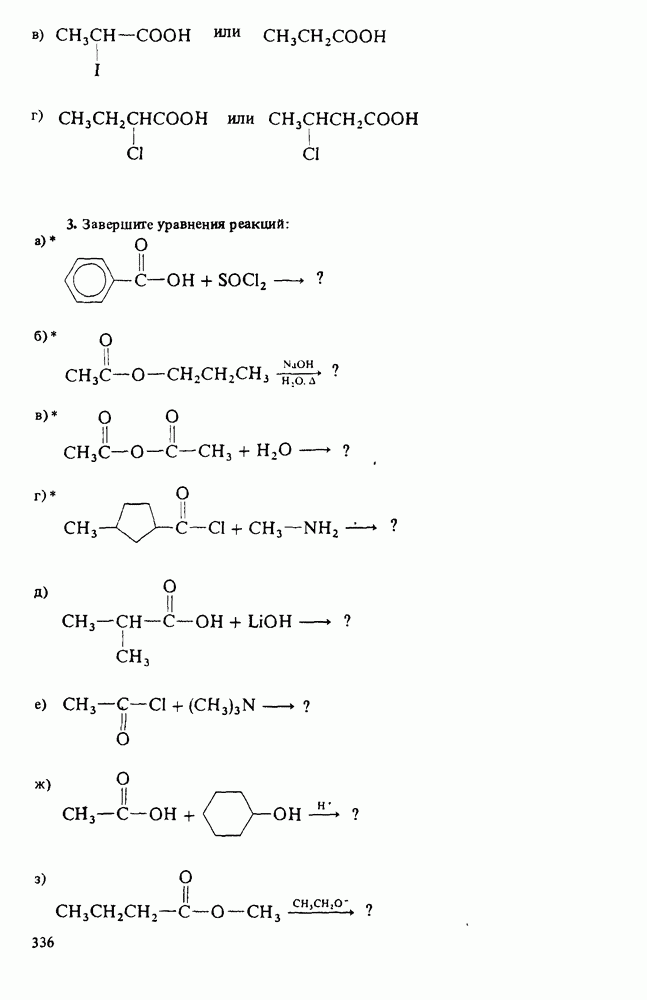| << Предыдущий параграф | Следующий параграф >> |
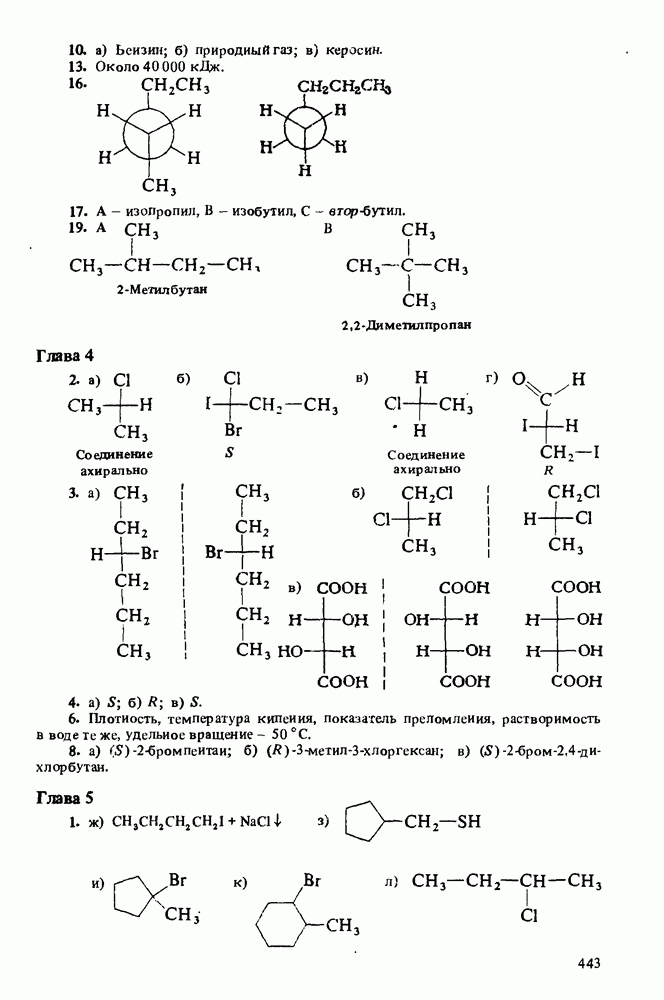
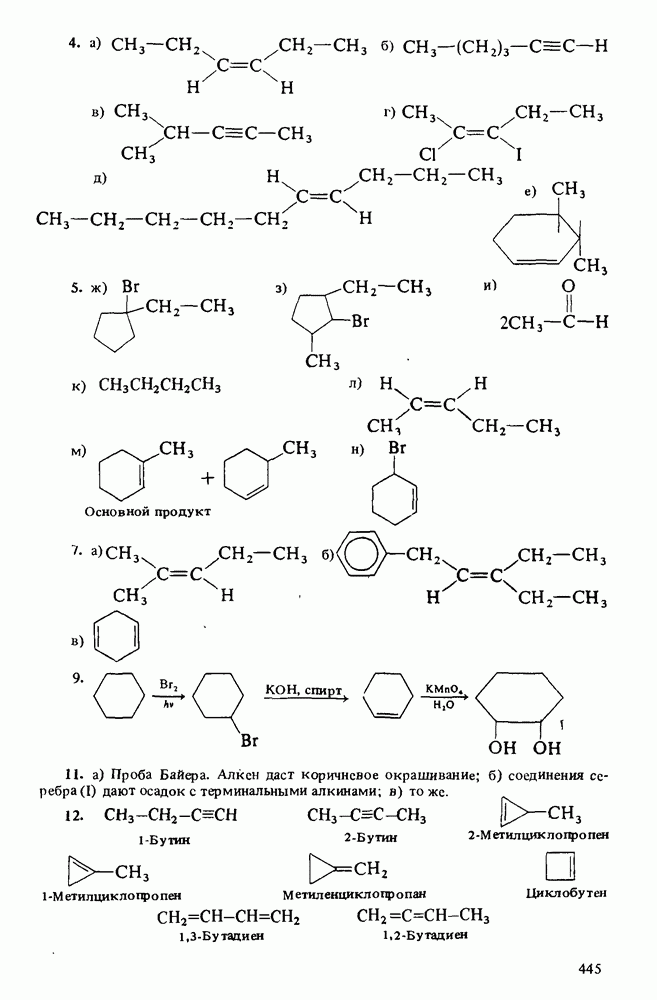
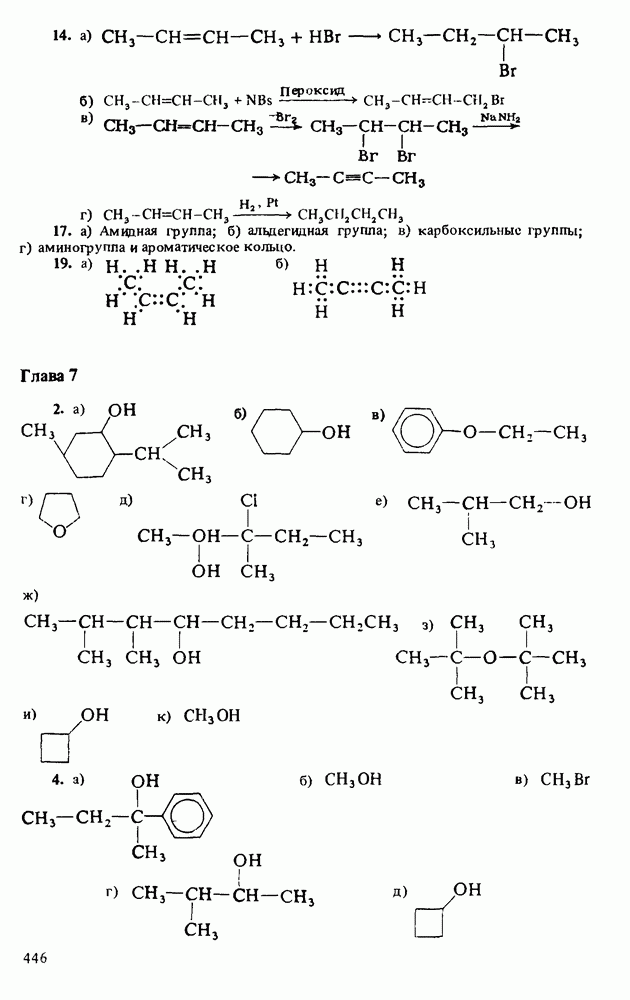
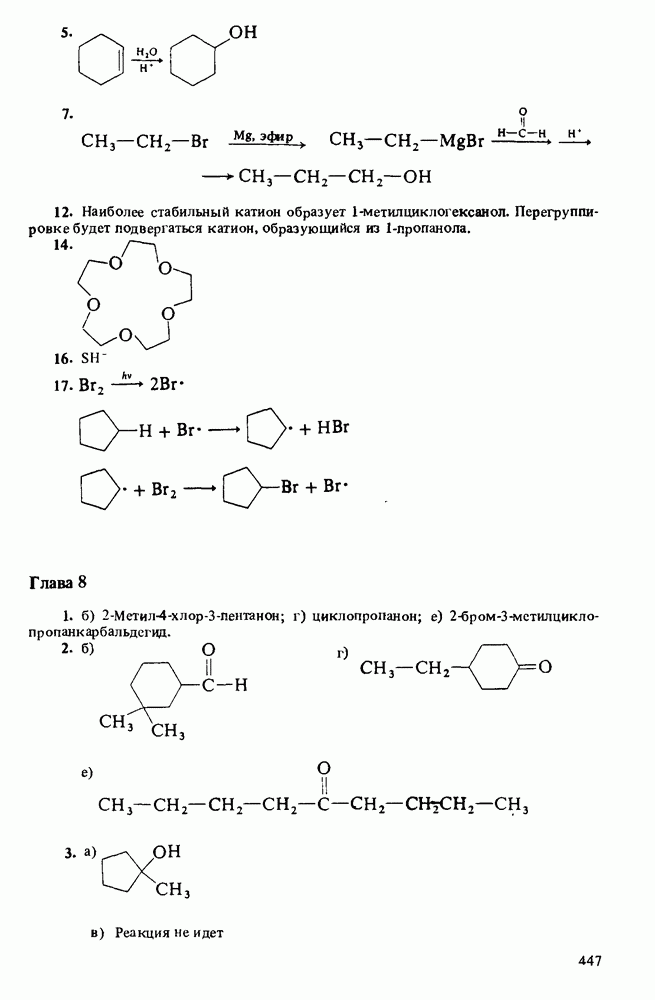
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
МОЮЩИЕ СРЕДСТВА
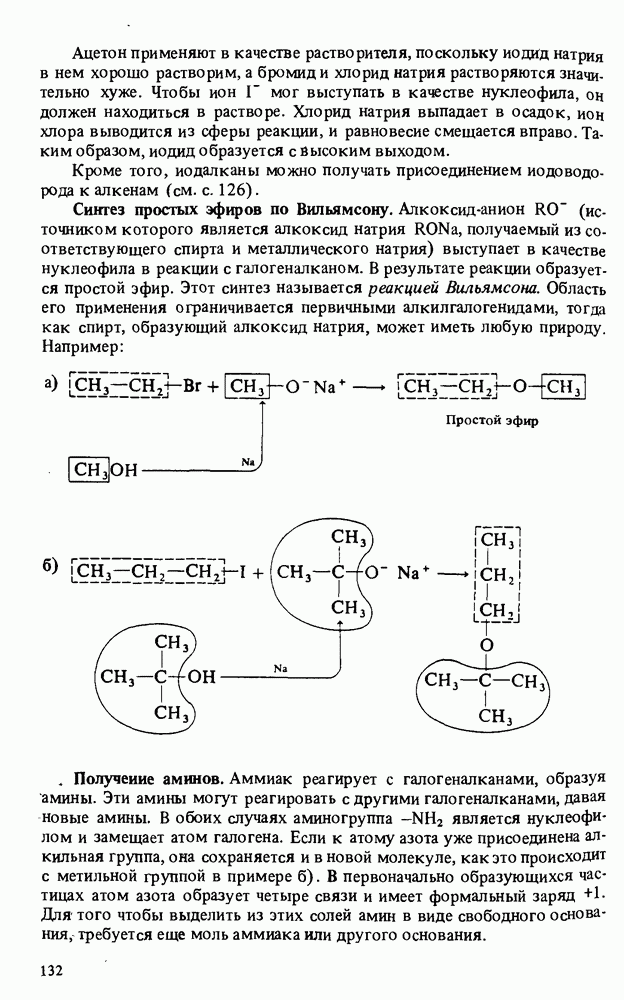
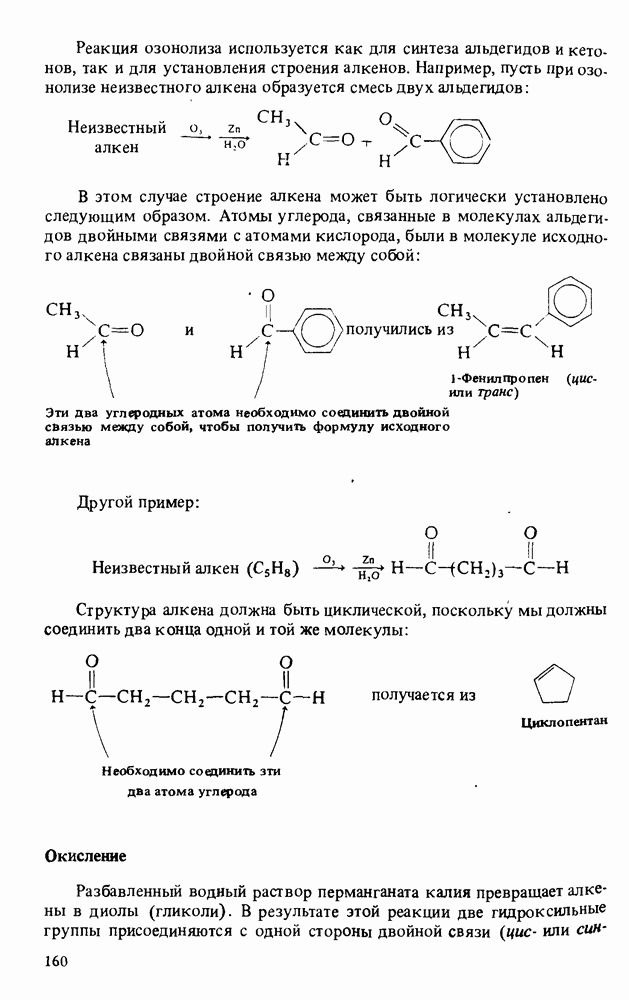
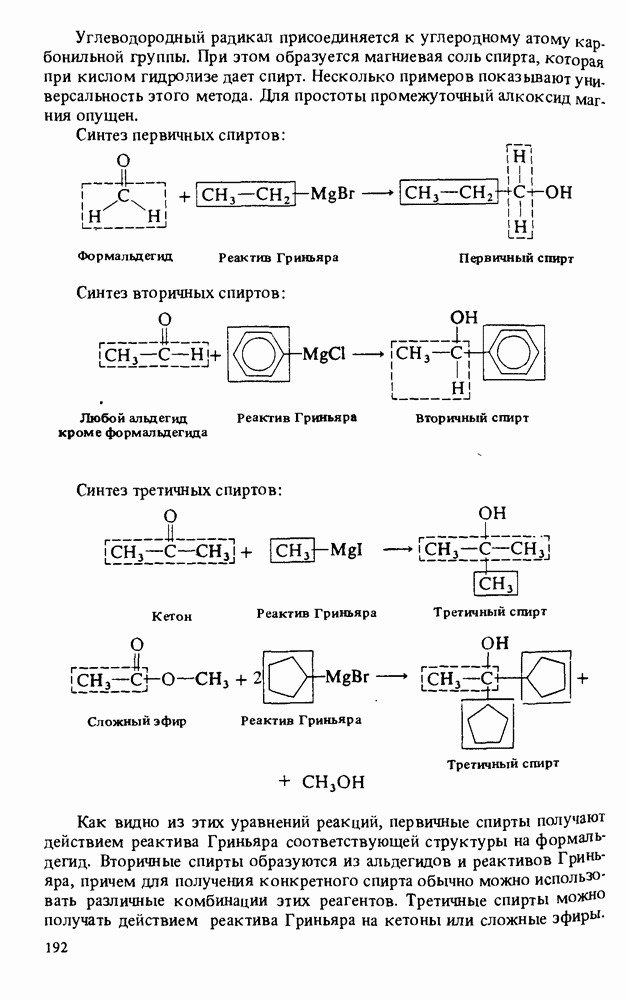
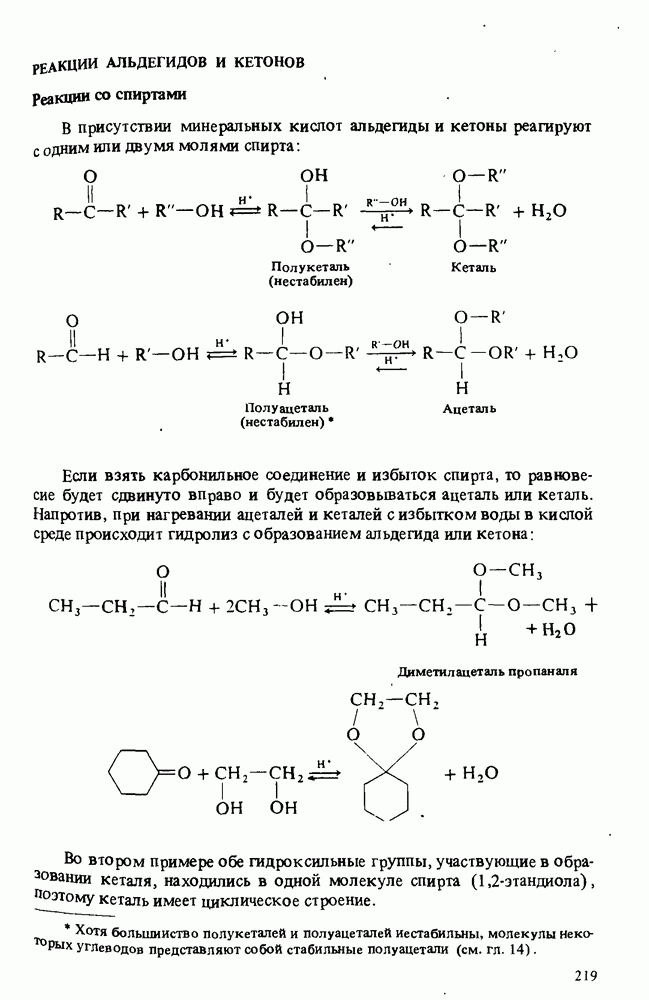
Одним из древнейших химических продуктов является мыло. Оно представляет собой соли карбоновых кислот с длинными углеводородными цепями:

Мыло получают взаимодействием животных или растительных жиров с водной щелочью например с гидроксидом натрия NaOH. Жиры представляют собой сложные эфиры длинноцепных жирных кислот и глицерина.
Каждая молекула содержит три сложноэфирные группы. Гидроксид натрия разрушает сложные эфиры. При этом образуется глицерин (1,2,3-пропантриол) и натриевые соли жирных кислот (мыло):

С давних времен и до двадцатых годов нашего века в Америке было принято изготовлять мыло дома. Эта традиция окончательно исчезла только в шестидесятых годах. Щелочь, необходимую для варки мыла, получали, промывая древесную золу дождевой водой и затем испаряя воду. Образовавшийся крепкий раствор щелочи кипятили на огне с обрезками свиного и говяжьего жира. В 1900-х годах стал доступен технический гидроксид натрия и его стали использовать при варке мыла. Мыло, полученное таким образом в домашних условиях, разъедало кожу, так как содержало остатки гидроксида натрия, который снимал с кожи естественную жировую пленку.
Современное мыло, выпускаемое промышленностью, может содержать душистые вещества или дезодоранты, быть окрашенным, или иметь в своем составе бактерицидные препараты.
Жидкое мыло представляет собой концентрированный раствор мыла в воде, который легко извлечь из бутылки или тюбика. Для мытья сильно загрязненных поверхностей используют мыло, содержащее песок или порошок пемзы, которые играют роль абразива. Иногда используют мыло с добавками отбеливателя.
Вещества, используемые в качестве моющих средств, называются поверхностно-активными веществами или эмульгаторами. Эти соединения обладают способностью адсорбироваться на поверхности раздела между полярными и неполярными веществами, что приводит к образованию

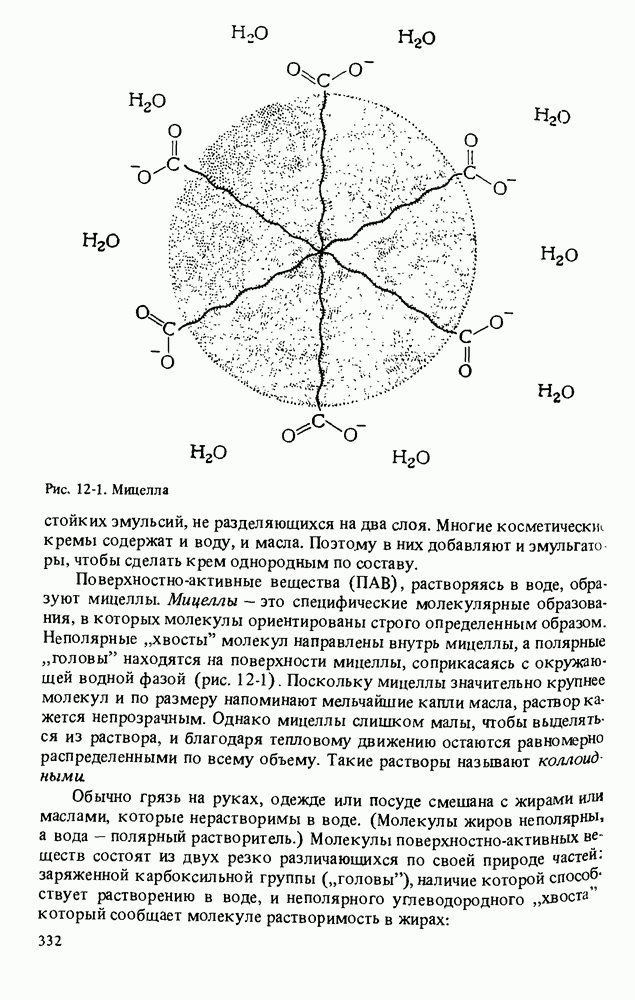
Рис. 12-1. Мицелла
стойких эмульсий, не разделяющихся на два слоя. Многие косметически кремы содержат и воду, и масла. Поэтому в них добавляют и эмульгаторы, чтобы сделать крем однородным по составу.
Поверхностно-активные вещества (ПАВ), растворяясь в воде, образуют мицеллы. Мицеллы - это специфические молекулярные образования, в которых молекулы ориентированы строго определенным образом. Неполярные "хвосты" молекул направлены внутрь мицеллы, а полярные "головы" находятся на поверхности мицеллы, соприкасаясь с окружающей водной фазой (рис. 12-1). Поскольку мицеллы значительно крупнее молекул и по размеру напоминают мельчайшие капли масла, раствор кажется непрозрачным. Однако мицеллы слишком малы, чтобы выделяться из раствора, и благодаря тепловому движению остаются равномерно распределенными по всему объему. Такие растворы называют коллоидными
Обычно грязь на руках, одежде или посуде смешана с жирами или маслами, которые нерастворимы в воде. (Молекулы жиров неполярны, а вода - полярный растворитель.) Молекулы поверхностно-активных веществ состоят из двух резко различающихся по своей природе частей: заряженной карбоксильной группы ("головы"), наличие которой способствует растворению в воде, и неполярного углеводородного "хвоста" который сообщает молекуле растворимость в жирах:

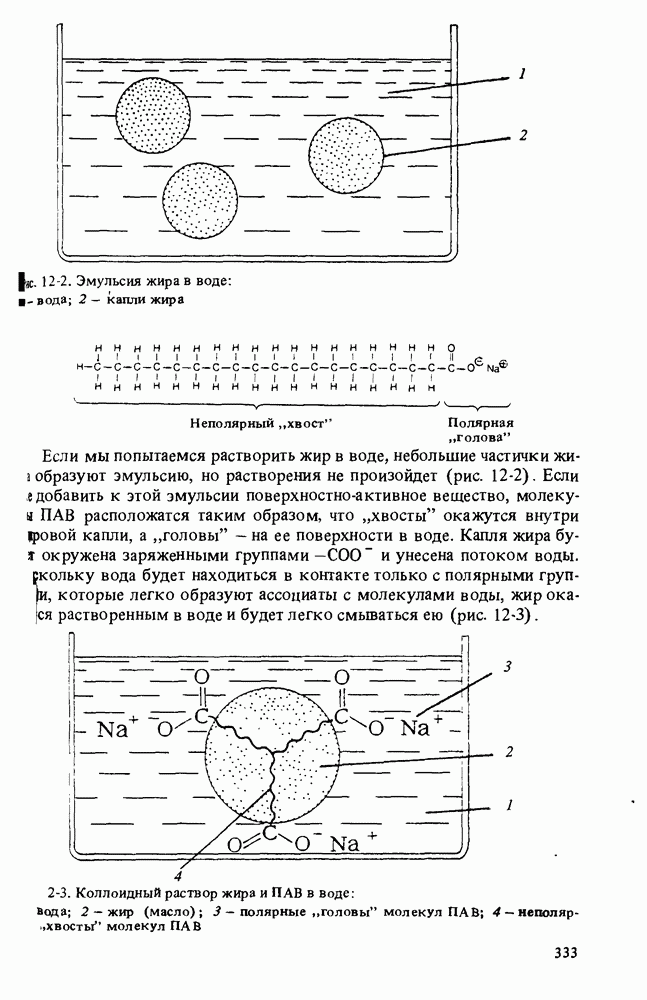
Рис. 12-2. Эмульсия жира в воде: - вода; 2 — капли жира

Если мы попытаемся растворить жир в воде, небольшие частички жира образуют эмульсию, но растворения не произойдет (рис. 12-2). Если не добавить к этой эмульсии поверхностно-активное вещество, молекулы ПАВ расположатся таким образом, что "хвосты" окажутся внутри групповой капли, а "головы" — на ее поверхности в воде. Капля жира будет окружена заряженными группами  и унесена потоком воды.
и унесена потоком воды.
Поскольку вода будет находиться в контакте только с полярными группами, которые легко образуют ассоциаты с молекулами воды, жир окажутся растворенным в воде и будет легко смываться ею (рис. 12-3).

Рис. 12-3. Коллоидный раствор жира и ПАВ в воде: 1 - вода; 2 — жир (масло)  полярные "головы" молекул ПАВ; 4 - неполяр "хвосты" молекул ПАВ
полярные "головы" молекул ПАВ; 4 - неполяр "хвосты" молекул ПАВ
СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 12
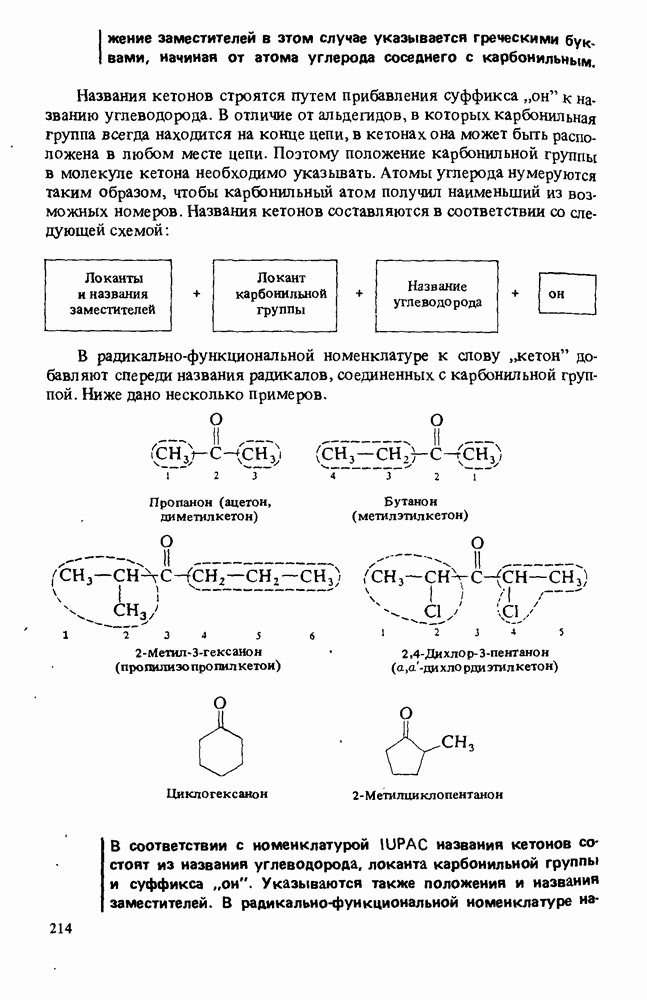
1. Названия карбоновых кислот строятся путем добавления окончания "овая кислота" к названию углеводорода. Названия сложных эфиров состоят из одного слова, включающего название алкильного радикала исходного спирта, название алкана от которого образовано название кислоты, и суффикса "оат". Названия амидов образуются из корня названия кислоты и окончания "амид".
2. Сила (кислотность) карбоновых кислот определяется природой заместителей во фрагменте, соединенном с карбоксильной группой. Наличие электроотрицательных атомов вызывает увеличение кислотности, а введение алкильных групп ослабляет силу кислоты.
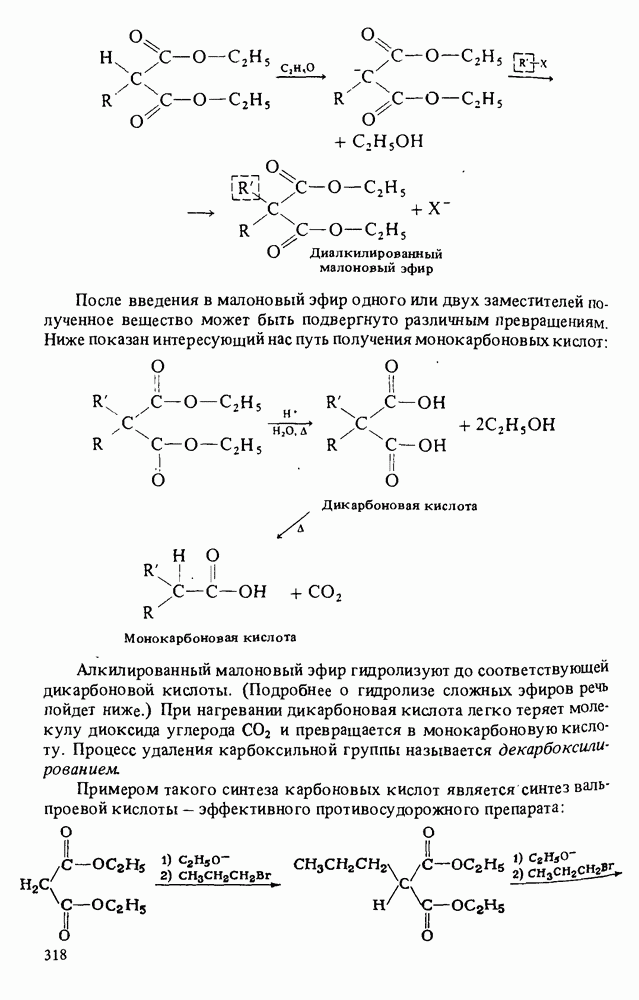
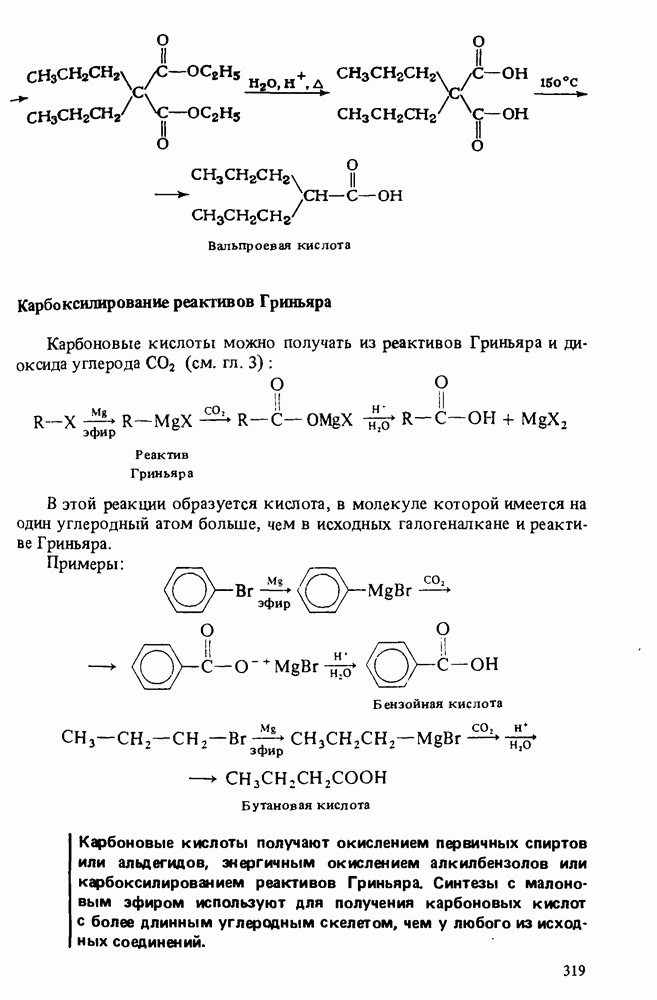
3. Карбоновые кислоты получают окислением первичных спиртов или альдегидов, окислением боковой цепи ароматических соединений, карбоксилированием реактивов, Гриньяра или с помошью синтезов на основе малонового эфира.
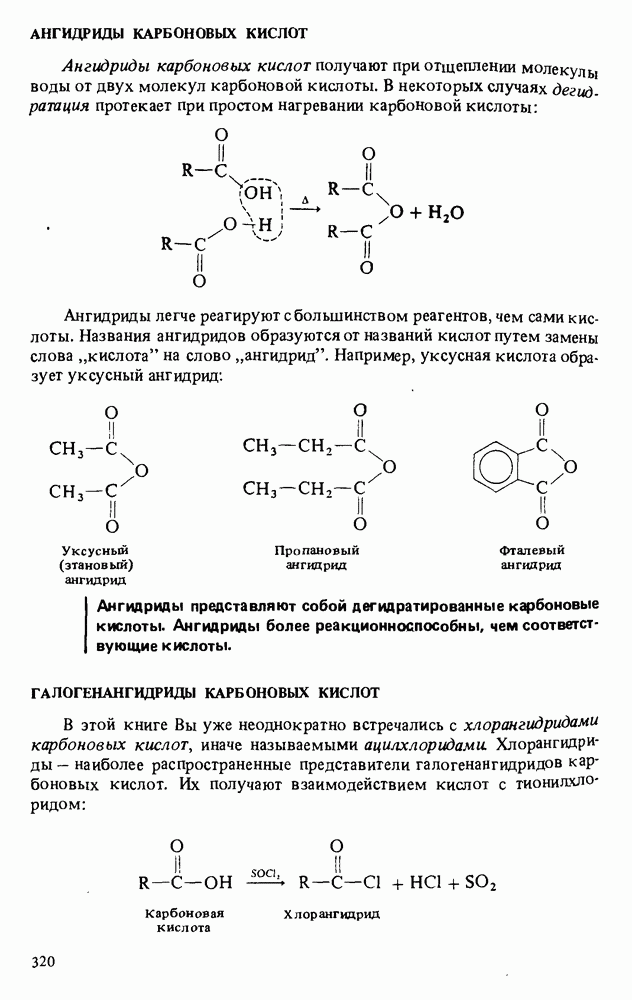
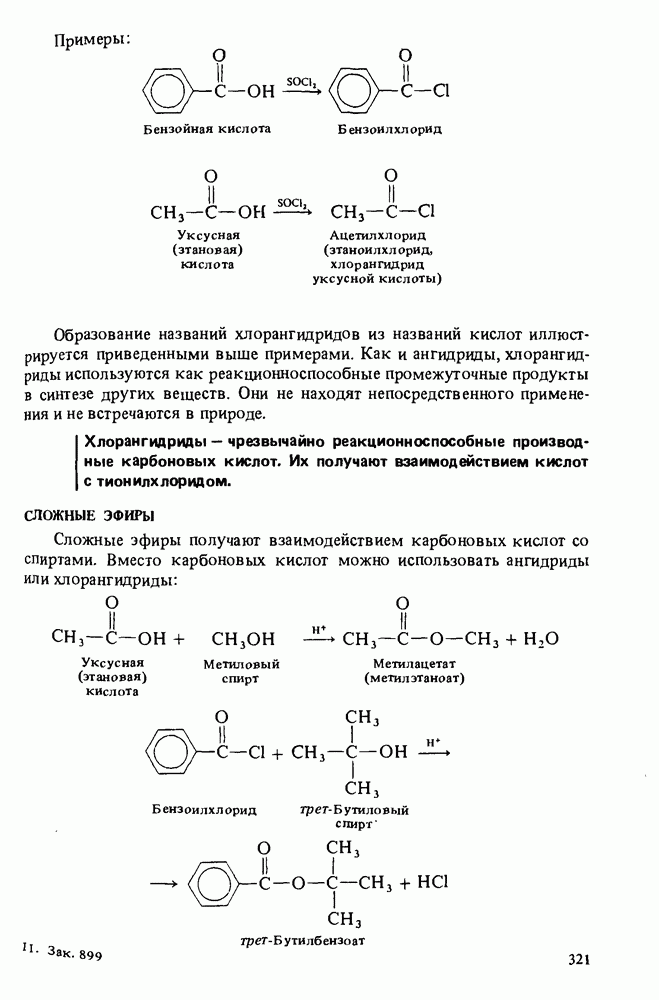
4. Хлорангидриды карбоновых кислот образуются при обработке кислот тионилхлоридом; ангидриды карбоновых кислот получают путем дегидратации кислот или при взаимодействии их солей с хлорангидридами.
5. Сложные эфиры и амиды можно получать действием карбоновых кислот, их ангидридов или хлорангидридов на спирты и амины (или аммиак) соответственно.
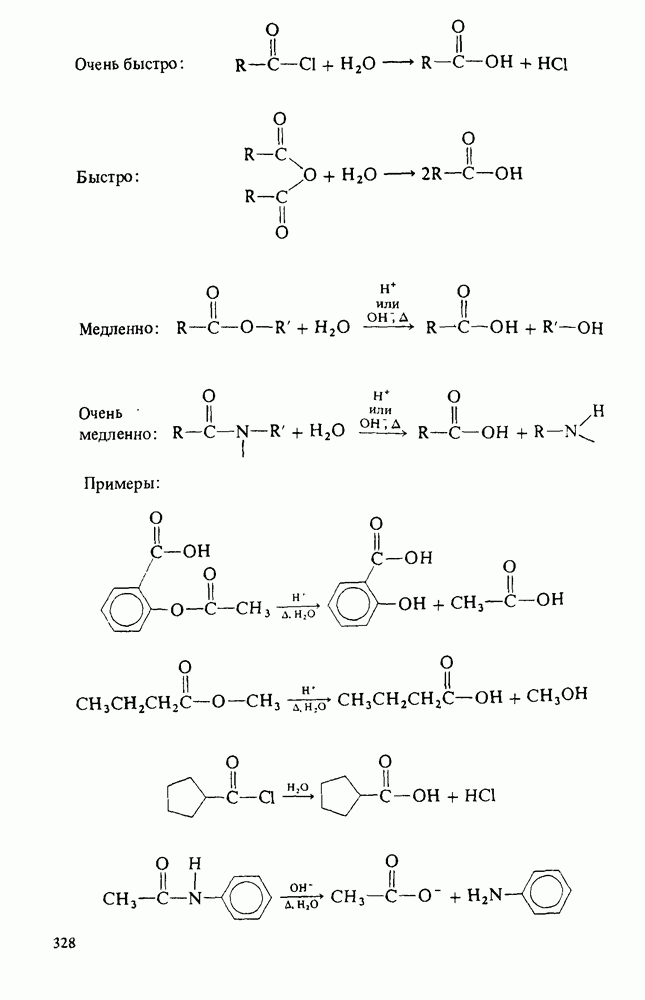
6. Все производные карбоновых кислот могут быть гидролизованы до исходной кислоты.
7. Многие пахучие вещества и лекарственные препараты представляют собой сложные эфиры. Полиэфиры и полиамиды являются наиболее широко распространенными типами искусственных волокон. Мыла представляют собой соли длинноцепных карбоновых кислот.
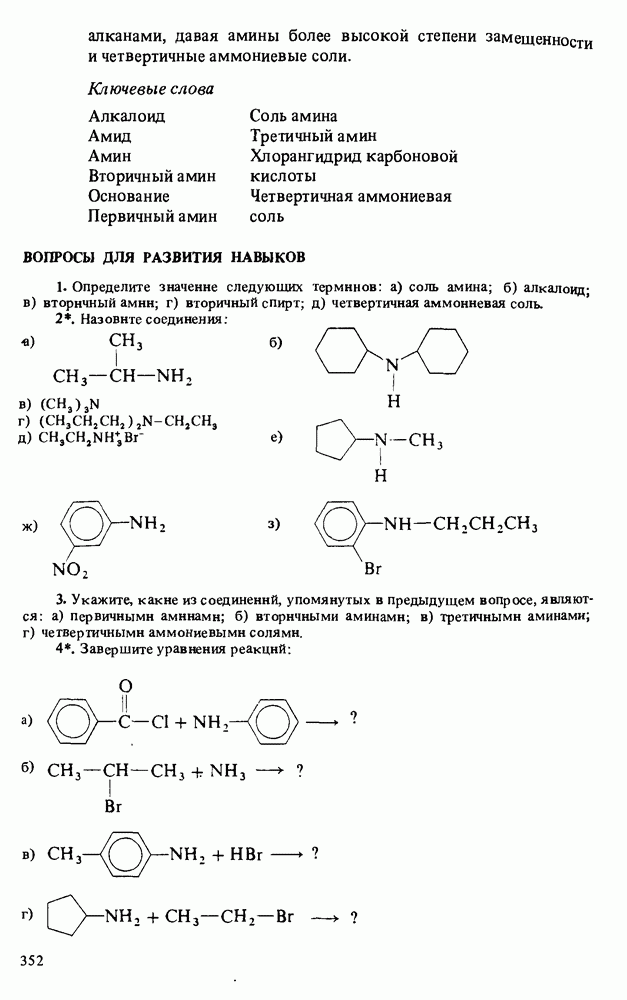
Ключевые слова
(см. скан)
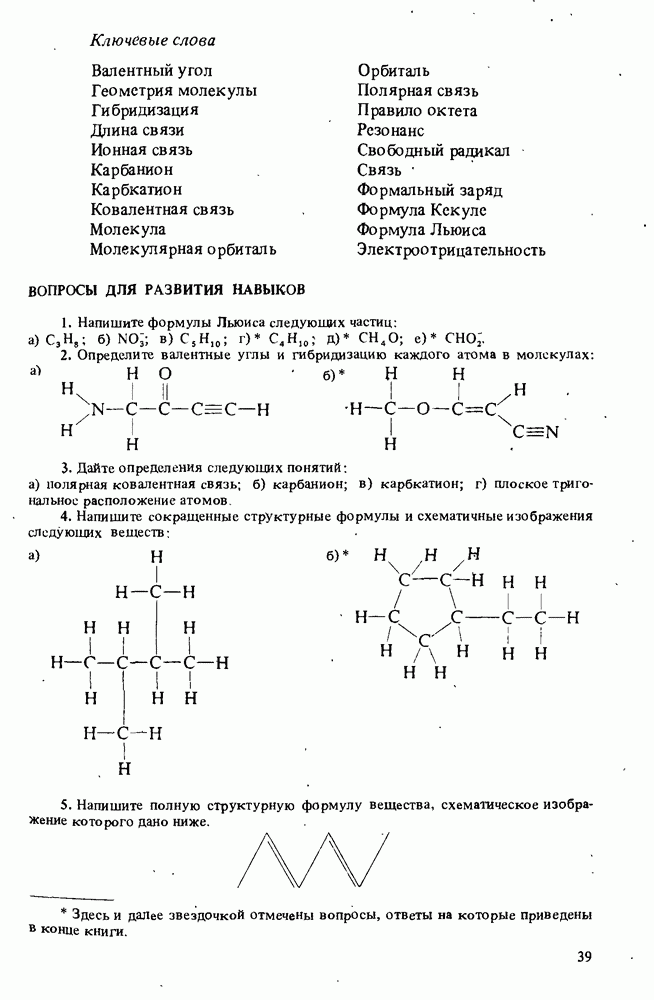
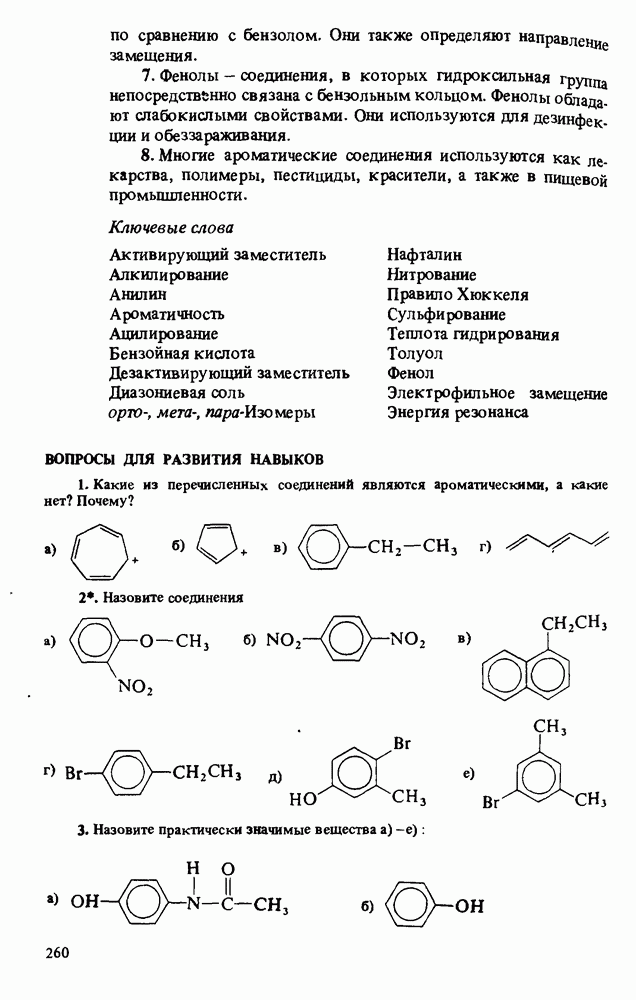
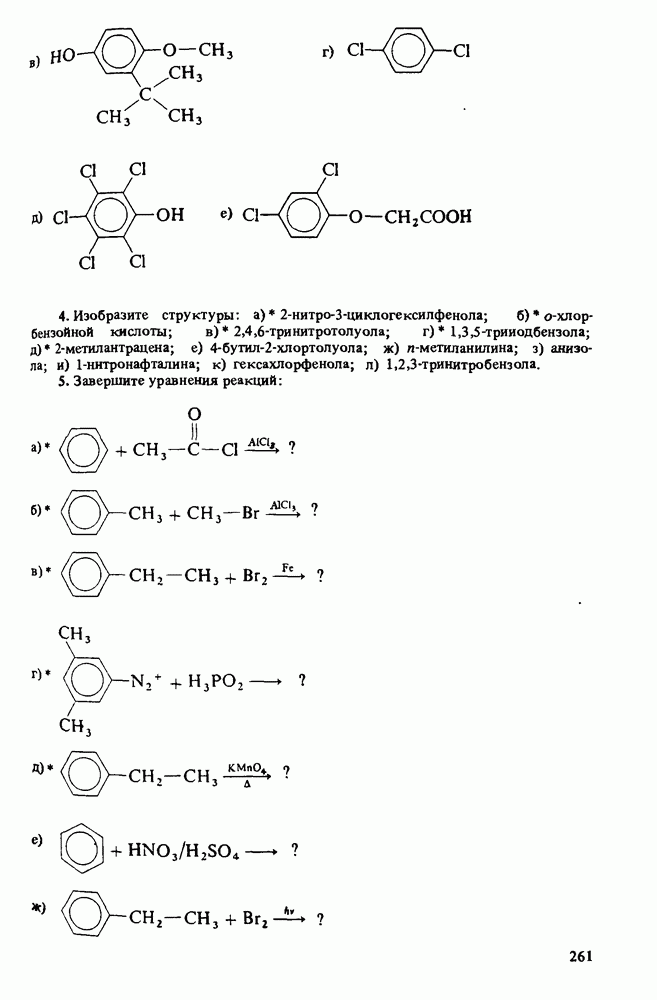
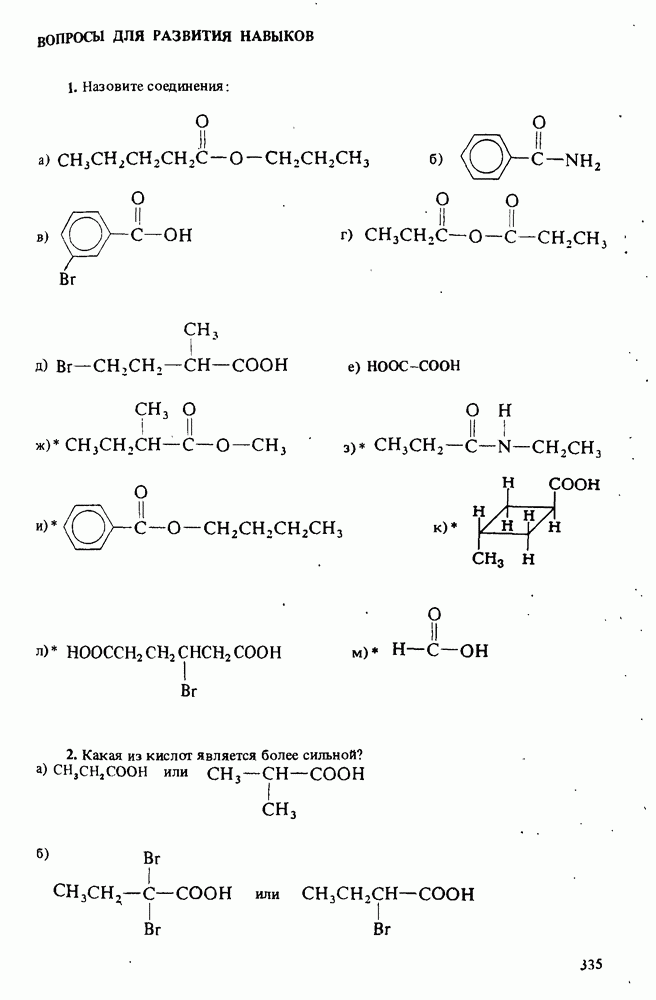
ВОПРОСЫ ДЛЯ РАЗВИТИЯ НАВЫКОВ
(см. скан)
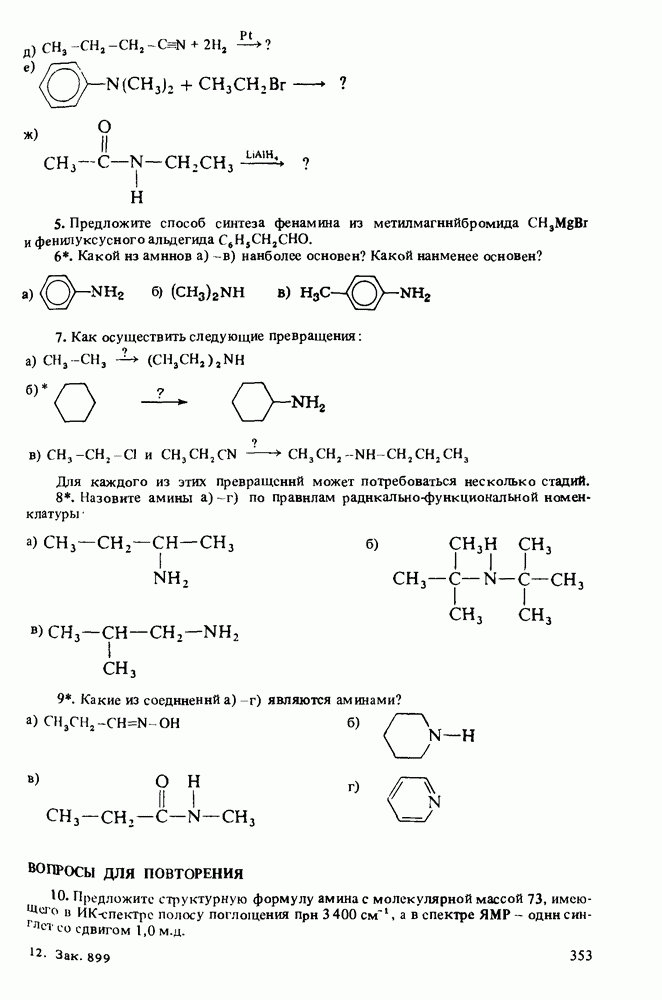
(см. скан)
(см. скан)
(см. скан)
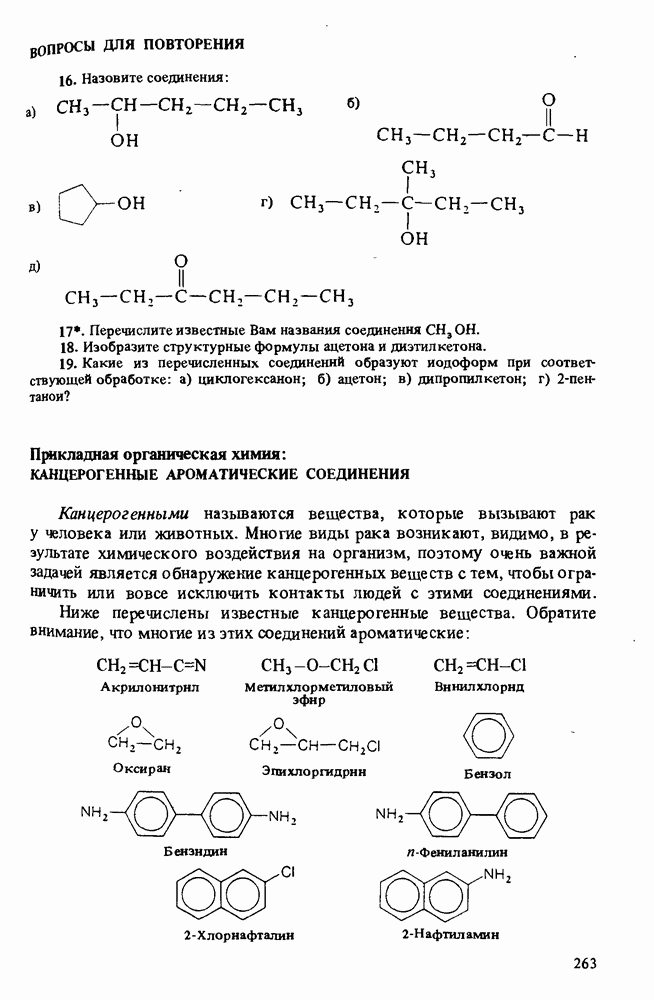
ВОПРОСЫ ДЛЯ ПОВТОРЕНИЯ
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Глава 1. КЛЮЧЕВЫЕ ПОНЯТИЯ ХИМИИ
- АТОМНАЯ ТЕОРИЯ
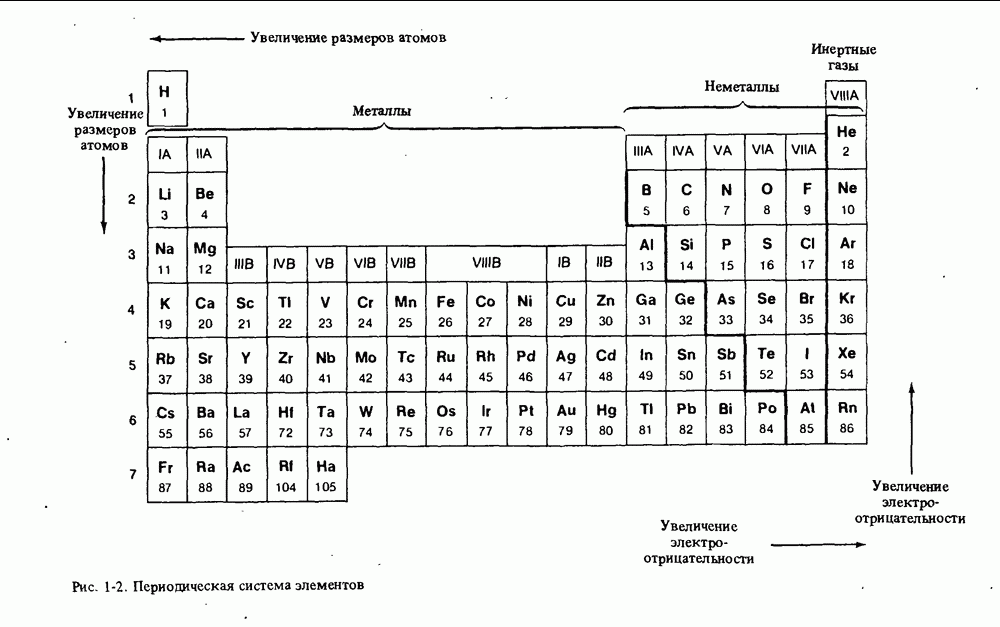
- ПЕРИОДИЧЕСКАЯ СИСТЕМА
- ХИМИЧЕСКАЯ СВЯЗЬ
- ФОРМУЛЫ ЛЬЮИСА
- ФОРМАЛЬНЫЙ ЗАРЯД
- РЕЗОНАНС
- ГЕОМЕТРИЯ МОЛЕКУЛ
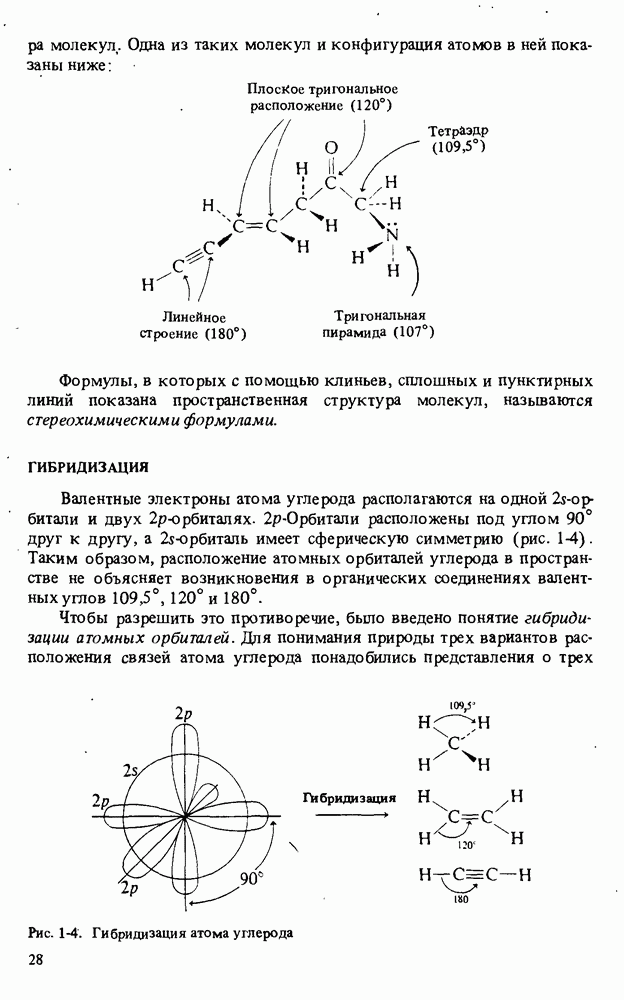
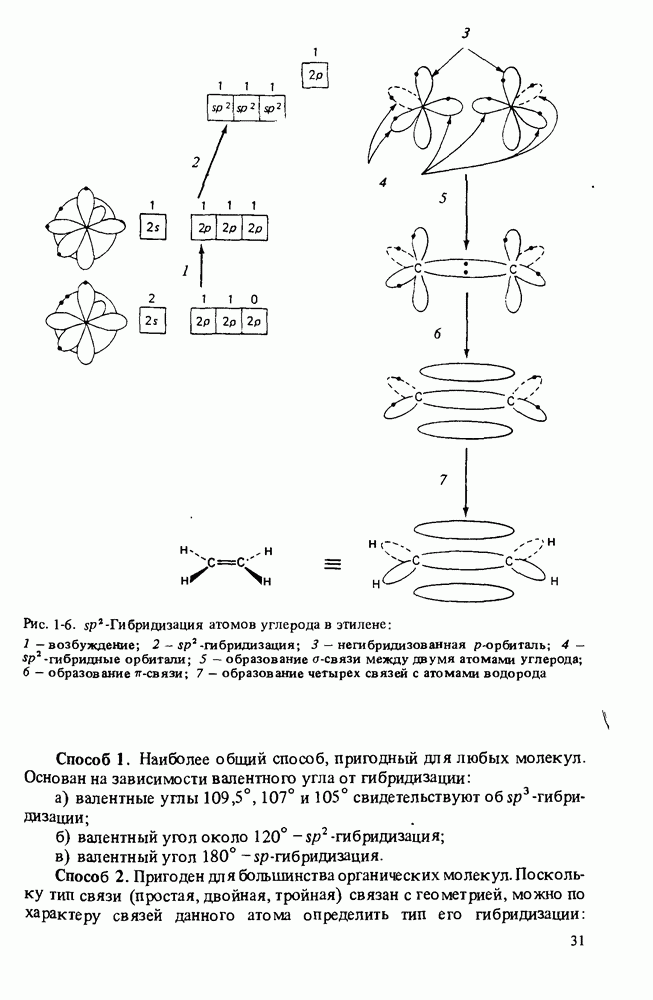
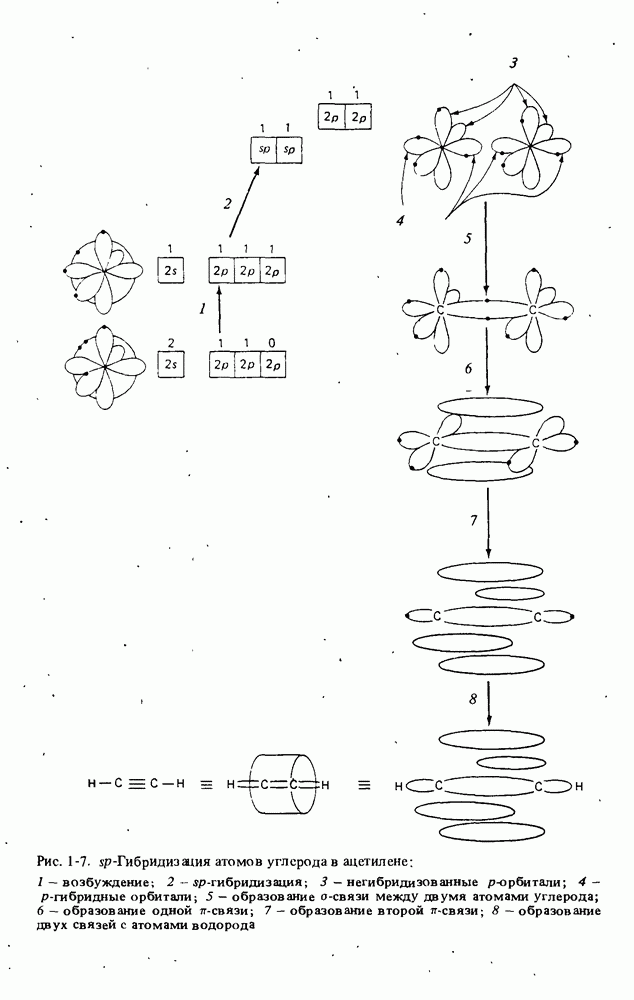
- ГИБРИДИЗАЦИЯ
- ХИМИЧЕСКИЕ ФОРМУЛЫ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 1
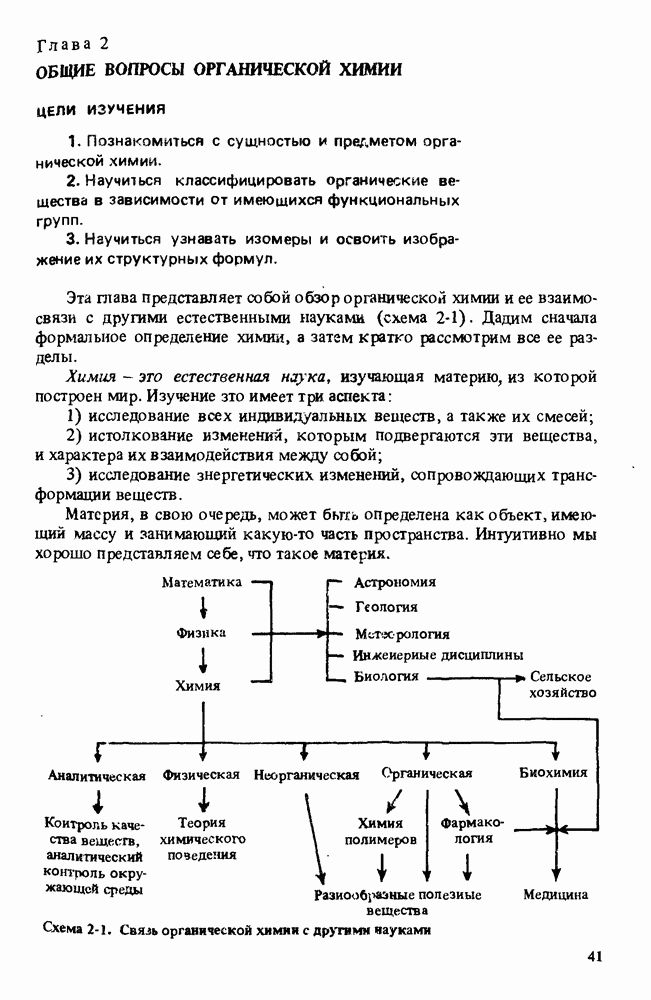
- Глава 2. ОБЩИЕ ВОПРОСЫ ОРГАНИЧЕСКОЙ ХИМИИ
- РАЗДЕЛЫ ХИМИИ
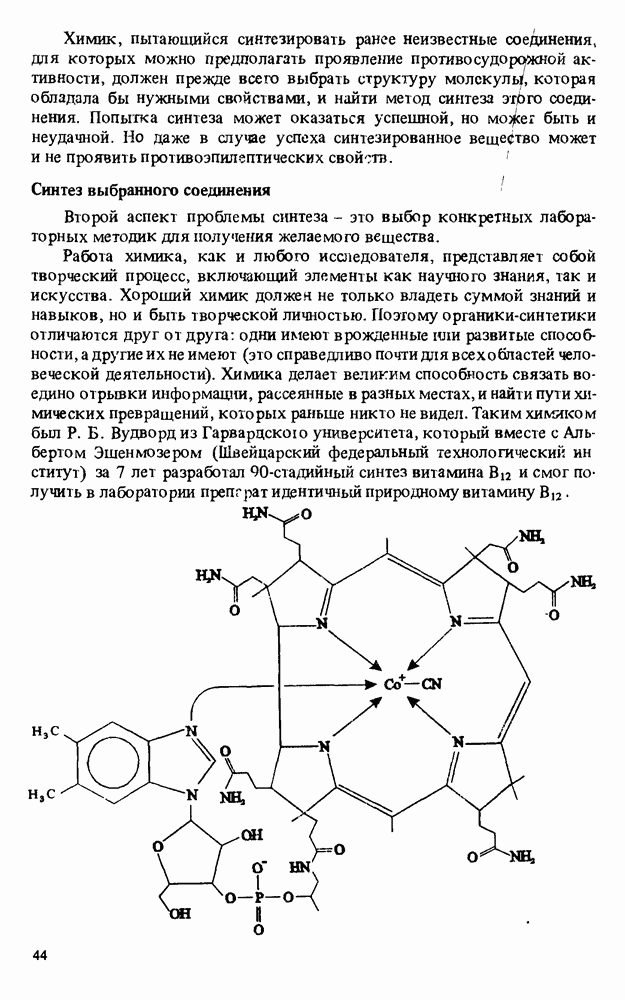
- СИНТЕТИЧЕСКАЯ ОРГАНИЧЕСКАЯ ХИМИЯ
- ПОЛЕЗНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА
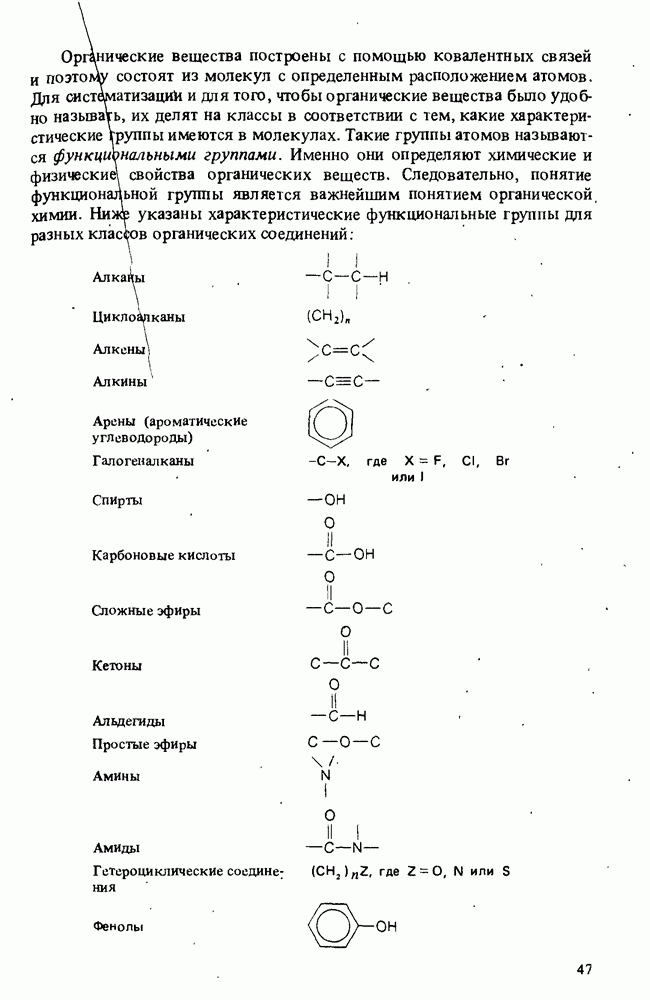
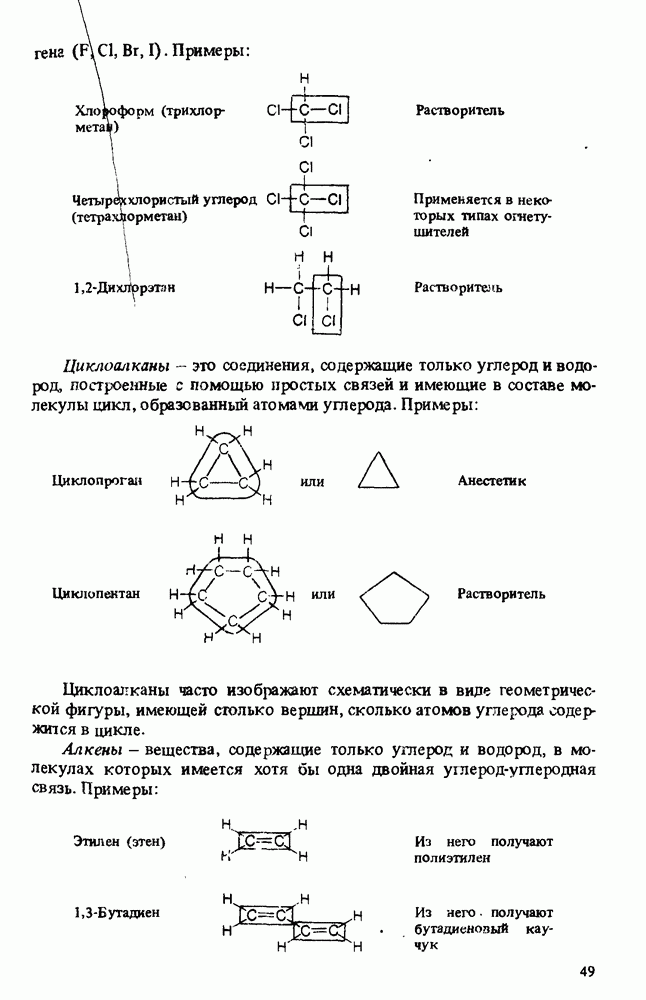
- КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- ИЗОМЕРИЯ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 2
- Прикладная органическая химия: ХИМИЧЕСКИЙ СИНТЕЗ И МЕДИЦИНСКИЕ ИССЛЕДОВАНИЯ
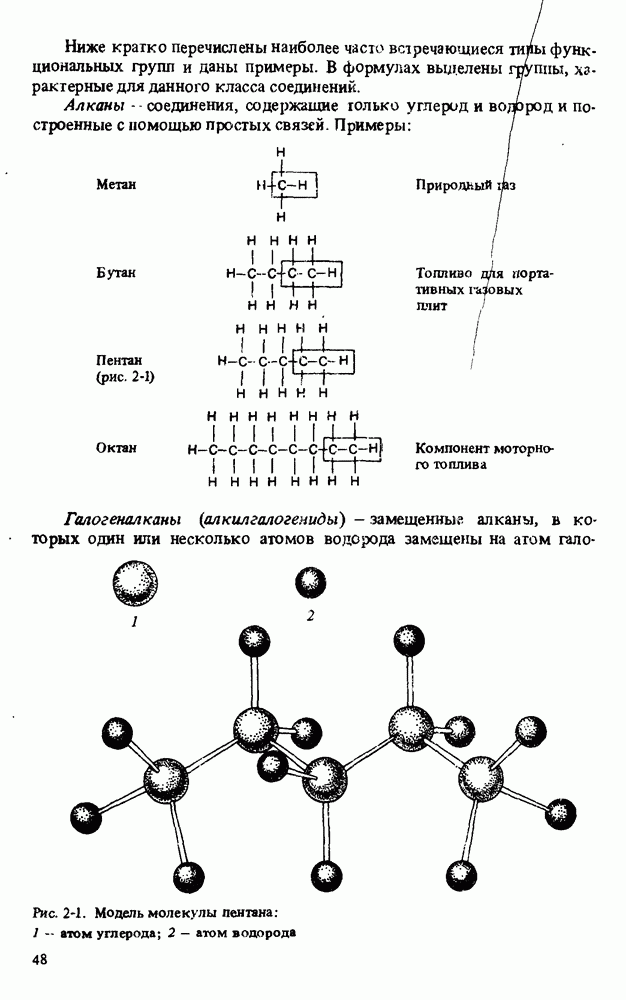
- Глава 3. АЛКАНЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
- СТРОЕНИЕ АЛКАНОВ
- ПОЛУЧЕНИЕ АЛКАНОВ
- РЕАКЦИИ АЛКАНОВ
- ХИМИЯ НЕФТИ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ. ИЗУЧЕНИЕ РЕАКЦИЙ
- Глава 4. СТЕРЕОХИМИЯ И ОПТИЧЕСКАЯ АКТИВНОСТЬ
- СПОСОБЫ ИЗОБРАЖЕНИЯ ЭНАНТИОМЕРОВ
- ОБОЗНАЧЕНИЕ АБСОЛЮТНОЙ КОНФИГУРАЦИИ
- НАЗВАНИЯ ХИРАЛЬНЫХ МОЛЕКУЛ
- ИЗОБРАЖЕНИЕ МОЛЕКУЛ С ПРОТИВОПОЛОЖНОЙ КОНФИГУРАЦИЕЙ
- D,L-НОМЕНКЛАТУРА ЭНАНТИОМЕРОВ
- ТЕРМИНОЛОГИЯ, ПРИМЕНЯЕМАЯ В СТЕРЕОХИМИИ
- ЗНАЧЕНИЕ ОПТИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ
- Глава 5. ОРГАНИЧЕСКИЕ ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- ПОЛУЧЕНИЕ ГАЛОГЕНАЛКАНОВ
- РЕАКЦИИ ГАЛОГЕНАЛКАНОВ
- ПРАКТИЧЕСКИ ВАЖНЫЕ ГАЛОГЕНАЛКАНЫ
- Прикладная органическая химия: ОРГАНИЧЕСКИЕ ПЕСТИЦИДЫ
- Глава 6. НЕНАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
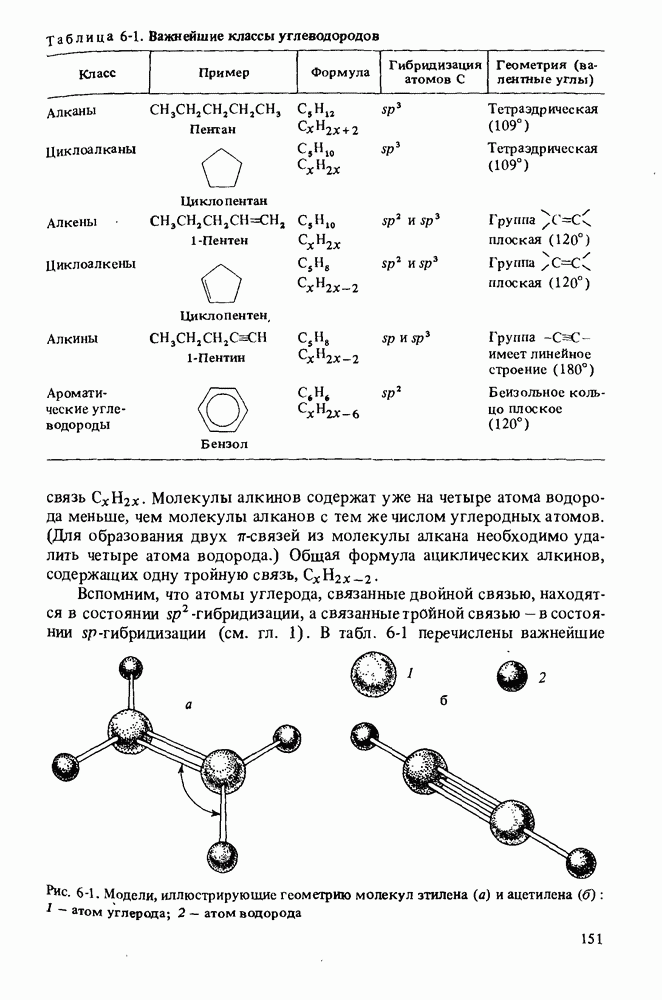
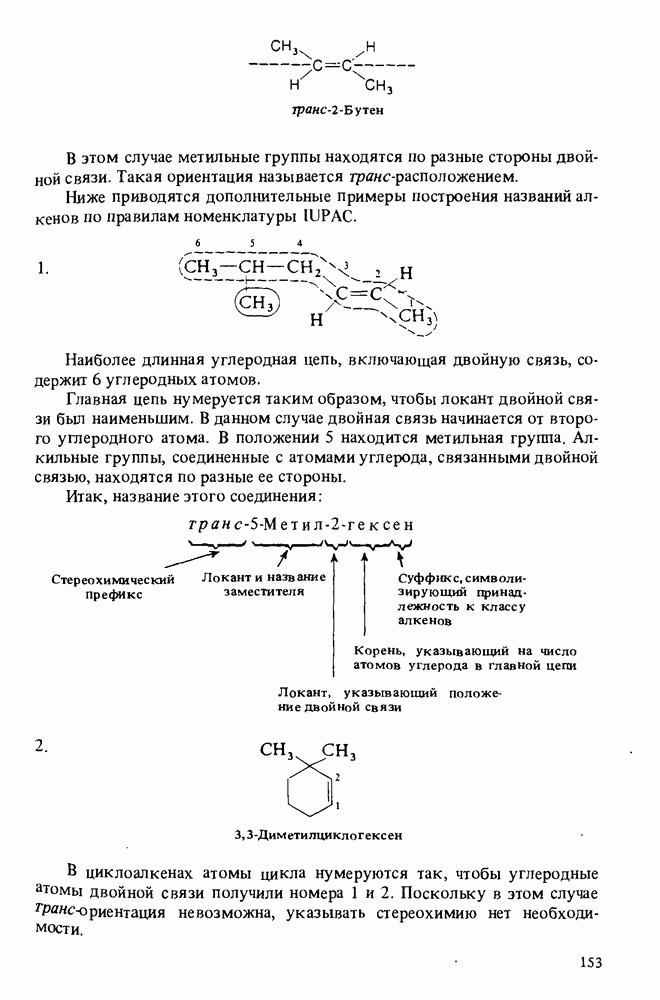
- НОМЕНКЛАТУРА АЛКЕНОВ
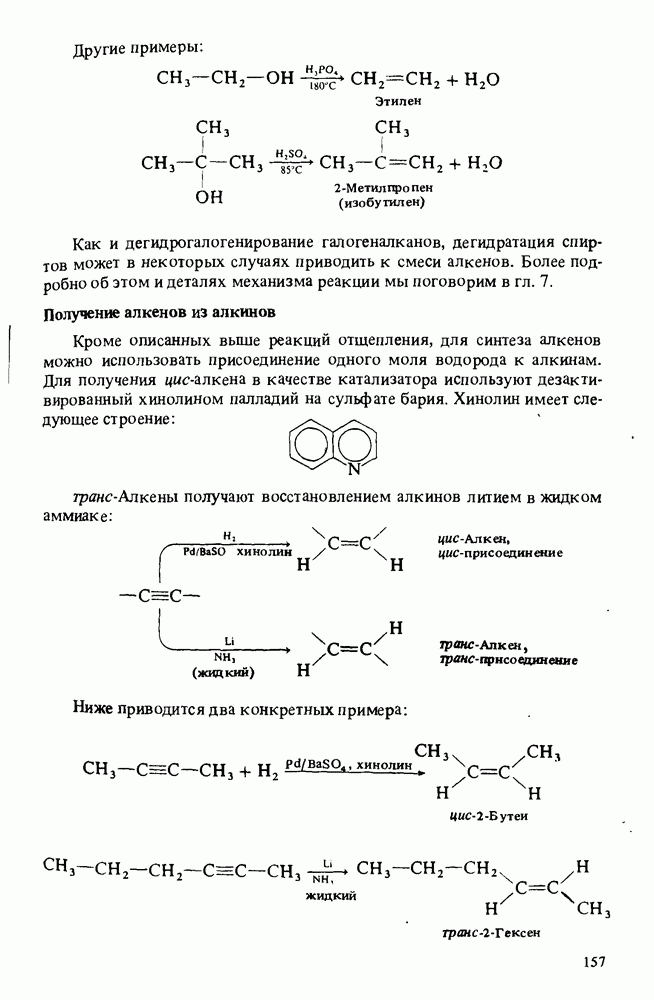
- ПОЛУЧЕНИЕ АЛКЕНОВ
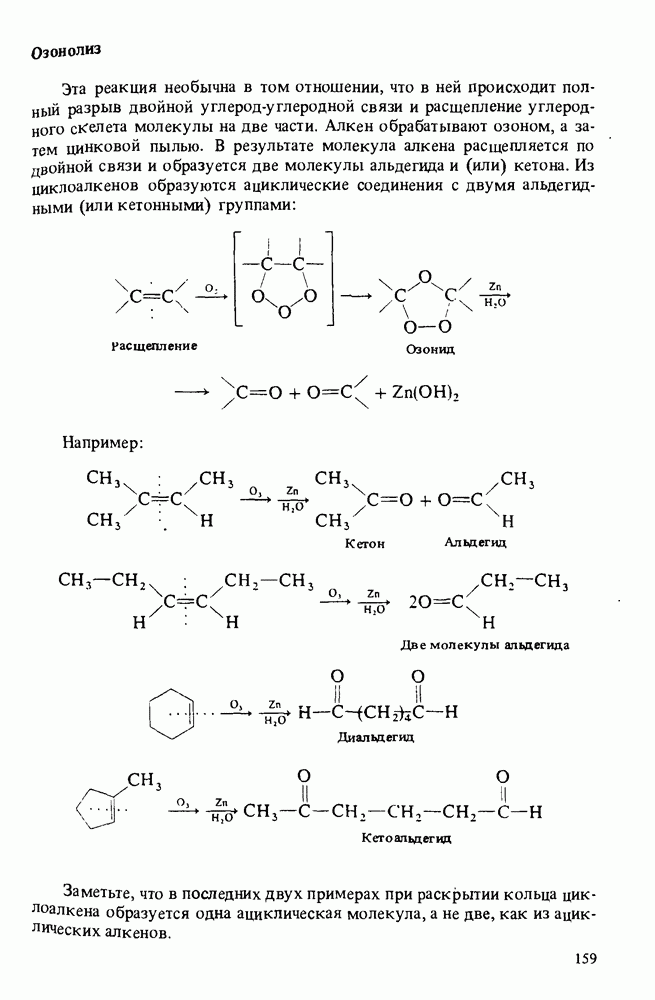
- ОСНОВНЫЕ РЕАКЦИИ АЛКЕНОВ
- ПОЛИМЕРЫ
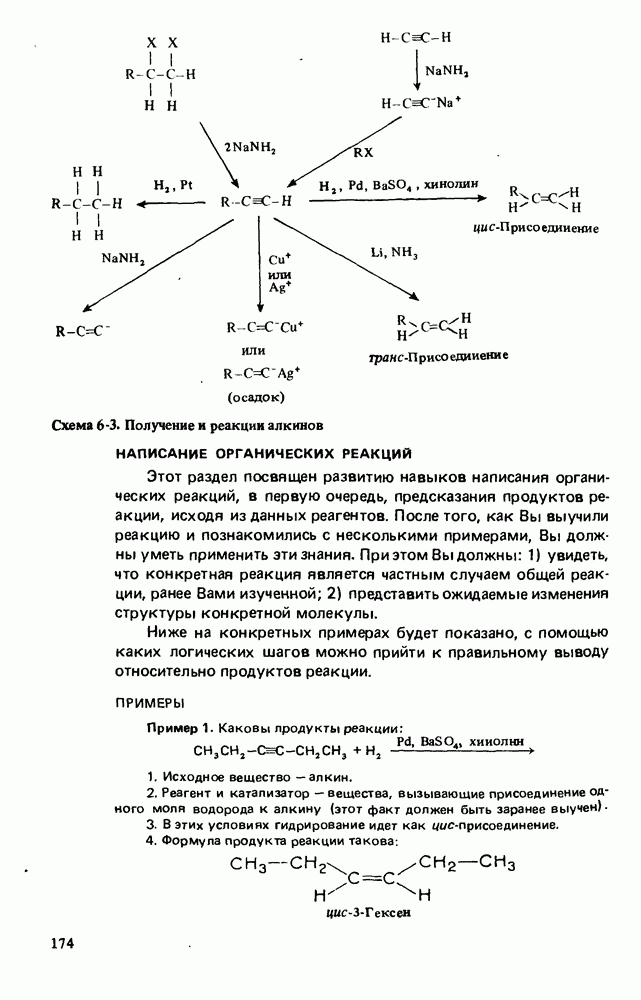
- НОМЕНКЛАТУРА АЛКИНОВ
- ПОЛУЧЕНИЕ АЛКИНОВ
- РЕАКЦИИ АЛКИНОВ
- НАПИСАНИЕ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- Глава 7. СПИРТЫ И ПРОСТЫЕ ЭФИРЫ
- НОМЕНКЛАТУРА СПИРТОВ
- НЕКОТОРЫЕ ВАЖНЫЕ ВЕЩЕСТВА, СОДЕРЖАЩИЕ СПИРТОВУЮ ГРУППУ
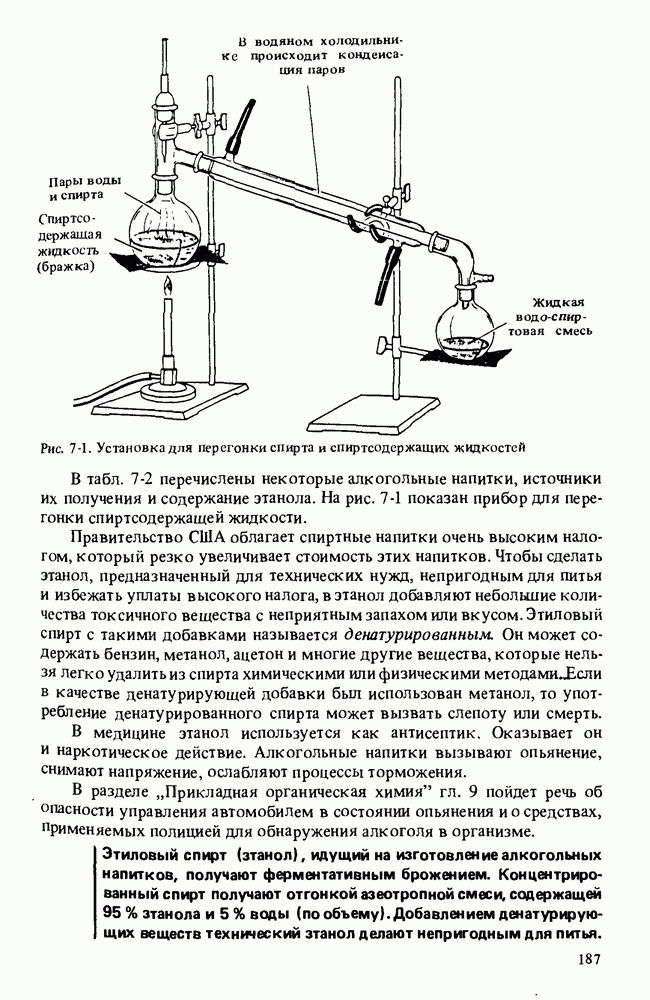
- ЭТИЛОВЫЙ СПИРТ. ПРОИЗВОДСТВО СПИРТНЫХ НАПИТКОВ
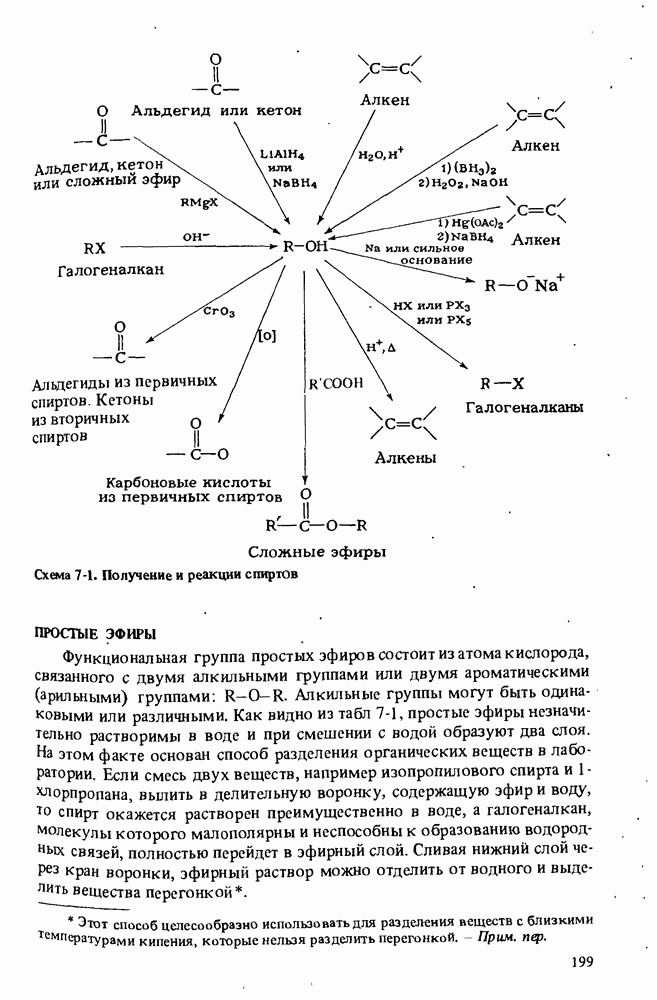
- ПОЛУЧЕНИЕ СПИРТОВ
- РЕАКЦИИ СПИРТОВ
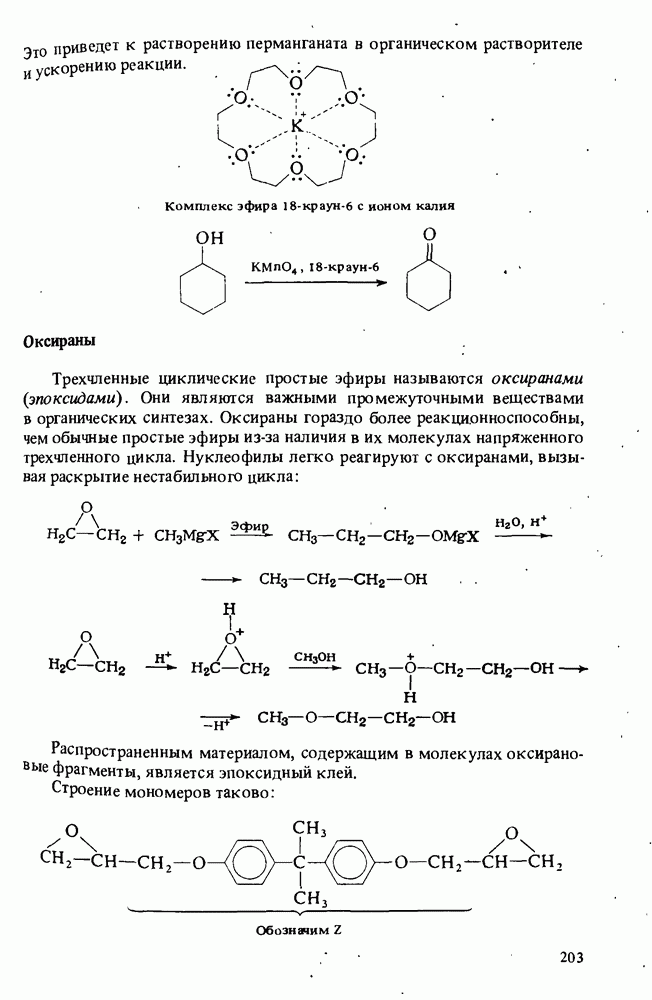
- ПРОСТЫЕ ЭФИРЫ
- Прикладная органическая химия: ВЕЩЕСТВА, ОБЛАДАЮЩИЕ АЛЛЕЛОХИМИЧЕСКИМ ДЕЙСТВИЕМ. ФЕРОМОНЫ
- Глава 8. АЛЬДЕГИДЫ И КЕТОНЫ
- ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ
- РЕАКЦИИ АЛЬДЕГИДОВ И КЕТОНОВ
- Глава 9. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- НОМЕНКЛАТУРА АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ
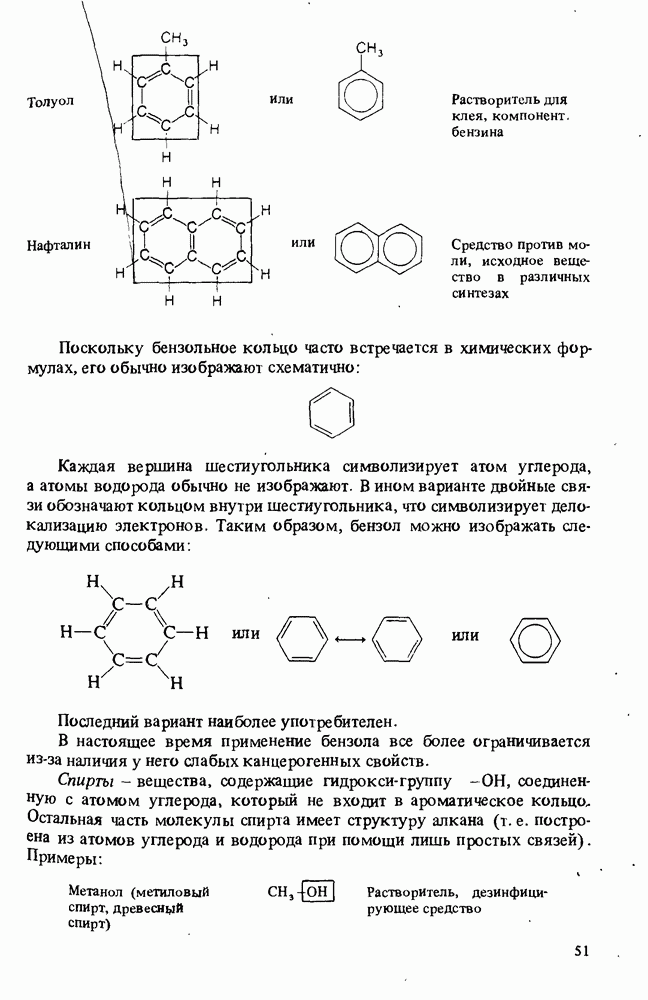
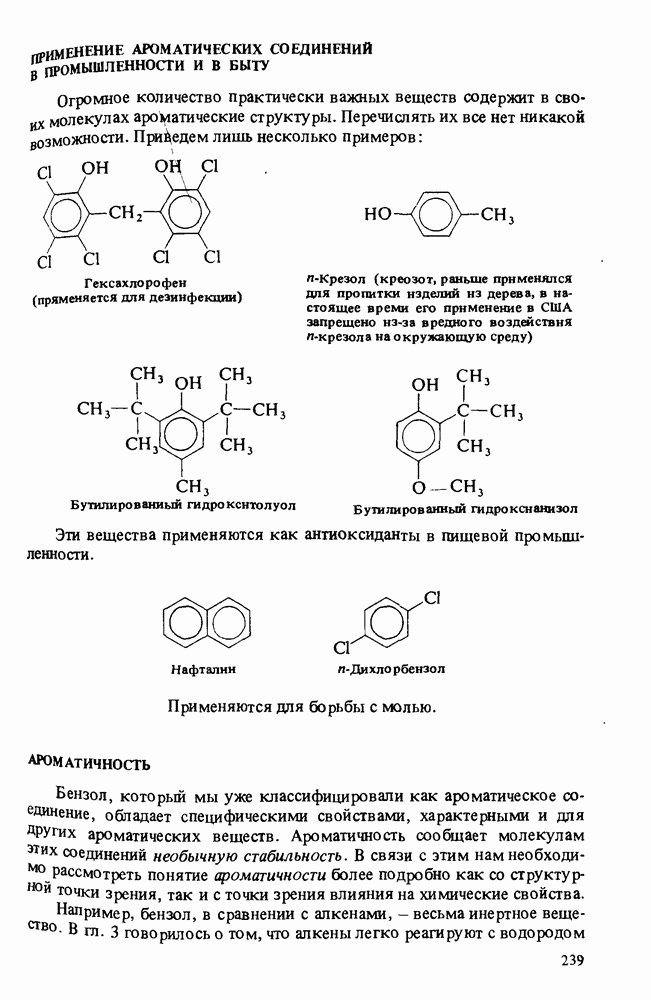
- ПРИМЕНЕНИЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ В ПРОМЫШЛЕННОСТИ И В БЫТУ
- АРОМАТИЧНОСТЬ
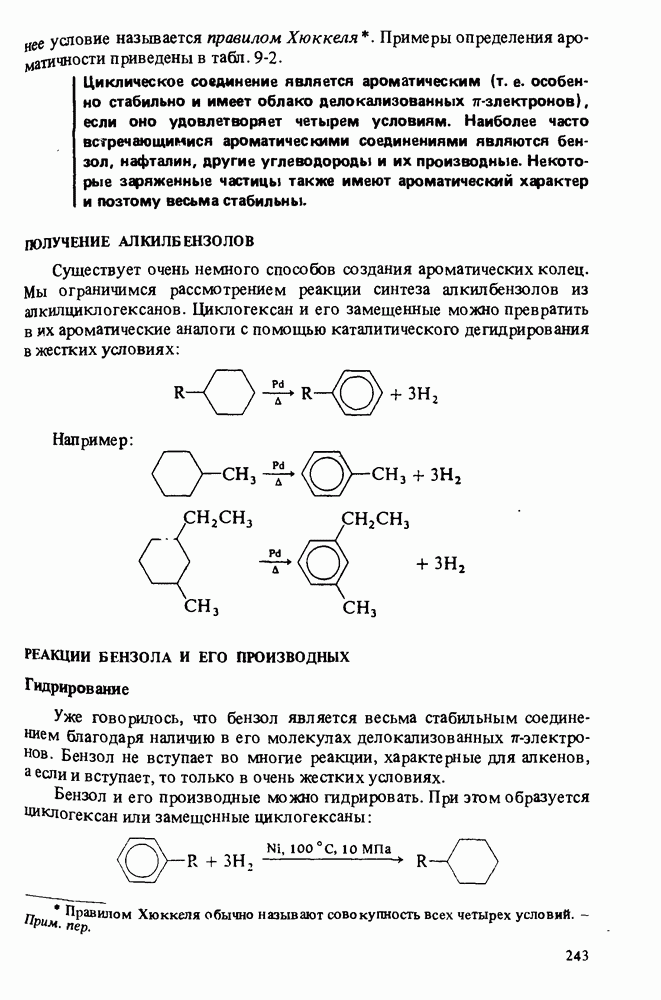
- ПОЛУЧЕНИЕ АЛКИЛЬБЕНЗОЛОВ
- РЕАКЦИИ БЕНЗОЛА И ЕГО ПРОИЗВОДНЫХ
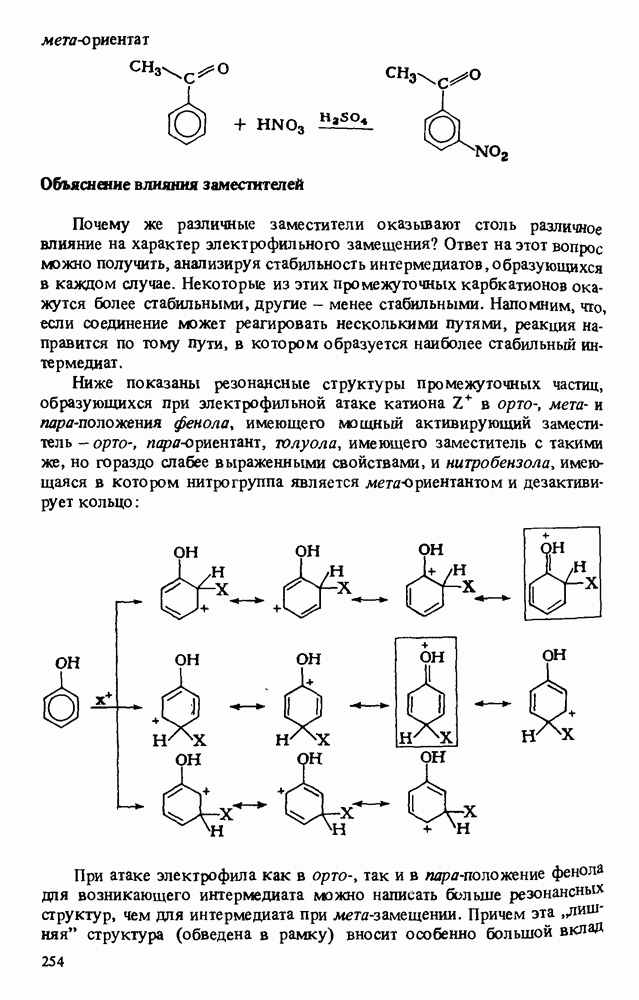
- АРОМАТИЧЕСКОЕ ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ
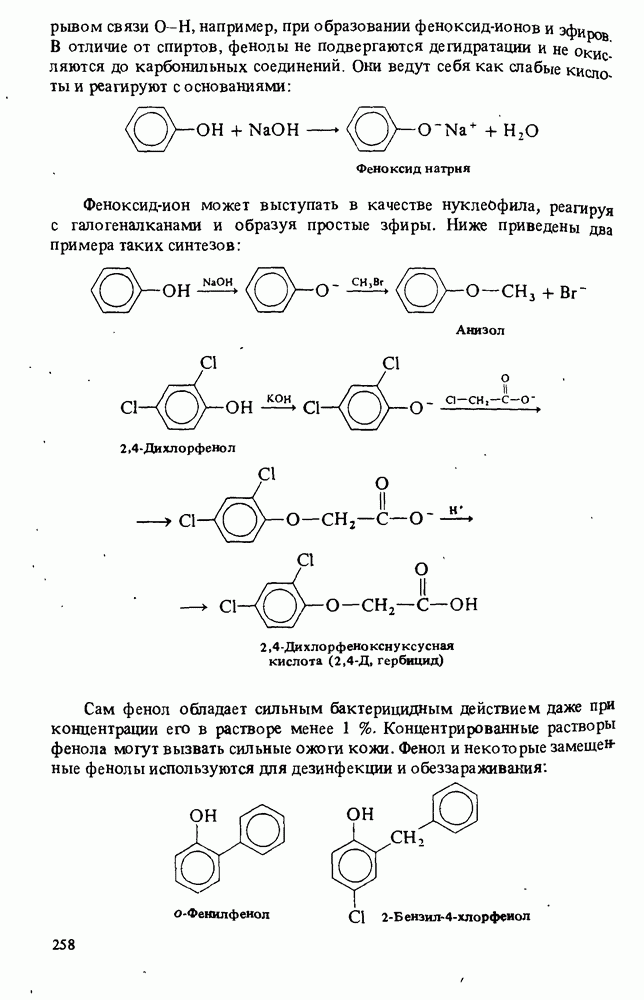
- ФЕНОЛЫ
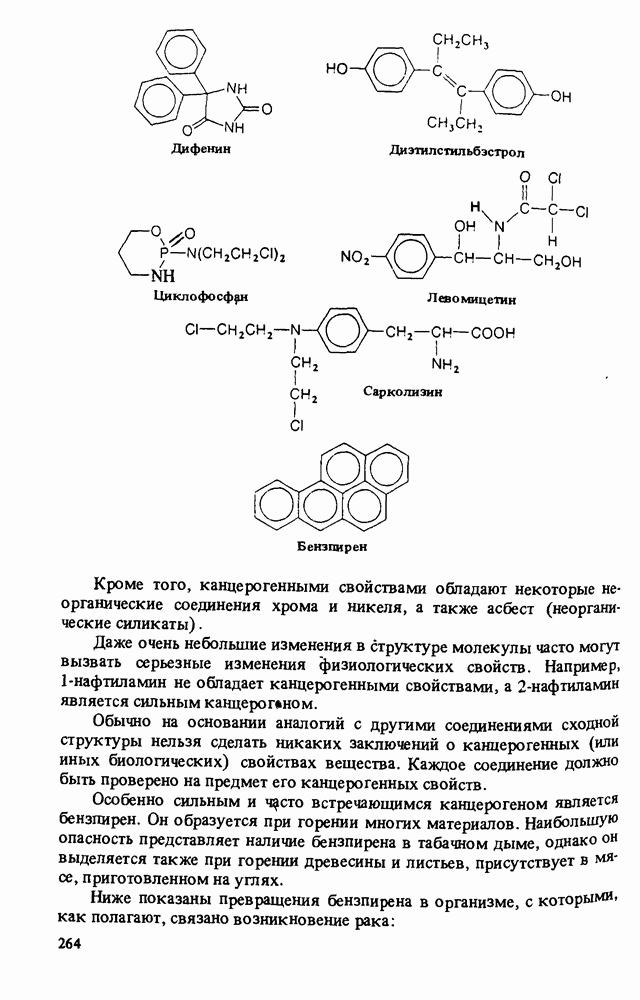
- Прикладная органическая химия: КАНЦЕРОГЕННЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- Глава 10. ОРГАНИЧЕСКИЙ СИНТЕЗ
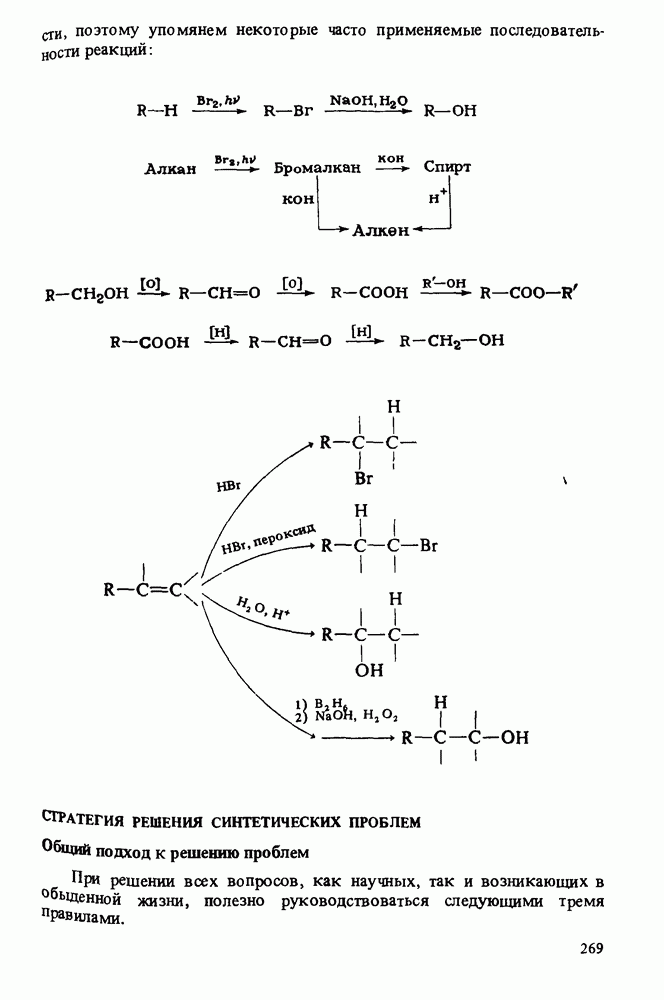
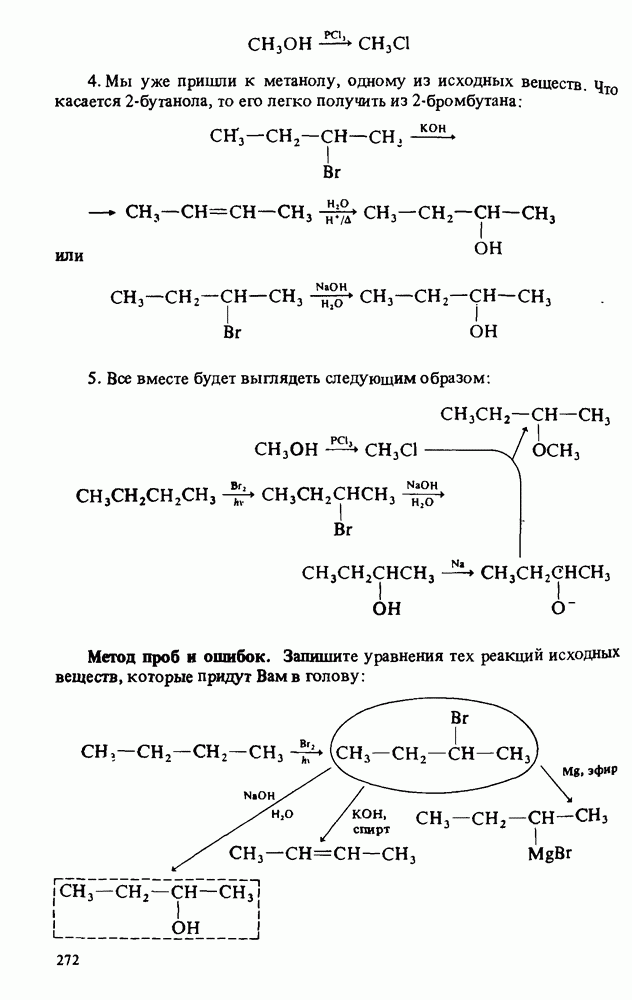
- СТРАТЕГИЯ РЕШЕНИЯ СИНТЕТИЧЕСКИХ ПРОБЛЕМ
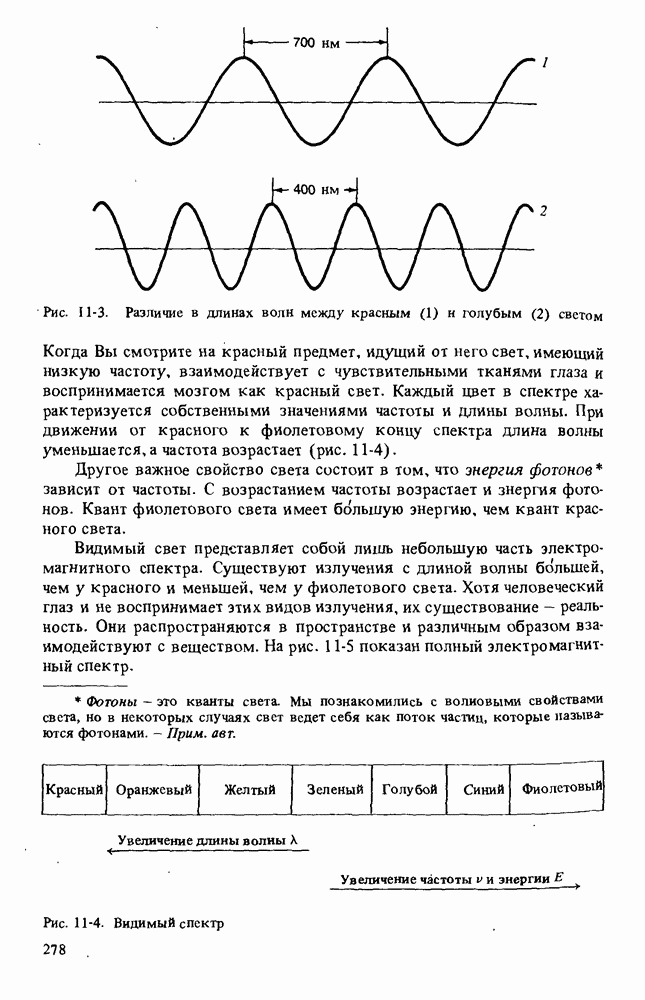
- Глава 11. МОЛЕКУЛЯРНАЯ СПЕКТРОСКОПИЯ
- ИНФРАКРАСНАЯ СПЕКТРОСКОПИЯ
- СПЕКТРОСКОПИЯ ЯДЕРНОГО МАГНИТНОГО РЕЗОНАНСА
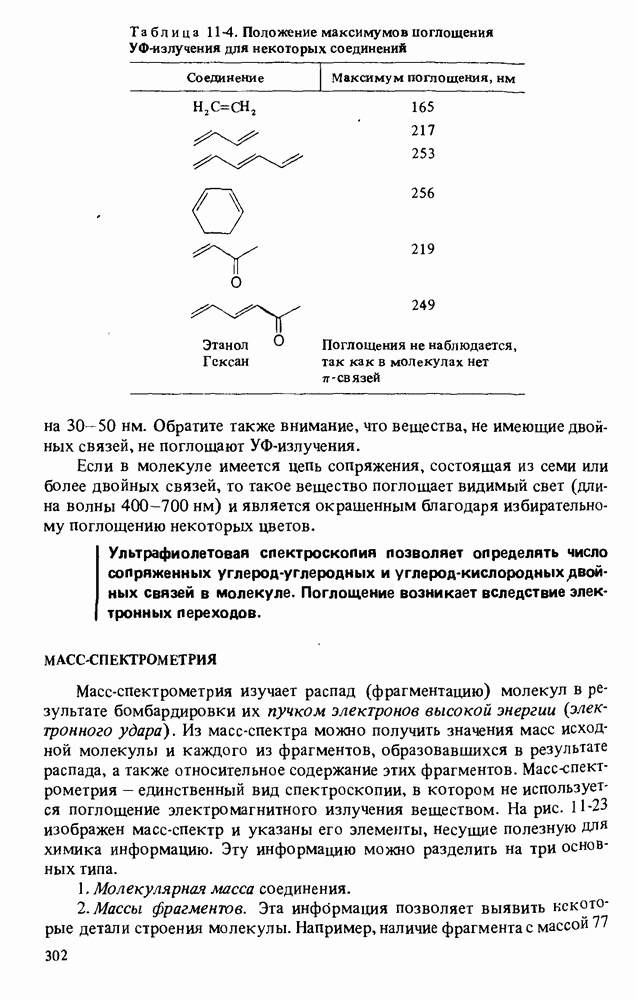
- УЛЬТРАФИОЛЕТОВАЯ СПЕКТРОСКОПИЯ
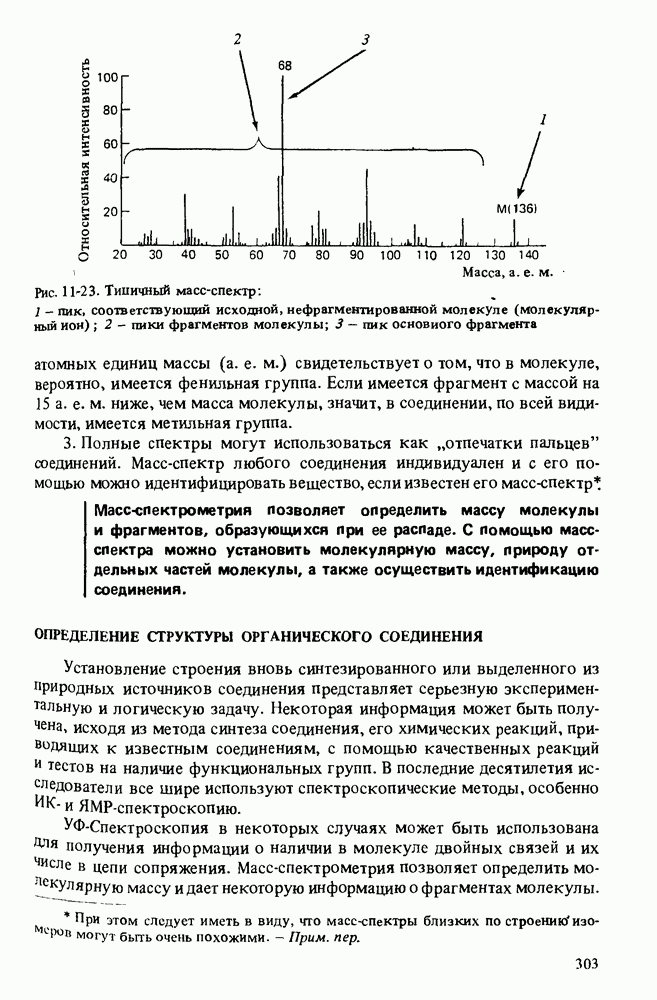
- МАСС-СПЕКТРОМЕТРИЯ
- ОПРЕДЕЛЕНИЕ СТРУКТУРЫ ОРГАНИЧЕСКОГО СОЕДИНЕНИЯ
- Прикладная органическая химия: ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ АЛКОГОЛЯ В КРОВИ
- Глава 12. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
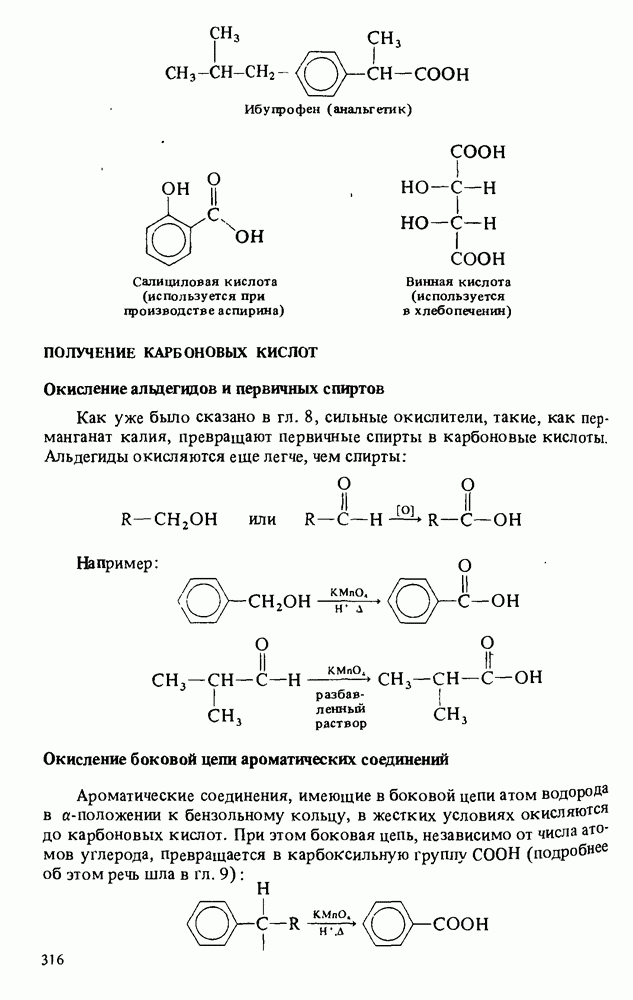
- ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ
- АНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
- ГАЛОГЕНАНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
- СЛОЖНЫЕ ЭФИРЫ
- СОЛИ
- АМИДЫ
- ГИДРОЛИЗ ПРОИЗВОДНЫХ КАРБОНОВЫХ КИСЛОТ
- СИНТЕТИЧЕСКИЕ ВОЛОКНА
- МОЮЩИЕ СРЕДСТВА
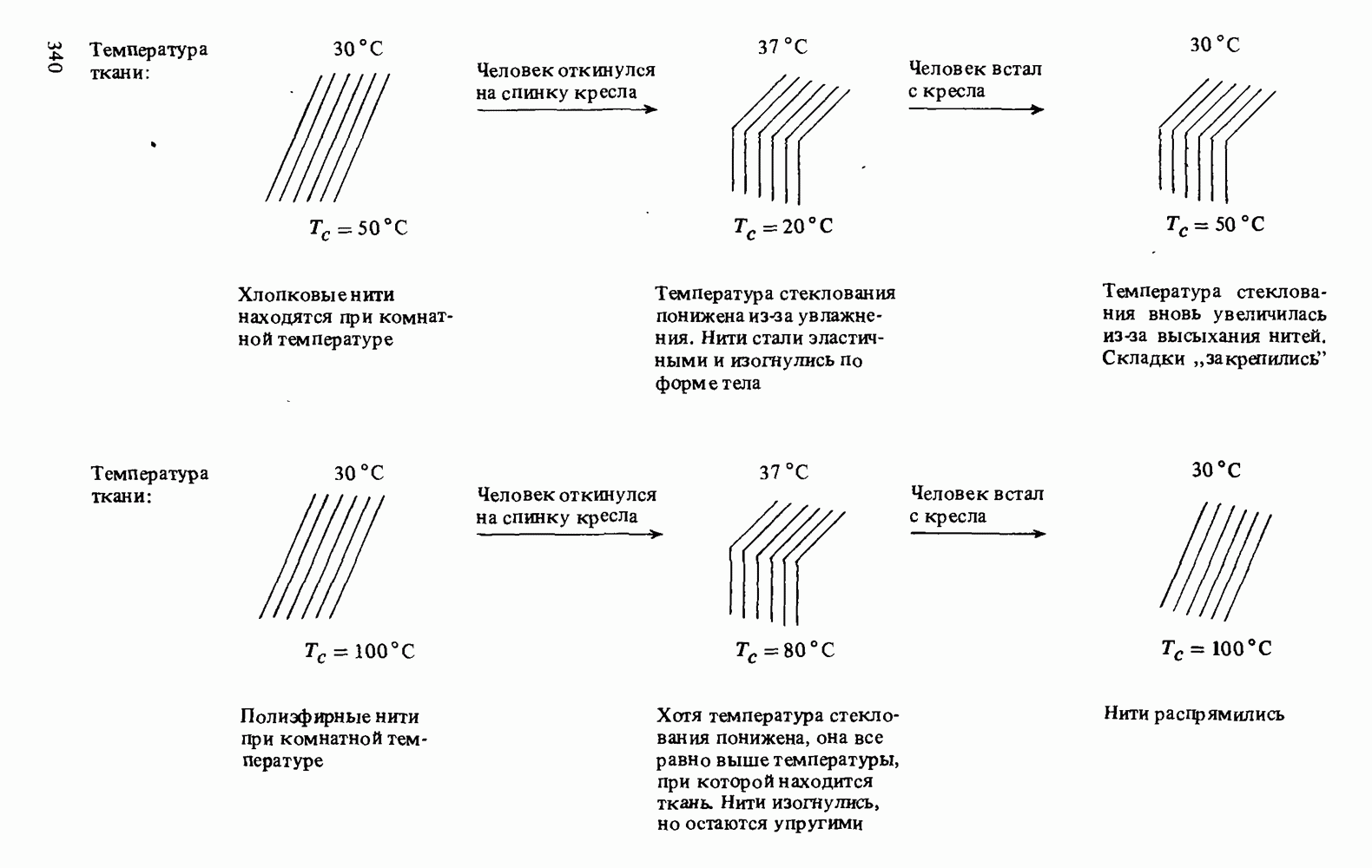
- Прикладная органическая химия: СВОЙСТВА ВОЛОКОН
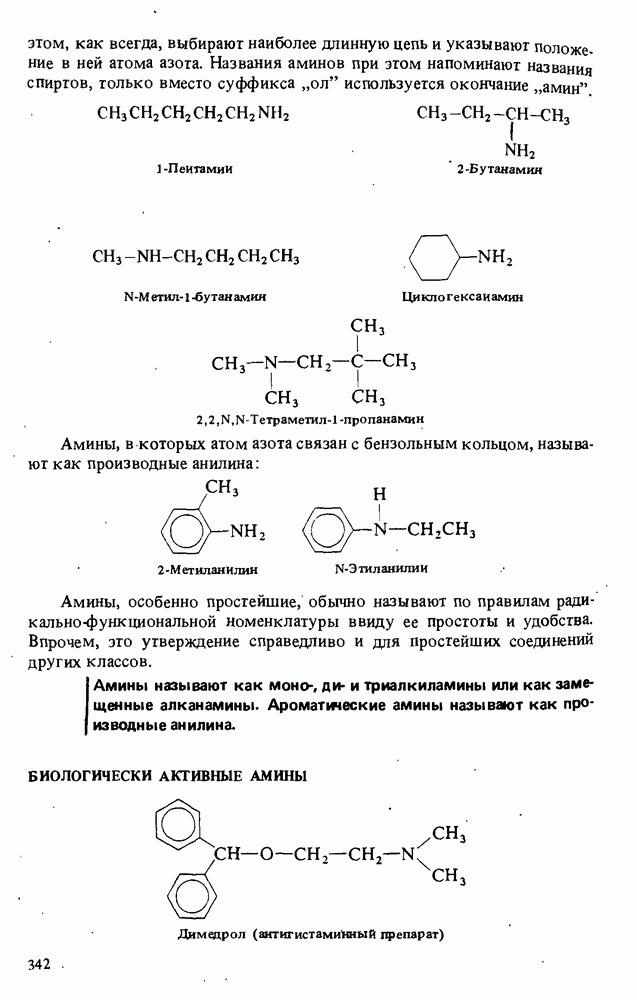
- Глава 13. АМИНЫ
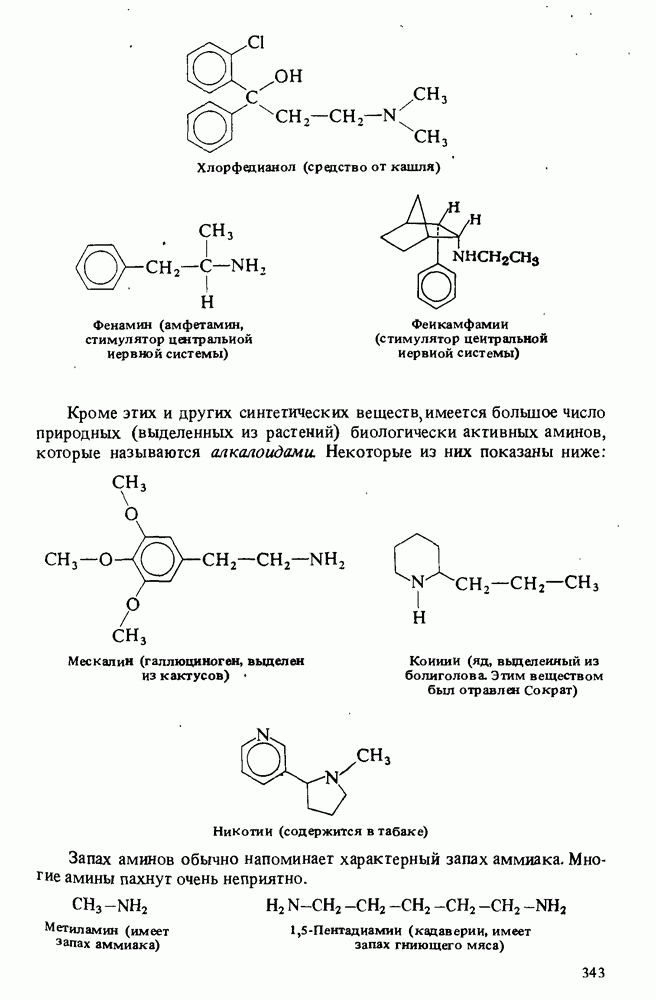
- БИОЛОГИЧЕСКИ АКТИВНЫЕ АМИНЫ
- ОСНОВНОСТЬ АМИНОВ
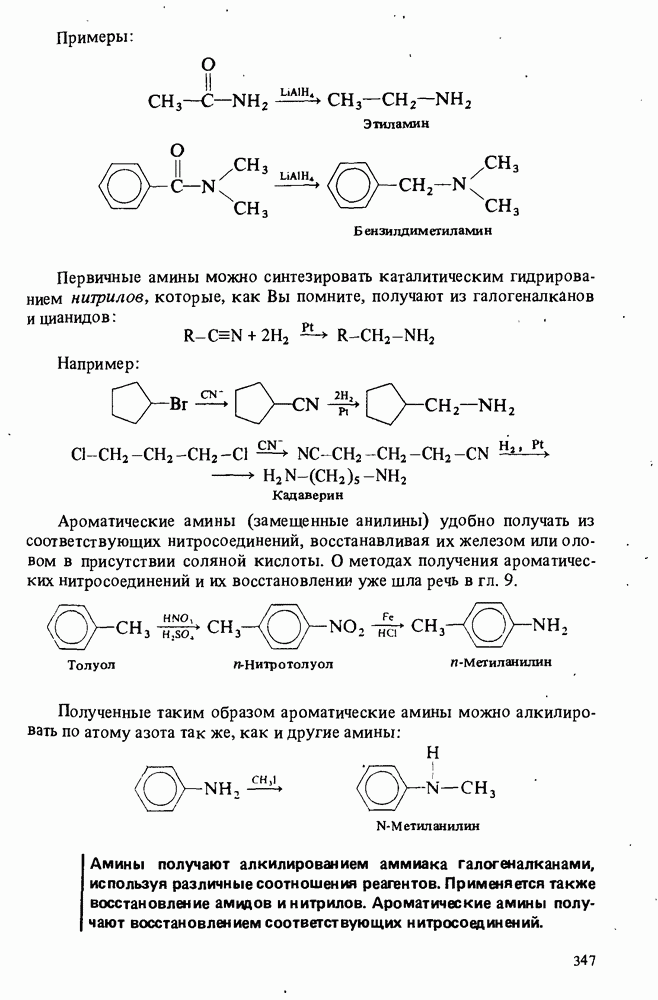
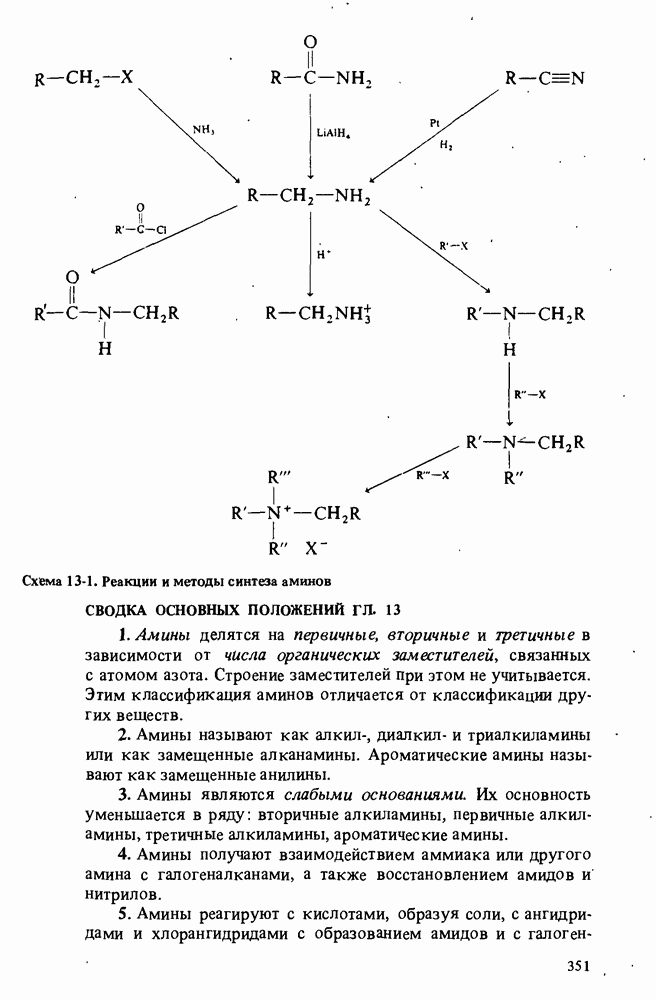
- ПОЛУЧЕНИЕ АМИНОВ
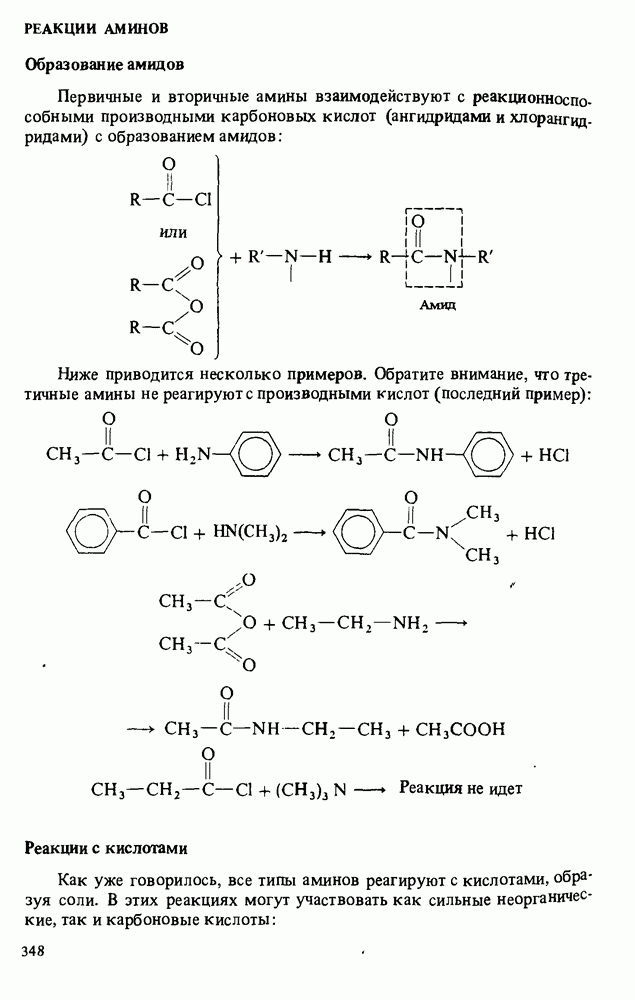
- РЕАКЦИИ АМИНОВ
- Прикладная органическая химия: ПОЛИМЕРЫ, ПОДВЕРГАЮЩИЕСЯ БИОЛОГИЧЕСКОЙ ДЕСТРУКЦИИ
- Глава 14. УГЛЕВОДЫ
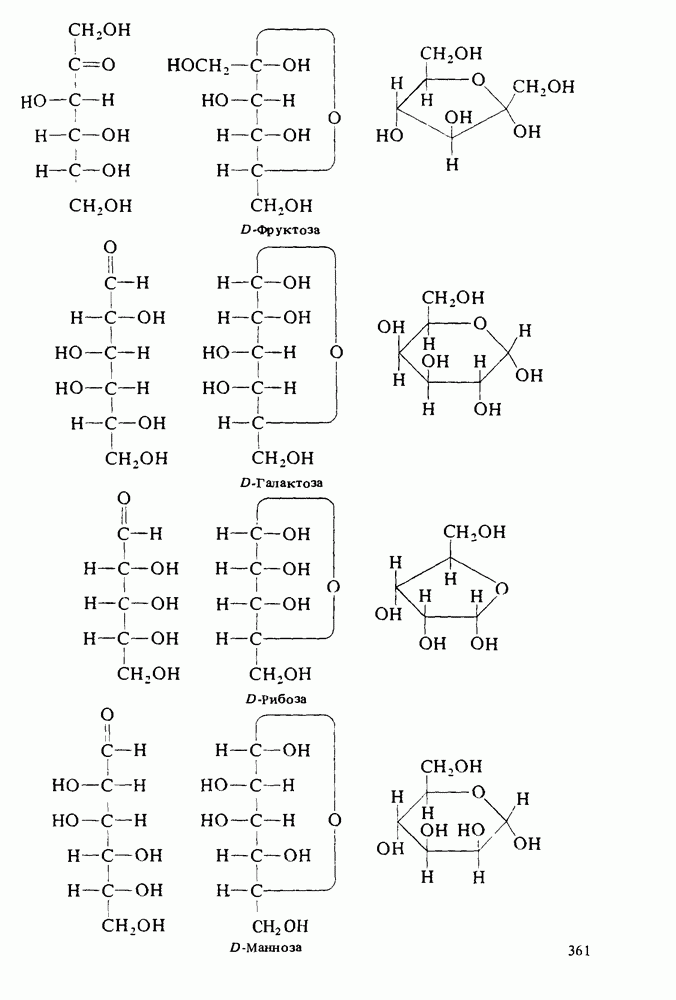
- МОНОСАХАРИДЫ
- РЕАКЦИИ МОНОСАХАРИДОВ
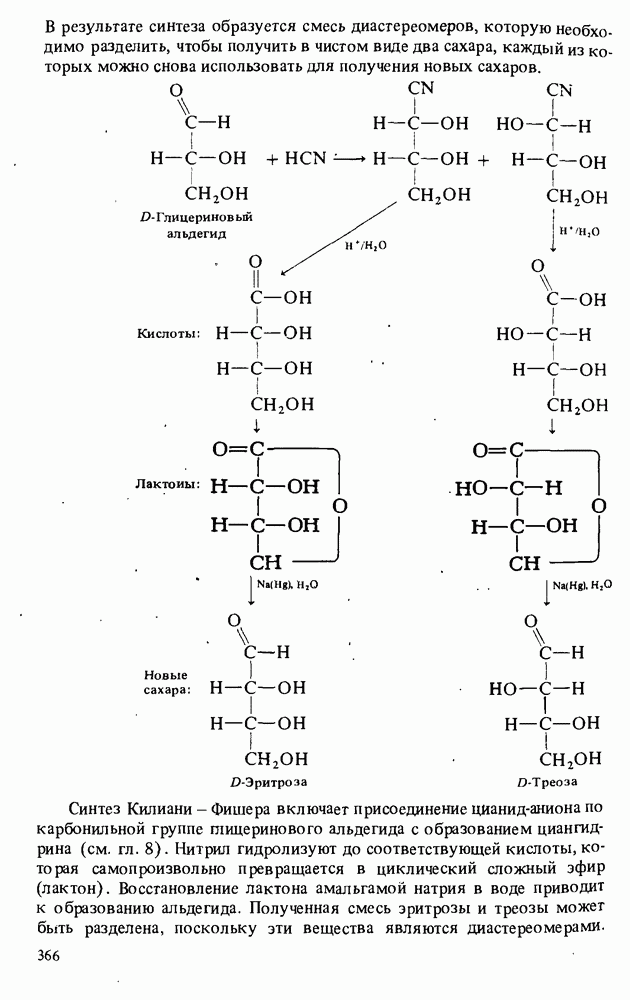
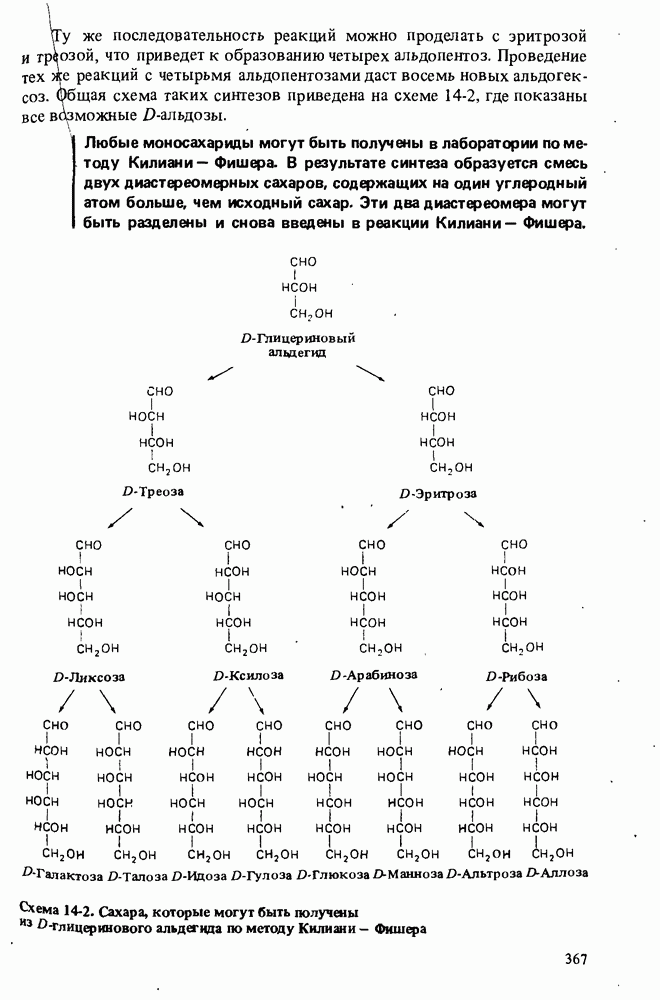
- СИНТЕЗЫ САХАРОВ
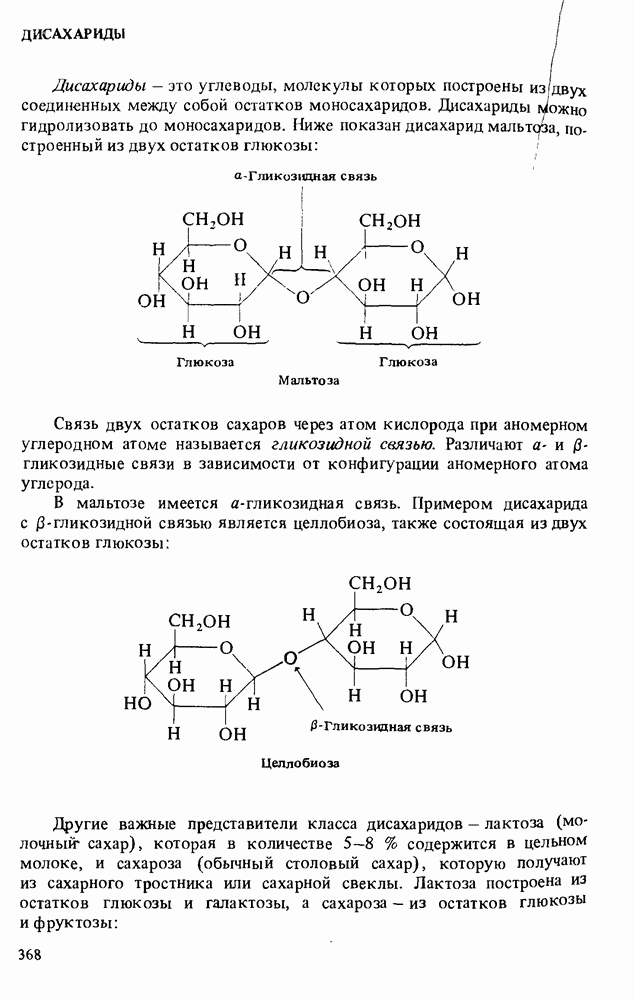
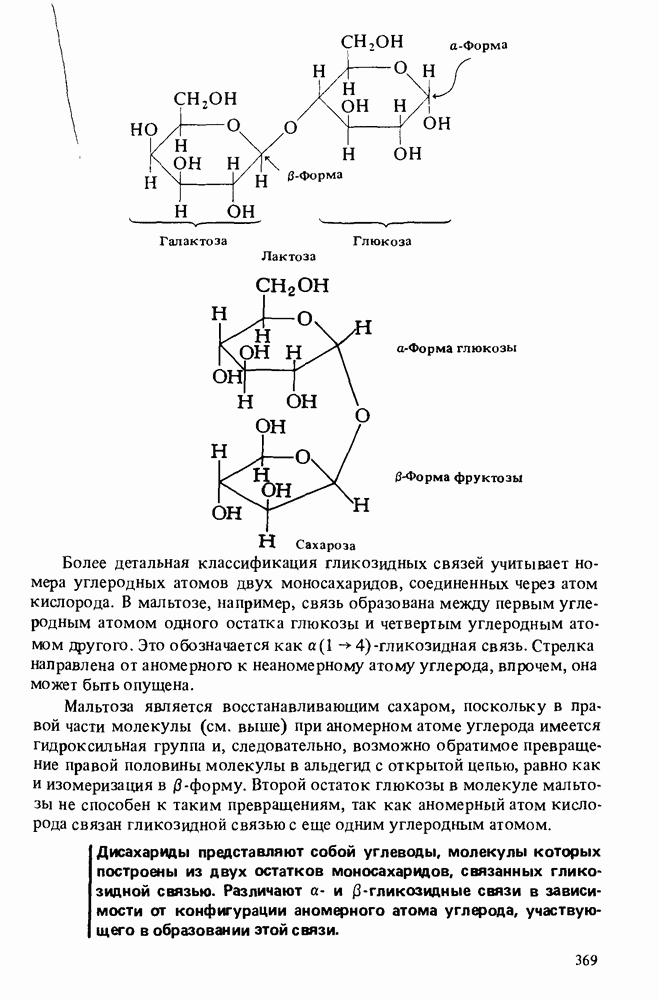
- ДИСАХАРИДЫ
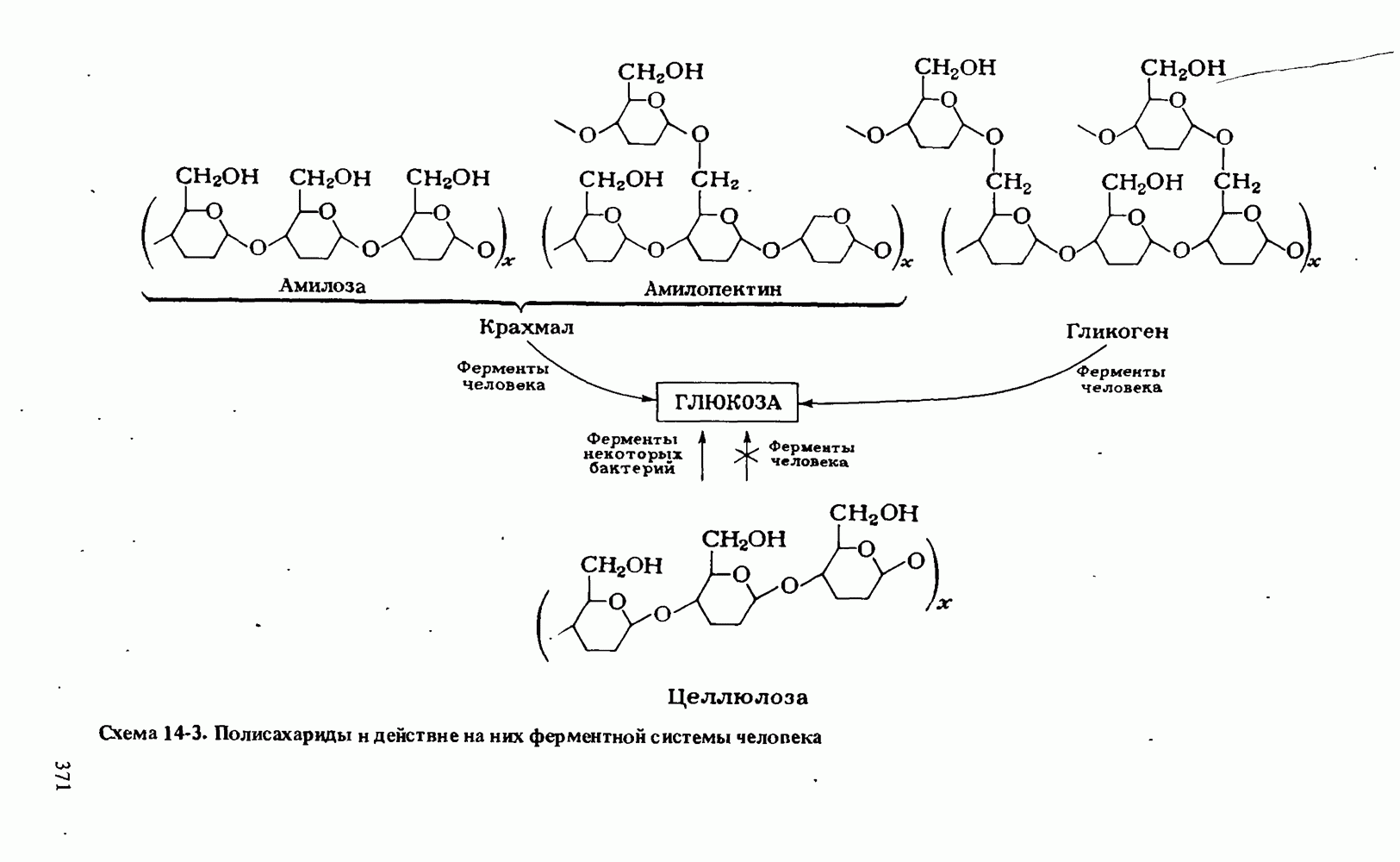
- ПОЛИСАХАРИДЫ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА УГЛЕВОДОВ
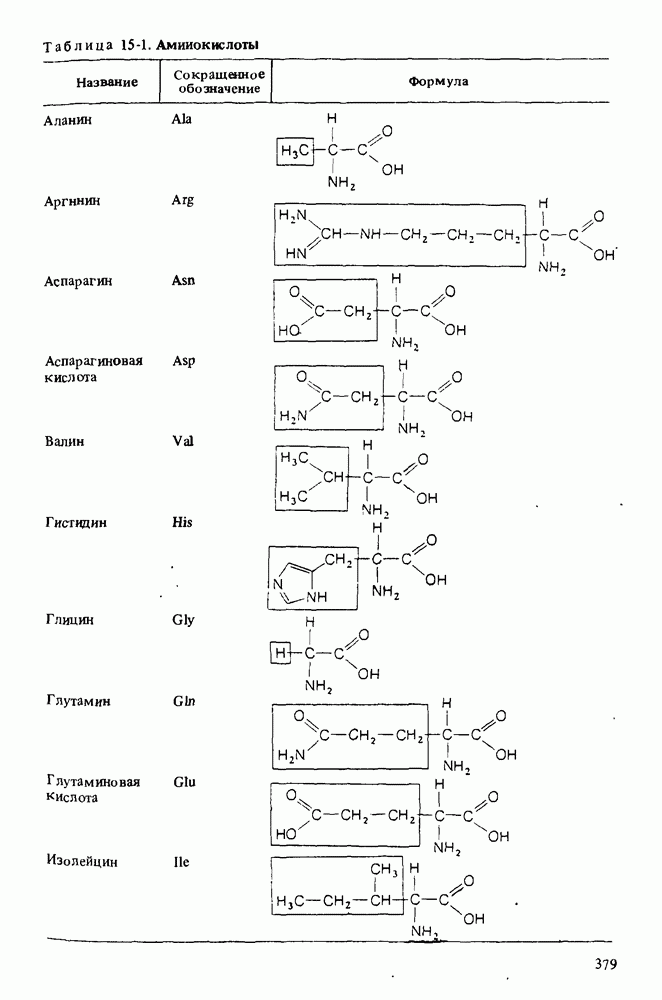
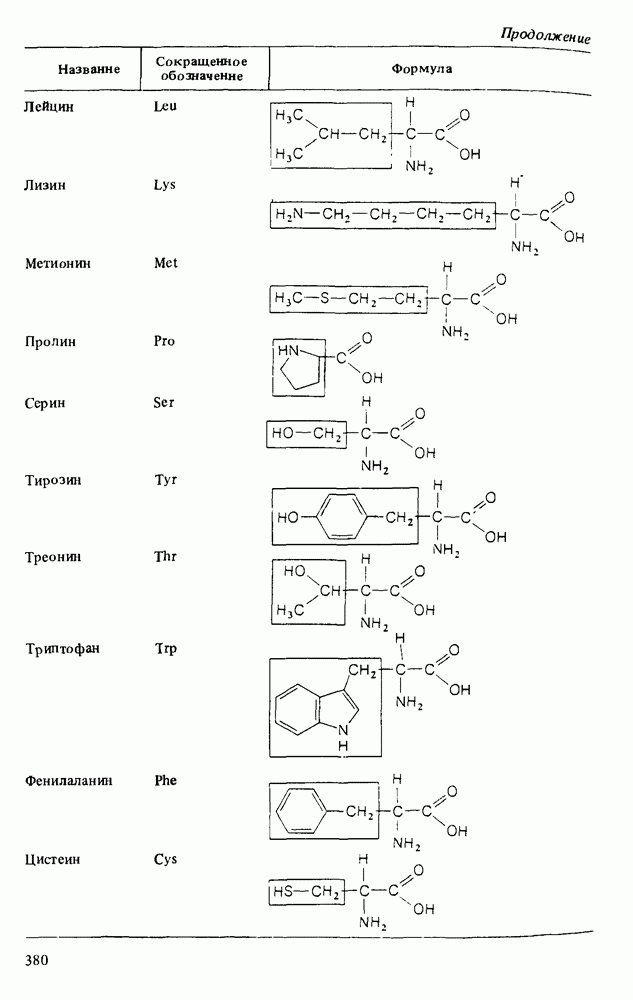
- Глава 15. АМИНОКИСЛОТЫ И БЕЛКИ
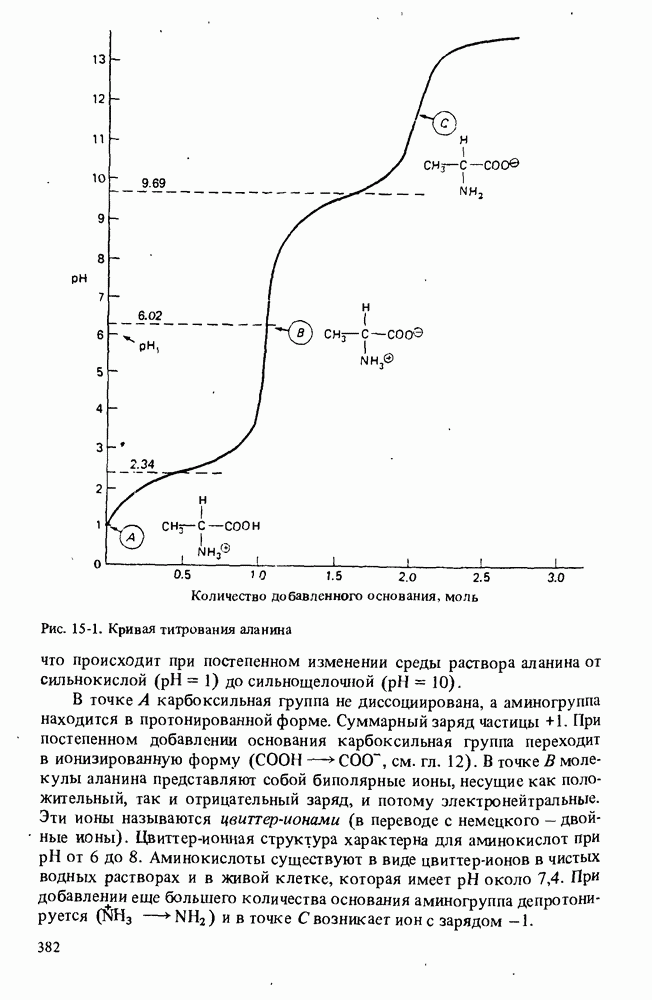
- КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА АМИНОКИСЛОТ
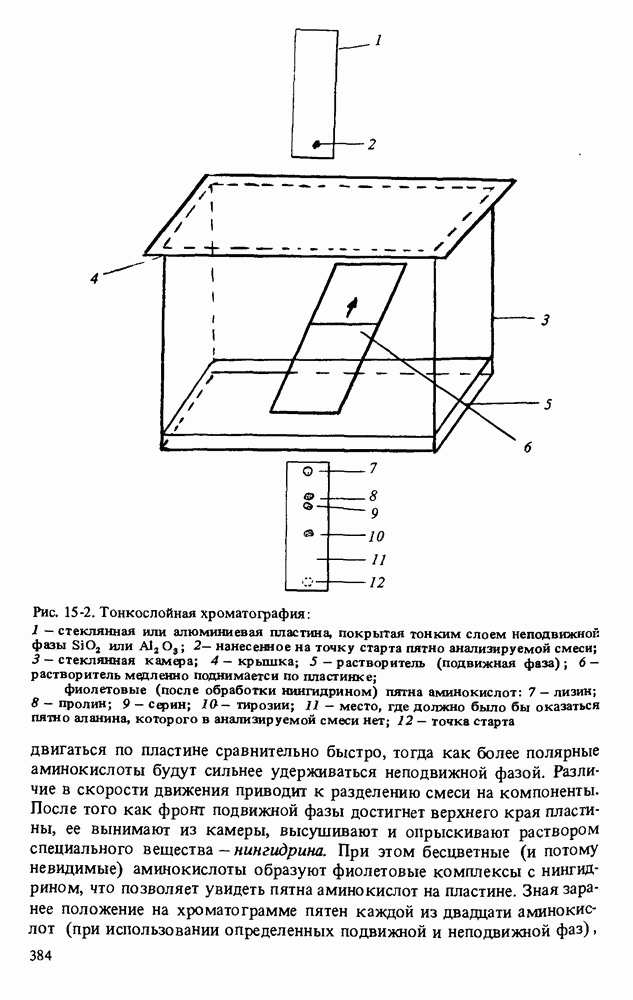
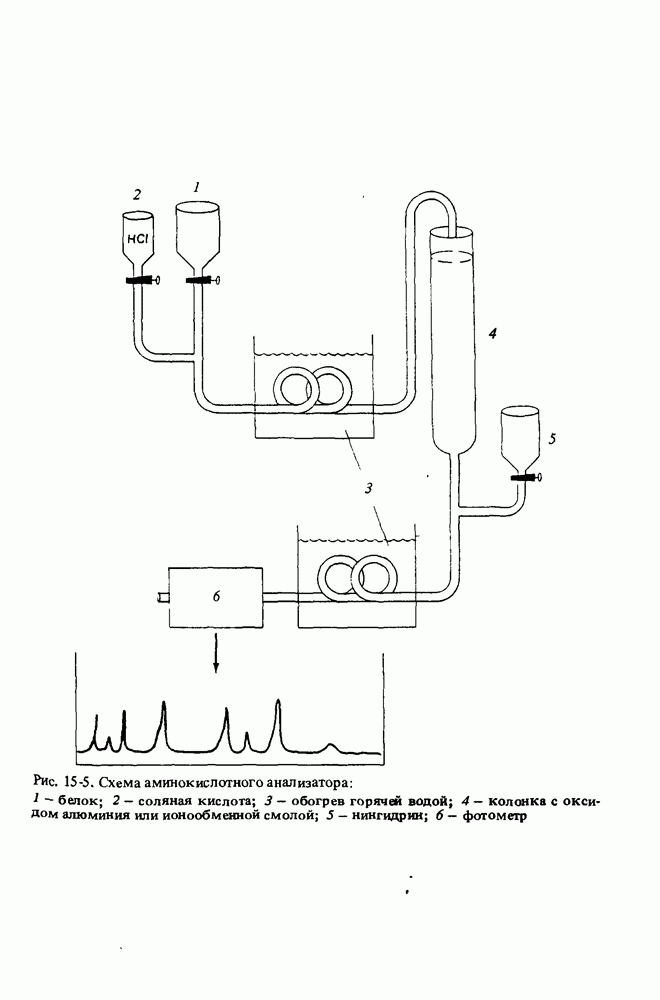
- АНАЛИЗ АМИНОКИСЛОТ
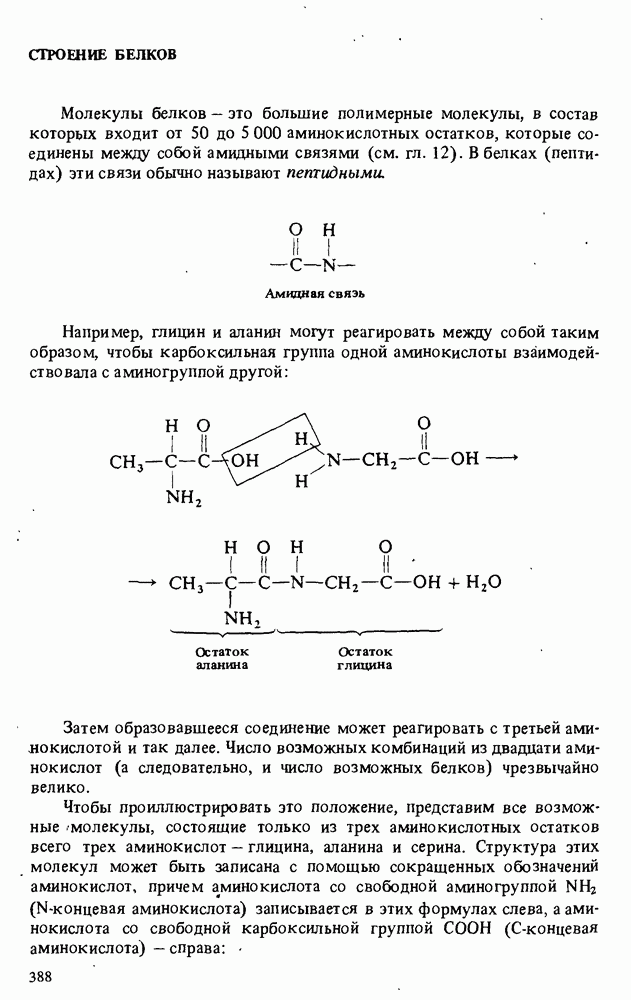
- СТРОЕНИЕ БЕЛКОВ
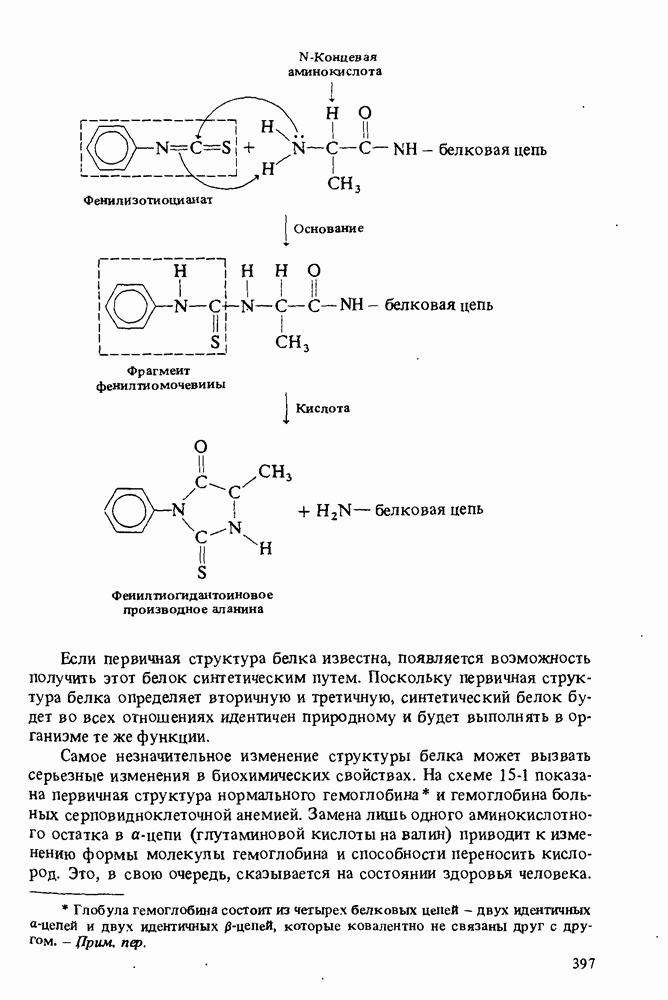
- УСТАНОВЛЕНИЕ ПЕРВИЧНОЙ СТРУКТУРЫ БЕЛКОВ
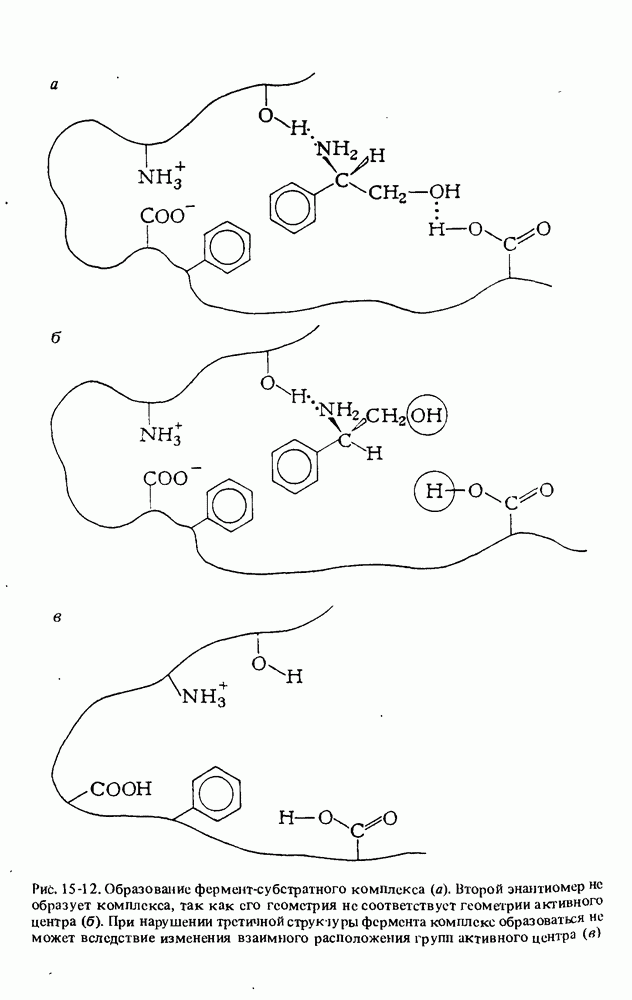
- ФЕРМЕНТЫ
- Глава 16. ЛИПИДЫ
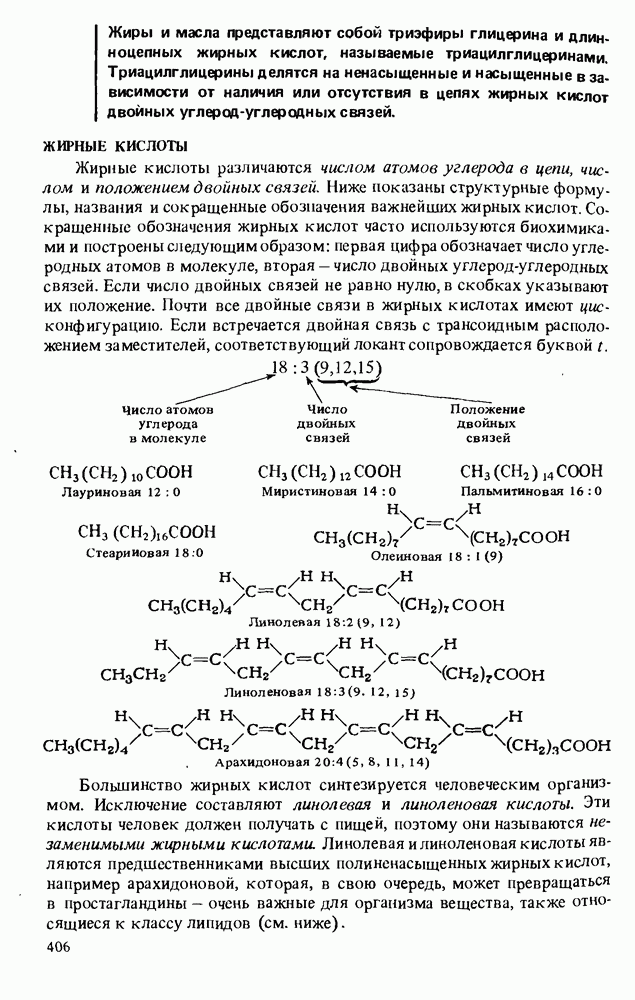
- ЖИРНЫЕ КИСЛОТЫ
- НАЗВАНИЯ ТРИАЦИЛГЛИЦЕРИНОВ
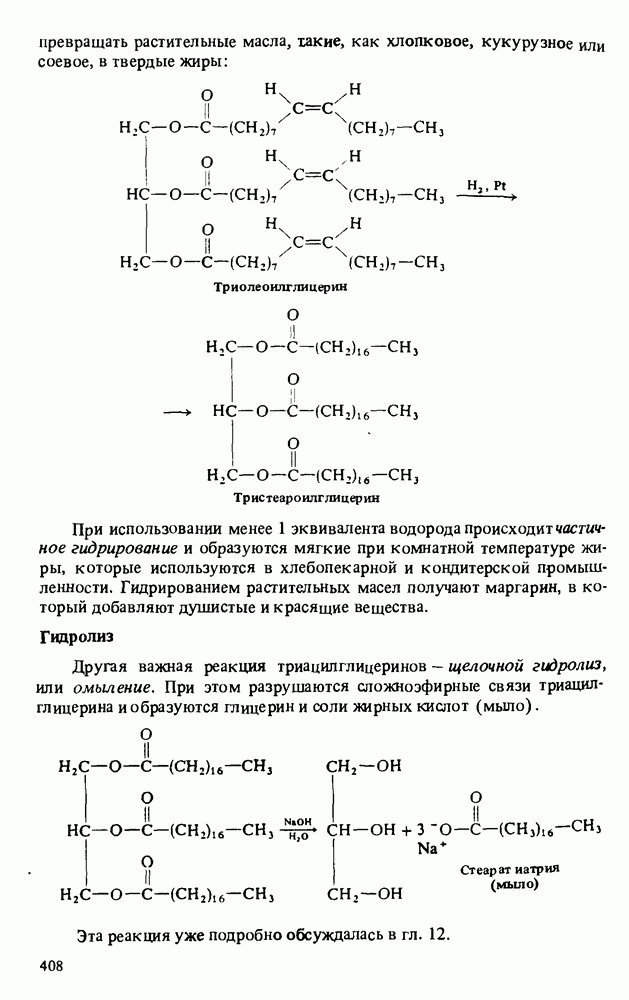
- РЕАКЦИИ ТРИАЦИЛГЛИЦЕРИНОВ
- ЛИПИДЫ, ОТЛИЧНЫЕ ОТ ТРИАЦИЛГЛИЦЕРИНОВ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА ЛИПИДОВ
- Глава 17. НУКЛЕИНОВЫЕ КИСЛОТЫ
- РИБОНУКЛЕИНОВЫЕ КИСЛОТЫ
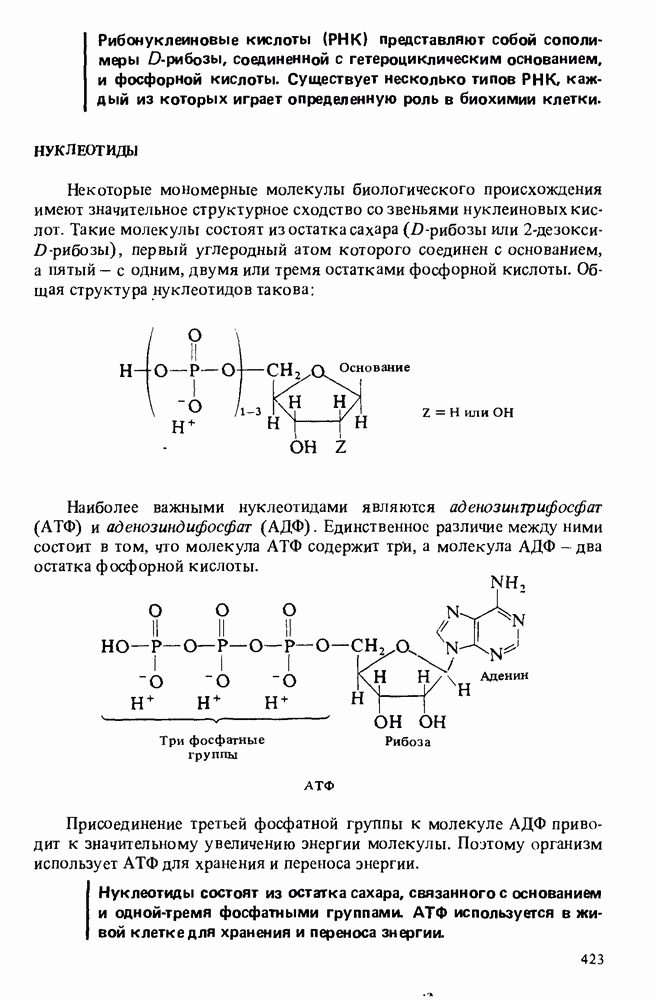
- НУКЛЕОТИДЫ
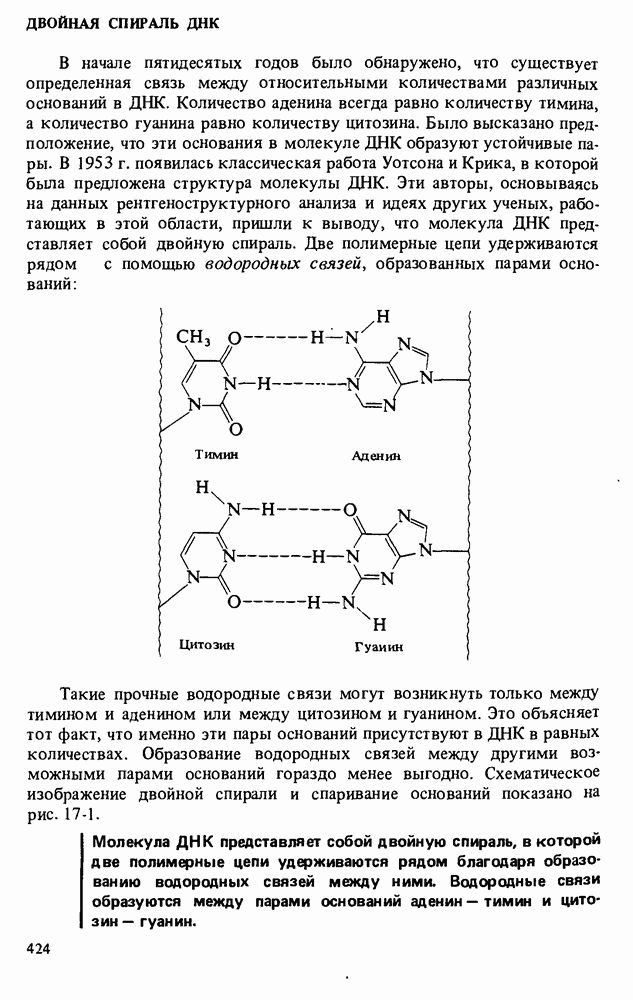
- ДВОЙНАЯ СПИРАЛЬ ДНК
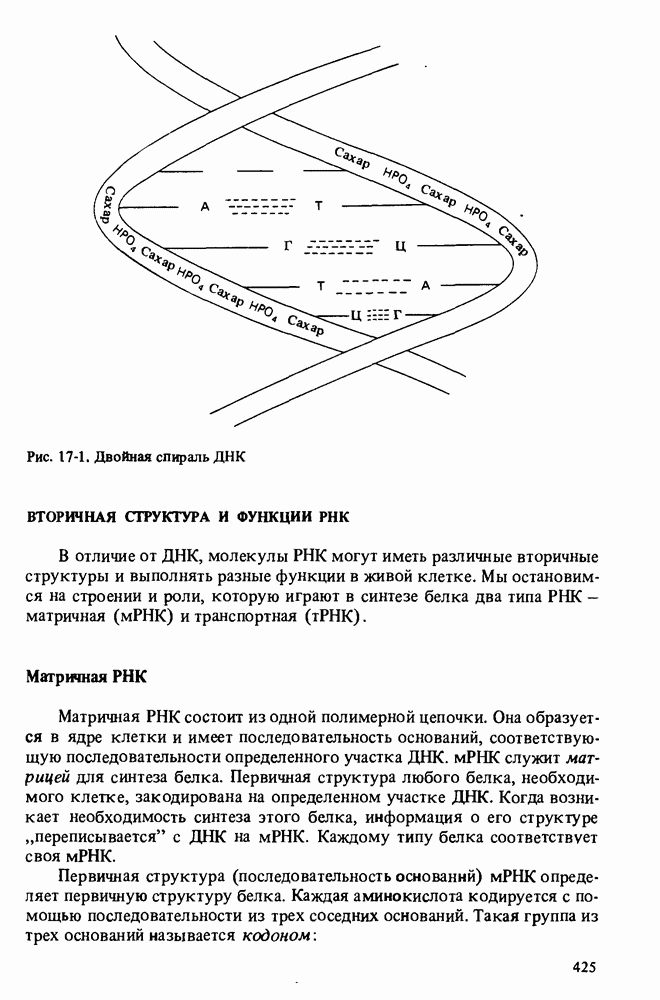
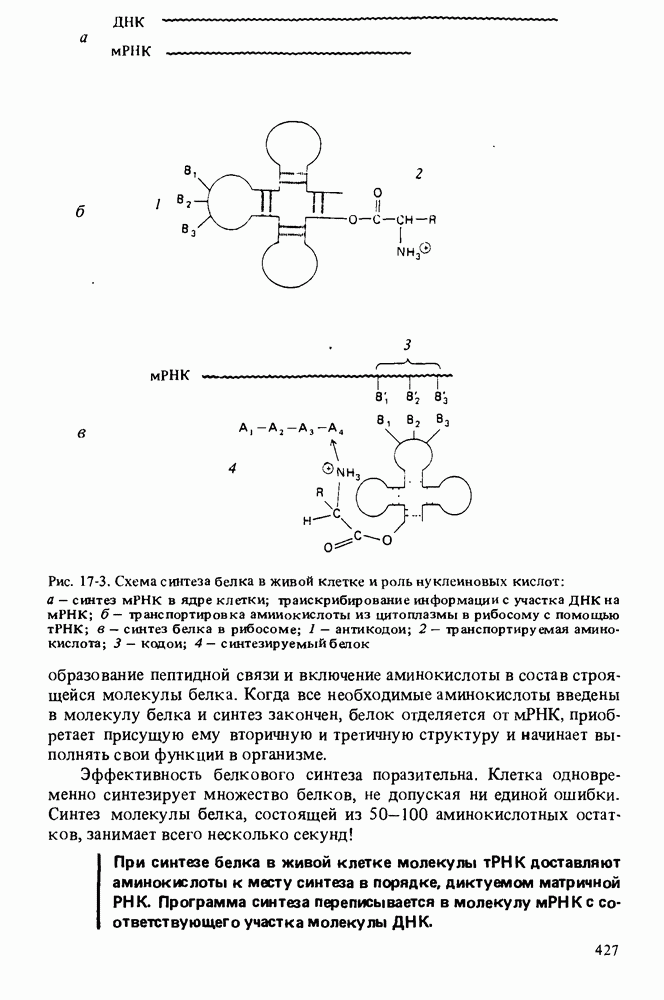
- ВТОРИЧНАЯ СТРУКТУРА И ФУНКЦИИ РНК
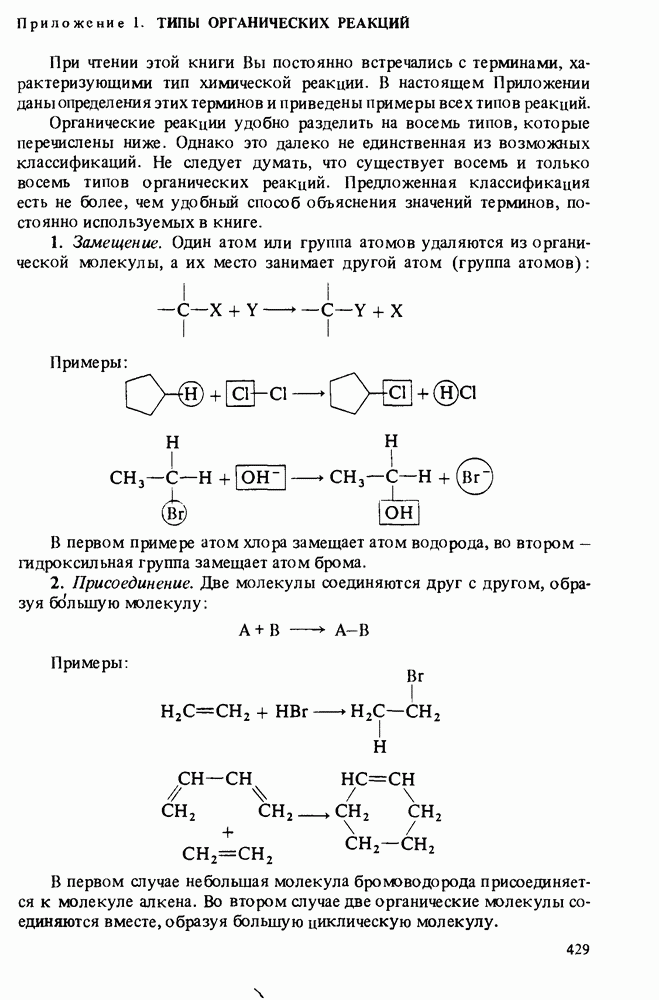
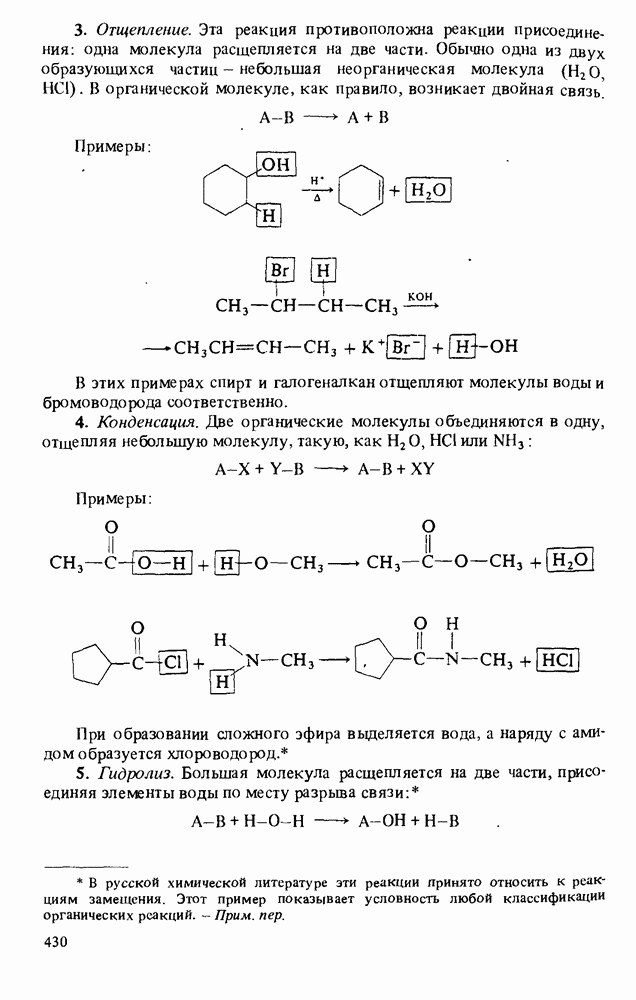
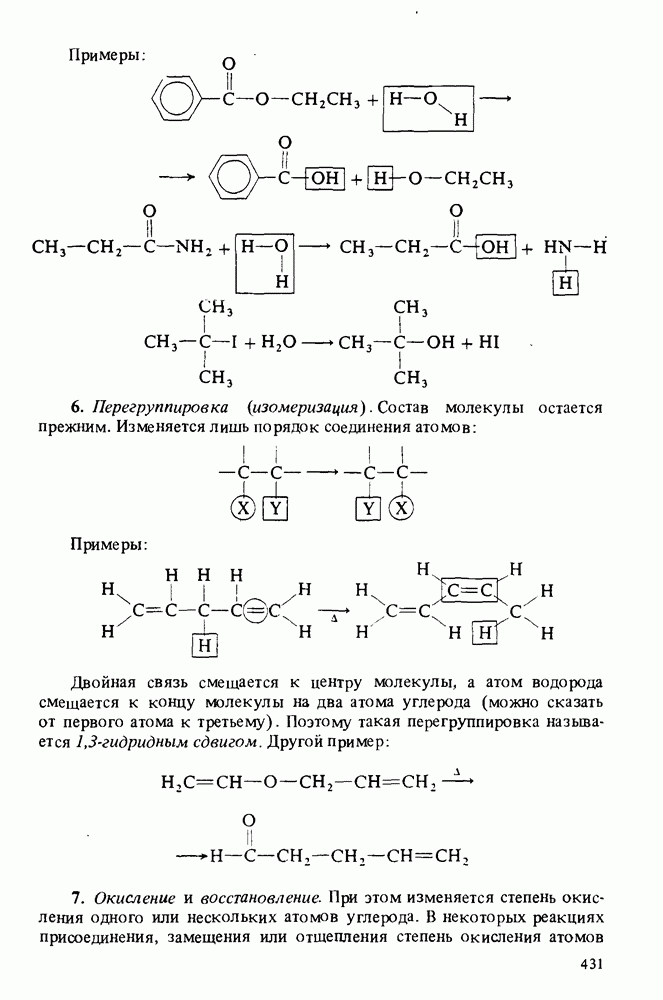
- Приложение 1. ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
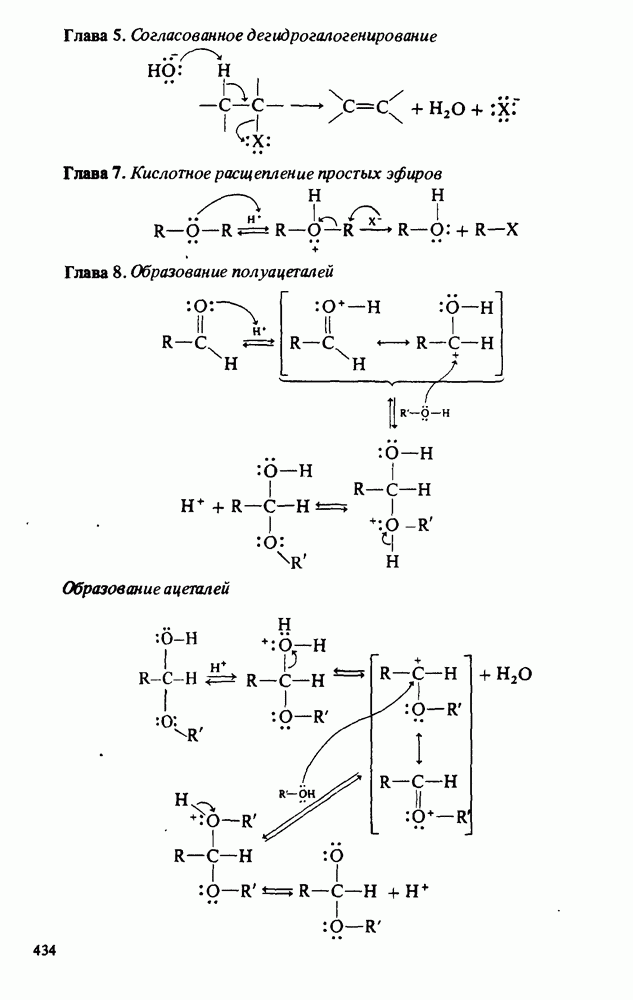
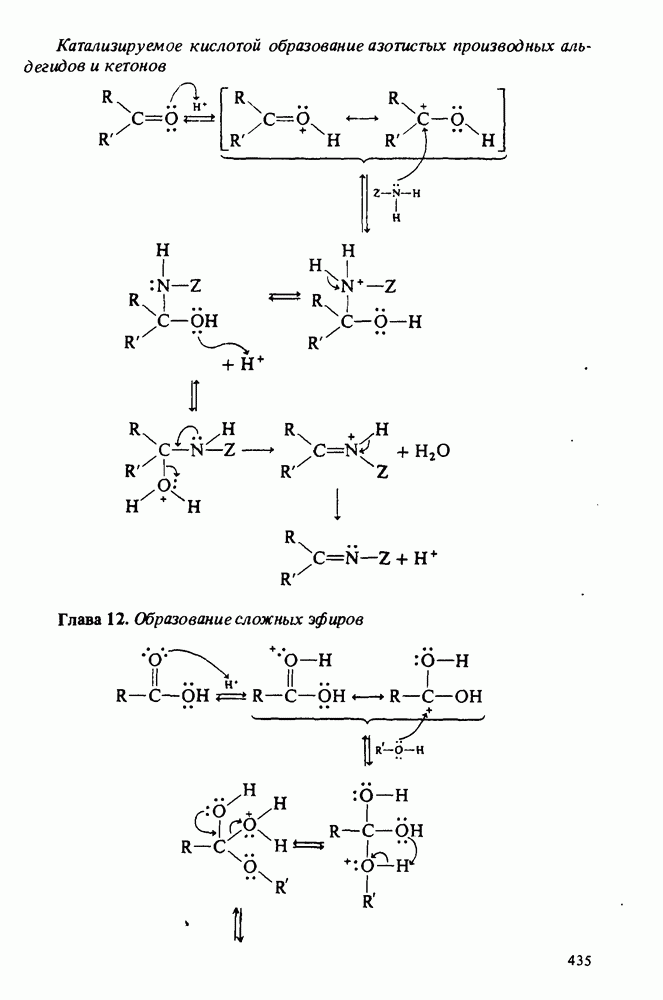
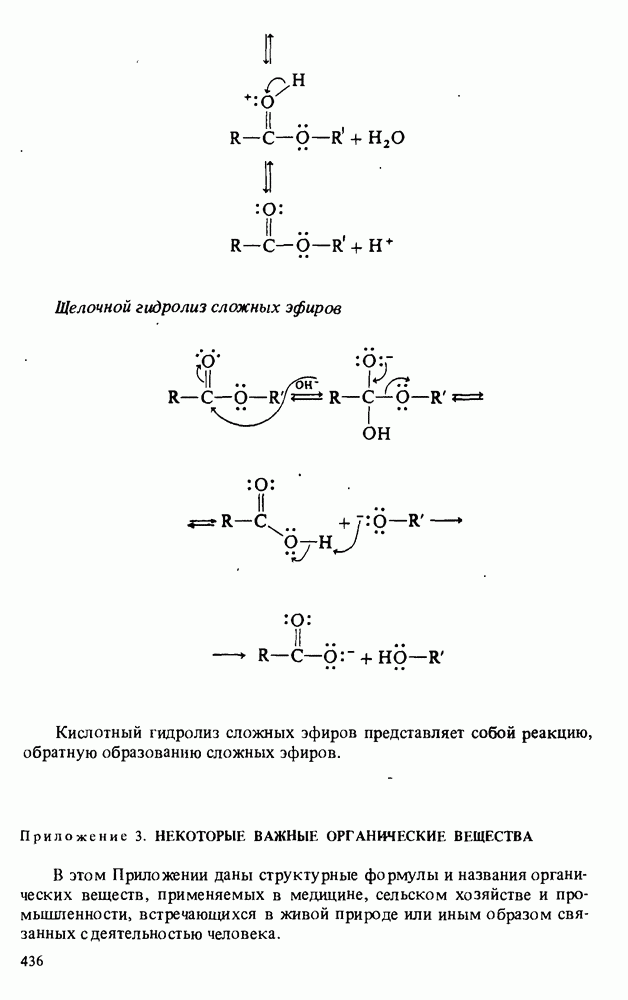
- Приложение 2. МЕХАНИЗМЫ НЕКОТОРЫХ РЕАКЦИЙ
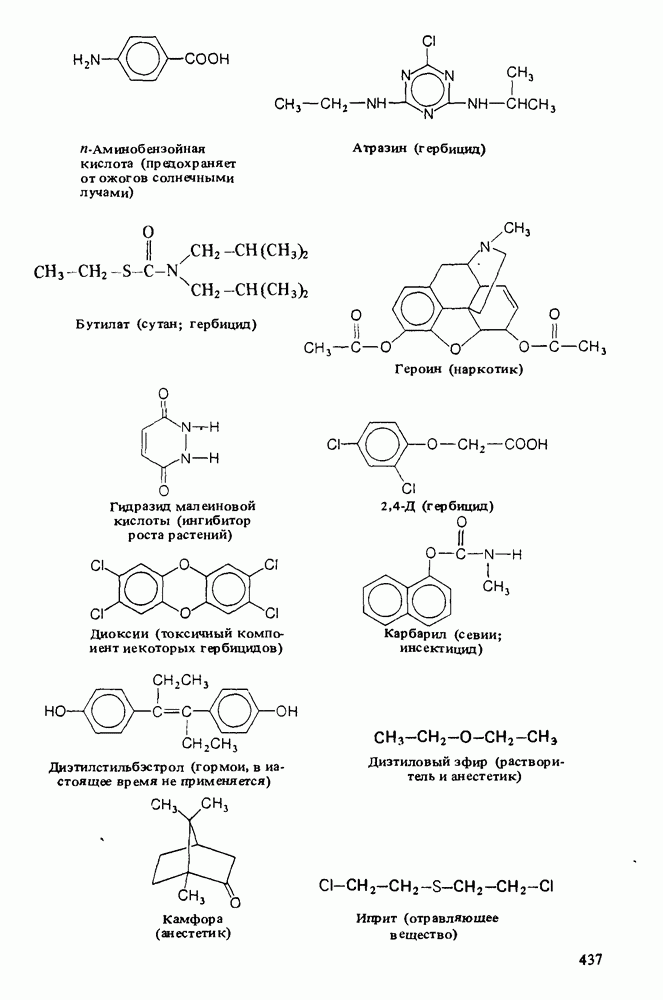
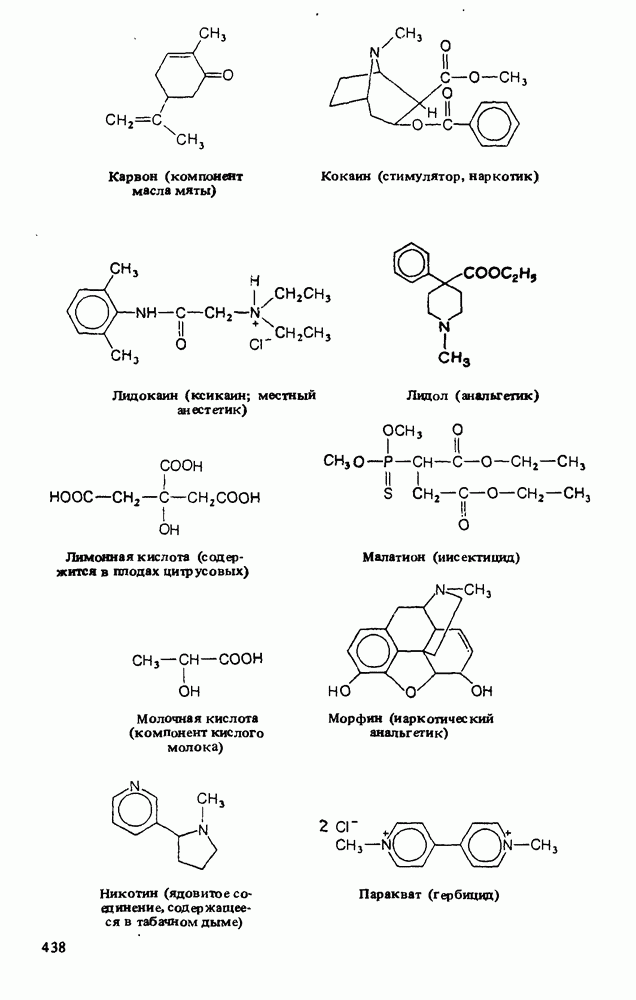
- Приложение 3. НЕКОТОРЫЕ ВАЖНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА