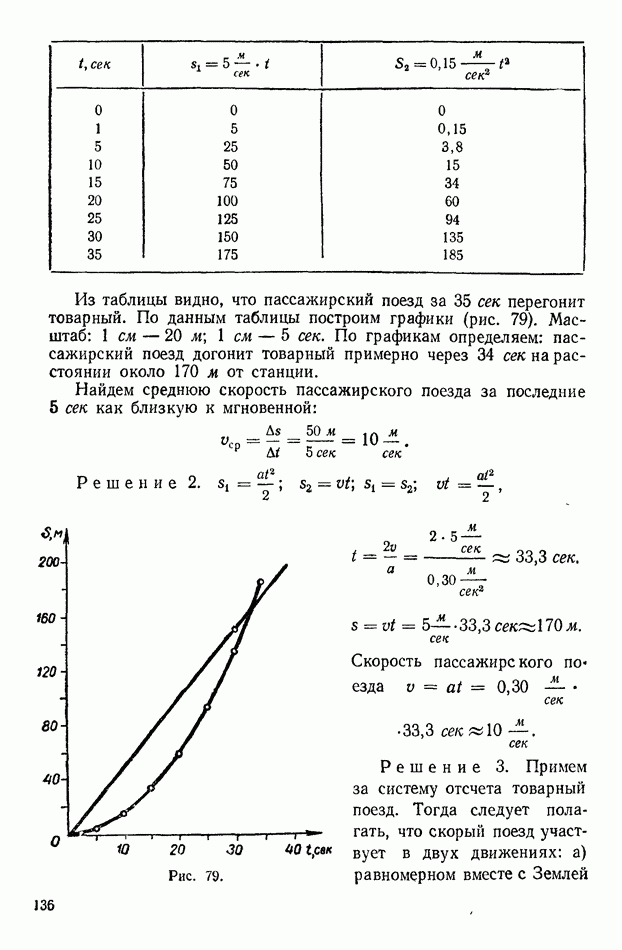
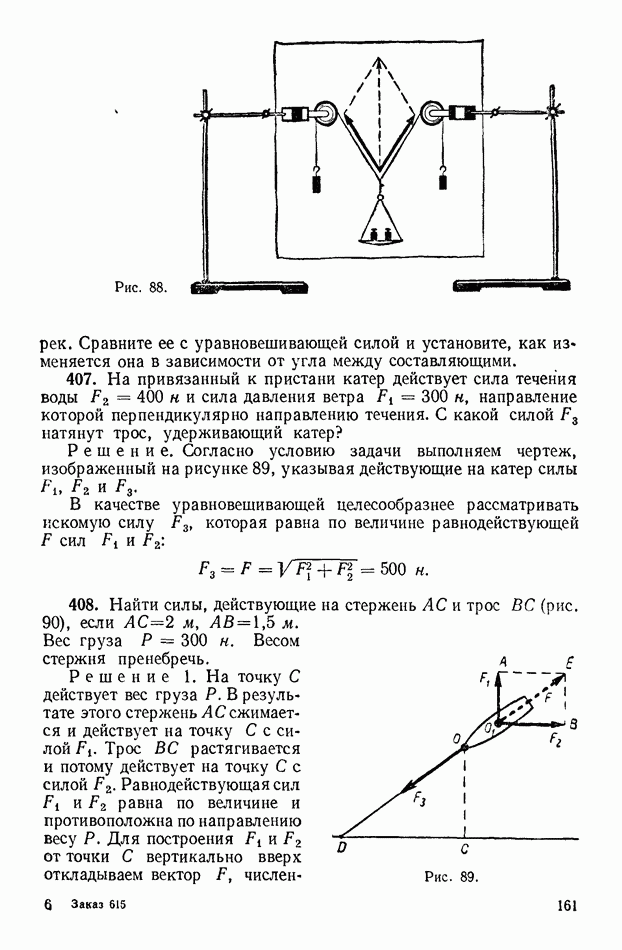
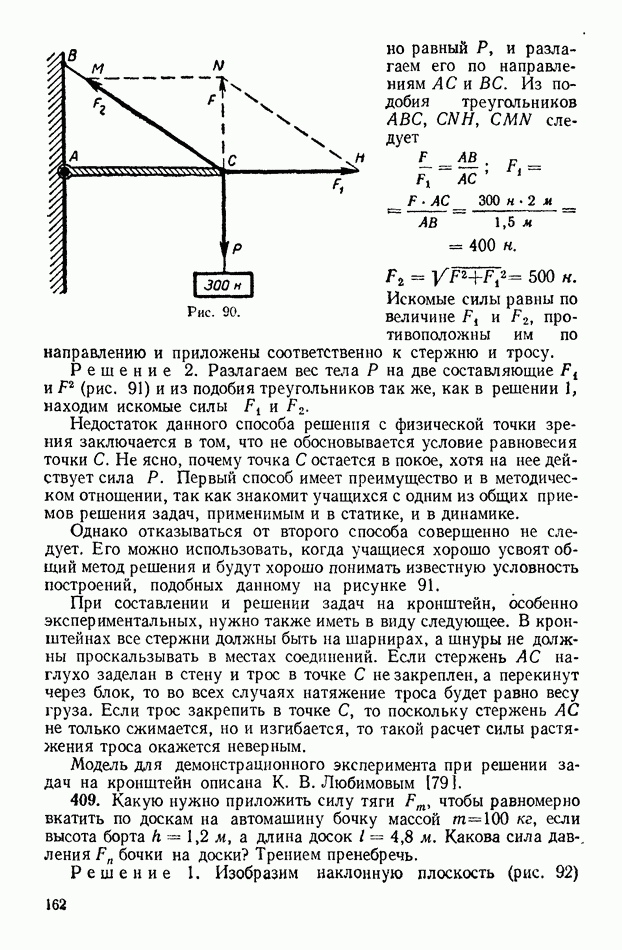
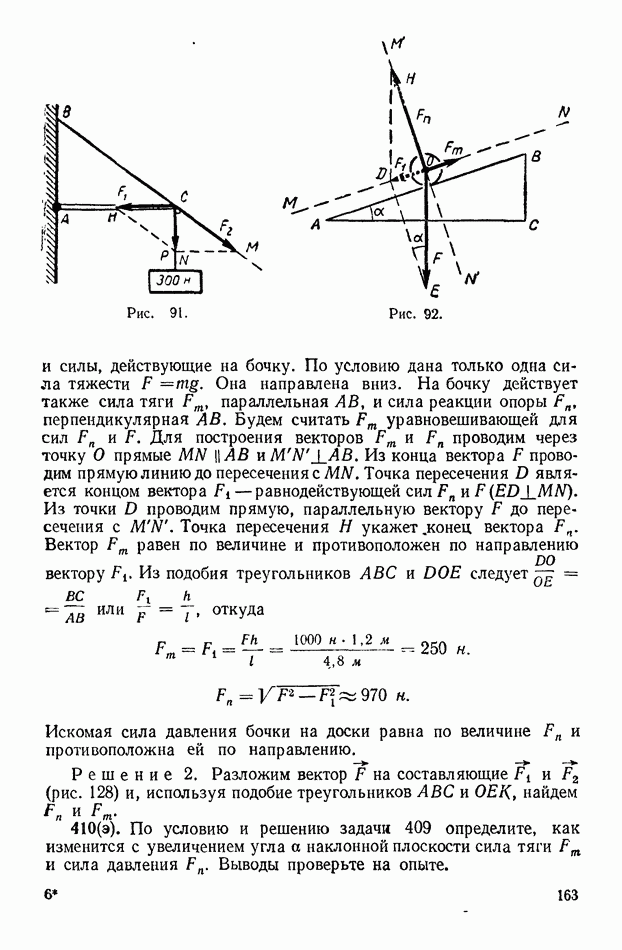
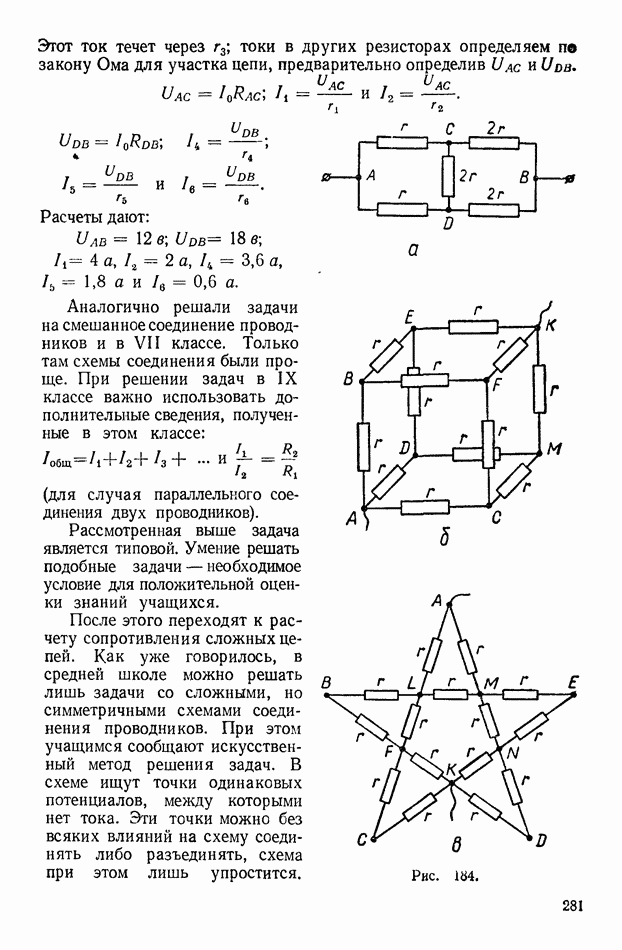
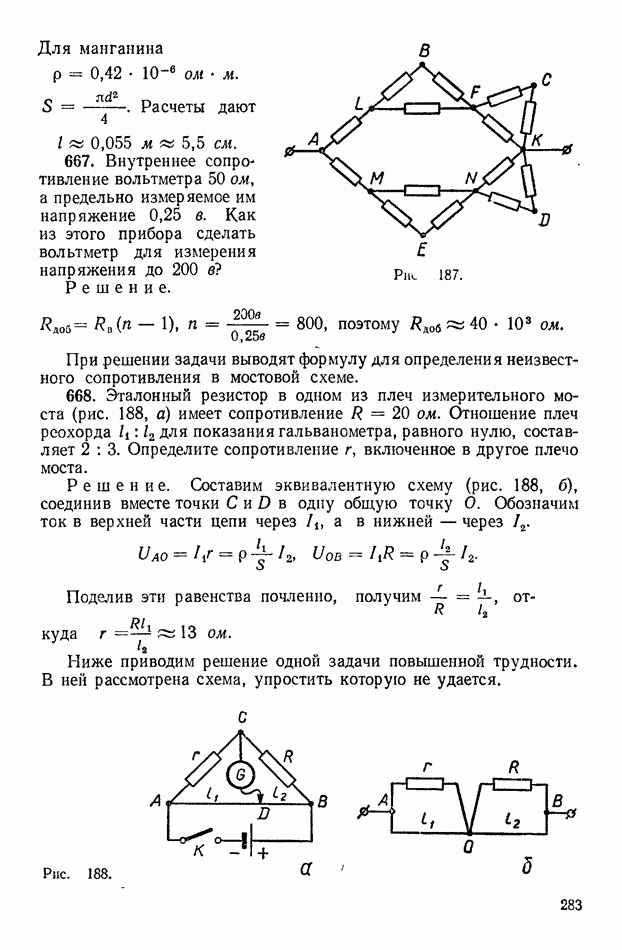
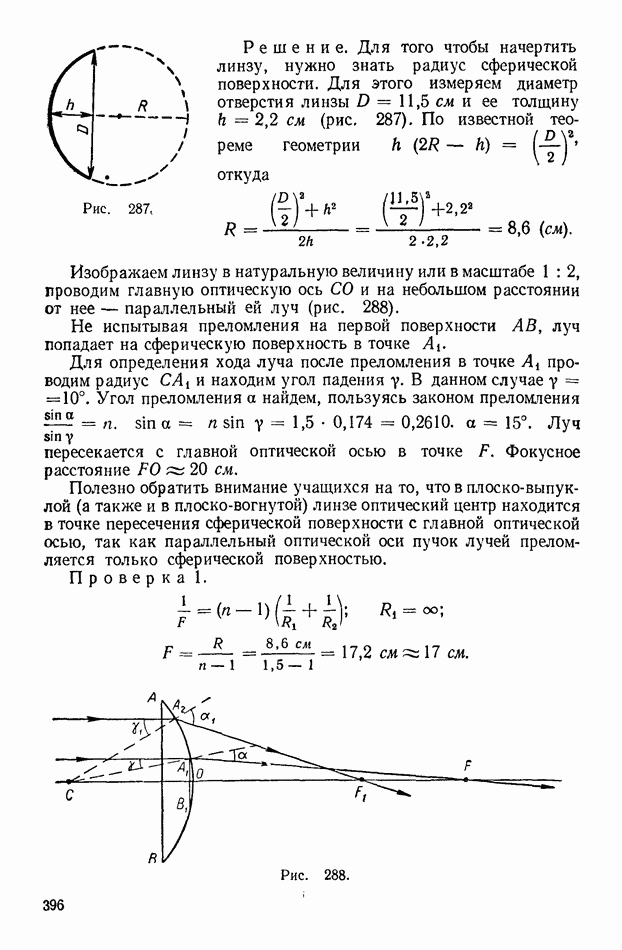
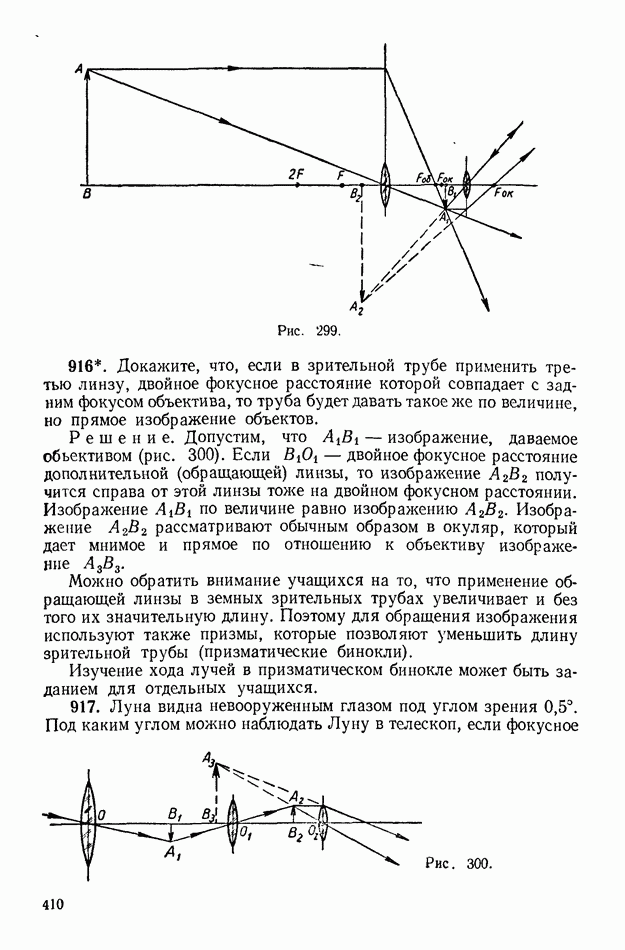
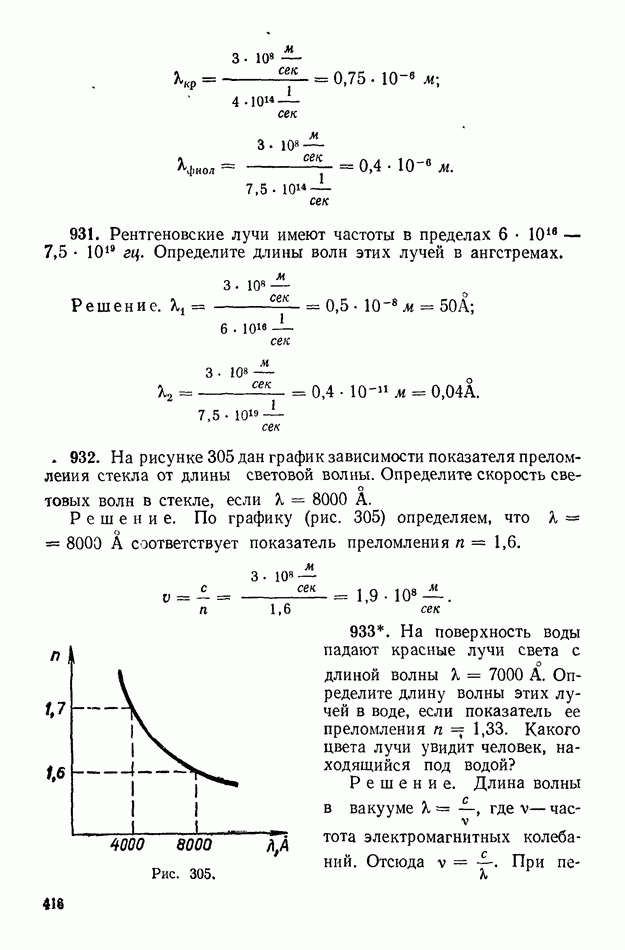
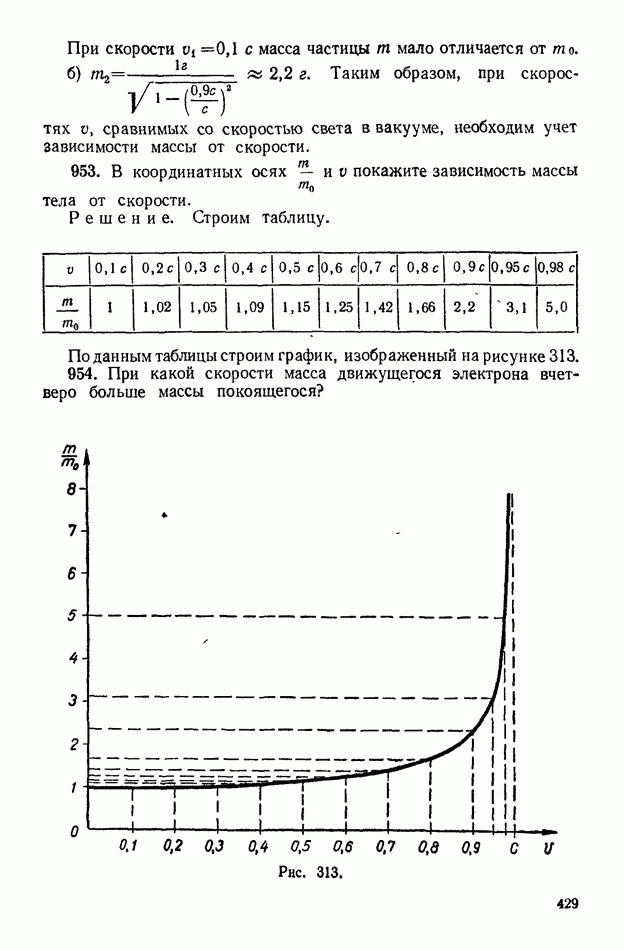
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
2. Электрический ток в электролитах
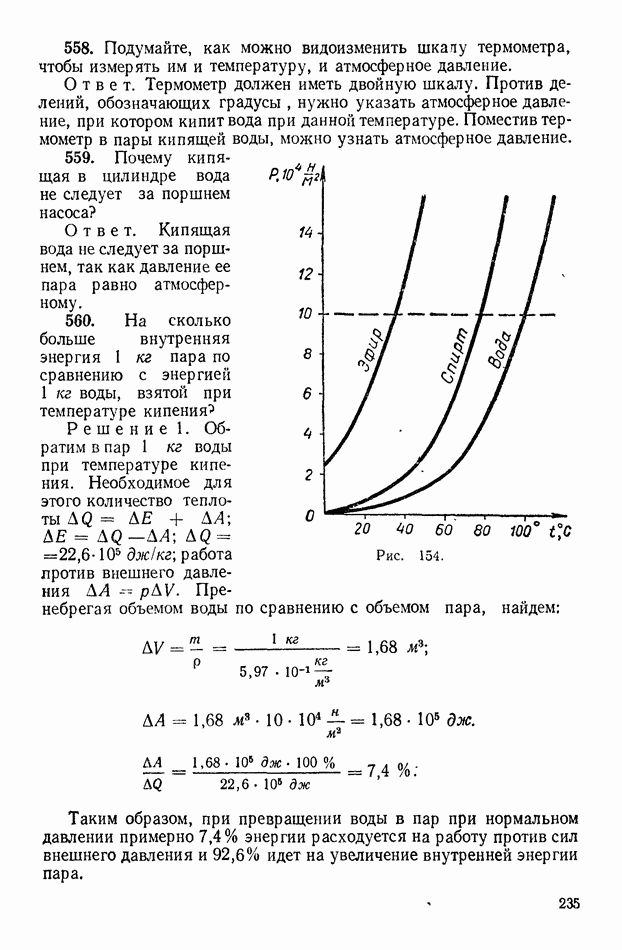
При прохождении тока через электролит на электродах выделяется вещество, масса которого  (первый закон Фарадея), где I — сила тока,
(первый закон Фарадея), где I — сила тока,  время протекания тока,
время протекания тока, 
коэффициент пропорциональности, получивший название электрохимического эквивалента вещества.
Причина электролиза состоит в том, что электролит диссоциирует на ионы, которые движутся под действием электрического поля между электродами и оседают на этих электродах.
В формуле первого закона Фарадея I — полный ток в электролите, равный сумме токов как положительных, так и отрицательных ионов. Обычно это вызывает затруднение у учащихся, которые считают, что к катоду движутся положительные ионы и надо брать ток, равный только току положительных ионов.
Второй закон Фарадея утверждает пропорциональность электрохимических  и химических
и химических  эквивалентов вещества, т. е.
эквивалентов вещества, т. е.  Величина
Величина  где
где  число Фарадея, равное заряду, который должен пройти через электролит, чтобы выделить из него вещество, масса которого численно равна химическому эквиваленту. Химический эквивалент вещества
число Фарадея, равное заряду, который должен пройти через электролит, чтобы выделить из него вещество, масса которого численно равна химическому эквиваленту. Химический эквивалент вещества  где
где  атомный вес,
атомный вес,  валентность вещества.
валентность вещества.
Объединенный закон Фарадея имеет вид 
Задачи по электролизу в основном и сводятся к определению входящих в данную формулу величин.
При выделении вещества на электродах возникает так называемая э.д.с. поляризации —  Ток в цепи уменьшается и становится равным
Ток в цепи уменьшается и становится равным  где
где  напряжение между электродами в электролитической ванне,
напряжение между электродами в электролитической ванне,  сопротивление цепи. В большинстве задач в средней школе Епол не учитывают, так как рассматривают случай, когда
сопротивление цепи. В большинстве задач в средней школе Епол не учитывают, так как рассматривают случай, когда  .
.
Вначале решают тренировочные задачи типа 725, 726, потом более сложные.
725. При серебрении изделия за  на катоде отложилось
на катоде отложилось  серебра. Определите силу тока при электролизе.
серебра. Определите силу тока при электролизе.
Решение. По первому закону электролиза  откуда
откуда  Значение
Значение  берем из таблиц.
берем из таблиц.

Серебро, как и все металлы, откладывается на катоде, так как ионы металла положительные.
726. Сколько никеля выделится при электролизе за время  при токе
при токе  если известно, что атомный вес никеля
если известно, что атомный вес никеля  а валентность
а валентность 
Решение. Массу никеля определяем по объединенному
закону Фарадея 
727. При электролизе раствора  была затрачена энергия
была затрачена энергия  Определить массу выделившегося цинка
Определить массу выделившегося цинка  если напряжение на зажимах ванны
если напряжение на зажимах ванны 
Решение. По первому закону Фарадея  Неизвестное значение
Неизвестное значение  выразим через работу тока А и напряжение
выразим через работу тока А и напряжение  откуда
откуда  или
или  Тогда
Тогда  Для цинка
Для цинка  Учтем также, что
Учтем также, что  .
.

728. Сколько времени из раствора  будет наращиваться слой меди толщиной
будет наращиваться слой меди толщиной  при плотности тока в электролите
при плотности тока в электролите  поляризации не учитывать.
поляризации не учитывать.
Решение. В условии задачи не случайно оговорено, что электролиз идет в растворе  В этом случае валентность меди
В этом случае валентность меди  и электрохимический эквивалент меди
и электрохимический эквивалент меди  Возможен электролиз и при одновалентных ионах меди.
Возможен электролиз и при одновалентных ионах меди.
В формулы по законам электролиза входит сила тока  а не плотность тока
а не плотность тока  но
но  площадь поперечного сечения проводника электролита между электродами.
площадь поперечного сечения проводника электролита между электродами.
По первому закону Фарадея  Отсюда искомая величина
Отсюда искомая величина  Выразим массу
Выразим массу  через плотность меди
через плотность меди  и объем
и объем  где
где  толщина слоя меди,
толщина слоя меди,  площадь поверхности электрода:
площадь поверхности электрода:  Тогда
Тогда  Подставив численные значения
Подставив численные значения  получим
получим

729. Определите массу серебра, выделившегося на катоде при электролизе азотнокислого серебра за время  если к ванне приложено напряжение
если к ванне приложено напряжение  сопротивление ванны
сопротивление ванны  ом, а э.д.с. поляризации Еиол
ом, а э.д.с. поляризации Еиол  в.
в.
Решение. По первому закону Фарадея  Ток в цепи
Ток в цепи
с учетом э.д.с. поляризации  Вычисления дают значение
Вычисления дают значение

730. Определите стоимость получения  рафинированной меди, если электролиз идет при напряжении
рафинированной меди, если электролиз идет при напряжении  установки
установки  тариф
тариф  поляризации не учитывать.
поляризации не учитывать.
Решение. Рафинированная медь получается при электролизе  т. е. медь здесь двухвалентна. В этом случае
т. е. медь здесь двухвалентна. В этом случае  Тариф
Тариф 
Стоимость электроэнергии

поэтому 
Величину  определяем по первому закону Фарадея:
определяем по первому закону Фарадея: 

Вычисления дают значение

731. Сколько атомов хлора и железа выделится из раствора хлористого железа при пропускании через электролит в течение  тока силой
тока силой 
Решение. Хлор одновалентен  Масса выделившегося хлора
Масса выделившегося хлора  где
где  число атомов, а
число атомов, а  масса одного атома хлора. Массу
масса одного атома хлора. Массу  находят по первому закону Фарадея:
находят по первому закону Фарадея:  Из таблиц для хлора
Из таблиц для хлора  Масса одного атома (иона) хлора
Масса одного атома (иона) хлора  где А — масса килограмм-атома,
где А — масса килограмм-атома,  число атомов в килограмм-атоме. Известно, что
число атомов в килограмм-атоме. Известно, что  (число Авогадро). Хлор имеет атомный вес
(число Авогадро). Хлор имеет атомный вес 

Железо двухвалентно  значит, число ионов железа, прошедших через раствор, и число выделившихся атомов в 2 раза меньше числа ионов хлора.
значит, число ионов железа, прошедших через раствор, и число выделившихся атомов в 2 раза меньше числа ионов хлора.
Хлор выделяется на аноде, а железо на катоде.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ГЛАВА 1. ВИДЫ ЗАДАЧ И ОБЩИЕ ВОПРОСЫ МЕТОДИКИ ИХ РЕШЕНИЯ
- 1. Задачи как средство обучения и воспитания учащихся на занятиях по физике
- 2. Классификация задач
- 3. Методика решения физической задачи
- ГЛАВА 2. МЕТОДИКА РЕШЕНИЯ ЗАДАЧ РАЗНЫХ ТИПОВ
- 2. Экспериментальные задачи
- 3. Вычислительные задачи
- 4. Графические задачи
- ГЛАВА 3. МЕТОДИКА ПРОВЕДЕНИЯ ЗАНЯТИЙ ПО РЕШЕНИЮ ЗАДАЧ
- 2. Решение задач на уроках
- 3. Решение задач на внеклассных занятиях
- 4. О некоторых особенностях решения задач в различных классах
- 6 Класс
- 1. Существование молекул. Размеры молекул
- 2. Движение молекул
- 3. Молекулярные силы
- 4. Особенности строения газов, жидкостей и твердых тел
- ГЛАВА 5. ДВИЖЕНИЕ И СИЛЫ
- 1. Механическое движение. Скорость
- 2. Масса. Плотность вещества
- 3. Инерция
- 4. Сила тяжести. Вес тел
- 5. Графическое изображение и сложение сил
- 6. Сила давления. Давление
- 7. Сила трения. Силы взаимодействия молекул
- ГЛАВА 6. ДАВЛЕНИЕ ЖИДКОСТЕЙ И ГАЗОВ (ГИДРО- И АЭРОСТАТИКА)
- 2. Весовое давление жидкости
- 3. Атмосферное давление
- 4. Архимедова сила
- ГЛАВА 7. РАБОТА И МОЩНОСТЬ. ПОНЯТИЕ ОБ ЭНЕРГИИ
- 1. Механическая работа
- 2. Мощность
- 3. Рычаги. Блоки
- 4. Механическая энергия
- 7 КЛАСС
- ГЛАВА 8. ТЕПЛОПЕРЕДАЧА И РАБОТА
- 2. Способы передачи теплоты
- 3. Количество теплоты. Удельная теплоемкость
- 4. Теплота сгорания топлива. Тепловая отдача
- ГЛАВА 9. ИЗМЕНЕНИЕ АГРЕГАТНЫХ СОСТОЯНИЙ ВЕЩЕСТВА
- 1. Плавление и отвердевание
- 2. Испарение
- 3. Кипение и конденсация
- ГЛАВА 10. ТЕПЛОВЫЕ МАШИНЫ
- ГЛАВА 11. СТРОЕНИЕ АТОМА
- ГЛАВА 12. СИЛА ТОКА, НАПРЯЖЕНИЕ, СОПРОТИВЛЕНИЕ
- 1. Электрический ток. Электрическая цепь
- 2. Сила тока
- 3. Напряжение
- 4. Сопротивление проводников
- 5. Закон Ома для участка цепи
- 6. Соединения проводников
- ГЛАВА 13. РАБОТА И МОЩНОСТЬ ТОКА
- 1. Работа и мощность тока
- 2. Тепловое действие тока
- ГЛАВА 14. ЭЛЕКТРОМАГНИТНЫЕ ЯВЛЕНИЯ
- 2. Постоянные магниты
- 3. Движение проводника с током в магнитном поле
- 8 КЛАСС
- 1. Система отсчета. Относительность механического движения. Сложение перемещений
- 2. Скорость. Сложение скоростей
- ГЛАВА 16. НЕРАВНОМЕРНОЕ ДВИЖЕНИЕ
- 2. Ускорение
- 3: Скорость при равнопеременном движении
- 4. Перемещение и путь в равнопеременном движении
- 5. Движение по окружности
- ГЛАВА 17. ЗАКОНЫ ДВИЖЕНИЯ
- 1. Первый закон Ньютона (закон инерции)
- 2. Закон сохранения импульса (количества движения)
- 3. Второй закон Ньютона
- 4. Третий закон Ньютона
- ГЛАВА 18. СИЛЫ В ПРИРОДЕ
- 1. Гравитационные силы
- 2. Силы упругости
- 3. Силы трения
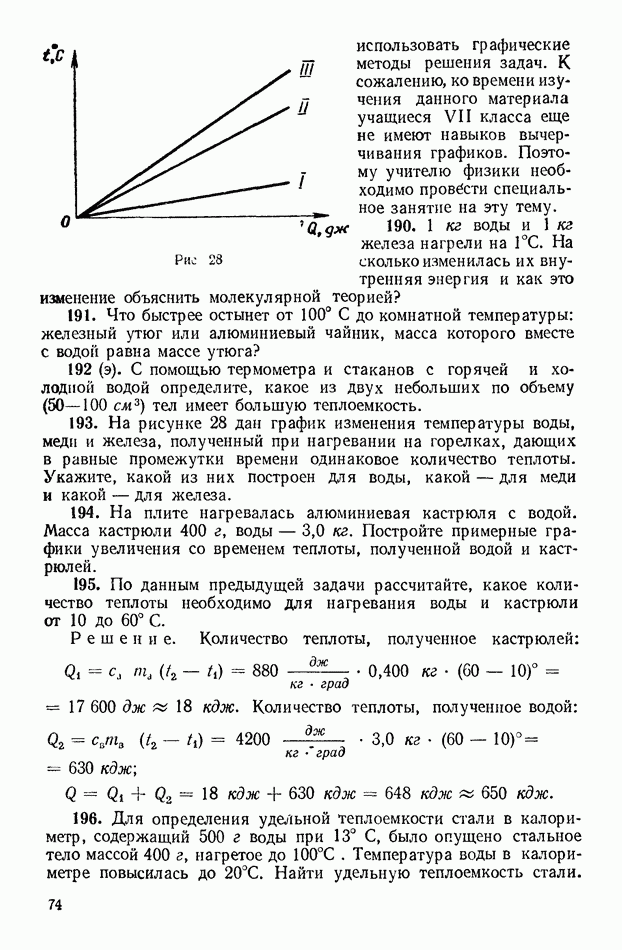
- ГЛАВА 19. РАВНОВЕСИЕ ТЕЛ (СТАТИКА)
- 1. Сложение и разложение сил
- 2. Момент силы. Равновесие тел, имеющих ось вращения
- 3. Центр тяжести. Виды равновесия. Устойчивость тел
- ГЛАВА 20. ПРИМЕНЕНИЕ ЗАКОНОВ ДВИЖЕНИЯ НЬЮТОНА
- 1. Прямолинейное движение под действием постоянной силы
- 2. Движение тела, брошенного горизонтально и под углом к горизонту
- 3. Движение по окружности
- 4. Движение планет и искусственных спутников
- ГЛАВА 21. РАБОТА И ЭНЕРГИЯ
- 1. Работа и мощность
- 2. Механическая энергия
- 3. Движение жидкостей и газов
- 9 КЛАСС
- 1. Основы молекулярно — кинетической теории
- 2. Свойства газов
- ГЛАВА 23. ВНУТРЕННЯЯ ЭНЕРГИЯ ИДЕАЛЬНОГО ГАЗА
- 2. Работа при расширении газа
- ГЛАВА 24. СВОЙСТВА ПАРОВ
- 2. Кипение
- 3. Сжижение газов. Критическое состояние вещества
- 4. Влажность
- ГЛАВА 25. СВОЙСТВА ЖИДКОСТЕЙ И ТВЕРДЫХ ТЕЛ
- 2. Смачивание и несмачивание. Давление под кривой поверхностью, капиллярные явления
- 3. Свойства твердых тел
- 4. Тепловое расширение жидкостей и твердых тел
- ГЛАВА 26. ЭЛЕКТРИЧЕСКОЕ ПОЛЕ
- 2. Напряженность электрического поля
- 3. Потенциал электрического поля
- 4. Электрическая емкость
- ГЛАВА 27. ЭЛЕКТРИЧЕСКИЙ ТОК В МЕТАЛЛАХ. ЗАКОНЫ ПОСТОЯННОГО ТОКА
- 2. Соединения проводников
- 3. Закон Ома для полной цепи
- 4. Работа, мощность, тепловое действие тока
- 5. Термоток
- ГЛАВА 28. ЭЛЕКТРОМАГНЕТИЗМ
- 1. Магнитное поле тока
- 2. Электромагнитная индукция
- ГЛАВА 29. ОСНОВЫ ЭЛЕКТРОНИКИ
- 2. Электрический ток в электролитах
- 3. Электрический ток в газах
- 4. Электрические свойства полупроводников
- 10 КЛАСС
- ГЛАВА 30. МЕХАНИЧЕСКИЕ КОЛЕБАНИЯ И ВОЛНЫ. ЗВУК
- 2. Колебания математического маятника
- 3. Упругие колебания. Превращение энергии при колебательном движении
- 4. Сдвиг фаз. Сложение колебаний
- 5. Распространение колебаний в упругой среде. Волны
- 6. Интерференция и дифракция волн
- 7. Инфразвук и ультразвук
- ГЛАВА 31. ПЕРЕМЕННЫЙ ТОК
- ГЛАВА 32. ЭЛЕКТРОМАГНИТНЫЕ КОЛЕБАНИЯ И ВОЛНЫ
- ГЛАВА 33. ВОЛНОВЫЕ СВОЙСТВА СВЕТА
- 1. Скорость света
- 2. Интерференция и дифракция света
- ГЛАВА 34. ГЕОМЕТРИЧЕСКАЯ ОПТИКА
- 2. Отражение света
- 3. Преломление света
- 4. Линзы
- 5. Оптические приборы
- ГЛАВА 35. ИЗЛУЧЕНИЕ И СПЕКТРЫ
- 1. Явление дисперсии и спектры
- 2. Фотометрия и законы освещенности
- ГЛАВА 36. ДЕЙСТВИЕ СВЕТА. КВАНТЫ СВЕТА
- 1. Кванты света
- 2. Фотоэффект
- ГЛАВА 37. ОСНОВЫ ТЕОРИИ ОТНОСИТЕЛЬНОСТИ
- ГЛАВА 38. ФИЗИКА АТОМНОГО ЯДРА