| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
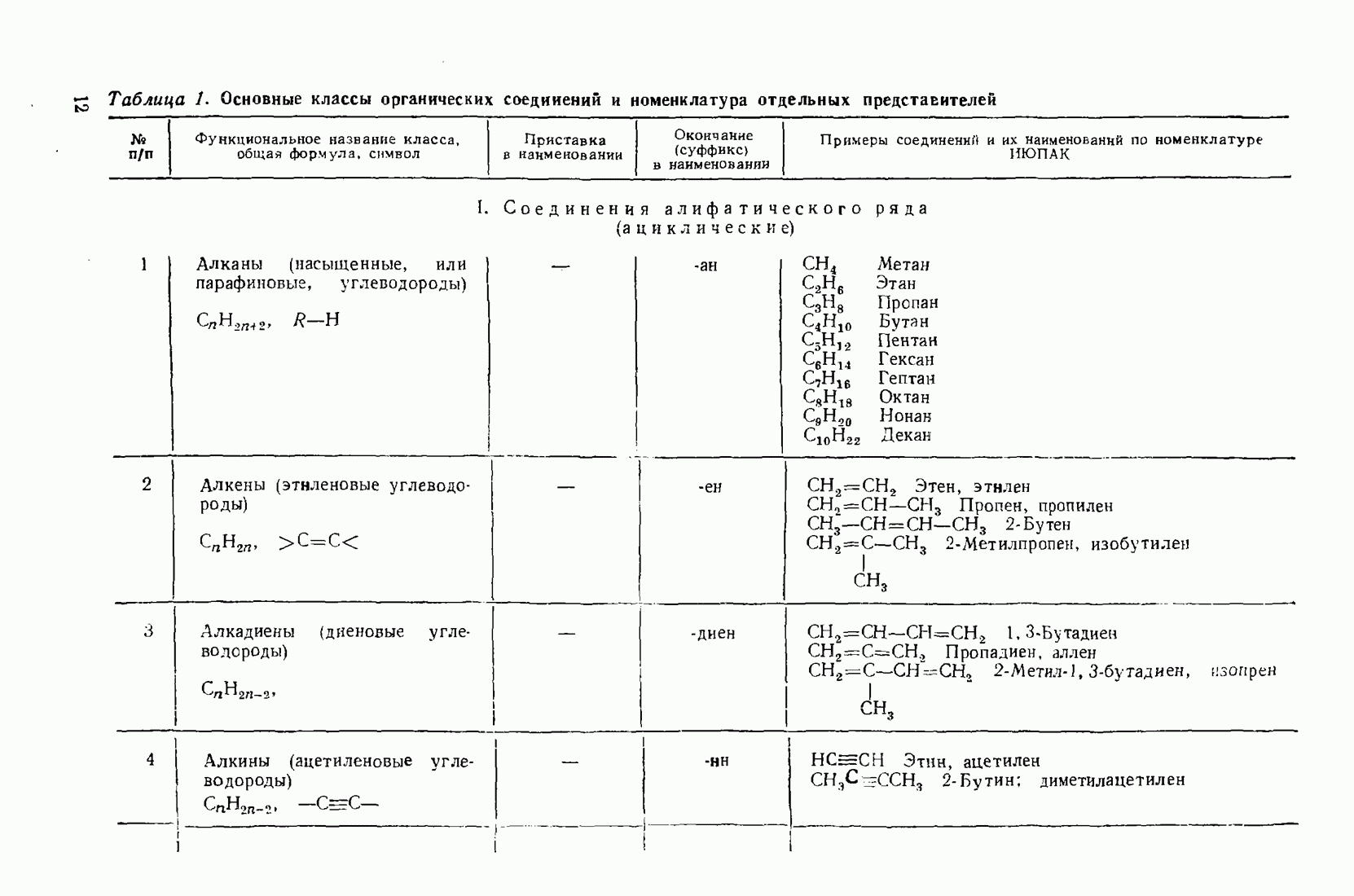
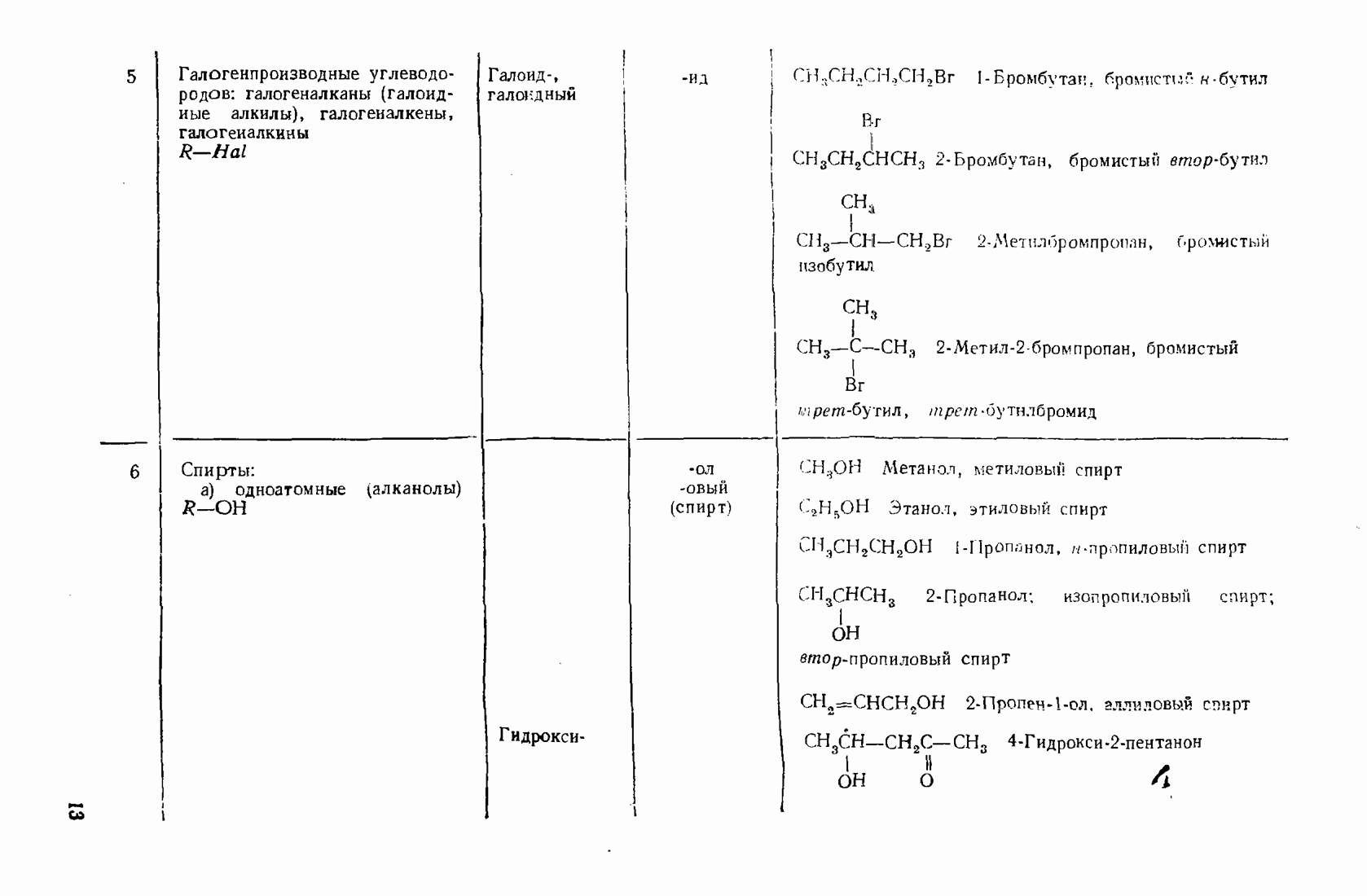
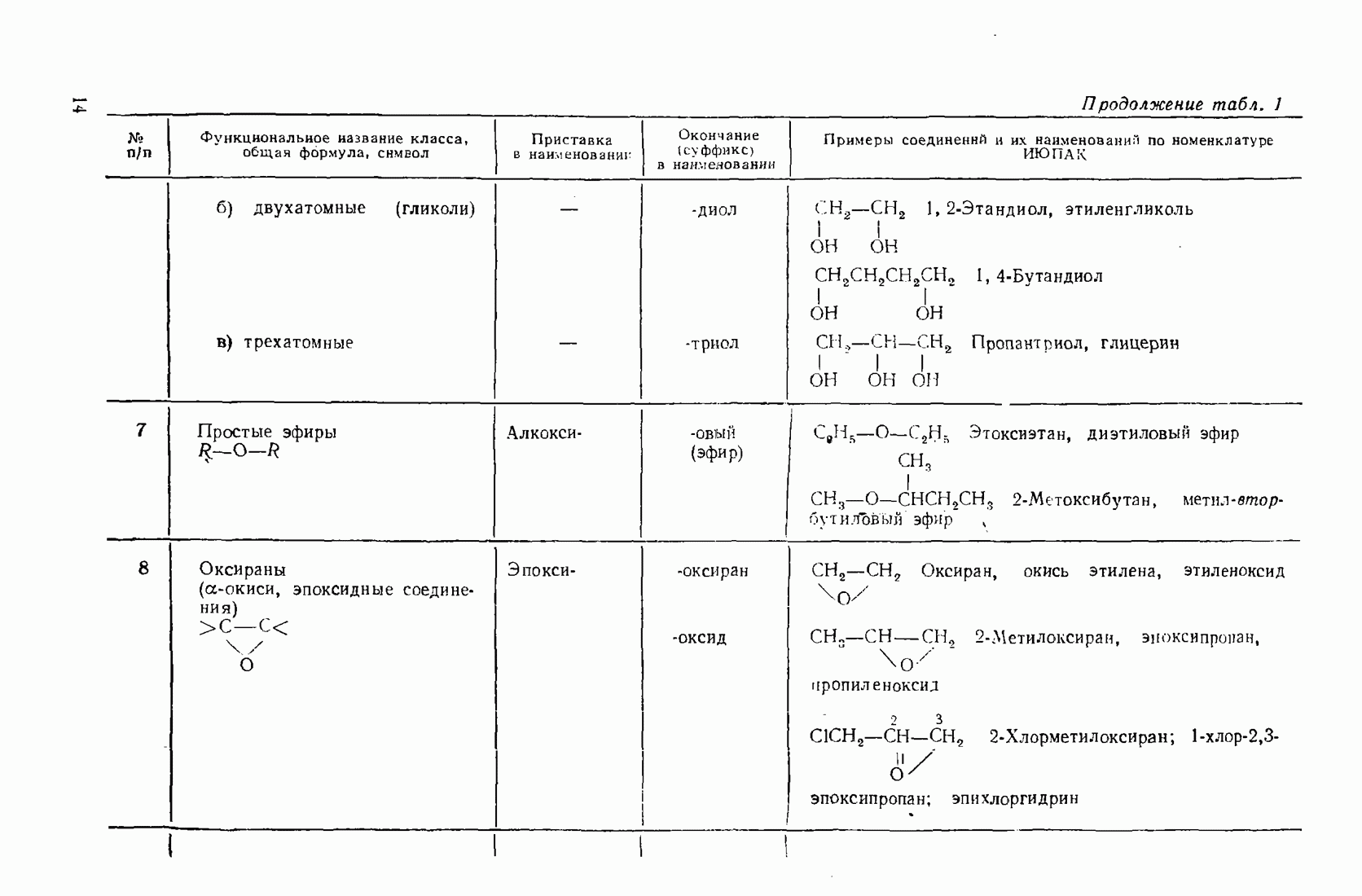
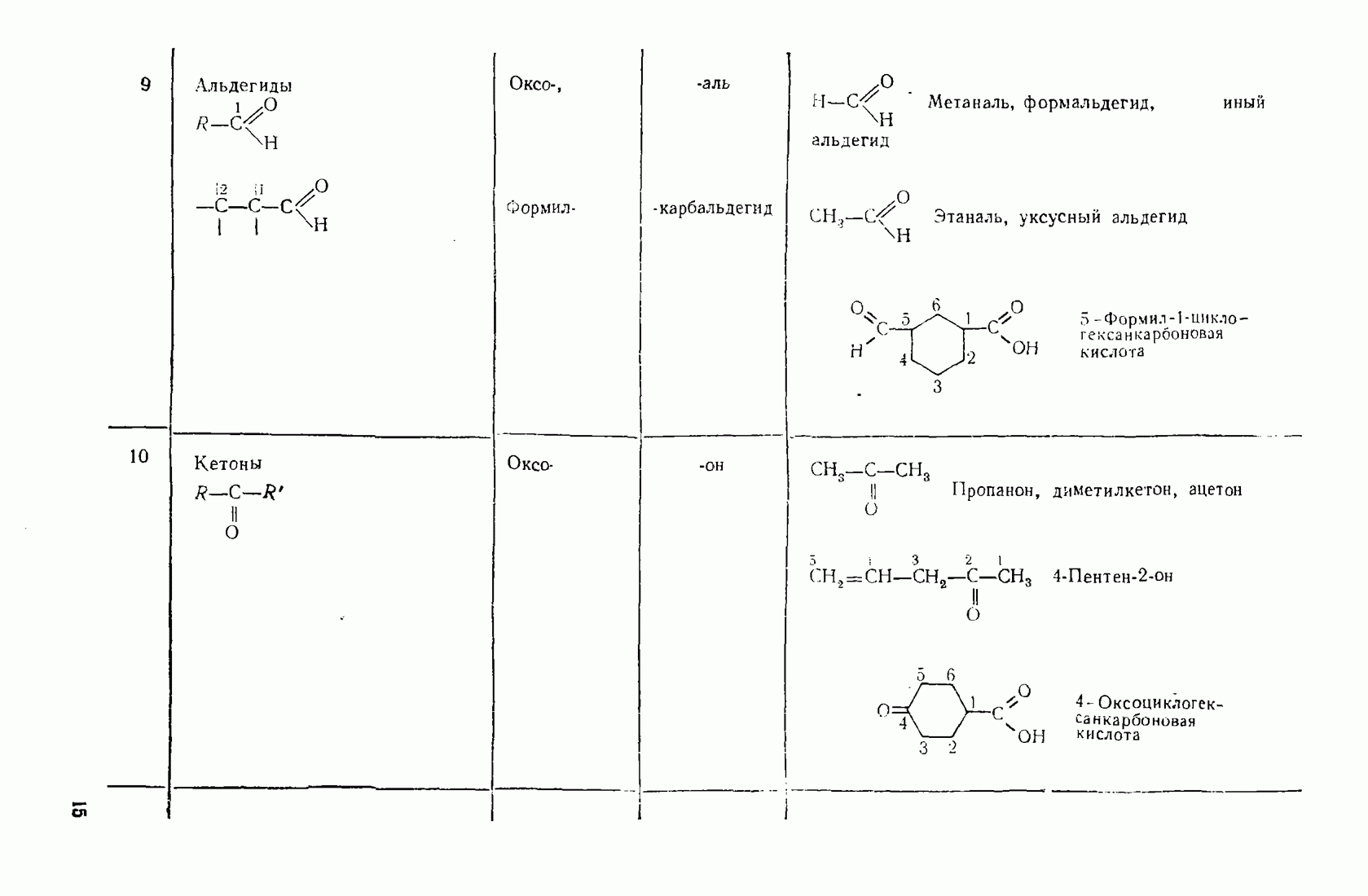
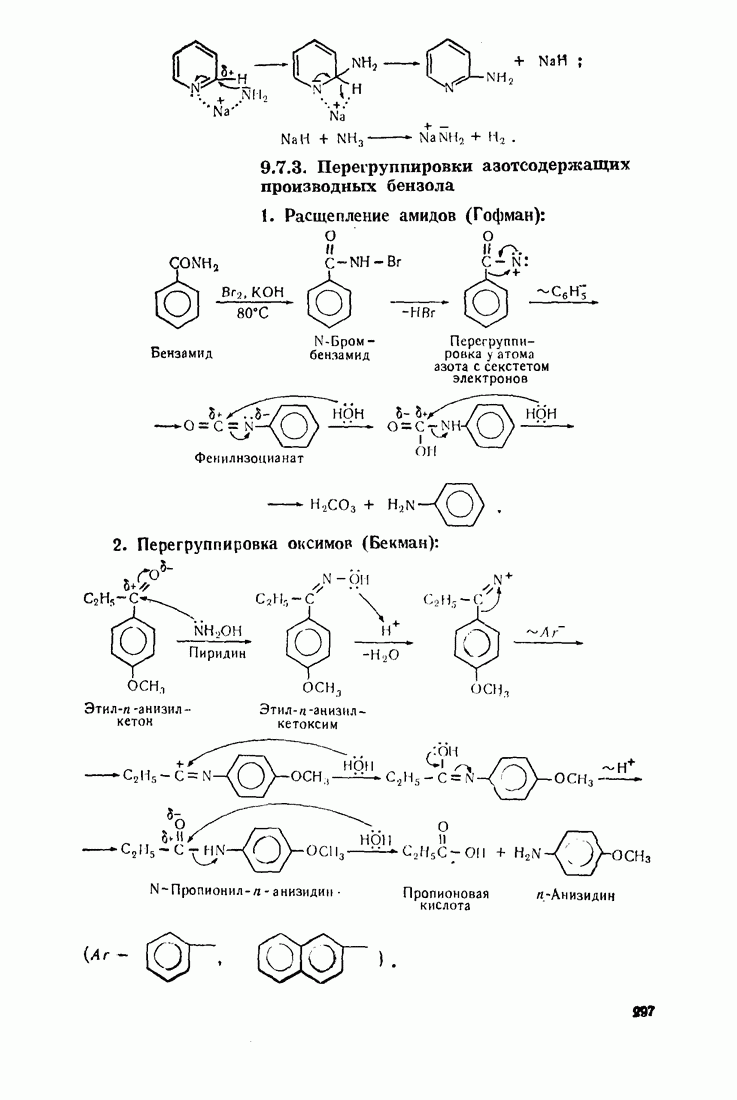
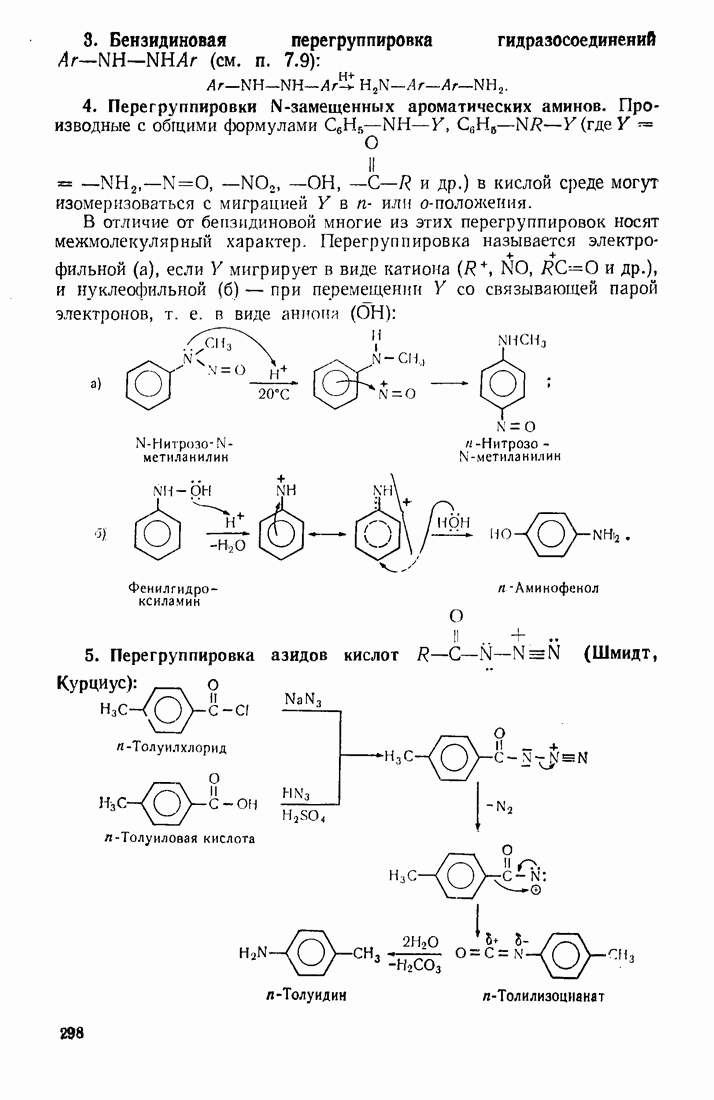
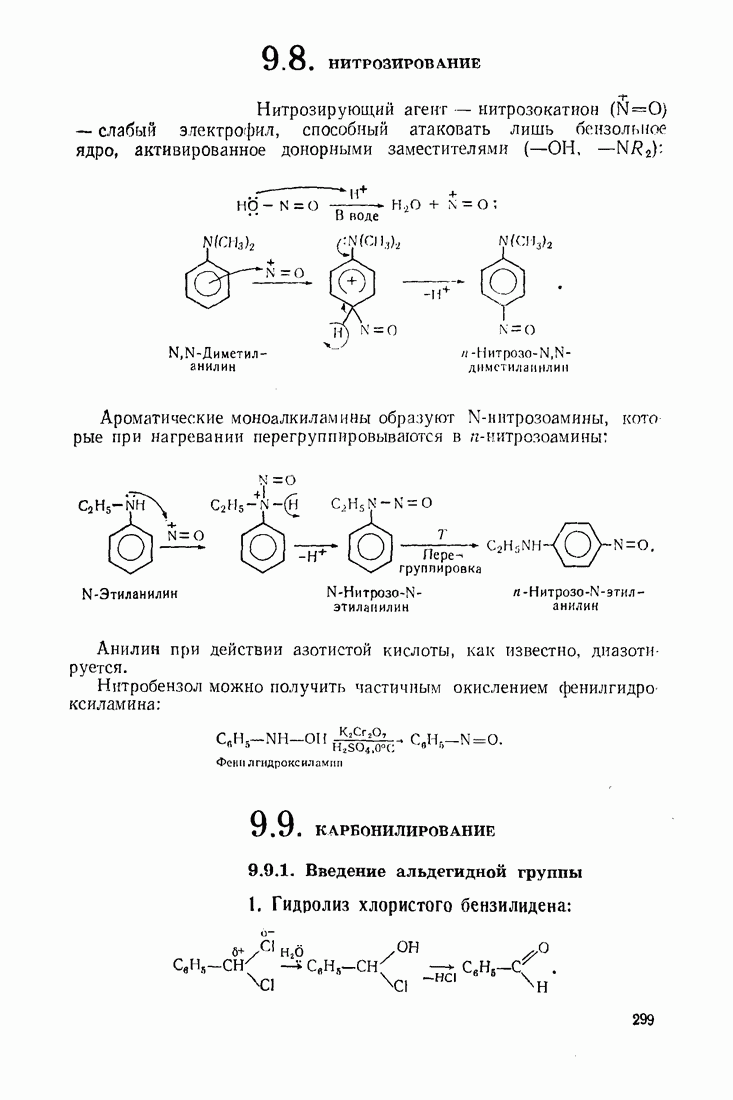
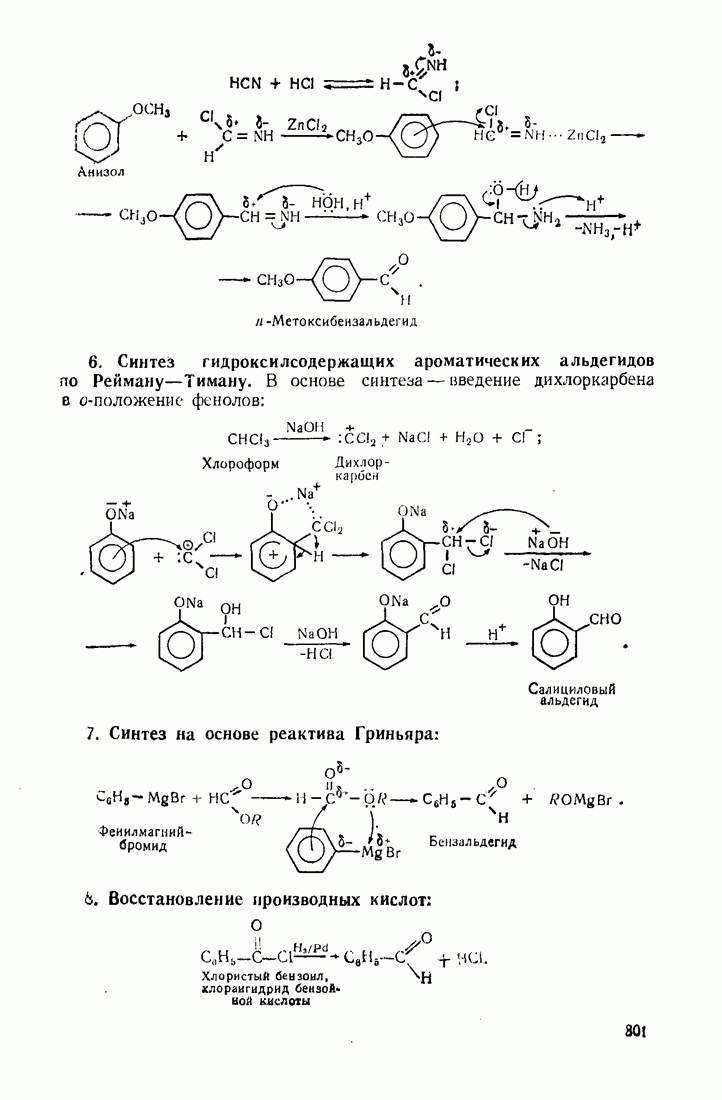
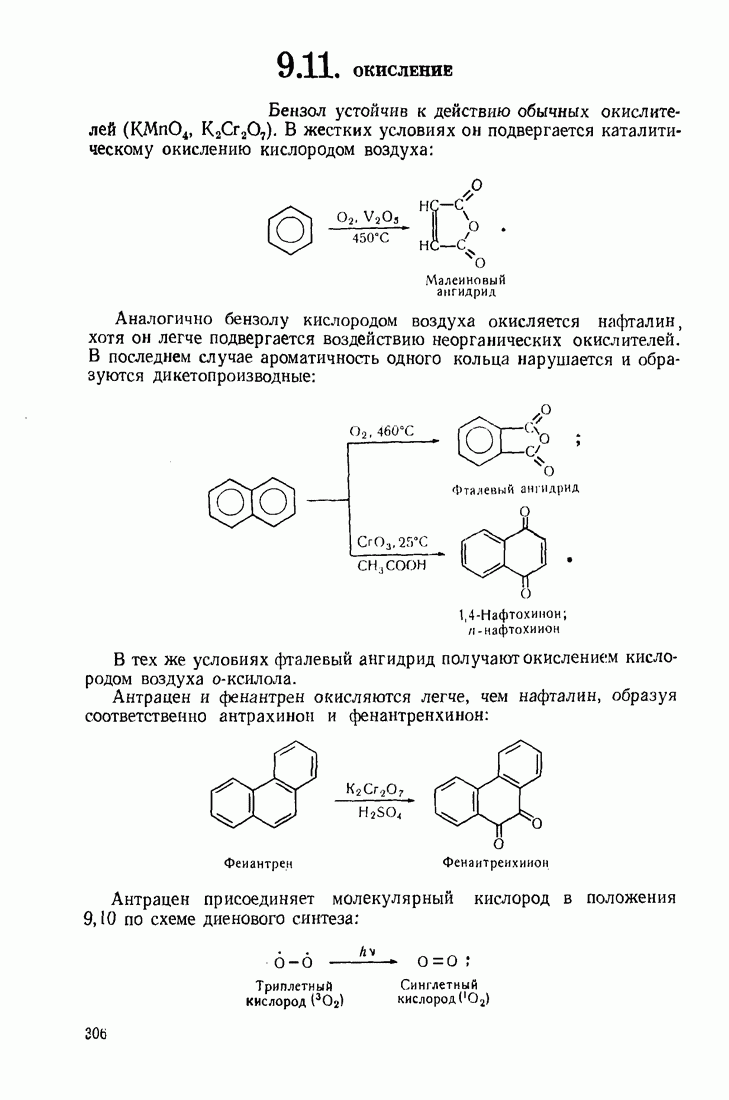
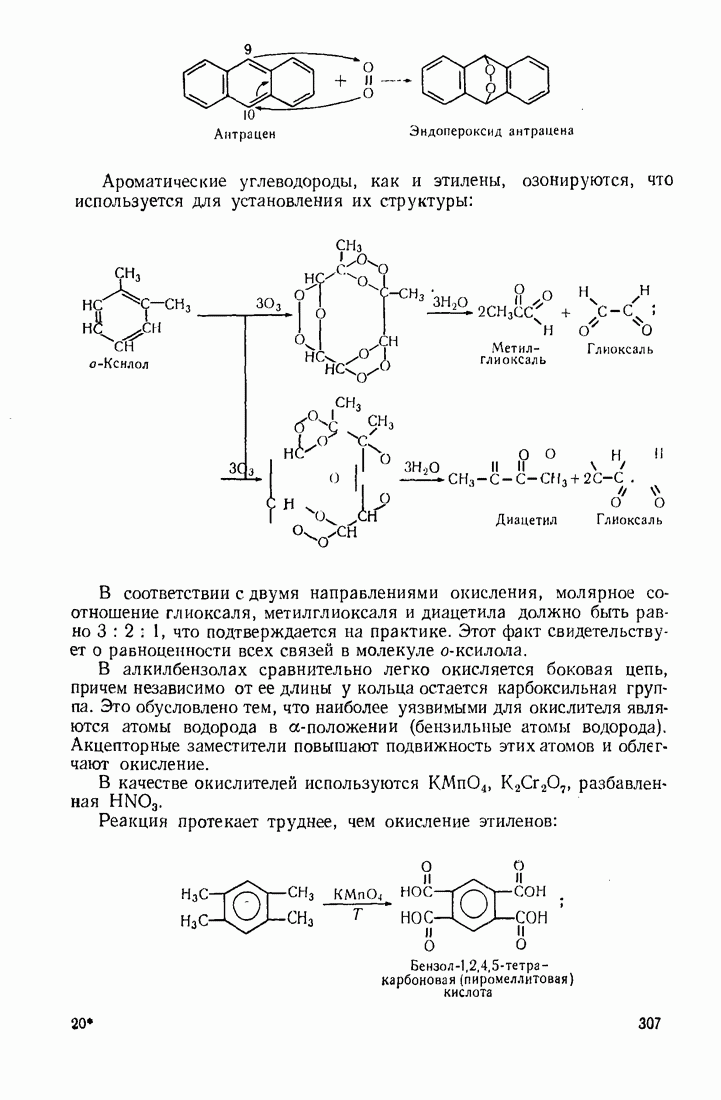
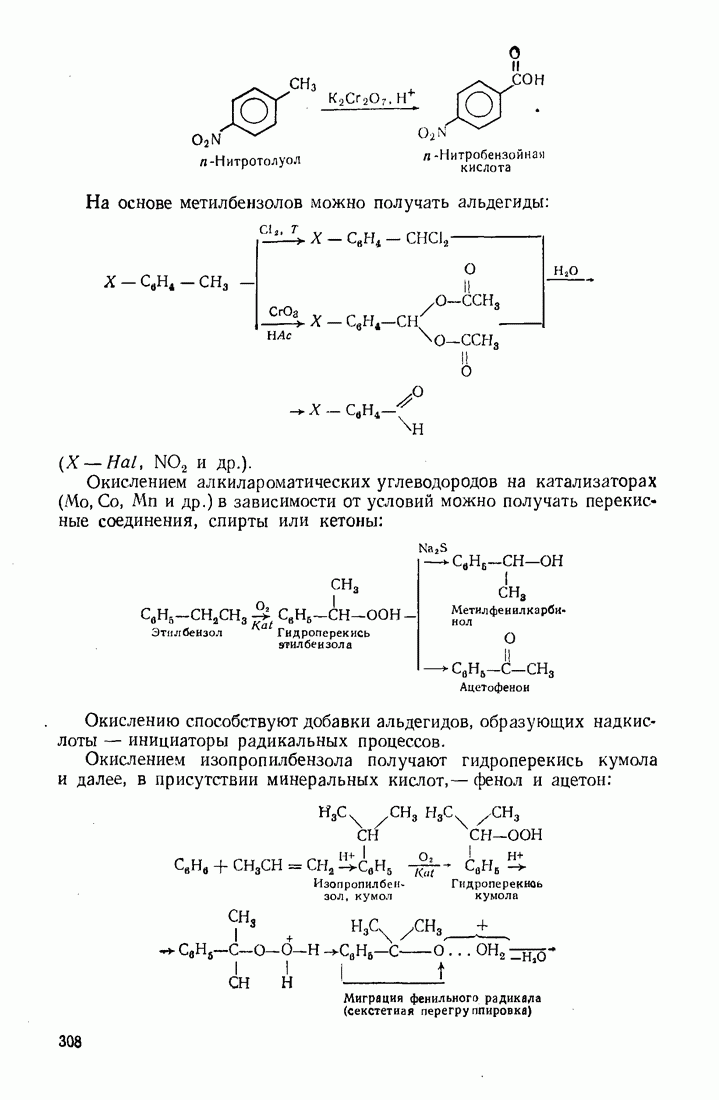
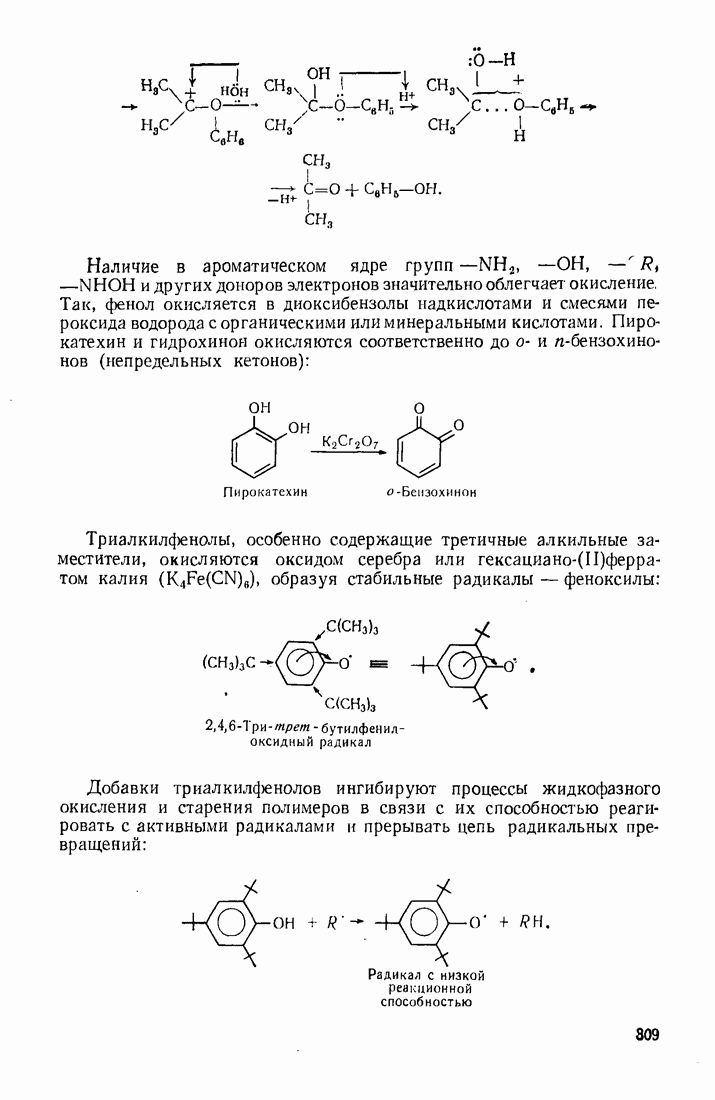
11.3. МЕГАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
Реакционная способность металлооргаиических соединений в значительной мере зависит от полярности связи  которая, в свою очередь, определяется электроотрицательностью элемента. Чем более выражен ионный характер этой связи (табл. 12), тем выше активность соединения.
которая, в свою очередь, определяется электроотрицательностью элемента. Чем более выражен ионный характер этой связи (табл. 12), тем выше активность соединения.
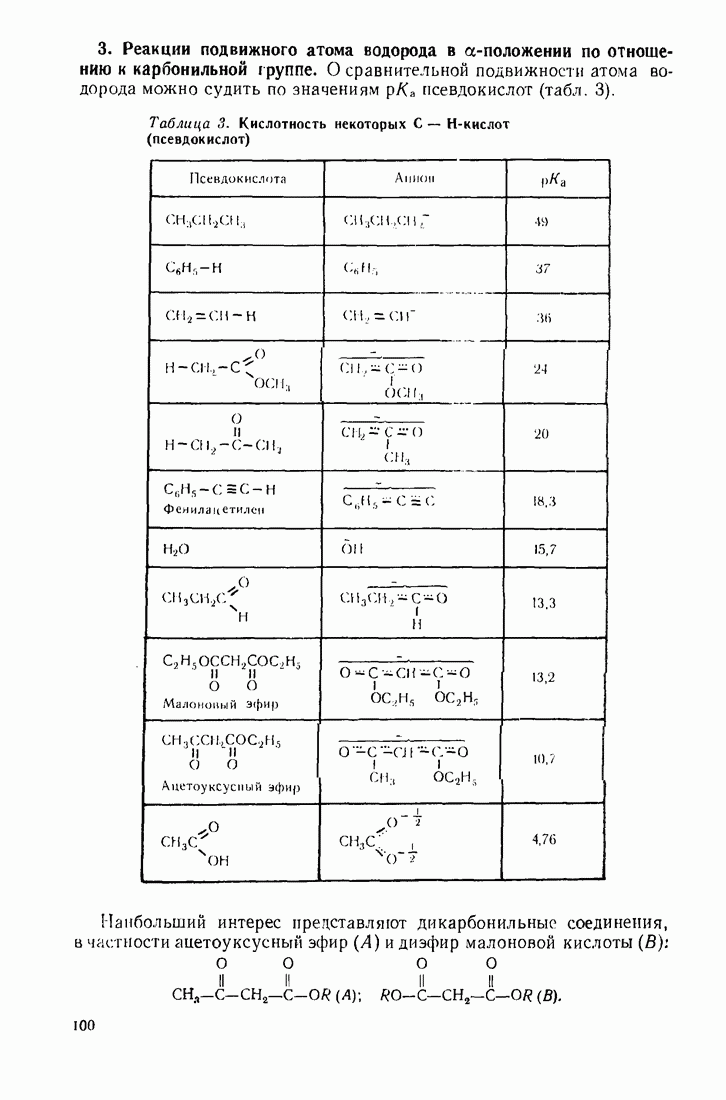
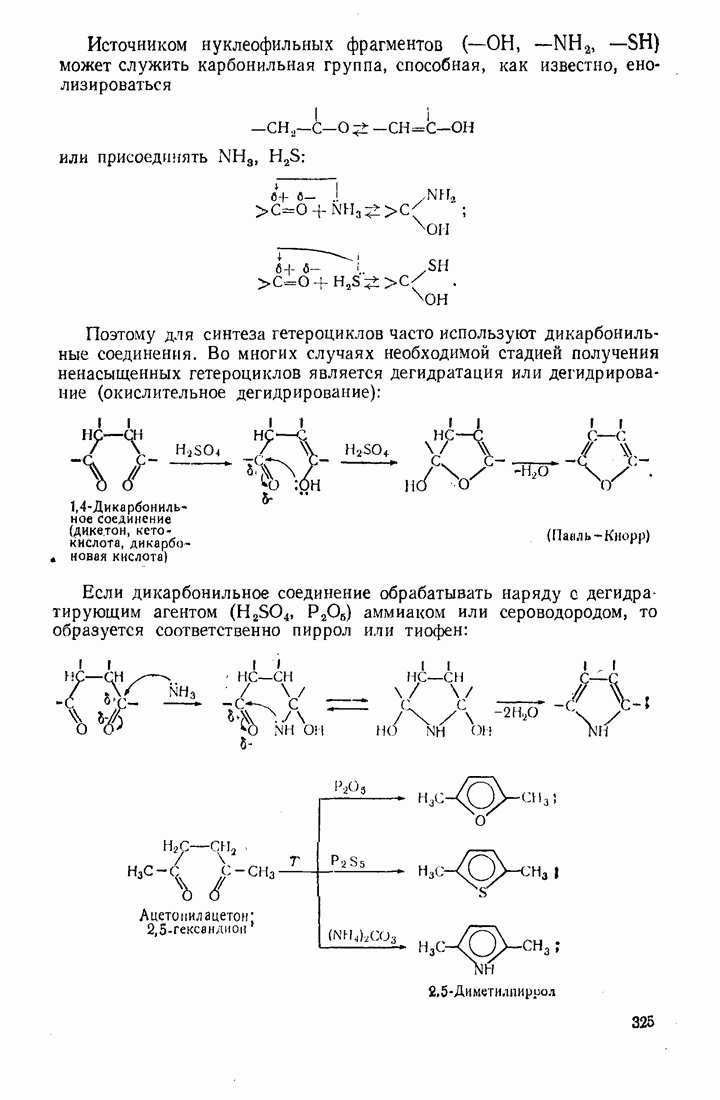
Таблица 12. (см. скан) Степень ионности связи  по Полингу
по Полингу
Атом металла, включенный в связь  всегда является объектом нуклеофильной атаки, а атом углерода, несущий отрицательный заряд, — электрофильной.
всегда является объектом нуклеофильной атаки, а атом углерода, несущий отрицательный заряд, — электрофильной.
Металлоорганические соединения можно рассматривать как псевдооснования, способные передавать электрофильному реагенту пару электронов группой атомов (в виде алкиланиона):

Если валентность элемента больше единицы, то увеличение количества связей  в соединении повышает его реакционную способность.
в соединении повышает его реакционную способность.
11.3.1. Органические соединения щелочных металлов
Соединения лития, натрия, калия содержат сильно поляризованную связь и представляют собой ионные, солеобразные, нерастворимые в органических растворителях вещества. Несколько своеобразны соединения лития. Сравнительно высокая степень ковалентности связи  делает их растворимыми в инертных растворителях.
делает их растворимыми в инертных растворителях.
Соединения этой группы чрезвычайно активны, разлагаются при контакте с влагой и кислородом воздуха и сравнительно легко взаимодействуют с такими слабыми нуклеофилами, как олефины.
На практике чаще всего используются литийпроизводные (бутил-литий  реже — соединения натрия и калия (амилнатрий
реже — соединения натрия и калия (амилнатрий 
Соединения щелочных металлов получают следующими основными способами:

В реакциях обмена (4,5) более активный металл замещает менее активный, более сильная  -кислота вытесняет слабую;
-кислота вытесняет слабую;
6) натрии и калин расщепляют простые ароматические эфиры, особенно легко эта реакция протекает для бензпловых эфиров:

Наиболее характерные реакции органических производных щелочных металлов:
1. Присоединение по углерод-углеродным и полярным кратным связями  и др.
и др.


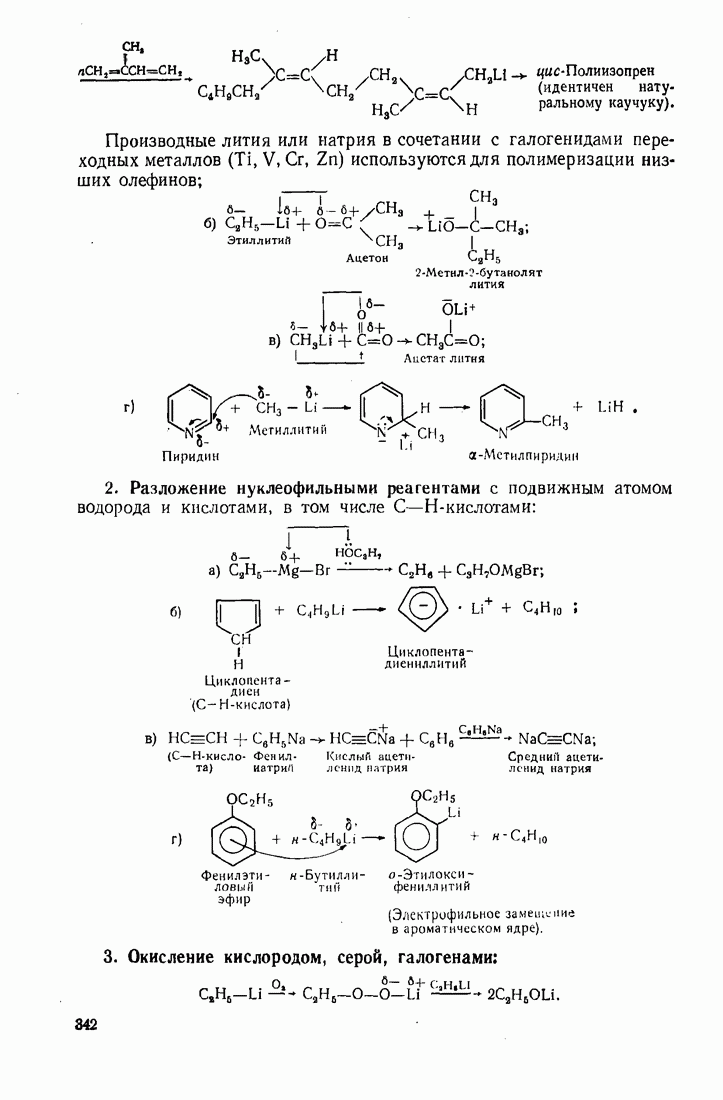
Производные лития или натрия в сочетании с галогенидами переходных металлов  используются для полимеризации низших олефинов;
используются для полимеризации низших олефинов;
(см. скан)
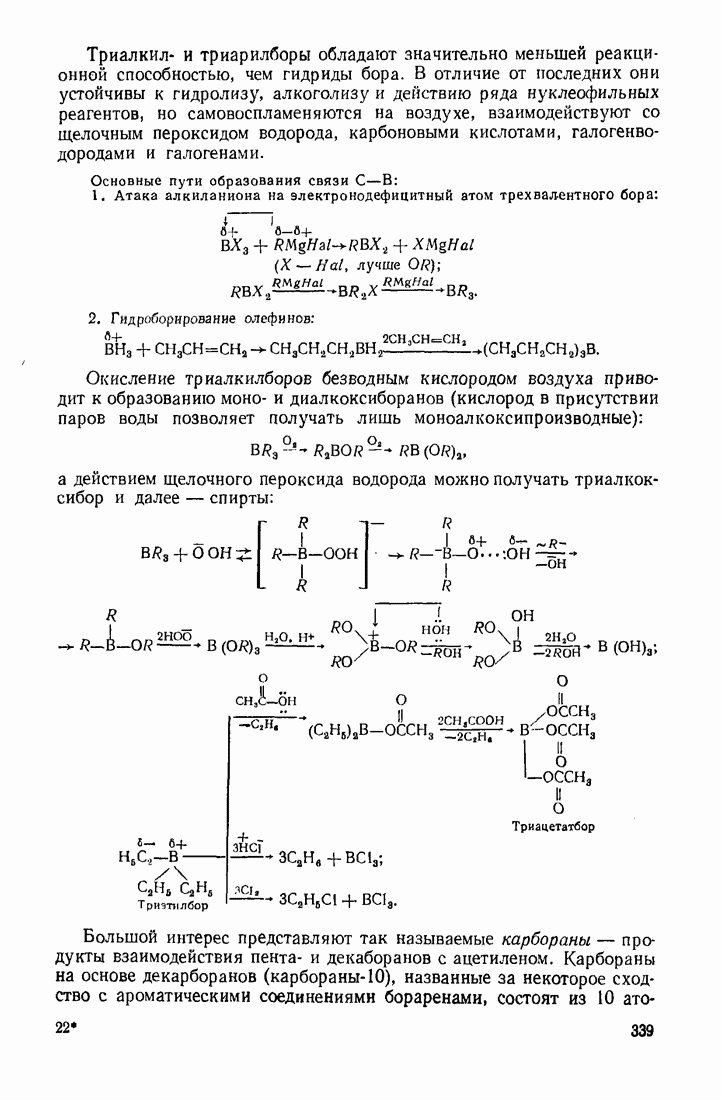
2. Разложение нуклеофильными реагентами с подвижным атомом водорода и кислотами, в том числе  -кислотами:
-кислотами:
(см. скан)
3. Окисление кислородом, серой, галогенами:

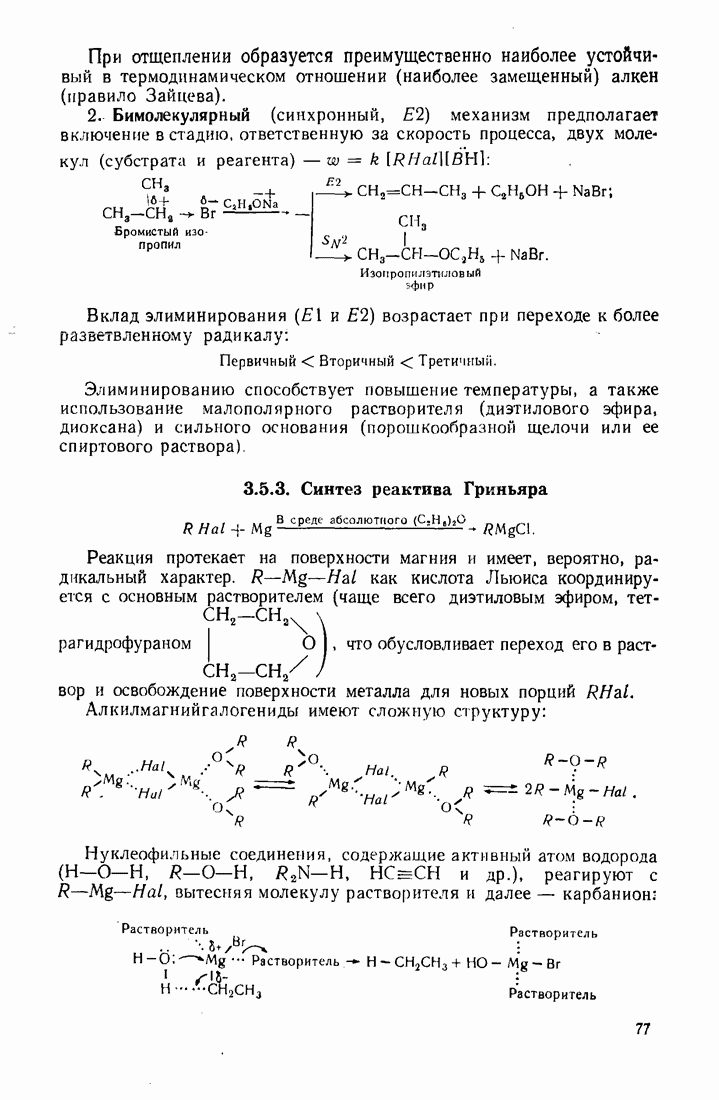
4. Реакции отщепления (алкилметалл является источником сильного основания 

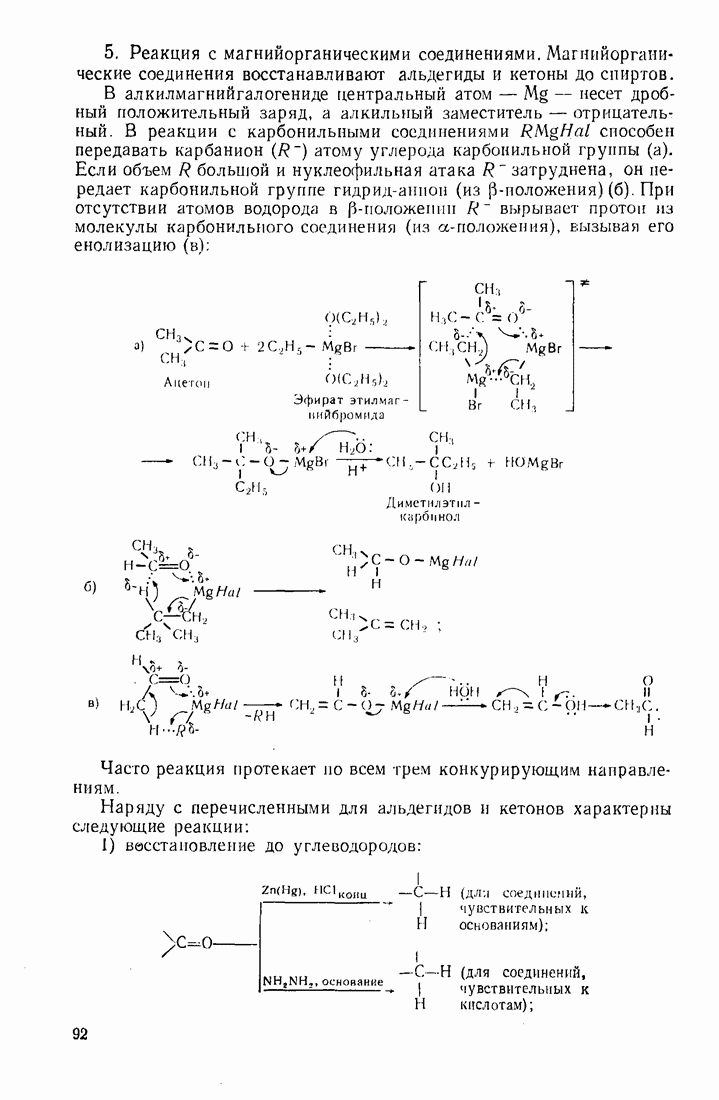
11.3.2. Магнийорганические соединения
Магний, как и другие элементы второй группы, может образовывать полные и смешанные  углеродсодержащие соединения.
углеродсодержащие соединения.
Наиболее доступными и важными в практическом отношении являются алкил- или арилмагнийгалогениды (реактивы Гриньяра):

Легкость внедрения  по связи С-Hal возрастает в ряду галогенов:
по связи С-Hal возрастает в ряду галогенов: 
Арилгалогениды, особенно арилхлориды, вступают в реакцию труднее соответствующих алкилпроизводных. Магнийорганические фториды не образуются.
 и
и  -Дибромбензолы и дибромнафталин образуют бифункциональные производные. В алифатическом ряду димагнийгалогениды получают лишь при использовании соединений с атомами галогенов, изолированными не менее чем четырьмя атомами углерода. Исключение составляют галогеналканы с перфорированными алкильными радикалами.
-Дибромбензолы и дибромнафталин образуют бифункциональные производные. В алифатическом ряду димагнийгалогениды получают лишь при использовании соединений с атомами галогенов, изолированными не менее чем четырьмя атомами углерода. Исключение составляют галогеналканы с перфорированными алкильными радикалами.
В химическом отношении магнийорганические соединения менее активны, чем производные щелочных металлов, что делает их более удобными в работе.
Реактивы Гриньяра вступают во многие реакции, свойственные соединениям металлов первой группы.
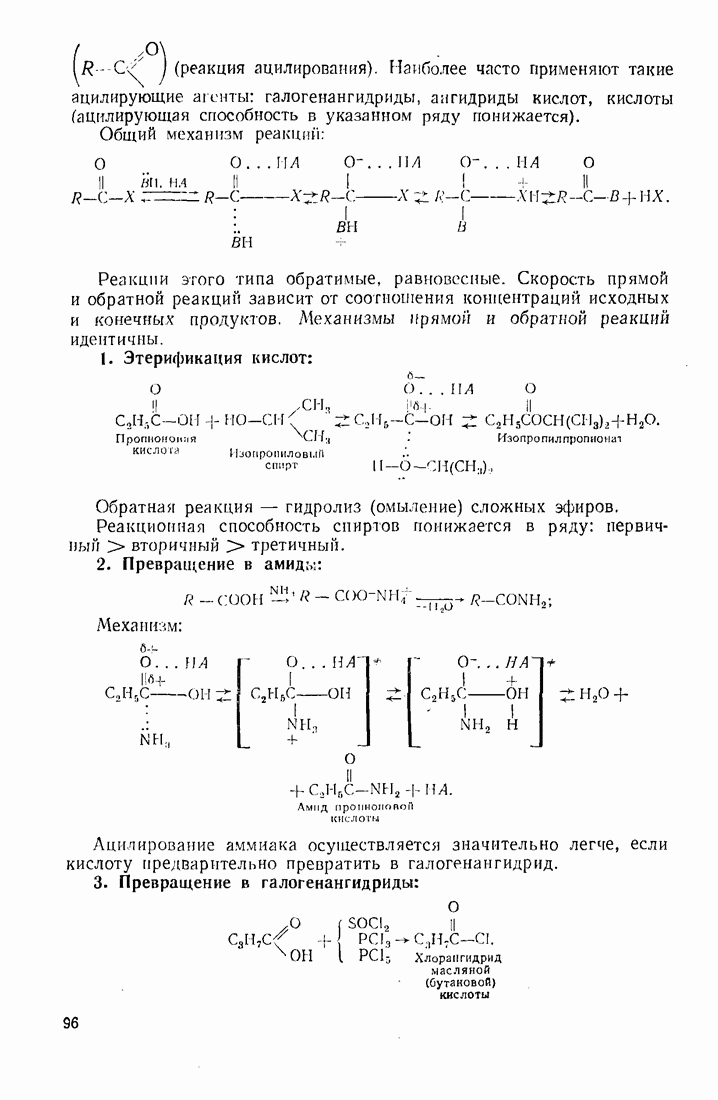
1. Разложение  -кислотами, в том числе нуклеофильными реагентами с подвижным атомом водорода (карбоновыми кислотами, водой, спиртами, аммиаком, аминами, амидами и т. д.):
-кислотами, в том числе нуклеофильными реагентами с подвижным атомом водорода (карбоновыми кислотами, водой, спиртами, аммиаком, аминами, амидами и т. д.):

2. Присоединение к полярным кратным связям  и малым гетероциклам
и малым гетероциклам 
(см. скан)
Алкилмагнийгалогениды в отличие от производных щелочных металлов присоединяются к олефиновым связям с большим трудом:

В реакции с  -ненасыщенным сложным эфиром осуществляется 1,4-присоединение:
-ненасыщенным сложным эфиром осуществляется 1,4-присоединение:

В случае  -ненасыщенных кетонов и альдегидов такое 1,4-присоединение конкурирует с обычным присоединением по карбонильной группе.
-ненасыщенных кетонов и альдегидов такое 1,4-присоединение конкурирует с обычным присоединением по карбонильной группе.
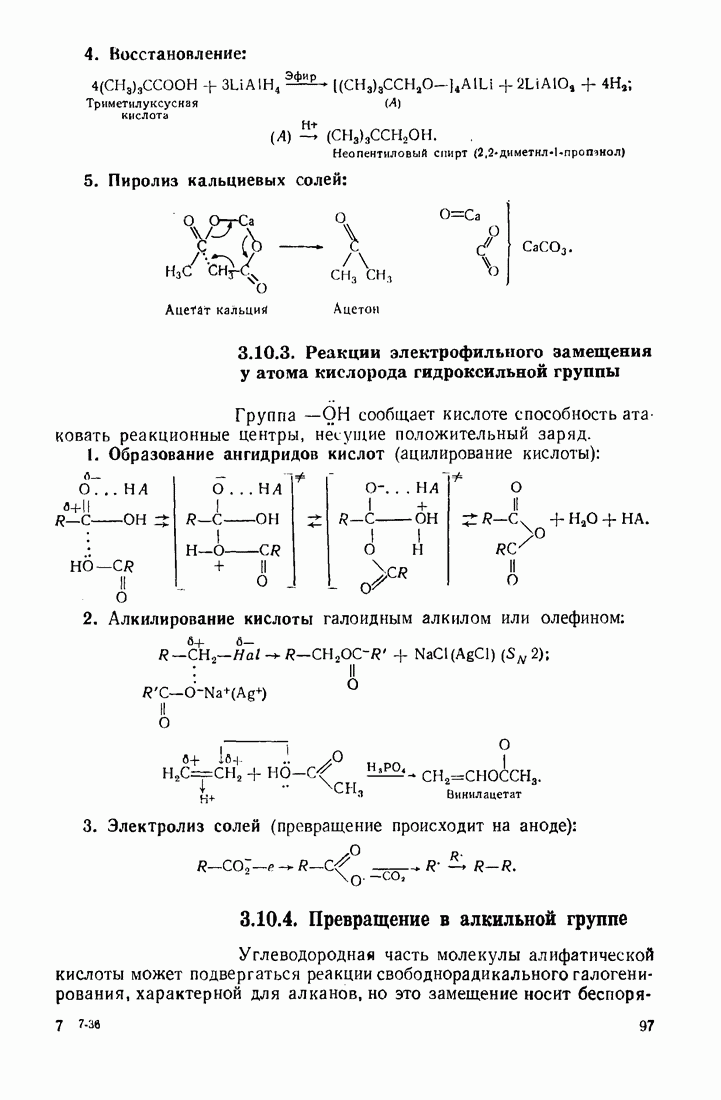
3. Окисление алкилмагнийгалогенидов кислородом, серой, галогенами:

11.3.3. Цинк- и кадмийорганические соединения
Соединения цинка и кадмия — летучие жидкости с малополяризованными связями 
В основу способов их получения положены реакции алкилирования металла и замещения одного металла другим. В последнем случае образуется, как правило, более стабильное металлоорганическое соединение. Исключение составляет ртуть, способная восстанавливаться из диалкнлпроизводных многими металлами:

Производные цинка и в еще большей мере — производные кадмия по реакционной способности уступают магнийорганическим соединениям. Они не реагируют с углекислым газом, однако легко разлагаются кислородом воздуха (цинкпроизводные — самовоспламеняются) и нуклеофильньши реагентами с подвижным атомом водорода.
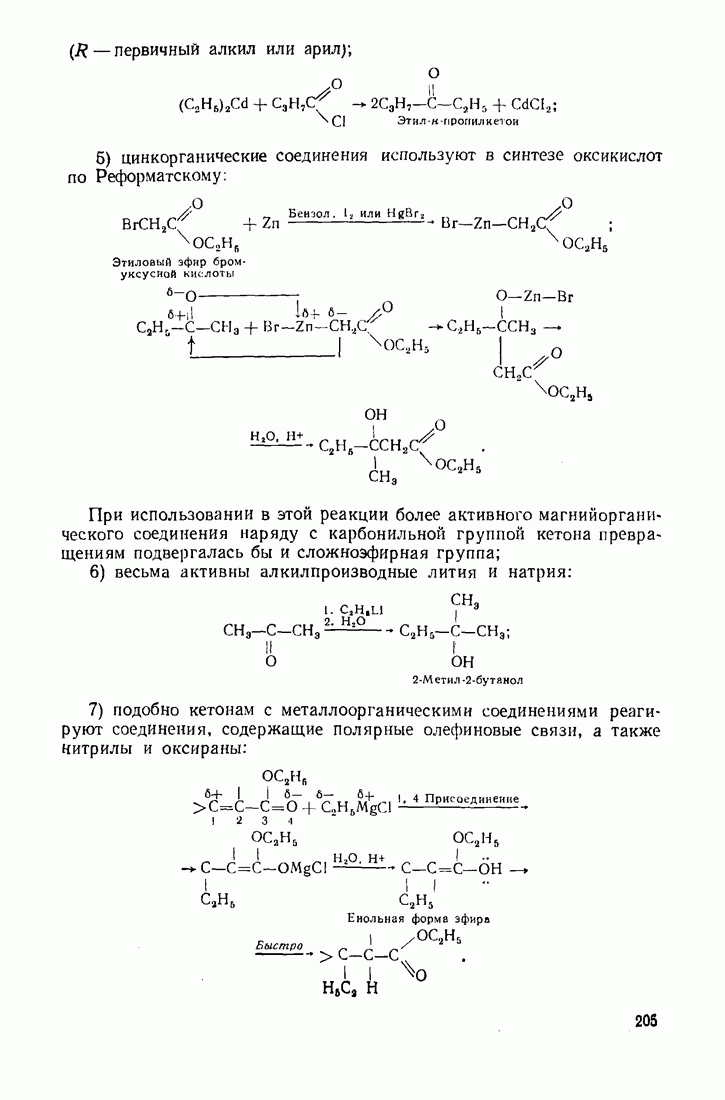
Умеренная активность алкилцинкгалогенидов позволяет успешно применять их для синтеза оксикислот из сложных эфиров, содержащих в  -положении галоген (Реформатский), и кетонов (альдегидов), не затрагивая сложноэфирную карбонильную группу:
-положении галоген (Реформатский), и кетонов (альдегидов), не затрагивая сложноэфирную карбонильную группу:

Алкилцинкгалогениды более удобны, чем магнийпроизводные, для получения кетонов из галогенангидридов кислот, так как в условиях синтеза они не реагируют с образующимся кетоном.
Кадмийорганические соединения могут замещать подвижные атомы галогена на алкильный радикал, но не реагируют с карбонильными соединениями и нитрилами:

11.3.4. Алюминийорганические соединения
Представляют интерес следующие соединения алюминия: алкилалюминийгидриды —  алкил-алюминийхлориды —
алкил-алюминийхлориды —  алкилалюминийгидриды лития:
алкилалюминийгидриды лития:

Основные способы получения алюминийтриалкилов:

Триметилалюминий образует димер, в котором мономеры удерживаются за счет трехцентровых орбиталей: одновалентный радикал  связывает два атома алюминия:
связывает два атома алюминия:

Алюминийорганические соединения энергично разлагаются водой, спиртами, кислотами, значительно легче присоединяются по карбонильной группе оксосоедииений и оксида углерода ( чем реактивы Гриньяра, окисляются кислородом воздуха (низшие представители самовоспламеняются на воздухе):
чем реактивы Гриньяра, окисляются кислородом воздуха (низшие представители самовоспламеняются на воздухе):

Замечательным свойством алюминийтриалкилов является присоединение к олефинам (Циглер):


Полимеризующую активность алюминийтриалкила значительно повышают добавки галогенидов некоторых металлов:  (чаще всего используется
(чаще всего используется  Смешанные катализаторы (катализаторы Циглера-Натта) позволяют осуществлять полимеризацию этилена, пропилена, изобутилена и других олефинов при низком давлении. При этом образуются стереорегулярные полимеры, т. е. полимеры с однотипным расположением звеньев относительно двойной связи
Смешанные катализаторы (катализаторы Циглера-Натта) позволяют осуществлять полимеризацию этилена, пропилена, изобутилена и других олефинов при низком давлении. При этом образуются стереорегулярные полимеры, т. е. полимеры с однотипным расположением звеньев относительно двойной связи  или транс-положении).
или транс-положении).
11.3.5. Органические производные некоторых тяжелых металлов
Органические соединения ртути, свинца, олова и сурьмы в химическом отношении довольно инертны. Так, ртутьорганические соединения не окисляются на воздухе, не разлагаются водой и не реагируют с карбонильными соединениями. Полные органические производные (например, более активны, чем смешанные  где X —галоген или другой анион).
где X —галоген или другой анион).
Основные методы синтеза:
1) реакции обмена металлов между магнийорганическнми соединениями и хлоридами металлов:

2) реакция прямого введения металла в связь 
(см. скан)
Диалкилртуть, а еще легче диарилртуть, реагирует с концентрированными минеральными кислотами, теряя один радикал;
восстанавливается водородом и металлами  и др.). окисляется галогенидами:
и др.). окисляется галогенидами:

Так называемые квазикомплексные ртутьорганические соединения  получаемые присоединением солей ртути
получаемые присоединением солей ртути  к этиленовым и ацетиленовым соединениям, регенерируют исходные непредельные под действием ионов галогенов:
к этиленовым и ацетиленовым соединениям, регенерируют исходные непредельные под действием ионов галогенов:

Связь  в органических соединениях тяжелых металлов легко претерпевает гомолитический разрыв, генерируя алкильные радикалы:
в органических соединениях тяжелых металлов легко претерпевает гомолитический разрыв, генерируя алкильные радикалы:

Тетраалкилпроизводные свинца  и др.) используют в качестве антидетонаторов, а оловоорганические соединения, например малеат дибутилолова, — в качестве ингибиторов окислительных процессов старения полимеров (каучуков, поливинилхлорида).
и др.) используют в качестве антидетонаторов, а оловоорганические соединения, например малеат дибутилолова, — в качестве ингибиторов окислительных процессов старения полимеров (каучуков, поливинилхлорида).
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. Введение
- 1.1. Предмет органической химии
- 1.2. Основные этапы развития органической химии
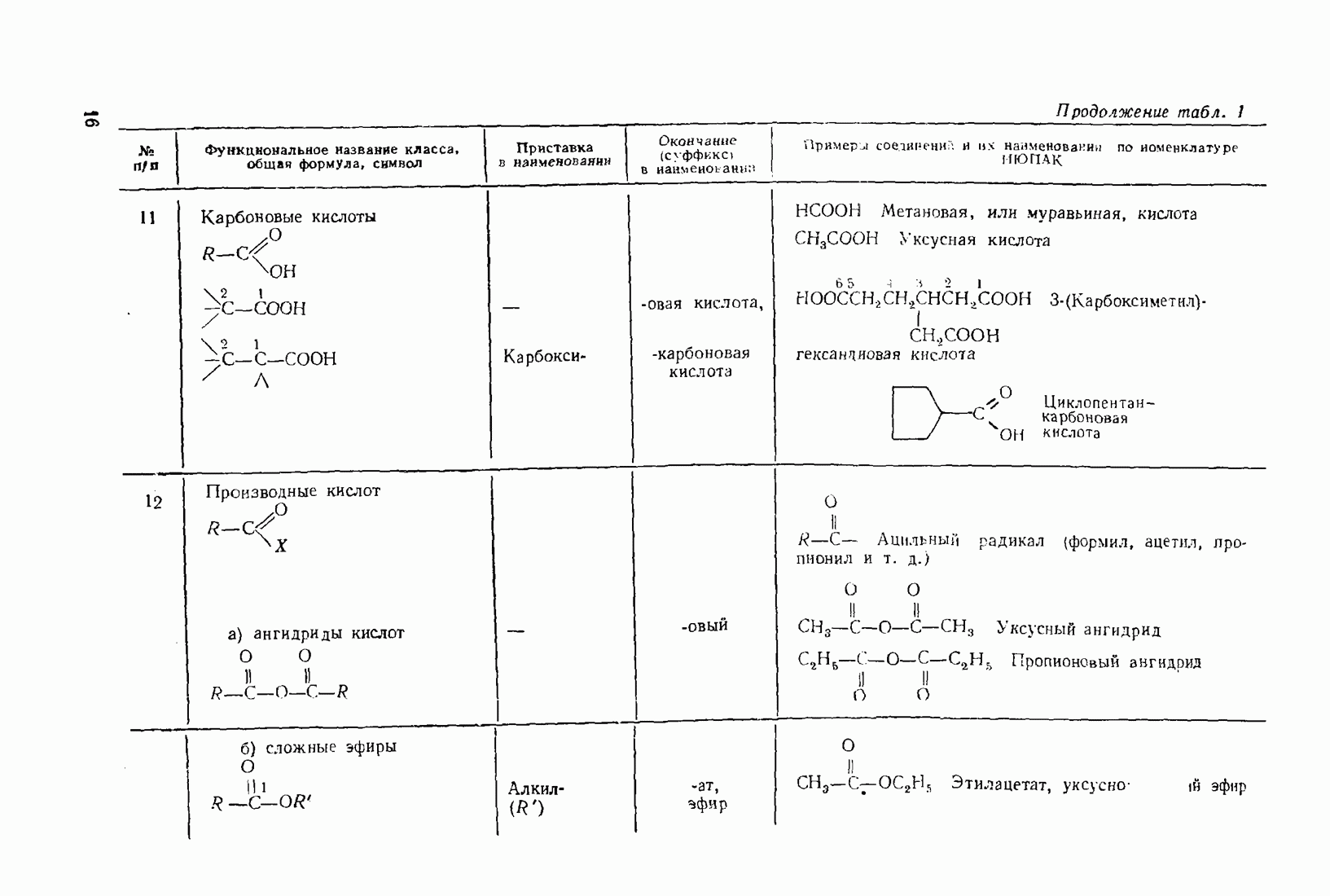
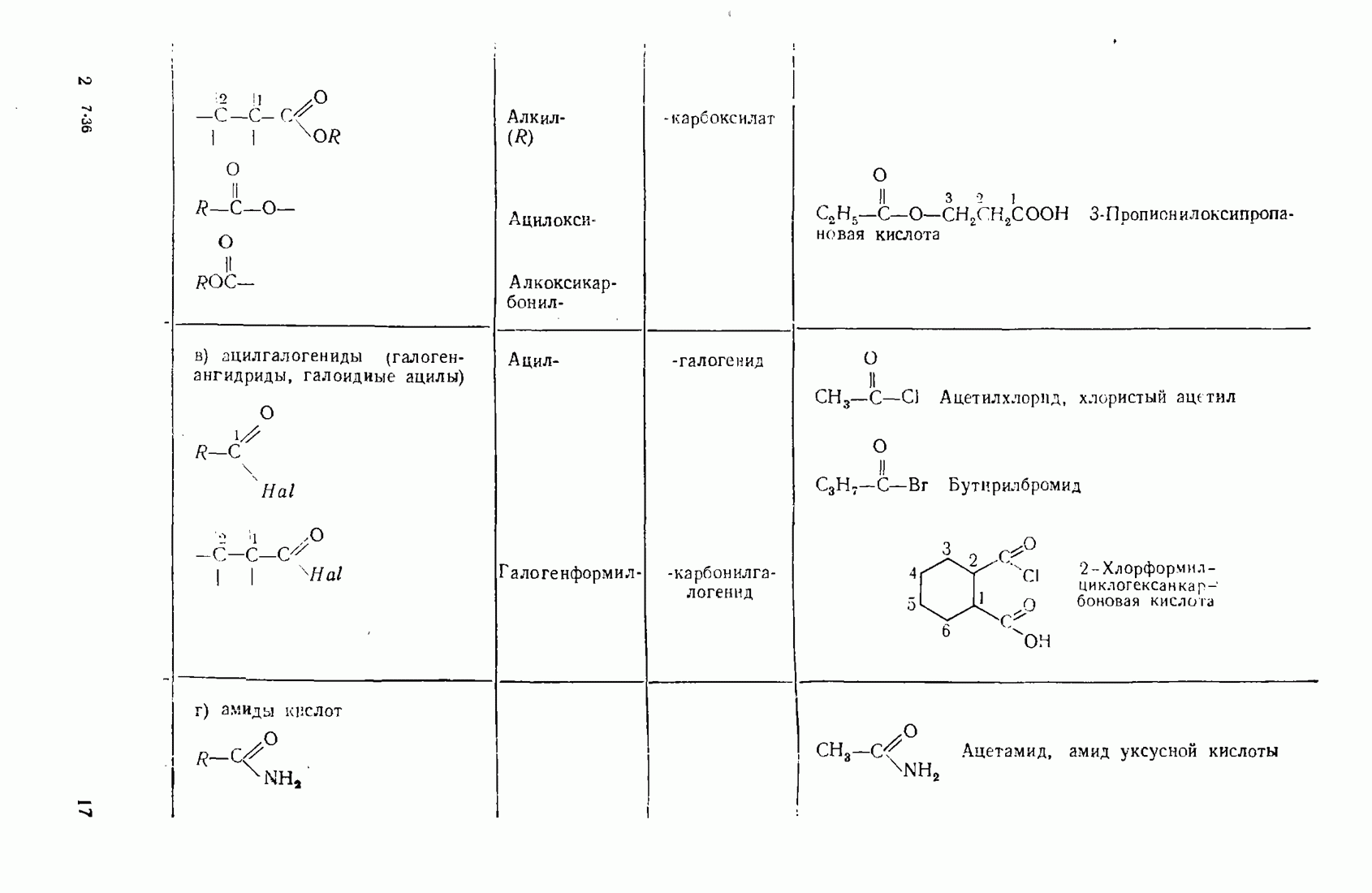
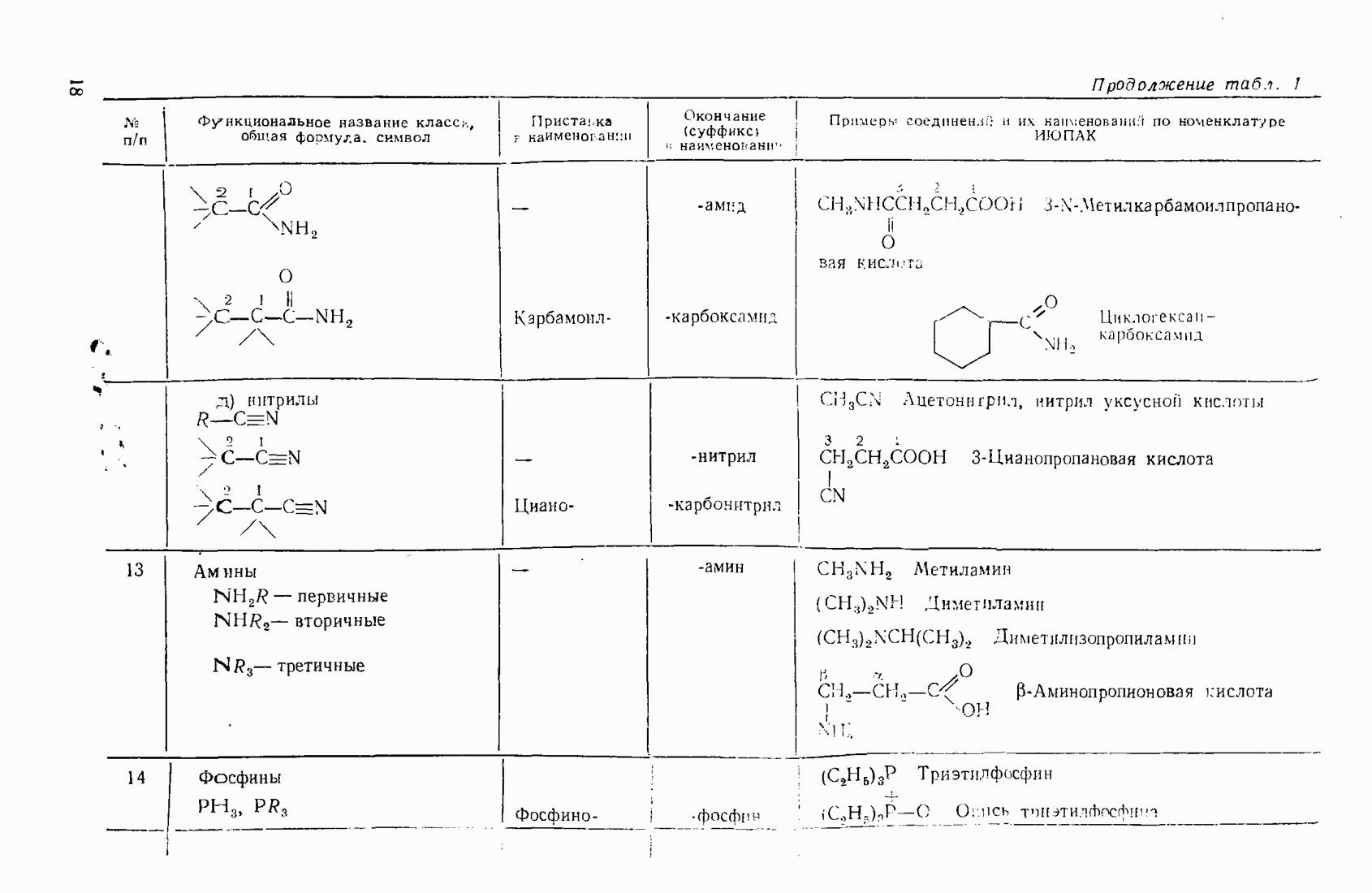
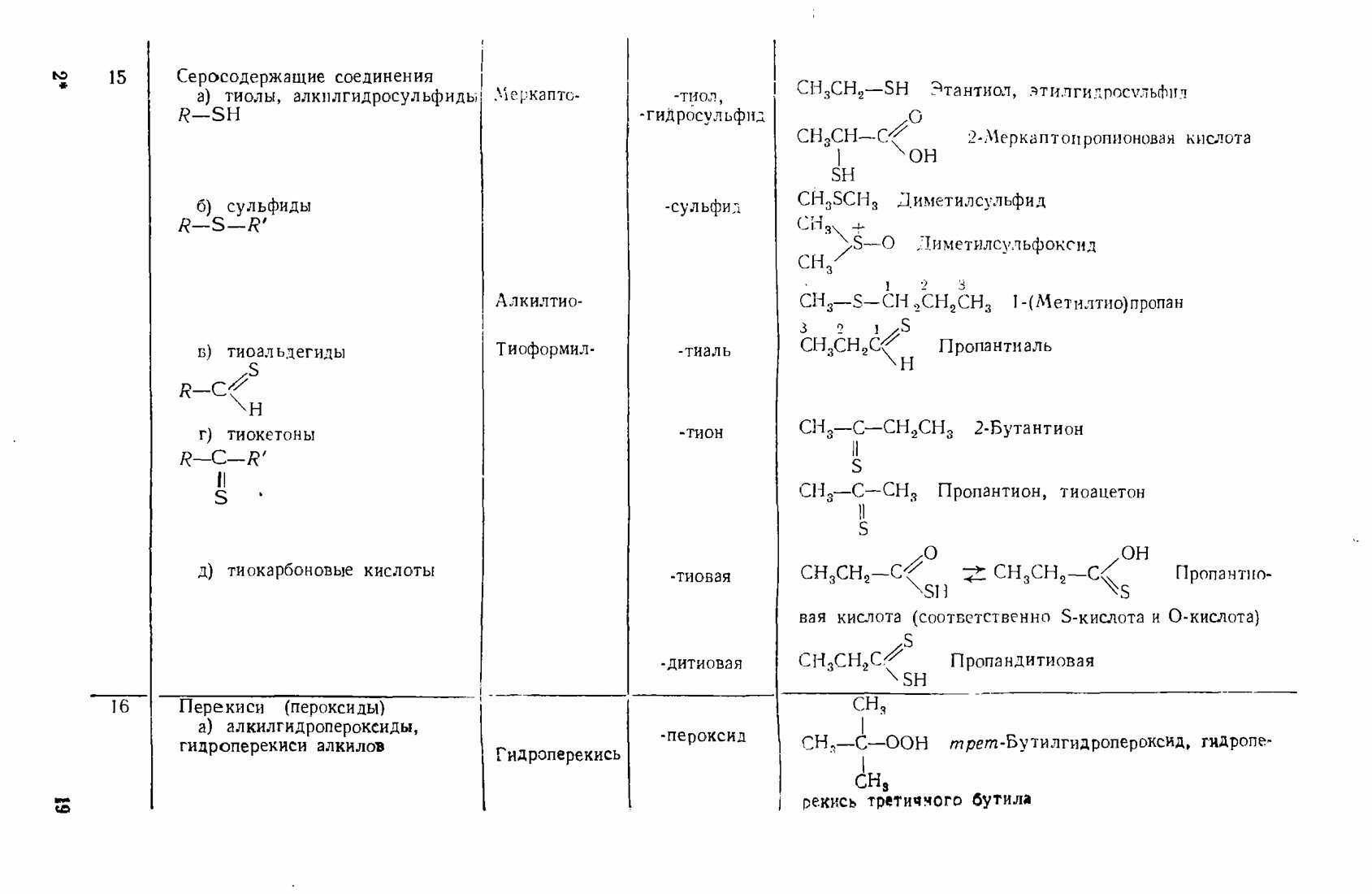
- 1.3. Классификация и номенклатура органических соединений
- 2 Общие теоретические положения органической химии
- 2.1. Природа химической связи
- 2.1.1. Типы химических связей
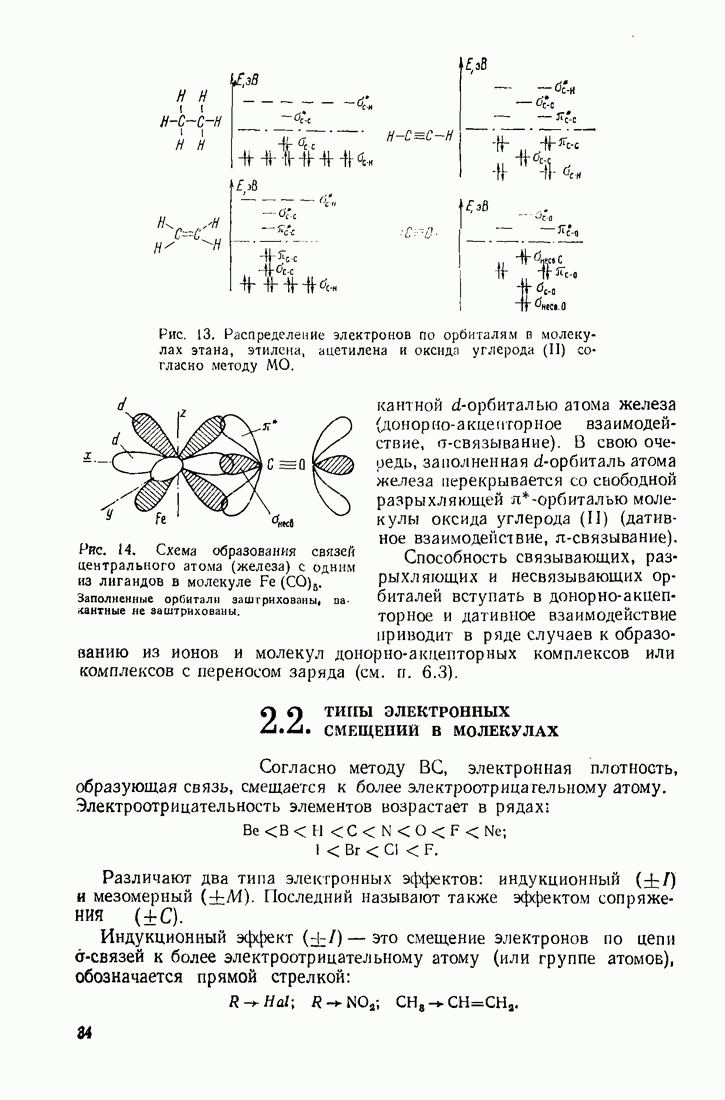
- 2.1.2. Молекулярные орбитали
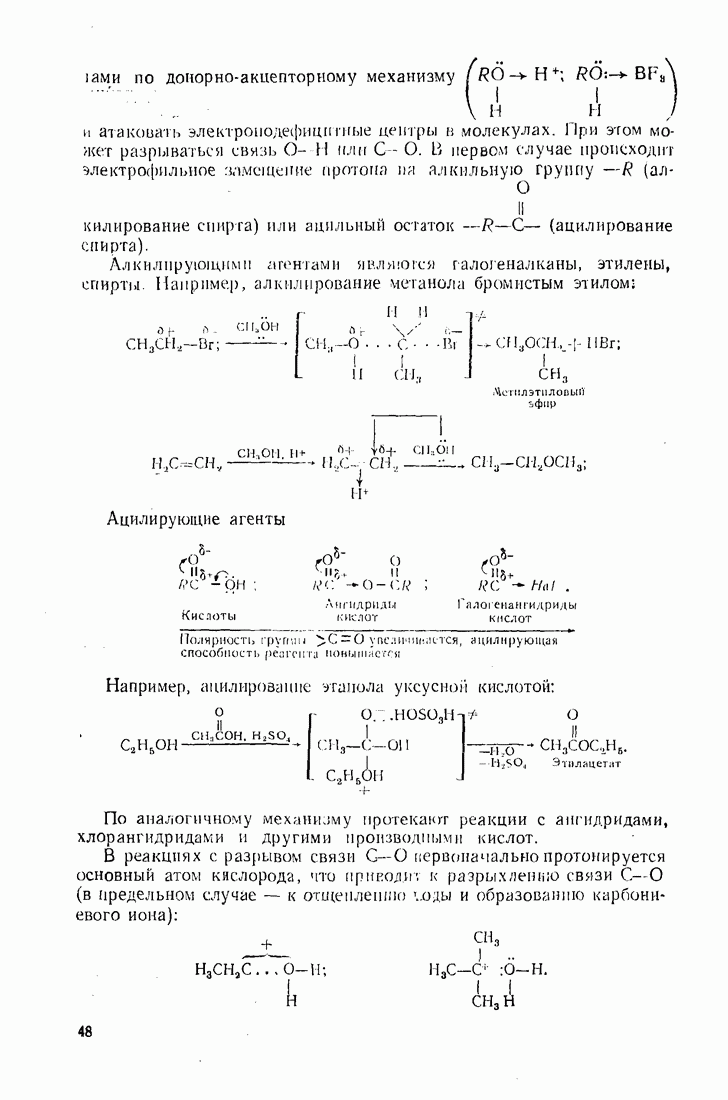
- 2.2. ТИПЫ ЭЛЕКТРОННЫХ СМЕЩЕНИЙ В МОЛЕКУЛАХ
- 2.3. ОБЩИЕ ПРЕДСТАВЛЕНИЯ ОБ ОРГАНИЧЕСКОЙ РЕАКЦИИ
- 2.4. КЛАССИФИКАЦИЯ РЕАГЕНТОВ И РЕАКЦИЙ
- 2.5. КРАТКАЯ ХАРАКТЕРИСТИКА РЕАКЦИОННОЙ СПОСОБНОСТИ НЕКОТОРЫХ СОЕДИНЕНИЙ АЛИФАТИЧЕСКОГО РЯДА
- 2.5.1. Алканы (парафины)
- 2.5.2. Непредельные углеводороды
- 2.5.3. Галогеналканы (галоидные алкилы R-Hal)
- 2.5.4. Спирты (R0Н)
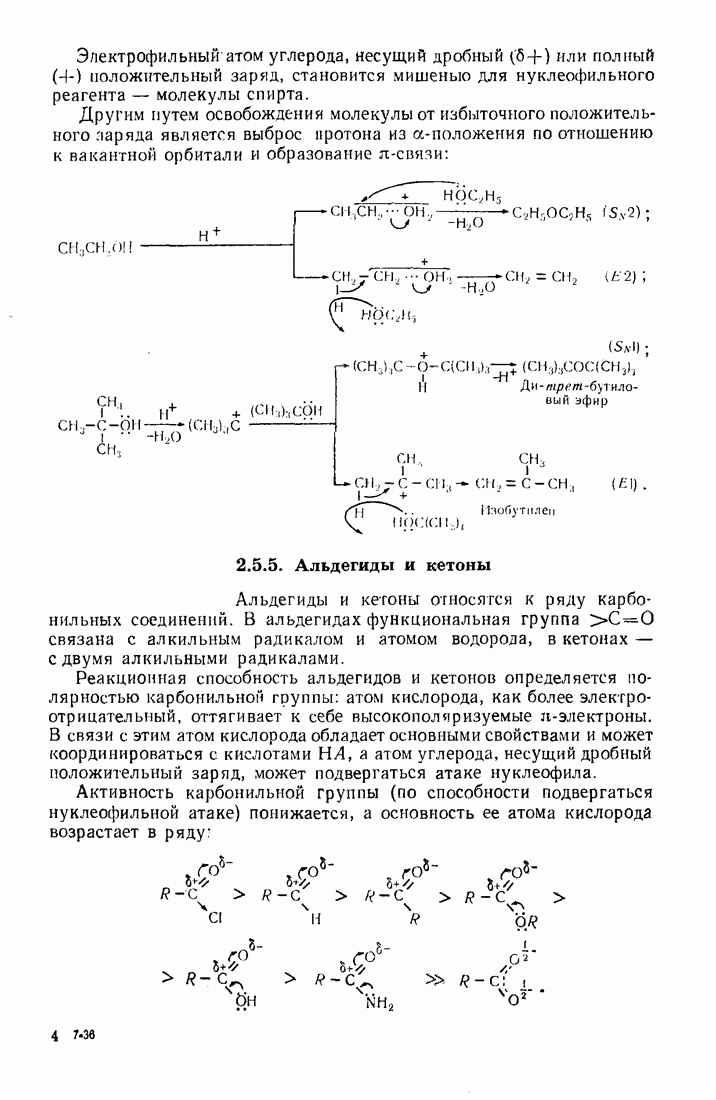
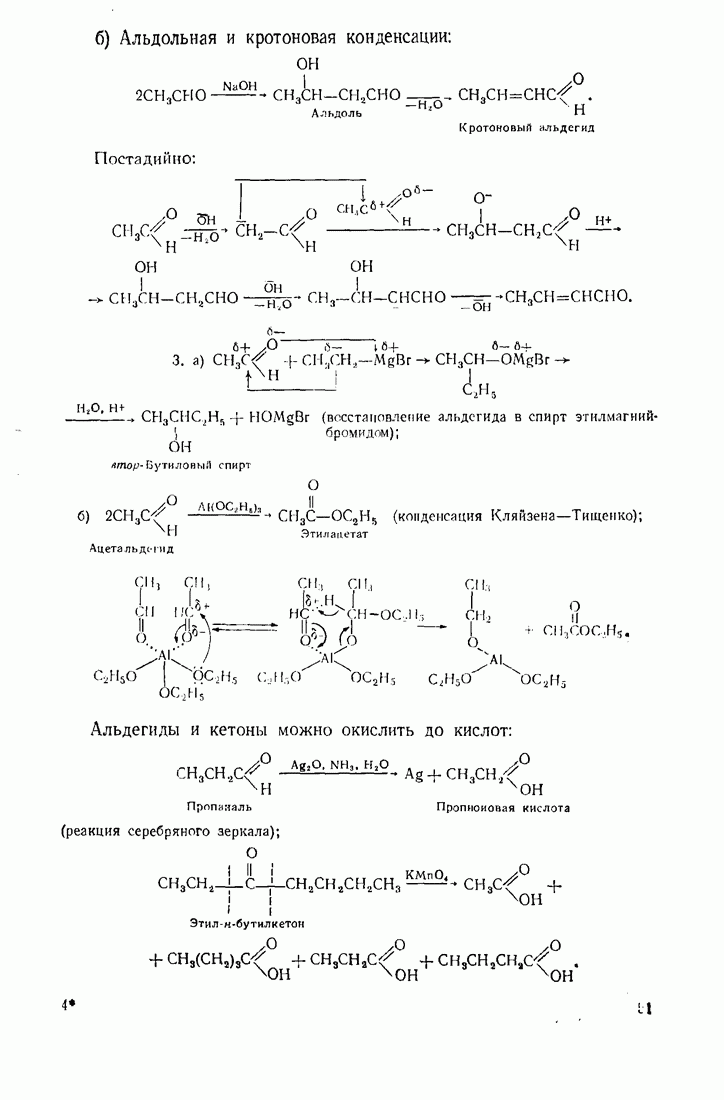
- 2.5.5. Альдегиды и кетоны
- 2.5.6. Карбоновые кислоты (R-СООН) и их производные (R-СО-X)
- 2.5.7. Амины (NH2R, NHR2, NR3)
- 3. Реакционная способность соединений алифатического ряда
- 3.1. Алканы (насыщенные углеводороды)
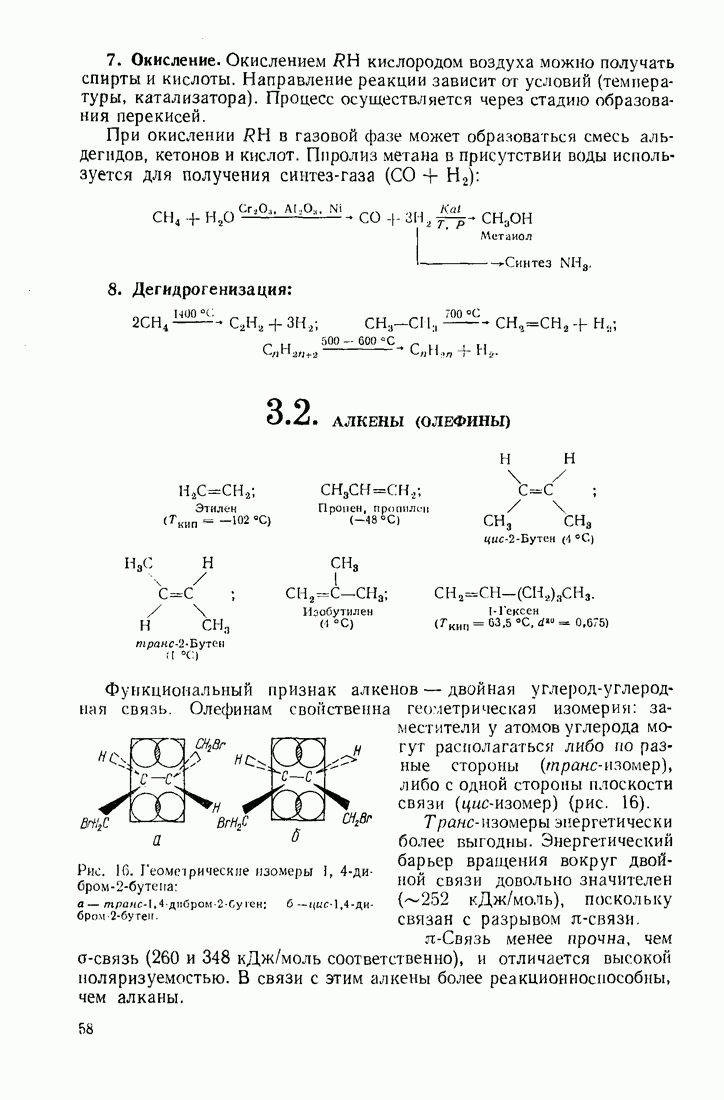
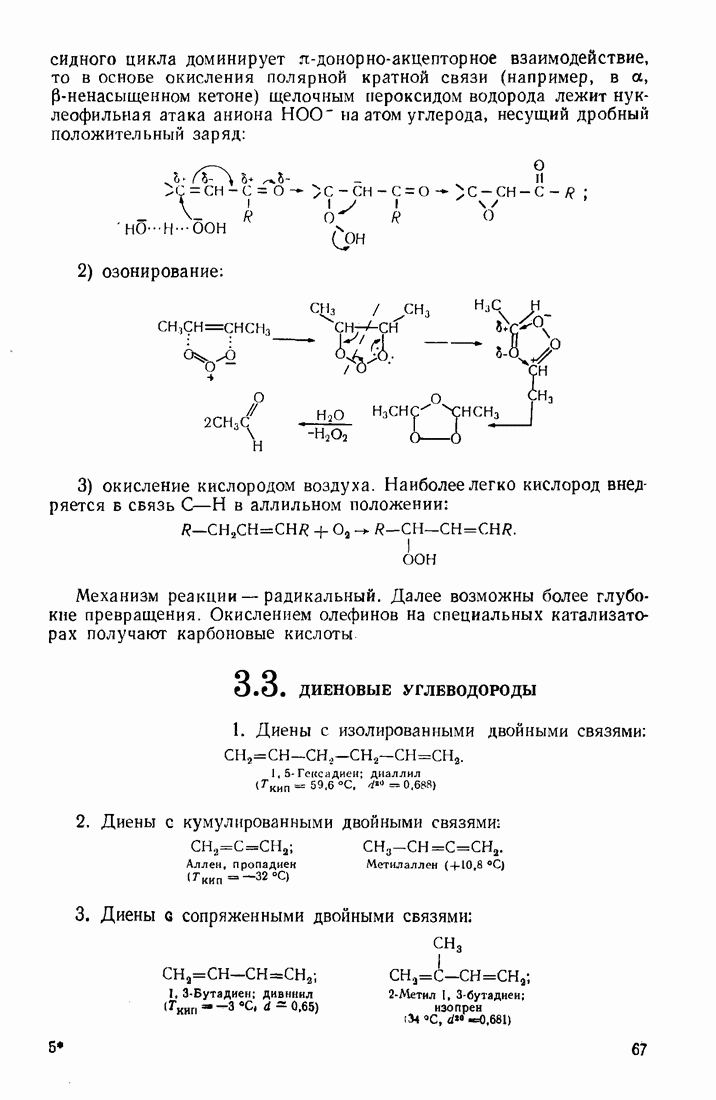
- 3.2. АЛКЕНЫ (ОЛЕФИНЫ)
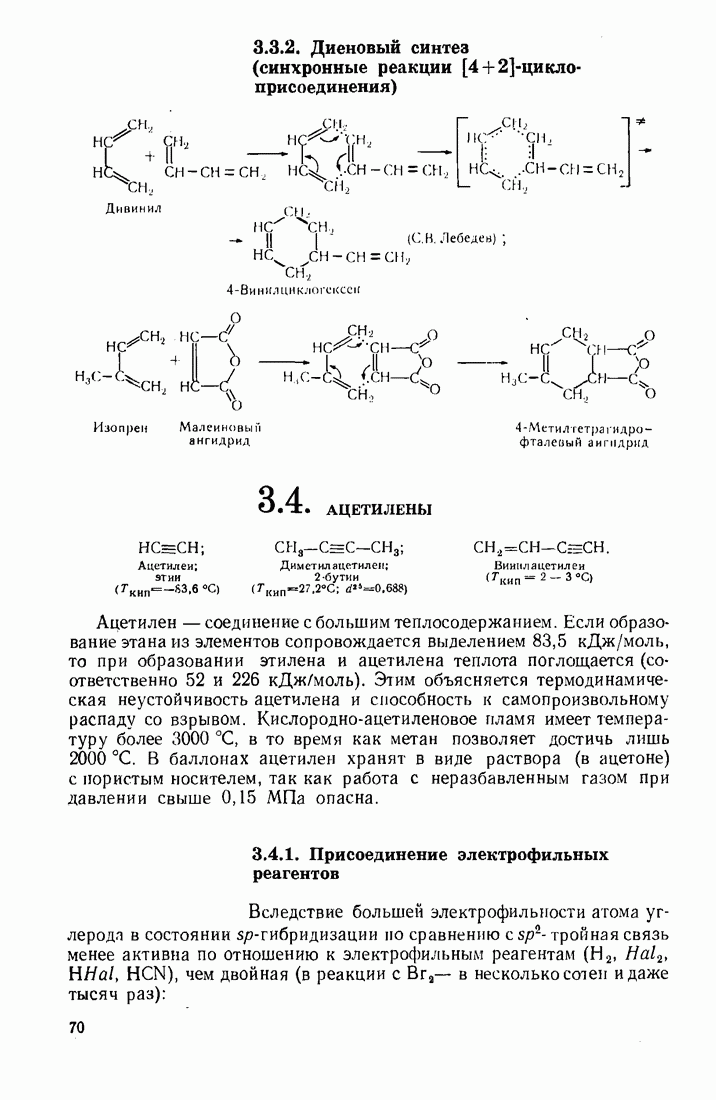
- 3.3. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ
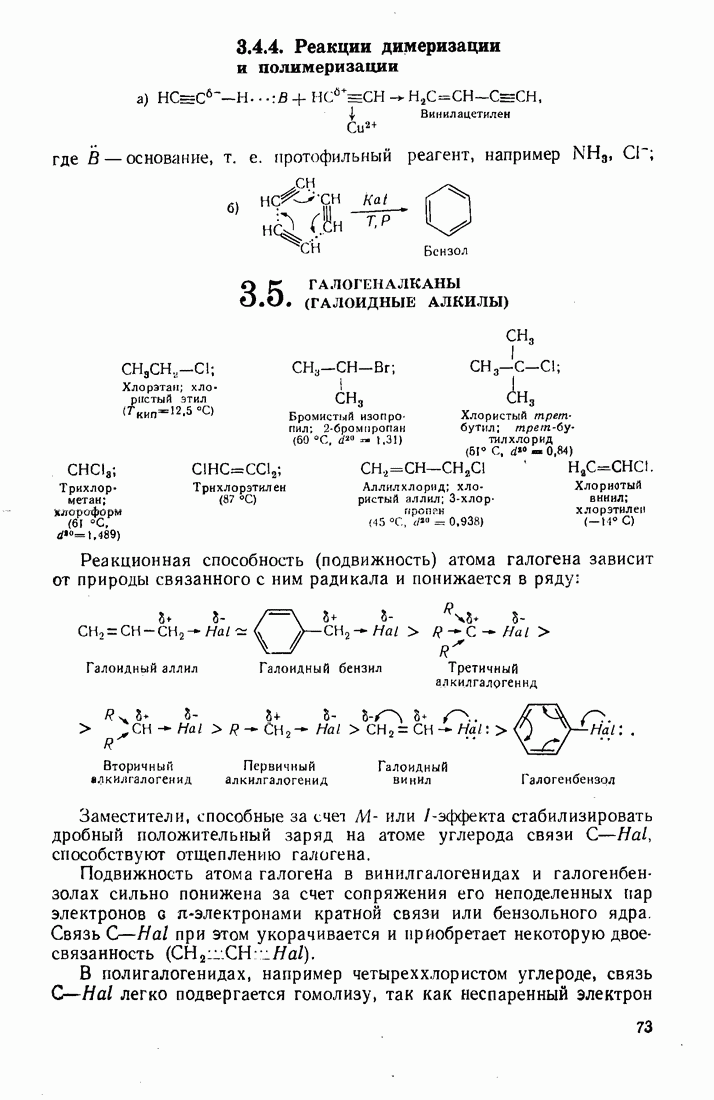
- 3.4. АЦЕТИЛЕНЫ
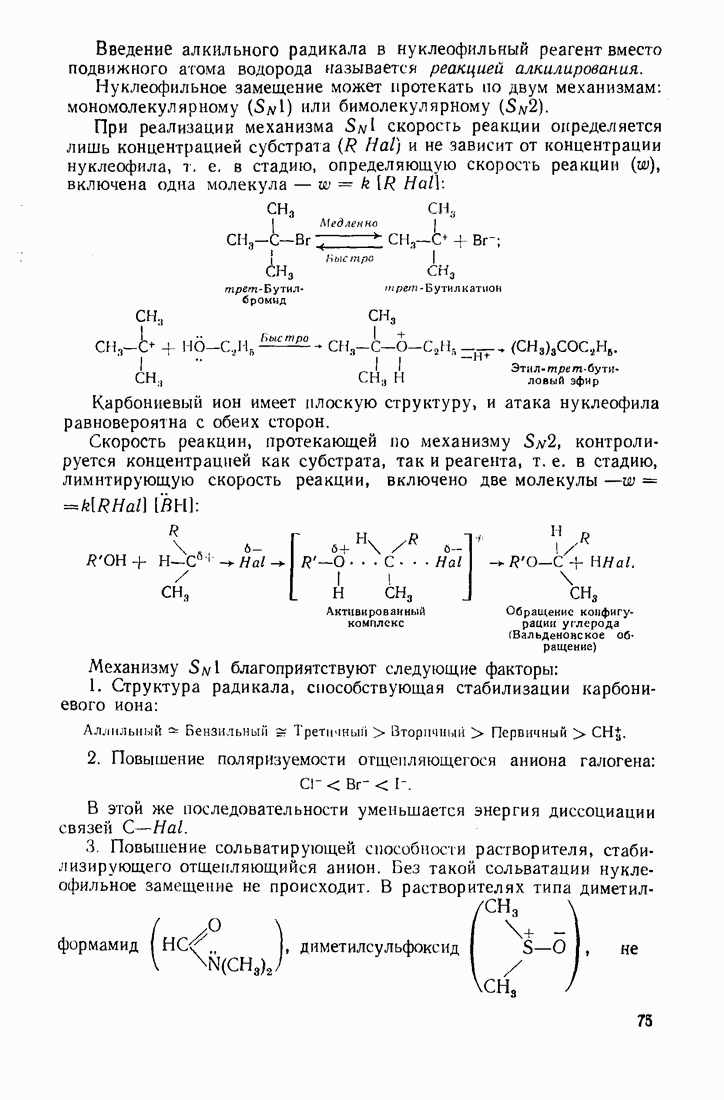
- 3.5. ГАЛОГЕНАЛКАНЫ (ГАЛОИДНЫЕ АЛКИЛЫ)
- 3.6. СПИРТЫ
- 3.7. ПРОСТЫЕ ЭФИРЫ (R-O-R)
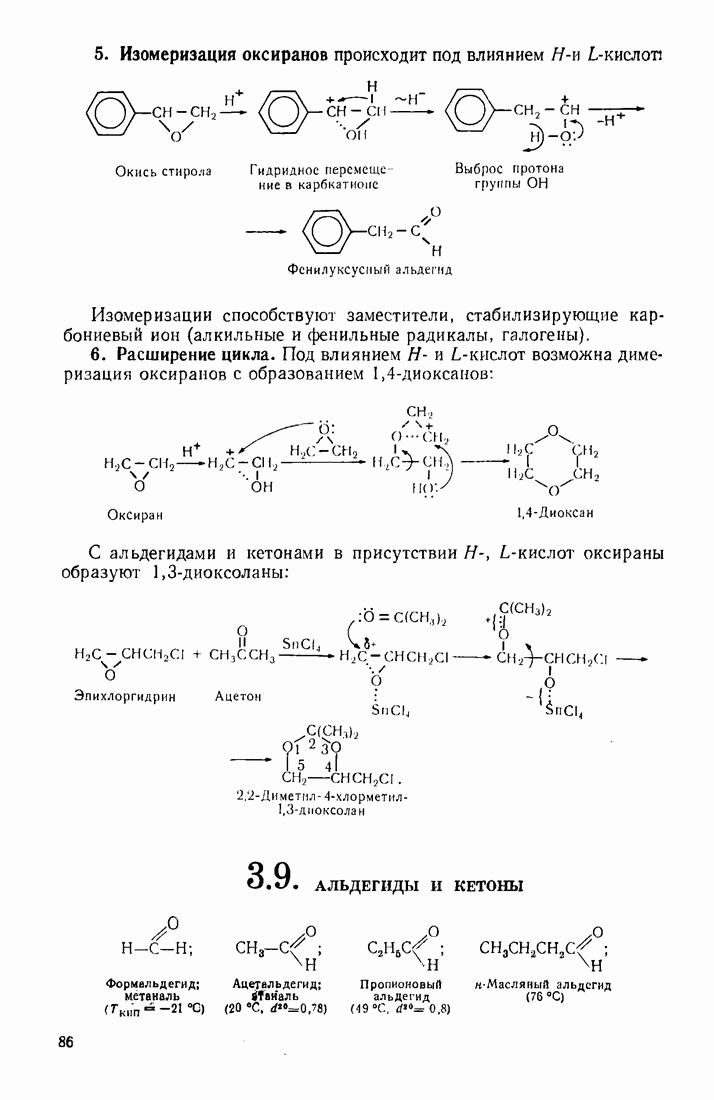
- 3.8. ОКСИРАНЫ (ЭПОКСИДНЫЕ СОЕДИНЕНИЯ, a-ОКИСИ)
- 3.9. АЛЬДЕГИДЫ И КЕТОНЫ
- 3.10. КАРБОНОВЫЕ КИСЛОТЫ
- 3.11. НЕКОТОРЫЕ ПРОИЗВОДНЫЕ КИСЛОТ
- 3.12. АМИНЫ
- 3.13. ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.14. СЕРООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.15. ОРГАНИЧЕСКИЕ ПЕРЕКИСИ (ПЕРОКСИДНЫЕ СОЕДИНЕНИЯ)
- 3.16. ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- 3.17. ГЕТЕРОАНАЛОГИ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- 3.18. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
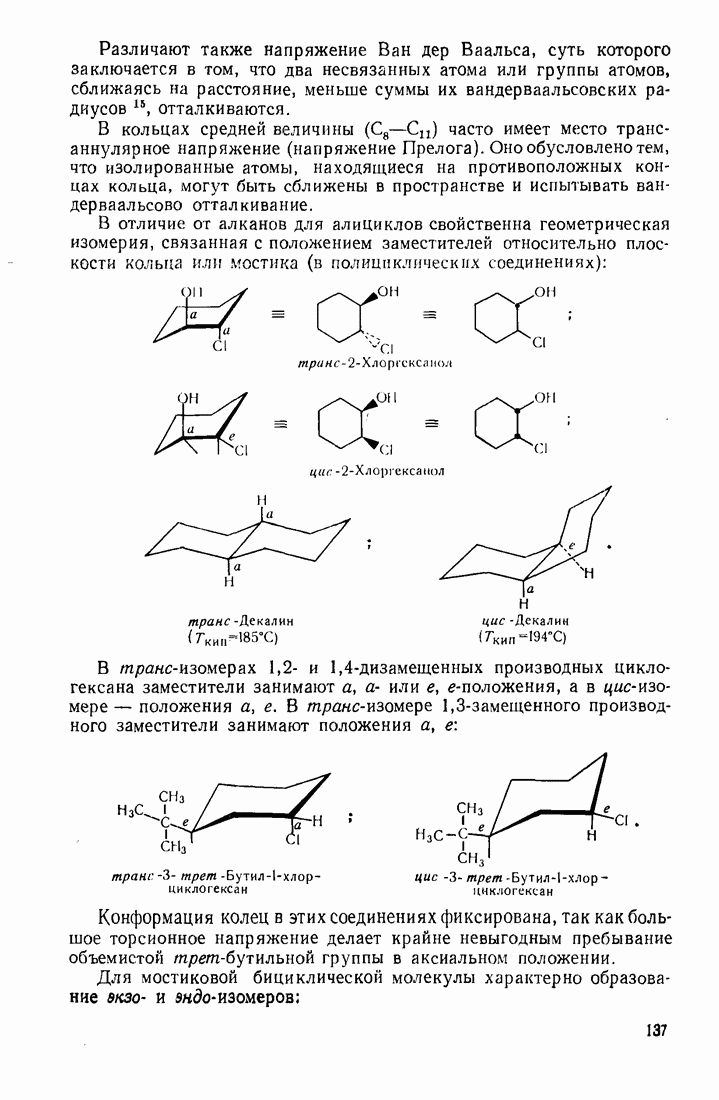
- 3.18.2. Пространственное расположение и напряженность циклов
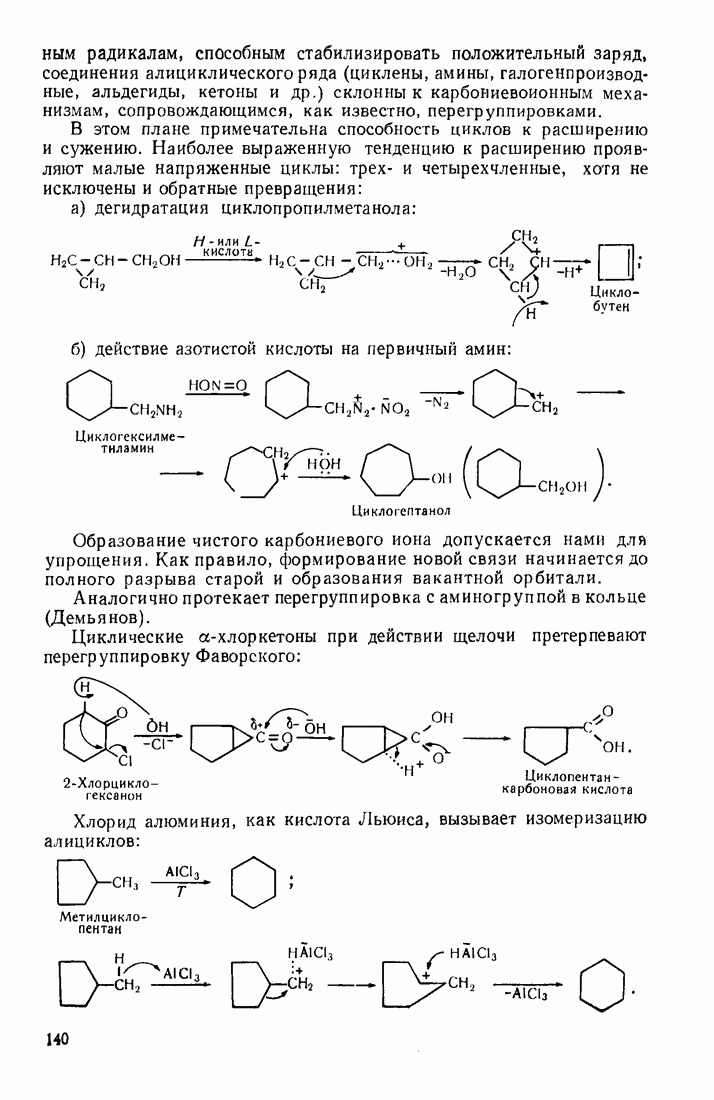
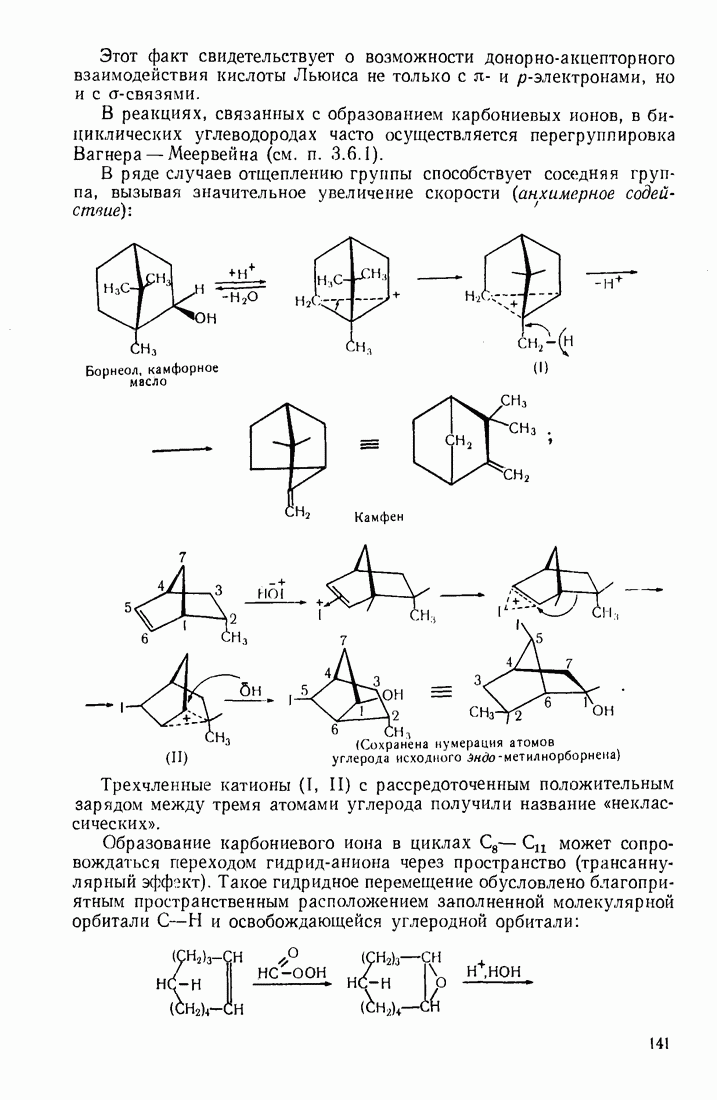
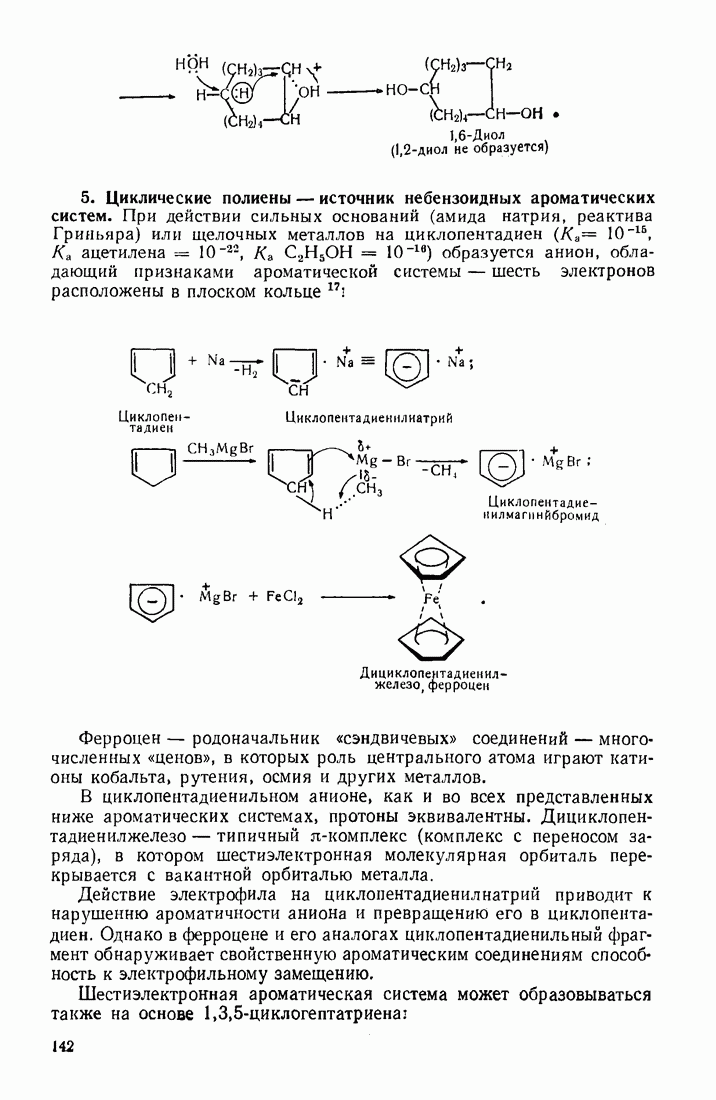
- 3.18.3. Особенности химических свойств алициклических соединений
- 4. Полифункциональные производные алифатического ряда
- 4.1. ДВУХОСНОВНЫЕ КАРБОНОВЫЕ КИСЛОТЫ
- 4.2. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
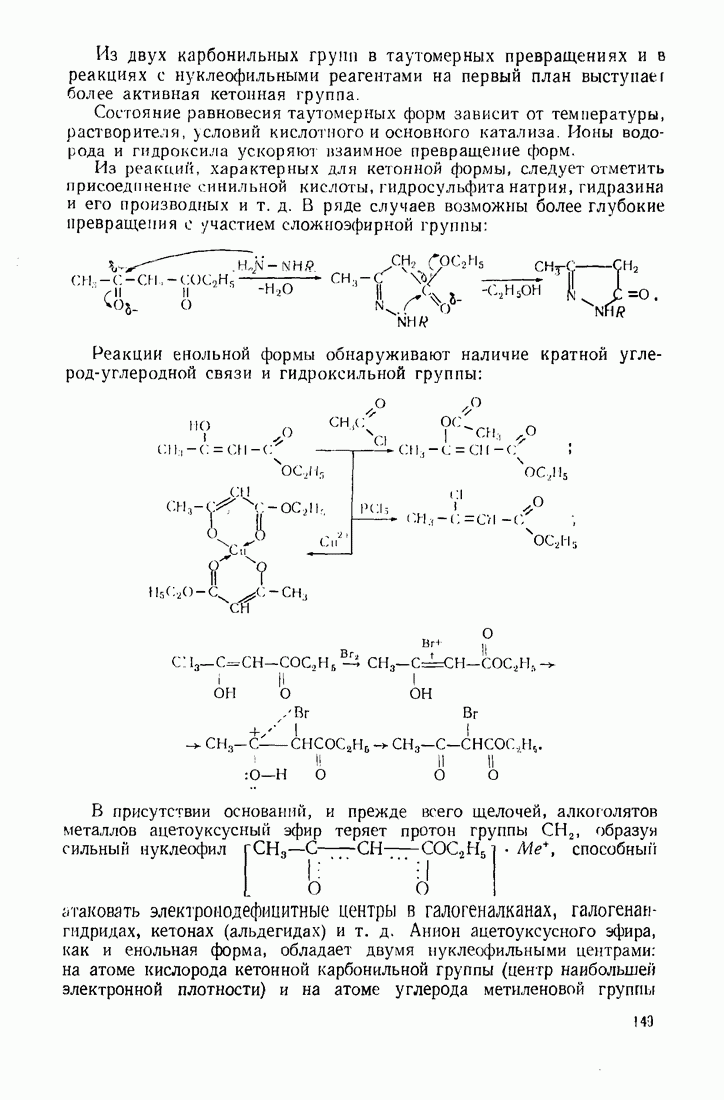
- 4.3. ОКСОКИСЛОТЫ (АЛЬДЕГИДО- И КЕТОКИСЛОТЫ)
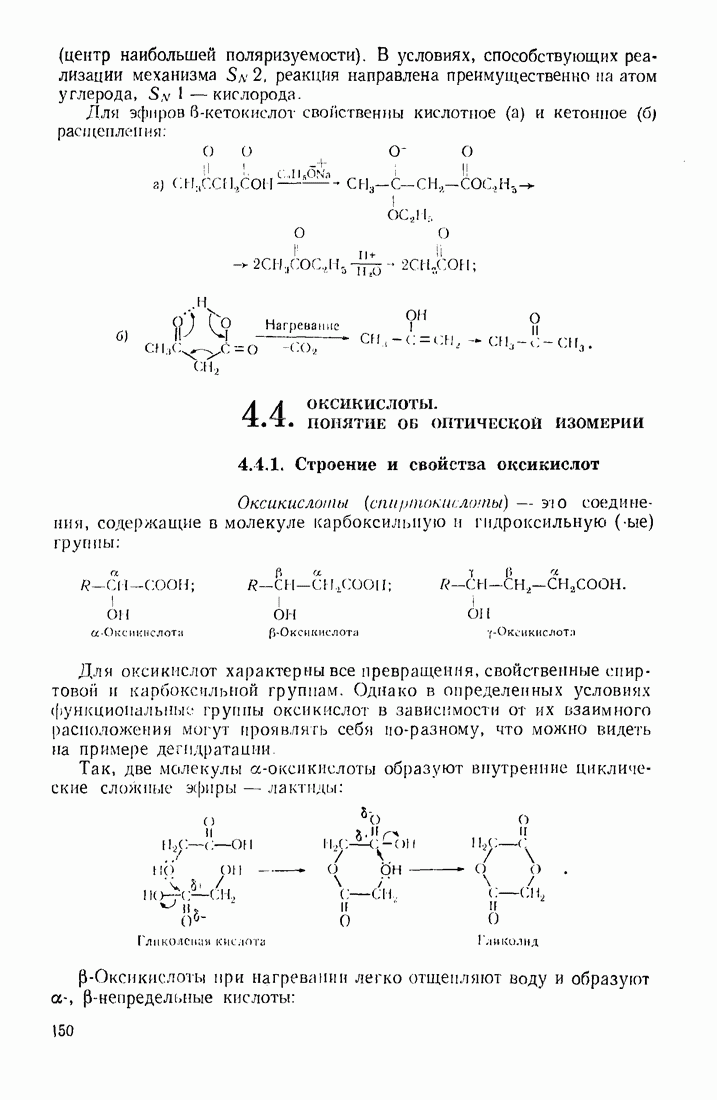
- 4.4. ОКСИКИСЛОТЫ. ПОНЯТИЕ ОБ ОПТИЧЕСКОЙ ИЗОМЕРИИ
- 4.5. УГЛЕВОДЫ
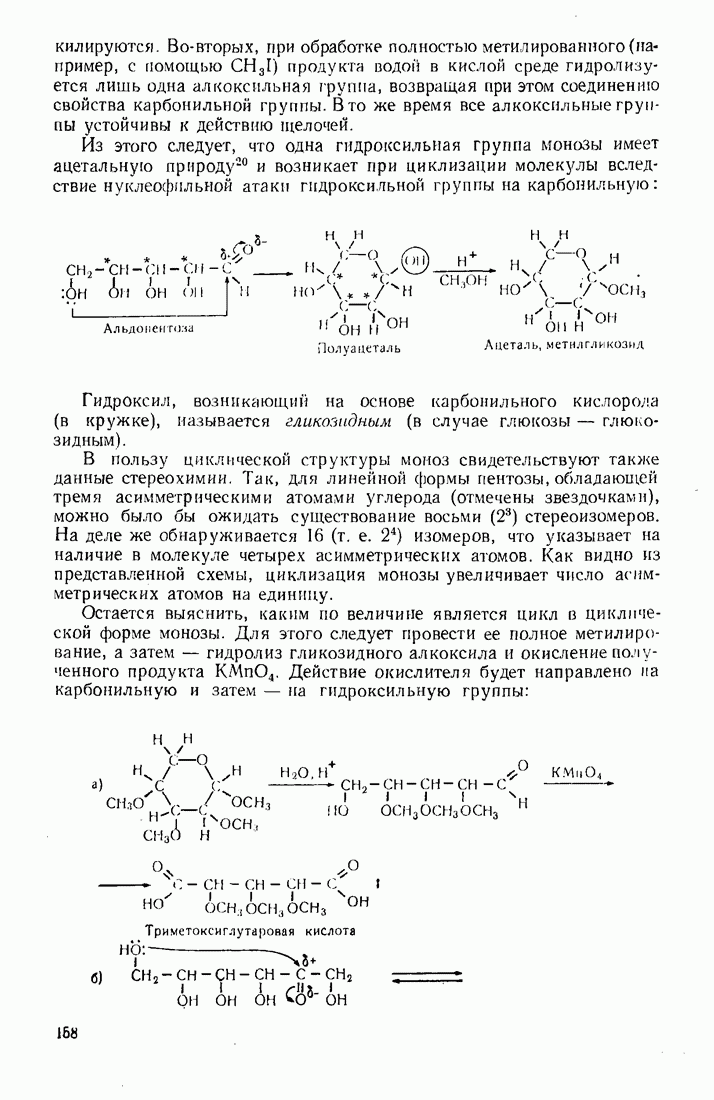
- 4.5.2. Стереохимия моносахаридов
- 4.5.3. Дисахариды
- 4.5.4. Полисахариды
- 4.5.5. Нахождение в природе и пути превращения углеводов
- 4.6. АМИНОКИСЛОТЫ
- 5. Методы синтеза органических юединений алифатическою рада
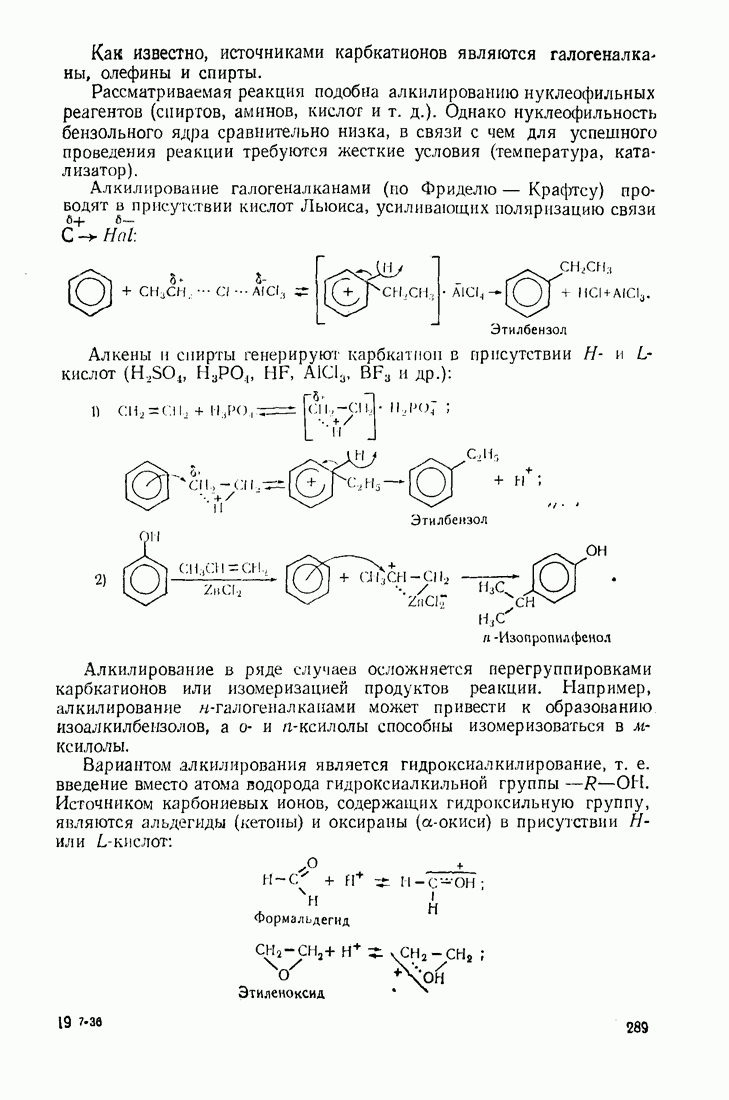
- 5.1. АЛКИЛИРОВАНИЕ
- 5.2. АЦИЛИРОВАНИЕ
- 5.3. ГАЛОГЕНИРОВАНИЕ
- 5.4. ГИДРОКСИЛИРОВАНИЕ
- 5.5. КАРБОНИЛИРОВАНИЕ (ВВЕДЕНИЕ КАРБОНИЛЬНОЙ ГРУППЫ)
- 5.6. КАРБОКСИЛИРОВАНИЕ
- 5.7. ЭПОКСИДИРОВАНИЕ (ОКСИРАНИРОВАИИЕ)
- 5.8. АМИНИРОВАНИЕ
- 5.9. ОКИСЛЕНИЕ
- 5.10. ВОССТАНОВЛЕНИЕ
- 5.11. АЛКАНЫ
- 5.12 АЛКЕНЫ
- 5.13. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ (1,3-ДИЕНЫ)
- 5.14. АЦЕТИЛЕНЫ
- 5.15 АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 5.16. ГАЛОГЕН АЛКАНЫ
- 5.17. СПИРТЫ
- 5.18. АЛЬДЕГИДЫ И КЕТОНЫ
- 5.19. КАРБОНОВЫЕ КИСЛОТЫ
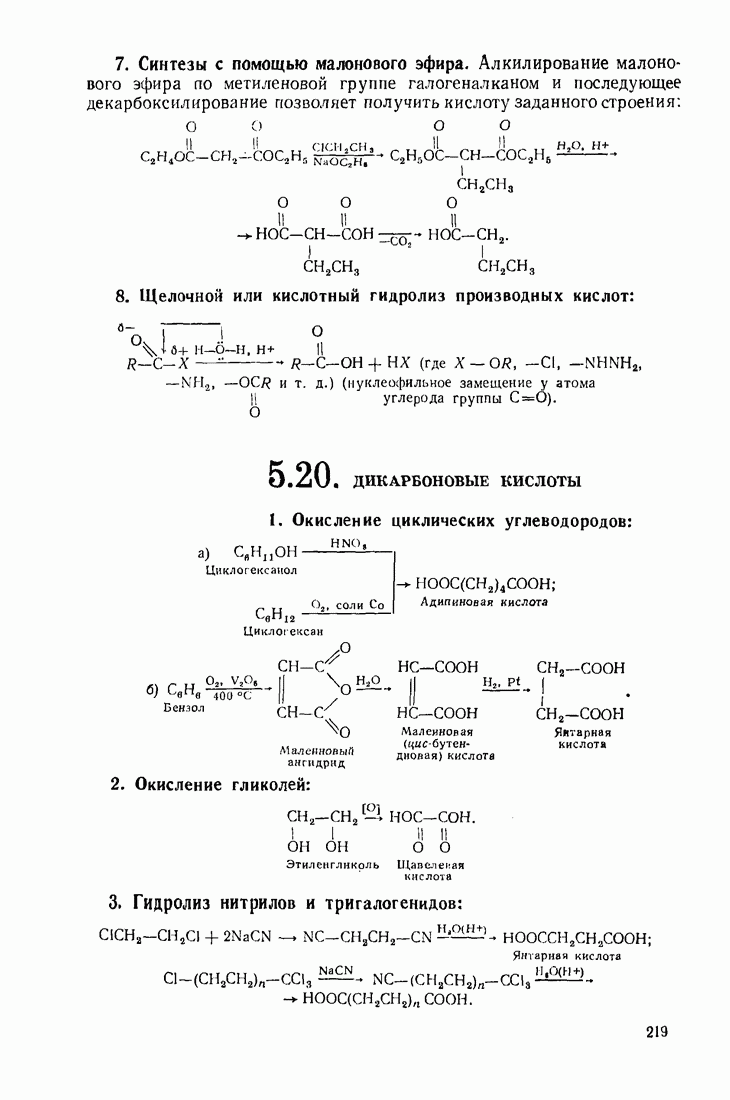
- 5.20. ДИКАРБОНОВЫЕ КИСЛОТЫ
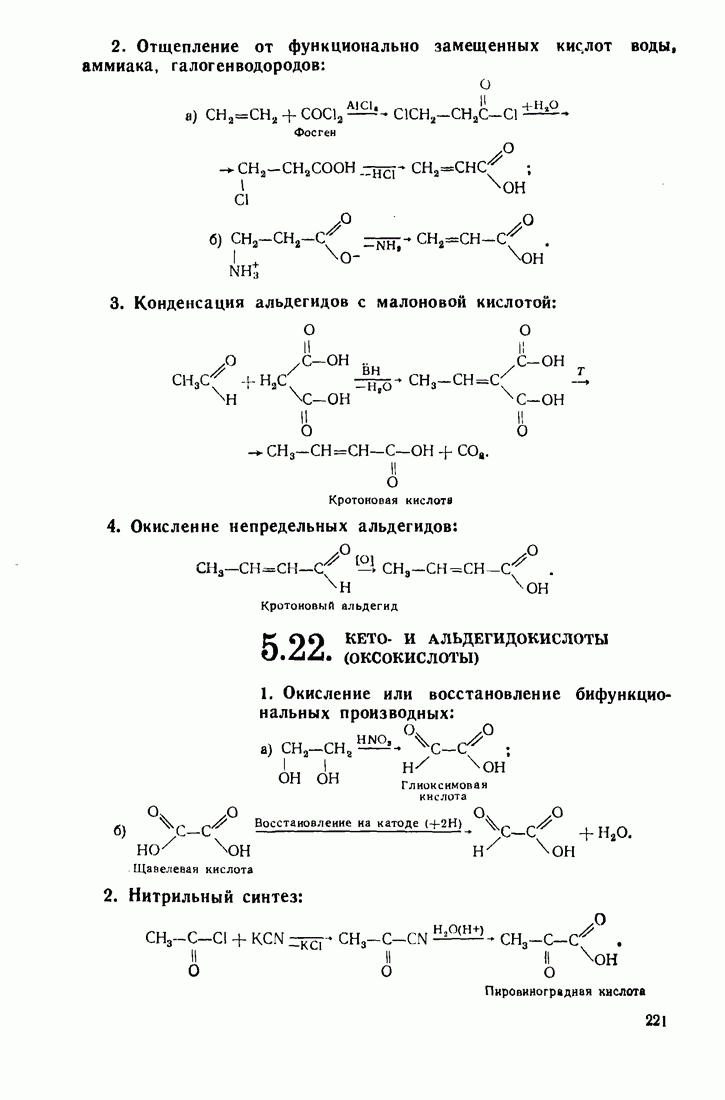
- 5.21. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 5.22. КЕТО- И АЛЬДЕГИДОКИСЛОТЫ (ОКСОКИСЛОТЫ)
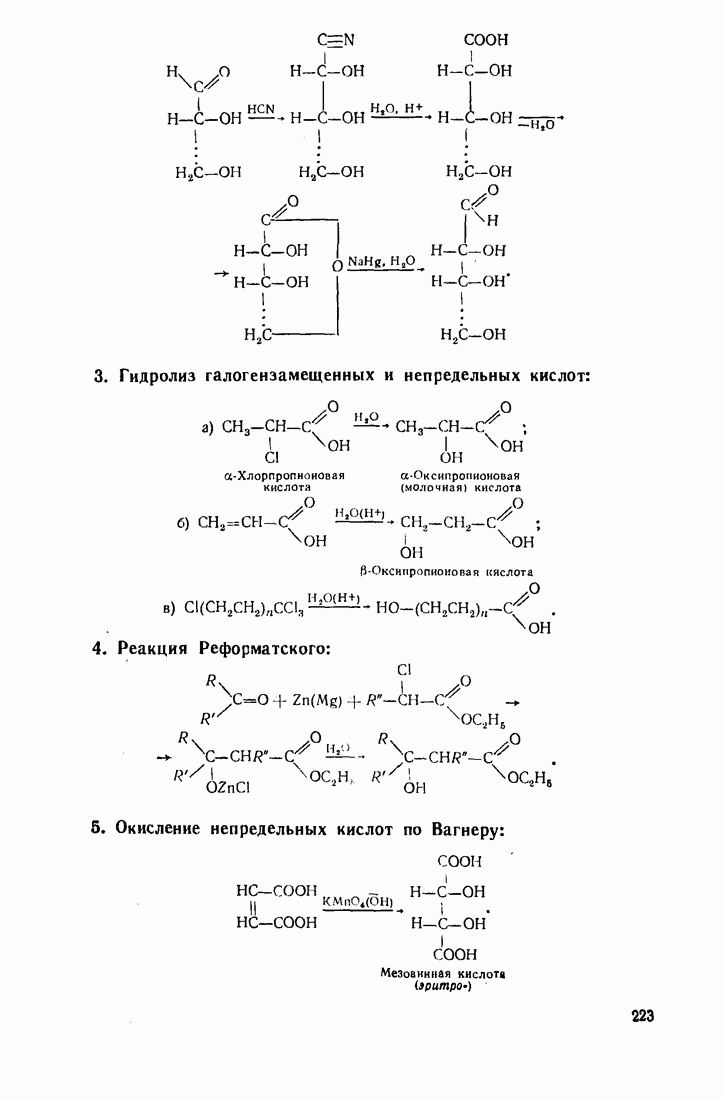
- 5.23. ОКСИКИСЛОТЫ
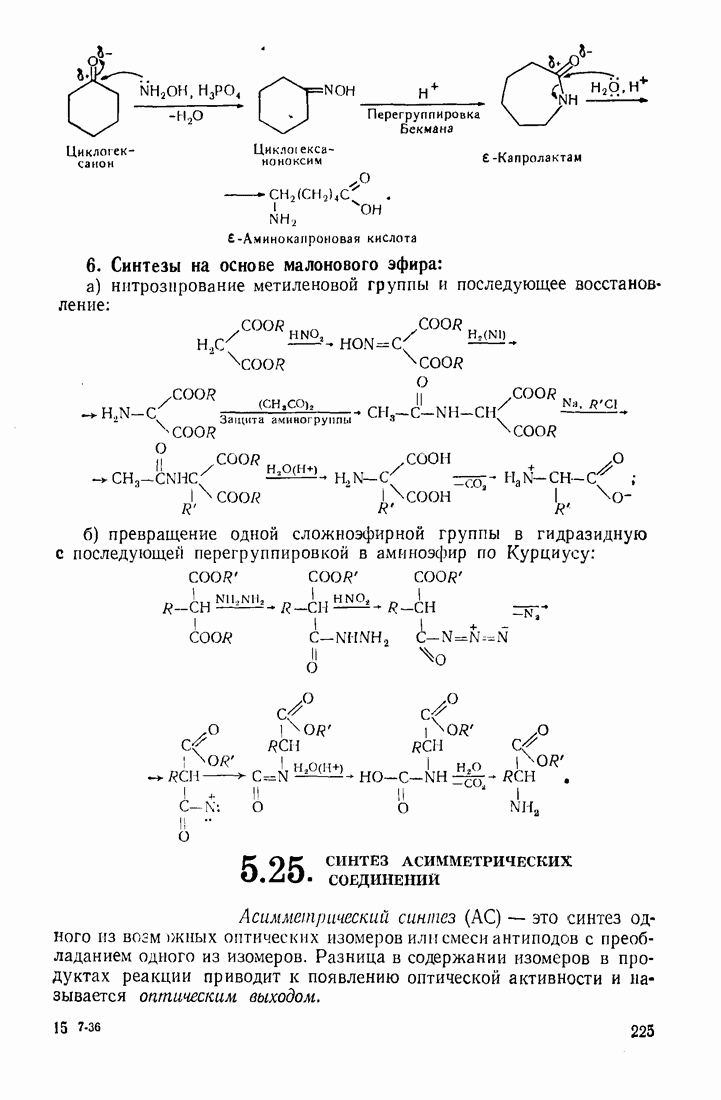
- 5.24. АМИНОКИСЛОТЫ
- 5.25 СИНТЕЗ АСИММЕТРИЧЕСКИХ СОЕДИНЕНИЙ
- 6. Некоторые понятия физической органической химии
- 6.1. СВЯЗЬ СОСТАВА И СТРОЕНИЯ СОЕДИНЕНИЙ С ФИЗИЧЕСКИМИ СВОЙСТВАМИ
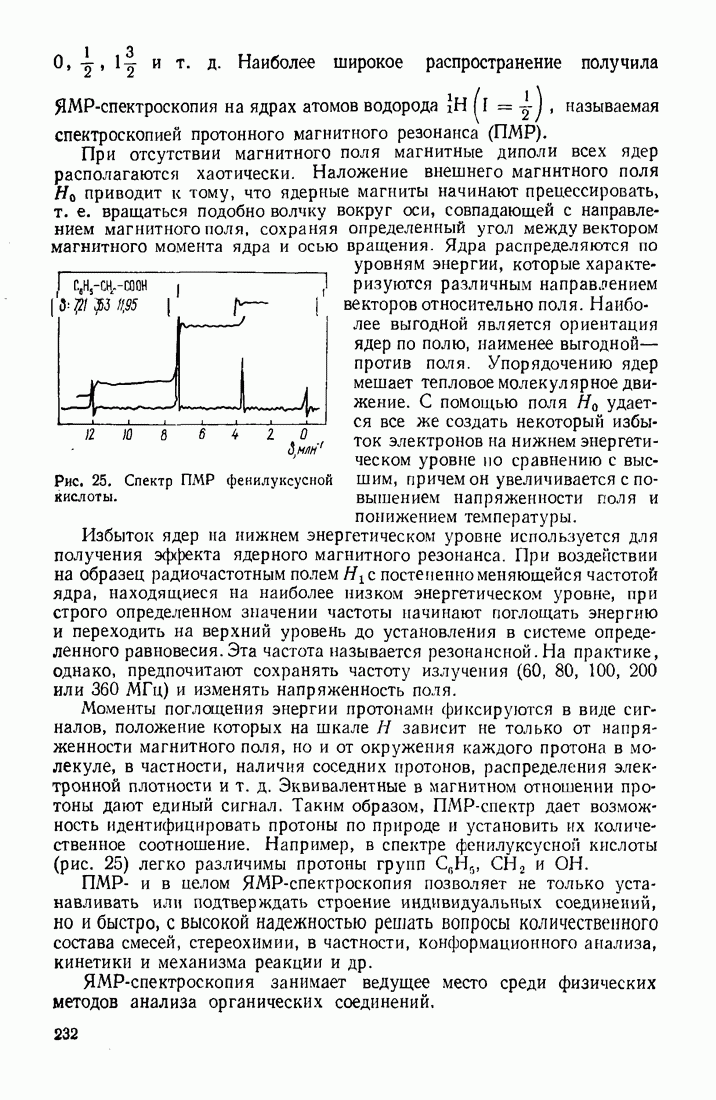
- 6.2. ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 6.3. КИСЛОТЫ И ОСНОВАНИЯ В ОРГАНИЧЕСКОЙ ХИМИИ
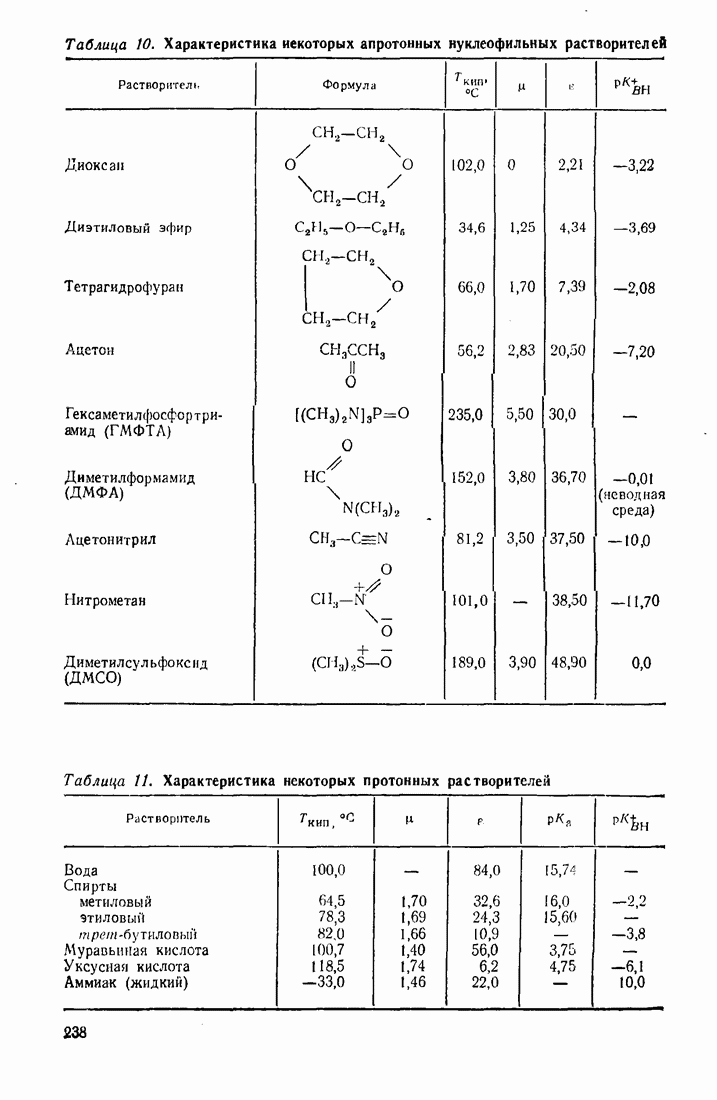
- 6.4. ОРГАНИЧЕСКИЕ РАСТВОРИТЕЛИ И ИХ ВЛИЯНИЕ НА СКОРОСТЬ И МЕХАНИЗМ РЕАКЦИЙ
- 6.5. КАТАЛИЗ ОРГАНИЧЕСКИХ РЕАКЦИЙ
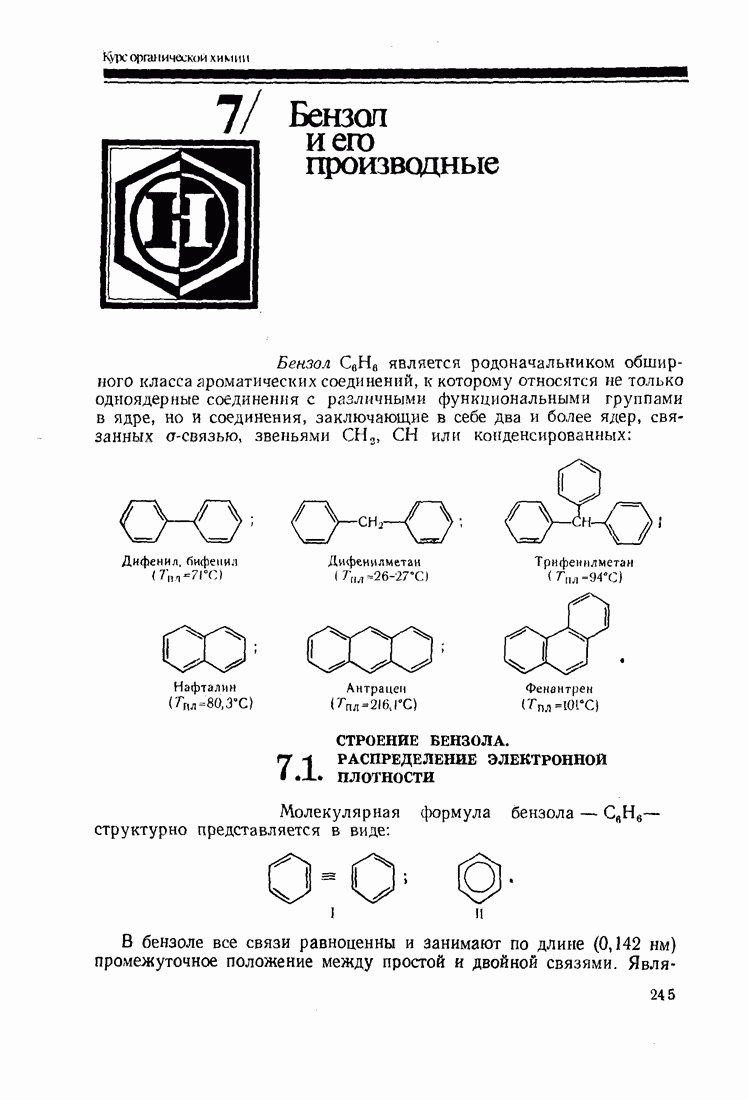
- 7. Бензол и его производные
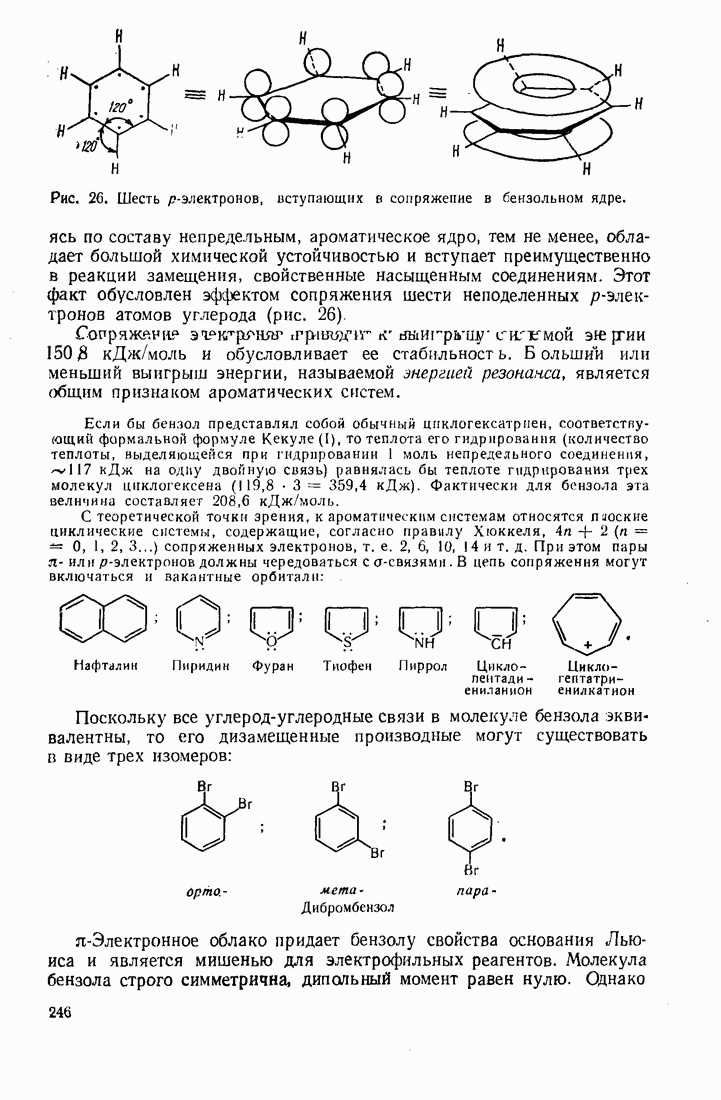
- 7.1. СТРОЕНИЕ БЕНЗОЛА. РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОННОЙ ПЛОТНОСТИ
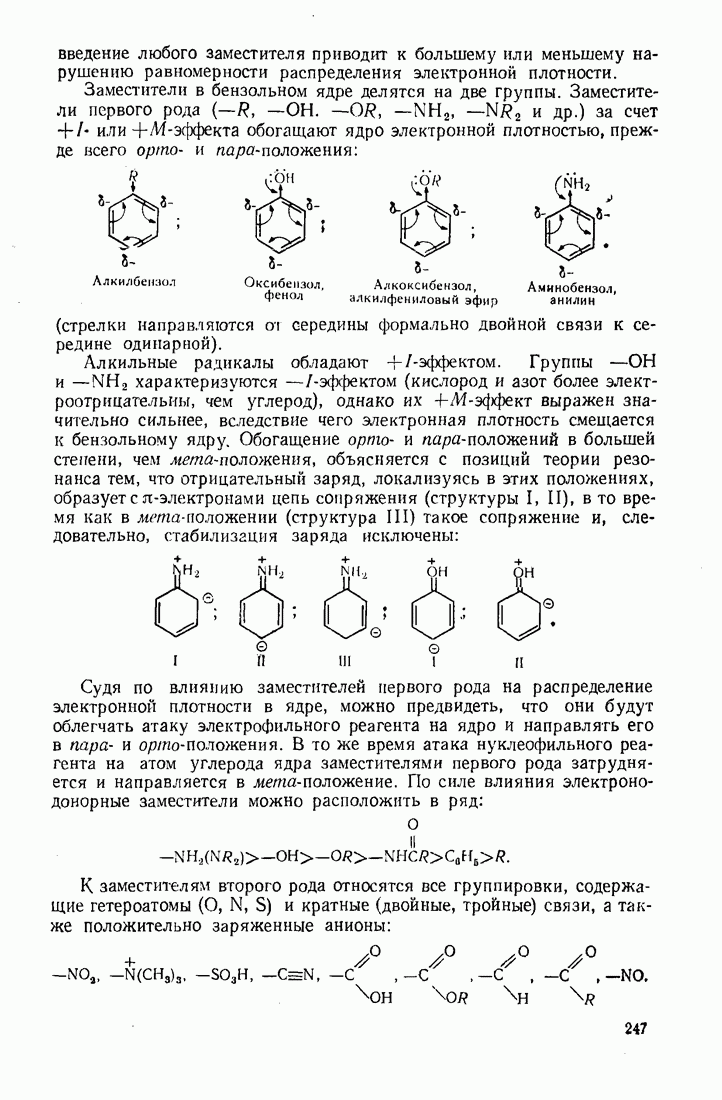
- 7.2. ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
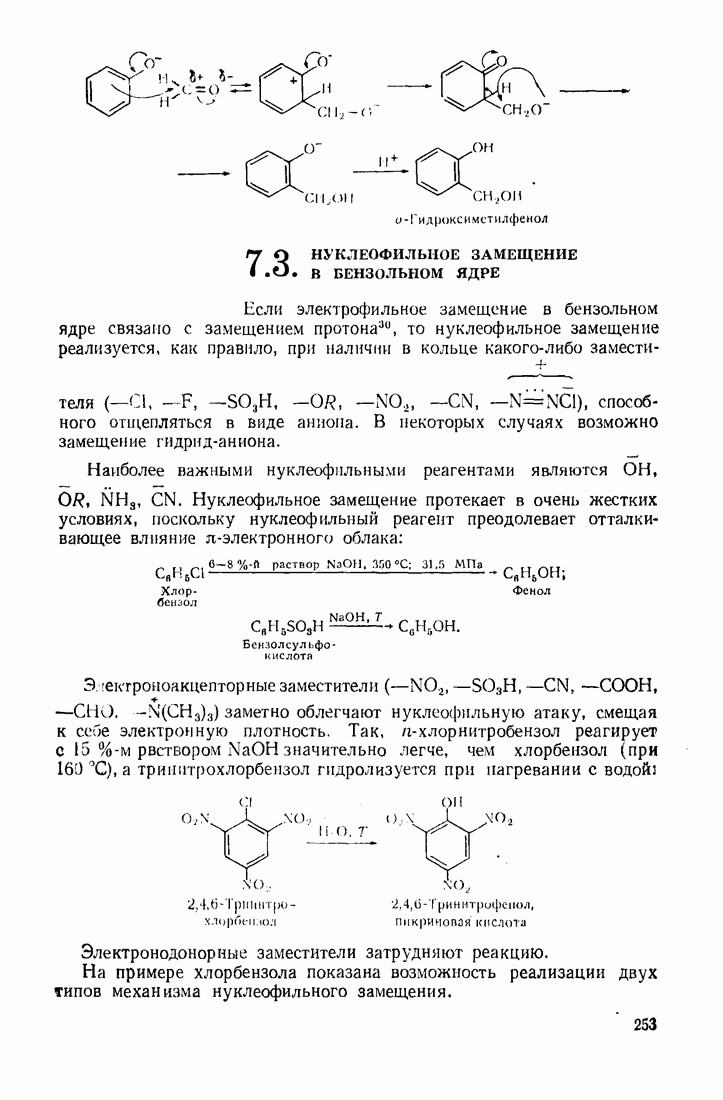
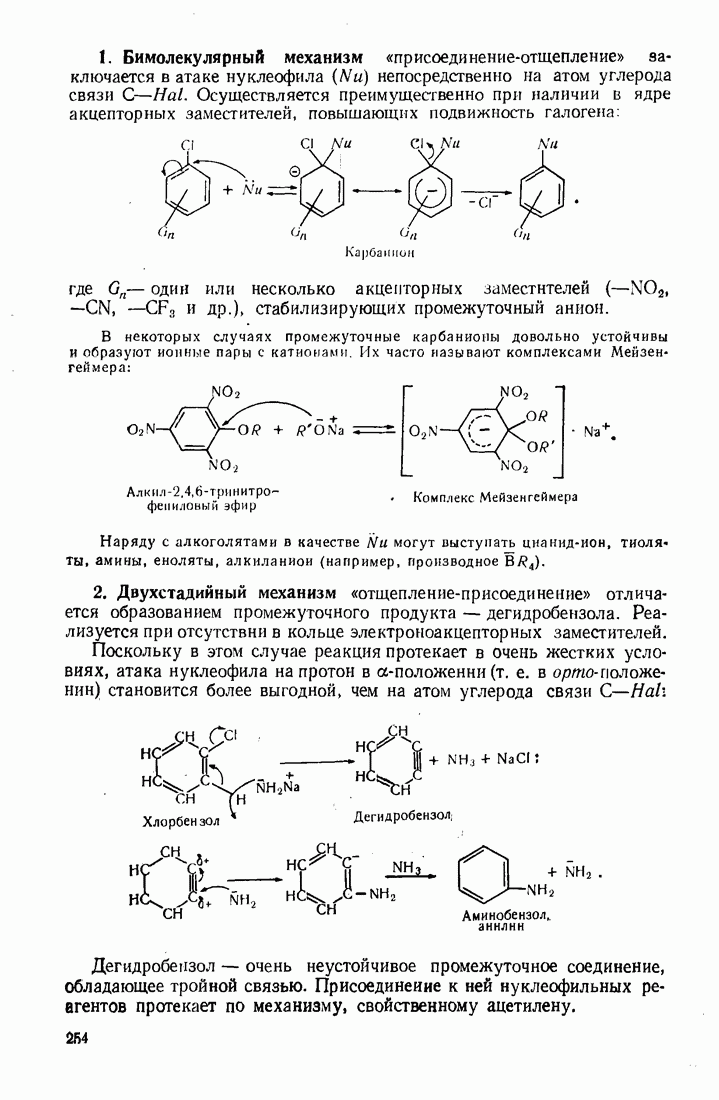
- 7.3. НУКЛЕОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
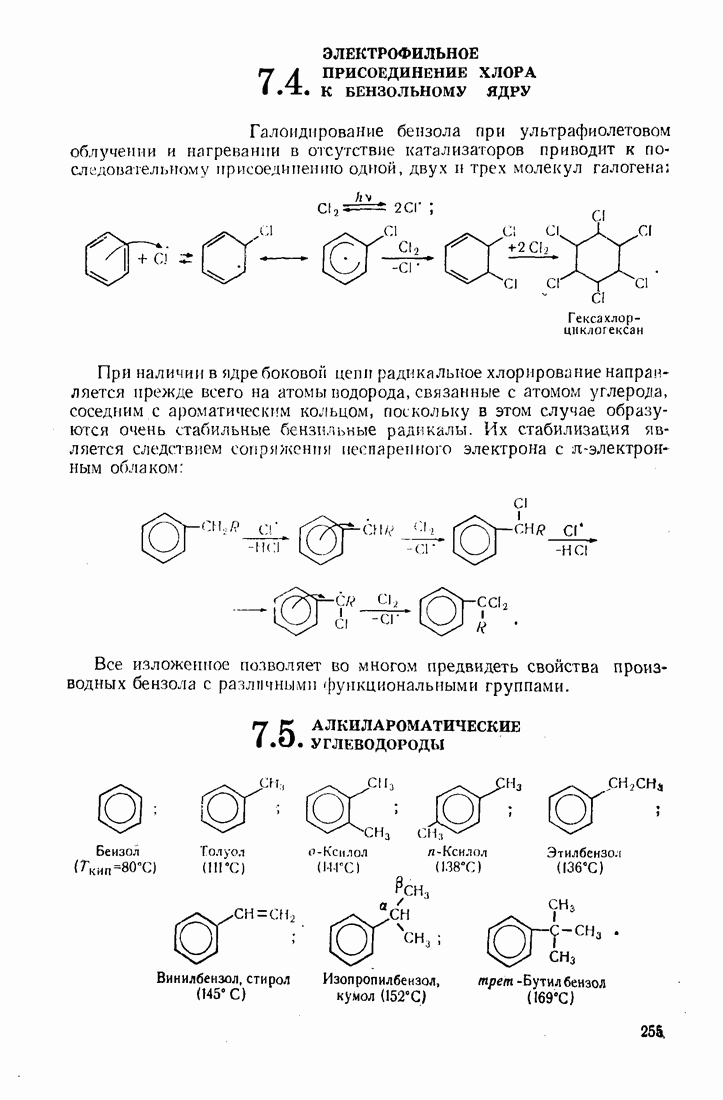
- 7.4. ЭЛЕКТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ ХЛОРА К БЕНЗОЛЬНОМУ ЯДРУ
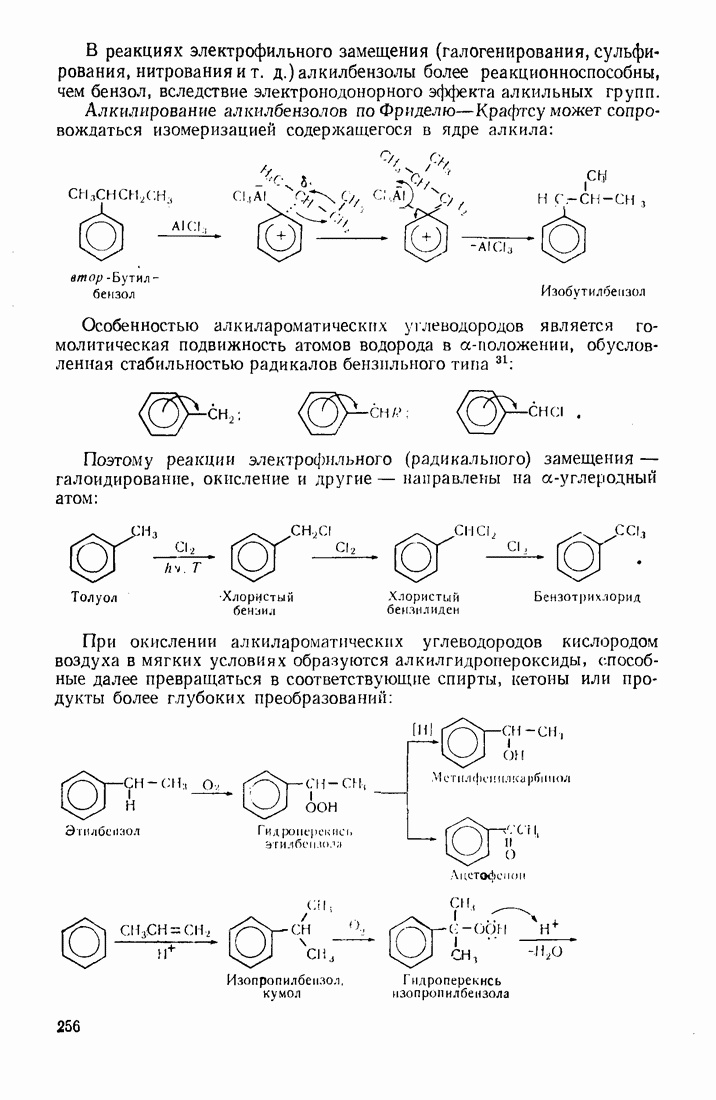
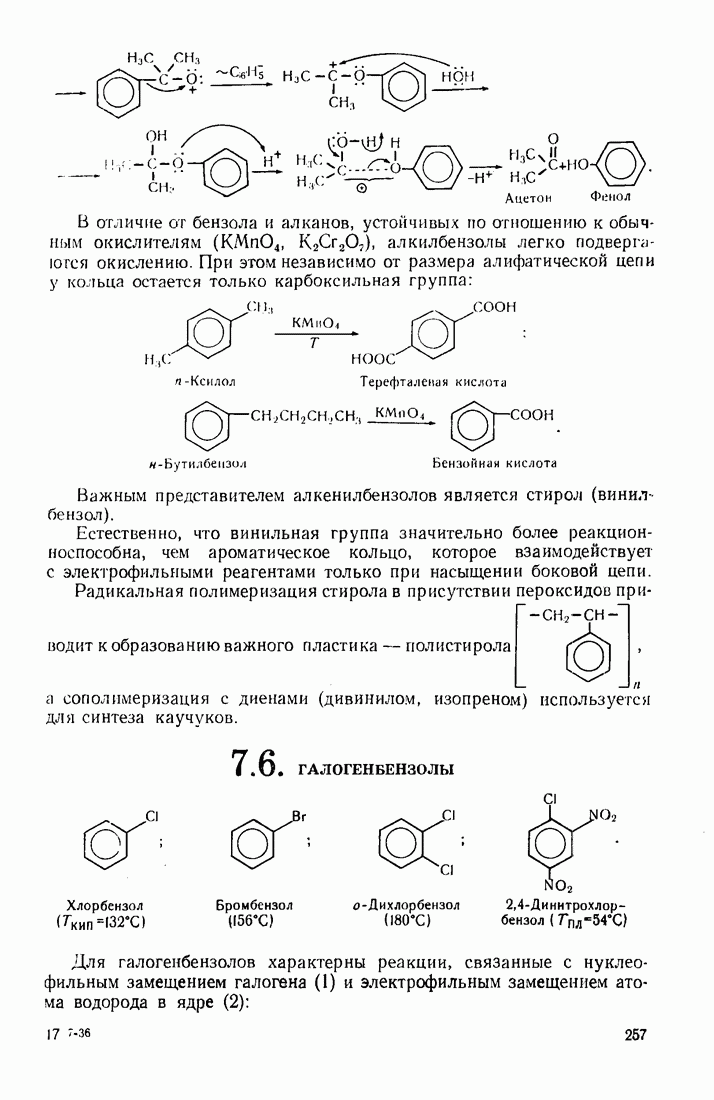
- 7.5. АЛКИЛАРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
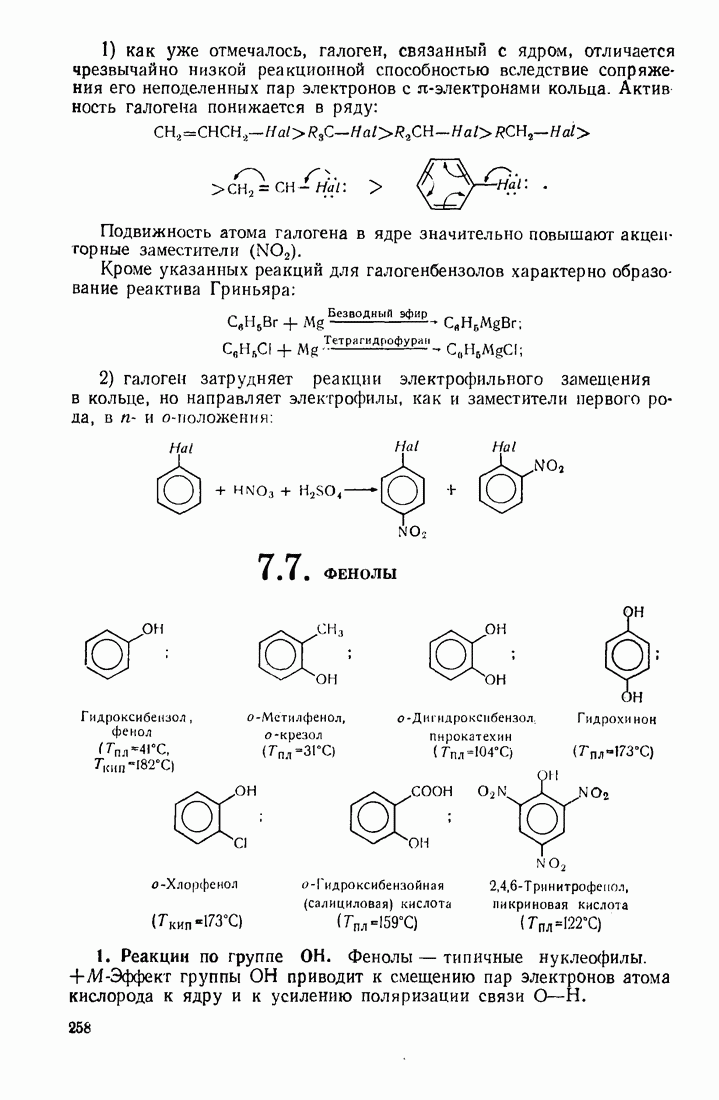
- 7.6. ГАЛОГЕНБЕНЗОЛЫ
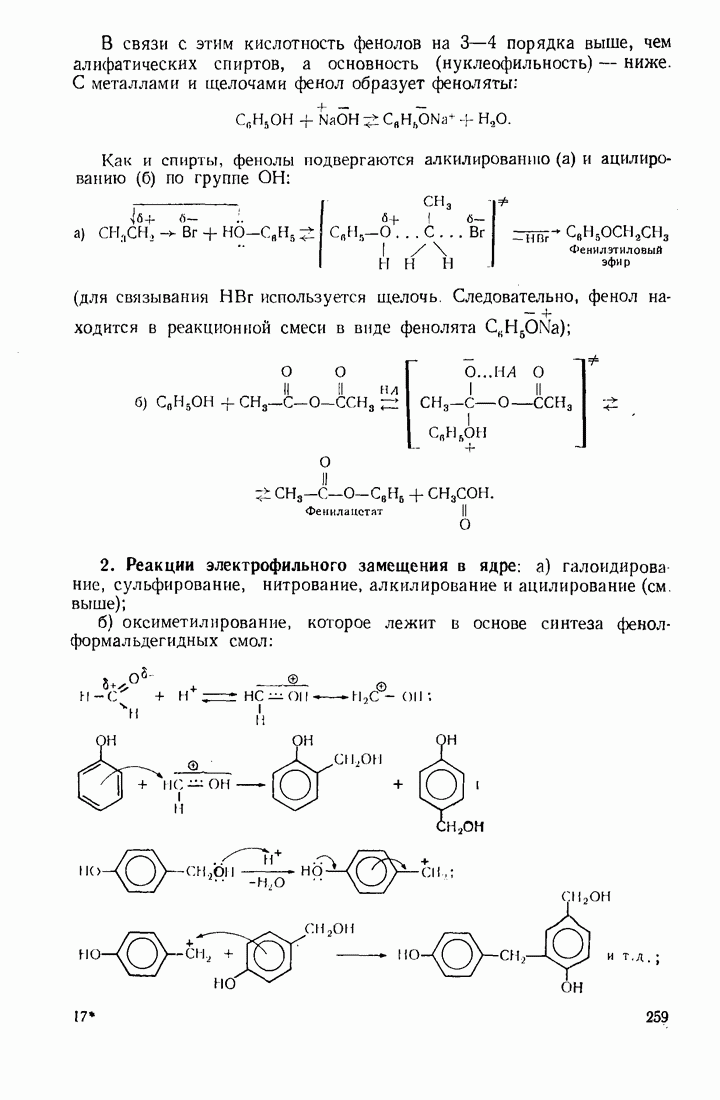
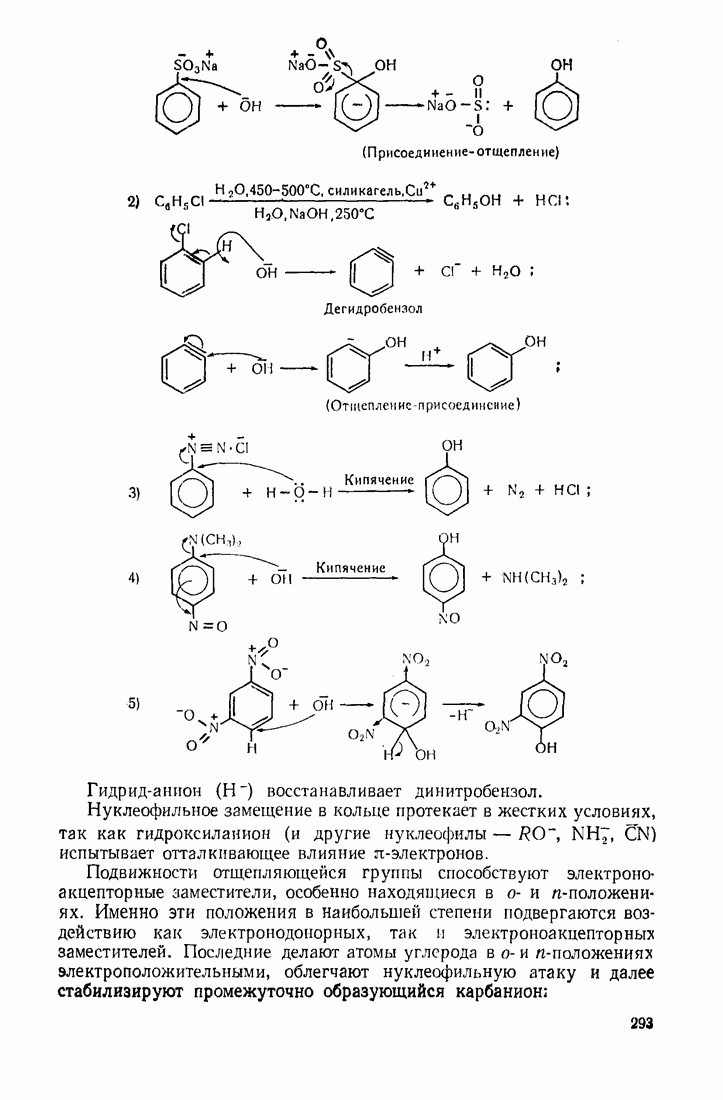
- 7.7. ФЕНОЛЫ
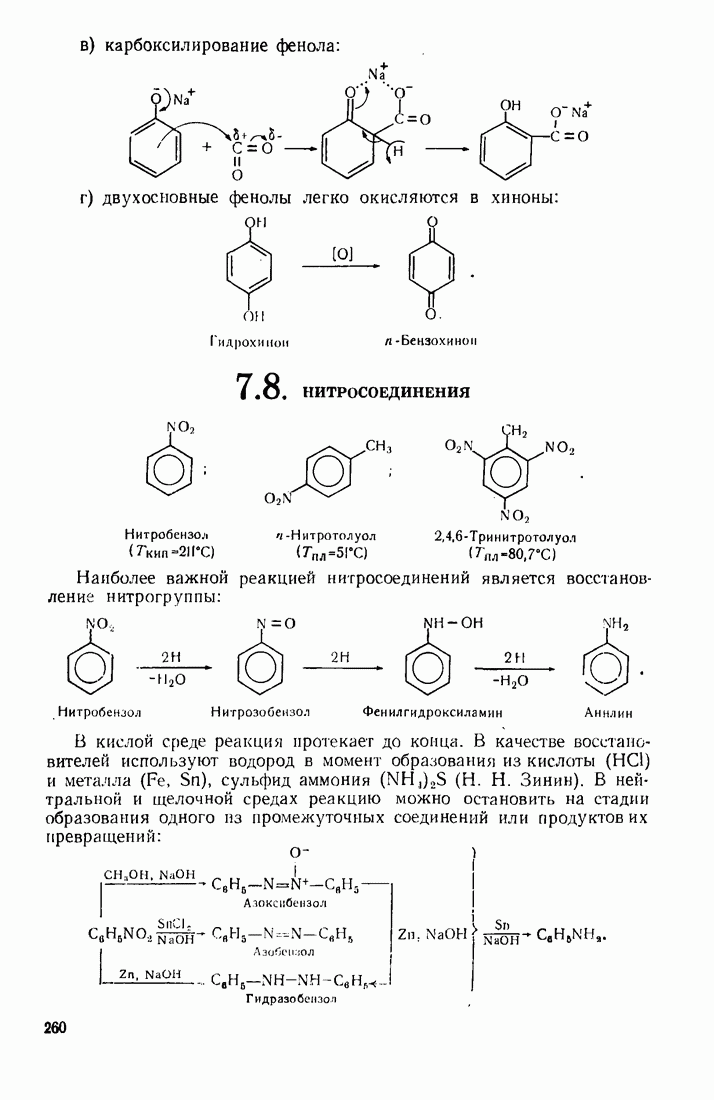
- 7.8. НИТРОСОЕД ИНЕНИЯ
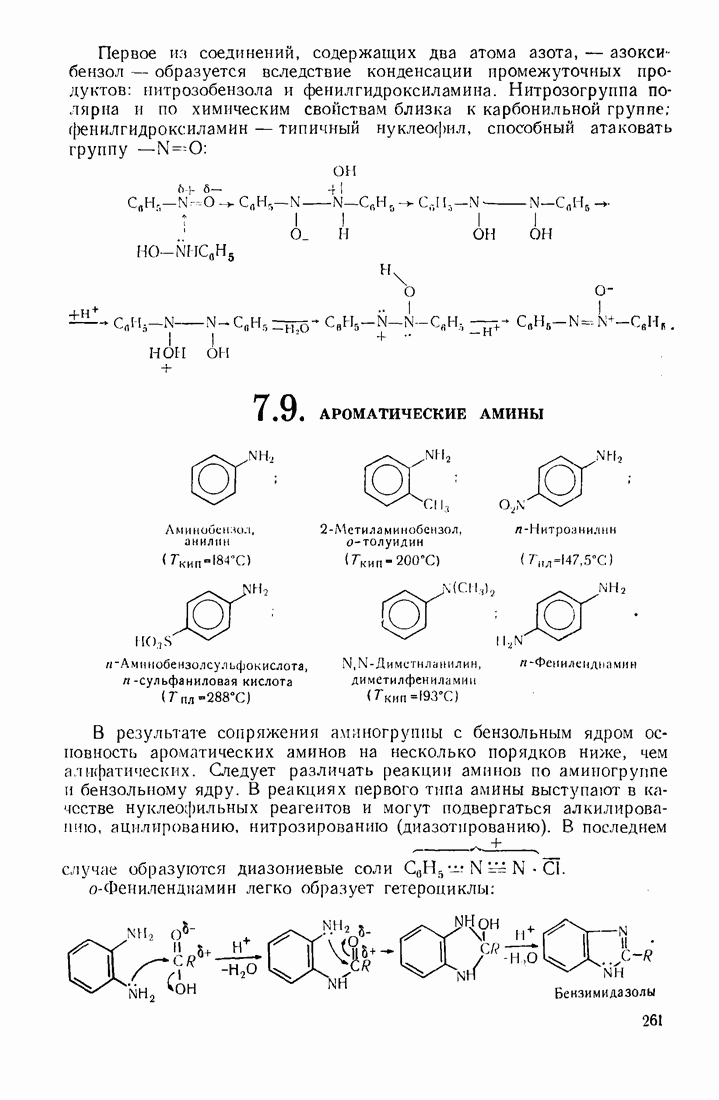
- 7.9. АРОМАТИЧЕСКИЕ АМИНЫ
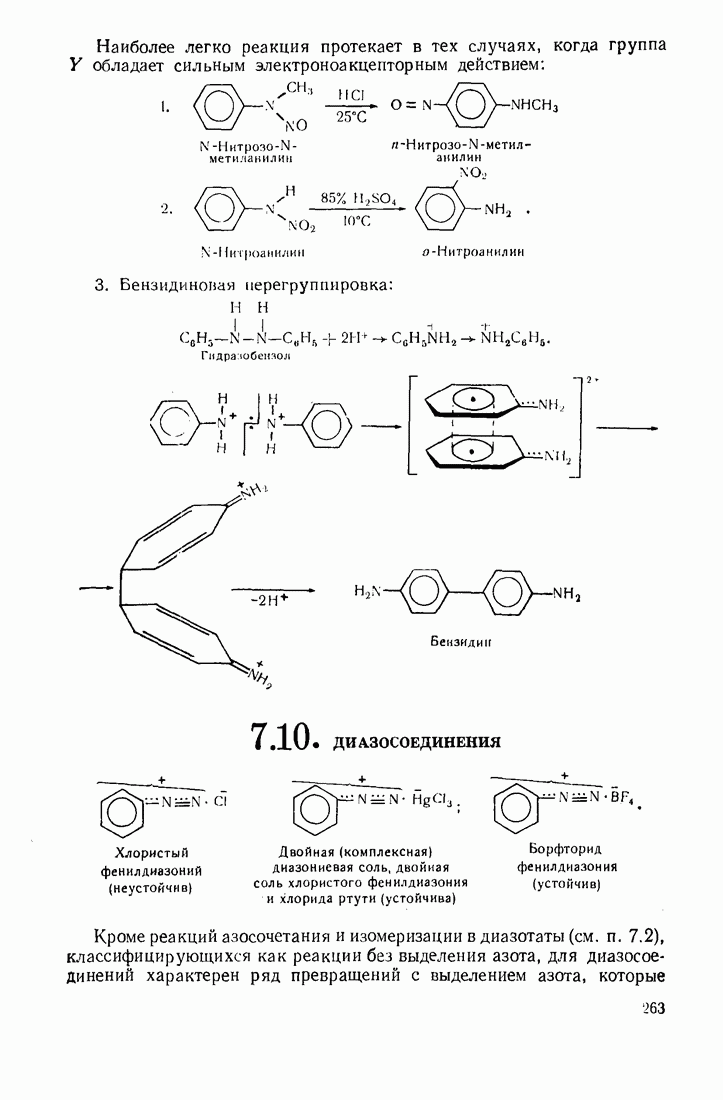
- 7.10. ДИАЗОСОЕДИНЕНИЯ
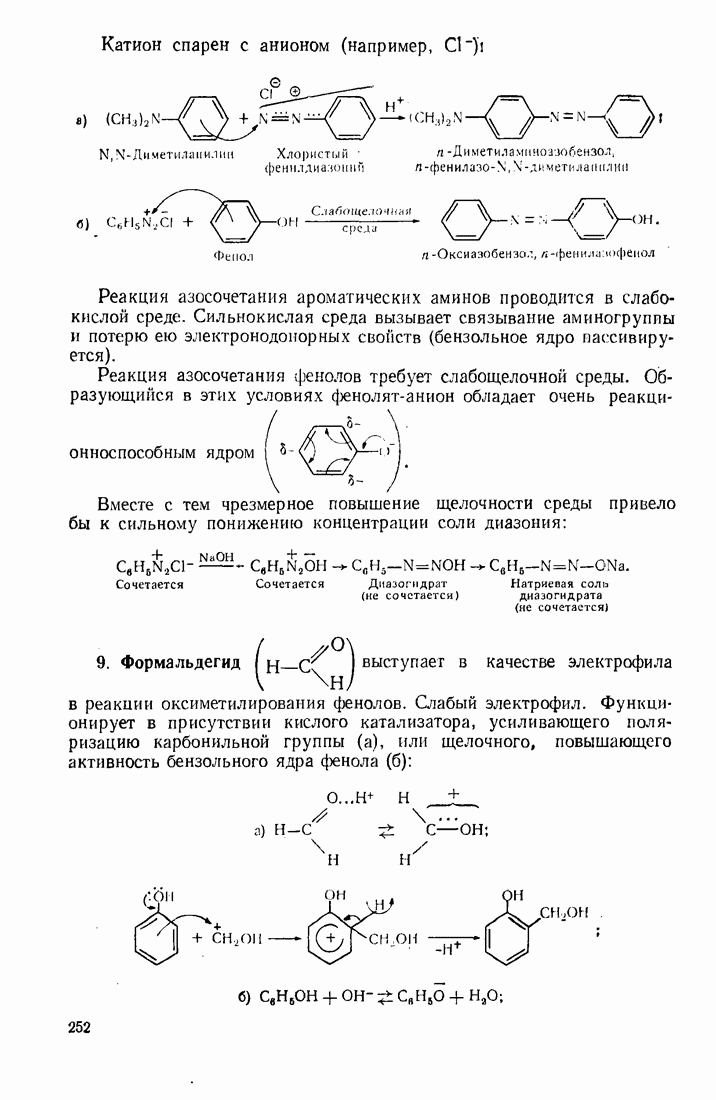
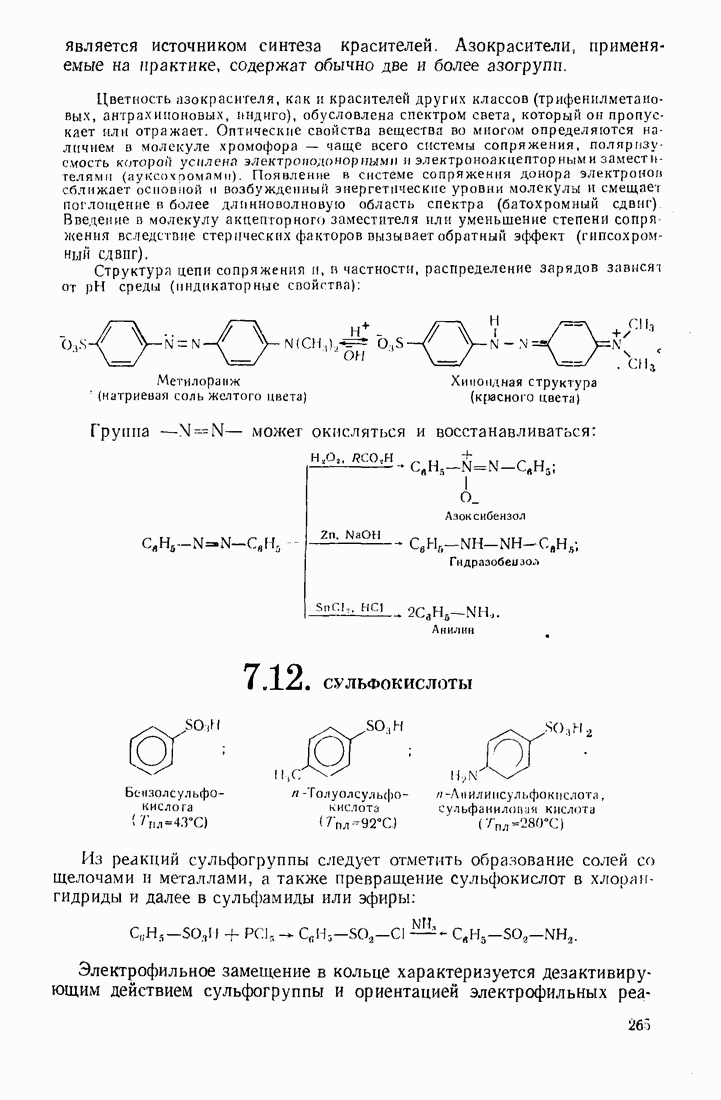
- 7.11. АЗОСОЕДИНЕНИЯ
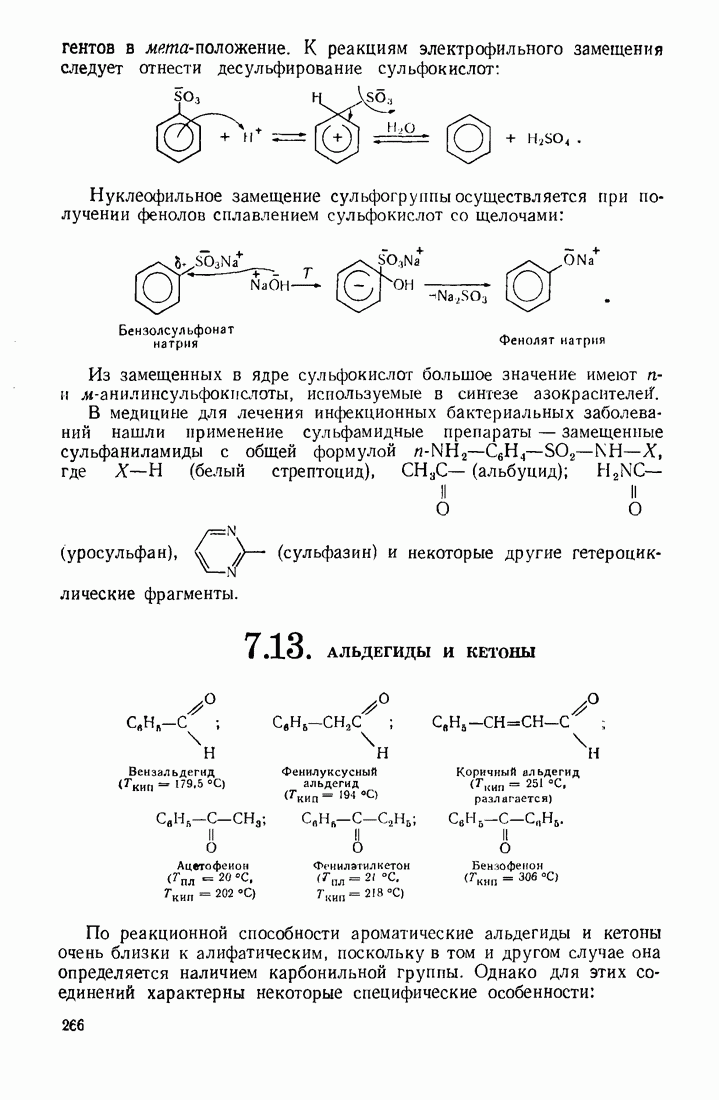
- 7.12. СУЛЬФОКИСЛОТЫ
- 7.13. АЛЬДЕГИДЫ И КЕТОНЫ
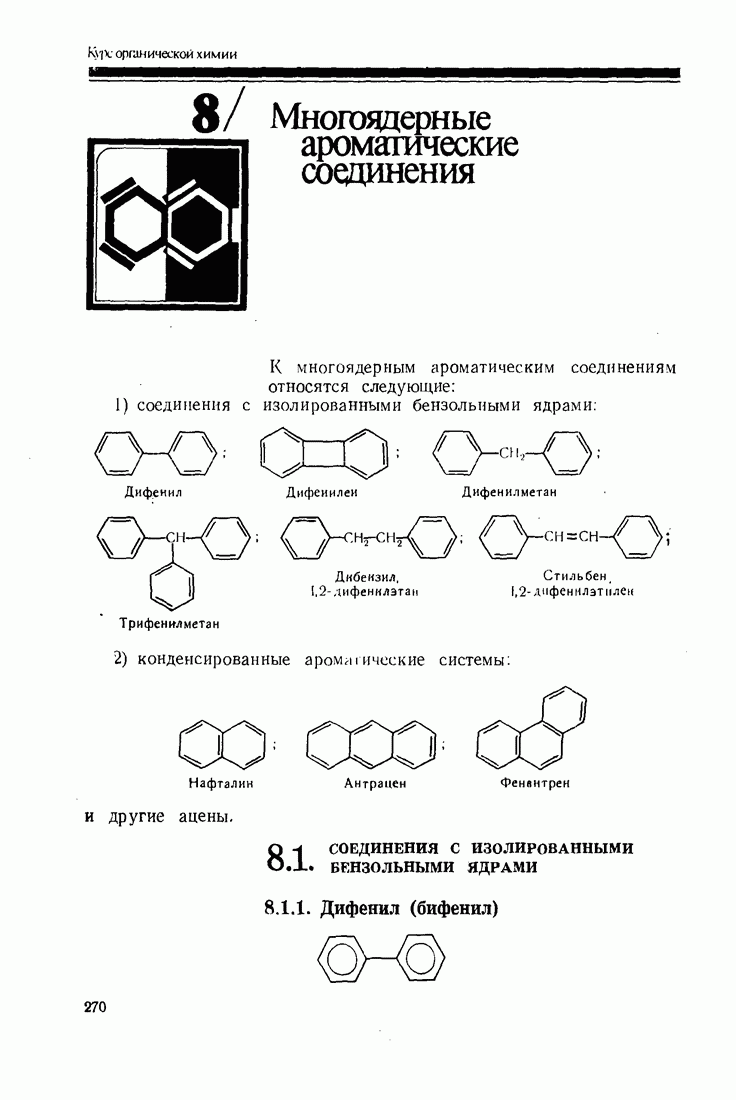
- 8. Многоядерные ароматические соединения
- 8.1. СОЕДИНЕНИЯ С ИЗОЛИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЯДРАМИ
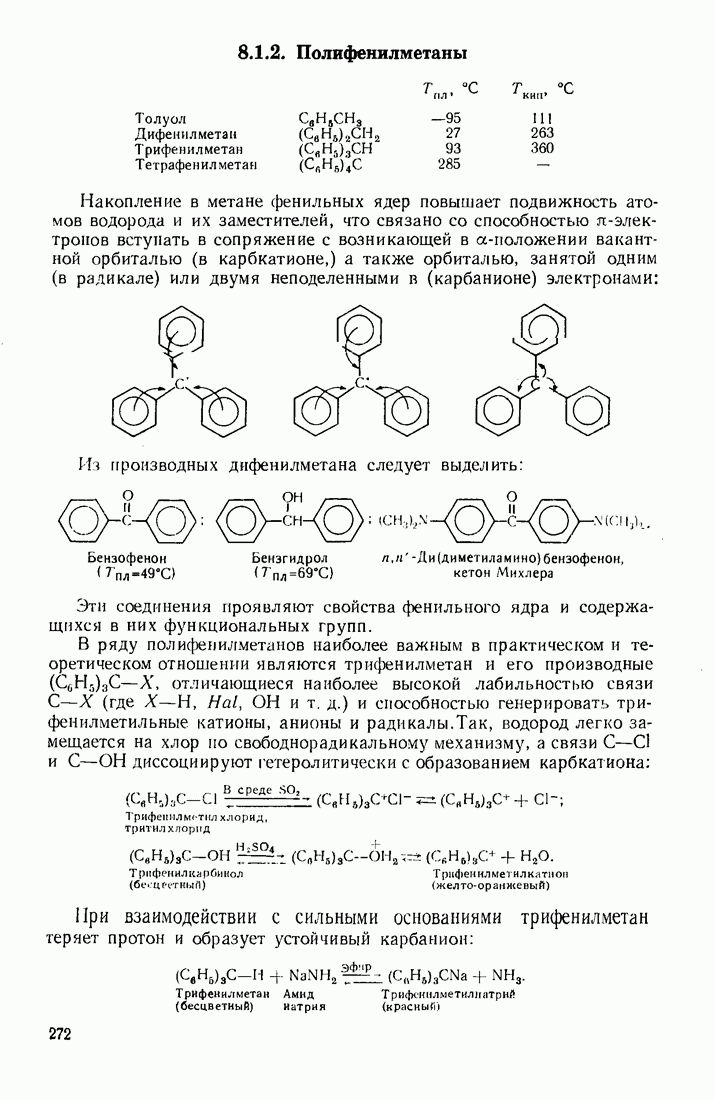
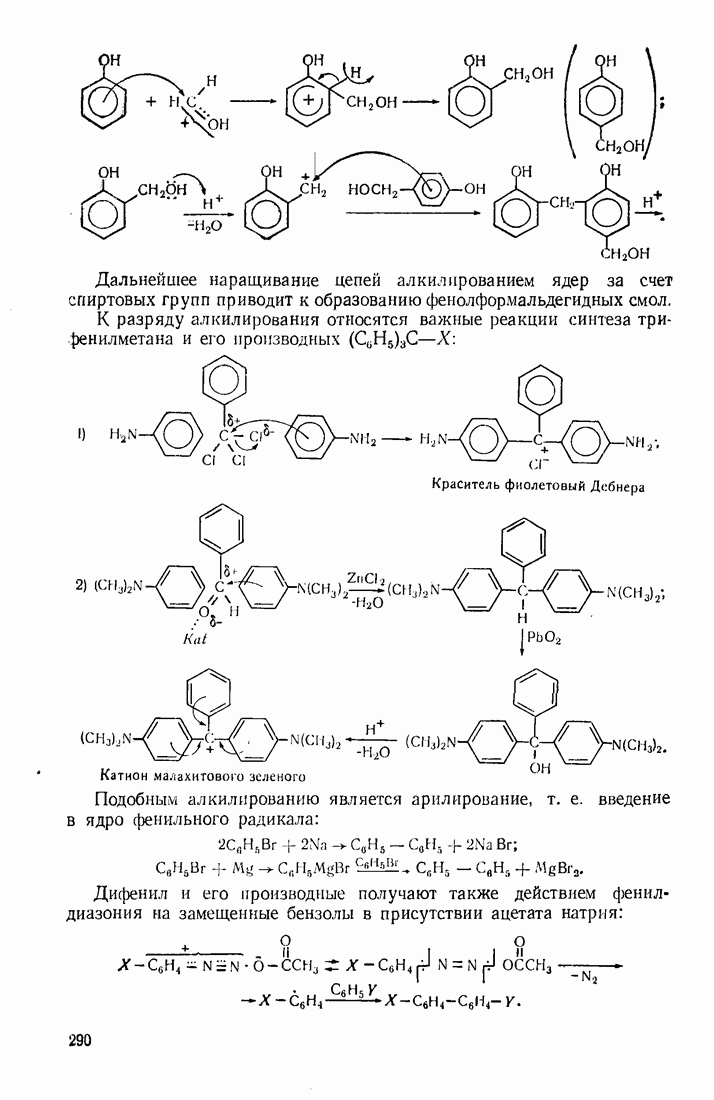
- 8.1.2. Полифенилметаны
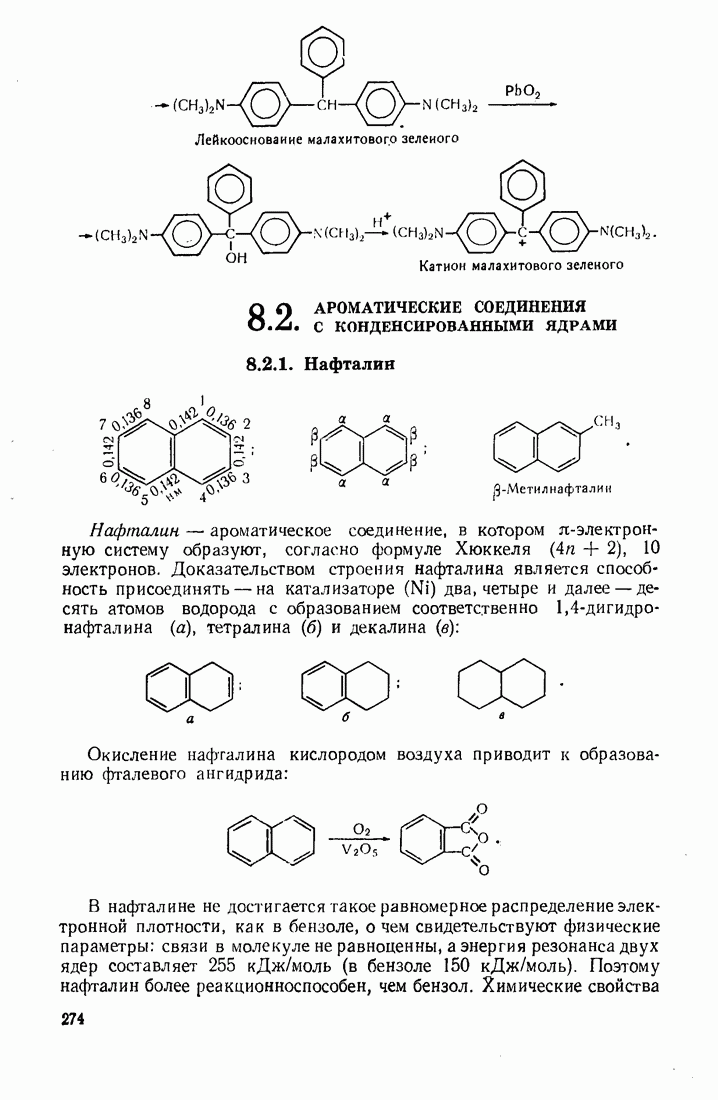
- 8.2. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ С КОНДЕНСИРОВАННЫМИ ЯДРАМИ
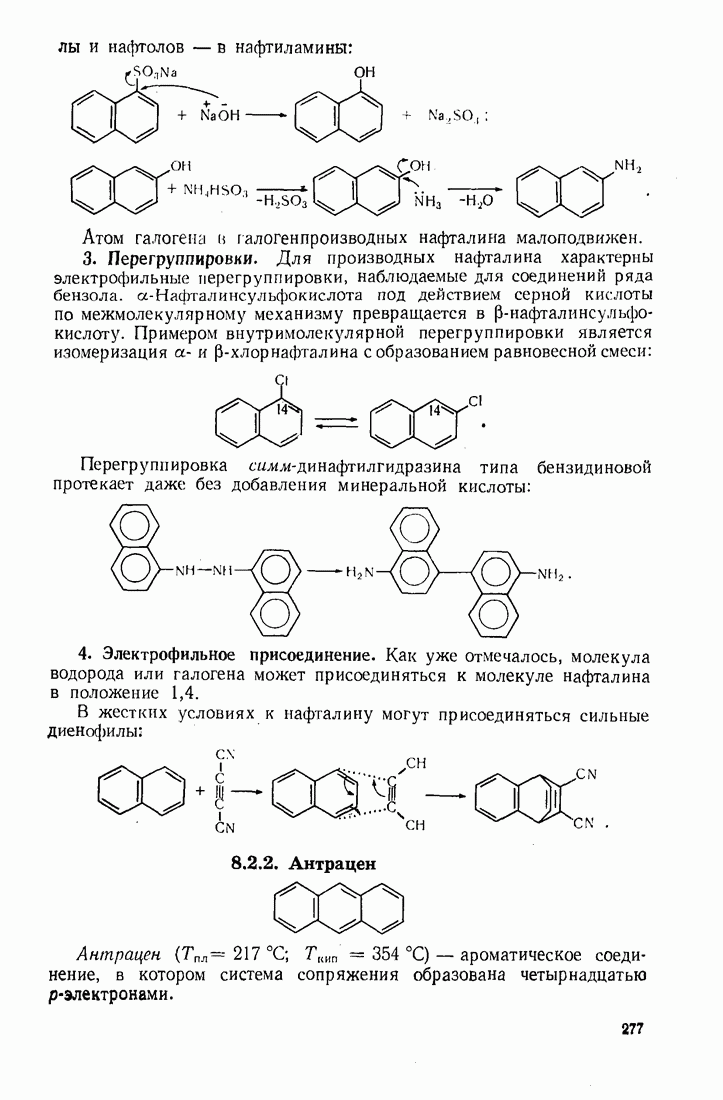
- 8.2.2. Антрацен
- 8.2.3. Фенантрен
- 9. Методы синтеза в ряду ароматических соединений
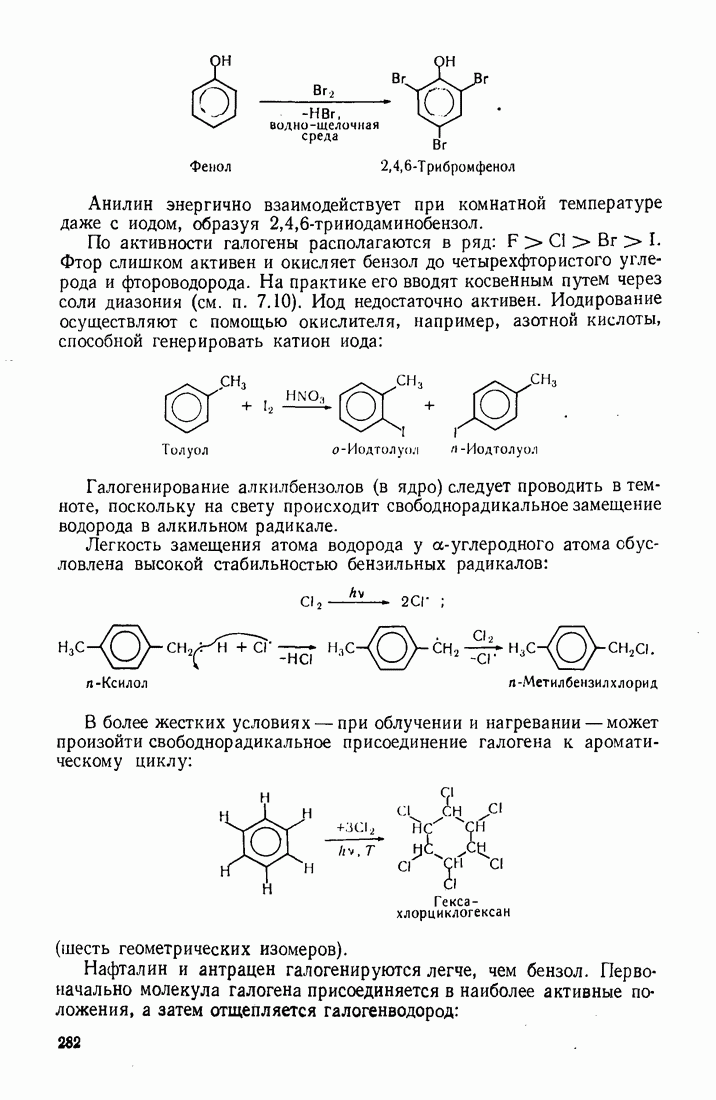
- 9.1. ГАЛОГЕНИРОВАНИЕ
- 9.2. НИТРОВАНИЕ
- 9.3. СУЛЬФИРОВАНИЕ
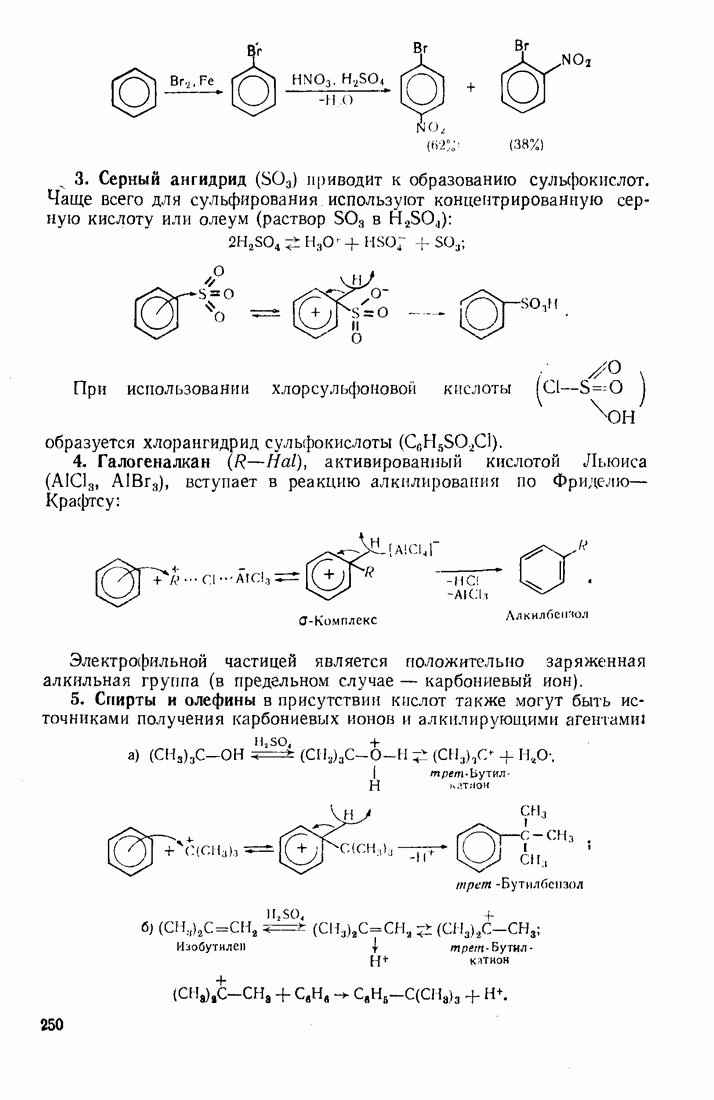
- 9.4. АЛКИЛИРОВАНИЕ
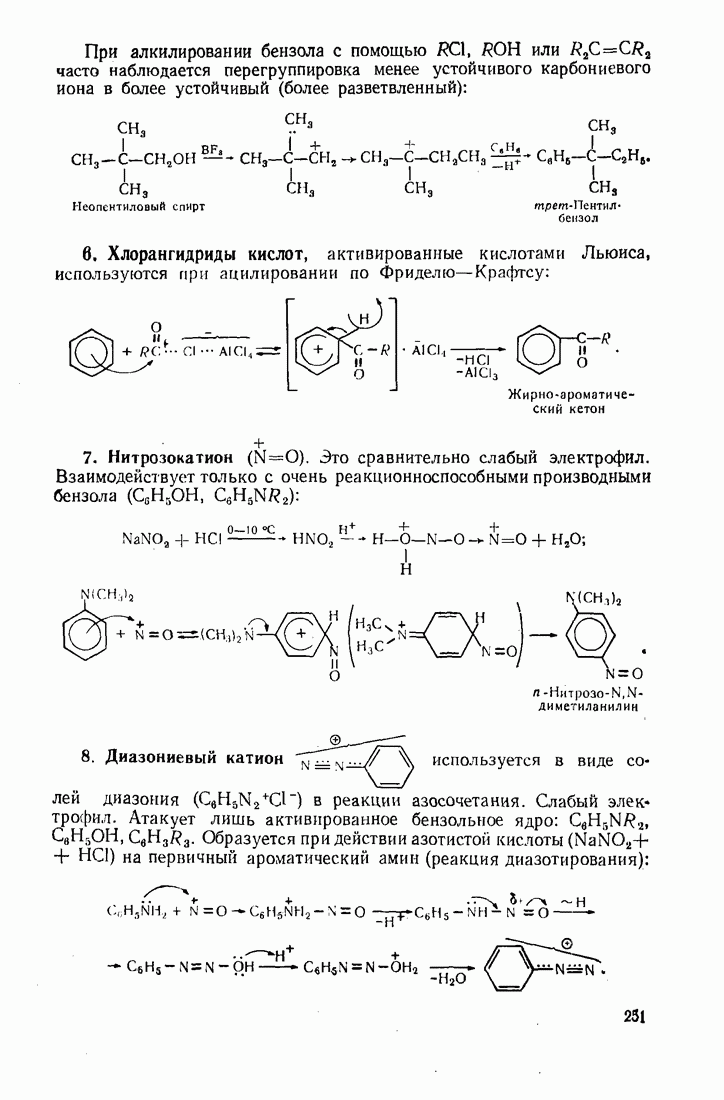
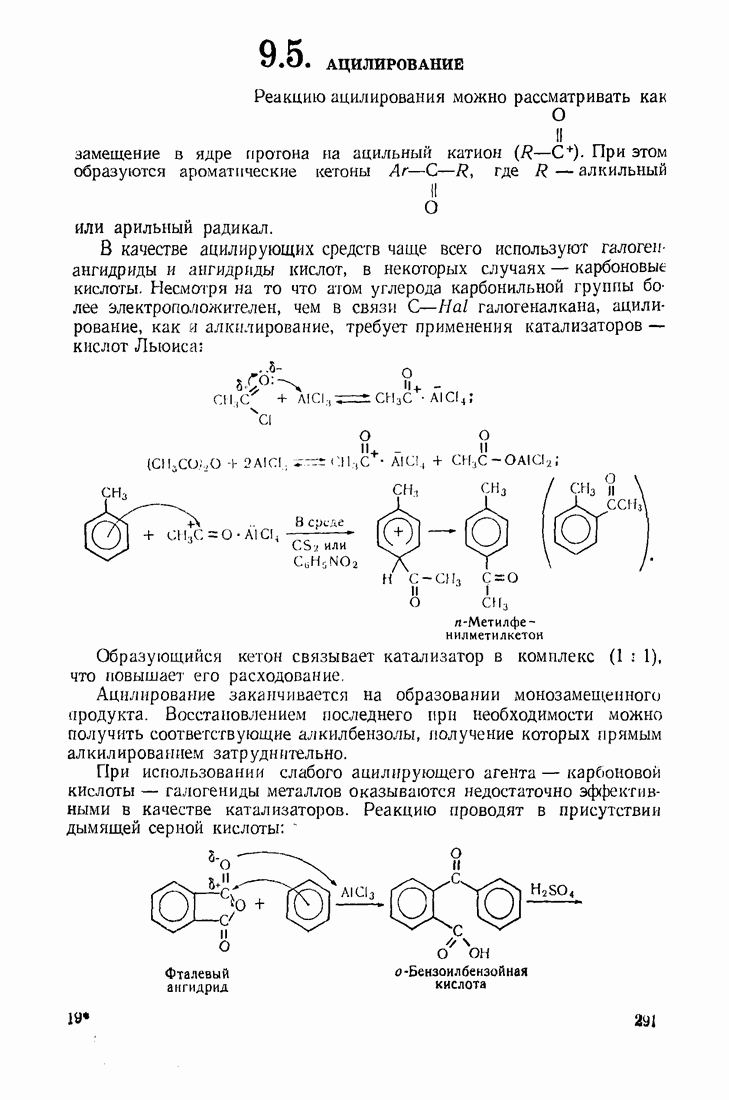
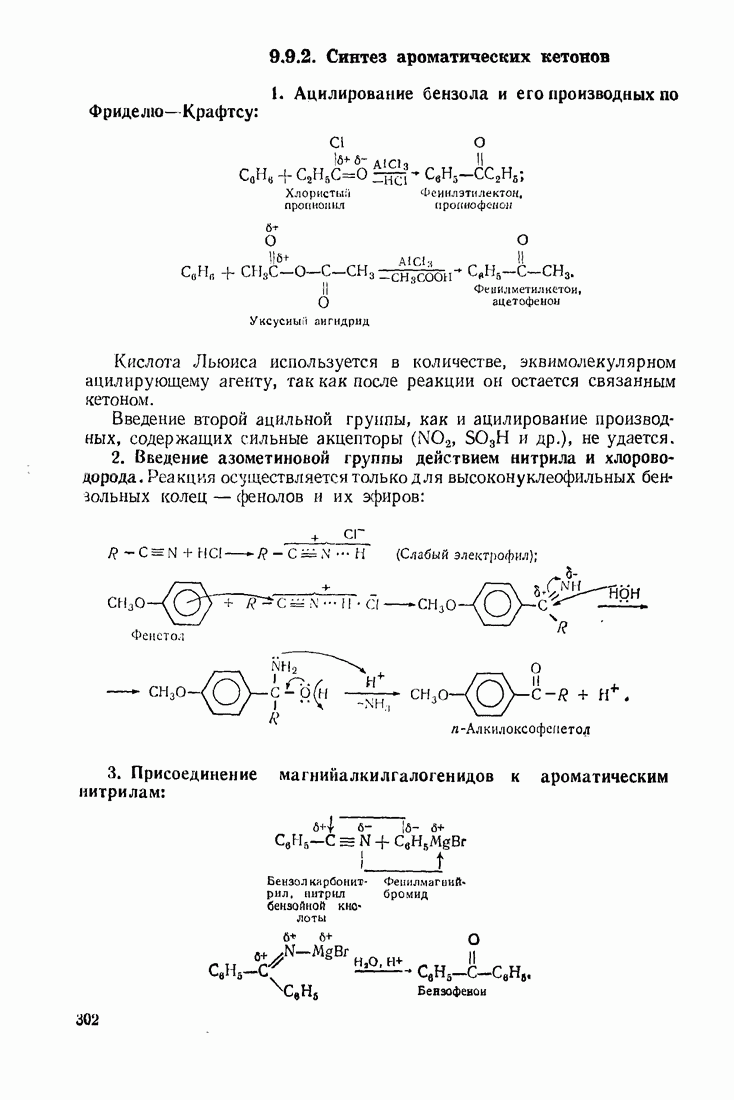
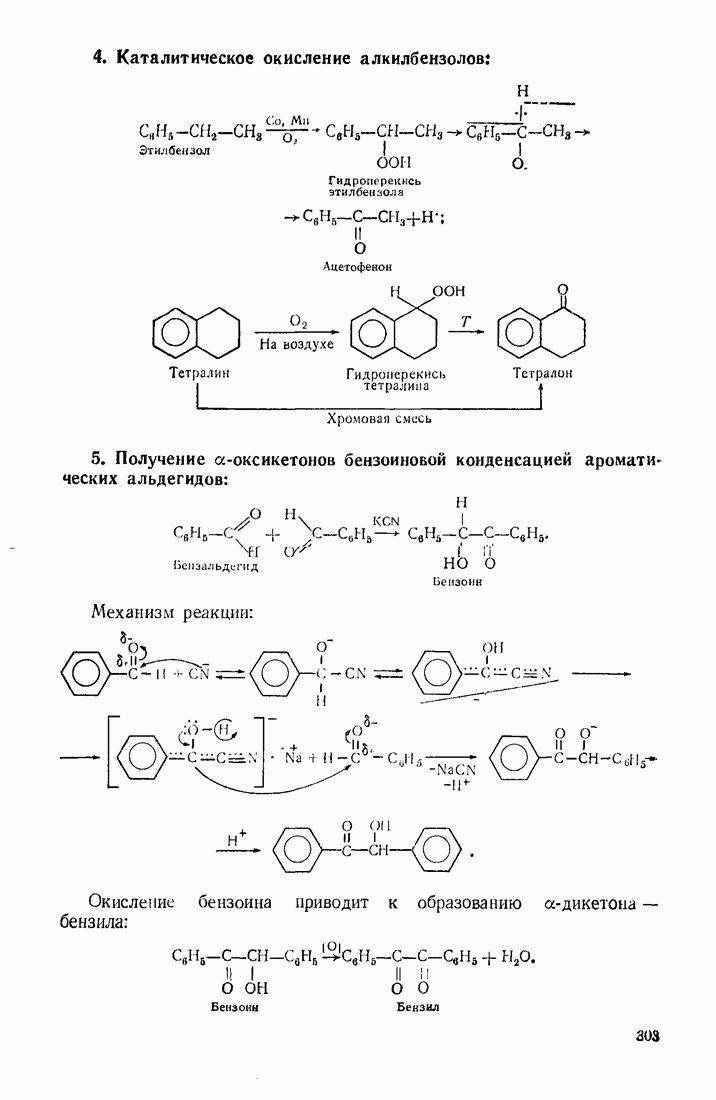
- 9.5. АЦИЛИРОВАНИЕ
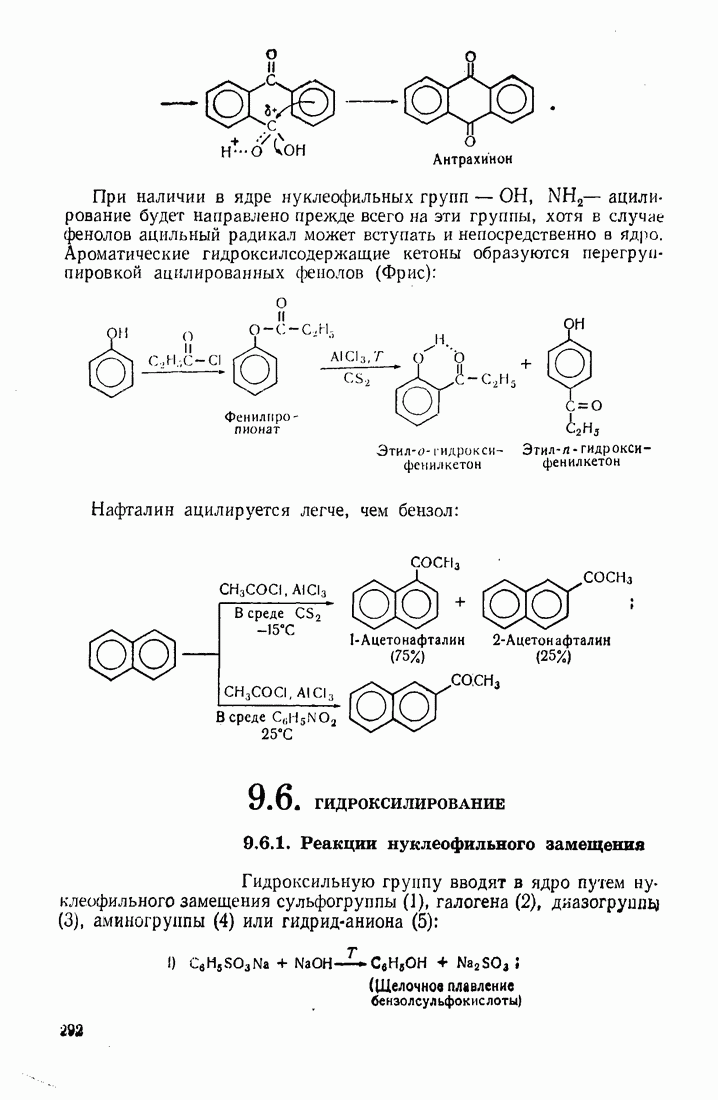
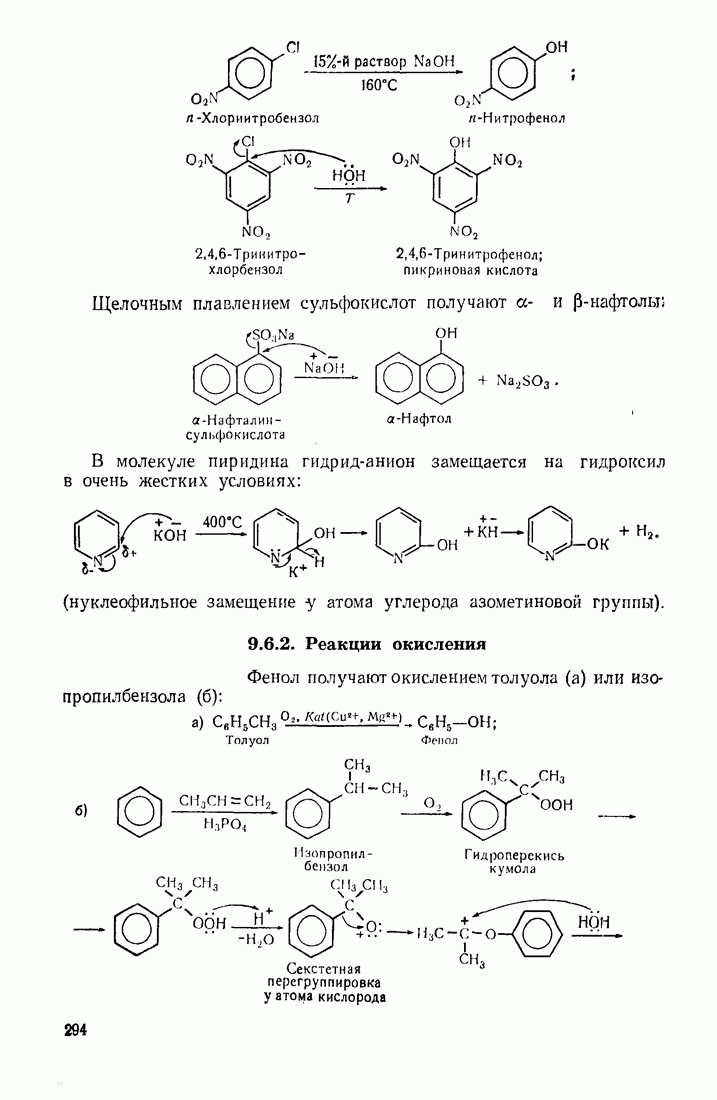
- 9.6. ГИДРОКСИЛИРОВАНИЕ
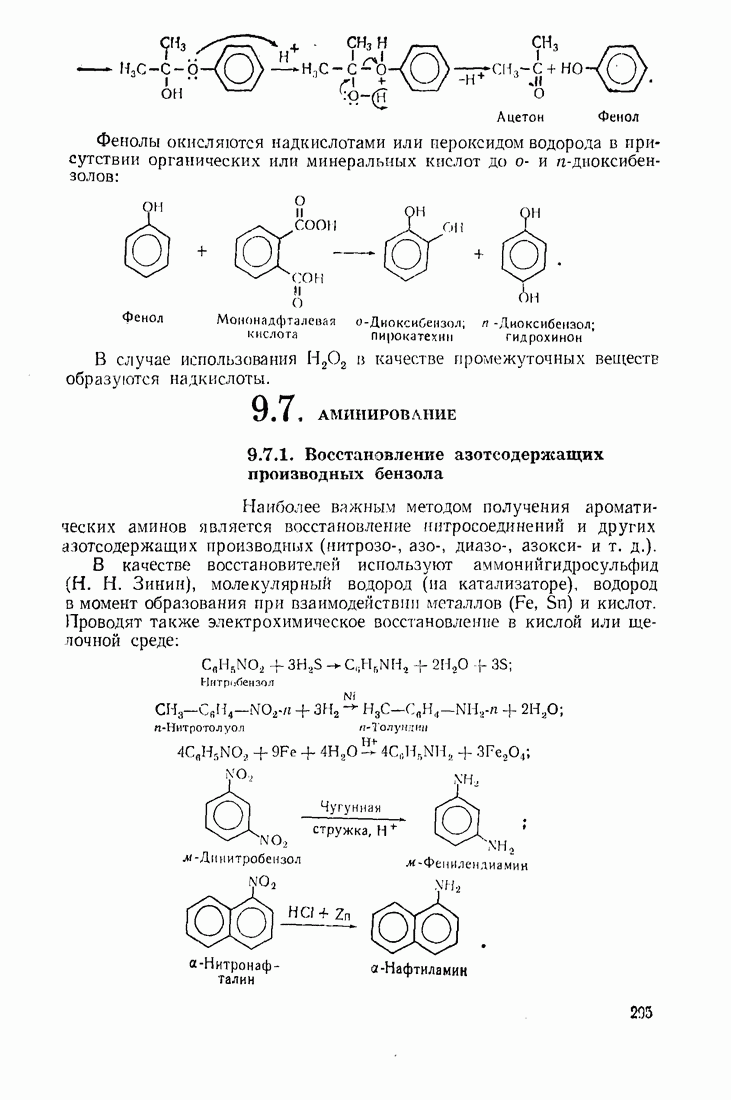
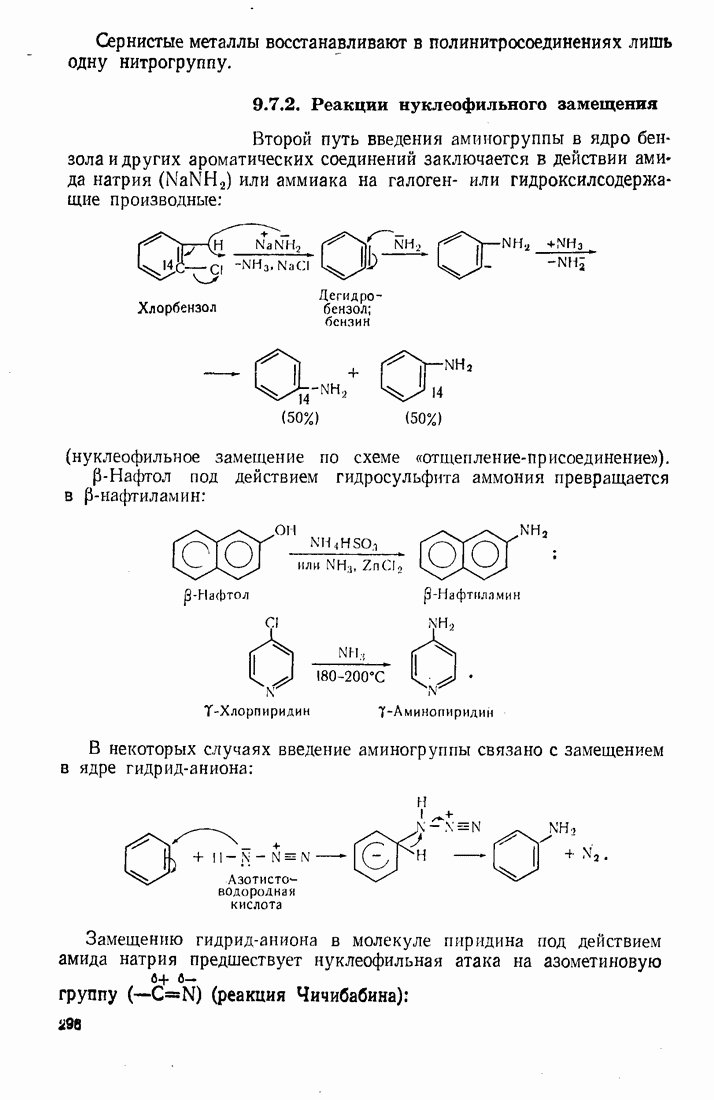
- 9.7. АМИНИРОВАНИЕ
- 9.8. НИТРОЗИРОВАНИЕ
- 9.9. КАРБОНИЛИРОВАНИЕ
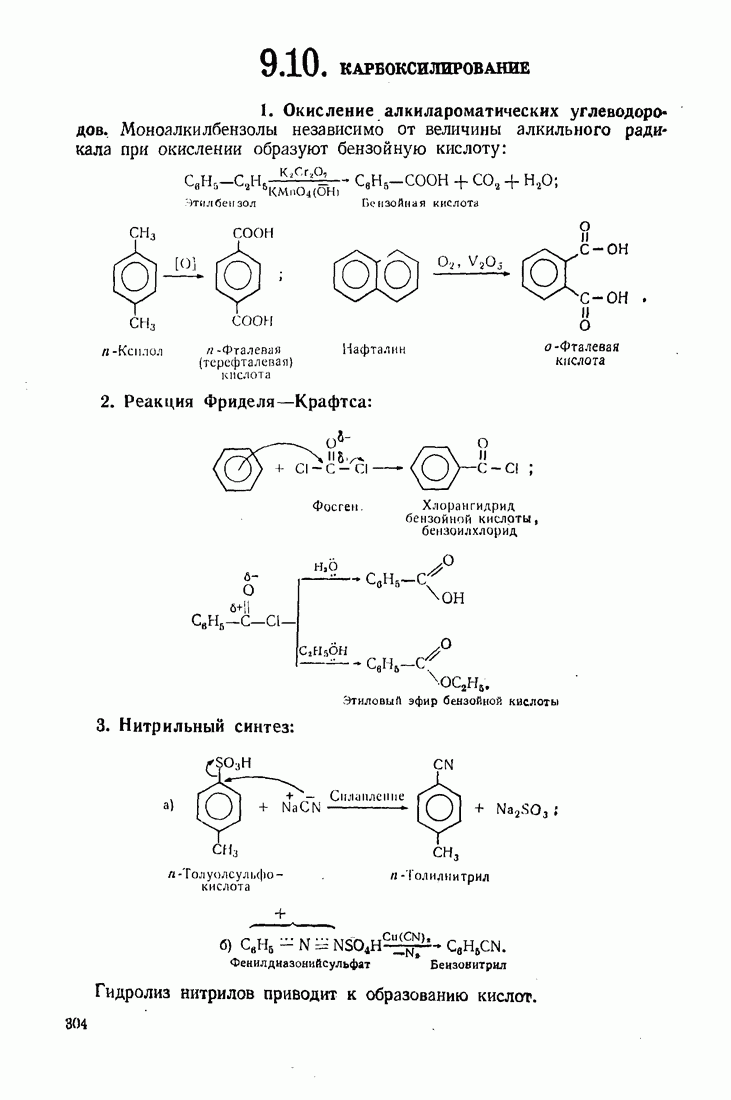
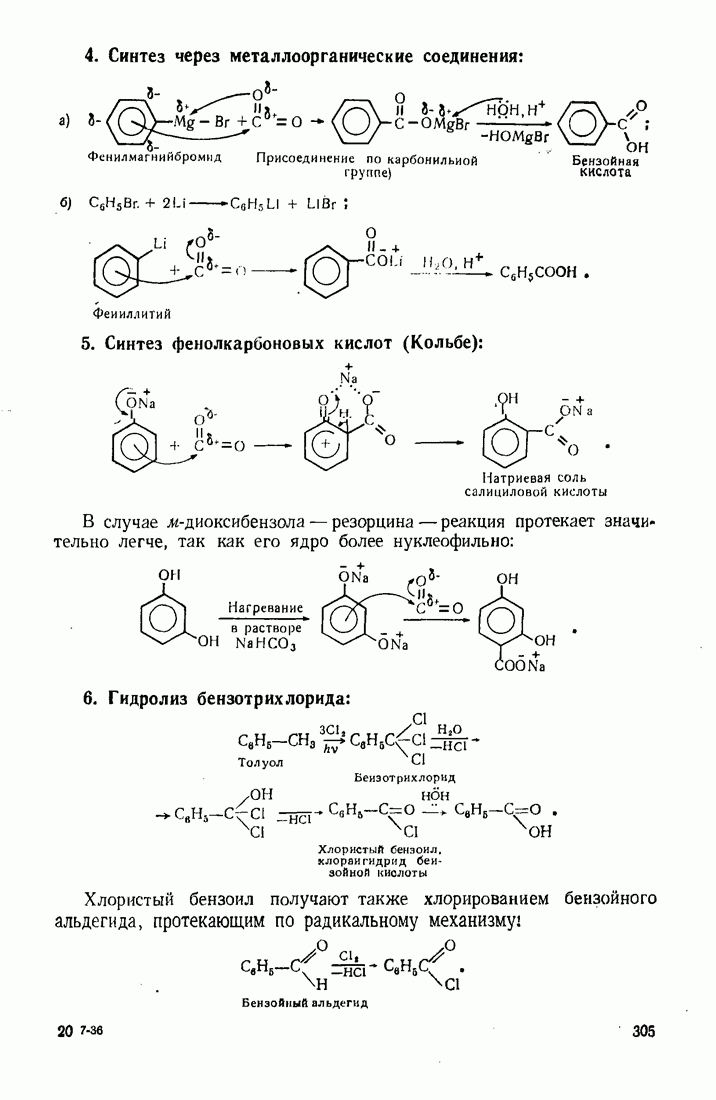
- 9.10. КАРБОКСИЛИРОВАНИЕ
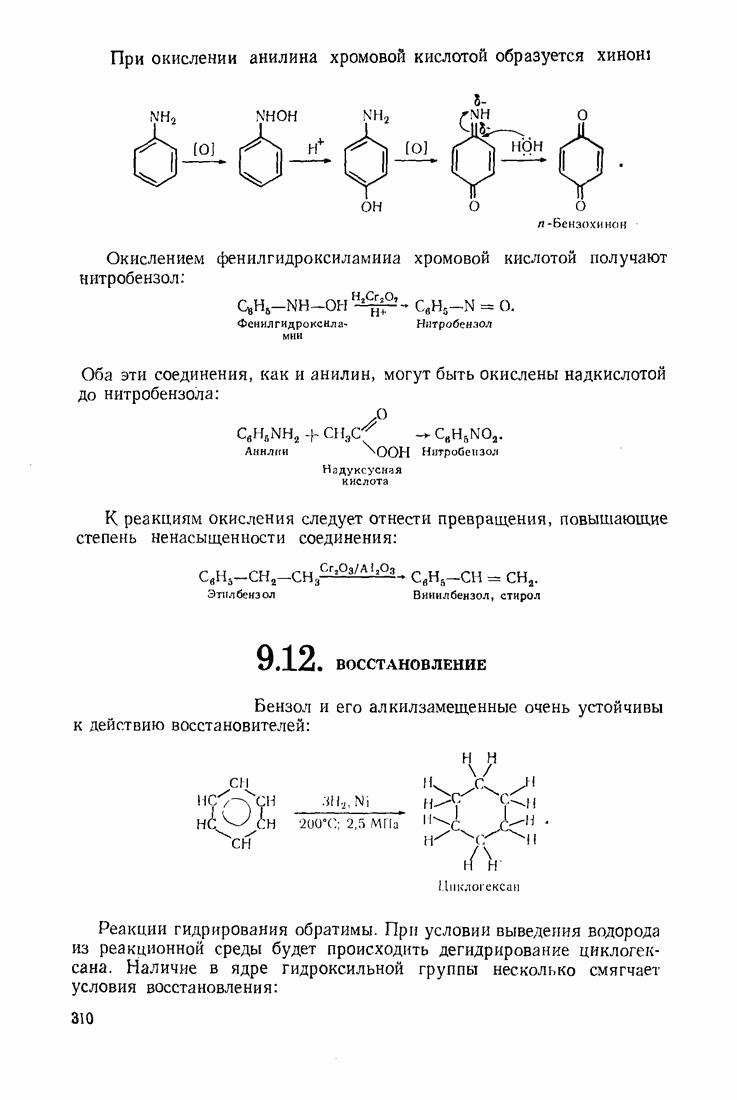
- 9.11. ОКИСЛЕНИЕ
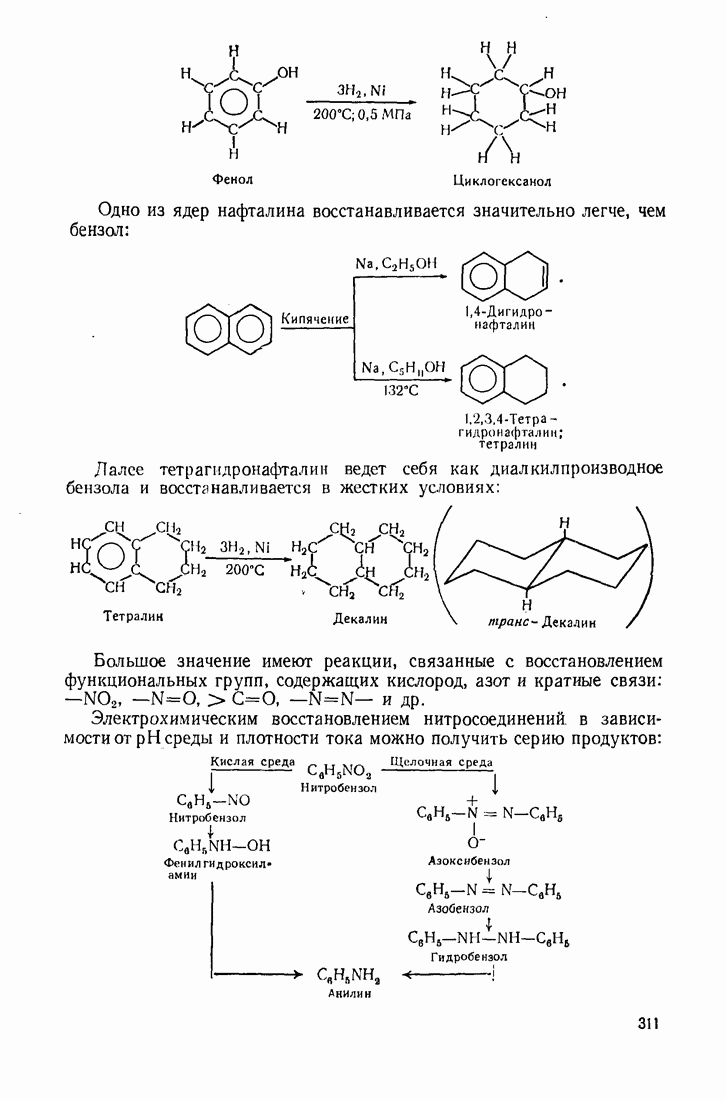
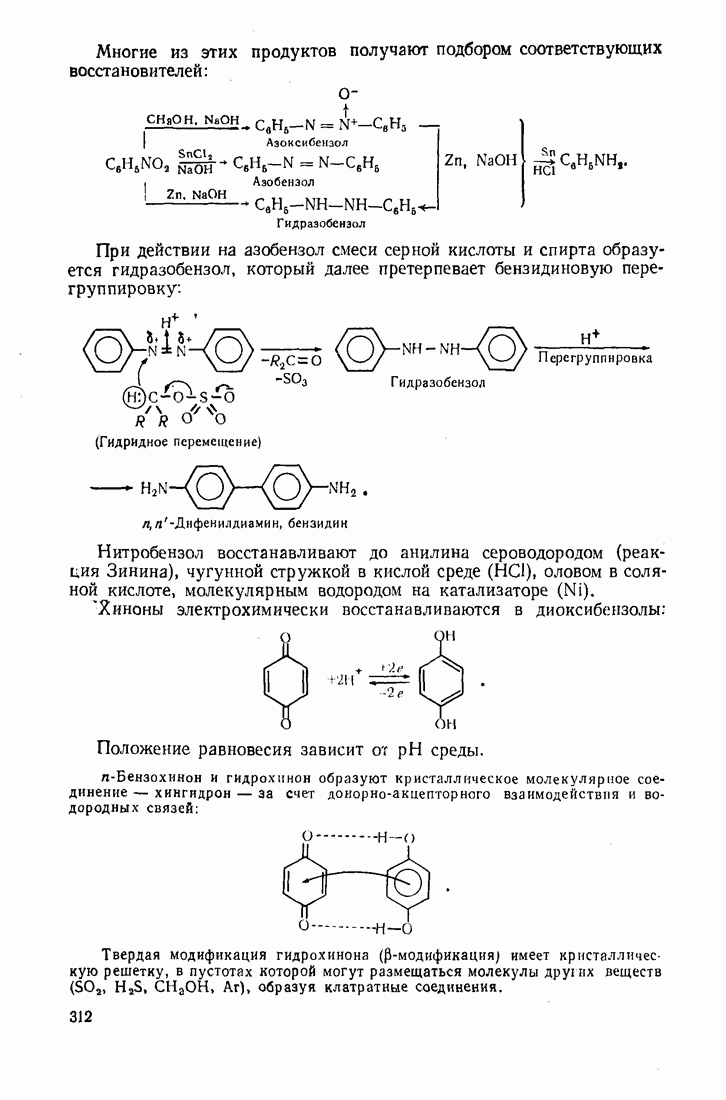
- 9.12. ВОССТАНОВЛЕНИЕ
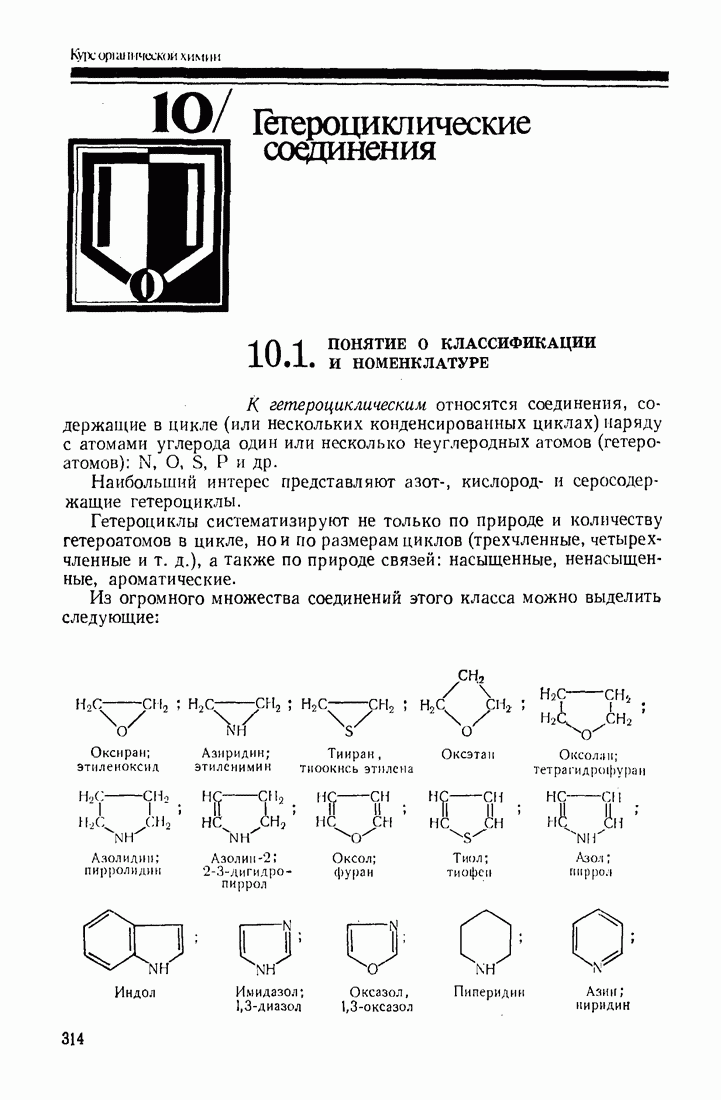
- 10. Гетероциклические соединения
- 10.2. ОБЩАЯ ХАРАКТЕРИСТИКА СТРОЕНИЯ И РЕАКЦИОННОЙ СПОСОБНОСТИ
- 10.3. ПЯТИ- И ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
- 10.4. ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
- 10.5. МЕТОДЫ СИНТЕЗА ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
- 10.6. П0НЯТИЕ О ПРИРОДНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЯХ
- 11. Зпементоорганические соединения
- 11.2. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ НЕКОТОРЫХ НЕМЕТАЛЛОВ
- 11.3. МЕГАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 11.4. ОРГАНИЧЕСКИЕ ПРОИЗВОДНЫЕ ПЕРЕХОДНЫХ МЕТАЛЛОВ
- 12. Сырье и основные направления развития промышленности органического синтеза
- 12.1.1. Нефть и сопутствующий природный газ
- 12.1.2. Углехимическое сырье
- 12.1.3. Лесохимическое и сельскохозяйственное сырье
- 12.1.4. Основные направления химической переработки нефти и альтернативные виды сырья
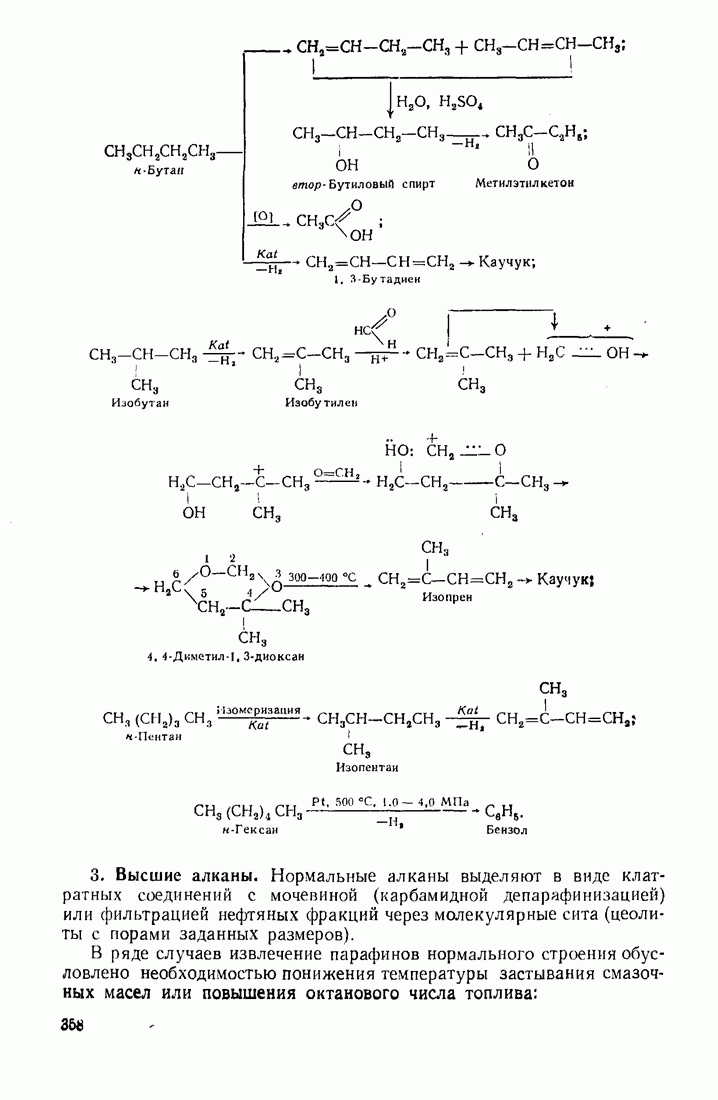
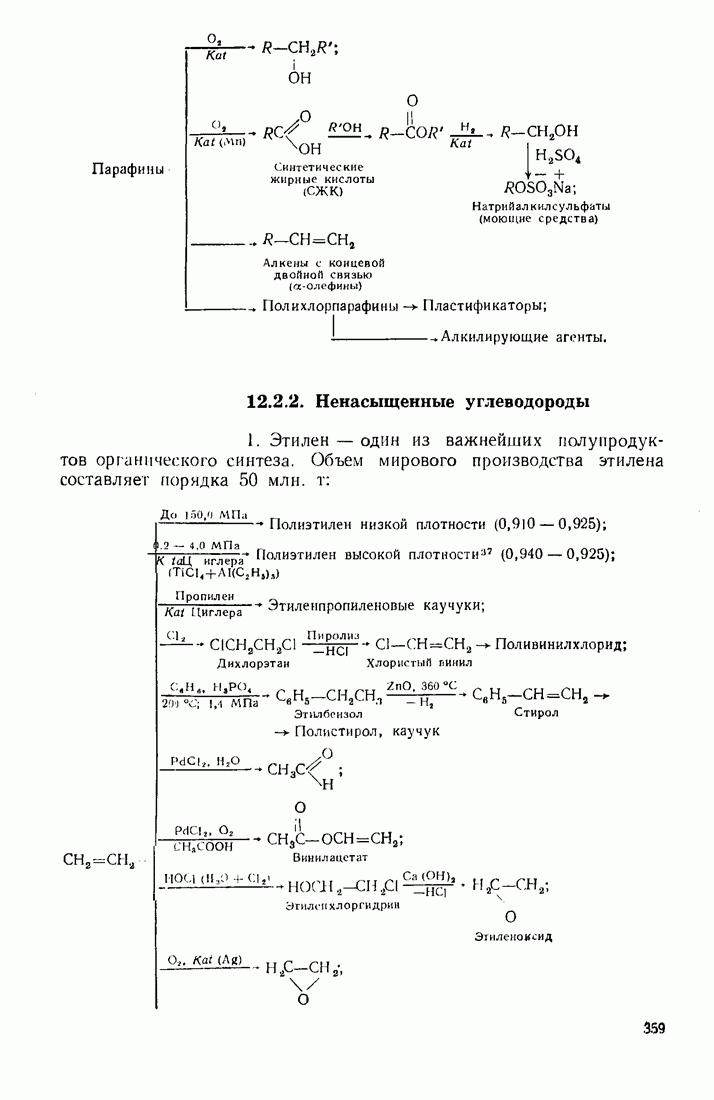
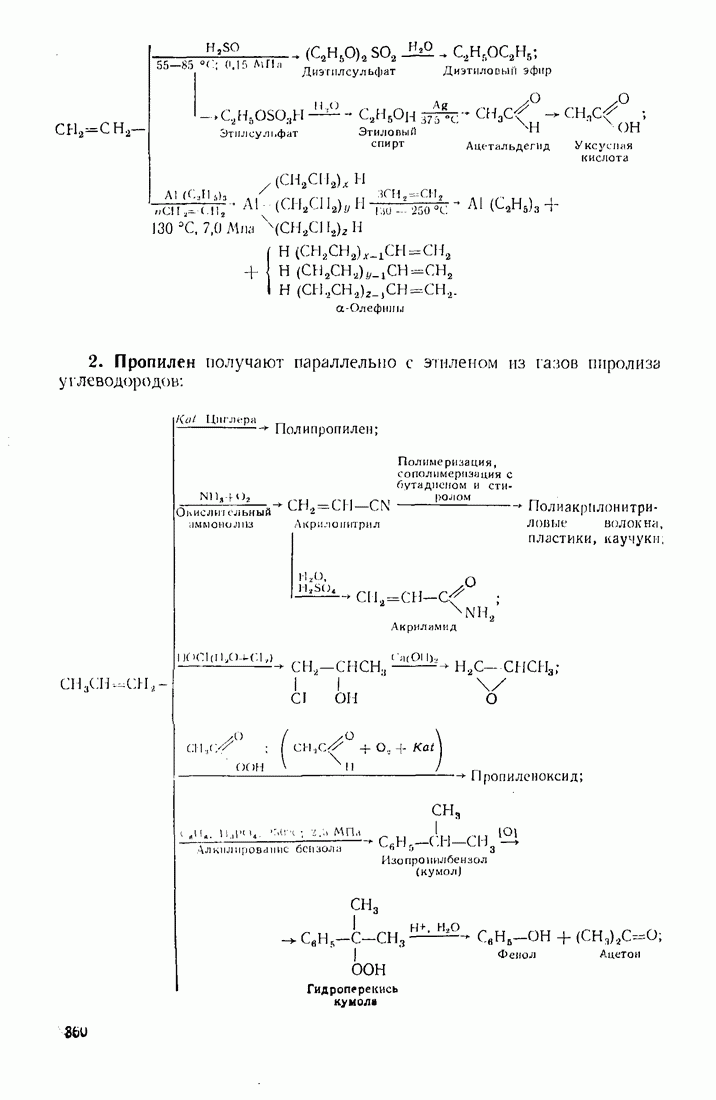
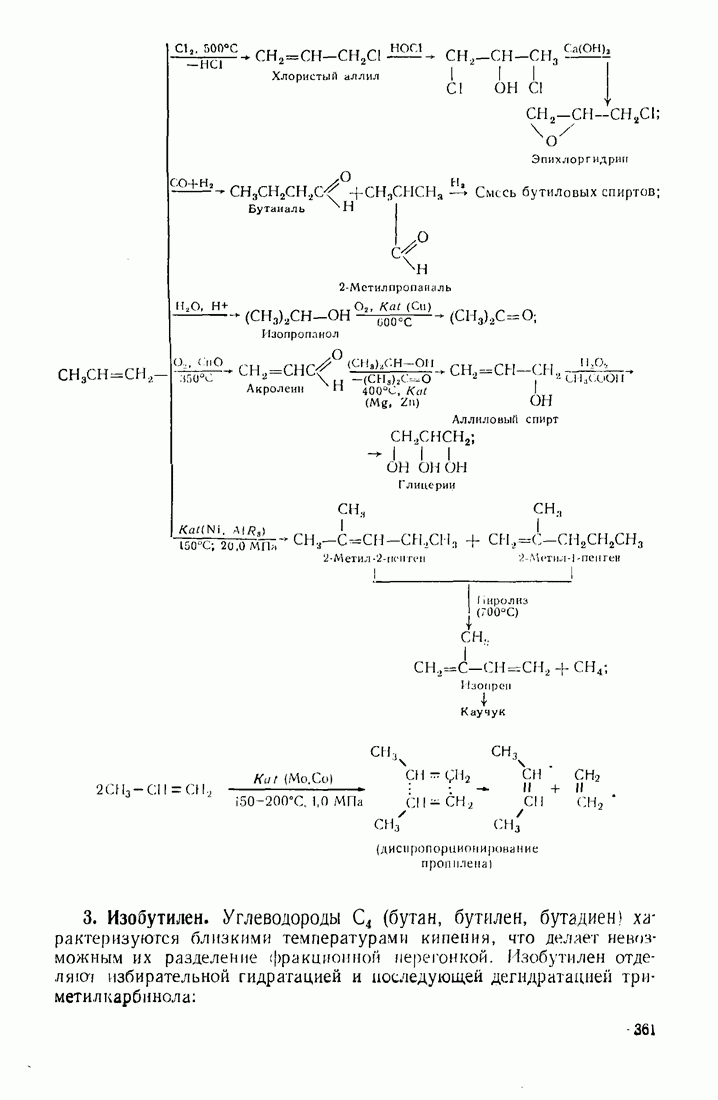
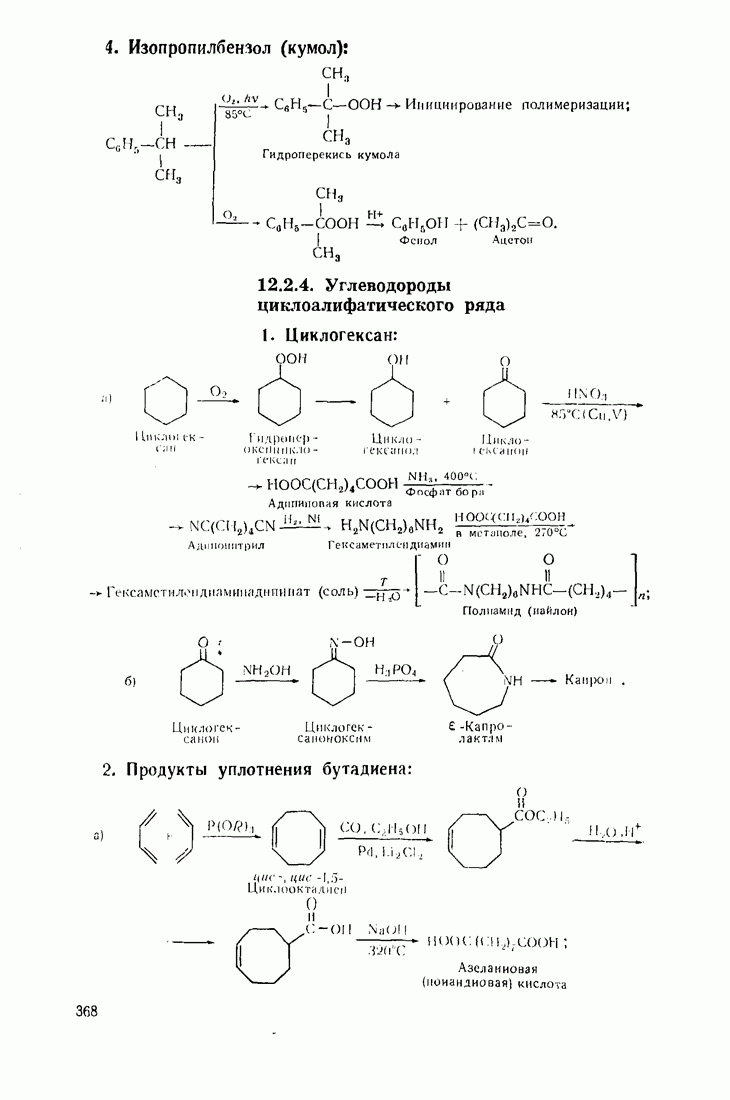
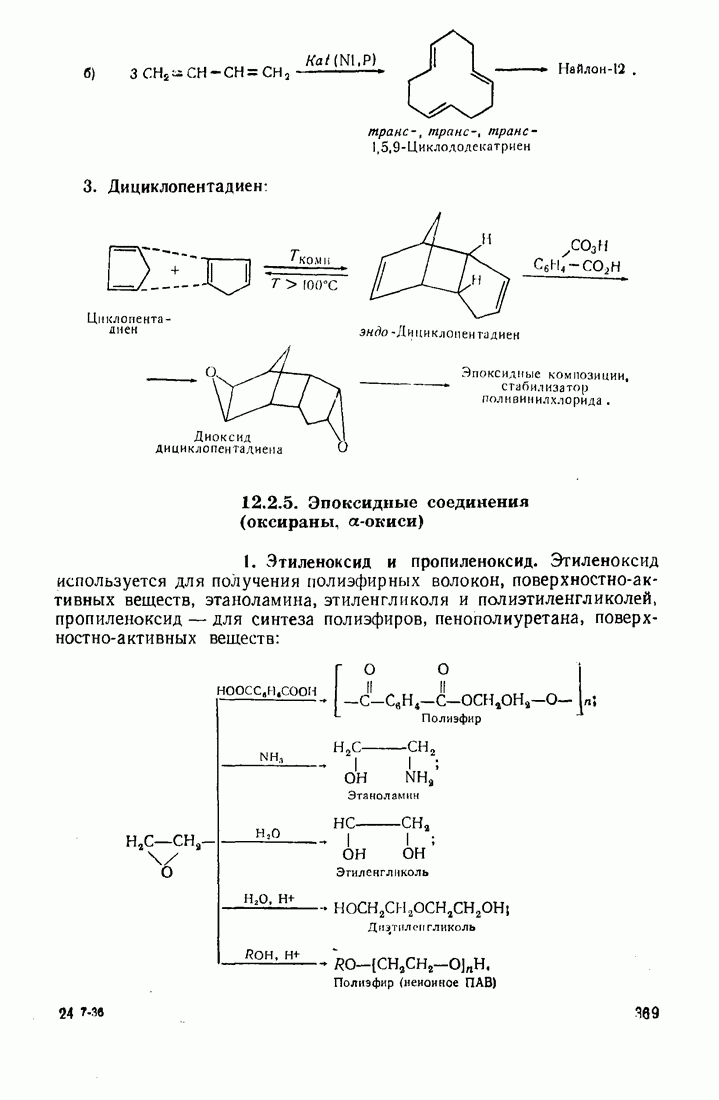
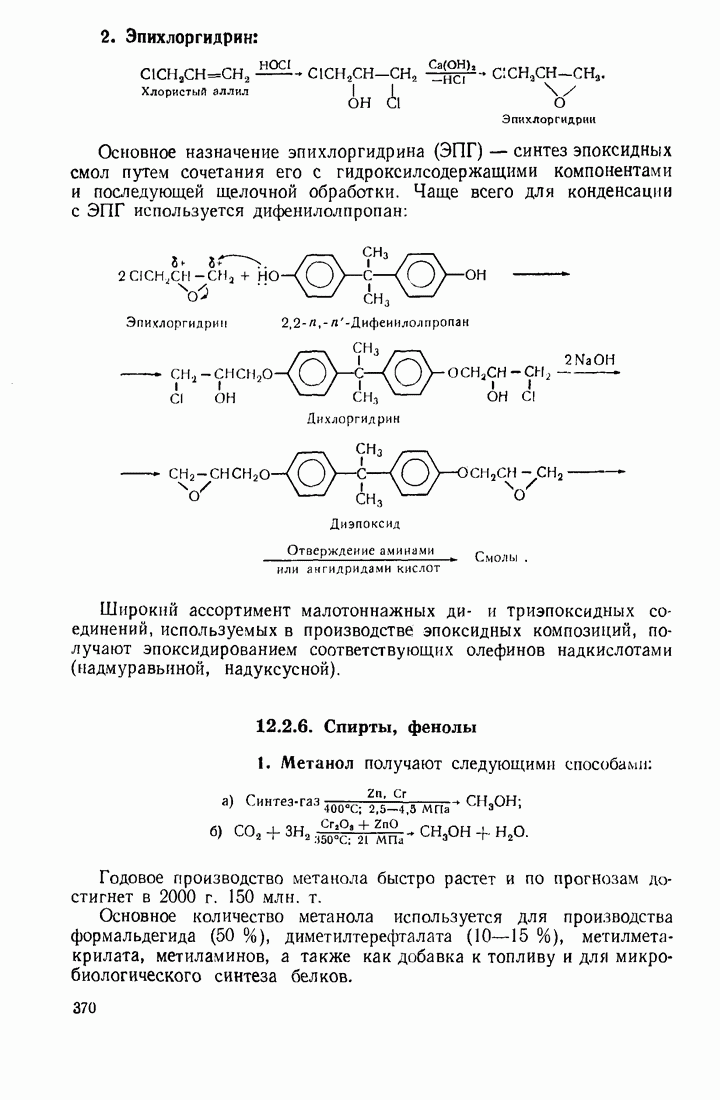
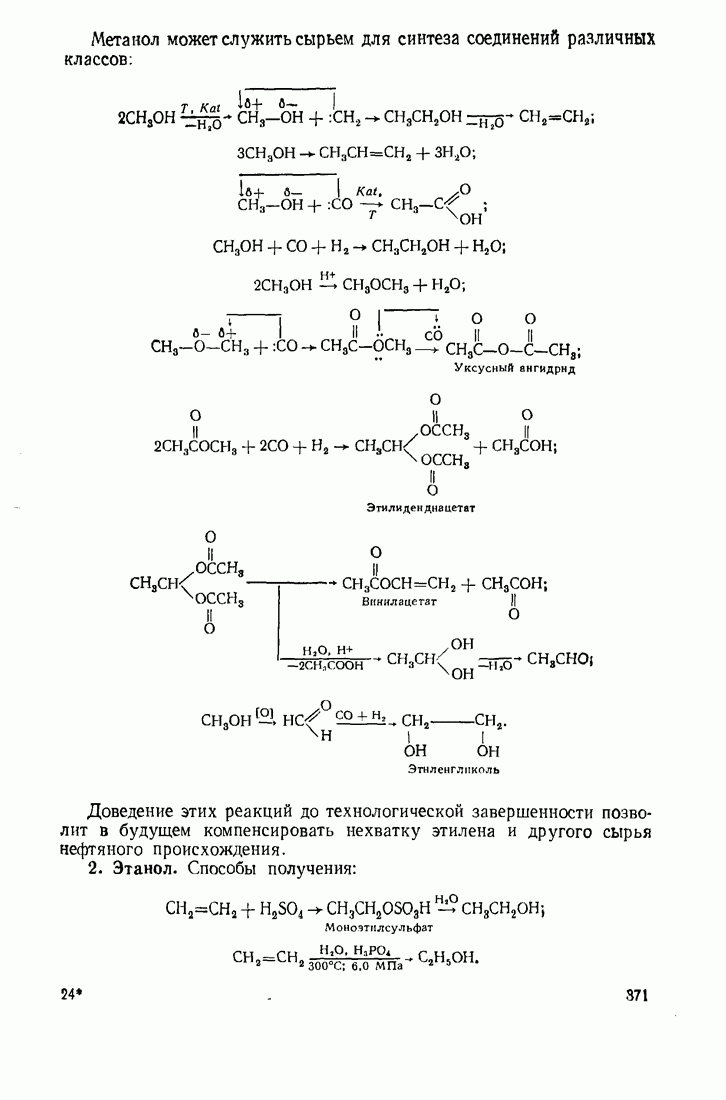
- 12.2. ПУТИ ИСПОЛЬЗОВАНИЯ УГЛЕВОДОРОДОВ И ИХ ПРОИЗВОДНЫХ
- 12.3. РАЗВИТИЕ ХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИ В СССР В ДВЕНАДЦАТОЙ ПЯТИЛЕТКЕ