| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
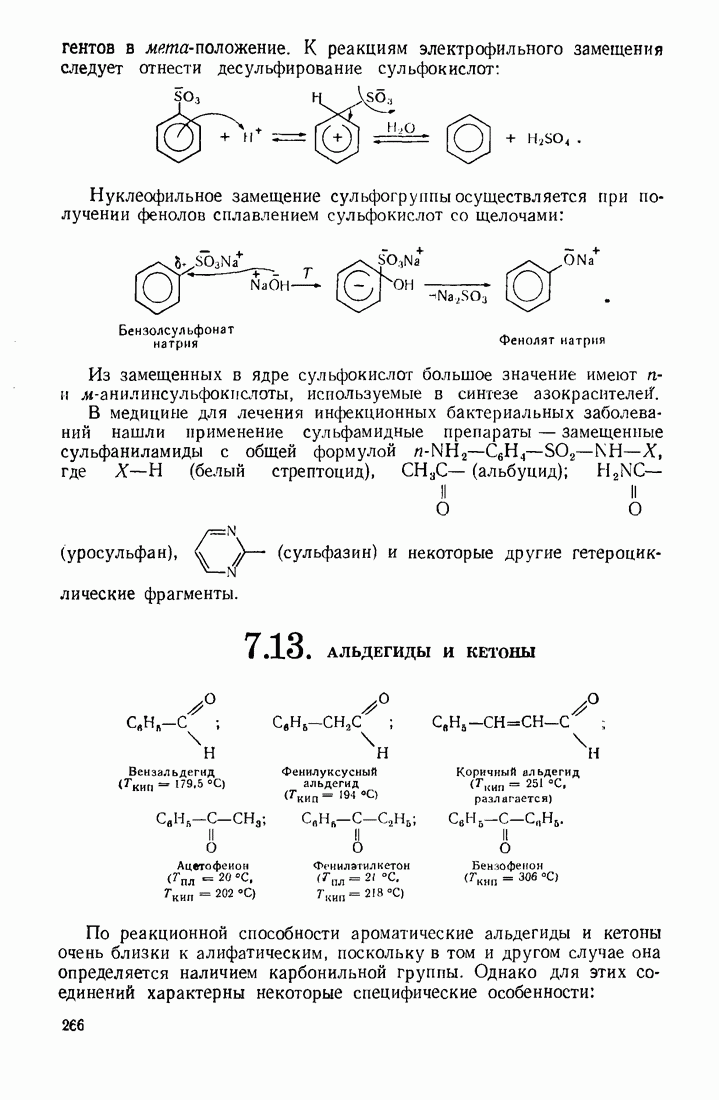
3.9. АЛЬДЕГИДЫ И КЕТОНЫ


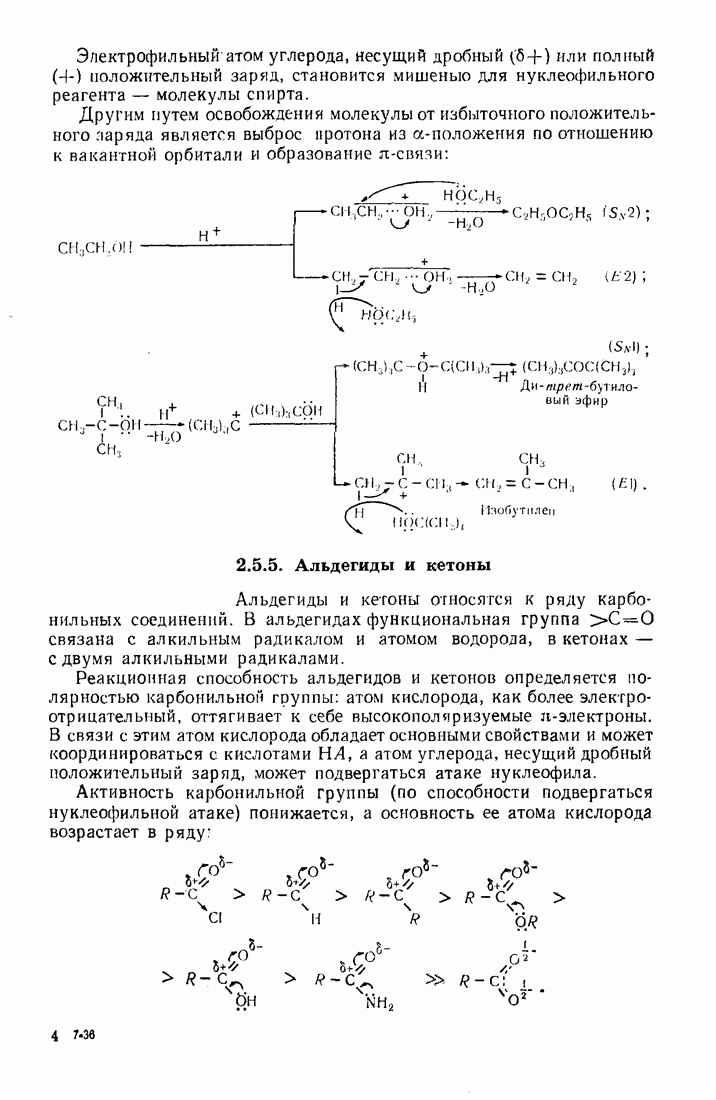
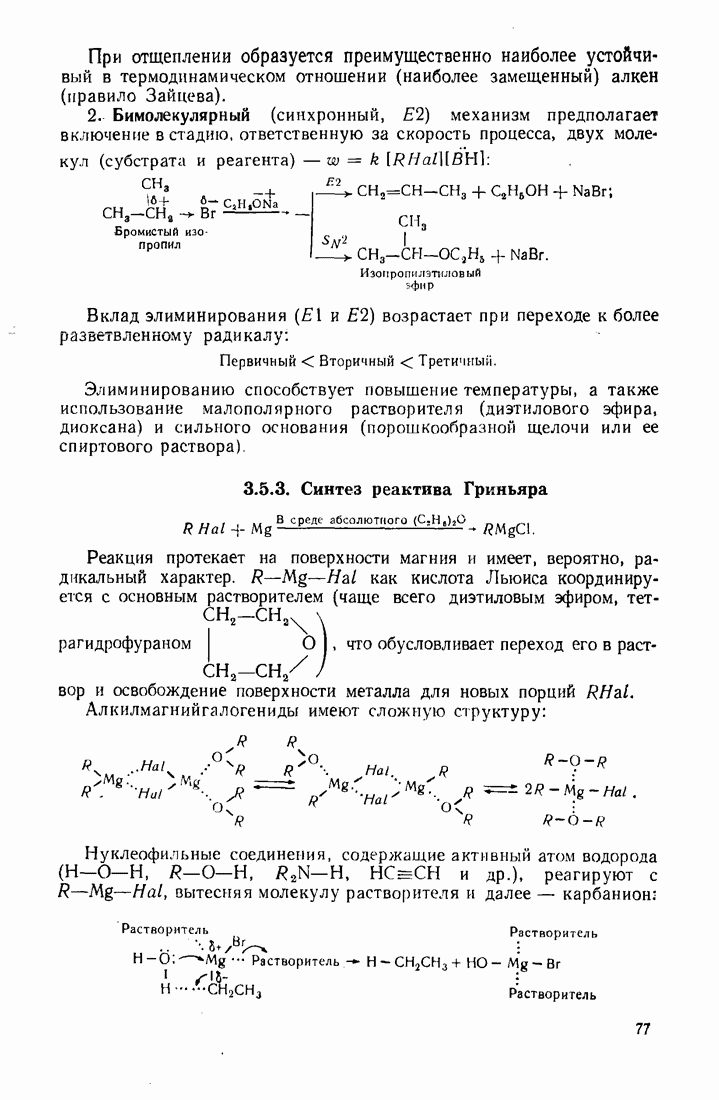
Реакционная способность альдегидов и кетонов обусловлена полярной карбонильной группой и подвижностью атомов водорода в  -положении:
-положении:  Альдегиды и кетоны относятся к числу наиболее активных карбонильных соединений (см. п. 2.5.5), уступая в полярности карбонильной группы лишь галогенангидридам кислот.
Альдегиды и кетоны относятся к числу наиболее активных карбонильных соединений (см. п. 2.5.5), уступая в полярности карбонильной группы лишь галогенангидридам кислот.
Наиболее типичными для альдегидов являются реакции нуклеофильного присоединения по карбонильной группе, которые подвержены кислотному или основному катализу. Кислота - катализатор координируется по атому кислорода карбонильной группы, несущему дробный отрицательный заряд, усиливает поляризацию карбонильной группы и облегчает атаку нуклеофила. Основание - катализатор повышает активность реагента, образуя на его основе нуклеофильную частицу:

Реакции альдегидов и кетонов можно разделить на три группы 1) с истинными основаниями; 2) о нсевдокислотами; 3) с криптооснованиями.
3.9.1. Реакции с основаниями
Основания, или нуклеофильные реагенты  гидросульфит натрия
гидросульфит натрия  гидразин
гидразин  гидроксиламин
гидроксиламин  фенилпроизводные аммиака, гидразина, гидроксиламина и др.
фенилпроизводные аммиака, гидразина, гидроксиламина и др.
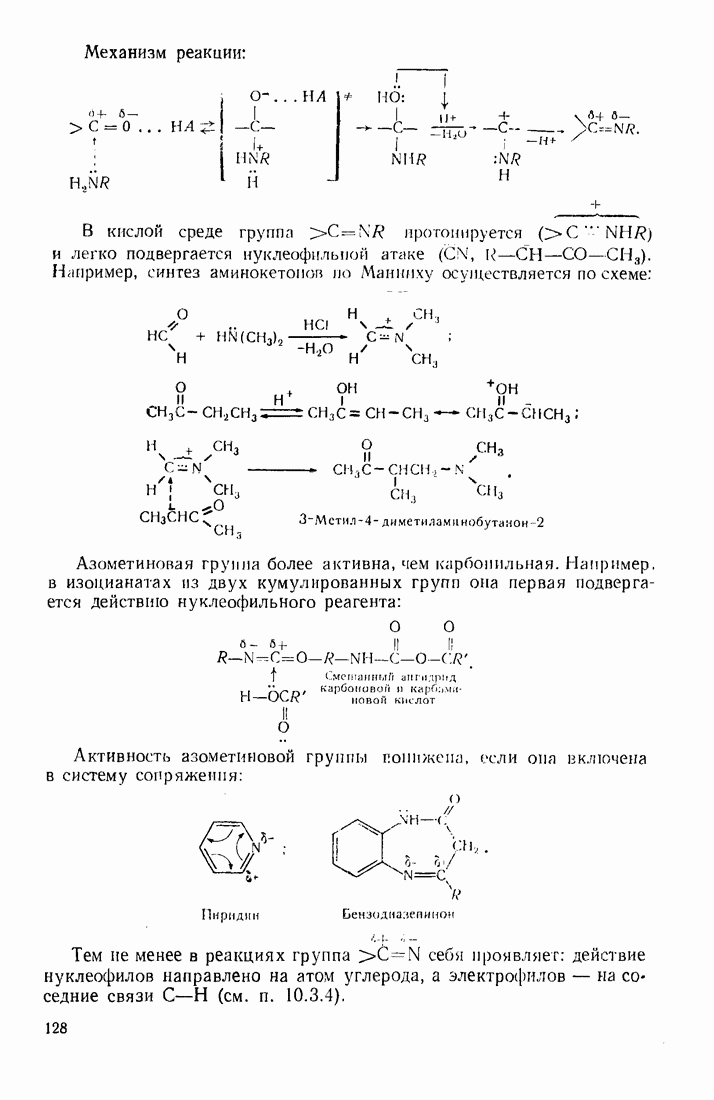
Обычно реакции с основаниями катализируются кислотами. Общий механизм реакций с основаниями:

Далее возможны более глубокие превращения, связанные с протонизацией групы  и отщеплением воды
и отщеплением воды
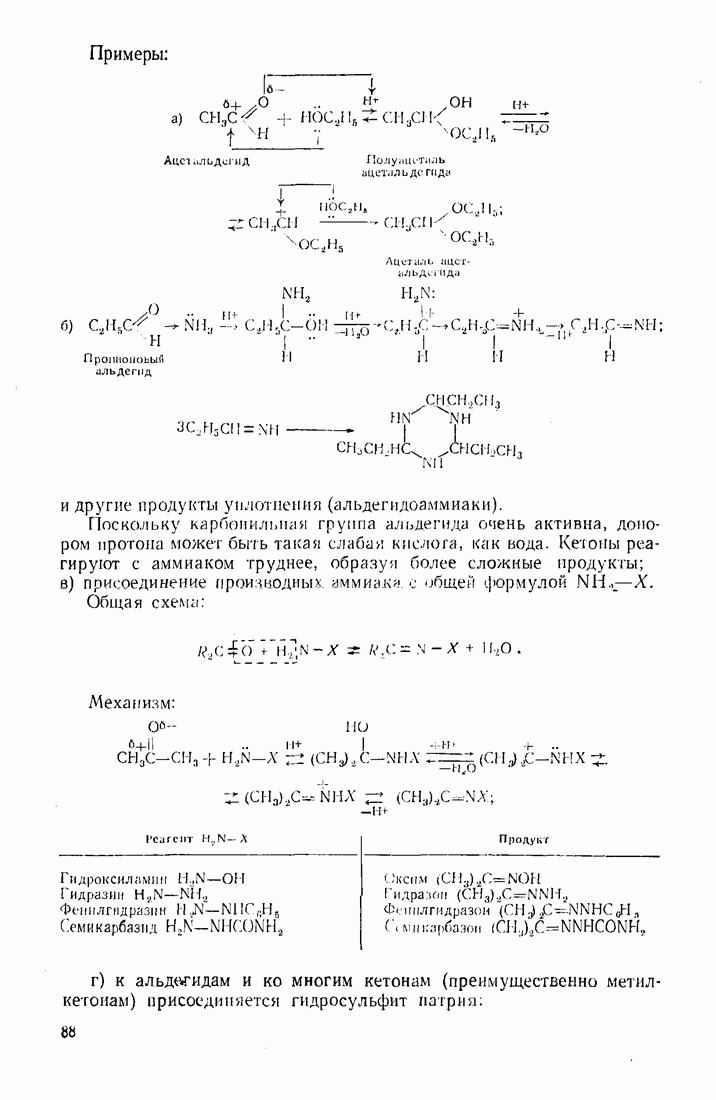
Примеры:
(см. скан)
и другие продукты уплотнения (альдегидоаммиаки).
Поскольку карбонильная группа альдегида очень активна, донором протона может быть такая слабая кислота, как вода. Кетоны реагируют с аммиаком труднее, образуя более сложные продукты; в) присоединение производных, аммиака, о общей формулой 
Общая схема:

Механизм:
(см. скан)
г) к альдегидам и ко многим кетонам (преимущественно метил-кетонам) присоединяется гидросульфит натрия:

Кетоны с объемными радикалами в реакцию не вступают в связи с пространственными препятствиями.
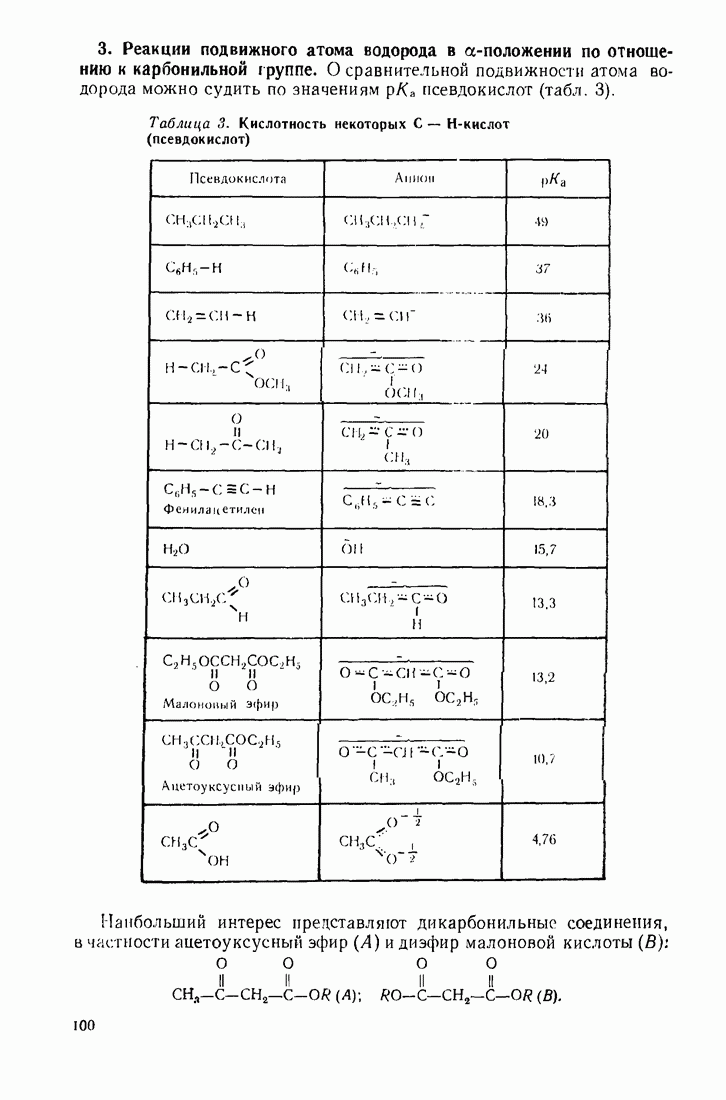
3.9.2. Реакции с псевдокислотами
Псевдокислоты (слабые кислоты) — это соединения, способные при взаимодействии с сильными основаниями отщеплять протон и генерировать нуклеофильиую частицу: синильная кислота  ацетилен
ацетилен  альдегиды, кетоны, нитроалканы и другие
альдегиды, кетоны, нитроалканы и другие  -кислоты.
-кислоты.

В альдегидах и кетопах протон отщепляется лишь из  -положения, так как остающаяся пара электронов стабилизируется за счет сопряжения
-положения, так как остающаяся пара электронов стабилизируется за счет сопряжения  карбонильной группой. Поскольку аннон всегда спарен с катионом (или протоном), енольную форму альдегидов и кетонов можно рассматривать как нуклеофил с двумя реакционными центрами: на атомах углерода (центр наиболее высокой поляризуемости) и кислорода — центр наибольшей электронной плотности:
карбонильной группой. Поскольку аннон всегда спарен с катионом (или протоном), енольную форму альдегидов и кетонов можно рассматривать как нуклеофил с двумя реакционными центрами: на атомах углерода (центр наиболее высокой поляризуемости) и кислорода — центр наибольшей электронной плотности:

Енолизации способствуют как кислоты, так и основания-:

Примеры:

(см. скан)
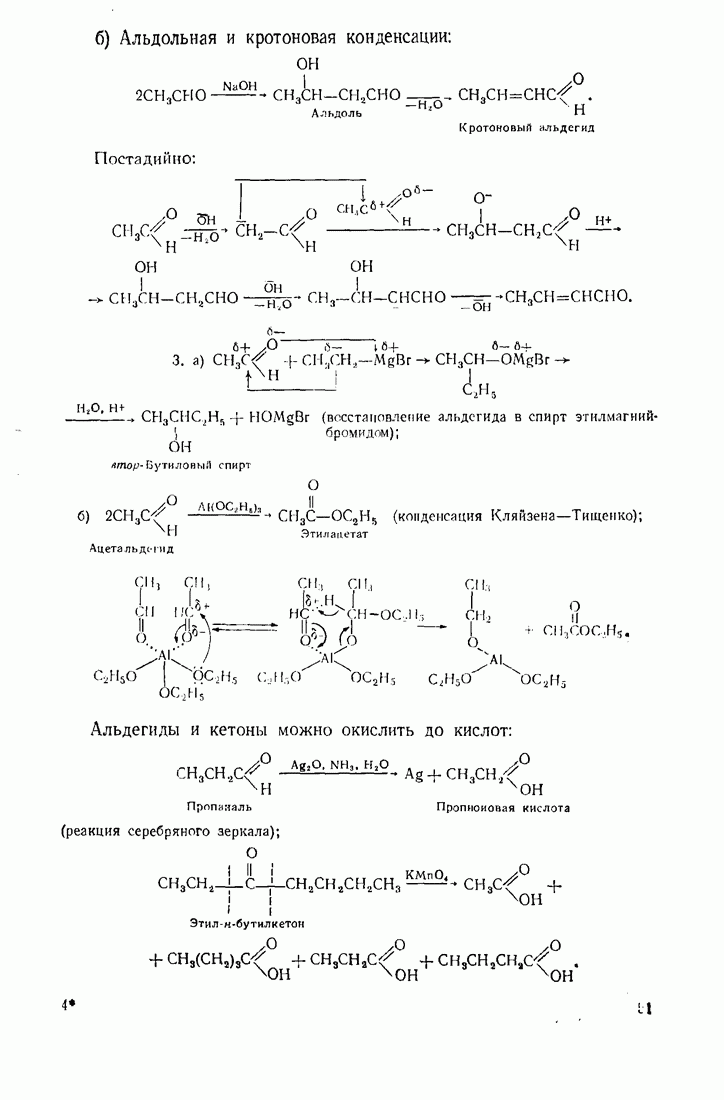
в) альдольная конденсация:
(см. скан)
Атомы водорода группы  в альдоле еще более подвижны, чем в альдегиде, так как они находятся между двумя акцепторами. Вследствие этого легко протекает кротоновая конденсация:
в альдоле еще более подвижны, чем в альдегиде, так как они находятся между двумя акцепторами. Вследствие этого легко протекает кротоновая конденсация:

3.9.3. Реакции с криптооснованиями
Криптооснования (или скрытые основания) проявляют основные свойства лишь в ходе реакции и способны отдавать пару электронов с протоном или группой атомов в виде гидрид-аниона  карбаниона
карбаниона  алкоксианиона
алкоксианиона  . К этому ряду соединений относятся гидриды металлов
. К этому ряду соединений относятся гидриды металлов  и др.), алкоголяты металлов
и др.), алкоголяты металлов  магнийорганические
магнийорганические  и другие элемеитоорганическпе соединения.
и другие элемеитоорганическпе соединения.
Анионы  как кинетически самостоятельные частицы, в растворе не существуют и передаются от реагента к субстрату в хелатных (циклических) комплексах.
как кинетически самостоятельные частицы, в растворе не существуют и передаются от реагента к субстрату в хелатных (циклических) комплексах.
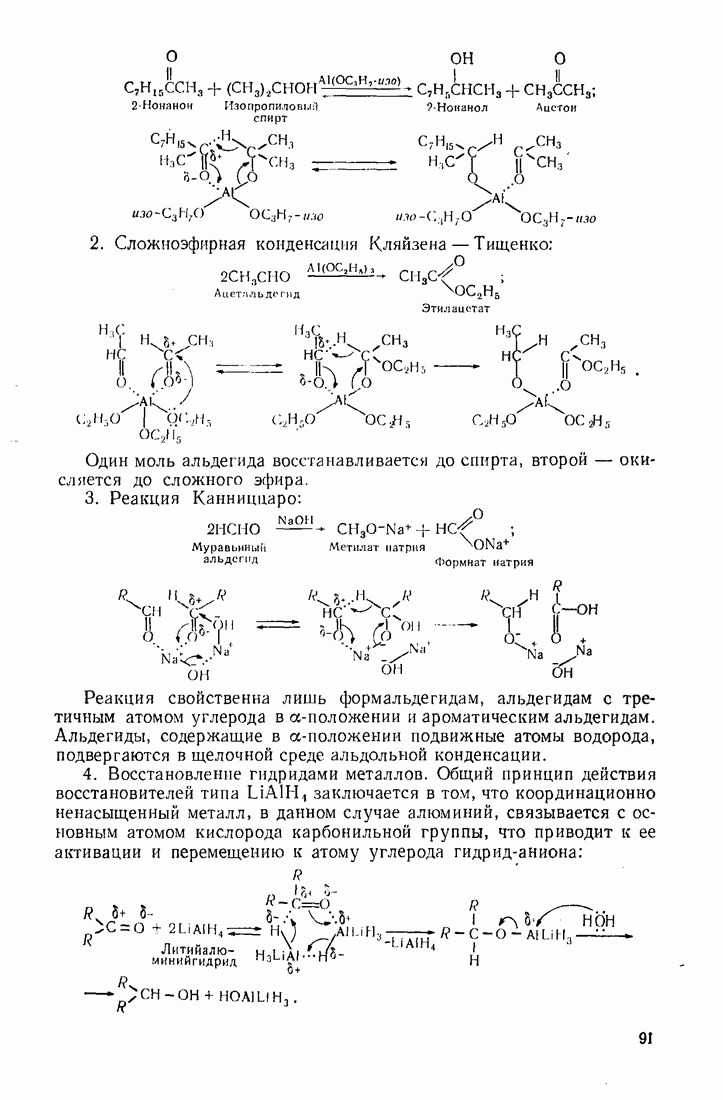
1. Реакция восстановления кетонов алкоголятами металлов по Меервейну-Понидорфу. Общая схема:

(см. скан)
2. Сложноэфирная конденсация Кляйзена — Тищенко:
(см. скан)
Один моль альдегида восстанавливается до спирта, второй — окисляется до сложного эфира.
3. Реакция Канниццаро:
(см. скан)
Реакция свойственна лишь формальдегидам, альдегидам с третичным атомом углерода в  -положении и ароматическим альдегидам. Альдегиды, содержащие в
-положении и ароматическим альдегидам. Альдегиды, содержащие в  -положении подвижные атомы водорода, подвергаются в щелочной среде альдольной конденсации.
-положении подвижные атомы водорода, подвергаются в щелочной среде альдольной конденсации.
4. Восстановление гидридами металлов. Общий принцип действия восстановителей типа  заключается в том, что координационно ненасыщенный металл, в данном случае алюминий, связывается с основным атомом кислорода карбонильной группы, что приводит к ее активации и перемещению к атому углерода гидрид-аниона:
заключается в том, что координационно ненасыщенный металл, в данном случае алюминий, связывается с основным атомом кислорода карбонильной группы, что приводит к ее активации и перемещению к атому углерода гидрид-аниона:
(см. скан)
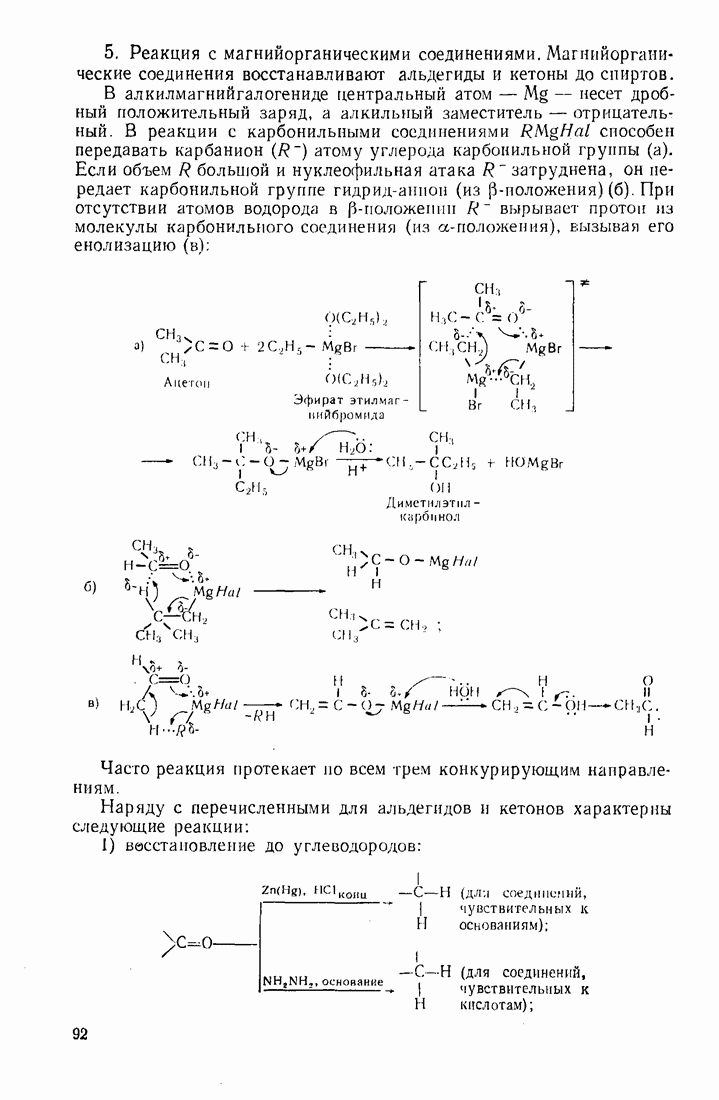
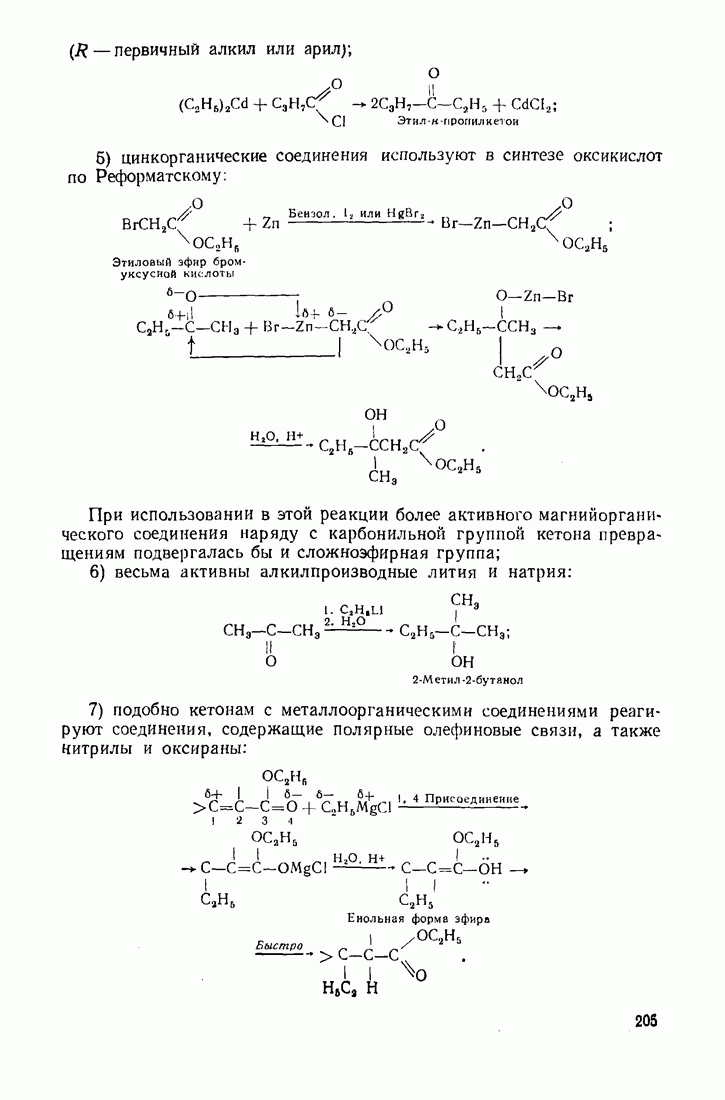
5. Реакция с магнийоргаиическими соединениями. Магнийорганические соединения восстанавливают альдегиды и кетоны до спиртов.
В алкилмагнийгалогениде центральный атом —  несет дробный положительный заряд, а алкильный заместитель — отрицательный. В реакции с карбонильными соединениями
несет дробный положительный заряд, а алкильный заместитель — отрицательный. В реакции с карбонильными соединениями  способен передавать карбанион
способен передавать карбанион  атому углерода карбонильной группы (а). Если объем
атому углерода карбонильной группы (а). Если объем  большой и нуклеофильная атака
большой и нуклеофильная атака  затруднена, он передает карбонильной группе гидрид-анион (из
затруднена, он передает карбонильной группе гидрид-анион (из  -положения) (б). При отсутствии атомов водорода в
-положения) (б). При отсутствии атомов водорода в  -положении
-положении  вырывает протон из молекулы карбонильного соединения (из
вырывает протон из молекулы карбонильного соединения (из  -положения), вызывая его енолизацию (в);
-положения), вызывая его енолизацию (в);
(см. скан)
Часго реакция протекает по всем трем конкурирующим направлениям.
Наряду с перечисленными для альдегидов и кетонов характерны следующие реакции:
1) восстановление до углеводородов:

2) восстановление в спирты:

3) окисление:

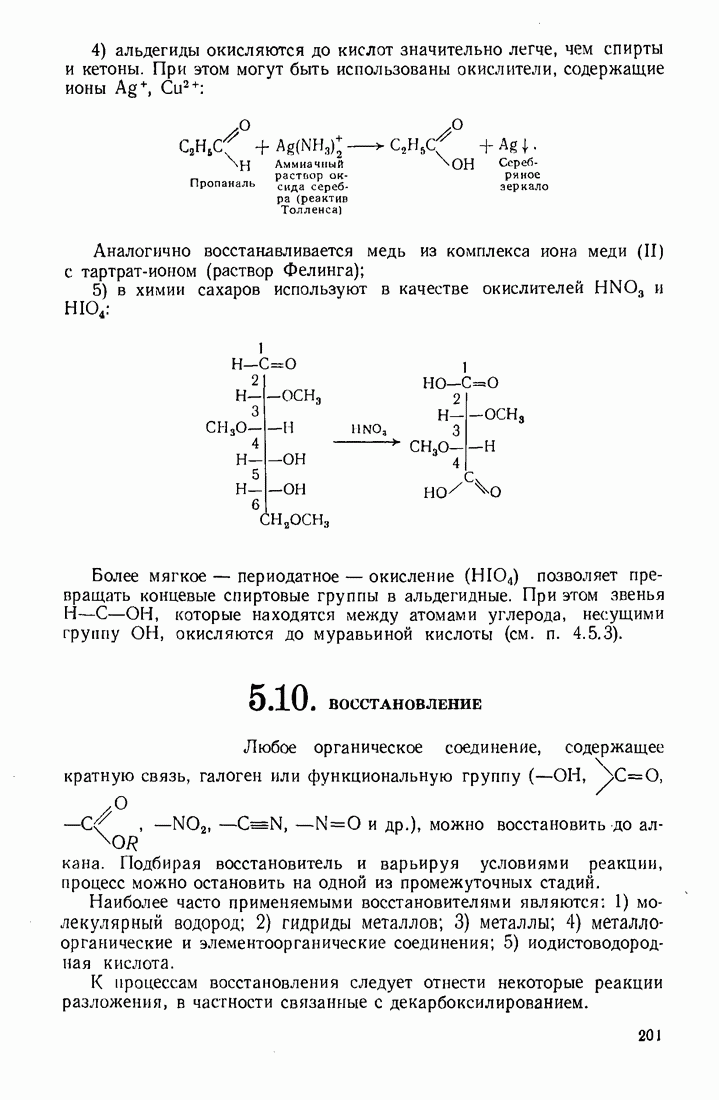
Окисление альдегидов аммиачным раствором оксида серебра (II) называется реакцией серебряного зеркала (проба Толленса). Кетоны в таких условиях не окисляются. Например:

Кетоны окисляются только сильными окислителями при нагревании. Перманганат калия окисляет кетоны с разрывом углеродной цепи по обе стороны карбонпла. При разных радикалах  образуется смесь четырех кислот:
образуется смесь четырех кислот:

4) полимеризация низших представителей альдегидов (муравьиного и уксусного):

| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. Введение
- 1.1. Предмет органической химии
- 1.2. Основные этапы развития органической химии
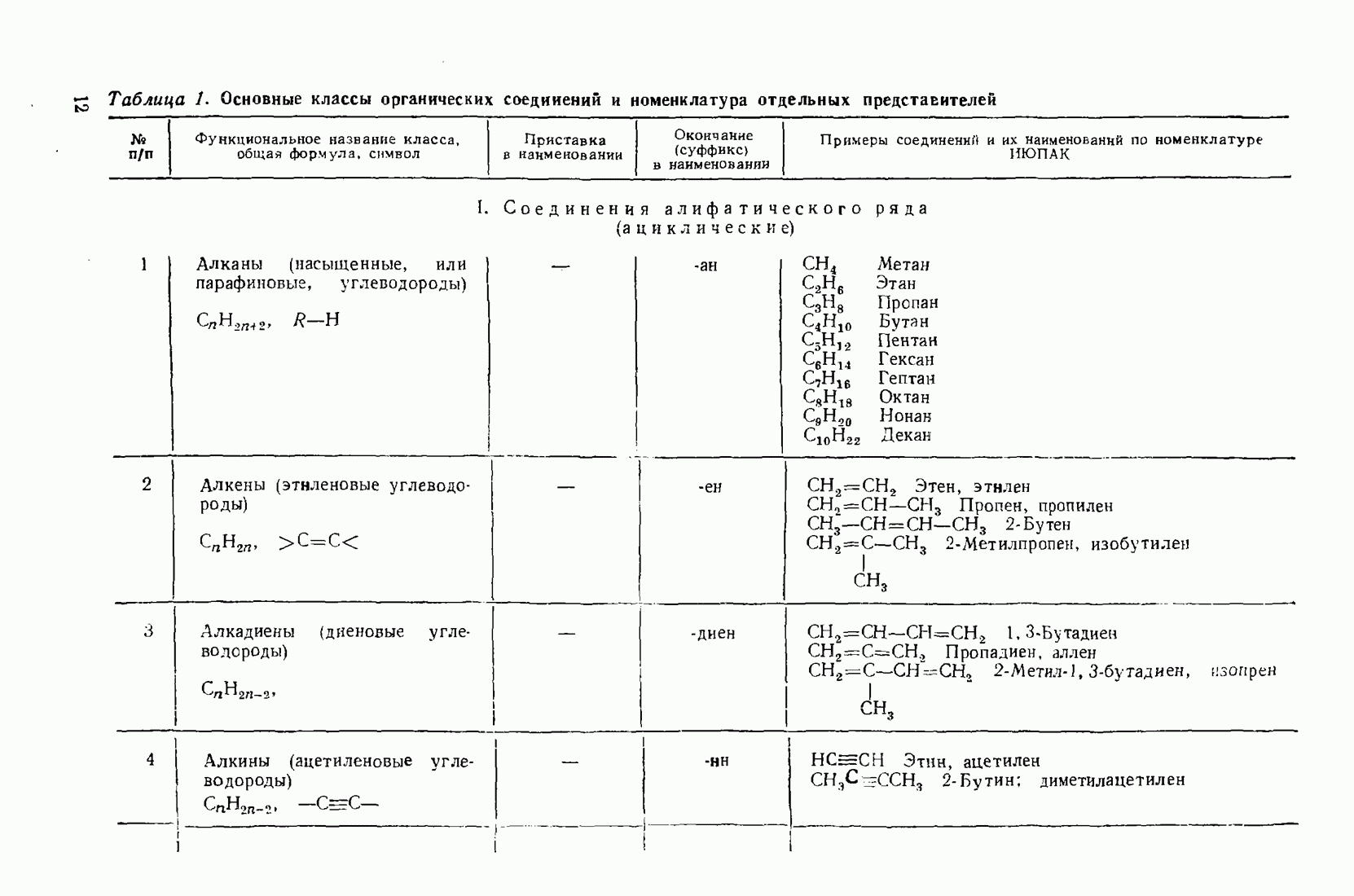
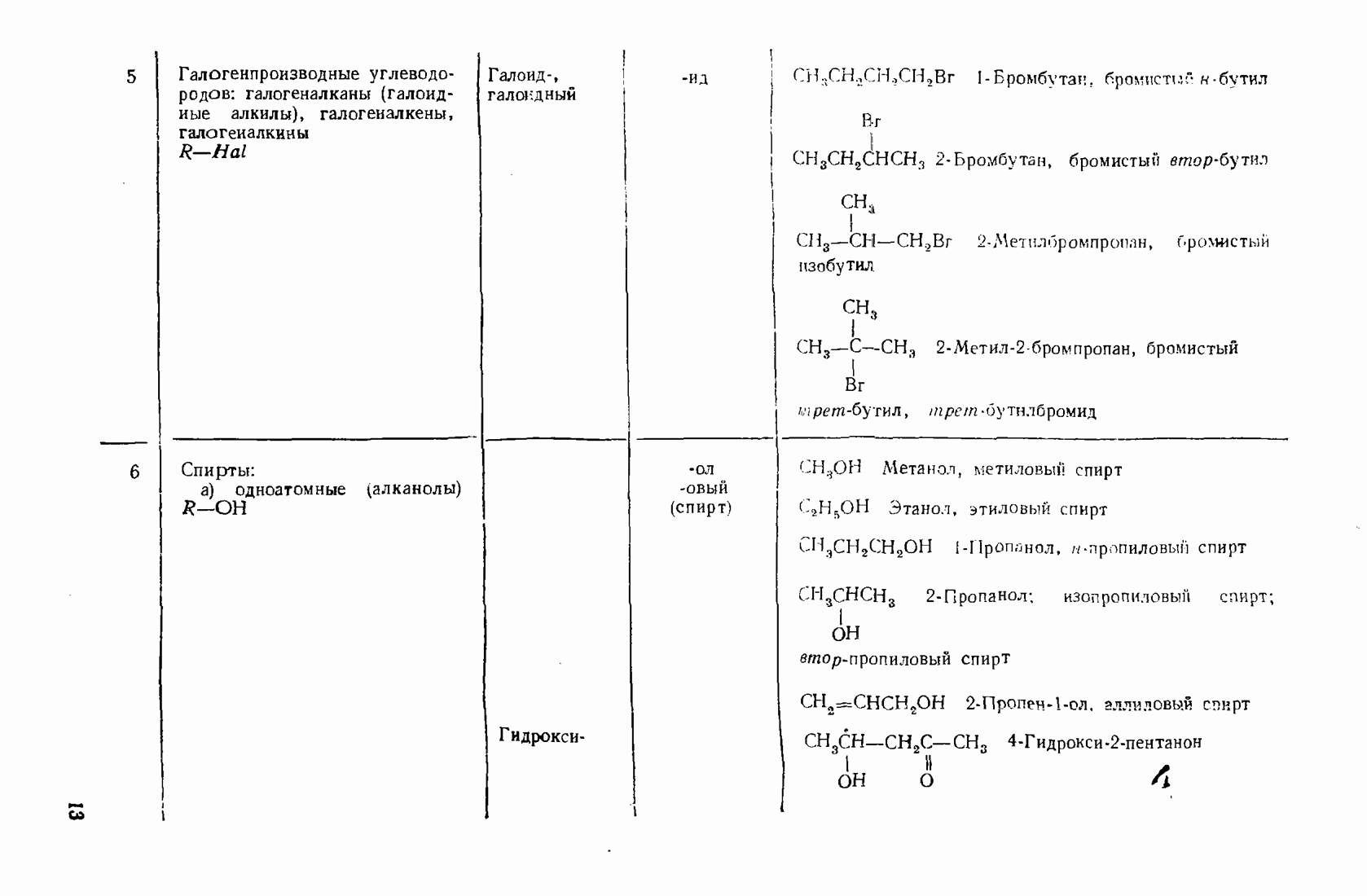
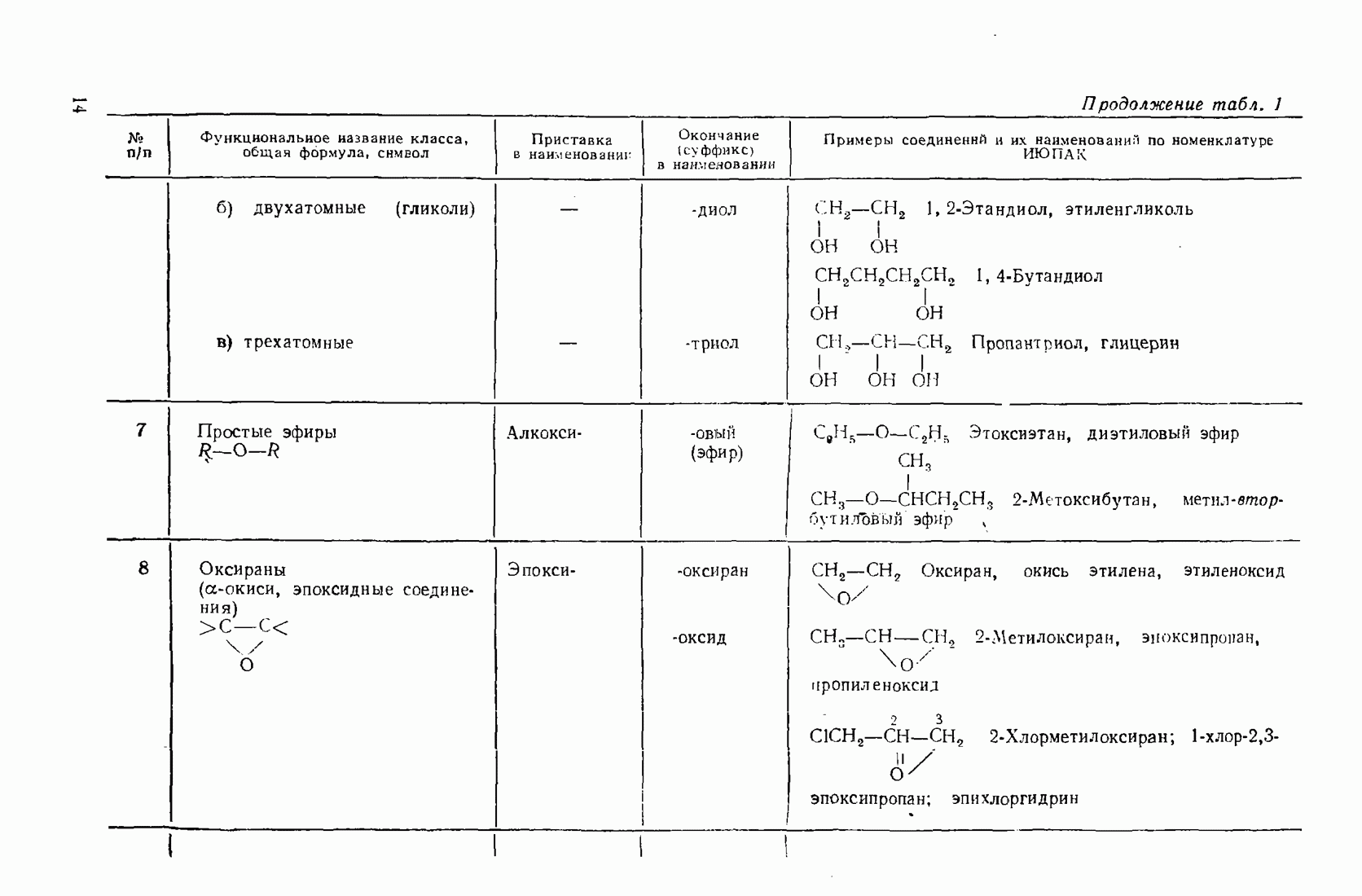
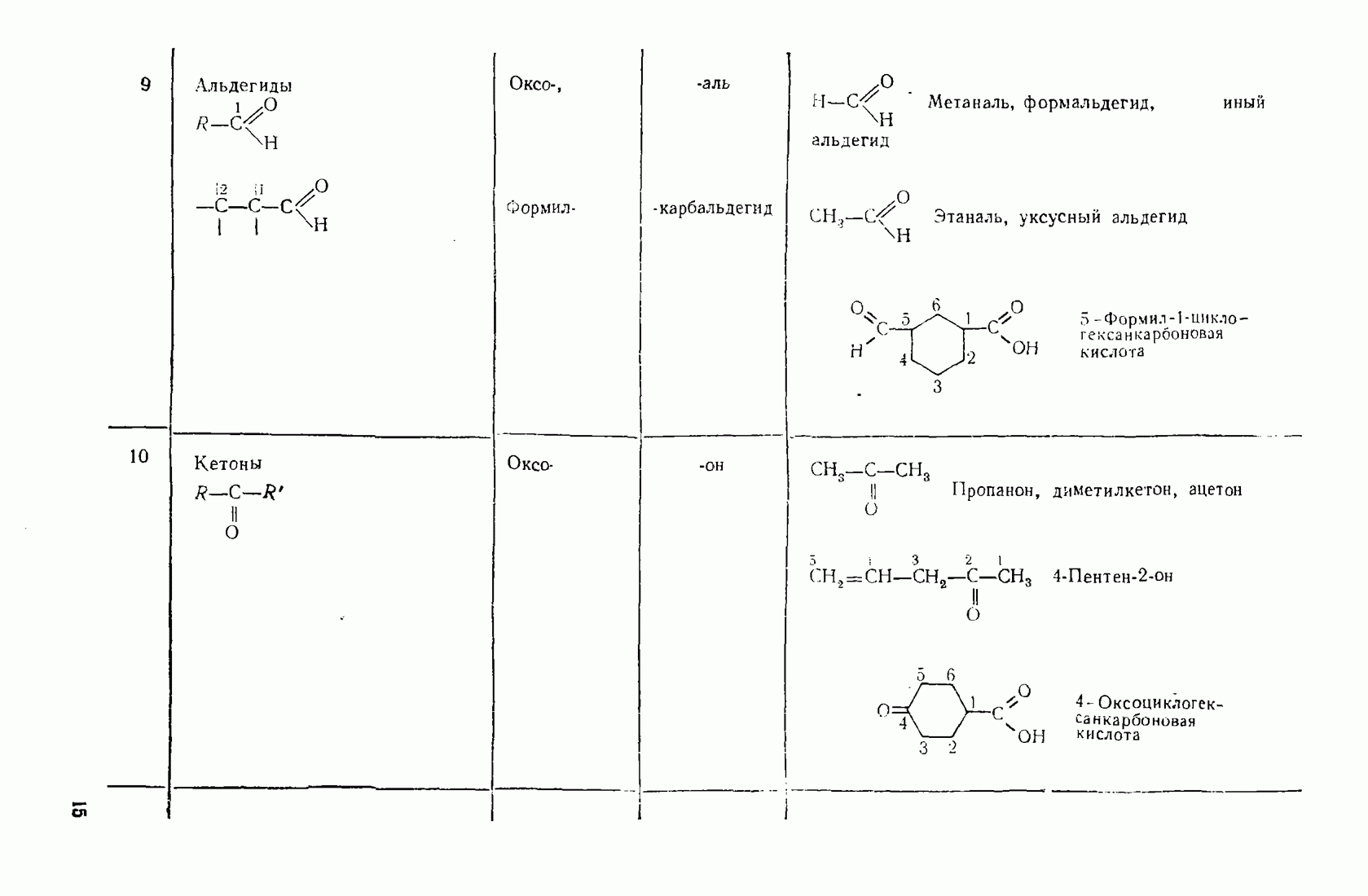
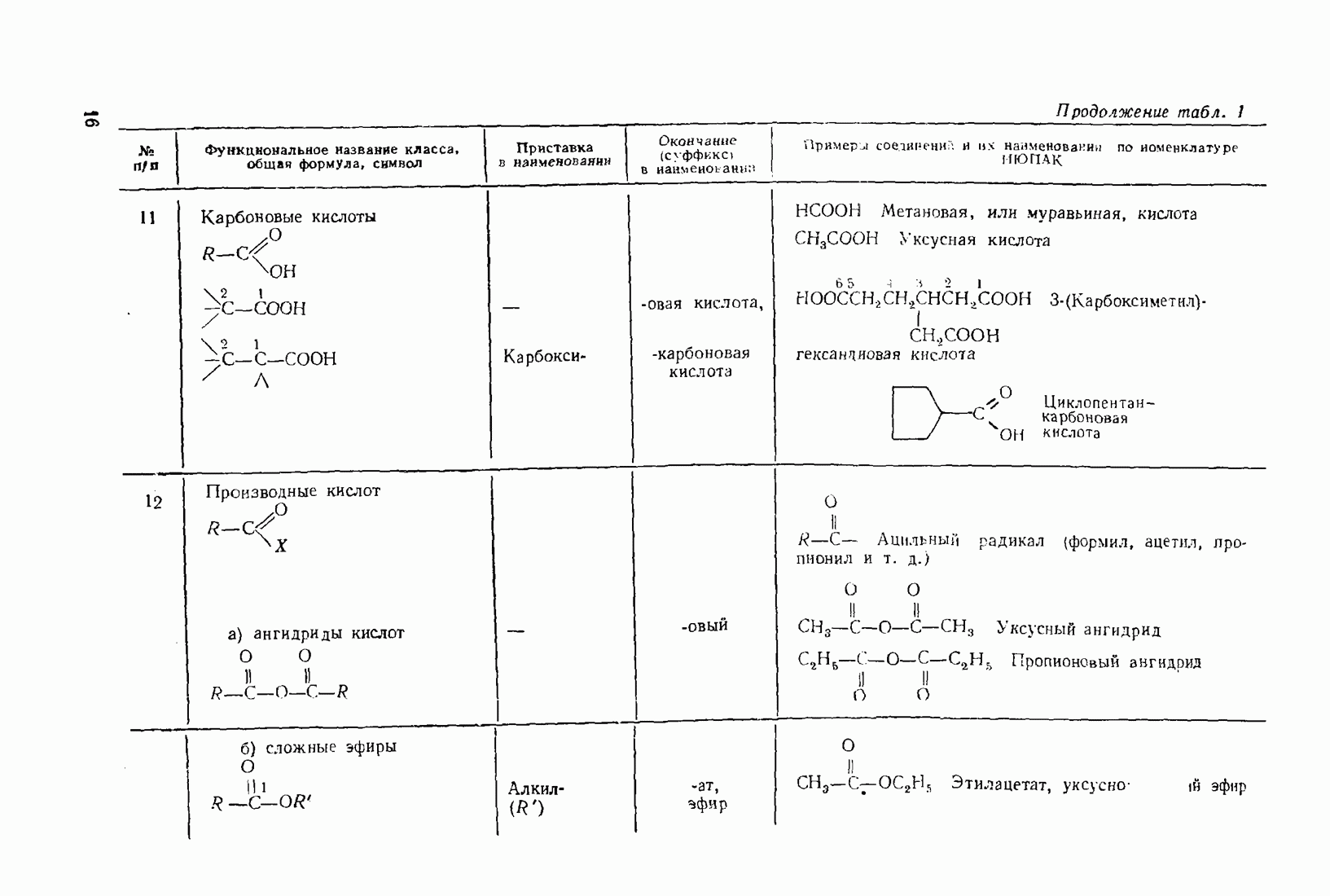
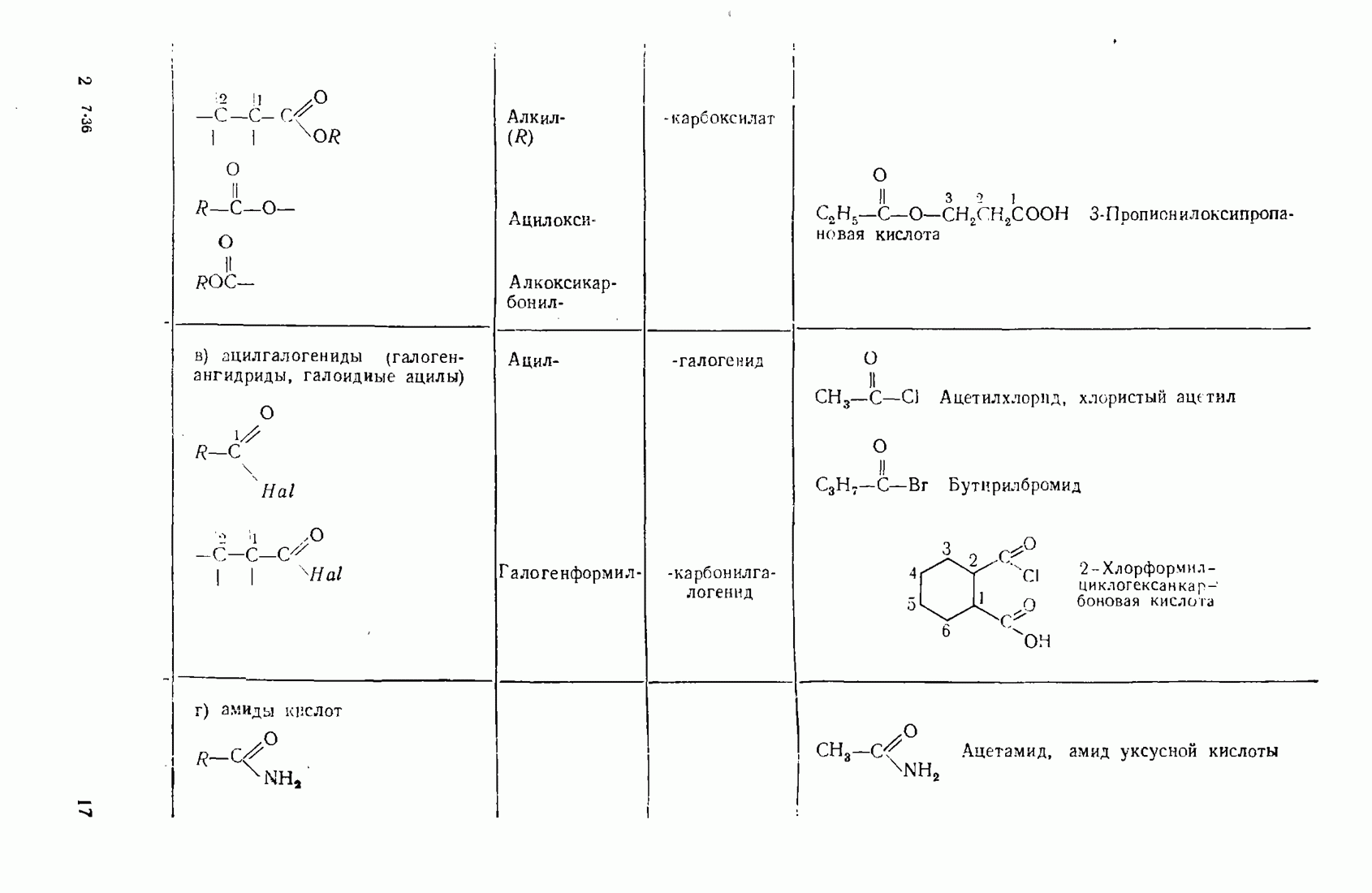
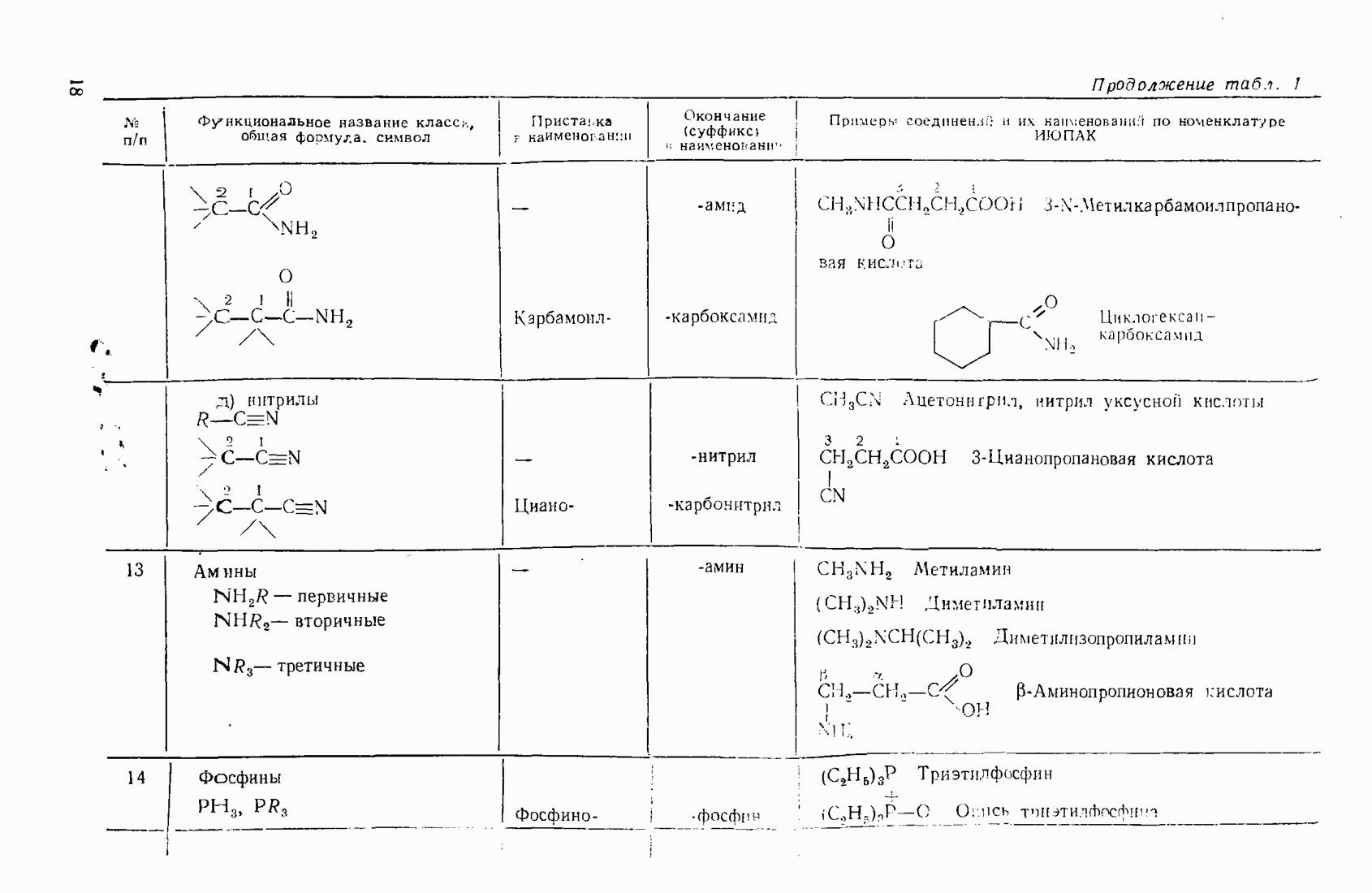
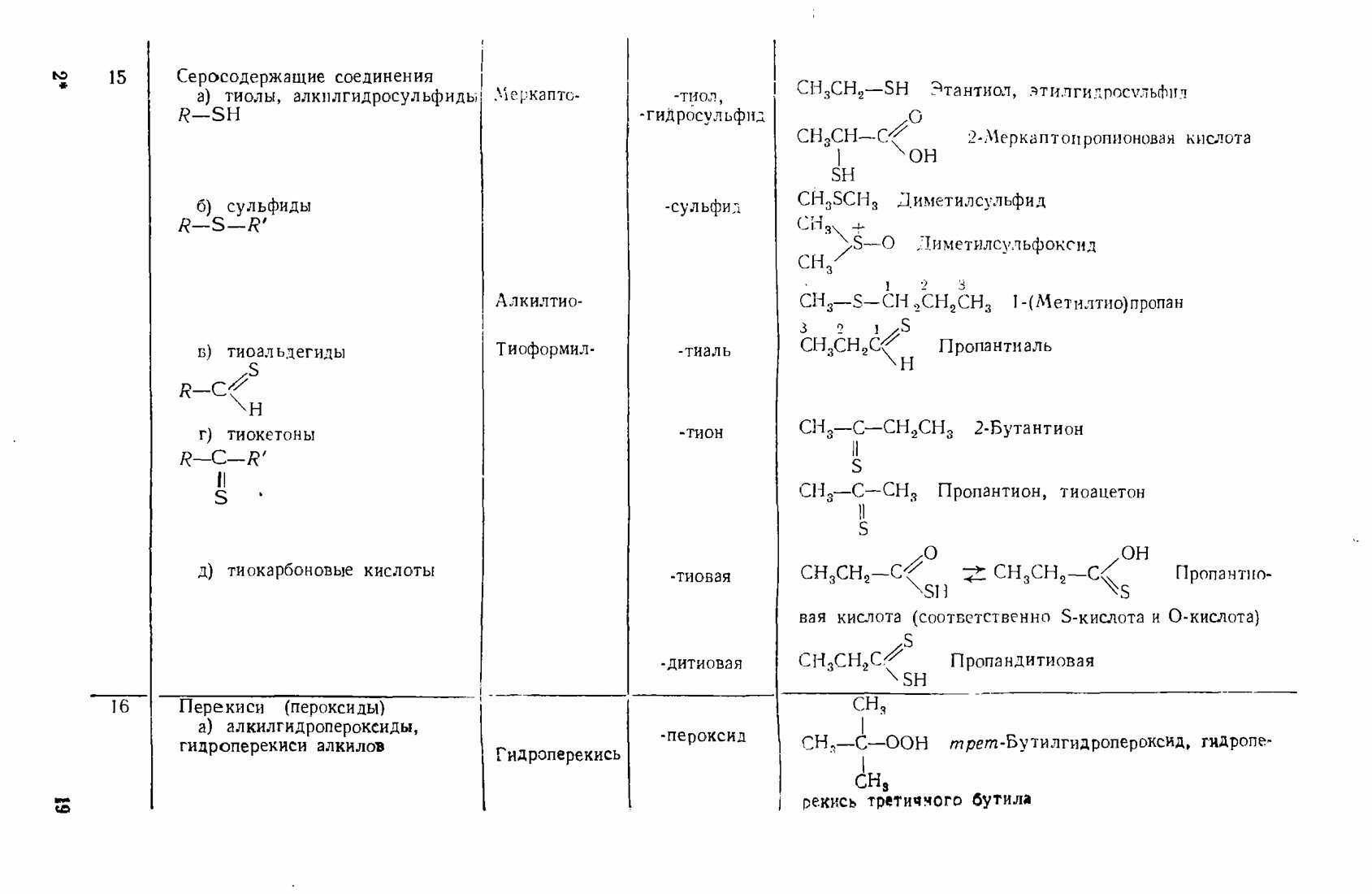
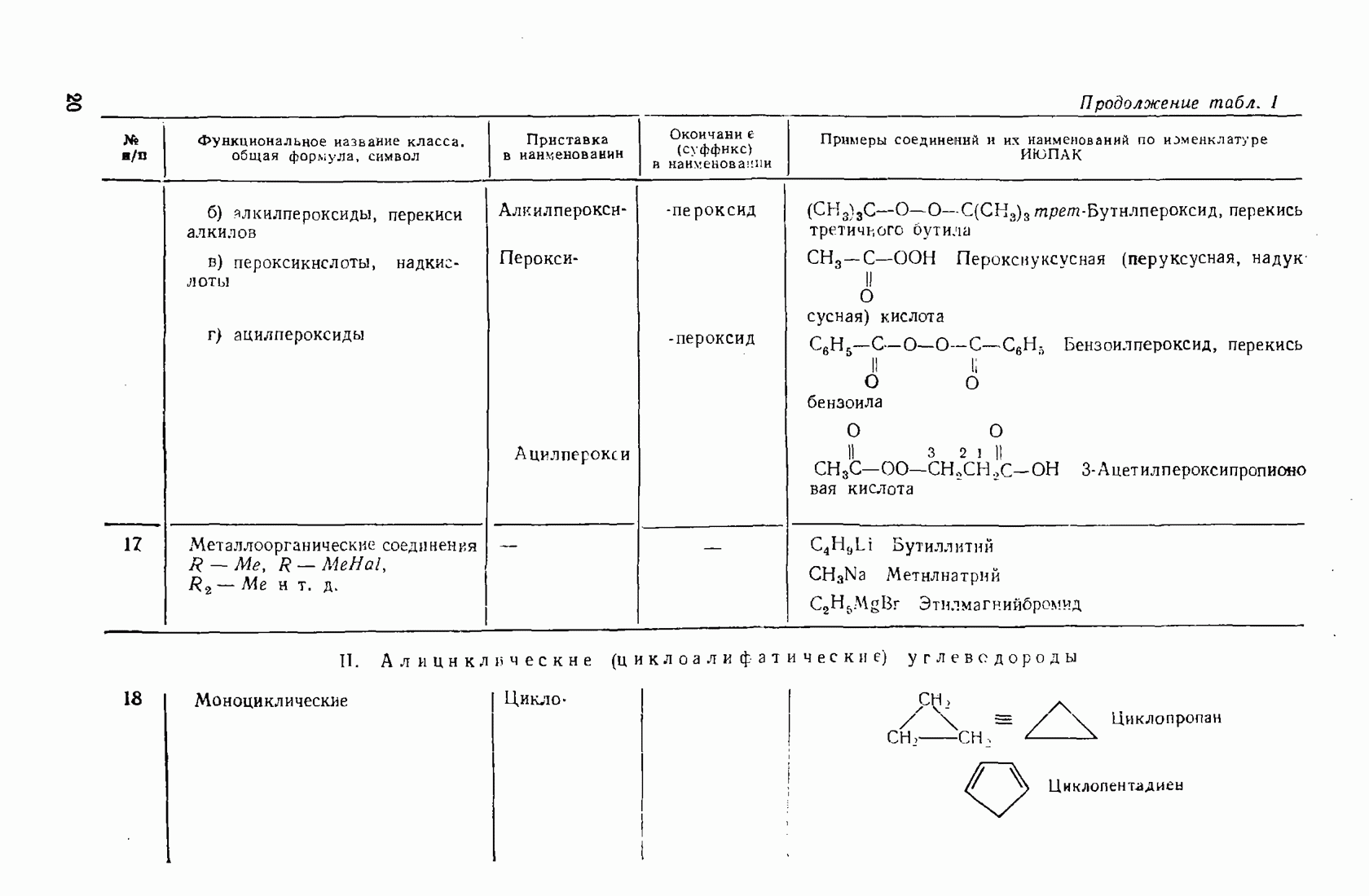
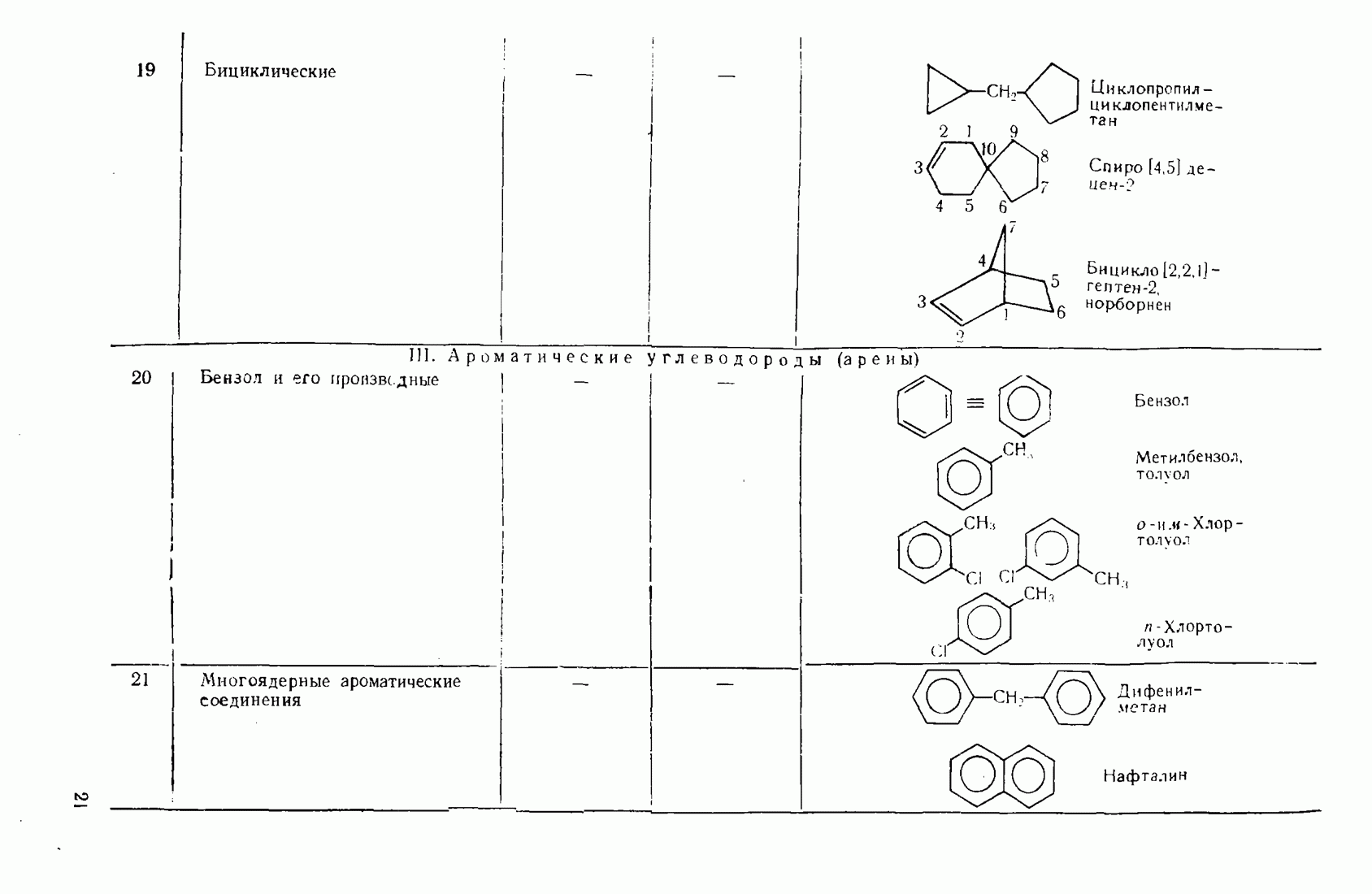
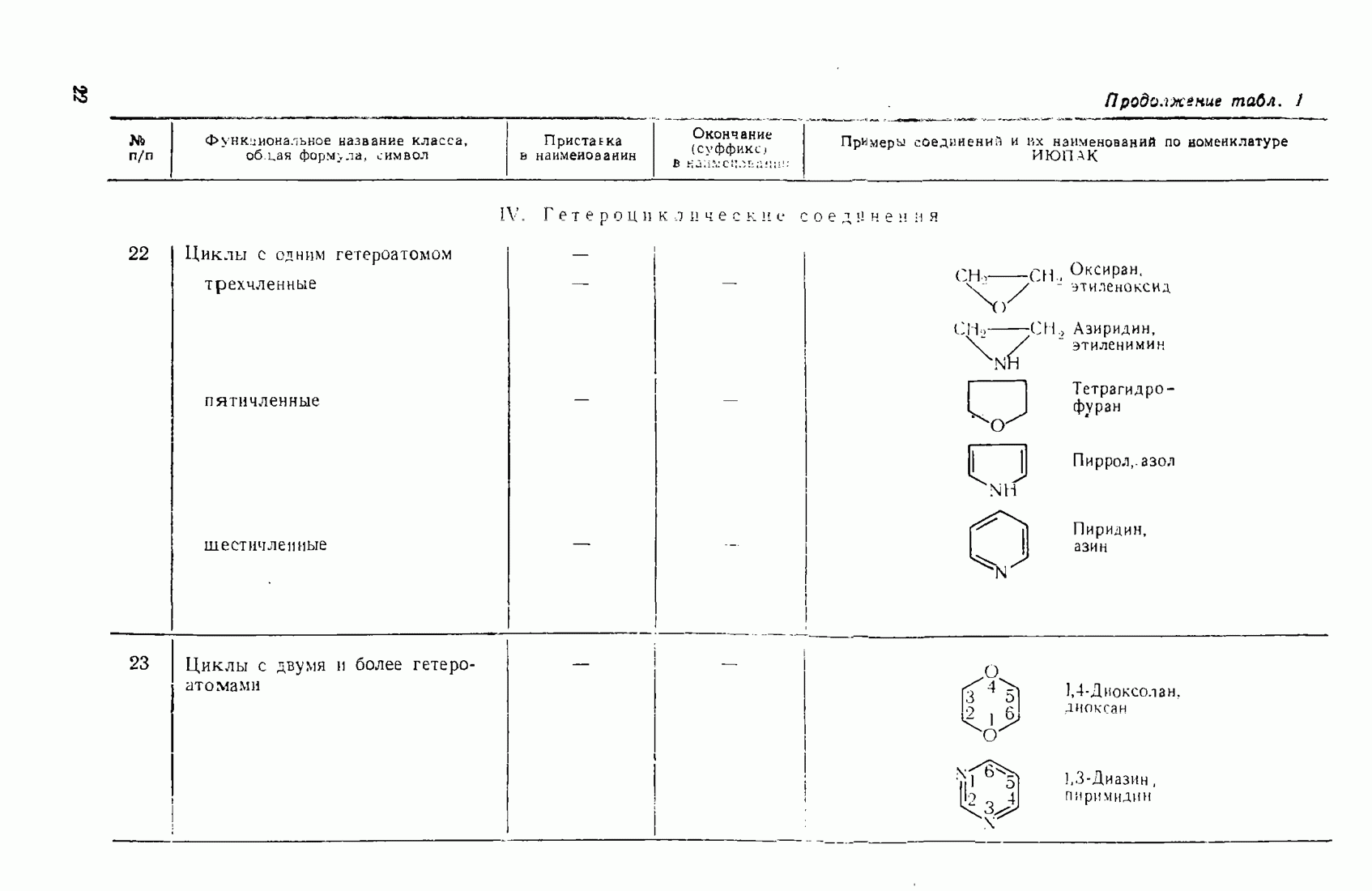
- 1.3. Классификация и номенклатура органических соединений
- 2 Общие теоретические положения органической химии
- 2.1. Природа химической связи
- 2.1.1. Типы химических связей
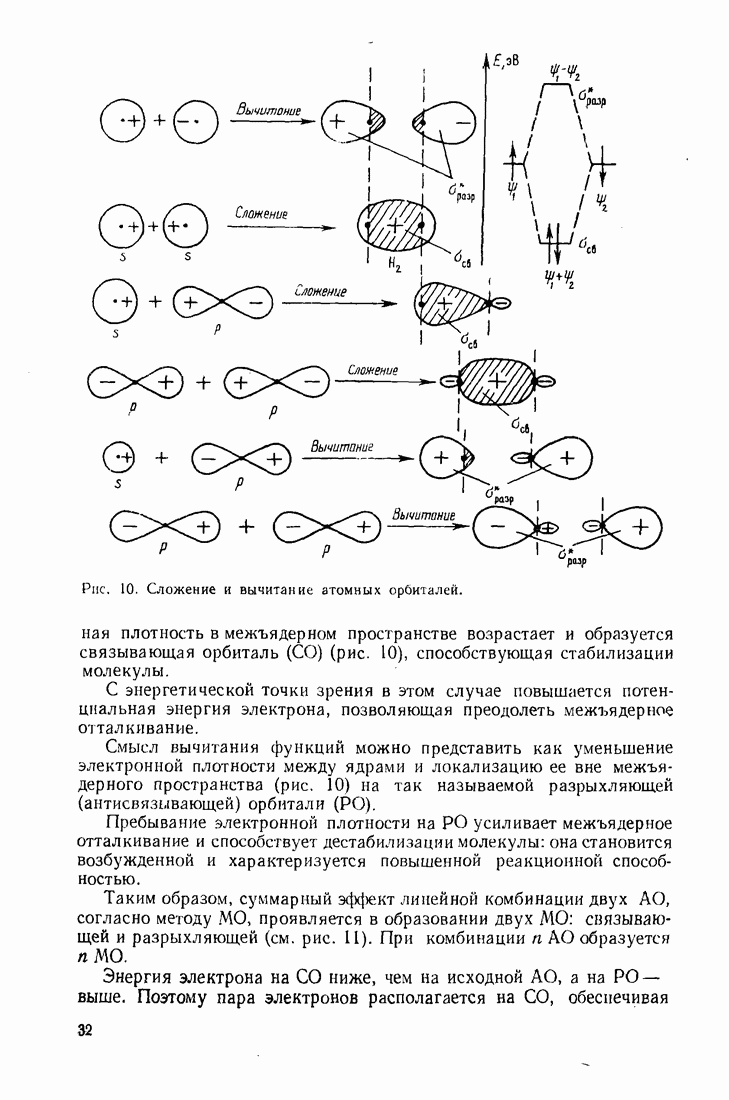
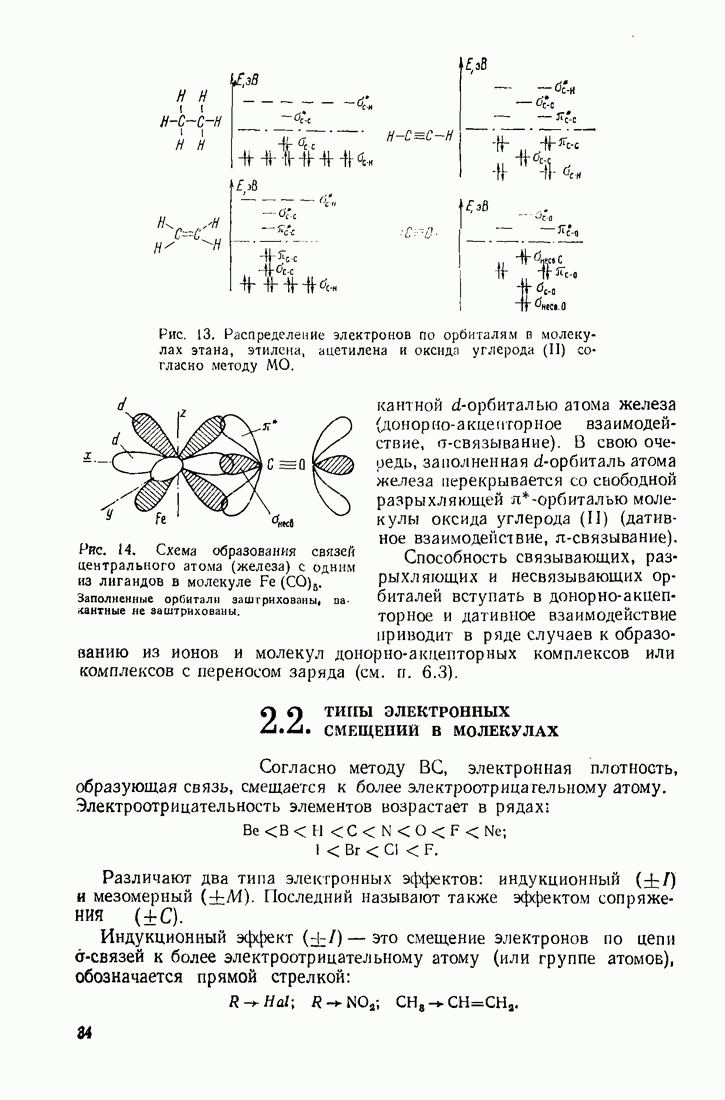
- 2.1.2. Молекулярные орбитали
- 2.2. ТИПЫ ЭЛЕКТРОННЫХ СМЕЩЕНИЙ В МОЛЕКУЛАХ
- 2.3. ОБЩИЕ ПРЕДСТАВЛЕНИЯ ОБ ОРГАНИЧЕСКОЙ РЕАКЦИИ
- 2.4. КЛАССИФИКАЦИЯ РЕАГЕНТОВ И РЕАКЦИЙ
- 2.5. КРАТКАЯ ХАРАКТЕРИСТИКА РЕАКЦИОННОЙ СПОСОБНОСТИ НЕКОТОРЫХ СОЕДИНЕНИЙ АЛИФАТИЧЕСКОГО РЯДА
- 2.5.1. Алканы (парафины)
- 2.5.2. Непредельные углеводороды
- 2.5.3. Галогеналканы (галоидные алкилы R-Hal)
- 2.5.4. Спирты (R0Н)
- 2.5.5. Альдегиды и кетоны
- 2.5.6. Карбоновые кислоты (R-СООН) и их производные (R-СО-X)
- 2.5.7. Амины (NH2R, NHR2, NR3)
- 3. Реакционная способность соединений алифатического ряда
- 3.1. Алканы (насыщенные углеводороды)
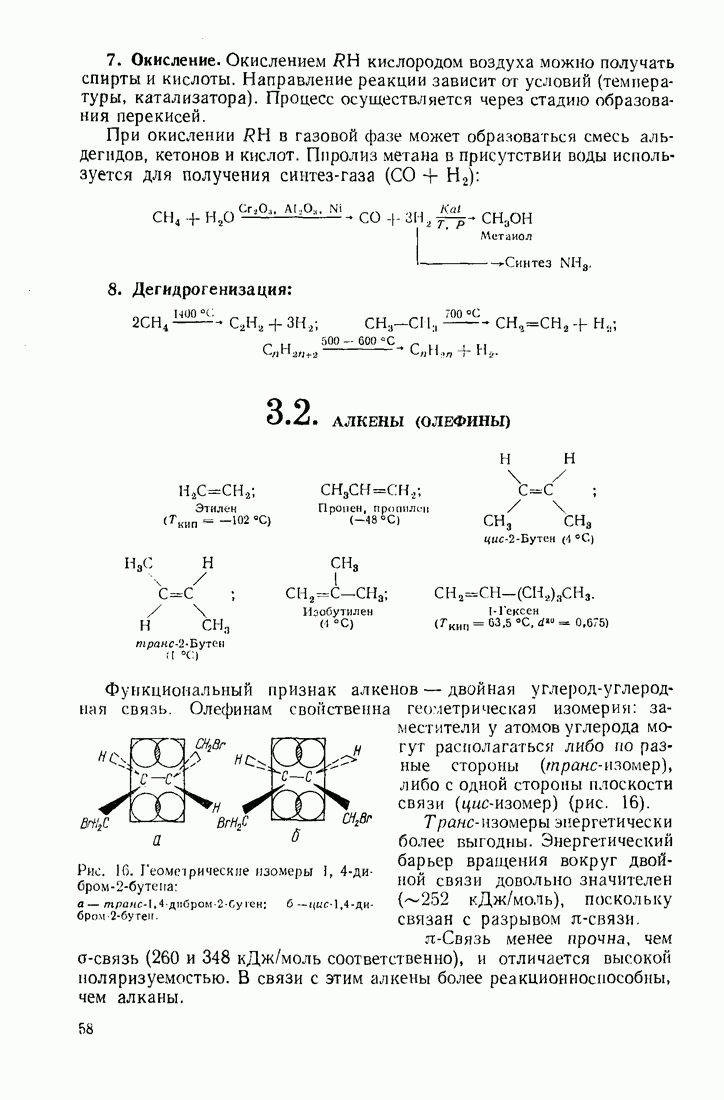
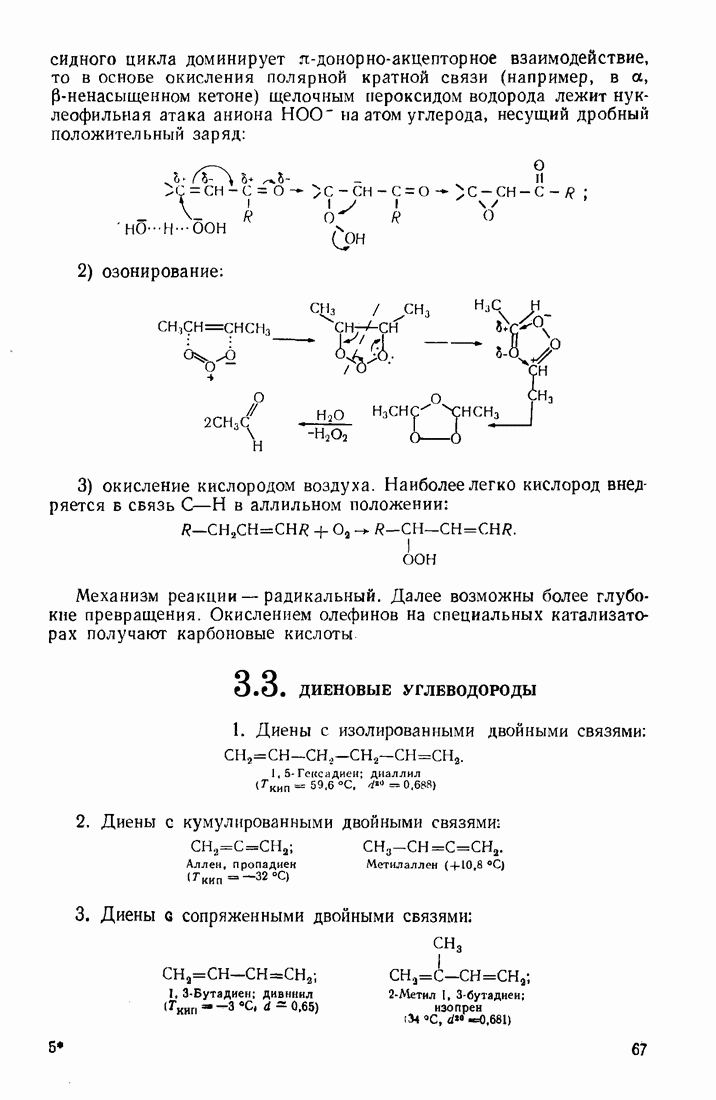
- 3.2. АЛКЕНЫ (ОЛЕФИНЫ)
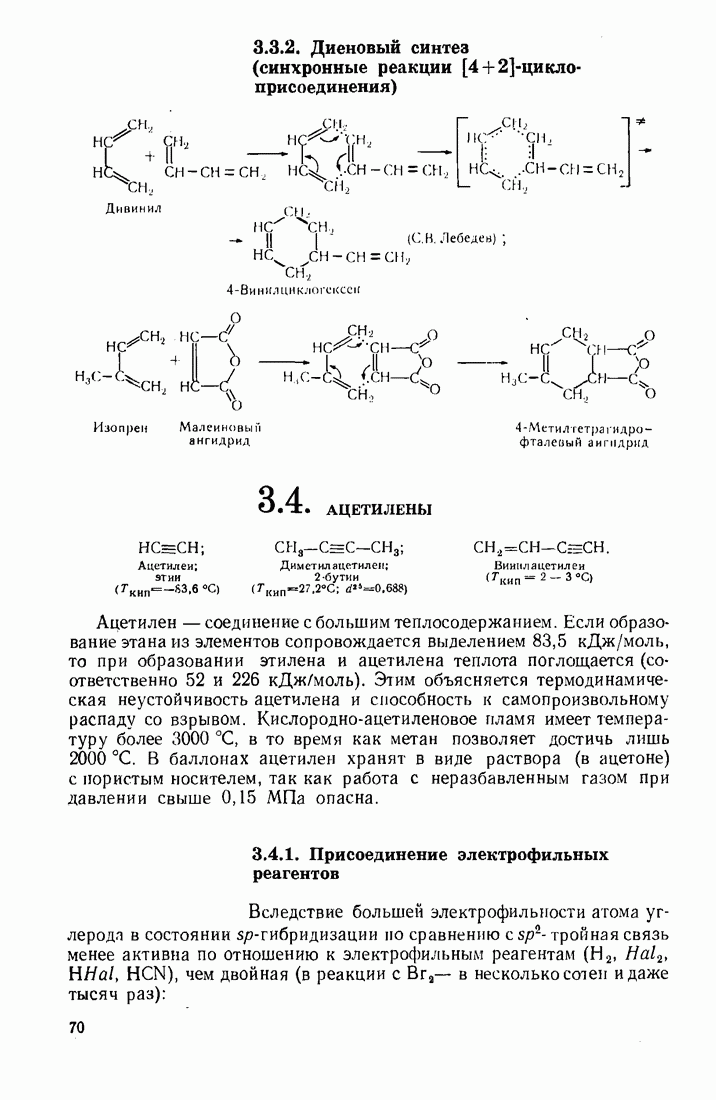
- 3.3. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ
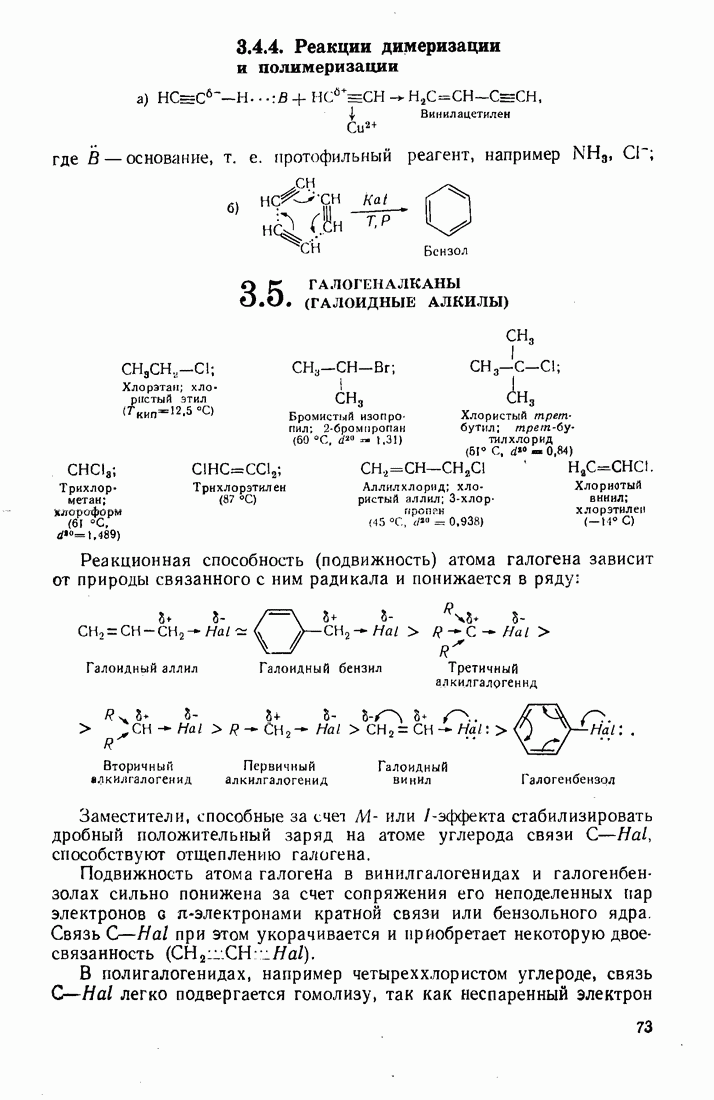
- 3.4. АЦЕТИЛЕНЫ
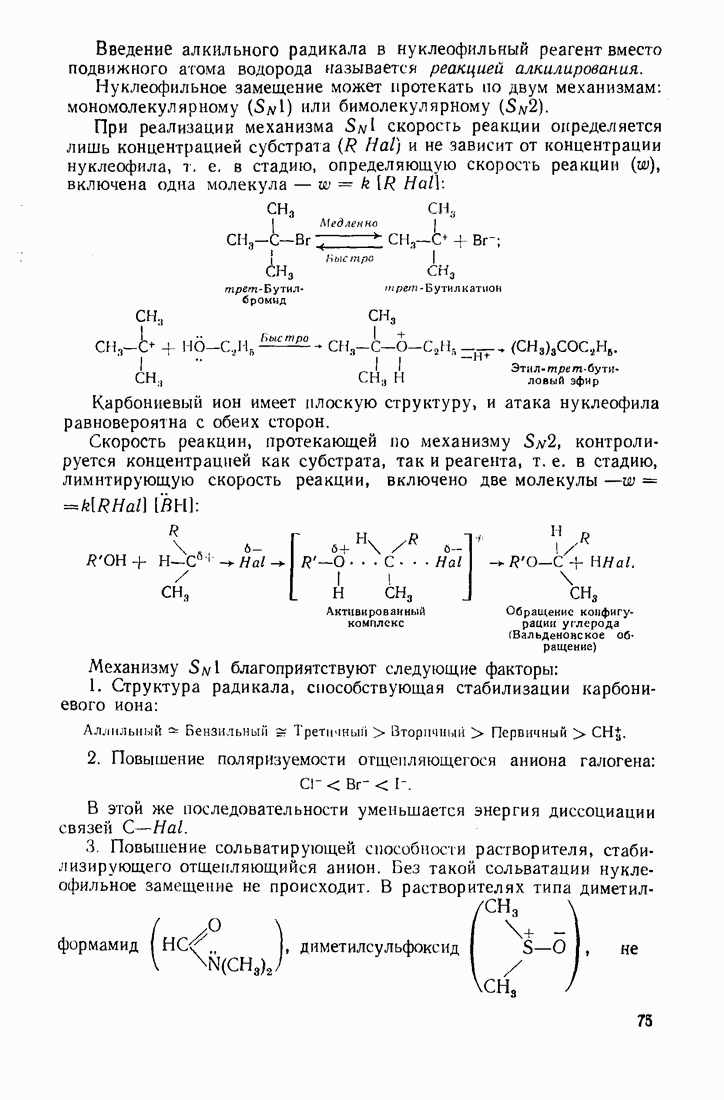
- 3.5. ГАЛОГЕНАЛКАНЫ (ГАЛОИДНЫЕ АЛКИЛЫ)
- 3.6. СПИРТЫ
- 3.7. ПРОСТЫЕ ЭФИРЫ (R-O-R)
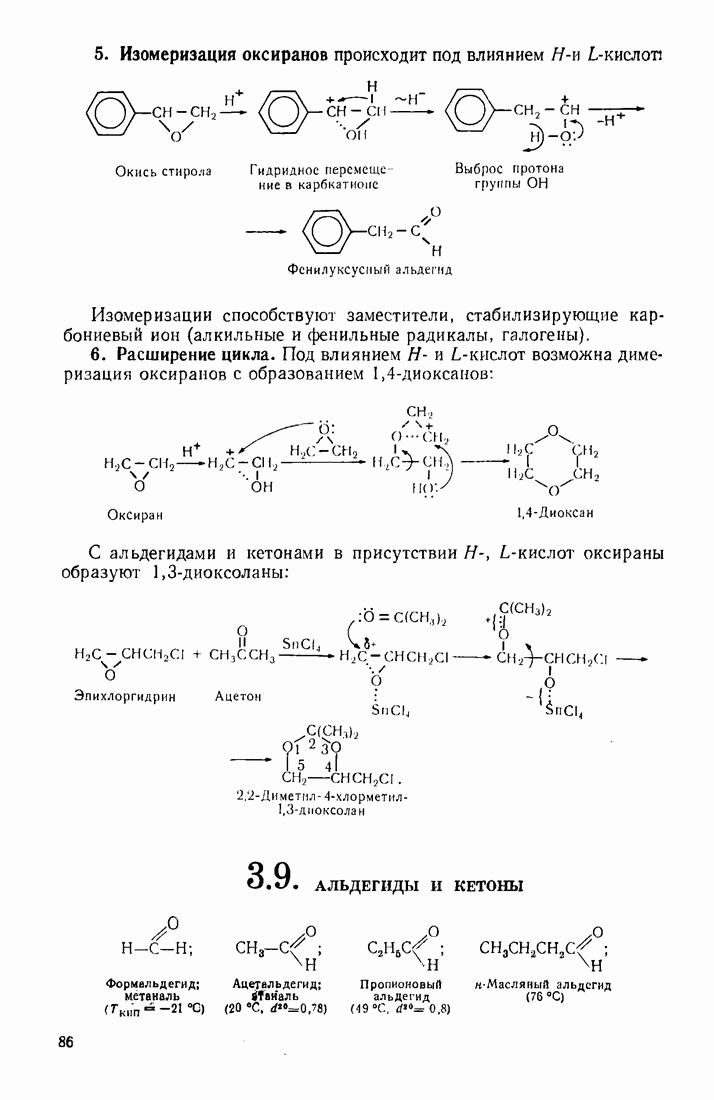
- 3.8. ОКСИРАНЫ (ЭПОКСИДНЫЕ СОЕДИНЕНИЯ, a-ОКИСИ)
- 3.9. АЛЬДЕГИДЫ И КЕТОНЫ
- 3.10. КАРБОНОВЫЕ КИСЛОТЫ
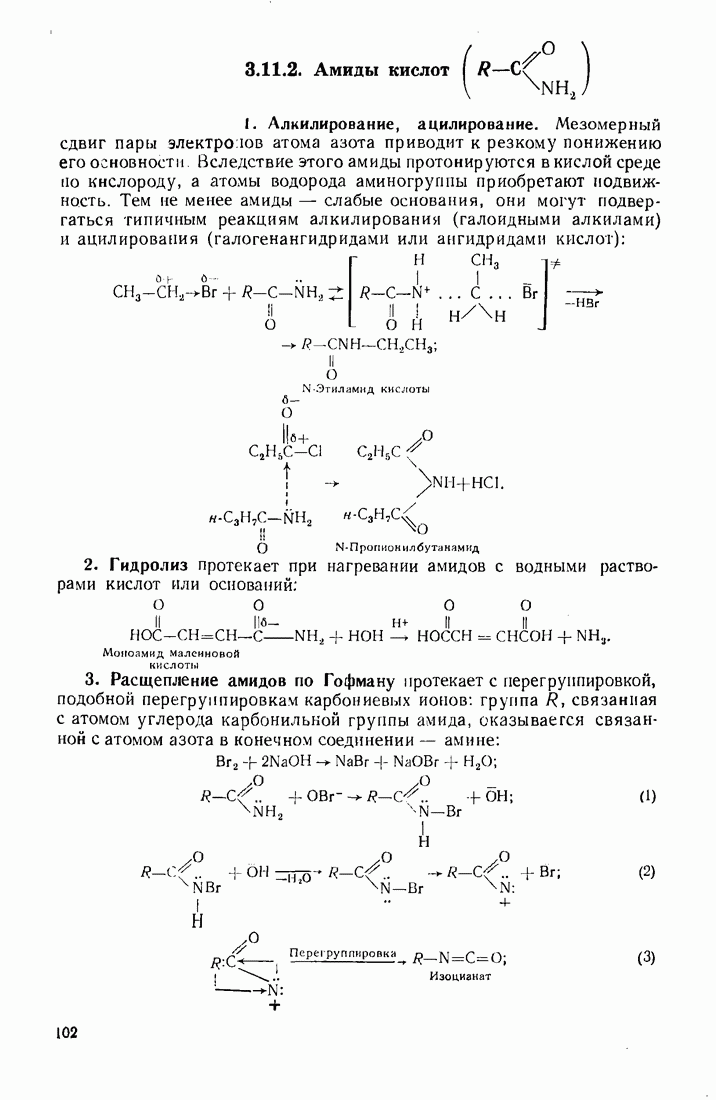
- 3.11. НЕКОТОРЫЕ ПРОИЗВОДНЫЕ КИСЛОТ
- 3.12. АМИНЫ
- 3.13. ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.14. СЕРООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.15. ОРГАНИЧЕСКИЕ ПЕРЕКИСИ (ПЕРОКСИДНЫЕ СОЕДИНЕНИЯ)
- 3.16. ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- 3.17. ГЕТЕРОАНАЛОГИ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- 3.18. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.18.2. Пространственное расположение и напряженность циклов
- 3.18.3. Особенности химических свойств алициклических соединений
- 4. Полифункциональные производные алифатического ряда
- 4.1. ДВУХОСНОВНЫЕ КАРБОНОВЫЕ КИСЛОТЫ
- 4.2. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 4.3. ОКСОКИСЛОТЫ (АЛЬДЕГИДО- И КЕТОКИСЛОТЫ)
- 4.4. ОКСИКИСЛОТЫ. ПОНЯТИЕ ОБ ОПТИЧЕСКОЙ ИЗОМЕРИИ
- 4.5. УГЛЕВОДЫ
- 4.5.2. Стереохимия моносахаридов
- 4.5.3. Дисахариды
- 4.5.4. Полисахариды
- 4.5.5. Нахождение в природе и пути превращения углеводов
- 4.6. АМИНОКИСЛОТЫ
- 5. Методы синтеза органических юединений алифатическою рада
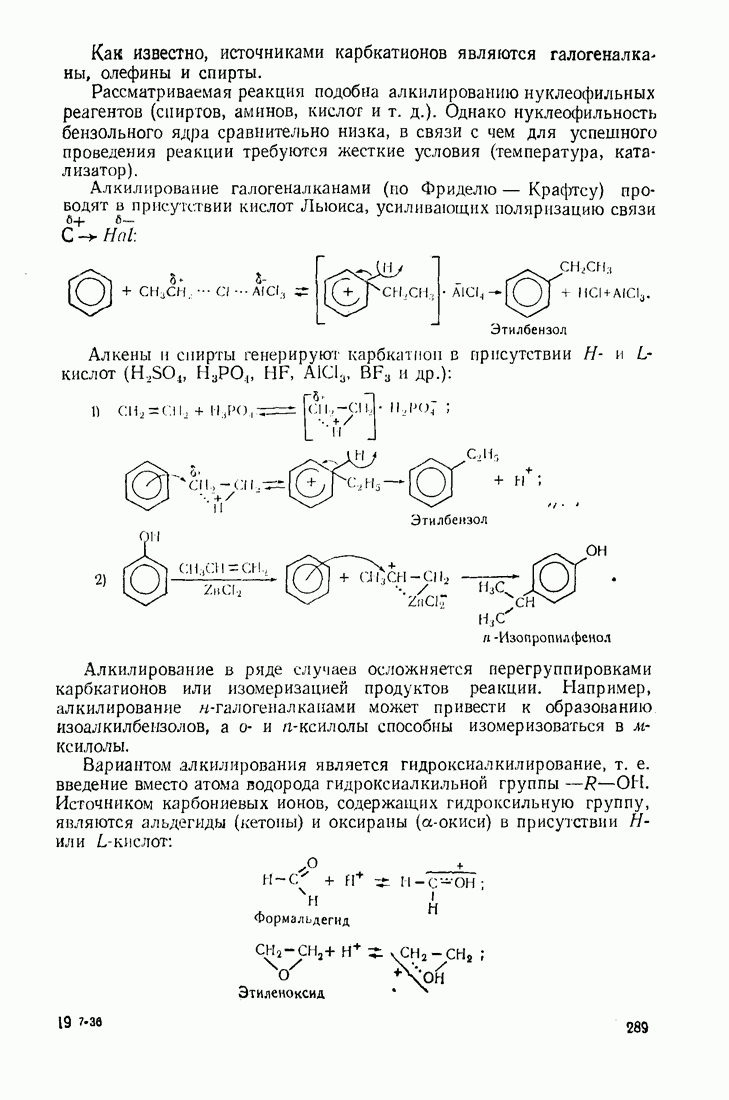
- 5.1. АЛКИЛИРОВАНИЕ
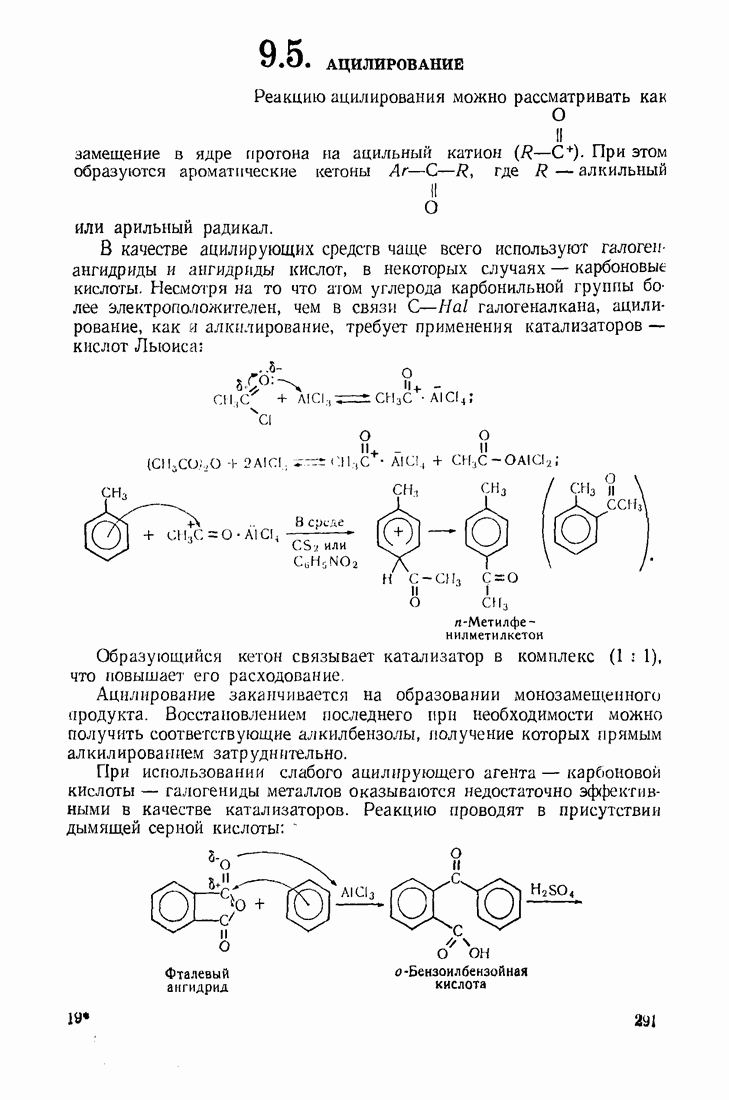
- 5.2. АЦИЛИРОВАНИЕ
- 5.3. ГАЛОГЕНИРОВАНИЕ
- 5.4. ГИДРОКСИЛИРОВАНИЕ
- 5.5. КАРБОНИЛИРОВАНИЕ (ВВЕДЕНИЕ КАРБОНИЛЬНОЙ ГРУППЫ)
- 5.6. КАРБОКСИЛИРОВАНИЕ
- 5.7. ЭПОКСИДИРОВАНИЕ (ОКСИРАНИРОВАИИЕ)
- 5.8. АМИНИРОВАНИЕ
- 5.9. ОКИСЛЕНИЕ
- 5.10. ВОССТАНОВЛЕНИЕ
- 5.11. АЛКАНЫ
- 5.12 АЛКЕНЫ
- 5.13. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ (1,3-ДИЕНЫ)
- 5.14. АЦЕТИЛЕНЫ
- 5.15 АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 5.16. ГАЛОГЕН АЛКАНЫ
- 5.17. СПИРТЫ
- 5.18. АЛЬДЕГИДЫ И КЕТОНЫ
- 5.19. КАРБОНОВЫЕ КИСЛОТЫ
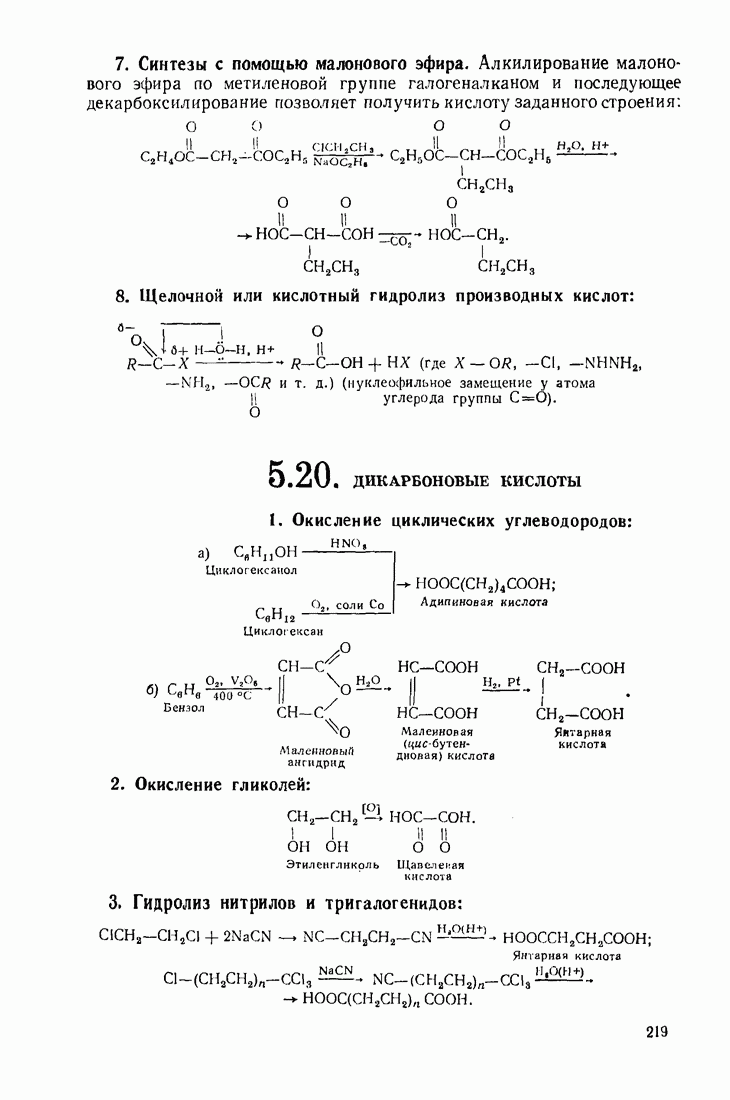
- 5.20. ДИКАРБОНОВЫЕ КИСЛОТЫ
- 5.21. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
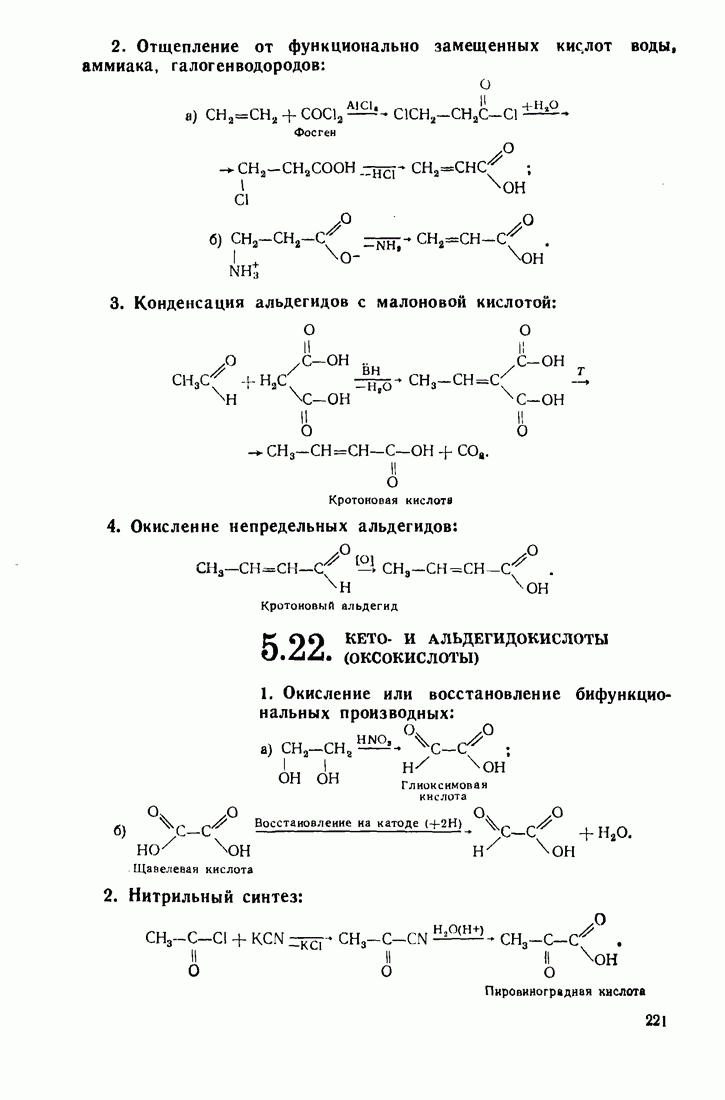
- 5.22. КЕТО- И АЛЬДЕГИДОКИСЛОТЫ (ОКСОКИСЛОТЫ)
- 5.23. ОКСИКИСЛОТЫ
- 5.24. АМИНОКИСЛОТЫ
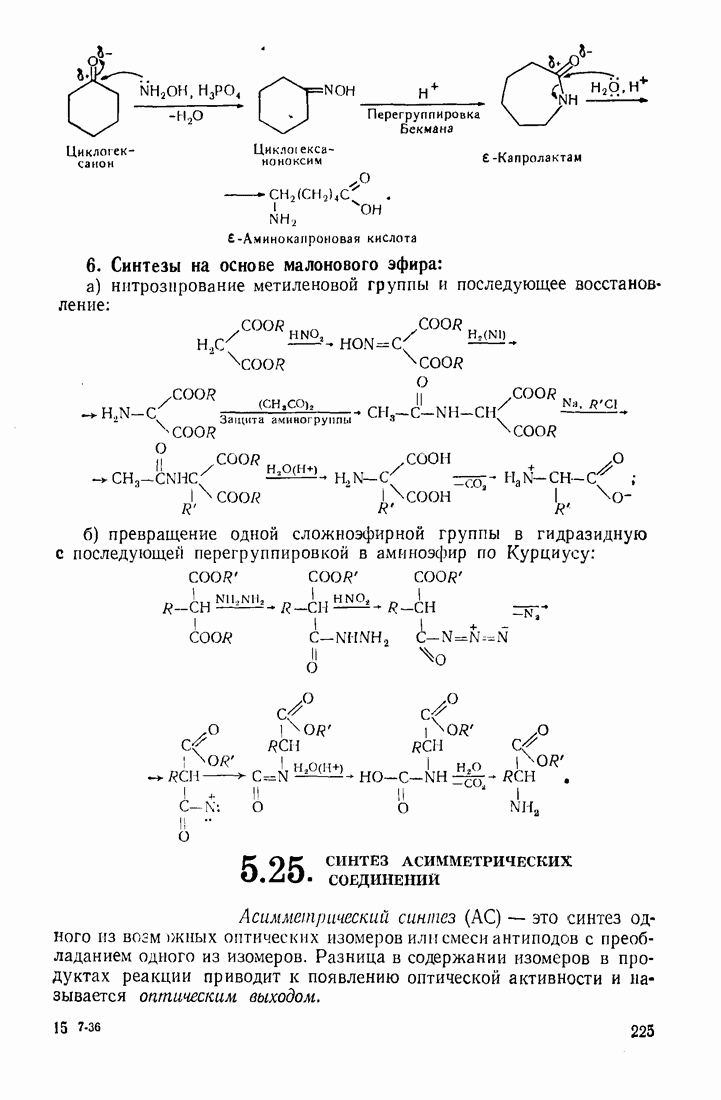
- 5.25 СИНТЕЗ АСИММЕТРИЧЕСКИХ СОЕДИНЕНИЙ
- 6. Некоторые понятия физической органической химии
- 6.1. СВЯЗЬ СОСТАВА И СТРОЕНИЯ СОЕДИНЕНИЙ С ФИЗИЧЕСКИМИ СВОЙСТВАМИ
- 6.2. ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 6.3. КИСЛОТЫ И ОСНОВАНИЯ В ОРГАНИЧЕСКОЙ ХИМИИ
- 6.4. ОРГАНИЧЕСКИЕ РАСТВОРИТЕЛИ И ИХ ВЛИЯНИЕ НА СКОРОСТЬ И МЕХАНИЗМ РЕАКЦИЙ
- 6.5. КАТАЛИЗ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- 7. Бензол и его производные
- 7.1. СТРОЕНИЕ БЕНЗОЛА. РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОННОЙ ПЛОТНОСТИ
- 7.2. ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
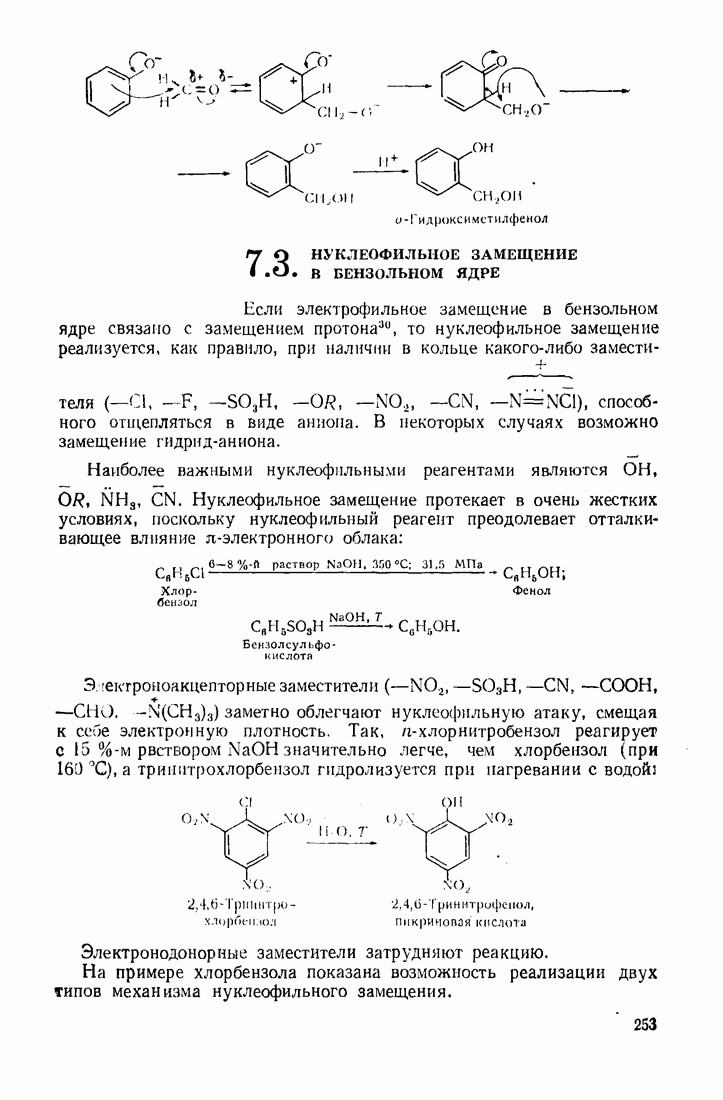
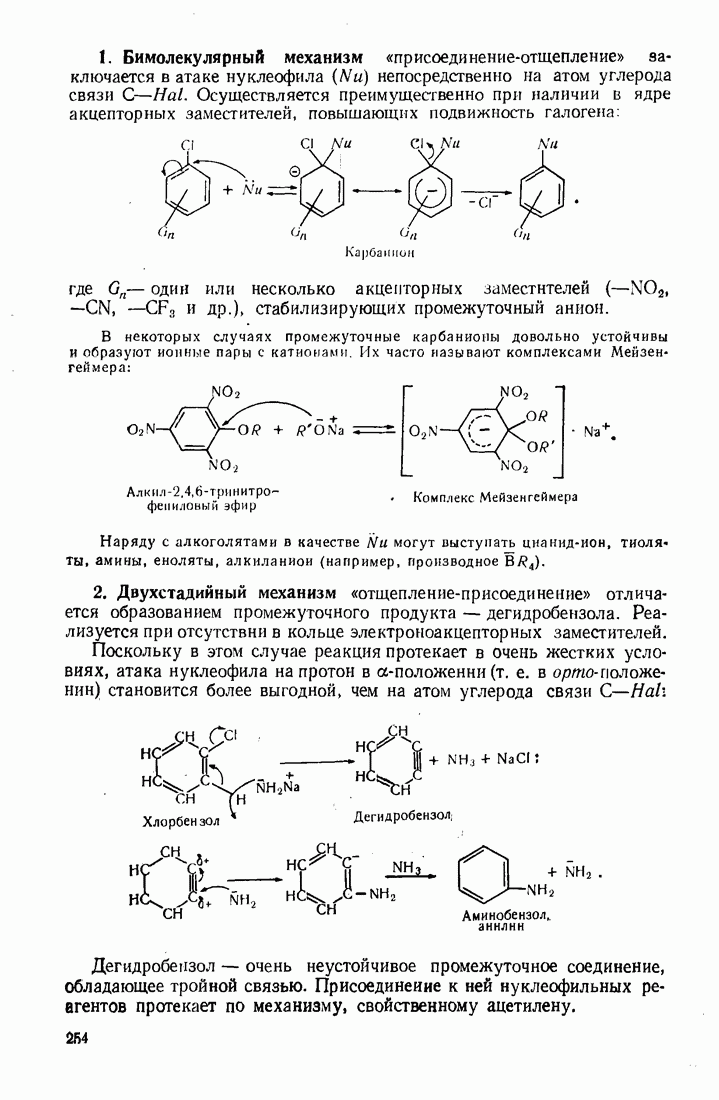
- 7.3. НУКЛЕОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
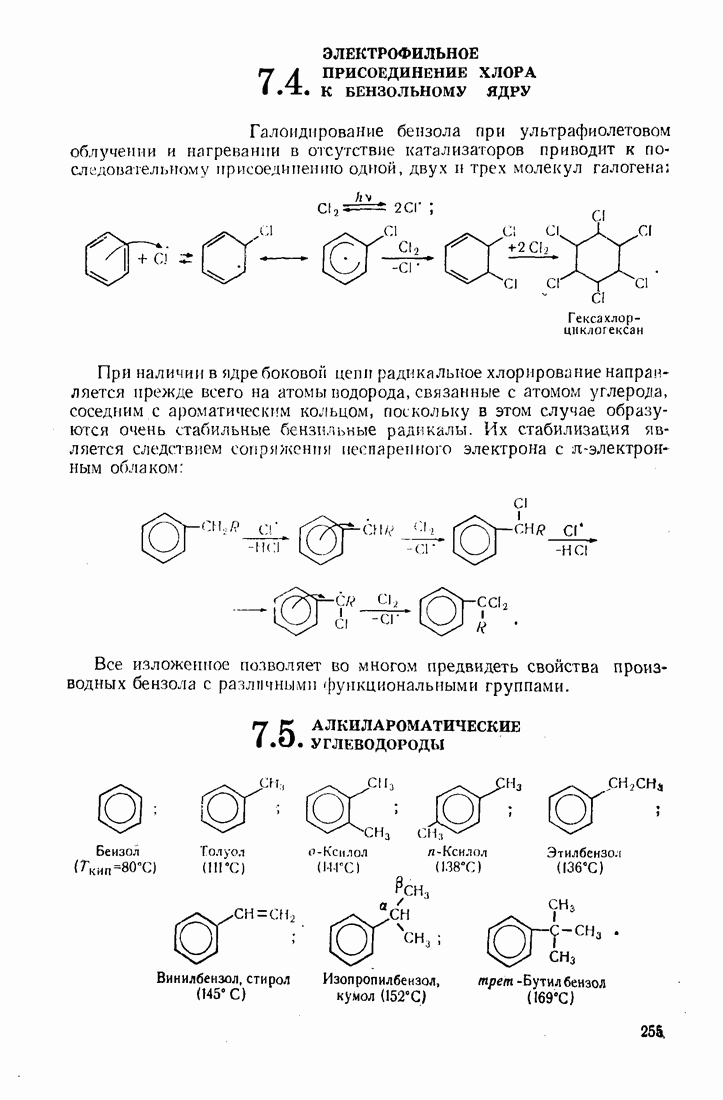
- 7.4. ЭЛЕКТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ ХЛОРА К БЕНЗОЛЬНОМУ ЯДРУ
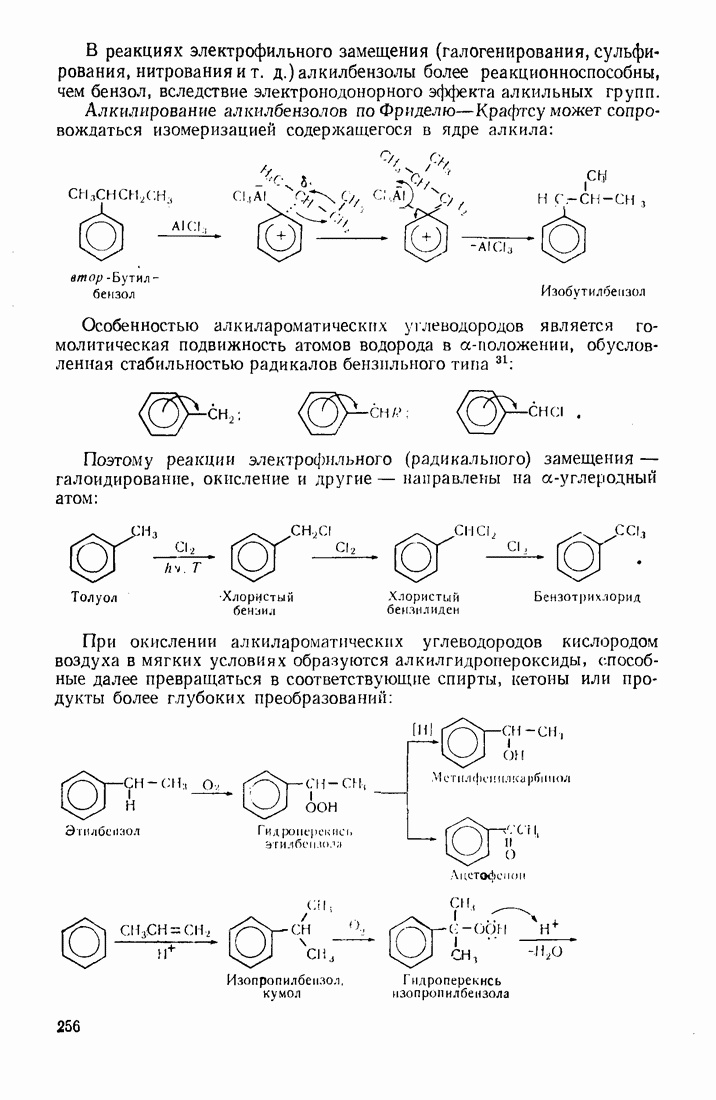
- 7.5. АЛКИЛАРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
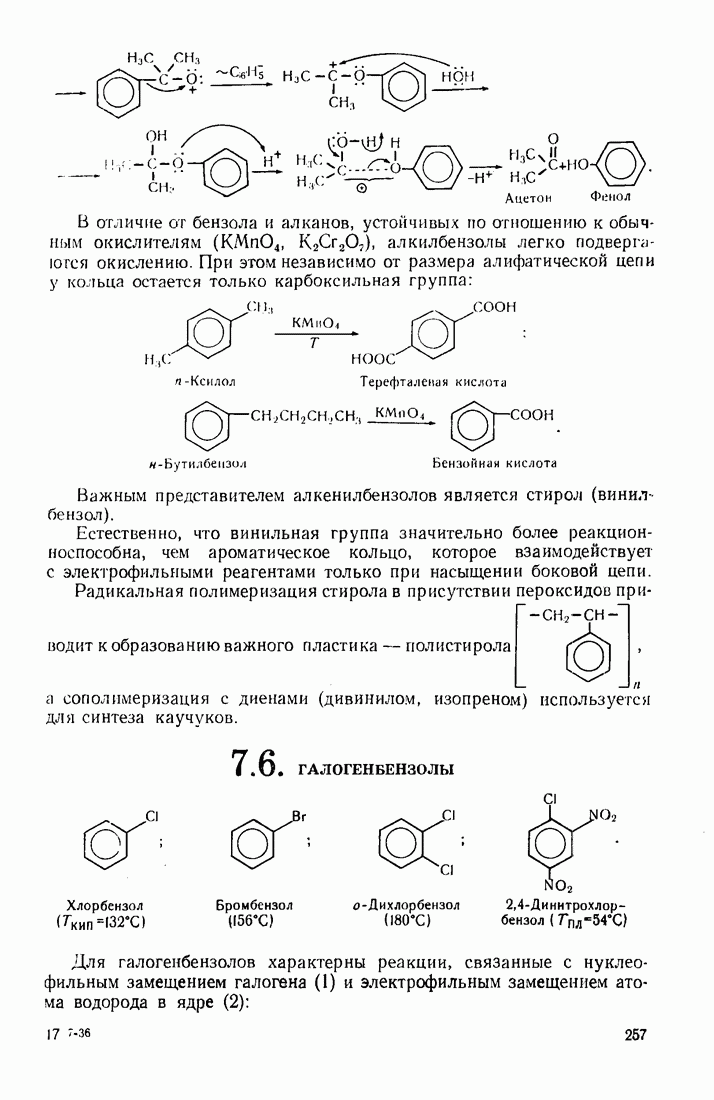
- 7.6. ГАЛОГЕНБЕНЗОЛЫ
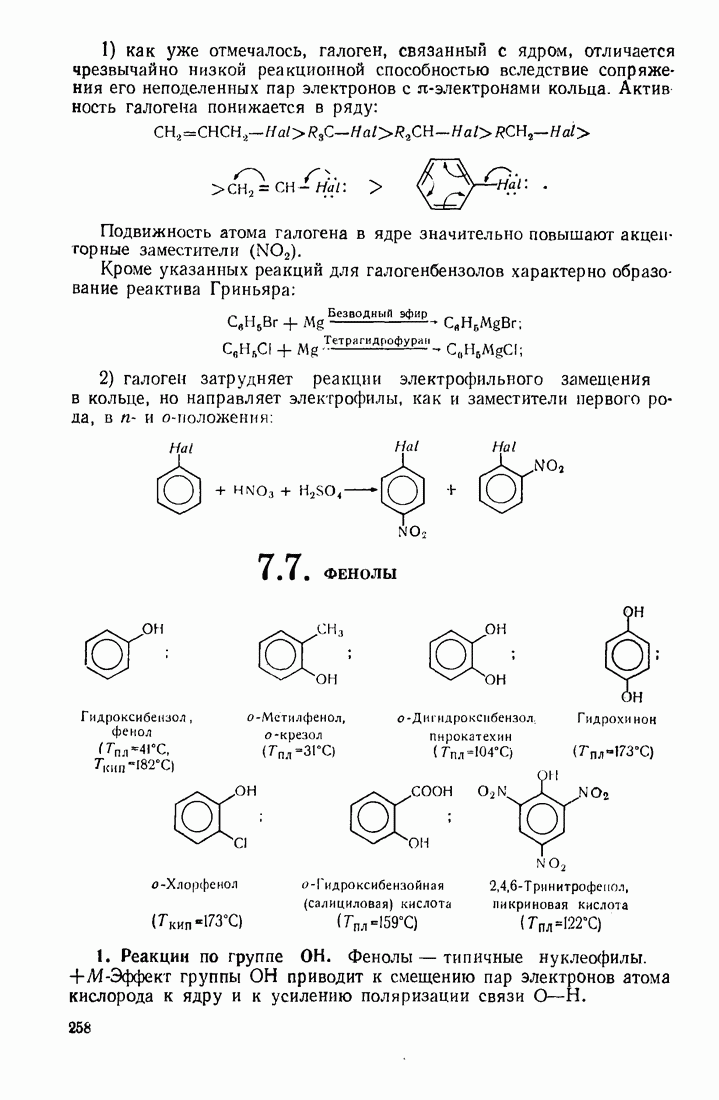
- 7.7. ФЕНОЛЫ
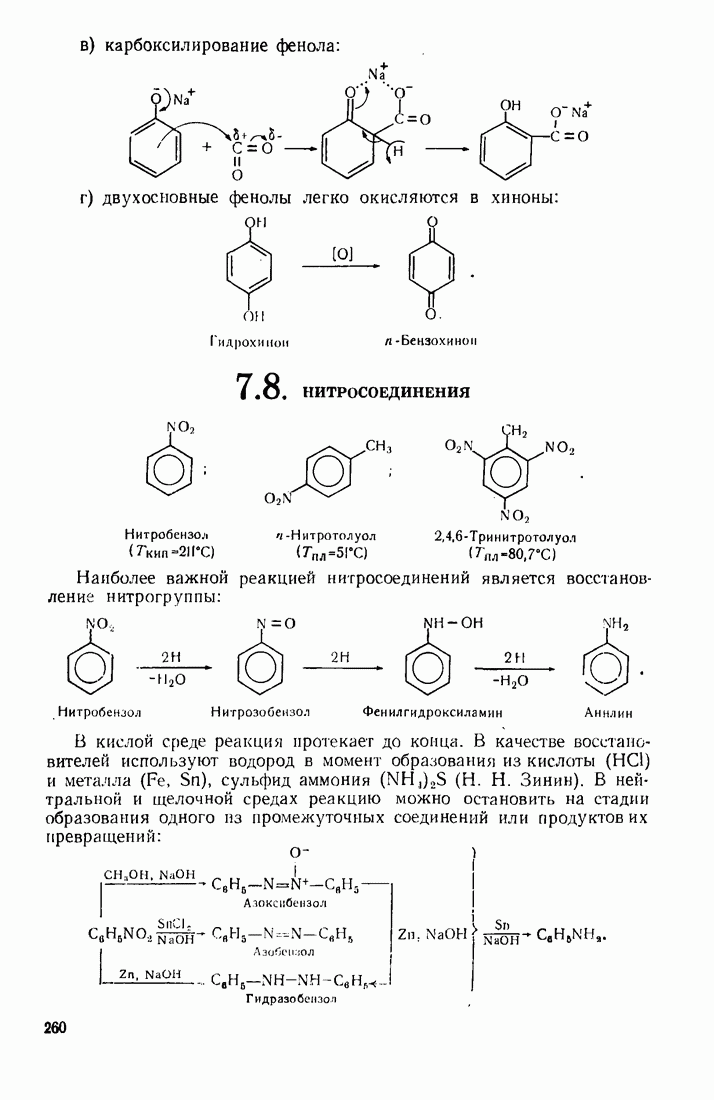
- 7.8. НИТРОСОЕД ИНЕНИЯ
- 7.9. АРОМАТИЧЕСКИЕ АМИНЫ
- 7.10. ДИАЗОСОЕДИНЕНИЯ
- 7.11. АЗОСОЕДИНЕНИЯ
- 7.12. СУЛЬФОКИСЛОТЫ
- 7.13. АЛЬДЕГИДЫ И КЕТОНЫ
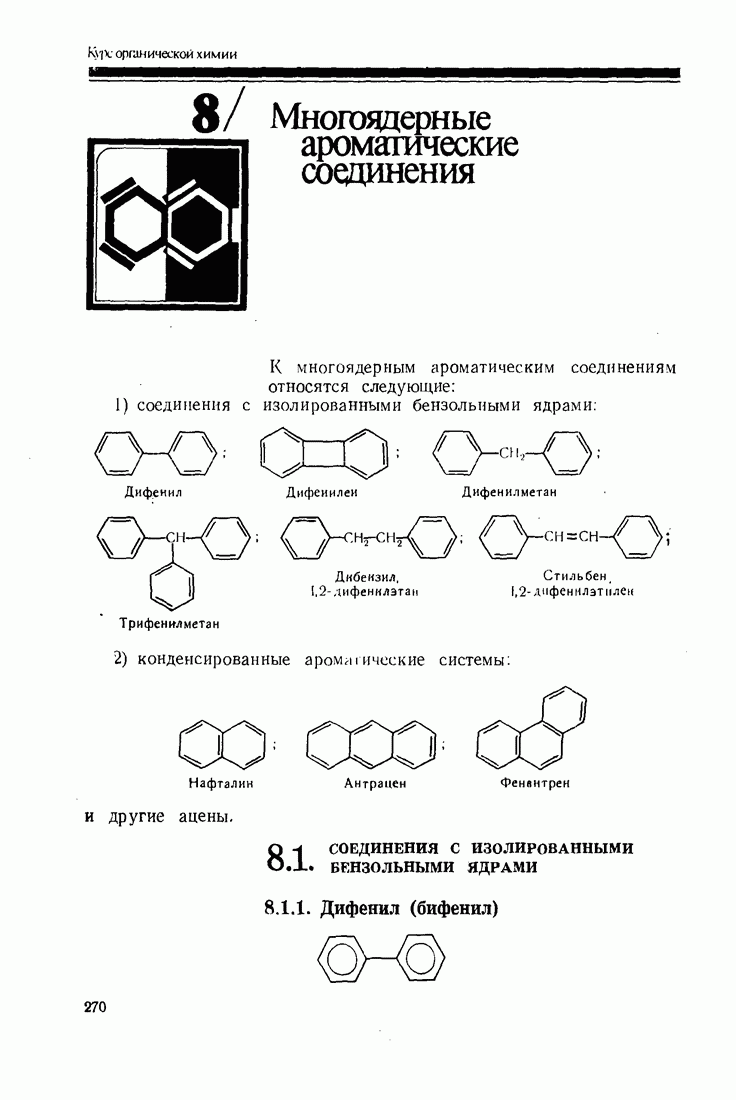
- 8. Многоядерные ароматические соединения
- 8.1. СОЕДИНЕНИЯ С ИЗОЛИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЯДРАМИ
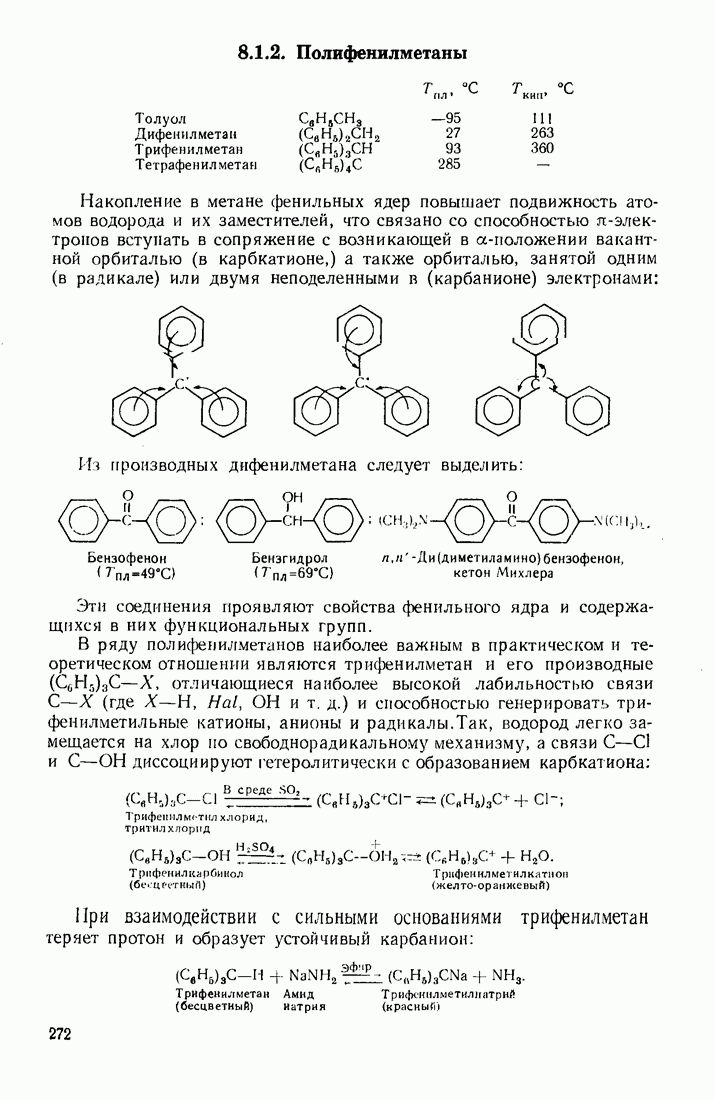
- 8.1.2. Полифенилметаны
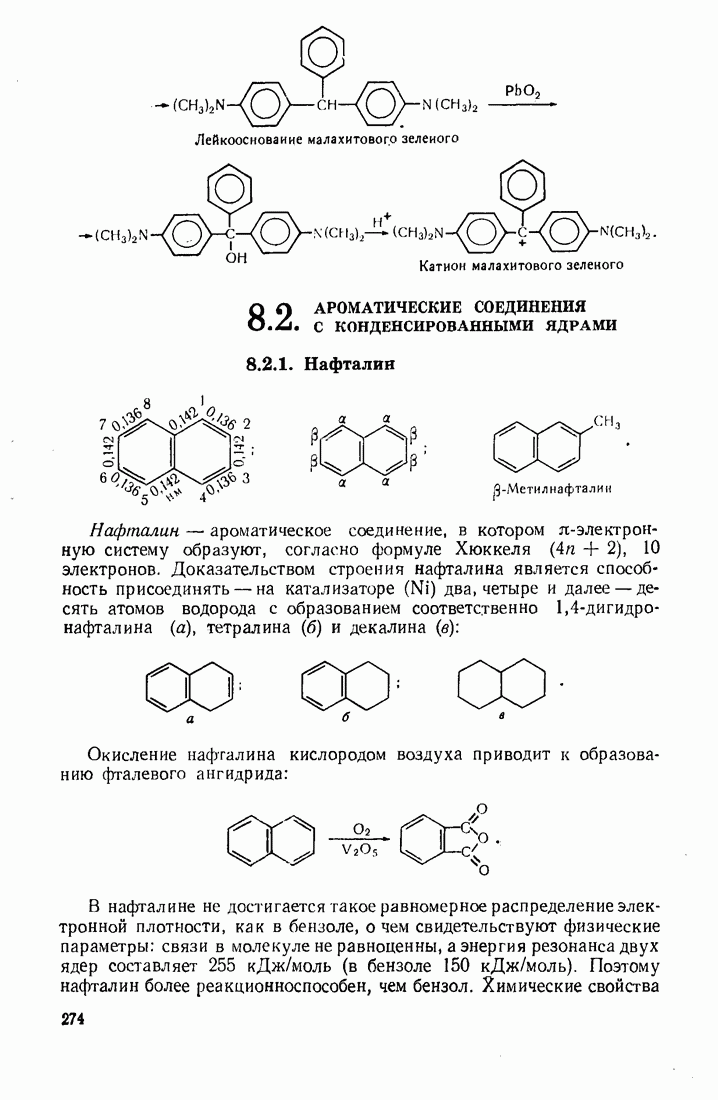
- 8.2. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ С КОНДЕНСИРОВАННЫМИ ЯДРАМИ
- 8.2.2. Антрацен
- 8.2.3. Фенантрен
- 9. Методы синтеза в ряду ароматических соединений
- 9.1. ГАЛОГЕНИРОВАНИЕ
- 9.2. НИТРОВАНИЕ
- 9.3. СУЛЬФИРОВАНИЕ
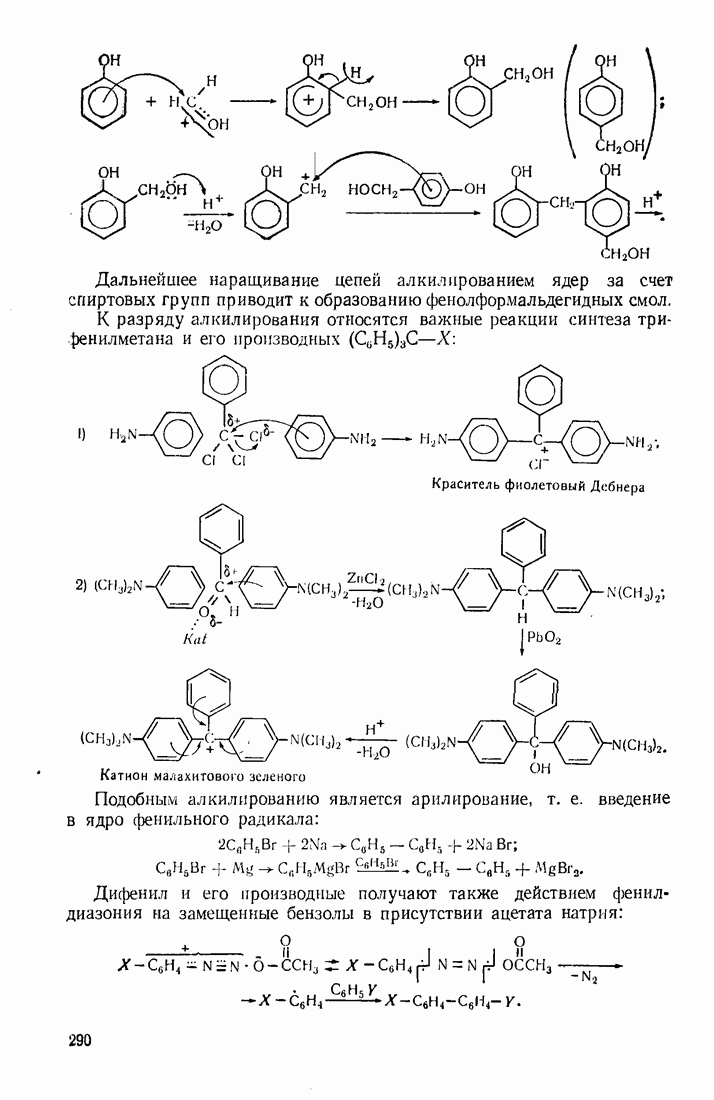
- 9.4. АЛКИЛИРОВАНИЕ
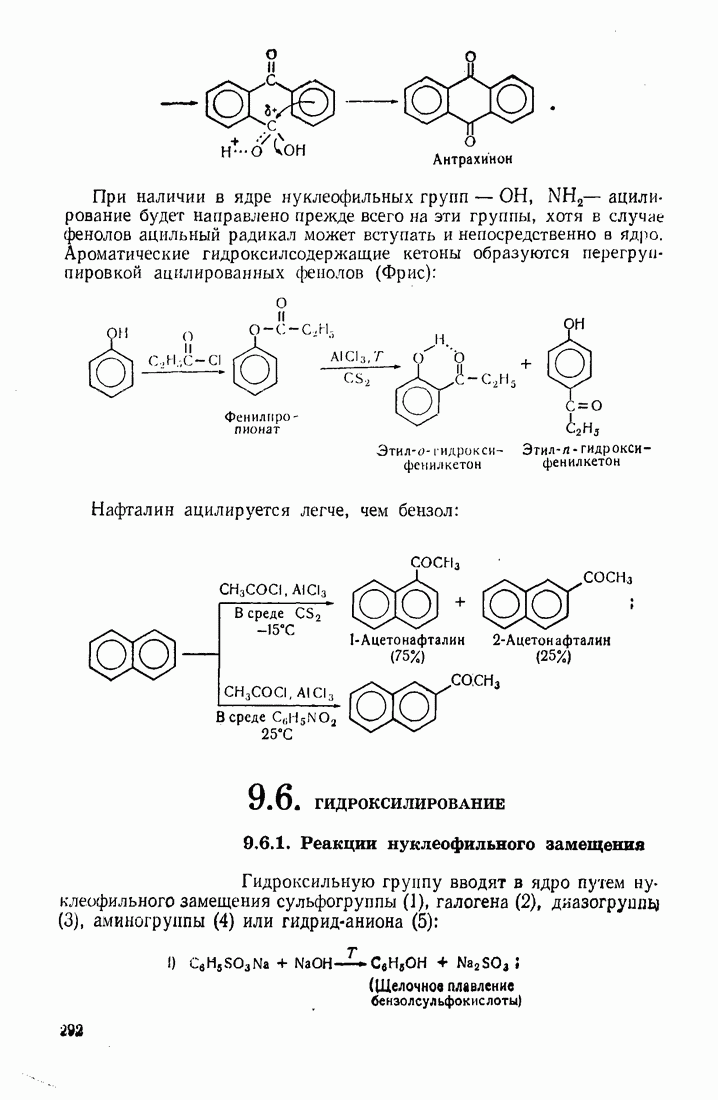
- 9.5. АЦИЛИРОВАНИЕ
- 9.6. ГИДРОКСИЛИРОВАНИЕ
- 9.7. АМИНИРОВАНИЕ
- 9.8. НИТРОЗИРОВАНИЕ
- 9.9. КАРБОНИЛИРОВАНИЕ
- 9.10. КАРБОКСИЛИРОВАНИЕ
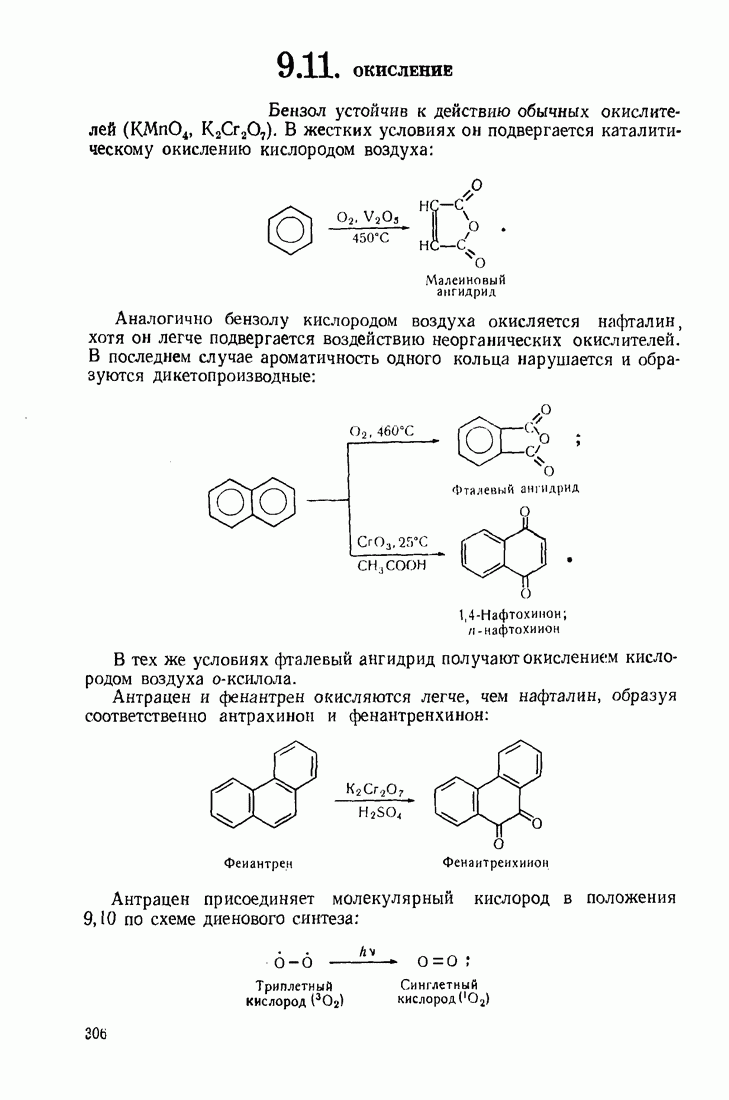
- 9.11. ОКИСЛЕНИЕ
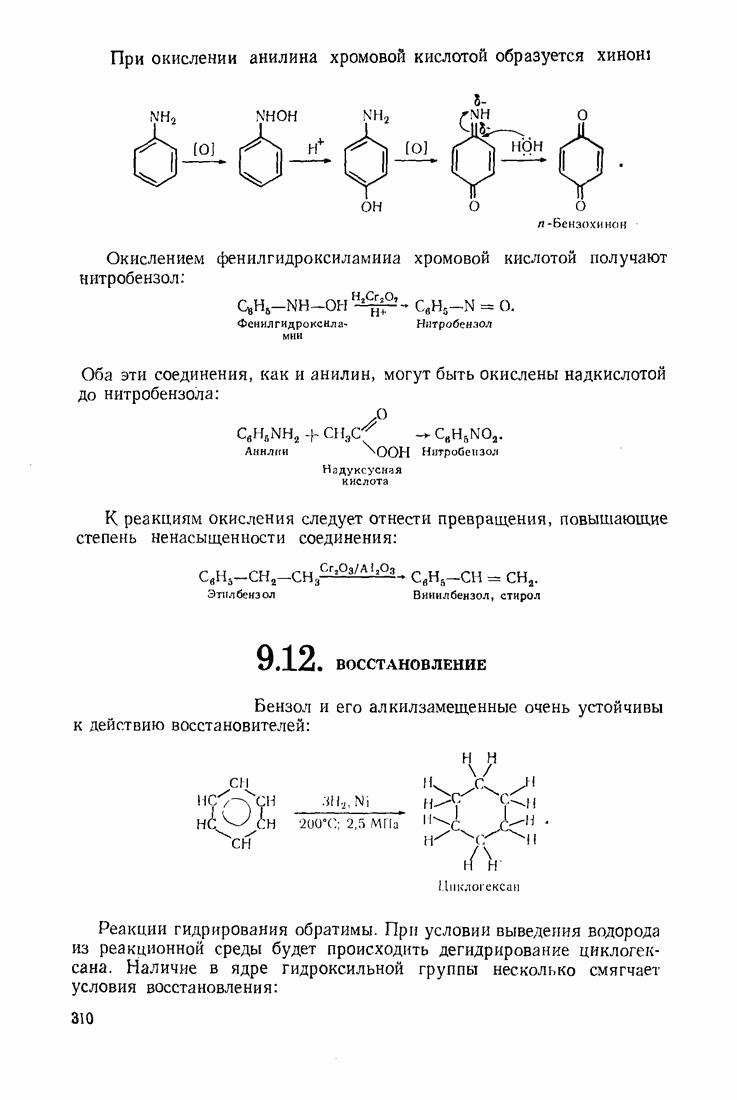
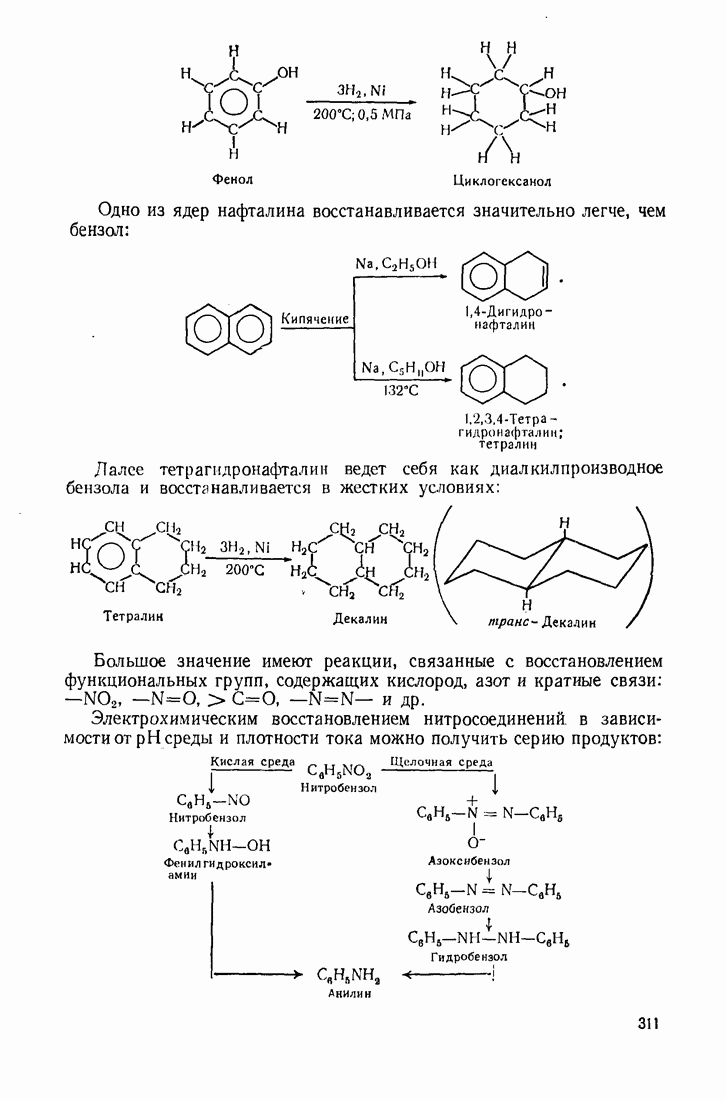
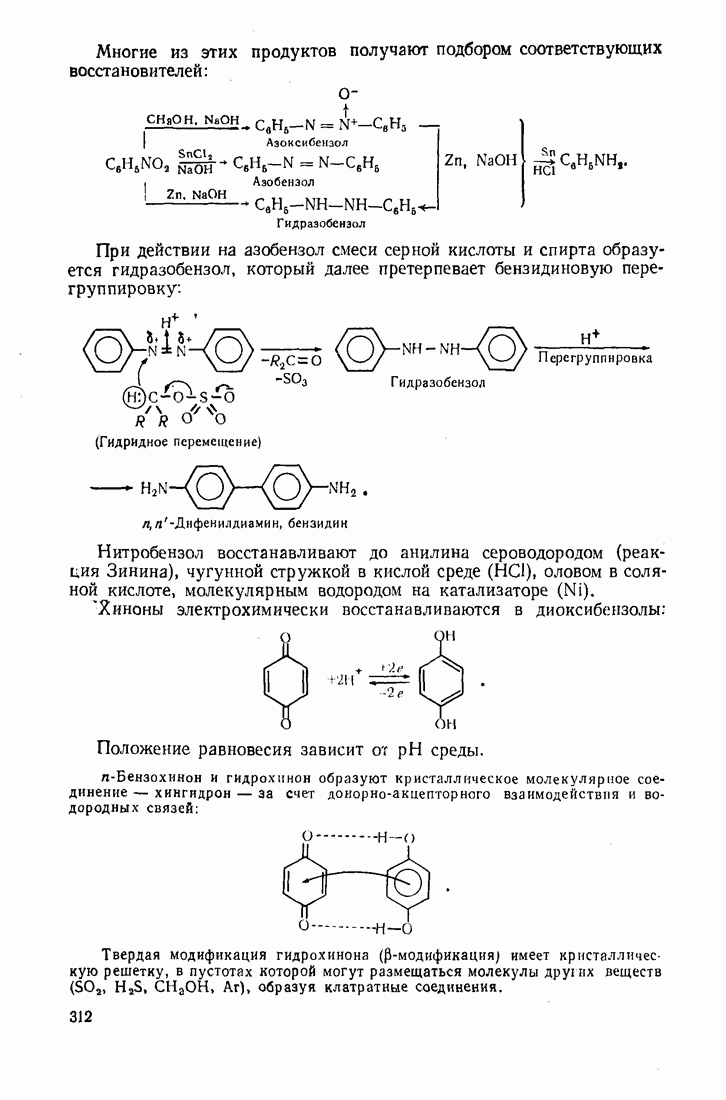
- 9.12. ВОССТАНОВЛЕНИЕ
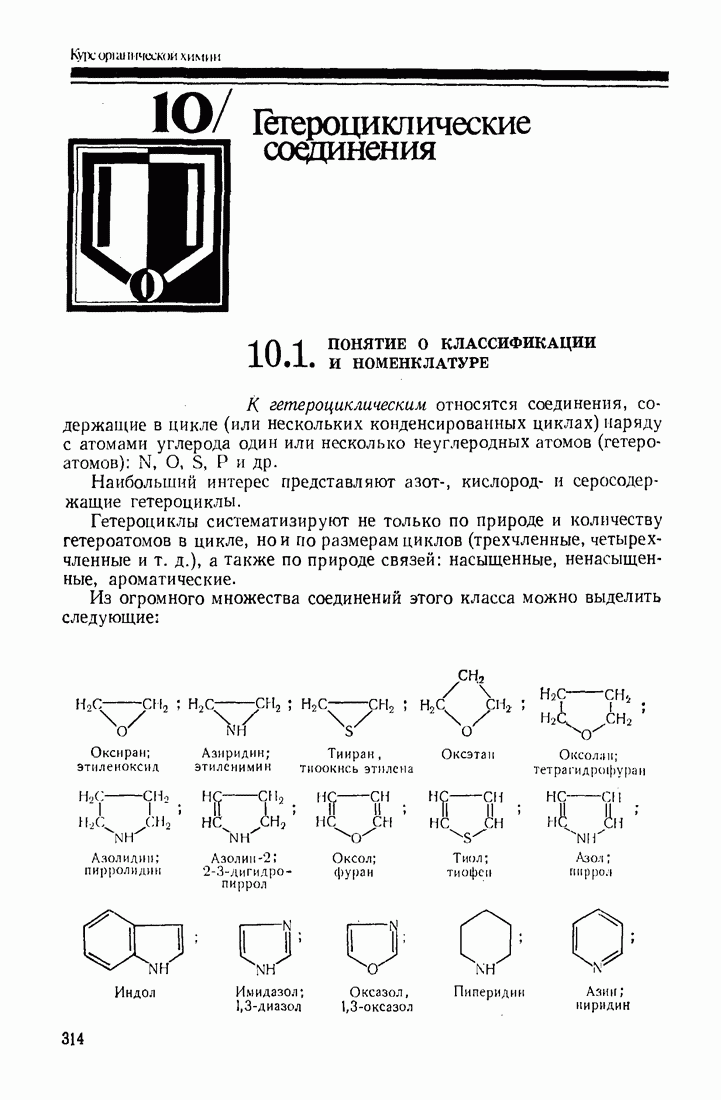
- 10. Гетероциклические соединения
- 10.2. ОБЩАЯ ХАРАКТЕРИСТИКА СТРОЕНИЯ И РЕАКЦИОННОЙ СПОСОБНОСТИ
- 10.3. ПЯТИ- И ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
- 10.4. ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
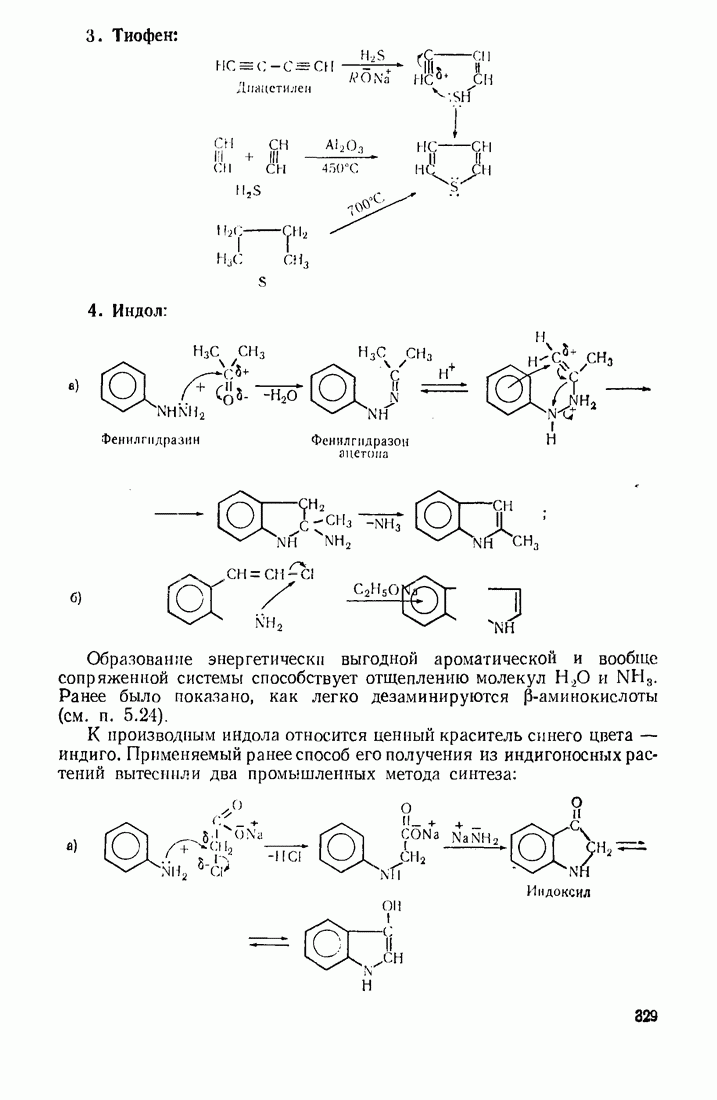
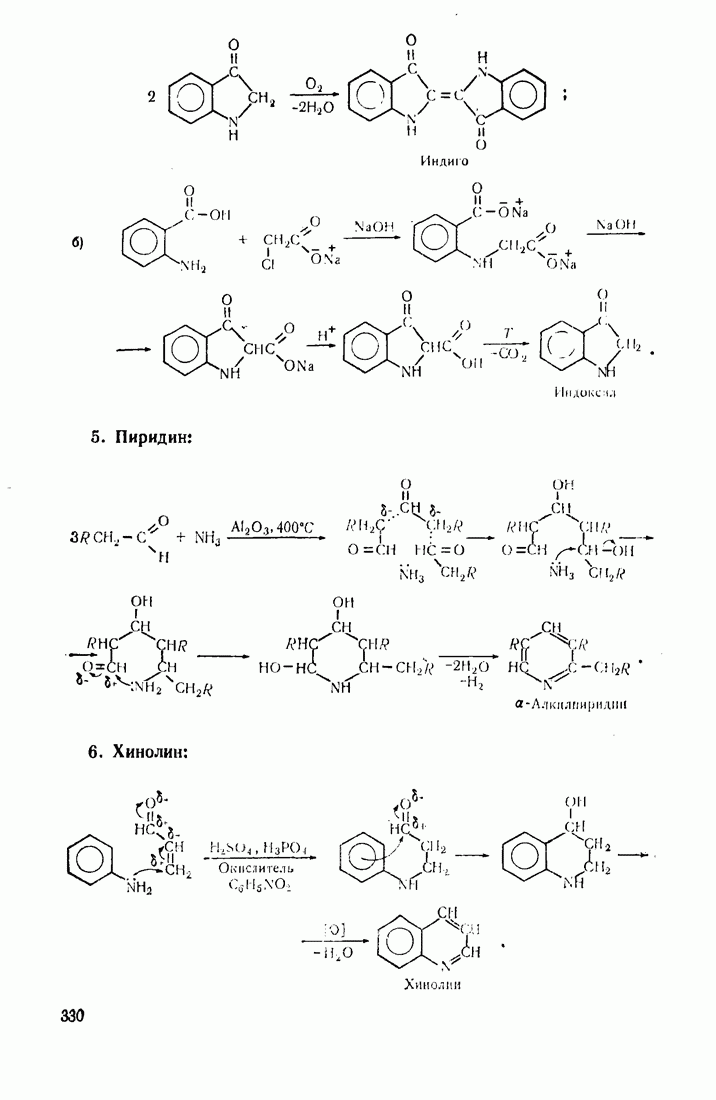
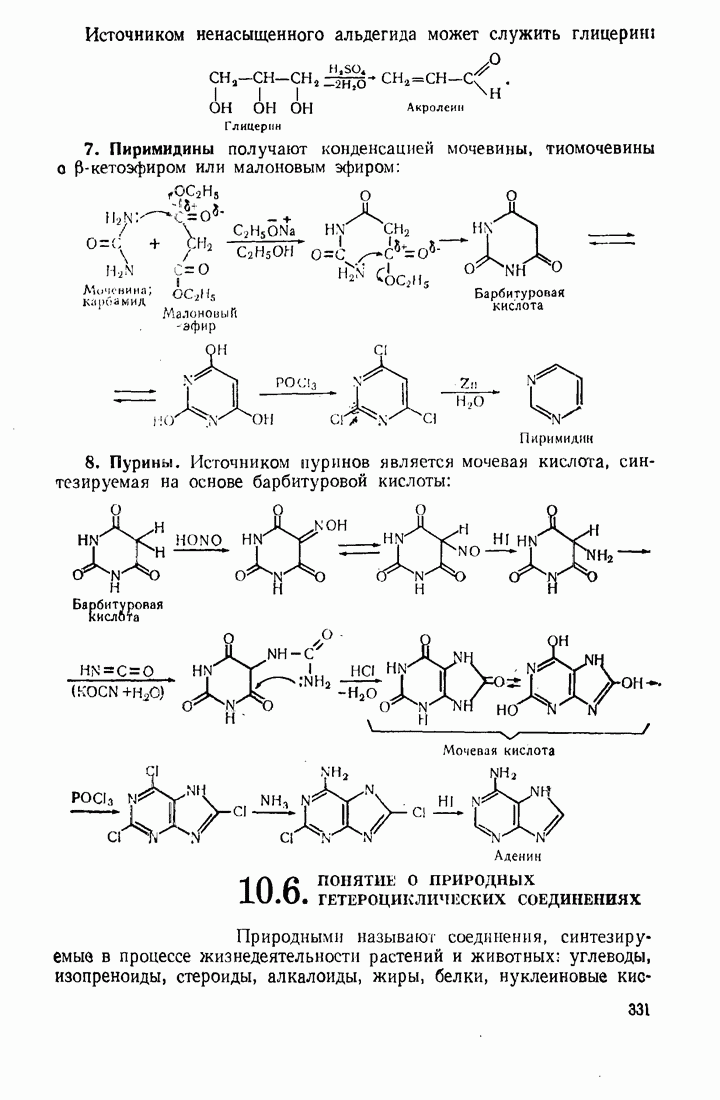
- 10.5. МЕТОДЫ СИНТЕЗА ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
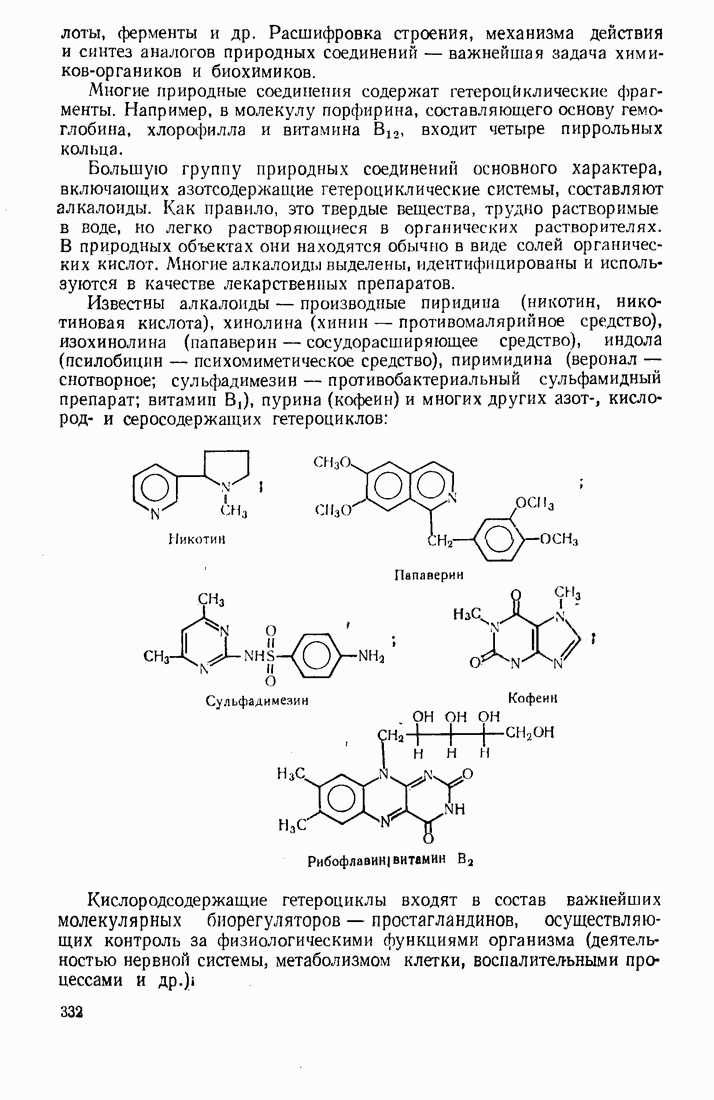
- 10.6. П0НЯТИЕ О ПРИРОДНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЯХ
- 11. Зпементоорганические соединения
- 11.2. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ НЕКОТОРЫХ НЕМЕТАЛЛОВ
- 11.3. МЕГАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 11.4. ОРГАНИЧЕСКИЕ ПРОИЗВОДНЫЕ ПЕРЕХОДНЫХ МЕТАЛЛОВ
- 12. Сырье и основные направления развития промышленности органического синтеза
- 12.1.1. Нефть и сопутствующий природный газ
- 12.1.2. Углехимическое сырье
- 12.1.3. Лесохимическое и сельскохозяйственное сырье
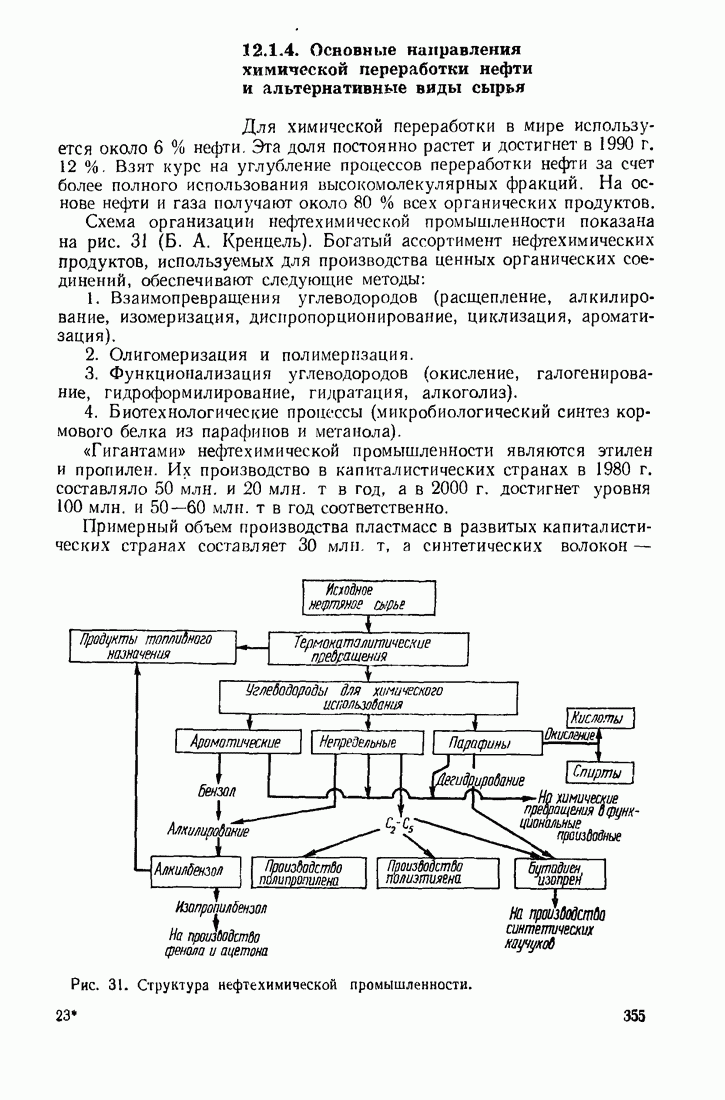
- 12.1.4. Основные направления химической переработки нефти и альтернативные виды сырья
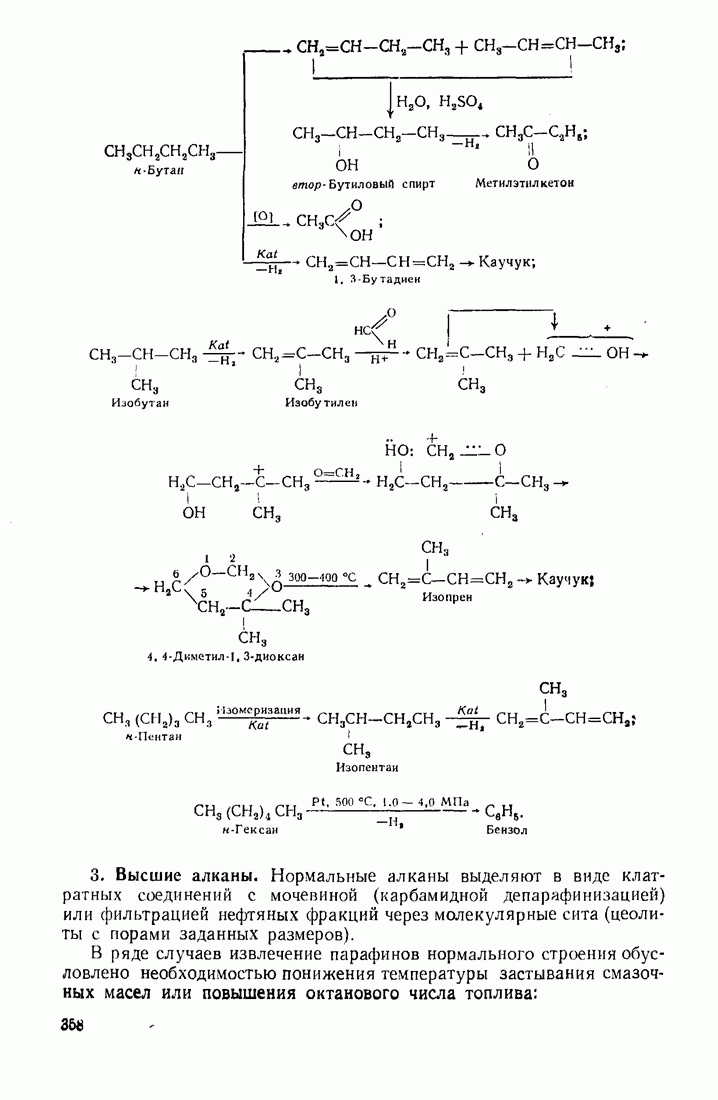
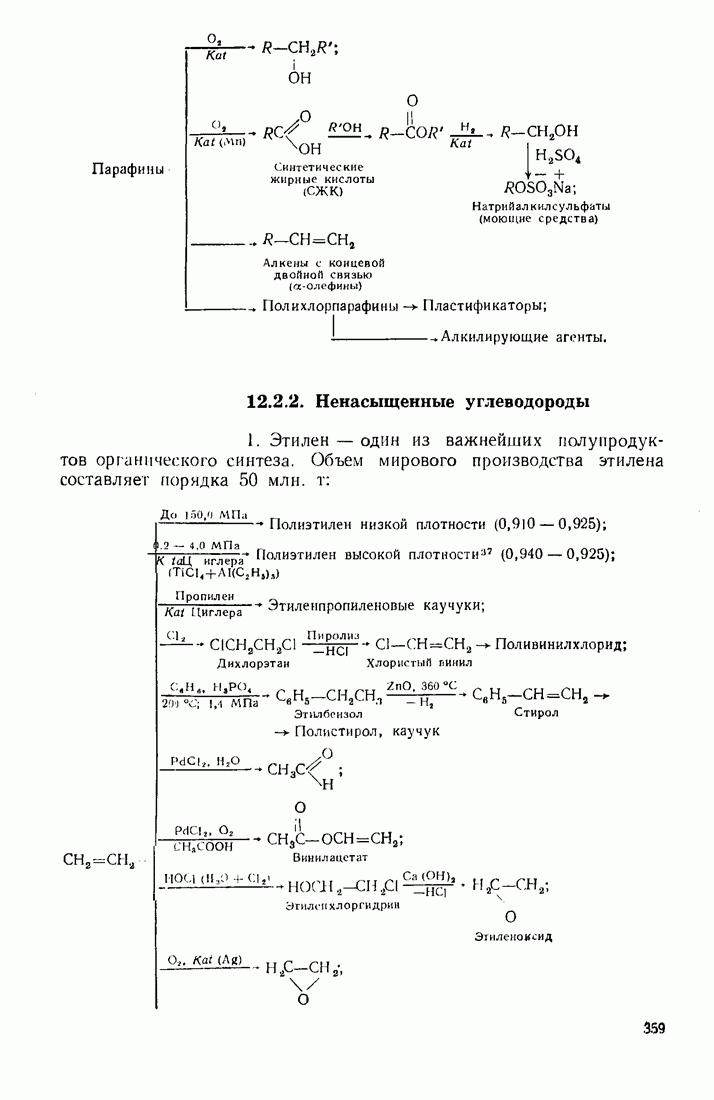
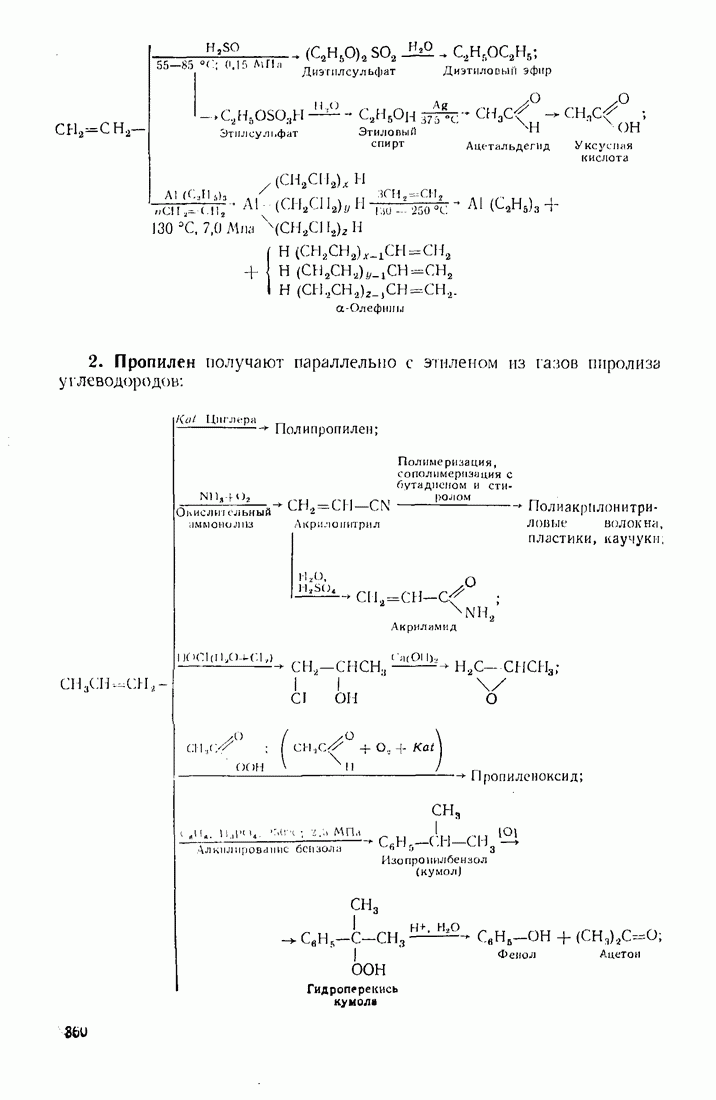
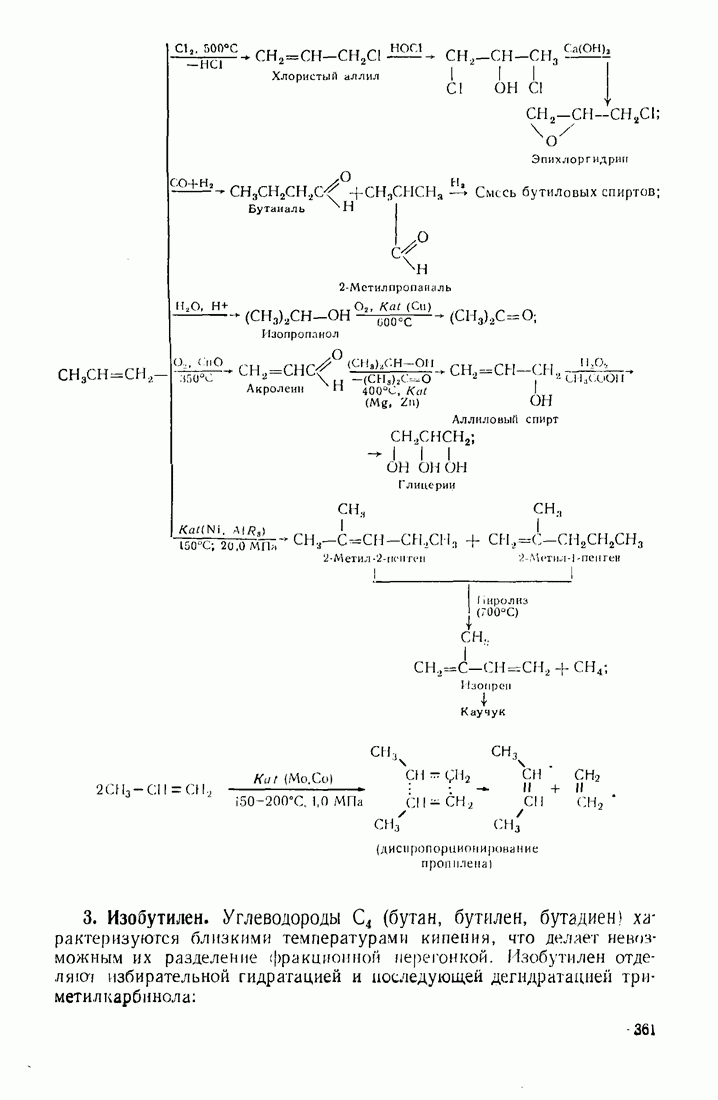
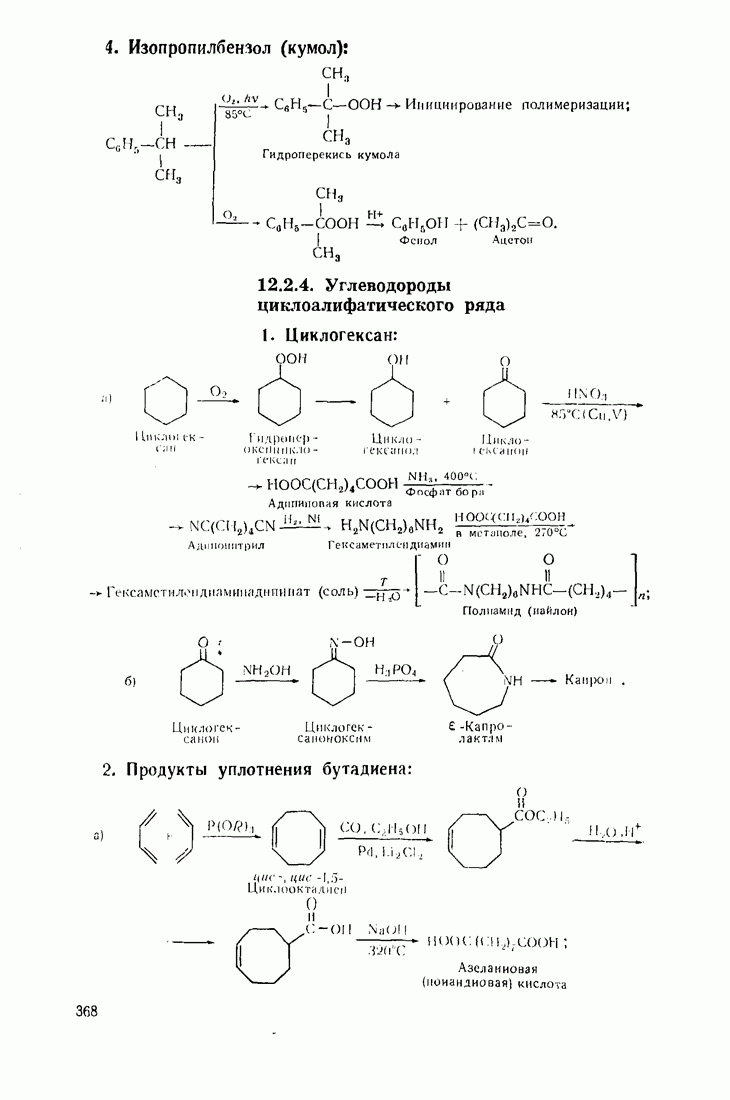
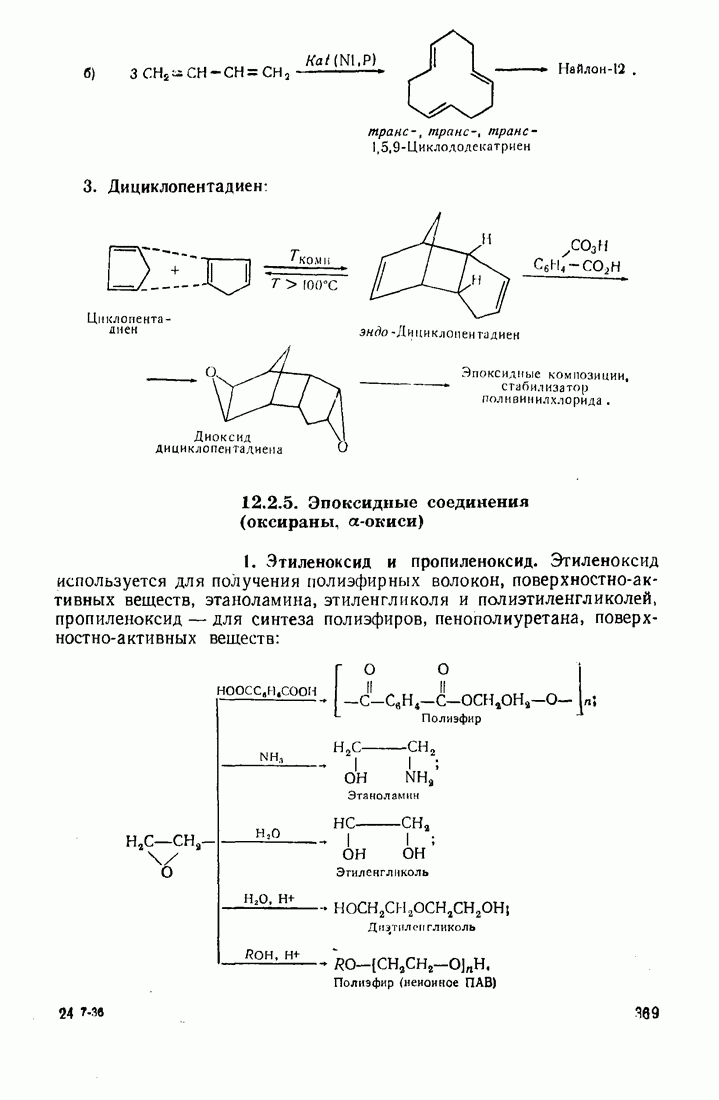
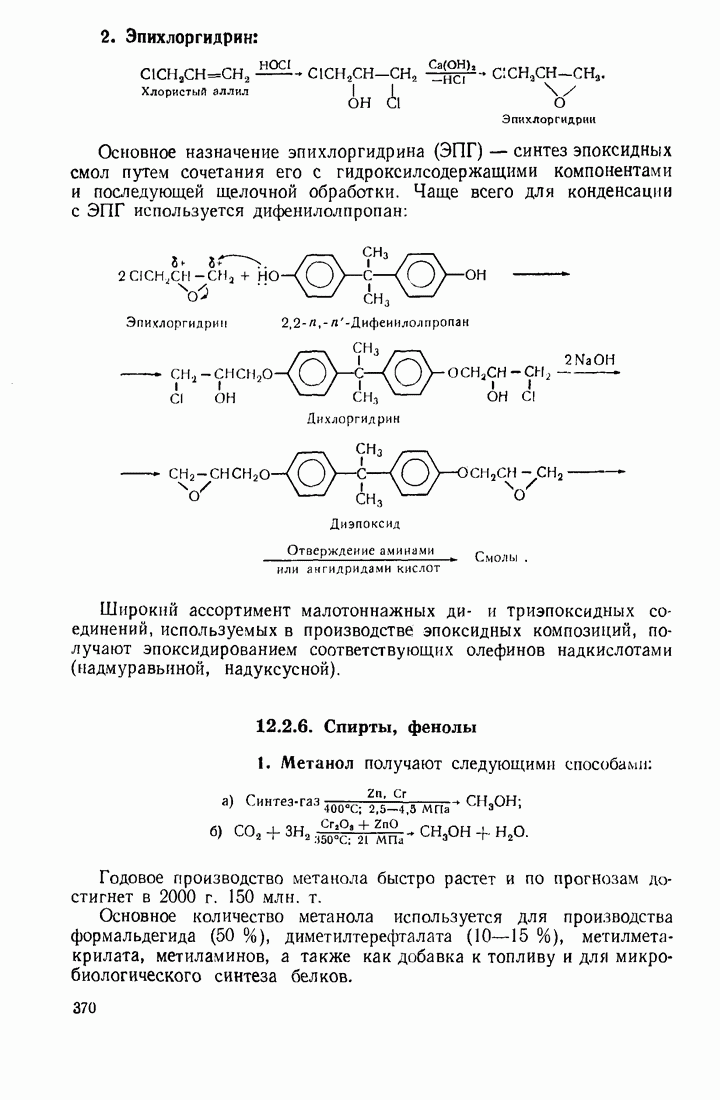
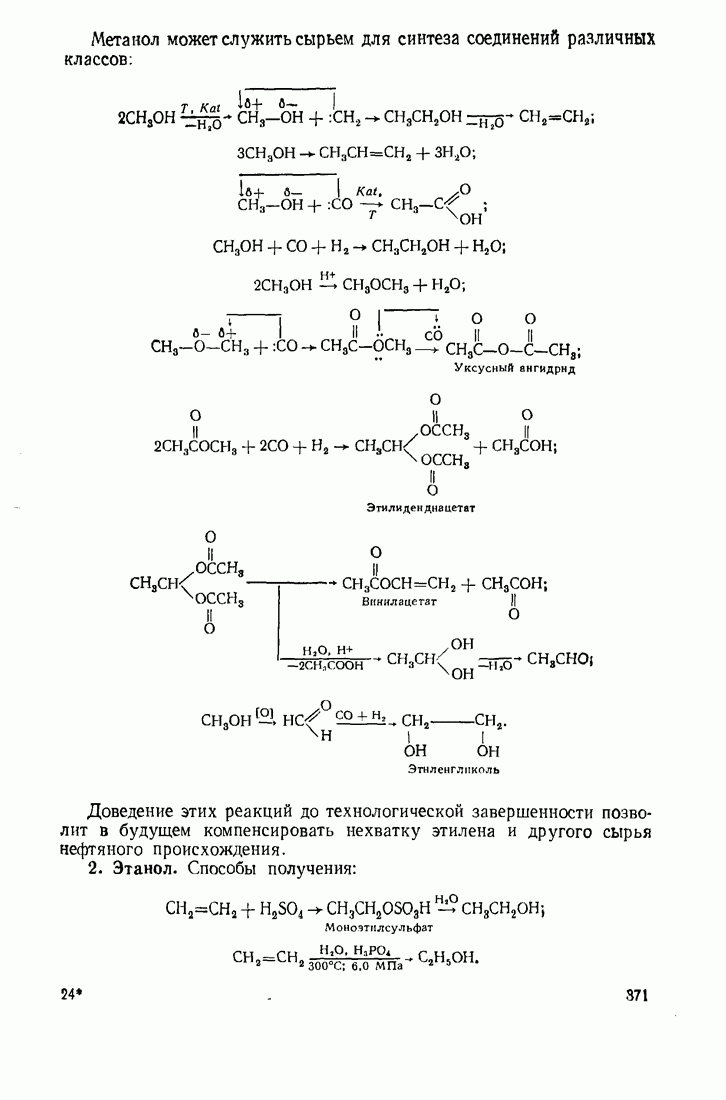
- 12.2. ПУТИ ИСПОЛЬЗОВАНИЯ УГЛЕВОДОРОДОВ И ИХ ПРОИЗВОДНЫХ
- 12.3. РАЗВИТИЕ ХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИ В СССР В ДВЕНАДЦАТОЙ ПЯТИЛЕТКЕ