| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Константы равновесия
Энергия (точнее, свободная энергия) химического процесса в соответствии с одним из фундаментальнейших уравнений химической термодинамики связана с константой равновесия этого процесса простым, но многозначительным равенством:  Это позволяет переписать уравнение для энергии процесса в индифферентном либо условно-индифферентном растворителе в
Это позволяет переписать уравнение для энергии процесса в индифферентном либо условно-индифферентном растворителе в


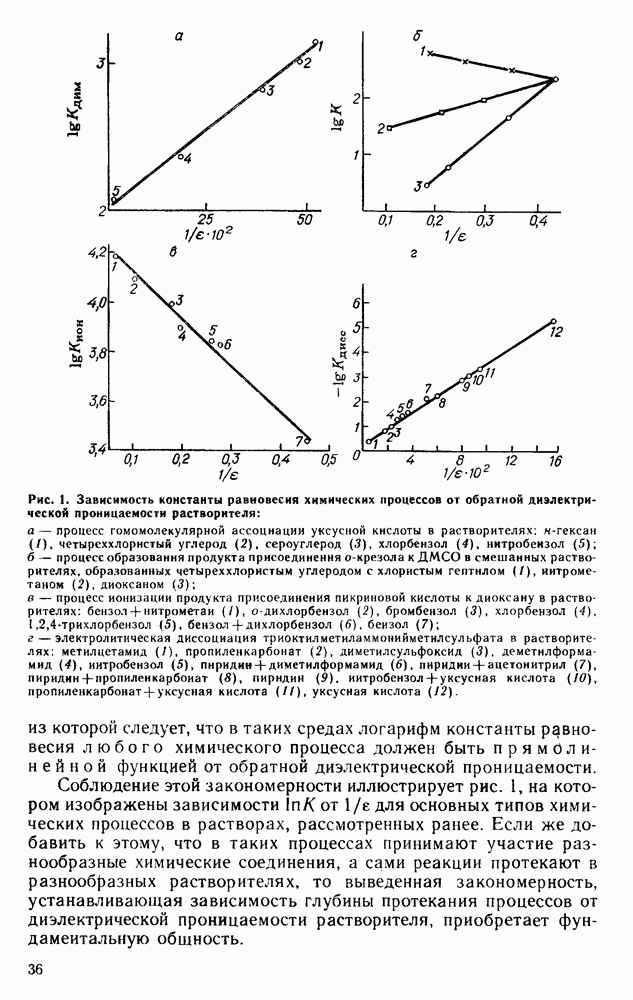
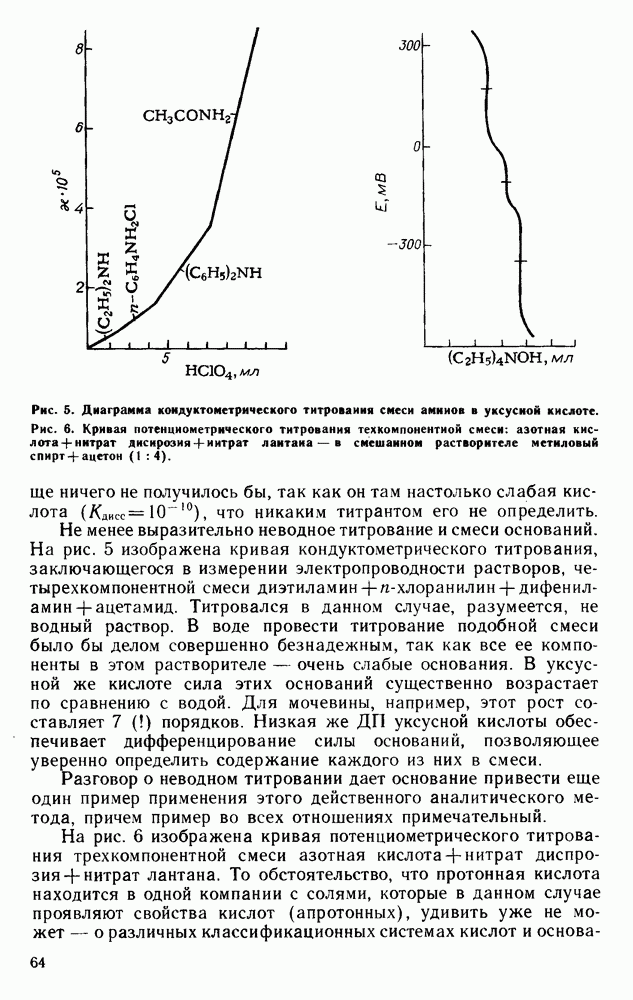
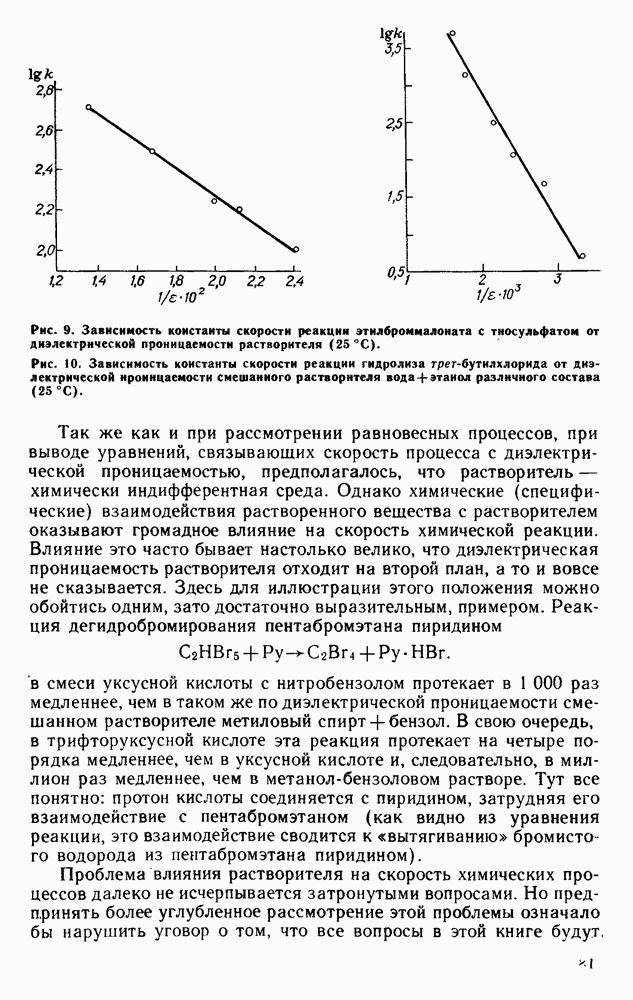
Рис. 1. Зависимость константы равновесия химических процессов от обратной диэлектрической проницаемости растворителя:
а — процесс гомомолекулярной ассоциации уксусной кислоты в растворителях:  -гексан
-гексан  четыреххлорнстый углерод (2), сероуглерод (3), хлорбензол (4), нитробензол (5); б - процесс образования продукта присоединения
четыреххлорнстый углерод (2), сероуглерод (3), хлорбензол (4), нитробензол (5); б - процесс образования продукта присоединения  -крезола к ДМСО в смешанных растворителях, образованных четыреххлористым углеродом с хлористым гептилом
-крезола к ДМСО в смешанных растворителях, образованных четыреххлористым углеродом с хлористым гептилом  нитрометаном (2), диоксаном (3); в — процесс ионизации продукта присоединения пикриновой кислоты к диоксану в растворителях:
нитрометаном (2), диоксаном (3); в — процесс ионизации продукта присоединения пикриновой кислоты к диоксану в растворителях:  нитрометан
нитрометан  -дихлорбензол (2), бромбензол (3), хлорбензол (4),
-дихлорбензол (2), бромбензол (3), хлорбензол (4),  -трихлорбензол (5), бензол+дихлорбензол (6), бензол (7); г - электролитическая диссоциация триоктилметиламмонийметилсульфата в растворителях: метилцетамид (1), пропиленкарбонат (2), диметилсульфоксид (3), деметнлформамид (4), нитробензол (5), пиридин+диметилформамид (6), пиридин
-трихлорбензол (5), бензол+дихлорбензол (6), бензол (7); г - электролитическая диссоциация триоктилметиламмонийметилсульфата в растворителях: метилцетамид (1), пропиленкарбонат (2), диметилсульфоксид (3), деметнлформамид (4), нитробензол (5), пиридин+диметилформамид (6), пиридин  ацетонитрил (7), пиридин+пропиленкарбонат (8), пиридин (9), нитробензол+уксусная кислота (10), пропиленкарбонат+уксусная кислота (11), уксусная кислота (12).
ацетонитрил (7), пиридин+пропиленкарбонат (8), пиридин (9), нитробензол+уксусная кислота (10), пропиленкарбонат+уксусная кислота (11), уксусная кислота (12).
из которой следует, что в таких средах логарифм константы равновесия любого химического процесса должен быть прямолинейной функцией от обратной диэлектрической проницаемости.
Соблюдение этой закономерности иллюстрирует рис. 1, на котором изображены зависимости  от
от  для основных типов химических процессов в растворах, рассмотренных ранее. Если же добавить к этому, что в таких процессах принимают участие разнообразные химические соединения, а сами реакции протекают в разнообразных растворителях, то выведенная закономерность, устанавливающая зависимость глубины протекания процессов от диэлектрической проницаемости растворителя, приобретает фундаментальную общность.
для основных типов химических процессов в растворах, рассмотренных ранее. Если же добавить к этому, что в таких процессах принимают участие разнообразные химические соединения, а сами реакции протекают в разнообразных растворителях, то выведенная закономерность, устанавливающая зависимость глубины протекания процессов от диэлектрической проницаемости растворителя, приобретает фундаментальную общность.
Таким образом, изменение растворителя ведет прежде всего к изменению константы равновесия процессов, протекающих в растворе.
Все сказанное о процессах в растворах приводит к несомненному выводу, который в дальнейшем станет и вовсе очевидным: ход этих процессов в сильнейшей степени зависит от химических и физических свойств растворителя. Многообразие же этих свойств в сочетании с внушительным перечнем жидкостей, выступающих в роли растворителя, делает желательным, даже необходимым рассмотрение проблемы, название которой
| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- ЧТО ТАКОЕ КИСЛОТЫ И ОСНОВАНИЯ?
- Кислота — еще одно определение
- Без растворителя
- Отступление (нелирическое)
- «Ониевые соли»
- Отступление (нелирическое)
- Сольвосистемы
- Отступление очередное, почти лирическое
- Сановный протон
- Кислоты, основания, заряды…
- Теория ЖМКО
- Отступления, лирическое и нелирическое
- РАВНОВЕСИЯ В РАСТВОРАХ
- Распад и объединение молекул
- Продукты присоединения
- «Химические привидения»
- Дискуссии, споры…
- Посолить суп…
- Откуда берутся ионы?
- Общая схема равновесий в растворах
- ВЛИЯНИЕ РАСТВОРИТЕЛЯ НА ОТДЕЛЬНЫЕ СТАДИИ РАВНОВЕСИЯ В РАСТВОРАХ
- Константы равновесия
- КЛАССИФИКАЦИЯ РАСТВОРИТЕЛЕЙ
- Донорные и акцепторные числа растворителей
- Управлять растворителем…
- РАСТВОРИТЕЛЬ КАК СРЕДСТВО УПРАВЛЕНИЯ ХИМИЧЕСКИМИ ПРОЦЕССАМИ
- Управление молекулярным состоянием веществ в растворах
- Управление гетеромолекулярной ассоциацией
- И активисты, и лентяи
- Управление ионизацией
- Управление электролитической диссоциацией
- ДИФФЕРЕНЦИРУЮЩЕЕ И НИВЕЛИРУЮЩЕЕ ДЕЙСТВИЯ РАСТВОРИТЕЛЕЙ НА СИЛУ ЭЛЕКТРОЛИТОВ
- Дифференцирующее и нивелирующее
- Отступление — кислотно-основное
- И физика, и химия
- Небольшое отступление, или как следует сравнивать силу электролитов
- Кислотные растворители
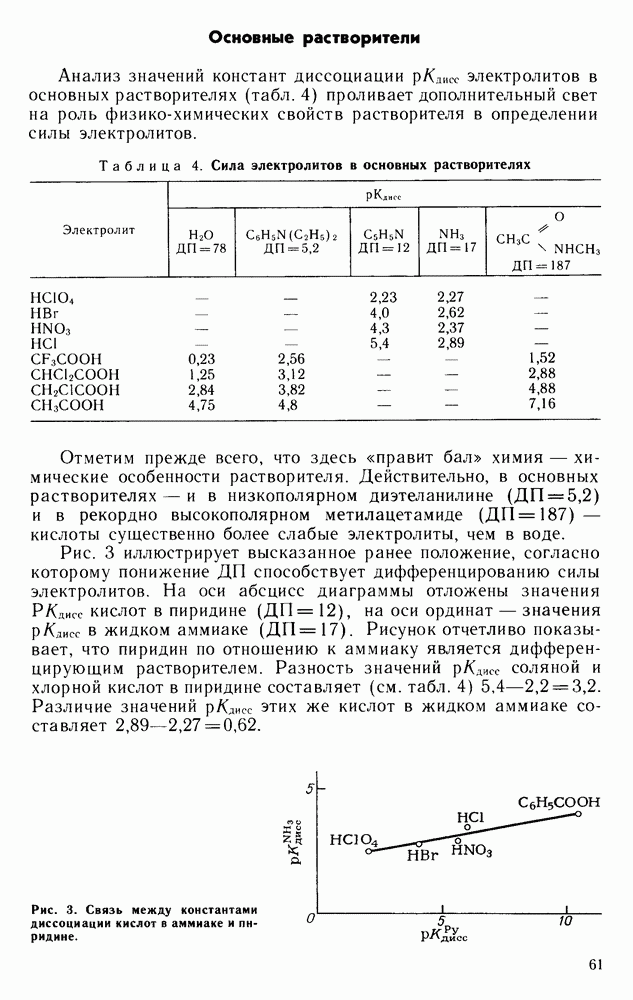
- Основные растворители
- Амфотерные растворители
- Отступление о достоинствах и недостатках объемного анализа
- Титрование в неводных растворителях
- РАСТВОРИМОСТЬ В НЕВОДНЫХ РАСТВОРИТЕЛЯХ
- Некоторые количественные закономерности
- О ХИМИЧЕСКИХ ФОРМАХ СУЩЕСТВОВАНИЯ ЖИВОГО ВЕЩЕСТВА ВО ВСЕЛЕННОЙ
- «Подходящий растворитель»
- ЭЛЕКТРОЛИЗ НЕВОДНЫХ РАСТВОРОВ
- Ряды напряжений в неводных растворах
- Только не из воды
- КИНЕТИКА РЕАКЦИЙ В НЕВОДНЫХ РАСТВОРИТЕЛЯХ
- Типы взаимодействий и их скорость в растворе
- СИНТЕЗЫ В НЕВОДНЫХ РАСТВОРАХ
- БИБЛИОГРАФИЧЕСКИЙ СПИСОК РЕКОМЕНДАТЕЛЬНОЙ ЛИТЁРАТУРЫ