| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 204. Энергетические уровни атомов
Опыты по
рассеянию ![]() -
частиц обнаружили существование в атомах тяжелого положительного ядра и
электронной оболочки. Дальнейшие сведения о свойствах атомов дало изучение
таких атомных процессов, которые сопровождаются изменением внутренней энергии
атома. Сюда относятся столкновения атомов с электронами, испускание и
поглощение света атомами и др. Исследуя эти процессы, удалось установить
своеобразные и очень важные закономерности, которым подчиняется внутренняя
энергия атомов.
-
частиц обнаружили существование в атомах тяжелого положительного ядра и
электронной оболочки. Дальнейшие сведения о свойствах атомов дало изучение
таких атомных процессов, которые сопровождаются изменением внутренней энергии
атома. Сюда относятся столкновения атомов с электронами, испускание и
поглощение света атомами и др. Исследуя эти процессы, удалось установить
своеобразные и очень важные закономерности, которым подчиняется внутренняя
энергия атомов.
Столкновения
электронов с атомами. Наиболее
простые условия для изучения передачи энергии от электронов к атомам могут быть
осуществлены в устройстве, изображенном на рис. 359. Из трубки 1 выкачан
воздух, и в нее введено небольшое количество одноатомных паров какого-нибудь
вещества, например ртути. Электроны, испускаемые накаленным катодом 2, ускоряются
разностью потенциалов ![]() действующей между катодом 2 и
металлической сеткой 4. Благодаря очень малой концентрации атомов электроны
пролетают короткий путь между катодом и первой сеткой без столкновений и
приобретают энергию
действующей между катодом 2 и
металлической сеткой 4. Благодаря очень малой концентрации атомов электроны
пролетают короткий путь между катодом и первой сеткой без столкновений и
приобретают энергию ![]() .
.

Рис. 359. Устройство для измерения потери
энергии электроном при движении в парах ртути: 1 – стеклянная трубка
заполненная парами ртути (давление тысячи доли ![]() ), 2 – накаленный катод (нагреватель
на чертеже не указан); 3 – анод, 4 и 5 – редкие металлические сетки,
соединенные между собой,
), 2 – накаленный катод (нагреватель
на чертеже не указан); 3 – анод, 4 и 5 – редкие металлические сетки,
соединенные между собой, ![]() и
и ![]() ускоряющая и тормозящая разность
потенциалов
ускоряющая и тормозящая разность
потенциалов
За
первой сеткой 4 на пути между нею и второй сеткой 5 электрическое поле равно
нулю, так как сетки находятся при одинаковом потенциале, и энергия электрона
может измениться только за счет соударения с атомом. Путь между сетками
выбирается достаточно длинным, так что каждый электрон испытывает хотя бы одно
соударение. Далее, на пути между второй сеткой и анодом действует разность
потенциалов ![]() ,
тормозящая электроны; ввиду этого до анода могут дойти только те электроны,
энергия которых больше
,
тормозящая электроны; ввиду этого до анода могут дойти только те электроны,
энергия которых больше ![]() .
.
Постепенно
увеличивая ![]() ,
определим запирающую разность потенциалов, т. е. то наименьшее значение
,
определим запирающую разность потенциалов, т. е. то наименьшее значение ![]() , при котором
электроны не доходят до анода и ток через гальванометр прекращается. Измерив
запирающую разность потенциалов, можно установить, теряют ли электроны энергию
при столкновениях с атомами. В самом деле, если на пути между сетками электроны
не теряют энергии, то запирающая разность потенциалов будет равна ускоряющей; в
противном случае она будет меньше. При этом, если каждый электрон отдает
энергию
, при котором
электроны не доходят до анода и ток через гальванометр прекращается. Измерив
запирающую разность потенциалов, можно установить, теряют ли электроны энергию
при столкновениях с атомами. В самом деле, если на пути между сетками электроны
не теряют энергии, то запирающая разность потенциалов будет равна ускоряющей; в
противном случае она будет меньше. При этом, если каждый электрон отдает
энергию ![]() ,
то превышение ускоряющего напряжения над тормозящим составит
,
то превышение ускоряющего напряжения над тормозящим составит ![]() .
.
Опыты
такого рода, проведенные с парами ртути, дали замечательный результат.
Оказалось, что передача энергии от электронов к атомам существенно зависит от
энергии электрона. Пока энергия электронов меньше, чем ![]() (т. е.
(т. е. ![]() ), электроны вовсе не
теряют энергии при соударениях с атомами (т. е.
), электроны вовсе не
теряют энергии при соударениях с атомами (т. е. ![]() ). Но когда энергия электронов
достигает (или немного превышает)
). Но когда энергия электронов
достигает (или немного превышает) ![]() (
(![]() ), потеря энергии при соударениях
сразу становится большой (т. е.
), потеря энергии при соударениях
сразу становится большой (т. е. ![]() ). При этом при столкновении
электрон отдает, а значит, атом ртути воспринимает всегда о дну и ту же порцию
энергии, равную
). При этом при столкновении
электрон отдает, а значит, атом ртути воспринимает всегда о дну и ту же порцию
энергии, равную ![]() . Очевидно, эта величина
характеризует свойство атома ртути: энергия его может меняться только на
конечную величину, равную
. Очевидно, эта величина
характеризует свойство атома ртути: энергия его может меняться только на
конечную величину, равную ![]() . Меньшую энергию атом ртути не
воспринимает.
. Меньшую энергию атом ртути не
воспринимает.
При изучении механики, теплоты, электричества мы не встречались с подобным явлением: энергия любого тела или системы тел в принципе могла изменяться непрерывно, т. е. сколь угодно малыми порциями. В случае же атома ртути непрерывное изменение энергии невозможно — энергия ртутного атома меняется только прерывно, т. е. на конечную величину.
Делая соответствующие опыты с другими веществами, мы приходим к тому же заключению о прерывности {дискретности) энергетических состояний атомов.
Исследование оптических спектров. Как известно (§ 173), элементы в газообразном состоянии обладают линейчатыми спектрами испускания и поглощения света. Каждому элементу свойственны определенные спектральные линии, отличные от линий других элементов. Так как атомы газа находятся в среднем на больших расстояниях и не влияют друг на друга, частоты линейчатого спектра элемента должны определяться свойствами отдельного атома этого элемента.
В гл. XXI мы выяснили, что световая энергия
существует в виде мельчайших неделимых порций — квантов; атомы должны,
следовательно, изучать и поглощать свет такими же порциями, квантами. Энергия
кванта пропорциональна частоте света ![]() , т. е. равна
, т. е. равна ![]() , где
, где ![]() — постоянная Планка. Энергия
испущенного атомом кванта по закону сохранения энергии равна разности энергий
атома до после излучения, т. е.
— постоянная Планка. Энергия
испущенного атомом кванта по закону сохранения энергии равна разности энергий
атома до после излучения, т. е.
![]() , (204.1)
, (204.1)
где ![]() — энергия
начального состояния атома (до излучения);
— энергия
начального состояния атома (до излучения); ![]() — энергия конечного состояния атома
(после излучения).
— энергия конечного состояния атома
(после излучения).
Соотношение
(204.1) связывает изменение энергии атома при испускании или поглощении света с
частотой последнего ![]() . Если бы энергия атома могла
испытывать всевозможные изменения, то в атомном спектре присутствовали бы
всевозможные частоты и он был бы сплошным подобно спектру раскаленного твердого
тела. В действительности же атомный спектр (т. е. спектр испускания или
поглощения одноатомного газа) не сплошной, а линейчатый. Он содержит только
некоторые определенные характерные для данного атома частоты. Следовательно,
энергия атома не может испытывать всевозможные, любые изменения. Энергия атома
может изменяться только на некоторые определенные значения. Зная спектр
вещества, нетрудно найти эти значения с помощью соотношения (204.1).
. Если бы энергия атома могла
испытывать всевозможные изменения, то в атомном спектре присутствовали бы
всевозможные частоты и он был бы сплошным подобно спектру раскаленного твердого
тела. В действительности же атомный спектр (т. е. спектр испускания или
поглощения одноатомного газа) не сплошной, а линейчатый. Он содержит только
некоторые определенные характерные для данного атома частоты. Следовательно,
энергия атома не может испытывать всевозможные, любые изменения. Энергия атома
может изменяться только на некоторые определенные значения. Зная спектр
вещества, нетрудно найти эти значения с помощью соотношения (204.1).
Так,
например, спектр поглощения ртутного пара содержит следующие линии (в порядке
убывания длин волн); ![]() и т. д. Подставляя в (204.1),
находим для первой линии
и т. д. Подставляя в (204.1),
находим для первой линии
![]() ,
,
или
![]()
Для второй
и третьей линий получаем соответственно ![]() и
и ![]() . Атом ртути может, таким образом,
воспринимать энергию только в виде порций, равных
. Атом ртути может, таким образом,
воспринимать энергию только в виде порций, равных ![]() и т. д. Наименьшая
воспринимаемая порция оказывается равной
и т. д. Наименьшая
воспринимаемая порция оказывается равной ![]() в согласии с результатом,
полученным из опытов по соударениям электронов с атомами.
в согласии с результатом,
полученным из опытов по соударениям электронов с атомами.
Итак, оба рассмотренных нами класса явлений — оптические спектры и взаимодействие атомов с электронами — указывают на прерывный (дискретный) характер внутренней энергии атомов. Энергия атома не может изменяться непрерывно. Она изменяется скачками на определенные, конечные порции, различные для разных атомов. Отсюда следует, что энергия атома не может быть любой, а может принимать только некоторые избранные значения, характерные для каждого атома. Возможные значения внутренней энергии атома получили название энергетических или квантовых уровней.
Схема энергетических уровней атома водорода, построенная на основании спектральных данных, изображена на рис. 360 в виде ряда параллельных линий. Расстояние между двумя линиями равно разности энергий двух состояний водородного атома и, следовательно, пропорционально частоте кванта, излучаемого при переходе из одного состояния в другое (более низкое). Поэтому расстояния между уровнями выражают в некотором масштабе частоты спектральных линий водорода.

Рис. 360. Схема энергетических уровней атома
водорода. Горизонтальные линии — энергетические уровни (![]() — номер уровня). За
начало отсчета но шкале энергий принята наименьшая внутренняя энергия атома
водорода, т. е. энергия уровня
— номер уровня). За
начало отсчета но шкале энергий принята наименьшая внутренняя энергия атома
водорода, т. е. энергия уровня ![]() . Вертикальные линии — переходы с
верхних энергетических уровней на нижние. Длина такой линии дает энергию
. Вертикальные линии — переходы с
верхних энергетических уровней на нижние. Длина такой линии дает энергию ![]() светового
кванта, излучаемого при данном переходе. Переходы группируются в серии; серия
Лаймана — переходы с уровней
светового
кванта, излучаемого при данном переходе. Переходы группируются в серии; серия
Лаймана — переходы с уровней ![]() на уровень
на уровень ![]() , серия Бальмера —
переходы с уровней
, серия Бальмера —
переходы с уровней ![]() на уровень
на уровень ![]() и т. д. (см. также §
175)
и т. д. (см. также §
175)
Атом,
находящийся в одном из высших энергетических состояний (обозначенных номером ![]() на рис. 360),
через небольшой промежуток времени (около
на рис. 360),
через небольшой промежуток времени (около ![]() ) перейдет в более бедное энергией
состояние, испуская соответствующий квант. Из низшего энергетического состояния
) перейдет в более бедное энергией
состояние, испуская соответствующий квант. Из низшего энергетического состояния
![]() атом
не может самопроизвольно (без сообщения энергии извне) перейти в другое
состояние. Следовательно, низшее состояние является устойчивым). При нормальных
условиях все атомы находятся в низшем энергетическом состоянии, и газ не
светится.
атом
не может самопроизвольно (без сообщения энергии извне) перейти в другое
состояние. Следовательно, низшее состояние является устойчивым). При нормальных
условиях все атомы находятся в низшем энергетическом состоянии, и газ не
светится.
Сообщая
атому энергию, мы можем возбудить его, т. е. перевести из нормального (низшего)
состояния в одно из высших энергетических состоянии. В случае водорода
расстояние от низшего энергетического уровня ![]() до ближайшего высшего уровня
составляет
до ближайшего высшего уровня
составляет ![]() .
Это наименьшая порция энергии и, которую находящийся в низшем состоянии
водородный атом может поглотить. Меньшей энергии атом водорода не может
воспринять, ибо у него не существует состояний, энергия которых отличается от
энергии нормального состояния меньше чем на
.
Это наименьшая порция энергии и, которую находящийся в низшем состоянии
водородный атом может поглотить. Меньшей энергии атом водорода не может
воспринять, ибо у него не существует состояний, энергия которых отличается от
энергии нормального состояния меньше чем на ![]() . Для атома ртути аналогичная величина
равна, как мы видели,
. Для атома ртути аналогичная величина
равна, как мы видели, ![]() .
.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие к первому изданию
- Раздел первый. Колебания и волны
- Глава I. Основные понятия. Механические колебания
- § 1. Периодические движения. Период
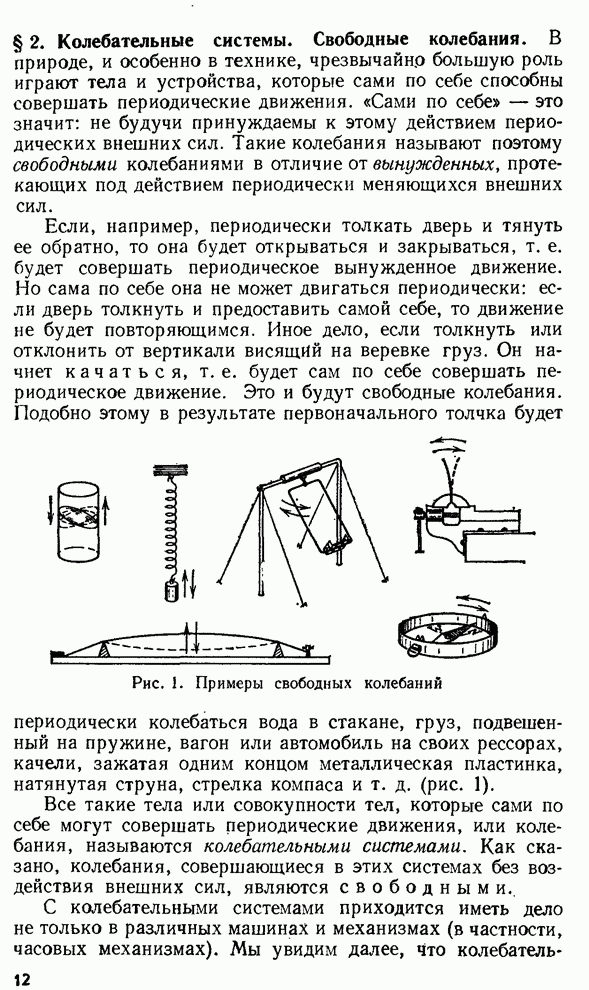
- § 2. Колебательные системы
- § 3. Маятник; кинематика его колебаний
- § 4. Колебания камертона
- § 5. Гармоническое колебание. Частота
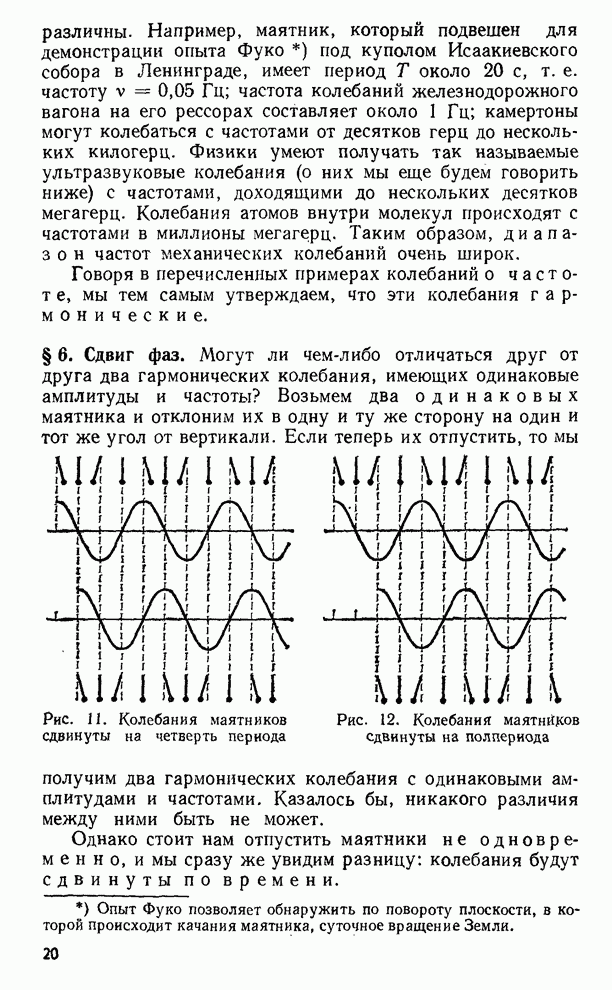
- § 6. Сдвиг фаз
- § 7. Динамика колебаний маятника
- § 8. Формула периода математического маятника
- § 9. Упругие колебания
- § 10. Крутильные колебания
- § 11. Влияние трения. Затухание
- § 12. Вынужденные колебания
- § 13. Резонанс
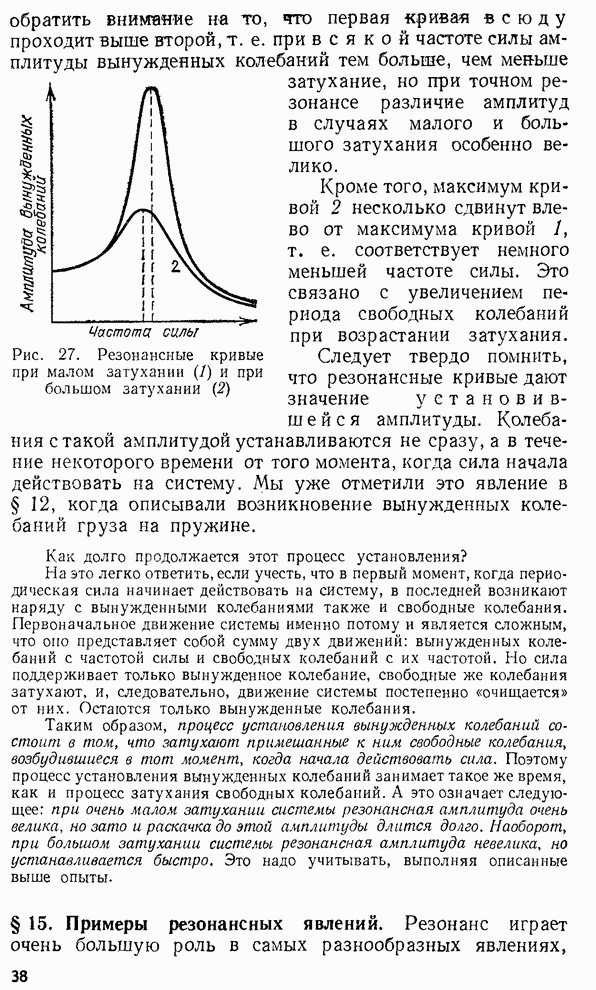
- § 14. Влияние трения на резонансные явления
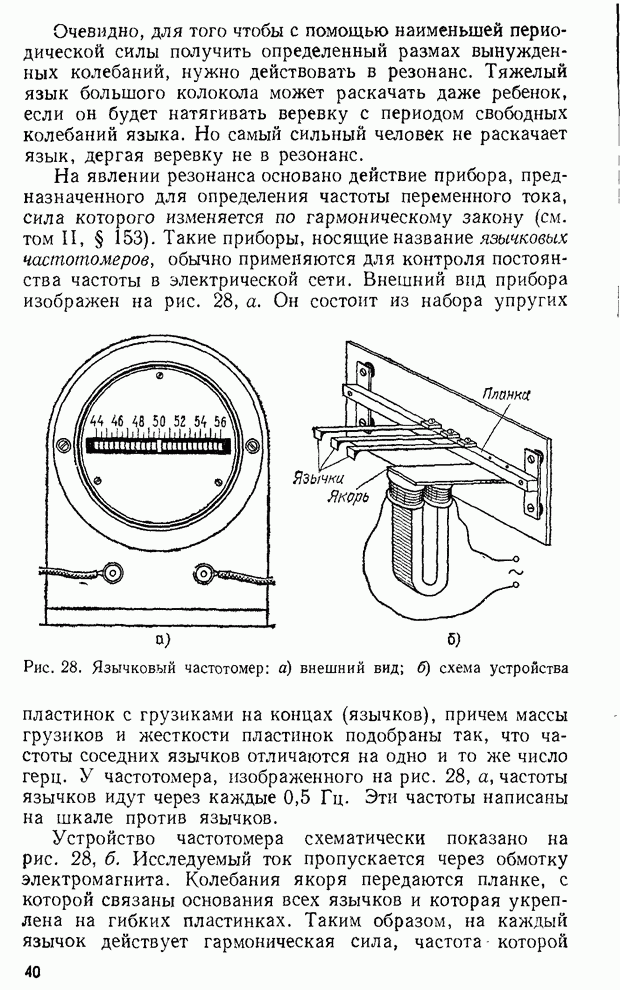
- § 15. Примеры резонансных явлений
- § 16. Резонансные явления при действии негармонической периодической силы
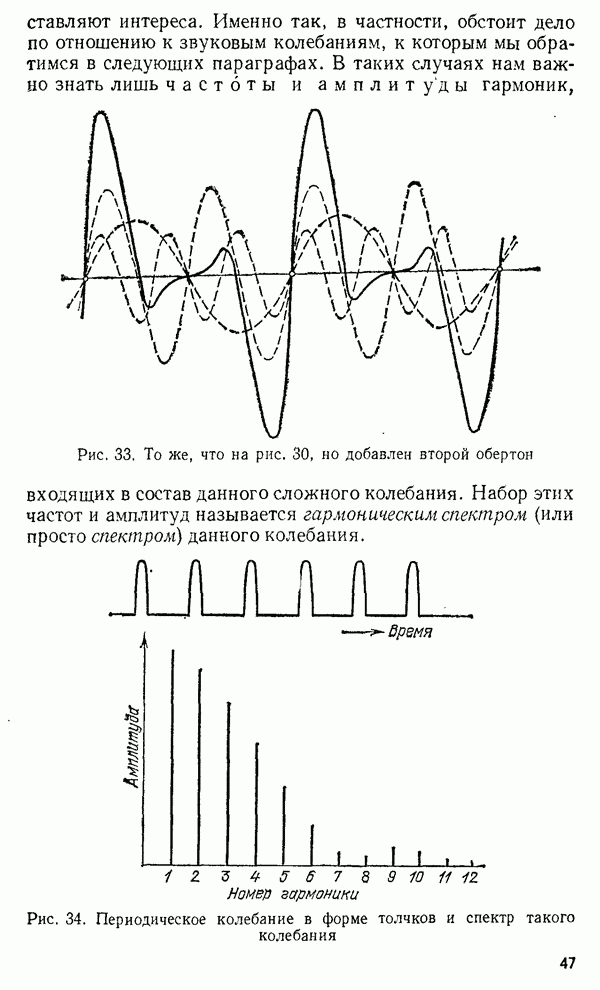
- § 17. Форма периодических колебаний и ее связь с гармоническим составом этих колебаний
- Глава II. Звуковые колебания
- § 18. Звуковые колебания
- § 19. Предмет акустики
- § 20. Музыкальный тон. Громкость и высота тона
- § 21. Тембр
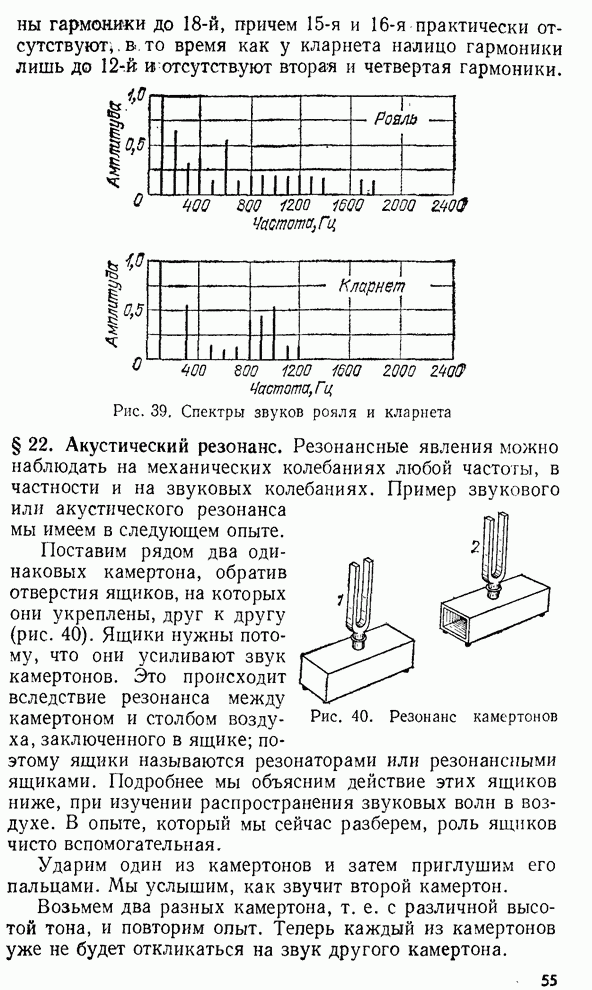
- § 22. Акустический резонанс
- § 23. Запись и воспроизведение звука
- § 24. Анализ и синтез звука
- § 25. Шумы
- Глава III. Электрические колебания
- § 26. Электрические колебания. Методы их наблюдения
- § 27. Колебательный контур
- § 28. Аналогия с механическими колебаниями. Формула Томсона
- § 29. Электрический резонанс
- § 30. Незатухающие колебания. Автоколебательные системы
- § 31. Ламповый генератор электрических колебаний
- Глава IV. Волновые явления
- § 32. Учение о колебаниях
- § 33. Волновые явления
- § 34. Скорость распространения волн
- § 35. Радиолокация, гидроакустическая локация и звукометрия
- § 36. Поперечные волны в шнуре
- § 37. Продольные волны в столбе воздуха
- § 38. Волны на поверхности жидкости
- § 39. Перенос энергии волнами
- § 40. Отражение волн
- § 41. Дифракция
- § 42. Направленное излучение
- Глава V. Интерференция волн
- § 43. Наложение волн
- § 44. Интерференция волн
- § 45. Условия образования максимумов и минимумов
- § 46. Интерференция звуковых волн
- § 47. Стоячие волны
- § 48. Колебания упругих тел как стоячие волны
- § 49. Свободные колебания струны
- § 50. Стоячие волны в пластинках и других протяженных телах
- § 51. Резонанс при наличии многих собственных частот
- § 52. Условия хорошего излучения звука
- § 53. Бинауральный эффект. Звукопеленгация
- Глава VI. Электромагнитные волны
- § 54. Электромагнитные волны
- § 55. Условия хорошего излучения электромагнитных волн
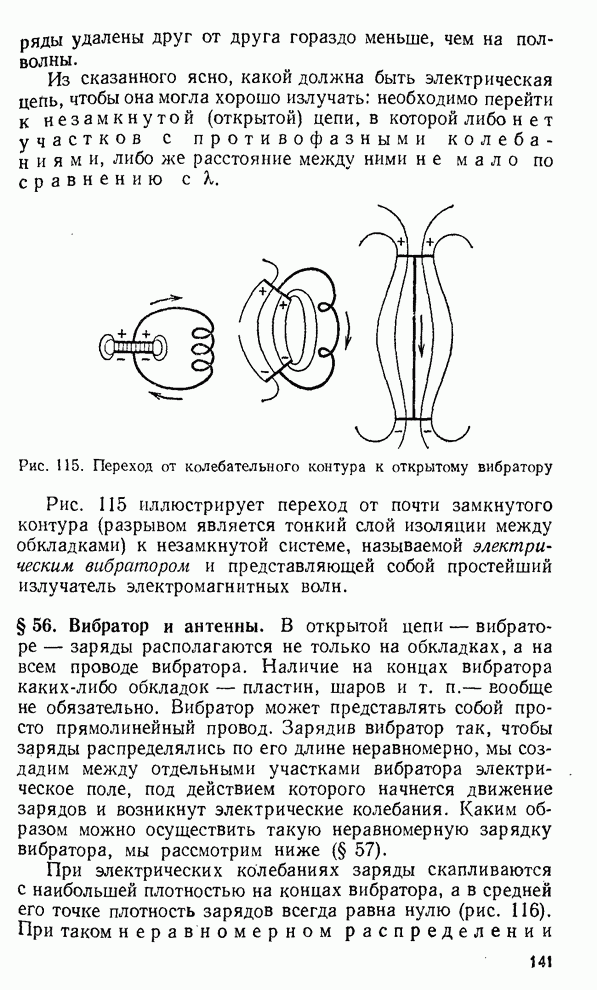
- § 56. Вибратор и антенны
- § 57. Опыты Герца по получению и исследованию электромагнитных волн. Опыты Лебедева
- § 58. Электромагнитная теория света. Шкала электромагнитных волн
- § 59 Опыты с электромагнитными волнами
- § 60. Изобретение радио Поповым
- § 61. Современная радиосвязь
- § 62. Другие применения радио
- § 63. Распространение радиоволн
- § 64. Заключительные замечания
- Раздел второй. Геометрическая оптика
- Глава VII. Общая характеристика световых явлений
- § 65. Разнообразные действия света
- § 66. Интерференция света. Цвета тонких пленок
- § 67. Краткие сведения из истории оптики
- Глава VIII. Фотометрия и светотехника
- § 68. Энергия излучения. Световой поток
- § 69. Точечные источники света
- § 70. Сила света и освещенность
- § 71. Законы освещенности
- § 72. Единицы световых величин
- § 73. Яркость источников
- § 74. Задачи светотехники
- § 75. Приспособления для концентрации светового потока
- § 76. Отражающие и рассеивающие тела
- § 77. Яркость освещенных поверхностей
- § 78. Световые измерения и измерительные приборы
- Глава IX. Основные законы геометрической оптики
- § 79. Прямолинейное распространение волн
- § 80. Прямолинейное распространение света и световые лучи
- § 81. Законы отражения и преломления света
- § 82. Обратимость световых лучей
- § 83. Показатель преломления
- § 84. Полное внутреннее отражение
- § 85. Преломление в плоскопараллельной пластинке
- § 86. Преломление в призме
- Глава X. Применение отражения и преломления света для получения изображений
- § 87. Источник света и его изображение
- § 88. Преломление в линзе
- § 89. Изображение в линзе точек, лежащих на главной оптической оси. Формула линзы.
- § 90. Применения формулы тонкой линзы. Действительные и мнимые изображения.
- § 91. Изображение точечного источника и протяженного объекта в плоском зеркале. Изображение точечного источника в сферическом зеркале
- § 92. Фокус и фокусное расстояние сферического зеркала
- § 93. Связь между положениями источника и его изображения на главной оси сферического зеркала
- § 94. Способы изготовления линз и зеркал
- § 95. Изображение протяженных объектов в сферическом зеркале и линзе
- § 96. Увеличение при изображении объектов в сферическом зеркале и линзе
- § 97. Построение изображений в сферическом зеркале и линзе
- § 98. Оптическая сила линз
- Глава XI. Оптические системы и их погрешности
- § 99. Оптическая система
- § 100. Главные плоскости и главные точки системы
- § 101. Построение изображений в системе
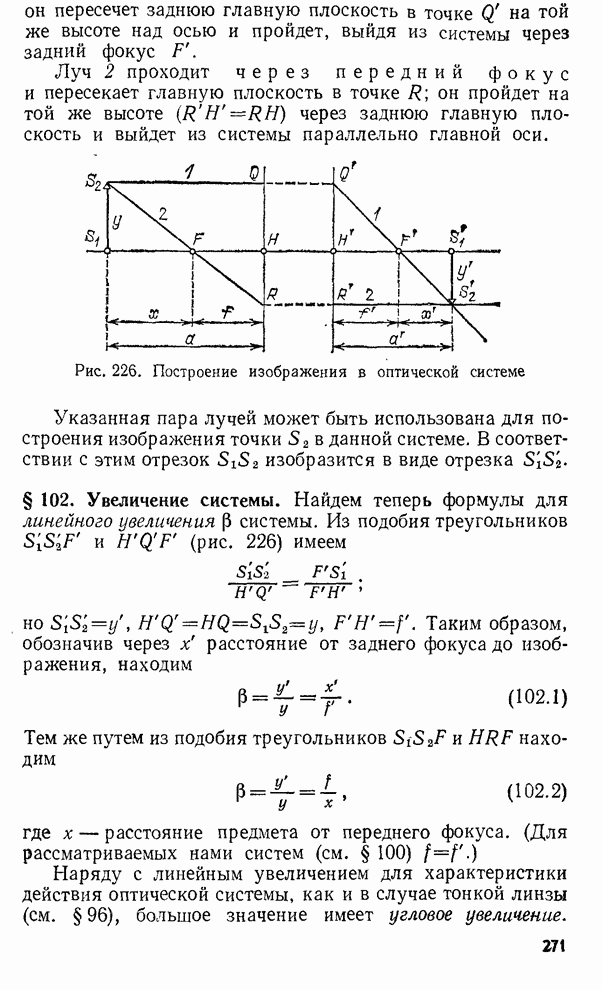
- § 102. Увеличение системы
- § 103. Недостатки оптических систем
- § 104. Сферическая аберрация
- § 105. Астигматизм
- § 106. Хроматическая аберрация
- § 107. Ограничение пучков в оптических системах
- § 108. Светосила линзы
- § 109. Яркость изображения
- Глава XII. Оптические приборы
- § 110. Проекционные оптические приборы
- § 111. Фотографический аппарат
- § 112. Глаз как оптическая система
- § 113. Оптические приборы, вооружающие глаз
- § 114. Лупа
- § 115. Микроскоп
- § 116. Разрешающая способность микроскопа
- § 117. Зрительные трубы
- § 118. Увеличение зрительной трубы
- § 119. Телескопы
- § 120. Яркость изображения для протяженных и точечных источников
- § 121. «Ночезрительная труба» Ломоносова
- § 122. Зрение двумя глазами и восприятие глубины пространства. Стереоскоп.
- Раздел третий. Физическая оптика
- Глава XIII. Интерференция света
- § 123. Геометрическая и физическая оптика
- § 124. Опытное осуществление интерференции света
- § 125. Объяснение цветов тонких пленок
- § 126. Кольца Ньютона
- § 127. Определение длины световой волны с помощью колец Ньютона
- Глава XIV. Дифракция света
- § 128. Пучки лучей и форма волновой поверхности
- § 129. Принцип Гюйгенса
- § 130. Законы отражения и преломления света на основе принципа Гюйгенса
- § 131. Принцип Гюйгенса в толковании Френеля
- § 132. Простейшие дифракционные явления
- § 133. Объяснение дифракции по методу Френеля
- § 134. Разрешающая сила оптических инструментов
- § 135. Дифракционные решетки
- § 136. Дифракционная решетка как спектральный прибор
- § 137. Изготовление дифракционных решеток
- § 138. Дифракция при косом падении света на решетку
- Глава XV. Физические принципы оптической голографии
- § 139. Фотография и голография
- § 140. Запись голограммы с помощью плоской опорной волны
- § 141. Получение оптических изображений по методу восстановления волнового фронта
- § 142. Голографирование по методу встречных световых пучков
- § 143. Использование голографии в оптической интерферометрии
- Глава XVI. Поляризация света и поперечность световых волн
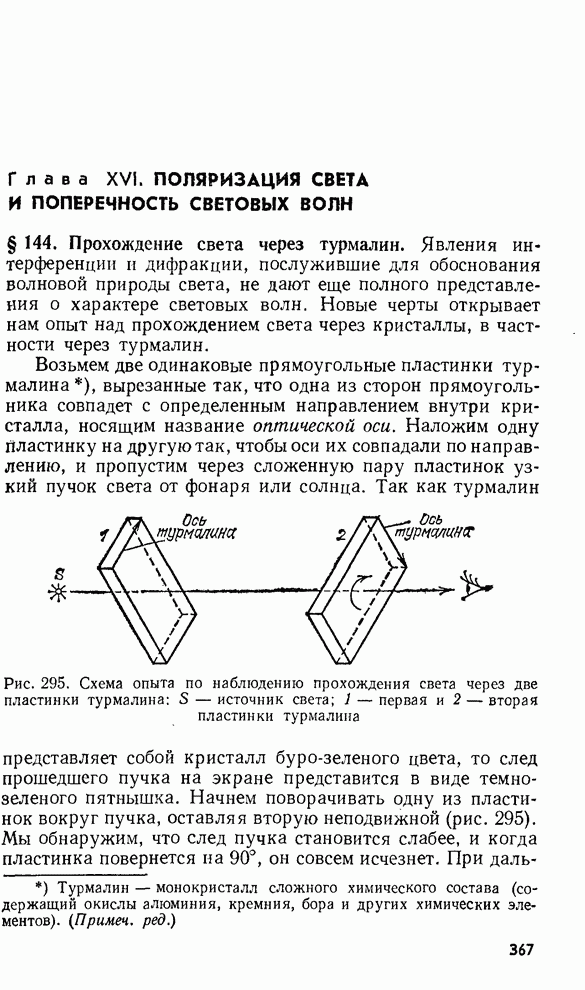
- § 144. Прохождение света через турмалин
- § 145. Гипотезы, объясняющие наблюдаемые явления. Понятие о поляризованном свете
- § 146. Механическая модель явлений поляризации
- § 147. Поляроиды
- § 148. Поперечность световых волн и электромагнитная теория света
- Глава XVII. Шкала электромагнитных волн
- § 149. Способы исследования электромагнитных волн различной длины
- § 150. Инфракрасное и ультрафиолетовое излучение
- § 151. Открытие рентгеновских лучей
- § 152. Различные действия рентгеновских лучей
- § 153. Устройство рентгеновской трубки
- § 154. Происхождение и природа рентгеновских лучей
- § 155. Шкала электромагнитных волн
- Глава XVIII. Скорость света
- § 156. Первые попытки определения скорости света
- § 157. Определение скорости света Рёмером
- § 158. Определение скорости света по методу вращающегося зеркала
- Глава XIX. Дисперсия света и цвета тел
- § 159. Состояние вопроса о цвете тел до исследований Ньютона
- § 160. Основное открытие Ньютона в оптике
- § 161. Истолкование наблюдений Ньютона
- § 162. Дисперсия показателя преломления различных материалов
- § 163. Дополнительные цвета
- § 164. Спектральный состав света различных источников
- § 165. Свет и цвета тел
- § 166. Коэффициенты поглощения, отражения и пропускания
- § 167. Цветные тела, освещенные белым светом
- § 168. Цветные тела, освещенные цветным светом
- § 169. Маскировка и демаскировка
- § 170. Насыщенность цветов
- § 171. Цвет неба и зорь
- Глава XX. Спектры и спектральные закономерности
- § 172. Спектральные аппараты
- § 173. Типы спектров испускания
- § 174. Происхождение спектров различных типов
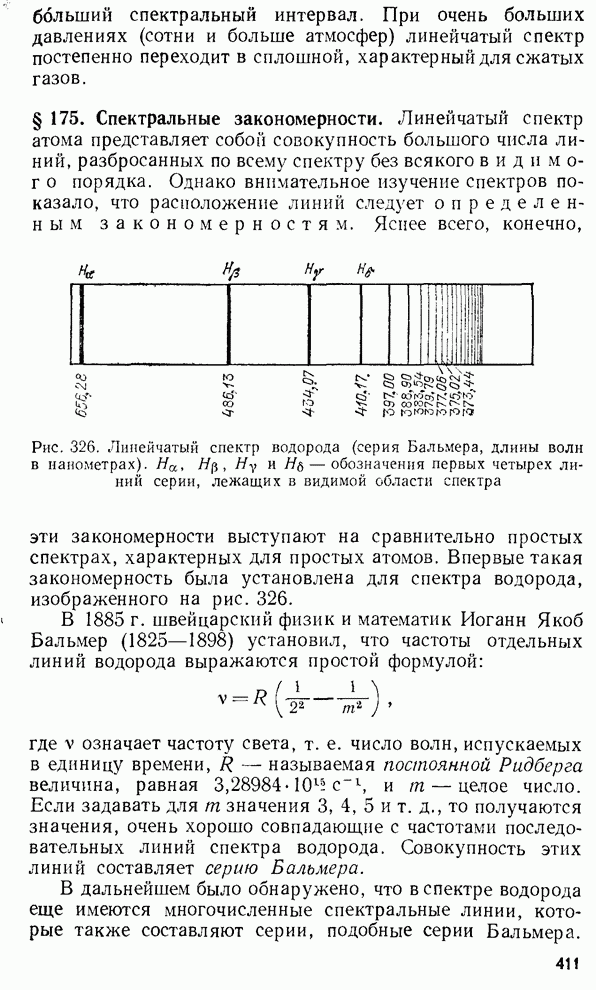
- § 175. Спектральные закономерности
- § 176. Спектральный анализ по спектрам испускания
- § 177. Спектры поглощения жидких и твердых тел
- § 178. Спектры поглощения атомов. Линии Фраунгофера
- § 179. Излучение накаленных тел. Абсолютно черное тело
- § 180. Зависимость излучения накаленных тел от температуры. Лампы накаливания
- § 181. Оптическая пирометрия
- XXI. Действия света
- § 182. Действия света на вещество. Фотоэлектрический эффект
- § 183. Законы фотоэлектрического эффекта
- § 184. Понятие о световых квантах
- § 185. Применение фотоэлектрических явлений
- § 186. Фотолюминесценция. Правило Стокса
- § 187. Физический смысл правила Стока
- § 188. Люминесцентный анализ
- § 189. Фотохимические действия света
- § 190. Роль длины волны в фотохимических процессах
- § 191. Фотография
- § 192. Фотохимическая теория зрения
- § 193. Длительность зрительного ощущения
- Раздел четвертый. Атомная и ядерная физика
- Глава XXII. Строение атома
- § 194. Представление об атомах
- § 195. Постоянная Авогадро. Размеры и массы атомов
- § 196. Элементарный электрический заряд
- § 197. Единицы заряда, массы и энергии в атомной физике
- § 198. Измерение массы заряженных частиц. Масс-спектрограф
- § 199. Масса электрона. Зависимость массы от скорости
- § 200. Закон Эйнштейна
- § 201. Массы атомов; изотопы
- § 202. Разделение изотопов. Тяжелая вода
- § 203. Ядерная модель атома
- § 204. Энергетические уровни атомов
- § 205. Вынужденное излучение света. Квантовые генераторы
- § 206. Атом водорода. Своеобразие законов движения электрона в атоме
- § 207. Многоэлектронные атомы. Происхождение оптических и рентгеновских спектров атомов
- § 208. Периодическая система элементов Менделеева
- § 209. Квантовые и волновые свойства фотонов
- § 210. Понятие о квантовой (волновой) механике
- Глава XXIII. Радиоактивность
- § 211. Открытие радиоактивности. Радиоактивные элементы
- § 212. L-, B-, Г- излучение. Камера Вильсона
- § 213. Способы регистрации заряженных частиц
- § 214. Природа радиоактивного излучения
- § 215. Радиоактивный распад и радиоактивные превращения
- § 216. Применения радиоактивности
- § 217. Ускорители
- Глава XXIV. Атомные ядра и ядерная энергия
- § 218. Понятие о ядерных реакциях
- § 219. Ядерные реакции и превращение элементов
- § 220. Свойства нейтронов
- § 221. Ядерные реакции под действием нейтронов
- § 222. Искусственная радиоактивность
- § 223. Позитрон
- § 224. Применение закона Эйнштейна к процессам аннигиляции и образования пар
- § 225. Строение атомного ядра
- § 226. Ядерная энергия. Источник энергии звезд.
- § 227. Деление урана
- § 228. Применения незатухающей цепной реакции деления. Атомная и водородная бомбы
- § 229. Ядерные реакторы и их применения
- Глава XXV. Элементарные частицы
- § 230. Общие замечания
- § 231. Нейтрино
- § 232. Ядерные силы. Мезоны
- § 233. Частицы и античастицы
- § 234. Частицы и взаимодействия
- § 235. Детекторы элементарных частиц
- § 236. Парадокс часов
- § 237. Космическое излучение (космические лучи)
- Глава XXVI. Новые достижения в физике элементарных частиц
- § 238. Ускорители и экспериментальная техника
- § 239. Адроны и кварки
- § 240. Кварковая структура андронов
- § 241. Кварковая модель и процессы образования и распада адронов
- § 242. Лептоны. Промежуточные бозоны. Единство всех взаимодействий
- Заключение