| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
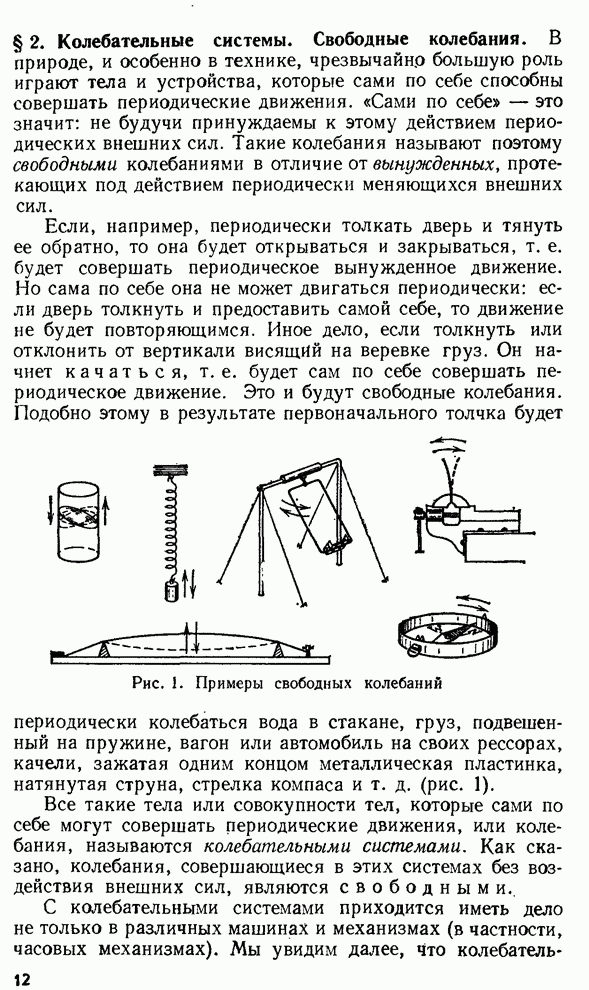
§ 210. Понятие о квантовой (волновой) механике
Изучение строения атома привело к выводу, что поведение электронов в атоме, так же как поведение фотонов, противоречит привычным законам классической физики, т. е. законам, установленным в опытах с телами макроскопических размеров. Существование дискретных уровней энергии электронной оболочки атома, закономерности переходов между уровнями и заполнения этих энергетических состояний невозможно было объяснить, пользуясь обычными представлениями механики и законами электромагнетизма.
Важный шаг в разъяснении этих противоречий был сделан в 1923 г. французским физиком Луи де Бройлем (р. 1892). Он выдвинул и обосновал предположение о том, что не только фотоны, но и любые частицы обладают волновыми свойствами, которые не учитываются классическими законами, но играют существенную роль в атомных явлениях.
Кванты
электромагнитного излучения — фотоны, как мы видели выше, характеризуются
импульсом ![]() .
Вместе с тем световая волна с частотой
.
Вместе с тем световая волна с частотой ![]() имеет длину
имеет длину ![]() . Исключая из этих выражений частоту, получаем связь между
длиной волны и импульсом фотона
. Исключая из этих выражений частоту, получаем связь между
длиной волны и импульсом фотона
![]() (210.1)
(210.1)
Если в
самом деле, в рамках представления о корпускулярно-волновом дуализме, свойства
фотонов и других частиц подобны друг другу, то это соотношение должно быть
применимо теперь к любым частицам. Таким образом, была получена формула для
длины волны де Бройля, т. е. для длины волны, которую следует сопоставить
частице с импульсом ![]() , чтобы описать ее волновые
свойства. Эта формула также имеет вид (210.1). Если скорость частицы с массой
покоя
, чтобы описать ее волновые
свойства. Эта формула также имеет вид (210.1). Если скорость частицы с массой
покоя ![]() мала
по сравнению со скоростью .света, то формула для длины волны де Бройля примет
вид
мала
по сравнению со скоростью .света, то формула для длины волны де Бройля примет
вид
![]() (210.2)
(210.2)
Для проверки справедливости гипотезы де Бройля были произведены опыты по рассеянию электронов на кристаллах.
В свое время рассеяние рентгеновского излучения па кристаллах было использовано для доказательства их волновой природы (см. § 154). Благодаря интерференции вторичных волн, испускаемых правильно расположенными атомами кристалла, рассеяние происходит не в любых направлениях, а только под некоторыми определенными углами к падающему пучку. На фотопленке, расположенной позади рассеивающего кристалла (рис. 373), помимо центрального пятна от прямого пучка, получается система пятен от рассеянного (дифрагированного) излучения. Пример такого снимка приведен на рис. 374, а.

Рис. 373. Схема опыта по наблюдению дифракции рентгеновского излучения на кристаллах: 1 - рентгеновская трубка. 2 — свинцовая диафрагма, вырезающая узкий пучок рентгеновского излучения 3), 4 — поликристалический образец, 5 — фотопленка (в черной бумаге), б и 7 — пучки рассеянного кристаллом рентгеновского излучения

Рис. 374. Фотоснимки дифракции
рентгеновского излучения ![]() и электронов
и электронов ![]() на поликристаллическом
золоте
на поликристаллическом
золоте
Оказалось, что если кристалл вместо рентгеновского излучения облучать электронами, то рассеянные электроны также образуют на пленке систему колец, аналогичную кольцам от рассеянного рентгеновского излучения (рис. 374, б). Отсюда следовал удивительный вывод: электроны способны к интерференции, т. е. они обладают волновыми свойствами.
В
дальнейшем дифракционные явления наблюдались и с другими частицами — с атомами,
молекулами, нейтронами. Эти опыты неопровержимо доказали, что мельчайшие
частицы вещества в некоторых явлениях ведут себя, как волны. Опыты позволили
также определить длину волны, которая должна быть связана с данной частицей,
чтобы объяснить ее дифракцию. Было найдено полное согласие с формулой де Бройля
(210.2): длина волны оказалась обратно пропорциональной произведению массы ![]() частицы на ее
скорость
частицы на ее
скорость ![]() ,
а коэффициент пропорциональности — равным постоянной Планка
,
а коэффициент пропорциональности — равным постоянной Планка ![]() .
.
Постоянная
Планка очень мала: ![]() ; ввиду этого длина волны де Бройля
для частиц сколько-нибудь заметной массы совершенно ничтожна. Согласно формуле
де Бройля пылинке массы один микрограмм
; ввиду этого длина волны де Бройля
для частиц сколько-нибудь заметной массы совершенно ничтожна. Согласно формуле
де Бройля пылинке массы один микрограмм ![]() , летящей со скоростью
, летящей со скоростью ![]() , соответствует
длина волны
, соответствует
длина волны ![]() .
Эта величина исчезающе мала по сравнению даже с размерами атомных ядер.
.
Эта величина исчезающе мала по сравнению даже с размерами атомных ядер.
Иначе
обстоит дело с электронами или атомами, массы которых несравненно меньше
микрограмма. При не слишком большой скорости им соответствует длина волны того
же порядка, что и длины волн рентгеновского излучения. Так, для атома гелия с
энергией ![]() (энергия
теплового движения при комнатной температуре)
(энергия
теплового движения при комнатной температуре) ![]() ; для электрона с энергией
; для электрона с энергией ![]() .
.
Из оптики мы знаем, что волновой характер света проявляется весьма отчетливо в тех случаях, когда длины волн сравнимы с размерами тел, с которыми свет взаимодействует. Так, при прохождении света через отверстие размером в несколько длин волн или при отражении от дифракционной решетки с малым расстоянием между штрихами и т. д. нельзя не учитывать волновых свойств света. Напротив, при прохождении света через окно квартиры или при отражении от зеркала с редкими царапинами дифракционные явления можно не принимать во внимание; они практически незаметны. Точно так же волновые свойства частиц имеют значение только тогда, когда длина волны де Бройля не мала по сравнению с размерами объектов, с которыми происходит взаимодействие. В процессах взаимодействия атомов с электронами и другими мельчайшими частицами, для которых длина волны де Бройля порядка атомных размеров, волновые свойства частиц играют существенную и даже определяющую роль. Тем более это относится к процессам, связанным с поведением электронов внутри атомов или молекул.
При взаимодействии частиц макроскопических размеров, для которых, как мы видели, длина волны де Бройля в миллиарды раз меньше их размеров, учет волновых свойств совершенно излишен. Вот почему классическая механика, которая была выведена из наблюдений над большими телами и в которой о волновых свойствах тел даже и не подозревали, прекрасно удовлетворяет задачам, возникающим при исследовании движения небесных светил, частей механизмов и т. д. Но именно поэтому классическая механика совершенно непригодна для трактовки атомных явлений. Для решения задач этого типа нельзя уже ограничиться механикой Ньютона, и необходимо разработать более совершенную механику, которая учитывала бы волновые свойства вещества.
Эта важная задача была решена к исходу 20-х годов. Основные заслуги в ее решении принадлежат немецкому физику Вернеру Гейзенбергу (1901—1976), австрийскому физику Эрвину Шредингеру (1887—1961) и английскому физику Полю Дираку (1902—1984).
Совокупность законов движения частиц вещества, учитывающая их волновые свойства, получила название волновой или квантовой механики. Квантовая механика решила обширный круг вопросов, связанных с поведением частиц атомного мира. Сюда относятся поведение электронов в атомах и молекулах и взаимодействие атомов друг с другом: излучение и поглощение света, соударения электронов и других частиц с атомами, ферромагнетизм и другие явления. Квантовая механика предсказала также ряд новых явлений; все предсказания неизменно оправдывались на опыте. Успех квантовой механики в объяснении атомных явлений доказывает, что она правильно отражает объективные закономерности природы.
Остановимся на некоторых вопросах, связанных с квантовым характером явлении в атомах, более подробно и покажем, как с помощью волновых представлений могут быть получены формулы для энергетических уровней атомов.
Электрическое поле ядра удерживает электрон атома в некоторой области пространства вблизи ядра. Рассматривая электрон как волну, мы не можем говорить о четко ограниченном объеме, в котором эта волна сосредоточена, подобно тому как при колебаниях воздуха в открытой трубе (рис. 107) нельзя указать резкую границу, за которой колебаний нет. Будем понимать под размером атома размер основной области сосредоточения электронной волны.
Последовательные волновые представления о поведении электрона в атоме могут быть получены с помощью законов квантовой механики. Такие квантовомеханическне расчеты позволяют, в частности, найти определенные состояния, в которых может находиться атом, и определить дискретные уровни энергии этих состояний. Однако законы квантовой механики выражаются в довольно сложной математической форме, и мы не можем на них останавливаться.
Некоторые следствия этих законов можно, впрочем довольно просто, установить, опираясь на понятие волны де Бройля. Для примера рассмотрим атом водорода.
Вспомним, что в планетарной модели атома (§ 206) говорилось о движении электрона вокруг ядра по некоторым разрешенным орбитам. И хотя в квантовой механике, в которой электрон описывается как некоторая волна, нельзя говорить о движении по орбите, мы все же воспользуемся представлением об «орбите» электрона и используем свойства волн де Бройля, связанных с электроном, для того чтобы указать, как не «орбиты» являются разрешенными. Такой подход хотя и не является последовательным и строгим, но обладает большой наглядностью и позволяет получить результаты, очень близкие к точным квантовомеханическим расчетам.
Итак,
рассмотрим движение электрона в атоме водорода по Кругловой орбите радиуса ![]() . Потребуем,
чтобы разрешенными были только такие орбиты, на которых укладывается целое
число длин волн де Бройля, т.е. орбиты, для которых выполняется условие
. Потребуем,
чтобы разрешенными были только такие орбиты, на которых укладывается целое
число длин волн де Бройля, т.е. орбиты, для которых выполняется условие
![]() . (210.3)
. (210.3)
При выполнении условия (210.3), называемого условием квантования орбиты, любой произвольной точке на орбите соответствует определенная фаза колебания, связанного с волной.
В самом деле, задавая на орбите какую-либо точку, мы видим, что волна после полного Оборота по орбите приходит в эту точку с той же самой фазой.
Таким образом, выполнение условия квантования делает волновую картину определенной и однозначной. Если же это условие не выполняется, то после полного оборота волна придет в исходную точку уже с другой фазой, затем опять с новой фазой и т. д. То есть в этом случае никакой однозначной волновой картины нет. Таким образом, волновое движение электронов в ограниченном пространстве сводится, как и в других волновых явлениях, к образованию «стоячих волн» (см. §§ 47— 50, 56, 59).
Эти
стоячие волны удовлетворяют «граничному условию» (210.2), которое связывает кинетическую энергию
электрона ![]() с
размерами атома. Действительно, воспользовавшись формулой де Бройля
с
размерами атома. Действительно, воспользовавшись формулой де Бройля ![]() , получаем
, получаем
![]() (210.4)
(210.4)
Потенциальная
энергия электрона на орбите ![]() (см. (206.1)). Полная энергия атома,
т.е. сумма кинетической и потенциальной энергии электрона
(см. (206.1)). Полная энергия атома,
т.е. сумма кинетической и потенциальной энергии электрона
![]()
Это выражение удобно переписать в виде
 (210.5)
(210.5)
График
зависимости ![]() от
от
![]() приведен
на рис. 375. При уменьшении размера атома его анергия уменьшается, проходит через минимум, а затем
возрастает. Атом будет находиться в устойчивом состоянии, когда его размер
соответствует минимуму энергии. В самом деле, в этом случае любое изменение
размера атома требует затраты энергии и самопроизвольно происходить не может.
приведен
на рис. 375. При уменьшении размера атома его анергия уменьшается, проходит через минимум, а затем
возрастает. Атом будет находиться в устойчивом состоянии, когда его размер
соответствует минимуму энергии. В самом деле, в этом случае любое изменение
размера атома требует затраты энергии и самопроизвольно происходить не может.

Рис. 375. Изменение энергии атома при
изменении его размера. Приведены графики функции (210.5) при значении параметра
![]() и
и ![]() . По оси ординат
отложена энергия в единицах
. По оси ординат
отложена энергия в единицах ![]() , по оси абсцисс – радиус атома в
единицах
, по оси абсцисс – радиус атома в
единицах ![]() .
В этих единицах формула (210.5) принимает вид
.
В этих единицах формула (210.5) принимает вид ![]() . Штриховыми линиями показаны
минимумы энергии, отвечающие основному
. Штриховыми линиями показаны
минимумы энергии, отвечающие основному ![]() и первому возбужденному
и первому возбужденному ![]() уровням атома
водорода
уровням атома
водорода
Энергия ![]() проходит через минимум при значениях
проходит через минимум при значениях ![]() , обращающих в
нуль, положительно определенный член — квадрат скобки в выражении (210.5). Таким
образом, энергия устойчивых состояний атома равна
, обращающих в
нуль, положительно определенный член — квадрат скобки в выражении (210.5). Таким
образом, энергия устойчивых состояний атома равна
 , (210.6)
, (210.6)
где ![]() — электрическая
постоянная, равная
— электрическая
постоянная, равная ![]() ,
, ![]() — масса электрона,
— масса электрона, ![]() — главное квантовое число, которое
указывает номер энергетического уровня. Значению
— главное квантовое число, которое
указывает номер энергетического уровня. Значению ![]() соответствует минимальная энергия
атома.
соответствует минимальная энергия
атома.
Отметим, что строгое квантовомеханическое решение задачи об энергетических уровнях атома водорода приводит к результату, совпадающему с выражением (210.6).
Совокупность
энергетических уровней атома водорода, определяемая формулой (210.6), в
точности совпадает с приведенной на рис. 360 (за начало отсчета энергии на рис.
360 принято основное состояние атома ![]() , т. е. к выражению (210.6)
прибавлена константа
, т. е. к выражению (210.6)
прибавлена константа ![]() ).
).
Точное решение указывает также, что вполне
устойчивым является лишь основное состояние атома;. отвечающее самому нижнему
энергетическому уровня ![]() . Остальные состояния
. Остальные состояния ![]() оказываются не вполне
устойчивыми — со временем они переходят в более низкие состояния, излучая
избыток энергии в виде светового кванта.
оказываются не вполне
устойчивыми — со временем они переходят в более низкие состояния, излучая
избыток энергии в виде светового кванта.
Теперь мы можем понять причину устойчивости атома, т.е. невозможности падения электрона на ядро. Этому препятствует быстрое возрастание кинетической энергии электрона, сопровождающее уменьшение его длины волны де Бройля при сокращении размеров атома (см. (210.4)).
Отметим еще раз, что квантовая механика не находится в противоречии с классической механикой Ньютона. Все выводы ньютоновой механики заключены в квантовой механике и могут быть получены из этой последней как приближенные решения, вполне пригодные для тех случаев, когда волновые свойства частиц не играют существенной роли. Аналогичным образом обстоит дело и с теорией относительности (см. § 199, 200) — она переходит в механику Ньютона, когда скорости частиц малы по сравнению со скоростью света. В атомной физике часто приходится сталкиваться с явлениями, в которых и волновые свойства существенны, и скорости частиц велики. В этих случаях необходимо принимать во внимание как квантовую теорию, так и теорию относительности — пользоваться так называемой релятивистской квантовой механикой.
Следует указать, что современная физика столкнулась уже с задачами, полного решения которых не в состоянии дать и релятивистская квантовая механика. Сюда относятся вопросы о некоторых свойствах атомных ядер и о взаимодействии и свойствах частиц, их составляющих. Для такого рода вопросов требуется дальнейшее усовершенствование квантовой механики, которое в настоящее время еще не проведено.
1. Пройдя разность потенциалов ![]() , частица приобрела
энергию
, частица приобрела
энергию ![]() .
Каков заряд частицы?
.
Каков заряд частицы?
2. Найдите скорость атома гелия, кинетическая
энергия которого равна ![]() .
.
3. Найдите энергию (в электронвольтах),
выделяющуюся при образовании
одной молекулы ![]() из
углерода и кислорода, если теплота образования
из
углерода и кислорода, если теплота образования ![]() равна
равна ![]() .
.
4. Ион описывает в магнитном поле окружность
радиуса ![]() .
Какой радиус траектории будет иметь, в том же поле вчетверо более тяжелый ион, обладающий
тем же зарядом и а) той; же скоростью; б) той же энергией?
.
Какой радиус траектории будет иметь, в том же поле вчетверо более тяжелый ион, обладающий
тем же зарядом и а) той; же скоростью; б) той же энергией?
5. Радиус траектории иона ![]() (
(![]() , где
, где ![]() — элементарный заряд, а
— элементарный заряд, а ![]() ) равен
) равен ![]() . Найдите радиус траектории
в том же магнитном поле частицы с вдвое большим отношением заряда к массе, ускоренной
той же разностью потенуиалов. Рассмотрите случаи:
. Найдите радиус траектории
в том же магнитном поле частицы с вдвое большим отношением заряда к массе, ускоренной
той же разностью потенуиалов. Рассмотрите случаи:
а) ![]() (ион
(ион ![]() )
)
и
б) ![]() (ион
(ион ![]() ).
).
6. Вычислите радиус траектории однократно заряженного иона с массой ![]() в магнитном поле
в магнитном поле ![]() , если ион был
ускорен разностью потенциалов
, если ион был
ускорен разностью потенциалов ![]() .
.
7. Две одинаковые частицы, но одна быстрая, а другая медленная, движутся по окружности в одном и том же магнитном поле. Которая из частиц совершает обороты быстрее?
8. Напишите выражение для времени
одного оборота заряженной частицы в магнитном поле. Вычислите время обороты
частицы с зарядом ![]() и массой
и массой ![]() в магнитном поле
в магнитном поле ![]()
9. Во сколько раз масса движущая электрон и атома водорода больше соответствующей массы покоя, если кинетическая энергия равна 1 кэВ, 1 МэВ, 1 ГэВ.
10. Снаряды массой ![]() движется со скоростью
движется со скоростью ![]() . Найдите
дополнительную массу снаряда, обусловленную движением.
. Найдите
дополнительную массу снаряда, обусловленную движением.
11. Покажите, что для малых скоростей ![]() из
релятивистской формулы для кинетической энергии (199.2) следует классическое
выражение
из
релятивистской формулы для кинетической энергии (199.2) следует классическое
выражение ![]() .
.
Указание.

12. Используя формулу (199.2)
зависимости массы от скорости, найти отношение массы движущегося тела к массе
покоя для скоростей движения ![]() .
.
13. Насколько увеличится масса ![]() гелия в
результате нагревания
гелия в
результате нагревания ![]() (теплоемкость
(теплоемкость ![]() газообразного гелия при
постоянном объеме равна
газообразного гелия при
постоянном объеме равна ![]() )?
)?
14. Найдите расстояние между центрами щелей приемников в
массе-спектрографе (по схеме рис.354), служащем для разделения изотопов урана ![]() и
и ![]() , если радиус траектории
ионов
, если радиус траектории
ионов ![]() равен
равен
![]() .
.
15. Ток пучка ионов урана ![]() в
масс-спектрографе равен
в
масс-спектрографе равен ![]() . Какое количество
. Какое количество ![]() выделится на
приемнике за сутки?
выделится на
приемнике за сутки?
16. Свечение атомарного водорода
возбуждают электронами с энергией ![]() . Кванты какой энергии будут
испускаться? Используйте схему энергетических уровней водорода (рис. 360).
. Кванты какой энергии будут
испускаться? Используйте схему энергетических уровней водорода (рис. 360).
17. Используя схему рис.360, найдите длины волн линий в спектре поглощения атомарного водорода.
18. Вычислите электростатическую
(кулоновскую) и гравитационную силы взаимодействия электрона с ядром в атоме
водорода. Радиус атома примите равным ![]() .
Гравитационная постоянная равна
.
Гравитационная постоянная равна ![]() .
.
19. Пользуясь законами сохранения энергии и импульса для упругого комптоновского рассеяния фотонов на электронах (209.5), получите выражение для изменения длины волны фотона (209.4).
20. Вычислите длину волны светового
кванта с энергией ![]() и длину волны де Бройля электрона и
протона такой же энергии.
и длину волны де Бройля электрона и
протона такой же энергии.
21. Объясните, почему при рассеянии на
кристаллах медленных нейтронов (энергия ![]() ) наблюдаются резкие дифракционные
явления (рассеяние происходит только в некоторых направлениях), в то время как
при рассеянии более быстрых нейтронов (энергия
) наблюдаются резкие дифракционные
явления (рассеяние происходит только в некоторых направлениях), в то время как
при рассеянии более быстрых нейтронов (энергия ![]() ) эти явления незаметны.
) эти явления незаметны.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие к первому изданию
- Раздел первый. Колебания и волны
- Глава I. Основные понятия. Механические колебания
- § 1. Периодические движения. Период
- § 2. Колебательные системы
- § 3. Маятник; кинематика его колебаний
- § 4. Колебания камертона
- § 5. Гармоническое колебание. Частота
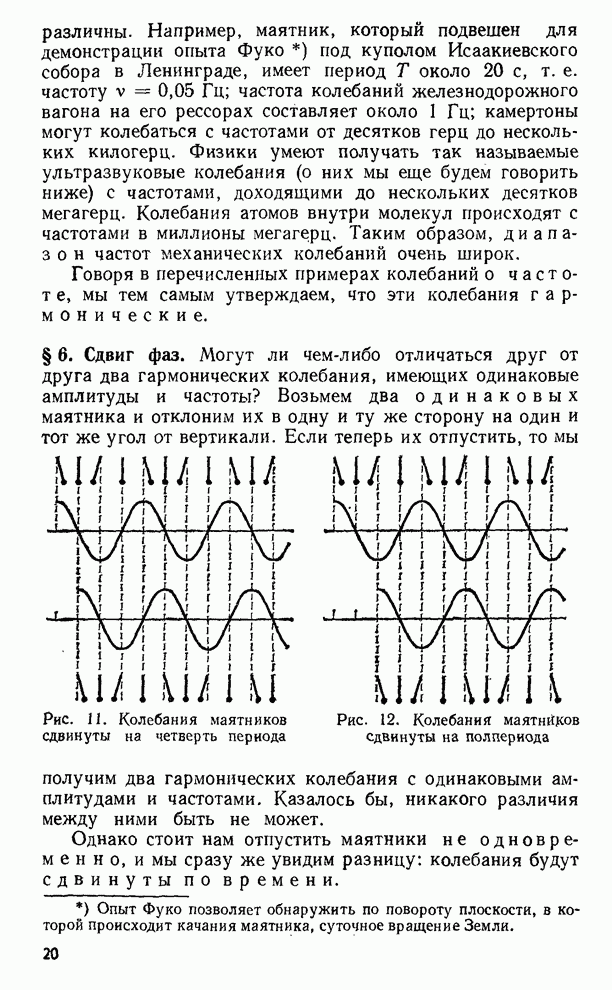
- § 6. Сдвиг фаз
- § 7. Динамика колебаний маятника
- § 8. Формула периода математического маятника
- § 9. Упругие колебания
- § 10. Крутильные колебания
- § 11. Влияние трения. Затухание
- § 12. Вынужденные колебания
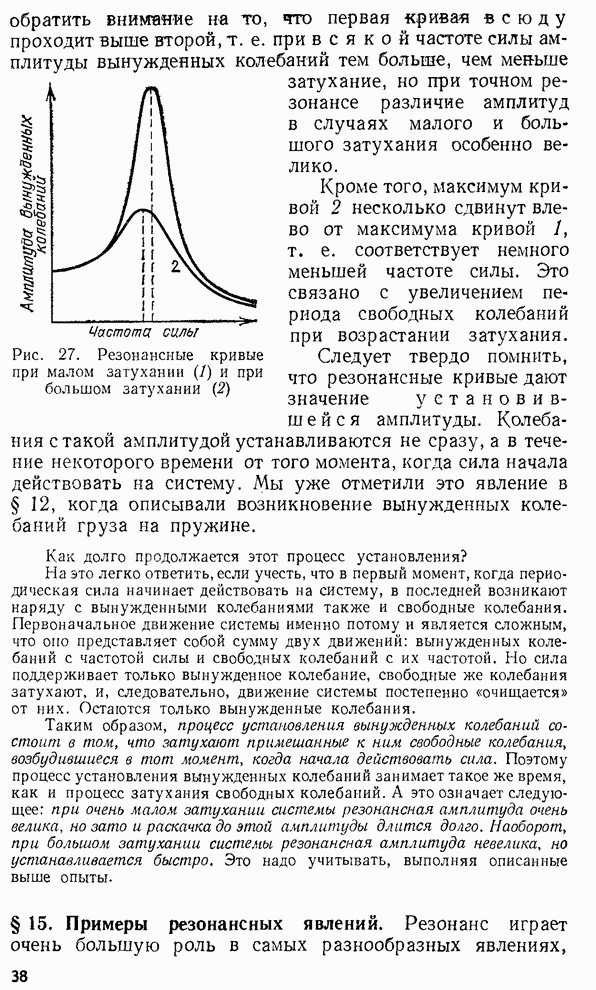
- § 13. Резонанс
- § 14. Влияние трения на резонансные явления
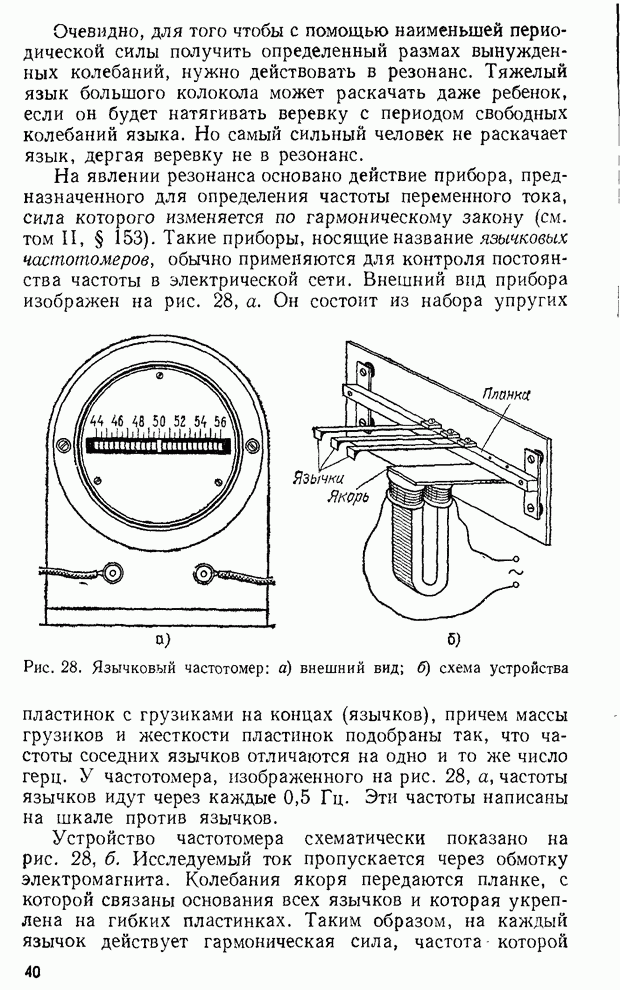
- § 15. Примеры резонансных явлений
- § 16. Резонансные явления при действии негармонической периодической силы
- § 17. Форма периодических колебаний и ее связь с гармоническим составом этих колебаний
- Глава II. Звуковые колебания
- § 18. Звуковые колебания
- § 19. Предмет акустики
- § 20. Музыкальный тон. Громкость и высота тона
- § 21. Тембр
- § 22. Акустический резонанс
- § 23. Запись и воспроизведение звука
- § 24. Анализ и синтез звука
- § 25. Шумы
- Глава III. Электрические колебания
- § 26. Электрические колебания. Методы их наблюдения
- § 27. Колебательный контур
- § 28. Аналогия с механическими колебаниями. Формула Томсона
- § 29. Электрический резонанс
- § 30. Незатухающие колебания. Автоколебательные системы
- § 31. Ламповый генератор электрических колебаний
- Глава IV. Волновые явления
- § 32. Учение о колебаниях
- § 33. Волновые явления
- § 34. Скорость распространения волн
- § 35. Радиолокация, гидроакустическая локация и звукометрия
- § 36. Поперечные волны в шнуре
- § 37. Продольные волны в столбе воздуха
- § 38. Волны на поверхности жидкости
- § 39. Перенос энергии волнами
- § 40. Отражение волн
- § 41. Дифракция
- § 42. Направленное излучение
- Глава V. Интерференция волн
- § 43. Наложение волн
- § 44. Интерференция волн
- § 45. Условия образования максимумов и минимумов
- § 46. Интерференция звуковых волн
- § 47. Стоячие волны
- § 48. Колебания упругих тел как стоячие волны
- § 49. Свободные колебания струны
- § 50. Стоячие волны в пластинках и других протяженных телах
- § 51. Резонанс при наличии многих собственных частот
- § 52. Условия хорошего излучения звука
- § 53. Бинауральный эффект. Звукопеленгация
- Глава VI. Электромагнитные волны
- § 54. Электромагнитные волны
- § 55. Условия хорошего излучения электромагнитных волн
- § 56. Вибратор и антенны
- § 57. Опыты Герца по получению и исследованию электромагнитных волн. Опыты Лебедева
- § 58. Электромагнитная теория света. Шкала электромагнитных волн
- § 59 Опыты с электромагнитными волнами
- § 60. Изобретение радио Поповым
- § 61. Современная радиосвязь
- § 62. Другие применения радио
- § 63. Распространение радиоволн
- § 64. Заключительные замечания
- Раздел второй. Геометрическая оптика
- Глава VII. Общая характеристика световых явлений
- § 65. Разнообразные действия света
- § 66. Интерференция света. Цвета тонких пленок
- § 67. Краткие сведения из истории оптики
- Глава VIII. Фотометрия и светотехника
- § 68. Энергия излучения. Световой поток
- § 69. Точечные источники света
- § 70. Сила света и освещенность
- § 71. Законы освещенности
- § 72. Единицы световых величин
- § 73. Яркость источников
- § 74. Задачи светотехники
- § 75. Приспособления для концентрации светового потока
- § 76. Отражающие и рассеивающие тела
- § 77. Яркость освещенных поверхностей
- § 78. Световые измерения и измерительные приборы
- Глава IX. Основные законы геометрической оптики
- § 79. Прямолинейное распространение волн
- § 80. Прямолинейное распространение света и световые лучи
- § 81. Законы отражения и преломления света
- § 82. Обратимость световых лучей
- § 83. Показатель преломления
- § 84. Полное внутреннее отражение
- § 85. Преломление в плоскопараллельной пластинке
- § 86. Преломление в призме
- Глава X. Применение отражения и преломления света для получения изображений
- § 87. Источник света и его изображение
- § 88. Преломление в линзе
- § 89. Изображение в линзе точек, лежащих на главной оптической оси. Формула линзы.
- § 90. Применения формулы тонкой линзы. Действительные и мнимые изображения.
- § 91. Изображение точечного источника и протяженного объекта в плоском зеркале. Изображение точечного источника в сферическом зеркале
- § 92. Фокус и фокусное расстояние сферического зеркала
- § 93. Связь между положениями источника и его изображения на главной оси сферического зеркала
- § 94. Способы изготовления линз и зеркал
- § 95. Изображение протяженных объектов в сферическом зеркале и линзе
- § 96. Увеличение при изображении объектов в сферическом зеркале и линзе
- § 97. Построение изображений в сферическом зеркале и линзе
- § 98. Оптическая сила линз
- Глава XI. Оптические системы и их погрешности
- § 99. Оптическая система
- § 100. Главные плоскости и главные точки системы
- § 101. Построение изображений в системе
- § 102. Увеличение системы
- § 103. Недостатки оптических систем
- § 104. Сферическая аберрация
- § 105. Астигматизм
- § 106. Хроматическая аберрация
- § 107. Ограничение пучков в оптических системах
- § 108. Светосила линзы
- § 109. Яркость изображения
- Глава XII. Оптические приборы
- § 110. Проекционные оптические приборы
- § 111. Фотографический аппарат
- § 112. Глаз как оптическая система
- § 113. Оптические приборы, вооружающие глаз
- § 114. Лупа
- § 115. Микроскоп
- § 116. Разрешающая способность микроскопа
- § 117. Зрительные трубы
- § 118. Увеличение зрительной трубы
- § 119. Телескопы
- § 120. Яркость изображения для протяженных и точечных источников
- § 121. «Ночезрительная труба» Ломоносова
- § 122. Зрение двумя глазами и восприятие глубины пространства. Стереоскоп.
- Раздел третий. Физическая оптика
- Глава XIII. Интерференция света
- § 123. Геометрическая и физическая оптика
- § 124. Опытное осуществление интерференции света
- § 125. Объяснение цветов тонких пленок
- § 126. Кольца Ньютона
- § 127. Определение длины световой волны с помощью колец Ньютона
- Глава XIV. Дифракция света
- § 128. Пучки лучей и форма волновой поверхности
- § 129. Принцип Гюйгенса
- § 130. Законы отражения и преломления света на основе принципа Гюйгенса
- § 131. Принцип Гюйгенса в толковании Френеля
- § 132. Простейшие дифракционные явления
- § 133. Объяснение дифракции по методу Френеля
- § 134. Разрешающая сила оптических инструментов
- § 135. Дифракционные решетки
- § 136. Дифракционная решетка как спектральный прибор
- § 137. Изготовление дифракционных решеток
- § 138. Дифракция при косом падении света на решетку
- Глава XV. Физические принципы оптической голографии
- § 139. Фотография и голография
- § 140. Запись голограммы с помощью плоской опорной волны
- § 141. Получение оптических изображений по методу восстановления волнового фронта
- § 142. Голографирование по методу встречных световых пучков
- § 143. Использование голографии в оптической интерферометрии
- Глава XVI. Поляризация света и поперечность световых волн
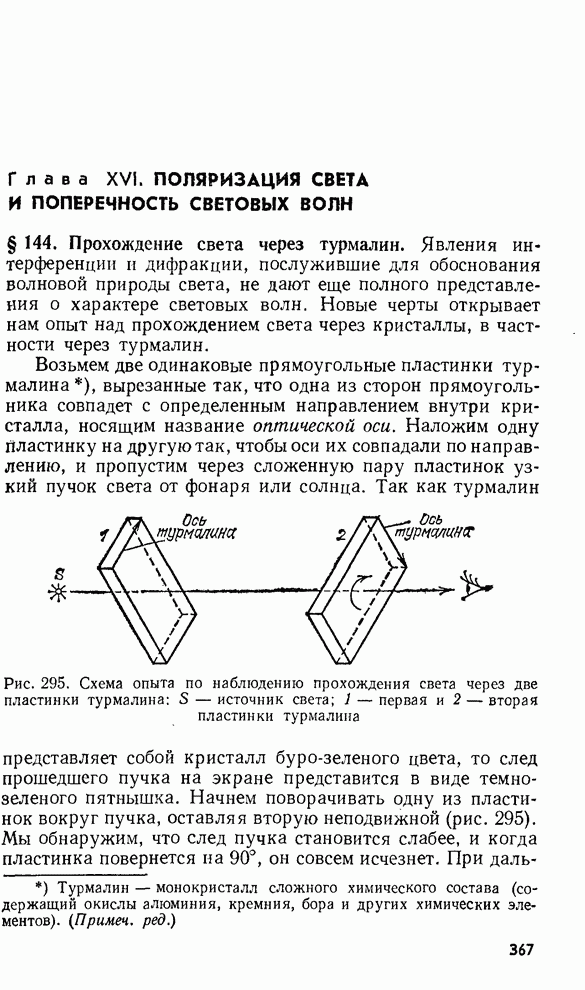
- § 144. Прохождение света через турмалин
- § 145. Гипотезы, объясняющие наблюдаемые явления. Понятие о поляризованном свете
- § 146. Механическая модель явлений поляризации
- § 147. Поляроиды
- § 148. Поперечность световых волн и электромагнитная теория света
- Глава XVII. Шкала электромагнитных волн
- § 149. Способы исследования электромагнитных волн различной длины
- § 150. Инфракрасное и ультрафиолетовое излучение
- § 151. Открытие рентгеновских лучей
- § 152. Различные действия рентгеновских лучей
- § 153. Устройство рентгеновской трубки
- § 154. Происхождение и природа рентгеновских лучей
- § 155. Шкала электромагнитных волн
- Глава XVIII. Скорость света
- § 156. Первые попытки определения скорости света
- § 157. Определение скорости света Рёмером
- § 158. Определение скорости света по методу вращающегося зеркала
- Глава XIX. Дисперсия света и цвета тел
- § 159. Состояние вопроса о цвете тел до исследований Ньютона
- § 160. Основное открытие Ньютона в оптике
- § 161. Истолкование наблюдений Ньютона
- § 162. Дисперсия показателя преломления различных материалов
- § 163. Дополнительные цвета
- § 164. Спектральный состав света различных источников
- § 165. Свет и цвета тел
- § 166. Коэффициенты поглощения, отражения и пропускания
- § 167. Цветные тела, освещенные белым светом
- § 168. Цветные тела, освещенные цветным светом
- § 169. Маскировка и демаскировка
- § 170. Насыщенность цветов
- § 171. Цвет неба и зорь
- Глава XX. Спектры и спектральные закономерности
- § 172. Спектральные аппараты
- § 173. Типы спектров испускания
- § 174. Происхождение спектров различных типов
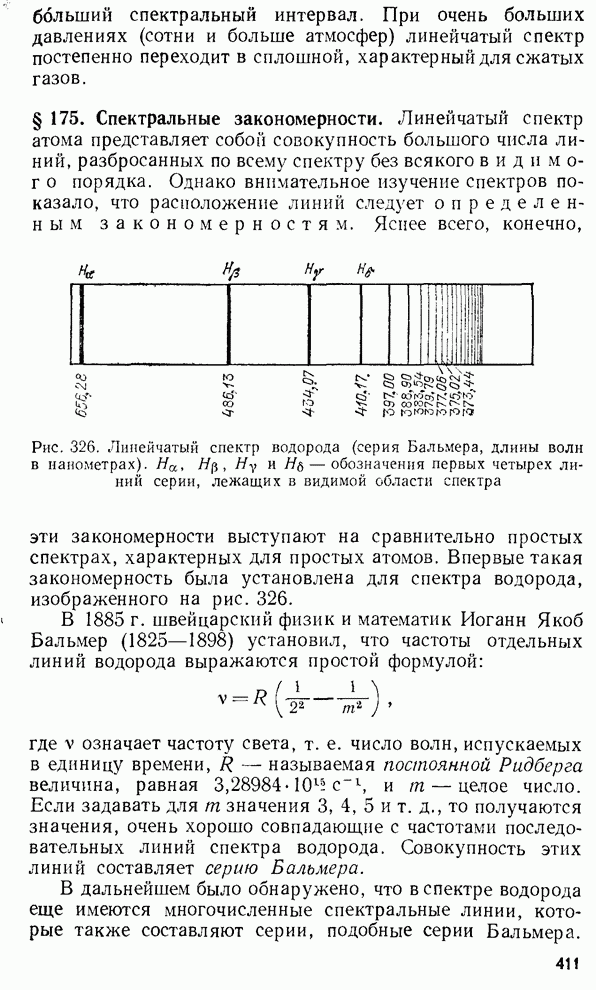
- § 175. Спектральные закономерности
- § 176. Спектральный анализ по спектрам испускания
- § 177. Спектры поглощения жидких и твердых тел
- § 178. Спектры поглощения атомов. Линии Фраунгофера
- § 179. Излучение накаленных тел. Абсолютно черное тело
- § 180. Зависимость излучения накаленных тел от температуры. Лампы накаливания
- § 181. Оптическая пирометрия
- XXI. Действия света
- § 182. Действия света на вещество. Фотоэлектрический эффект
- § 183. Законы фотоэлектрического эффекта
- § 184. Понятие о световых квантах
- § 185. Применение фотоэлектрических явлений
- § 186. Фотолюминесценция. Правило Стокса
- § 187. Физический смысл правила Стока
- § 188. Люминесцентный анализ
- § 189. Фотохимические действия света
- § 190. Роль длины волны в фотохимических процессах
- § 191. Фотография
- § 192. Фотохимическая теория зрения
- § 193. Длительность зрительного ощущения
- Раздел четвертый. Атомная и ядерная физика
- Глава XXII. Строение атома
- § 194. Представление об атомах
- § 195. Постоянная Авогадро. Размеры и массы атомов
- § 196. Элементарный электрический заряд
- § 197. Единицы заряда, массы и энергии в атомной физике
- § 198. Измерение массы заряженных частиц. Масс-спектрограф
- § 199. Масса электрона. Зависимость массы от скорости
- § 200. Закон Эйнштейна
- § 201. Массы атомов; изотопы
- § 202. Разделение изотопов. Тяжелая вода
- § 203. Ядерная модель атома
- § 204. Энергетические уровни атомов
- § 205. Вынужденное излучение света. Квантовые генераторы
- § 206. Атом водорода. Своеобразие законов движения электрона в атоме
- § 207. Многоэлектронные атомы. Происхождение оптических и рентгеновских спектров атомов
- § 208. Периодическая система элементов Менделеева
- § 209. Квантовые и волновые свойства фотонов
- § 210. Понятие о квантовой (волновой) механике
- Глава XXIII. Радиоактивность
- § 211. Открытие радиоактивности. Радиоактивные элементы
- § 212. L-, B-, Г- излучение. Камера Вильсона
- § 213. Способы регистрации заряженных частиц
- § 214. Природа радиоактивного излучения
- § 215. Радиоактивный распад и радиоактивные превращения
- § 216. Применения радиоактивности
- § 217. Ускорители
- Глава XXIV. Атомные ядра и ядерная энергия
- § 218. Понятие о ядерных реакциях
- § 219. Ядерные реакции и превращение элементов
- § 220. Свойства нейтронов
- § 221. Ядерные реакции под действием нейтронов
- § 222. Искусственная радиоактивность
- § 223. Позитрон
- § 224. Применение закона Эйнштейна к процессам аннигиляции и образования пар
- § 225. Строение атомного ядра
- § 226. Ядерная энергия. Источник энергии звезд.
- § 227. Деление урана
- § 228. Применения незатухающей цепной реакции деления. Атомная и водородная бомбы
- § 229. Ядерные реакторы и их применения
- Глава XXV. Элементарные частицы
- § 230. Общие замечания
- § 231. Нейтрино
- § 232. Ядерные силы. Мезоны
- § 233. Частицы и античастицы
- § 234. Частицы и взаимодействия
- § 235. Детекторы элементарных частиц
- § 236. Парадокс часов
- § 237. Космическое излучение (космические лучи)
- Глава XXVI. Новые достижения в физике элементарных частиц
- § 238. Ускорители и экспериментальная техника
- § 239. Адроны и кварки
- § 240. Кварковая структура андронов
- § 241. Кварковая модель и процессы образования и распада адронов
- § 242. Лептоны. Промежуточные бозоны. Единство всех взаимодействий
- Заключение