| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
14.7.2. Техника синтеза пептидов
14.7.2.1. Защитные группы
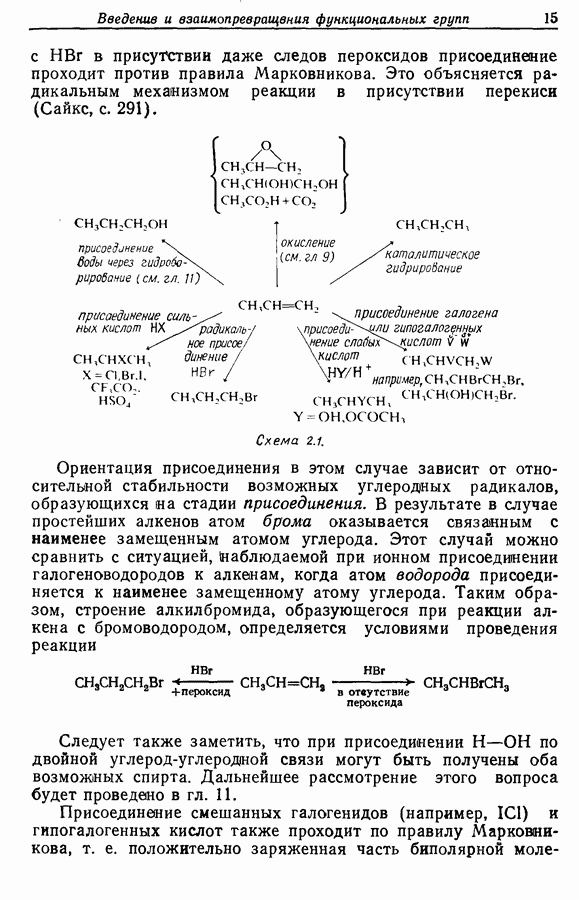
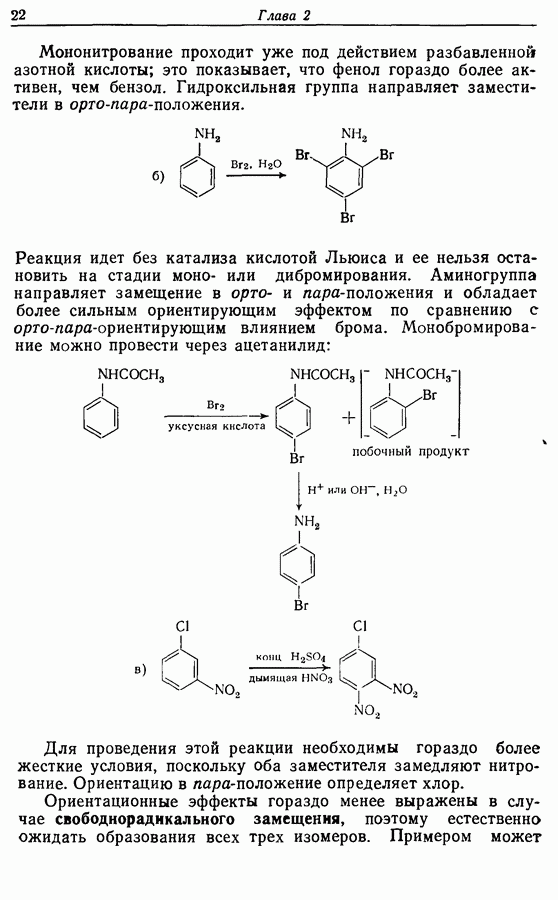
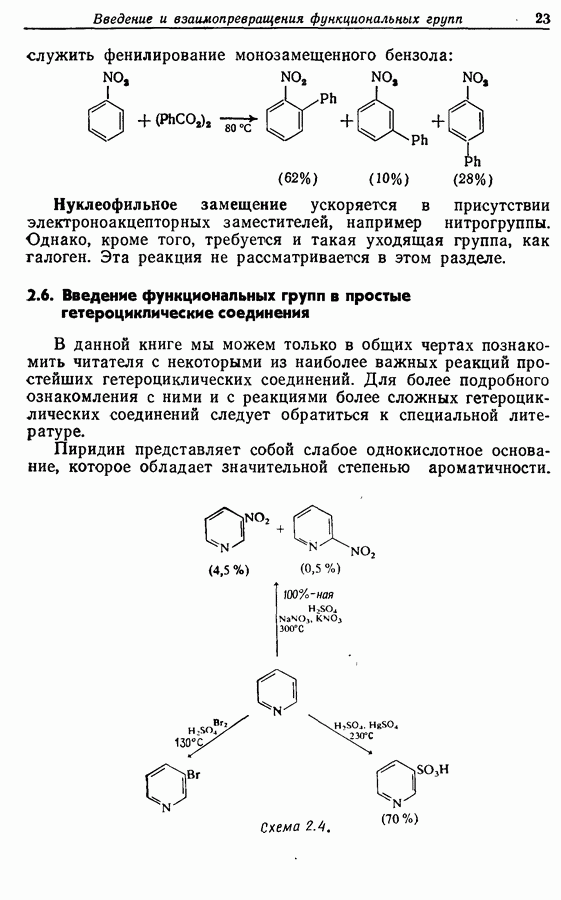
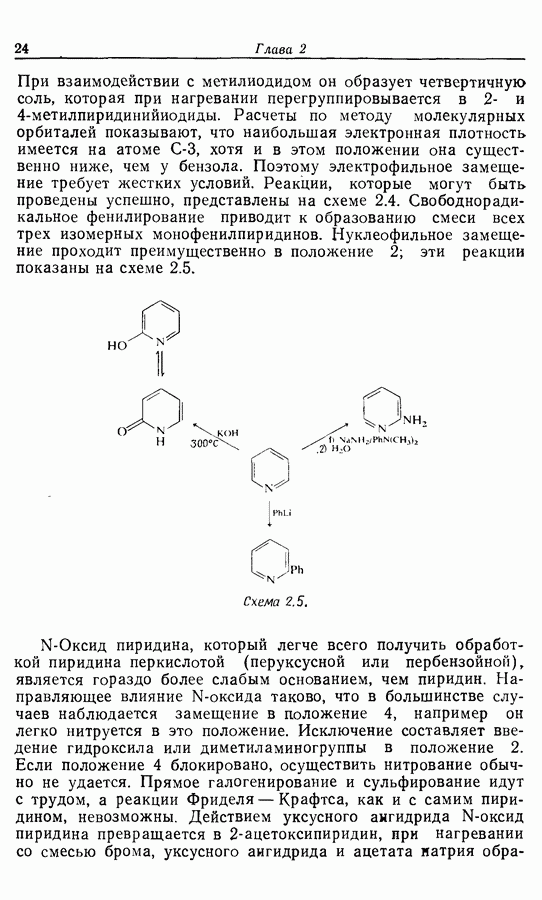
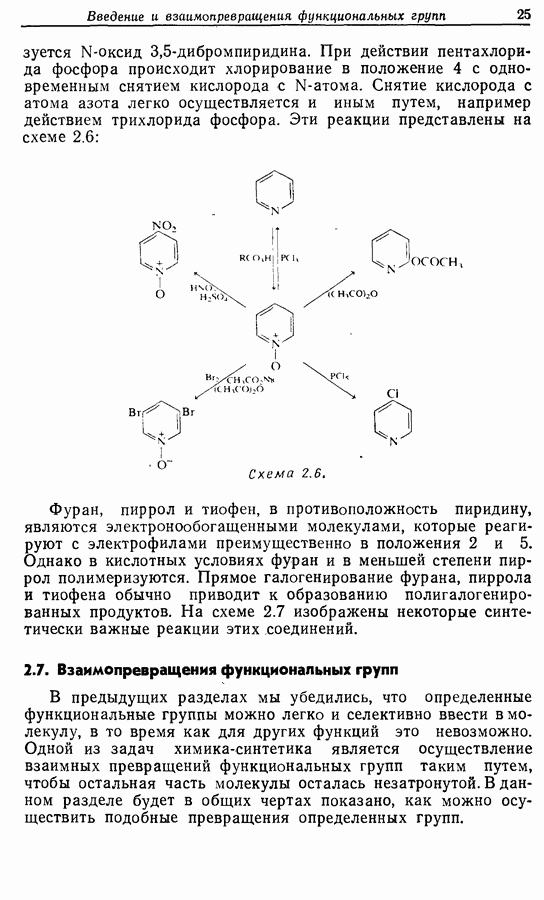
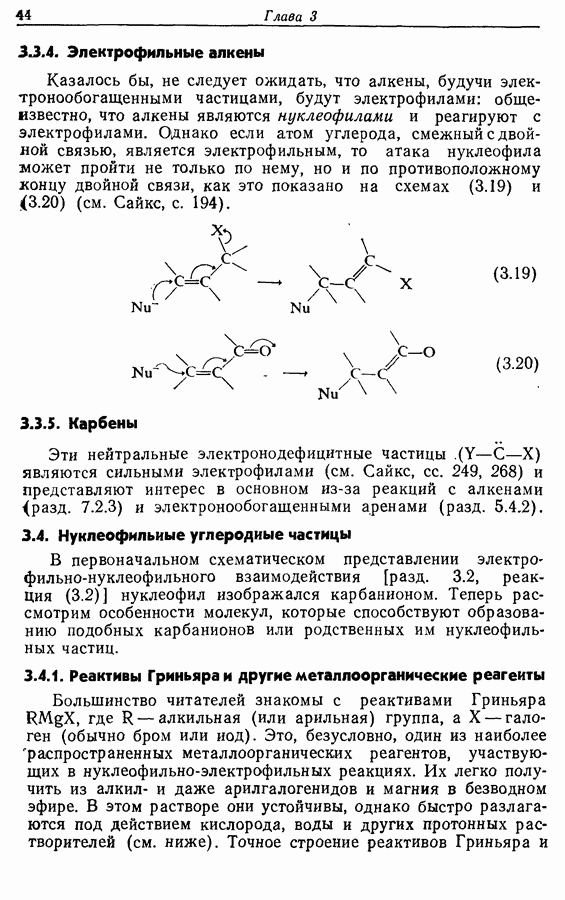
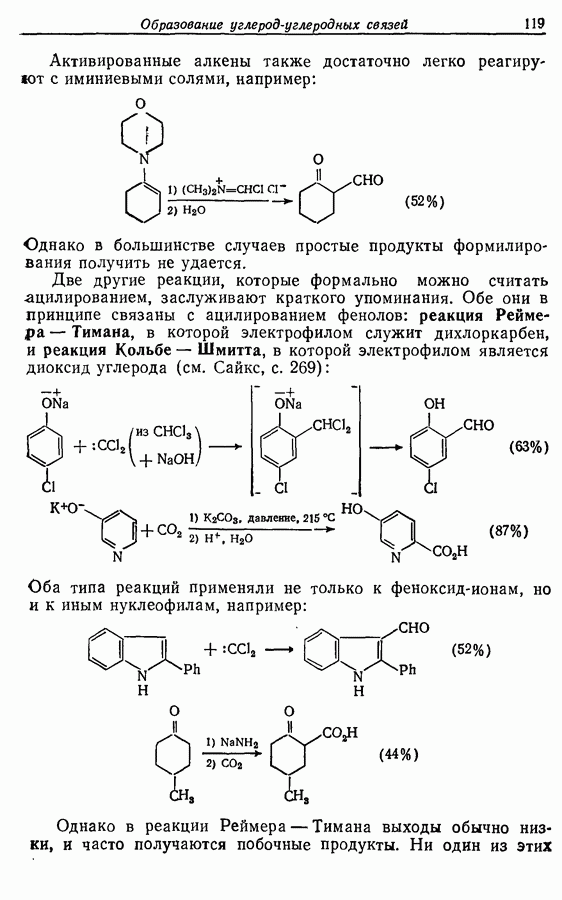
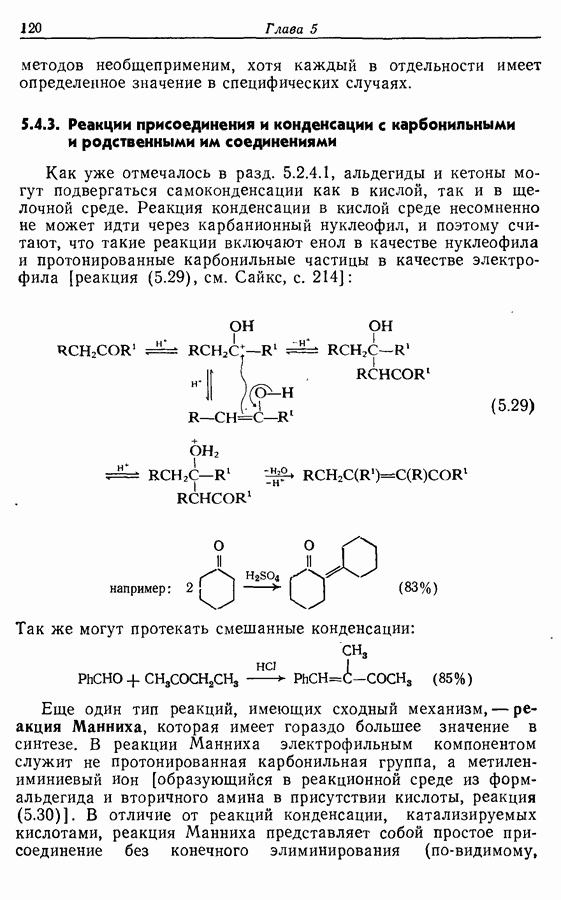
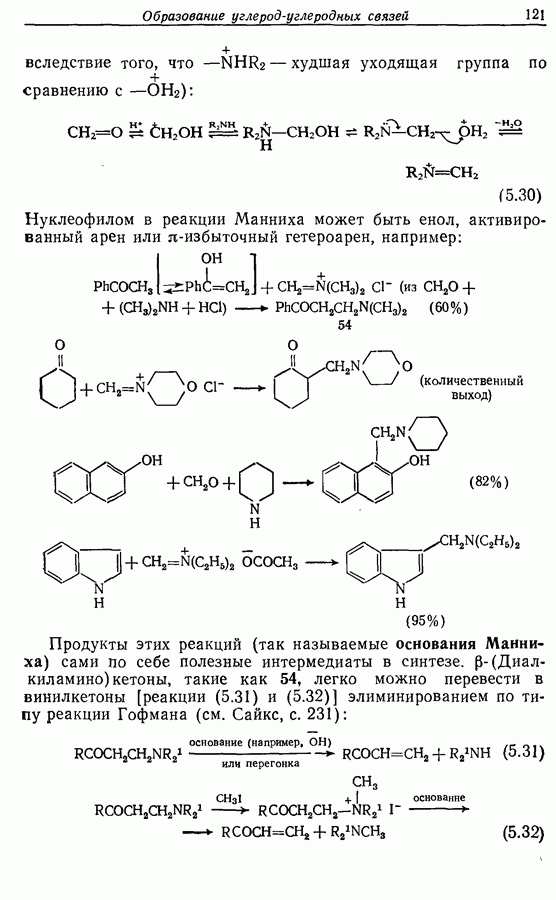
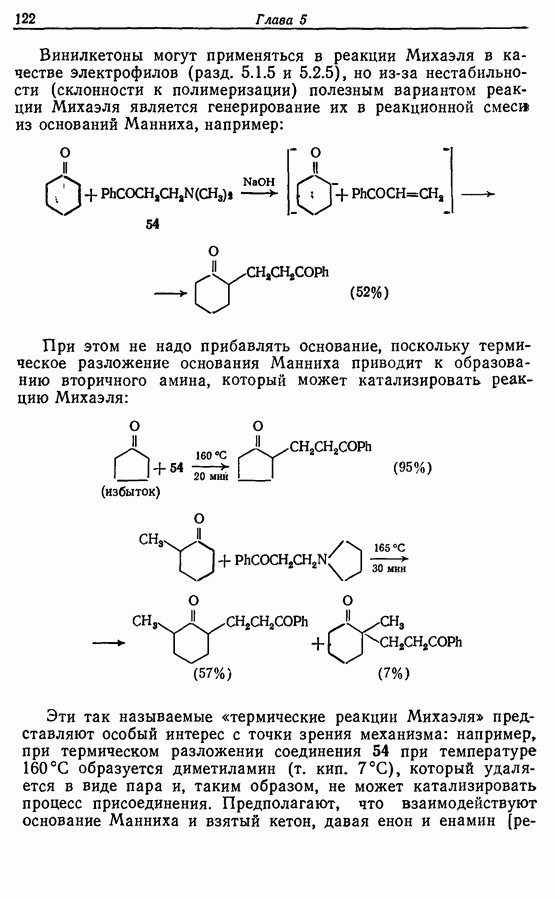
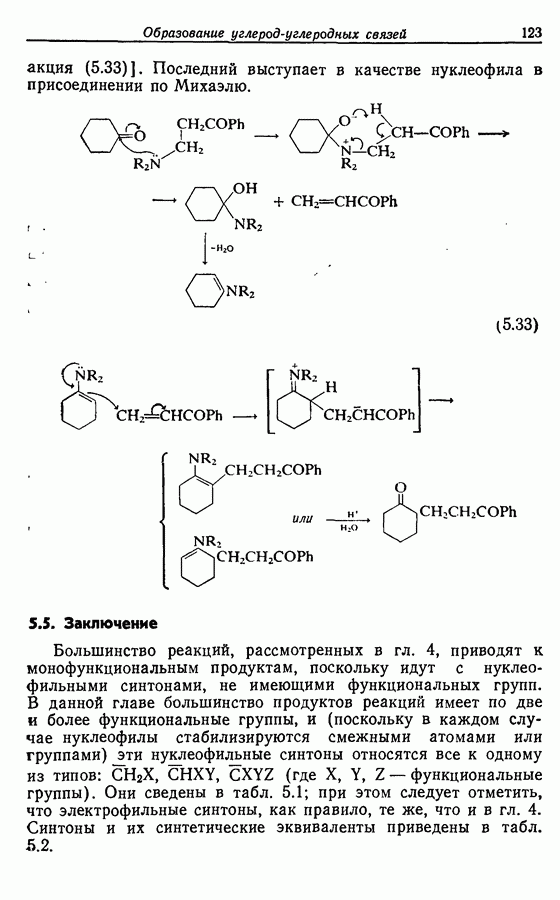
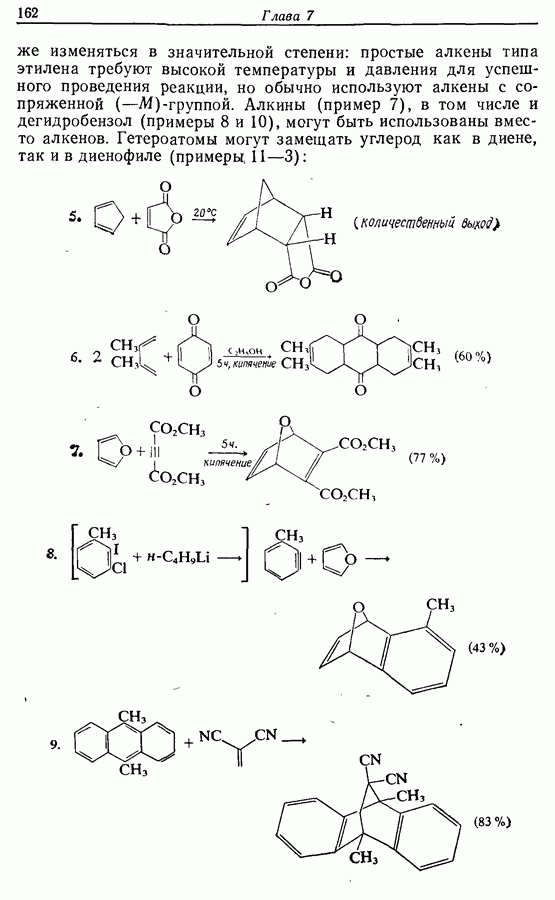
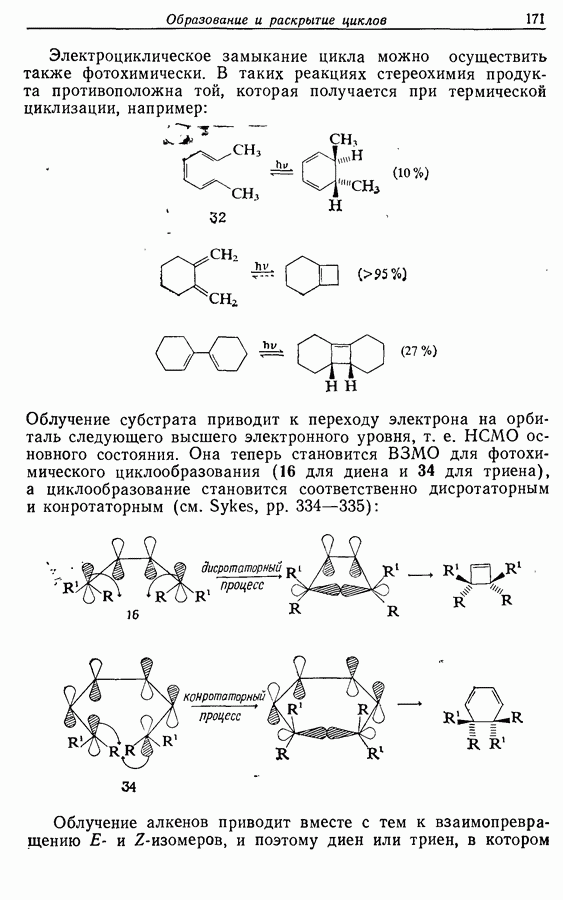
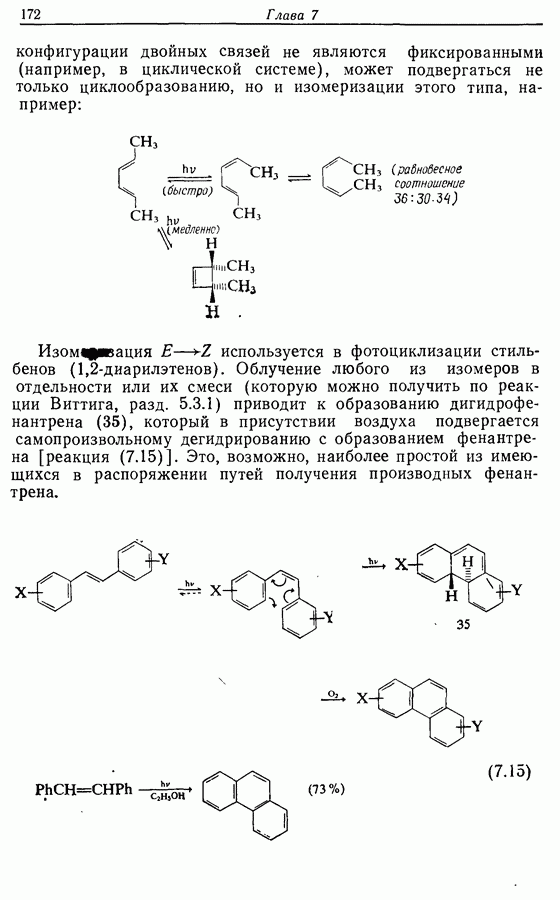
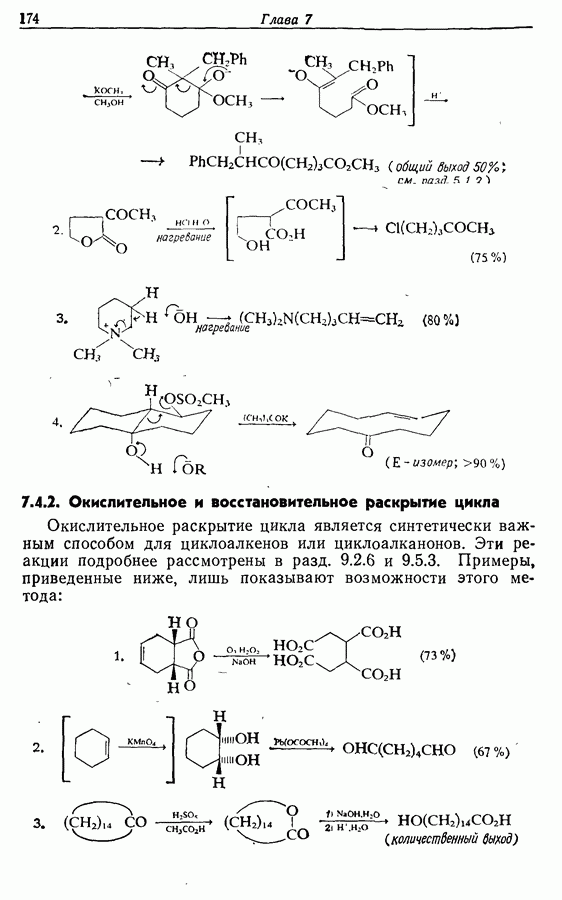
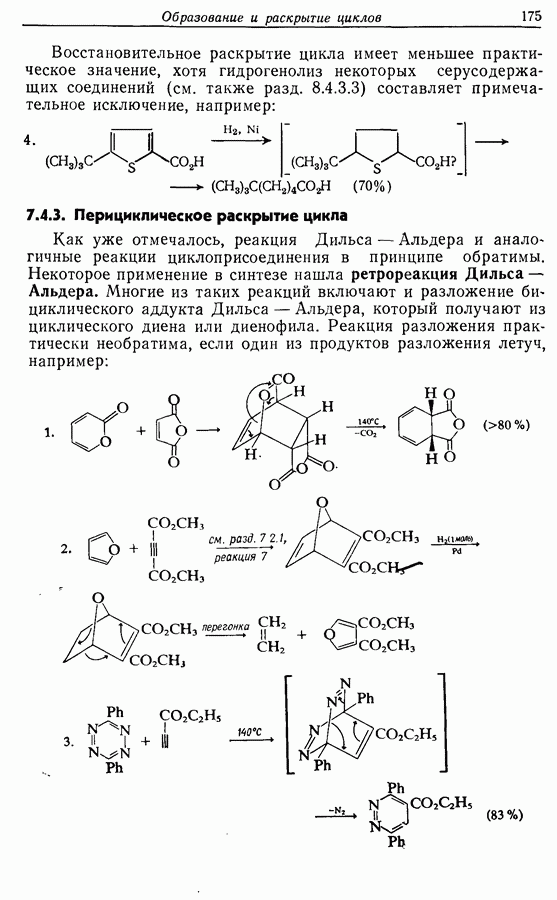
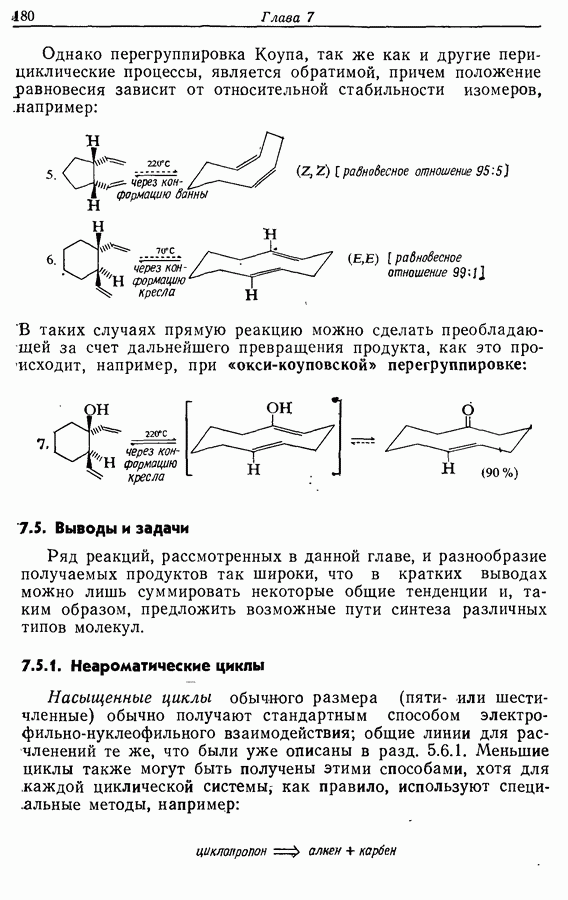
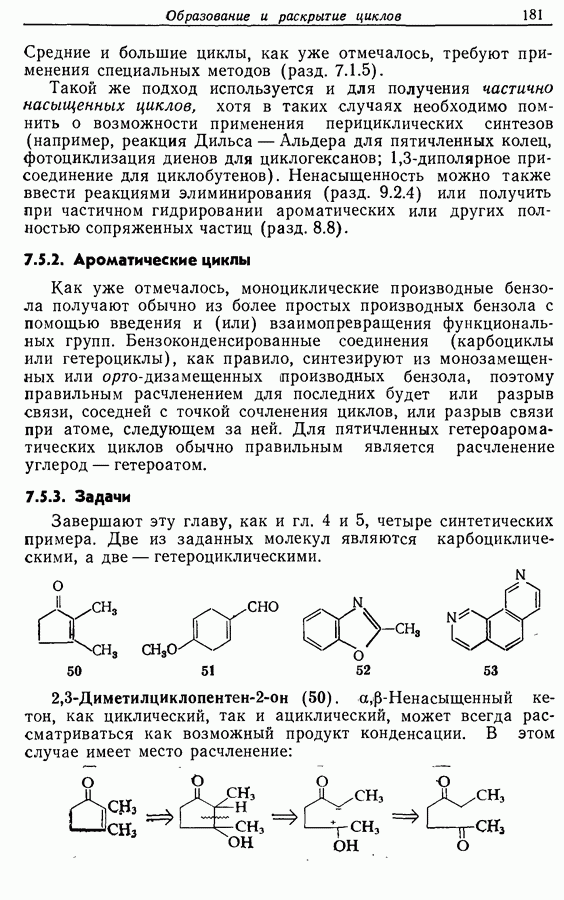
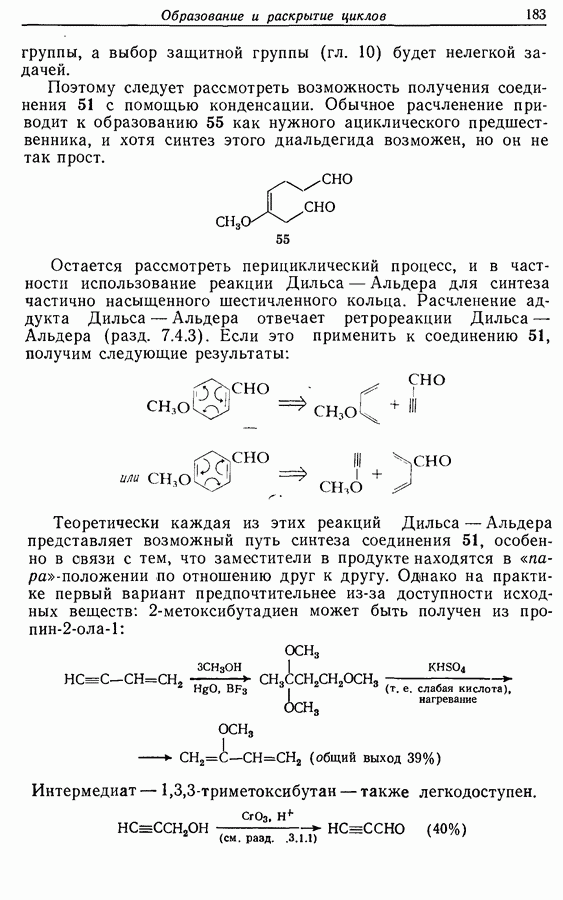
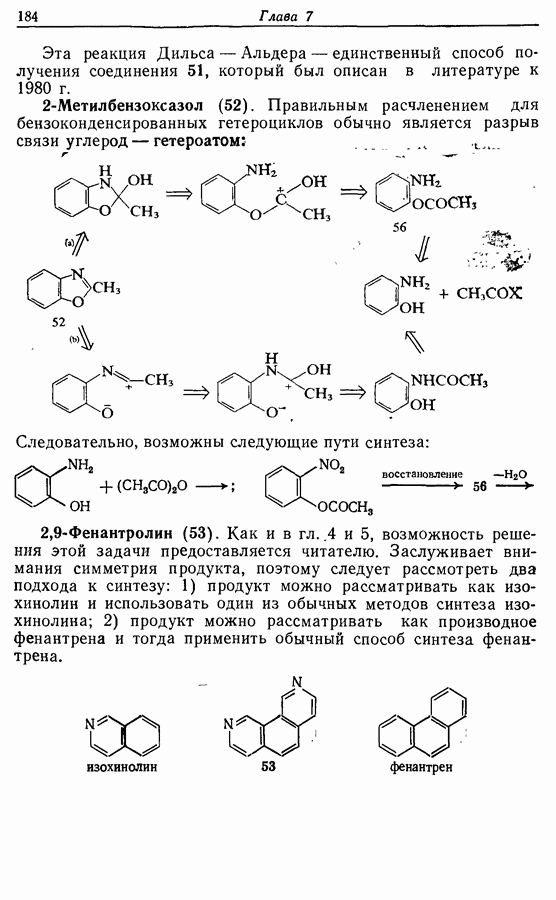
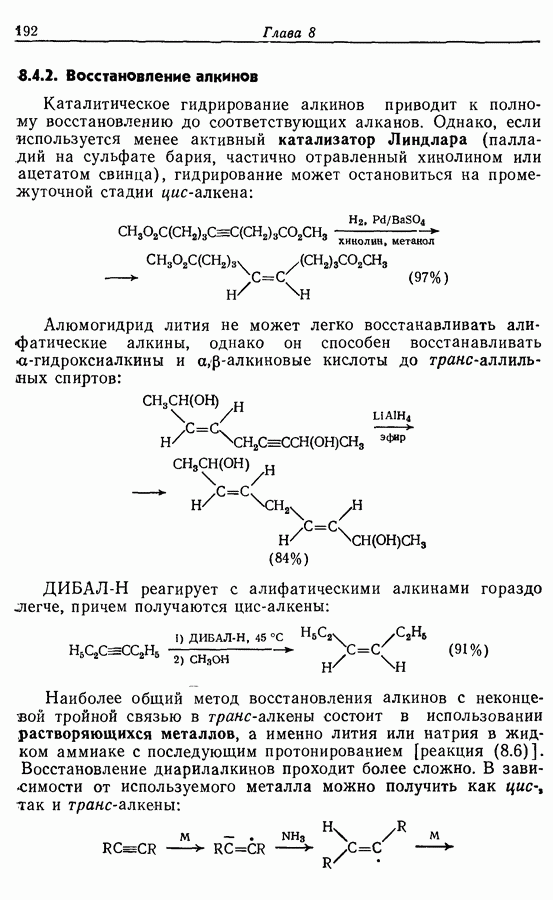
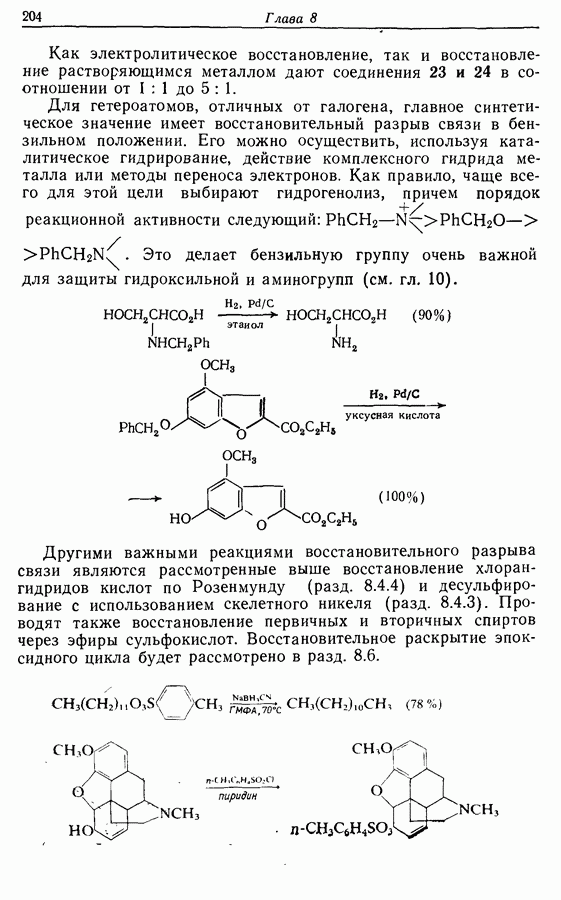
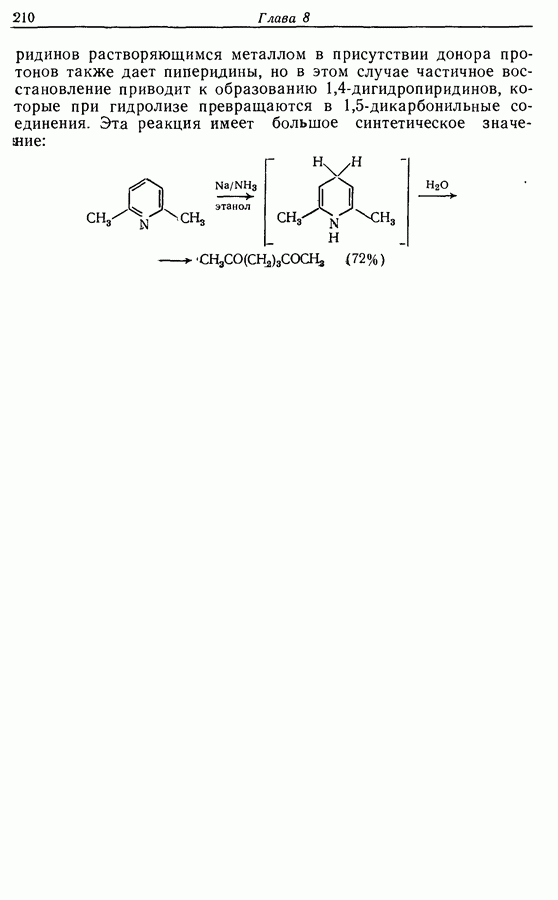
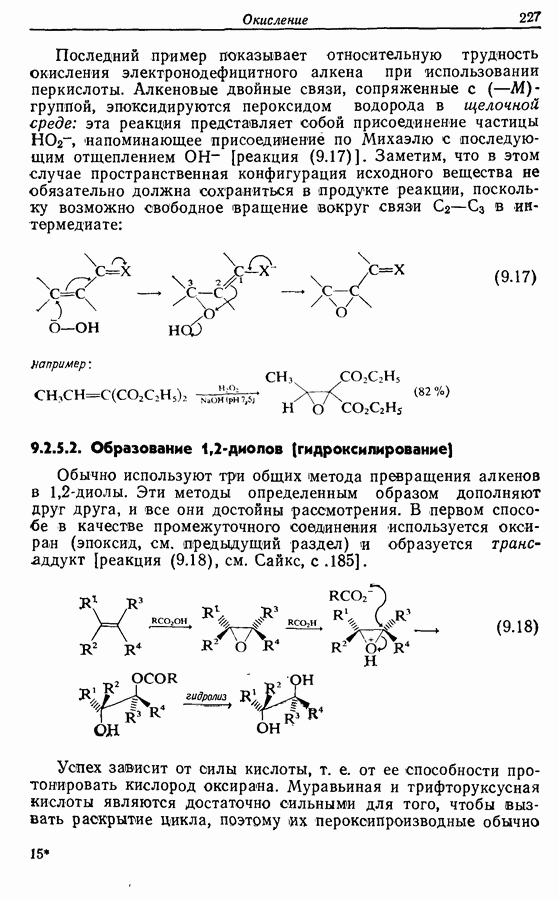
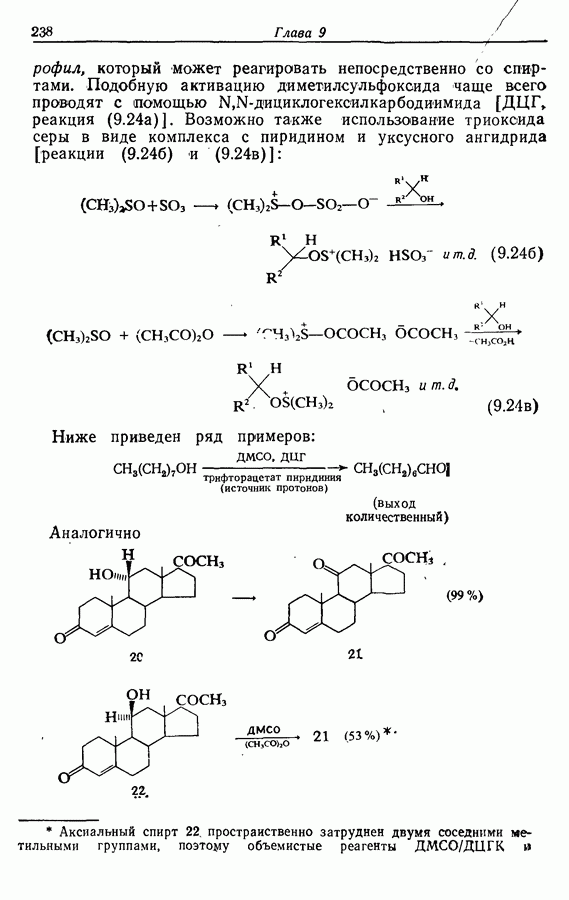
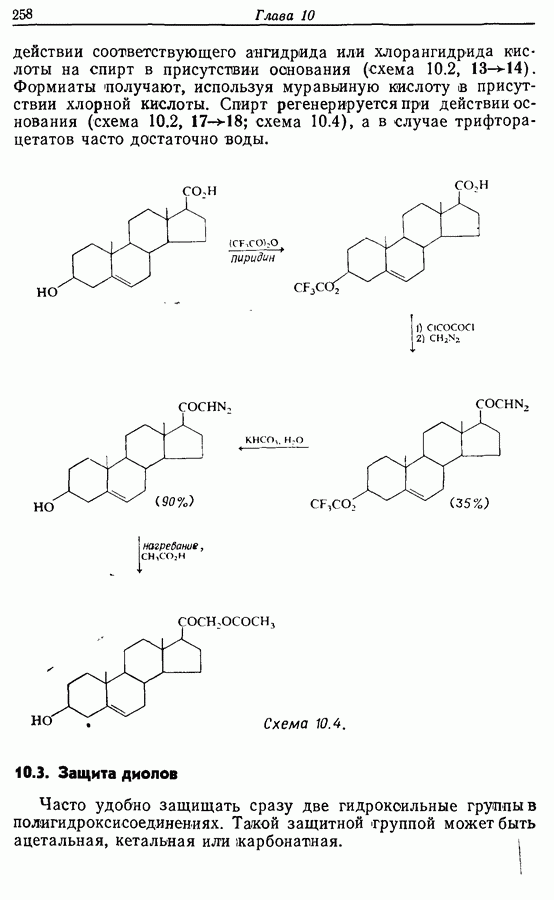
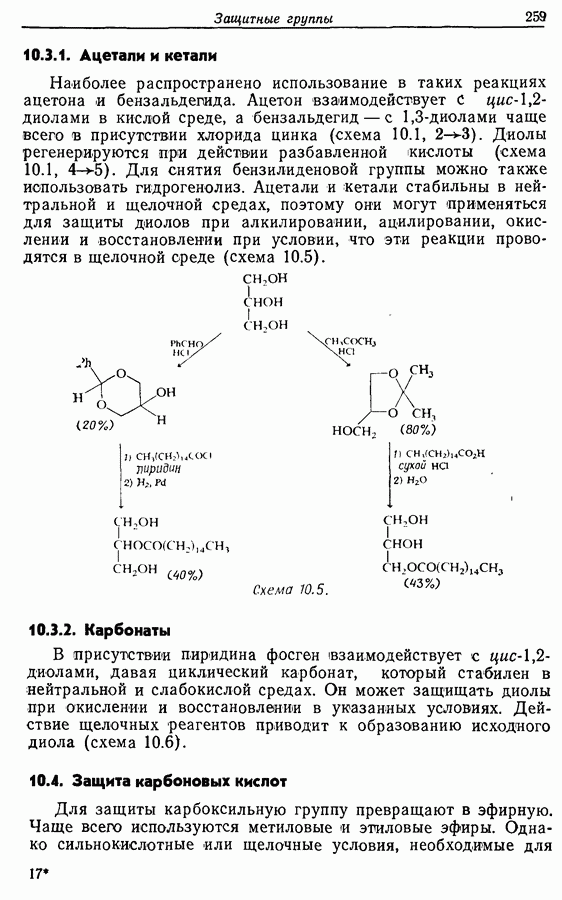
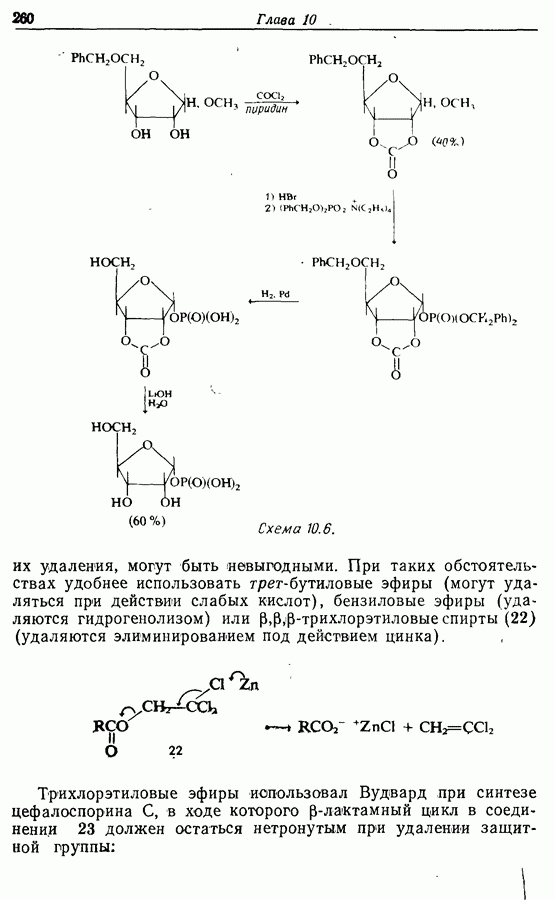
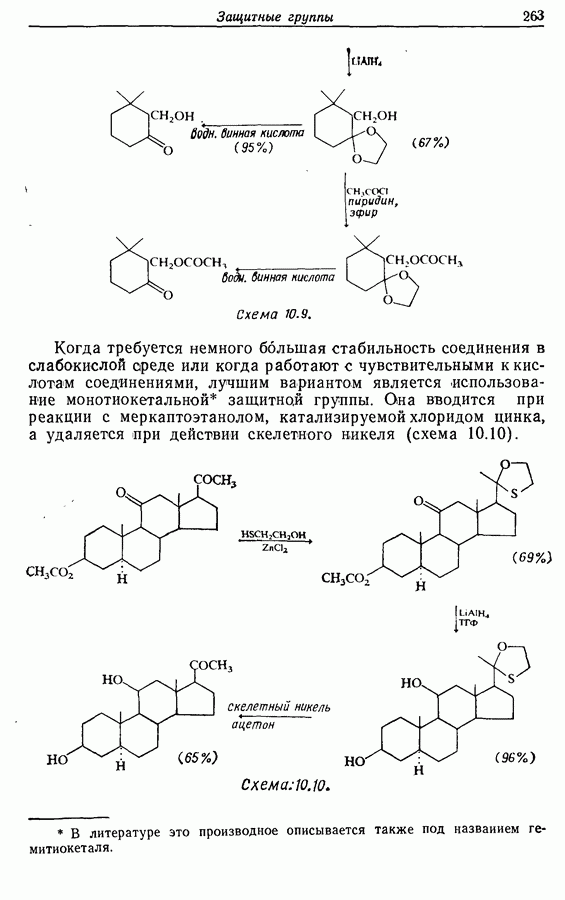
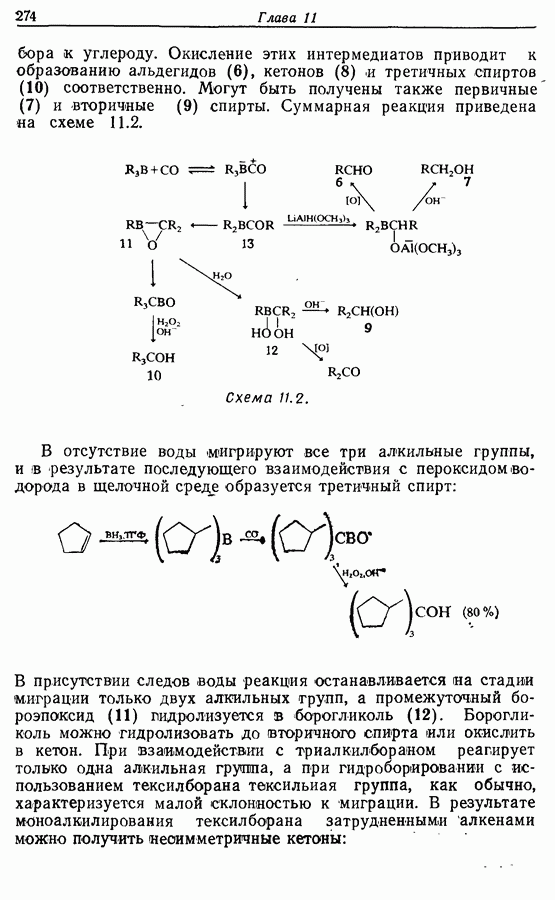
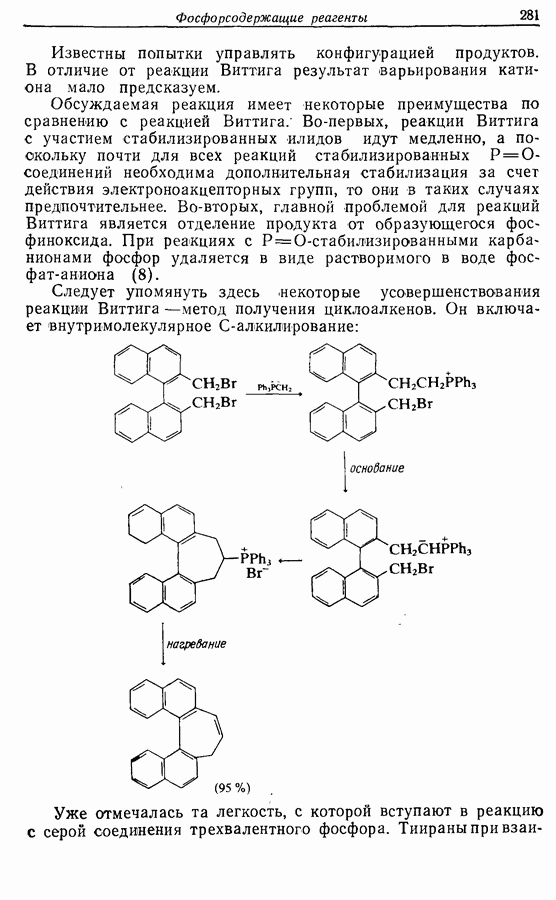
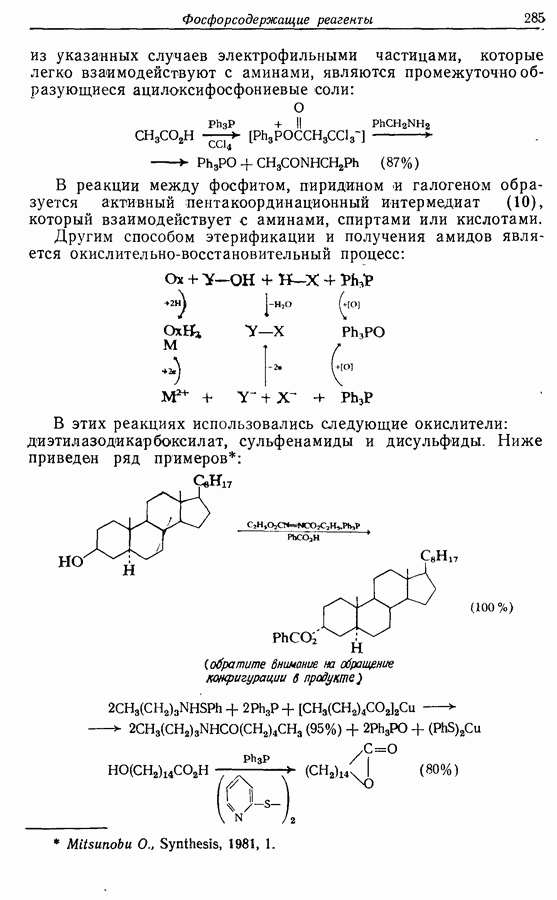
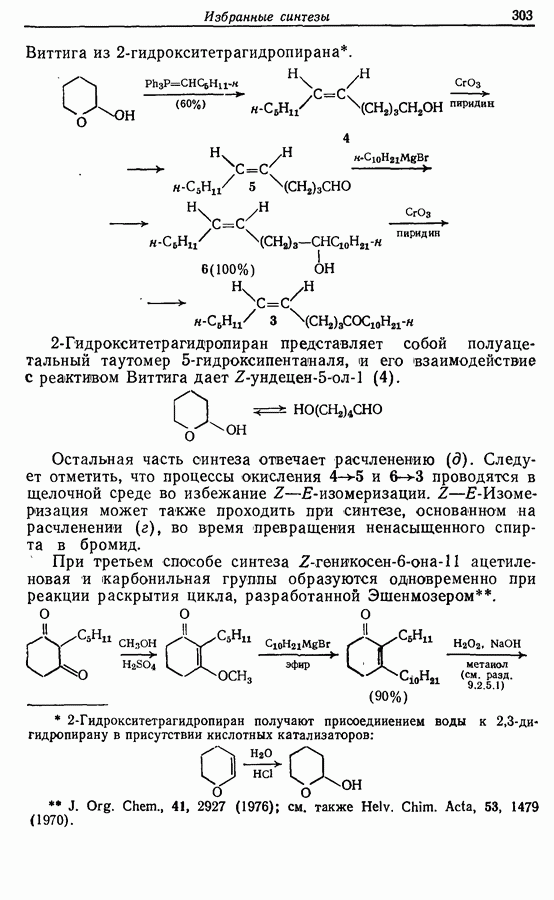
Для того чтобы аминокислоты могли соединяться друг с другом в правильном порядке, необходимо защитить аминогруппу в одном компоненте и карбоксильную группу в другом. Чаще всего для защиты аминогрупп используют бензилоксикарбонильную и трет-бутилоксикарбонильную группы, поскольку в большинстве случаев это приводит к уменьшению рацемизации на соседних центрах.
Кислотные группы часто защищают, переводя в бензильные сложные эфиры. При твердофазном синтезе аминокислота связывается с полимером в виде замещенного бензильного сложного эфира.
Другие функциональные группы также могут потребовать защиты. В частности, гуанидильную группу нитруют, а гидроксильные группы переводят в бензильные простые эфиры.

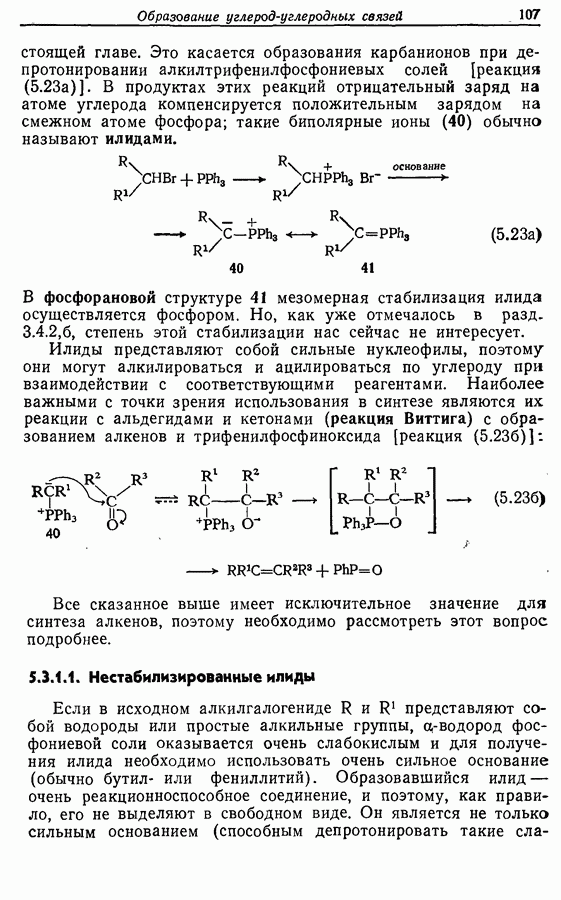
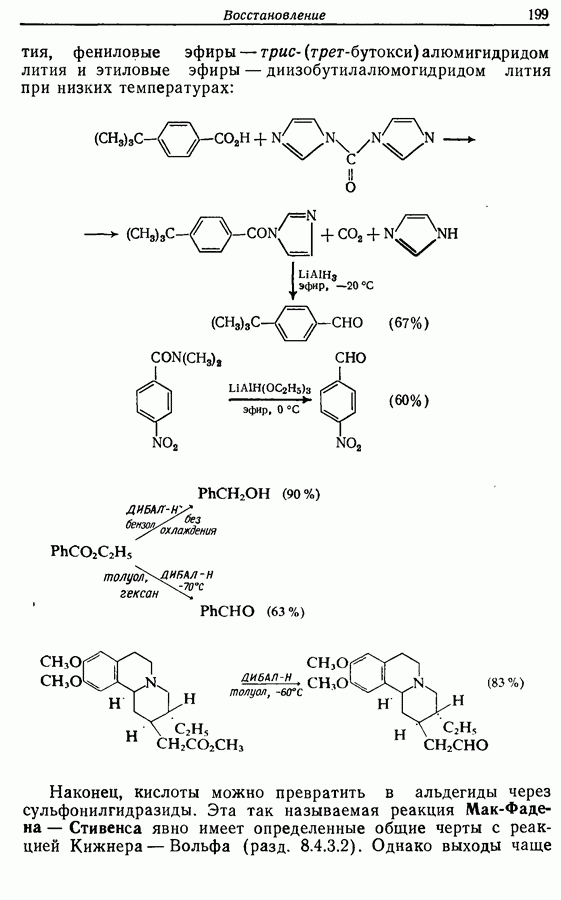
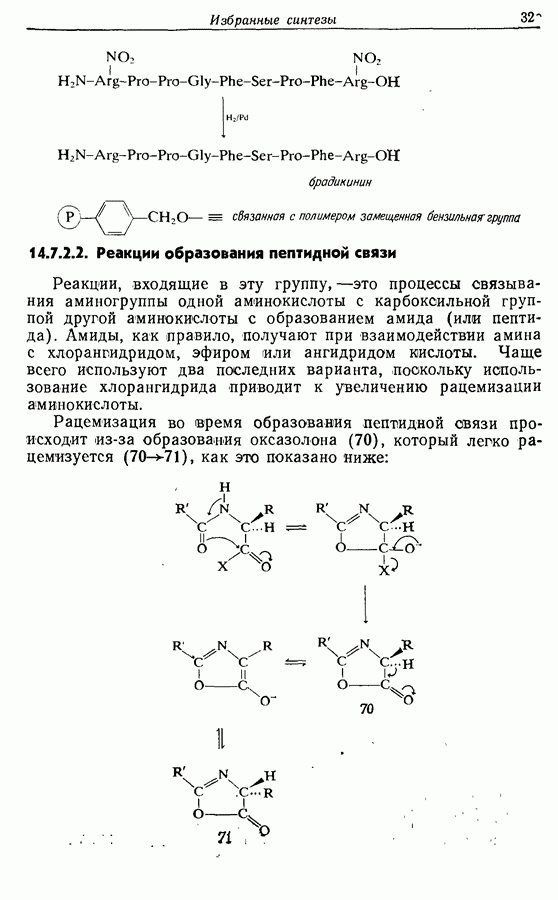
Бензильные группы удаляются из продукта при действии  в трифторуксусной кислоте, а нитрогруппы — при каталитическом гидрировании, как показано ниже на примере заключительных стадий твердофазного синтеза брадикинина:
в трифторуксусной кислоте, а нитрогруппы — при каталитическом гидрировании, как показано ниже на примере заключительных стадий твердофазного синтеза брадикинина:


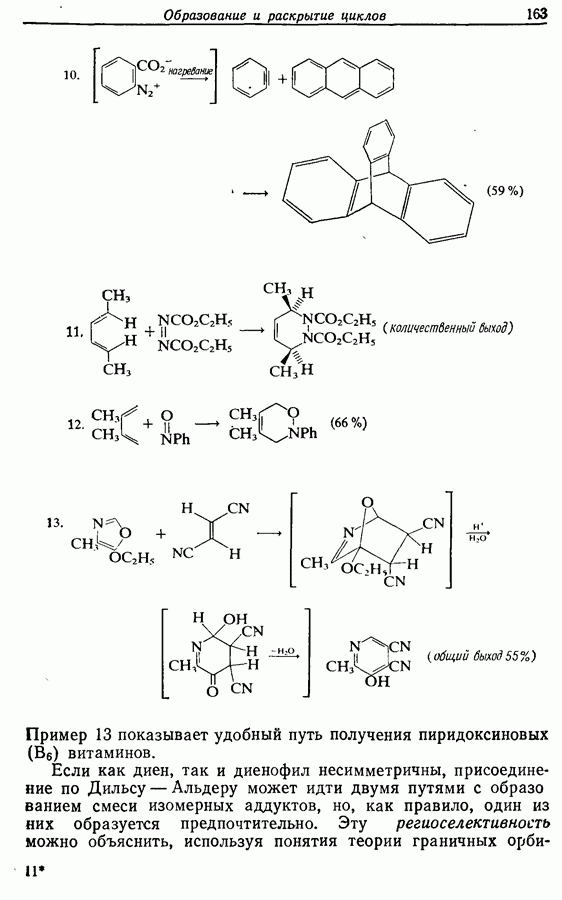
14.7.2.2. Реакции образования пептидной связи
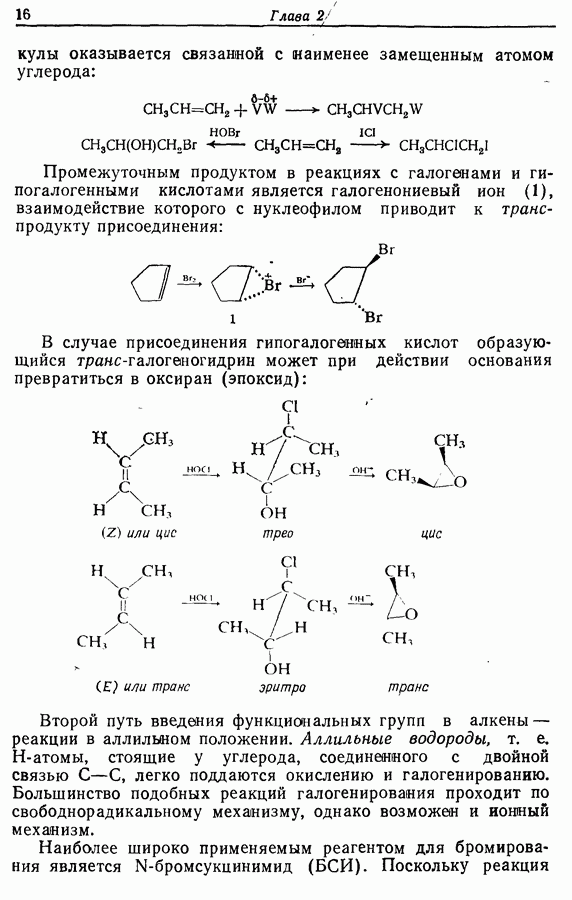
Реакции, входящие в эту группу, — это процессы связывания аминогруппы одной аминокислоты с карбоксильной группой другой аминокислоты с образованием амида (или пептида). Амиды, как правило, получают при взаимодействии амина с хлораншдридом, эфиром или ангидридом кислоты. Чаще всего используют два последних варианта, поскольку использование хлорангидрида приводит к увеличению рацемизации аминокислоты.
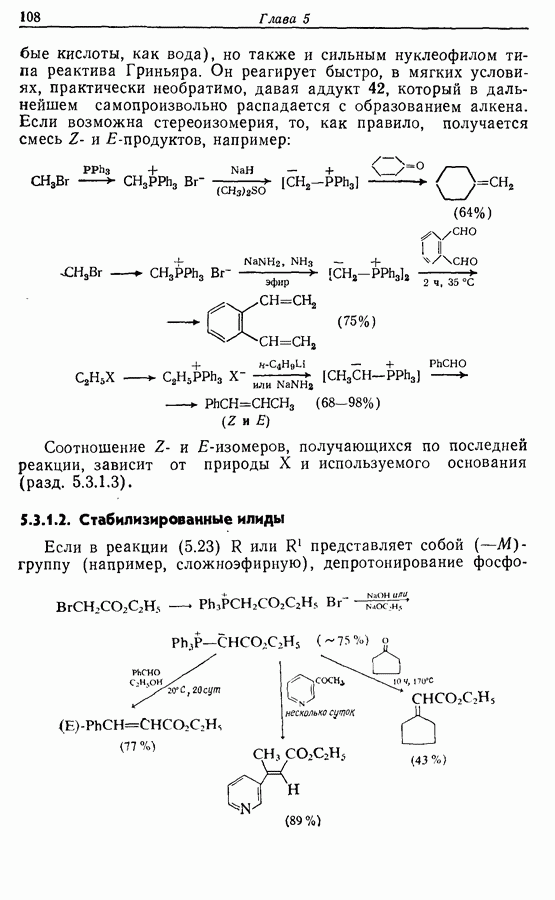
Рацемизация во время образования пептидной связи происходит из-за образования оксазолона (70), который легко рацемизуется  как это показано ниже:
как это показано ниже:

Скорость рацемизации зависит от природы групп  может быть как защитной группой для свободных аминогрупп [в этом случае рацемизация может быть снижена, если
может быть как защитной группой для свободных аминогрупп [в этом случае рацемизация может быть снижена, если  представляет собой
представляет собой  или
или  так и остатком пептидной цепи. В последнем случае почти ничего нельзя сделать для того, чтобы изменить степень рацемизации.
так и остатком пептидной цепи. В последнем случае почти ничего нельзя сделать для того, чтобы изменить степень рацемизации.  - это радикал используемой аминокислоты и поэтому не может быть модифицирован. X — это группа, применяемая для активации кислоты, и именно поэтому было проведено большое число исследований для того, чтобы найти лучший способ активации карбоксильной группы при малой степени рацемизации. Рассмотрим теперь несколько наиболее часто используемых методов активации карбоксильной группы.
- это радикал используемой аминокислоты и поэтому не может быть модифицирован. X — это группа, применяемая для активации кислоты, и именно поэтому было проведено большое число исследований для того, чтобы найти лучший способ активации карбоксильной группы при малой степени рацемизации. Рассмотрим теперь несколько наиболее часто используемых методов активации карбоксильной группы.
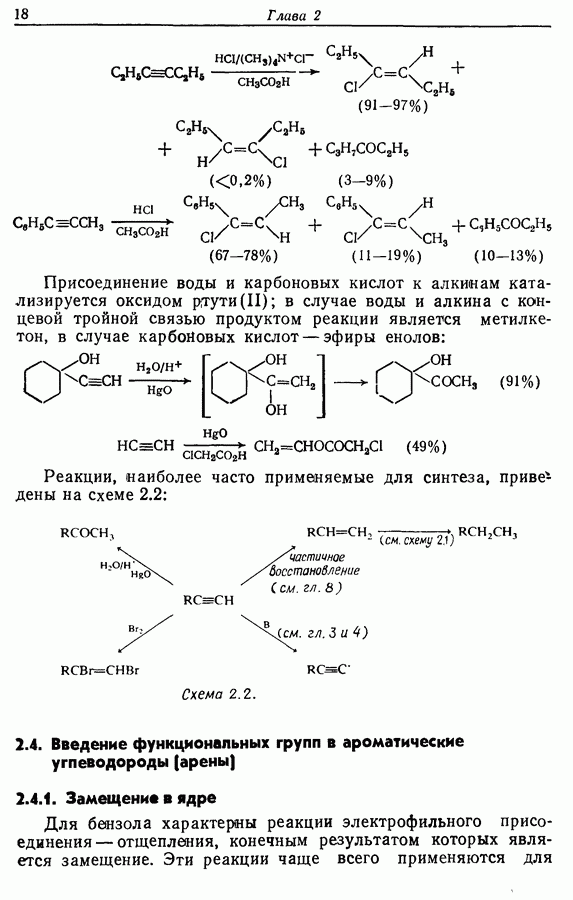
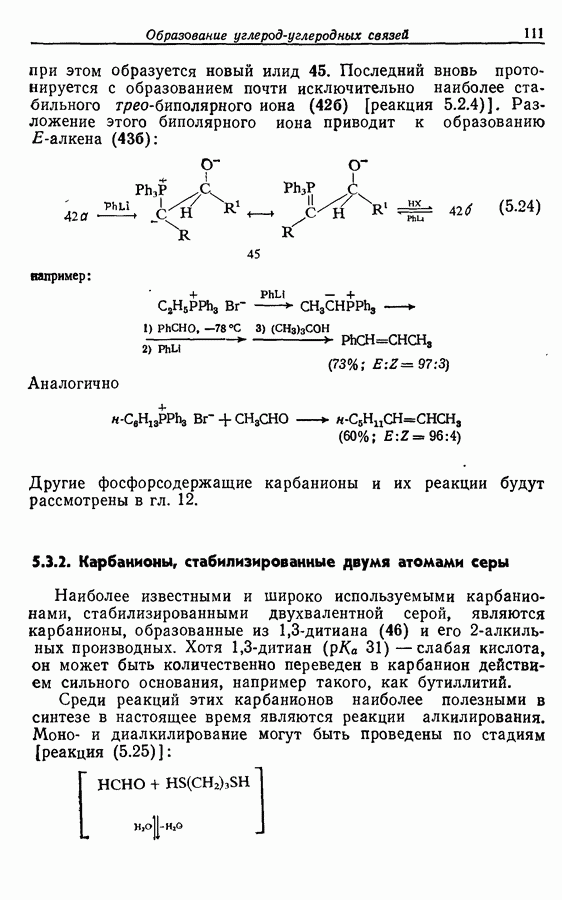
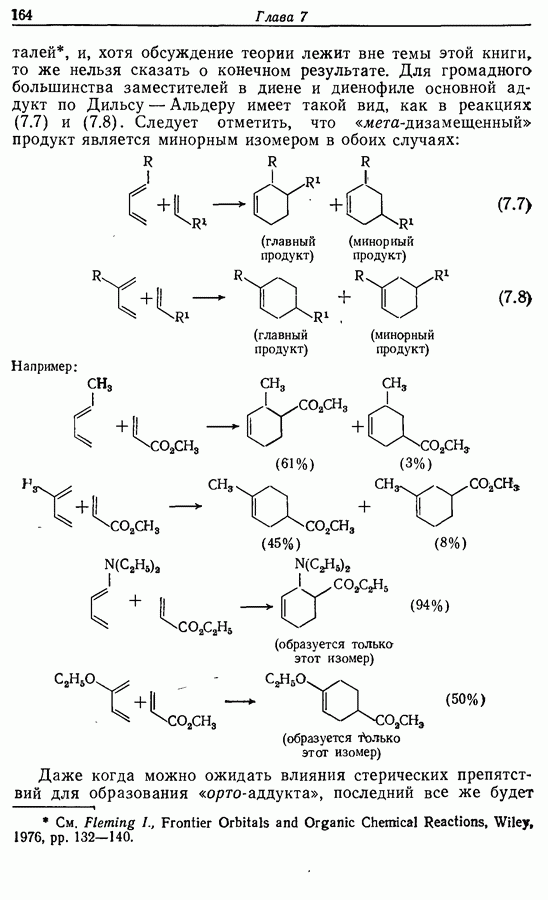
Азидный метод. Последовательность реакций, составляющая метод, приведена ниже:

Главное преимущество этого метода — небольшая рацемизация, однако он обладает и двумя существенными недостатками: во-первых, довольно большое число стадий  во-вторых, возможность перегруппировки азида (72) в изоцианат (73), что приводит к производному мочевины (74), которое трудно отделить от пептида:
во-вторых, возможность перегруппировки азида (72) в изоцианат (73), что приводит к производному мочевины (74), которое трудно отделить от пептида:

Этот метод часто используют в блочном синтезе, когда нет возможности связывать блоки через глициновые или пролиновые фрагменты (разд. 14.7.3),
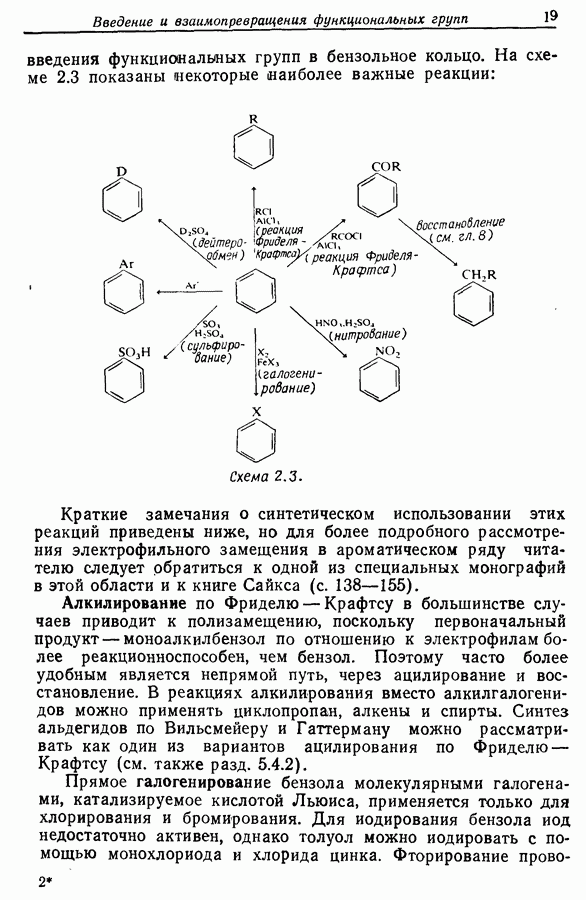
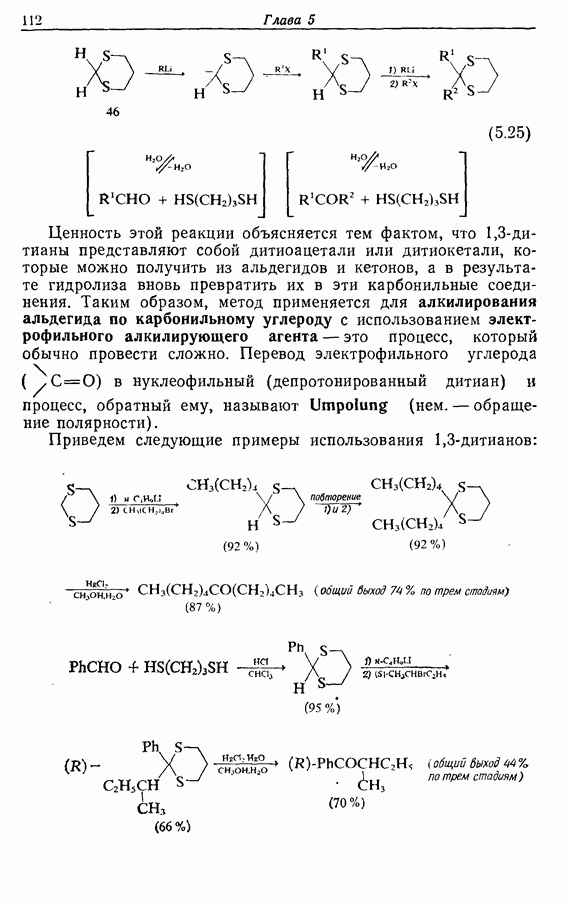
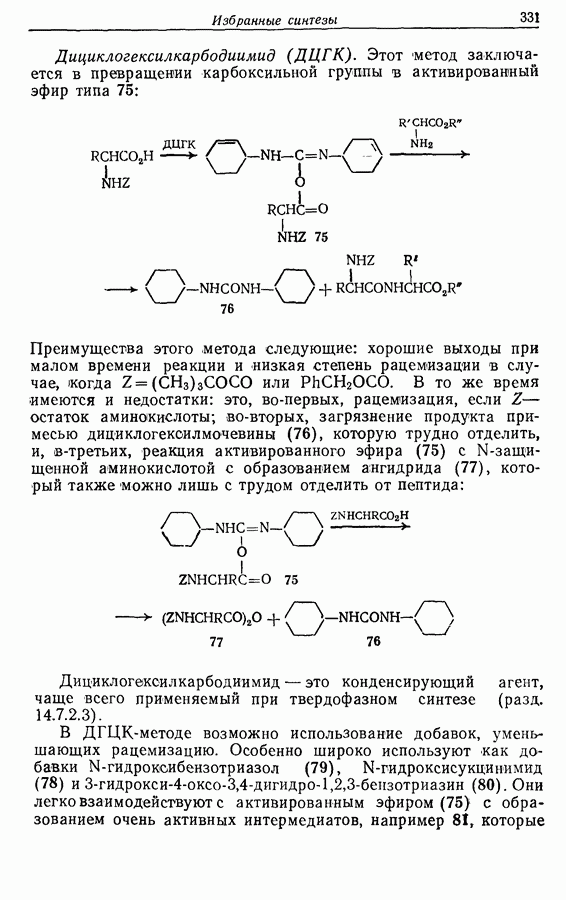
Дициклогексилкарбодиимид  Этот метод заключается в превращении карбоксильной группы в активированный эфир типа 75:
Этот метод заключается в превращении карбоксильной группы в активированный эфир типа 75:

Преимущества этого метода следующие: хорошие выходы при малом времени реакции и низкая степень рацемизации в случае, когда  или
или  В то же время имеются и недостатки: это, во-первых, рацемизация, если
В то же время имеются и недостатки: это, во-первых, рацемизация, если  остаток аминокислоты; во-вторых, загрязнение продукта примесью дициклогексилмочевины (76), которую трудно отделить, и, в-третьих, реакция активированного эфира (75) с
остаток аминокислоты; во-вторых, загрязнение продукта примесью дициклогексилмочевины (76), которую трудно отделить, и, в-третьих, реакция активированного эфира (75) с  -защищенной аминокислотой с образованием ангидрида (77), который также можно лишь с трудом отделить от пептида:
-защищенной аминокислотой с образованием ангидрида (77), который также можно лишь с трудом отделить от пептида:

Дициклогексилкарбодиимид — это конденсирующий агент, чаще всего применяемый при твердофазном синтезе (разд. 14.7.2.3).
В ДГЦК-методе возможно использование добавок, уменьшающих рацемизацию. Особенно широко используют как добавки  -гидроксибензотриазол (79),
-гидроксибензотриазол (79),  -гидроксисукцинимид (78) и
-гидроксисукцинимид (78) и  Они легко взаимодействуют с активированным эфиром (75) с образованием очень активных интермедиатов, например
Они легко взаимодействуют с активированным эфиром (75) с образованием очень активных интермедиатов, например  которые
которые
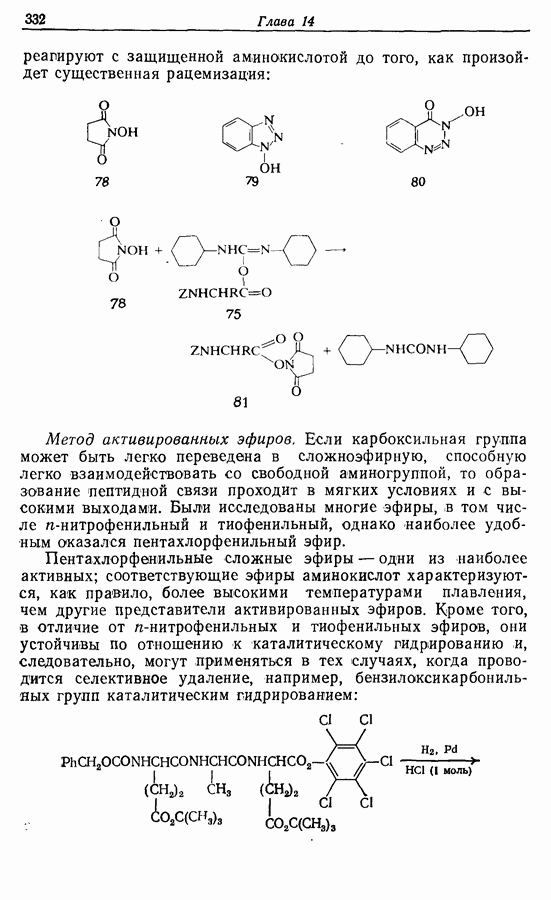
реагируют с защищенной аминокислотой до того, как произойдет существенная рацемизация:

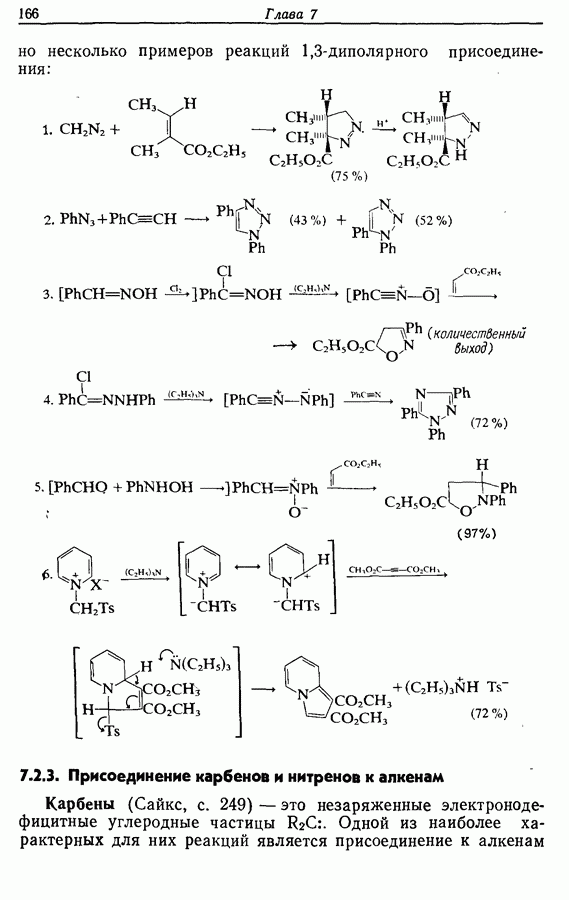
Метод активированных эфиров. Если карбоксильная группа может быть легко переведена в сложноэфирную, способную легко взаимодействовать со свободной аминогруппой, то образование пептидной связи проходит в мягких условиях и с высокими выходами. Были исследованы многие эфиры, в том числе  -нитрофенильный и тиофенильный, однако наиболее удобным оказался пентахлорфенильный эфир.
-нитрофенильный и тиофенильный, однако наиболее удобным оказался пентахлорфенильный эфир.
Пентахлорфенильные сложные эфиры — одни из наиболее активных; соответствующие эфиры аминокислот характеризуются, как правило, более высокими температурами плавления, чем другие представители активированных эфиров. Кроме того, в отличие от  -нитрофенильных и тиофенильных эфиров, они устойчивы по отношению к каталитическому гидрированию и, следовательно, могут применяться в тех случаях, когда проводится селективное удаление, например, бензилоксикарбонильных групп каталитическим гидрированием:
-нитрофенильных и тиофенильных эфиров, они устойчивы по отношению к каталитическому гидрированию и, следовательно, могут применяться в тех случаях, когда проводится селективное удаление, например, бензилоксикарбонильных групп каталитическим гидрированием:


Рацемизация особенно низка: считают, что это результат стерических требований атомов хлора в положениях 2 и 6, что препятствует образованию оксазолона.
Пентахлорфенильные эфиры можно получить из аминокислот или реакцией с пентахлорфенолом в присутствии дициклогексилкарбодиимида, или реакцией с пентахлорфенилтрихлор-ацетатом в присутствии триэтиламина:

14.7.2.3. Твердофазный синтез пептидов
Один из важных успехов в пептидном синтезе был достигнут в 1962 г., когда Меррифильд впервые описал синтез тетрапептида  с помощью твердофазного метода, который с тех пор часто связывают с его именем. Этот метод состоит из следующих стадий:
с помощью твердофазного метода, который с тех пор часто связывают с его именем. Этот метод состоит из следующих стадий:
1. Присоединение  -защищенной аминокислоты к сополимеру стирола с дивинилбензолом, в котором 5% его фенильных групп хлорметилировано (82):
-защищенной аминокислоты к сополимеру стирола с дивинилбензолом, в котором 5% его фенильных групп хлорметилировано (82):


Следует отметить, что  — это замещенный бензильный сложный эфир, следовательно, в ходе этой стадии не только происходит присоединение аминогруппы к сополимеру, но также осуществляется защита карбоксильной группы.
— это замещенный бензильный сложный эфир, следовательно, в ходе этой стадии не только происходит присоединение аминогруппы к сополимеру, но также осуществляется защита карбоксильной группы.
2. Удаление  -защитной группы (стадия А).
-защитной группы (стадия А).
3. Реакция свободной аминогруппы с  -защищенной аминокислотой, чаще всего с
-защищенной аминокислотой, чаще всего с  в качестве конденсирующего агента (с добавками или без них) (стадия Б):
в качестве конденсирующего агента (с добавками или без них) (стадия Б):

4. Повторение стадий  с использованием
с использованием  -защищен-ных аминокислот до тех пор, пока все заданные аминокислоты не окажутся связанными.
-защищен-ных аминокислот до тех пор, пока все заданные аминокислоты не окажутся связанными.
5. Снятие защищенного пептида с полимера; чаще всего для этого применяют  в трифторуксусной кислоте. Этот реагент удаляет также и другие защитные группы, в том числе и
в трифторуксусной кислоте. Этот реагент удаляет также и другие защитные группы, в том числе и  -бензилоксикарбонил,
-бензилоксикарбонил,  -бутилокоикарбонил и О-бензил.
-бутилокоикарбонил и О-бензил.
6. Удаление других защитных групп.

Может оказаться невыгодным синтезировать таким способом пептид, содержащий более 15 аминокислотных единиц, но рибонуклеаза, которая состоит из 124 аминокислотных единиц, была синтезирована целиком с помощью твердофазных реакций блочным методом (разд. 14.7.1).
Опубликовано большое число обзоров и книг, содержащих критические оценки метода Меррифильда. Мы можем лишь перечислить некоторые из основных достоинств и ограничений метода.
Достоинства метода: 1) реакции идут быстро с высокими выходами; 2) почти не происходит рацемизации (или она очень мала), если  трет-бутил или бензилоксикарбонил, поскольку реакция идет по
трет-бутил или бензилоксикарбонил, поскольку реакция идет по  -защищенной аминокислоте; 3) очистка промежуточных соединений представляет не что иное, как отмывку полимера от неполимерных реагентов, если реакция доведена до конца; 4) метод может быть автоматизирован (синтез нонапептида может проводиться примерно за
-защищенной аминокислоте; 3) очистка промежуточных соединений представляет не что иное, как отмывку полимера от неполимерных реагентов, если реакция доведена до конца; 4) метод может быть автоматизирован (синтез нонапептида может проводиться примерно за 
Ограничения метода: 1) неполное присоединение С-конце-вой аминокислоты к бензильным группам полимера может приводить к образованию примесей, например при синтезе пентапептида  может быть образована цепь
может быть образована цепь  при реакции второй аминокислоты с оставшейся в первой стадии бензильной группой. Эта реакция конкурирует со стадией
при реакции второй аминокислоты с оставшейся в первой стадии бензильной группой. Эта реакция конкурирует со стадией  неполное присоединение
неполное присоединение  -защищенной аминокислоты к свободной аминогруппе (стадия
-защищенной аминокислоты к свободной аминогруппе (стадия  может привести к образованию сокращенных пептидов (например,
может привести к образованию сокращенных пептидов (например,  и неправильной последовательности (например,
и неправильной последовательности (например,  отсутствие аналитических методов определения примесей, которые могут применяться без отделения пептида от полимера. Такое определение может быть очень расточительным, требовать много времени и само по себе приводит к распаду продукта.
отсутствие аналитических методов определения примесей, которые могут применяться без отделения пептида от полимера. Такое определение может быть очень расточительным, требовать много времени и само по себе приводит к распаду продукта.
14.7.3. Синтез пептида с высокой молекулярной массой — основного трипсинного ингибитора (BTI) из поджелудочной железы быка
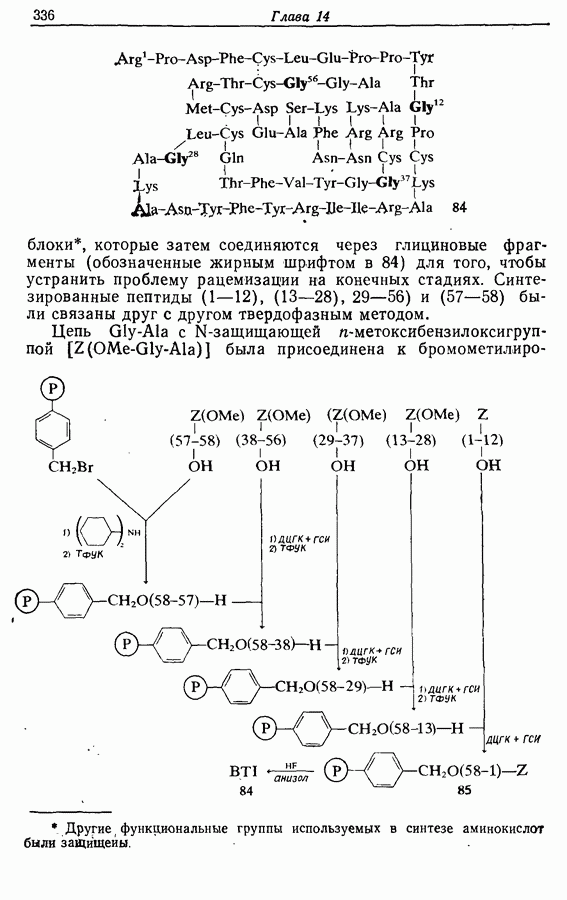
Установлено, что этот пептид, состоящий из 58 аминокислотных единиц (молекулярная масса 6500), имеет последовательность аминокислотных единиц, приведенную на стр. 336.
Синтез этого пептида, описанный в ряде статей, служит иллюстрацией стратегии, применяемой в подобных случаях.
В методе используются предварительно синтезированные

блоки, которые затем соединяются через глициновые фрагменты (обозначенные жирным шрифтом в 84) для того, чтобы устранить проблему рацемизации на конечных стадиях. Синтезированные пептиды (1—12), (13—28), 29—56) и (57—58) были связаны друг с другом твердофазным методом.
Цепь  -защищающей
-защищающей  -метоксибензилоксигруппой
-метоксибензилоксигруппой  была присоединена к
была присоединена к

бромометилированному сополимеру стирола с дивинилбензолом. Каждый пептидный блок  и (1—12)] был присоединен к растущей пептидной цепи, при этом в качестве конденсирующего агента использовали дициклогексилкарбодиимид (ДЦГК с добавкой N-гидроксисукцинимида (ГСИ). Активный пептид отделяли от полимера, защитные группы удаляли действием
и (1—12)] был присоединен к растущей пептидной цепи, при этом в качестве конденсирующего агента использовали дициклогексилкарбодиимид (ДЦГК с добавкой N-гидроксисукцинимида (ГСИ). Активный пептид отделяли от полимера, защитные группы удаляли действием  Все это можно записать в виде схемы (см. стр. 336; ТФУК - трифторуксусная кислота).
Все это можно записать в виде схемы (см. стр. 336; ТФУК - трифторуксусная кислота).
Общий выход продукта 85 составил около 40%, из которых может быть получено лишь 10% очищенного активного 84.
Блоки были синтезированы связыванием фрагментов, полученных либо линейным, либо конвергентным синтезом. При построении блока (1—12) связывание фрагментов проводили по пролиновым звеньям, так как при этом рацемизация минимальна. В большинстве случаев связывание проводилось методом активированного эфира с использованием пентахлорфенильных (РСР) или  -нитрофенильных
-нитрофенильных  эфиров. Схема синтеза
эфиров. Схема синтеза  -бензилоксикарбонилзащищенного блока
-бензилоксикарбонилзащищенного блока  приведена ниже.
приведена ниже.

В тех случаях, когда пролиновые звенья не могут быть использованы в качестве места связывания фрагментов, их соединение проводят азидным методом, при котором меньше рацемизация.
Общая активность продукта (80%) выше, чем в случае постадийного синтеза по Меррифильду (30%).
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ВВЕДЕНИЕ И ВЗАИМОПРЕВРАЩЕНИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП
- 2.1. Введение функциональных групп в апканы
- 2.2. Введение функциональных групп в алкены
- 2.3. Введение функциональных групп в апкины
- 2.4. Введение функциональных групп в ароматические углеводороды (арены)
- 2.5. Введение функциональных групп в производные бензола
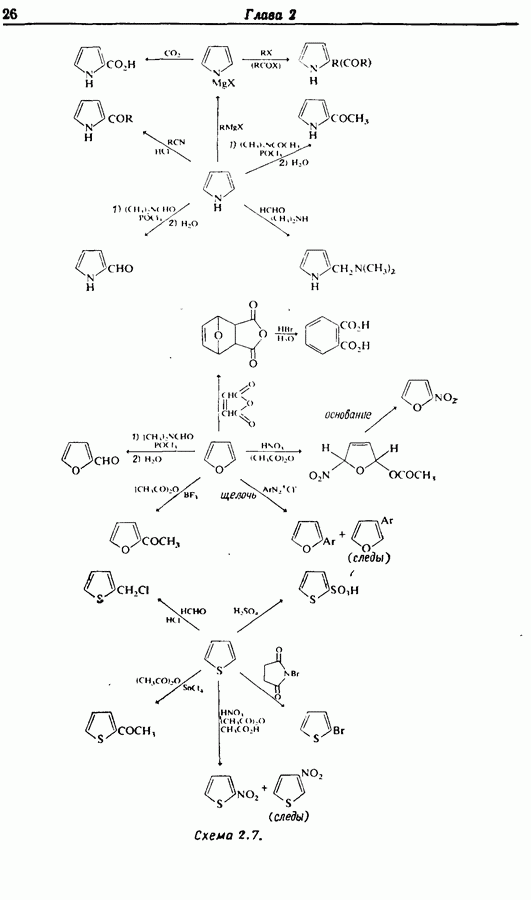
- 2.6. Введение функциональных групп в простые гетероциклические соединения
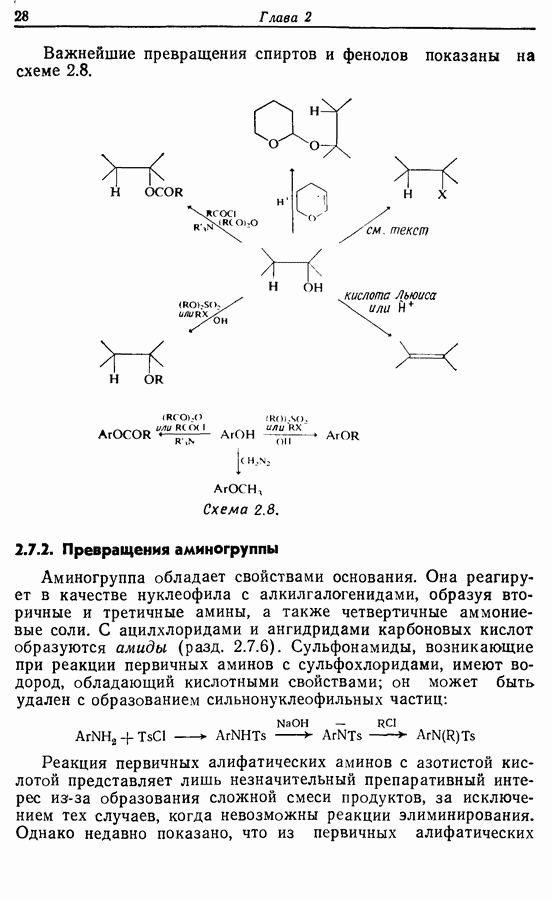
- 2.7. Взаимопревращения функциональных групп
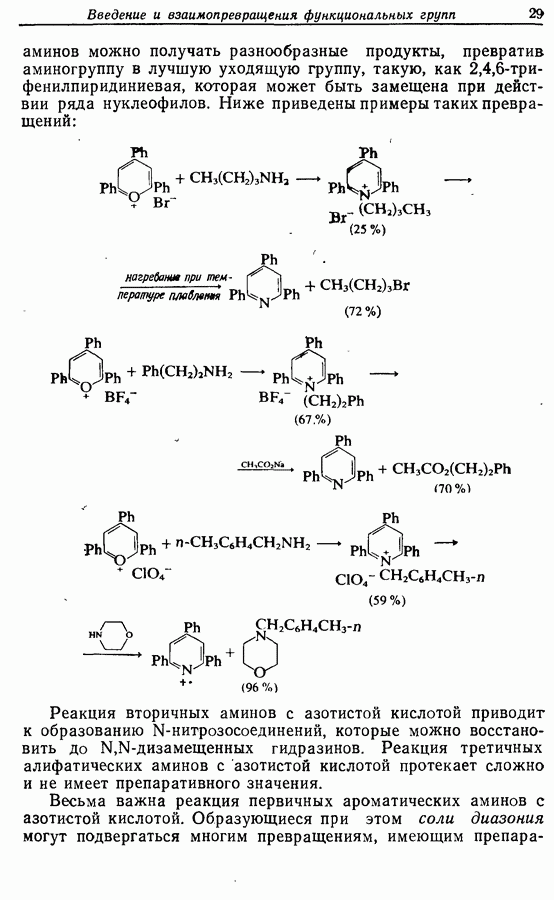
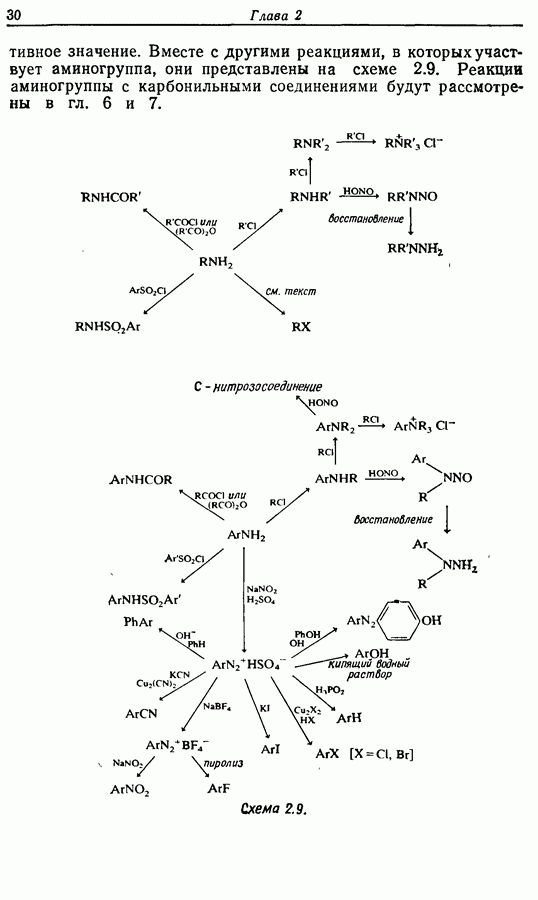
- 2.7.2. Превращения аминогруппы
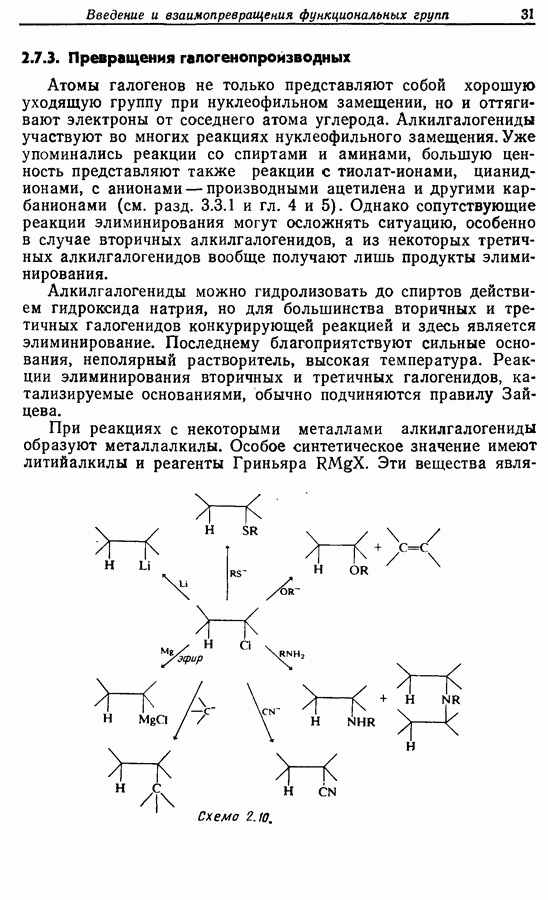
- 2.7.3. Превращения галогенопроизводных
- 2.7.4. Превращения нитросоединений
- 2.7.5. Превращения альдегидов и кетонов
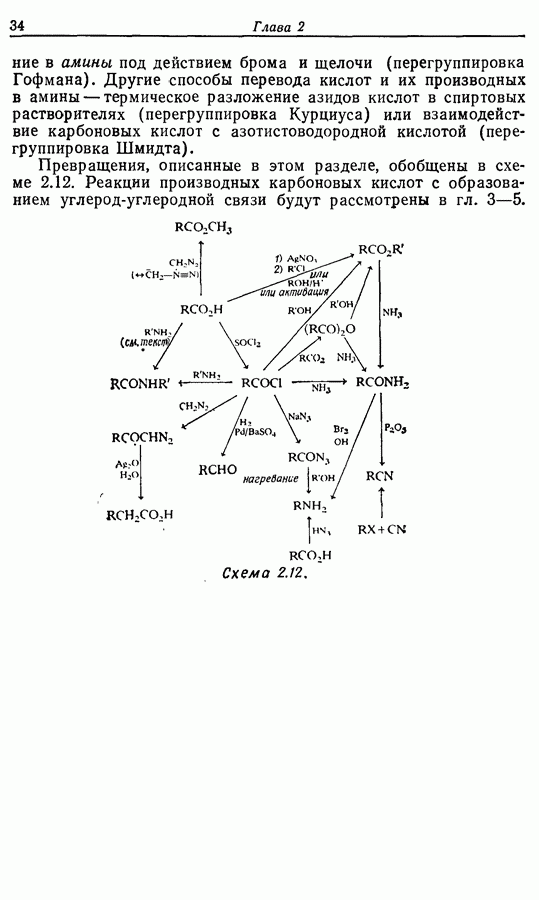
- 2.7.6. Превращения кислот и их производных
- 3. ПРИНЦИПЫ ОБРАЗОВАНИЯ УГЛЕРОД-УГЛЕРОДНОЙ СВЯЗИ
- 3.2. Расчленение и синтоны
- 3.3. Электрофильные углеродные частицы
- 3.4. Нуклеофильиые углеродные частицы
- 3.4.2. Стабилизированные карбанионы
- 3.4.3. Алкены, арены и гетероарены
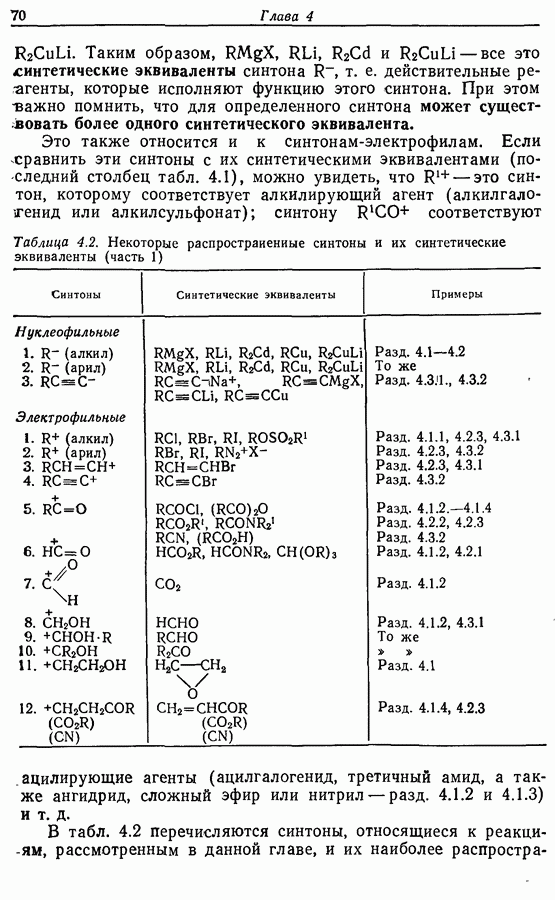
- 4. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: РЕАКЦИИ МЕТАЛЛООРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 4.1. Реактивы Гриньяра и электрофилы
- 4.2. Другие металлоорганические реактивы и электрофилы
- 4.2.2. Цинк- и кадмийорганические соединения
- 4.2.3. Органические соединения меди (I)
- 4.3. Реакции нуклеофилов, образованных из алкинов-1
- 4.3.2. Алкинильные соединения меди (I)
- 4.4. Выводы
- 4.5. Примеры
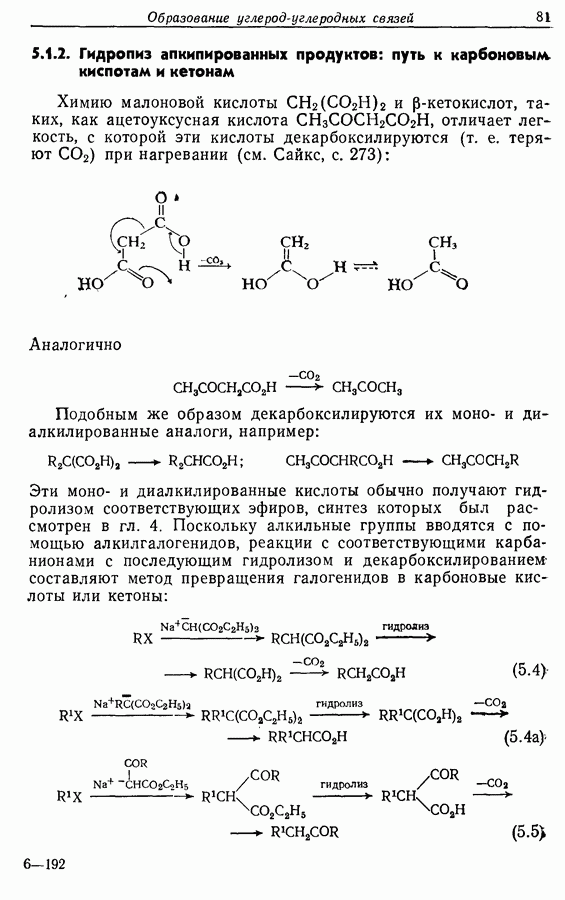
- 5. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: ИСПОЛЬЗОВАНИЕ СТАБИЛИЗИРОВАННЫХ КАРБАНИОНОВ И РОДСТВЕННЫХ НУКЛЕОФИЛОВ
- 5.1.1. Алкилирование
- 5.1.2. Гидролиз алкинированных продуктов: путь к карбоновым кислотам и кетонам
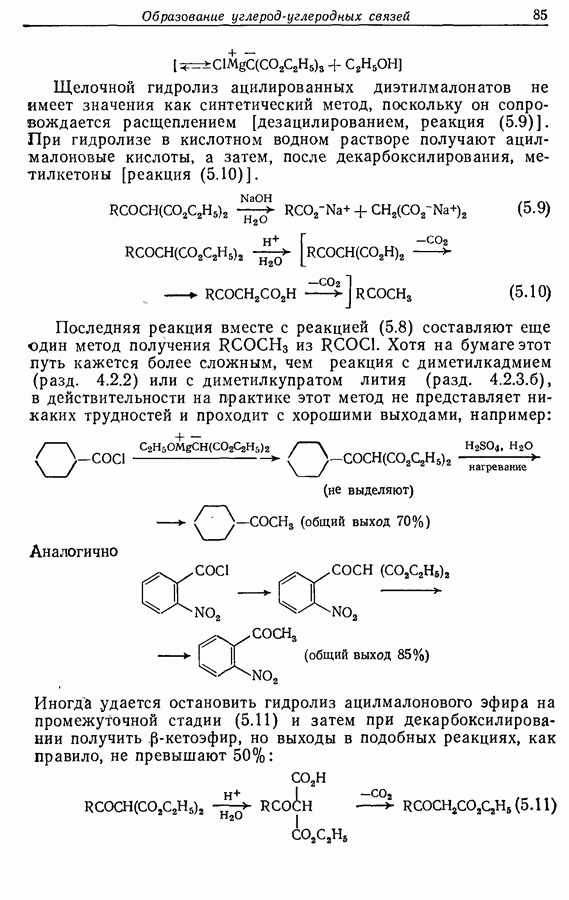
- 5.1.3. Ацилирование
- 5.1.4. Реакции конденсации
- 5.1.5. Реакции с соединениями типа … и родственными системами: реакция Михаэля
- 5.2. Карбанионы, стабилизированные одной (-М)-группой
- 5.2.3. Косвенные пути получения a-алкилированных альдегидов и кетонов
- 5.2.4. Реакции конденсации
- 5.2.5. Реакция Михаэля
- 5.3. Карбанионы, стабилизированные соседними атомами фосфора или серы
- 5.3.2. Карбанионы, стабилизированные двумя атомами серы
- 5.4. Алкены, арены и гетероарены как нуклеофилы
- 5.4.3. Реакции присоединения и конденсации с карбонильными и родственными им соединениями
- 5.5. Заключение
- 5.6. Задачи
- 6. ОБРАЗОВАНИЕ СВЯЗЕЙ УГЛЕРОДА С ГЕТЕРОАТОМОМ: ОСНОВНЫЕ ПРИНЦИПЫ
- 6.1. Связи углерод — галоген
- 6.2. Связи углерод — кислород и углерод — сера
- 6.3. Связи углерод — азот
- 6.3.2. Электрофильный азот и нуклеофильный углерод
- 6.3.3. Нитрозосоединения, включая нитриты
- 7. ОБРАЗОВАНИЕ И РАСКРЫТИЕ ЦИКЛОВ
- 7.1. Внутримолекулярная циклизация в результате электрофильно-нуклеофильного взаимодействия
- 7.1.2. Условия внутримолекулярного циклообразования. Правила Болдуина
- 7.1.3. Присоединение по Михаэлю в процессах циклизации
- 7.1.4. Образование ароматических и гетероароматических циклов
- 7.2. Циклоприсоединение
- 7.2.2. 1,3-Диполярное циклоприсоединение
- 7.2.3. Присоединение карбенов и нитренов к алкенам
- 7.3. Электроциклическое циклообразование
- 7.4. Раскрытие цикла
- 7.5. Выводы и задачи
- 8. ВОССТАНОВЛЕНИЕ
- 8.1. Каталитическое гидрирование
- 8.2. Восстановление гидридами металлов
- 8.3. Восстановление растворяющимися металлами
- 8.4. Восстановление определенных функциональных групп
- 8.4.2. Восстановление алкинов
- 8.4.3. Восстановление альдегидов и кетонов
- 8.4.4. Восстановление карбоновых кислот и их производных
- 8.4.5. Восстановление нитрилов
- 8.4.6. Восстановление иминов и оксимов, включая восстановительное алкилирование
- 8.5. Восстановительное расщепление связи углерод — гетероатом
- 8.6. Восстановительное раскрытие цикла в эпоксидах
- 8.7. Восстановление a,b-ненасыщенных карбонильных соединений
- 8.8. Восстановление сопряженных диенов
- 8.9. Восстановление ароматических и гетероароматических соединений
- 9. ОКИСЛЕНИЕ
- 9.2. Окисление углеводородов
- 9.2.2. Аллильное окисление
- 9.2.3. Бензильное окисление
- 9.2.4. Дегидрирование алканов, алкильных групп и алкенов
- 9.2.5. Окислительное присоединение к алкенам
- 9.2.6. Окислительная деструкция алкенов
- 9.2.7. Окисление алкинов
- 9.3. Окисление спиртов и их производных
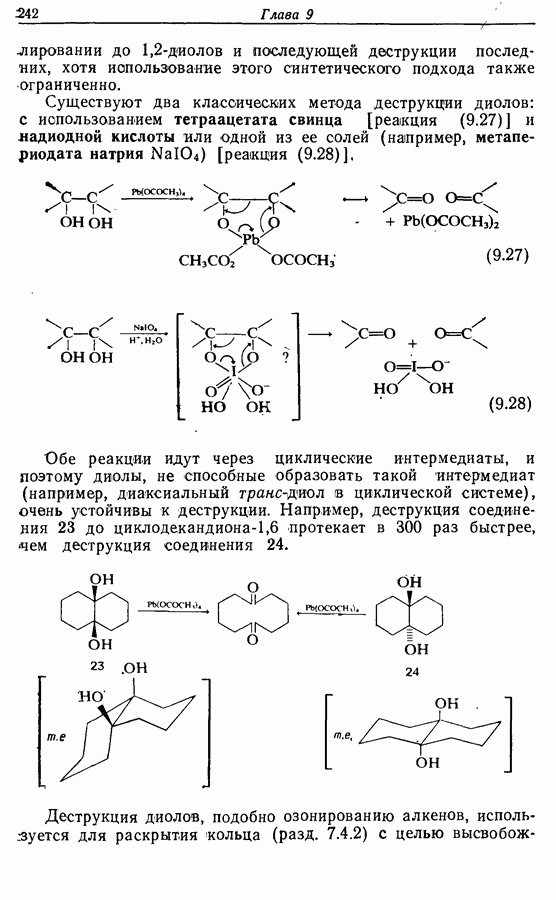
- 9.3.2. Окислительная деструкция 1,2-диолов
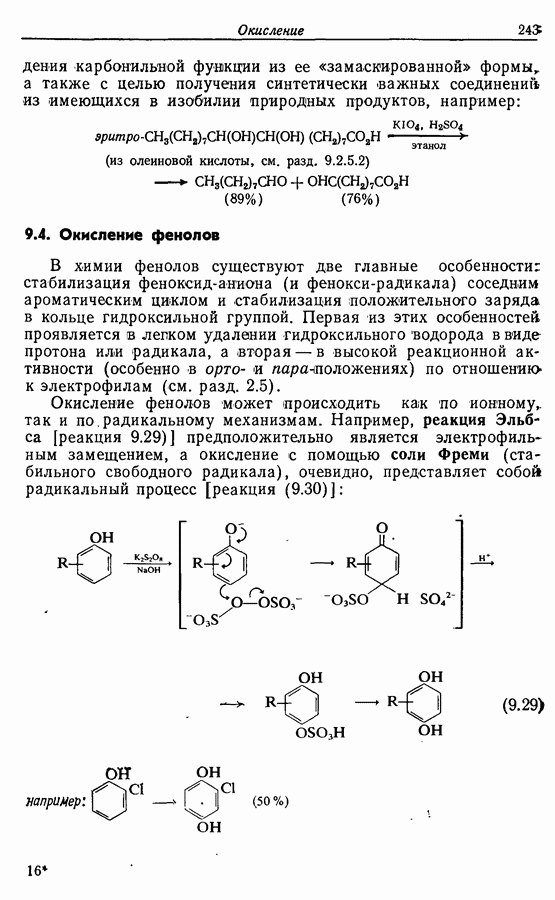
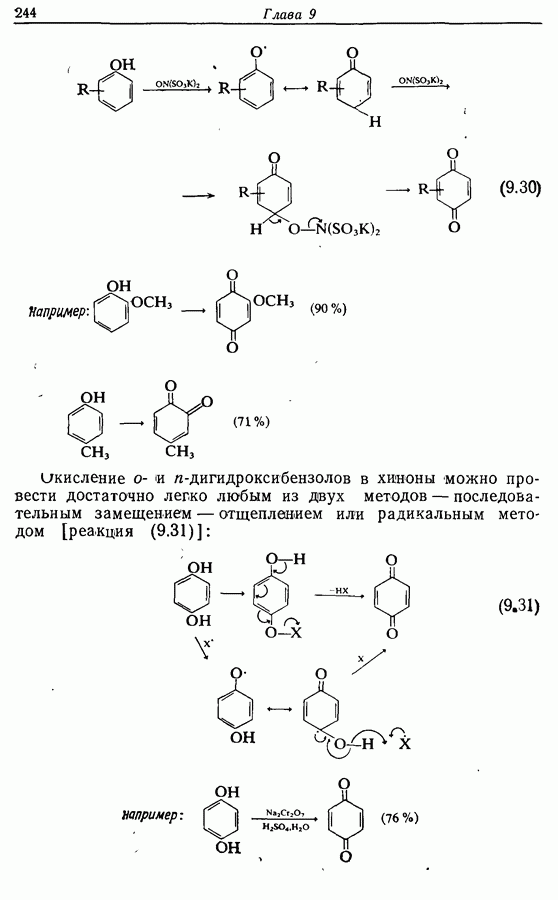
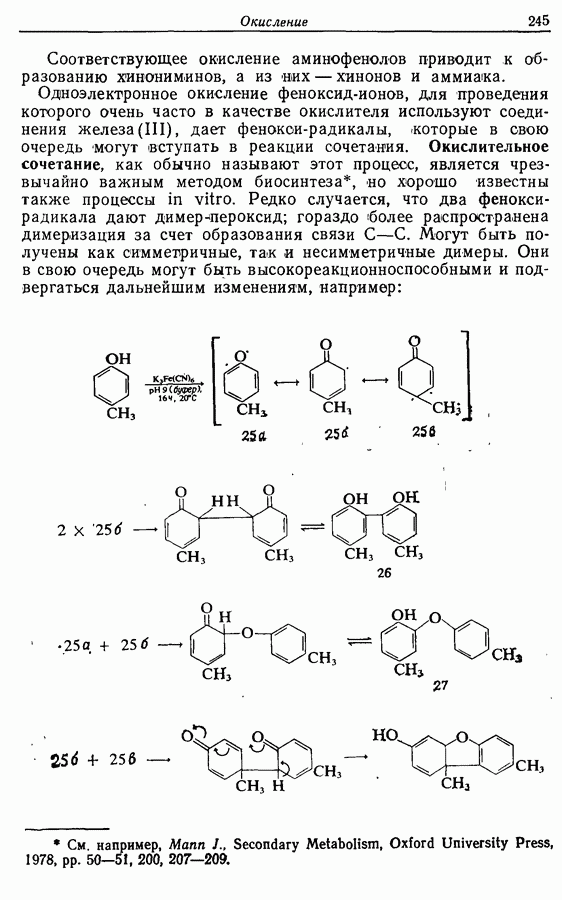
- 9.4. Окисление фенолов
- 9.5. Окисление альдегидов и кетонов
- 9.5.2. Окисление в 1,2-дикарбонильные соединения
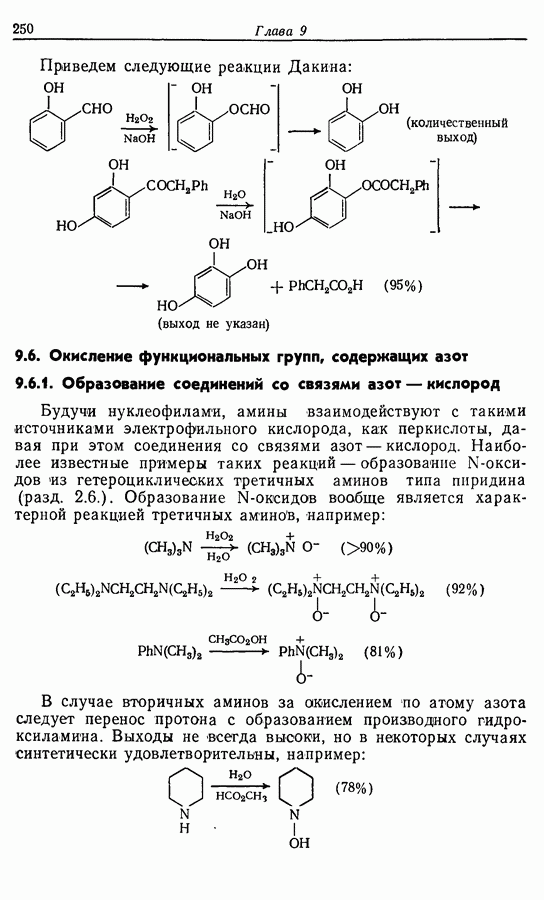
- 9.5.3. Окисление до сложных эфиров: реакции Байера — Виллигера и Дакина
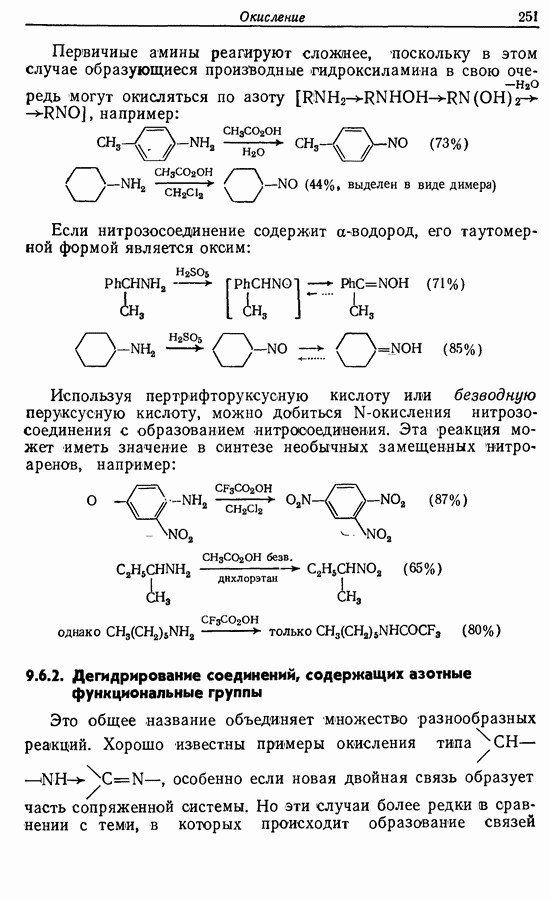
- 9.6. Окисление функциональных групп, содержащих азот
- 9.6.2. Дегидрирование соединений, содержащих азотные функциональные группы
- 9.7. Окисление серусодержащих функциональных групп
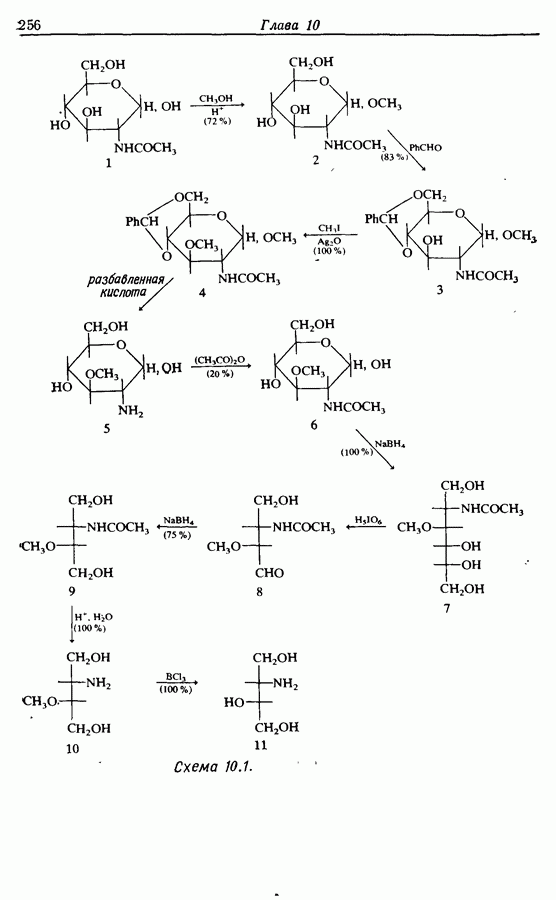
- 10. ЗАЩИТНЫЕ ГРУППЫ
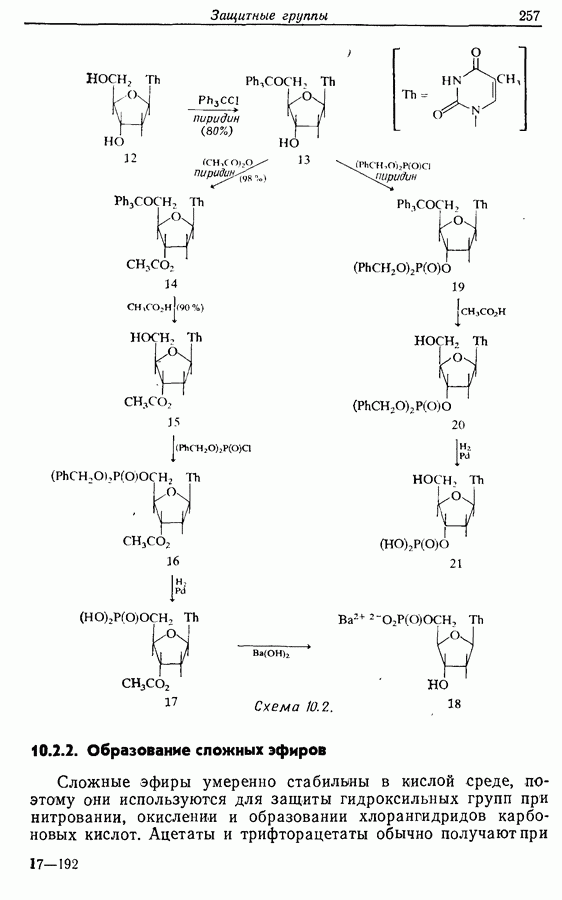
- 10.2. Защита спиртов
- 10.3. Защита диолов
- 10.4. Защита карбоновых кислот
- 10.5. Защита аминогрупп
- 10.6. Защита карбонильных групп
- 11. БОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 11.1. Гидроборирование алкенов при действии борана
- 11.2. Гидроборирование алкенов действием алкилборанов
- 11.3. Реакции борорганических соединений
- 11.4. Гидроборирование диенов
- 11.5. Гидроборирование алкинов
- 12. ФОСФОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 12.1. Введение в химию фосфорорганических соединений
- 12.2. Образование углерод-углеродных двойных связей
- 12.3. Превращения функциональных групп
- 12.4. Реакции дезоксигенирования
- 13. КРЕМНИЙСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 13.1. Введение в химию кремнийорганических соединений
- 13.2. Синтез кремнийорганических соединений
- 13.3. Реакции с образованием углерод-углеродных связей
- 13.4. Синильная защита спиртов
- 14. ИЗБРАННЫЕ СИНТЕЗЫ
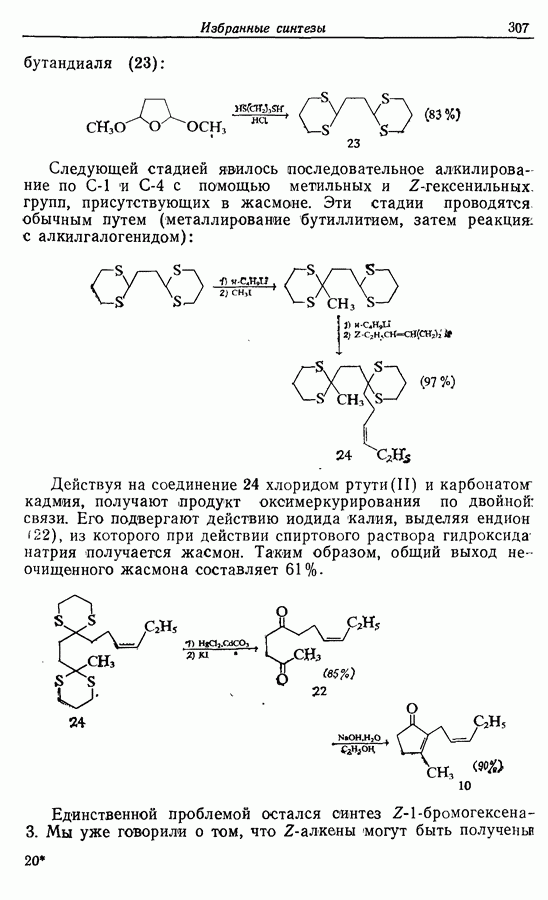
- 14.2. Z-Геникосен-6-он-11
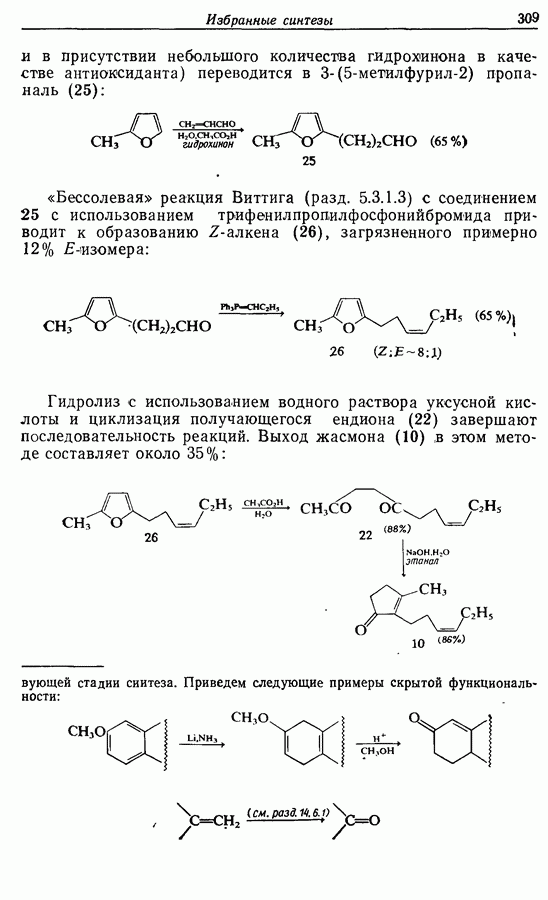
- 14.3. Синтез Z-жасмона
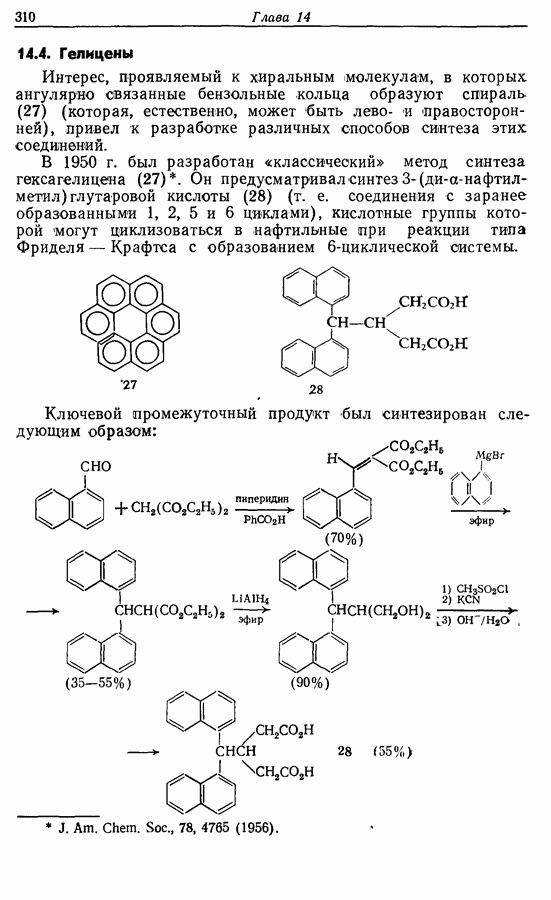
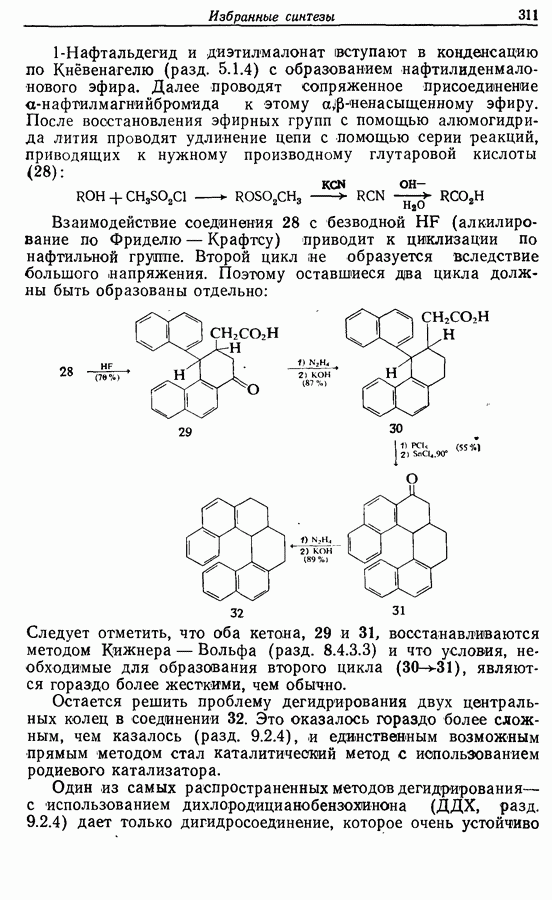
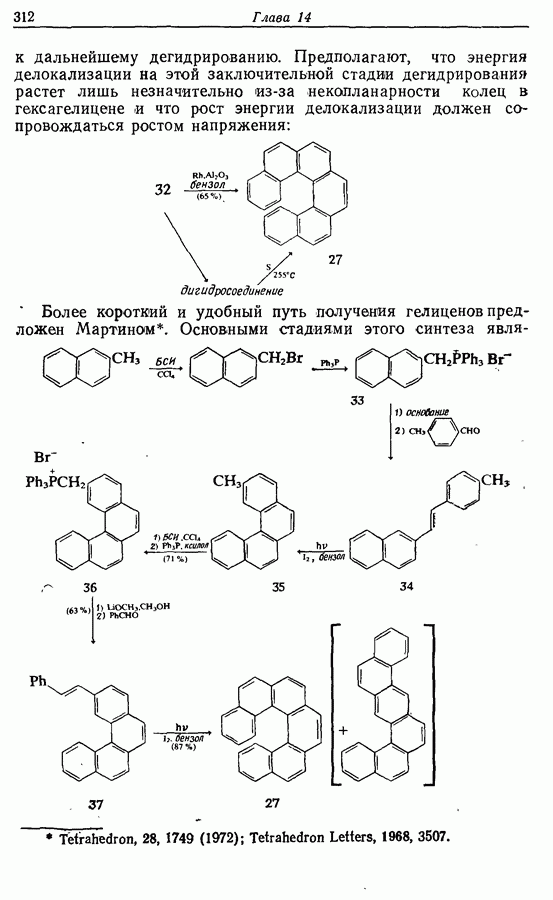
- 14.4. Гелицены
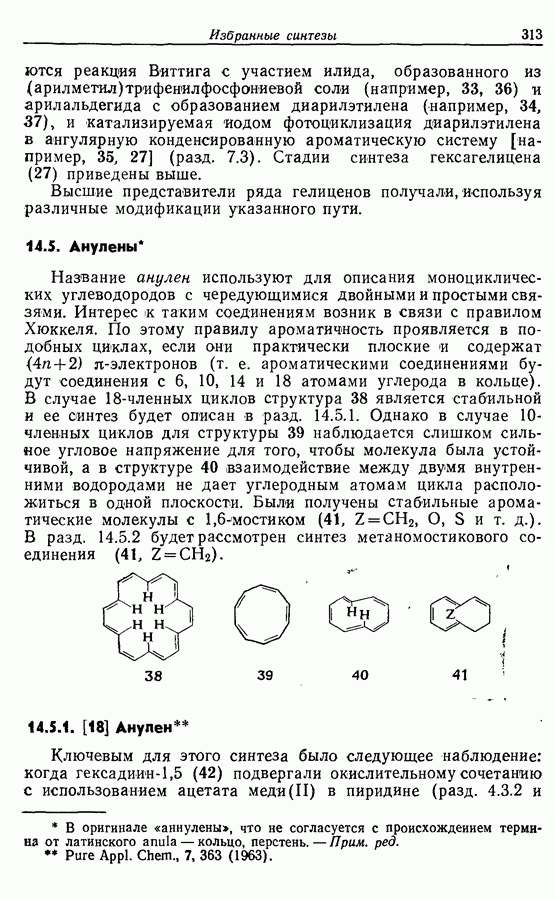
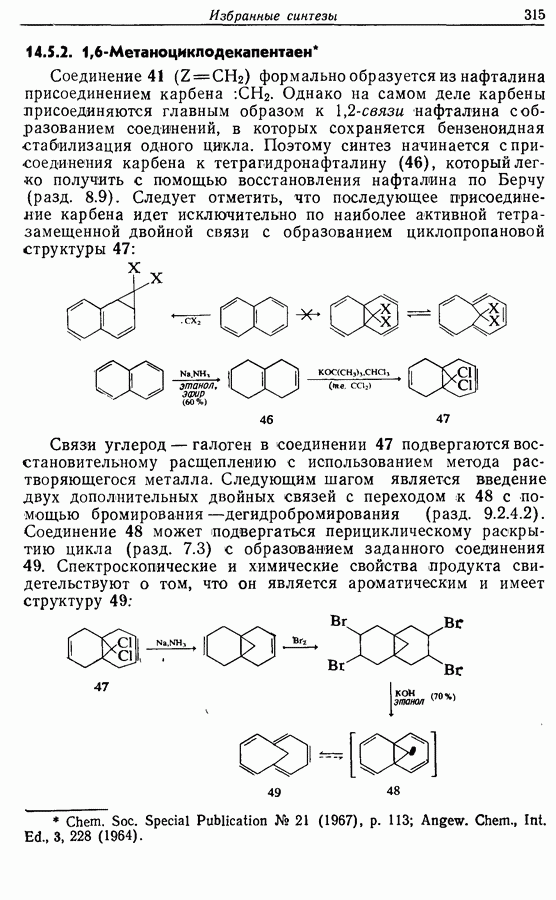
- 14.5. Анулены
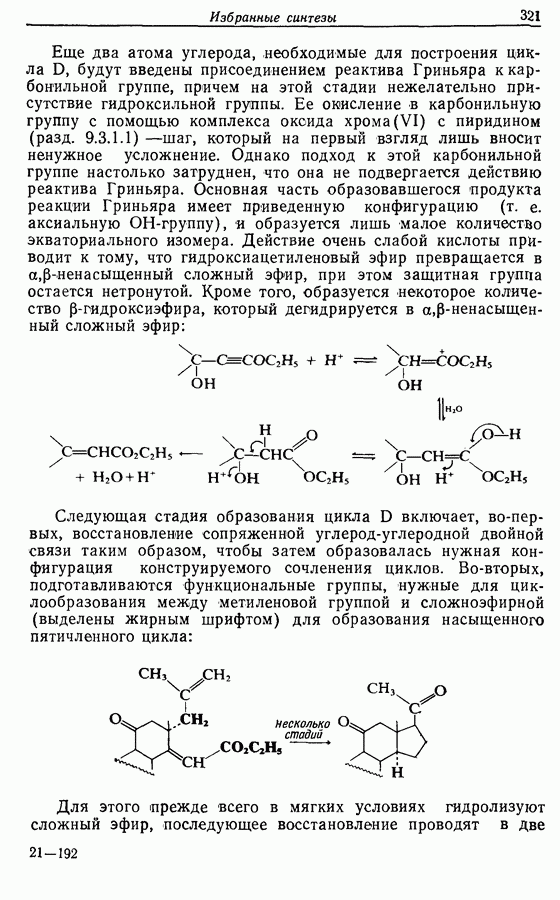
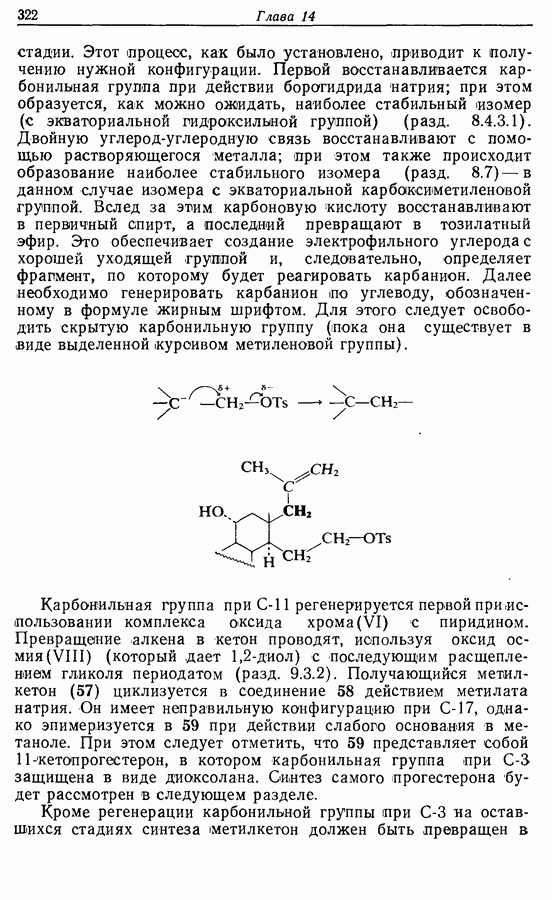
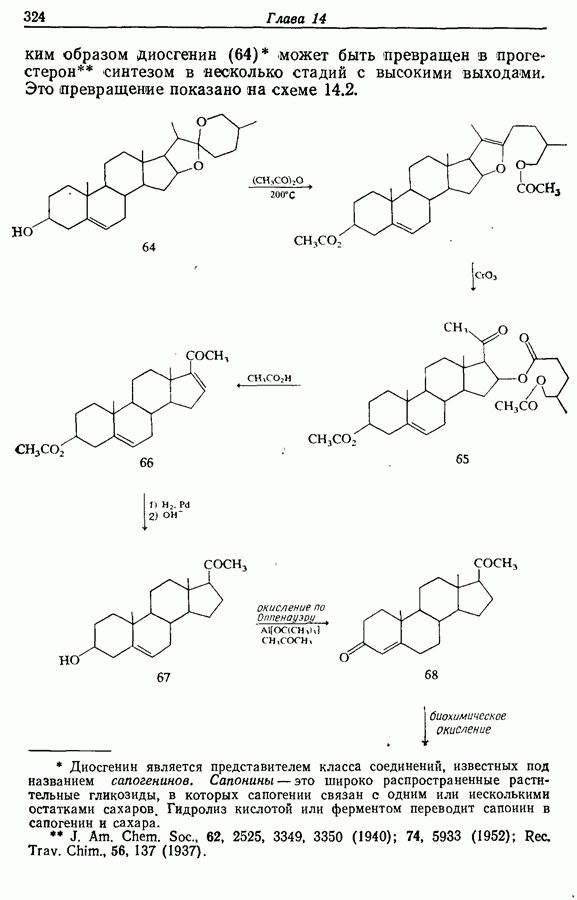
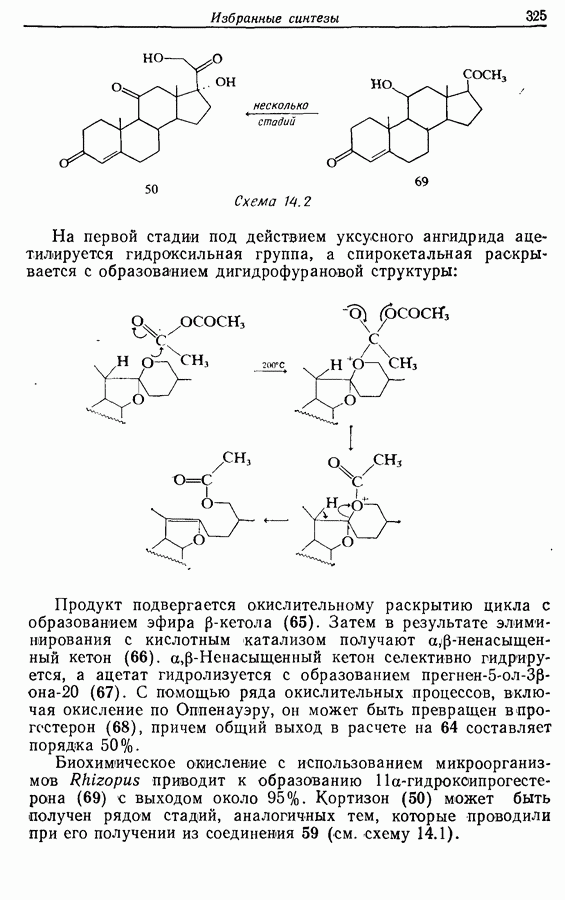
- 14.6. Синтезы стероидов
- 14.6.2. Превращение растительных стероидов в стероидные гормоны
- 14.7. Синтез пептидов
- 14.7.2. Техника синтеза пептидов
- ЛИТЕРАТУРА