| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
4. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: РЕАКЦИИ МЕТАЛЛООРГАНИЧЕСКИХ СОЕДИНЕНИЙ
До сих пор реакции образования углерод-углеродной связи рассматривались лишь в общих чертах. Теперь обсудим некоторые наиболее важные из этих процессов, при этом начнем с тех, которые, по крайней мере на бумаге, являются самыми простыми: это реакции металлоорганических соединений.
4.1. Реактивы Гриньяра и электрофилы
Как уже отмечалось в разд. 3.4.1, реактив Гриньяра  в эфирном растворе (обычно в диэтиловом эфире или тетра-гидрофуране) выступает в качестве источника нестабилизированных карбанионов
в эфирном растворе (обычно в диэтиловом эфире или тетра-гидрофуране) выступает в качестве источника нестабилизированных карбанионов  обычно алкил или арил, но может быть также алкенилом или алкинилом, разд. 4.1.5).
обычно алкил или арил, но может быть также алкенилом или алкинилом, разд. 4.1.5).
4.1.1. Алкилирование
Реактивы Гриньяра при алкилировании образуют алканы:

Например:

Хотя в приведенных выше реакциях получены хорошие выходы, все же это лишь исключения из общего правила: алкилироваиие реактивов Гриньяра часто происходит с очень малыми выходами (особенно в тех случаях, когда уходящая группа  галоген) из-за побочных реакций. Такими реакциями являются отщепление галогеноводорода или
галоген) из-за побочных реакций. Такими реакциями являются отщепление галогеноводорода или
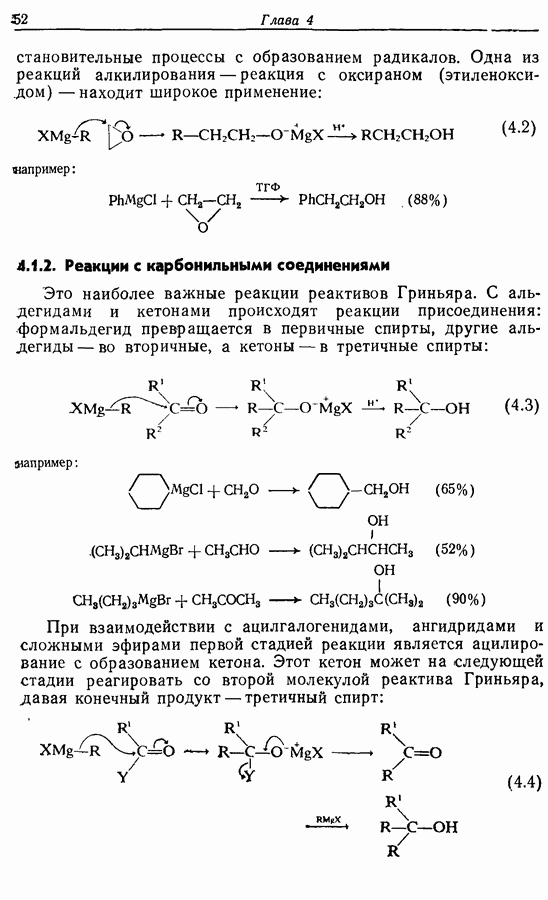
окислительно-восстановительные процессы с образованием радикалов. Одна из реакций алкилирования — реакция с оксираном (этиленоксидом) — находит широкое применение:

например:

4.1.2. Реакции с карбонильными соединениями
Это наиболее важные реакции реактивов Гриньяра. С альдегидами и кетонами происходят реакции присоединения: формальдегид превращается в первичные спирты, другие альдегиды — во вторичные, а кетоны — в третичные спирты:

например:

При взаимодействии с ацилгалогенидами, ангидридами и сложными эфирами первой стадией реакции является ацилирование с образованием кетона. Этот кетон может на следующей стадии реагировать со второй молекулой реактива Гриньяра, давая конечный продукт — третичный спирт:

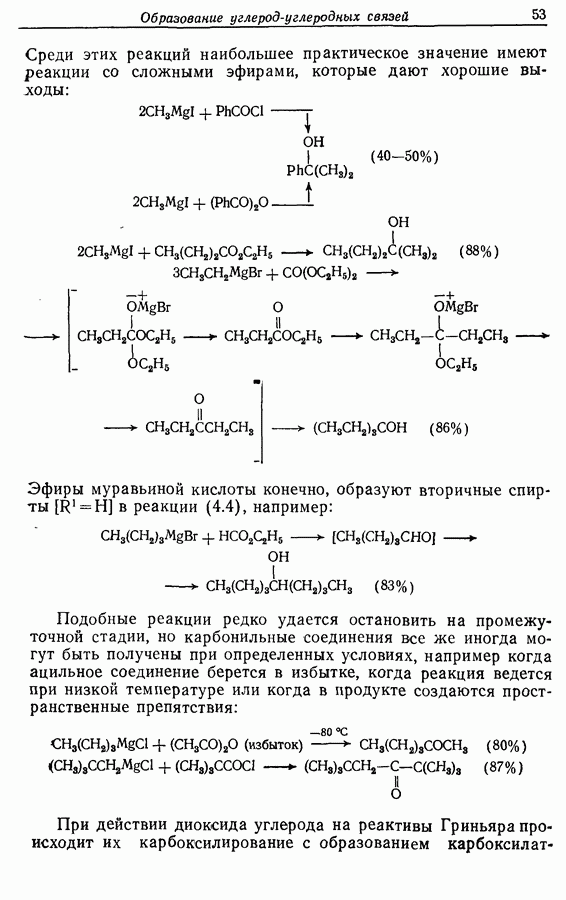
Среди этих реакций наибольшее практическое значение имеют реакции со сложными эфирами, которые дают хорошие выводы:

Эфиры муравьиной кислоты конечно, образуют вторичные спирты  в реакции (4.4), например:
в реакции (4.4), например:

Подобные реакции редко удается остановить на промежуточной стадии, но карбонильные соединения все же иногда могут быть получены при определенных условиях, например когда ацильное соединение берется в избытке, когда реакция ведется при низкой температуре или когда в продукте создаются пространственные препятствия:

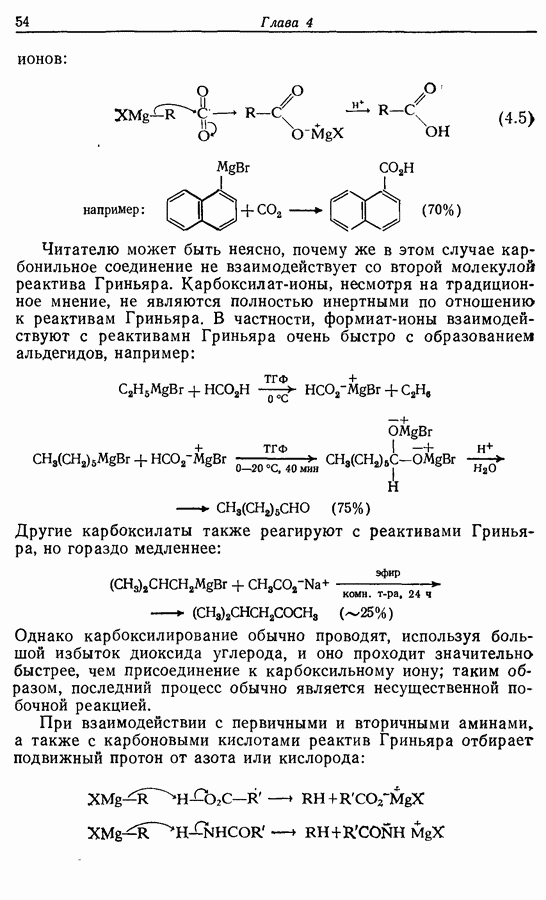
При действии диоксида углерода на реактивы Гриньяра происходит их карбоксилирование с образованием
карбоксилат-ионов:

Читателю может быть неясно, почему же в этом случае карбонильное соединение не взаимодействует со второй молекулой реактива Гриньяра. Карбоксилат-ионы, несмотря на традиционное мнение, не являются полностью инертными по отношению к реактивам Гриньяра. В частности, формиат-ионы взаимодействуют с реактивами Гриньяра очень быстро с образованием альдегидов, например:

Другие карбоксилаты также реагируют с реактивами Гриньяра, но гораздо медленнее:

Однако карбоксилирование обычно проводят, используя большой избыток диоксида углерода, и оно проходит значительно быстрее, чем присоединение к карбоксильному иону; таким образом, последний процесс обычно является несущественной побочной реакцией.
При взаимодействии с первичными и вторичными аминами а также с карбоновыми кислотами реактив Гриньяра отбирает подвижный протон от азота или кислорода:

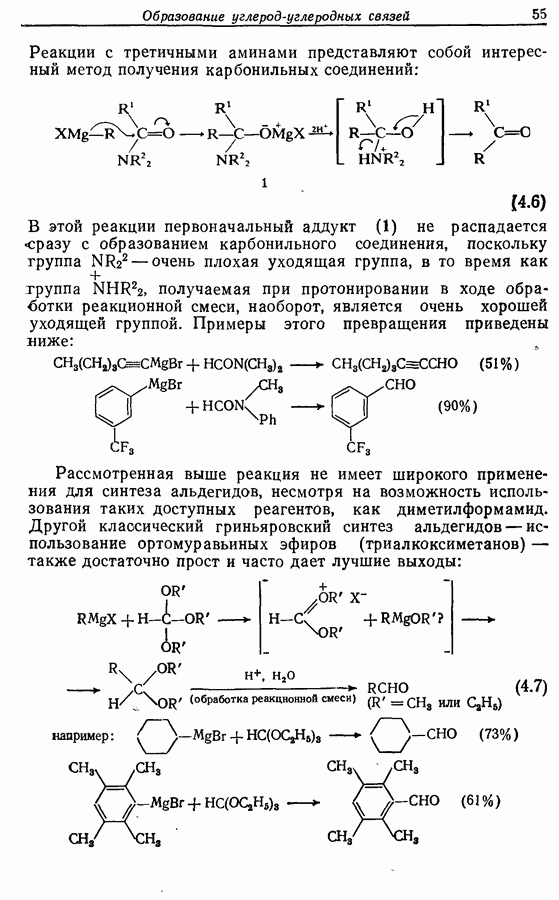
Реакции с третичными аминами представляют собой интересный метод получения карбонильных соединений:

В этой реакции первоначальный аддукт (1) не распадается сразу с образованием карбонильного соединения, поскольку группа  очень плохая уходящая группа, в то время как группа
очень плохая уходящая группа, в то время как группа  получаемая при протонировании в ходе обработки реакционной смеси, наоборот, является очень хорошей уходящей группой. Примеры этого превращения приведены ииже:
получаемая при протонировании в ходе обработки реакционной смеси, наоборот, является очень хорошей уходящей группой. Примеры этого превращения приведены ииже:

Рассмотренная выше реакция не имеет широкого применения для синтеза альдегидов, несмотря на возможность использования таких доступных реагентов, как диметилформамид. Другой классический гриньяровский синтез альдегидов — использование ортомуравьиных эфиров (триалкоксиметанов) — также достаточно прост и часто дает лучшие выходы:

Современный метод, в котором используют формиат-ионы (см. выше), также дает хорошую возможность синтеза альдегидов.
4.1.3. Реакции с соединениями, содержащими группы ...
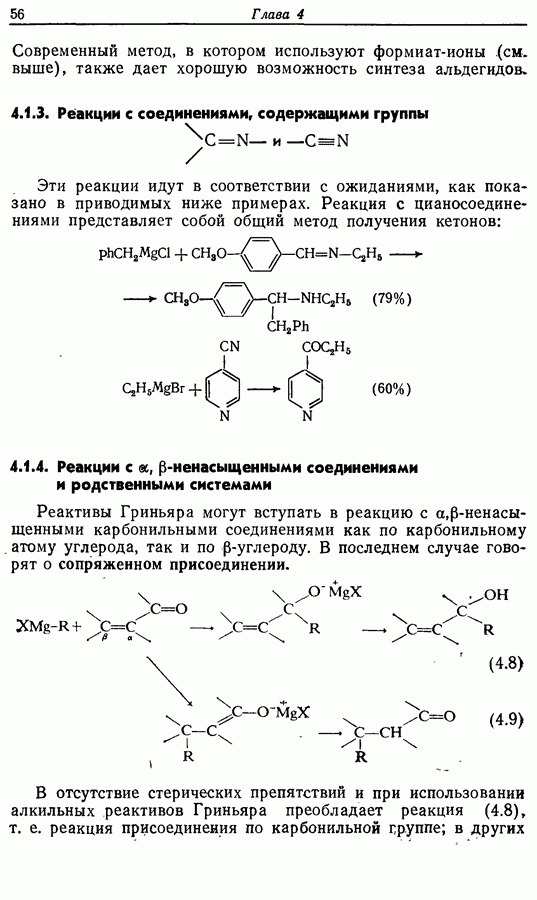
Эти реакции идут в соответствии с ожиданиями, как показано в приводимых ниже примерах. Реакция с цианосоединениями представляет собой общий метод получения кетонов:

4.1.4. Реакции с ...-ненасыщенными соединениями и родственными системами
Реактивы Гриньяра могут вступать в реакцию с  -ненасы-щенными карбонильными соединениями как по карбонильному
-ненасы-щенными карбонильными соединениями как по карбонильному  атому углерода, так и по
атому углерода, так и по  -углероду. В последнем случае говорят о сопряженном присоединении.
-углероду. В последнем случае говорят о сопряженном присоединении.

В отсутствие стерических препятствий и при использовании алкильных реактивов Гриньяра преобладает реакция (4.8), т. е. реакция присоединения по карбонильной группе; в других
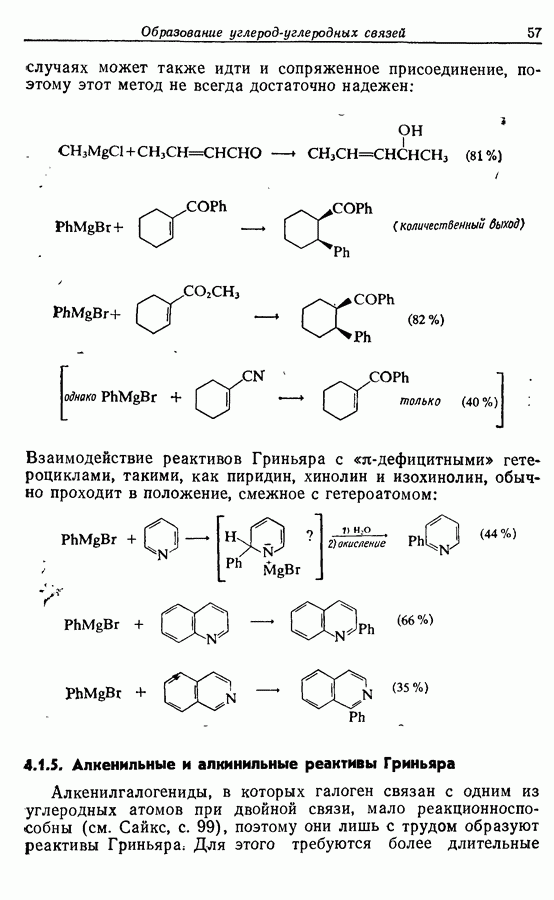
случаях может также идти и сопряженное присоединение, поэтому этот метод не всегда достаточно надежен:

Взаимодействие реактивов Гриньяра с  -дефицитными» гетероциклами, такими, как пиридин, хинолин и изохинолин, обычно проходит в положение, смежное с гетероатомом:
-дефицитными» гетероциклами, такими, как пиридин, хинолин и изохинолин, обычно проходит в положение, смежное с гетероатомом:

4.1.5. Алкенильные и алкинильные реактивы Гриньяра
Алкенилгалогениды, в которых галоген связан с одним из углеродных атомов при двойной связи, мало реакционноспособны (см. Сайке, с. 99), поэтому они лишь с трудом образуют реактивы Гриньяра; Для этого требуются более длительные
промежутки времени и более высокие температуры, чем в случае алкил- и арилгалогенидов. Например, обычно вместо диэтилового эфира используют тетрагидрофуран  кип. 65 °С) и для полного завершения реакции с магнием требуется несколько часов.
кип. 65 °С) и для полного завершения реакции с магнием требуется несколько часов.
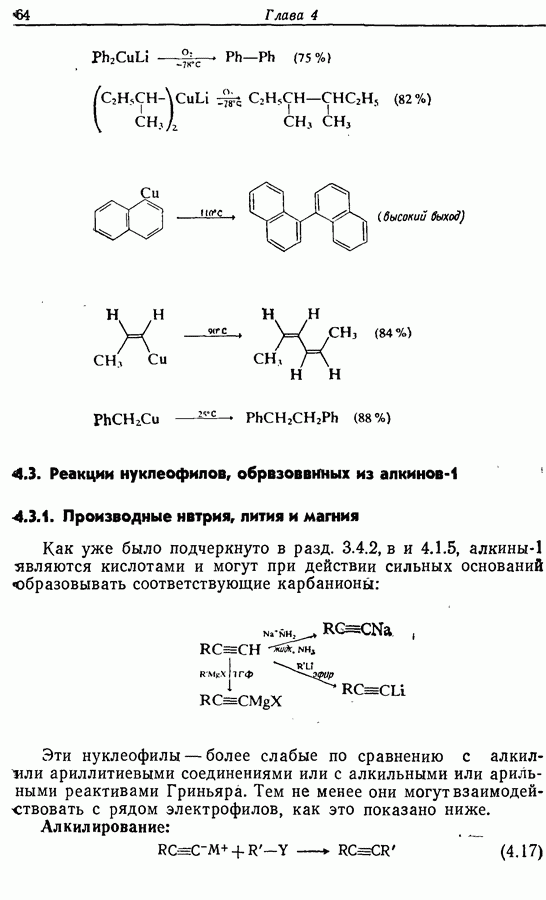
Алкинильные реактивы Гриньяра  , напротив,, относительно легко получить, однако образуются они не из алкинилгалогенидов. Как уже отмечалось в разд. 3.4.2, в, алкины-1 — слабые кислоты, которые могут депротонироваться сильными основаниями, такими, как реактивы Гриньяра:
, напротив,, относительно легко получить, однако образуются они не из алкинилгалогенидов. Как уже отмечалось в разд. 3.4.2, в, алкины-1 — слабые кислоты, которые могут депротонироваться сильными основаниями, такими, как реактивы Гриньяра:

Если  низшая алкильная группа (например,
низшая алкильная группа (например,  или
или  то
то  газ (метан или этан), который удаляется из раствора алкинильного реактива Гриньяра.
газ (метан или этан), который удаляется из раствора алкинильного реактива Гриньяра.
Использование алкинильных реактивов Гриньяра рассмотрено в разд. 4.3.1.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ВВЕДЕНИЕ И ВЗАИМОПРЕВРАЩЕНИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП
- 2.1. Введение функциональных групп в апканы
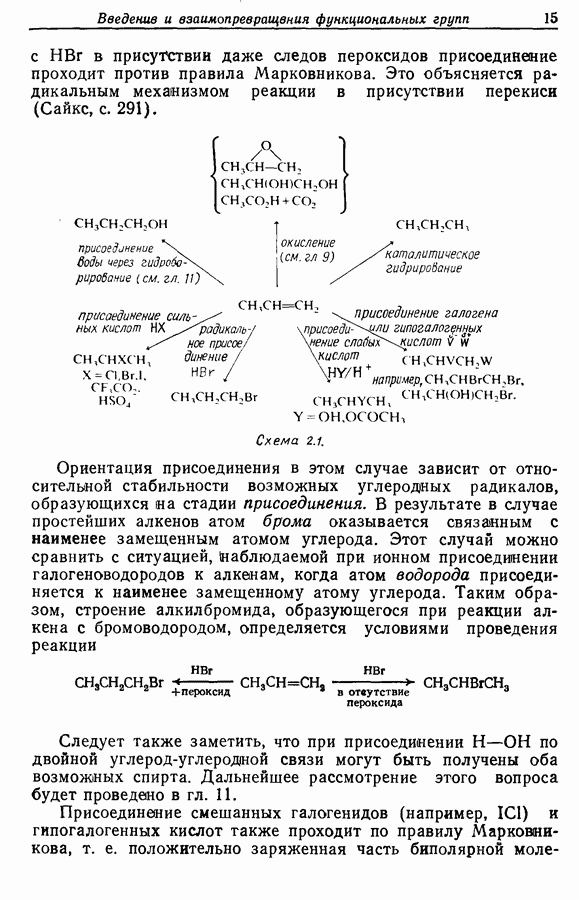
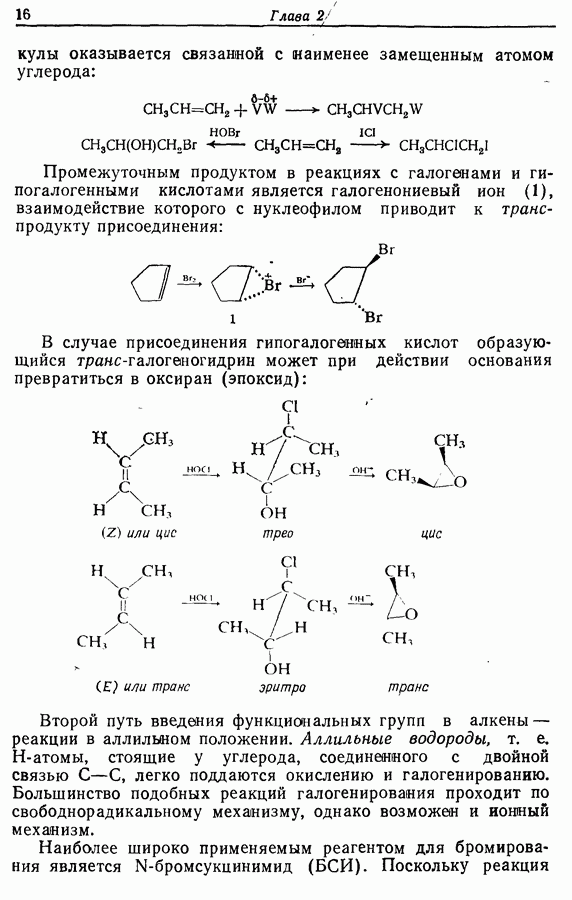
- 2.2. Введение функциональных групп в алкены
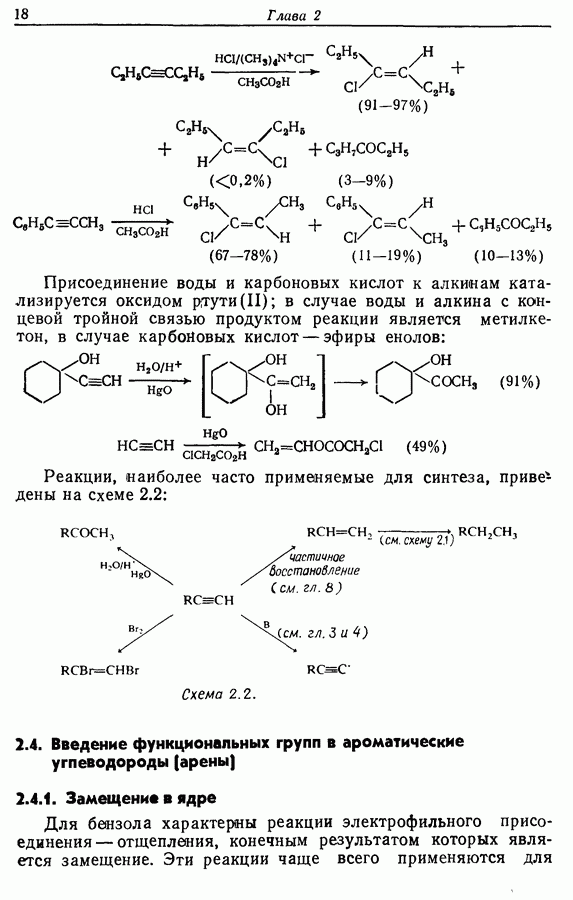
- 2.3. Введение функциональных групп в апкины
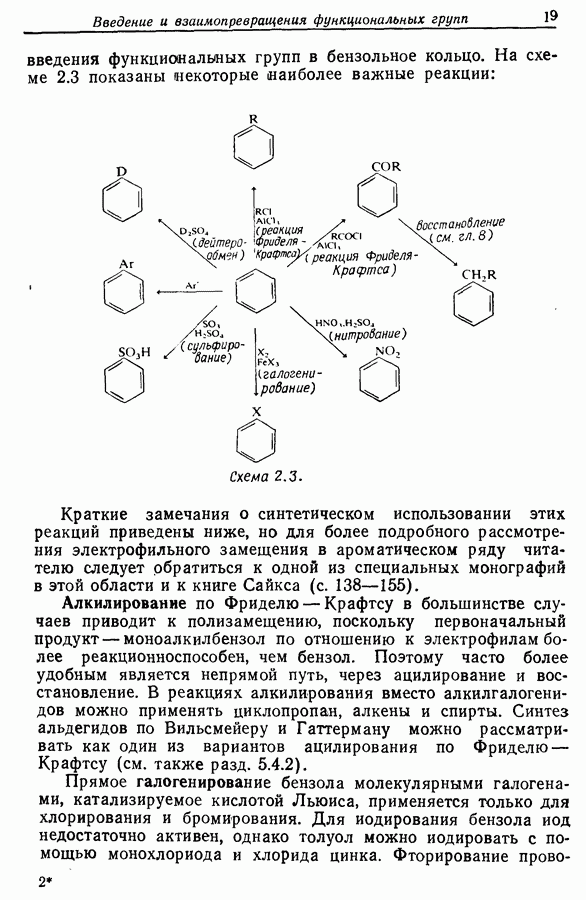
- 2.4. Введение функциональных групп в ароматические углеводороды (арены)
- 2.5. Введение функциональных групп в производные бензола
- 2.6. Введение функциональных групп в простые гетероциклические соединения
- 2.7. Взаимопревращения функциональных групп
- 2.7.2. Превращения аминогруппы
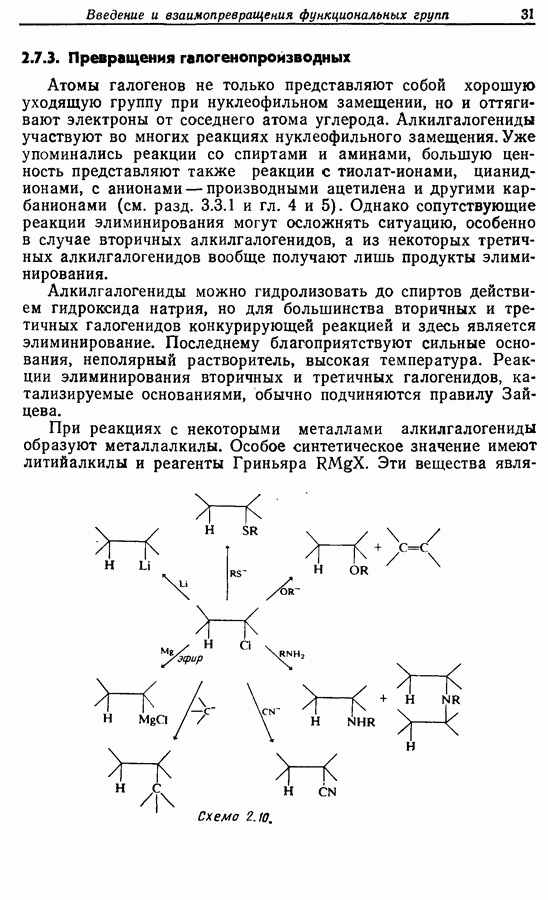
- 2.7.3. Превращения галогенопроизводных
- 2.7.4. Превращения нитросоединений
- 2.7.5. Превращения альдегидов и кетонов
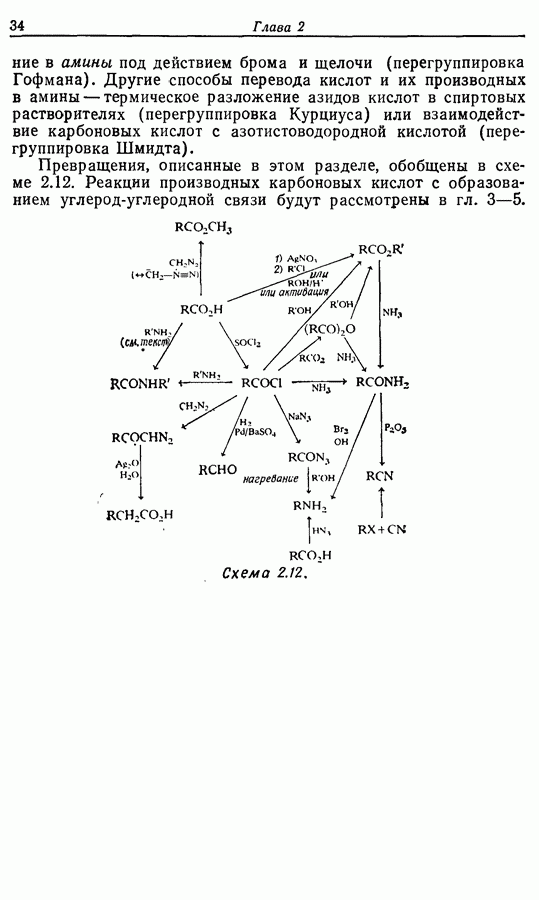
- 2.7.6. Превращения кислот и их производных
- 3. ПРИНЦИПЫ ОБРАЗОВАНИЯ УГЛЕРОД-УГЛЕРОДНОЙ СВЯЗИ
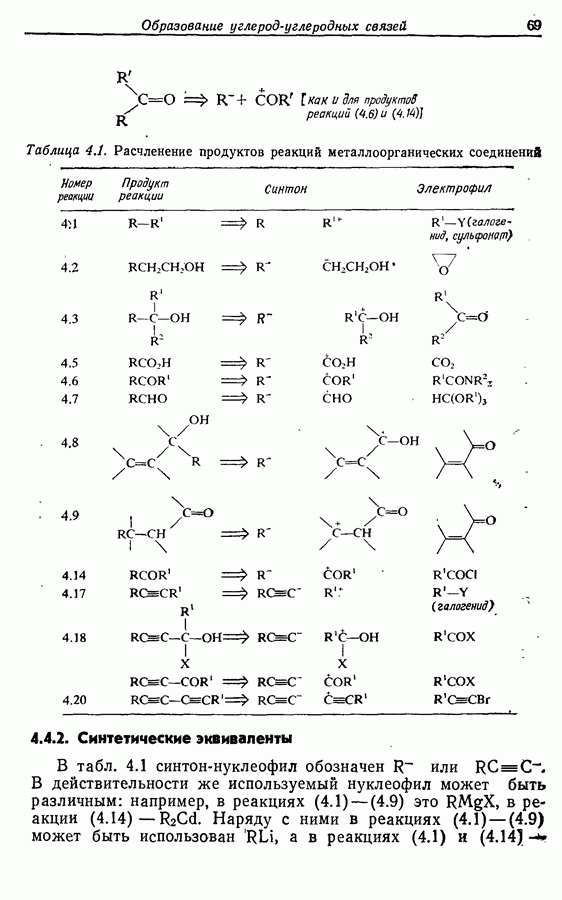
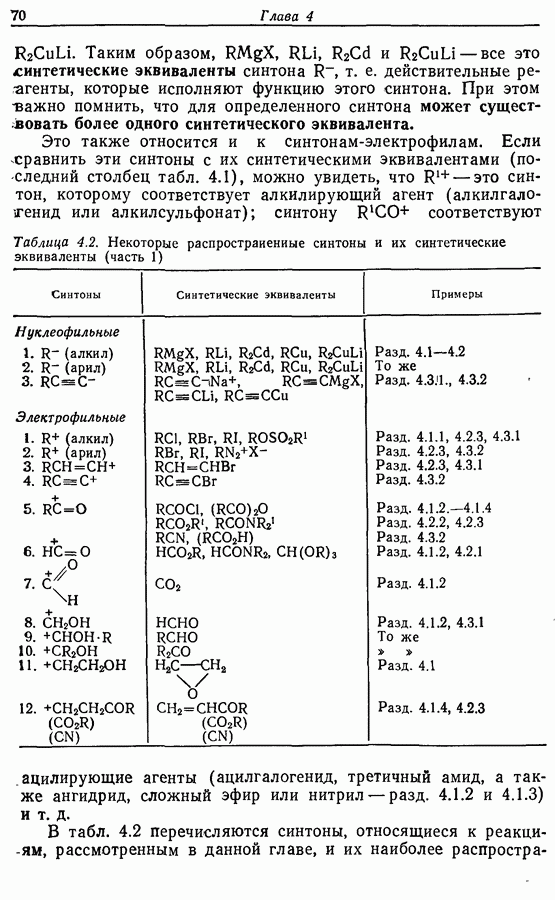
- 3.2. Расчленение и синтоны
- 3.3. Электрофильные углеродные частицы
- 3.4. Нуклеофильиые углеродные частицы
- 3.4.2. Стабилизированные карбанионы
- 3.4.3. Алкены, арены и гетероарены
- 4. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: РЕАКЦИИ МЕТАЛЛООРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 4.1. Реактивы Гриньяра и электрофилы
- 4.2. Другие металлоорганические реактивы и электрофилы
- 4.2.2. Цинк- и кадмийорганические соединения
- 4.2.3. Органические соединения меди (I)
- 4.3. Реакции нуклеофилов, образованных из алкинов-1
- 4.3.2. Алкинильные соединения меди (I)
- 4.4. Выводы
- 4.5. Примеры
- 5. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: ИСПОЛЬЗОВАНИЕ СТАБИЛИЗИРОВАННЫХ КАРБАНИОНОВ И РОДСТВЕННЫХ НУКЛЕОФИЛОВ
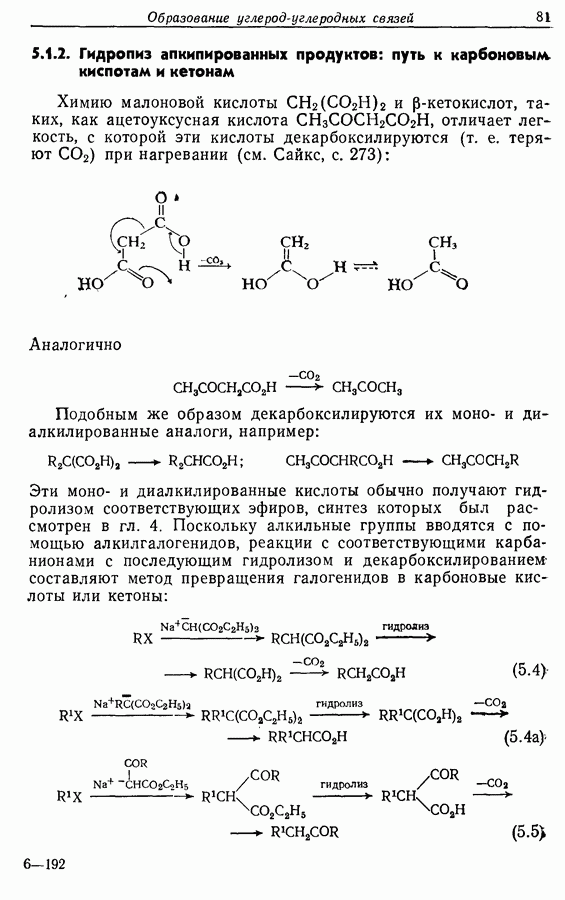
- 5.1.1. Алкилирование
- 5.1.2. Гидролиз алкинированных продуктов: путь к карбоновым кислотам и кетонам
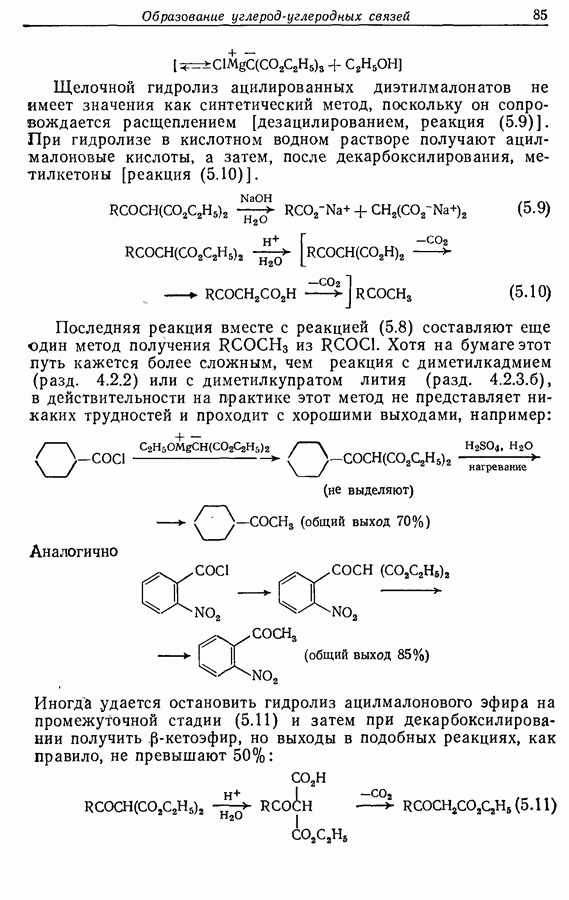
- 5.1.3. Ацилирование
- 5.1.4. Реакции конденсации
- 5.1.5. Реакции с соединениями типа … и родственными системами: реакция Михаэля
- 5.2. Карбанионы, стабилизированные одной (-М)-группой
- 5.2.3. Косвенные пути получения a-алкилированных альдегидов и кетонов
- 5.2.4. Реакции конденсации
- 5.2.5. Реакция Михаэля
- 5.3. Карбанионы, стабилизированные соседними атомами фосфора или серы
- 5.3.2. Карбанионы, стабилизированные двумя атомами серы
- 5.4. Алкены, арены и гетероарены как нуклеофилы
- 5.4.3. Реакции присоединения и конденсации с карбонильными и родственными им соединениями
- 5.5. Заключение
- 5.6. Задачи
- 6. ОБРАЗОВАНИЕ СВЯЗЕЙ УГЛЕРОДА С ГЕТЕРОАТОМОМ: ОСНОВНЫЕ ПРИНЦИПЫ
- 6.1. Связи углерод — галоген
- 6.2. Связи углерод — кислород и углерод — сера
- 6.3. Связи углерод — азот
- 6.3.2. Электрофильный азот и нуклеофильный углерод
- 6.3.3. Нитрозосоединения, включая нитриты
- 7. ОБРАЗОВАНИЕ И РАСКРЫТИЕ ЦИКЛОВ
- 7.1. Внутримолекулярная циклизация в результате электрофильно-нуклеофильного взаимодействия
- 7.1.2. Условия внутримолекулярного циклообразования. Правила Болдуина
- 7.1.3. Присоединение по Михаэлю в процессах циклизации
- 7.1.4. Образование ароматических и гетероароматических циклов
- 7.2. Циклоприсоединение
- 7.2.2. 1,3-Диполярное циклоприсоединение
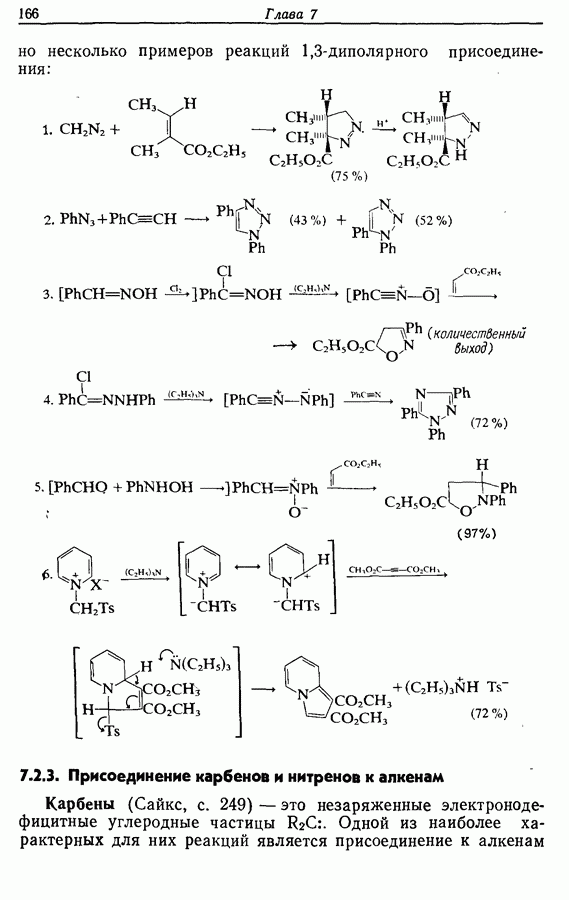
- 7.2.3. Присоединение карбенов и нитренов к алкенам
- 7.3. Электроциклическое циклообразование
- 7.4. Раскрытие цикла
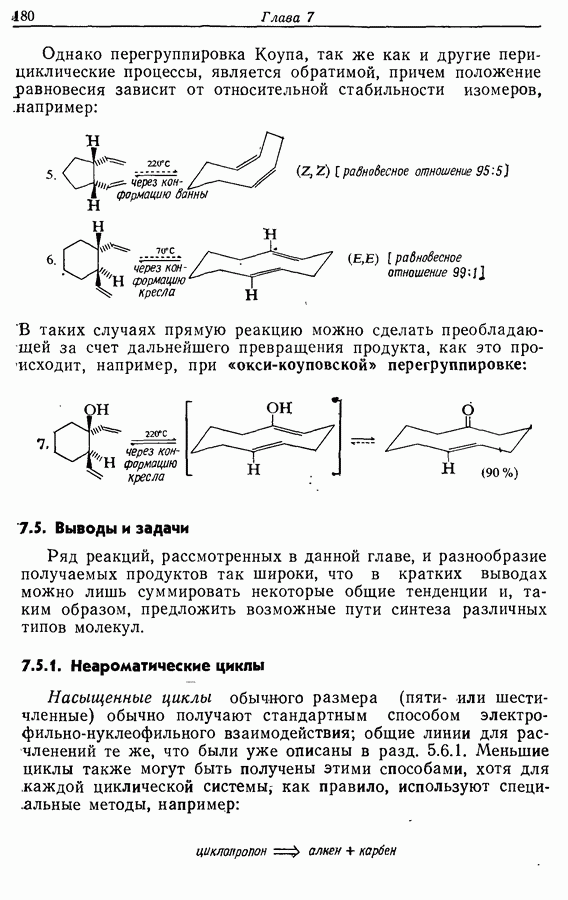
- 7.5. Выводы и задачи
- 8. ВОССТАНОВЛЕНИЕ
- 8.1. Каталитическое гидрирование
- 8.2. Восстановление гидридами металлов
- 8.3. Восстановление растворяющимися металлами
- 8.4. Восстановление определенных функциональных групп
- 8.4.2. Восстановление алкинов
- 8.4.3. Восстановление альдегидов и кетонов
- 8.4.4. Восстановление карбоновых кислот и их производных
- 8.4.5. Восстановление нитрилов
- 8.4.6. Восстановление иминов и оксимов, включая восстановительное алкилирование
- 8.5. Восстановительное расщепление связи углерод — гетероатом
- 8.6. Восстановительное раскрытие цикла в эпоксидах
- 8.7. Восстановление a,b-ненасыщенных карбонильных соединений
- 8.8. Восстановление сопряженных диенов
- 8.9. Восстановление ароматических и гетероароматических соединений
- 9. ОКИСЛЕНИЕ
- 9.2. Окисление углеводородов
- 9.2.2. Аллильное окисление
- 9.2.3. Бензильное окисление
- 9.2.4. Дегидрирование алканов, алкильных групп и алкенов
- 9.2.5. Окислительное присоединение к алкенам
- 9.2.6. Окислительная деструкция алкенов
- 9.2.7. Окисление алкинов
- 9.3. Окисление спиртов и их производных
- 9.3.2. Окислительная деструкция 1,2-диолов
- 9.4. Окисление фенолов
- 9.5. Окисление альдегидов и кетонов
- 9.5.2. Окисление в 1,2-дикарбонильные соединения
- 9.5.3. Окисление до сложных эфиров: реакции Байера — Виллигера и Дакина
- 9.6. Окисление функциональных групп, содержащих азот
- 9.6.2. Дегидрирование соединений, содержащих азотные функциональные группы
- 9.7. Окисление серусодержащих функциональных групп
- 10. ЗАЩИТНЫЕ ГРУППЫ
- 10.2. Защита спиртов
- 10.3. Защита диолов
- 10.4. Защита карбоновых кислот
- 10.5. Защита аминогрупп
- 10.6. Защита карбонильных групп
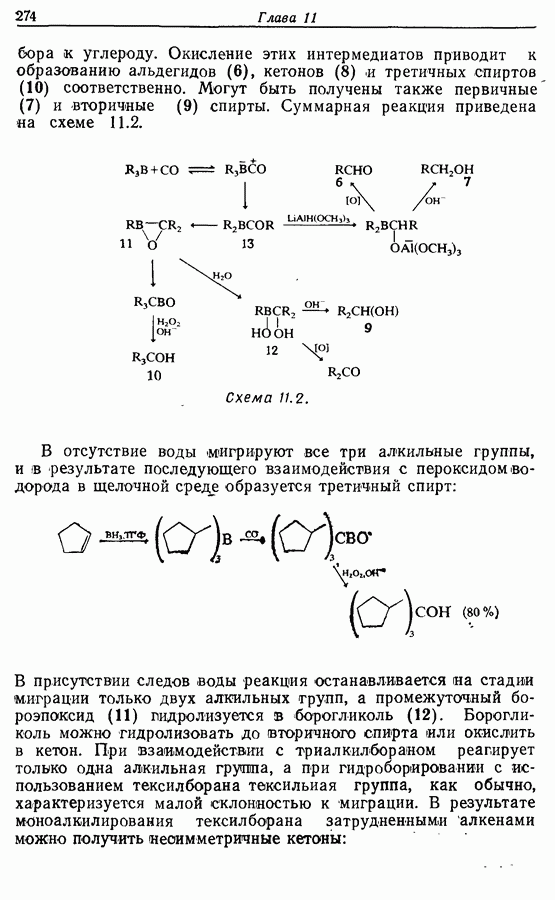
- 11. БОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 11.1. Гидроборирование алкенов при действии борана
- 11.2. Гидроборирование алкенов действием алкилборанов
- 11.3. Реакции борорганических соединений
- 11.4. Гидроборирование диенов
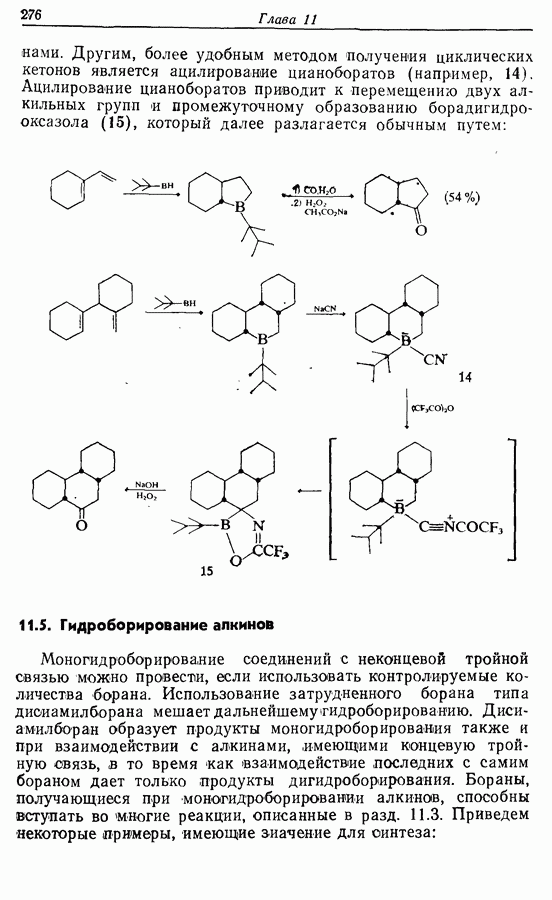
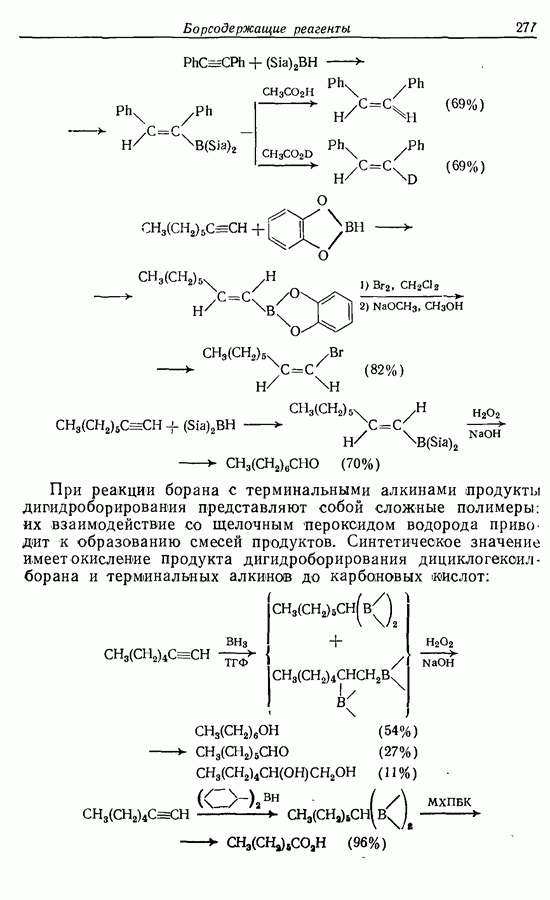
- 11.5. Гидроборирование алкинов
- 12. ФОСФОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
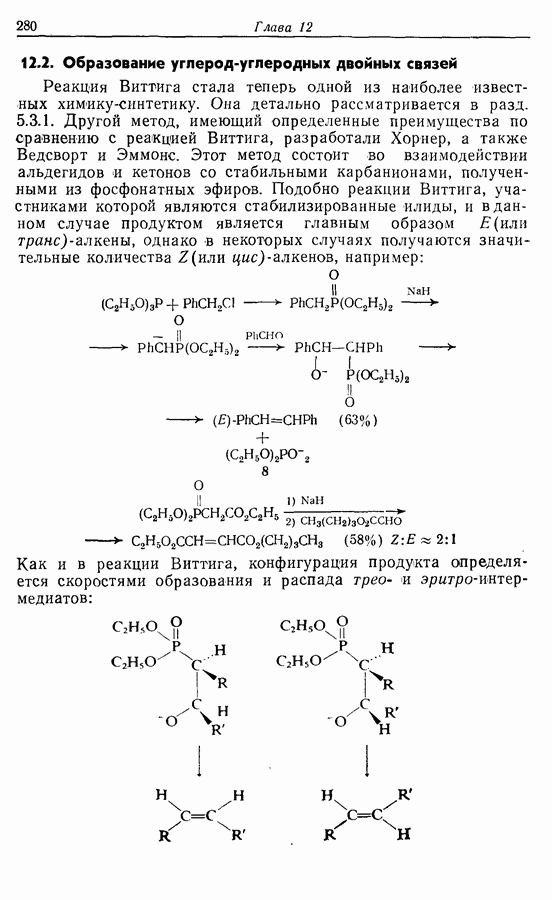
- 12.1. Введение в химию фосфорорганических соединений
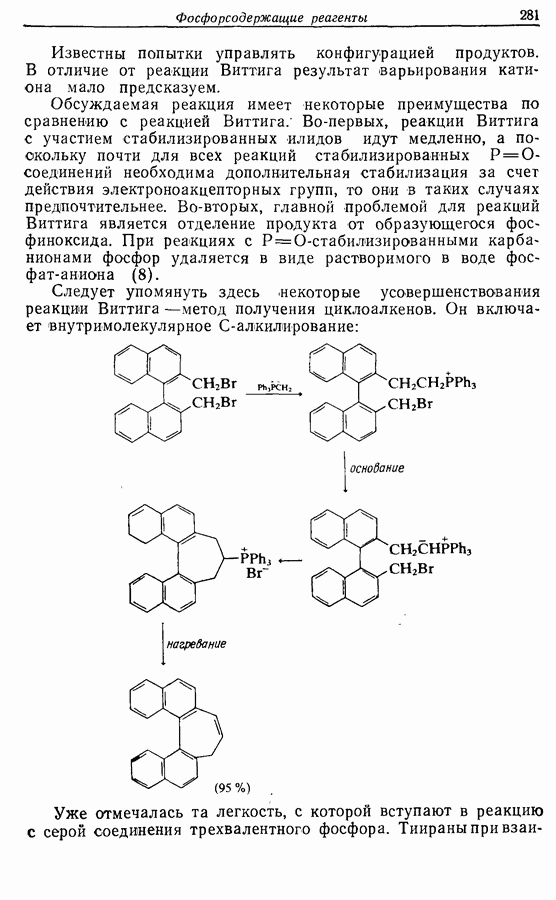
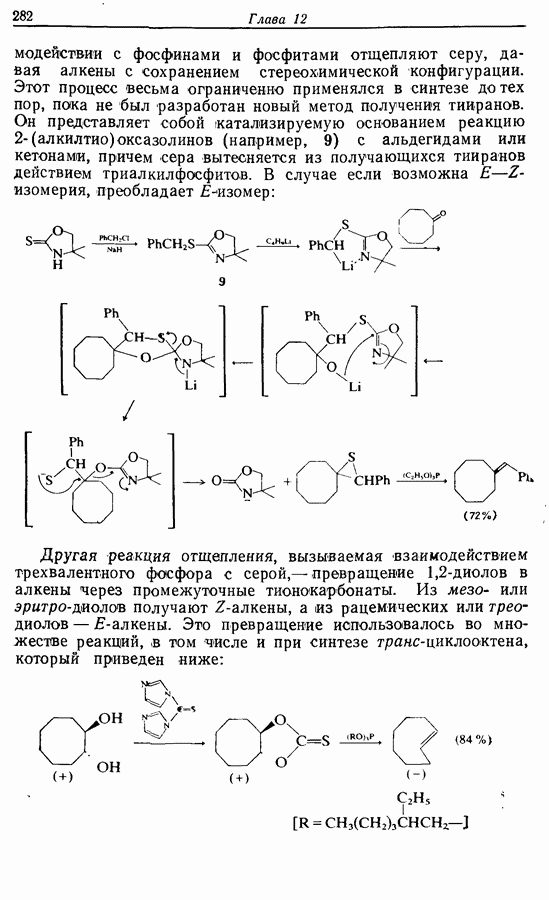
- 12.2. Образование углерод-углеродных двойных связей
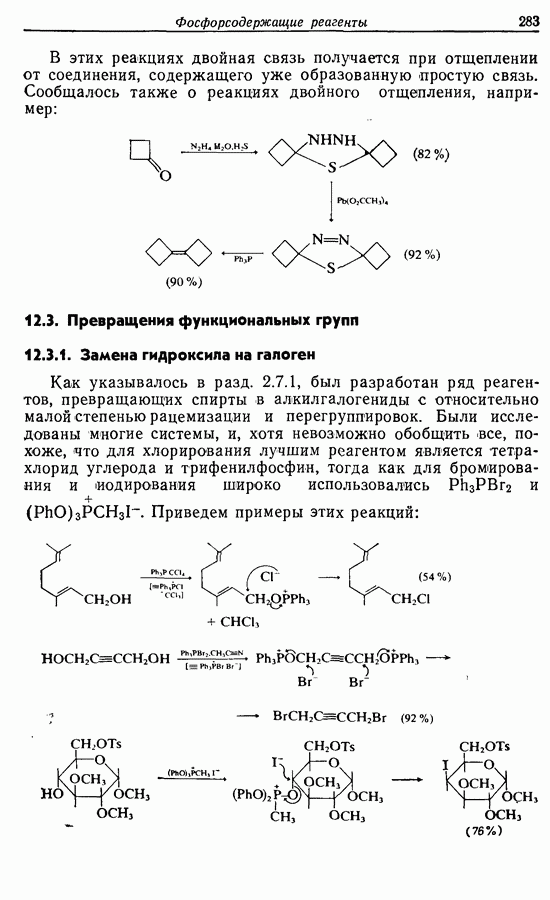
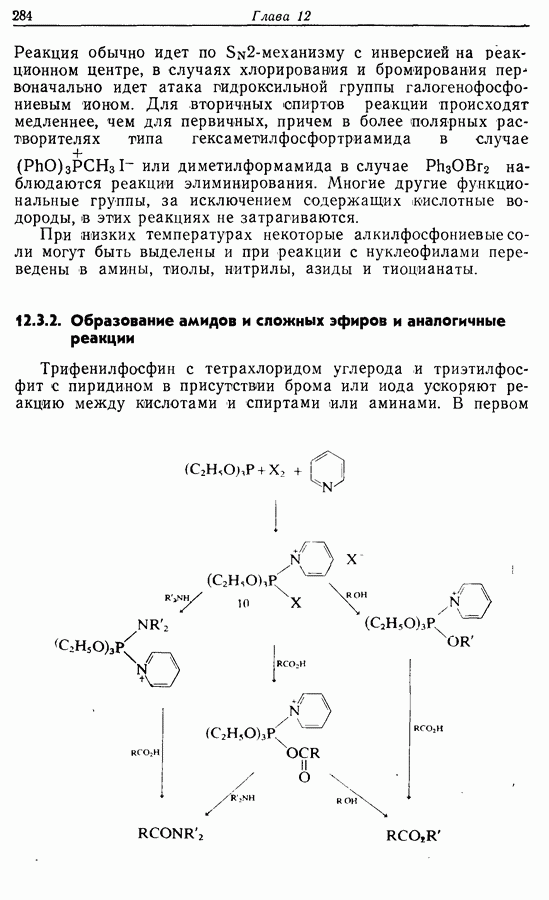
- 12.3. Превращения функциональных групп
- 12.4. Реакции дезоксигенирования
- 13. КРЕМНИЙСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 13.1. Введение в химию кремнийорганических соединений
- 13.2. Синтез кремнийорганических соединений
- 13.3. Реакции с образованием углерод-углеродных связей
- 13.4. Синильная защита спиртов
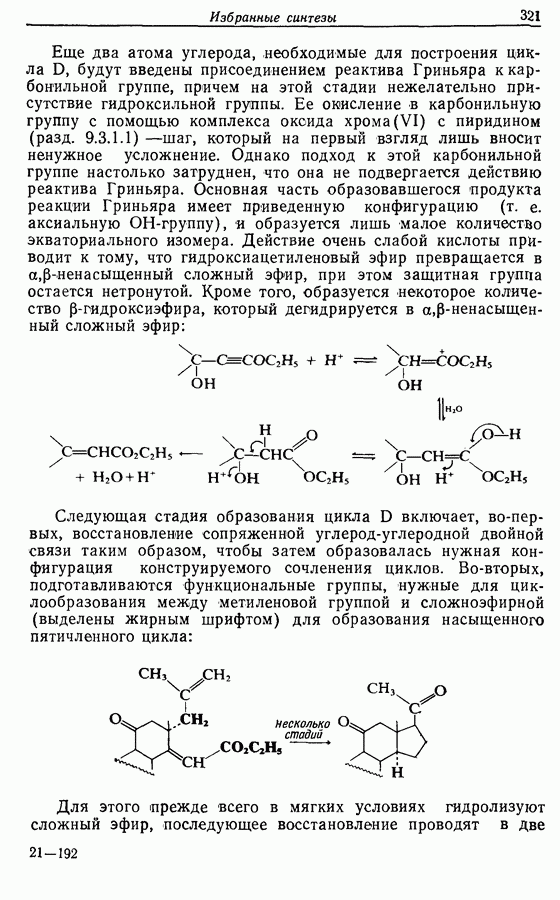
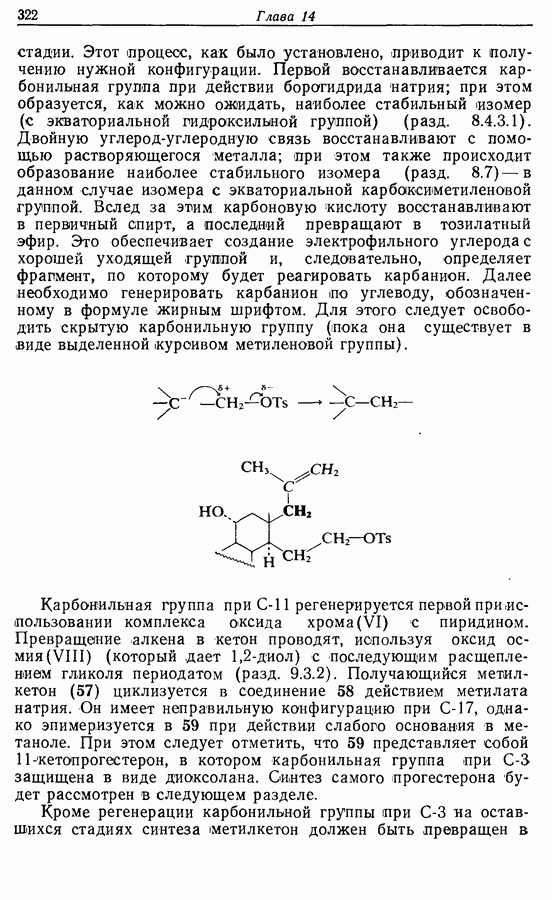
- 14. ИЗБРАННЫЕ СИНТЕЗЫ
- 14.2. Z-Геникосен-6-он-11
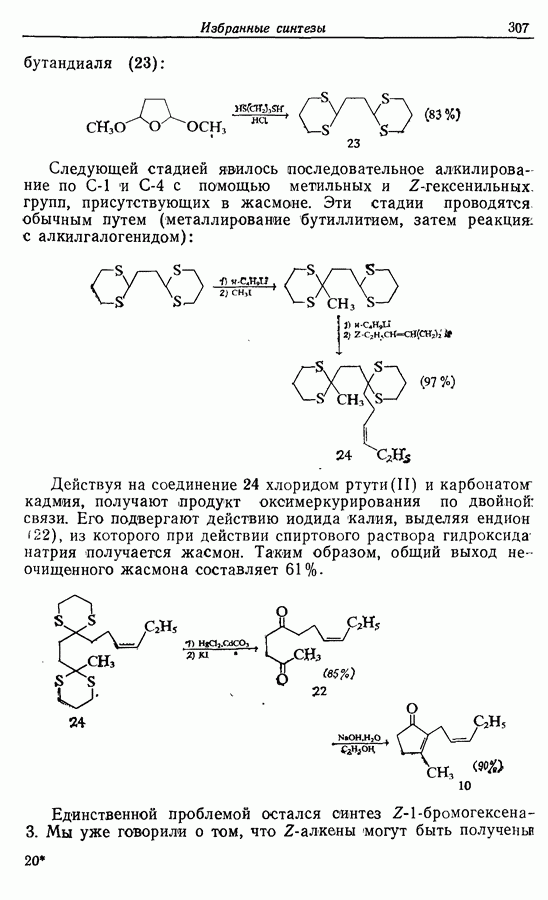
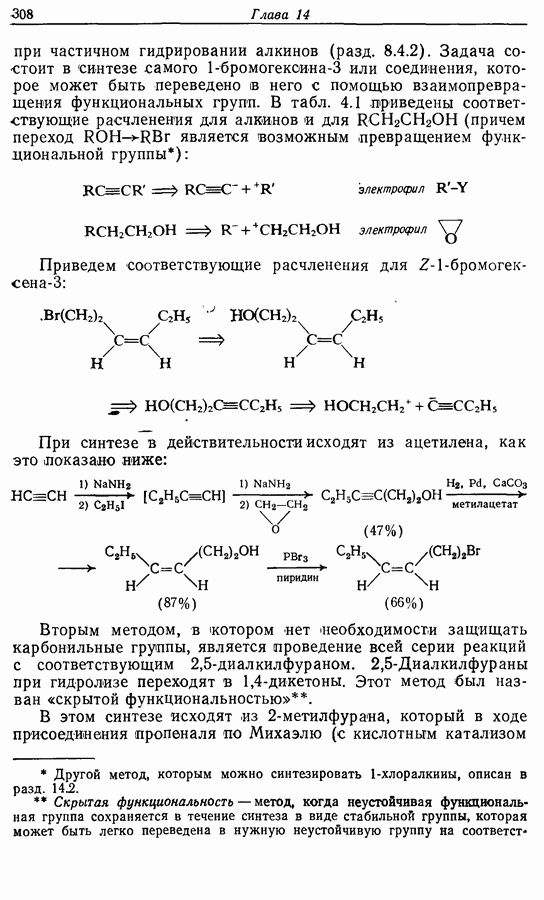
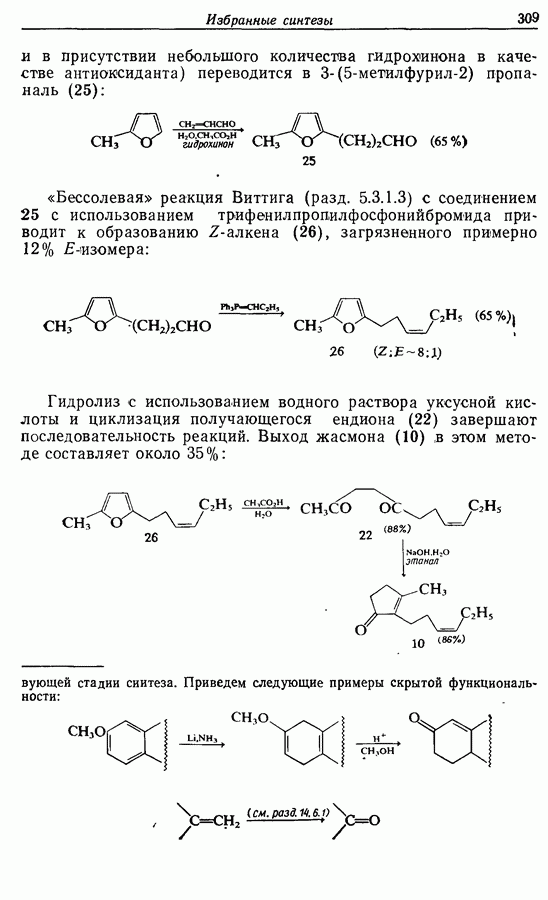
- 14.3. Синтез Z-жасмона
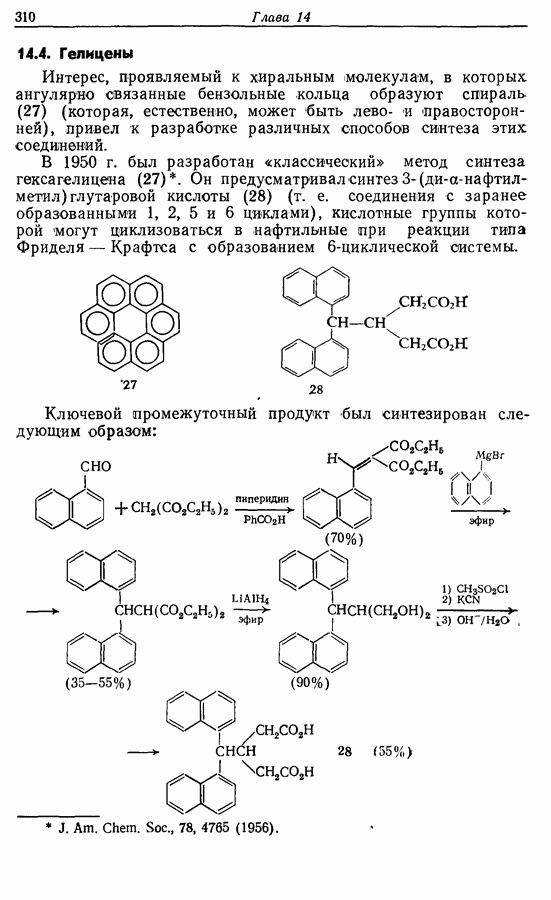
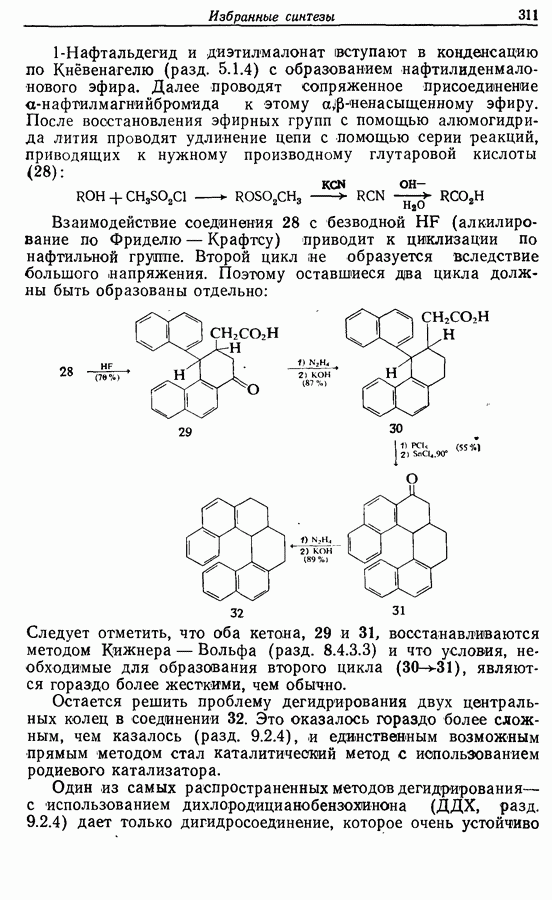
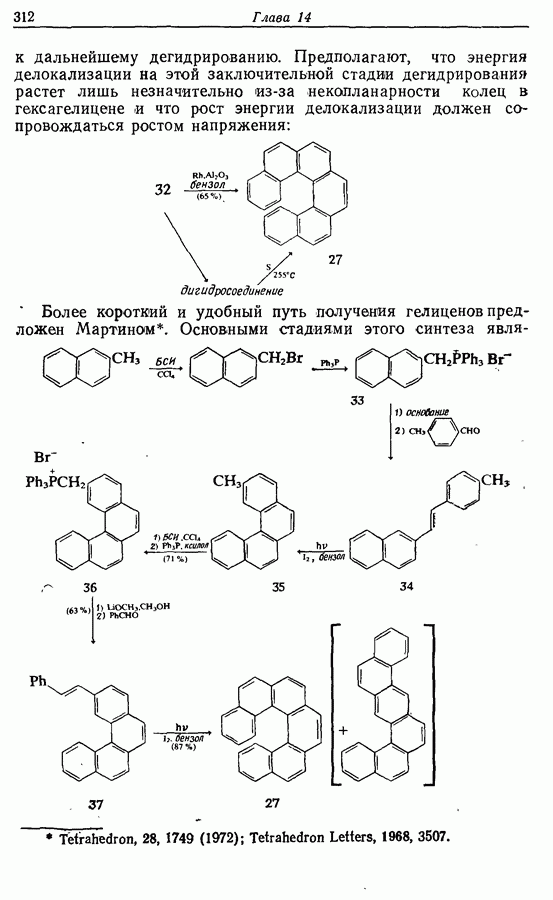
- 14.4. Гелицены
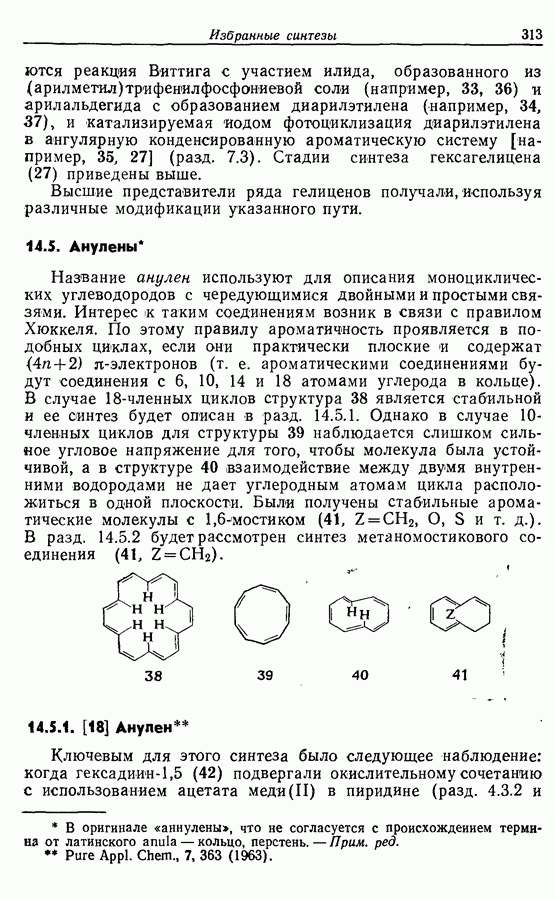
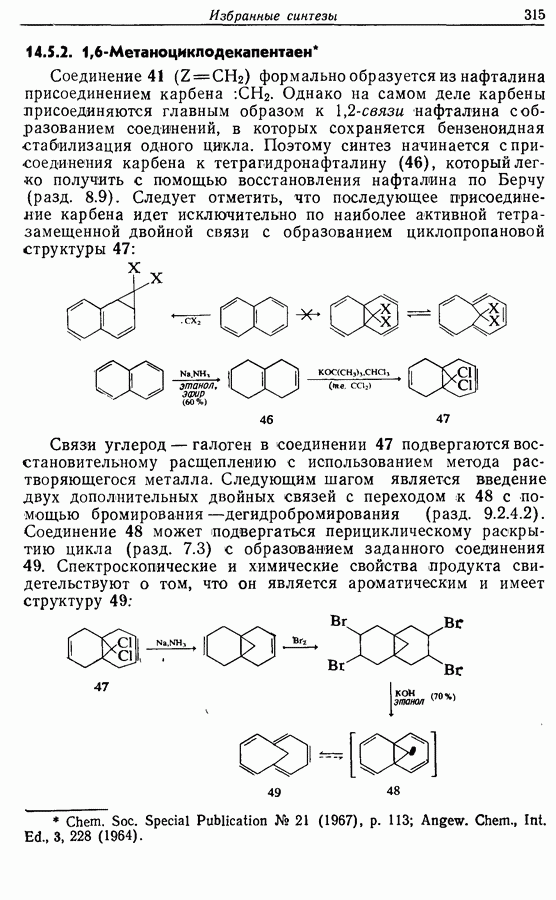
- 14.5. Анулены
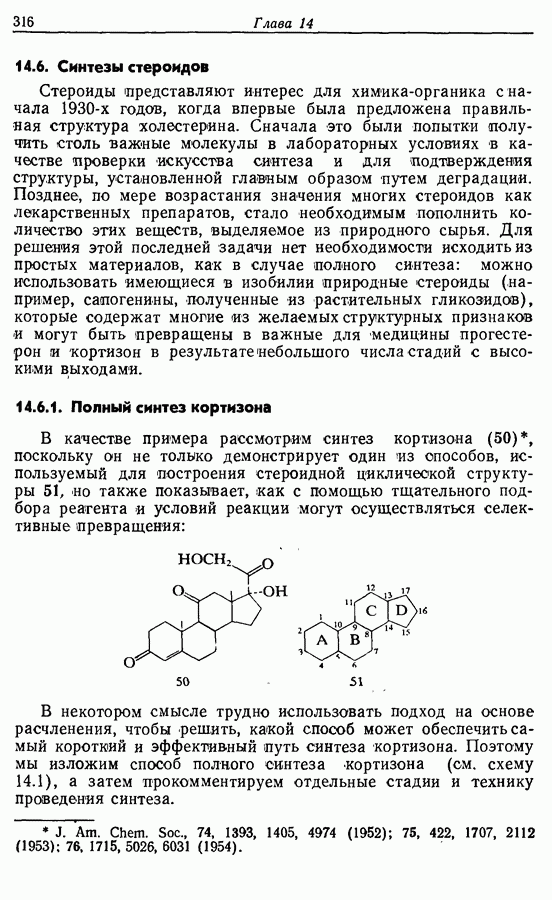
- 14.6. Синтезы стероидов
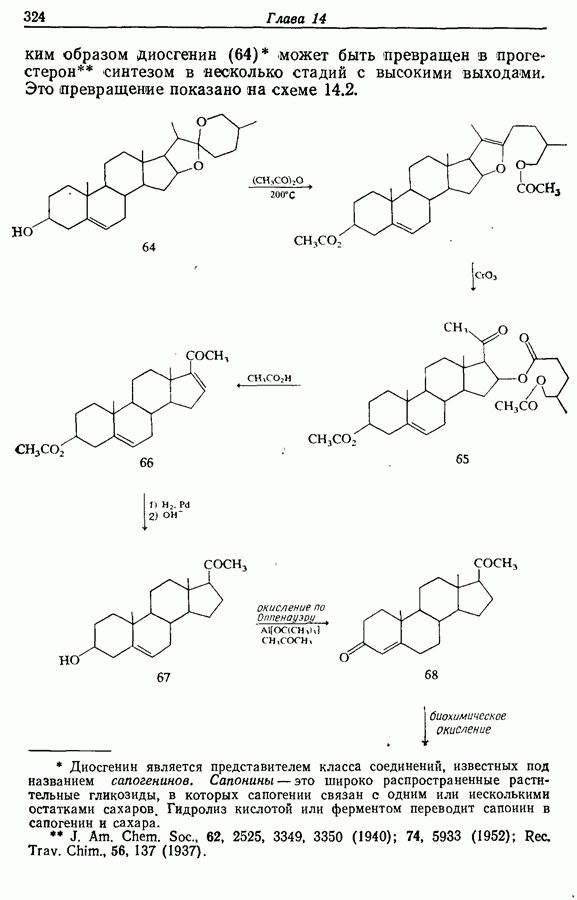
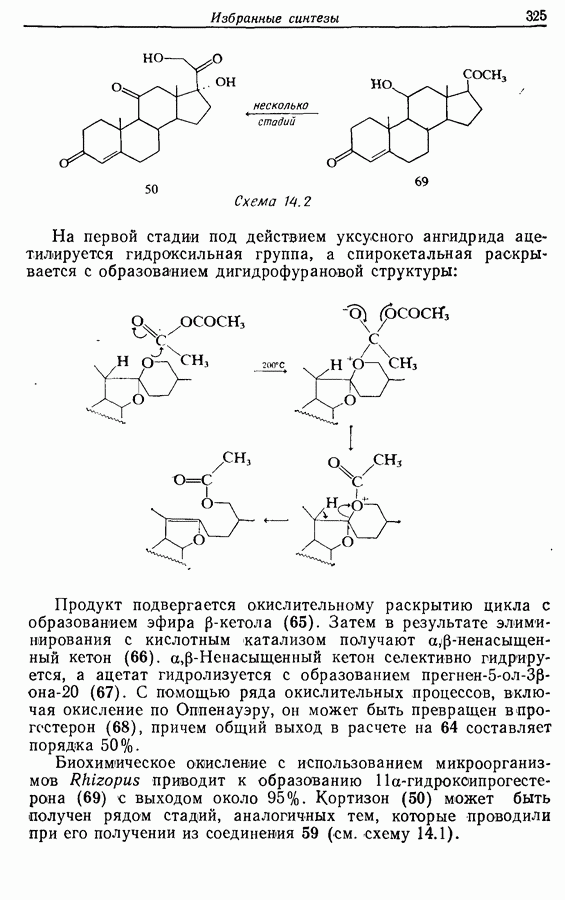
- 14.6.2. Превращение растительных стероидов в стероидные гормоны
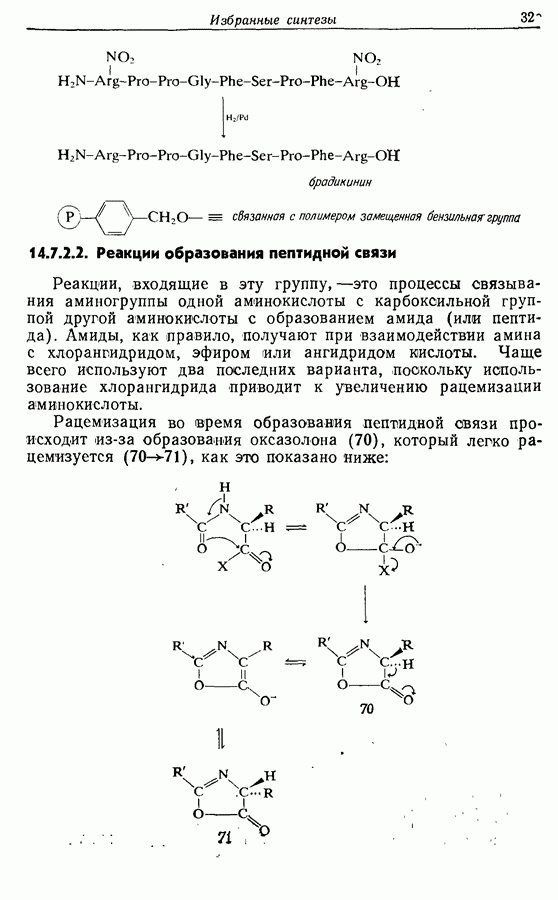
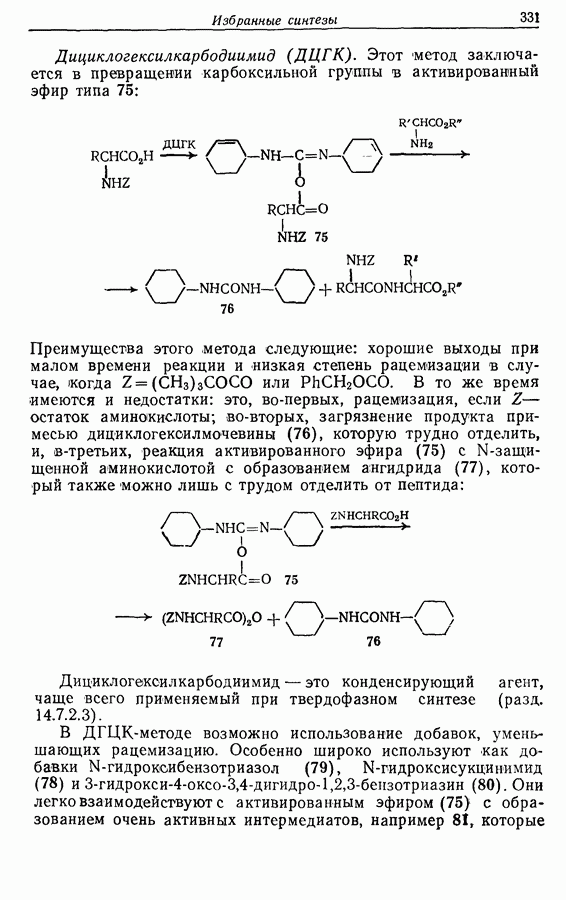
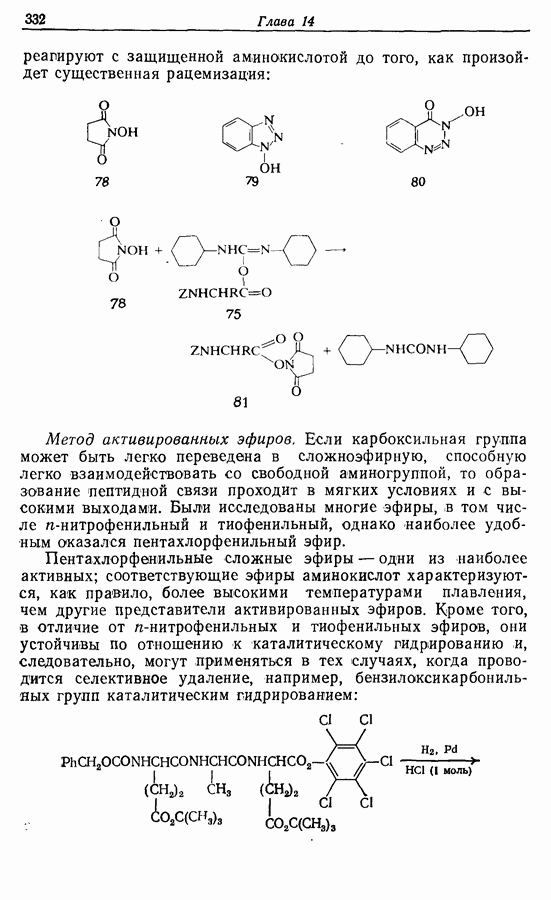
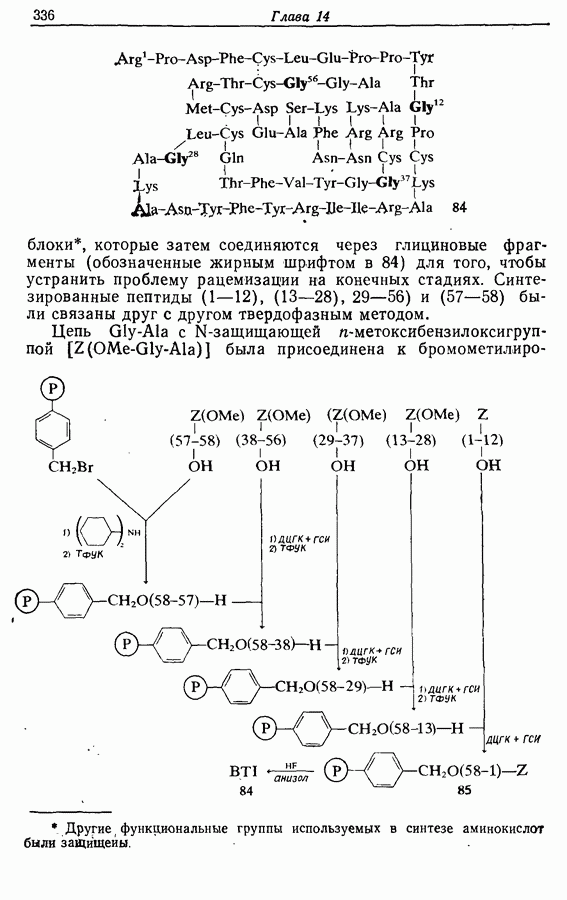
- 14.7. Синтез пептидов
- 14.7.2. Техника синтеза пептидов
- ЛИТЕРАТУРА