| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
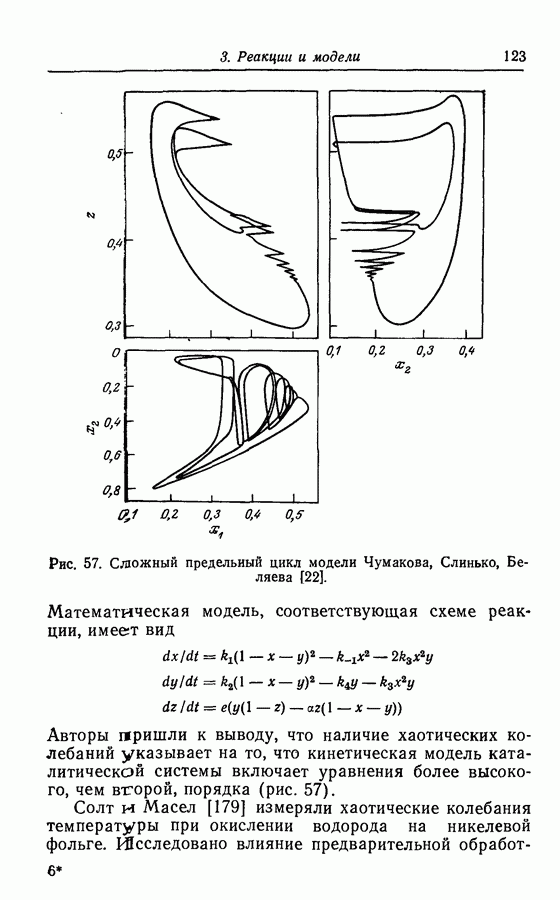
3.2. Периодические водные часы (реакция Бриггса—Раушера) [21]
Йодными часами была названа реакция, открытая Бриггсом и Раушером в 1973 г. Она несколько похожа на реакцию Брея иодат — пероксид водорода [17] и, кроме того, включает некоторые элементы реакции Белоусова (см. разд. 3.3). В состав реакционной системы входят:

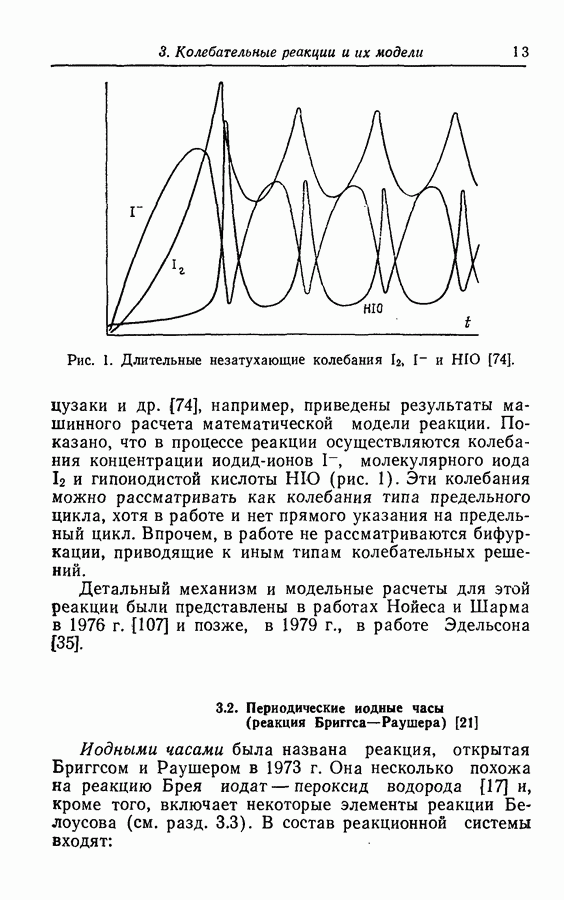
В процессе этой реакции периодически изменяются концентрации иода  и иодид-ионов
и иодид-ионов  . Колебания концентрации иодид-ионов показаны на рис. 2.
. Колебания концентрации иодид-ионов показаны на рис. 2.

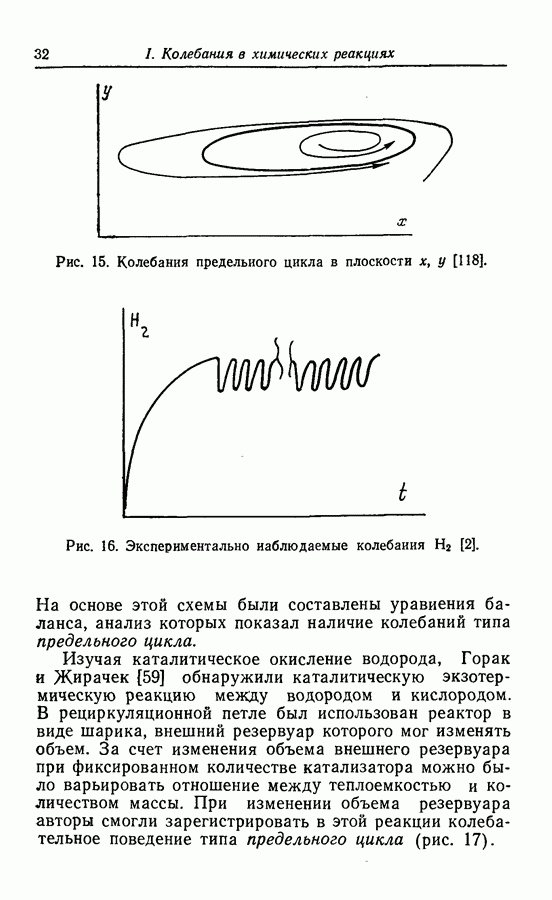
Рис. 2. Колебания концентрации иодид-иона в реакции Бриггса — Раушера [21].
Замена малоновой кислоты ацетилацетоном ( -пен-тандионом) приводит к уменьшению продолжительности колебательного режима, а замена марганца (II) (в качестве катализатора) на ионы церия (III) — к увеличению частоты колебаний.
-пен-тандионом) приводит к уменьшению продолжительности колебательного режима, а замена марганца (II) (в качестве катализатора) на ионы церия (III) — к увеличению частоты колебаний.
Схема реакции [15, 30]. При математическом моделировании этой реакции, рассматриваемом ниже, были получены различные решения. Было показано, что для некоторых значений параметров, кроме трех особых решений, двух устойчивых и одного неустойчивого, существует и предельный цикл (множественность решений). Реакция исследовалась несколькими группами ученых. Модель Буассонада [15] состоит из двух частей, первая из которых описывает концентрационные колебания. При этом введение дополнительной схемы привело
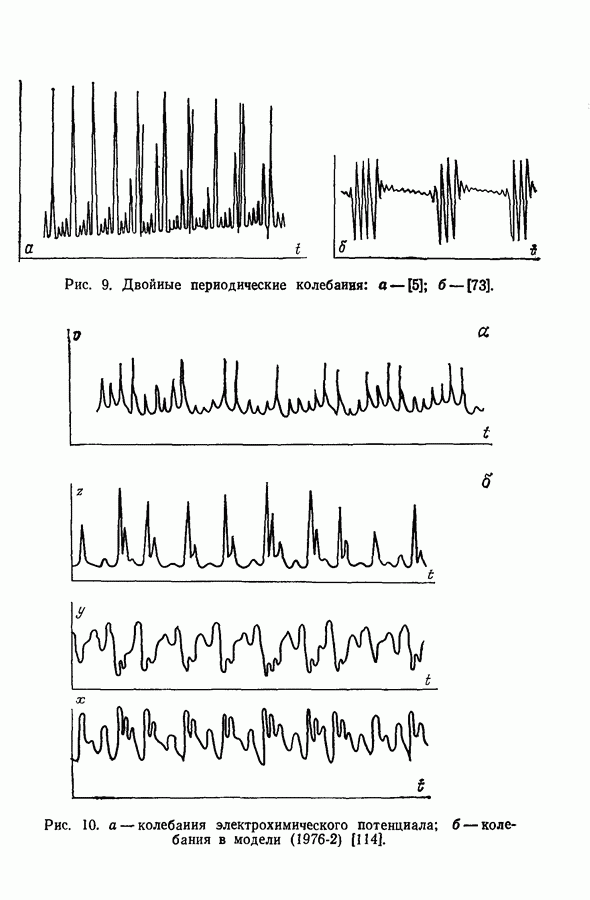
к двойным колебаниям, у которых период короче начального периода реакции. Возможность осуществления подобных двойных колебаний в других системах обсуждалась ранее в работах [13, 73, 113а, 3б, 3в] (см. разд. 3.3-3.5). Двойные колебания в системе Бриггса—Раушера были получены в работе Буассонада [15] в соответствии со следующей схемой:

Дифференциальные уравнения [15]. Кинетические Уравнения для представленной выше схемы в дифференциальной форме составляют следующую модель:

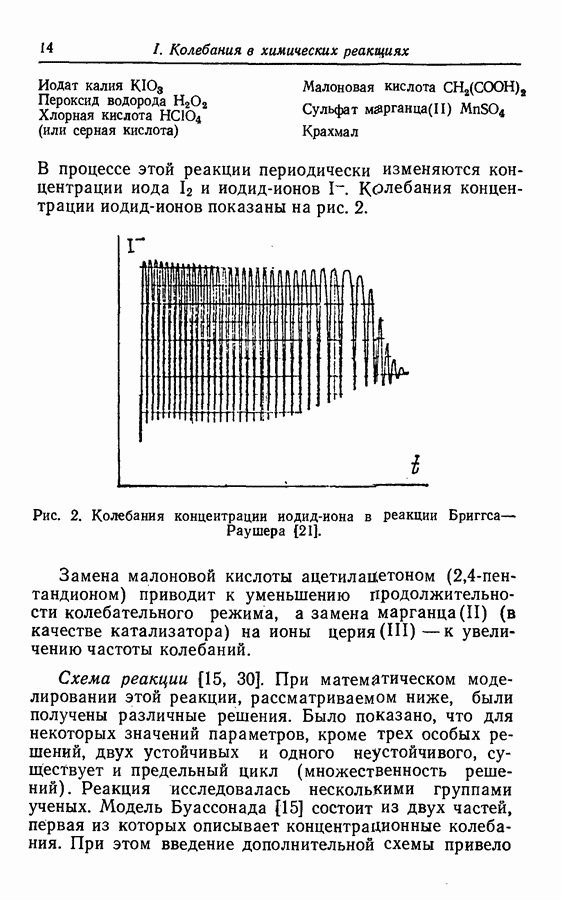
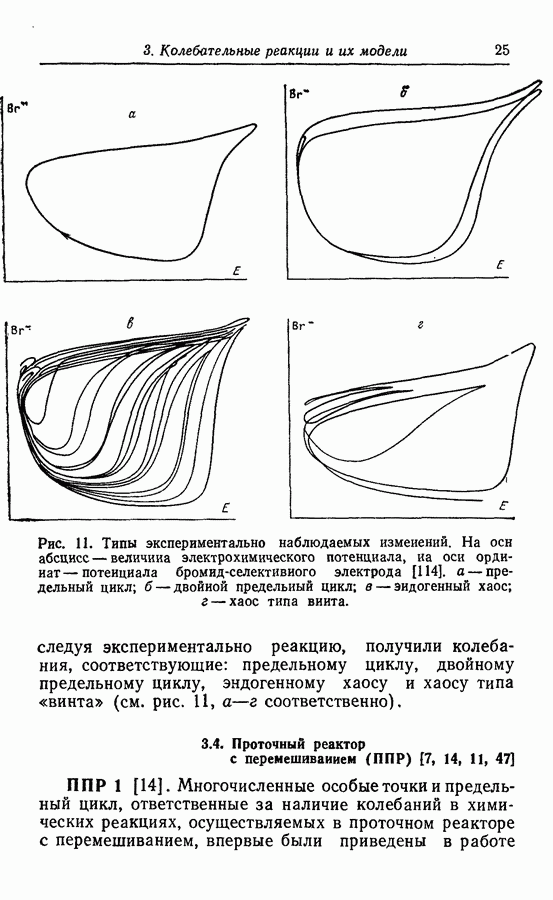
Колебания компоненты У показаны на рис. 3. В работе Буассонада показано также, что данная система имеет либо одну особую точку, либо множество особых точек (три) и один предельный цикл.
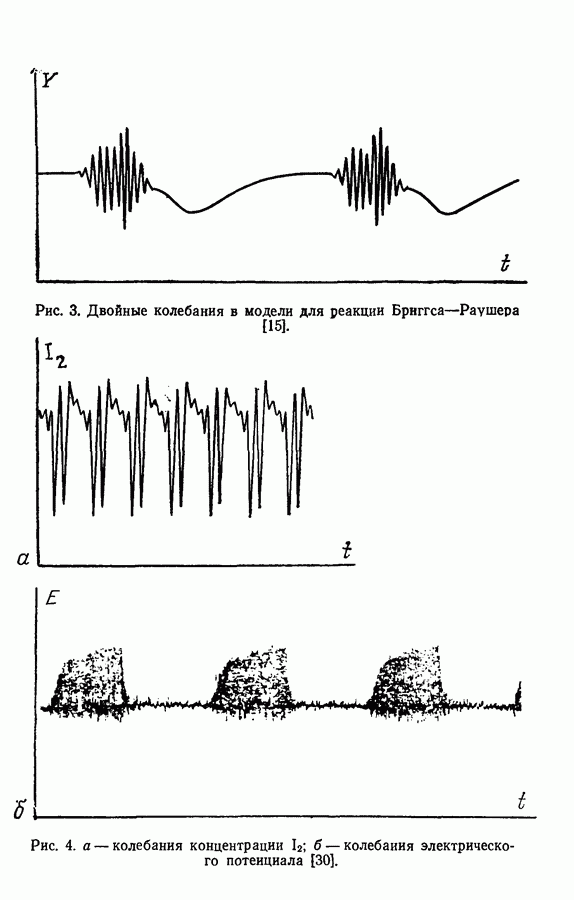
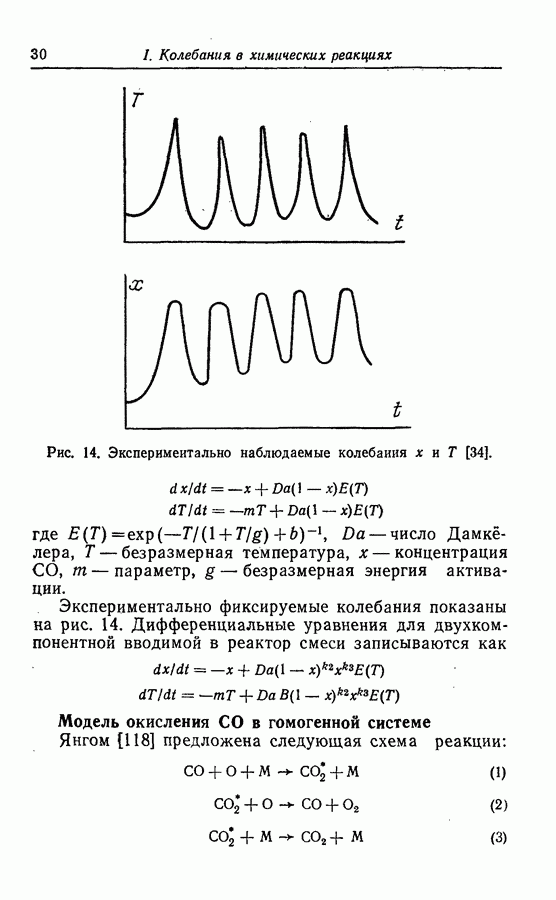
В 1975 г. Пакольт с сотр. [82, 83] привели результаты экспериментального исследования реакции Бриггса — Раушера, включая область существования колебания в координатах концентраций  Колебания, приведенные в работе Де Кеппера и др. [30] в 1976 г., показаны на рис. 4.
Колебания, приведенные в работе Де Кеппера и др. [30] в 1976 г., показаны на рис. 4.
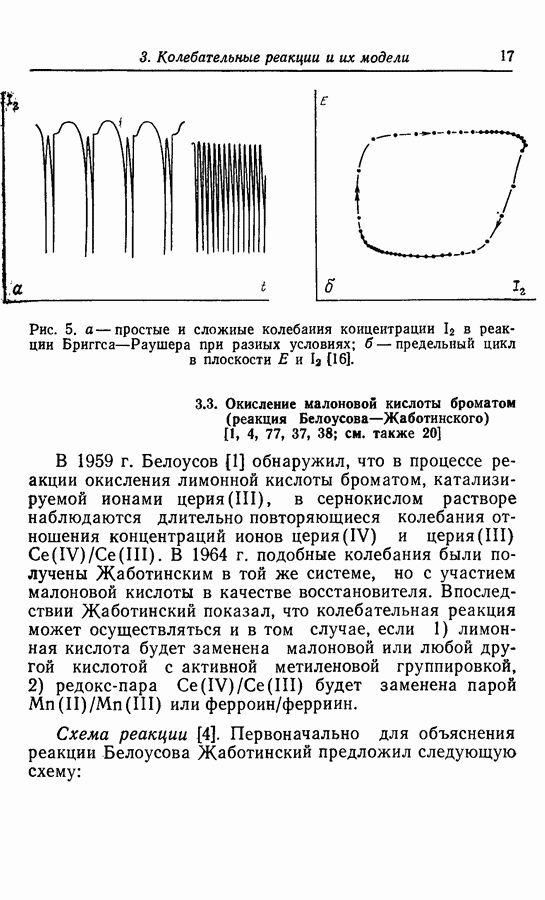
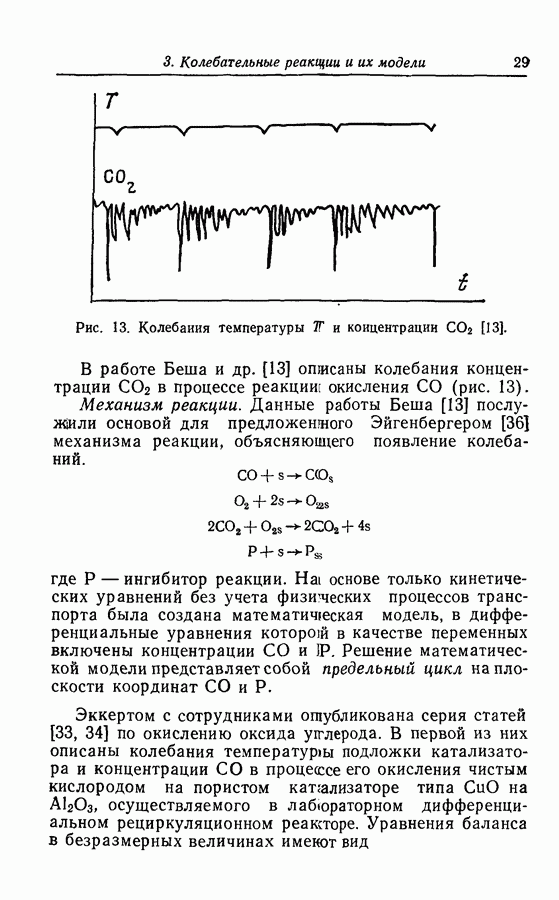
В 1980 г. Буассонад и Де Кеппер [16] опубликовали интересные результаты исследования рассматриваемой реакции: наличие простых и сложных колебаний концентрации молекулярного иода, запись которых представлена на рис. 5 вместе с простым предельным циклом для этой системы.
(см. скан)
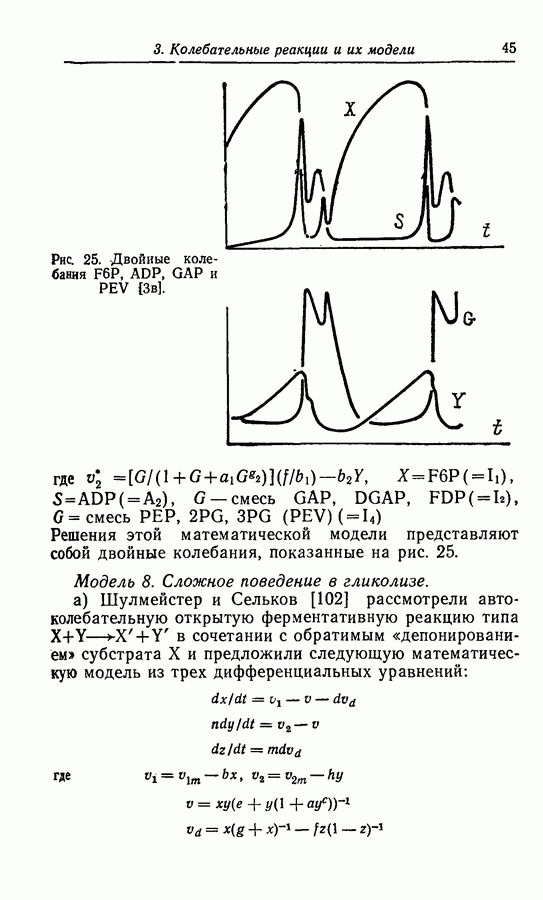
Рис. 3. Двойные колебания в модели для реакции Бриггса—Раушера [15].
(см. скан)
Рис. 4. а — колебания концентрации b; б — колебания электрического потенциала [30].
(см. скан)
Рис. 5. а — простые и сложные колебания концентрации 12 в реакции Бриггса—Раушера при разных условиях; б — предельный цикл в плоскости Е и  [16].
[16].
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- Часть I. КОЛЕБАНИЯ В ХИМИЧЕСКИХ РЕАКЦИЯХ
- 3. Колебательные реакции и их модели
- 3.1. Разложение пероксида водорода, катализируемое иодатом (реакция Брея—Либавски)
- 3.2. Периодические водные часы (реакция Бриггса—Раушера) [21]
- 3.3. Окисление малоновоб кислоты броматом (реакция Белоусова—Жаботинского)
- 3.4. Проточный реактор с перемешиванием (ППР) [7, 14, II, 47]
- 3.5. Реакции на твердых катализаторах
- 3.6. Колебания в гликолизе
- 3.7. Реакции, катализируемые пероксидазой
- 3.8. Разложение дитионита натрия
- 3.9. Бимолекулярная модель
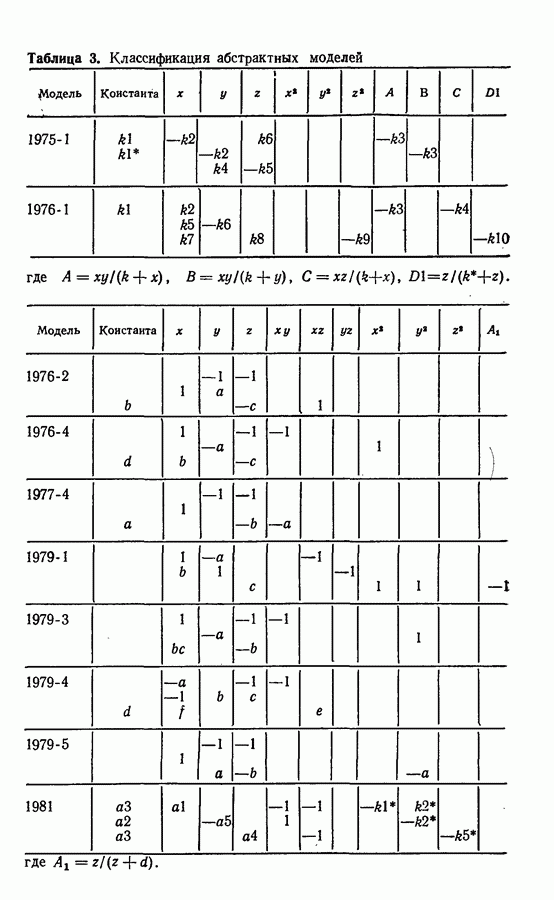
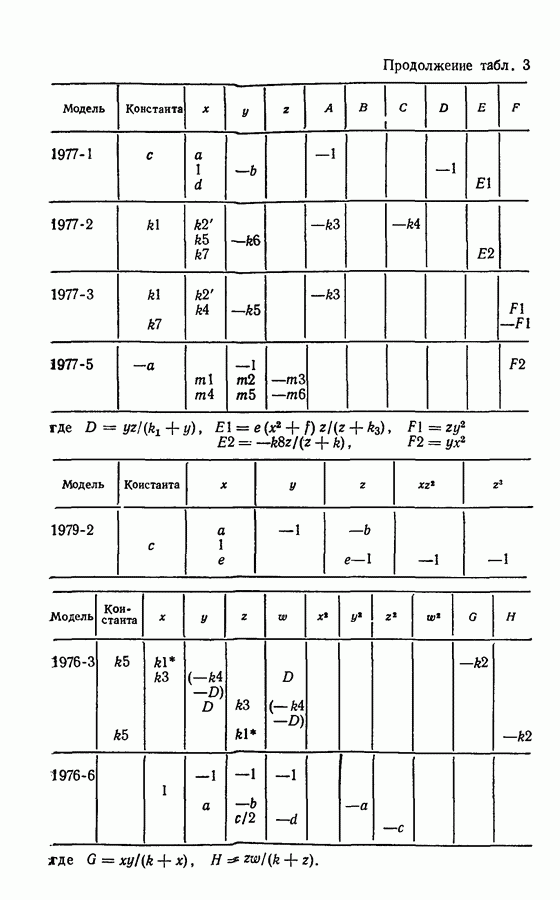
- 3.10. Абстрактные системы реакций и их модели
- 3.11. Некаталитические реакции
- 3.12. Таблица колебательных реакций
- 4. Характеристики колебательных систем
- 4.2. Нелинейность систем
- 4.3. Параметры системы
- 4.4. Число решений
- 5. Глобальный анализ
- 5.2. Бифуркации как способ поиска колебаний
- 6. Классификация колебаний
- 6.2. Типы компонентов колебательных химических реакций
- 6.3. Типы колебательных математических решений
- 7. Состояние исследований и дальнейшие направления их развития
- Часть II. РАЗВИТИЕ ИССЛЕДОВАНИЙ ХИМИЧЕСКИХ КОЛЕБАНИЙ В ПОСЛЕДНЕЕ ВРЕМЯ
- 3. Реакции и модели, проявляющие колебания
- 3.1. Разложение пероксида водорода, катализируемое иодатом (реакция Брея—Либавски)
- 3.2. Колебательные йодные часы (реакция Бриггса—Раушера)
- 3.3. Окисление малоновой кислоты броматом (реакция Белоусова—Жаботинского)
- 3.4. Проточный реактор с перемешиванием
- 3.5. Реакции на твердых катализаторах
- 3.6. Колебания в гликолизе
- 3.7. Реакции, катализируемые пероксидазой
- 3.8. Разложение дитионита натрия
- 3.9. Бимолекулярная модель
- 3.10. Абстрактные системы реакций
- 3.11. Некаталитические реакции
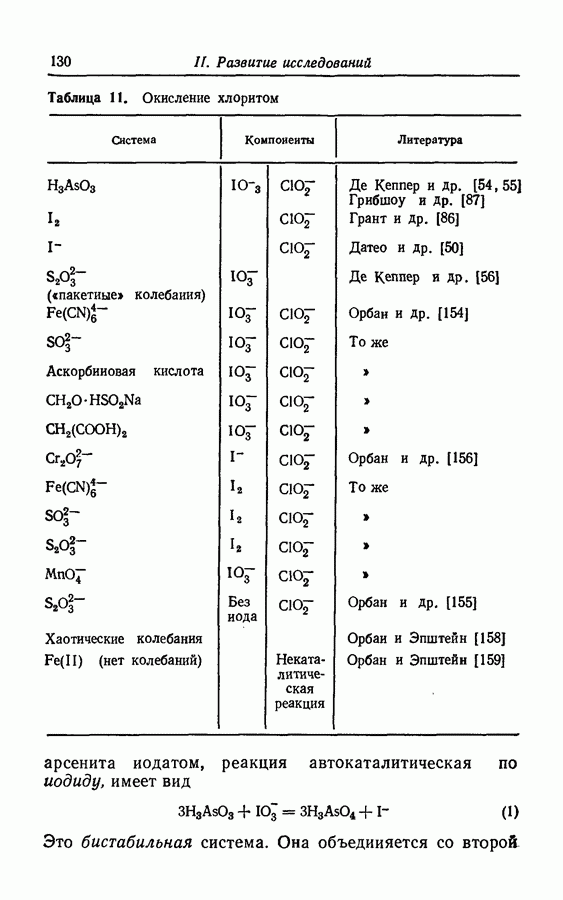
- 3.12. Окисление хлоритом
- 3.13. Разноплановые исследования
- 3.14. Общие модели и математические методы