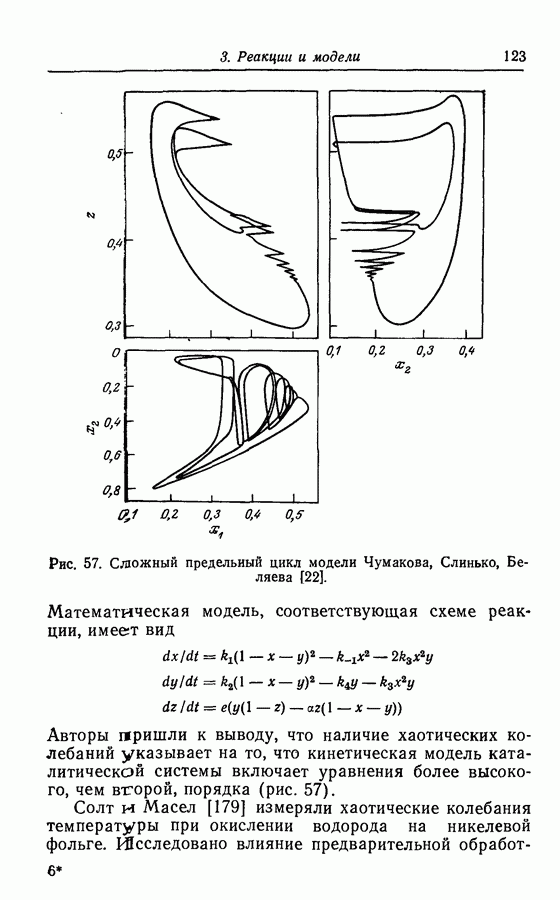
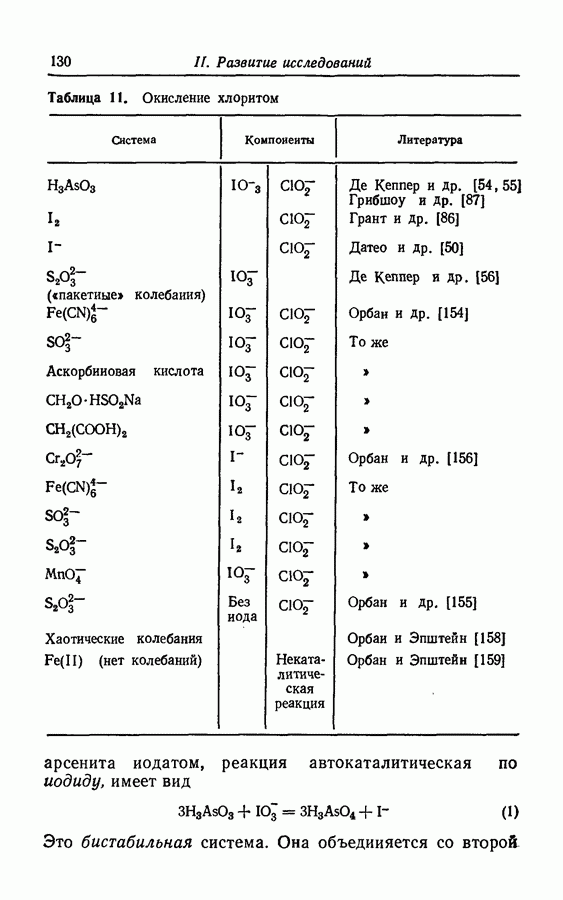
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
3.5. Реакции на твердых катализаторах
Каталитическое разложение  . Первыми работами в области колебательных гетерогенных каталитических систем были работы Хьюго [60, 61], описавшего периодические флуктуации параметров при экзотермическом разложении
. Первыми работами в области колебательных гетерогенных каталитических систем были работы Хьюго [60, 61], описавшего периодические флуктуации параметров при экзотермическом разложении  на катализаторе из оксида меди (II).
на катализаторе из оксида меди (II).
Каталитическое окисление СО. В 1972 г. была опубликована работа Хьюго и Якубица [62] (см. также [61]), в которой изложены результаты исследования окисления СО в изотермических условиях на катализаторе, представляющем собой решетку из платиновой проволоки; процесс сопровождался незатухающими колебаниями. В работе был приведен сложный механизм реакции, включающий концентрации активированных молекул и объясняющий наличие концентрационных колебаний, однако дальнейшего развития это исследование не получило.

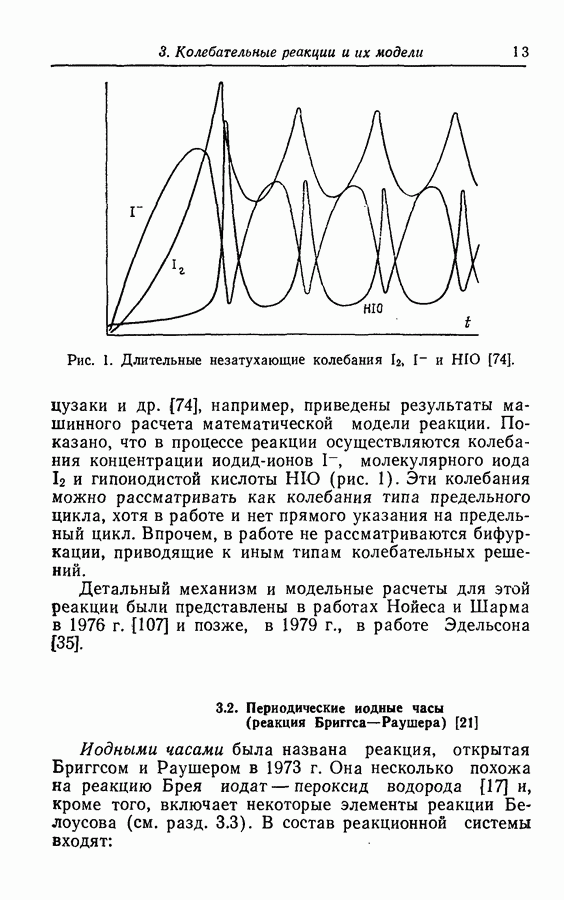
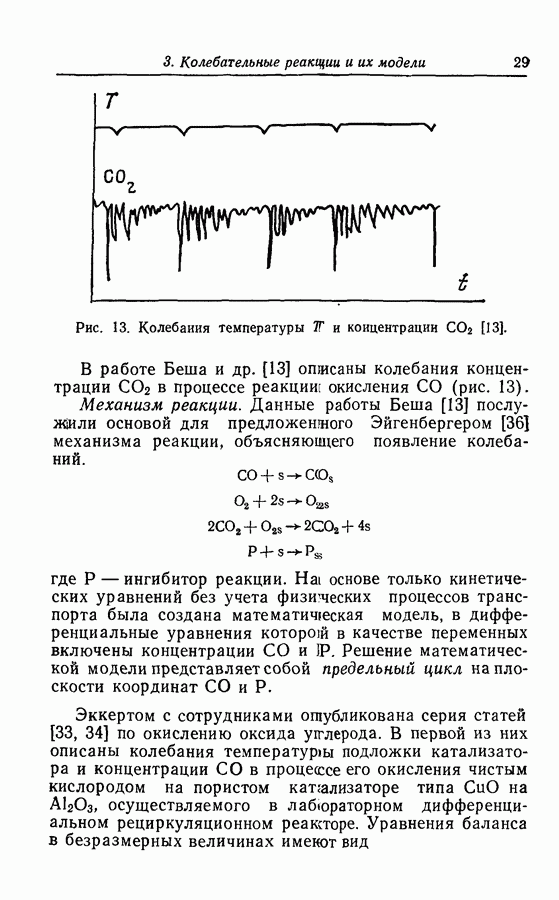
Рис. 13. Колебания температуры  и концентрации
и концентрации  [13].
[13].
В работе Беша и др. [13] описаны колебания концентрации  в процессе реакциш окисления СО (рис. 13).
в процессе реакциш окисления СО (рис. 13).
Механизм реакции. Данные работы Беша [13] послужили основой для предложенмого Эйгенбергером [36] механизма реакции, объясняющего появление колебаний.

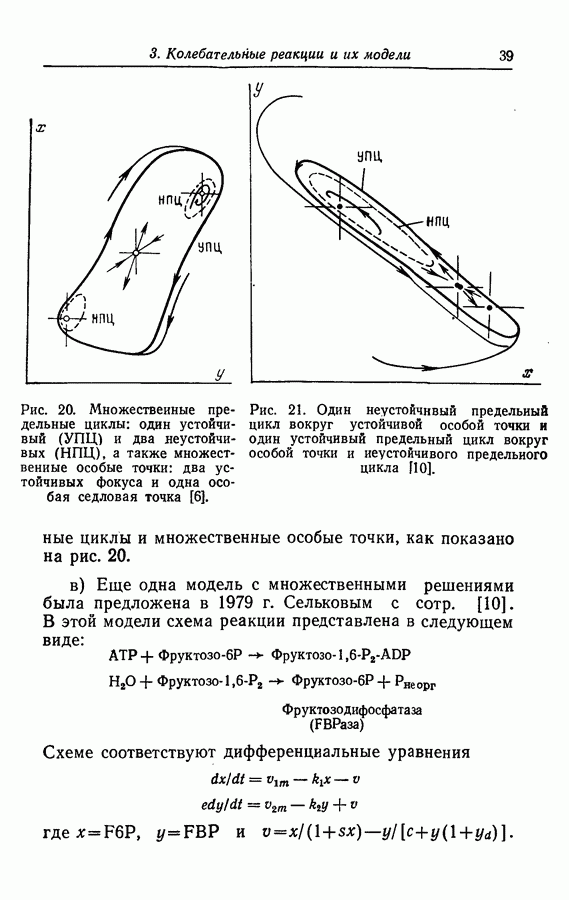
где P — ингибитор реакции.  основе только кинетических уравнений без учета физических процессов транспорта была создана математическая модель, в дифференциальные уравнения которой в качестве переменных включены концентрации
основе только кинетических уравнений без учета физических процессов транспорта была создана математическая модель, в дифференциальные уравнения которой в качестве переменных включены концентрации  . Решение математической модели представляет собой предельный цикл на плоскости координат
. Решение математической модели представляет собой предельный цикл на плоскости координат  .
.
Эккертом с сотрудниками ощубликована серия статей [33, 34] по окислению оксида угглерода. В первой из них описаны колебания температурил подложки катализатора и концентрации СО в процессе его окисления чистым кислородом на пористом катализаторе типа  на
на  осуществляемого в лабюраторном дифференциальном рециркуляционном реакторе. Уравнения баланса в безразмерных величинах имекот вид
осуществляемого в лабюраторном дифференциальном рециркуляционном реакторе. Уравнения баланса в безразмерных величинах имекот вид

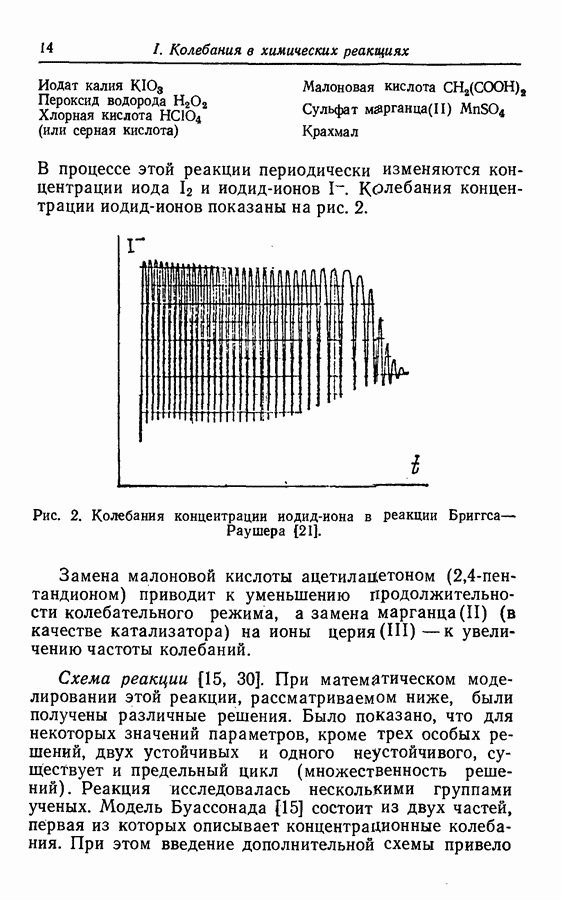
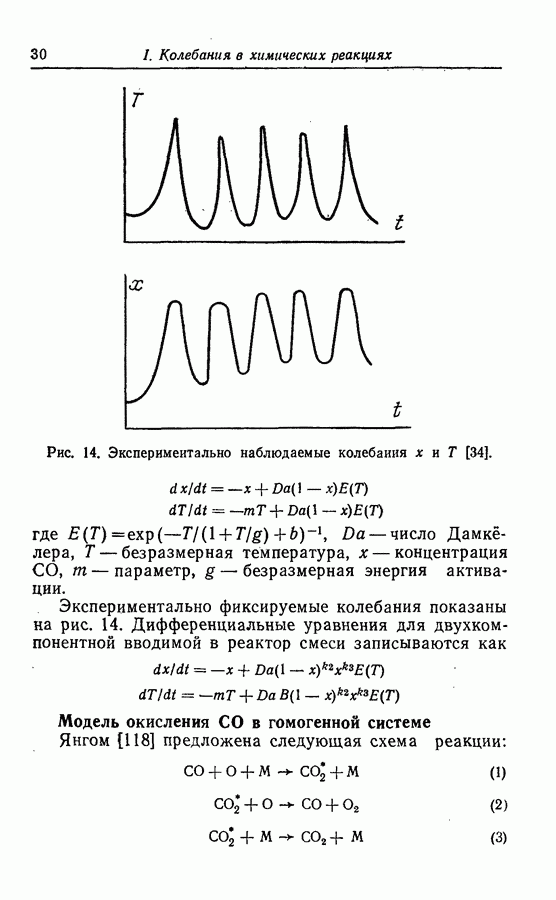
Рис. 14. Экспериментально наблюдаемые колебания х и Т [34].

где  — число Дамкёлера, Т — безразмерная температура, х — концентрация СО, m — параметр, g — безразмерная энергия активации.
— число Дамкёлера, Т — безразмерная температура, х — концентрация СО, m — параметр, g — безразмерная энергия активации.
Экспериментально фиксируемые колебания показаны на рис. 14. Дифференциальные уравнения для двухкомпонентной вводимой в реактор смеси записываются как

Модель окисления СО в гомогенной системе
Янгом [118] предложена следующая схема реакции:


На основании схемы реакции предложена система дифференциальных уравнений:

где  — концентрации
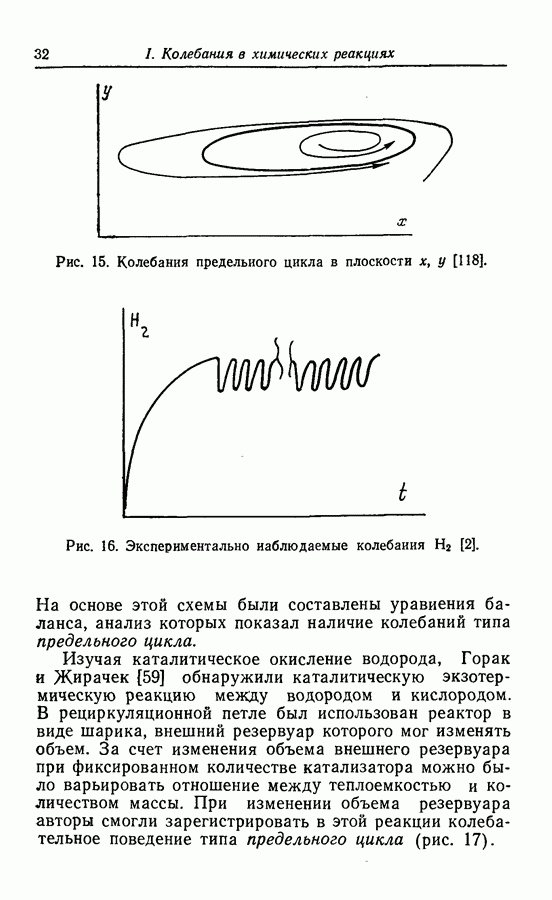
— концентрации  соответственно. Результаты расчета этой модели представляют собой колебания типа предельного цикла, показанного на рис. 15.
соответственно. Результаты расчета этой модели представляют собой колебания типа предельного цикла, показанного на рис. 15.
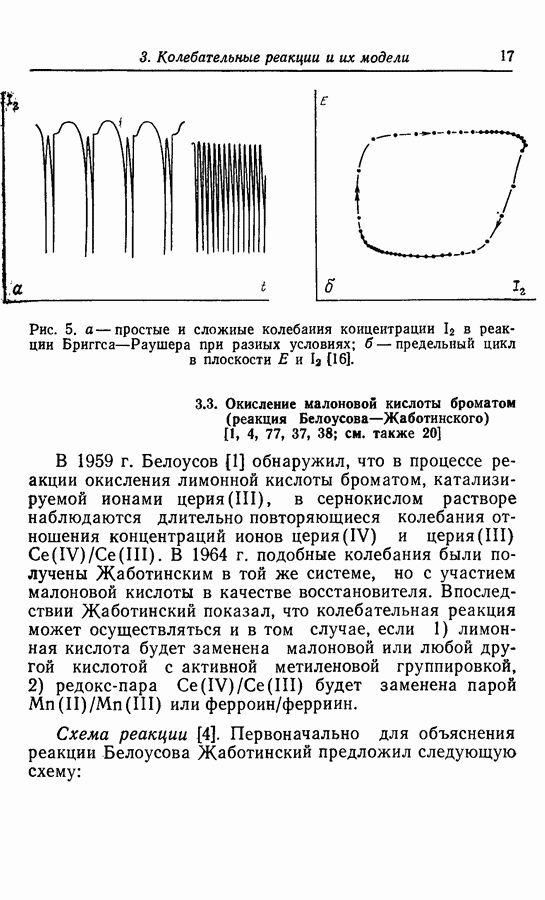
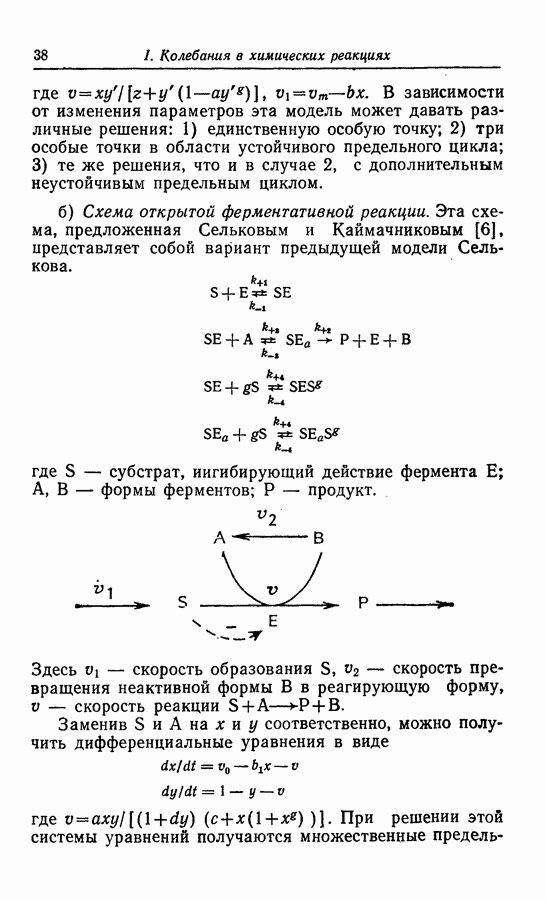
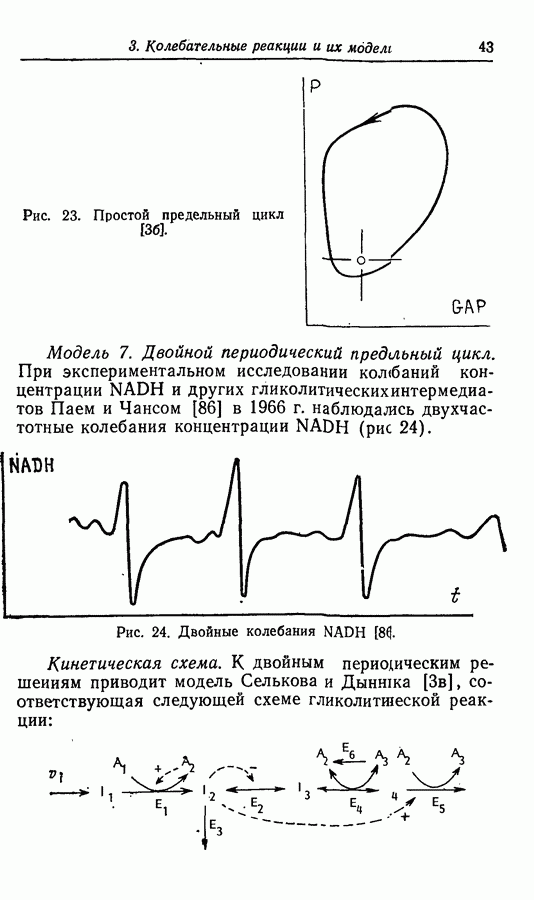
Каталитическое окисление водорода. При исследовании каталитического окисления водорода Беляевым [2] было найдено, что продукты реакции являются ее катализаторами, и таким образом обнаружено явление обратной связи. Было установлено несколько стационарных состояний для реакций каталитического окисления водорода на никелевой фольге, а также для реакции взаимодействия водорода с СО, и описаны устойчивые автоколебания скорости окисления водорода на никелевой фольге в изотермических условиях (рис. 16).
В этой же реакции Горак и Жирачек [59] наблюдали три стационарных состояния и показали, что устойчивость этих состояний зависит от отношения объема реактора к концентрации катализатора.
Механизм реакции. Пикиос и Лусс [84] предложили следующую схему механизма реакции:


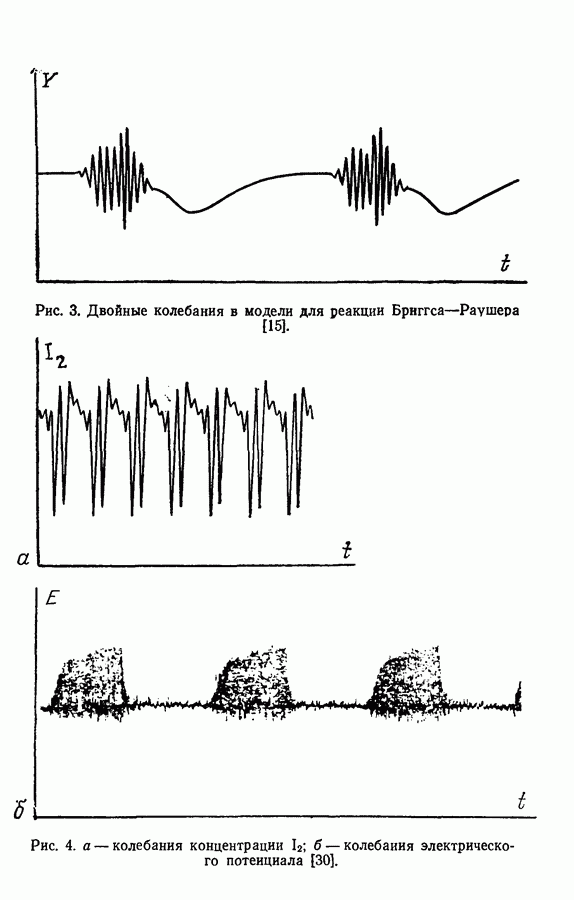
Рис. 15. Колебания предельного цикла в плоскости х, у [118].

Рис. 16. Экспериментально наблюдаемые колебания  [2].
[2].
На основе этой схемы были составлены уравнения баланса, анализ которых показал наличие колебаний типа предельного цикла.
Изучая каталитическое окисление водорода, Горак и Жирачек [59] обнаружили каталитическую экзотермическую реакцию между водородом и кислородом. В рециркуляционной петле был использован реактор в виде шарика, внешний резервуар которого мог изменять объем. За счет изменения объема внешнего резервуара при фиксированном количестве катализатора можно было варьировать отношение между теплоемкостью и количеством массы. При изменении объема резервуара авторы смогли зарегистрировать в этой реакции колебательное поведение типа предельного цикла (рис. 17).

Рис. 17. Колебания предельного цикла, полученные как результат влияния объема реактора V на устойчивость стационарных состояний [58].
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- Часть I. КОЛЕБАНИЯ В ХИМИЧЕСКИХ РЕАКЦИЯХ
- 3. Колебательные реакции и их модели
- 3.1. Разложение пероксида водорода, катализируемое иодатом (реакция Брея—Либавски)
- 3.2. Периодические водные часы (реакция Бриггса—Раушера) [21]
- 3.3. Окисление малоновоб кислоты броматом (реакция Белоусова—Жаботинского)
- 3.4. Проточный реактор с перемешиванием (ППР) [7, 14, II, 47]
- 3.5. Реакции на твердых катализаторах
- 3.6. Колебания в гликолизе
- 3.7. Реакции, катализируемые пероксидазой
- 3.8. Разложение дитионита натрия
- 3.9. Бимолекулярная модель
- 3.10. Абстрактные системы реакций и их модели
- 3.11. Некаталитические реакции
- 3.12. Таблица колебательных реакций
- 4. Характеристики колебательных систем
- 4.2. Нелинейность систем
- 4.3. Параметры системы
- 4.4. Число решений
- 5. Глобальный анализ
- 5.2. Бифуркации как способ поиска колебаний
- 6. Классификация колебаний
- 6.2. Типы компонентов колебательных химических реакций
- 6.3. Типы колебательных математических решений
- 7. Состояние исследований и дальнейшие направления их развития
- Часть II. РАЗВИТИЕ ИССЛЕДОВАНИЙ ХИМИЧЕСКИХ КОЛЕБАНИЙ В ПОСЛЕДНЕЕ ВРЕМЯ
- 3. Реакции и модели, проявляющие колебания
- 3.1. Разложение пероксида водорода, катализируемое иодатом (реакция Брея—Либавски)
- 3.2. Колебательные йодные часы (реакция Бриггса—Раушера)
- 3.3. Окисление малоновой кислоты броматом (реакция Белоусова—Жаботинского)
- 3.4. Проточный реактор с перемешиванием
- 3.5. Реакции на твердых катализаторах
- 3.6. Колебания в гликолизе
- 3.7. Реакции, катализируемые пероксидазой
- 3.8. Разложение дитионита натрия
- 3.9. Бимолекулярная модель
- 3.10. Абстрактные системы реакций
- 3.11. Некаталитические реакции
- 3.12. Окисление хлоритом
- 3.13. Разноплановые исследования
- 3.14. Общие модели и математические методы