| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ТЕРМОДИНАМИЧЕСКИЙ КОНТРОЛЬ
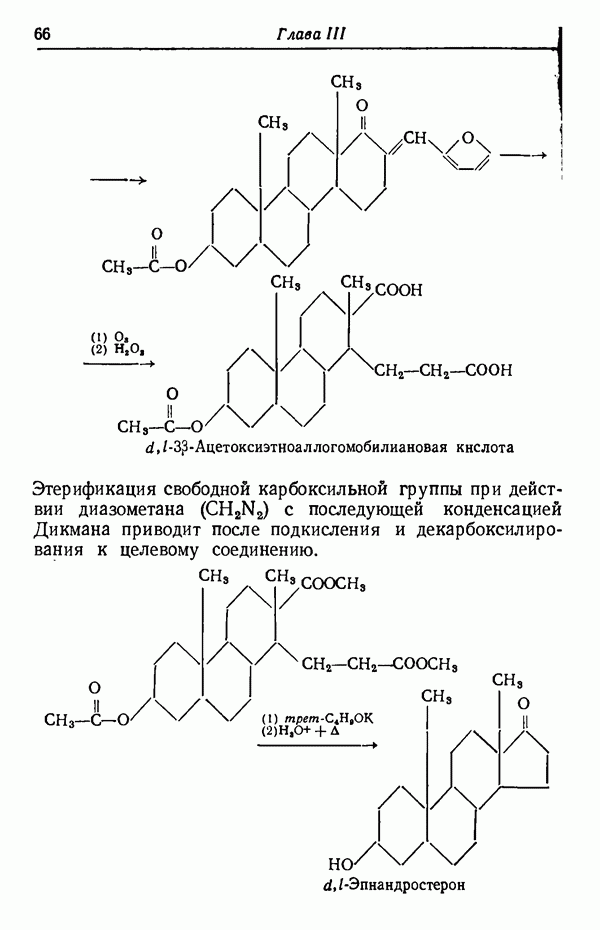
Химическая термодинамика помогает понять роль соотношения энергий исходного и конечного состояний реагирующей системы. О степени образования изомеров  в той или иной реакции при отсутствии кинетических данных можно судить по уравнению зависимости свободной энергии от константы равновесия. С другой стороны, кинетическая информация дает сравнительные скорости образования двух изомеров. Следовательно, если реакцию останавливают до достижения равновесия, то соотношение полученных изомеров представляет собой результат кинетического контроля, а изомер, полученный в преобладающем количестве, не обязательно термодинамически наиболее стабилен. В условиях же равновесия основным продуктом реакции будет наиболее термодинамически устойчивый изомер.
в той или иной реакции при отсутствии кинетических данных можно судить по уравнению зависимости свободной энергии от константы равновесия. С другой стороны, кинетическая информация дает сравнительные скорости образования двух изомеров. Следовательно, если реакцию останавливают до достижения равновесия, то соотношение полученных изомеров представляет собой результат кинетического контроля, а изомер, полученный в преобладающем количестве, не обязательно термодинамически наиболее стабилен. В условиях же равновесия основным продуктом реакции будет наиболее термодинамически устойчивый изомер.
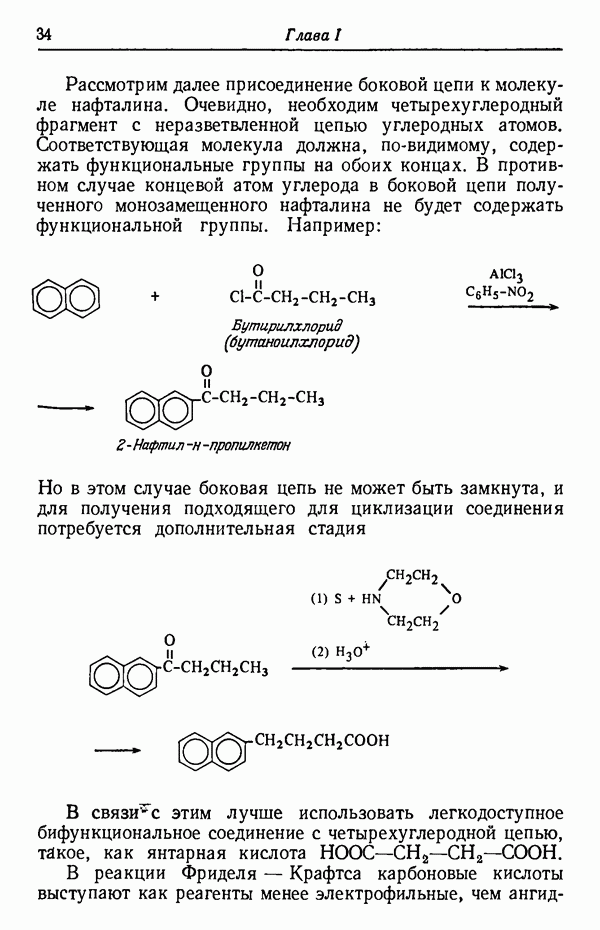
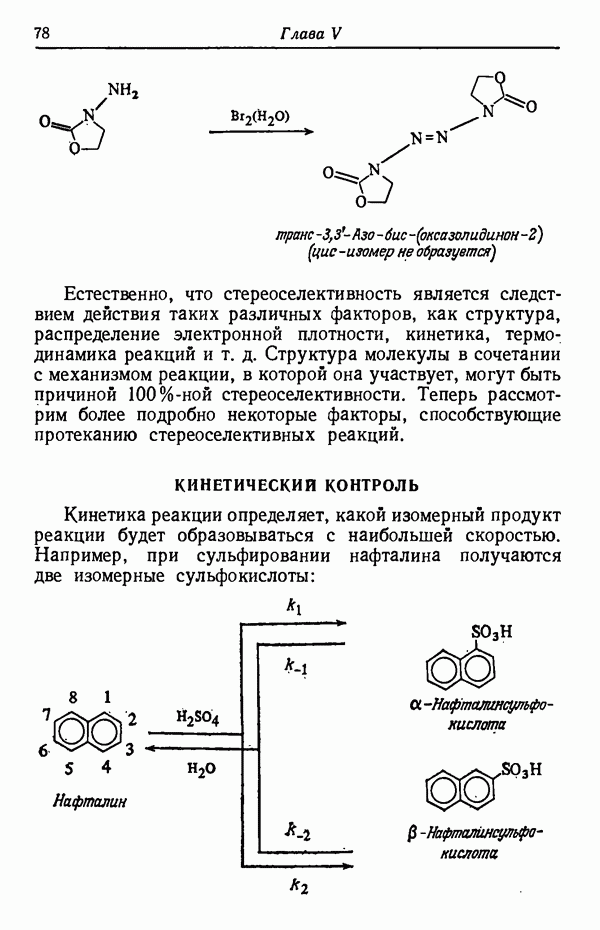
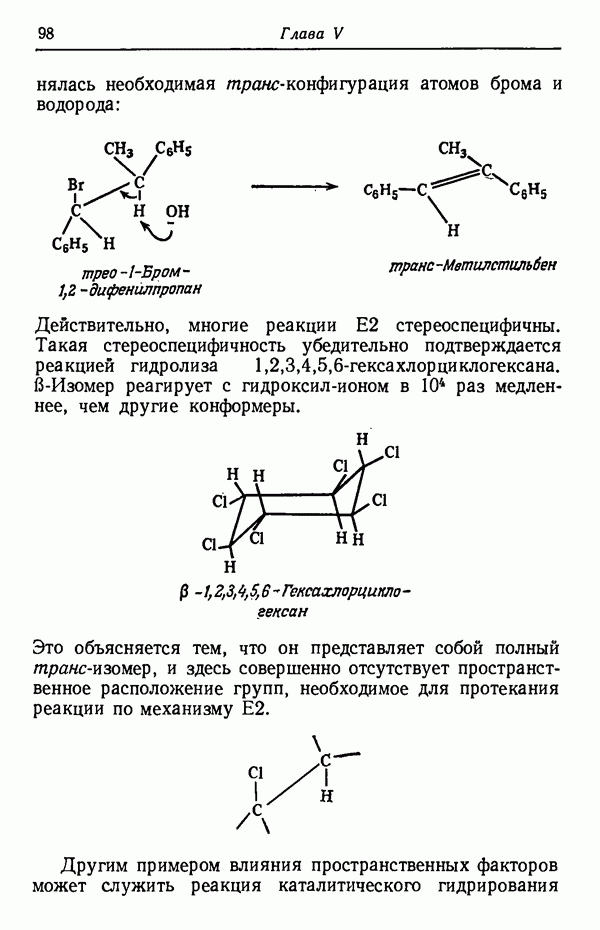
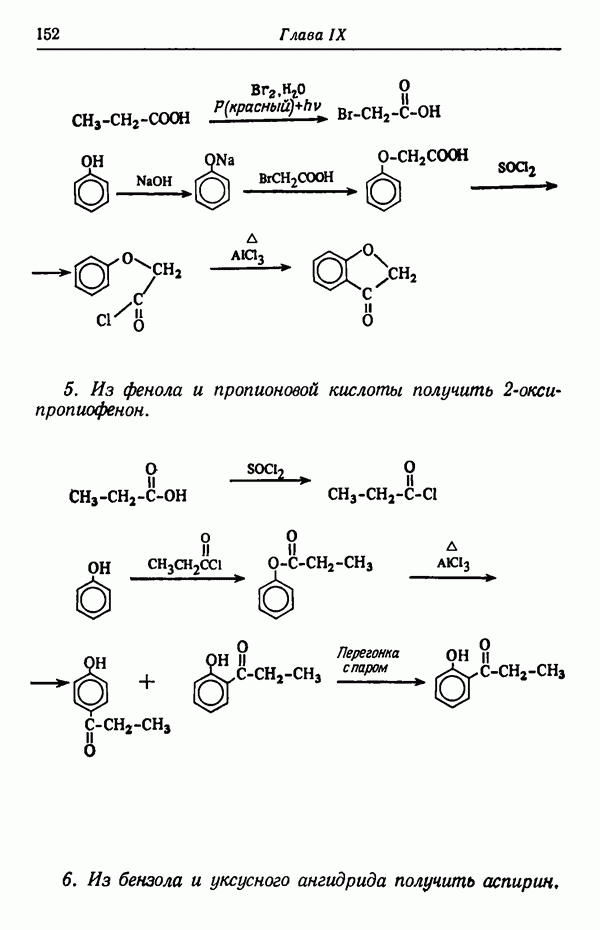
Ранее говорилось о том, что основным продуктом сульфирования нафталина при 80° С является  -изомер, а при 160°С реакция приводит главным образом к продукту
-изомер, а при 160°С реакция приводит главным образом к продукту  -замещения. Причина этой кажущейся аномалии заключается не в том, что при 160° С скорость образования
-замещения. Причина этой кажущейся аномалии заключается не в том, что при 160° С скорость образования  -изомера выше, а в том, что при 80° С реакция достигает положения равновесия очень медленно и останавливается прежде, чем соотношение изомеров, полученных в условиях кинетического контроля, достигает равновесного значения. Но при 160° С реакция быстро достигает положения равновесия, в условиях которого образуется термодинамически более стабильный
-изомера выше, а в том, что при 80° С реакция достигает положения равновесия очень медленно и останавливается прежде, чем соотношение изомеров, полученных в условиях кинетического контроля, достигает равновесного значения. Но при 160° С реакция быстро достигает положения равновесия, в условиях которого образуется термодинамически более стабильный  -изомер; иначе говоря, действует термодинамический контроль.
-изомер; иначе говоря, действует термодинамический контроль.
При сульфировании нафталина образование каждого продукта  или
или  -изомера) связано с различными значениями энергии активации
-изомера) связано с различными значениями энергии активации  и изменения свободной энергии
и изменения свободной энергии 

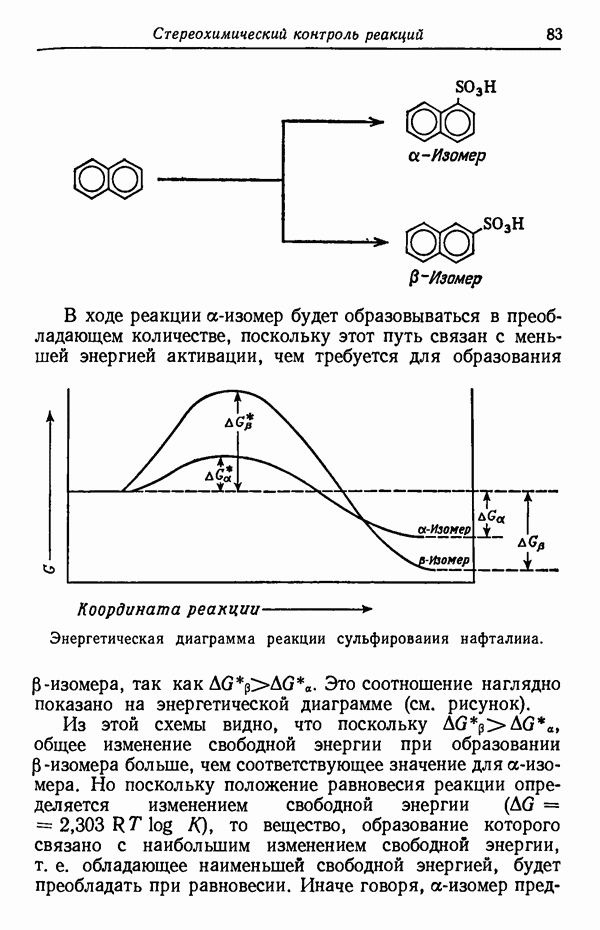
В ходе реакции  -изомер будет образовываться в преобладающем количестве, поскольку этот путь связан с меньшей энергией активации, чем требуется для образования
-изомер будет образовываться в преобладающем количестве, поскольку этот путь связан с меньшей энергией активации, чем требуется для образования  -изомера, так как
-изомера, так как  Это соотношение наглядно показано на энергетической диаграмме (см. рисунок).
Это соотношение наглядно показано на энергетической диаграмме (см. рисунок).

Энергетическая диаграмма реакции сульфирования нафталина. Из этой схемы видно, что поскольку  общее изменение свободной энергии при образовании
общее изменение свободной энергии при образовании  -изомера больше, чем соответствующее значение для
-изомера больше, чем соответствующее значение для  -изо-мера. Но поскольку положение равновесия реакции определяется изменением свободной энергии
-изо-мера. Но поскольку положение равновесия реакции определяется изменением свободной энергии  то вещество, образование которого связано с наибольшим изменением свободной энергии, т. е. обладающее наименьшей свободной энергией, будет преобладать при равновесии. Иначе говоря,
то вещество, образование которого связано с наибольшим изменением свободной энергии, т. е. обладающее наименьшей свободной энергией, будет преобладать при равновесии. Иначе говоря,  -изомер
-изомер
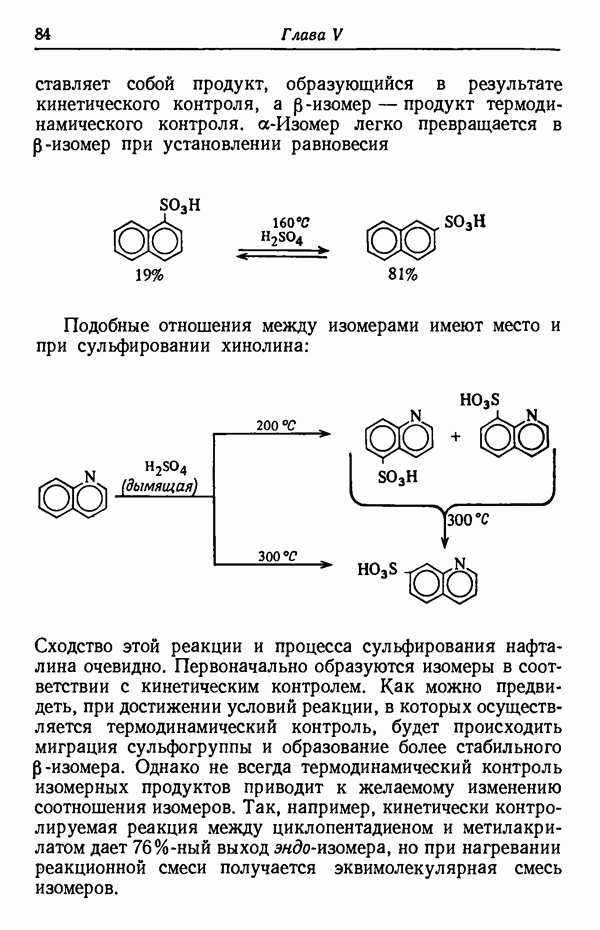
представляет собой продукт, образующийся в результате кинетического контроля,  -изомер — продукт термодинамического контроля.
-изомер — продукт термодинамического контроля.  легко превращается в
легко превращается в  -изомер при установлении равновесия
-изомер при установлении равновесия

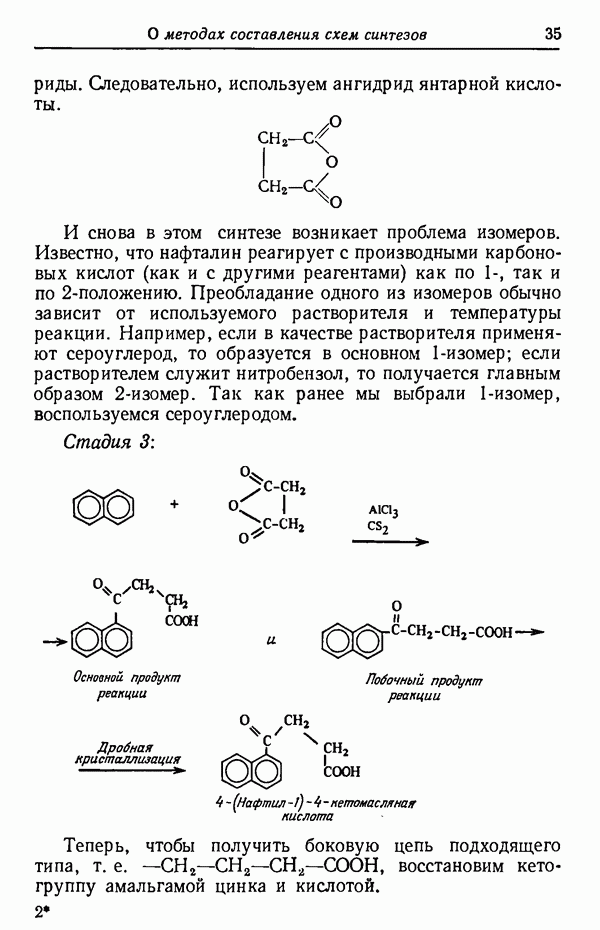
Подобные отношения между изомерами имеют место и при сульфировании хинолина:

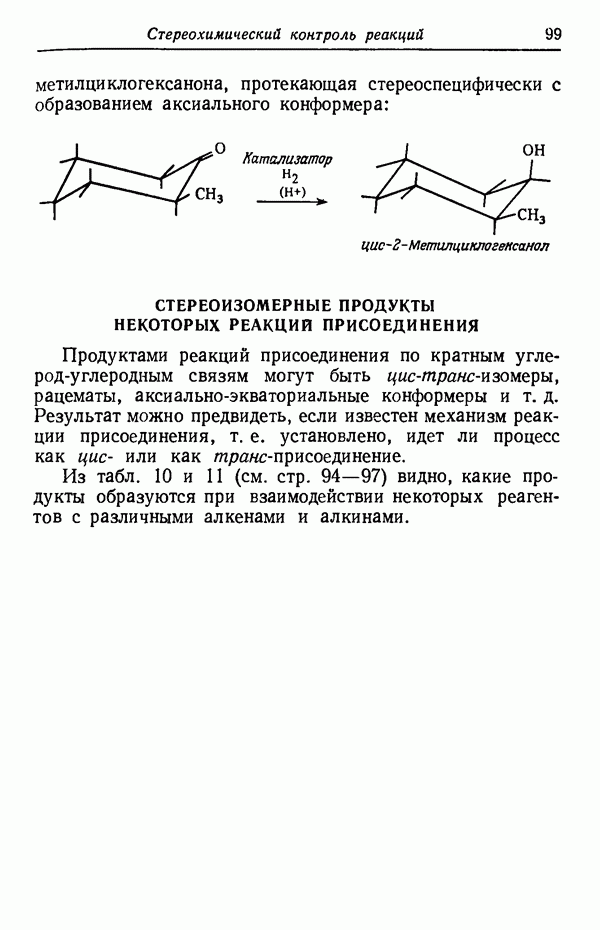
Сходство этой реакции и процесса сульфирования нафталина очевидно. Первоначально образуются изомеры в соответствии с кинетическим контролем. Как можно предвидеть, при достижении условий реакции, в которых осуществляется термодинамический контроль, будет происходить миграция сульфогруппы и образование более стабильного  -изомера. Однако не всегда термодинамический контроль изомерных продуктов приводит к желаемому изменению соотношения изомеров. Так, например, кинетически контролируемая реакция между циклопентадиеном и метилакрилатом дает 76%-ный выход эндо-изомера, но при нагревании реакционной смеси получается эквимолекулярная смесь изомеров.
-изомера. Однако не всегда термодинамический контроль изомерных продуктов приводит к желаемому изменению соотношения изомеров. Так, например, кинетически контролируемая реакция между циклопентадиеном и метилакрилатом дает 76%-ный выход эндо-изомера, но при нагревании реакционной смеси получается эквимолекулярная смесь изомеров.
(см. скан)
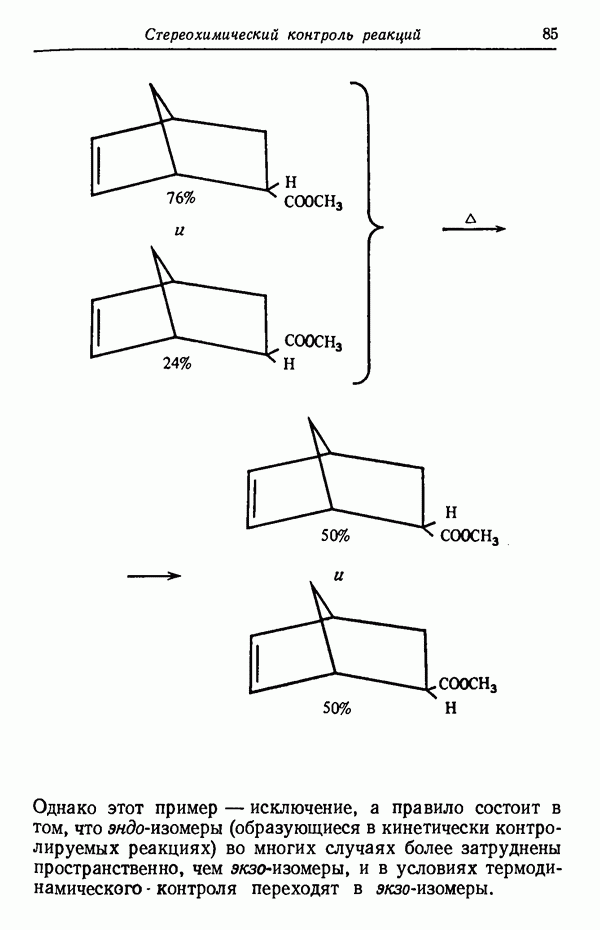
Однако этот пример — исключение, а правило состоит в том, что эндо-изомеры (образующиеся в кинетически контролируемых реакциях) во многих случаях более затруднены пространственно, чем экзо-изомеры, и в условиях термодинамического контроля переходят в экзо-изомеры.
(см. скан)
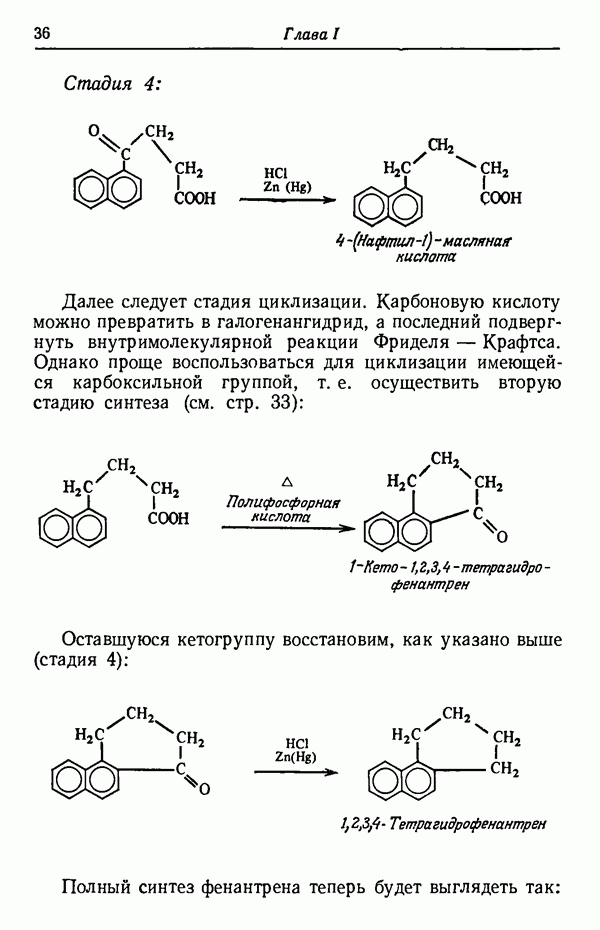
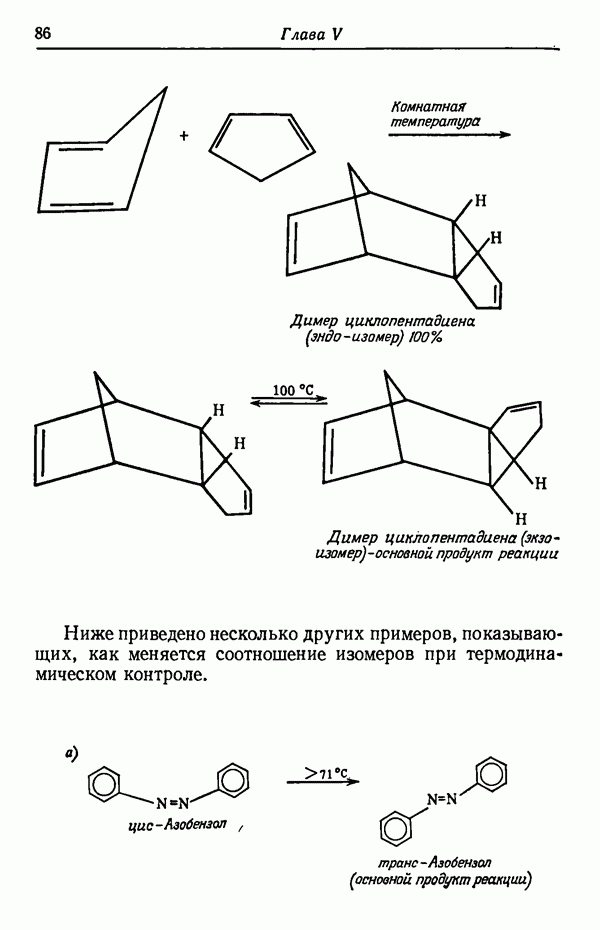
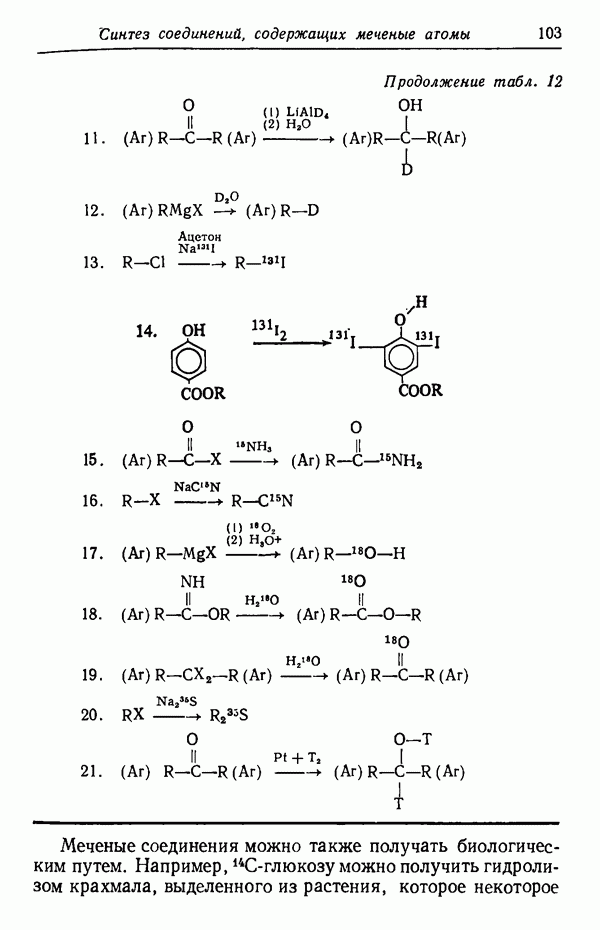
Ниже приведено несколько других примеров, показывающих, как меняется соотношение изомеров при термодинамическом контроле.
(см. скан)
(см. скан)
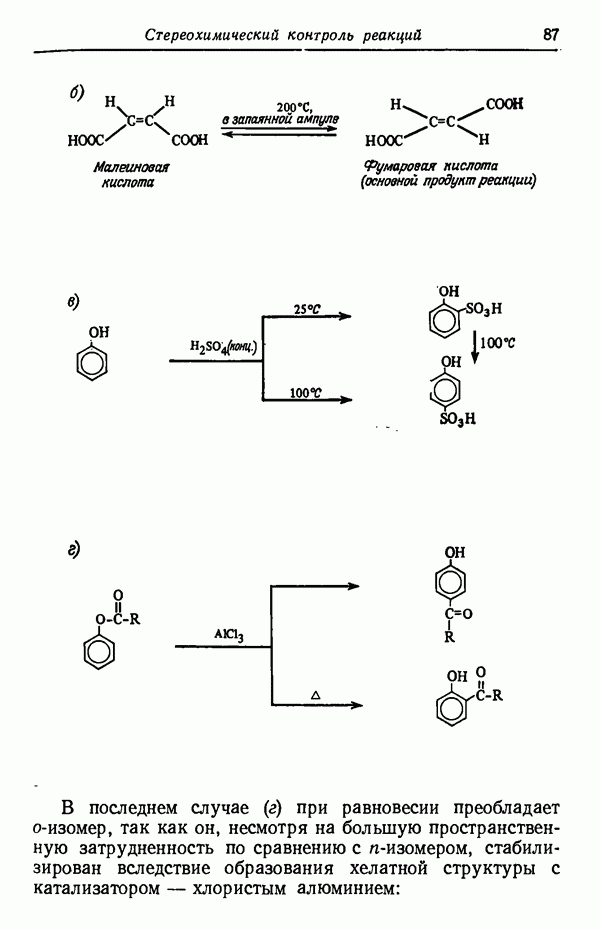
В последнем случае  при равновесии преобладает
при равновесии преобладает  -изомер, так как он, несмотря на большую пространственную затрудненность по сравнению с
-изомер, так как он, несмотря на большую пространственную затрудненность по сравнению с  -изомером, стабилизирован вследствие образования хелатной структуры с катализатором — хлористым алюминием:
-изомером, стабилизирован вследствие образования хелатной структуры с катализатором — хлористым алюминием:

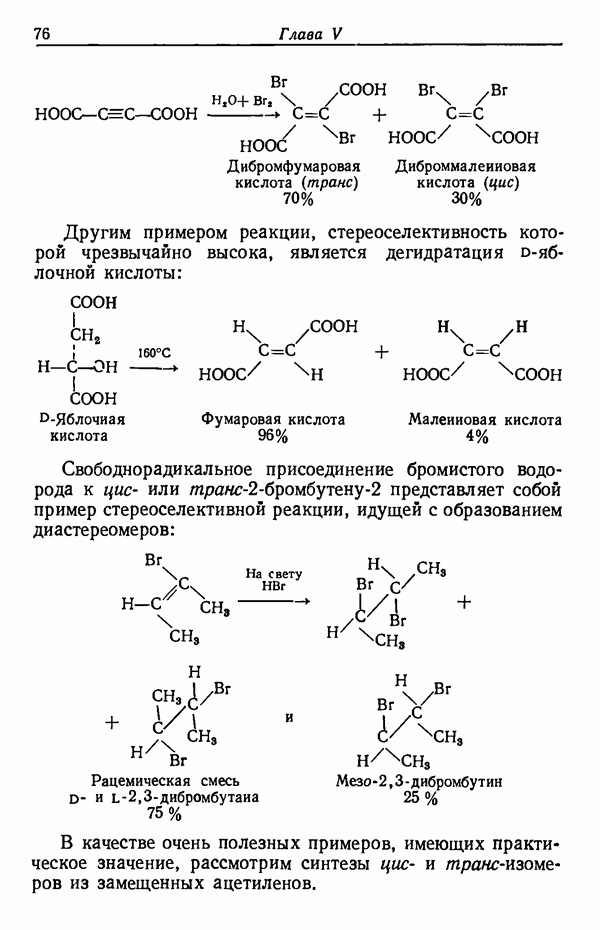
Для цис-транс-изомеров установлено, что обычно транс-изомеры более стабильны и образование их термодинамически более выгодно.
Под стабильностью понимается «термодинамическая стабильность», мерой которой является свободная энергия образования изомера, а не «термохимическая стабильность», мерой которой является теплота образования при постоянных температуре и давлении (изменение энтальпии). Таким образом, термохимическая стабильность отличается от термодинамической на величину изменения энтропии образования в соответствии с известным уравнением Гиббса

В большинстве случаев изомеры, обладающие более низкой энтальпией, имеют более низкую свободную энергию, поскольку обычно разница в энтропии между изомерами мала.
При рассмотрении превращений цис-транс-изомеров следует учитывать, что барьер вращения вокруг двойной углерод-углеродной связи составляет примерно 40—50 ккал/моль. Поскольку эта величина значительно меньше, чем значение энергии диссоциации насыщенной углерод-углеродной связи (74—84 ккал/моль), а также энергии связи  (98 ккал/моль), то равновесие цис-транс-превращения устанавливается значительно ниже температуры, необходимой для разрыва углерод-углеродных и углерод-водородных связей, т. е. раньше, чем наступает общее разложение молекулы.
(98 ккал/моль), то равновесие цис-транс-превращения устанавливается значительно ниже температуры, необходимой для разрыва углерод-углеродных и углерод-водородных связей, т. е. раньше, чем наступает общее разложение молекулы.
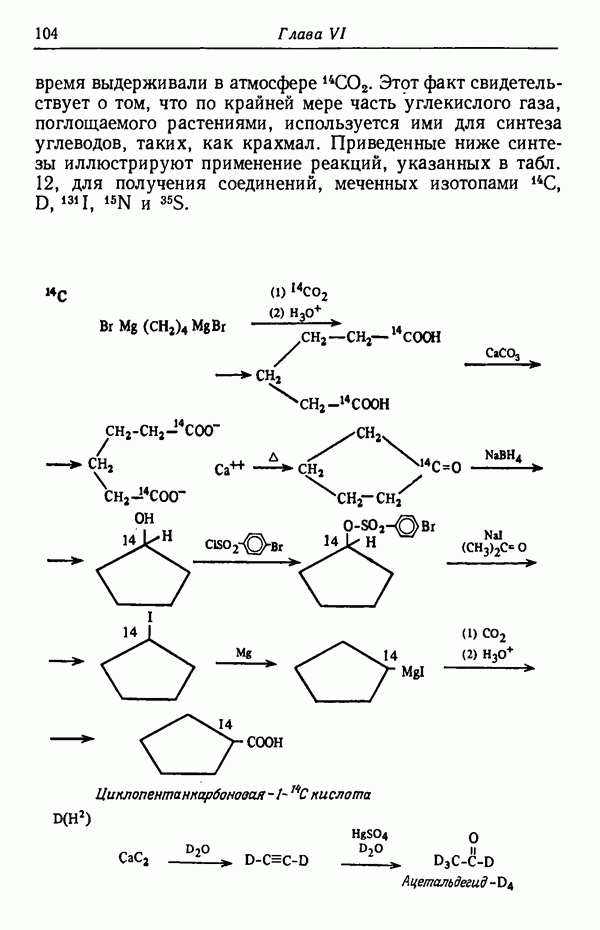
цис- и транс-Изомеры могут превращаться друг в друга не только в термических процессах, но также при действии кислот, оснований и свободнорадикальных катализаторов.
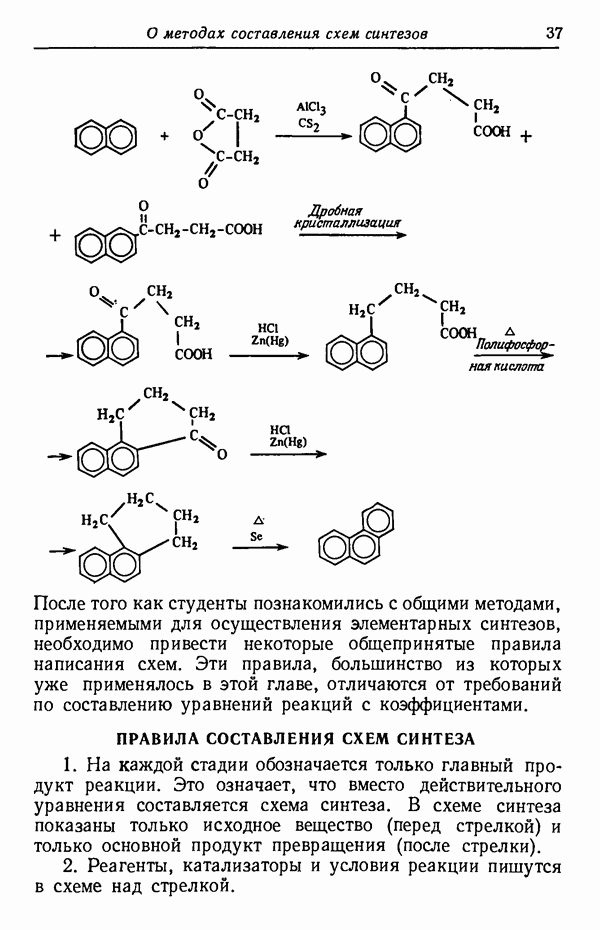
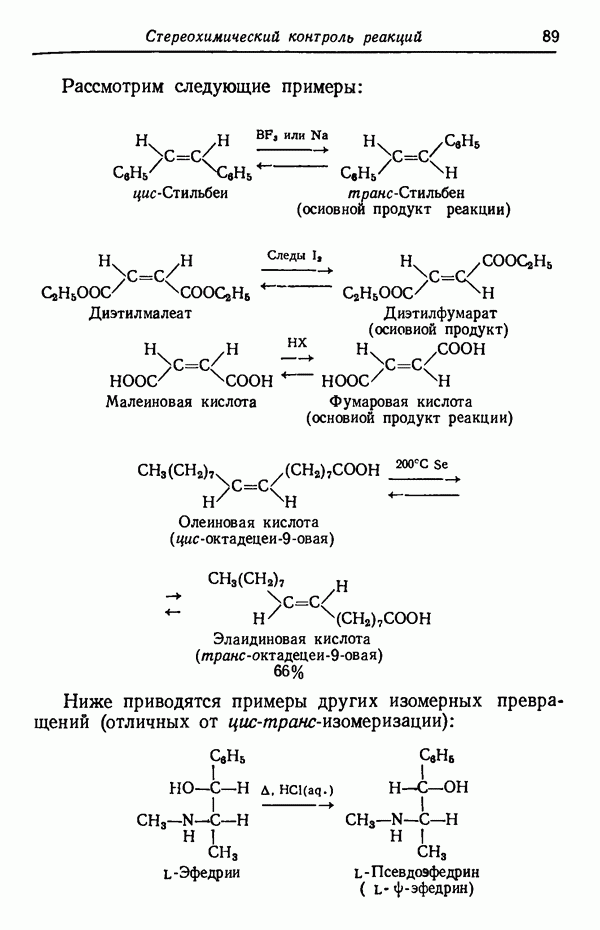
Рассмотрим следующие примеры:
(см. скан)
Ниже приводятся примеры других изомерных превращений (отличных от цис-транс-изомеризации):


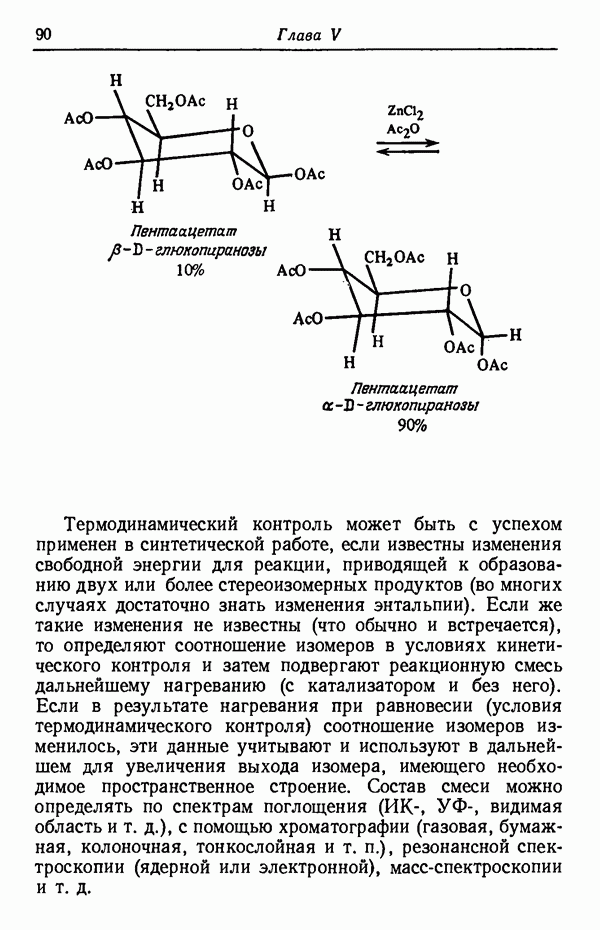
Термодинамический контроль может быть с успехом применен в синтетической работе, если известны изменения свободной энергии для реакции, приводящей к образованию двух или более стереоизомерных продуктов (во многих случаях достаточно знать изменения энтальпии). Если же такие изменения не известны (что обычно и встречается), то определяют соотношение изомеров в условиях кинетического контроля и затем подвергают реакционную смесь дальнейшему нагреванию (с катализатором и без него). Если в результате нагревания при равновесии (условия термодинамического контроля) соотношение изомеров изменилось, эти данные учитывают и используют в дальнейшем для увеличения выхода изомера, имеющего необходимое пространственное строение. Состав смеси можно определять по спектрам поглощения  видимая область и т. д.), с помощью хроматографии (газовая, бумажная, колоночная, тонкослойная и т. п.), резонансной спектроскопии (ядерной или электронной), масс-спектроскопии и
видимая область и т. д.), с помощью хроматографии (газовая, бумажная, колоночная, тонкослойная и т. п.), резонансной спектроскопии (ядерной или электронной), масс-спектроскопии и 
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Глава I. О МЕТОДАХ СОСТАВЛЕНИЯ СХЕМ МНОГОСТАДИЙНЫХ СИНТЕЗОВ
- СОСТАВЛЕНИЕ СХЕМЫ СИНТЕЗА, ИСХОДЯ ИЗ КОНЕЧНОГО СОЕДИНЕНИЯ
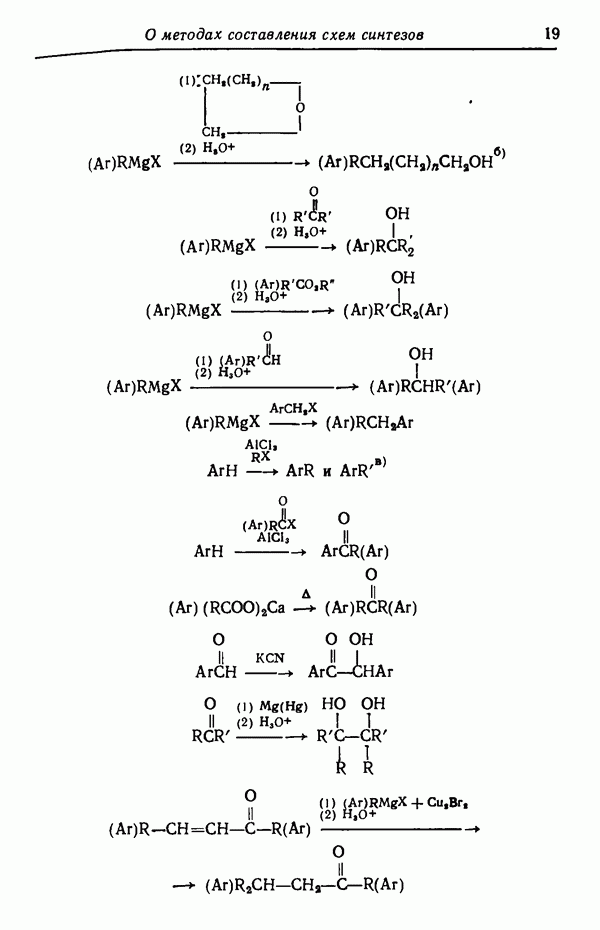
- НАРАЩИВАНИЕ УГЛЕРОДНОЙ ЦЕПИ
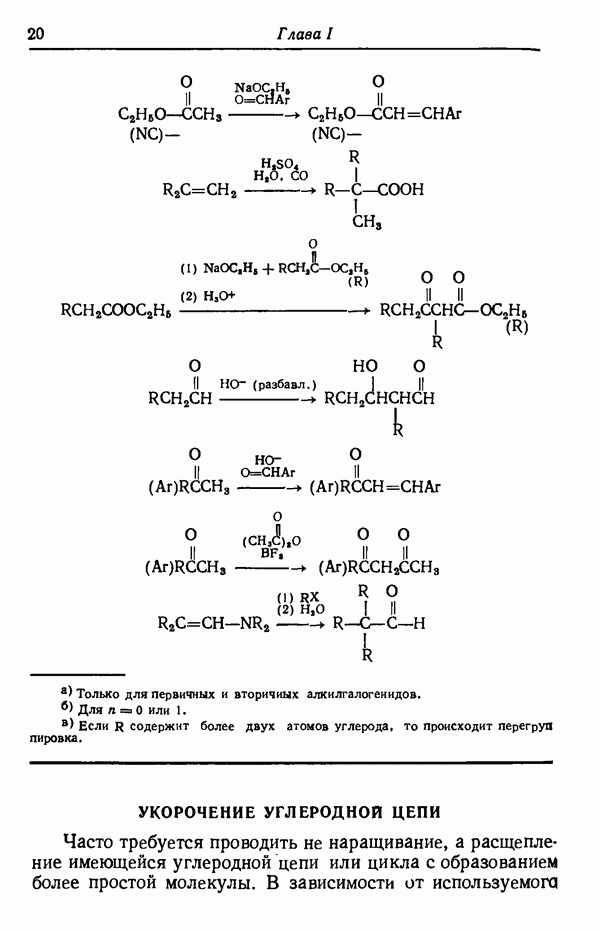
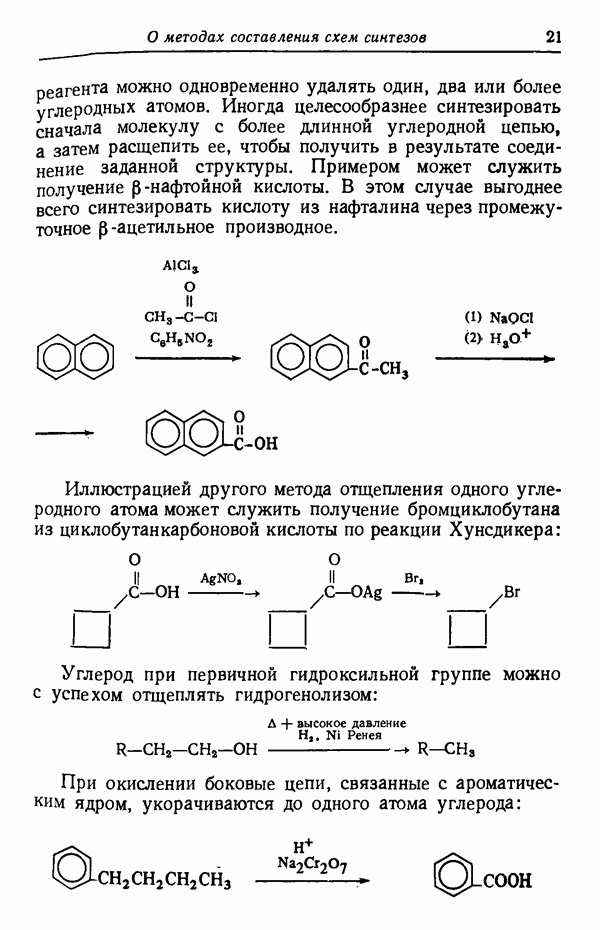
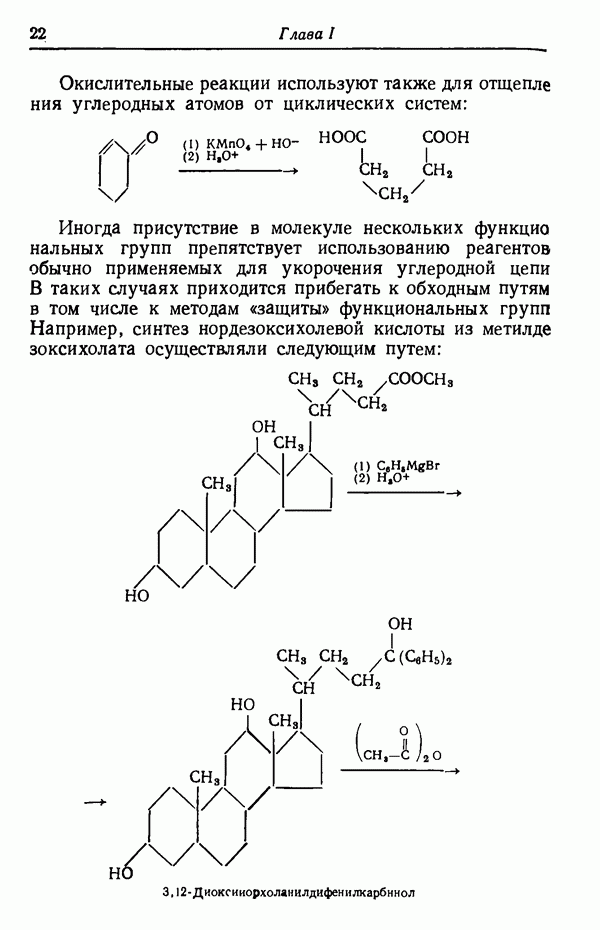
- УКОРОЧЕНИЕ УГЛЕРОДНОЙ ЦЕПИ
- РЕАКЦИИ ЦИКЛИЗАЦИИ
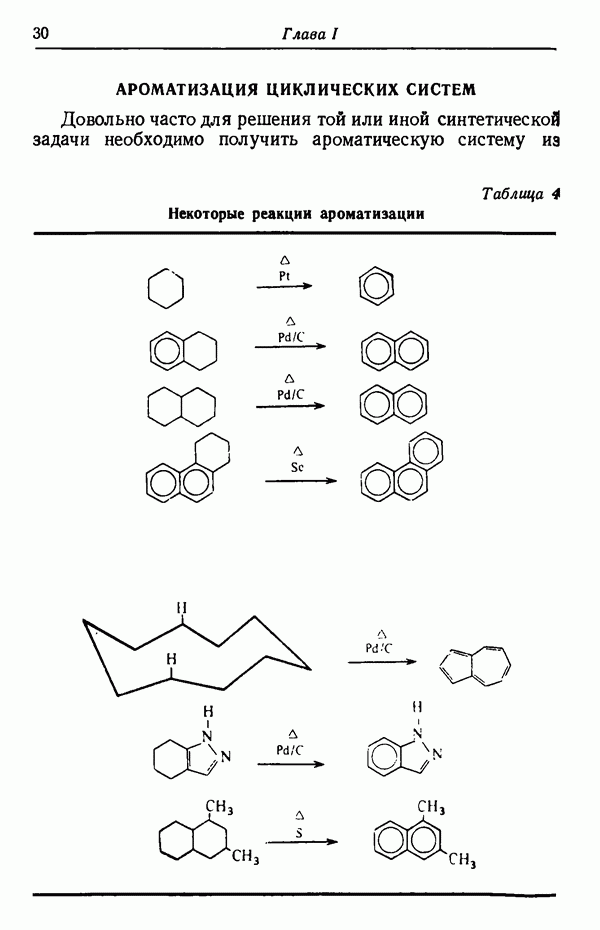
- АРОМАТИЗАЦИЯ ЦИКЛИЧЕСКИХ СИСТЕМ
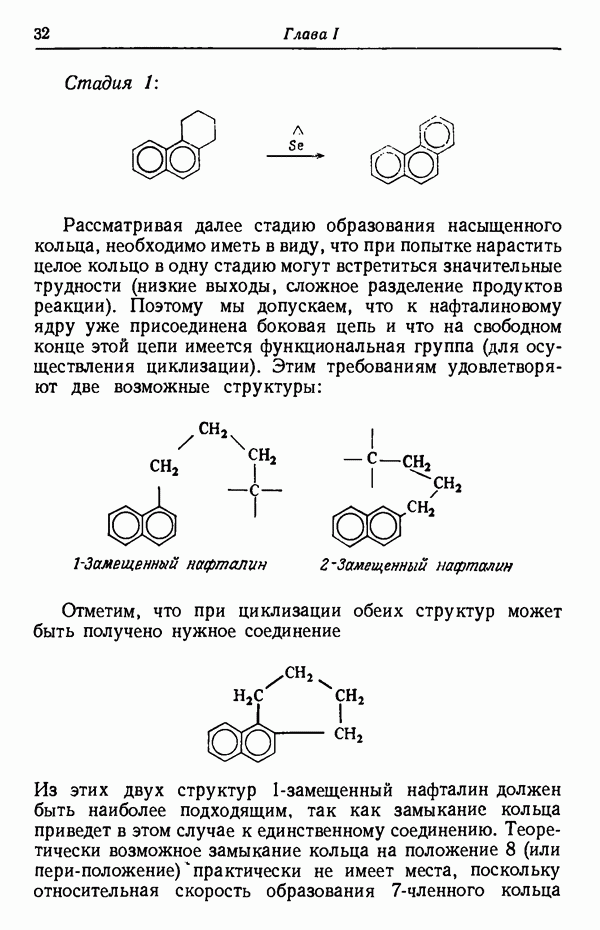
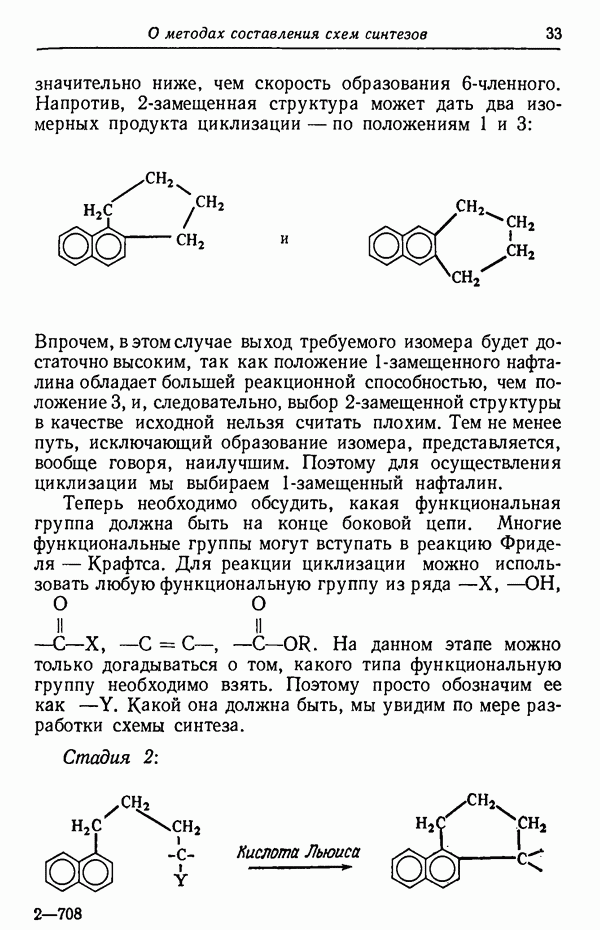
- СИНТЕЗ ФЕНАНТРЕНА ИЗ НАФТАЛИНА
- ПРАВИЛА СОСТАВЛЕНИЯ СХЕМ СИНТЕЗА
- Глава II. СИНТЕЗ НЕКОТОРЫХ НАИБОЛЕЕ ЧАСТО ИСПОЛЬЗУЕМЫХ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ
- РЕАКТИВЫ ГРИНЬЯРА
- СОЛИ ДИАЗОНИЯ
- ПОЛУЧЕНИЕ ВАЖНЕЙШИХ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ
- Глава III. ЗАЩИТА ФУНКЦИОНАЛЬНЫХ ГРУПП В ПРОЦЕССЕ СИНТЕЗА
- ГРУППЫ —О —Н
- ГРУППЫ -NH2 И — NHR
- ГРУППЫ C=O
- ГРУППЫ C-H
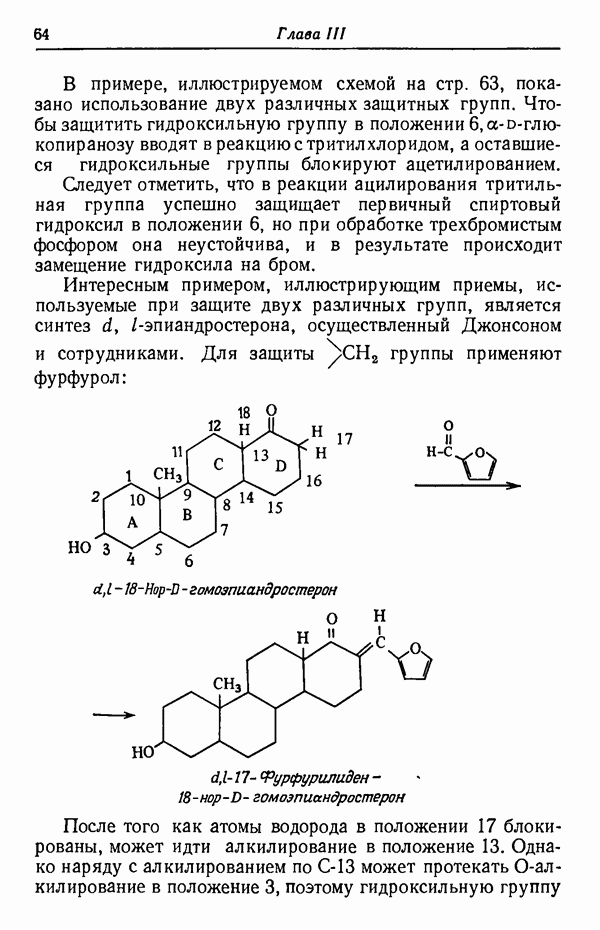
- ОДНОВРЕМЕННАЯ ЗАЩИТА НЕСКОЛЬКИХ ГРУПП
- Глава IV. СПЕЦИФИЧЕСКИЕ МЕТОДЫ, ПРИМЕНЯЕМЫЕ В АРОМАТИЧЕСКОМ РЯДУ
- ПОСЛЕДУЮЩИЕ ПРЕВРАЩЕНИЯ ЗАМЕСТИТЕЛЯ ПОСЛЕ ИСПОЛЬЗОВАНИЯ ЕГО ОРИЕНТИРУЮЩЕГО ВЛИЯНИЯ
- ЭЛИМИНИРОВАНИЕ ЗАМЕСТИТЕЛЯ ПОСЛЕ ИСПОЛЬЗОВАНИЯ ЕГО ОРИЕНТИРУЮЩЕГО ВЛИЯНИЯ
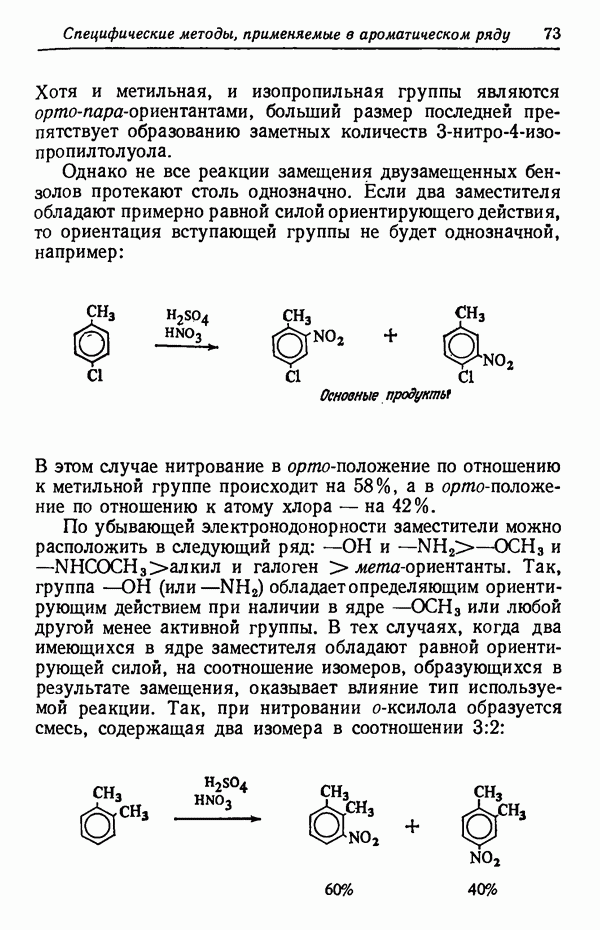
- ОРИЕНТАЦИЯ В ПОЛИЗАМЕЩЕННЫХ БЕНЗОЛАХ
- ВЛИЯНИЕ РАСТВОРИТЕЛЕЙ НА СООТНОШЕНИЕ ИЗОМЕРОВ
- Глава V. СТЕРЕОХИМИЧЕСКИЙ КОНТРОЛЬ РЕАКЦИЙ
- КИНЕТИЧЕСКИЙ КОНТРОЛЬ
- ТЕРМОДИНАМИЧЕСКИЙ КОНТРОЛЬ
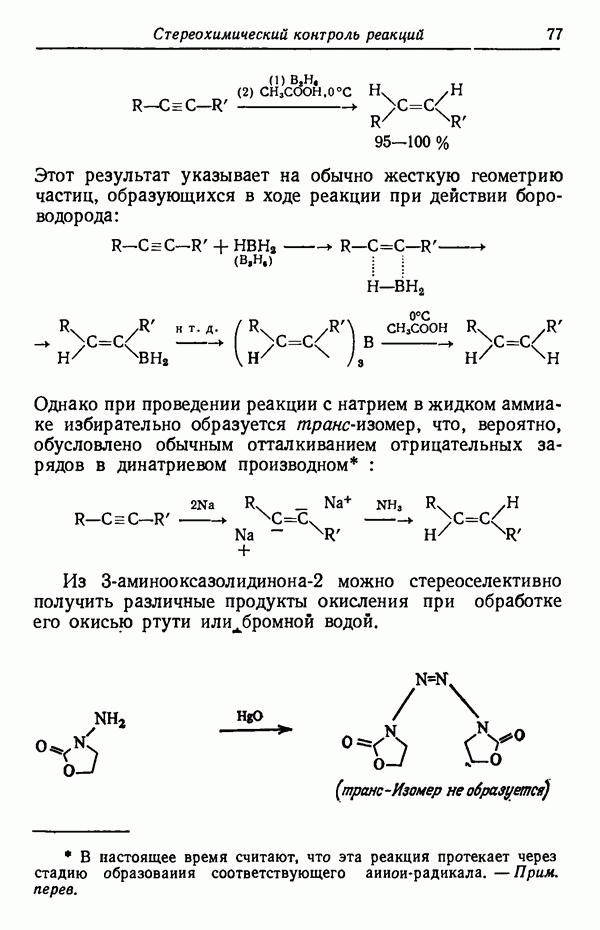
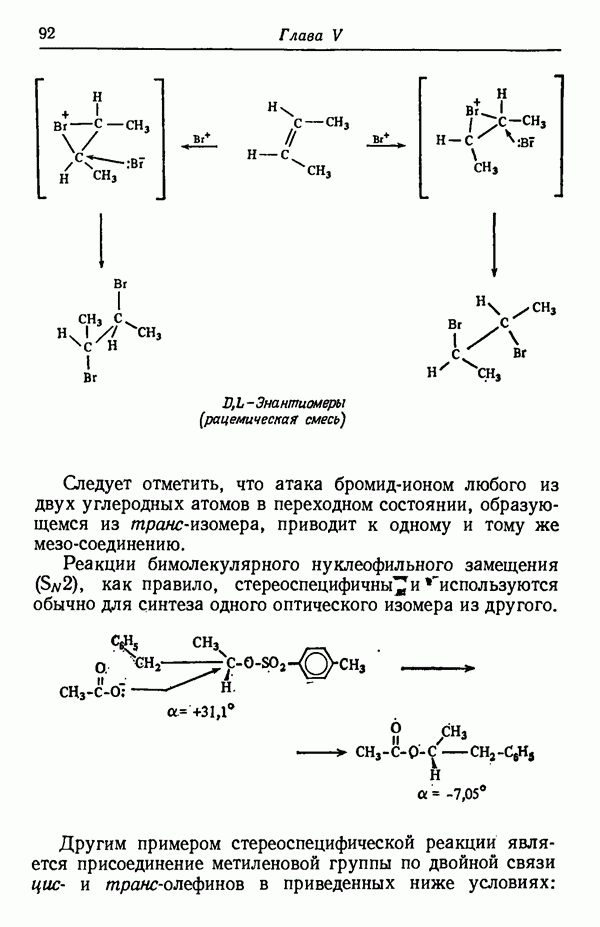
- СТЕРЕОСПЕЦИФИЧНОСТЬ
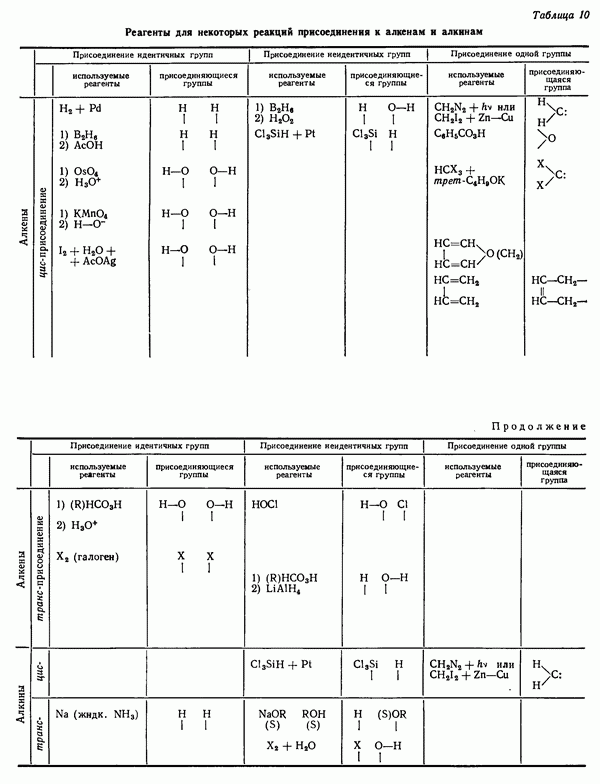
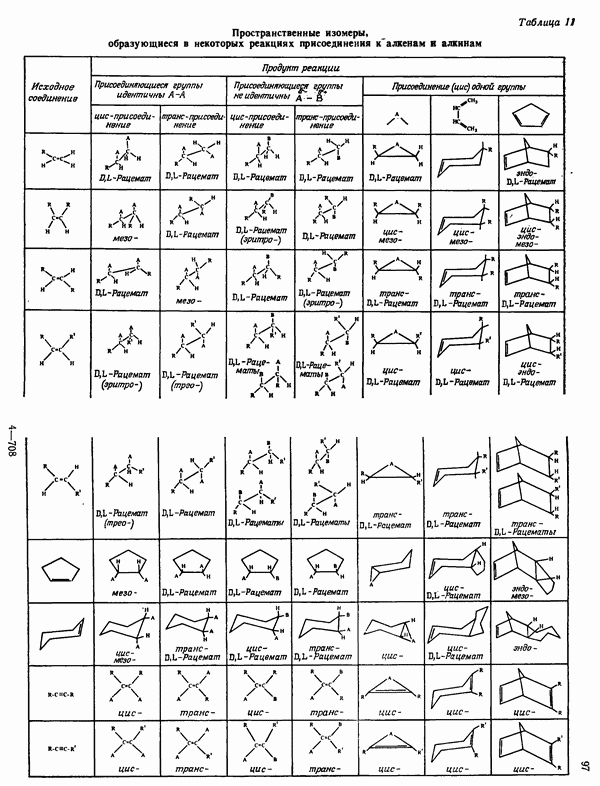
- СТЕРЕОИЗОМЕРНЫЕ ПРОДУКТЫ НЕКОТОРЫХ РЕАКЦИЙ ПРИСОЕДИНЕНИЯ
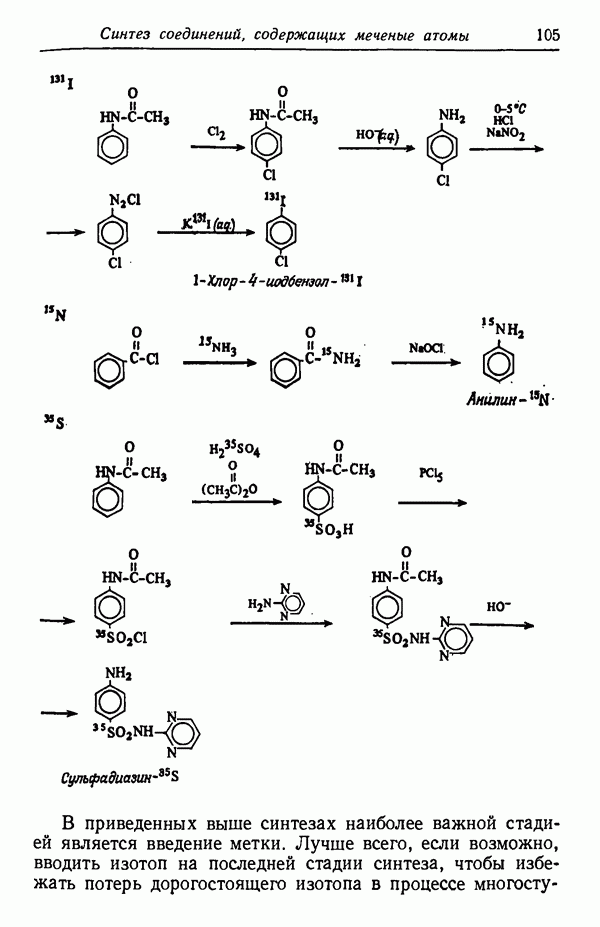
- Глава VI. СИНТЕЗ СОЕДИНЕНИЙ, СОДЕРЖАЩИХ МЕЧЕНЫЕ АТОМЫ (ИЗОТОПЫ)
- СИНТЕЗ МЕЧЕНЫХ СОЕДИНЕНИЙ
- МОЛЕКУЛЫ, СОДЕРЖАЩИЕ НЕСКОЛЬКО МЕТОК
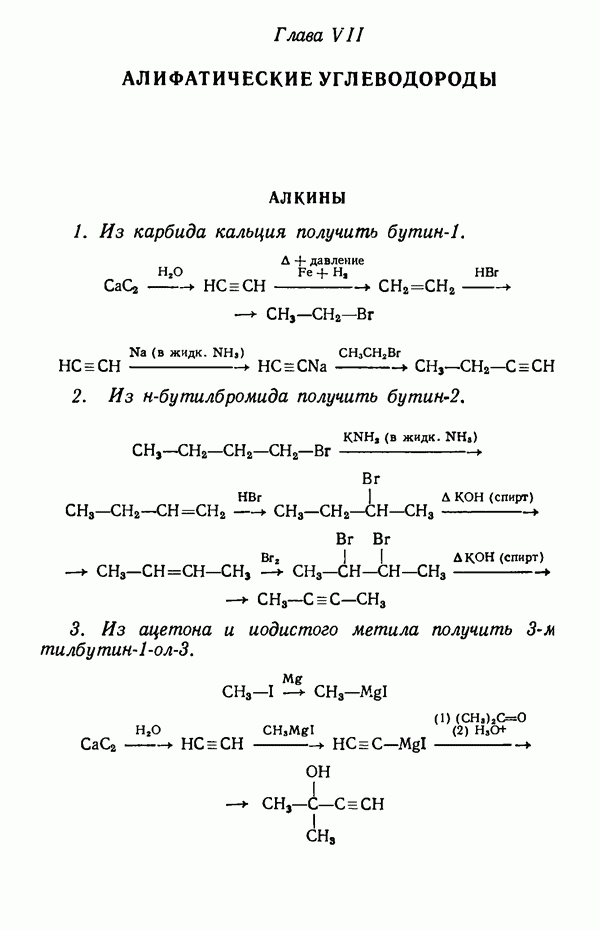
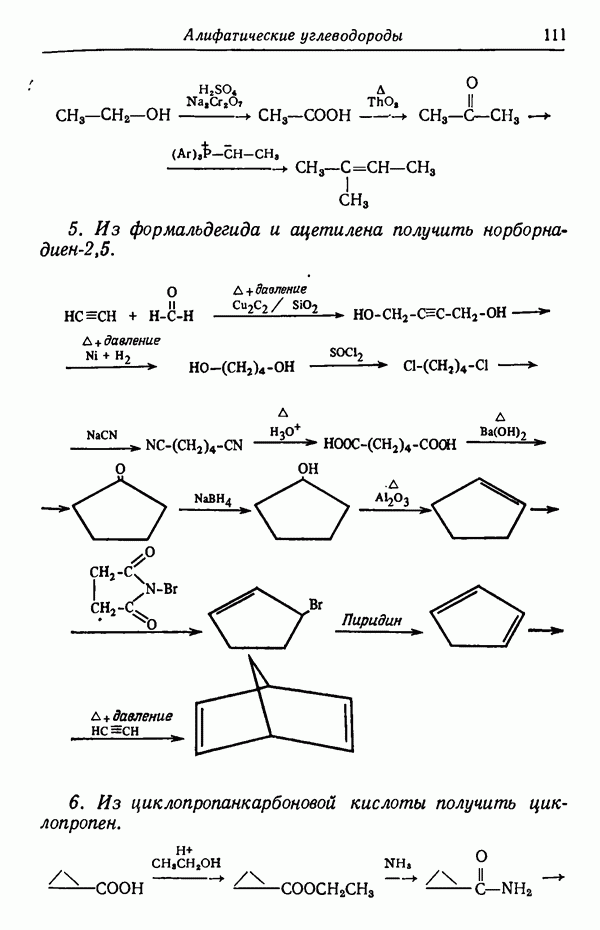
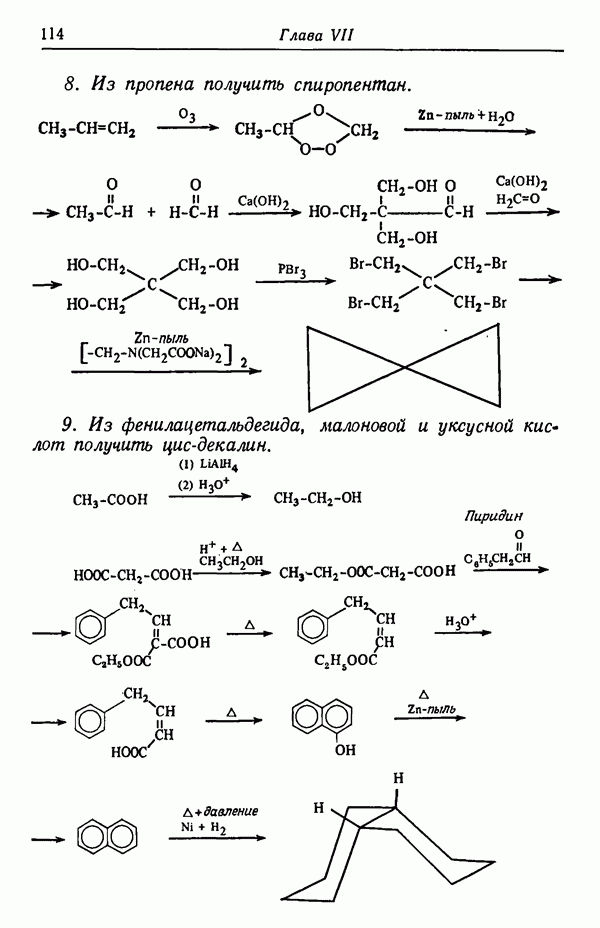
- Глава VII. АЛИФАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
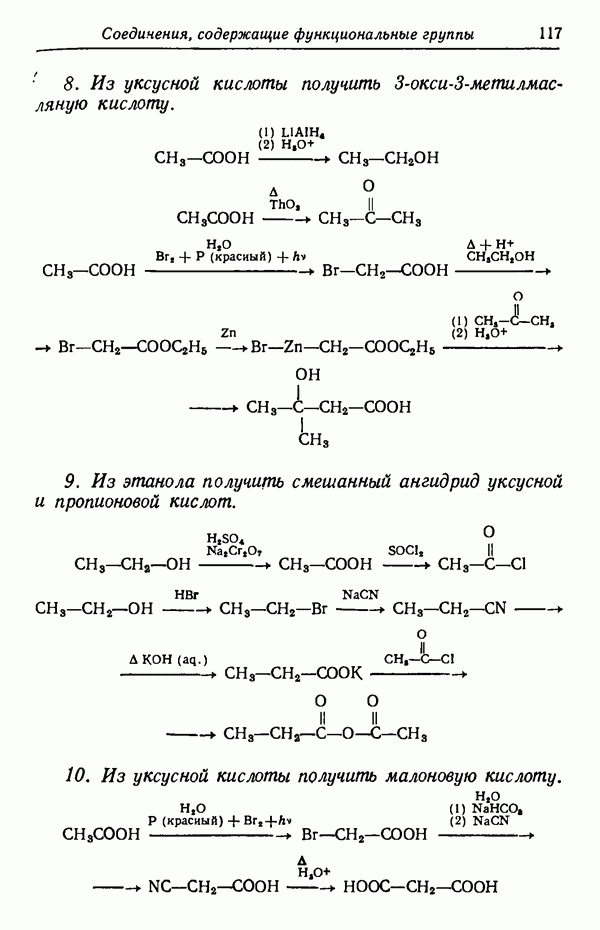
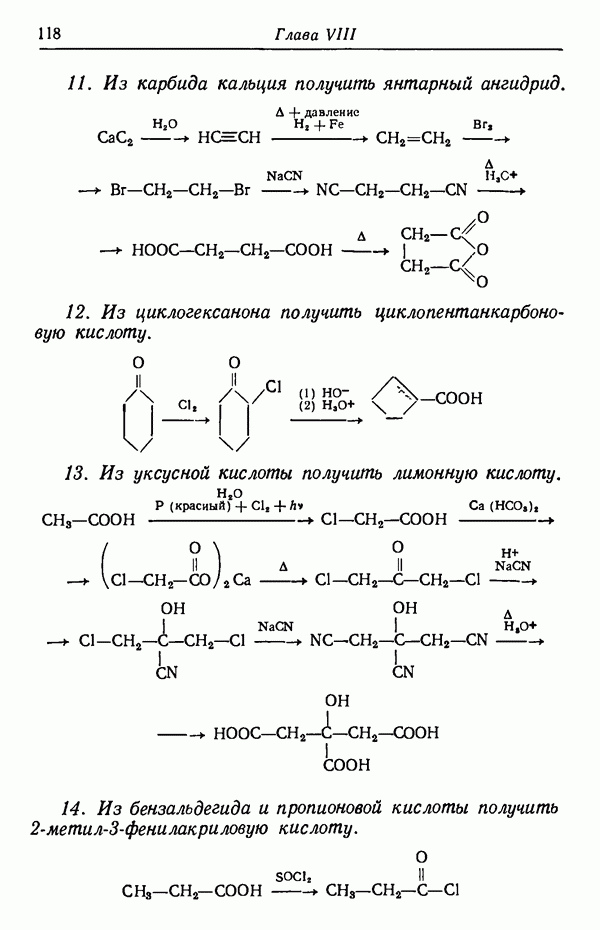
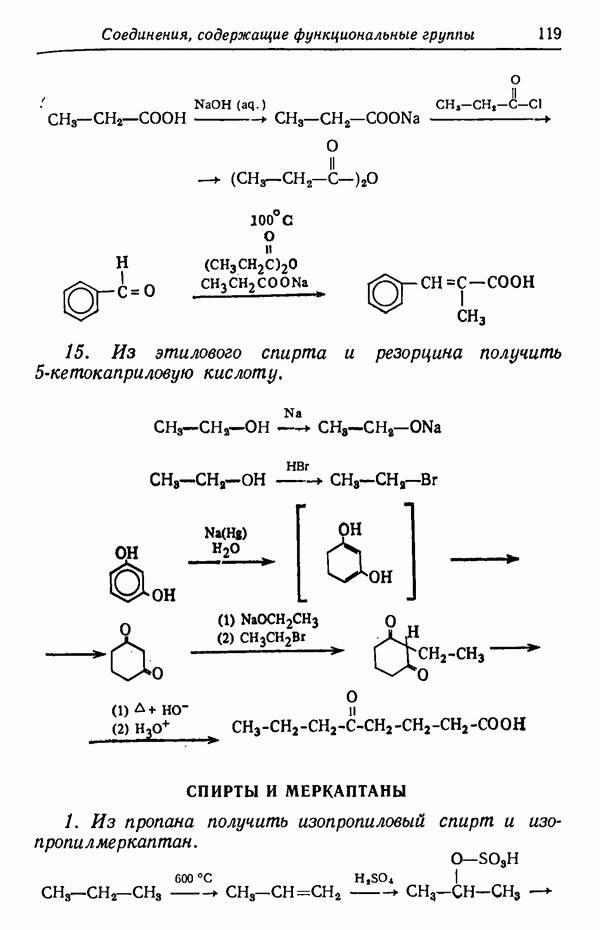
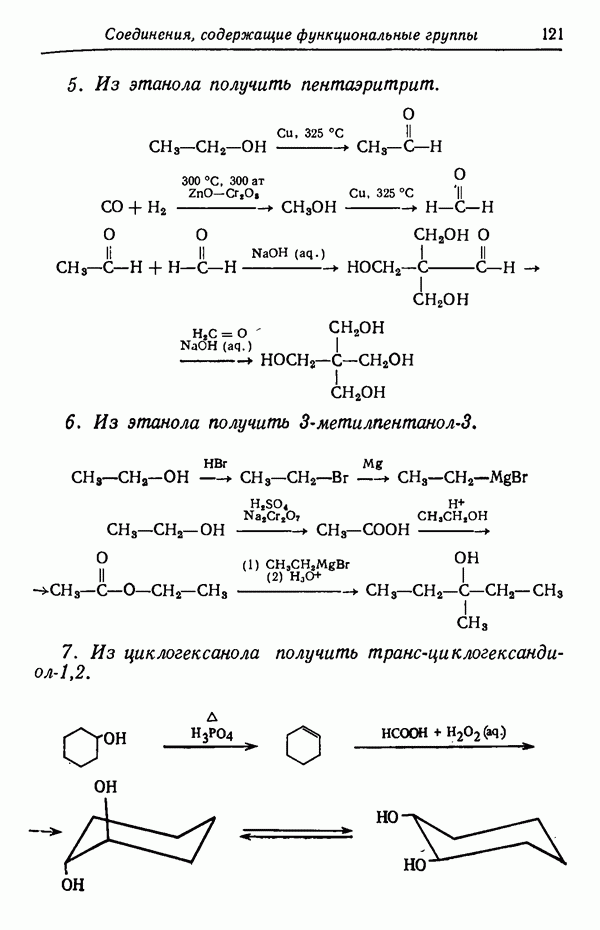
- Глава VIII. СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- Глава IX. ОДНОЯДЕРНЫЕ АРОМАТИЧЕСКИЕ СИСТЕМЫ