| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
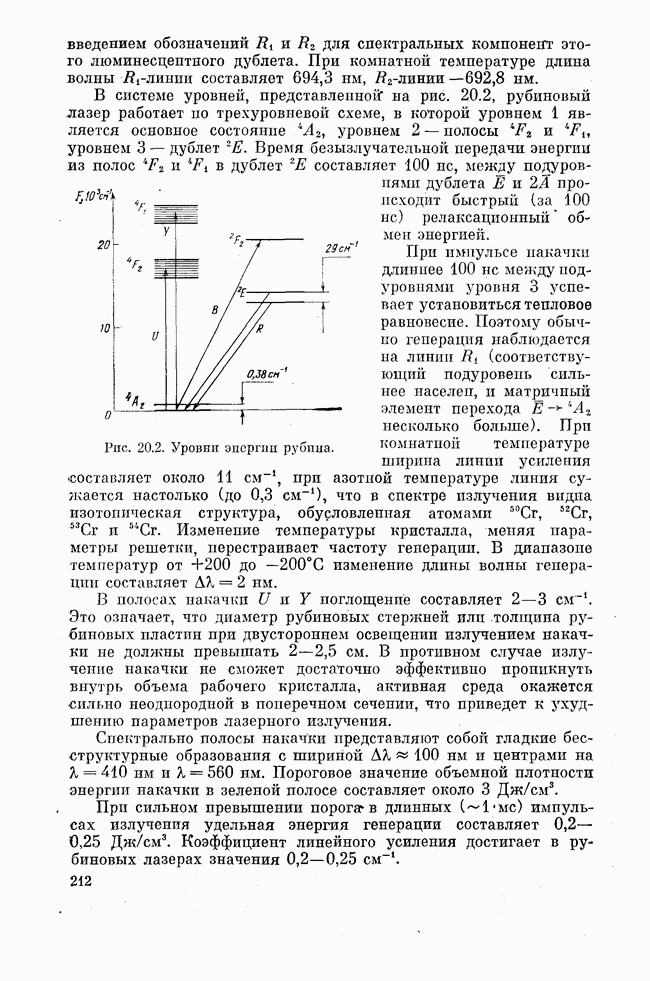
Лекция семнадцатая. ХИМИЧЕСКИЕ ЛАЗЕРЫ
Экзотермические реакции и колебательная энергия. Колебательно-поступательная, колебательно-колебательная и вращательно-поступательная релаксация. Полная и частичная инверсии. Скорость химической накачай. Цепные реакции. К. п. д. инициирования и химический к. п. д. Химические лазеры импульсного и непрерывного действия. Параметры лазеров. Йодный фотодиссоциационный лазер.
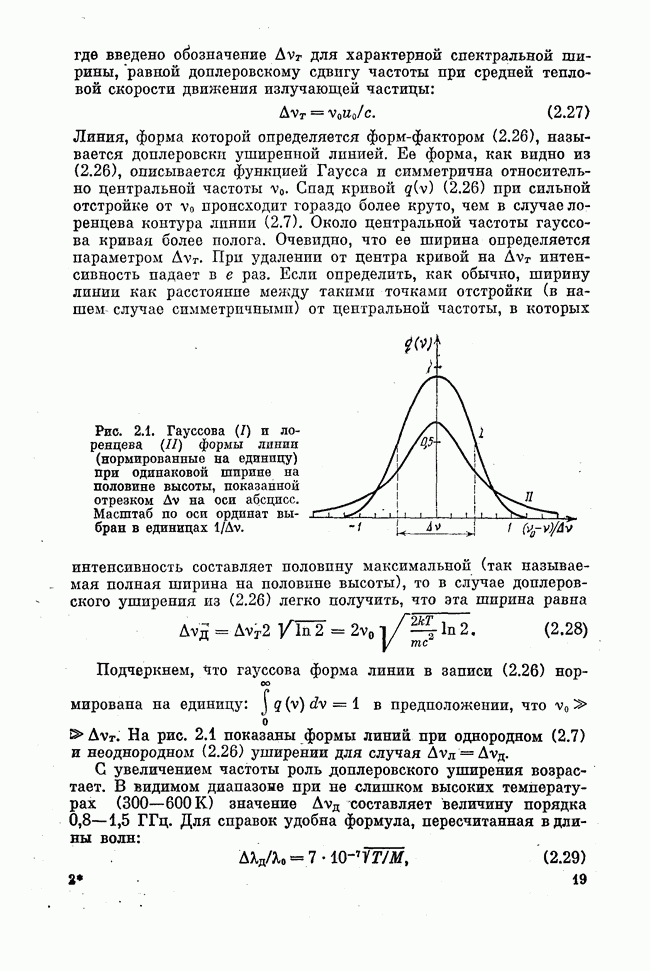
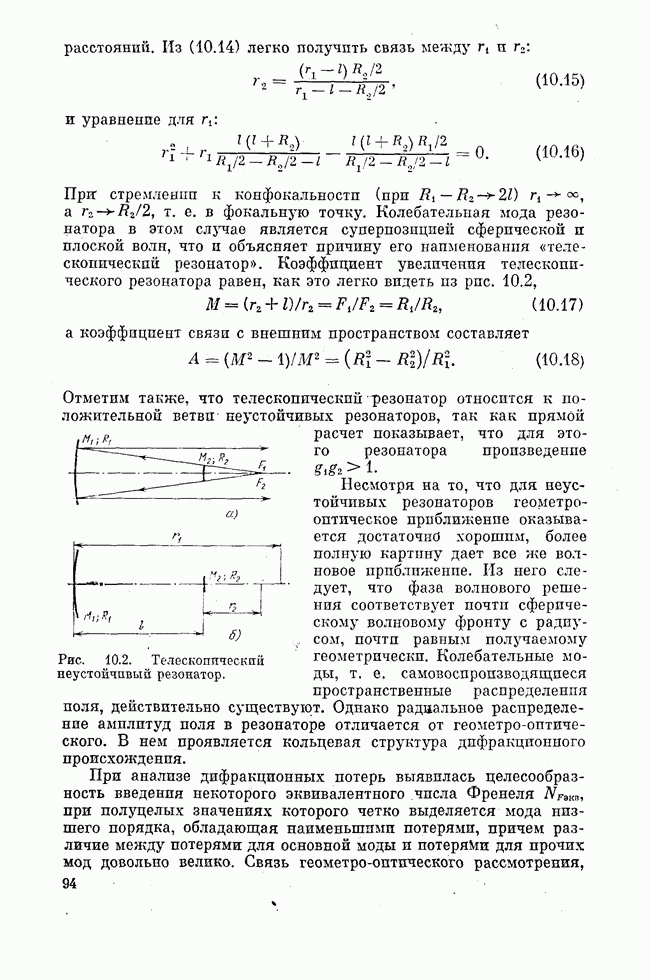
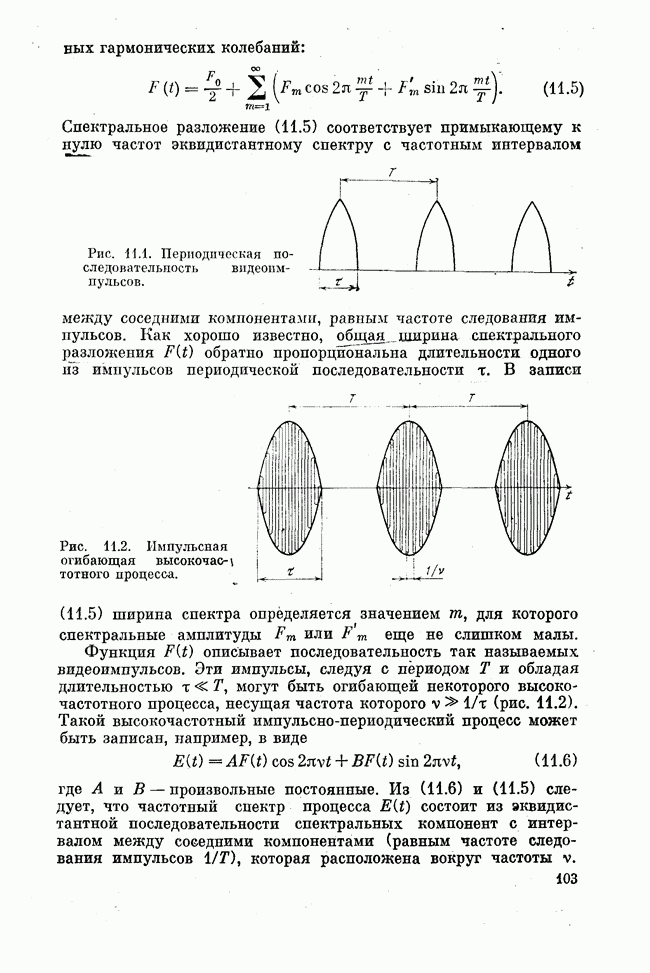
Итак, лазеры, инверсия населенностей в активной среде которых создается за счет неравновесного распределения среди продуктов химической реакции энергии, выделившейся в процессе реакции, непосредственно в реакционном объеме, называются химическими лазерами. Другими словами, излучение химического лазера есть прямой непосредственный результат химической реакции, а не результат какого-то побочного действия химической реакции, например нагрева или взрывообразного роста давления, как в случае газодинамических лазеров с исходной химической энергетикой (стационарное или взрывное сгорание топлива).
Излучение химического лазера является эффектом, обратным фотохимическому эффекту, в котором химическая реакция возникает как прямой, непосредственный результат поглощения атомом или молекулой фотона, а не как результат какого-то побочного действия света, например нагрева реагентов при поглощении
света. Фотохимическое стимулирование осуществляется для проведения эндотермических реакций. Очевидно, что для создания химических лазеров могут привлекаться только экзотермические химические реакции.
Интерес к химическим лазерам обусловлен тем, что во многих экзотермических химических реакциях выделяется большая энергия на единицу массы реагентов. Примеры хорошо известны — органические топлива, пороха и т. п.
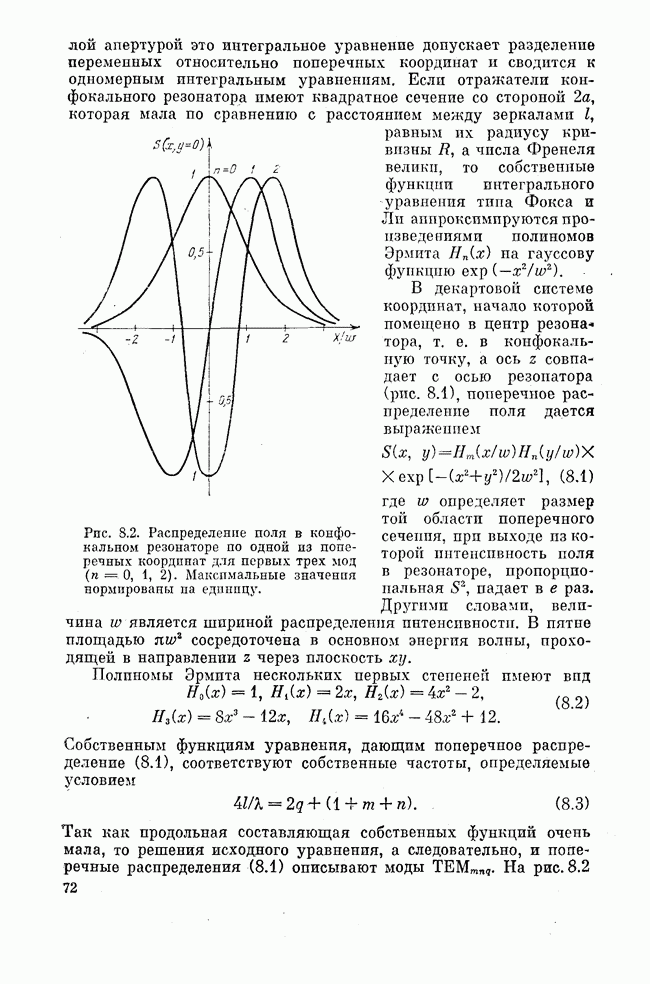
Анализируя реакции, проводимые в газовой фазе, легко видеть, что колебательные степени свободы молекул являются хорошим аккумулятором энергии, выделившейся при химической реакции. Во-первых, при молекулярных химических реакциях перестраиваются химические связи молекул, рвутся одни связи, создаются новые связи, на сохраняющихся связях происходят замещения одних связываемых ядер другими и т. д. Колебательные моды молекул локализуются, как мы знаем, по связям в структуре молекул. Следовательно, энергия высвобождается при экзотермической реакции через перестраиваемую в ходе реакции химическую связь и локализуется в виде колебательной энергии молекул. Во-вторых, в газовой фазе колебательная (или, говоря более точно, колебательно-поступательная) релаксация происходит относительно медленно.
В силу изложенного химические лазеры работают, главным образом, на переходах между колебательными уровнями молекул. Важно знать поэтому, как химическая энергия распределяется между колебательными уровнями молекул в результате реакции и в каких реакциях и у каких молекул возможно инверсное распределение этой энергии.
Простейший случай можно представить реакцией замещения
 (17.1)
(17.1)
Ряд элементарных реакций типа (17.1) подробно изучен. Так, спектроскопическими методами найдено, что в реакции

отношение колебательной энергии к полной энергии, выделившейся при реакции, составляет  . При этом относительные населенности на уровнях
. При этом относительные населенности на уровнях  составляют соответственно 0,31, 1,0, 0,48. Примерно такова же ситуация в реакциях
составляют соответственно 0,31, 1,0, 0,48. Примерно такова же ситуация в реакциях  и т. д. Как правило, во всех реакциях образования галогеноводородов по схеме (17.1) в результате экзотермического замещения возникает инверсия населенностей.
и т. д. Как правило, во всех реакциях образования галогеноводородов по схеме (17.1) в результате экзотермического замещения возникает инверсия населенностей.
Полная колебательная инверсия

возникшая в акте перестройки внутримолекулярной связи, может существовать только в течение некоторого определенного конечного
времени. Релаксационные процессы устремляют неравновесную систему к равновесию, которому отвечает больцмановское распределение населенностей с температурой, соответствующей энергии, выделившейся при реакции. Как мы знаем, молекула обладает колебательными, вращательными и поступательными степенями свободы. Термализация энерговыделения экзотермической реакции предполагает равнораспределение этой энергии по всем степеням свободы молекулы. Другими словами, в равновесии все виды движения молекулы характеризуются одной и той же температурой Т. Физическим процессом, приводящим к установлению этого равновесия, являются межмолекулярные газокинетические столкновения. Мы знаем, что при столкновениях эффективен квазирезонансный обмен энергией. При колебательно-поступательной (V — Т) релаксации, когда

условия квазирезонансности сильно нарушены. Поэтому для  -релаксации требуется много, иногда много сотен или тысяч, газокинетических столкновений. Именно поэтому время
-релаксации требуется много, иногда много сотен или тысяч, газокинетических столкновений. Именно поэтому время  -релаксации велико.
-релаксации велико.
Вместе с тем при столкновениях молекул возможен обмен квантами колебательной энергии  между колебательными уровнями с различными значениями колебательного квантового числа F. Если ангармонизм молекулы мал, то дефицит энергии при такой передаче (см. (15.7)) также мал:
между колебательными уровнями с различными значениями колебательного квантового числа F. Если ангармонизм молекулы мал, то дефицит энергии при такой передаче (см. (15.7)) также мал:

я колебательно-колебательный обмен (колебательно-колебательная  ) релаксация) происходит практически со скоростью газокинетических столкновений. При V —
) релаксация) происходит практически со скоростью газокинетических столкновений. При V —  -релаксации сохраняется общее число колебательных квантов, т. е. энергия, полученная системой молекул в результате (в нашем случае) химической реакции в виде колебательной энергии, сохраняется как колебательная энергия. Изменяется распределение энергии по уровням. Если ангармонизм молекул мал, получающееся в процессе F —
-релаксации сохраняется общее число колебательных квантов, т. е. энергия, полученная системой молекул в результате (в нашем случае) химической реакции в виде колебательной энергии, сохраняется как колебательная энергия. Изменяется распределение энергии по уровням. Если ангармонизм молекул мал, получающееся в процессе F —  -релаксации распределение близко к больцмановскому с некоторой эффективной колебательной температурой
-релаксации распределение близко к больцмановскому с некоторой эффективной колебательной температурой  . Очевидно, что при этом полная колебательная инверсия (17.3) исчезает.
. Очевидно, что при этом полная колебательная инверсия (17.3) исчезает.
За время  -релаксации происходит и вращательно-поступательная (R — Т) релаксация, приводящая в равновесие вращательные и поступательные степени свободы, характеризуемые в результате некоторой единой температурой Т. Быстрое установление равновесия во вращательно-поступательном резервуаре обусловлено квазирезонансностью обмена энергией при соответствующих столкновениях в силу малости вращательной энергии:
-релаксации происходит и вращательно-поступательная (R — Т) релаксация, приводящая в равновесие вращательные и поступательные степени свободы, характеризуемые в результате некоторой единой температурой Т. Быстрое установление равновесия во вращательно-поступательном резервуаре обусловлено квазирезонансностью обмена энергией при соответствующих столкновениях в силу малости вращательной энергии:

Сечения  и
и  -релаксаций близки к газокинетическому
-релаксаций близки к газокинетическому
сечению. Как правило,  -релаксация идет несколько быстрее
-релаксация идет несколько быстрее  -релаксации. Но
-релаксации. Но  -релаксация, как уже неоднократно подчеркивалось, идет много медленнее, поэтому в течение длительного времени, равного многим (сотням или тысячам) интервалам между газокинетическими столкновениями,
-релаксация, как уже неоднократно подчеркивалось, идет много медленнее, поэтому в течение длительного времени, равного многим (сотням или тысячам) интервалам между газокинетическими столкновениями,  . Если выбраны такие реакции типа (17.1), для которых экзотермичность реализуется в преимущественно колебательном энерговыделении, то тогда в течение относительно длительного времени
. Если выбраны такие реакции типа (17.1), для которых экзотермичность реализуется в преимущественно колебательном энерговыделении, то тогда в течение относительно длительного времени

В этой ситуации возможна так называемая частичная инверсия, условие которой для уровня  расположенного выше уровня
расположенного выше уровня  записывается в виде
записывается в виде

Это условие выполняется, в отличие от условия полной инверсии (17.3), только для некоторых 
Рассмотрим этот вопрос несколько подробнее. Больцмановское распределение по колебательно-вращательным уровням при квазиравновесных колебательной и вращательной температурах  и
и  принимает вид
принимает вид

где энергия  вращательного подуровня J колебательного уровня F принята равной
вращательного подуровня J колебательного уровня F принята равной
 (17.10)
(17.10)
(что справедливо для двухатомных или линейных молекул), а  и
и  обозначают соответственно колебательную и вращательную статистические суммы. Условие частичной инверсии выполняется в случае, если
обозначают соответственно колебательную и вращательную статистические суммы. Условие частичной инверсии выполняется в случае, если

При этом правила отбора для колебательно-вращательных переходов  позволяют упростить (17.11) с помощью соотношений
позволяют упростить (17.11) с помощью соотношений  :
:

Иначе говоря, частичная инверсия реализуется только в Р-ветви (значение  для вращательного подуровня верхнего лазерного уровня на единицу меньше, чем для вращательного подуровня нижнего уровня) и для значений J нижнего уровня, определяемых
для вращательного подуровня верхнего лазерного уровня на единицу меньше, чем для вращательного подуровня нижнего уровня) и для значений J нижнего уровня, определяемых
запасом колебательной энергии, т. е. значением 
 (17.13)
(17.13)
В то же время при полной колебательной инверсии возможно усиление на всех трех ветвях: Р, Q и R.
Возможность существования частичной инверсии является; важной особенностью молекулярных систем. В колебательно-вращательных спектрах инверсия может осуществляться не только за счет различия в  населенностях колебательных уровней. Существенное значение имеет распределение населенностей в колебательном уровне по вращательным подуровням. Для переходов Р-ветви, идущих в поглощении от
населенностях колебательных уровней. Существенное значение имеет распределение населенностей в колебательном уровне по вращательным подуровням. Для переходов Р-ветви, идущих в поглощении от  нижнего к
нижнего к  верхнего колебательного уровня, а в излучении от
верхнего колебательного уровня, а в излучении от  верхнего к J нижнего, реализуется своебразная ситуация.
верхнего к J нижнего, реализуется своебразная ситуация.
Представим себе для простоты рассуждений такую картину: населенности двух колебательных уровней  и
и  равны друг другу. Полной инверсии нет. Распределения населенностей по подуровням в этих двух колебательных уровнях полностью тождественны друг другу и являются больцмановскими. Подуровень
равны друг другу. Полной инверсии нет. Распределения населенностей по подуровням в этих двух колебательных уровнях полностью тождественны друг другу и являются больцмановскими. Подуровень  населен сильнее, чем J. В свою очередь, J населен сильнее, чем
населен сильнее, чем J. В свою очередь, J населен сильнее, чем  и т. д. При равенстве колебательных населенностей уровней
и т. д. При равенстве колебательных населенностей уровней  а
а  их подуровни
их подуровни  населены одинаково. Аналогично, одинаково населены подуровни
населены одинаково. Аналогично, одинаково населены подуровни  и т. д. Следовательно, педуровень
и т. д. Следовательно, педуровень  населен сильнее, чем подуровень
населен сильнее, чем подуровень  Более низко расположенный подуровень верхнего уровня является нижним на шкале вращательных энергий, так как на своем колебательном уровне его вращательная энергия меньше. Но он расположен выше на шкале колебательных энергий, и поэтому для колебательно-вращательного перехода в Р-ветви возможна инверсия, названная выше частичной. Обычно обозначают символом J подуровень нижнего колебательного уровня. При отсутствии инверсии колебательных населенностей перехода
Более низко расположенный подуровень верхнего уровня является нижним на шкале вращательных энергий, так как на своем колебательном уровне его вращательная энергия меньше. Но он расположен выше на шкале колебательных энергий, и поэтому для колебательно-вращательного перехода в Р-ветви возможна инверсия, названная выше частичной. Обычно обозначают символом J подуровень нижнего колебательного уровня. При отсутствии инверсии колебательных населенностей перехода  частичная инверсия может осуществляться только для переходов
частичная инверсия может осуществляться только для переходов  , т. е. в Р-ветви для значений
, т. е. в Р-ветви для значений  даваемых формулой (17.13).
даваемых формулой (17.13).
Итак, пока не прошла  -релаксация, существует полная колебательная инверсия, обусловленная характером распределеления энергии элементарного экзотермического химического акта по колебательным состояниям молекул продуктов реакции. Пока не прошла
-релаксация, существует полная колебательная инверсия, обусловленная характером распределеления энергии элементарного экзотермического химического акта по колебательным состояниям молекул продуктов реакции. Пока не прошла  -релаксация, существует частичная вращательная инверсия в Р-ветви. Различать эти два вида инверсии легко по спектру возможных частот генерации.
-релаксация, существует частичная вращательная инверсия в Р-ветви. Различать эти два вида инверсии легко по спектру возможных частот генерации.
По достижении инверсии все свойства химических лазеров полностью совпадают со свойствами всех остальных молекулярных газовых лазеров, что, впрочем, справедливо и при любом другом способе создания активной среды.
Важнейшим же вопросом для химических лазеров является вопрос о выборе химической реакции, создающей инверсию.
Рассмотрим простую модель (рис. 17.1). Пусть уровень 2 заселяется в процессе химической реакции со скоростью W. Тогда в рассматриваемом двухуровневом приближении скоростные уравнения имеют вид

где смысл времен  ясен из рис. 17.1. Стационарное значение разности населенностей
ясен из рис. 17.1. Стационарное значение разности населенностей
 (17.15)
(17.15)
достигает максимального значения
 (17.16)
(17.16)
где  при
при  . Это максимальное значение должно превышать некоторое пороговое для генерации значение
. Это максимальное значение должно превышать некоторое пороговое для генерации значение  . Следовательно, скорость химической накачки должна превышать некоторое значение, определяемое плотностью пороговой инверсии и эффективным временем релаксации:
. Следовательно, скорость химической накачки должна превышать некоторое значение, определяемое плотностью пороговой инверсии и эффективным временем релаксации:
 (17.17)
(17.17)

Рис. 17.1. К рассмотрению кинетики накачки химического лазера.
Примем теперь, что скорость химической накачки тождественна скорости химической реакции. Пусть рассматриваемая реакция может быть записана в виде
 (17.18)
(17.18)
Тогда скорость получения продукта  определяется произведением концентраций исходных реагентов
определяется произведением концентраций исходных реагентов  и так называемой константы скорости реакции К:
и так называемой константы скорости реакции К:
 (17.19)
(17.19)
Величина К подчиняется закону Аррениуса:
 (17.20)
(17.20)
где  — так называемая энергия активации реакции, а предэкспоненциальный множитель
— так называемая энергия активации реакции, а предэкспоненциальный множитель  слабо зависит от температуры и всегда меньше величины, определяемой числом газокинетических столкновений
слабо зависит от температуры и всегда меньше величины, определяемой числом газокинетических столкновений 
 (17.21)
(17.21)
При 300 К и обычных значениях энергии активации  ккал/моль) константа скорости реакции очень мала
ккал/моль) константа скорости реакции очень мала  , что не может обеспечить выполнения условия (17.17). Для химической накачки нужны реакции с энергией активации, исчисляемой единицами килокалорий на моль. (Для справок заметим, что энергии 1 эВ соответствует энергия 23 ккал/моль.) Столь малые энергии активации могут быть только у реакций с участием свободных атомов или свободных радикалов. Но приготовление свободных химически активных атомов или свободных радикалов крайне энергоемко. Энерговыделение радикальных реакций при 300 К составляет величину того же порядка, что и затраты энергии на приготовление радикалов.
, что не может обеспечить выполнения условия (17.17). Для химической накачки нужны реакции с энергией активации, исчисляемой единицами килокалорий на моль. (Для справок заметим, что энергии 1 эВ соответствует энергия 23 ккал/моль.) Столь малые энергии активации могут быть только у реакций с участием свободных атомов или свободных радикалов. Но приготовление свободных химически активных атомов или свободных радикалов крайне энергоемко. Энерговыделение радикальных реакций при 300 К составляет величину того же порядка, что и затраты энергии на приготовление радикалов.
При рассмотрении вопроса о химической накачке возникает, таким образом, проблема такого снижения затрат энергии на создание радикалов, при котором инициирование химической реакции типа (17.18) не было бы энергоемким. Тогда излучательный энергосъем, примерно равный энерговыделению химической реакции, мог бы заметно превышать энергию инициирования реакции. В идеальном предельном случае можно было бы надеяться на осуществление чисто химического лазерного эффекта, получаемого без каких-либо затрат энергии на инициирование реакции.
Обсуждаемая проблема решается использованием цепных и самоподдерживающихся химических реакций. В этих реакциях каждый химически активный центр (радикал, атом) воспроизводится в процессе реакции. Многократное использование радикалов перерабатывает в излучение запас химической энергии смеси. Многократность включения радикалов в реакции в ходе цепного химического процесса может перекрыть энергозатраты на создание того небольшого числа радикалов, которое нужно для начала развития цепного процесса.
Действительно, чтобы реализовать реакции типа (17.1) или (17.18), нужно иметь атомы (радикалы) А и (или) В. В простейшем случае мы имеем двухатомные молекулы  . Тогда продукт АВ обычно может быть получен в реакции
. Тогда продукт АВ обычно может быть получен в реакции
 (17.22)
(17.22)
Но эта прямая нецепная реакция имеет большую эйёргию активации и идет со скоростью, недостаточной для образования инверсии выше пороговой.
Применим теперь внешнее инициирующее воздействие, например подвергнем газ воздействию интенсивной вспышки достаточно
жесткого УФ излучения. В результате часть молекул диссоциирует:
 (17.23)
(17.23)
и возможно установление быстрой цепной реакции:
 (17.24)
(17.24)
Второй акт в цепи (17.24) восстанавливает исходную ситуацию, и выработка желаемого продукта АВ продолжается в отсутствие инициирующего воздействия. Однако реальная цепь не бесконечна, активные центры существуют конечное время и в конце концов гибнут. При анализе цепных реакций используется понятие химической длины цепи  , равной отношению концентрации молекулярного продукта АВ к концентрации исходных (инициирующих) радикалов А.
, равной отношению концентрации молекулярного продукта АВ к концентрации исходных (инициирующих) радикалов А.
По существу, длина v определяется отношением скорости самого медленного акта цепи к скорости гибели активных центров. Очевидно, что чем длиннее цепь, тем меньше доля энергии первого инициирования в общем энергобалансе реакции и, следовательно, тем выше к. п. д. возможного лазера. Но для лазерного эффекта нужен не просто молекулярный продукт АВ, нужны возбужденные молекулы АВ. Всегда существующие релаксационные процессы приводят к гибели возбуждения, т. е. гибели инверсии. Поэтому работу химического лазера следует характеризовать, вводя понятие лазерной длины цепи  определяемой как отношение скорости выработки возбужденных молекул АВ к скорости гибели инверсии из-за релаксации. Причины гибели радикалов и релаксации инверсии, в принципе, одинаковы
определяемой как отношение скорости выработки возбужденных молекул АВ к скорости гибели инверсии из-за релаксации. Причины гибели радикалов и релаксации инверсии, в принципе, одинаковы  газокинетические столкновения. Но релаксация протекает быстрее, поэтому
газокинетические столкновения. Но релаксация протекает быстрее, поэтому  и имеппо лазерная длина цепи определяет к. п. д. лазера.
и имеппо лазерная длина цепи определяет к. п. д. лазера.
Пусть на создание исходного радикала требуется энергия  . Каждый радикал сработал
. Каждый радикал сработал  раз. Энергозатраты источника инициирования (его к. п. д. равен
раз. Энергозатраты источника инициирования (его к. п. д. равен  ), приходящиеся тогда на один акт полезного излучения, составляют
), приходящиеся тогда на один акт полезного излучения, составляют  . Если энерговыделение акта реакции образования одной молекулы АВ равно АН и доля этой энергии
. Если энерговыделение акта реакции образования одной молекулы АВ равно АН и доля этой энергии  идет в нужное нам колебание молекулы АВ, то в одном акте излучается энергия
идет в нужное нам колебание молекулы АВ, то в одном акте излучается энергия  инициирования химического лазера, называемый также часто внешним к. п. д., оказывается равным
инициирования химического лазера, называемый также часто внешним к. п. д., оказывается равным
 (17.25)
(17.25)
Этот коэффициент при большой лазерной длине цепи может превышать, даже значительно превышать, 100%. Именно в этом заключено преимущество химических лазеров.
Наряду с к. п. д. инициирования представляет интерес величина химического к. п. д. лазера  , по определению равного
, по определению равного
«отношению энергии лазерного излучения  к общему запасу химической энергии в системе
к общему запасу химической энергии в системе  :
:
 (17.26)
(17.26)
Величина  важна прежде всего потому, что химическая энергия отнюдь не является даровой, она заключена в исходных реактивах, приготовление которых может быть весьма энергоемким.
важна прежде всего потому, что химическая энергия отнюдь не является даровой, она заключена в исходных реактивах, приготовление которых может быть весьма энергоемким.
Из предыдущего рассмотрения очевидно, что
 (17.27)
(17.27)
где  — исходное число радикалов при инициировании.
— исходное число радикалов при инициировании.
Запас химической энергии в системе определяется величиной энерговыделения реакции образования одной молекулы АВ и тем, сколько таких молекул может быть образовано заданным составом реагентов исходной смеси. Последнее равняется числу тех молекул исходной смеси, которые входят в результирующий молекулярный продукт в стехиометрически меньшей концентрации. Это число, обозначаемое символом  в случае реакции тика (17.22), или, точнее говоря, реакций (17.23), (17.24), равно концентрации
в случае реакции тика (17.22), или, точнее говоря, реакций (17.23), (17.24), равно концентрации  молекул
молекул  Будем исходить из простейшего случая. Тогда
Будем исходить из простейшего случая. Тогда
 (17.28)
(17.28)
Химический к. п. д., как и к. п. д. инициирования, тем больше, чем длиннее лазерная цепь и чем больше к. п. д. реакции  Вместе с тем глубина инициирования, т. е. относительное число активных центров
Вместе с тем глубина инициирования, т. е. относительное число активных центров  созданных источником инициирования. также определяет К сожалению, дальнейшее сравнение
созданных источником инициирования. также определяет К сожалению, дальнейшее сравнение  проводить трудно, так как лазерная длина цепи
проводить трудно, так как лазерная длина цепи  сложным образом зависит от кинетики ценной реакции и от начальной концентрации радикалов
сложным образом зависит от кинетики ценной реакции и от начальной концентрации радикалов  Часто с ростом степени инициации длина цепи
Часто с ростом степени инициации длина цепи  уменьшается, при этом
уменьшается, при этом  могут возрастать, а
могут возрастать, а  — падать. В реальных условиях ищется компромиссное решение.
— падать. В реальных условиях ищется компромиссное решение.
Упомянутые в начале этой лекции галогеноводородные лазеры работают в среднем ИК диапазоне. Для них характерны следующие длины волн:  -лазер — 2,7 мкм,
-лазер — 2,7 мкм,  -лазер — 3,7 мкм,
-лазер — 3,7 мкм,  -лазер — 4,2 мкм,
-лазер — 4,2 мкм,  -лазер — 4,3 мкм. При этом следует иметь в виду, что сложная структура колебательно-вращательных переходов в этих молекулах при сильном колебательном возбуждении позволяет получать генерацию на многих линиях в широком диапазоне в окрестности указанных длин волн. Все эти длины волн интересны сами по себе, но обращает на себя внимание величина кванта излучения
-лазер — 4,3 мкм. При этом следует иметь в виду, что сложная структура колебательно-вращательных переходов в этих молекулах при сильном колебательном возбуждении позволяет получать генерацию на многих линиях в широком диапазоне в окрестности указанных длин волн. Все эти длины волн интересны сами по себе, но обращает на себя внимание величина кванта излучения  -лазера, совпадающая с энергией колебания
-лазера, совпадающая с энергией колебания  молекулы
молекулы  Поэтому химически возбужденный DF может быть с успехом применен для создания химических
Поэтому химически возбужденный DF может быть с успехом применен для создания химических
 -лазеров путем использования резонансной передачи энергии возбуждения.
-лазеров путем использования резонансной передачи энергии возбуждения.
К настоящему времени разработаны как импульсные химические лазеры, так и химические лазеры непрерывного действия.
В импульсных лазерах во взаимно стабильной смеси газов; импульсное инициирование включает цепную реакцию, приводящую к излучению. Следует только помнить, что реакция должна быть быстрой, так как в медленно протекающей квазистационарной реакции релаксационные процессы приводят к гибели инверсии, уравновесив все степени свободы. Здесь просматривается аналогия с газодинамическим лазером, охлаждение газа в котором также должно быть быстрым.
Для импульсного инициирования применяются разного рода процессы фотолиза и радиолиза, главным образом УФ диссоциация и диссоциация электронным пучком. В качестве источников УФ излучения применяются искровые разряды, взрывающиеся проволочки, скользящие разряды, кварцевые лампы. Характерная длительность импульсов излучения этих источников составляет примерно 1 мкс. Электронные пучки могут обеспечивать более кратковременное воздействие (1—100 нс), но их общая эффективность ниже.
Для получения инверсии желательны наиболее простые молекулы — продукты реакций, предпочтительнее всего — двухатомные гетероядерные молекулы типа АВ. В противном случае усложняются процессы  -релаксации, да и в первичном акте экзотермической реакции произойдет перераспределение химической энергии по степеням свободы молекулы.
-релаксации, да и в первичном акте экзотермической реакции произойдет перераспределение химической энергии по степеням свободы молекулы.
Наилучшим примером является  -лазер. Генерация наблюдается главным образом, в колебательной полосе перехода
-лазер. Генерация наблюдается главным образом, в колебательной полосе перехода  в диапазоне 2,7 мкм. Для получения сначала атомарного фтора, а затем фтороводорода используются смеси мо-лекул-фтороносителей типа
в диапазоне 2,7 мкм. Для получения сначала атомарного фтора, а затем фтороводорода используются смеси мо-лекул-фтороносителей типа  или фреонов с водородом или водородсодержащими молекулами. Так, в смеси
или фреонов с водородом или водородсодержащими молекулами. Так, в смеси  в отношении
в отношении 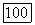 при общем давлении 1 атм и инициировании электронным пучком получен энергосъем
при общем давлении 1 атм и инициировании электронным пучком получен энергосъем 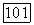 в импульсе длительностью 30 нс. К. п. д. инициирования достигал 800%. Здесь следует обратить внимание на важную особенность химических лазеров, обусловленную их химической природой. Смесь абсолютно чистых водорода
в импульсе длительностью 30 нс. К. п. д. инициирования достигал 800%. Здесь следует обратить внимание на важную особенность химических лазеров, обусловленную их химической природой. Смесь абсолютно чистых водорода 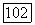 и фтора
и фтора 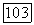 нестабильна: Правилом, а не исключением, являются ее самопроизвольные взрывы. Добавление кислорода и
нестабильна: Правилом, а не исключением, являются ее самопроизвольные взрывы. Добавление кислорода и 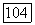 стабилизирует смесь. Выбор исходной смеси газов представляет, таким образом, в химических лазерах серьезную проблему не только с точки зрения релаксационной кинетики, но и с точки зрения кинетики цепных реакций взрывного типа.
стабилизирует смесь. Выбор исходной смеси газов представляет, таким образом, в химических лазерах серьезную проблему не только с точки зрения релаксационной кинетики, но и с точки зрения кинетики цепных реакций взрывного типа.
Большой интерес, особенно для автономных применений, имеет 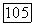 -лазер, основанный на уже упомянутой передаче энергии
-лазер, основанный на уже упомянутой передаче энергии
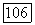 . В импульсах длительностью несколько микросекунд на волне 10,6 мкм получен энергосъем до 150 Дж/л.
. В импульсах длительностью несколько микросекунд на волне 10,6 мкм получен энергосъем до 150 Дж/л.
Непрерывный режим работы химических лазеров возможен 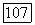 , при смешивании газов, например в сопловых блоках. Так как смешивать в потоке можно взаимно совершенно нестабильные реагенты, а затем быстро, со скоростью, близкой к звуковой, удалять продукты их реакции, то становится возможным чисто химический лазер без инициирования. Наиболее интересен здесь
, при смешивании газов, например в сопловых блоках. Так как смешивать в потоке можно взаимно совершенно нестабильные реагенты, а затем быстро, со скоростью, близкой к звуковой, удалять продукты их реакции, то становится возможным чисто химический лазер без инициирования. Наиболее интересен здесь 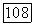 -лазер, в котором возбужденные молекулы DF возникают в ходе цепной реакции, поджигаемой при смешивании устойчивого радикала
-лазер, в котором возбужденные молекулы DF возникают в ходе цепной реакции, поджигаемой при смешивании устойчивого радикала 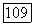 с молекулярным фтором, что дает атомарный фтор, служащий активным центром цепной реакции:
с молекулярным фтором, что дает атомарный фтор, служащий активным центром цепной реакции:
 (17.30)
(17.30)
К возбужденному DF ниже по потоку подмешивается 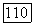 возбуждаемый по хорошо известной схеме
возбуждаемый по хорошо известной схеме
 (17.32)
(17.32)
Отработка газодинамической системы, реализующейтакую схему, представляет известные трудности ввиду взрывоопасности используемых смесей и высокой токсичности продуктов реакции. На рис. 17.2 показана соответствующая схема проточного реакционного сосуда, снабженного на выхлопе лазерным резонатором.

Рис. 17.2. Схема проточного реакционного сосуда химического 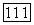 -лазера. Волнистая стрелка показывает выход излучения Через частично прозрачное зеркало.
-лазера. Волнистая стрелка показывает выход излучения Через частично прозрачное зеркало.
Но существу, эта схема близка к газодинамическому лазеру и встречается с теми же трудностями конструирования резонатора лазера с быстрым поперечным протоком активного вещества. Дриведенная мощность такого лазера может достичь сотен ватт в пересчете на скорость расхода активного вещества 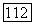 .
.
По-видимому, в строгом смысле слова химическими следует считать такие лазеры с химическим механизмом возбуждения
активной среды, для которых к. п. д. инициирования (внешний к. п. д.) превышает единицу.
Примером обратной ситуации является йодный 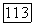 фотодиссоциационный лазер.
фотодиссоциационный лазер.
В фотохимии хорошо известно, что в некоторых случаях атомы охотнее вступают в реакции присоединения, будучи электронно возбуждены. Следовательно, при диссоциации могут возникать электронно возбужденные атомы. Это означает, что по крайней мере часть энергии связи атомов в молекуле может затратиться на возбуждение осколка молекулы. Если фрагментом диссоциации является атом, то возбужденными могут оказаться только его электронные уровни энергии. Но исходная молекула устойчива, следовательно, на разрыв связи необходимо затратить энергию, очевидно, большую той доли энергии, которая в результате разного рода перераспределений выделится в виде электронной энергии атома.
Имея в виду релаксационные процессы, мы понимаем, что диссоциацию надо проводить быстро. При этом дальнейшее использование возбужденных продуктов диссоциации для их цепного размножения недопустимо, так как оно приведет к гибели возбуждения. Поэтому наиболее удобна прямая импульсная фотодиссоциация. Из изложенного ясно, что к. п. д. инициирования в рассматриваемом случае меньше единицы. С этой точки зрения фотодиссоциационные лазеры отличаются от тех химических лазеров, которым посвящена в основном эта лекция. Следует все же помнить, что в рамках более общего определения, приведенного в начале лекции, фотодиссоциационные лазеры являются химическими лазерами.
Наибольшую известность приобрел йодный лазер на волне 1,315 мкм, возбужденные атомы иода в котором получаются путем импульсного фотолиза молекул 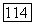 . Реакция происходит по схеме
. Реакция происходит по схеме
 (17.33)
(17.33)
Возбужденное состояние иода 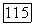 опустошается излучательными переходами
опустошается излучательными переходами 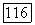 в рамках одной и той же электронной конфигурации иода
в рамках одной и той же электронной конфигурации иода 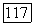 . Излучение немонохроматического источника поглощается в широкой молекулярной полосе поглощения, возбужденные атомы излучают в узкой линии, характерной для атомных спектров.
. Излучение немонохроматического источника поглощается в широкой молекулярной полосе поглощения, возбужденные атомы излучают в узкой линии, характерной для атомных спектров.
Так как фотодиссоциации могут быть подвергнуты большие объемы; газа 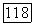 , то йодный лазер этого типа представляется весьма перспективным для получения высокой импульсной энергии.
, то йодный лазер этого типа представляется весьма перспективным для получения высокой импульсной энергии.
Источником УФ диссоциации излучения служат импульсные кварцевые лампы, взрывающиеся проволочки, открытые разряды.
Кроме молекул 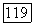 , в качестве источника возбужденных атомов, иода нашли применение молекулы
, в качестве источника возбужденных атомов, иода нашли применение молекулы 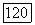 .
.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ЧАСТЬ ПЕРВАЯ. ОСНОВЫ ФИЗИКИ ЛАЗЕРОВ
- Лекция первая. КОЭФФИЦИЕНТЫ ЭЙНШТЕЙНА
- Лекция вторая. ШИРИНА ЛИНИИ
- Лекция третья. УСИЛЕНИЕ
- Лекция четвертая. КОЭФФИЦИЕНТЫ ЭЙНШТЕЙНА И МАТРИЧНЫЙ ЭЛЕМЕНТ ОПЕРАТОРА ПЕРЕХОДА
- Лекция пятая. ЛАЗЕРЫ-УСИЛИТЕЛИ
- Лекция шестая. ГЕНЕРАЦИЯ
- Лекция седьмая. ОТКРЫТЫЕ РЕЗОНАТОРЫ
- Лекция восьмая. ГАУССОВЫ ПУЧКИ
- Лекция девятая. УСТОЙЧИВОСТЬ РЕЗОНАТОРОВ
- Лекция десятая. НЕУСТОЙЧИВЫЕ РЕЗОНАТОРЫ
- Лекция одиннадцатая. СИНХРОНИЗАЦИЯ МОД
- Лекция двенадцатая. ИСТОРИЯ КВАНТОВОЙ ЭЛЕКТРОНИКИ. ОСНОВНЫЕ ФОРМУЛЫ
- ЧАСТЬ ВТОРАЯ. ЛАЗЕРЫ
- Лекция тринадцатая. ГАЗОВЫЕ ЛАЗЕРЫ. ГЕЛИЙ-НЕОНОВЫЙ ЛАЗЕР
- Лекция четырнадцатая. ИОННЫЕ ЛАЗЕРЫ. ЛАЗЕРЫ НА ПАРАХ МЕТАЛЛОВ
- Лекция пятнадцатая. CO2-ЛАЗЕРЫ
- Лекция шестнадцатая. СO2-ЛАЗЕРЫ (продолжение)
- Лекция семнадцатая. ХИМИЧЕСКИЕ ЛАЗЕРЫ
- Лекция восемнадцатая. CO-ЛАЗЕРЫ, ГАЗОВЫЕ ЛАЗЕРЫ НА ЭЛЕКТРОННЫХ ПЕРЕХОДАХ В МОЛЕКУЛАХ
- Лекция девятнадцатая. ВСПОМОГАТЕЛЬНОЕ ИЗЛУЧЕНИЕ НАКАЧКИ В СИСТЕМАХ СО МНОГИМИ УРОВНЯМИ ЭНЕРГИИ
- Лекция двадцатая. РУБИНОВЫЙ И НЕОДИМОВЫЙ ЛАЗЕРЫ
- Лекция двадцать первая. БЕЗЫЗЛУЧАТЕЛЬНАЯ РЕЛАКСАЦИЯ В ТВЕРДОМ ТЕЛЕ
- Лекция двадцать вторая. ЛАЗЕРЫ НА КРАСИТЕЛЯХ
- Лекция двадцать третья. ЛАЗЕРЫ НА ЦЕНТРАХ ОКРАСКИ
- Лекция двадцать четвертая. ПОЛУПРОВОДНИКОВЫЕ ЛАЗЕРЫ
- Лекция двадцать пятая. ПОЛУПРОВОДНИКОВЫЕ ЛАЗЕРЫ (продолжение)
- Лекция двадцать шестая. ЛАЗЕРЫ НА СВОБОДНЫХ ЭЛЕКТРОНАХ
- Лекция двадцать седьмая. СЕМНАДЦАТЬ НАИБОЛЕЕ ИЗВЕСТНЫХ ЛАЗЕРОВ
- Заключение. ТЕНДЕНЦИИ РАЗВИТИЯ