| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
Вопросы и задачи
1. Автомобильный антифриз. В качестве вещества, понижающего температуру замерзания воды в радиаторе автомобиля, обычно используется зтиленгликоль - спирт, содержащий две гидроксильные группы ( ). Рассчитайте, какова должна быть приблизительная концентрация этиленгликоля, которая будет достаточной для предотвращения замерзания воды при — 18 °С.
). Рассчитайте, какова должна быть приблизительная концентрация этиленгликоля, которая будет достаточной для предотвращения замерзания воды при — 18 °С.
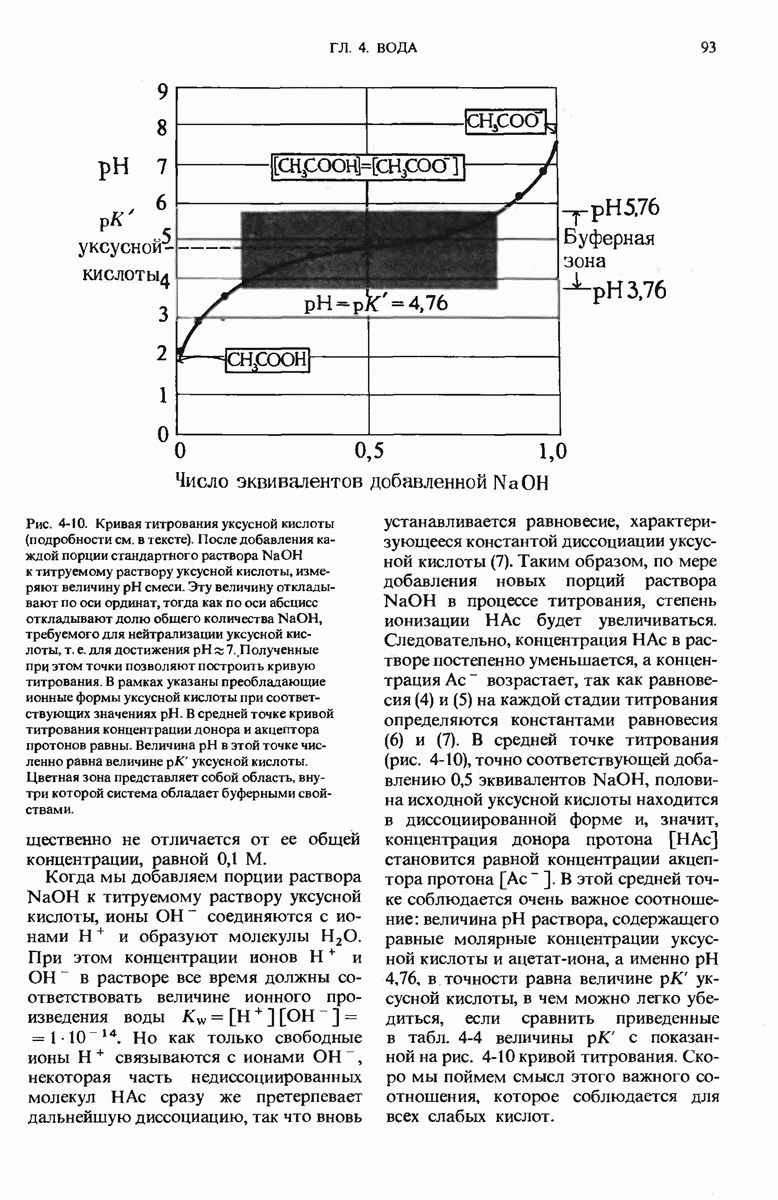
2. Имитация уксуса. Один из способов приготовления уксуса (отнюдь не лучший) состоит просто в том, что уксусную кислоту, единственный кислый компонент уксуса, разводят водой до нужного pH (см. табл. 4-4 и рис. 4-9) и добавляют соответствующие приправы. Уксусная кислота при 25 °С представляет собой жидкость с плотностью 1,049 г/мл. Рассчитайте, какое количество уксусной кислоты нужно растворить в дистиллированной воде, чтобы получить 1 л раствора, имитирующего уксус.
3. Кислотность желудочной соляной кислоты. В клинических лабораториях для определения кислотности желудочного сока оттитровывают 10,0 мл желудочного сока, взятого через несколько часов после еды, 0,1 н. раствором NaOH до нейтральной реакции. Допустим, что для этого потребовалось 7,2 мл раствора NaOH. Так как желудок к этому времени уже не содержит непереваренной пищи или напитков, никаких буферов в нем нет. Какова величина pH желудочного сока?
4. Измерение содержания ацетилхолина по изменению pH. Концентрацию нейромедиатора ацетилхолина можно определить по изменению pH, сопровождающему гидролиз ацетилхолина. При инкубации ацетилхолина с каталитическими количествами фермента ацетилхолинэстеразы он количественно превращается в холин и уксусную кислоту, которая диссоциирует с образованием ацетат-иона и иона водорода:

Согласно данным анализа, водный раствор, содержащий неизвестное количество ацетилхолина объемом 15 мл, имел pH 7,65. После инкубации с ацетилхолин-эстеразой pH раствора снизился до 6,87. Сколько молей ацетилхолина содержалось в 15 мл исходного раствора, если считать, что в анализируемой смеси отсутствовали буферы?
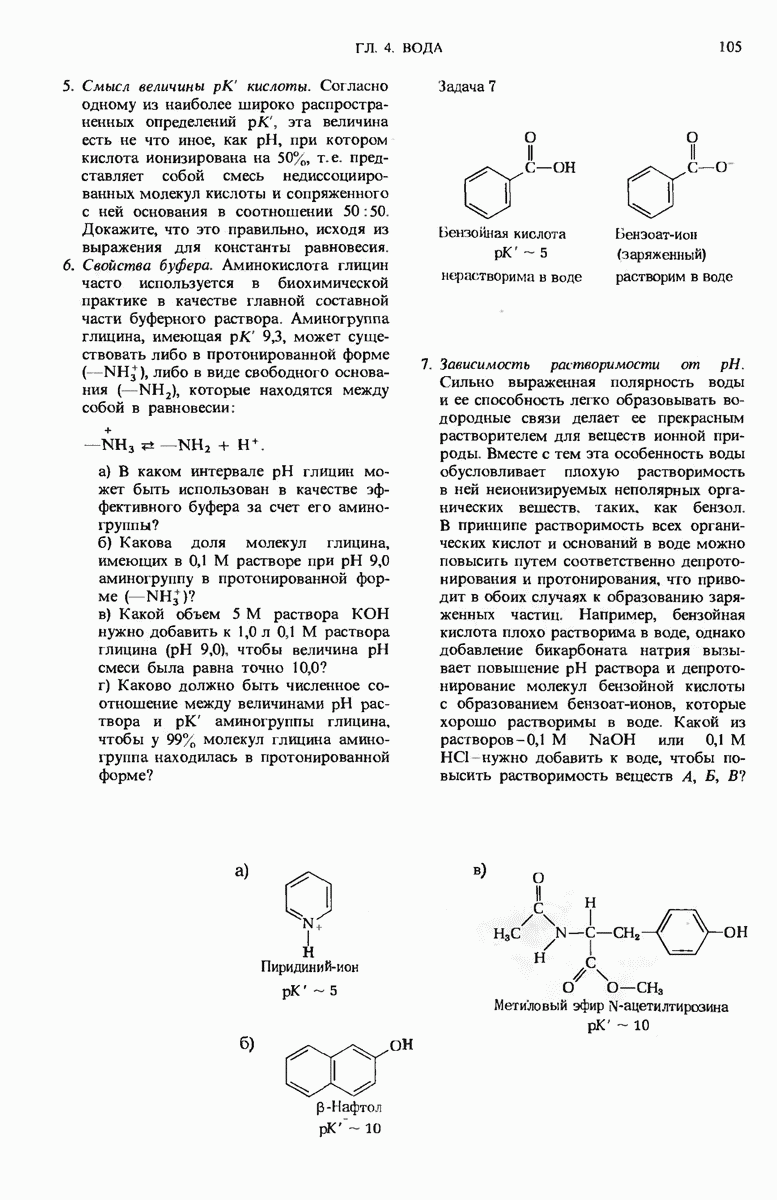
5. Смысл величины  кислоты. Согласно одному из наиболее широко распространенных определений
кислоты. Согласно одному из наиболее широко распространенных определений  эта величина есть не что иное, как pH, при котором кислота ионизирована на 50%, т.е. представляет собой смесь недиссоциированных молекул кислоты и сопряженного с ней основания в соотношении 50 :50. Докажите, что это правильно, исходя из выражения для константы равновесия.
эта величина есть не что иное, как pH, при котором кислота ионизирована на 50%, т.е. представляет собой смесь недиссоциированных молекул кислоты и сопряженного с ней основания в соотношении 50 :50. Докажите, что это правильно, исходя из выражения для константы равновесия.
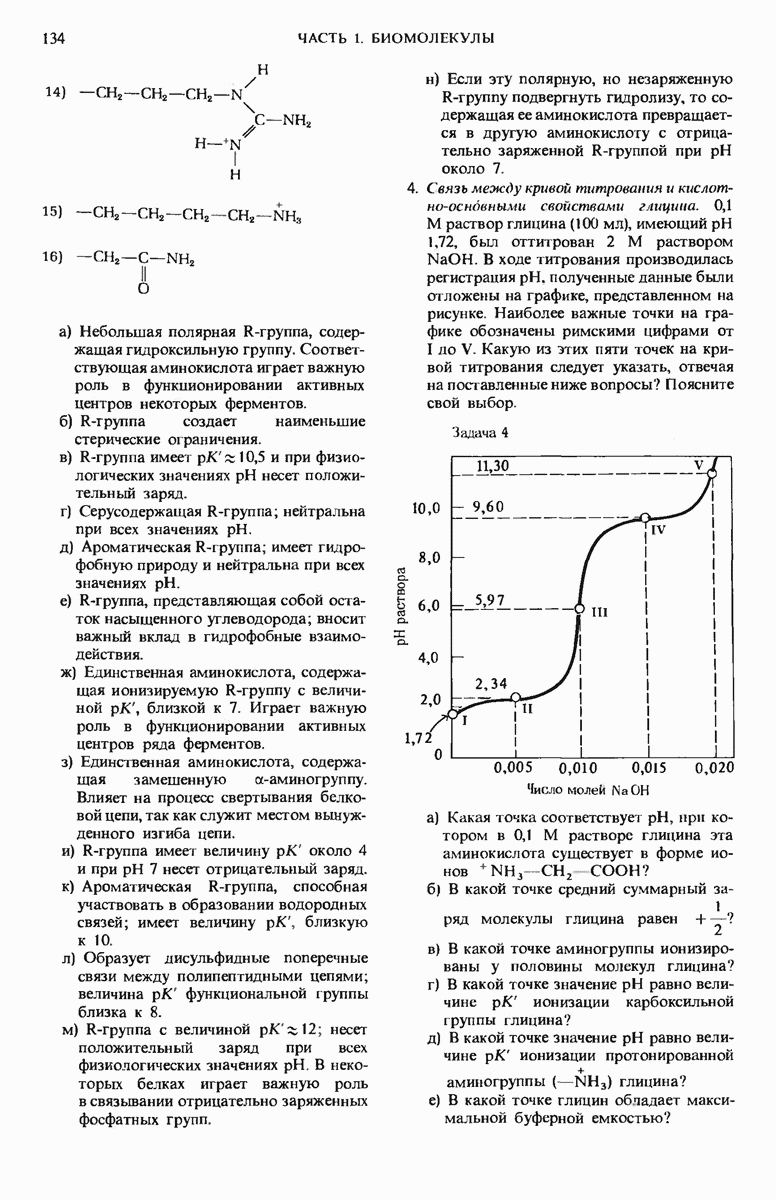
6. Свойства буфера. Аминокислота глицин часто используется в биохимической практике в качестве главной составной части буферного раствора. Аминогруппа глицина, имеющая  может существовать либо в протонированной форме
может существовать либо в протонированной форме  либо в виде свободного основания
либо в виде свободного основания  которые находятся между собой в равновесии:
которые находятся между собой в равновесии:

а) В каком интервале pH глицин может быть использован в качестве эффективного буфера за счет его аминогруппы?
б) Какова доля молекул глицина, имеющих в 0,1 М растворе при pH 9,0 аминогруппу в протонированной форме  ?
?
в) Какой объем 5 М раствора КОН нужно добавить к  раствора глицина (pH 9,0), чтобы величина pH смеси была равна точно 10,0?
раствора глицина (pH 9,0), чтобы величина pH смеси была равна точно 10,0?
г) Каково должно быть численное соотношение между величинами pH раствора и  аминогруппы глицина, чтобы у 99% молекул глицина аминогруппа находилась в протонированной форме?
аминогруппы глицина, чтобы у 99% молекул глицина аминогруппа находилась в протонированной форме?
Задача 7

7. Зависимость растворимости от pH. Сильно выраженная полярность воды и ее способность легко образовывать водородные связи делает ее прекрасным растворителем для веществ ионной природы. Вместе с тем эта особенность воды обусловливает плохую растворимость в ней неионизируемых неполярных органических вешеств, таких, как бензол. В принципе растворимость всех органических кислот и оснований в воде можно повысить путем соответственно депротонирования и протонирования, что приводит в обоих случаях к образованию заряженных частиц. Например, бензойная кислота плохо растворима в воде, однако добавление бикарбоната натрия вызывает повышение pH раствора и депротонирование молекул бензойной кислоты с образованием бензоат-ионов, которые хорошо растворимы в воде. Какой из растворов  или
или  нужно добавить к воде, чтобы повысить растворимость веществ А, Б, В?
нужно добавить к воде, чтобы повысить растворимость веществ А, Б, В?

8. Лечение сыпи, возникающей на коже при соприкосновении с растением сумахом. Содержащиеся в тканях сумаха производные пирокатехола с длинными цепями алкильных групп вызывают характерную зудящую сыпь.

Если вы случайно дотронулись до сумаха, то какой способ обработки пораженного участка кожи из перечисленных ниже вы изберете и почему?
(а) Промывание поверхности кожи холодной водой.
(б) Промывание поверхности кожи разбавленным уксусом или лимонным соком.
(в) Промывание поверхности кожи мылом и водой.
(г) Промывание поверхности кожи мылом, водой и пищевой (питьевой) содой (бикарбонатом натрия).
9. Величина pH и всасывание лекарственных веществ. Широко используемый лекаственный препарат аспирин представляет собой слабую кислоту с 

Аспирин всасывается в кровь человека через клетки слизистой желудка и тонкого кишечника. Для того чтобы вещество всасывалось, оно должно легко проходить через клеточные мембраны. Возможность прохождения вещества через клеточную мембрану определяется полярностью его молекул: ионизированные (заряженные) и сильно полярные молекулы проходят медленно, тогда как нейтральные гидрофобные молекулы проходят сквозь мембраны быстро. Где аспирин легче всасывается в кровяной поток - в желудке или в тонком кишечнике, если величина pH желудочного сока в желудке близка к 1, а в тонком кишечнике к 6? Дайте четкое обоснование своего выбора.
10. Приготовление стандартного буфера для калибровки рН-метра. Стеклянный электрод. используемый в имеющихся в продаже pH-метрах, дает электрический сигнал, величина которого пропорциональна концентрации ионов водорода. Для того чтобы по величине сигнала можно было правильно судить о величине pH, необходимо провести калибровку стеклянного электрода, используя для этого стандартные растворы с известной концентрацией нонов водорода. Определите, какие количества (в граммах) первичного кислого фосфата натрия  мол. масса 138,01) и вторичною кислого фосфата натрия
мол. масса 138,01) и вторичною кислого фосфата натрия  мол. масса 141,98) необходимы для приготовления 1 л стандартного буфера с
мол. масса 141,98) необходимы для приготовления 1 л стандартного буфера с  в котором суммарная концентрация фосфатов равна 0,100 М. (Мол. масса смеси фосфатов будет зависеть от их соотношения). Величина
в котором суммарная концентрация фосфатов равна 0,100 М. (Мол. масса смеси фосфатов будет зависеть от их соотношения). Величина  первичного кислого фосфата при 25 С равна 6,86.
первичного кислого фосфата при 25 С равна 6,86.
11. Контроль pH крови путем изменения интенсивности дыхания.
а) Парциальное давление  в легких может быстро меняться в зависимости от интенсивности и глубины дыхания. Известно, что для избавления от икоты необходимо повысить концентрацию
в легких может быстро меняться в зависимости от интенсивности и глубины дыхания. Известно, что для избавления от икоты необходимо повысить концентрацию  в легких. Этого можно добиться, если частично задержать дыхание, медленно и неглубоко вдыхая воздух (гиповентиляция), или вдыхать и выдыхать воздух, прижав к лицу бумажный пакет В этих условиях парциальное давление
в легких. Этого можно добиться, если частично задержать дыхание, медленно и неглубоко вдыхая воздух (гиповентиляция), или вдыхать и выдыхать воздух, прижав к лицу бумажный пакет В этих условиях парциальное давление  в воздушном пространстве легких превысит нормальное. Объясните. почему эти процедуры влияют на pH крови.
в воздушном пространстве легких превысит нормальное. Объясните. почему эти процедуры влияют на pH крови.
б) Бегуны на короткие дистанции непосредственно перед стартом обычно интенсивно и глубоко дышат (гипервентиляция) примерно в течение 1, 2 мин для удаления  из легких. Величина pH крови может подскочить при этом до 7,60. Объясните, почему pH крови повышается в этих условиях.
из легких. Величина pH крови может подскочить при этом до 7,60. Объясните, почему pH крови повышается в этих условиях.
в) Во время бега на короткую дистанцию мышцы производят большое количество молочной кислоты из запасов глюкозы. Исходя из этого факта, объясните, почему перед стремительным бегом полезна гипервентиляция?
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРОВ ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- Благодарности
- ЧАСТЬ I. БИОМОЛЕКУЛЫ
- ГЛАВА 1. БИОХИМИЯ-МОЛЕКУЛЯРНАЯ ЛОГИКА ЖИВЫХ ОРГАНИЗМОВ
- 1.1. Для живой материи характерны некоторые отличительные особенности
- 1.2. Биохимия стремится понять природу живого состояния
- 1.3. Все живые организмы содержат органические макромолекулы, построенные по общему плану
- 1.4. Обмен веществ и энергии в живых организмах
- 1.5. Ферменты, играющие роль катализаторов в живых клетках, управляют сложно организованной сетью химических реакций
- 1.6. Клетки используют энергию в химической форме
- 1.7. Процессы клеточного метаболизма находятся под постоянным контролем
- 1.8. Живые организмы способны к точному самовоспроизведению
- ГЛАВА 2. КЛЕТКИ
- 2.1. Все клетки обладают некоторыми общими структурными характеристиками
- 2.2. Клетки должны иметь очень малые размеры
- 2.3. Существуют два больших класса клеток — прокариотические и эукариотические
- 2.4. Прокариоты — самые простые и самые мелкие клетки
- 2.5. Escherichia coli — самая известная из прокариотических клеток
- 2.6. Эукариотические клетки крупнее и сложнее прокариотических
- 2.7. Ядро эукариот — это очень сложная структура
- 2.8. Митохондрии — «силовые установки» эукариотических клеток, поставляющие энергию
- 2.9. Эндоплазматический ретикулум образует каналы в цитоплазме
- 2.10. Тельца Гольджи — секреторные органеллы
- 2.11. Лизосомы — контейнеры с гидролитическими ферментами
- 2.12. Пероксисомы — пузырьки, разрушающие перекись водорода
- 2.13. Микрофиламенты участвуют в сократительных процессах клеток
- 2.14. Микротрубочки также связаны с клеточными движениями
- 2.15. Микрофиламенты, микротрубочки и микротрабекулярная сеть образуют цитоскелет
- 2.16. Реснички и жгутики позволяют клеткам передвигаться
- 2.17. В цитоплазме содержатся также гранулярные тельца
- 2.18. Цитозоль — непрерывная водная фаза цитоплазмы
- 2.19. Клеточная мембрана имеет большую площадь поверхности
- 2.20. На поверхности многих животных клеток имеются также «антенны»
- 2.21. Эукариотические клетки растений имеют некоторые специфические особенности
- 2.22. Вирусы — надмолекулярные паразиты
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 3. СОСТАВ ЖИВОЙ МАТЕРИИ: БИОМОЛЕКУЛЫ
- 3.1. Химический состав живой материи отличается от химического состава земной коры
- 3.2. Большинство биомолекул содержит углерод
- 3.3. Биомолекулы имеют специфическую форму и определенные размеры
- 3.4. Функциональные группы органических биомолекул определяют их химические свойства
- 3.5. Многие биомолекулы асимметричны
- 3.6. Основные классы биомолекул в клетках представлены очень крупными молекулами
- 3.7. Макромолекулы образуются из небольших молекул, играющих роль строительных блоков
- 3.8. Молекулы, используемые в качестве строительных блоков, имеют простую структуру
- 3.9. Структурная иерархия в молекулярной организации клеток
- 3.10. Биомолекулы первыми возникли в процессе химической эволюции
- 3.11. Химическую эволюцию можно воспроизвести в лабораторных условиях
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 4. ВОДА
- 4.1. Необычные физические свойства воды обусловлены ее способностью участвовать в образовании водородных связей
- 4.2. Водородные связи широко распространены в биологических системах и играют в них важную роль
- 4.3. Вода как растворитель обладает необычными свойствами
- 4.4. Растворенные вещества изменяют свойства воды
- 4.5. Состояние равновесия обратимых реакций характеризуется константой равновесия
- 4.6. Ионизацию воды можно охарактеризовать величиной константы равновесия
- 4.7. Шкала pH: обозначения концентраций ионов Н+ и ОН-
- 4.8. Свойства кислот и оснований тесно связаны со свойствами воды
- 4.9. Слабые кислоты имеют характерные кривые титрования
- 4.10. Буферы — это смеси слабых кислот и сопряженных с ними оснований
- 4.11. Фосфат и бикарбонат — важные биологические буферные системы
- 4.12. Приспособленность живых организмов к водной среде
- 4.13. «Кислые» дожди загрязняют наши озера и реки
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 5. АМИНОКИСЛОТЫ И ПЕПТИДЫ
- 5.1. Общие структурные свойства аминокислот
- 5.2. Почти все аминокислоты содержат асимметрический атом углерода
- 5.3. Стереоизомеры обозначаются в соответствии с их абсолютной конфигурацией
- 5.4. Оптически активные аминокислоты в белках представляют собой L-стереоизомеры
- 5.5. Классификация аминокислот на основе их R-групп
- 5.6. Восемь аминокислот содержат неполярные R-группы
- 5.7. Семь аминокислот содержат незаряженные полярные R-группы
- 5.8. Две аминокислоты содержат отрицательно заряженные (кислые) R-группы
- 5.9. Три аминокислоты содержат положительно заряженные (основные) R-группы
- 5.10. В некоторых белках присутствуют нестандартные аминокислоты
- 5.11. В водных растворах аминокислоты ионизированы
- 5.12. Аминокислоты могут вести себя и как кислоты, и как основания
- 5.13. Аминокислоты имеют характерные кривые титрования
- 5.14. По кривой титрования можно предсказать, какой электрический заряд несет данная аминокислота
- 5.15. Аминокислоты различаются по своим кислотно-основным свойствам
- 5.16. Кислотно-основные свойства аминокислот служат основой для аминокислотного анализа
- 5.17. Электрофорез на бумаге позволяет разделять аминокислоты в соответствии с их электрическим зарядом
- 5.18. Ионообменная хроматография служит более эффективным способом разделения аминокислот
- 5.19. Химические реакции, характерные для аминокислот
- 5.20. Пептиды — это цепочки аминокислот
- 5.21. Разделение пептидов может быть основано на различиях в их ионизационных свойствах
- 5.22. Химические реакции, характерные для пептидов
- 5.23. Некоторые пептиды обладают высокой биологической активностью
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 6. БЕЛКИ: КОВАЛЕНТНАЯ СТРУКТУРА И БИОЛОГИЧЕСКИЕ ФУНКЦИИ
- 6.1. Белки обладают множеством различных биологических функций
- 6.2. Белки можно классифицировать также по форме их молекул
- 6.3. В ходе гидролиза брлки распадаются на аминокислоты
- 6.4. Некоторые белки имеют в своем составе не только аминокислоты, но и другие химические группы
- 6.5. Белки — это очень крупные молекулы
- 6.6. Белки можно выделить и подвергнуть очистке
- 6.7. Определение аминокислотной последовательности полипептидных цепей
- 6.8. Инсулин — это первый белок, для которого была установлена аминокислотная последовательность
- 6.9. В настоящее время известны последовательности многих других белков
- 6.10. Гомологичные белки разных видов имеют гомологичные последовательности
- 6.11. Различия между гомологичными белками можно выявить по иммунной реакции
- 6.12. Белки претерпевают структурные изменения, называемые денатурацией
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 7. ФИБРИЛЛЯРНЫЕ БЕЛКИ
- 7.1. Термины «конфигурация» и «конформация» имеют разный смысл
- 7.2. Как это ни парадоксально, нативные белки имеют только одну или всего лишь несколько конформаций
- 7.3. a-Кератины — фибриллярные белки, синтезируемые клетками эпидермиса
- 7.4. Рентгеноструктурный анализ показывает, что в кератинах имеются повторяющиеся структурные единицы
- 7.5. Рентгеноструктурные исследования пептидов свидетельствуют о жесткости и плоской конфигурации пептидных групп
- 7.6. В a-кератине полипептидные цепи имеют форму a-спирали
- 7.7. Некоторые аминокислотные остатки препятствуют образованию a-спирали
- 7.8. В a-кератинах содержится много аминокислот, способствующих образованию a-спиральной структуры
- 7.9. В нативных a-кератинах a-спиральные полипептидные цепи скручены наподобие каната
- 7.10. a-Кератины нерастворимы в воде из-за преобладания в их составе аминокислот с неполярными R-группами
- 7.11. b-Кератины имеют другую конформацию полипептидной цепи, называемую b-структурой
- 7.12. Перманентная завивка волос — пример биохимической технологии
- 7.13. Коллаген и эластин — главные фибриллярные белки соединительных тканей
- 7.14. Коллаген — самый распространенный белок у высших животных
- 7.15. Коллаген обладает как обычными, так и необычными свойствами
- 7.16. Полипептиды в коллагене представляют собой трехцепочечные спиральные структуры
- 7.17. Структура эластина придает особые свойства эластической ткани
- 7.18. Что говорят нам фибриллярные белки о структуре белков?
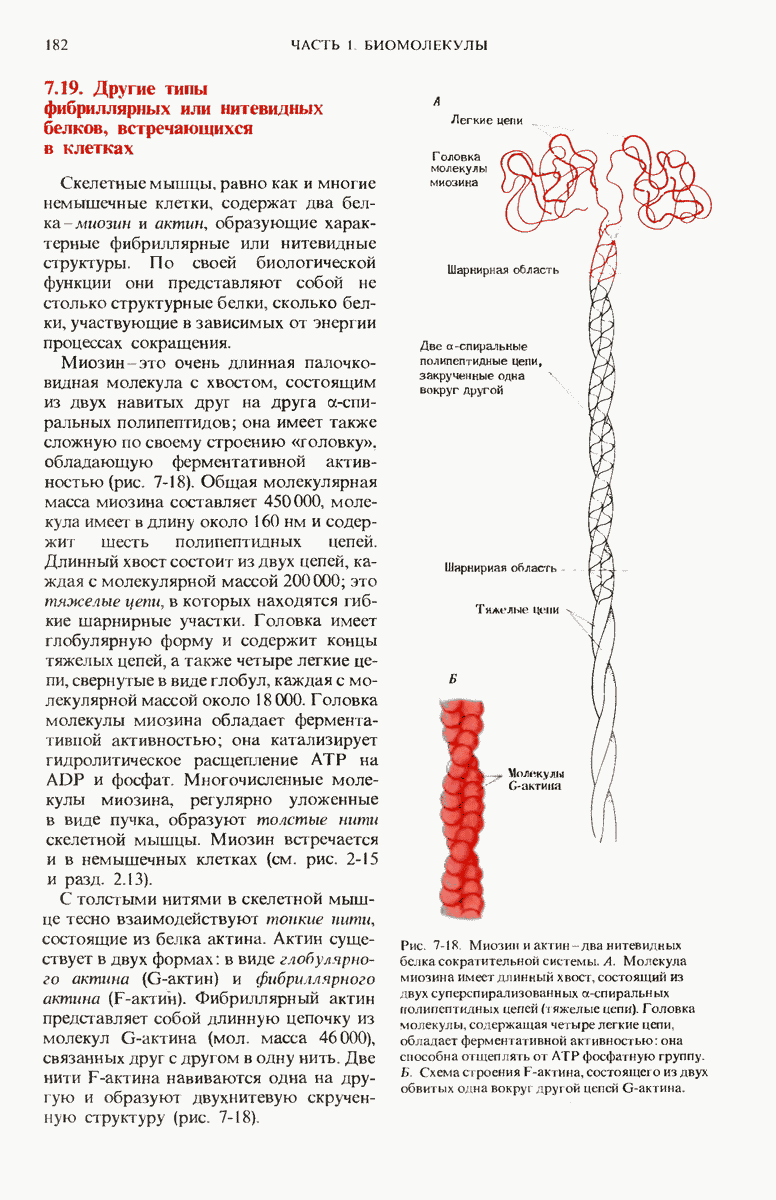
- 7.19. Другие типы фибриллярных или нитевидных белков встречающихся в клетках
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 8. ГЛОБУЛЯРНЫЕ БЕЛКИ: СТРУКТУРА И ФУНКЦИЯ ГЕМОГЛОБИНА
- 8.1. Полипептидные цепи глобулярных белков свернуты в плотную компактную структуру
- 8.2. Рентгеноструктурный анализ миоглобина — выдающееся достижение в исследовании белков
- 8.3. Миоглобины, выделенные из разных видов, имеют сходную конформацию
- 8.4. Глобулярные белки различных типов имеют неодинаковую структуру
- 8.5. Аминокислотная последовательность белка определяет его третичную структуру
- 8.6. Силы, стабилизирующие третичную структуру глобулярных белков
- 8.7. Свертывание полипептидных цепей происходит с очень высокой скоростью
- 8.8. Олигомерные белки имеют как третичную, так и четвертичную структуру
- 8.9. Метод рентгеноструктурного анализа позволил установить как третичную, так и четвертичную структуру гемоглобина
- 8.10. По своей третичной структуре a- и b-цепи гемоглобина очень сходны с миоглобином
- 8.11. Была установлена четвертичная структура и некоторых других олигомерных белков
- 8.12. Эритроциты — специализированные клетки, переносящие кислород
- 8.13. Для миоглобина и гемоглобина характерны разные кривые связывания кислорода
- 8.14. Кооперативное связывание кислорода делает гемоглобин более эффективным переносчиком кислорода
- 8.15. Гемоглобин служит также переносчиком С02 и ионов H+
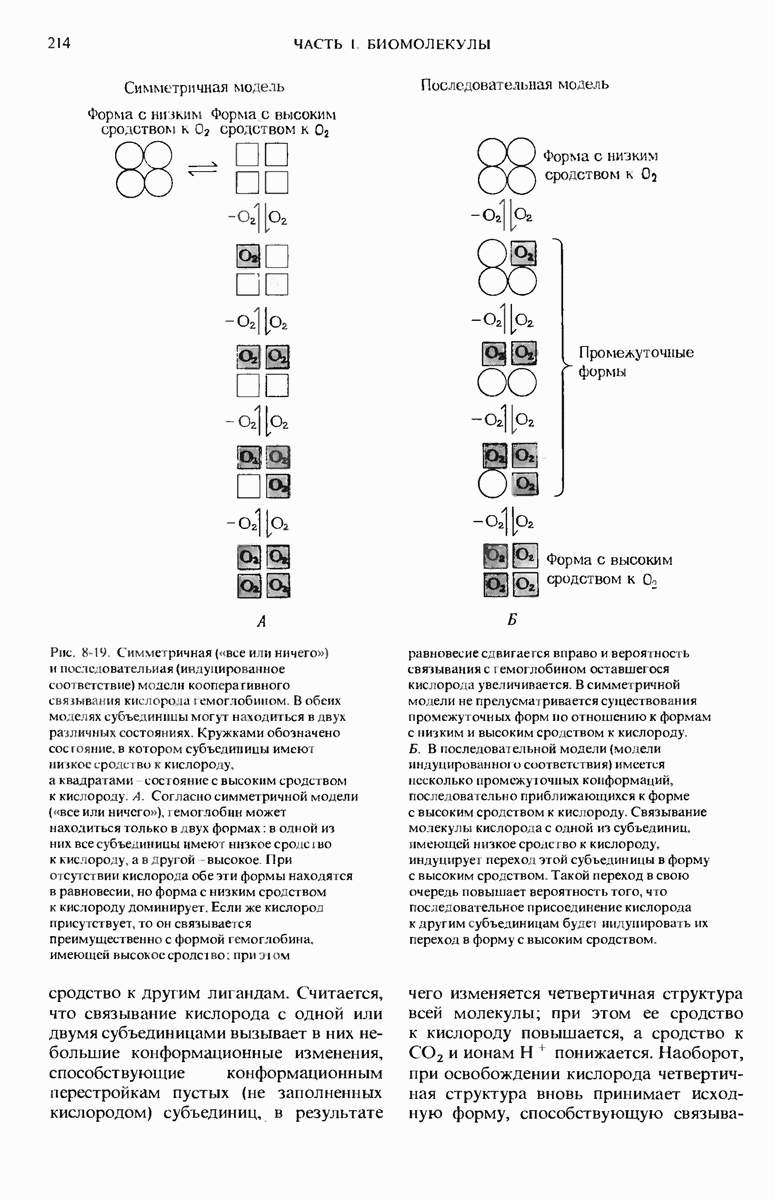
- 8.16. Оксигенация гемоглобина вызывает изменение его пространственной конформации
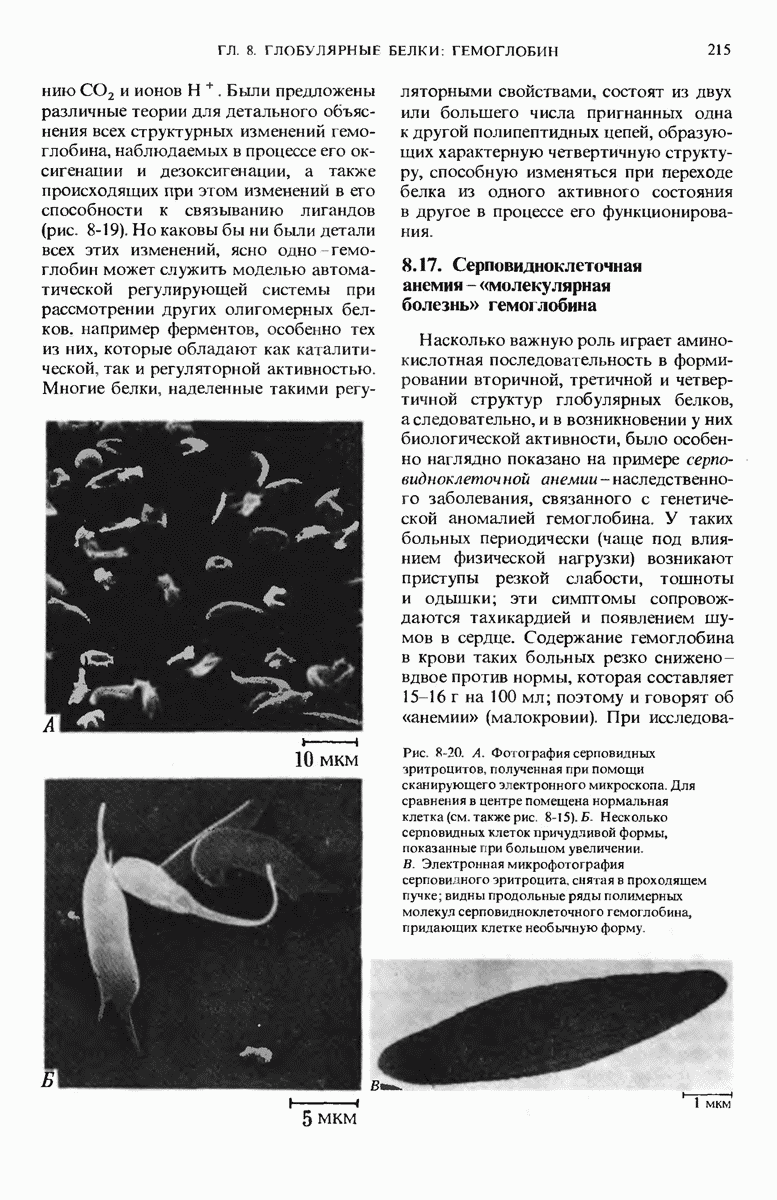
- 8.17. Серповидноклеточная анемия — «молекулярная болезнь» гемоглобина
- 8.18. Гемоглобин больных серповидноклеточной анемиеи имеет измененную аминокислотную последовательность
- 8.19. Серповидная форма эритроцитов обусловлена склонностью молекул гемоглобина S к агрегации
- 8.20. «Неправильные» аминокислоты появляются в белках в результате генных мутаций
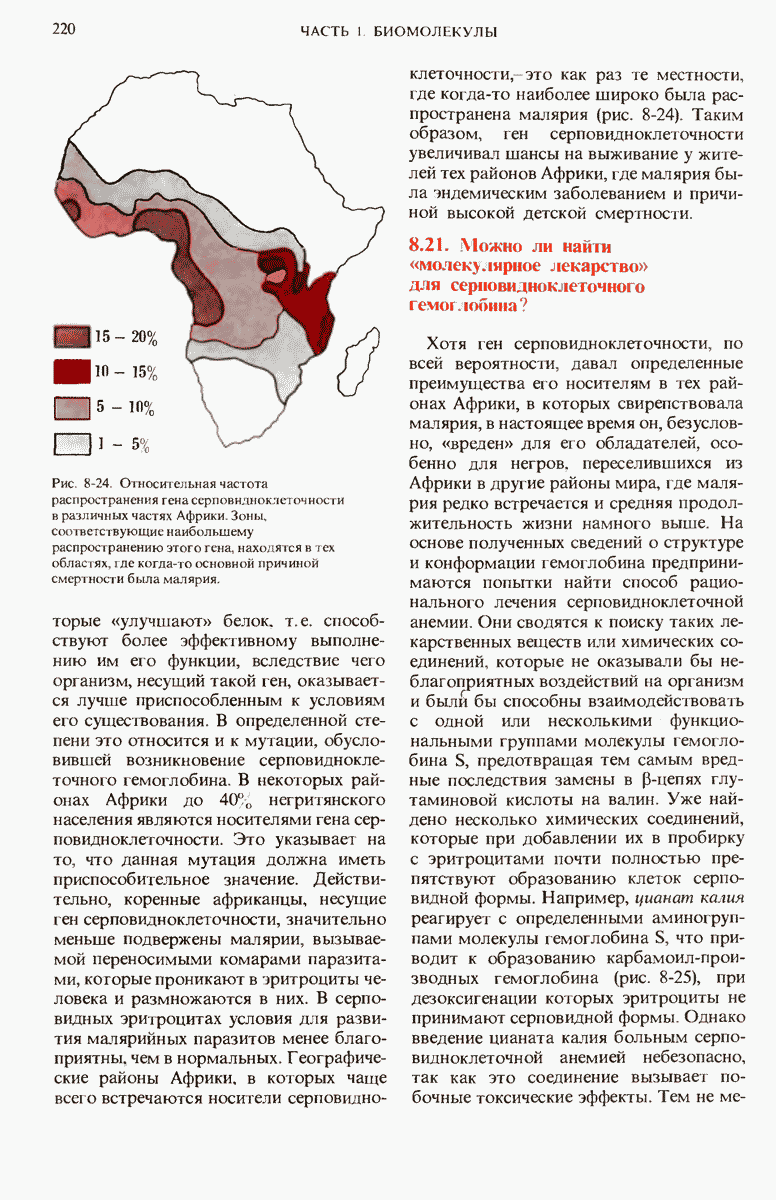
- 8.21. Можно ли найти «молекулярное лекарство» для серновидноклеточного гемоглобина?
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 9. ФЕРМЕНТЫ
- 9.1. История биохимии — это в значительной мере история исследования ферментов
- 9.2. Ферменты обнаруживают все свойства белков
- 9.3. Ферменты классифицируются на основе реакций, которые они катализируют
- 9.4. Ферменты ускоряют химические реакции, снижая энергию активации
- 9.5. Концентрация субстрата оказывает огромное влияние на скорость реакций, катализируемых ферментами
- 9.6. Существует количественная связь между концентрацией субстрата и скоростью ферментативной реакции
- 9.7. Каждый фермент имеет характерную величину Км для данного субстрата
- 9.8. Многие ферменты катализируют реакции с участием двух субстратов
- 9.9. Каждый фермент имеет определенный оптимум pH
- 9.10. Количество фермента можно определить по его активности
- 9.11. Ферменты проявляют специфичность по отношению к своим субстратам
- 9.12. Ферменты можно ингибировать определенными химическими соединениями
- 9.13. Существуют обратимые ингибиторы двух типов — конкурентные и неконкурентные
- 9.14. Неконкурентное ингибирование тоже обратимо, но не может быть ослаблено или устранено повышением концентрации субстрата
- 9.15. Факторы, определяющие каталитическую эффективность ферментов
- 9.16. Рентгеноструктурный анализ выявил важные структурные особенности ферментов
- 9.17. В ферментных системах есть «дирижер», роль которого выполняет регуляторный фермент
- 9.18. Аллостерические ферменты регулируются путем нековалентного присоединения к ним молекул модуляторов
- 9.19. Аллостерические ферменты ингибируются или активируются их модуляторами
- 9.20. Поведение аллостерических ферментов не описывается уравнением Михаэлиса — Ментеи
- 9.21. Субъединицы аллостерических ферментов сообщаются между собой
- 9.22. Некоторые ферменты регулируются путем обратной ковалентной модификации
- 9.23. Многие ферменты существуют в нескольких формах
- 9.24. Нарушение каталитической активности ферментов может быть обусловлено мутациями
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 10. ВИТАМИНЫ И МИКРОЭЛЕМЕНТЫ: ИХ РОЛЬ В ФУНКЦИОНИРОВАНИИ ФЕРМЕНТОВ
- 10.1. Витамины — незаменимые органические микрокомпоненты пищи
- 10.2. Витамины являются важными компонентами коферментов и простетических групп ферментов
- 10.3. Витамины можно разделить на два класса
- 10.4. Тиамин (витамин B1) функционирует в форме тиаминпирофосфата
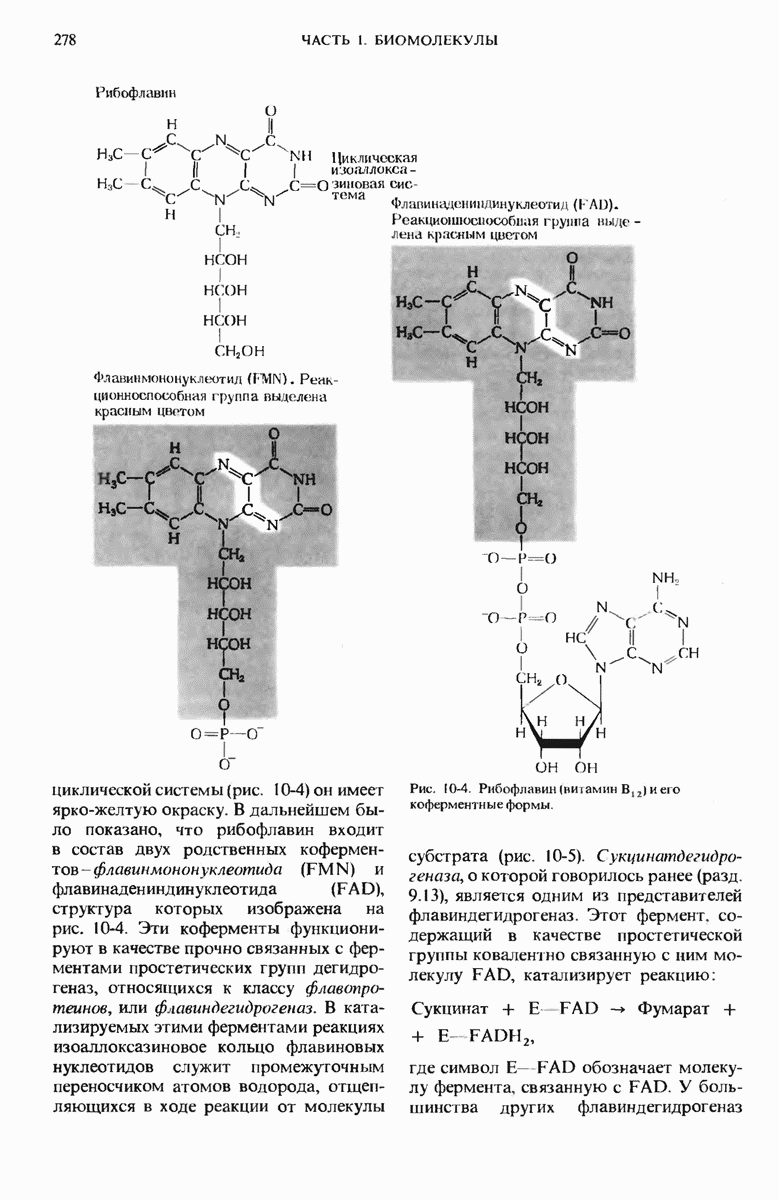
- 10.5. Рибофлавин (витамин В2) — компонент флавиновых нуклеотидов
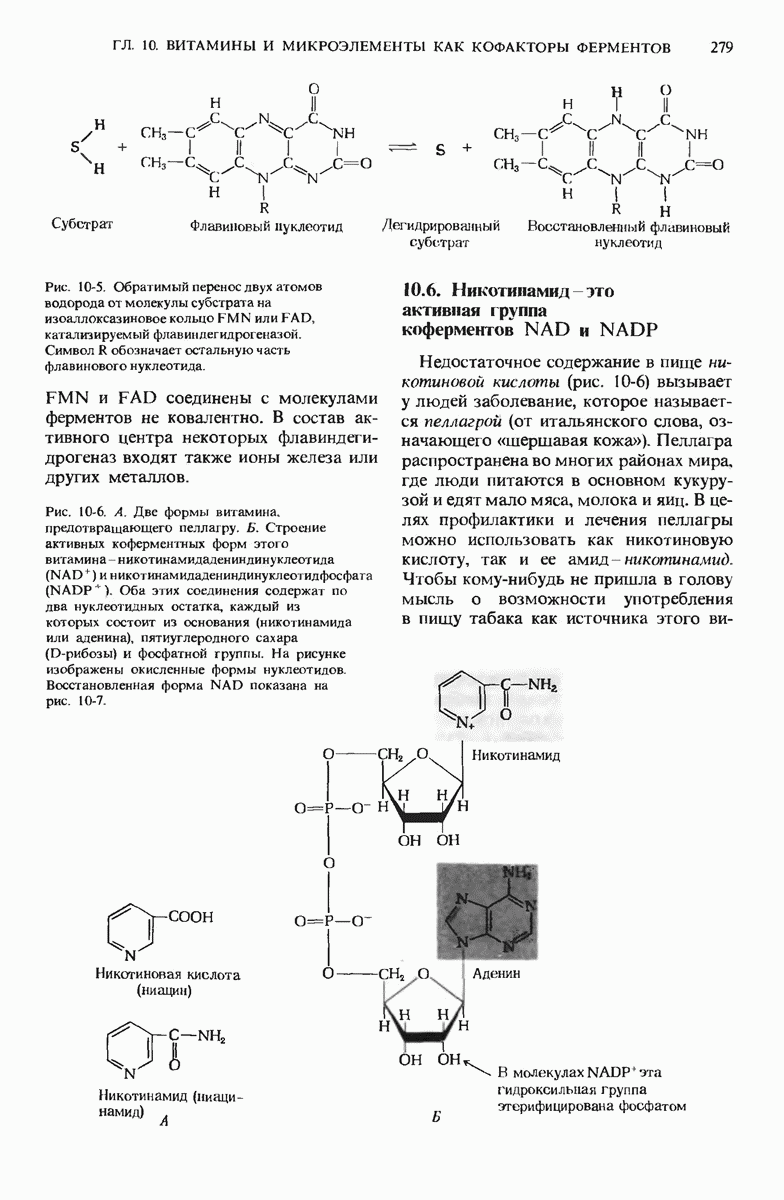
- 10.6. Никотинамид — это активная группа коферментов NAD и NADP
- 10.7. Пантотеновая кислота — компонент кофермента А
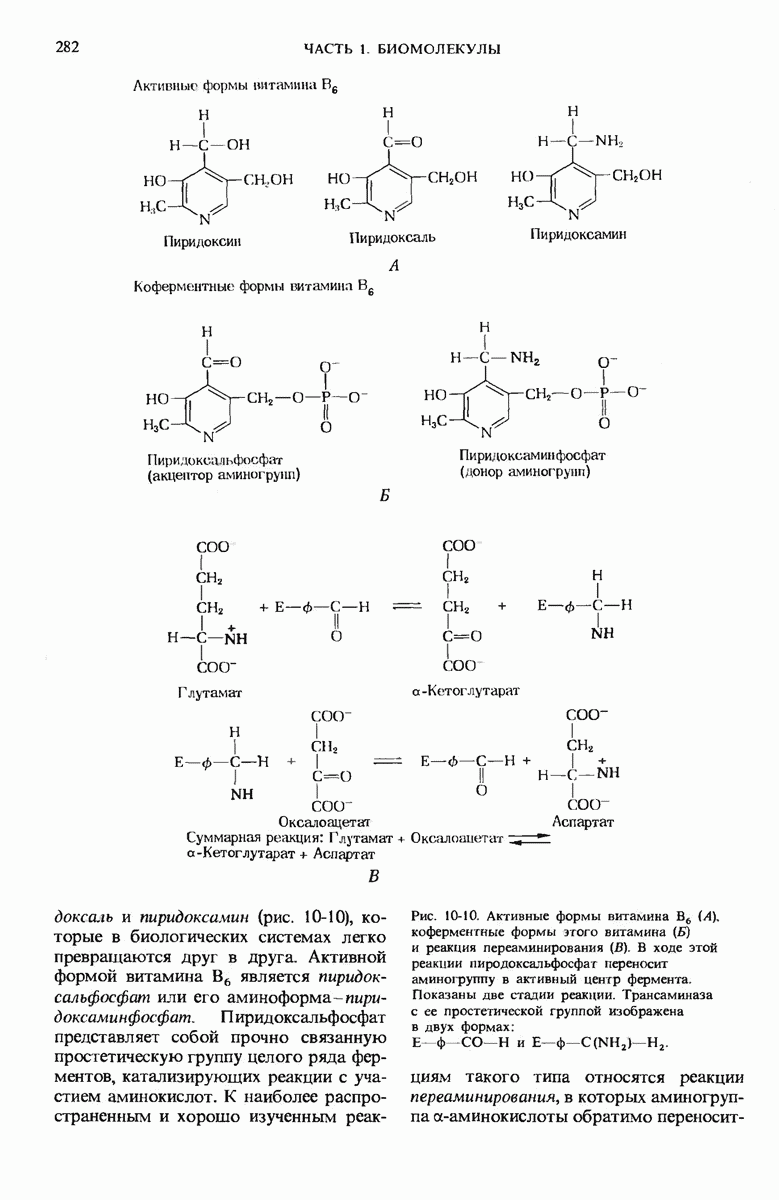
- 10.8. Пиридоксин (витамин В6) играет важную роль в метаболизме аминокислот
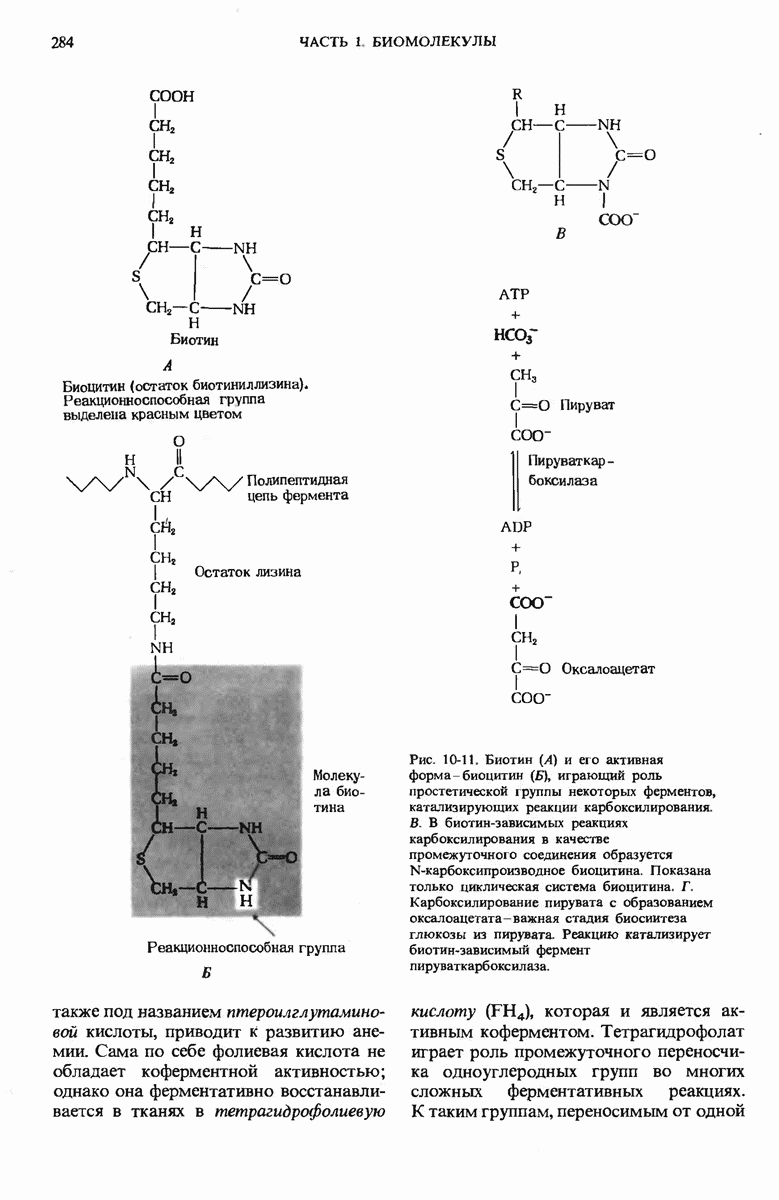
- 10.9. Биотин является активным компонентом биоцитина — простетической группы некоторых ферментов, катализирующих реакции карбоксилирования
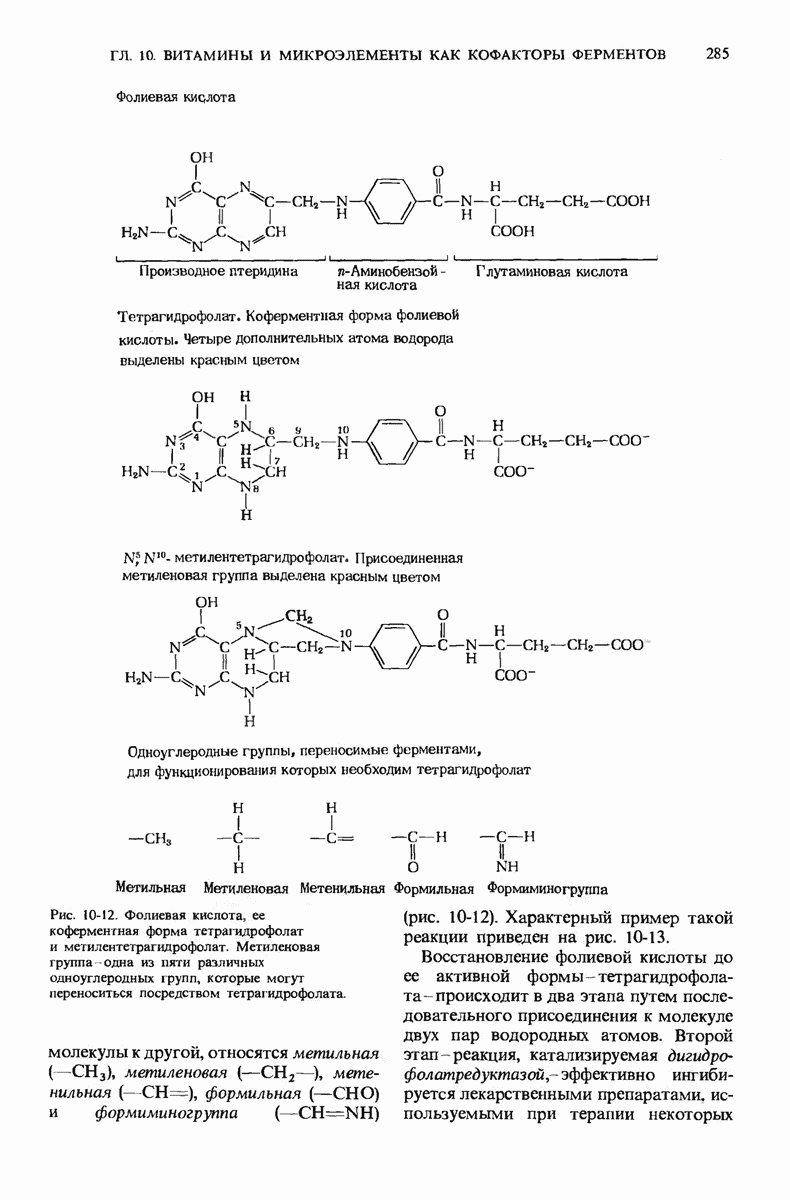
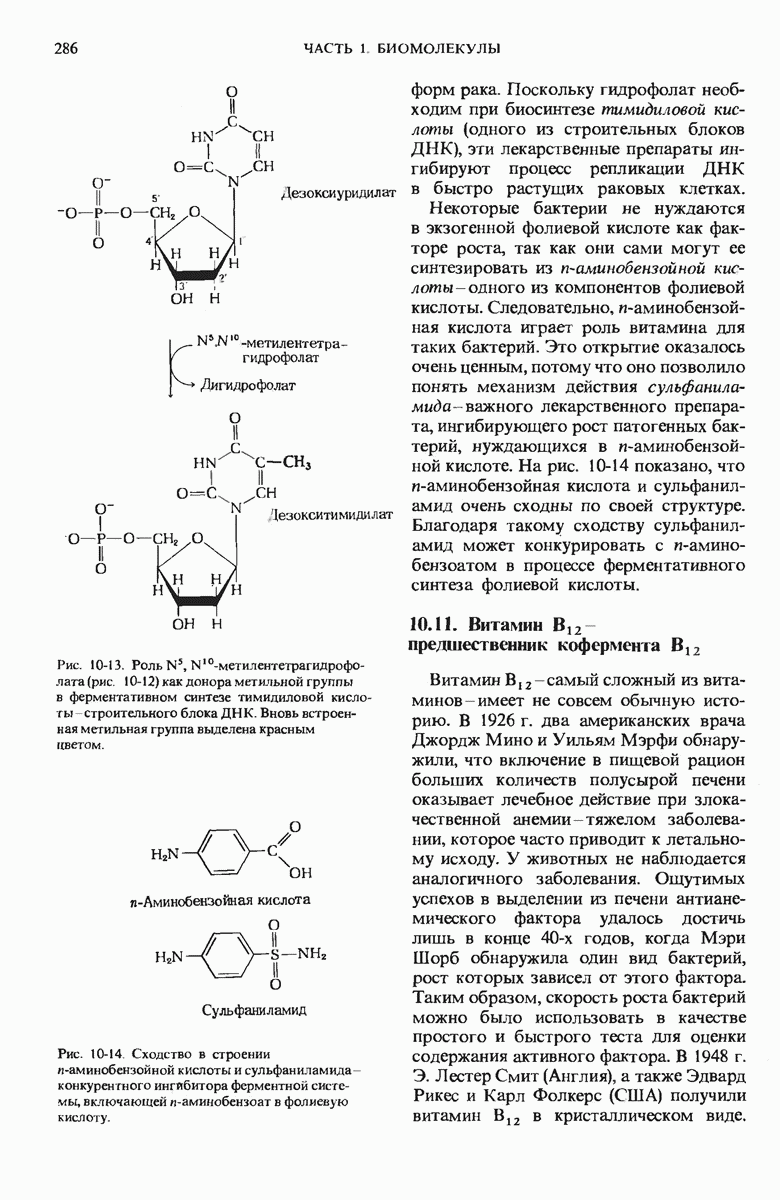
- 10.10. Фолиевая кислота служит предшественником кофермента тетрагидрофолиевой кислоты
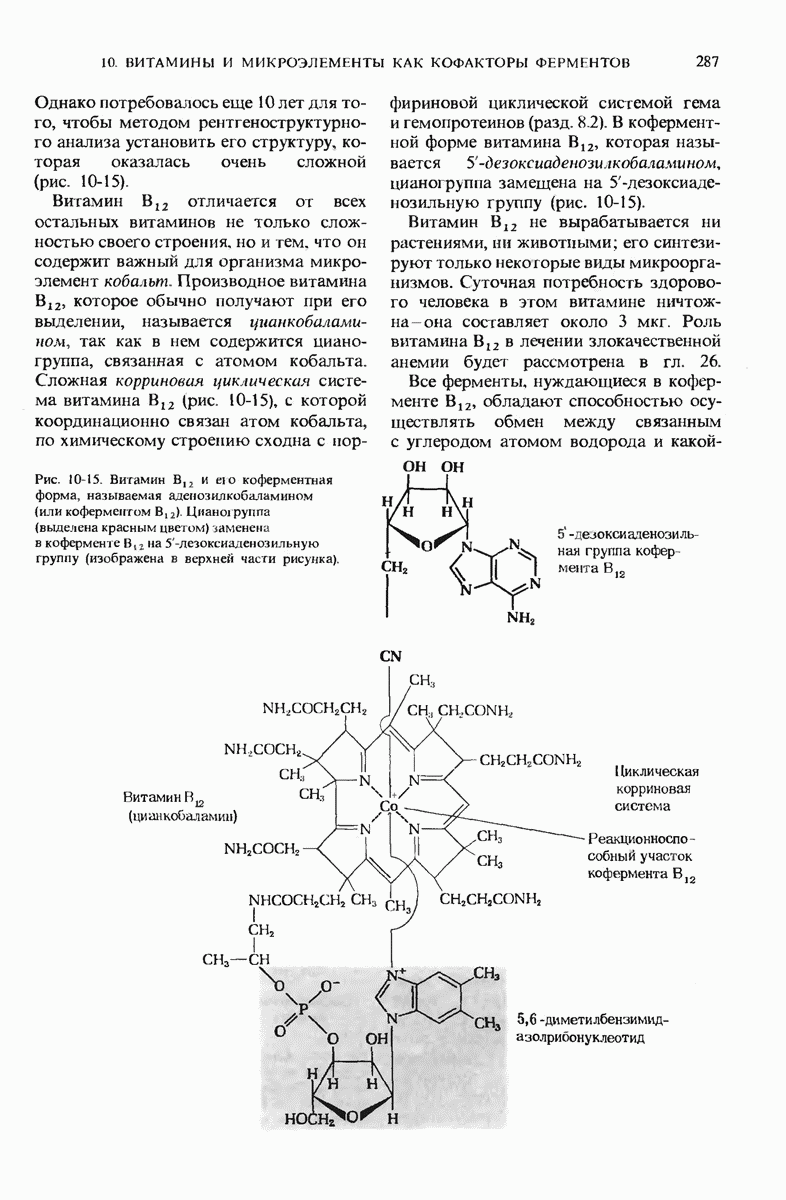
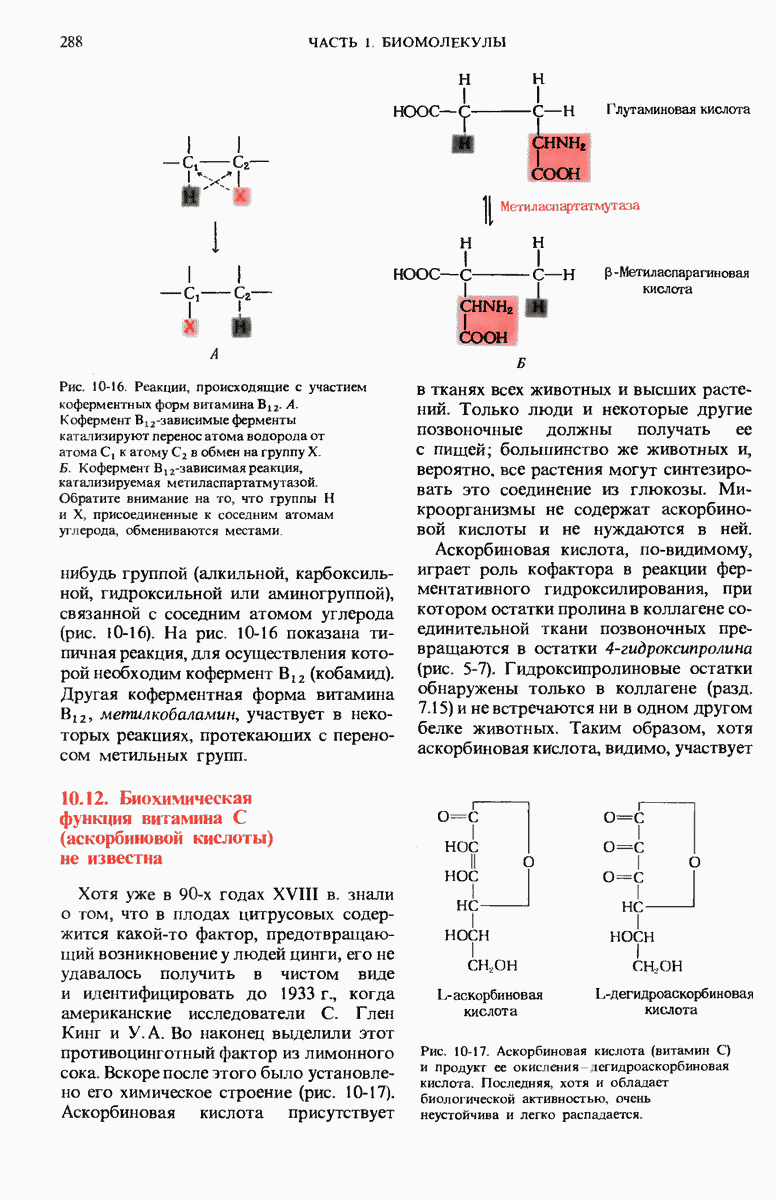
- 10.11. Витамин B12 — предшественник кофермента В12
- 10.12. Биохимическая функция витамина С (аскорбиновой кислоты) не известна
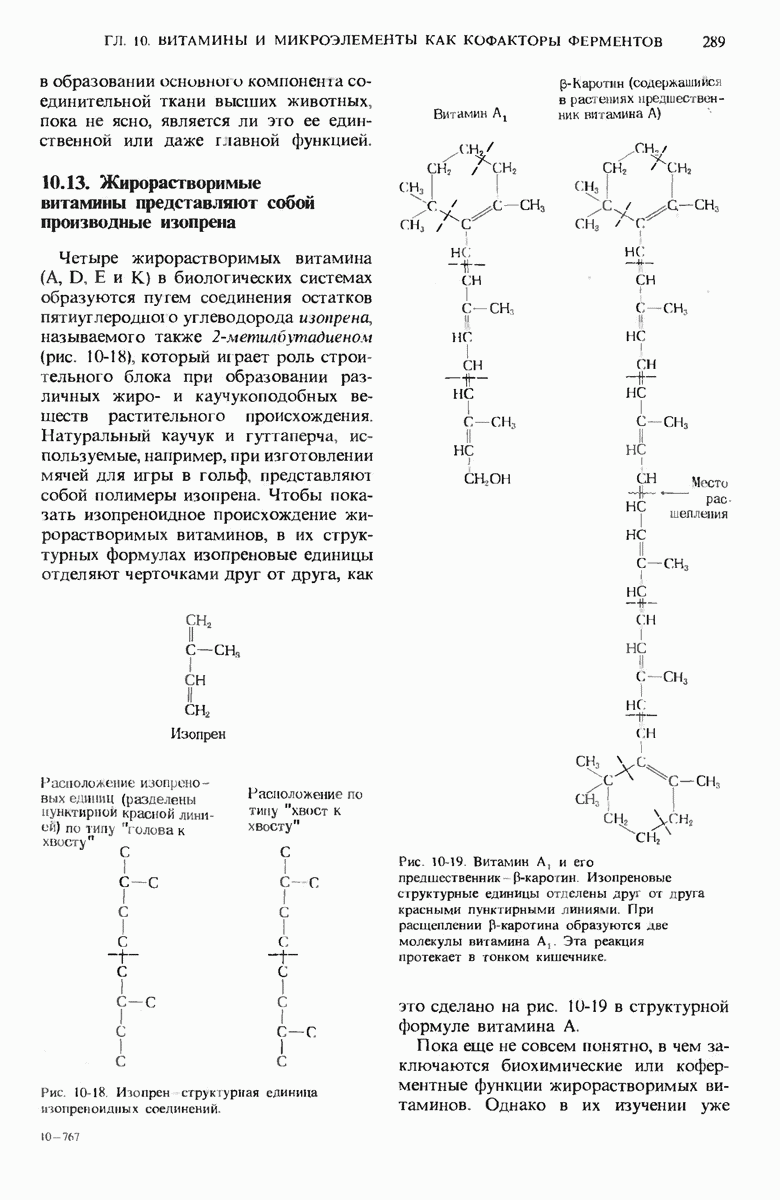
- 10.13. Жирорастворимые витамины представляют собой производные изопрена
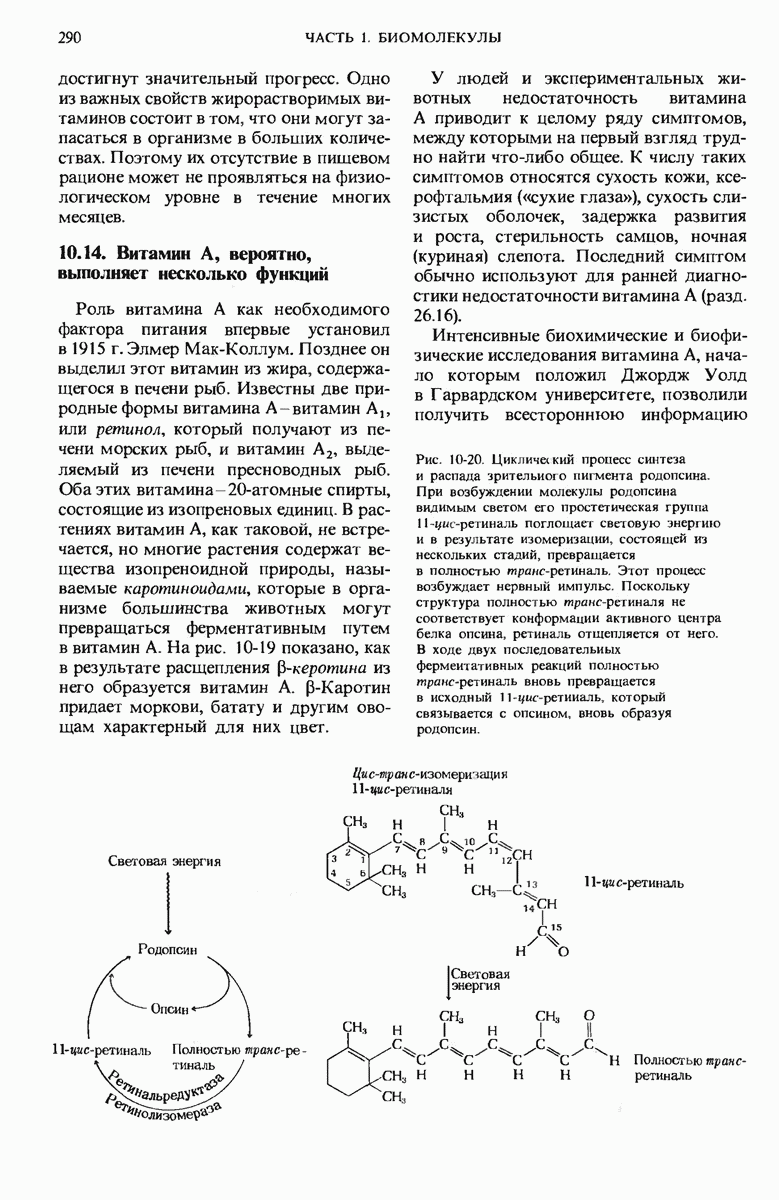
- 10.14. Витамин А, вероятно, выполняет несколько функций
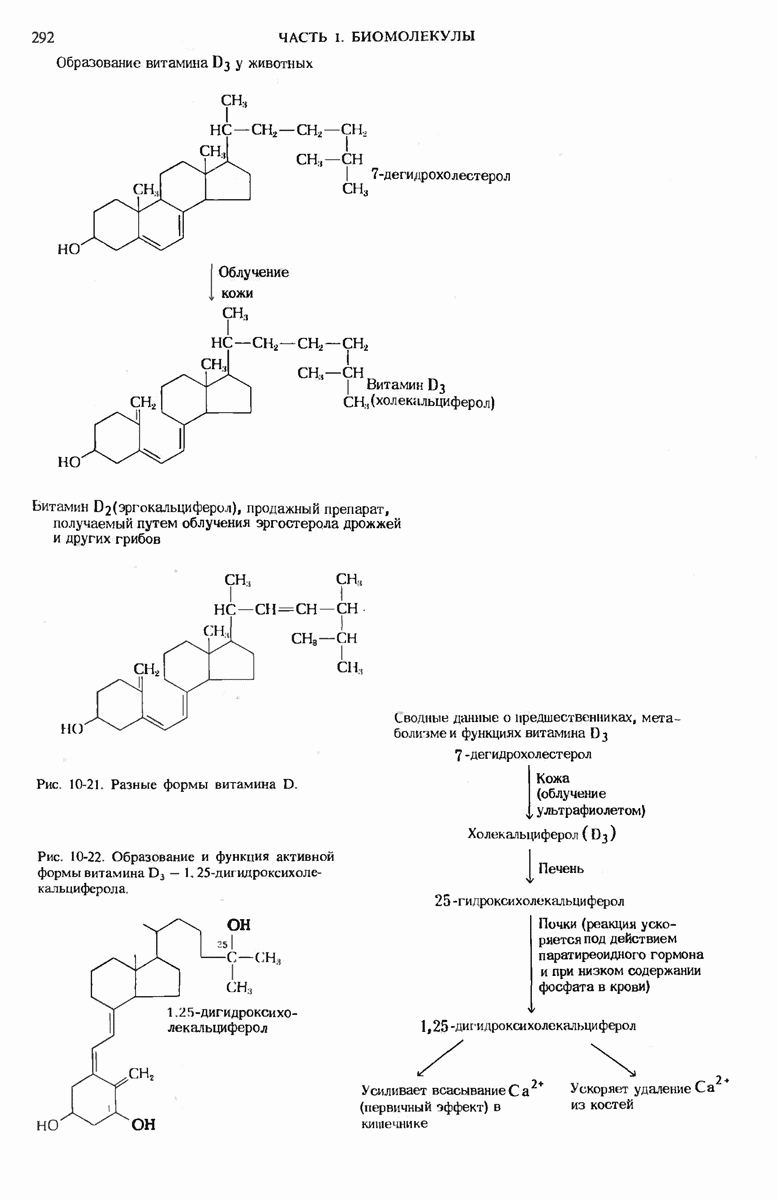
- 10.15. Витамин D — предшественник гормона
- 10.16. Витамин Е защищает клеточные мембраны от кислорода
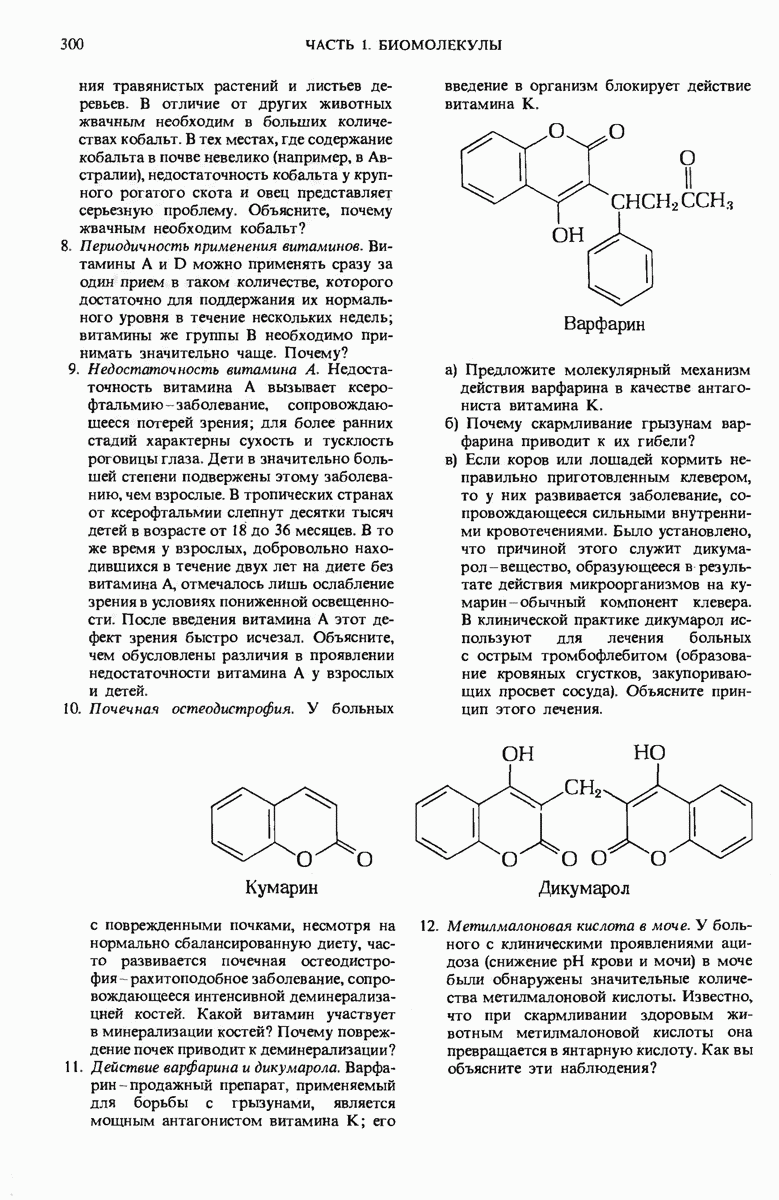
- 10.17. Витамин К-компонент карбокснлнрукнцего фермента
- 10.18. В пище животных должны содержаться многочисленные неорганические вещества
- 10.19. Для действия многих ферментов требуется железо
- 10.20. В некоторых окислительных ферментах содержится также медь
- 10.21. Для действия многих ферментов необходим цинк
- 10.22. Некоторым ферментам требуются ионы марганца
- 10.23. В состав витамина В12 входит кобальт
- 10.24. Селен является и незаменимым микроэлементом, и ядом
- 10.25. Для некоторых ферментов требуются другие микроэлементы
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и залами
- ГЛАВА 11. УГЛЕВОДЫ: СТРОЕНИЕ И БИОЛОГИЧЕСКИЕ ФУНКЦИИ
- 11.1. Углеводы делятся на три класса в зависимости от числа остатков сахаров
- 11.2. Существует два семейства моносахаридов: альдозы и кетозы
- 11.3. Моносахариды обычно содержат несколько асимметрических центров
- 11.4. Типичные моносахариды имеют циклическую структуру
- 11.5. Простые моносахариды могут служить восстановителями
- 11.6. Дисахариды содержат две моносахаридные единицы
- 11.7. Полисахариды содержат большое число моносахаридных остатков
- 11.8. Некоторые полисахариды представляют собой форму запасания «клеточного топлива»
- 11.9. Целлюлоза — наиболее распространенный структурный полисахарид
- 11.10. Клеточные стенки содержат в больших количествах структурные и защитные полисахариды
- 11.11. Гликопротеины — гибридные молекулы
- 11.12. На поверхности клеток животных присутствуют гликопротеины
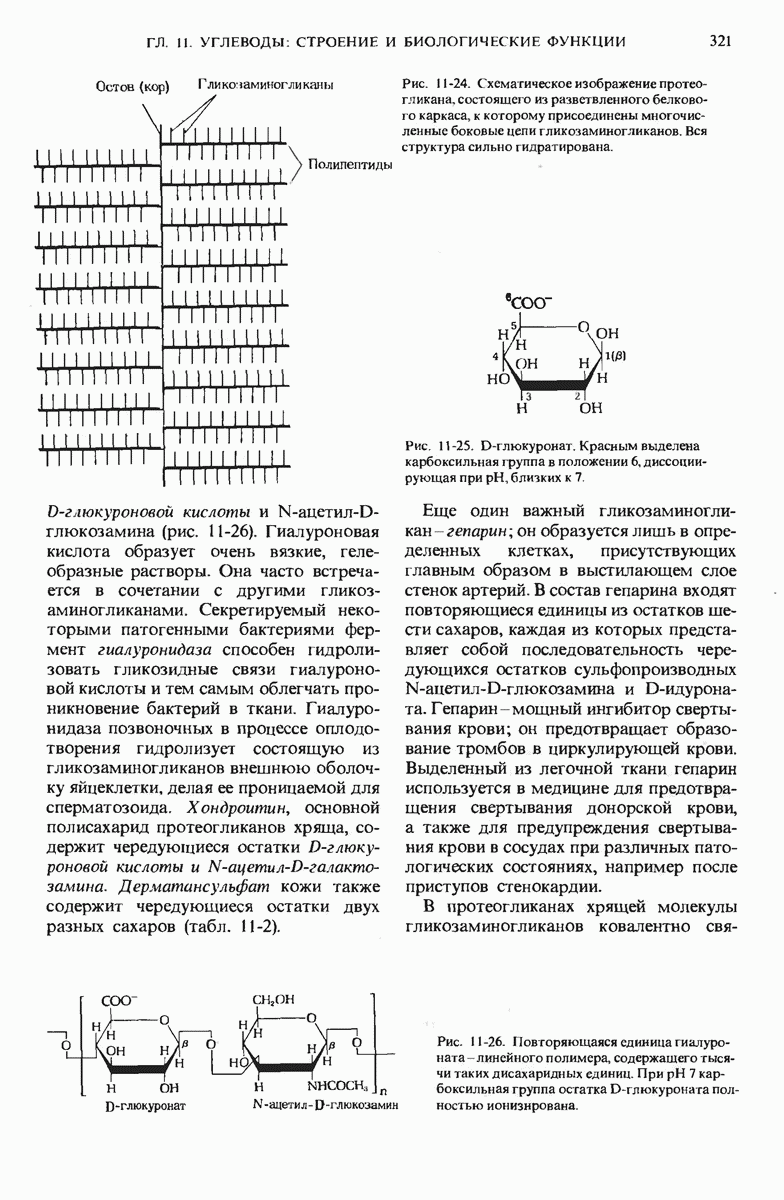
- 11.13. Гликозаминогликаны и протеогликаны — важные компоненты соединительной ткани
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 12. ЛИПИДЫ И МЕМБРАНЫ
- 12.1. Жирные кислоты — структурные компоненты большинства липидов
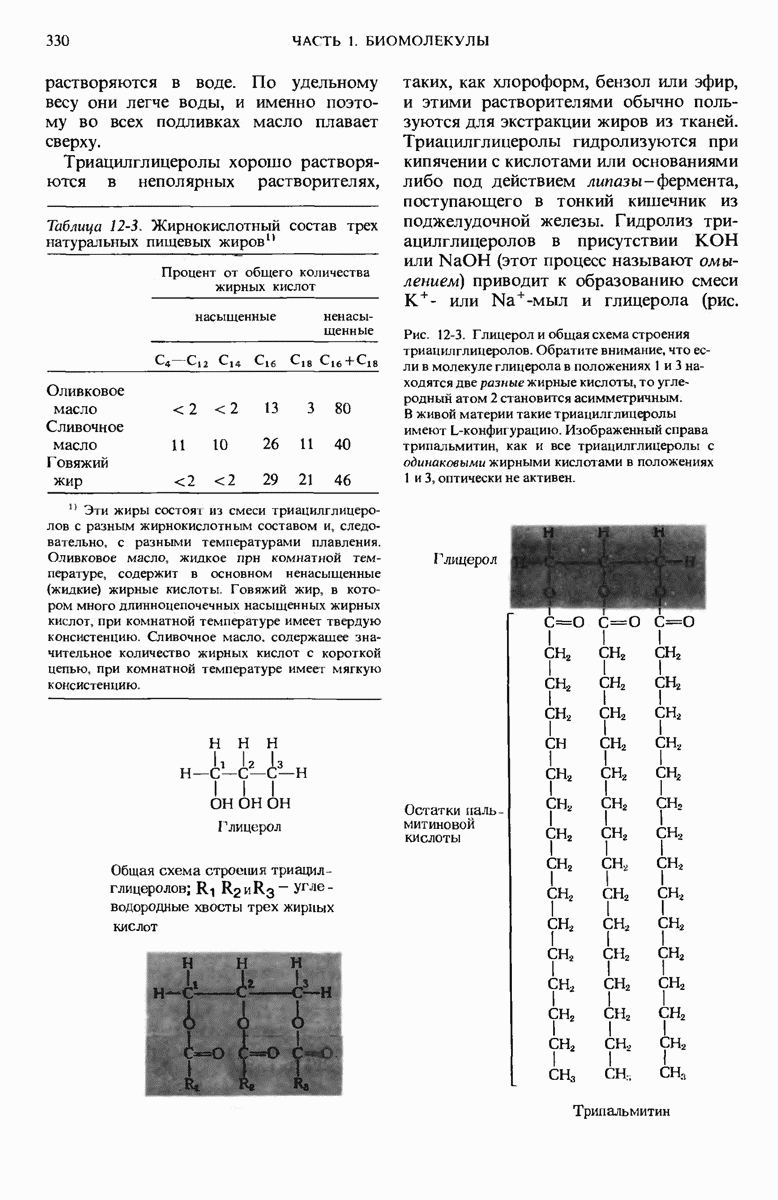
- 12.2. Триацилглицеролы — это глицероловые эфиры жирных кислот
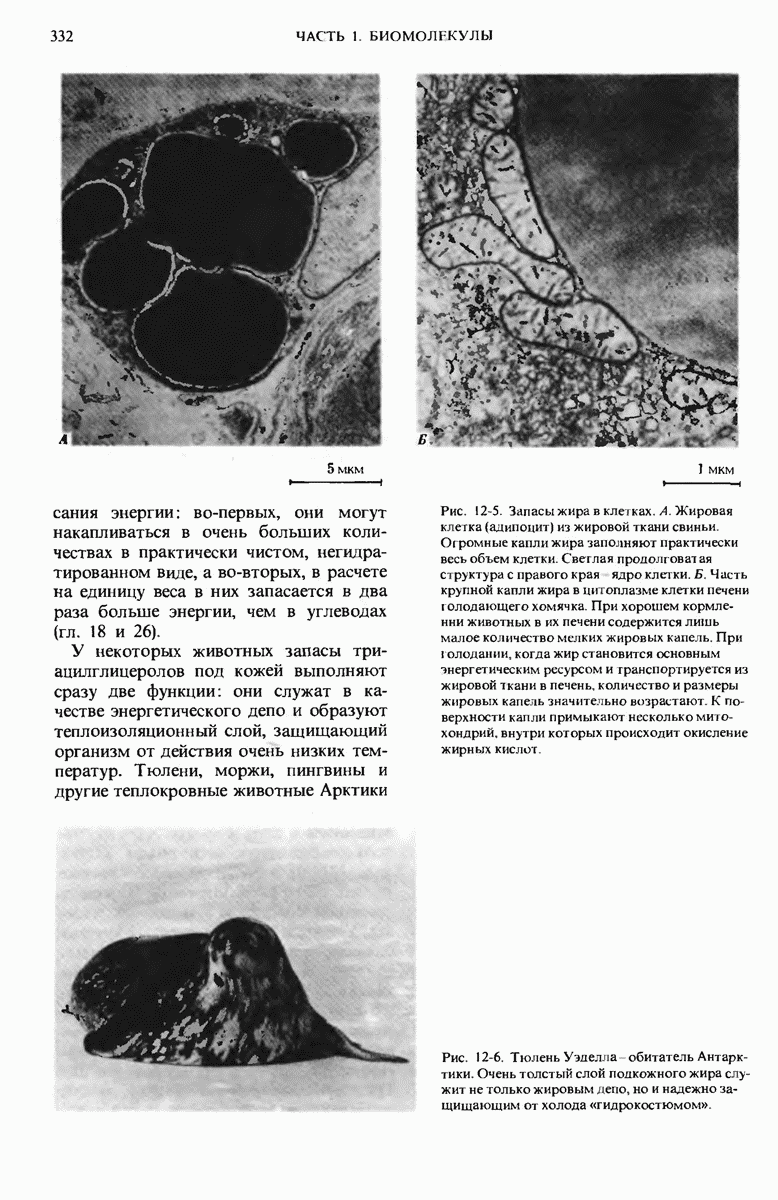
- 12.3. Триацилглицеролы — форма запасания липидов
- 12.4. Воска — эфиры жирных кислот и длинноцепочечных спиртов
- 12.5. Фосфолипиды — основные липидные компоненты мембран
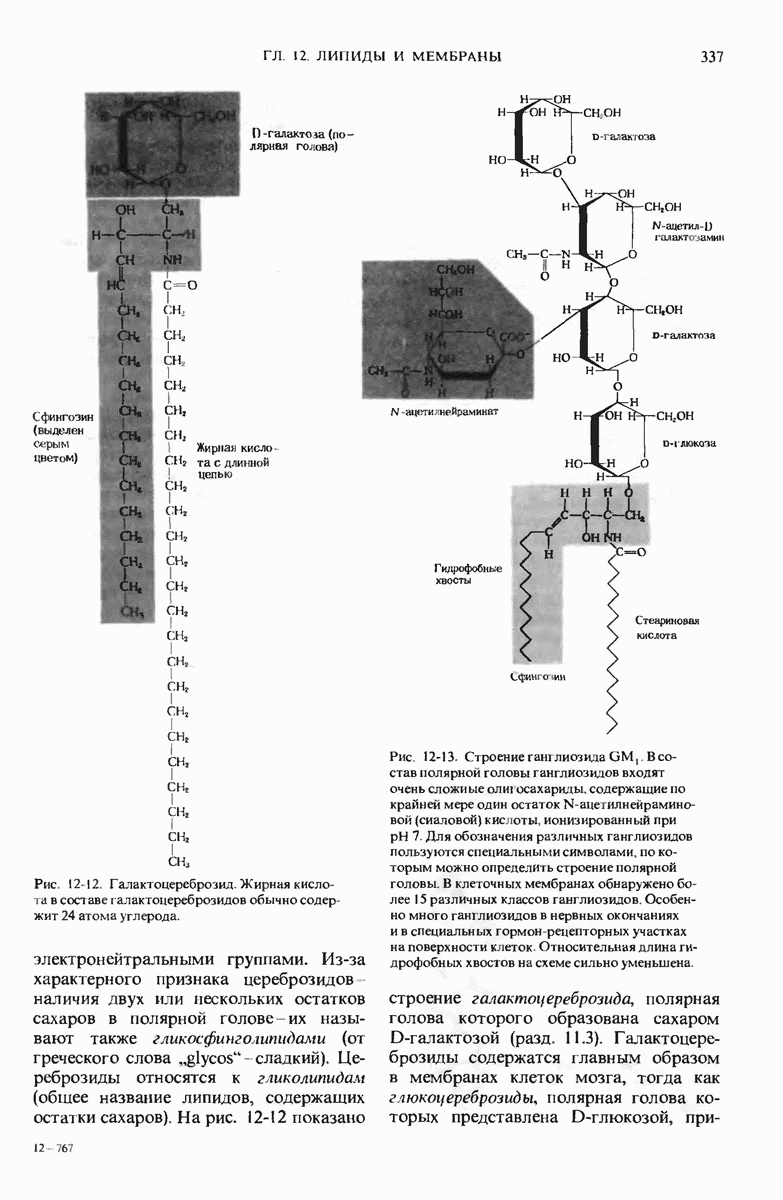
- 12.6. Сфинголипиды — также важные компоненты мембран
- 12.7. Стероиды — неомыляемые липиды, обладающие специфическими функциями
- 12.8. Липопротеины сочетают свойства липидов и белков
- 12.9. Полярные липиды образуют мицеллы, монослои и бислои
- 12.10. Полярные липиды и белки — основные компоненты мембран
- 12.11. Мембраны имеют жидкостно-мозаичную структуру
- 12.12. Мембраны асимметричны, т.е. имеют неравноценные стороны
- 12.13. Мембраны эритроцитов исследованы очень подробно
- 12.14. Лектины — специфические белки, способные связываться с определенными клетками и вызывать их агглютинацию
- 12.15. Мембраны имеют очень сложные функции
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ПРИЛОЖЕНИЕ ОТВЕТЫ