| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
1.7. Структура полимеров, стекла и керамики
Полимерами называют вещества с большой молекулярной массой  которых молекулы состоят из одинаковых групп атомов-звеньев (рис. 1.26). Каждое звено представляет собой измененную молекулу исходного низкомолекулярного вещества-мономера. При получении полимеров молекулы мономеров объединяются друг с другом и образуют длинные линейные молекулы или макромолекулы, в которых атомы соединены ковалентными связями. В зависимости от характера связей между линейными молекулами полимеры разделяют на термопластичные и термореактивные. Различие между ними особенно четко обнаруживается при нагреве.
которых молекулы состоят из одинаковых групп атомов-звеньев (рис. 1.26). Каждое звено представляет собой измененную молекулу исходного низкомолекулярного вещества-мономера. При получении полимеров молекулы мономеров объединяются друг с другом и образуют длинные линейные молекулы или макромолекулы, в которых атомы соединены ковалентными связями. В зависимости от характера связей между линейными молекулами полимеры разделяют на термопластичные и термореактивные. Различие между ними особенно четко обнаруживается при нагреве.
Термопластичные полимеры способны многократно размягчаться при нагреве и твердеть при охлаждении без изменения своих свойств.
Термореактивные полимеры при нагреве остаются твердыми вплоть до полного термического разложения. Это различие поведения при нагреве объясняется тем, что у термопластичных полимеров между молекулами действуют относительно слабые силы Ван-дер-Ваальса. При нагреве связи между

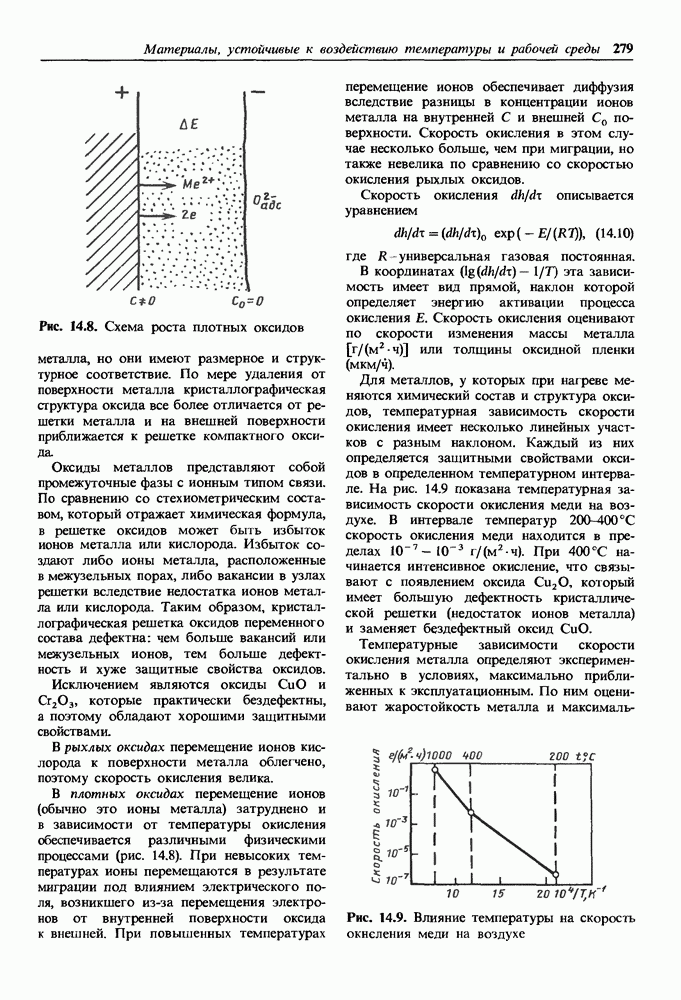
Рис. 1.26. Схема строения линейной макромолекулы
молекулами значительно ослабляются, материал становится мягким и податливым. У термореактивных полимеров кроме сил Ван-дер-Ваальса имеются поперечные ковалентные связи между молекулами. Благодаря им термореактивный материал остается твердым при нагреве.
Линейные молекулы имеют главные цепи и боковые группы (см. рис. 1.26). При молекулярной массе  — 10б в линейной молекуле объединяются сотни звеньев и длина главной цепи во много раз больше размеров боковых групп. У большинства полимеров главные цепи состоят преимущественно из атомов углерода, у кремнийорганических полимеров они образованы чередующимися атомами кислорода и кремния.
— 10б в линейной молекуле объединяются сотни звеньев и длина главной цепи во много раз больше размеров боковых групп. У большинства полимеров главные цепи состоят преимущественно из атомов углерода, у кремнийорганических полимеров они образованы чередующимися атомами кислорода и кремния.
Боковые группы образуют атомы (водород, галоиды), радикалы ( и др.), короткие полимерные цепи из нескольких звеньев. Очевидно, что при наличии боковых групп нескольких видов имеются возможности разместить их вдоль главной цепи как неупорядоченно, так и в определенном порядке. Полимеры с неупорядоченным чередованием групп называются нерегулярными, а с упорядоченным - регулярными.
и др.), короткие полимерные цепи из нескольких звеньев. Очевидно, что при наличии боковых групп нескольких видов имеются возможности разместить их вдоль главной цепи как неупорядоченно, так и в определенном порядке. Полимеры с неупорядоченным чередованием групп называются нерегулярными, а с упорядоченным - регулярными.
Структура молекул определяется способом производства полимера. При обработке полимеров (нагрев, растворение и т. д.) структура молекул почти не изменяется, и нельзя, например, нерегулярный полимер сделать регулярным.
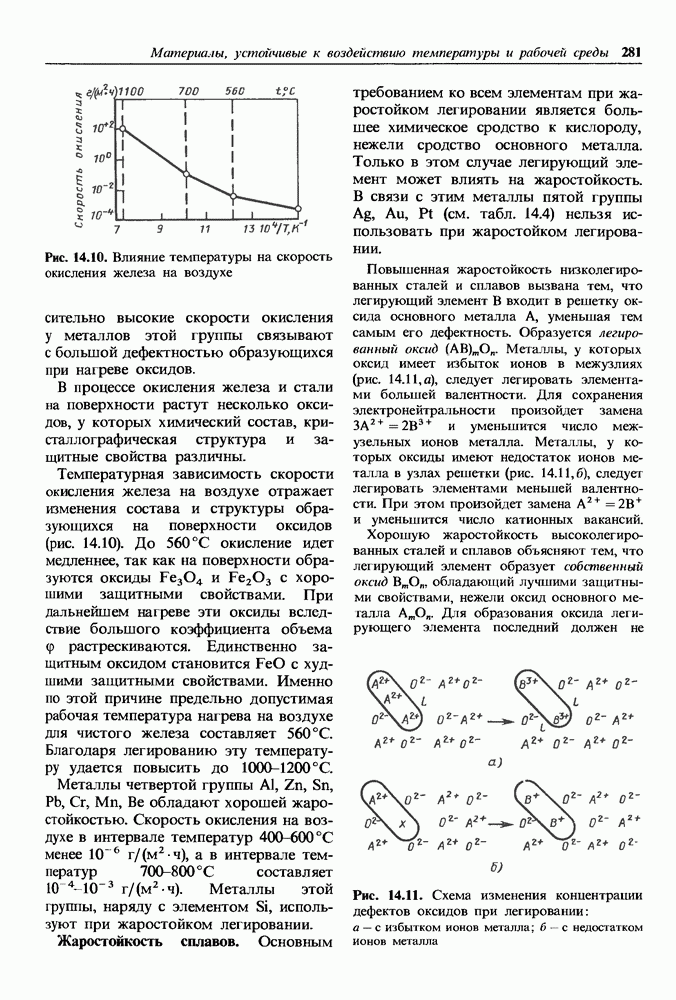
Общая структура полимеров складывается из структуры молекул и надмолекулярной структуры, т. е. взаимной укладки линейных молекул в полимерном веществе. Надмолекулярная структура появляется под влиянием сил притяжения между молекулами и теплового движения самих молекул. Наиболее характерной и важной формой теплового движения макромолекул являются повороты частей молекул по отношению друг к другу (рис. 1.27). Равновесному состоянию соответствуют определенные значения углов между связями а (см. рис. 1.27).

Рис. 1.27. Схема поворотов вокруг связей в главной цепи макромолекулы
Форма линейной молекулы все время изменяется. Установлено, что ее равновесной формой является эллипсоид. Любые неравновесные изменения формы молекулы быстро уничтожаются при тепловом движении, когда повороты вокруг связей внутри макромолекулы легко осуществляются. Для нерегулярных полимеров характерны пачечные структуры, когда на сравнительно больших участках главные цепи соседних молекул располагаются параллельно. У регулярных полимеров типичными надмолекулярными структурами являются кристаллы. Пачечные структуры и кристаллы образуются при повышенных температурах, когда внутри макромолекулы легко происходят сдвиги, повороты и т. д.
Макромолекулы в полимерном веществе не упакованы плотно, и мерой плотности упаковки является так называемый свободный объем, т. е. разность между фактическим удельным объемом вещества и теоретическим удельным объемом при самой плотной упаковке. При нагреве свободный объем увеличивается. В зависимости от свободного объема полимерное вещество находится в одном из физических состояний: стеклообразном, высокоэластичном, вязкотекучем. Переходы из одного состояния
в другое происходят без выделения или поглощения теплоты. Температуры переходов называются температурами стеклования  и текучести
и текучести 
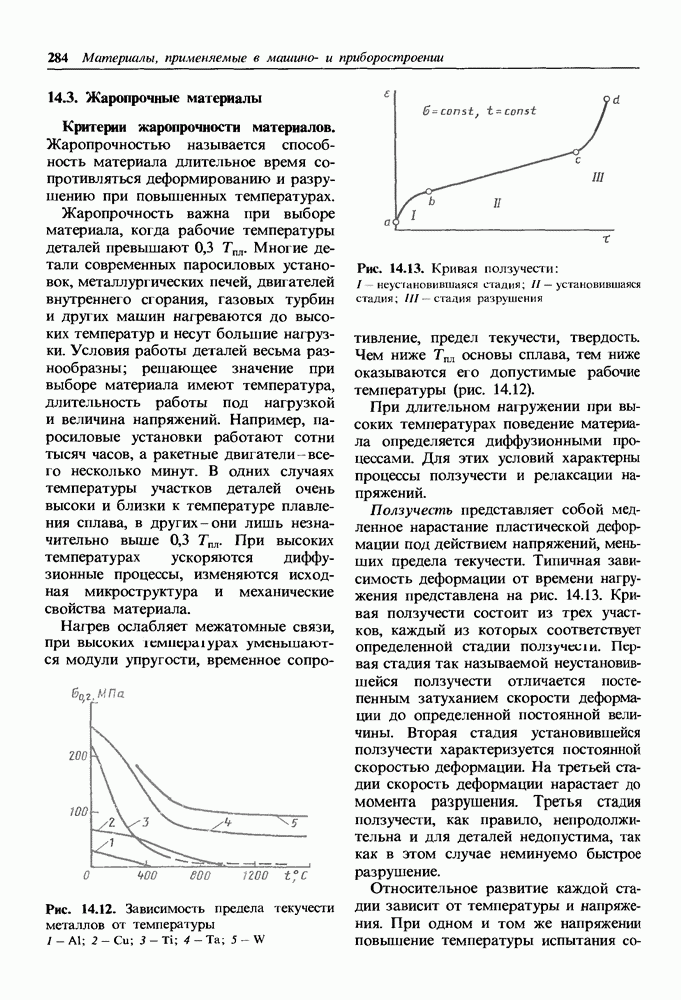
Различия между физическими состояниями полимеров наглядно проявляются при деформировании (рис. 1.28). В стеклообразном состоянии повороты вокруг связей в макромолекулах затруднены, полимер является упругим твердым телом. Под нагрузкой упругая деформация не превышает нескольких процентов и падает до нуля при снятии нагрузки. При деформации происходит искажение валентных углов а.
Высокоэластичное состояние появляется тогда, когда свободный объем становится  . В зтом состоянии полимер ведет себя как эластичное тело. Под действием нагрузки скрученные макромолекулы выпрямляются и вытягиваются, деформация достигает 500-800%. Расстояния между атомами в макромолекулах при этом меняются незначительно. При снятии нагрузки тепловое движение за доли секунды возвращает макромолекулы к равновесным формам, и поэтому высокоэластичная деформация обратима.
. В зтом состоянии полимер ведет себя как эластичное тело. Под действием нагрузки скрученные макромолекулы выпрямляются и вытягиваются, деформация достигает 500-800%. Расстояния между атомами в макромолекулах при этом меняются незначительно. При снятии нагрузки тепловое движение за доли секунды возвращает макромолекулы к равновесным формам, и поэтому высокоэластичная деформация обратима.
В вязкотекучем состоянии полимер ведет себя как вязкая жидкость. Под нагрузкой макромолекулы выпрямляются и скользят друг относительно друга. Главную часть деформации составляет необратимое вязкое течение. Течение прекращается после прекращения действия нагрузки, и вязкая жидкость сохраняет полученную форму. Нагрев сопровождается разрывом ковалентных связей в макромолекулах. Число таких разрывов заметно повышается выше  а начиная с температуры разложения гразр термический распад макромолекул с выделением низкомолекулярных соединений быстро приводит к полному разрушению полимера.
а начиная с температуры разложения гразр термический распад макромолекул с выделением низкомолекулярных соединений быстро приводит к полному разрушению полимера.
Таким образом, молекулярная структура полимера остается неизменной в разных физических состояниях (если не учитывать разрывов ковалентных связей в отдельных макромолекулах при нагреве). В то же время надмолекулярная структура легко изменяется. Неравновесные надмолекулярные структуры при нагреве выше  заменяются равновесными. При охлаждении ниже
заменяются равновесными. При охлаждении ниже  в материале легко фиксируются неравновесные надмолекулярные структуры. Если растянуть нагретый выше
в материале легко фиксируются неравновесные надмолекулярные структуры. Если растянуть нагретый выше  термопластичный полимер и, не снимая нагрузки, охладить его ниже
термопластичный полимер и, не снимая нагрузки, охладить его ниже  то высокоэластичное состояние «замораживается», вытянутые макромолекулы сохранят свою форму и после снятия нагрузки. Ориентация молекул по направлению растягивающего усилия обусловливает анизотропию свойств. Отклонения надмолекулярной структуры от равновесной имеются в изделиях из полимеров и влияют на прочность. Регулярные полимеры кристаллизуются при переохлаждении ниже равновесной температуры кристаллизации
то высокоэластичное состояние «замораживается», вытянутые макромолекулы сохранят свою форму и после снятия нагрузки. Ориентация молекул по направлению растягивающего усилия обусловливает анизотропию свойств. Отклонения надмолекулярной структуры от равновесной имеются в изделиях из полимеров и влияют на прочность. Регулярные полимеры кристаллизуются при переохлаждении ниже равновесной температуры кристаллизации  Кристаллизация регулярных полимеров сопровождается выделением теплоты и
Кристаллизация регулярных полимеров сопровождается выделением теплоты и

Рис. 1.28. Зависимость деформации полимеров от температуры: а — термопластичный аморфный полимер; I — стеклообразное состояние; II — высокоэластичное состояние; III — текучее состояние; б — полимер с редкими поперечными связками; в — термопластичный кристаллический полимер; г — полимер с частыми поперечными связями
уменьшением объема. При кристаллизации гибкие макромолекулы укладываются в порядке, который соответствует определенной кристаллической решетке. Степень кристаллизации обычно высока, не менее 60-70%, однако полная кристаллизация не достигается. Температура кристаллизации  лежит выше
лежит выше  и благодаря кристаллам полимерные материалы остаются упругими и твердыми в интервале температур
и благодаря кристаллам полимерные материалы остаются упругими и твердыми в интервале температур  при которых соответствующие по химическому составу некристаллические полимеры находятся в высокоэластичном состоянии.
при которых соответствующие по химическому составу некристаллические полимеры находятся в высокоэластичном состоянии.
Надмолекулярные структуры в термореактивных полимерах зависят от плотности поперечных связей. При небольшой плотности поперечных связей образуются как пачечные структуры, так и кристаллы. При увеличении плотности поперечных связей возможность образования надмолекулярных структур уменьшается.
В кристаллических полимерах размеры кристаллов и их форма зависят от конкретных условий кристаллизации, и механические свойства определяются полученной структурой.
Стекло представляет собой аморфное вещество, образующееся при сплавлении оксидов или безоксидных соединений. Стеклообразующими являются оксиды  а также некоторые бескислородные соединения мышьяка, селена, теллура.
а также некоторые бескислородные соединения мышьяка, селена, теллура.
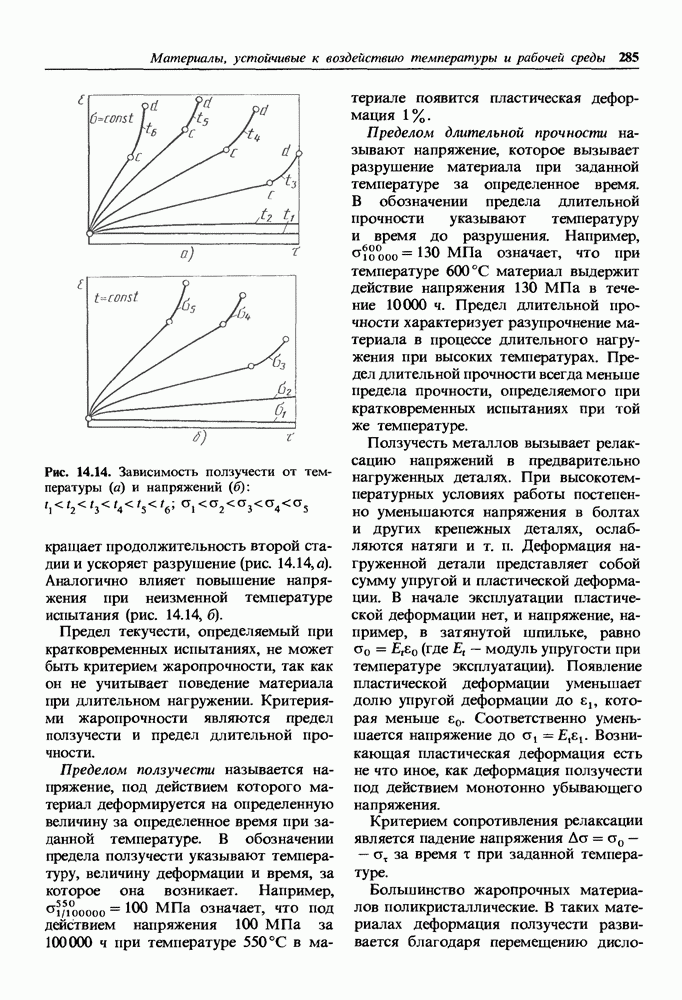
Основу стекла образует объемная сетка из однородных структурных элементов. В наиболее простом по составу кварцевом стекле такими элементами являются тетраэдры  которые соединяются своими вершинами (рис. 1.29). Из таких же тетраэдров образована структура кристаллического кварца. Различие между двумя веществами одинакового химического состава объясняется размещением
которые соединяются своими вершинами (рис. 1.29). Из таких же тетраэдров образована структура кристаллического кварца. Различие между двумя веществами одинакового химического состава объясняется размещением  Углы между связями кремний — кислород в соседних тетраэдрах в кварцевом стекле меняются в широких пределах (120 — 180°), чем и объясняется неупорядоченное расположение тетраэдров
Углы между связями кремний — кислород в соседних тетраэдрах в кварцевом стекле меняются в широких пределах (120 — 180°), чем и объясняется неупорядоченное расположение тетраэдров 

Рис. 1.29. Расположение тетраэдров  в стекле (а — угол между связями
в стекле (а — угол между связями 
В кристаллическом кварце тетраэдры  размещены упорядоченно и образуют кристаллическую решетку, в этом случае значения углов между связями
размещены упорядоченно и образуют кристаллическую решетку, в этом случае значения углов между связями  находятся в более узком интервале. Структура аморфного стекла возникает при охлаждении стеклянной массы, когда повышение ее вязкости препятствует кристаллизации.
находятся в более узком интервале. Структура аморфного стекла возникает при охлаждении стеклянной массы, когда повышение ее вязкости препятствует кристаллизации.
Основную массу промышленных стекол составляют силикатные стекла с добавками других оксидов. Эти стекла по сравнению с кварцевым стеклом размягчаются при более низких температурах и легче перерабатываются в изделия. В силикатных стеклах атомы соединяются ковалентно-ионными связями; в объемную сетку кроме кремния и кислорода входят также алюминий, титан, германий, бериллий; ионы щелочных и щелочно-земельных металлов размещаются в ячейках этой сетки. Усложнение химического состава силикатных стекол приводит к изменению их свойств, в том числе и цвета, и является причиной структурной неоднородности.
При охлаждении однофазный расплав расслаивается на две или несколько жидких фаз разного химического состава. Затвердевшее стекло имеет многофазную структуру, каждая из фаз остается аморфной. Расслоение силикатных стекол - характерная особенность их структуры.
При определенном соотношении содержания кремния, кислорода и других
элементов очень трудно предупредить зарождение и рост кристаллов. Кристаллизация или «расстекловывание» с образованием крупных кристаллов отрицательно влияет на прочность и прозрачность стекла. Кристаллизацию предупреждают подбором химического состава стекла и условий его варки.
Напряжения в стеклянных изделиях из-за различия плотности в разных участках устраняют нагревом, достаточным для перестройки элементов структуры и выравнивания плотности.
Керамикой называют материалы, полученные при высокотемпературном спекании минеральных порошков. При нагреве исходные вещества взаимодействуют между собой, образуя кристаллическую и аморфную фазу. Керамика представляет собой пористый материал, содержащий ковалентные или ионные кристаллы — сложные оксиды, карбиды или твердые растворы на их основе. Аморфная фаза является стеклом, которое по своему химическому составу отличается от кристаллов. Керамический материал содержит одну или несколько кристаллических фаз, отдельные виды керамики совсем не имеют стекла в своей структуре. Как правило, керамика имеет поликристаллическую структуру с прослойками стекла и с беспорядочным расположением зерен и поэтому однородна по свойствам.
Характерной особенностью керамических материалов является хрупкость. Сопротивление разрушению тем выше, чем мельче кристаллы и чем меньше пористость. Например, плотная микрокристаллическая керамика на основе  с размерами зерен 1-5 мкм в 5-6 раз прочнее обычной. Изделия из плотной мелкозернистой керамики - тонкой керамики - получают по более сложной технологии, и поэтому такие изделия дороги. Пористую керамику используют в качестве огнеупорных материалов, фильтров, диэлектриков в электротехнике. Более прочную плотную керамику применяют для некоторых деталей машин.
с размерами зерен 1-5 мкм в 5-6 раз прочнее обычной. Изделия из плотной мелкозернистой керамики - тонкой керамики - получают по более сложной технологии, и поэтому такие изделия дороги. Пористую керамику используют в качестве огнеупорных материалов, фильтров, диэлектриков в электротехнике. Более прочную плотную керамику применяют для некоторых деталей машин.
Ситаллы или стеклокристаллические материалы получают из стекол специального состава при помощи контролируемой кристаллизации. Структура ситаллов представляет собой смесь очень мелких (размерами  мкм), беспорядочно ориентированных кристаллов (60-95%) и остаточного стекла
мкм), беспорядочно ориентированных кристаллов (60-95%) и остаточного стекла  Исходное стекло по химическому составу отличается от остаточного стекла, в котором накапливаются ионы, не входящие в состав кристаллов. Такая структура создается в стеклянных изделиях после двойного отжига: первый отжиг нужен для формирования центров кристаллизации, второй - для выращивания кристаллов на готовых центрах. Для образования кристаллов в стекла вводят
Исходное стекло по химическому составу отличается от остаточного стекла, в котором накапливаются ионы, не входящие в состав кристаллов. Такая структура создается в стеклянных изделиях после двойного отжига: первый отжиг нужен для формирования центров кристаллизации, второй - для выращивания кристаллов на готовых центрах. Для образования кристаллов в стекла вводят  и другие соединения.
и другие соединения.
В зависимости от условий образования центров кристаллизации ситаллы подразделяют на термоситаллы и фото-ситаллы. В термоситаллах для образования центров кристаллизации используют оксиды или фториды  и др. (несколько процентов). При отжиге термоситалла получается высокая и однородная плотность кристаллов. В фотоситаллах используют малые добавки золота, серебра, платины или меди. Центры кристаллизации формируются под действием облучения ультрафиолетовым светом и отжига. Необлученные участки остаются аморфными после отжига.
и др. (несколько процентов). При отжиге термоситалла получается высокая и однородная плотность кристаллов. В фотоситаллах используют малые добавки золота, серебра, платины или меди. Центры кристаллизации формируются под действием облучения ультрафиолетовым светом и отжига. Необлученные участки остаются аморфными после отжига.
Фотоситаллы применяют как фоточувствительные материалы. Термоситаллы имеют универсальное применение: как износостойкие материалы используются для деталей гидромашин, узлов трения, защитных эмалей; как прочные стабильные диэлектрики - для радиодеталей, плат и т. п.
| << Предыдущий параграф | Следующий параграф >> |
- Введение
- Глава 1. СТРОЕНИЕ И СВОЙСТВА МАТЕРИАЛОВ
- 1.1. Элементы кристаллографии
- 1.2. Влияние типа связи на структуру и свойства кристаллов
- Молекулярные кристаллы.
- Ковалентные кристаллы.
- Металлические кристаллы.
- Ионные кристаллы.
- 1.3. Фазовый состав сплавов
- Твердые растворы.
- Промежуточные фазы.
- 1.4. Дефекты кристаллов
- Линейные дефекты.
- Поверхностные дефекты.
- 1.5. Диффузия в металлах и сплавах
- 1.6. Жидкие кристаллы
- 1.7. Структура полимеров, стекла и керамики
- Глава 2. ФОРМИРОВАНИЕ СТРУКТУРЫ ЛИТЫХ МАТЕРИАЛОВ
- 2.1. Самопроизвольная кристаллизация
- 2.2. Несамопроизвольная кристаллизация
- 2.3. Форма кристаллов и строение слитков
- 2.4. Получение монокристаллов
- 2.5. Аморфное состояние металлов
- Глава 3. ВЛИЯНИЕ ХИМИЧЕСКОГО СОСТАВА НА РАВНОВЕСНУЮ СТРУКТУРУ СПЛАВОВ
- 3.1. Методы построения диаграмм состояния
- 3.2. Основные равновесные диаграммы состояния двойных сплавов
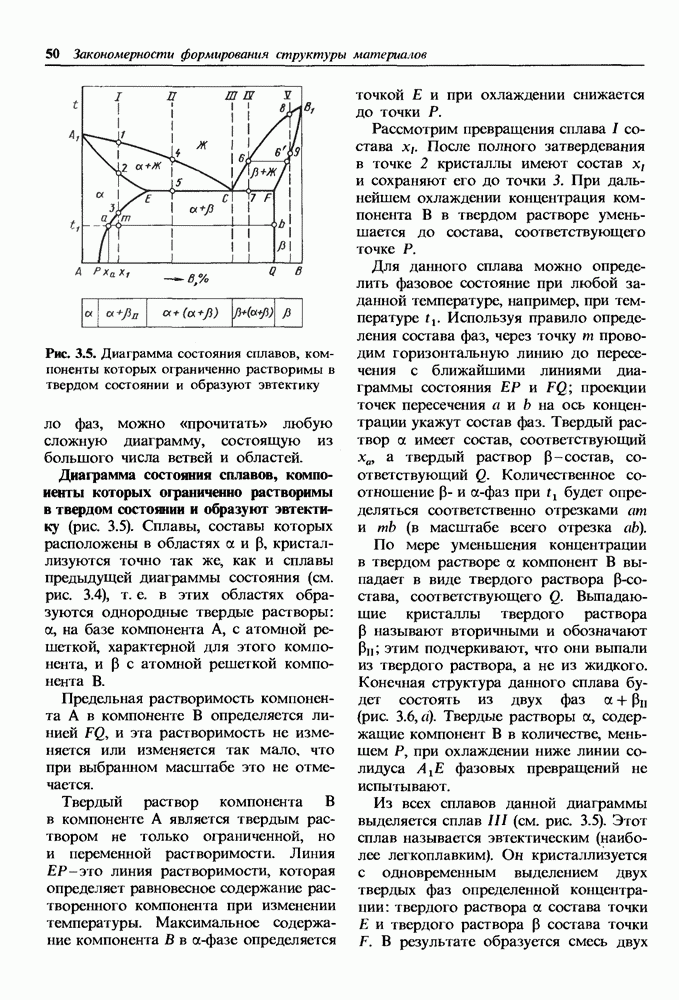
- Диаграмма состояния сплавов, компоненты которых ограниченно растворимы в твердом состоянии и образуют эвтектику
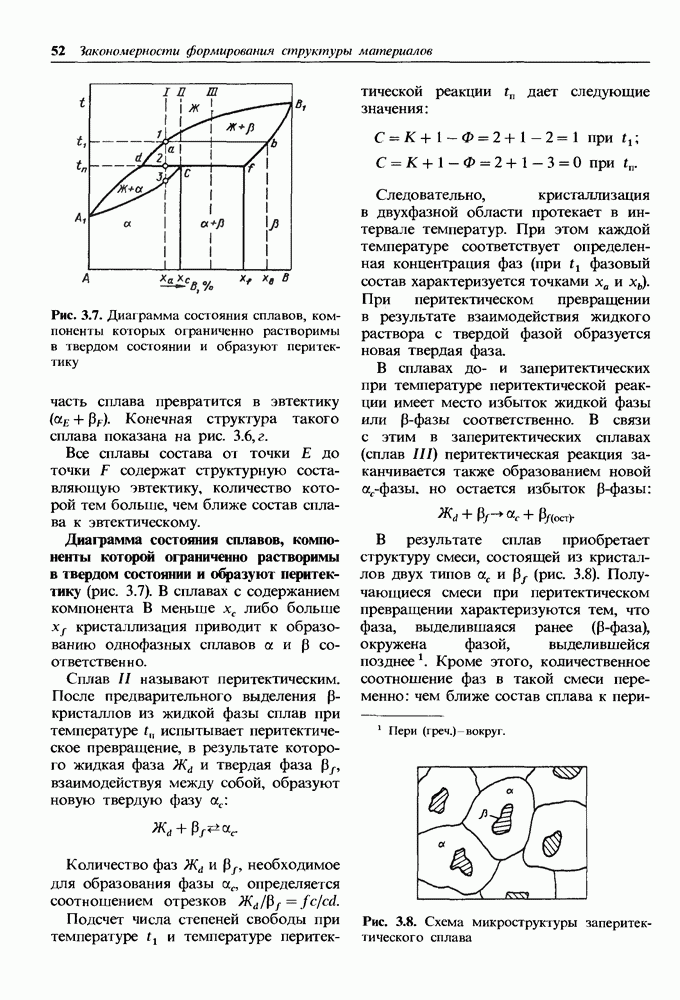
- Диаграмма состояния сплавов, компоненты которой ограниченно растворимы в твердом состоянии и образую! перитектику
- Диаграмма состояния сплавов с полиморфным превращением одного из компонентов.
- Диаграмма состояния сплавов с полиморфными превращениями компонентов и эвтектоидным превращением.
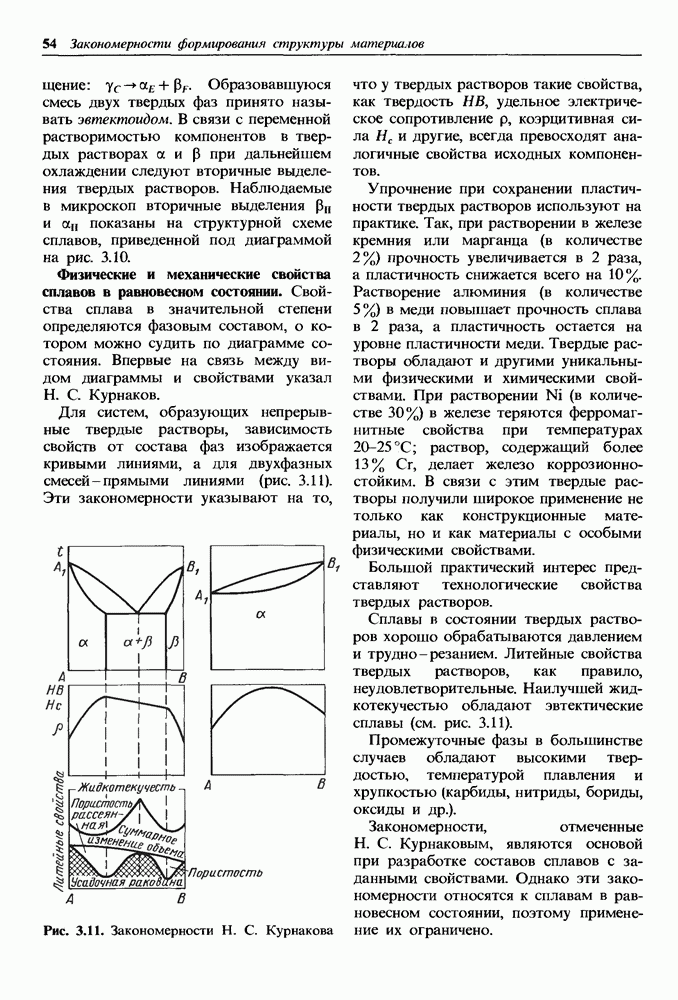
- Физические и механические свойства сплавов в равновесном состоянии.
- 3.3. Диаграмма состояния железоуглеродистых сплавов
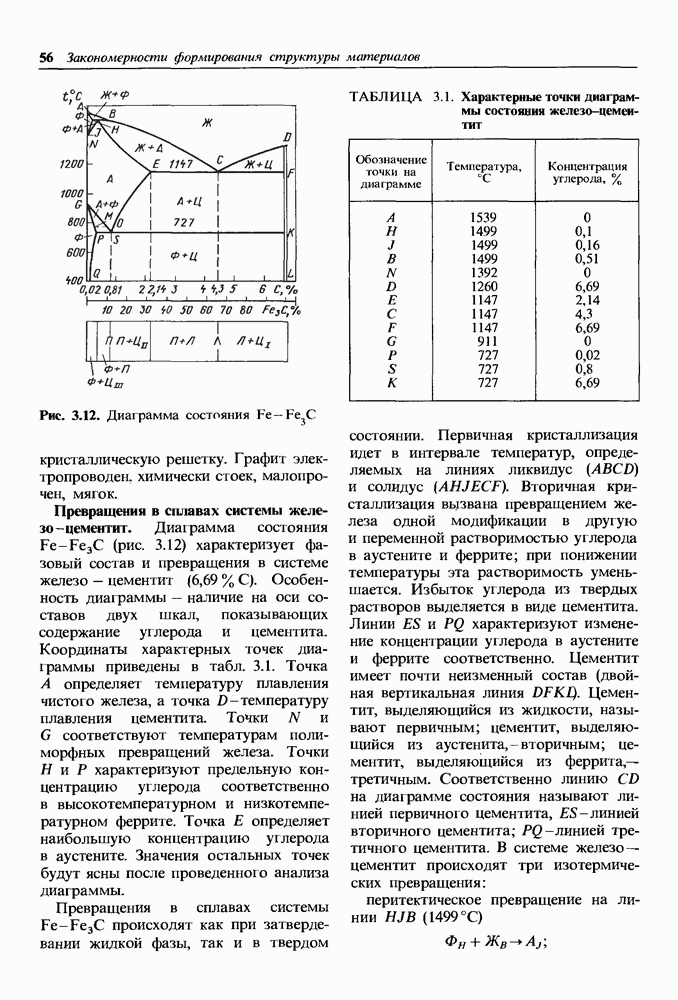
- Превращения в сплавах системы железо-цементит.
- Превращения в сплавах системы железо-графит.
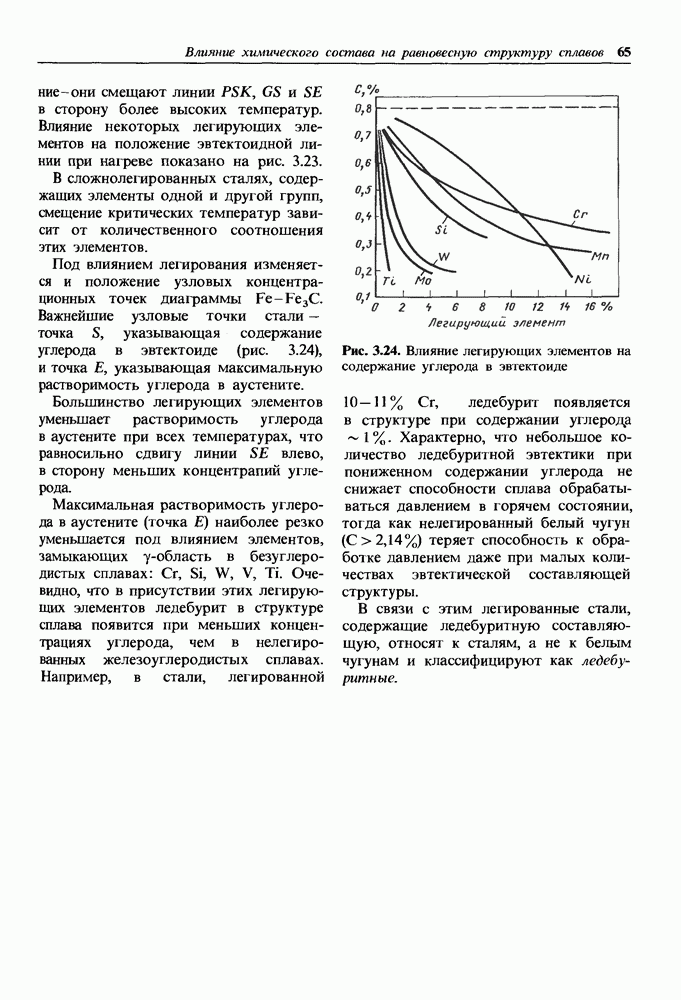
- 3.4. Влияние легирующих элементов на равновесную структуру сталей
- Карбиды в легированных сталях.
- Влияние легирующих элементов на температуры фазовых превращений сталей при нагреве и на состав точек S и Е диаграммы.
- Глава 4. ФОРМИРОВАНИЕ СТРУКТУРЫ ДЕФОРМИРОВАННЫХ МЕТАЛЛОВ И СПЛАВОВ
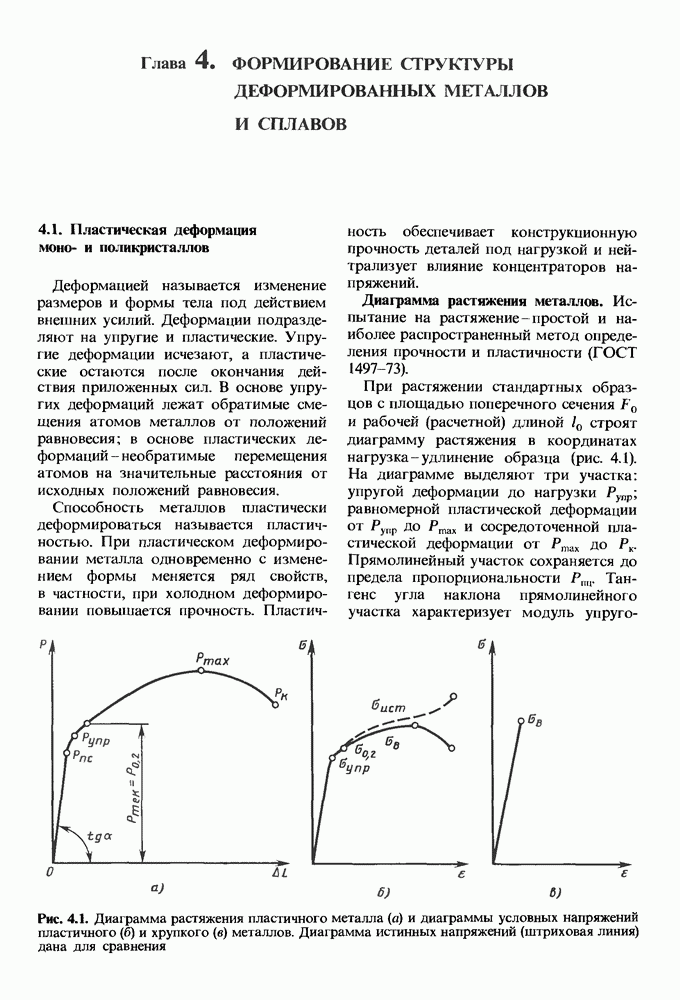
- 4.1. Пластическая деформация моно- и поликристаллов
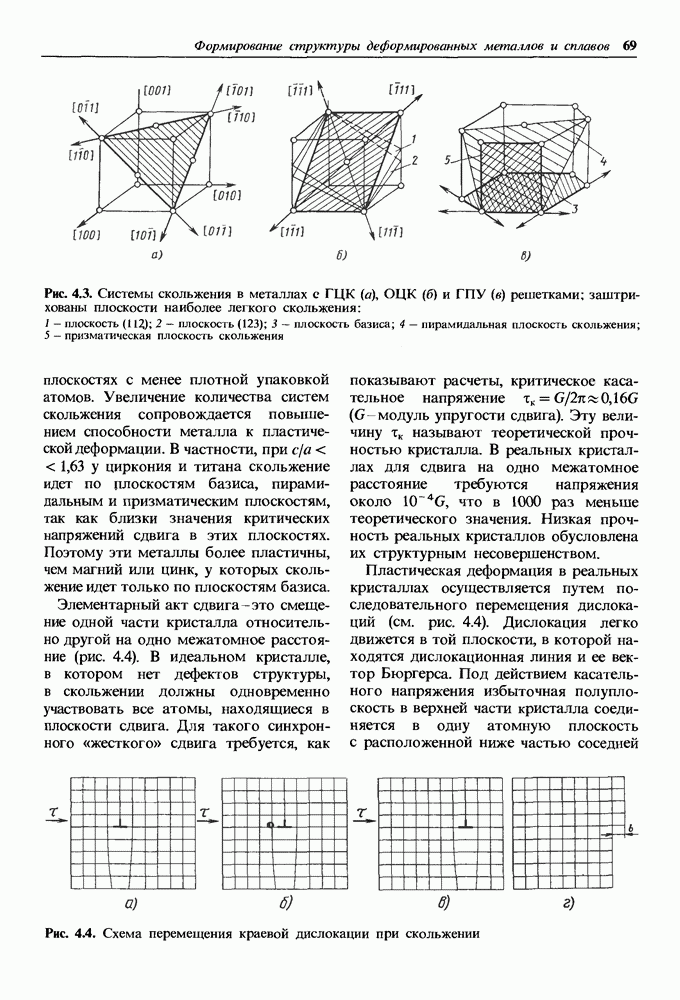
- Механизм пластической деформации
- Пластическая деформация поликристаллических металлов.
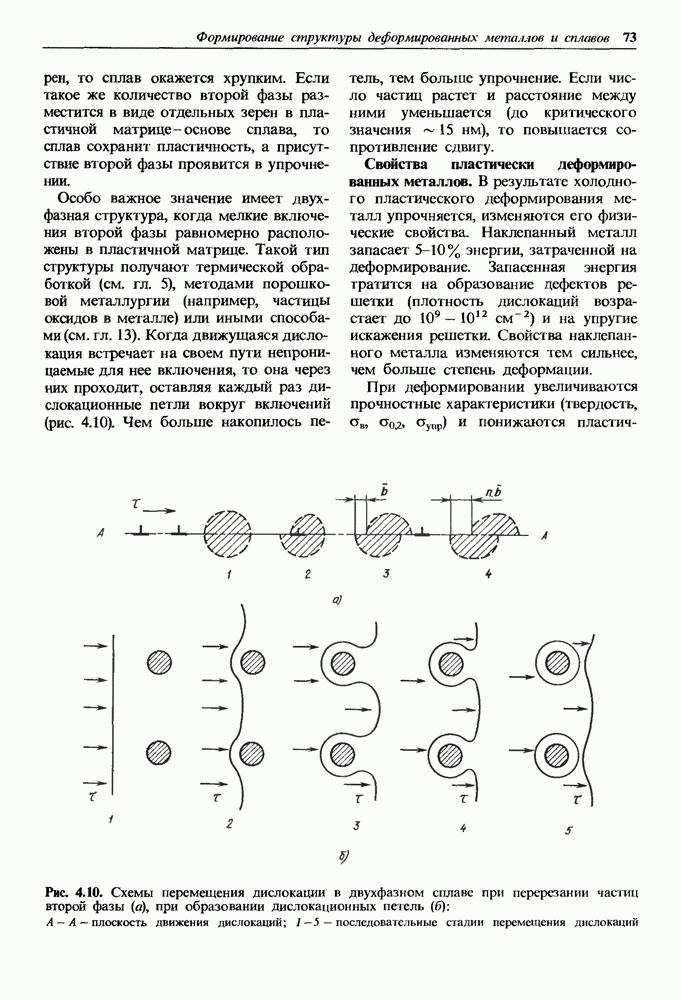
- Деформирование двухфазных сплавов оказывается более сложным.
- Свойства наклепанного металла изменяются тем сильнее, чем больше степень деформации.
- 4.2. Возврат и рекристаллизация
- Глава 5. ТЕРМИЧЕСКАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- 5.2. Основное оборудование для термической обработки
- 5.3. Термическая обработка сплавов, не связанная с фазовыми превращениями в твердом состоянии
- Рекристаллизационный отжиг.
- Диффузионный отжиг (гомогенизация).
- 5.4. Термическая обработка сплавов с переменной растворимостью компонентов в твердом состоянии
- 5.5. Термическая обработка сталей с эвтектоидным превращением
- Превращения аустенита при различных степенях переохлаждения.
- 5.6. Основные виды термической обработки стали
- Нормализация сталей.
- Закалка сталей.
- Закаливаемость в прокаливаемость сталей.
- Отпуск закаленных сталей.
- Глава 6. ХИМИКО-ТЕРМИЧЕСКАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- 6.2. Диффузионное насыщение углеродом и азотом
- Азотирование стали.
- Ионное азотирование и цементация.
- Одновременное насыщение поверхности стали углеродом и азотом.
- 6.3. Диффузионное насыщение сплавов металлами и неметаллами
- Раздел первый. Конструкционные материалы
- 7.1. Общие требования, предъявляемые к конструкционным материалам
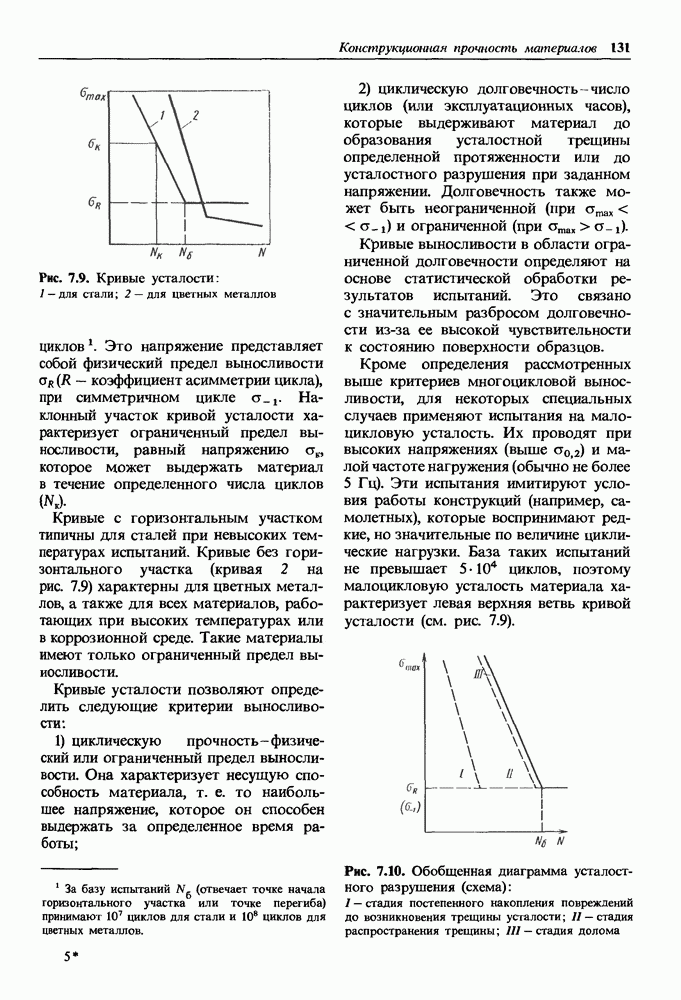
- 7.2. Конструкционная прочность материалов и критерии ее оценки
- 7.3. Методы повышения конструкционной прочности
- 7.4. Классификация конструкционных материалов
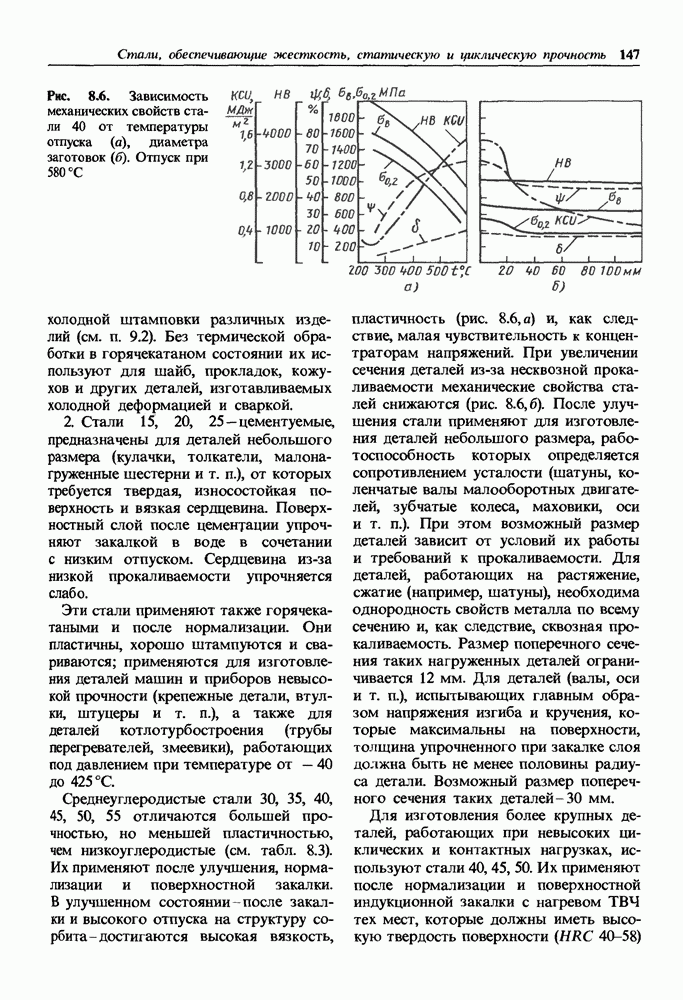
- Глава 8. СТАЛИ, ОБЕСПЕЧИВАЮЩИЕ ЖЕСТКОСТЬ, СТАТИЧЕСКУЮ И ЦИКЛИЧЕСКУЮ ПРОЧНОСТЬ
- 8.1. Классификация конструкционных сталей
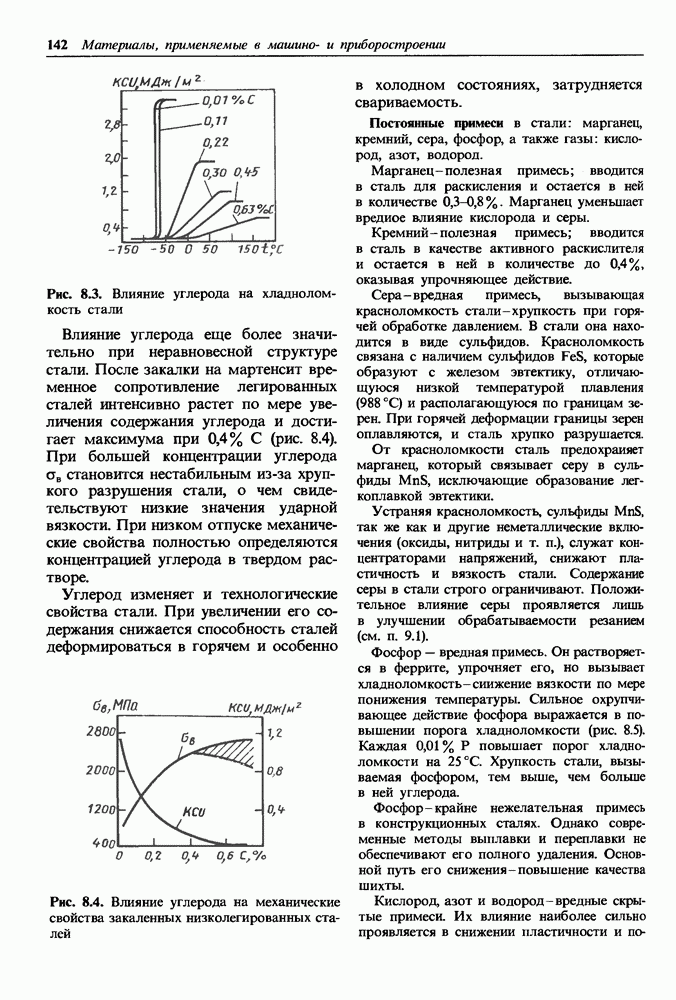
- 8.2. Влияние углерода и постоянных примесей на свойства стали
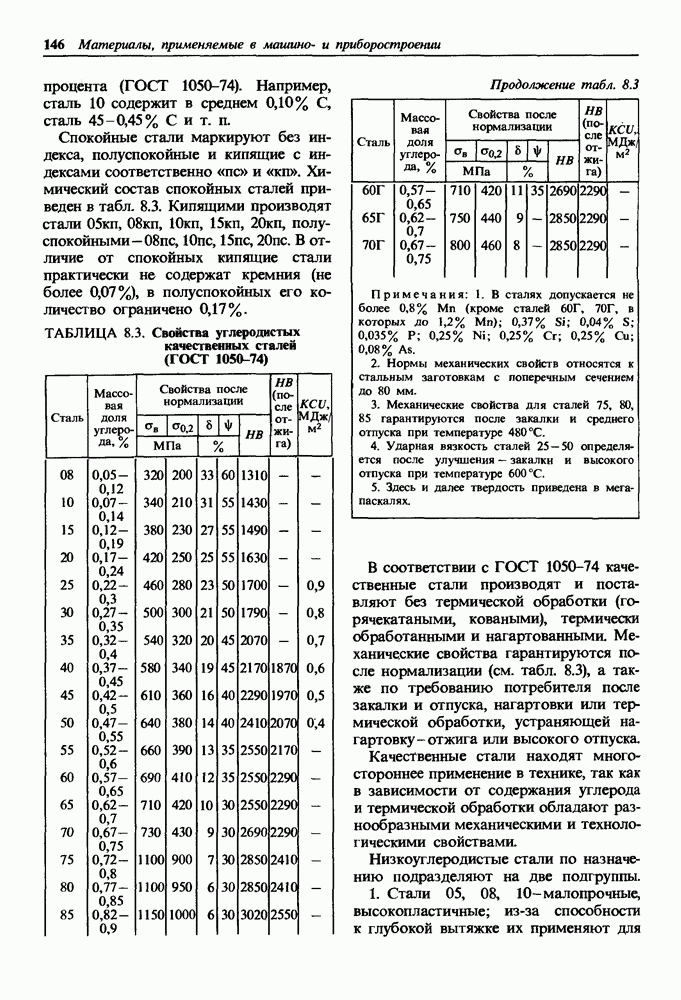
- 8.3. Углеродистые стали
- 8.4. Легированные стали
- Легированные стали нормальной и повышенной статической прочности.
- Легированные высокопрочные стали.
- Легированные стали с повышенной циклической прочностью.
- Глава 9. МАТЕРИАЛЫ С ОСОБЫМИ ТЕХНОЛОГИЧЕСКИМИ СВОЙСТВАМИ
- 9.1. Стали с улучшенной обрабатываемостью резанием
- 9.2. Стали с высокое технологической пластичностью и свариваемостью
- 9.3. Железоуглеродистые сплавы с высокими литейными свойствами
- Серые чугуны.
- Высокопрочные чугуны.
- Ковкие чугуны.
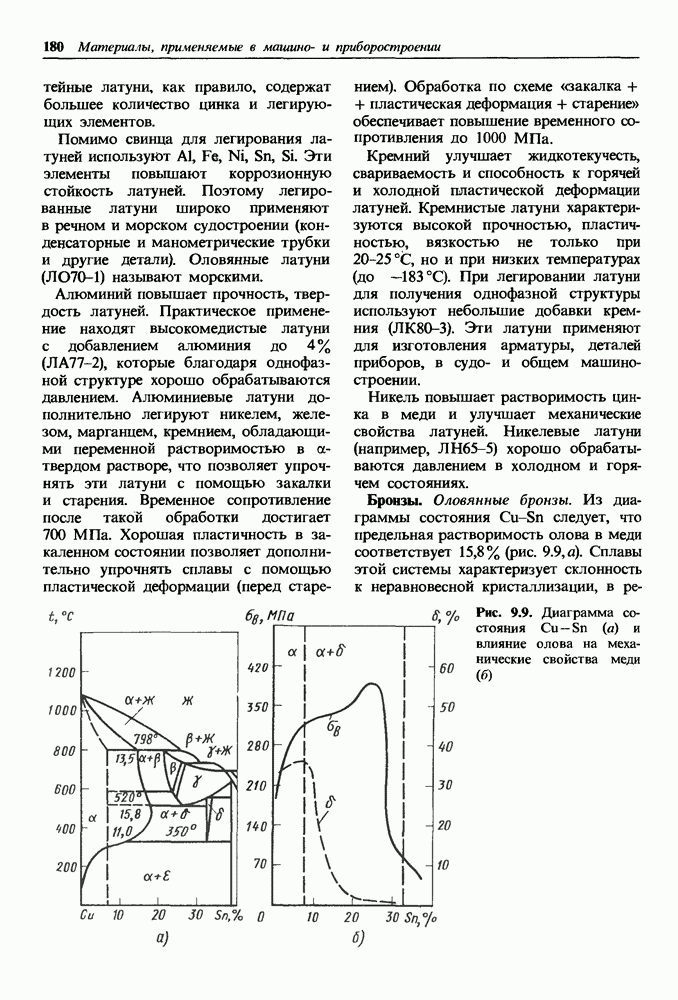
- 9.4. Медные сплавы
- Общая характеристика и классификация медных сплавов.
- Латуни.
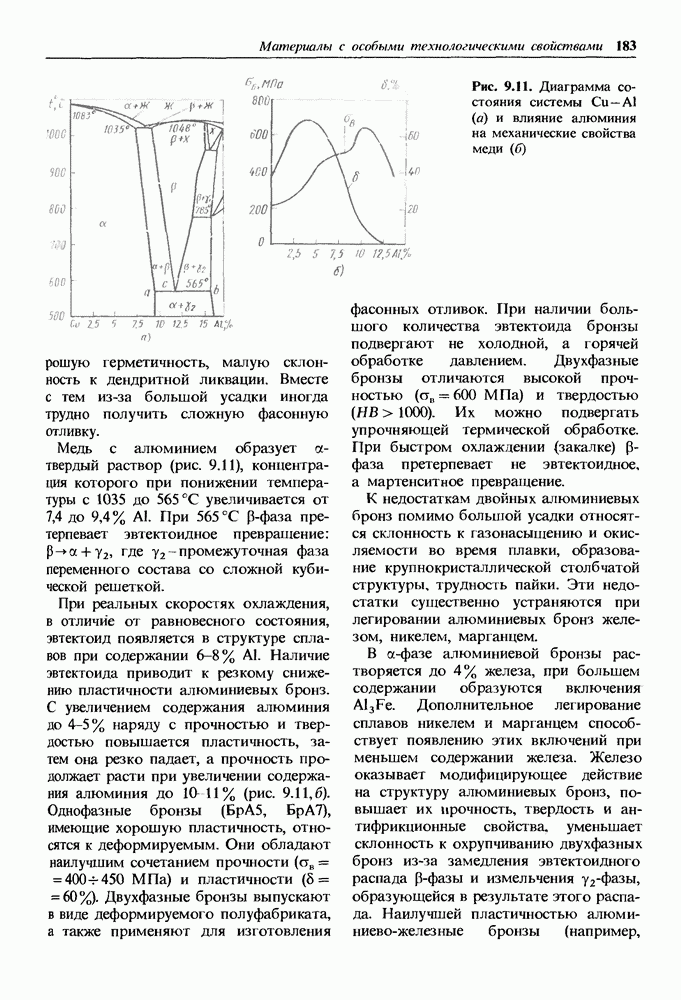
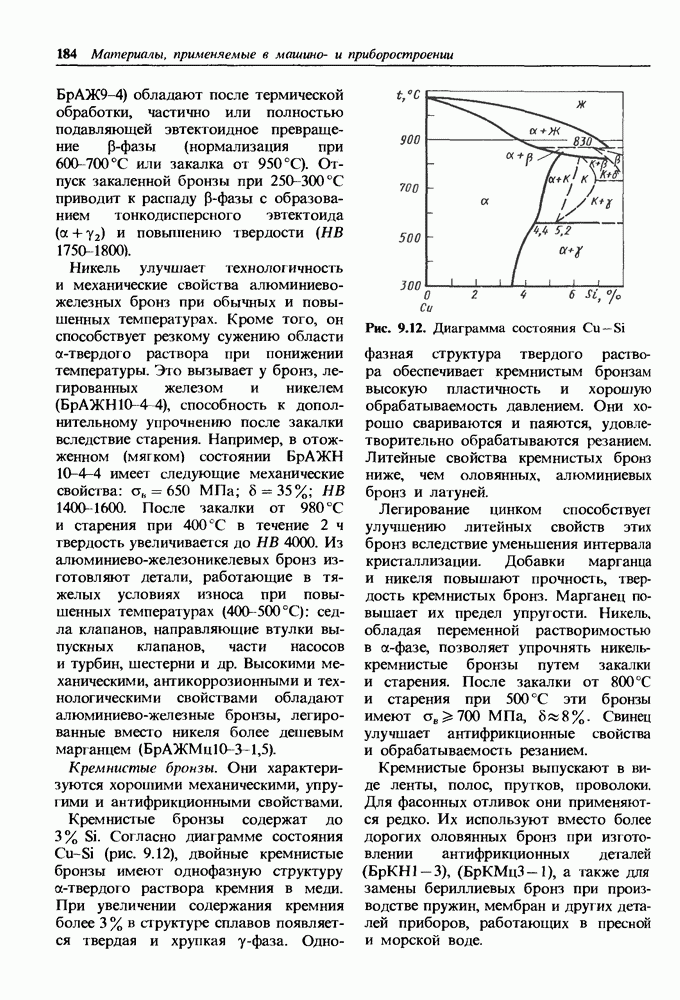
- Бронзы.
- Глава 10. ИЗНОСОСТОЙКИЕ МАТЕРИАЛЫ
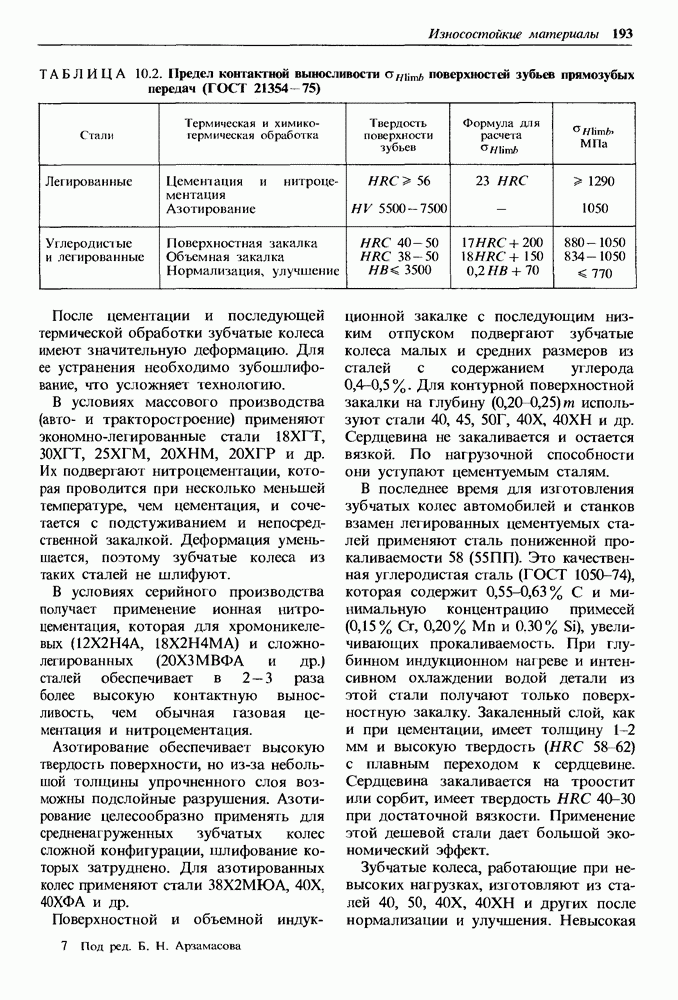
- 10.2. Закономерности изнашивания деталей, образующих пары трения, и пути уменьшения их износа
- 10.3. Материалы с высокой твердостью поверхности
- Материалы, устойчивые к усталостному виду изнашивания.
- Материалы, устойчивые к изнашиванию в условиях больших давлений и ударных нагрузок.
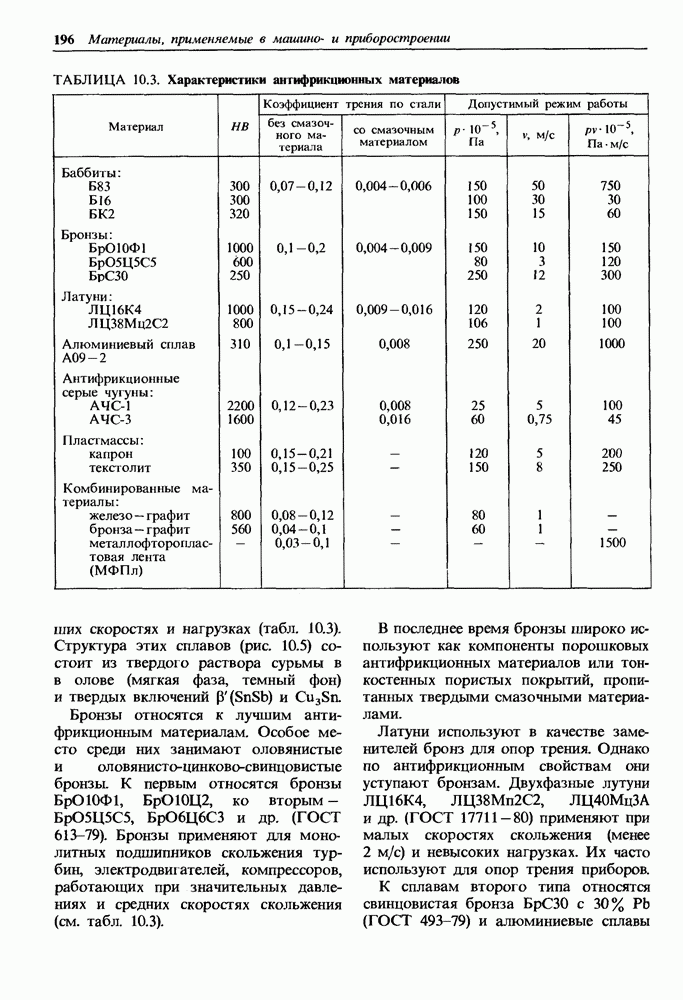
- 10.4. Антифрикционные материалы
- Неметаллические материалы.
- Комбинированные материалы.
- Минералы.
- 10.5. Фрикционные материалы
- Глава 11. МАТЕРИАЛЫ С ВЫСОКИМИ УПРУГИМИ СВОЙСТВАМИ
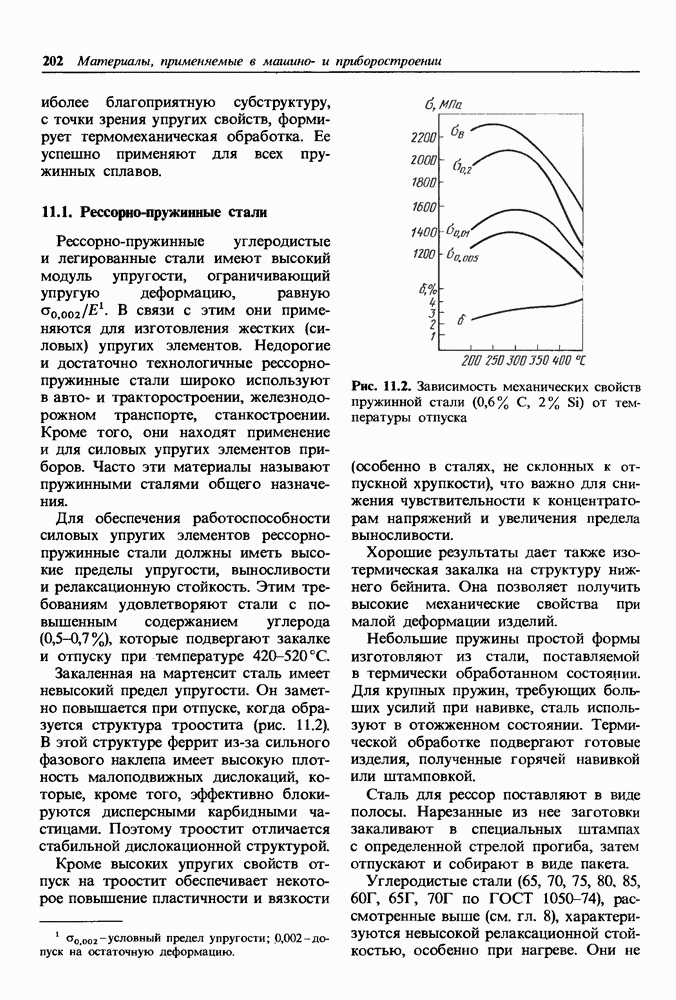
- 11.1. Рессорно-пружинные стали
- 11.2. Пружинные материалы приборостроения
- Глава 12. МАТЕРИАЛЫ С МАЛОЙ ПЛОТНОСТЬЮ
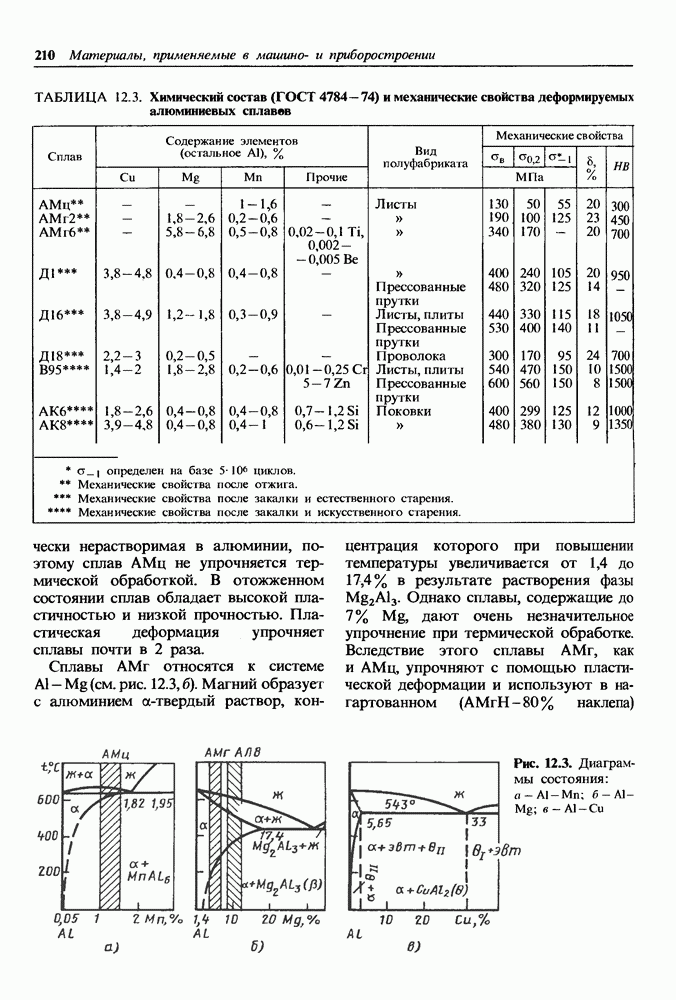
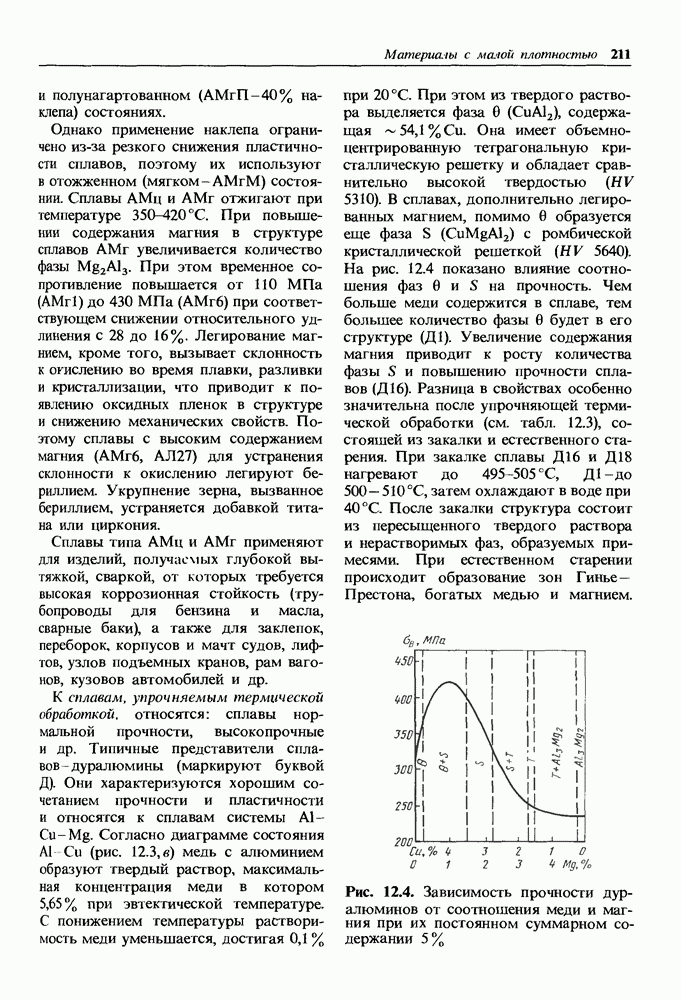
- 12.1. Сплавы на основе алюминия
- Общая характеристика и классификация алюминиевых сплавов.
- Деформируемые алюминиевые сплавы.
- Литейные алюминиевые сплавы.
- Гранулированные сплавы.
- 12.2. Сплавы на основе магния
- Общая характеристика и классификация магниевых сплавов.
- Деформируемые магниевые сплавы.
- Литейные магниевые сплавы.
- 12.3. Неметаллические материалы
- Механические свойства термопластичных пластмасс.
- Механические свойства термореактивных пластмасс.
- Глава 13. МАТЕРИАЛЫ С ВЫСОКОЙ УДЕЛЬНОЙ ПРОЧНОСТЬЮ
- 13.1. Титан и сплавы на его основе
- Влияние легирующих элементов на структуру и свойства титановых сплавов.
- Особенности термической обработки титановых сплавов.
- Промышленные титановые сплавы.
- 13.2. Бериллий и сплавы на его основе
- Бериллиевые сплавы.
- 13.3. Композиционные материалы
- Дисперсно-упрочненные композиционные материалы.
- Волокнистые композиционные материалы.
- Композиционные материалы на неметаллической основе.
- Композиционные материалы на металлической основе.
- Глава 14. МАТЕРИАЛЫ, УСТОЙЧИВЫЕ К ВОЗДЕЙСТВИЮ ТЕМПЕРАТУРЫ И РАБОЧЕЙ СРЕДЫ
- 14.1. Коррозионно-стойкие материалы
- Коррозионно-стойкие непассивирующиеся металлы.
- Коррозионностойкие пассивирующиеси металлы.
- Коррозионно-стойкие покрытия.
- 14.2. Жаростойкие материалы
- Жаростойкость металлов.
- Жаростойкость сплавов.
- 14.3. Жаропрочные материалы
- Основные группы жаропрочных материалов.
- 14.4. Хладостойкие материалы
- Основные группы хладостойких материалов.
- 14.5. Радиационно-стойкие материалы
- Влияние облучения на коррозионную стойкость.
- Раздел второй. Материалы с особыми физическими свойствами
- 15.1. Общие сведения о ферромагнетиках
- 15.2. Магнитно-мягкие материалы
- Низкочастотные магнитно-мягкие материалы
- Высокочастотные магнитно-мягкие материалы.
- Материалы со специальными магнитными свойствами.
- 15.3. Магнитно-твердые материалы
- Магнитно-твердые лнтые материалы.
- Порошковые магнитно-твердые материалы.
- Деформируемые магнитно-твердые сплавы.
- Глава 16. МАТЕРИАЛЫ С ОСОБЫМИ ТЕПЛОВЫМИ СВОЙСТВАМИ
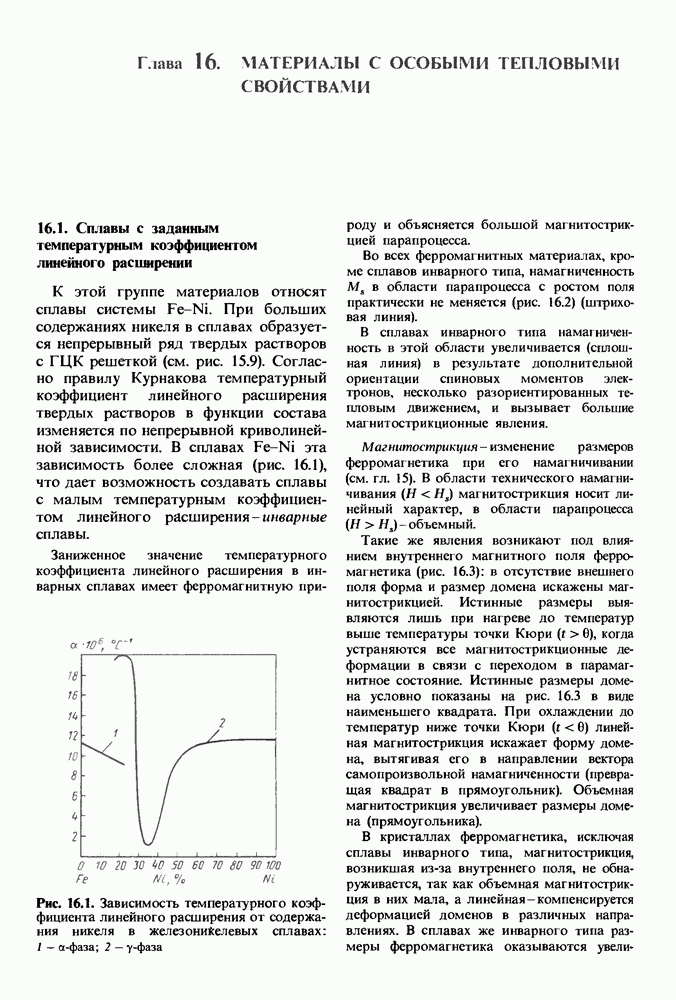
- 16.1. Сплавы с заданным температурным коэффициентом линейного расширении
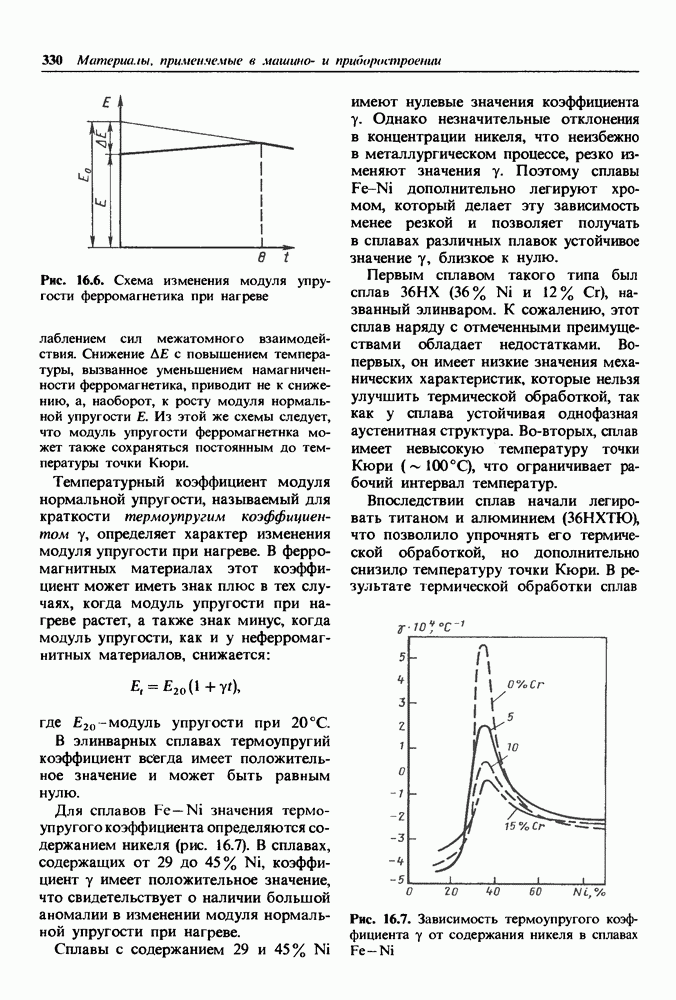
- 16.2. Сплавы с заданным температурным коэффициентом модуля упругости
- Глава 17. МАТЕРИАЛЫ С ОСОБЫМИ ЭЛЕКТРИЧЕСКИМИ СВОЙСТВАМИ
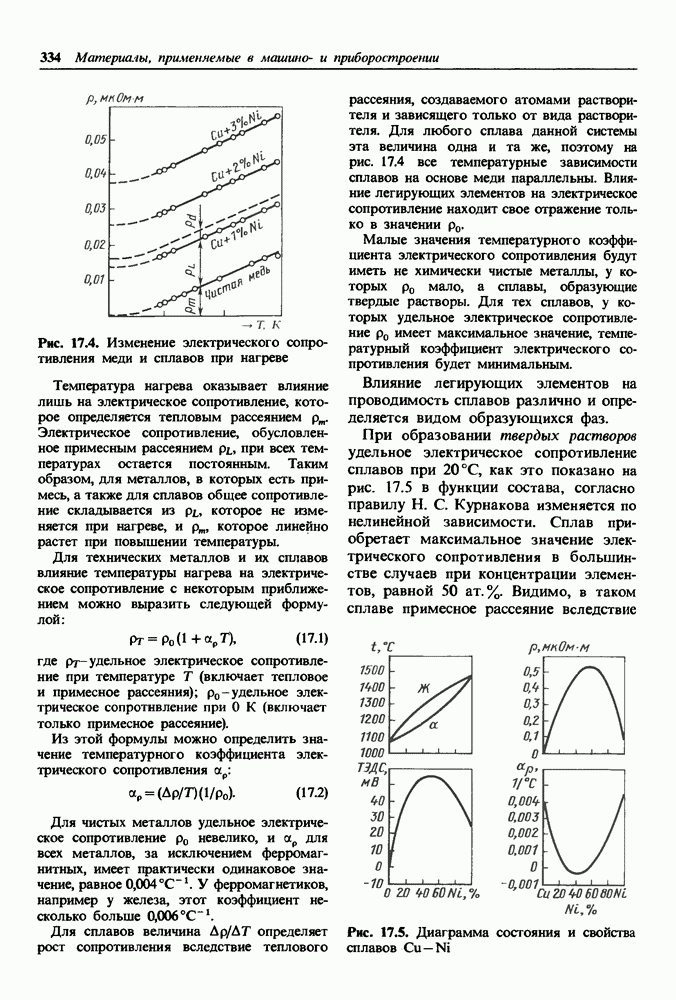
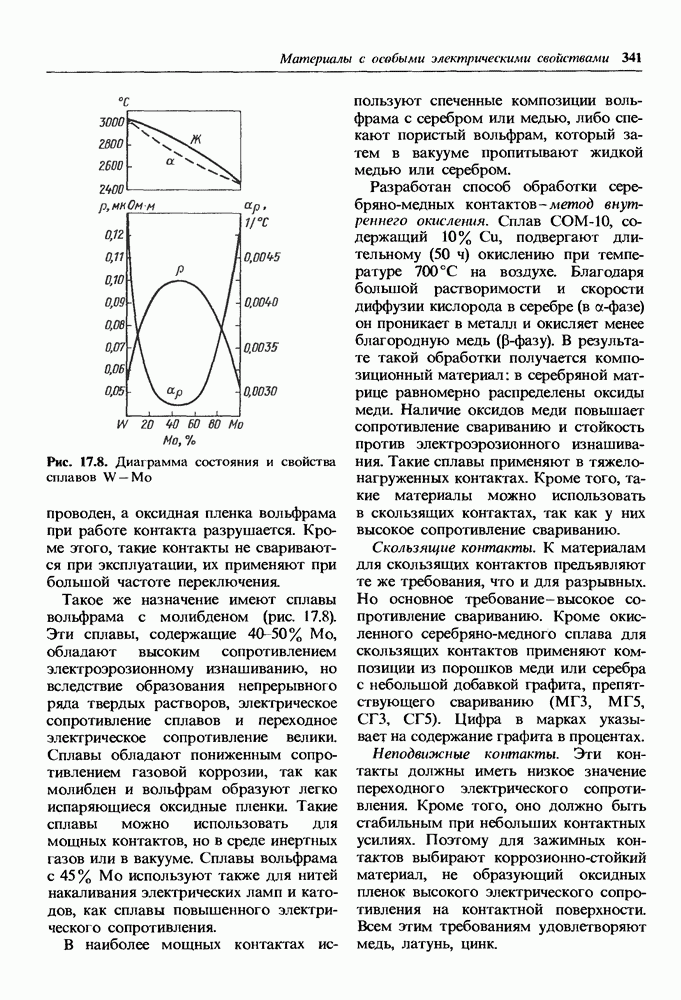
- 17.1. Материалы высокой электрической проводимости
- Проводниковые материалы.
- 17.2. Полупроводниковые материалы
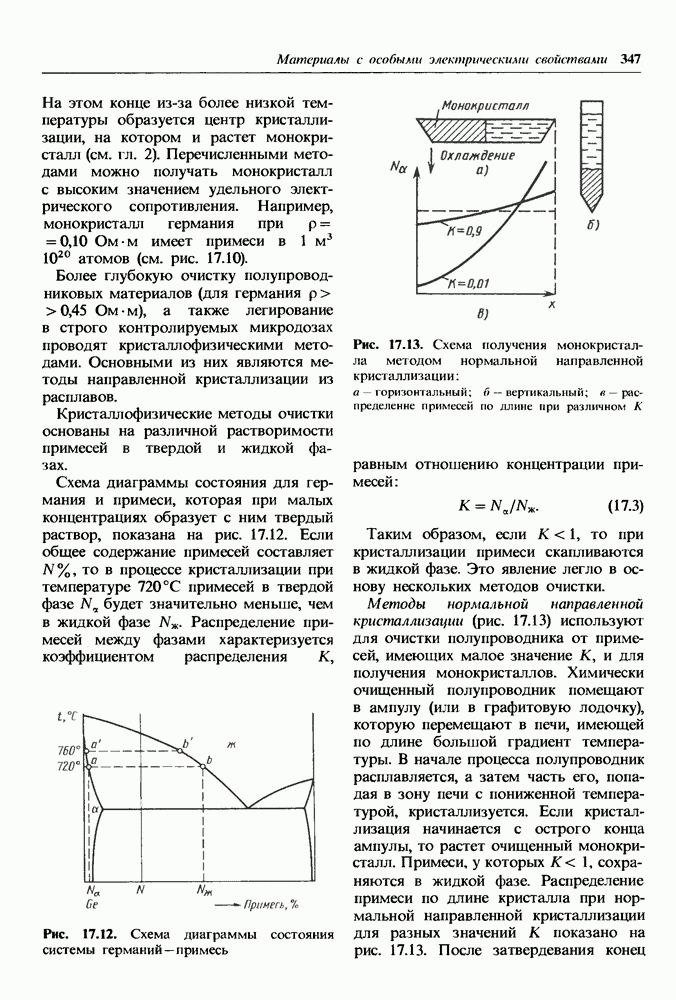
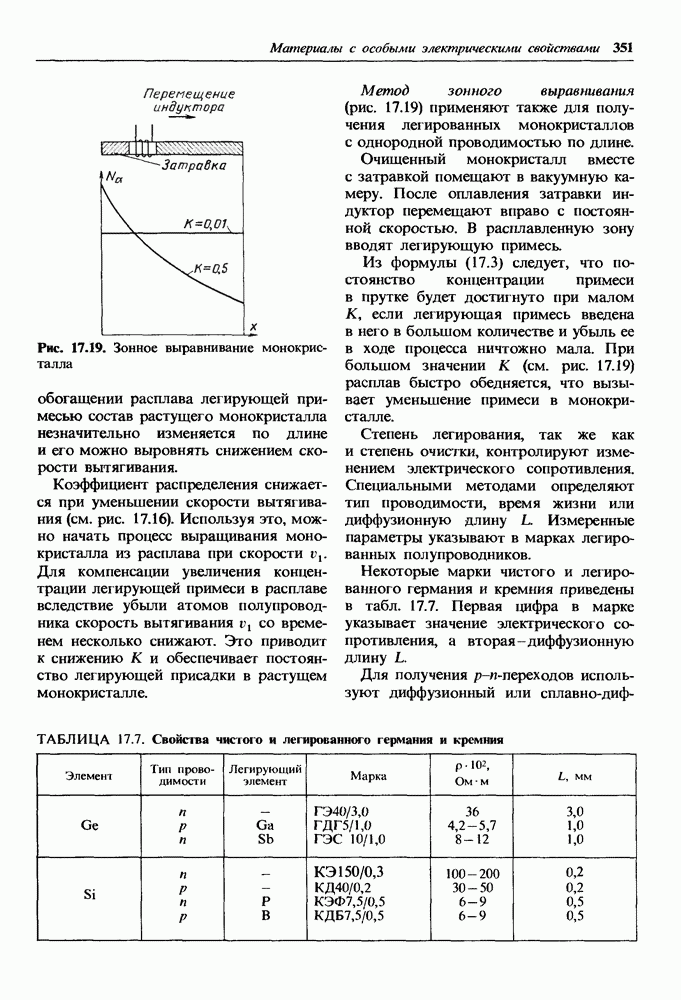
- Кристаллофизические методы получения сверхчистых материалов.
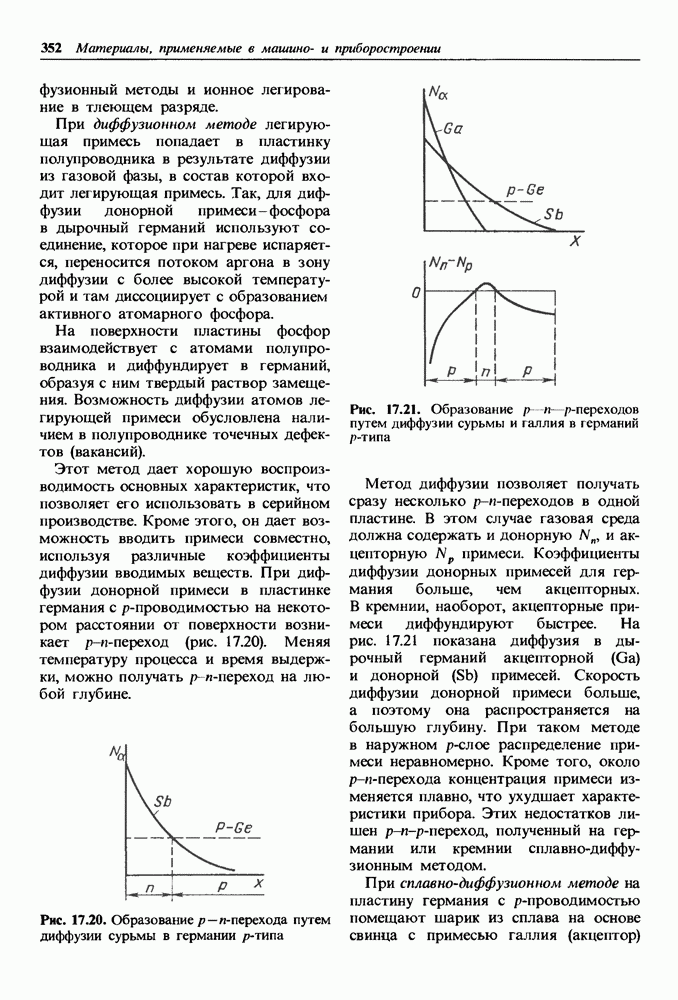
- Легирование полупроводников и получение p-n-переходов.
- 17.3. Диэлектрики
- Раздел третий. Инструментальные материалы
- Глава 18. МАТЕРИАЛЫ ДЛЯ РЕЖУЩИХ И ИЗМЕРИТЕЛЬНЫХ ИНСТРУМЕНТОВ
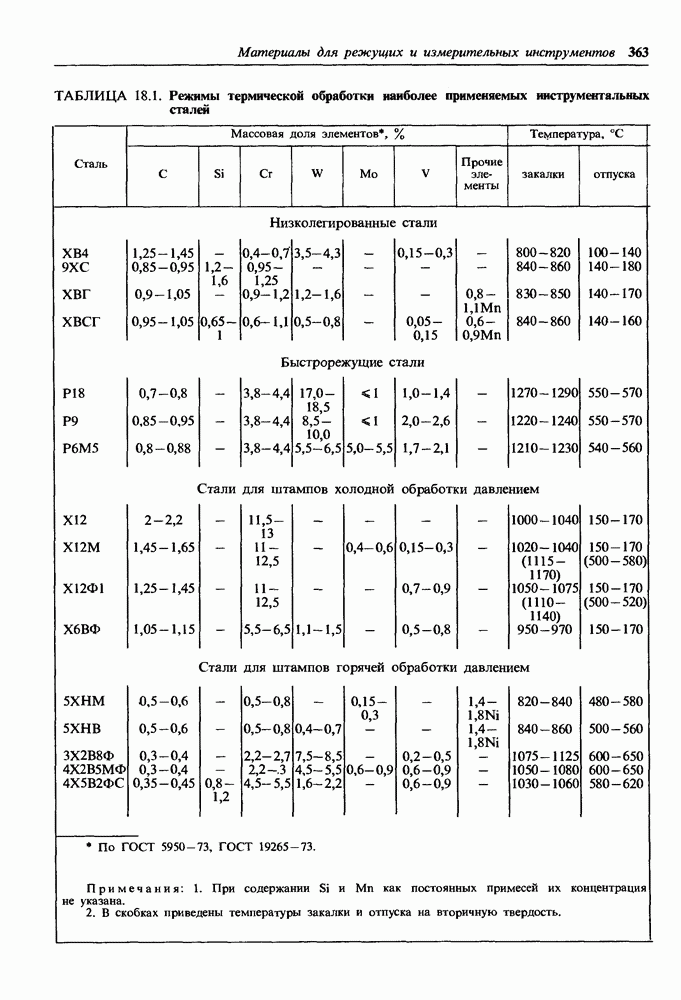
- 18.1. Материалы для режущих инструментов
- Низколегированные стали.
- Быстрорежущие стали.
- Спеченные твердые сплавы.
- Сверхтвердые материалы.
- 18.2. Стали для измерительных инструментов
- Глава 19. СТАЛИ ДЛЯ ИНСТРУМЕНТОВ ОБРАБОТКИ МЕТАЛЛОВ ДАВЛЕНИЕМ
- 19.1. Стали для инструментов холодной обработки давлением
- 19.2. Стали для инструментов горячей обработки давлением
- Приложение
- Список литературы