| << Предыдущий параграф | Следующий параграф >> |
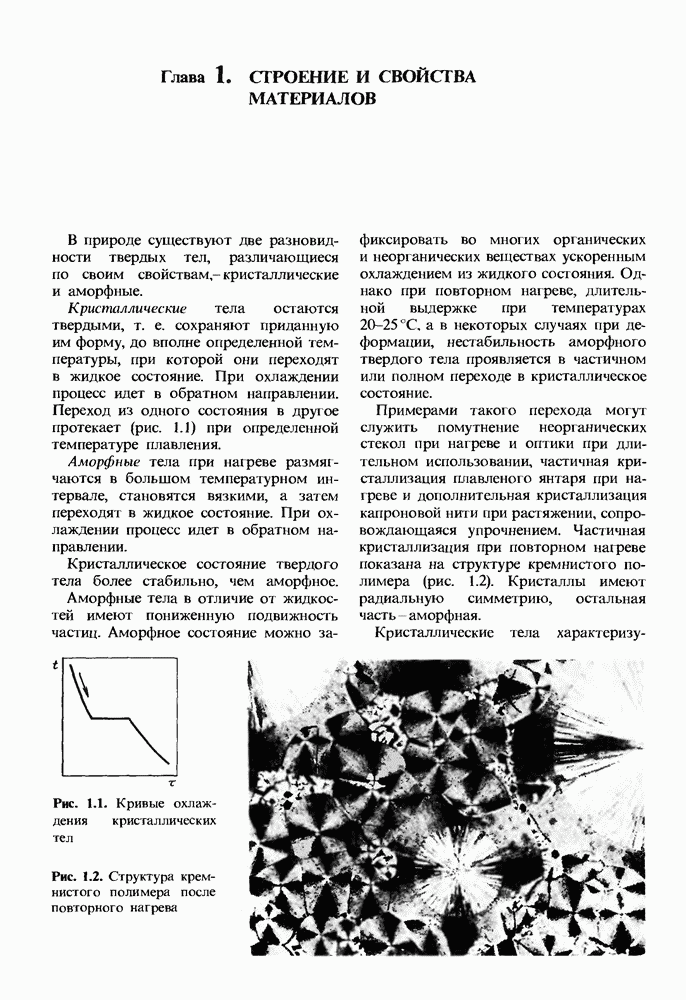
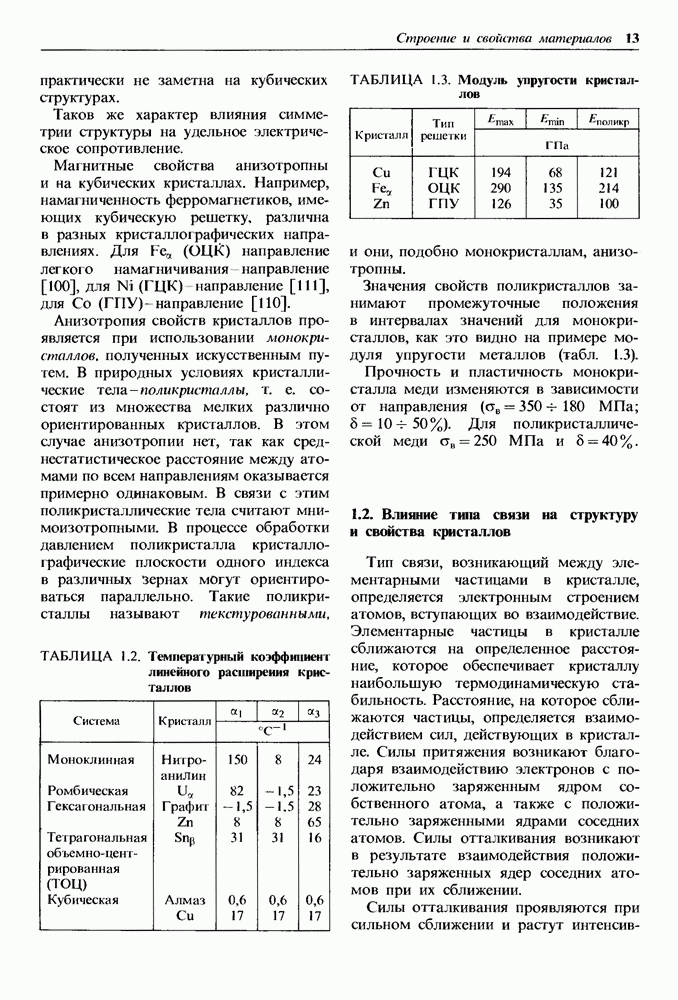
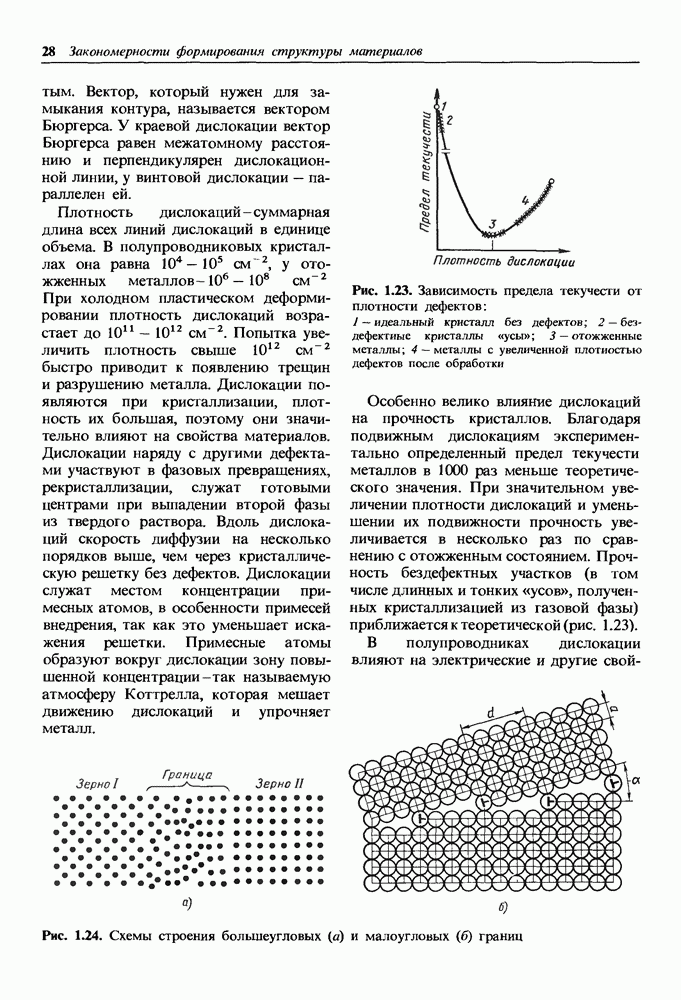
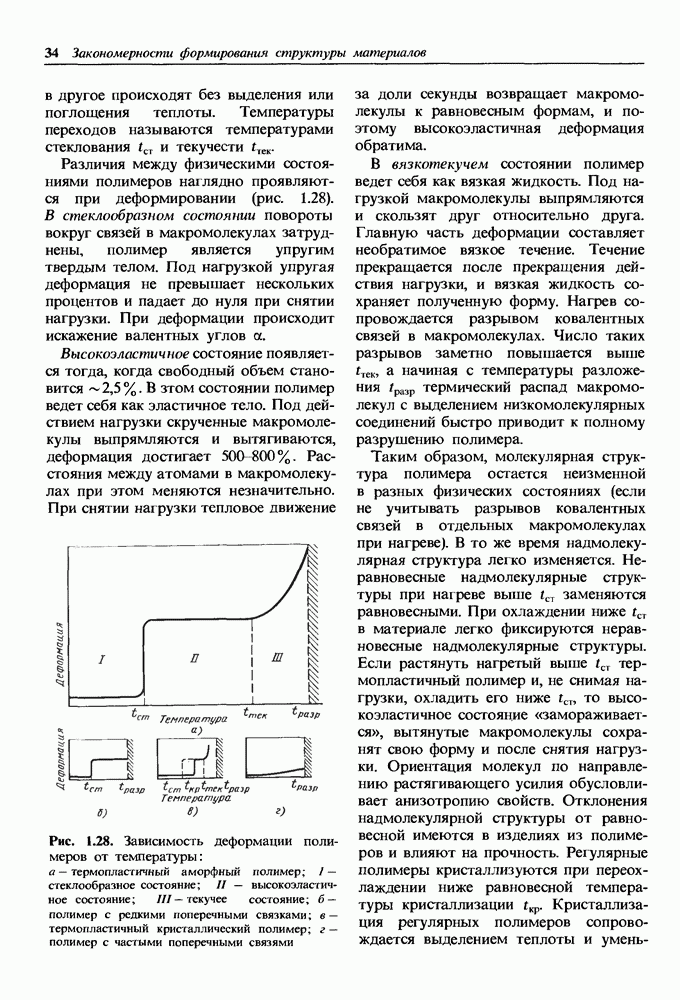
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Промежуточные фазы.
Кристаллы, образованные различными элементами и имеющие собственный тип кристаллической решетки, отличающийся от рещеток составляющих их элементов, называют промежуточной фазой.
В зависимости от природы элементов в промежуточных фазах может быть любой тип связи, который, в первую очередь, и определяет свойства кристаллов, в частности электрические свойства (см. п. 17.1).
Расположение атомов (или ионов) в решетке может быть неупорядоченным либо полностью или частично упорядоченным. Упорядочение, так же как и в твердых растворах, вызывает резкое изменение свойств - появление сверхпроводимости.
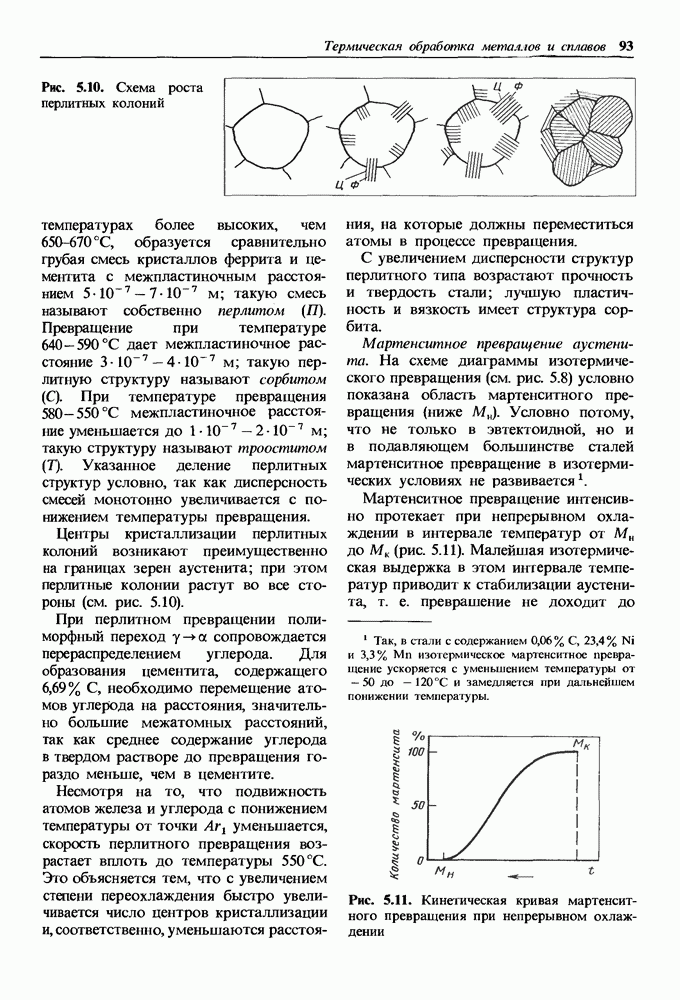
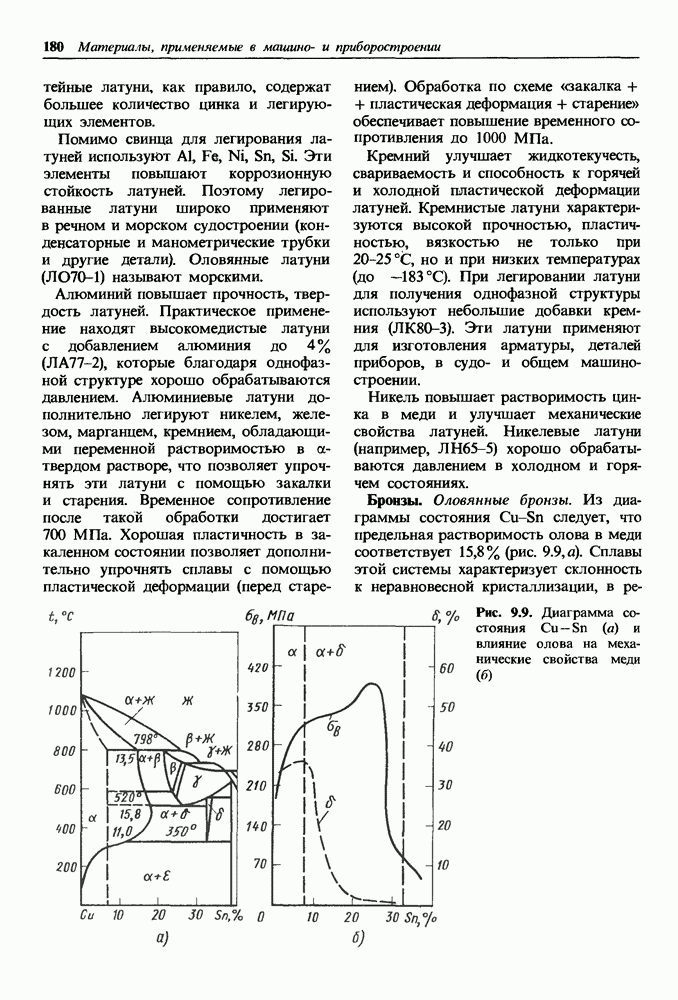
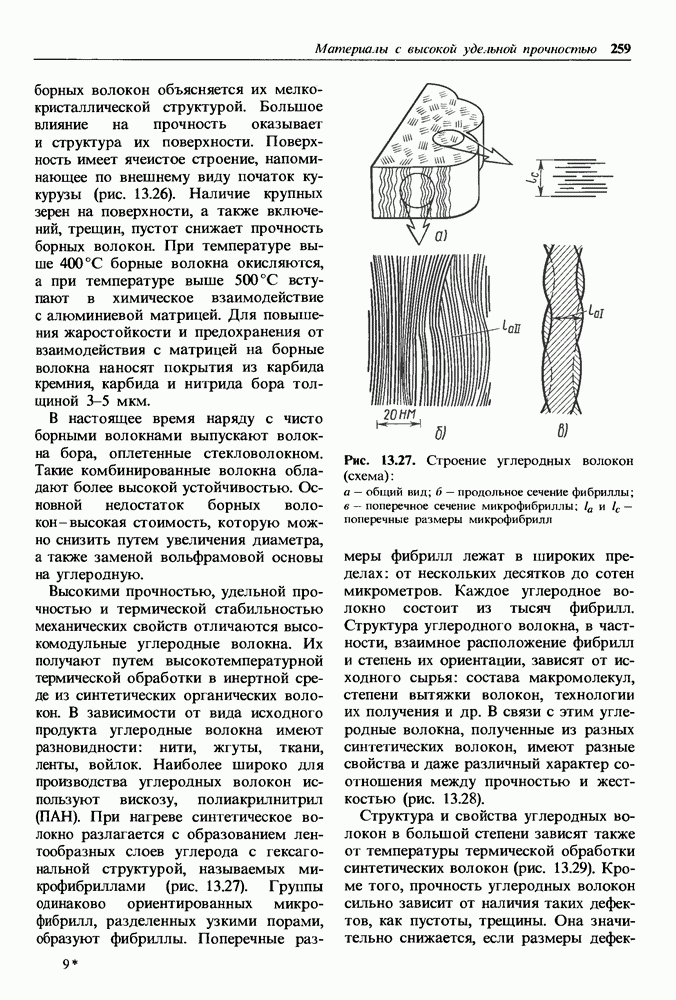
Промежуточные фазы, так же как и твердые растворы, являются кристаллами, в которых состав изменяется в некотором интервале концентраций, иногда очень малом. Переменный состав объясняется либо наличием небольших межузельных «лишних» атомов (или ионов) в кристаллической решетке промежуточной фазы, либо недостатком атомов в узлах решетки (рис. 1.17).
Промежуточные фазы обозначают так же, как и твердые растворы, буквами греческого алфавита. Однако допускаются обозначения и химическими

Рис. 1.17. Кристаллическая решетка  с дефицитом металлических ионов
с дефицитом металлических ионов
формулами, которые отражают состав (стехиометрический), при котором кристаллы не имеют дефектов — межузельных атомов и вакансий.
Пока не существует полной классификации многочисленных и разнообразных промежуточных фаз. Замечено, что структура промежуточной фазы зависит от трех факторов: относительного размера атомов, их валентности и от положения в периодической системе элементов, что определяет их электронную структуру.
Системы металл-неметалл. Фазы с ионным типом связи. К ним относятся простые и двойные оксиды металлов.
Простой оксид железа  имеет гранецентрированную пространственную решетку (см. рис. 1.14). Все кислородные узлы решетки заполнены, тогда как часть металлических узлов свободна. Таким образом, оксид
имеет гранецентрированную пространственную решетку (см. рис. 1.14). Все кислородные узлы решетки заполнены, тогда как часть металлических узлов свободна. Таким образом, оксид  имеет структуру с большим дефицитом металлических ионов, что определяет появление полупроводниковых свойств (см. п. 17.2).
имеет структуру с большим дефицитом металлических ионов, что определяет появление полупроводниковых свойств (см. п. 17.2).
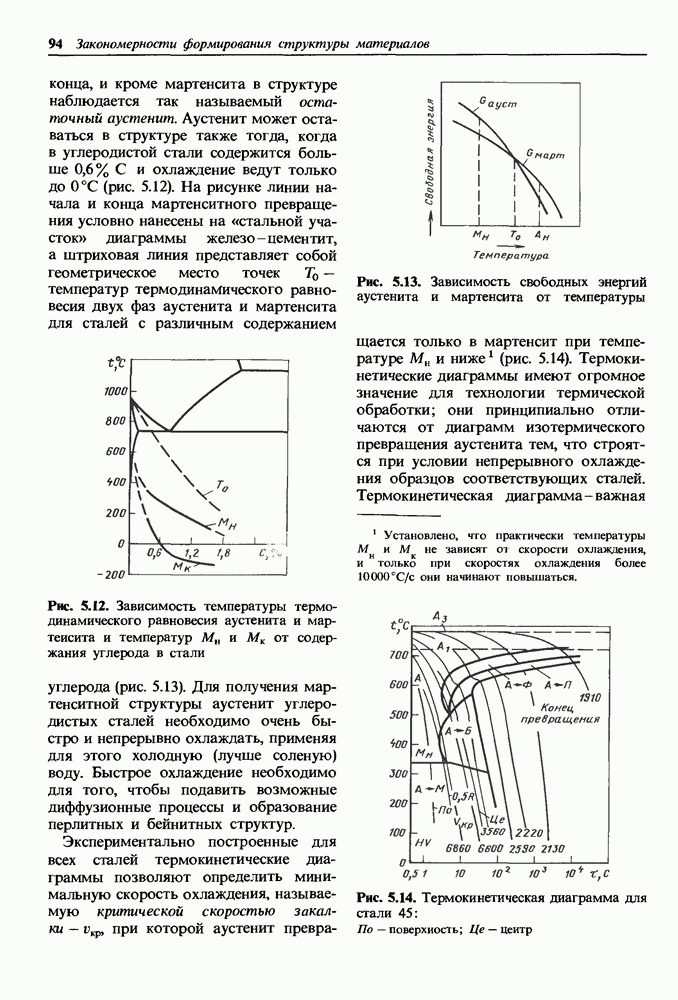
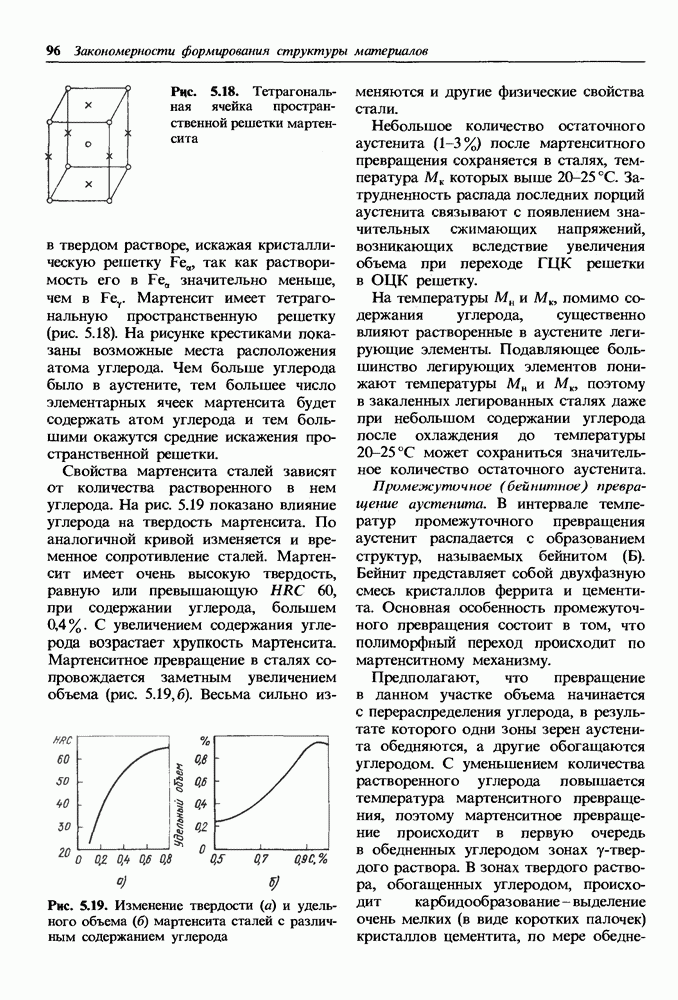
Оксид железа  двойной оксид
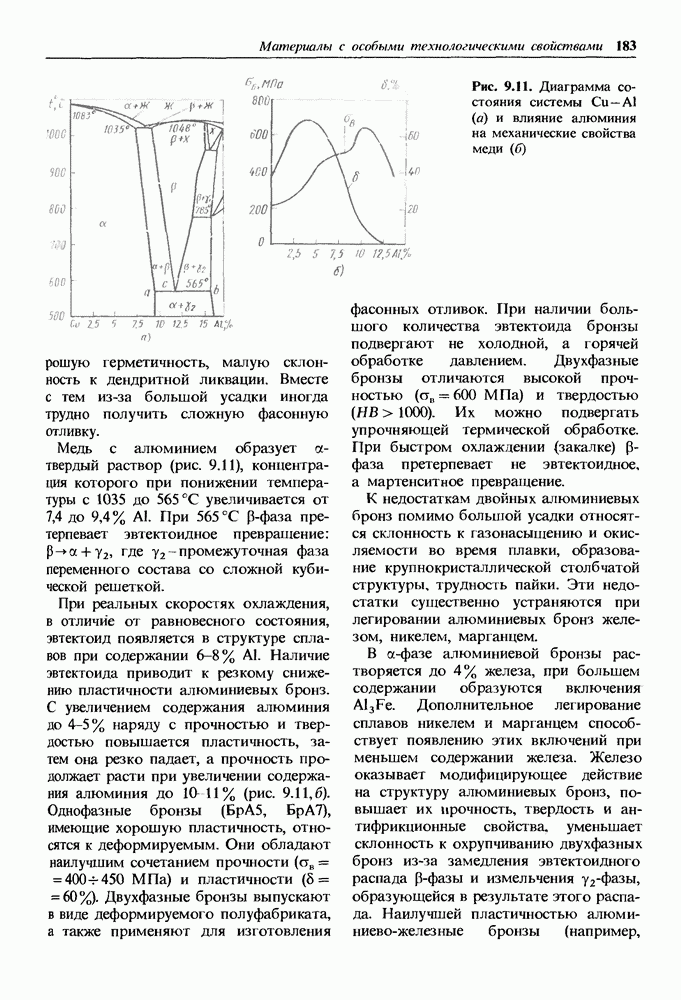
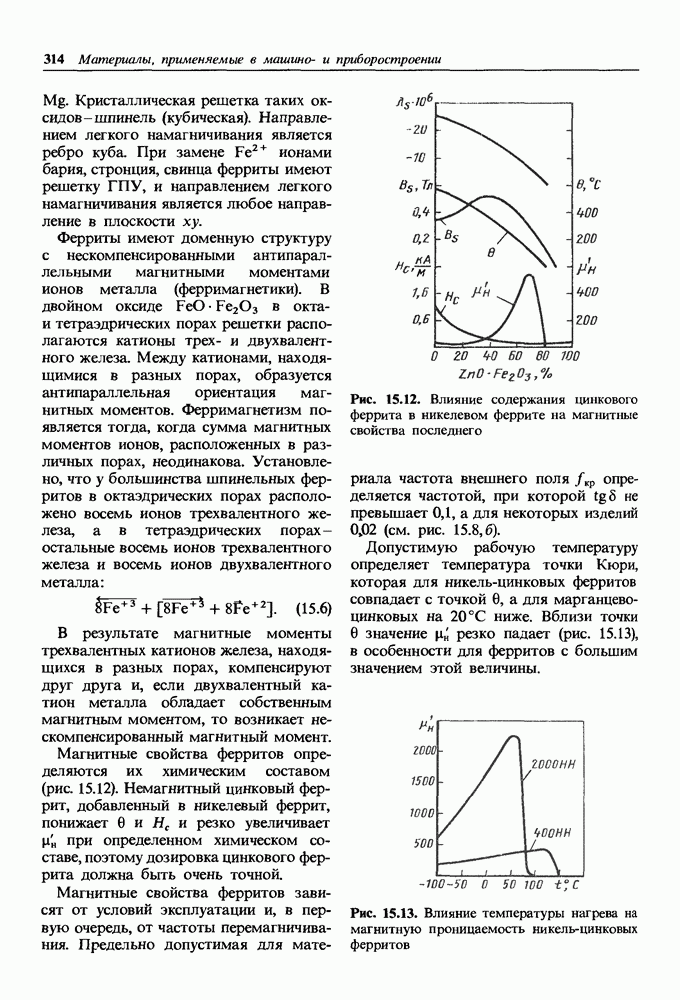
двойной оксид  (рис. 1.18). Кристаллическая решетка оксида-шпинель содержит двух-и трехвалентные ионы железа, расположенные в межузельных порах ионов кислорода. Два вида ионов железа и ионный тип связи обеспечивают оксиду особые магнитные свойства в высокочастотных полях. Большая плотность упаковки ионов в решетке, несмотря на небольшой дефицит ионов железа, способствует высокому сопротивлению химической коррозии.
(рис. 1.18). Кристаллическая решетка оксида-шпинель содержит двух-и трехвалентные ионы железа, расположенные в межузельных порах ионов кислорода. Два вида ионов железа и ионный тип связи обеспечивают оксиду особые магнитные свойства в высокочастотных полях. Большая плотность упаковки ионов в решетке, несмотря на небольшой дефицит ионов железа, способствует высокому сопротивлению химической коррозии.
Фазы с ионно-ковалентным типом связи. Такие фазы образуются при взаимодействии металлов  группы с неметаллами V-VI группы подгруппы В (например, некоторые сульфиды и фосфиды, так же как
группы с неметаллами V-VI группы подгруппы В (например, некоторые сульфиды и фосфиды, так же как  Эти фазы обладают полупроводниковыми свойствами.
Эти фазы обладают полупроводниковыми свойствами.
Фазы с металлическим типом связи. Фазы, в которых преобладает металлический тип связи, образуются при взаимодействии переходных металлов  . Фазы называются соответственно карбидами, нитридами, боридами, гидридами.
. Фазы называются соответственно карбидами, нитридами, боридами, гидридами.
Кристаллическая структура этих соединений зависит от относительных размеров атомов неметалла  и атомов металла
и атомов металла  Если отношение
Если отношение  образуются промежуточные фазы с простыми пространственными решетками, атомы неметалла в которых располагаются в порах. Эти промежуточные фазы называют фазами внедрения. Если отношение
образуются промежуточные фазы с простыми пространственными решетками, атомы неметалла в которых располагаются в порах. Эти промежуточные фазы называют фазами внедрения. Если отношение  то атом неметалла не может разместиться в поре, тогда образуются сложные пространственные решетки с большим числом атомов в элементарной ячейке.
то атом неметалла не может разместиться в поре, тогда образуются сложные пространственные решетки с большим числом атомов в элементарной ячейке.
Фазы внедрения. Эти фазы имеют кристаллические решетки, типичные для чистых металлов; чаще всего это плотноупакованные ГЦК и ГПУ решетки; при этом тип решетки не совпадает с типом решетки металла, образующего фазу внедрения (исключением являются некоторые гидриды). Атомы металла в фазах внедрения размещаются в узлах решетки, тогда как атомы неметалла закономерно распределяются в октаэдрических или тетраэдрических порах решетки. Тетраэдрические поры имеют меньший размер, поэтому в них могут разместиться лишь атомы водорода.
Химический состав фаз внедрения указывается формулами:  и
и

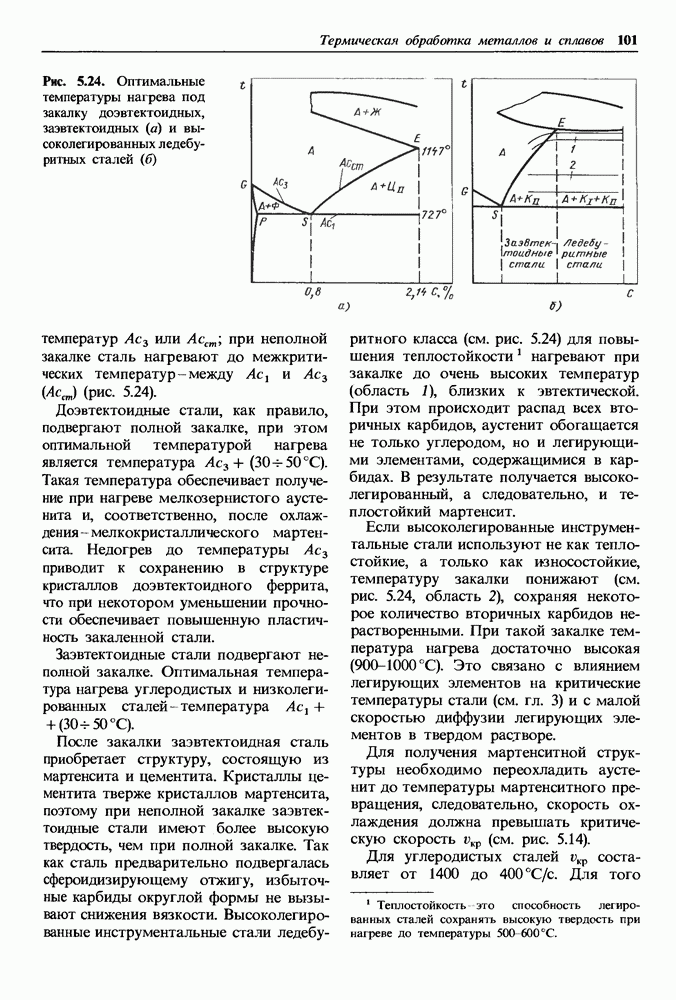
Рис. 1.18. Кристаллическая решетка  а — расположение ионов кислорода; б, в — металлический ион в тетраэдрической и октаэдрической порах
а — расположение ионов кислорода; б, в — металлический ион в тетраэдрической и октаэдрической порах
 , где
, где  металл, X - неметалл; однако это фазы переменного состава, в которых число неметаллических атомов отличается от стехиометрического состава.
металл, X - неметалл; однако это фазы переменного состава, в которых число неметаллических атомов отличается от стехиометрического состава.
К фазам внедрения типа  относятся следующие карбиды:
относятся следующие карбиды:  Вольфрам и молибден могут образовывать и фазы внедрения типа
Вольфрам и молибден могут образовывать и фазы внедрения типа  Примером фазы внедрения типа
Примером фазы внедрения типа  является нитрид железа
является нитрид железа  а фазы типа
а фазы типа  -гидрид циркония
-гидрид циркония 
В карбиде  фактическое содержание углерода, который располагается в междоузельных порах, может колебаться в пределах 38 — 50 ат. %. Очевидно, что только при 50 ат.
фактическое содержание углерода, который располагается в междоузельных порах, может колебаться в пределах 38 — 50 ат. %. Очевидно, что только при 50 ат.  углерода состав карбида точно описывается формулой
углерода состав карбида точно описывается формулой 
Указывалось, что в фазах внедрения преобладает металлическая связь, чем определяются такие свойства этих фаз, как высокая электропроводимость, положительный коэффициент электрического сопротивления, как у чистых металлов и твердых растворов на их основе. Некоторые фазы внедрения обладают сверхпроводимостью; однако есть свойства, которые указывают на значительную долю в фазах внедрения ковалентной связи. Большинство фаз внедрения чрезвычайно тугоплавки и имеют твердость, близкую к твердости алмаза. Фазы внедрения — это самые тугоплавкие и твердые промежуточные фазы.
Карбиды и нитриды, относящиеся к фазам внедрения, присутствуют в структуре многих коррозионно-стойких, износостойких и жаропрочных конструкционных сталей. Карбиды  служат основой спеченных твердых сплавов для режущих инструментов. Использование таких сплавов позволило увеличить скорости резания в десятки раз (см. гл. 18).
служат основой спеченных твердых сплавов для режущих инструментов. Использование таких сплавов позволило увеличить скорости резания в десятки раз (см. гл. 18).
К карбидам с отношением  относятся карбид железа (в сталях его называют цементитом), карбид марганца и карбиды хрома (например, в карбиде железа отношение
относятся карбид железа (в сталях его называют цементитом), карбид марганца и карбиды хрома (например, в карбиде железа отношение  Карбид железа
Карбид железа  и карбиды хрома
и карбиды хрома  - важнейшие промежуточные фазы в конструкционных и инструментальных сталях, во многом определяюшие их свойства. В последних карбидах преобладает металлическая связь, хотя имеется и определенная доля ковалентной связи.
- важнейшие промежуточные фазы в конструкционных и инструментальных сталях, во многом определяюшие их свойства. В последних карбидах преобладает металлическая связь, хотя имеется и определенная доля ковалентной связи.
Эти промежуточные фазы отличаются высокой твердостью и хрупкостью, они также достаточно тугоплавки, но уступают по этим свойствам карбидам, являющимся фазами внедрения.
Системы металл металл. При сплавлении металлов могут образовываться промежуточные фазы с металлическим типом связи. К ним относятся электронные фазы, фазы Лавеса и ст-фазы.
Электронные фазы. Это фазы переменного состава. Для максимального содержания металла более высокой валентности характерно совершенно определенное значение электронной концентрации -3/2, 21/13, 7/4, т. е. отношение числа валентных электронов к числу атомов. Фазы с указанными значениями электронной концентрации принято обозначать  и е-фазами соответственно.
и е-фазами соответственно.
Указанным электронным концентрациям можно приписать соответствующие химические формулы. Например, в сплавах меди с цинком, в которых могут образоваться все фазы с указанными концентрациями, такими формулами будут соответственно 
В большинстве сплавов  -фазы имеют ОЦК решетку, у-фазы сложную кубическую решетку с 52 атомами в элементарной ячейке и е-фазы-ГПУ решетку.
-фазы имеют ОЦК решетку, у-фазы сложную кубическую решетку с 52 атомами в элементарной ячейке и е-фазы-ГПУ решетку.
Свойства электронных соединений, в частности, механические свойства, зависят в значительной мере от степени упорядоченности расположения атомов компонентов в кристаллической решетке электронного соединения. Так,  -фазы с ОЦК решеткой во всех системах при высоких температурах неупорядочены, и в этом состоянии их свойства близки к свойствам твердых растворов, т. е. они не отличаются высокой твердостью и обладают хорошей пластичностью. При низких температурах неупорядоченные р-фазы неустойчивы: они либо распадаются на двухфазные смеси, либо упорядочиваются, как, например, в системе
-фазы с ОЦК решеткой во всех системах при высоких температурах неупорядочены, и в этом состоянии их свойства близки к свойствам твердых растворов, т. е. они не отличаются высокой твердостью и обладают хорошей пластичностью. При низких температурах неупорядоченные р-фазы неустойчивы: они либо распадаются на двухфазные смеси, либо упорядочиваются, как, например, в системе  Упорядоченные Р-фазы значительно более тверды и хрупки, у-фазы почти всегда упорядочены, причем вплоть до температуры плавления и во всех системах обладают хрупкостью, е-фазы всегда имеют неупорядоченное строение.
Упорядоченные Р-фазы значительно более тверды и хрупки, у-фазы почти всегда упорядочены, причем вплоть до температуры плавления и во всех системах обладают хрупкостью, е-фазы всегда имеют неупорядоченное строение.
Электронные соединения присутствуют в структуре многих сплавов на медной основе: латунях  бронзах
бронзах  и др.); они являются упрочняющими фазами (см. п. 9.4).
и др.); они являются упрочняющими фазами (см. п. 9.4).
Фазы Лавеса. Эти промежуточные фазы практически постоянного состава  образуются при взаимодействии металлов самых
образуются при взаимодействии металлов самых
различных групп периодической таблицы элементов; образование их определяется размерным фактором: атомный радиус элемента В меньше, чем атомный радиус элемента А, на 20-30%.
Фазы Лавеса имеют упорядоченные сложные кубические или гексагональные решетки; в магнитном поле они ведут себя как диамагнетики.
Фазы Лавеса, образованные переходными металлами  присутствуют в структуре некоторых жаропрочных сплавов и способствуют их упрочнению (см. п. 14.3).
присутствуют в структуре некоторых жаропрочных сплавов и способствуют их упрочнению (см. п. 14.3).
Сигма-фазы. Эти фазы переменного состава образуются при сплавлении переходных металлов, имеющих близкие размеры атомов;  -фазы имеют частично упорядоченную сложную решетку.
-фазы имеют частично упорядоченную сложную решетку.
В железных сплавах, содержащих больше  которые используются как коррозионно-стойкие конструкционные материалы, очень медленное охлаждение из области твердого раствора или изотермические выдержки при 800-600 °С приводят к образованию кристаллов
которые используются как коррозионно-стойкие конструкционные материалы, очень медленное охлаждение из области твердого раствора или изотермические выдержки при 800-600 °С приводят к образованию кристаллов  -фазы, которое сопровождается резким увеличением твердости и охрупчиванием сплавов.
-фазы, которое сопровождается резким увеличением твердости и охрупчиванием сплавов.
| << Предыдущий параграф | Следующий параграф >> |
- Введение
- Глава 1. СТРОЕНИЕ И СВОЙСТВА МАТЕРИАЛОВ
- 1.1. Элементы кристаллографии
- 1.2. Влияние типа связи на структуру и свойства кристаллов
- Молекулярные кристаллы.
- Ковалентные кристаллы.
- Металлические кристаллы.
- Ионные кристаллы.
- 1.3. Фазовый состав сплавов
- Твердые растворы.
- Промежуточные фазы.
- 1.4. Дефекты кристаллов
- Линейные дефекты.
- Поверхностные дефекты.
- 1.5. Диффузия в металлах и сплавах
- 1.6. Жидкие кристаллы
- 1.7. Структура полимеров, стекла и керамики
- Глава 2. ФОРМИРОВАНИЕ СТРУКТУРЫ ЛИТЫХ МАТЕРИАЛОВ
- 2.1. Самопроизвольная кристаллизация
- 2.2. Несамопроизвольная кристаллизация
- 2.3. Форма кристаллов и строение слитков
- 2.4. Получение монокристаллов
- 2.5. Аморфное состояние металлов
- Глава 3. ВЛИЯНИЕ ХИМИЧЕСКОГО СОСТАВА НА РАВНОВЕСНУЮ СТРУКТУРУ СПЛАВОВ
- 3.1. Методы построения диаграмм состояния
- 3.2. Основные равновесные диаграммы состояния двойных сплавов
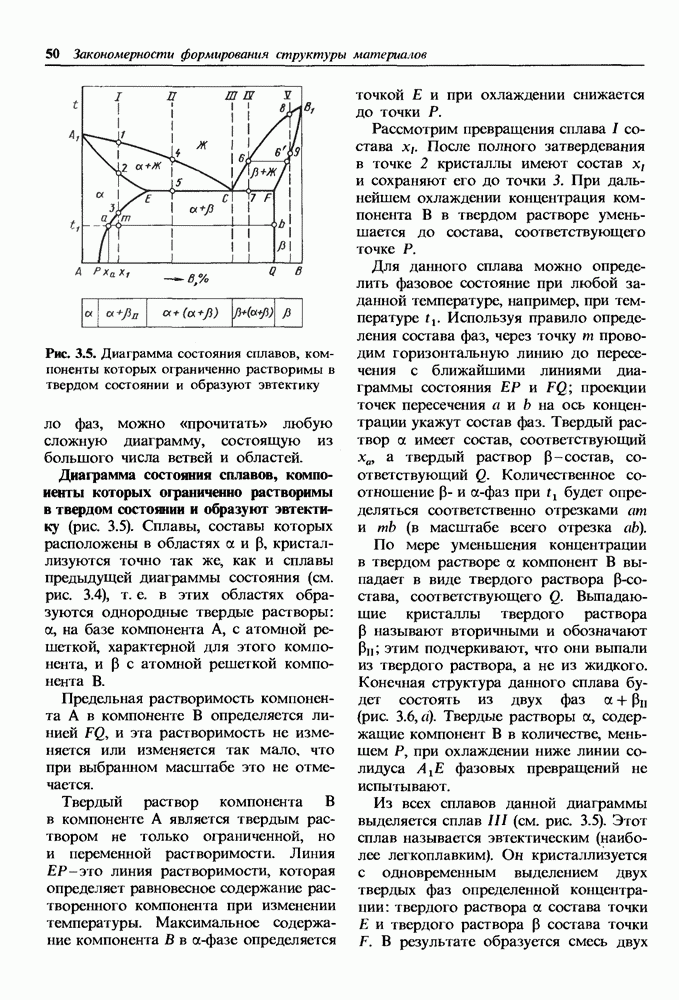
- Диаграмма состояния сплавов, компоненты которых ограниченно растворимы в твердом состоянии и образуют эвтектику
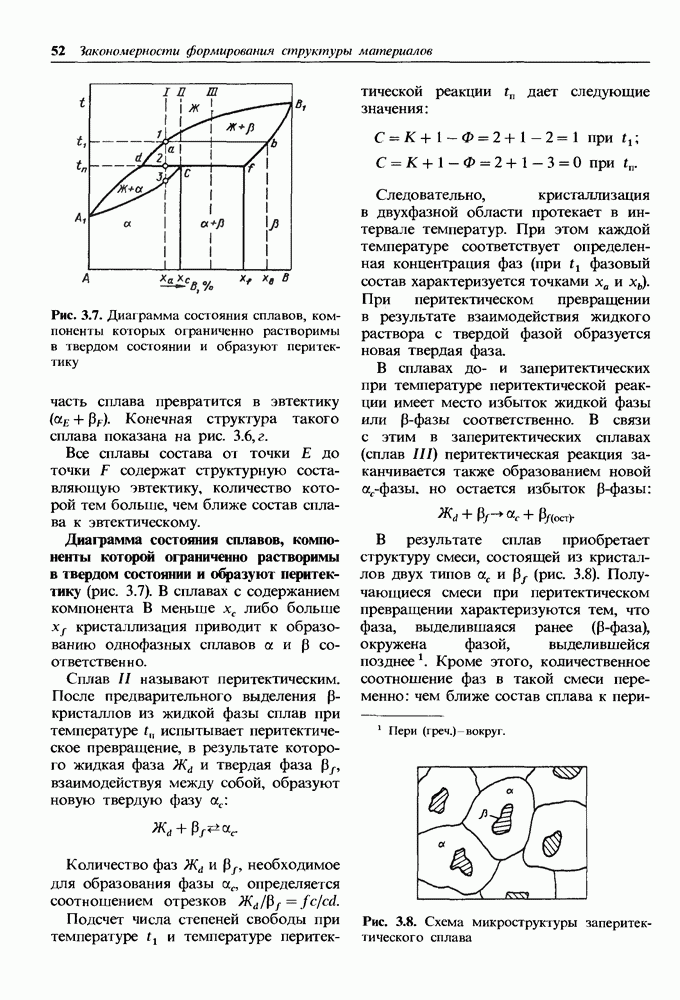
- Диаграмма состояния сплавов, компоненты которой ограниченно растворимы в твердом состоянии и образую! перитектику
- Диаграмма состояния сплавов с полиморфным превращением одного из компонентов.
- Диаграмма состояния сплавов с полиморфными превращениями компонентов и эвтектоидным превращением.
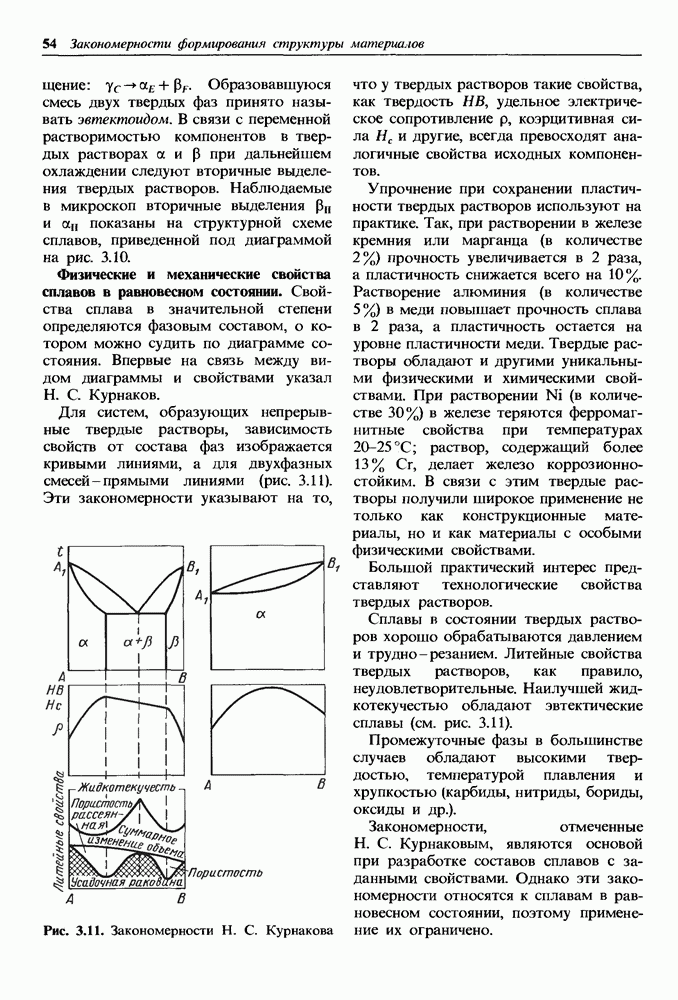
- Физические и механические свойства сплавов в равновесном состоянии.
- 3.3. Диаграмма состояния железоуглеродистых сплавов
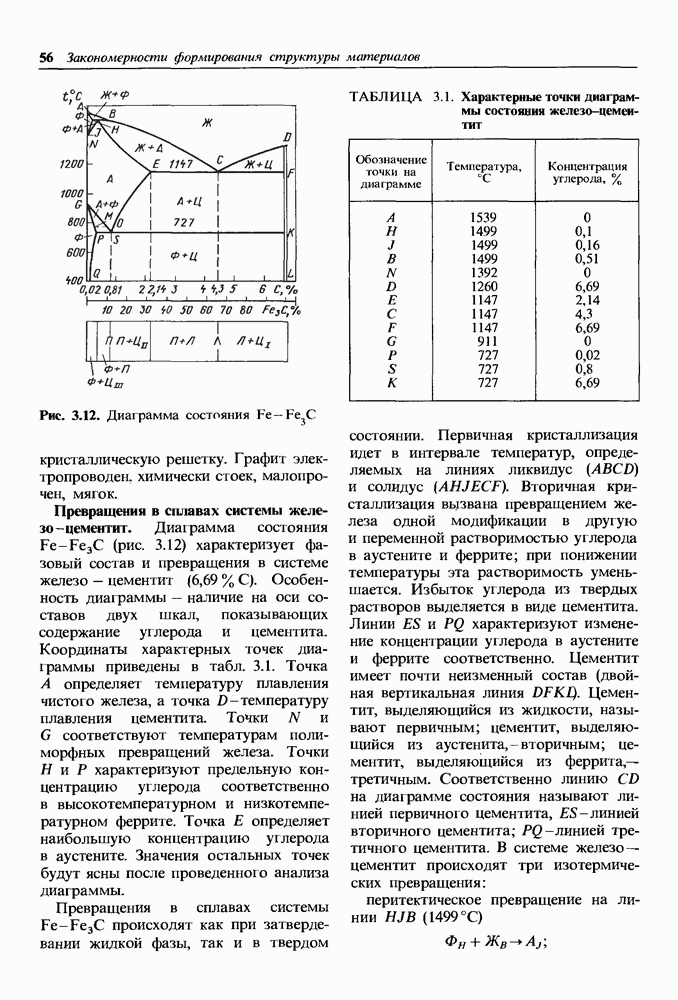
- Превращения в сплавах системы железо-цементит.
- Превращения в сплавах системы железо-графит.
- 3.4. Влияние легирующих элементов на равновесную структуру сталей
- Карбиды в легированных сталях.
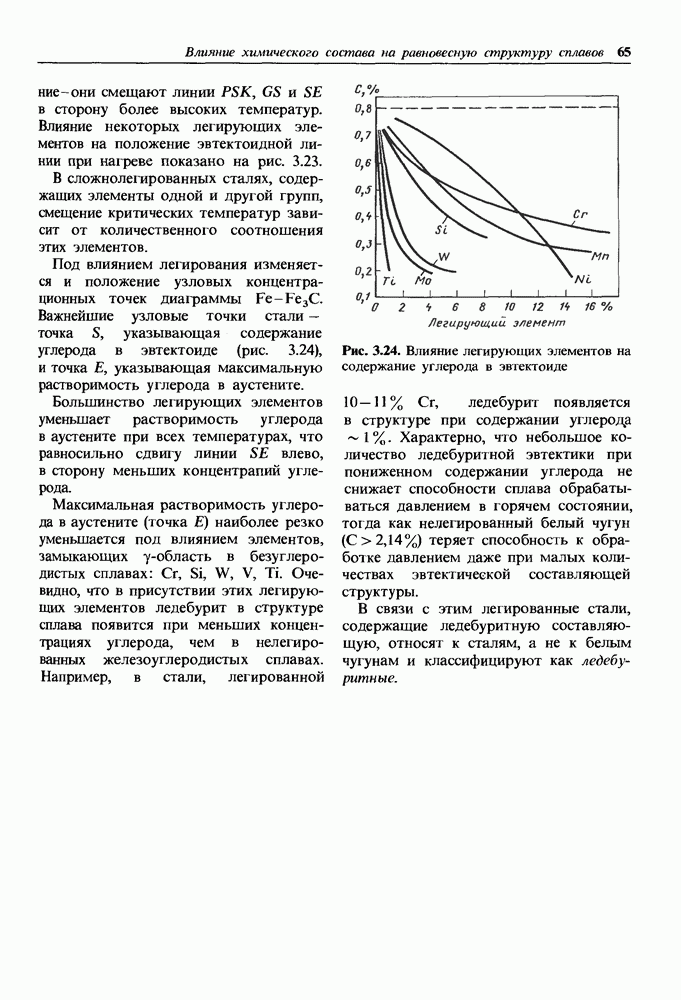
- Влияние легирующих элементов на температуры фазовых превращений сталей при нагреве и на состав точек S и Е диаграммы.
- Глава 4. ФОРМИРОВАНИЕ СТРУКТУРЫ ДЕФОРМИРОВАННЫХ МЕТАЛЛОВ И СПЛАВОВ
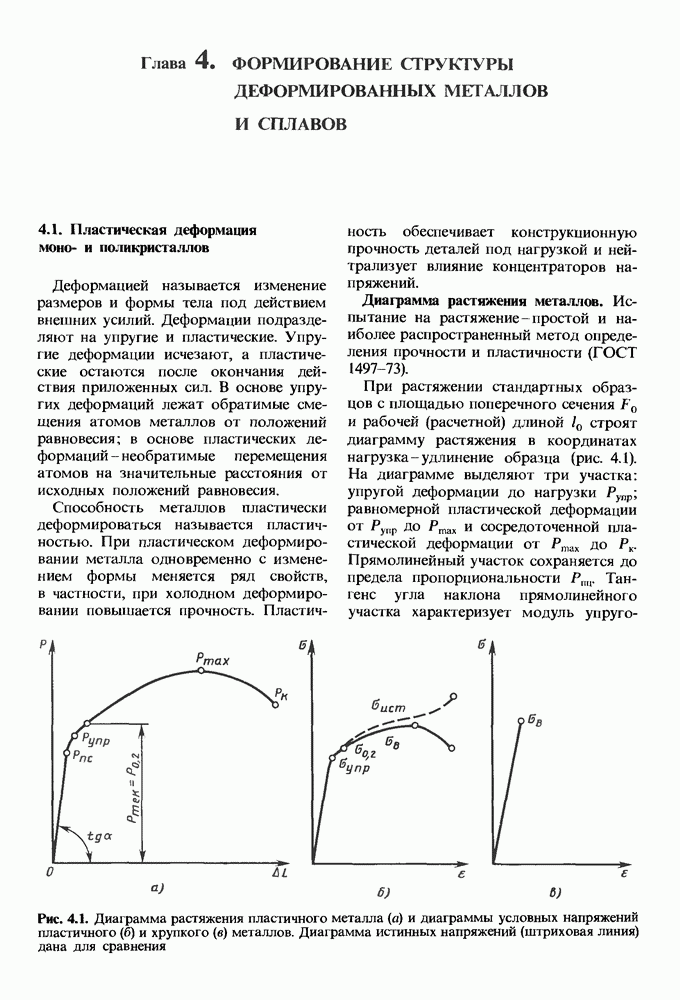
- 4.1. Пластическая деформация моно- и поликристаллов
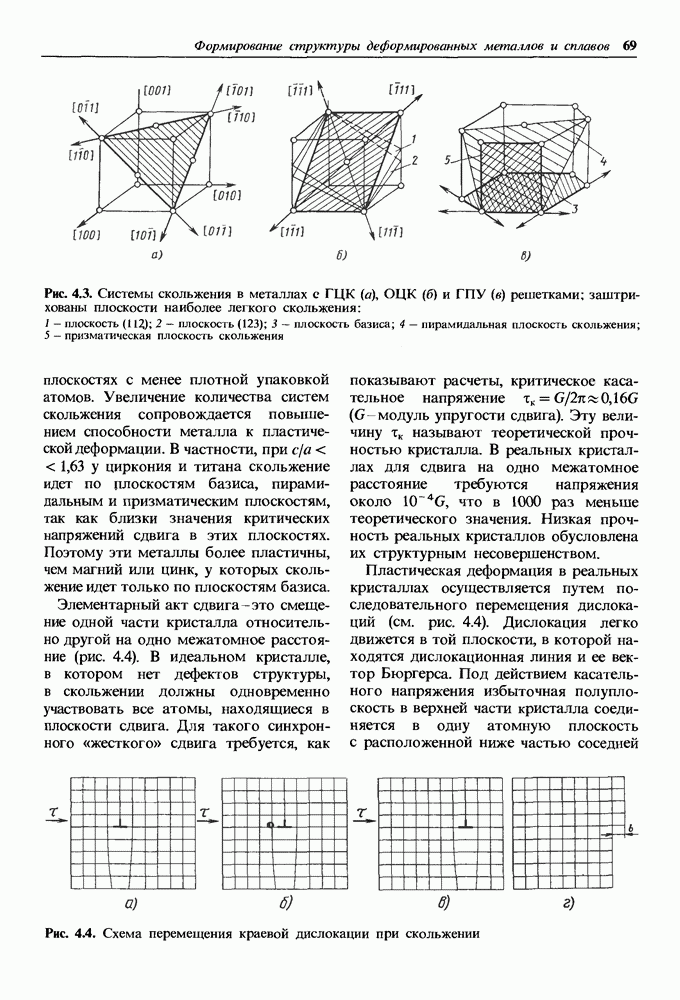
- Механизм пластической деформации
- Пластическая деформация поликристаллических металлов.
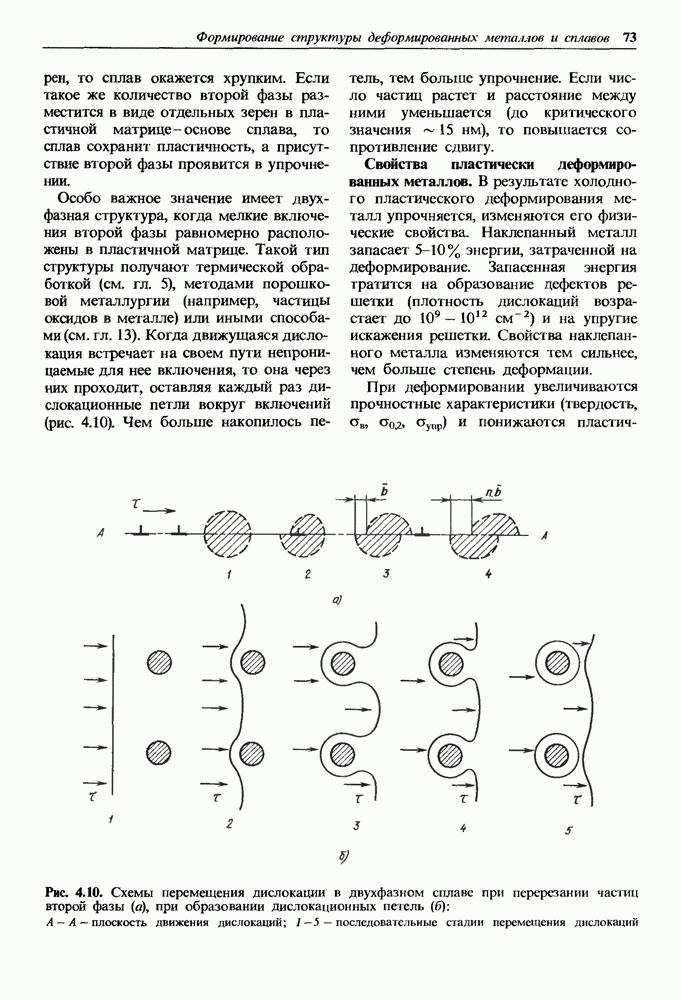
- Деформирование двухфазных сплавов оказывается более сложным.
- Свойства наклепанного металла изменяются тем сильнее, чем больше степень деформации.
- 4.2. Возврат и рекристаллизация
- Глава 5. ТЕРМИЧЕСКАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- 5.2. Основное оборудование для термической обработки
- 5.3. Термическая обработка сплавов, не связанная с фазовыми превращениями в твердом состоянии
- Рекристаллизационный отжиг.
- Диффузионный отжиг (гомогенизация).
- 5.4. Термическая обработка сплавов с переменной растворимостью компонентов в твердом состоянии
- 5.5. Термическая обработка сталей с эвтектоидным превращением
- Превращения аустенита при различных степенях переохлаждения.
- 5.6. Основные виды термической обработки стали
- Нормализация сталей.
- Закалка сталей.
- Закаливаемость в прокаливаемость сталей.
- Отпуск закаленных сталей.
- Глава 6. ХИМИКО-ТЕРМИЧЕСКАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- 6.2. Диффузионное насыщение углеродом и азотом
- Азотирование стали.
- Ионное азотирование и цементация.
- Одновременное насыщение поверхности стали углеродом и азотом.
- 6.3. Диффузионное насыщение сплавов металлами и неметаллами
- Раздел первый. Конструкционные материалы
- 7.1. Общие требования, предъявляемые к конструкционным материалам
- 7.2. Конструкционная прочность материалов и критерии ее оценки
- 7.3. Методы повышения конструкционной прочности
- 7.4. Классификация конструкционных материалов
- Глава 8. СТАЛИ, ОБЕСПЕЧИВАЮЩИЕ ЖЕСТКОСТЬ, СТАТИЧЕСКУЮ И ЦИКЛИЧЕСКУЮ ПРОЧНОСТЬ
- 8.1. Классификация конструкционных сталей
- 8.2. Влияние углерода и постоянных примесей на свойства стали
- 8.3. Углеродистые стали
- 8.4. Легированные стали
- Легированные стали нормальной и повышенной статической прочности.
- Легированные высокопрочные стали.
- Легированные стали с повышенной циклической прочностью.
- Глава 9. МАТЕРИАЛЫ С ОСОБЫМИ ТЕХНОЛОГИЧЕСКИМИ СВОЙСТВАМИ
- 9.1. Стали с улучшенной обрабатываемостью резанием
- 9.2. Стали с высокое технологической пластичностью и свариваемостью
- 9.3. Железоуглеродистые сплавы с высокими литейными свойствами
- Серые чугуны.
- Высокопрочные чугуны.
- Ковкие чугуны.
- 9.4. Медные сплавы
- Общая характеристика и классификация медных сплавов.
- Латуни.
- Бронзы.
- Глава 10. ИЗНОСОСТОЙКИЕ МАТЕРИАЛЫ
- 10.2. Закономерности изнашивания деталей, образующих пары трения, и пути уменьшения их износа
- 10.3. Материалы с высокой твердостью поверхности
- Материалы, устойчивые к усталостному виду изнашивания.
- Материалы, устойчивые к изнашиванию в условиях больших давлений и ударных нагрузок.
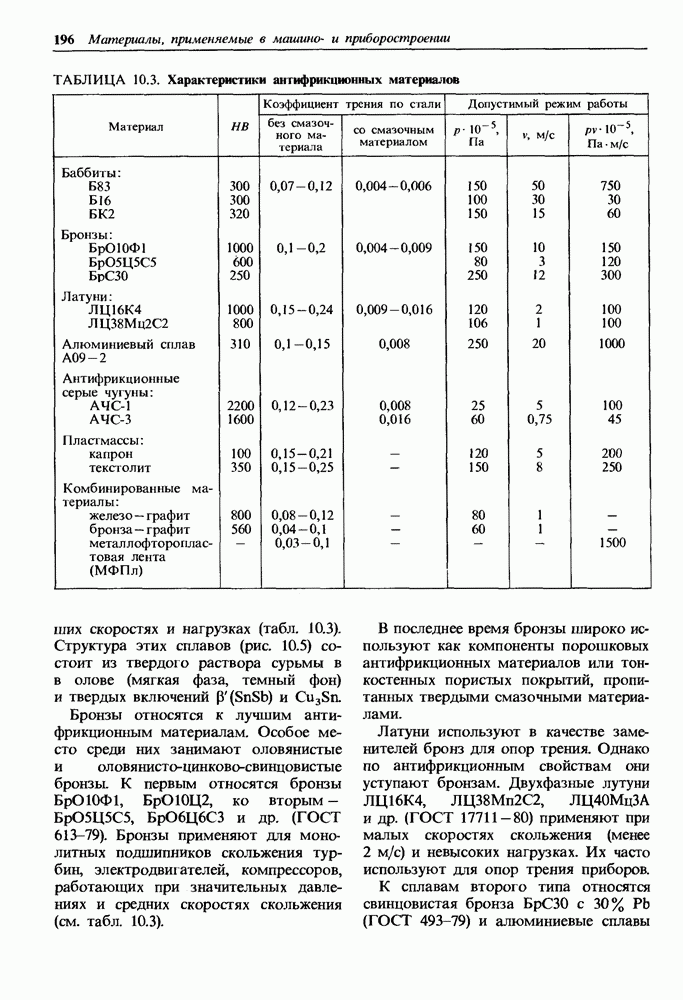
- 10.4. Антифрикционные материалы
- Неметаллические материалы.
- Комбинированные материалы.
- Минералы.
- 10.5. Фрикционные материалы
- Глава 11. МАТЕРИАЛЫ С ВЫСОКИМИ УПРУГИМИ СВОЙСТВАМИ
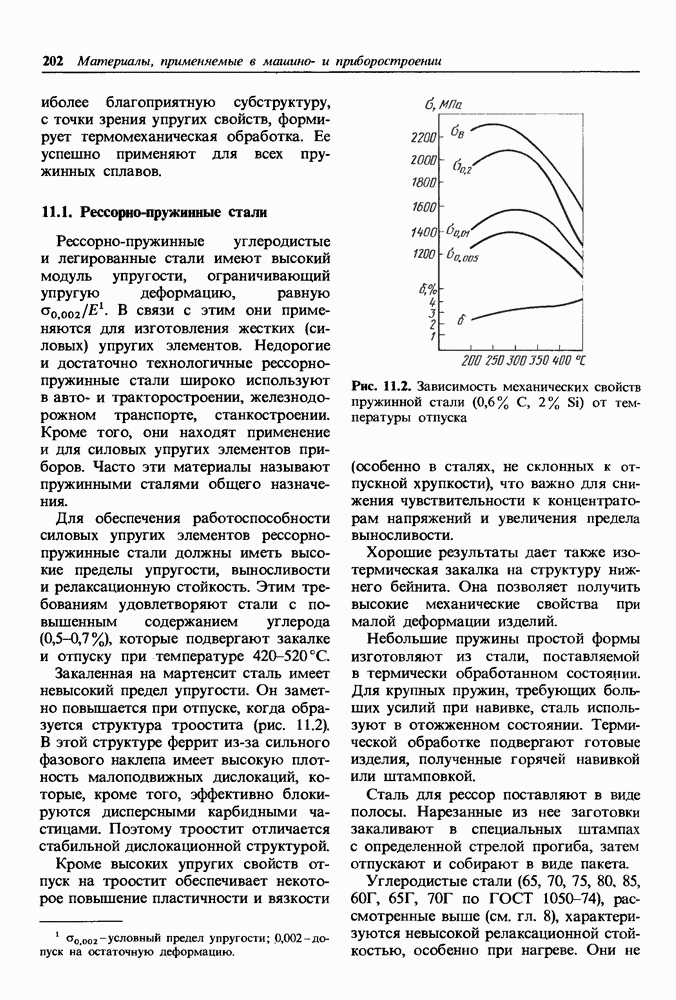
- 11.1. Рессорно-пружинные стали
- 11.2. Пружинные материалы приборостроения
- Глава 12. МАТЕРИАЛЫ С МАЛОЙ ПЛОТНОСТЬЮ
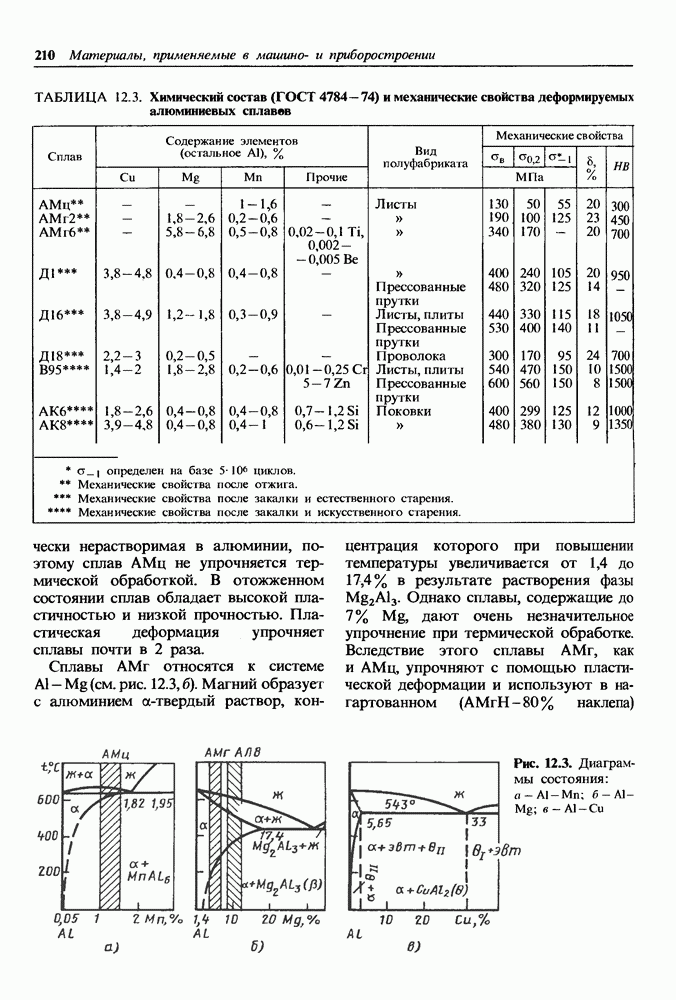
- 12.1. Сплавы на основе алюминия
- Общая характеристика и классификация алюминиевых сплавов.
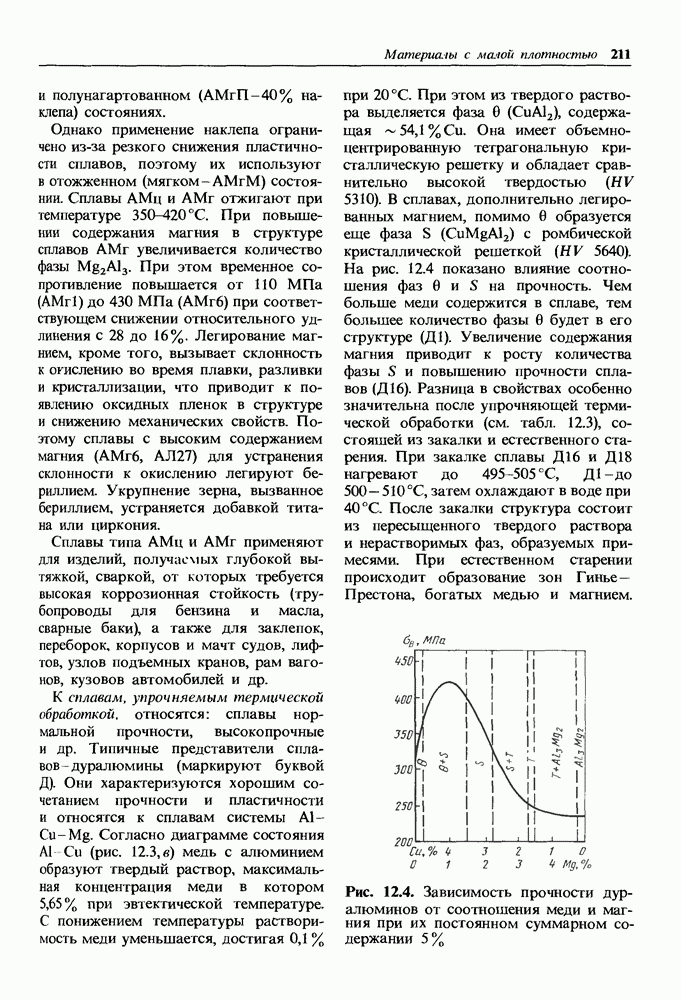
- Деформируемые алюминиевые сплавы.
- Литейные алюминиевые сплавы.
- Гранулированные сплавы.
- 12.2. Сплавы на основе магния
- Общая характеристика и классификация магниевых сплавов.
- Деформируемые магниевые сплавы.
- Литейные магниевые сплавы.
- 12.3. Неметаллические материалы
- Механические свойства термопластичных пластмасс.
- Механические свойства термореактивных пластмасс.
- Глава 13. МАТЕРИАЛЫ С ВЫСОКОЙ УДЕЛЬНОЙ ПРОЧНОСТЬЮ
- 13.1. Титан и сплавы на его основе
- Влияние легирующих элементов на структуру и свойства титановых сплавов.
- Особенности термической обработки титановых сплавов.
- Промышленные титановые сплавы.
- 13.2. Бериллий и сплавы на его основе
- Бериллиевые сплавы.
- 13.3. Композиционные материалы
- Дисперсно-упрочненные композиционные материалы.
- Волокнистые композиционные материалы.
- Композиционные материалы на неметаллической основе.
- Композиционные материалы на металлической основе.
- Глава 14. МАТЕРИАЛЫ, УСТОЙЧИВЫЕ К ВОЗДЕЙСТВИЮ ТЕМПЕРАТУРЫ И РАБОЧЕЙ СРЕДЫ
- 14.1. Коррозионно-стойкие материалы
- Коррозионно-стойкие непассивирующиеся металлы.
- Коррозионностойкие пассивирующиеси металлы.
- Коррозионно-стойкие покрытия.
- 14.2. Жаростойкие материалы
- Жаростойкость металлов.
- Жаростойкость сплавов.
- 14.3. Жаропрочные материалы
- Основные группы жаропрочных материалов.
- 14.4. Хладостойкие материалы
- Основные группы хладостойких материалов.
- 14.5. Радиационно-стойкие материалы
- Влияние облучения на коррозионную стойкость.
- Раздел второй. Материалы с особыми физическими свойствами
- 15.1. Общие сведения о ферромагнетиках
- 15.2. Магнитно-мягкие материалы
- Низкочастотные магнитно-мягкие материалы
- Высокочастотные магнитно-мягкие материалы.
- Материалы со специальными магнитными свойствами.
- 15.3. Магнитно-твердые материалы
- Магнитно-твердые лнтые материалы.
- Порошковые магнитно-твердые материалы.
- Деформируемые магнитно-твердые сплавы.
- Глава 16. МАТЕРИАЛЫ С ОСОБЫМИ ТЕПЛОВЫМИ СВОЙСТВАМИ
- 16.1. Сплавы с заданным температурным коэффициентом линейного расширении
- 16.2. Сплавы с заданным температурным коэффициентом модуля упругости
- Глава 17. МАТЕРИАЛЫ С ОСОБЫМИ ЭЛЕКТРИЧЕСКИМИ СВОЙСТВАМИ
- 17.1. Материалы высокой электрической проводимости
- Проводниковые материалы.
- 17.2. Полупроводниковые материалы
- Кристаллофизические методы получения сверхчистых материалов.
- Легирование полупроводников и получение p-n-переходов.
- 17.3. Диэлектрики
- Раздел третий. Инструментальные материалы
- Глава 18. МАТЕРИАЛЫ ДЛЯ РЕЖУЩИХ И ИЗМЕРИТЕЛЬНЫХ ИНСТРУМЕНТОВ
- 18.1. Материалы для режущих инструментов
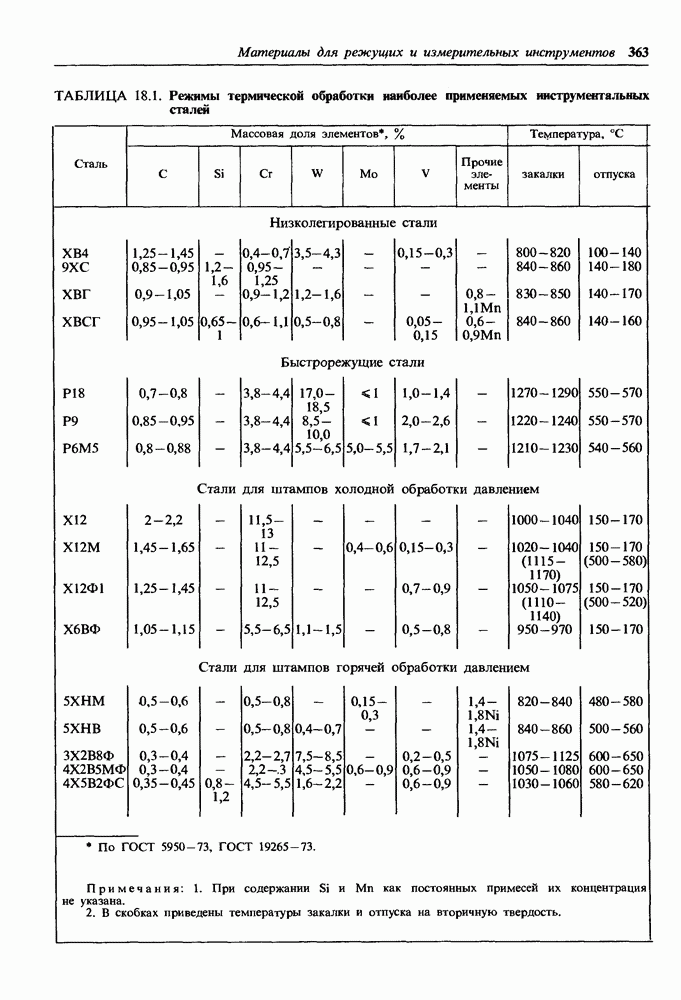
- Низколегированные стали.
- Быстрорежущие стали.
- Спеченные твердые сплавы.
- Сверхтвердые материалы.
- 18.2. Стали для измерительных инструментов
- Глава 19. СТАЛИ ДЛЯ ИНСТРУМЕНТОВ ОБРАБОТКИ МЕТАЛЛОВ ДАВЛЕНИЕМ
- 19.1. Стали для инструментов холодной обработки давлением
- 19.2. Стали для инструментов горячей обработки давлением
- Приложение
- Список литературы