| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
§ 262. Растворение твердых тел в жидкостях.
Хорошо известно, что если в воду опустить кусок сахара, то через некоторое время сахар исчезнет и получится однородное вещество (раствор). Сладкий вкус этого раствора показывает, что молекулы сахара распределились по всему объему раствора. Это распределение происходит вследствие молекулярного движения (диффузии); его можно значительно ускорить, если перемешивать раствор.
Растворение твердого вещества в жидкости по существу мало чем отличается от растворения жидкости в жидкости. И в этом случае молекулы растворенного вещества постепенно распределяются среди молекул растворителя. Масса растворенного вещества, приходящаяся на единицу объема растворителя, носит название концентрации раствора. Вещество растворяется в жидкости до некоторой определенной концентрации, которая зависит от природы растворителя и растворяемого вещества, а также от температуры.
Растворы, концентрация которых имеет предельное значение, называют насыщенными. Чем выше концентрация насыщенного раствора, тем больше растворимость вещества в данном растворителе. Особенно хорошим растворителем является вода, в которой очень многие вещества растворяются до значительных концентраций. В спирте растворимость, вообще говоря, хуже, в бензоле — еще хуже, хотя встречаются вещества, которые лучше растворяются в бензоле или спирте, чем в воде. Растворимость различных веществ в одном и том же растворителе может быть различной. Кроме того, растворимость может сильно зависеть от температуры. В табл. 14 указаны растворимости в воде некоторых веществ при различных температурах.
Таблица 14. Растворимость в воде некоторых веществ при различных температурах (в граммах на 100 мл)
|
Вещество |
Температура, |
||
|
0 |
18 |
100 |
|
|
Хлористое серебро |
0,00006 |
0,00013 |
- |
|
Углекислый литий |
1,5 |
1,3 |
0,8 |
|
Азотнокислый калий |
13 |
29 |
250 |
|
Хлористый натрий |
35,5 |
36,0 |
39,6 |
|
>> литий |
64 |
79 |
130 |
|
>> кальций |
50 |
71 |
155 |
|
>> цинк |
210 |
360 |
610 |
В большинстве случаев при повышении температуры растворимость повышается, причем нередко очень значительно (например, азотнокислый калий). Иногда изменение растворимости при нагревании невелико (хлористый натрий), а в редких случаях наблюдается даже уменьшение растворимости при нагревании (углекислый литий). Если насыщенный раствор азотнокислого калия или другого вещества, растворимость которого возрастает с температурой, охладить, то часть растворенного вещества выделится в виде твердого осадка. При некоторых условиях (чистота раствора и посуды, осторожное охлаждение) иногда удается получить растворы с концентрацией, превышающей предельную (пересыщенные растворы). Если в такой раствор бросить крупицу растворенного вещества, то сейчас же произойдет кристаллизация и концентрация раствора уменьшится до концентрации, соответствующей насыщению.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ОТ ИЗДАТЕЛЬСТВА
- ИЗ ПРЕДИСЛОВИЯ К ПЕРВОМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- Глава I. Кинематика
- § 1. Движение тел
- § 2. Кинематика. Относительность движения и покоя.
- § 3. Траектория движения
- § 4. Поступательное и вращательное движения тела
- § 5. Движение точки
- § 6. Описание движения точки
- § 7. Измерение длины
- § 8. Измерение промежутков времени
- § 9. Равномерное прямолинейное движение и его скорость
- § 10. Знак скорости при прямолинейном движении
- § 11. Единицы скорости
- § 12. Графики зависимости пути от времени
- § 13. Графики зависимости скорости от времени
- § 14. Неравномерное прямолинейное движение
- § 15. Мгновенная скорость
- § 16. Ускорение при прямолинейном движении
- § 17. Скорость прямолинейного равноускоренного движения
- § 18. Знак ускорения при прямолинейном движении
- § 19. Графики скорости при прямолинейном равноускоренном движении
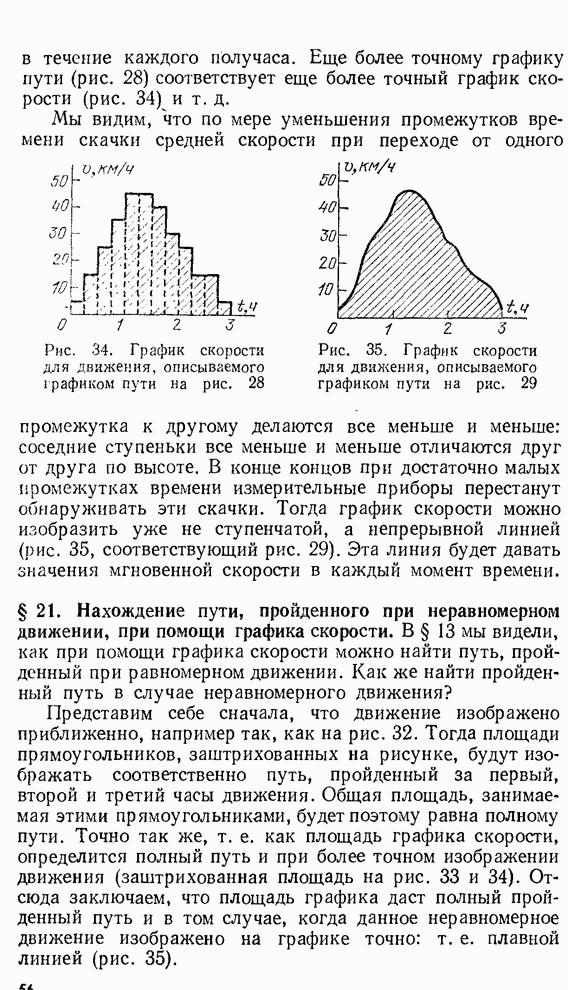
- § 20. Графики скорости при произвольном неравномерном движении
- § 21. Нахождение пути, пройденного при неравномерном движении, при помощи графика скорости
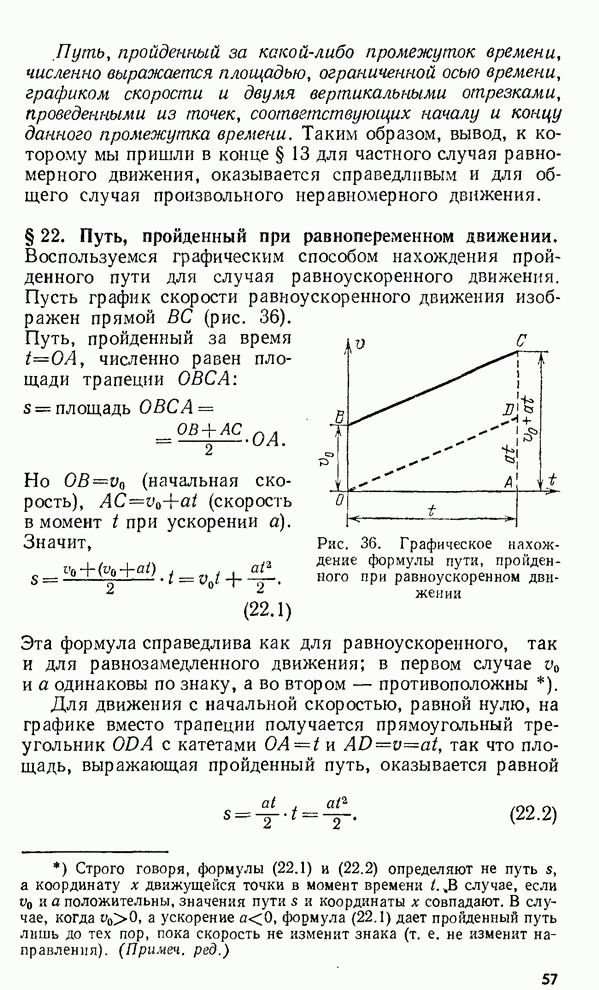
- § 22. Путь, пройденный при равнопеременном движении
- § 23. Векторы
- § 24. Разложение вектора на составляющие
- § 25. Криволинейное движение
- § 26. Скорость криволинейного движения
- § 27. Ускорение при криволинейном движении
- § 28. Движение относительно разных систем отсчета
- § 29. Кинематика космических движений
- Глава II. Динамика
- § 30. Задачи динамики
- § 31. Закон инерции
- § 32. Инерциальные системы отсчета
- § 33. Принцип относительности Галилея
- § 34. Силы
- § 35. Уравновешивающиеся силы. О покое тела и о движении по инерции
- § 36. Сила — вектор. Эталон силы
- § 37. Динамометры
- § 38. Точка приложения силы
- § 39. Равнодействующая сила
- § 40. Сложение сил, направленных по одной прямой
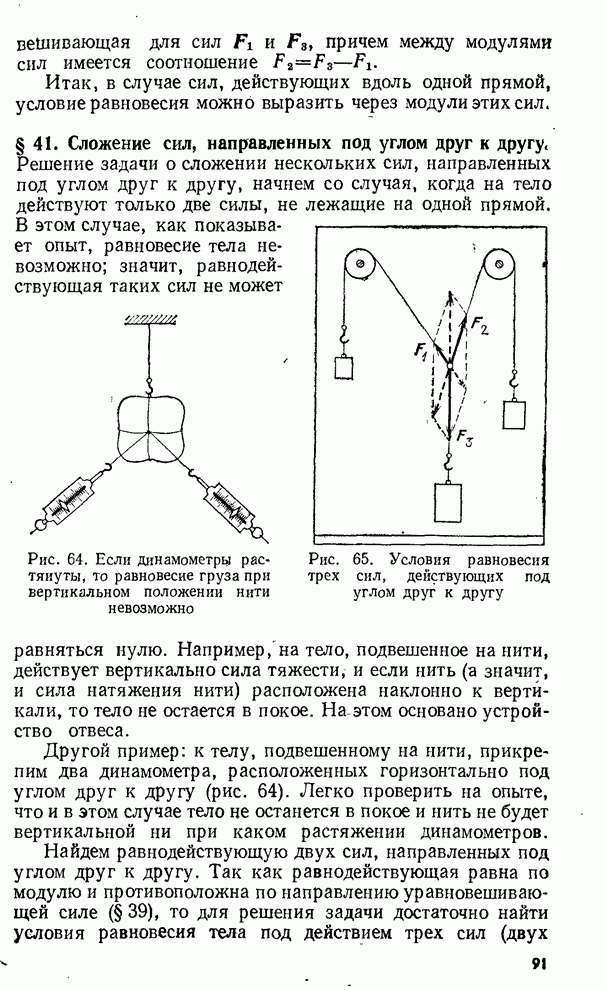
- § 41. Сложение сил, направленных под углом друг к другу
- § 42. Связь между силой и ускорением
- § 43. Масса тела
- § 44. Второй закон Ньютона
- § 45. Единицы силы и массы
- § 46. Системы единиц
- § 47. Третий закон Ньютона
- § 48. Примеры применения третьего закона Ньютона
- § 49. Импульс тела
- § 50. Система тел. Закон сохранения импульса
- § 51. Применения закона сохранения импульса
- § 52. Свободное падение тел
- § 53. Ускорение свободного падения
- § 54. Падение тела без начальной скорости и движение тела, брошенного вертикально вверх
- § 55. Вес тела
- § 56. Масса и вес
- § 57. Плотность вещества
- § 58. Возникновение деформаций
- § 59. Деформации в покоящихся телах, вызванные действием только сил, возникающих при соприкосновении
- § 60. Деформации в покоящихся телах, вызванные силой тяжести
- § 61. Деформации тела, испытывающего ускорение
- § 62. Исчезновение деформаций при падении тел
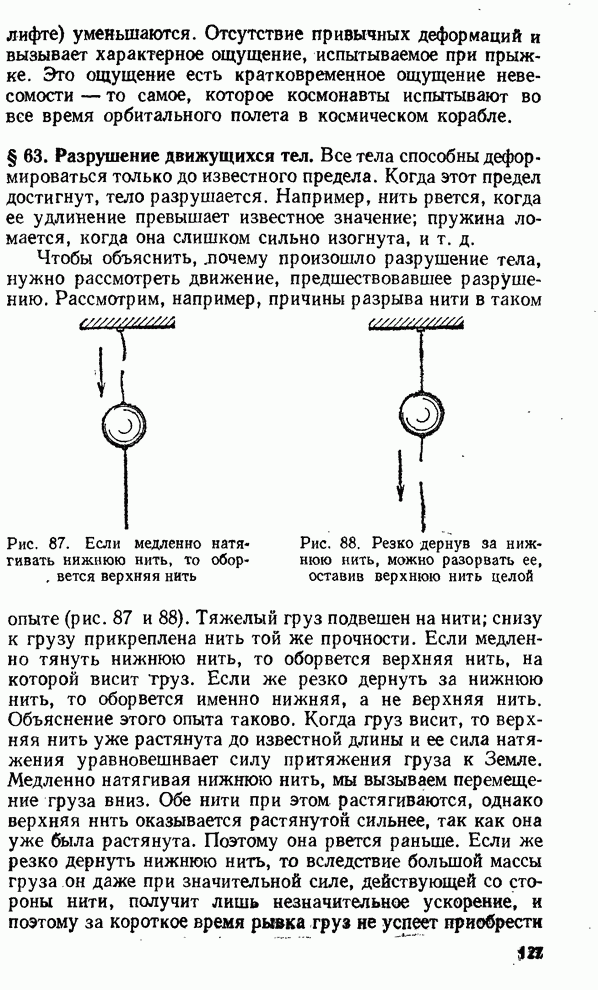
- § 63. Разрушение движущихся тел
- § 64. Силы трения
- § 65. Трение качения
- § 66. Роль сил трения
- § 67. Сопротивление среды
- § 68. Падение тел в воздухе
- Глава III. Статика
- § 69. Задачи статики
- § 70. Абсолютно твердое тело
- § 71. Перенос точки приложения силы, действующей на твердое тело
- § 72. Равновесие тела под действием трех сил
- § 73. Разложение сил на составляющие
- § 74. Проекции сил. Общие условия равновесия
- § 75. Связи. Силы реакции связей. Тело, закрепленное на оси
- § 76. Равновесие тела, закрепленного на оси
- § 77. Момент силы
- § 78. Измерение момента силы
- § 79. Пара сил
- § 80. Сложение параллельных сил. Центр тяжести
- § 81. Определение центра тяжести тел
- § 82. Различные случаи равновесия тела под действием силы тяжести
- § 83. Условия устойчивого равновесия под действием силы тяжести
- § 84. Простые машины
- § 85. Клин и винт
- Глава IV. Работа и энергия
- § 86. «Золотое правило» механики
- § 87. Применения «золотого правила»
- § 88. Работа силы
- § 89. Работа при перемещении, перпендикулярном к направлению силы
- § 90. Работа силы, направленной под любым углом к перемещению
- § 91. Положительная и отрицательная работа
- § 92. Единица работы
- § 93. О движении по горизонтальной плоскости
- § 94. Работа силы тяжести при движении по наклонной плоскости
- § 95. Принцип сохранения работы
- § 96. Энергия
- § 97. Потенциальная энергия
- § 98. Потенциальная энергия упругой деформации
- § 99. Кинетическая энергия
- § 100. Выражение кинетической энергии через массу и скорость тела
- § 101. Полная энергия тела
- § 102. Закон сохранения энергии
- § 103. Силы трения и закон сохранения механической энергии
- § 104. Превращение механической энергии во внутреннюю энергию
- § 105. Всеобщий характер закона сохранения энергии
- § 106. Мощность
- § 107. Расчет мощности механизмов
- § 108. Мощность, быстроходность и размеры механизма
- § 109. Коэффициент полезного действия механизмов
- Глава V. Криволинейное движение
- § 110. Возникновение криволинейного движения
- § 111. Ускорение при криволинейном движении
- § 112. Движение тела, брошенного в горизонтальном направлении
- § 113. Движение тела, брошенного под углом к горизонту
- § 114. Полет пуль и снарядов
- § 115. Угловая скорость
- § 116. Силы при равномерном движении по окружности
- § 117. Возникновение силы, действующей на тело, движущееся по окружности
- § 118. Разрыв маховиков
- § 119. Деформация тела, движущегося по окружности
- § 120. «Американские горки»
- § 121. Движение на закруглениях пути
- § 122. Движение подвешенного тела по окружности
- § 123. Движение планет
- § 124. Закон всемирного тяготения
- § 125. Искусственные спутники Земли
- Глава VI. Движение в неинерциальных системах отсчета и силы инерции
- § 126. Роль системы отсчета
- § 127. Движение относительно разных инерциальных систем отсчета
- § 128. Движение относительно инерциальной и неинерциальной систем отсчета
- § 129. Поступательно движущиеся неинерциальиые системы
- § 130. Силы инерции
- § 131. Эквивалентность сил инерции и сил тяготения
- § 132. Невесомость и перегрузки
- § 133. Является ли Земля инерциальиой системой отсчета?
- § 134. Вращающиеся системы отсчета
- § 135. Силы инерции при движении тела относительно вращающейся системы отсчета
- § 136. Доказательство вращения Земли
- § 137. Приливы
- Глава VII. Гидростатика
- § 138. Подвижность жидкости
- § 139. Силы давления
- § 140. Измерение сжимаемости жидкости
- § 141. «Несжимаемая» жидкость
- § 142. Силы давления в жидкости передаются во все стороны
- § 143. Направление сил давления
- § 144. Давление
- § 145. Мембранный манометр
- § 146. Независимость давления от ориентации площадки
- § 147. Единицы давления
- § 148. Определение сил давления по давлению
- § 149. Распределение давления внутри жидкости
- § 150. Закон Паскаля
- § 151. Гидравлический пресс
- § 152. Жидкость под действием силы тяжести
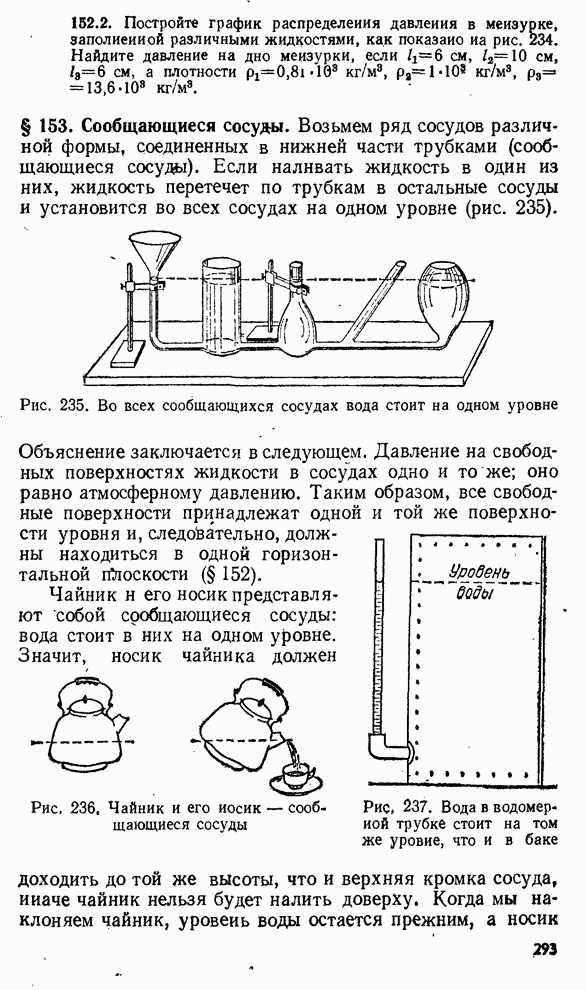
- § 153. Сообщающиеся сосуды
- § 154. Жидкостный манометр
- § 155. Устройство водопровода. Нагнетательный насос
- § 156. Сифон
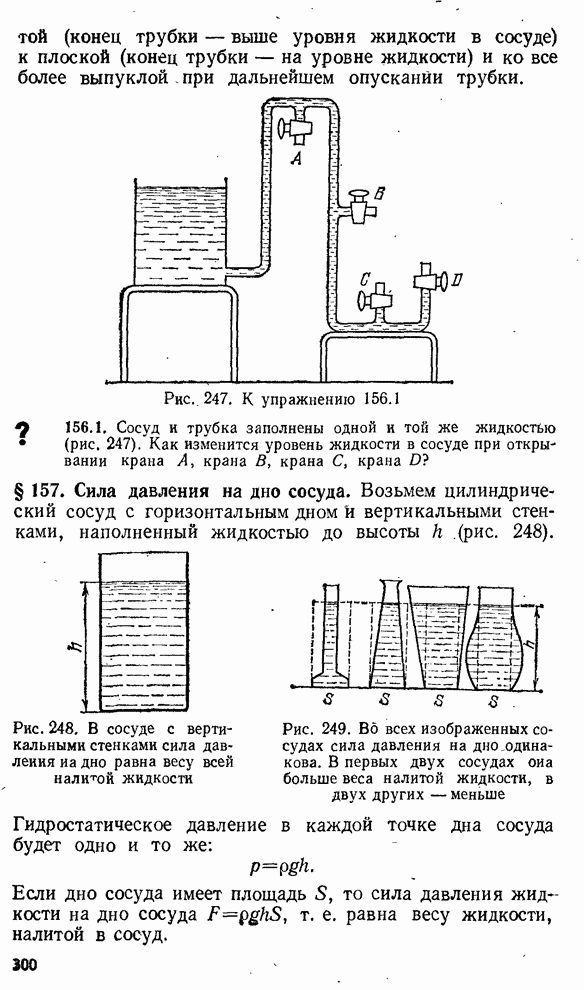
- § 157. Сила давления на дно сосуда
- § 158. Давление воды в морских глубинах
- § 159. Прочность подводной лодки
- § 160. Закон Архимеда
- § 161. Измерение плотности тел на основании закона Архимеда
- § 162. Плавание тел
- § 163. Плавание несплошных тел
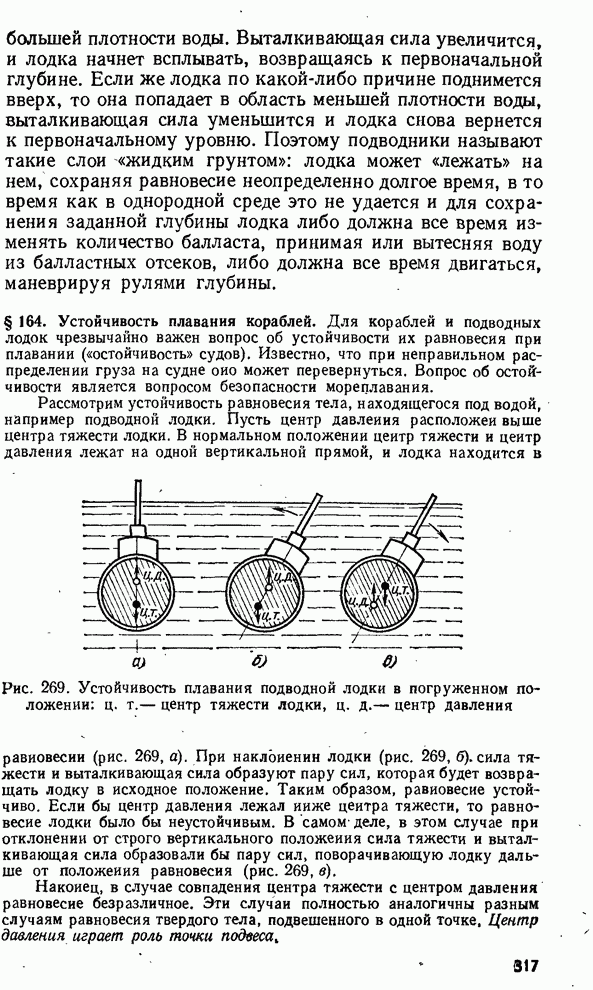
- § 164. Устойчивость плавания кораблей
- § 165. Всплывание пузырьков
- § 166. Тела, лежащие на дне сосуда
- Глава VIII. Аэростатика
- § 167. Механические свойства газов
- § 168. Атмосфера
- § 169. Давление атмосферы
- § 170. Другие опыты, показывающие существование атмосферного давления
- § 171. Разрежающие насосы
- § 172. Влияние атмосферного давления на уровень жидкости в трубке
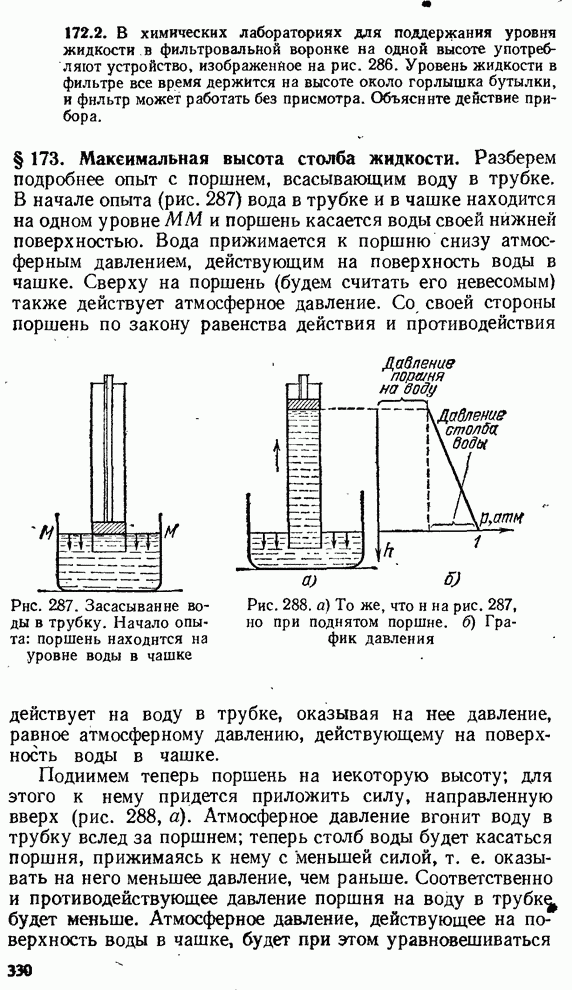
- § 173. Максимальная высота столба жидкости
- § 174. Опыт Торричелли. Ртутный барометр и барометр-анероид
- § 175. Распределение атмосферного давления по высоте
- § 176. Физиологическое действие пониженного давления воздуха
- § 177. Закон Архимеда для газов
- § 178. Воздушные шары и дирижабли
- § 179. Применение сжатого воздуха в технике
- Глава IX. Гидродинамика и аэродинамика
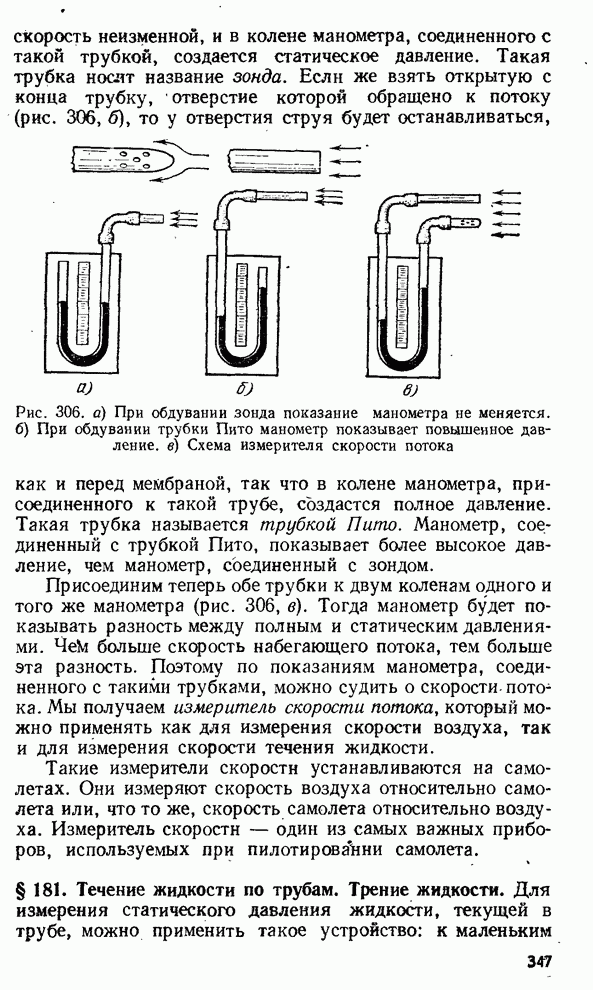
- § 180. Давление в движущейся жидкости
- § 181. Течение жидкости по трубам
- § 182. Закон Бернулли
- § 183. Жидкость в неинерциальных системах отсчета
- § 184. Реакция движущейся жидкости и ее использование
- § 185. Перемещение на воде
- § 186. Ракеты
- § 187. Реактивные двигатели
- § 188. Баллистические ракеты
- § 189. Взлет ракеты с Земли
- § 190. Сопротивление воздуха
- § 191. Эффект Магиуса и циркуляция
- § 192. Подъемная сила крыла и полет самолета
- § 193. Турбулентность в потоке жидкости или газа
- § 194. Ламинарное течение
- РАЗДЕЛ ВТОРОЙ. ТЕПЛОТА. МОЛЕКУЛЯРНАЯ ФИЗИКА
- Глава X. Тепловое расширение твердых и жидких тел
- § 195. Тепловое расширение твердых и жидких тел
- § 196. Термометры
- § 197. Формула линейного расширения
- § 198. Формула объемного расширения
- § 199. Связь между коэффициентами линейного и объемного расширения
- § 200. Измерение коэффициента объемного расширения жидкостей
- § 201. Особенности расширения воды
- Глава XI. Работа. Теплота. Закон сохранения энергии
- § 202. Изменения состояния тел
- § 203. Нагревание тел при совершении работы
- § 204. Изменение внутренней энергии тел при теплопередаче
- § 205. Единицы количества теплоты
- § 206. Зависимость внутренней энергии тела от его массы и вещества
- § 207. Теплоемкость тела
- § 208. Удельная теплоемкость
- § 209. Калориметр. Измерение теплоемкостей
- § 210. Закон сохранения энергии
- § 211. Невозможность «вечного двигателя»
- § 212. Различные виды процессов, при которых происходит передача теплоты
- Глава XII. Молекулярная теория
- § 213. Молекулы и атомы
- § 214. Размеры атомов и молекул
- § 215. Микромир
- § 216. Внутренняя энергия с точки зрения молекулярной теории
- § 217. Молекулярное движение
- § 218. Молекулярное движение в газах, жидкостях и твердых телах
- § 219. Броуновское движение
- § 220. Молекулярные силы
- Глава XIII. Свойства газов
- § 221. Давление газа
- § 222. Зависимость давления газа от температуры
- § 223. Формула, выражающая закон Шарля
- § 224. Закон Шарля с точки зрения молекулярной теории
- § 225. Изменение температуры газа при изменении его объема. Адиабатические и изотермические процессы
- § 226. Закон Бойля — Мариотта
- § 227. Формула, выражающая закон Бойля — Мариотта
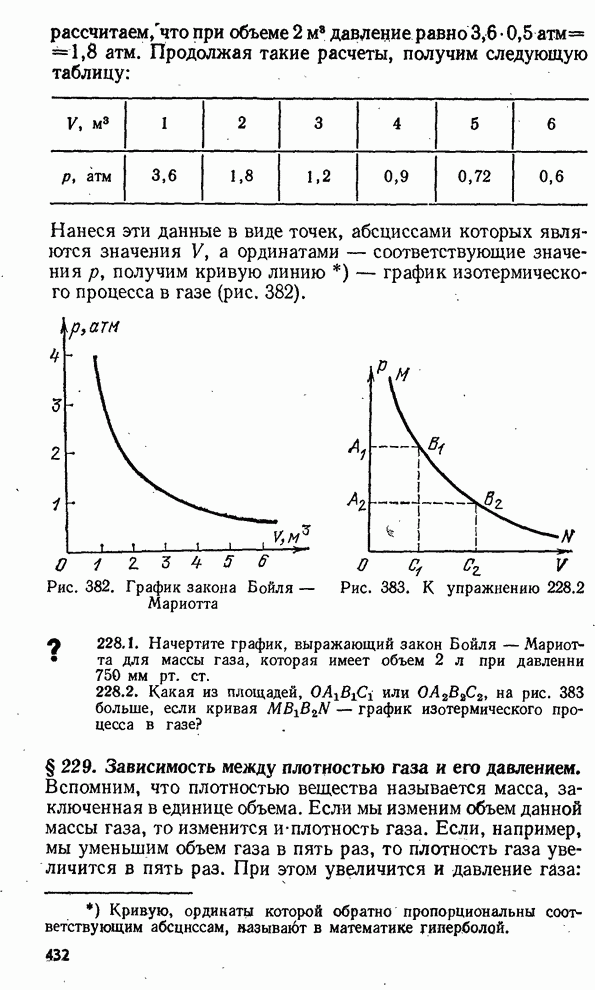
- § 228. График, выражающий закон Бойля — Мариотта
- § 229. Зависимость между плотностью газа и его давлением
- § 230. Молекулярное толкование закона Бойля — Мариотта
- § 231. Изменение объема газа при изменении температуры
- § 232. Закон Гей-Люссака
- § 233. Графики, выражающие законы Шарля и Гей-Люссака
- § 234. Термодинамическая температура
- § 235. Газовый термометр
- § 236. Объем газа и термодинамическая температура
- § 237. Зависимость плотности газа от температуры
- § 238. Уравнение состояния газа
- § 239. Закон Дальтона
- § 240. Плотность газов
- § 241. Закон Авогадро
- § 242. Моль. Постоянная Авогадро
- § 243. Скорости молекул газа
- § 244. Об одном из способов измерения скоростей движения молекул газа (опыт Штерна)
- § 245. Удельные теплоемкости газов
- § 246. Молярные теплоемкости
- § 247. Закон Дюлонга и Пти
- Глава XIV. Свойства жидкостей
- § 248. Строение жидкостей
- § 249. Поверхностная энергия
- § 250. Поверхностное натяжение
- § 251. Жидкостные пленки
- § 252. Зависимость поверхностного натяжения от температуры
- § 253. Смачивание и несмачивание
- § 254. Расположение молекул у поверхности тел
- § 255. Значение кривизны свободной поверхности жидкости
- § 256. Капиллярные явления
- § 257. Высота поднятия жидкости в капиллярных трубках
- § 258. Адсорбция
- § 259. Флотация
- § 260. Растворение газов
- § 261. Взаимное растворение жидкостей
- § 262. Растворение твердых тел в жидкостях
- Глава XV. Свойства твердых тел. Переход тел из твердого состояния в жидкое
- § 263. Введение
- § 264. Кристаллические тела
- § 265. Аморфные тела
- § 266. Кристаллическая решетка
- § 267. Кристаллизация
- § 268. Плавление и отвердевание
- § 269. Удельная теплота плавления
- § 270. Переохлаждение
- § 271. Изменение плотности веществ при плавлении
- § 272. Полимеры
- § 273. Сплавы
- § 274. Затвердевание растворов
- § 275. Охлаждающие смеси
- § 276. Изменения свойств твердого тела
- Глава XVI. Упругость и прочность
- § 277. Введение
- § 278. Упругие и пластические деформации
- § 279. Закон Гука
- § 280. Растяжение и сжатие
- § 281. Сдвиг
- § 282. Кручение
- § 283. Изгиб
- § 284. Прочность
- § 285. Твердость
- § 286. Что происходит при деформации тел
- § 287. Изменение энергии при деформации тел
- Глава XVII. Свойства паров
- § 288. Введение
- § 289. Пар насыщенный и ненасыщенный
- § 290. Что происходит при изменении объема жидкости и насыщенного пара
- § 291. Закон Дальтона для пара
- § 292. Молекулярная картина испарения
- § 293. Зависимость давления насыщенного пара от температуры
- § 294. Кипение
- § 295. Удельная теплота парообразования
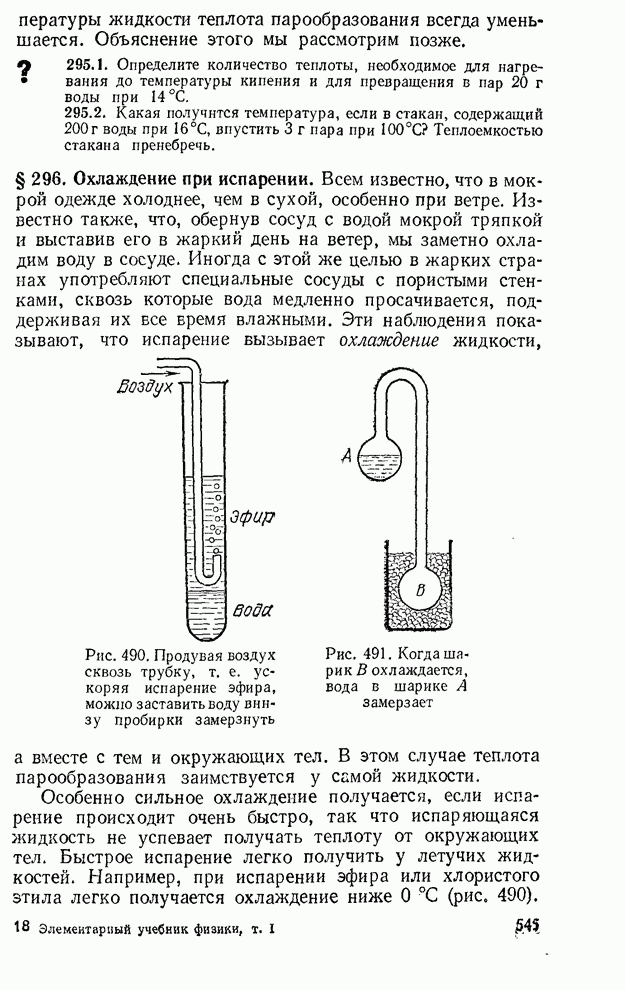
- § 296. Охлаждение при испарении
- § 297. Изменение внутренней энергии при переходе вещества из жидкого состояния в парообразное
- § 298. Испарение при кривых поверхностях жидкости
- § 299. Перегревание жидкости
- § 300. Пересыщение паров
- § 301. Насыщение пара при возгонке
- § 302. Превращение газа в жидкость
- § 303. Критическая температура
- § 304. Сжижение газов в технике
- § 305. Вакуумная техника
- § 306. Водяной пар в атмосфере
- Глава XVIII. Физика атмосферы
- § 307. Атмосфера
- § 308. Тепловой баланс Земли
- § 309. Адиабатические процессы в атмосфере
- § 310. Облака
- § 311. Искусственные осадки
- § 312. Ветер
- § 313. Предсказание погоды
- Глава XIX. Тепловые машины
- § 314. Условия, необходимые для работы тепловых двигателей
- § 315. Паросиловая станция
- § 316. Паровой котел
- § 317. Паровая турбина
- § 318. Поршневая паровая машина
- § 319. Конденсатор
- § 320. Коэффициент полезного действия теплового двигателя
- § 321. Коэффициент полезного действия паросиловой станции
- § 322. Бензиновый двигатель внутреннего сгорания
- § 323. Коэффициент полезного действия двигателя внутреннего сгорания
- § 324. Двигатель Дизеля
- § 325. Реактивные двигатели
- § 326. Передача теплоты от холодного тела к горячему
- Ответы и решения к упражнениям
- Предметный указатель