| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 13. ЗАВИСИМОСТЬ АГРЕГАТНОГО СОСТОЯНИЯ ВЕЩЕСТВА ОТ ТЕМПЕРАТУРЫ И ДАВЛЕНИЯ
Диаграмма состояний вещества. Чем выше температура жидкости, тем больше плотность и давление ее насыщенного пара. Геометрическим местом точек, отмечающих на диаграмме  равновесное состояние между жидким и газообразным агрегатными состояниями вещества, является кривая А К зависимости температуры кипения жидкости от давления (рис. 11). Точкам, лежащим выше кривой АК, но вправо от кривой АВ, соответствуют такие сочетания температуры и давления, при которых вещество находится в жидком состоянии. Точкам, лежащим ниже кривой парообразования САК, соответствуют такие сочетания давления и температуры, при которых вещество находится в газообразном состоянии.
равновесное состояние между жидким и газообразным агрегатными состояниями вещества, является кривая А К зависимости температуры кипения жидкости от давления (рис. 11). Точкам, лежащим выше кривой АК, но вправо от кривой АВ, соответствуют такие сочетания температуры и давления, при которых вещество находится в жидком состоянии. Точкам, лежащим ниже кривой парообразования САК, соответствуют такие сочетания давления и температуры, при которых вещество находится в газообразном состоянии.
Геометрическим местом точек, отмечающих равновесные состояния между твердым и жидким состояниями вещества, является кривая плавления АВ. При давлениях и температурах, соответствующих точкам этой кривой, твердое тело и расплав, приведенные в соприкосновение, находятся в динамическом равновесии. Число молекул, переходящих в единицу времени из жидкости в твердое тело, равно числу молекул, переходящих границу раздела между ними в противоположном направлении.
Кривая плавления идет почти вертикально, поскольку температура плавления слабо зависит от давления. На рисунке 11 она немного отклонена впраио.
Этим иллюстрируется повышение температуры плавления с увеличением давления, наблюдаемое у большинства веществ.
Для веществ, обладающих в твердом состоянии меньшей плотностью, чем в жидком состоянии (лед, висмут, серый чугун), увеличение давления способствует плавлению. Для таких геществ кривая плавления отклонена влево от вертикали.

Рис. 11. Диаграмма состояний вещества
Кривая СА на диаграмме состояний вещества отмечает сочетания значений давления и температуры, при которых устанавливается равновесие между процессами испарения молекул (атомов) твердого тела и конденсации их на поверхность твердого тела. Процесс испарения твердых тел называется сублимацией.
Конечно, сублимации сопутствует и обратный процесс — кристаллизация из пара. При определенных сочетаниях температуры к давления система кристалл — пар будет находиться в динамическом равновесии. С уменьшением температуры кристалла уменьшается и давление его насыщенного пара. Это отражено в ходе кривой сублимации СА.
Тройная точка. Кривые плавления и парообразования пересекаются в точке А. Эта точка называется тройной точкой, так как если при давлении  и температуре
и температуре  некоторые количества одного вещества в твердом, жидком и газообразном состояниях находятся в контакте, то без подведения или отвода тепла количество вещества, находящегося в каждом из трех состояний, остается неизменным.
некоторые количества одного вещества в твердом, жидком и газообразном состояниях находятся в контакте, то без подведения или отвода тепла количество вещества, находящегося в каждом из трех состояний, остается неизменным.
Рассмотрение диаграммы состояний вещества позволяет сделать вывод, что переход вещества при нагревании из твердого состояния в жидкое, наблюдаемый в большинстве обычных опытов, не является обязательным правилом. Он лишь свидетельствует о том, что у многих веществ давление  ниже нормального атмосферного давления
ниже нормального атмосферного давления  . Те же вещества, у которых давление
. Те же вещества, у которых давление  превышает
превышает  в результате нагревания при давлении
в результате нагревания при давлении  не плавятся, а переходят в газообразное состояние.
не плавятся, а переходят в газообразное состояние.
Например, при давлении  твердая углекислота при нагревании не плавится, а сублимирует. Это объясняется тем, что тройной точке соединения
твердая углекислота при нагревании не плавится, а сублимирует. Это объясняется тем, что тройной точке соединения  соответствует давление примерно в 5 раз выше
соответствует давление примерно в 5 раз выше 
Полиморфизм. Разнообразие возможных состояний вещества не исчерпывается тремя видами: твердым, жидким, газообразным. Практически все вещества в твердом состоянии могут существовать в двух или более кристаллических разновидностях (модификациях), отличающихся физическими свойствами. Это явление называется полиморфизмом. Известны четыре модификации железа, девять модификаций серы и т. д. Каждая модификация устойчива в определенном интервале температур и давлений. Из девяти кристаллических разновидностей воды только одна устойчива при атмосферном давлении. Остальные восемь модификаций льда существуют при высоких давлениях и имеют плотность большую, чем у воды. Одна из них при давлении  имеет температуру плавления +80 °С, т. е. существует горячий лед.
имеет температуру плавления +80 °С, т. е. существует горячий лед.
Упорядоченное расположение атомов или молекул в кристалле определяется действием сил межатомного и межмолекулярного взаимодействия. Тепловое движение атомов и молекул нарушает эту упорядоченную структуру. При изменениях температуры и давления изменяются средние расстояния между атомами и
молекулами. Это приводит к изменению величины сил взаимодействия между ними. С повышением температуры увеличивается размах тепловых колебаний атомов и молекул и им требуется больший объем, в котором они могли бы двигаться. При каждом сочетании давления и температуры реализуется тот тип укладки частиц, который в данных условиях наиболее устойчив.
Превращения кристаллов одного и того же вещества с различным типом решетки друг в друга происходят по законам, аналогичным законам плавления и испарения. Каждому давлению соответствует определенная температура, при которой оба типа кристаллов существуют, не превращаясь друг в друга, так как полиморфные переходы сопровождаются выделением или поглощением тепла.
На диаграмме состояний области, соответствующие различным кристаллическим модификациям, разграничиваются кривыми, представляющими собой геометрические места точек, отвечающих таким значениям давлений и температур, при которых две кристаллические модификации находятся в динамическом равновесии между собой (рис. 12).
Знание законов полиморфных превращений имеет важное значение в практике.
У многих кристаллов неустойчивая в данных условиях модификация может существовать длительное время, поскольку атомы твердого тела обладают ничтожно малой подвижностью. Например, алмаз при комнатной температуре и нормальном атмосферном давлении не превращается самопроизвольно в более устойчивую при этих условиях модификацию — графит. Поэтому алмазы, полученные при высоких температурах и давлениях, можно использовать в обычных условиях.
Разработка способа получения искусственных алмазов из графита имеет большую практическую ценность. Превращение графита в алмаз происходит при температуре 2000 °С и давлении  Па в течение нескольких часов. Эта труднейшая научно-техническая задача в нашей стране была решена в 1962 г. в Институте физики высоких давлений под руководством академика Л. Ф. Верещагина.
Па в течение нескольких часов. Эта труднейшая научно-техническая задача в нашей стране была решена в 1962 г. в Институте физики высоких давлений под руководством академика Л. Ф. Верещагина.
Искусственные алмазы в настоящее время изготовляются в значительных количествах и широко применяются в промышленности.
Приведем еще один пример применения явления полиморфизма.

Рис. 12. Диаграмма состояний углерода
Железо может существовать в нескольких кристаллических модификациях. При температуре ниже 898 °С атомы железа образуют кубическую объемно-центрированную решетку (а-железо). В интервале температур 910-1400 °С более устойчивой оказывается гранецентрированная решетка (у-железо). Если сталь нагреть до температуры выше температуры полиморфного перехода  к
к  -модификации и затем быстро охладить, то перестройка кристаллической решетки из
-модификации и затем быстро охладить, то перестройка кристаллической решетки из  в
в  -модификацию не успеет произойти. Образец с
-модификацию не успеет произойти. Образец с  -структурой при комнатной температуре обладает повышенной твердостью и прочностью. Это полиморфное превращение наряду с другими явлениями сопровождает процесс закалки стали и имеет большое значение в технике.
-структурой при комнатной температуре обладает повышенной твердостью и прочностью. Это полиморфное превращение наряду с другими явлениями сопровождает процесс закалки стали и имеет большое значение в технике.
| << Предыдущий параграф | Следующий параграф >> |
- МОЛЕКУЛЯРНАЯ ФИЗИКА
- § 2. ЧИСЛО АВОГАДРО
- § 3. ИДЕАЛЬНЫЙ ГАЗ
- § 4. ДАВЛЕНИЕ ИДЕАЛЬНОГО ГАЗА
- § 5. ГАЗОВЫЙ ТЕРМОМЕТР
- § 6. ТЕМПЕРАТУРА КАК МЕРА СРЕДНЕЙ КИНЕТИЧЕСКОЙ ЭНЕРГИИ МОЛЕКУЛ
- § 7. УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА
- § 8. РЕАЛЬНЫЕ ГАЗЫ
- § 9. СРЕДНЯЯ ДЛИНА СВОБОДНОГО ПРОБЕГА
- § 10. ДИФФУЗИЯ И БРОУНОВСКОЕ ДВИЖЕНИЕ
- § 11. СЖИЖЕНИЕ ГАЗОВ
- § 12. ОБЛАКА И ОСАДКИ
- § 13. ЗАВИСИМОСТЬ АГРЕГАТНОГО СОСТОЯНИЯ ВЕЩЕСТВА ОТ ТЕМПЕРАТУРЫ И ДАВЛЕНИЯ
- § 14. СТРОЕНИЕ КРИСТАЛЛОВ
- § 15. ПРОЦЕССЫ РОСТА КРИСТАЛЛОВ
- § 16. ПОЛУЧЕНИЕ МОНОКРИСТАЛЛОВ
- § 17. ПРИМЕНЕНИЯ КРИСТАЛЛИЧЕСКИХ ТЕЛ
- § 18. КРИСТАЛЛЫ И ЖИЗНЬ
- Глава 2. ТЕРМОДИНАМИКА
- § 19. ТЕРМОДИНАМИЧЕСКИЙ МЕТОД
- § 20. РАБОТА И КОЛИЧЕСТВО ТЕПЛОТЫ В ТЕРМОДИНАМИКЕ
- § 21. ТЕПЛОЕМКОСТЬ ГАЗОВ
- § 22. ТЕПЛОЕМКОСТЬ ТВЕРДЫХ ТЕЛ И ЖИДКОСТЕЙ
- § 23. ПОТРЕБЛЕНИЕ ЭНЕРГИИ
- § 24. ТЕПЛОВЫЕ ДВИГАТЕЛИ
- § 25. РАБОЧИЙ ЦИКЛ ТЕПЛОВОГО ДВИГАТЕЛЯ
- § 26. КПД ТЕПЛОВОГО ДВИГАТЕЛЯ
- § 27. ПАРОВАЯ МАШИНА
- § 28. ДВИГАТЕЛЬ ВНУТРЕННЕГО СГОРАНИЯ
- § 29. ПАРОВАЯ И ГАЗОВАЯ ТУРБИНЫ
- § 30. РЕАКТИВНЫЕ ДВИГАТЕЛИ
- § 31. ПРАКТИКУМ ПО РЕШЕНИЮ ЗАДАЧ
- ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
- ТЕРМОДИНАМИКА
- § 32. ЛАБОРАТОРНЫЕ И ПРАКТИЧЕСКИЕ ЗАДАНИЯ
- ЭЛЕКТРОДИНАМИКА
- Глава 3. ЭЛЕКТРИЧЕСКОЕ ПОЛЕ И ЭЛЕКТРИЧЕСКИЙ ТОК
- § 34. ПОТЕНЦИАЛ
- § 35. ДИЭЛЕКТРИКИ И ПРОВОДНИКИ В ЭЛЕКТРИЧЕСКОМ ПОЛЕ
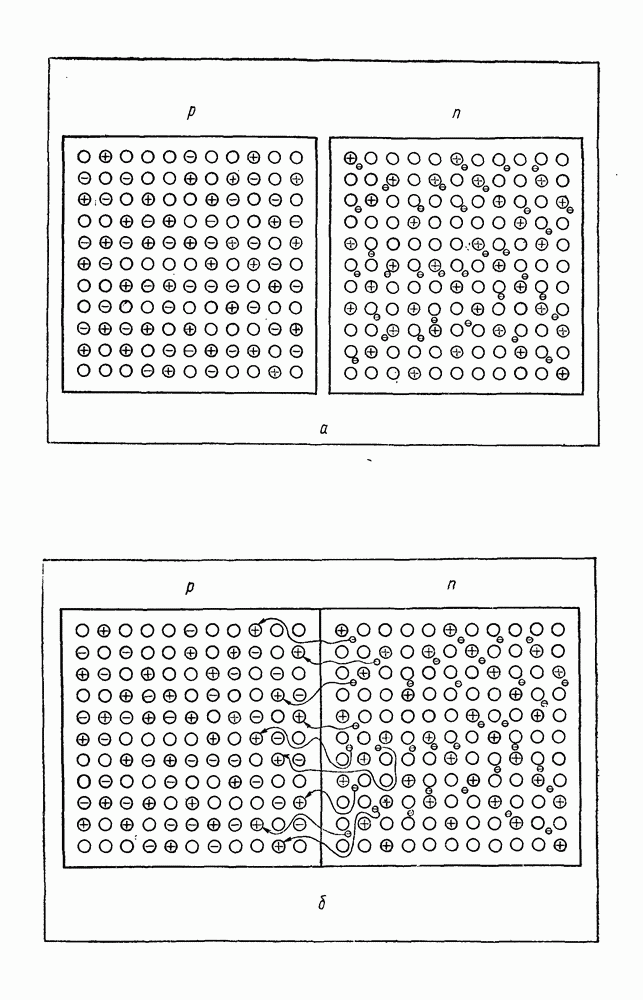
- § 36. СВОЙСТВА p-n-ПЕРЕХОДА
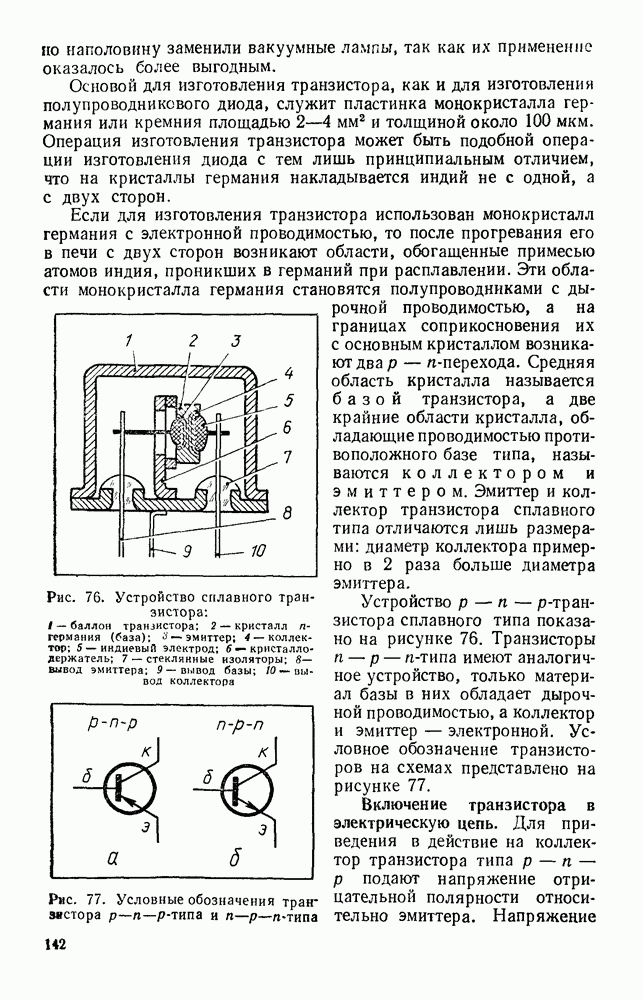
- § 37. ТРАНЗИСТОР
- Глава 4. МАГНЕТИЗМ
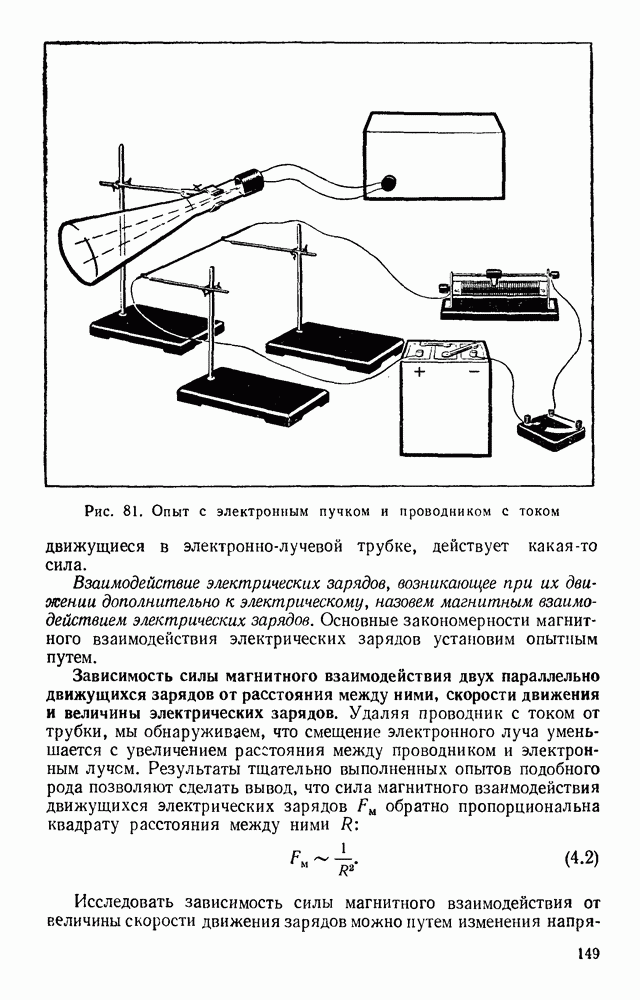
- § 38. МАГНИТНОЕ ВЗАИМОДЕЙСТВИЕ ДВИЖУЩИХСЯ ЭЛЕКТРИЧЕСКИХ ЗАРЯДОВ
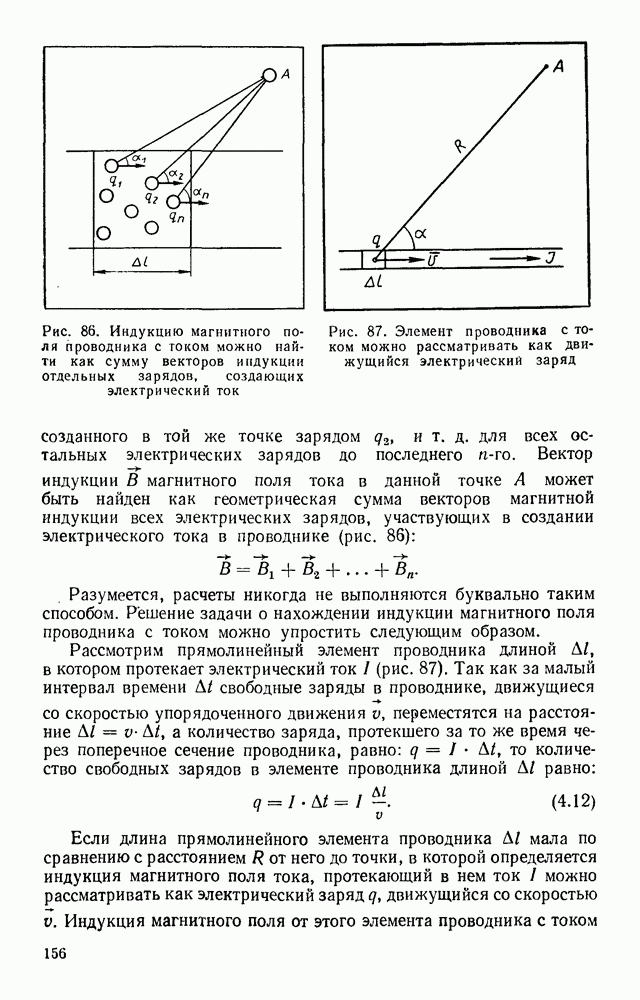
- § 39. МАГНИТНОЕ ПОЛЕ
- § 40. МАГНИТНОЕ ПОЛЕ ДВИЖУЩЕГОСЯ ЭЛЕКТРИЧЕСКОГО ЗАРЯДА
- § 41. МАГНИТНОЕ ПОЛЕ ТОКА В ВАКУУМЕ
- § 42. ДЕЙСТВИЕ МАГНИТНОГО ПОЛЯ НА ДВИЖУЩИЕСЯ ЭЛЕКТРИЧЕСКИЕ ЗАРЯДЫ
- § 43. МАГНИТНАЯ ПОСТОЯННАЯ ВАКУУМА
- § 44. ЭЛЕКТРИЧЕСКИЕ ГЕНЕРАТОРЫ
- § 45. ЭЛЕКТРОМАГНИТНОЕ ПОЛЕ
- § 46. ПРАКТИКУМ ПО РЕШЕНИЮ ЗАДАЧ
- ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
- § 47. ЛАБОРАТОРНЫЕ И ПРАКТИЧЕСКИЕ ЗАДАНИЯ
- Глава 5. ФИЗИЧЕСНИЙ ПРАКТИКУМ
- ЛАБОРАТОРНАЯ РАБОТА № 2. ОПРЕДЕЛЕНИЕ МОЛЯРНОЙ МАССЫ ГАЗА
- ЛАБОРАТОРНАЯ РАБОТА № 3. ОПРЕДЕЛЕНИЕ СКОРОСТИ РОСТА КРИСТАЛЛОВ
- ЛАБОРАТОРНАЯ РАБОТА № 4. ОПРЕДЕЛЕНИЕ ТВЕРДОСТИ СТАЛИ ДО И ПОСЛЕ ЗАКАЛКИ
- ЛАБОРАТОРНАЯ РАБОТА № 6. ОПРЕДЕЛЕНИЕ ХАРАКТЕРИСТИК ХОЛОДИЛЬНИКА
- ЛАБОРАТОРНАЯ РАБОТА № 6. ПОВЕРКА ЭЛЕКТРОИЗМЕРИТЕЛЬНЫХ ПРИБОРОВ
- ЛАБОРАТОРНАЯ РАБОТА № 7. ИЗУЧЕНИЕ ЭЛЕКТРОННОГО ОСЦИЛЛОГРАФА
- ЛАБОРАТОРНАЯ РАБОТА № 8. РАСЧЕТ И ИСПЫТАНИЕ СХЕМЫ АВТОМАТИЧЕСКОГО УПРАВЛЕНИЯ С ФОТОРЕЗИСТОРОМ
- ЛАБОРАТОРНАЯ РАБОТА № 9. ОПРЕДЕЛЕНИЕ КОЭФФИЦИЕНТА УСИЛЕНИЯ ТРАНЗИСТОРА ПО ТОКУ В СХЕМЕ С ОБЩИМ ЭМИТТЕРОМ
- ЛАБОРАТОРНАЯ РАБОТА № 10. ИЗМЕРЕНИЕ МАГНИТНОГО ПОТОКА ПОСТОЯННОГО МАГНИТА
- ЛАБОРАТОРНАЯ РАБОТА № 11. ОПРЕДЕЛЕНИЕ ИНДУКЦИИ МАГНИТНОГО ПОЛЯ ЗЕМЛИ
- ОТВЕТЫ К ЗАДАЧАМ