| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
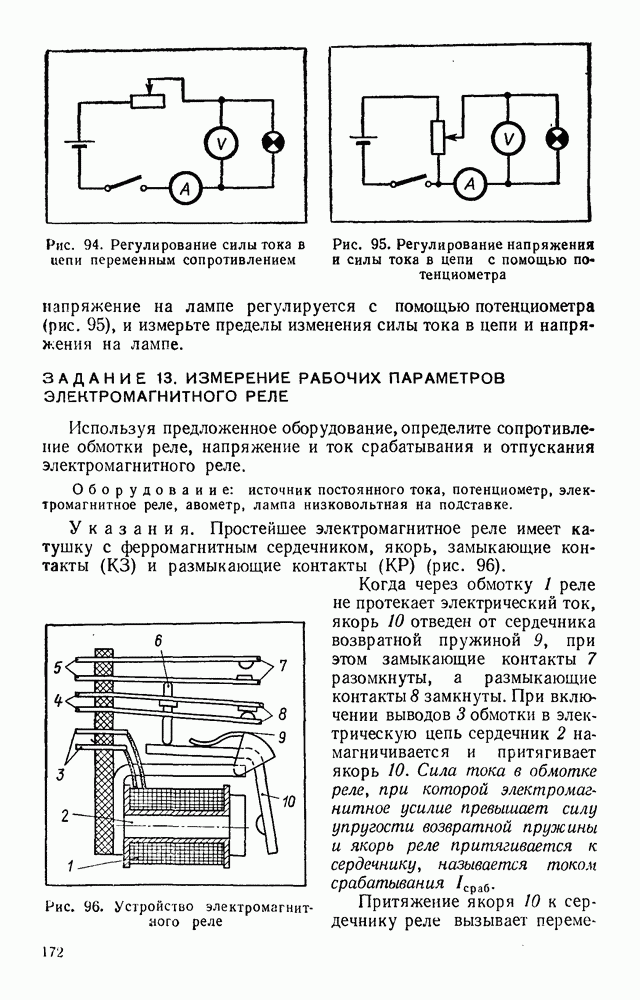
§ 32. ЛАБОРАТОРНЫЕ И ПРАКТИЧЕСКИЕ ЗАДАНИЯ
ЗАДАНИЕ 1. НАБЛЮДЕНИЕ СЦИНТИЛЛЯЦИЙ С ПОМОЩЬЮ СПИНТАРИСКОПА
Оборудование: школьный спинтарископ.
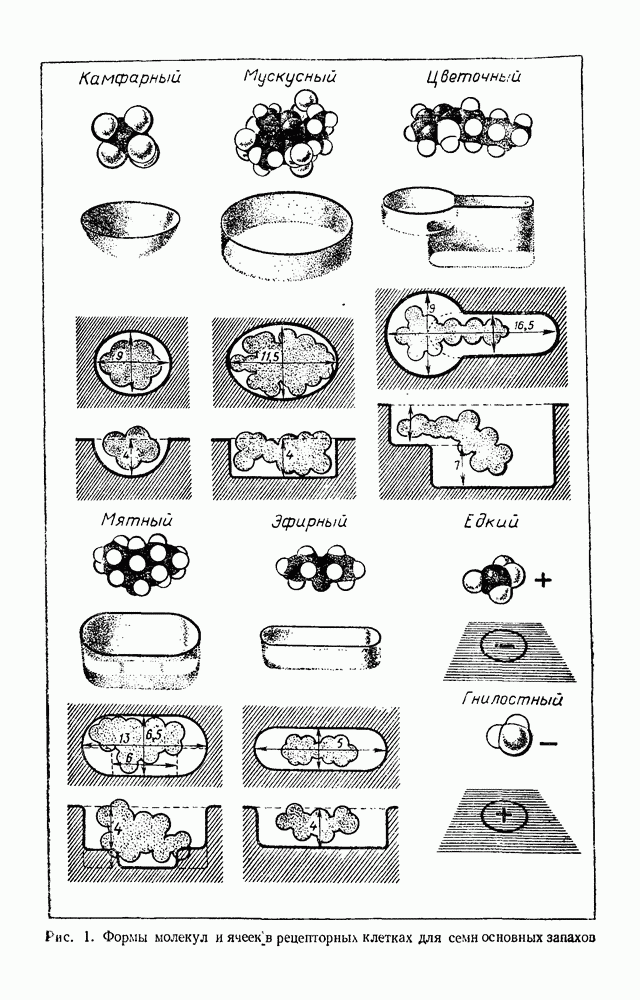
Содержание и метод выполнения задания Одним из самых простых способов регистрации отдельных атомов является сцинтилляционный способ. Сцинтилляцией называется световая вспышка, возникающая в некоторых кристаллах при попадании в них быстро движущихся атомов или других частиц.
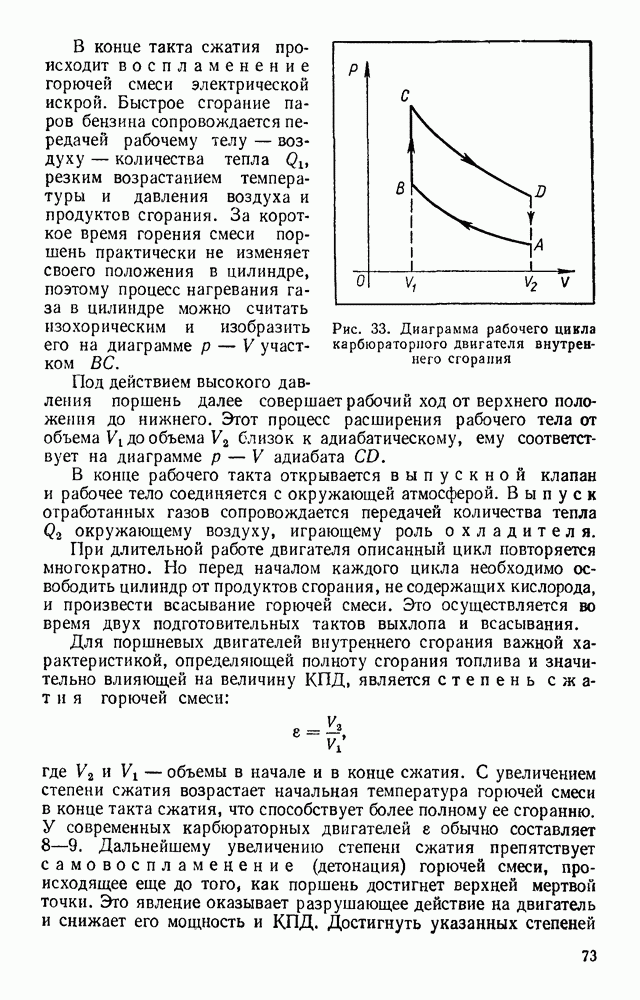
На рисунке 55 представлена схема устройства спинтарископа — прибора, предназначенного для наблюдения свечения экрана,

Рис. 55. Устройство спинтарископа
вызываемого отдельными  -частицами. На острие иглы 3 помещают источник
-частицами. На острие иглы 3 помещают источник  -частиц. Таким источником служит очень небольшое количество радиоактивного элемента плутония или радия. Иглу с радиоактивным препаратом помещают внутрь трубки 2 и укрепляют над экраном 4, покрытым сернистым цинком. На другой конец трубки навинчивают лупу 1.
-частиц. Таким источником служит очень небольшое количество радиоактивного элемента плутония или радия. Иглу с радиоактивным препаратом помещают внутрь трубки 2 и укрепляют над экраном 4, покрытым сернистым цинком. На другой конец трубки навинчивают лупу 1.
Человеческий глаз обладает очень большой чувствительностью к свету. Особенно замечательно свойство глаза приспосабливаться к различным интенсивностям света, в том числе и к очень слабым. После пребывания в темноте в течение 10—15 мин человек способен увидеть вспышку света, вызываемую отдельной  -частицей, т. е. обнаружить явление столкновения атома гелия с экраном.
-частицей, т. е. обнаружить явление столкновения атома гелия с экраном.
Порядок выполнения работы
1. Ознакомьтесь с устройством спинтарископа.
2. После 10-15-минутной выдержки в затемненном помещении пронаблюдайте сцинтилляции, вызываемые  -частицами.
-частицами.
ЗАДАНИЕ 2. ИЗМЕРЕНИЕ ВАКУУМА, СОЗДАВАЕМОГО НАСОСОМ
Измерьте давление воздуха в полом стеклянном шаре после откачивания из него воздуха с помощью насоса.
Оборудование: насос вакуумный ручной или вакуумный насос Комовского, шар полый стеклянный для взвешивания воздуха, сосуд с водой, цилиндр измерительный, зажим.
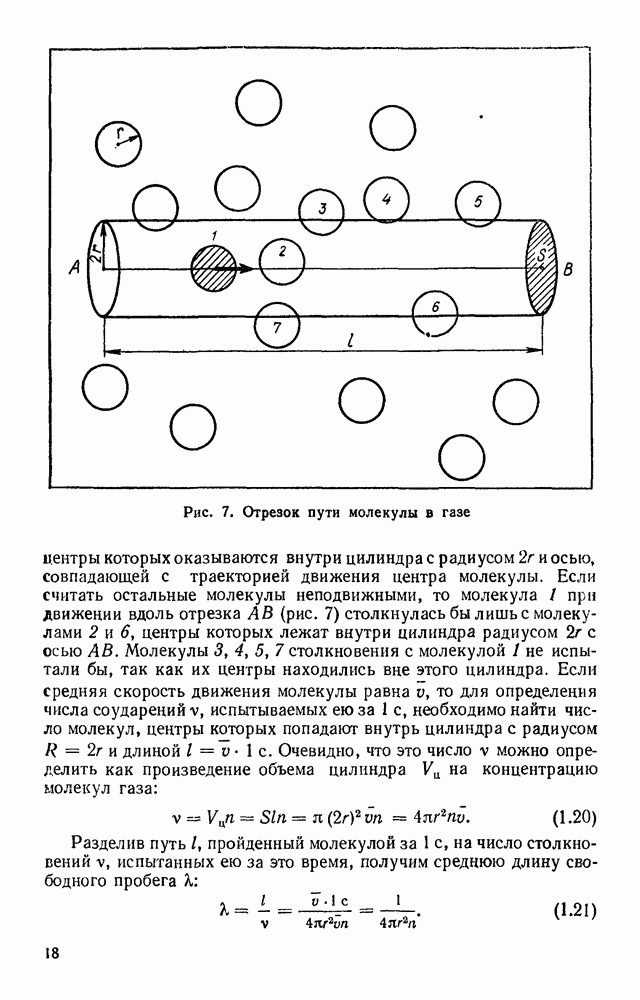
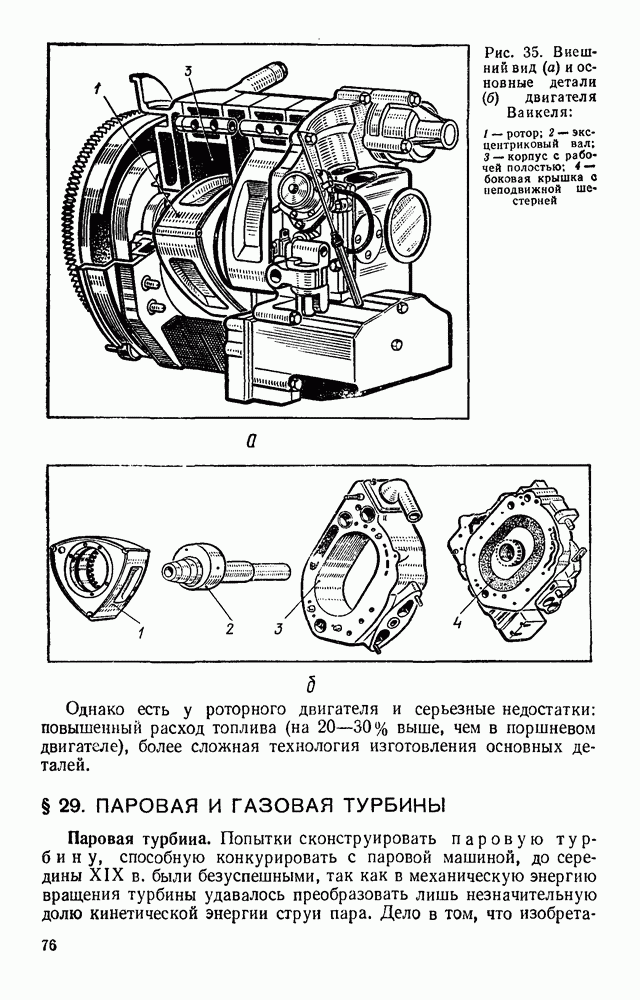
Указания. Ручной вакуумный насос двойного действия может служить для разрежения и нагнетания воздуха. Основными его деталями являются стальной цилиндр 1, поршень 3 из двух кожаных манжет, привернутых гайкой к штоку 2 с ручкой, и два клапана 4 из тонких резиновых трубок с прорезями (рис. 56).
Если в результате перемещения поршня давление воздуха в насосе становится меньше давления воздуха в сосуде, с которым соединен впускной клапан 4, то воздух из сосуда входит в насос через отверстие в резиновой трубке клапана до выравнивания давлений. При перемещении поршня в обратном направлении давление воздуха в насосе повышается, резиновая трубка впускного клапана

Рис. 56. Ручной вакуумный насос двойного действия
сжимается и поступление воздуха в сосуд через впускной клапан прекращается. Если при дальнейшем перемещении поршня давление воздуха в насосе превысит атмосферное давление, откроется аналогично устроенный выпускной клапан 4 и воздух выйдет через него в атмосферу.
Соединив с помощью резинового шланга ручной насос с полым стеклянным шаром, откачайте из него воздух. Перекрыв зажимом резиновый шланг, отсоедините насос.
Давление  воздуха, оставшегося в шаре после откачивания и занимающего весь объем шара
воздуха, оставшегося в шаре после откачивания и занимающего весь объем шара  можно определить, если
можно определить, если

Рис. 57. Заполнение шара водой
осуществить его изотермическое сжатие до атмосферного давления  Так как
Так как

при постоянных значениях  и Е (т. е. при постоянной температуре Т) выполняется соотношение:
и Е (т. е. при постоянной температуре Т) выполняется соотношение:

Измерив объем  занимаемый разреженным воздухом в шаре, и объем
занимаемый разреженным воздухом в шаре, и объем  занимаемый им при атмосферном давлении
занимаемый им при атмосферном давлении  можно определить давление
можно определить давление  разреженного воздуха в шаре:
разреженного воздуха в шаре:

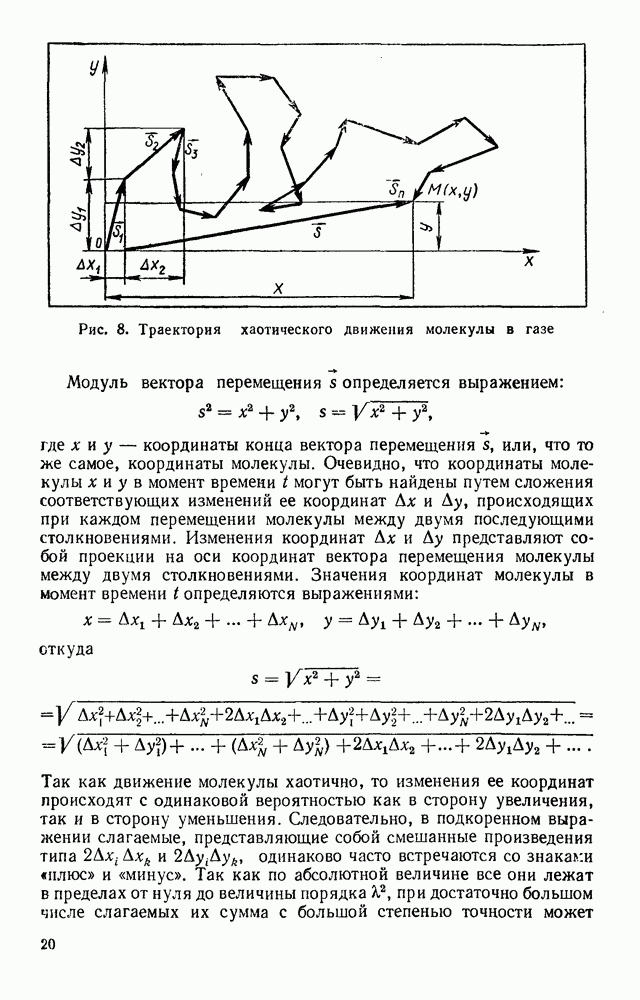
Атмосферное давление  определяется с помощью барометра, объем разреженного воздуха в шаре равен объему шара, а объем
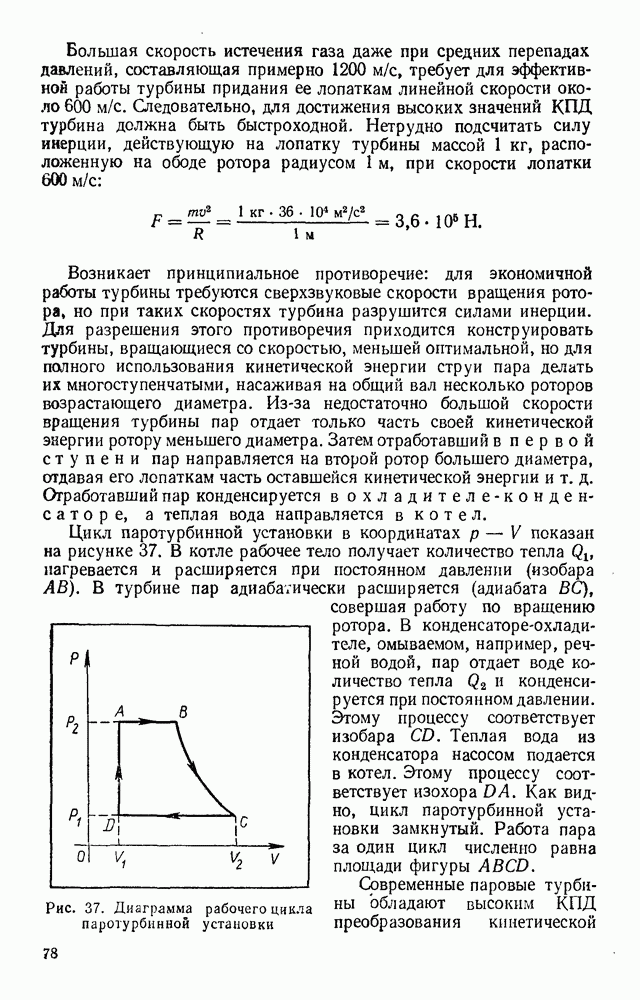
определяется с помощью барометра, объем разреженного воздуха в шаре равен объему шара, а объем  той же массы воздуха при атмосферном давлении можно найти следующим образом. Опустив шланг в сосуд с водой, откройте зажим. Так как давление воздуха в шаре ниже атмосферного, вода будет засасываться в шар до тех пор, пока давление воздуха в нем не станет равным атмосферному (рис. 57). Объем воздуха
той же массы воздуха при атмосферном давлении можно найти следующим образом. Опустив шланг в сосуд с водой, откройте зажим. Так как давление воздуха в шаре ниже атмосферного, вода будет засасываться в шар до тех пор, пока давление воздуха в нем не станет равным атмосферному (рис. 57). Объем воздуха  при атмосферном давлении можно найти как разность между объемом шара и объемом
при атмосферном давлении можно найти как разность между объемом шара и объемом  вошедшей в шар воды:
вошедшей в шар воды:

Для определения объема воды  ее следует вылить из шара в измерительный цилиндр.
ее следует вылить из шара в измерительный цилиндр.
Указание по технике безопасности: при откачивании воздуха шар должен находиться в защитном чехле.
ЗАДАНИЕ 3. ОПРЕДЕЛЕНИЕ АТМОСФЕРНОГО ДАВЛЕНИЯ
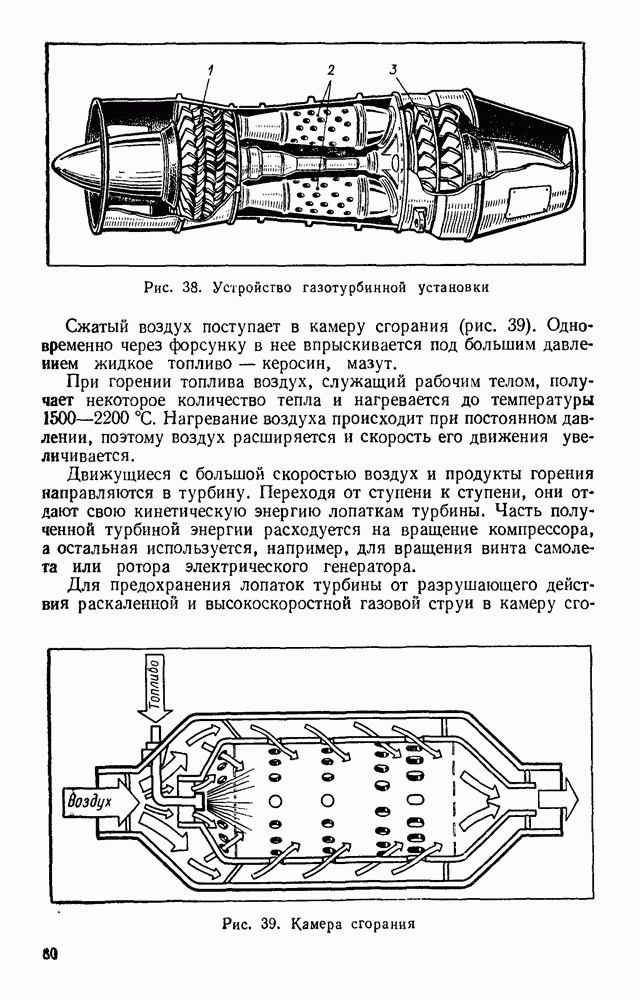
Используя предложенное оборудование, соберите установку по рисунку 58. Предложите метод определения атмосферного давления при помощи этой установки. Произведите необходимые измерения и определите атмосферное давление.
Оборудование: стеклянная трубка с пробкой, резиновый шланг, линейки, штативы, вода.
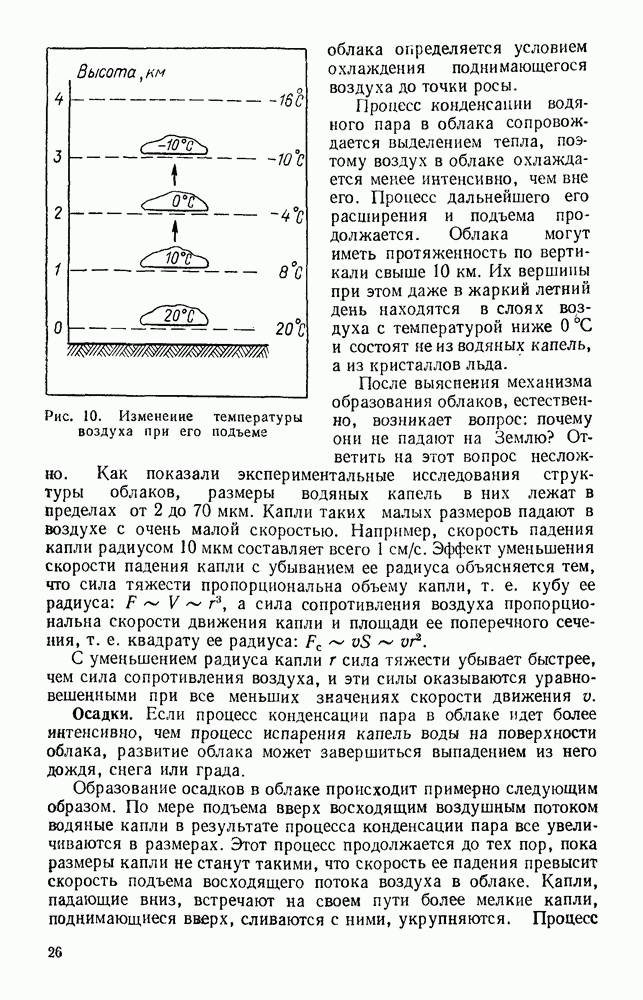
Указания. Для определения атмосферного давления можно осуществить изотермический процесс расширения определенной массы воздуха, заключенного в стеклянную трубку между поверхностью воды и резиновой пробкой.

Рис. 58. Установка для определения атмосферного давления воздуха
Атмосферное давление  можно определить, если в опыте будут измерены начальный объем воздуха У, изменения его давления
можно определить, если в опыте будут измерены начальный объем воздуха У, изменения его давления  и объема А К.
и объема А К.
Возможный вариант выполнения задания
Установив перемещением воронки с водой уровень воды в стеклянной трубке на расстоянии 10—15 см от ее верхнего конца, закроем пробкой отверстие в трубке. Воздух, заключенный в трубке, находится при атмосферном давлении  и занимает объем V.
и занимает объем V.
При опускании воронки на 1-1,5 м от первоначального положения давление воздуха в трубке уменьшается на величину  , где
, где  — разность уровней воды в трубке и воронке,
— разность уровней воды в трубке и воронке,  — плотность воды,
— плотность воды,  — ускорение свободного падения. Воздух, находящийся под пробкой, при понижении давления расширяется и занимает новый объем
— ускорение свободного падения. Воздух, находящийся под пробкой, при понижении давления расширяется и занимает новый объем 
Уравнение изотермы, составленной для двух состояний воздуха в трубке, позволяет определить атмосферное давление 

Так как  и
и  , где
, где  — площадь поперечного сечения стеклянной трубки, I — первоначальная длина столба воздуха,
— площадь поперечного сечения стеклянной трубки, I — первоначальная длина столба воздуха,  — изменение длины столба воздуха, то
— изменение длины столба воздуха, то

Следовательно, для определения атмосферного давления необходимо измерить первоначальную длину столба воздуха в трубке при одинаковой высоте уровня воды в трубке и воронке, длину  столба воздуха в трубке после опускания воронки и разность
столба воздуха в трубке после опускания воронки и разность  высот уровней воды в трубке и воронке во втором опыте.
высот уровней воды в трубке и воронке во втором опыте.
Определив давление атмосферного воздуха по результатам выполненных измерений, сравните полученное значение с показаниями барометра.
Контрольные вопросы
1. Исследуйте возможности повышения точности определения атмосферного давления данным методом.
2. Как устроены ртутный барометр и барометр-анероид?
ЗАДАНИЕ 4. НАБЛЮДЕНИЕ СЛЕДОВ a-ЧАСТИЦ В КАМЕРЕ ВИЛЬСОНА
Оборудование: камера для наблюдения следов  -частиц лабораторная, пробирка со смесью ацетона (25%), этилового спирта (60%) и воды (15%), пипетка.
-частиц лабораторная, пробирка со смесью ацетона (25%), этилового спирта (60%) и воды (15%), пипетка.
Содержание и метод выполнения задания
Образование капель жидкости в пересыщенном паре становится возможным при наличии так называемых центров конденсации. Центрами конденсации могут служить небольшие твердые частицы пыли, а также положительные и отрицательные ионы. Способность ионов служить центрами конденсации пересыщенного пара используется в камере Вильсона — приборе для регистрации быстрых заряженных частиц.
Школьная лабораторная камера Вильсона устроена следующим образом. На пластмассовое кольцо с двух сторон наклеены две прозрачные пластины из органического стекла (рис. 59). В кольцо вмонтирован штуцер, который через резиновый шланг соединен с резиновой грушей. В пластмассовое кольцо вмонтирован также металлический стержень, располагающийся по радиусу кольца. На конец этого стержня, находящийся в центре рабочего объема камеры, нанесен тонкий слой радиоактивного вещества, испускающего  -частицы.
-частицы.
 -Частицы, испускаемые радиоактивным веществом, представляют собой атомы гелия, лишенные электронной оболочки, т. е. являются двухзарядными положительными ионами. Вылетая из радиоактивного препарата со скоростью, близкой к скорости света,
-Частицы, испускаемые радиоактивным веществом, представляют собой атомы гелия, лишенные электронной оболочки, т. е. являются двухзарядными положительными ионами. Вылетая из радиоактивного препарата со скоростью, близкой к скорости света,  -частица сбивает электрон с оболочки практически каждого встретившегося на ее пути атома, в результате чего вдоль траектории движения
-частица сбивает электрон с оболочки практически каждого встретившегося на ее пути атома, в результате чего вдоль траектории движения  -частицы в газе образуется плотная колонка положительных и отрицательных ионов.
-частицы в газе образуется плотная колонка положительных и отрицательных ионов.
Если во время движения  -частицы в камере имеется пересыщенный пар, на ионах происходит конденсация
-частицы в камере имеется пересыщенный пар, на ионах происходит конденсация

Рис. 59. Камера Вильсона
капель жидкости и вдоль траектории движения частицы образуется полоска тумана — трек.
Для выполнения опытов камера предварительно с помощью резиновой груши наполняется насыщенными парами ацетона, спирта и воды. Переход паров в состояние пересыщения происходит в результате их охлаждения при быстром расширении.
Порядок выполнения задания
1. Откройте пробирку со смесью ацетона, этилового спирта и воды. Вставив в пробирку наконечник резиновой груши из комплекта лабораторной камеры Вильсона, произведите несколько сжатий и расширений, для того чтобы груша заполнилась насыщенными парами смеси.
2. Соедините резиновую грушу гибким шлангом с камерой Вильсона и произведите несколько легких сжатий и расширений груши для заполнения рабочего объема камеры насыщенными парами смеси.
3. Поместите камеру Вильсона на темную подставку. Если освещенность на месте проведения опыта мала, включите настольную лампу и осветите ею камеру сверху.
4. Для очищения рабочего объема камеры от ионов, возникших ранее, нужно наэлектризовать верхнюю плексигласовую крышку, натирая ее куском шерстяной ткани.
5. Для наблюдения следов  -частиц медленно сожмите грушу, а затем быстро отпустите ее. Если степень сжатия окажется удачной, на ионах, возникших вдоль траекторий движения
-частиц медленно сожмите грушу, а затем быстро отпустите ее. Если степень сжатия окажется удачной, на ионах, возникших вдоль траекторий движения  -частиц, произойдет конденсация пересыщенного пара, капельки тумана образуют трек — видимый след движения
-частиц, произойдет конденсация пересыщенного пара, капельки тумана образуют трек — видимый след движения  -частицы.
-частицы.
Если треки частиц в первом опыте не обнаружатся, повторяйте операции сжатия и разрежения несколько раз, изменяя степень сжатия.
Скорость расширения газа в камере, также оказывающую влияние на успешность результатов, можно регулировать, изменяя величину отверстия, через которое выходит воздух из камеры, с помощью регулировочного винта зажима на резиновом шланге.
ЗАДАНИЕ 5. ИЗУЧЕНИЕ КОЛЛЕКЦИИ КРИСТАЛЛИЧЕСКИХ ТЕЛ
Оборудование: лупа, коллекция минералов и горных пород, набор «Шкала твердости», коллекция «Металлы и сплавы».
Содержание и метод выполнения задания
Почти все твердые тела состоят из кристаллов, однако обнаружить их кристаллическое строение путем внешнего осмотра удается далеко не всегда. Характерный признак кристалла — наличие плоских граней. Большинство природных и искусственно изготовленных
твердых тел имеет поликристаллическое строение. При рассматривании невооруженным глазом заметить их кристаллическое строение трудно. Но если образец со свежей поверхностью излома и крупнозернистой структурой рассмотреть через лупу, то можно сделать вывод о его кристаллическом строении по характерному для кристаллов признаку — наличию плоских поверхностей у кристаллических зерен. На свежих изломах грани отдельных кристаллов обнажены особенно хорошо. Поворачивая образец, можно наблюдать поблескивание таких граней.
Порядок выполнения задания
1. Ознакомьтесь с различными видами кристаллов, рассмотрите кристаллы кварца, известкового шпата, каменной соли, сильвина, карналлита, гипса, апатита, полевого шпата, топаза, плавикового шпата. Выпишите химические формулы каждого из этих минералов.
2. Зарисуйте кристаллы кварца, исландского шпата, сильвина, гипса.
3. Используя лупу, осмотрите образцы магнезита, железного шпата, корунда, агата, кремния, яшмы, чугуна, железа, алюминия, меди, баббита. Выпишите химическую формулу каждого из образцов. Образцы, у которых вам удалось обнаружить кристаллическую структуру, запишите в одну колонку, образцы, у которых кристаллическую структуру вам обнаружить не удалось, — в другую.
4. С помощью лупы рассмотрите структуру образцов горных пород: гранита, песчаника, известняка, мрамора.
ЗАДАНИЕ 6. НАБЛЮДЕНИЕ ПРОЦЕССА РОСТА КРИСТАЛЛОВ
Оборудование: микроскоп, предметное стекло, стеклянная палочка, насыщенные растворы хлористого аммоння, щавелево-кислого аммония, поваренной соли, гидрохинона.
Содержание и метод выполнения задания
Раствором называется однородная смесь, в которой молекулы одного вещества равномерно распределены между молекулами другого. Взаимное растворение двух веществ имеет некоторые пределы, которые зависят от природы растворителя, растворяемого вещества и температуры.
Цель настоящей работы — наблюдение процесса роста кристаллов различных веществ в пересыщенном водном растворе. Для этого небольшое количество насыщенного раствора помещается на предметное стекло под объектив микроскопа. Испарение воды делает раствор пересыщенным, и в нем начинается кристаллизация. Процесс кристаллизации удобно наблюдать в микроскоп с 80-кратным увеличением, используя объектив с восьмикратным и окуляр с десятикратным увеличением.
Порядок выполнения работы
1. Поместите на столик микроскопа предметное стекло, отрегулируйте освещение и вращением микрометрического винта добейтесь получения четкого изображения поверхности предметного стекла. Наводку на резкость можно облегчить нанесением на поверхность стекла метки карандашом.
Внимание!
При наводке на резкость вращение винта следует производить с осторожностью, чтобы не допустить повреждения объектива при соприкосновении с предметным стеклом.
2. Выньте предметное стекло из зажимов и поместите на него с помощью стеклянной палочки каплю насыщенного раствора хлористого аммония.
3. Поместите стекло с каплей под объектив микроскопа так, чтобы в поле зрения был виден край капли, так как первые кристаллы образуются обычно на краю капли.
4. Пронаблюдайте процесс зарождения и роста кристаллов.
Результаты наблюдений занесите в отчет, который должен содержать описание процесса роста кристаллов и зарисовку картины, видимой в микроскоп.
5. Аналогичные наблюдения и зарисовки выполните с использованием раствора поваренной соли, щавелево-кислого аммония, гидрохинона.
ЗАДАНИЕ 7. ВЫРАЩИВАНИЕ КРИСТАЛЛОВ
Оборудование: порошок алюмокалиевых квасцов, термометр, дистиллированная вода, химические стаканы, электрическая плитка, воронка, стеклянная палочка, вата.
Содержание и метод выполнения задания
Существуют два простых способа выращивания кристаллов из пересыщенного раствора: путем охлаждения насыщенного раствора или путем его выпаривания. Первым этапом при любом из двух способов является приготовление насыщенного раствора.
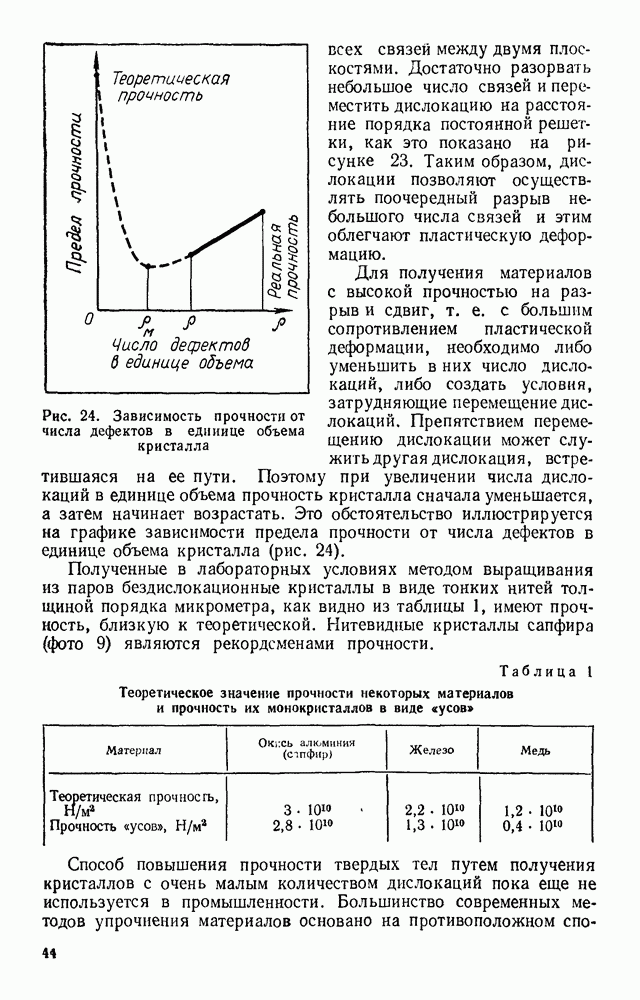
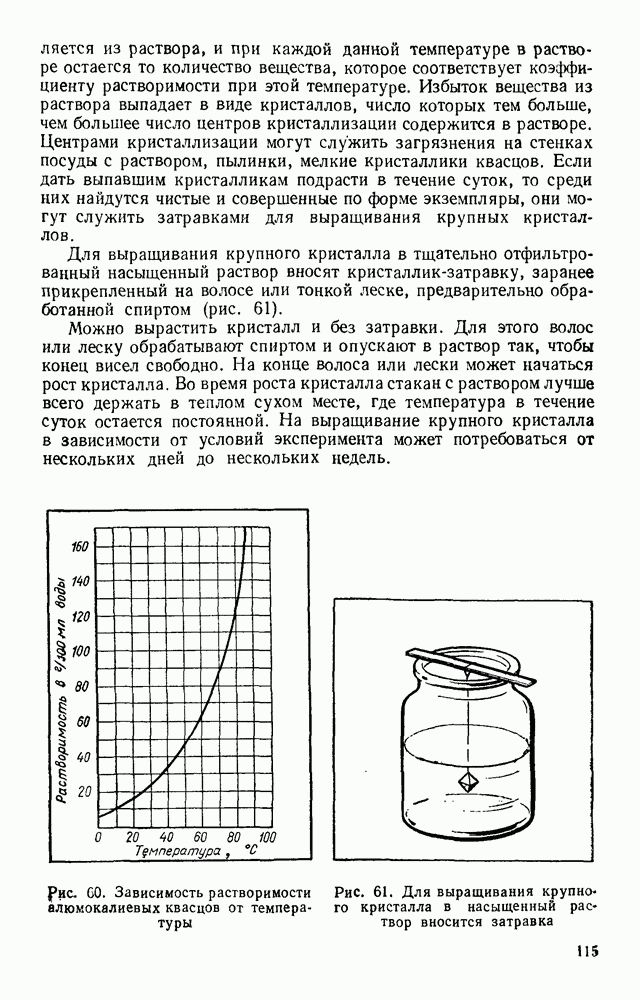
Растворимость любых веществ зависит от температуры. Обычно с повышением температуры растворимость увеличивается, а с понижением температуры — уменьшается. На рисунке 60 показана зависимость растворимости алюмокалиевых квасцов от температуры.
График позволяет увидеть, что при охлаждении насыщенного при 40 °С раствора до 20 °С в нем будет находиться около 15 г избыточного количества квасцов на 100 г воды. При отсутствии центров кристаллизации это вещество может оставаться в растворе, т. е. раствор будет пересыщенным.
С появлением центров кристаллизации избыток вещества
выделяется из раствора, и при каждой данной температуре в растворе остается то количество вещества, которое соответствует коэффициенту растворимости при этой температуре. Избыток вещества из раствора выпадает в виде кристаллов, число которых тем больше, чем большее число центров кристаллизации содержится в растворе. Центрами кристаллизации могут служить загрязнения на стенках посуды с раствором, пылинки, мелкие кристаллики квасцов. Если дать выпавшим кристалликам подрасти в течение суток, то среди них найдутся чистые и совершенные по форме экземпляры, они могут служить затравками для выращивания крупных кристаллов.
Для выращивания крупного кристалла в тщательно отфильтрованный насыщенный раствор вносят кристаллик-затравку, заранее прикрепленный на волосе или тонкой леске, предварительно обработанной спиртом (рис. 61).
Можно вырастить кристалл и без затравки. Для этого волос или леску обрабатывают спиртом и опускают в раствор так, чтобы конец висел свободно. На конце волоса или лески может начаться рост кристалла. Во время роста кристалла стакан с раствором лучше всего держать в теплом сухом месте, где температура в течение суток остается постоянной. На выращивание крупного кристалла в зависимости от условий эксперимента может потребоваться от нескольких дней до нескольких недель.

рис. 60. Зависимость растворимости алюмокалиевых квасцов от температуры

Рис. 61. Для выращивания крупного кристалла в насыщенный раствор вносится затравка
Порядок выполнения задания
1. Тщательно вымойте два стакана и воронку, подержите их над паром.
2. Налейте 100 г дистиллированной (или дважды прокипяченной) воды в стакан и нагрейте ее до 30 °С. Используя кривую растворимости, приведенную на рисунке 60, определите массу квасцов, необходимую для приготовления насыщенного раствора при 30 °С. Приготовьте насыщенный раствор и слейте его через ватный фильтр в чистый стакан.
3. Через сутки слейте раствор через ватный фильтр в чистый, заново вымытый пропаренный стакан. Среди множества кристаллов, оставшихся на дне первого стакана, выберите самый чистый кристалл правильной формы. Прикрепите кристалл-затравку к волосу или леске и подвесьте его в раствор. Волос или леску предварительно протрите ватой, смоченной спиртом. Можно также положить кристалл-затравку на дно стакана перед заливкой в него раствора. Поставьте стакан в теплое чистое место. В течение нескольких суток или недель не трогайте кристалл и не переставляйте стакан. В конце срока выращивания выньте кристалл из раствора, тщательно осушите бумажной салфеткой и уложите в специальную коробку. Руками кристалл не трогайте, иначе он потеряет прозрачность.
Домашнее лабораторное задание
Таким же способом, какой предложен в описании задания 7, приготовьте дома насыщенный раствор поваренной соли или сахара и попробуйте вырастить в нем крупные кристаллы.
ЗАДАНИЕ 8. ОПРЕДЕЛЕНИЕ УДЕЛЬНОЙ ТЕПЛОЕМКОСТИ СВИНЦА
Оборудование: свинец (дробь) 0,15-0,2 кг, картонная трубка термометр, воронка, линейка.
Содержание и метод выполнения задания
Для определения удельной теплоемкости свинца можно использовать явление нагревания твердых тел при пластической деформации. В картонный цилиндр насыпают дробь, начальная температура которой  предварительно измерена. Затем вертикально расположенный картонный цилиндр резко поворачивают вокруг горизонтальной оси на 180°. Поднятая на высоту
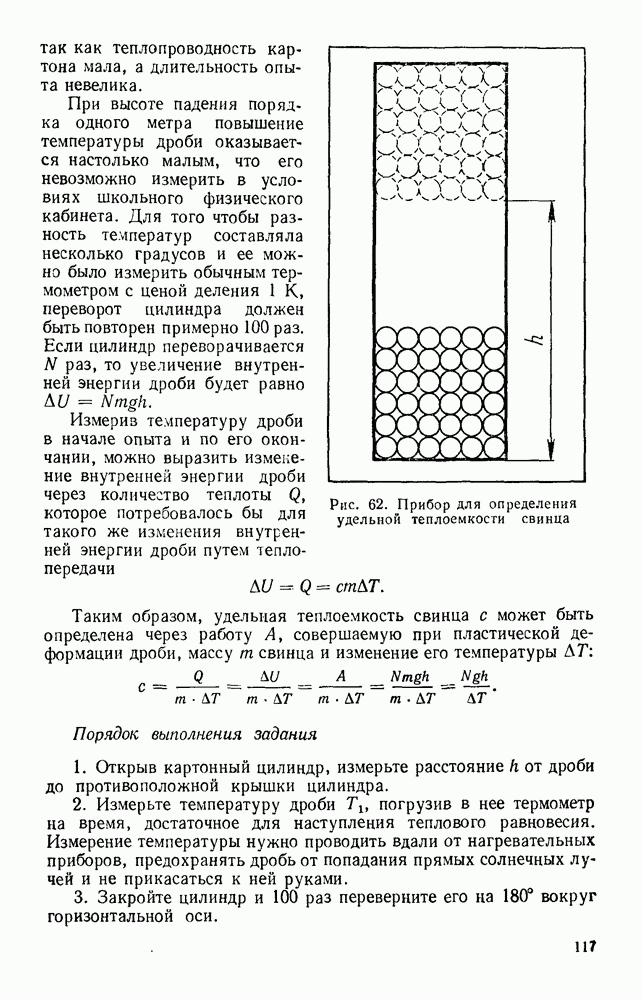
предварительно измерена. Затем вертикально расположенный картонный цилиндр резко поворачивают вокруг горизонтальной оси на 180°. Поднятая на высоту  (рис. 62) дробь падает, и ее потенциальная энергия превращается в кинетическую. При достижении дна цилиндра кинетическая энергия дроби расходуется на пластическую деформацию, сопровождающуюся увеличением внутренней энергии свинца. Потерями тепла можно пренебречь,
(рис. 62) дробь падает, и ее потенциальная энергия превращается в кинетическую. При достижении дна цилиндра кинетическая энергия дроби расходуется на пластическую деформацию, сопровождающуюся увеличением внутренней энергии свинца. Потерями тепла можно пренебречь,

Рис. 62. Прибор для определения удельной теплоемкости свинца
так как теплопроводность картона мала, а длительность опыта невелика.
При высоте падения порядка одного метра повышение температуры дроби оказывается настолько малым, что его невозможно измерить в условиях школьного физического кабинета. Для того чтобы разность температур составляла несколько градусов и ее можно было измерить обычным термометром с ценой деления 1 К, переворот цилиндра должен быть повторен примерно 100 раз.
Если цилиндр переворачивается  раз, то увеличение внутренней энергии дроби будет равно
раз, то увеличение внутренней энергии дроби будет равно 
Измерив температуру дроби в начале опыта и по его окончании, можно выразить изменение внутренней энергии дроби через количество теплоты  которое потребовалось бы для такого же изменения внутренней энергии дроби путем теплопередачи
которое потребовалось бы для такого же изменения внутренней энергии дроби путем теплопередачи

Таким образом, удельная теплоемкость свинца с может быть определена через работу А, совершаемую при пластической деформации дроби, массу  свинца и изменение его температуры
свинца и изменение его температуры 

Порядок выполнения задания
1. Открыв картонный цилиндр, измерьте расстояние  от дроби до противоположной крышки цилиндра.
от дроби до противоположной крышки цилиндра.
2. Измерьте температуру дроби  погрузив в нее термометр на время, достаточное для наступления теплового равновесия. Измерение температуры нужно проводить вдали от нагревательных приборов, предохранять дробь от попадания прямых солнечных лучей и не прикасаться к ней руками.
погрузив в нее термометр на время, достаточное для наступления теплового равновесия. Измерение температуры нужно проводить вдали от нагревательных приборов, предохранять дробь от попадания прямых солнечных лучей и не прикасаться к ней руками.
3. Закройте цилиндр и 100 раз переверните его на 180° вокруг горизонтальной оси.
4. Измерьте температуру дроби, учитывая указания, содержащиеся в пункте 2. Результаты измерений и вычислений занесите в отчетную таблицу и вычислите удельную теплоемкость свинца.
5. Через 15—20 мин повторите опыт.
Отчетная таблица

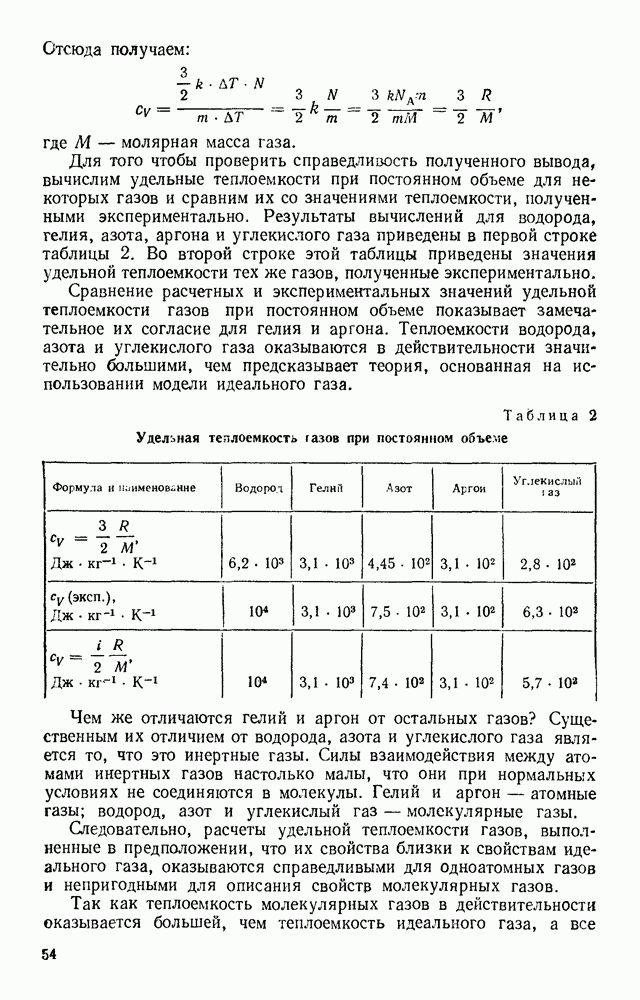
ЗАДАНИЕ 9. СРАВНЕНИЕ МОЛЯРНЫХ ТЕПЛОЕМКОСТЕЙ МЕТАЛЛОВ
Оборудование: алюминиевое, медное и железное тела массами 50-100 г, калориметр, мензурка, термометр, сосуде водой, электроплитка, весы с разновесом.
Содержание и метод выполнения задания
Из классической теории теплоемкости следует, что теплоемкость одного моля одинакова для всех веществ в твердом состоянии и равна:

Это предсказание теории легко проверить. Для этого достаточно определить количество тепла  отдаваемого твердым телом известной массы
отдаваемого твердым телом известной массы  при охлаждении в известном интервале температур
при охлаждении в известном интервале температур  .
.
Порядок выполнения задания
1. Определите с помощью весов массу калориметра  и массы медного, железного и алюминиевого тел. Результаты измерений занесите в отчетную таблицу.
и массы медного, железного и алюминиевого тел. Результаты измерений занесите в отчетную таблицу.
2. Опустите тела в сосуд с кипящей водой.
3. Налейте в калориметр  воды при комнатной температуре. Измерьте начальную температуру воды и калориметра
воды при комнатной температуре. Измерьте начальную температуру воды и калориметра 
4. Опустите в калориметр медное тело, нагретое до температуры 100 °С, и определите температуру 0 в калориметре после установления теплового равновесия.
5. Используя уравнение теплового баланса, вычислите количество теплоты  переданное медным телом калориметру и воде:
переданное медным телом калориметру и воде:

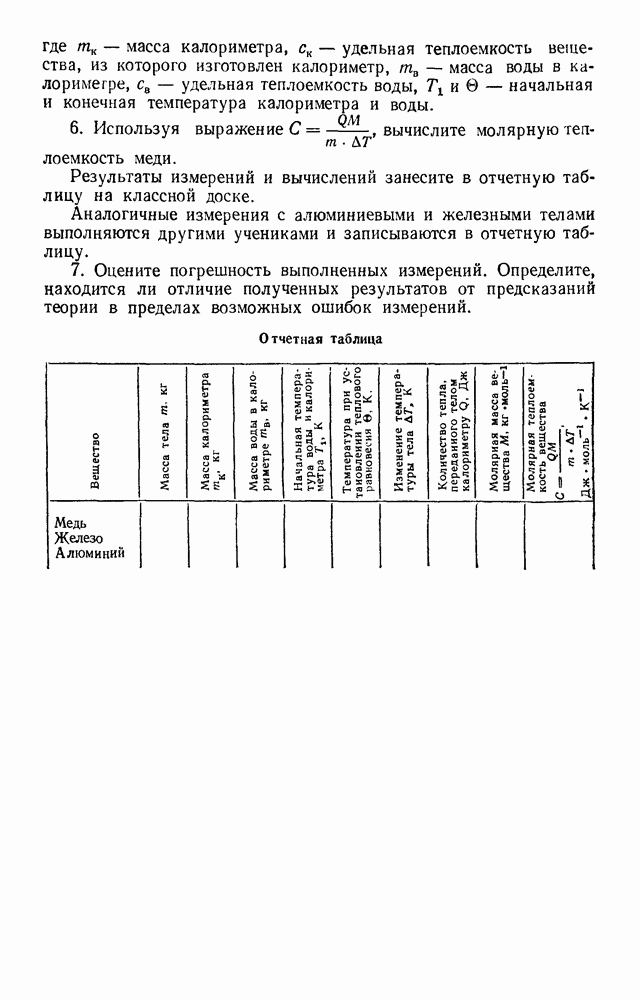
где  — масса калориметра,
— масса калориметра,  удельная теплоемкость вещества, из которого изготовлен калориметр,
удельная теплоемкость вещества, из которого изготовлен калориметр,  масса воды в калориметре,
масса воды в калориметре,  удельная теплоемкость воды,
удельная теплоемкость воды,  — начальная и конечная температура калориметра и воды.
— начальная и конечная температура калориметра и воды.
6. Используя выражение  вычислите молярную теплоемкость меди.
вычислите молярную теплоемкость меди.
Результаты измерений и вычислений занесите в отчетную таблицу на классной доске.
Аналогичные измерения с алюминиевыми и железными телами выполняются другими учениками и записываются в отчетную таблицу.
7. Оцените погрешность выполненных измерений. Определите, находится ли отличие полученных результатов от предсказаний теории в пределах возможных ошибок измерений.
Отчетная таблица

| << Предыдущий параграф | Следующий параграф >> |
- МОЛЕКУЛЯРНАЯ ФИЗИКА
- § 2. ЧИСЛО АВОГАДРО
- § 3. ИДЕАЛЬНЫЙ ГАЗ
- § 4. ДАВЛЕНИЕ ИДЕАЛЬНОГО ГАЗА
- § 5. ГАЗОВЫЙ ТЕРМОМЕТР
- § 6. ТЕМПЕРАТУРА КАК МЕРА СРЕДНЕЙ КИНЕТИЧЕСКОЙ ЭНЕРГИИ МОЛЕКУЛ
- § 7. УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА
- § 8. РЕАЛЬНЫЕ ГАЗЫ
- § 9. СРЕДНЯЯ ДЛИНА СВОБОДНОГО ПРОБЕГА
- § 10. ДИФФУЗИЯ И БРОУНОВСКОЕ ДВИЖЕНИЕ
- § 11. СЖИЖЕНИЕ ГАЗОВ
- § 12. ОБЛАКА И ОСАДКИ
- § 13. ЗАВИСИМОСТЬ АГРЕГАТНОГО СОСТОЯНИЯ ВЕЩЕСТВА ОТ ТЕМПЕРАТУРЫ И ДАВЛЕНИЯ
- § 14. СТРОЕНИЕ КРИСТАЛЛОВ
- § 15. ПРОЦЕССЫ РОСТА КРИСТАЛЛОВ
- § 16. ПОЛУЧЕНИЕ МОНОКРИСТАЛЛОВ
- § 17. ПРИМЕНЕНИЯ КРИСТАЛЛИЧЕСКИХ ТЕЛ
- § 18. КРИСТАЛЛЫ И ЖИЗНЬ
- Глава 2. ТЕРМОДИНАМИКА
- § 19. ТЕРМОДИНАМИЧЕСКИЙ МЕТОД
- § 20. РАБОТА И КОЛИЧЕСТВО ТЕПЛОТЫ В ТЕРМОДИНАМИКЕ
- § 21. ТЕПЛОЕМКОСТЬ ГАЗОВ
- § 22. ТЕПЛОЕМКОСТЬ ТВЕРДЫХ ТЕЛ И ЖИДКОСТЕЙ
- § 23. ПОТРЕБЛЕНИЕ ЭНЕРГИИ
- § 24. ТЕПЛОВЫЕ ДВИГАТЕЛИ
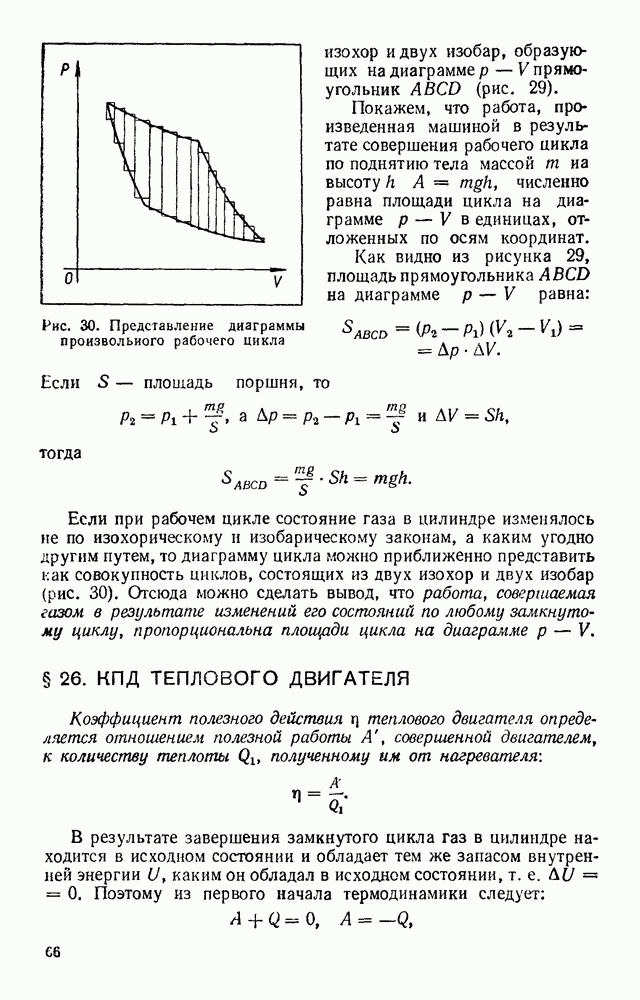
- § 25. РАБОЧИЙ ЦИКЛ ТЕПЛОВОГО ДВИГАТЕЛЯ
- § 26. КПД ТЕПЛОВОГО ДВИГАТЕЛЯ
- § 27. ПАРОВАЯ МАШИНА
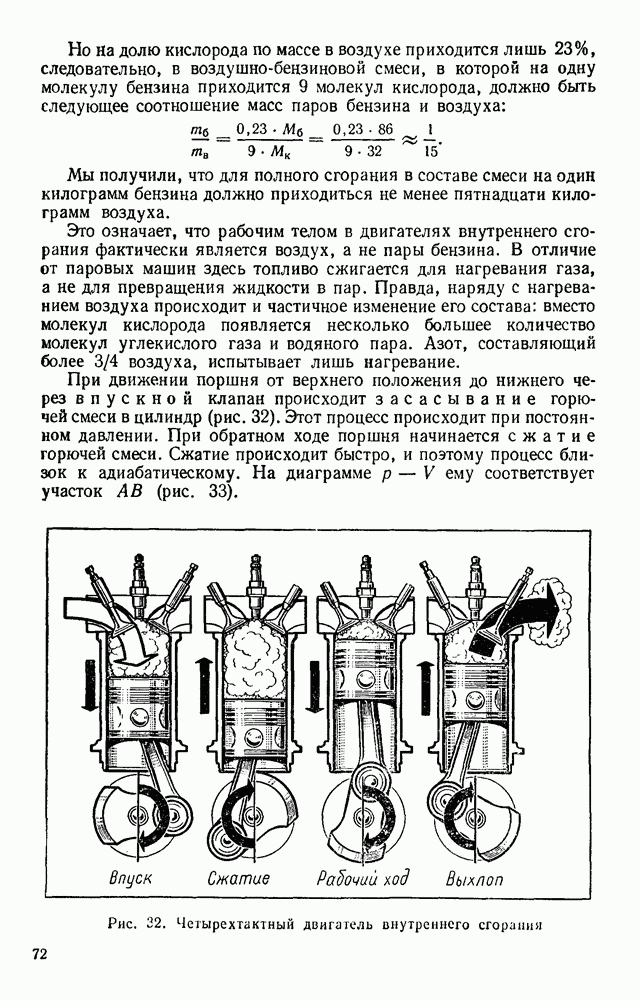
- § 28. ДВИГАТЕЛЬ ВНУТРЕННЕГО СГОРАНИЯ
- § 29. ПАРОВАЯ И ГАЗОВАЯ ТУРБИНЫ
- § 30. РЕАКТИВНЫЕ ДВИГАТЕЛИ
- § 31. ПРАКТИКУМ ПО РЕШЕНИЮ ЗАДАЧ
- ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
- ТЕРМОДИНАМИКА
- § 32. ЛАБОРАТОРНЫЕ И ПРАКТИЧЕСКИЕ ЗАДАНИЯ
- ЭЛЕКТРОДИНАМИКА
- Глава 3. ЭЛЕКТРИЧЕСКОЕ ПОЛЕ И ЭЛЕКТРИЧЕСКИЙ ТОК
- § 34. ПОТЕНЦИАЛ
- § 35. ДИЭЛЕКТРИКИ И ПРОВОДНИКИ В ЭЛЕКТРИЧЕСКОМ ПОЛЕ
- § 36. СВОЙСТВА p-n-ПЕРЕХОДА
- § 37. ТРАНЗИСТОР
- Глава 4. МАГНЕТИЗМ
- § 38. МАГНИТНОЕ ВЗАИМОДЕЙСТВИЕ ДВИЖУЩИХСЯ ЭЛЕКТРИЧЕСКИХ ЗАРЯДОВ
- § 39. МАГНИТНОЕ ПОЛЕ
- § 40. МАГНИТНОЕ ПОЛЕ ДВИЖУЩЕГОСЯ ЭЛЕКТРИЧЕСКОГО ЗАРЯДА
- § 41. МАГНИТНОЕ ПОЛЕ ТОКА В ВАКУУМЕ
- § 42. ДЕЙСТВИЕ МАГНИТНОГО ПОЛЯ НА ДВИЖУЩИЕСЯ ЭЛЕКТРИЧЕСКИЕ ЗАРЯДЫ
- § 43. МАГНИТНАЯ ПОСТОЯННАЯ ВАКУУМА
- § 44. ЭЛЕКТРИЧЕСКИЕ ГЕНЕРАТОРЫ
- § 45. ЭЛЕКТРОМАГНИТНОЕ ПОЛЕ
- § 46. ПРАКТИКУМ ПО РЕШЕНИЮ ЗАДАЧ
- ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
- § 47. ЛАБОРАТОРНЫЕ И ПРАКТИЧЕСКИЕ ЗАДАНИЯ
- Глава 5. ФИЗИЧЕСНИЙ ПРАКТИКУМ
- ЛАБОРАТОРНАЯ РАБОТА № 2. ОПРЕДЕЛЕНИЕ МОЛЯРНОЙ МАССЫ ГАЗА
- ЛАБОРАТОРНАЯ РАБОТА № 3. ОПРЕДЕЛЕНИЕ СКОРОСТИ РОСТА КРИСТАЛЛОВ
- ЛАБОРАТОРНАЯ РАБОТА № 4. ОПРЕДЕЛЕНИЕ ТВЕРДОСТИ СТАЛИ ДО И ПОСЛЕ ЗАКАЛКИ
- ЛАБОРАТОРНАЯ РАБОТА № 6. ОПРЕДЕЛЕНИЕ ХАРАКТЕРИСТИК ХОЛОДИЛЬНИКА
- ЛАБОРАТОРНАЯ РАБОТА № 6. ПОВЕРКА ЭЛЕКТРОИЗМЕРИТЕЛЬНЫХ ПРИБОРОВ
- ЛАБОРАТОРНАЯ РАБОТА № 7. ИЗУЧЕНИЕ ЭЛЕКТРОННОГО ОСЦИЛЛОГРАФА
- ЛАБОРАТОРНАЯ РАБОТА № 8. РАСЧЕТ И ИСПЫТАНИЕ СХЕМЫ АВТОМАТИЧЕСКОГО УПРАВЛЕНИЯ С ФОТОРЕЗИСТОРОМ
- ЛАБОРАТОРНАЯ РАБОТА № 9. ОПРЕДЕЛЕНИЕ КОЭФФИЦИЕНТА УСИЛЕНИЯ ТРАНЗИСТОРА ПО ТОКУ В СХЕМЕ С ОБЩИМ ЭМИТТЕРОМ
- ЛАБОРАТОРНАЯ РАБОТА № 10. ИЗМЕРЕНИЕ МАГНИТНОГО ПОТОКА ПОСТОЯННОГО МАГНИТА
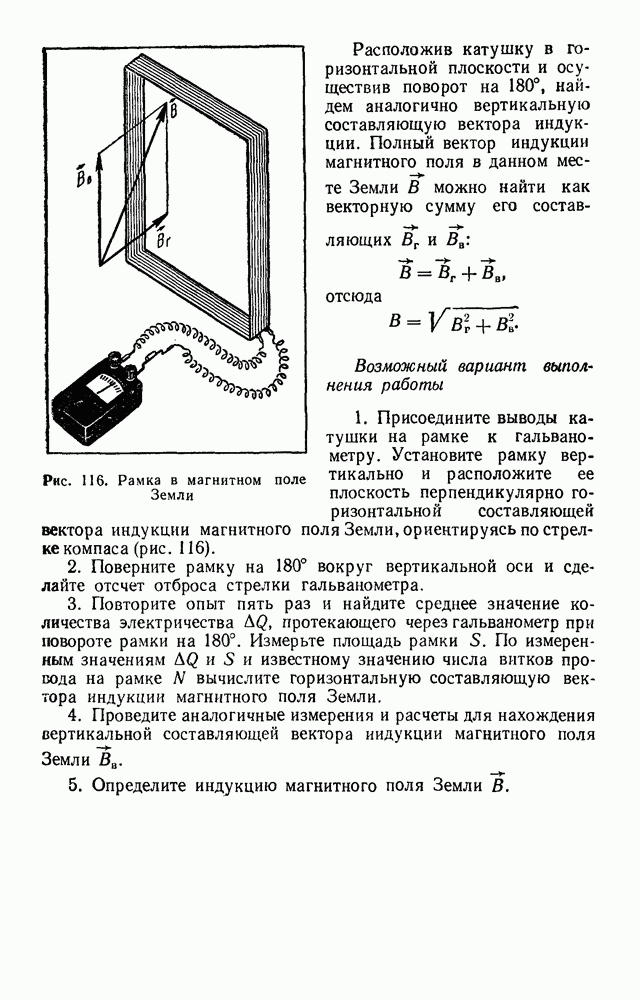
- ЛАБОРАТОРНАЯ РАБОТА № 11. ОПРЕДЕЛЕНИЕ ИНДУКЦИИ МАГНИТНОГО ПОЛЯ ЗЕМЛИ
- ОТВЕТЫ К ЗАДАЧАМ