| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Глава 2. ТЕРМОДИНАМИКА
§ 19. ТЕРМОДИНАМИЧЕСКИЙ МЕТОД
Границы применимости молекулярно-кинетической теории. Успешное применение молекулярно-кинетической теории для объяснения основных свойств газов, жидкостей и твердых тел делает заманчивой попытку количественного описания всех явлений в молекулярной физике лишь на основе применения молекулярнокинетической теории. Однако этот путь в большинстве случаев оказывается либо слишком сложным, либо принципиально неприменимым.
Попробуем, например, решить следующую задачу, используя лишь молекулярно-кинетическую теорию и законы механики.
В цилиндре под поршнем, способным перемещаться, находится идеальный газ. Объем газа V, его давление  температура
температура  Какими будут давление
Какими будут давление  и температура
и температура  газа, если тело массой
газа, если тело массой  упавшее на поршень с высоты
упавшее на поршень с высоты  вызвало уменьшение объема газа до
вызвало уменьшение объема газа до  (рис. 25)?
(рис. 25)?
Поскольку в условии задачи не упоминается о нагревании, кажется очевидным, что температура тела при любых изменениях объема и давления должна оставаться неизменной, т. е.  Изменение давления газа при изотермическом процессе должно быть обратно пропорциональным изменению его объема:
Изменение давления газа при изотермическом процессе должно быть обратно пропорциональным изменению его объема:

Казалось бы, задача решена. Однако проделаем следующий опыт. В прозрачный цилиндр из плексигласа поместим кусочек ваты, затем вставим поршень, снабженный штоком с большой рукояткой. Установим цилиндр с поршнем на столе вертикально, заменим удар тела массой  резким ударом ладони по рукоятке (рис. 26). Опыт показывает, что при быстром сжатии воздуха в цилиндре вата вспыхивает, т. е. температура воздуха в цилиндре существенно повышается, хотя теплопередача не происходит.
резким ударом ладони по рукоятке (рис. 26). Опыт показывает, что при быстром сжатии воздуха в цилиндре вата вспыхивает, т. е. температура воздуха в цилиндре существенно повышается, хотя теплопередача не происходит.
В результате чего же произошло изменение температуры воздуха в цилиндре и каким способом можно рассчитать это изменение?

Рис. 25. Сжатие газа в цилиндре

Рис. 26. «Воздушное огниво»
Можно предположить, что возрастание температуры газа при сжатии происходит в результате столкновений молекул с движущимся поршнем. Это предположение кажется мало правдоподобным, так как скорости теплового движения молекул воздуха при комнатной температуре имеют значения около 500 м/с, а скорость движения поршня не превышает нескольких метров в секунду. Однако приблизительный расчет показывает (§ 31, задача 23) возможность такого результата. Но можно ли считать полученный таким образом результат точным? Конечно, нет. В расчетах длины пути, пройденного молекулой, и числа ее столкновений с поршнем трудно учесть хаотический характер теплового движения молекул и изменение скорости их движения в результате взаимных столкновений. Не учитывалось в расчетах и отличие свойств реального газа от идеального.
Таким образом, молекулярно-кинетическая теория сталкивается с серьезными трудностями при попытке перейти от приблизительных качественных объяснений к точным количественным расчетам. Эти трудности связаны, с одной стороны, с неполнотой наших знаний о силах взаимодействия молекул, с другой стороны, они обусловлены чрезвычайно большим числом взаимодействующих между собой тел.
Термодинамика. Для анализа большого круга физических явлений и процессов, решения практических задач более продуктивным оказывается применение методов термодинамики.
Термодинамика изучает общие свойства тел и различные процессы в них, сопровождающиеся превращениями энергии, не используя какую-либо определенную модель строения вещества и не высказывая предположения о законах взаимодействия атомов и молекул. В основу ее положено небольшое число наиболее общих законов природы. Широкие возможности применения методов
термодинамики связаны с тем, что многие свойства тел обусловлены происходящими в них процессами превращения энергии из одних видов в другие. Сформулированный на основе обобщения всех известных в настоящее время в физике опытных данных закон сохранения и превращения энергии является одним из основных постулатов термодинамики.
Термодинамическая система. В термодинамике часто используется предположение о возможности выделения совокупности тел, не взаимодействующих с другими телами.
Совокупность физических тел, изолированная от взаимодействия с другими телами, называется изолированной термодинамической системой.
Состояние термодинамической системы полностью описывается некоторым числом независимых физических параметров. Например, состояние некоторой массы газа характеризуется объемом V, давлением  и температурой Т.
и температурой Т.
Различают равновесные и неравновесные состояния системы. Равновесным называется такое состояние термодинамической системы, при котором все ее параметры остаюпеся с течением времени неизменными без необходимости совершения какого-либо термодинамического процесса вне этой системы.
Любое изменение в термодинамической системе, сопровождающееся изменением хотя бы одного параметра системы, называется термодинамическим процессом. Изучение термодинамических процессов является одной из задач термодинамики.
Внутренняя энергия. Одним из важнейших параметров термодинамической системы является внутренняя энергия системы. Внутренней энергией системы называют совокупность всех видов энергии, которыми обладают тела, входящие в систему.
На основании результатов всех выполненных до сих пор опытов и наблюдений в термодинамике принимается закон сохранения и превращения энергии. Его можно сформулировать как закон постоянства внутренней энергии: при любых процессах в изолированной термодинамической системе внутренняя энергия остается неизменной:

Этот факт имеет принципиальное значение. Из него следует, что движение материи имеет меру, одинаково пригодную для количественной характеристики движения любой формы материи. Этой мерой движения является энергия.
Решение задачи. Возвращаясь к задаче, поставленной в начале параграфа, используем для ее решения термодинамический метод. Рассматривая Землю, тело массой  и газ в цилиндре с поршнем как изолированную термодинамическую систему, можно утверждать, что внутренняя энергия системы в результате падения тела с высоты
и газ в цилиндре с поршнем как изолированную термодинамическую систему, можно утверждать, что внутренняя энергия системы в результате падения тела с высоты  и сжатия газа в цилиндре остается неизменной. Однако при этом потенциальная энергия системы Земля — тела
и сжатия газа в цилиндре остается неизменной. Однако при этом потенциальная энергия системы Земля — тела
уменьшилась на величину  следовательно, внутренняя энергия газа в цилиндре должна увеличиться на равную величину:
следовательно, внутренняя энергия газа в цилиндре должна увеличиться на равную величину:

Это утверждение справедливо, если к моменту достижения значения объема газа  скорость тела массой
скорость тела массой  равна нулю и потерями энергии на нагревание стенок цилиндра и поршня можно пренебречь.
равна нулю и потерями энергии на нагревание стенок цилиндра и поршня можно пренебречь.
Считая газ в цилиндре идеальным, изменение его внутренней энергии  можно связать с изменением температуры
можно связать с изменением температуры 

откуда

где  — постоянная Больцмана,
— постоянная Больцмана,  — число молекул в цилиндре.
— число молекул в цилиндре.
Определив температуру  и зная объем газа
и зная объем газа  , можно определить его давление
, можно определить его давление  из уравнения состояния идеального газа.
из уравнения состояния идеального газа.
Таким образом, задача решена полностью. Однако при ее решении использовались и термодинамический метод, и элементы молекулярно-кинетической теории. Молекулярно-кинетическая теория оказалась необходимой для установления связи между изменениями внутренней энергии газа  и его температуры
и его температуры 
Покажем, что в термодинамике можно установить связь между внутренней энергией тела и его температурой и без использования молекулярно-кинетической теории.
| << Предыдущий параграф | Следующий параграф >> |
- МОЛЕКУЛЯРНАЯ ФИЗИКА
- § 2. ЧИСЛО АВОГАДРО
- § 3. ИДЕАЛЬНЫЙ ГАЗ
- § 4. ДАВЛЕНИЕ ИДЕАЛЬНОГО ГАЗА
- § 5. ГАЗОВЫЙ ТЕРМОМЕТР
- § 6. ТЕМПЕРАТУРА КАК МЕРА СРЕДНЕЙ КИНЕТИЧЕСКОЙ ЭНЕРГИИ МОЛЕКУЛ
- § 7. УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА
- § 8. РЕАЛЬНЫЕ ГАЗЫ
- § 9. СРЕДНЯЯ ДЛИНА СВОБОДНОГО ПРОБЕГА
- § 10. ДИФФУЗИЯ И БРОУНОВСКОЕ ДВИЖЕНИЕ
- § 11. СЖИЖЕНИЕ ГАЗОВ
- § 12. ОБЛАКА И ОСАДКИ
- § 13. ЗАВИСИМОСТЬ АГРЕГАТНОГО СОСТОЯНИЯ ВЕЩЕСТВА ОТ ТЕМПЕРАТУРЫ И ДАВЛЕНИЯ
- § 14. СТРОЕНИЕ КРИСТАЛЛОВ
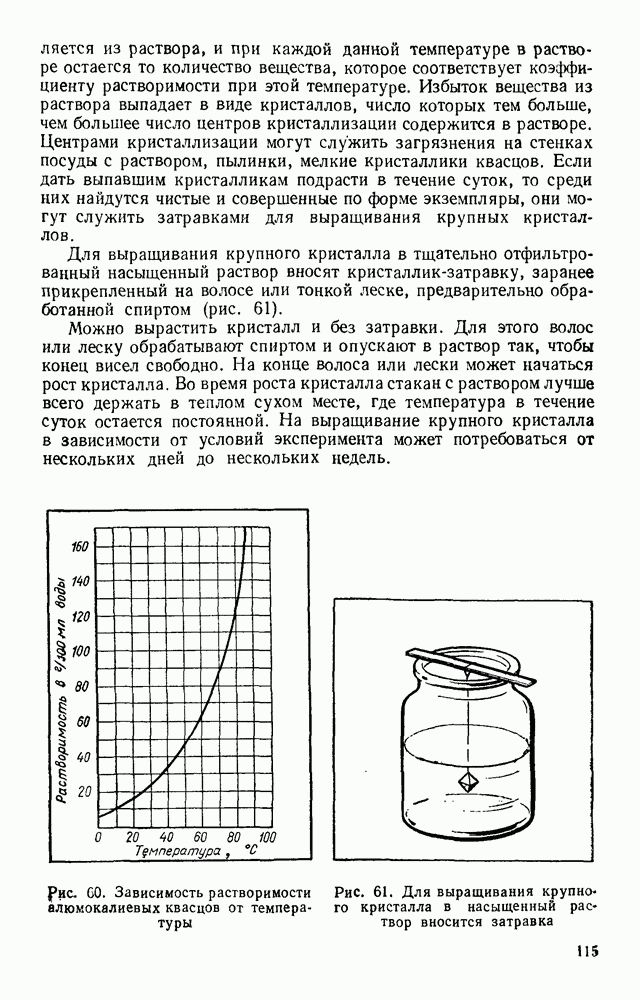
- § 15. ПРОЦЕССЫ РОСТА КРИСТАЛЛОВ
- § 16. ПОЛУЧЕНИЕ МОНОКРИСТАЛЛОВ
- § 17. ПРИМЕНЕНИЯ КРИСТАЛЛИЧЕСКИХ ТЕЛ
- § 18. КРИСТАЛЛЫ И ЖИЗНЬ
- Глава 2. ТЕРМОДИНАМИКА
- § 19. ТЕРМОДИНАМИЧЕСКИЙ МЕТОД
- § 20. РАБОТА И КОЛИЧЕСТВО ТЕПЛОТЫ В ТЕРМОДИНАМИКЕ
- § 21. ТЕПЛОЕМКОСТЬ ГАЗОВ
- § 22. ТЕПЛОЕМКОСТЬ ТВЕРДЫХ ТЕЛ И ЖИДКОСТЕЙ
- § 23. ПОТРЕБЛЕНИЕ ЭНЕРГИИ
- § 24. ТЕПЛОВЫЕ ДВИГАТЕЛИ
- § 25. РАБОЧИЙ ЦИКЛ ТЕПЛОВОГО ДВИГАТЕЛЯ
- § 26. КПД ТЕПЛОВОГО ДВИГАТЕЛЯ
- § 27. ПАРОВАЯ МАШИНА
- § 28. ДВИГАТЕЛЬ ВНУТРЕННЕГО СГОРАНИЯ
- § 29. ПАРОВАЯ И ГАЗОВАЯ ТУРБИНЫ
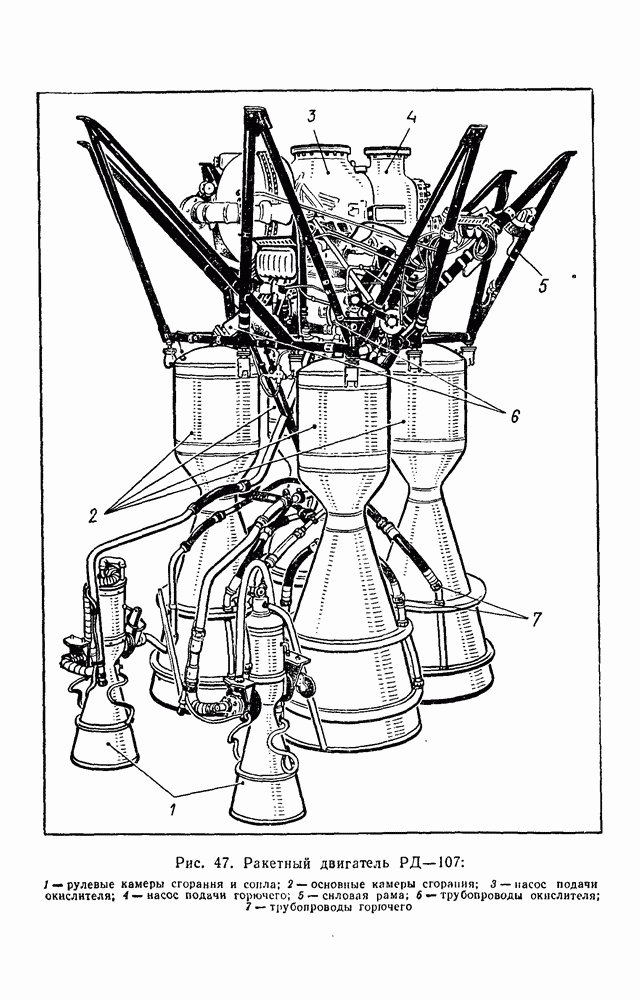
- § 30. РЕАКТИВНЫЕ ДВИГАТЕЛИ
- § 31. ПРАКТИКУМ ПО РЕШЕНИЮ ЗАДАЧ
- ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
- ТЕРМОДИНАМИКА
- § 32. ЛАБОРАТОРНЫЕ И ПРАКТИЧЕСКИЕ ЗАДАНИЯ
- ЭЛЕКТРОДИНАМИКА
- Глава 3. ЭЛЕКТРИЧЕСКОЕ ПОЛЕ И ЭЛЕКТРИЧЕСКИЙ ТОК
- § 34. ПОТЕНЦИАЛ
- § 35. ДИЭЛЕКТРИКИ И ПРОВОДНИКИ В ЭЛЕКТРИЧЕСКОМ ПОЛЕ
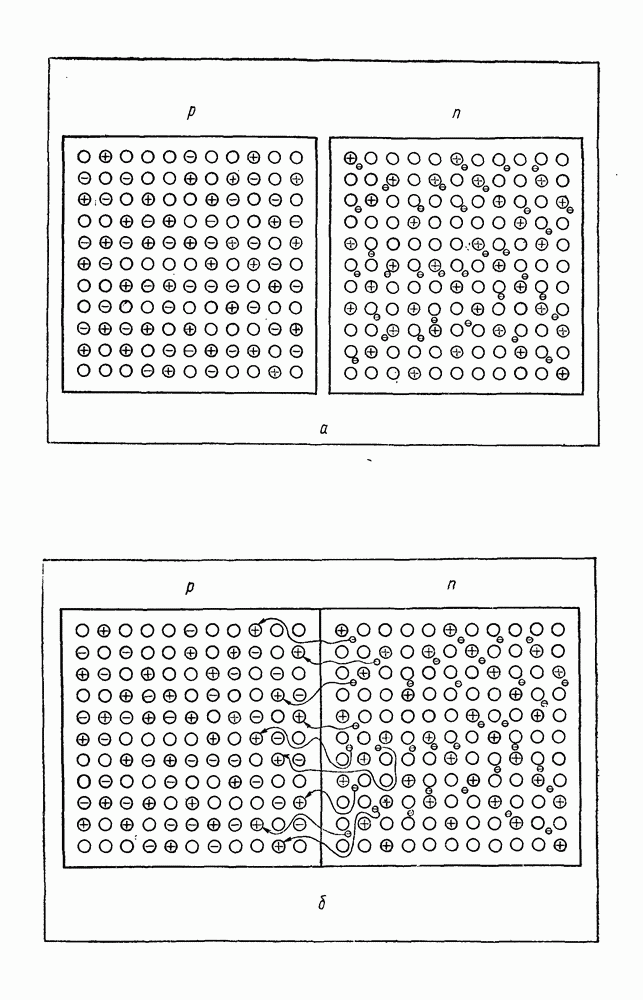
- § 36. СВОЙСТВА p-n-ПЕРЕХОДА
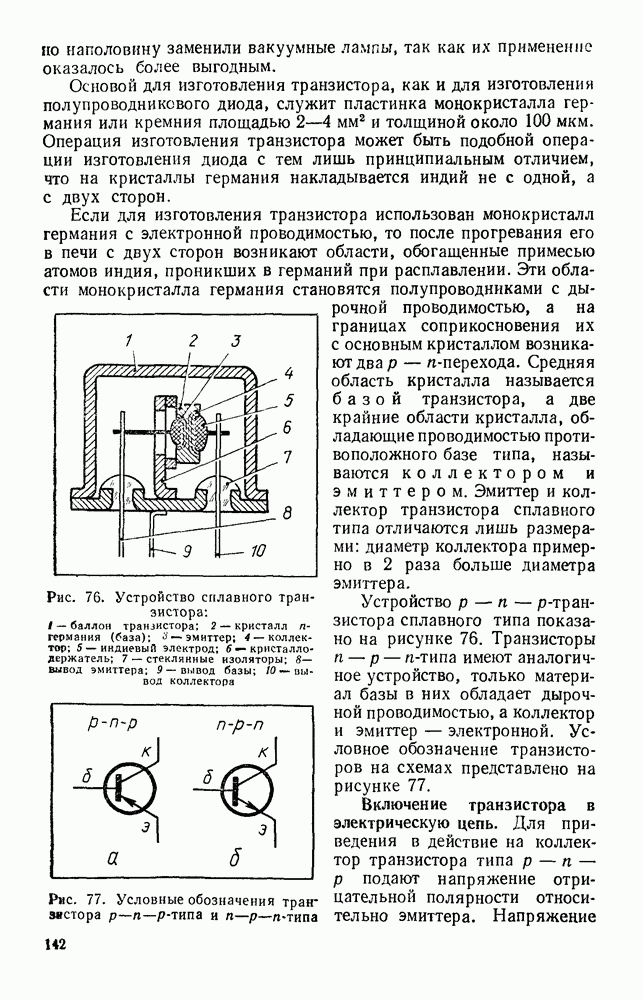
- § 37. ТРАНЗИСТОР
- Глава 4. МАГНЕТИЗМ
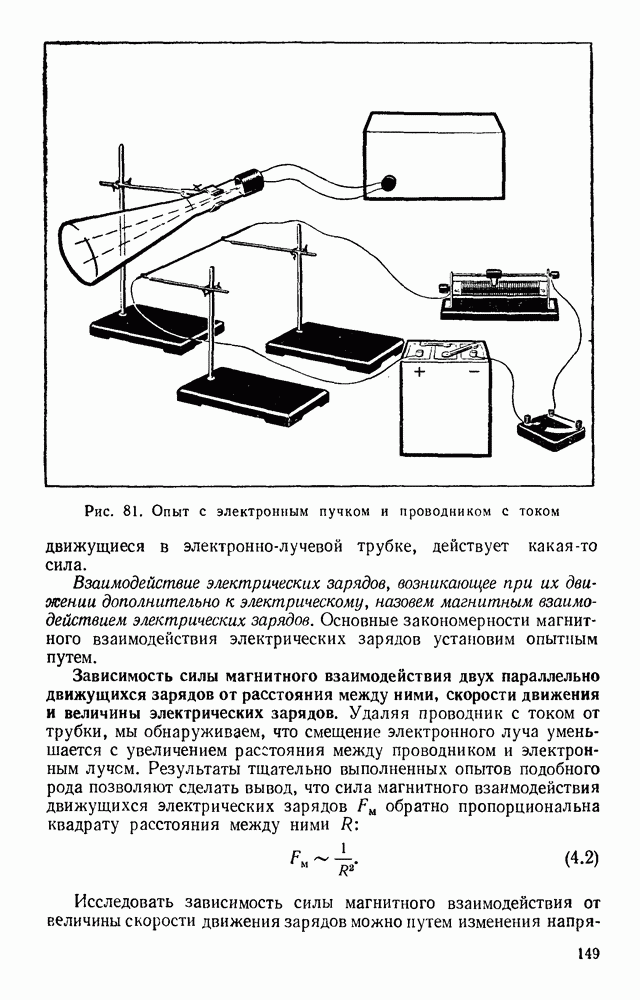
- § 38. МАГНИТНОЕ ВЗАИМОДЕЙСТВИЕ ДВИЖУЩИХСЯ ЭЛЕКТРИЧЕСКИХ ЗАРЯДОВ
- § 39. МАГНИТНОЕ ПОЛЕ
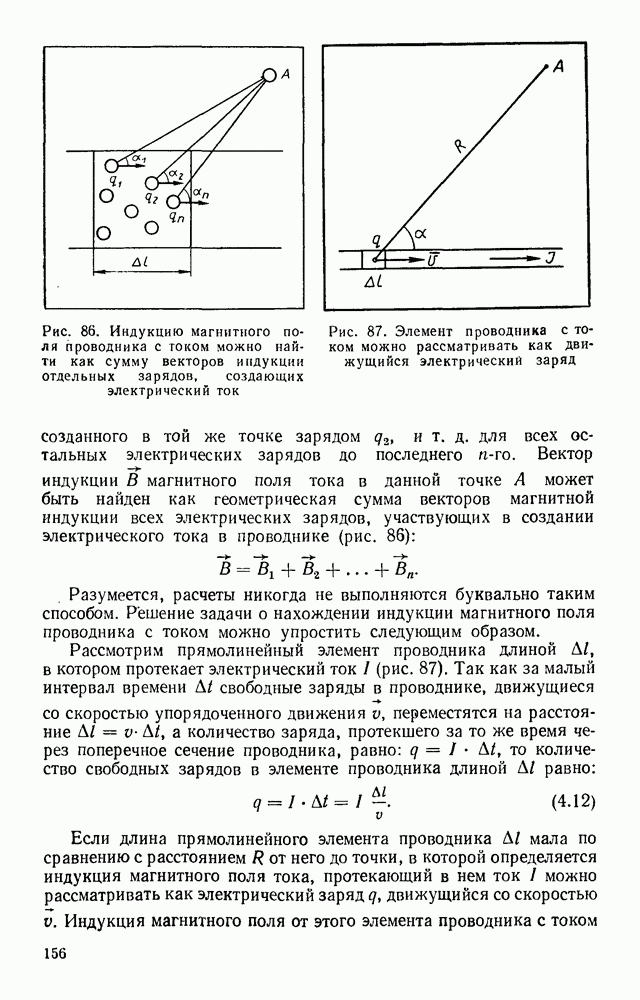
- § 40. МАГНИТНОЕ ПОЛЕ ДВИЖУЩЕГОСЯ ЭЛЕКТРИЧЕСКОГО ЗАРЯДА
- § 41. МАГНИТНОЕ ПОЛЕ ТОКА В ВАКУУМЕ
- § 42. ДЕЙСТВИЕ МАГНИТНОГО ПОЛЯ НА ДВИЖУЩИЕСЯ ЭЛЕКТРИЧЕСКИЕ ЗАРЯДЫ
- § 43. МАГНИТНАЯ ПОСТОЯННАЯ ВАКУУМА
- § 44. ЭЛЕКТРИЧЕСКИЕ ГЕНЕРАТОРЫ
- § 45. ЭЛЕКТРОМАГНИТНОЕ ПОЛЕ
- § 46. ПРАКТИКУМ ПО РЕШЕНИЮ ЗАДАЧ
- ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
- § 47. ЛАБОРАТОРНЫЕ И ПРАКТИЧЕСКИЕ ЗАДАНИЯ
- Глава 5. ФИЗИЧЕСНИЙ ПРАКТИКУМ
- ЛАБОРАТОРНАЯ РАБОТА № 2. ОПРЕДЕЛЕНИЕ МОЛЯРНОЙ МАССЫ ГАЗА
- ЛАБОРАТОРНАЯ РАБОТА № 3. ОПРЕДЕЛЕНИЕ СКОРОСТИ РОСТА КРИСТАЛЛОВ
- ЛАБОРАТОРНАЯ РАБОТА № 4. ОПРЕДЕЛЕНИЕ ТВЕРДОСТИ СТАЛИ ДО И ПОСЛЕ ЗАКАЛКИ
- ЛАБОРАТОРНАЯ РАБОТА № 6. ОПРЕДЕЛЕНИЕ ХАРАКТЕРИСТИК ХОЛОДИЛЬНИКА
- ЛАБОРАТОРНАЯ РАБОТА № 6. ПОВЕРКА ЭЛЕКТРОИЗМЕРИТЕЛЬНЫХ ПРИБОРОВ
- ЛАБОРАТОРНАЯ РАБОТА № 7. ИЗУЧЕНИЕ ЭЛЕКТРОННОГО ОСЦИЛЛОГРАФА
- ЛАБОРАТОРНАЯ РАБОТА № 8. РАСЧЕТ И ИСПЫТАНИЕ СХЕМЫ АВТОМАТИЧЕСКОГО УПРАВЛЕНИЯ С ФОТОРЕЗИСТОРОМ
- ЛАБОРАТОРНАЯ РАБОТА № 9. ОПРЕДЕЛЕНИЕ КОЭФФИЦИЕНТА УСИЛЕНИЯ ТРАНЗИСТОРА ПО ТОКУ В СХЕМЕ С ОБЩИМ ЭМИТТЕРОМ
- ЛАБОРАТОРНАЯ РАБОТА № 10. ИЗМЕРЕНИЕ МАГНИТНОГО ПОТОКА ПОСТОЯННОГО МАГНИТА
- ЛАБОРАТОРНАЯ РАБОТА № 11. ОПРЕДЕЛЕНИЕ ИНДУКЦИИ МАГНИТНОГО ПОЛЯ ЗЕМЛИ
- ОТВЕТЫ К ЗАДАЧАМ