| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
2. ХИМИЧЕСКИЕ СОЕДИНЕНИЯ
Химические соединения и родственные им по природе фазы в металлических сплавах многообразны. Характерные особенности химических соединений, образованных по закону нормальной валентности, приведены ниже.
1. Кристаллическая решетка отличается от решеток компонентов, образующих соединение.
2. В соединении всегда сохраняется простое кратное соотношение компонентов. Это позволяет выразить их состав простой формулой  где А и В — соответствующие элементы;
где А и В — соответствующие элементы;  — простые числа.
— простые числа.
3. Свойства соединения резко отличаются от свойств образующих его компонентов.
4. Температура плавления (диссоциации) постоянная.
5. Образование химического соединения сопровождается значительным тепловым эффектом.
В отличие от твердых растворов химические соединения обычно образуются между компонентами, имеющими большое различие в электронном строении атомов и кристаллических решеток.
В качестве примера типичных химических соединений с нормальной валентностью можно указать на соединения магния с элементами IV—VI групп периодической системы:  и др.
и др.
Соединения одних металлов с другими носят общее название интерметалладову или интерметаллических соединений.
Соединения металла с неметаллом (нитриды, карбиды, гидриды и т. д.), которые могут обладать металлической связью, нередко также называют металлическими соединениями.
Большое число химических соединений, образующихся в металлических сплавах, отличается по некоторым особенностям от типичных химических соединений, так как не подчиняется законам валентности и не имеет постоянного состава.
Ниже будут рассмотрены наиболее важные химические соединения, образующиеся в сплавах.
Фазы внедрения. Переходные металлы  образуют с углеродом, азотом, бором и водородом, т. е. с элементами, имеющими малый атомный радиус, соединения: карбиды, нитриды, бориды и гидриды. Они имеют общность строения и свойств и часто называются фазами внедрения.
образуют с углеродом, азотом, бором и водородом, т. е. с элементами, имеющими малый атомный радиус, соединения: карбиды, нитриды, бориды и гидриды. Они имеют общность строения и свойств и часто называются фазами внедрения.
Фазы внедрения имеют формулу  .
.
Кристаллическая структура фаз внедрения определяется соотношением атомных радиусов неметалла  и металла
и металла  Если
Если  то атомы металла в этих фазах расположены по типу одной из простых кристаллических решеток: кубической
то атомы металла в этих фазах расположены по типу одной из простых кристаллических решеток: кубической  или гексагональной
или гексагональной  в которую внедряются атомы неметалла, занимая в ней определенные поры.
в которую внедряются атомы неметалла, занимая в ней определенные поры.
Фазы внедрения являются фазами переменного состава. Карбиды и нитриды, относящиеся к фазам внедрения, обладают высокой твердостью.
Рассмотренные выше твердые растворы внедрения образуются при значительно меньшей концентрации второго компонента  и имеют решетку металла растворителя, тогда как фазы внедрения получают кристаллическую решетку, отличную от решетки металла.
и имеют решетку металла растворителя, тогда как фазы внедрения получают кристаллическую решетку, отличную от решетки металла.
Если условие  не выполняется, как это наблюдается для карбида железа, марганца и хрома, то образуются соединения с более сложными решетками, и такие соединения нельзя считать фазами внедрения. На базе фаз внедрения легко образуются твердые растворы вычитания, называемые иногда твердыми растворами с дефектной решеткой. В твердых растворах вычитания часть узлов решетки, которые должны быть заняты атомами одного из компонентов, оказываются свободными. В избытке по сравнению со стехиометрическим соотношением
не выполняется, как это наблюдается для карбида железа, марганца и хрома, то образуются соединения с более сложными решетками, и такие соединения нельзя считать фазами внедрения. На базе фаз внедрения легко образуются твердые растворы вычитания, называемые иногда твердыми растворами с дефектной решеткой. В твердых растворах вычитания часть узлов решетки, которые должны быть заняты атомами одного из компонентов, оказываются свободными. В избытке по сравнению со стехиометрическим соотношением  имеется другой компонент.
имеется другой компонент.
Растворы вычитания образуются, например, в карбидах  .
.
Электронные соединения. Эти соединения чаще образуются между одновалентными  металлами или металлами переходных групп
металлами или металлами переходных групп  , с одной стороны,
, с одной стороны,
и простыми металлами с валентностью от 2 до  , с другой стороны. Соединения этого типа имеют определенное отношение числа валентных электронов к числу атомов, т. е. определенную электронную концентрацию. Так, существуют соединения, у которых это отношение в одних случаях равно 3/2 (1,5); в других
, с другой стороны. Соединения этого типа имеют определенное отношение числа валентных электронов к числу атомов, т. е. определенную электронную концентрацию. Так, существуют соединения, у которых это отношение в одних случаях равно 3/2 (1,5); в других  в третьих
в третьих  Каждому из указанных соотношений соответствуют и определенные типы кристаллической решетки.
Каждому из указанных соотношений соответствуют и определенные типы кристаллической решетки.
Все соединения с электронной концентрацией, равной 3/2 (1,48), имеют кубическую объемно центрированную, сложную кубическую или гексагональную решетку и обозначаются как  -соединения. К соединениям этого типа относятся
-соединения. К соединениям этого типа относятся  и др.
и др.
Соединения с электронной концентрацией 21/13 (1,62) имеют сложную решетку и обозначаются  -фазой. К ним относятся соединения
-фазой. К ним относятся соединения  и др.
и др.
Соединения с электронной концентрацией 7/4 (1,75) имеют плотноупакованную гексагональную решетку и обозначаются  -фазой. К ним относятся соединения
-фазой. К ним относятся соединения  и др.
и др.
Электронные соединения подобно обычным химическим соединениям имеют кристаллическую решетку, отличную от решетки образующих их компонентов. Но в отличие от химических соединений с нормальной валентностью электронные соединения образуют с компонентами, из которых они состоят, твердые растворы в широком интервале концентраций.
Фазы Лавеса. Эти фазы имеют формулу  и образуются между компонентами типа А и В при отношении атомных диаметров
и образуются между компонентами типа А и В при отношении атомных диаметров  (чаще
(чаще  Фазы Лавеса имеют плотноупакованную кристаллическую решетку гексагональную
Фазы Лавеса имеют плотноупакованную кристаллическую решетку гексагональную  или гранецентрированную кубическую
или гранецентрированную кубическую  . К фазам Лавеса относятся
. К фазам Лавеса относятся  .
.
Кроме рассмотренных металлических соединений существует и ряд других, например фазы со структурой никельарсенида  а также фазы, обозначаемые
а также фазы, обозначаемые  но о них будет сказано при рассмотрении конкретных сплавов.
но о них будет сказано при рассмотрении конкретных сплавов.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ
- ЧАСТЬ I. МЕТАЛЛОВЕДЕНИЕ И ТЕРМИЧЕСКАЯ ОБРАБОТКА
- ГЛАВА 1. КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ
- 2. АТОМНО-КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА МЕТАЛЛОВ
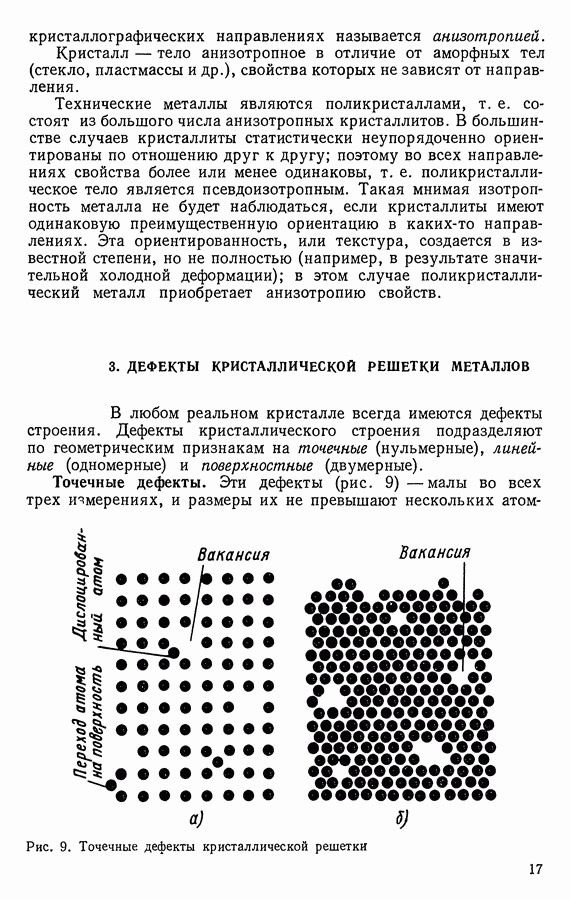
- 3. ДЕФЕКТЫ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ МЕТАЛЛОВ
- ГЛАВА II. ФОРМИРОВАНИЕ СТРУКТУРЫ МЕТАЛЛА ПРИ КРИСТАЛЛИЗАЦИИ
- 2. ГЕТЕРОГЕННОЕ ОБРАЗОВАНИЕ ЗАРОДЫШЕЙ
- 3. СТРОЕНИЕ МЕТАЛЛИЧЕСКОГО СЛИТКА
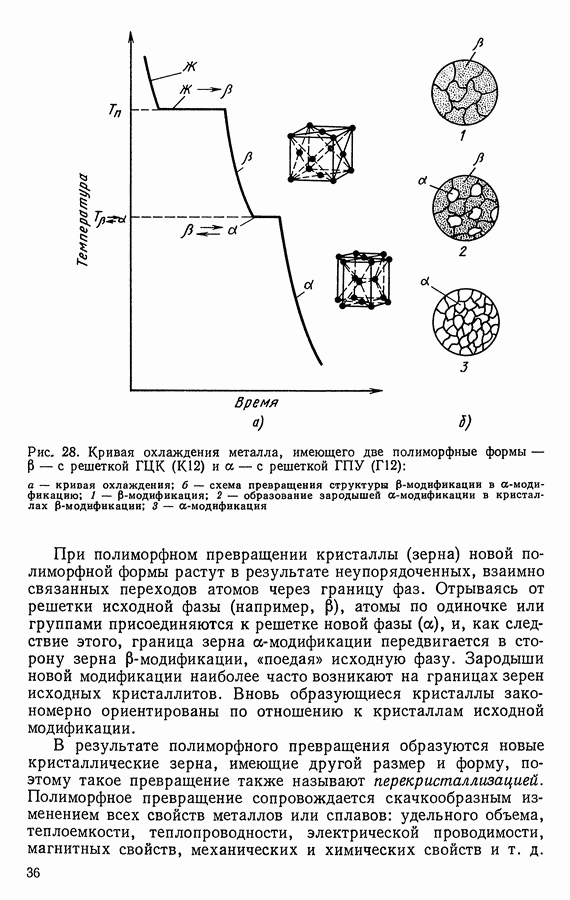
- 4. ПОЛИМОРФНЫЕ ПРЕВРАЩЕНИЯ
- ГЛАВА III. ФАЗЫ И СТРУКТУРА В МЕТАЛЛИЧЕСКИХ СПЛАВАХ
- 2. ХИМИЧЕСКИЕ СОЕДИНЕНИЯ
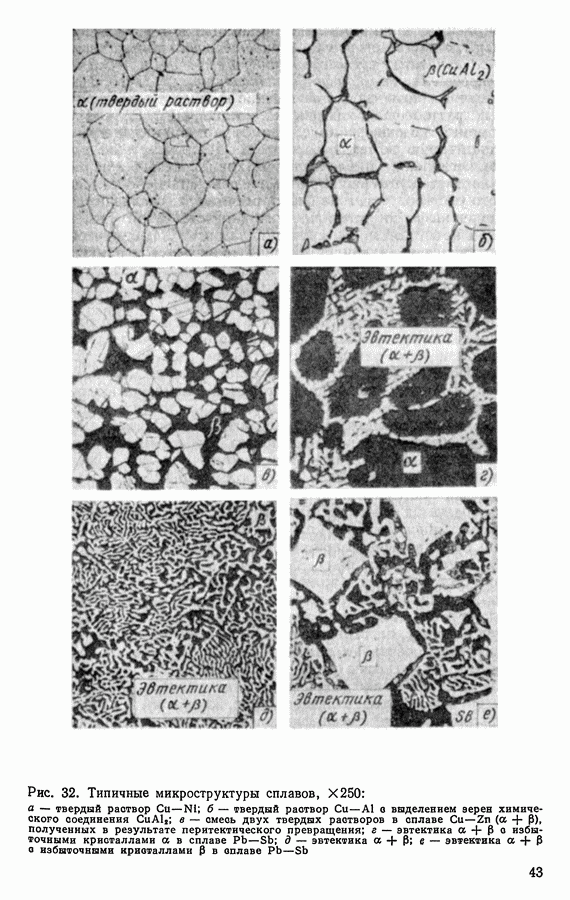
- 3. СТРУКТУРА СПЛАВОВ
- ГЛАВА IV. ФОРМИРОВАНИЕ СТРУКТУРЫ СПЛАВОВ ПРИ КРИСТАЛЛИЗАЦИИ
- 2. ДИАГРАММЫ ФАЗОВОГО РАВНОВЕСИЯ
- 3. ДИАГРАММА СОСТОЯНИЯ СПЛАВОВ, ОБРАЗУЮЩИХ НЕОГРАНИЧЕННЫЕ ТВЕРДЫЕ РАСТВОРЫ
- 4. ДИАГРАММЫ СОСТОЯНИЯ СПЛАВОВ, ОБРАЗУЮЩИХ ОГРАНИЧЕННЫЕ ТВЕРДЫЕ РАСТВОРЫ
- 5. ДИАГРАММЫ СОСТОЯНИЯ СПЛАВОВ, КОМПОНЕНТЫ КОТОРЫХ ИМЕЮТ ПОЛИМОРФНЫЕ ПРЕВРАЩЕНИЯ
- 6. ПОНЯТИЕ О ДИАГРАММАХ СОСТОЯНИЯ ТРОЙНЫХ СПЛАВОВ
- ГЛАВА V. ДЕФОРМАЦИЯ И РАЗРУШЕНИЕ МЕТАЛЛОВ
- 2. УПРУГАЯ И ПЛАСТИЧЕСКАЯ ДЕФОРМАЦИИ МЕТАЛЛОВ
- 3. СВЕРХПЛАСТИЧНОСТЬ МЕТАЛЛОВ И СПЛАВОВ
- 4. РАЗРУШЕНИЕ МЕТАЛЛОВ
- ГЛАВА VI. ВЛИЯНИЕ НАГРЕВА НА СТРУКТУРУ И СВОЙСТВА ДЕФОРМИРОВАННОГО МЕТАЛЛА
- 2. РЕКРИСТАЛЛИЗАЦИЯ
- 3. ХОЛОДНАЯ И ГОРЯЧАЯ ДЕФОРМАЦИИ
- ГЛАВА VII. МЕХАНИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ
- 2. МЕХАНИЧЕСКИЕ СВОЙСТВА, ОПРЕДЕЛЯЕМЫЕ ПРИ СТАТИЧЕСКИХ ИСПЫТАНИЯХ
- 3. ТВЕРДОСТЬ МЕТАЛЛОВ
- 4. МЕХАНИЧЕСКИЕ СВОЙСТВА, ОПРЕДЕЛЯЕМЫЕ ПРИ ДИНАМИЧЕСКИХ ИСПЫТАНИЯХ
- 5. МЕХАНИЧЕСКИЕ СВОЙСТВА ПРИ ПЕРЕМЕННЫХ (ЦИКЛИЧЕСКИХ) НАГРУЗКАХ
- 6. ИЗНАШИВАНИЕ МЕТАЛЛОВ
- 7. ПУТИ ПОВЫШЕНИЯ ПРОЧНОСТИ МЕТАЛЛОВ
- ГЛАВА VIII. ЖЕЛЕЗО И СПЛАВЫ НА ЕГО ОСНОВЕ
- 2. ДИАГРАММА СОСТОЯНИЯ ЖЕЛЕЗО — ЦЕМЕНТИТ (МЕТАСТАБИЛЬНОЕ РАВНОВЕСИЕ)
- 3. ДИАГРАММА СОСТОЯНИЯ ЖЕЛЕЗО — ГРАФИТ (СТАБИЛЬНОЕ РАВНОВЕСИЕ)
- 4. ВЛИЯНИЕ УГЛЕРОДА И ПОСТОЯННЫХ (ТЕХНОЛОГИЧЕСКИХ) ПРИМЕСЕЙ НА СВОЙСТВА СТАЛИ
- 5. ЛЕГИРУЮЩИЕ ЭЛЕМЕНТЫ В СТАЛИ
- 6. СТРУКТУРНЫЕ КЛАССЫ ЛЕГИРОВАННЫХ СТАЛЕЙ
- ГЛАВА IX. ЧУГУН
- 1. СЕРЫЙ И БЕЛЫЙ ЧУГУНЫ
- 2. ВЫСОКОПРОЧНЫЙ ЧУГУН С ШАРОВИДНЫМ ГРАФИТОМ
- 3. КОВКИЙ ЧУГУН
- 4. СПЕЦИАЛЬНЫЕ ЧУГУНЫ
- ГЛАВА X. ФАЗОВЫЕ ПРЕВРАЩЕНИЯ В СПЛАВАХ ЖЕЛЕЗА (ТЕОРИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ)
- 2. РОСТ ЗЕРНА АУСТЕНИТА ПРИ НАГРЕВЕ
- 3. ОБЩАЯ ХАРАКТЕРИСТИКА ПРЕВРАЩЕНИЯ ПЕРЕОХЛАЖДЕННОГО АУСТЕНИТА (ДИАГРАММА ИЗОТЕРМИЧЕСКОГО ПРЕВРАЩЕНИЯ АУСТЕНИТА)
- 4. ПЕРЛИТНОЕ ПРЕВРАЩЕНИЕ
- 5. МАРТЕНСИТНОЕ ПРЕВРАЩЕНИЕ В СТАЛИ
- 6. ПРОМЕЖУТОЧНОЕ (БЕЙНИТНОЕ) ПРЕВРАЩЕНИЕ
- 7. ИЗОТЕРМИЧЕСКОЕ ПРЕВРАЩЕНИЕ АУСТЕНИТА В ЛЕГИРОВАННЫХ СТАЛЯХ
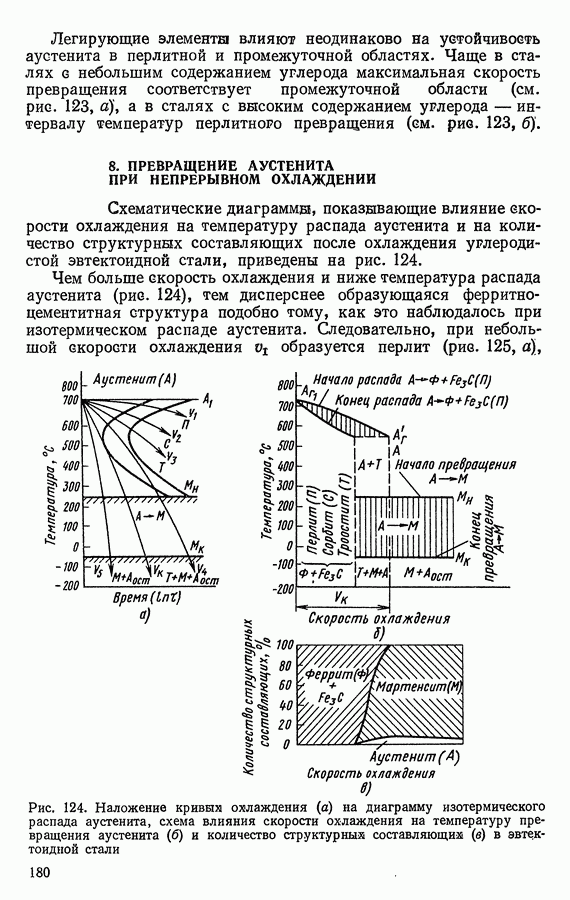
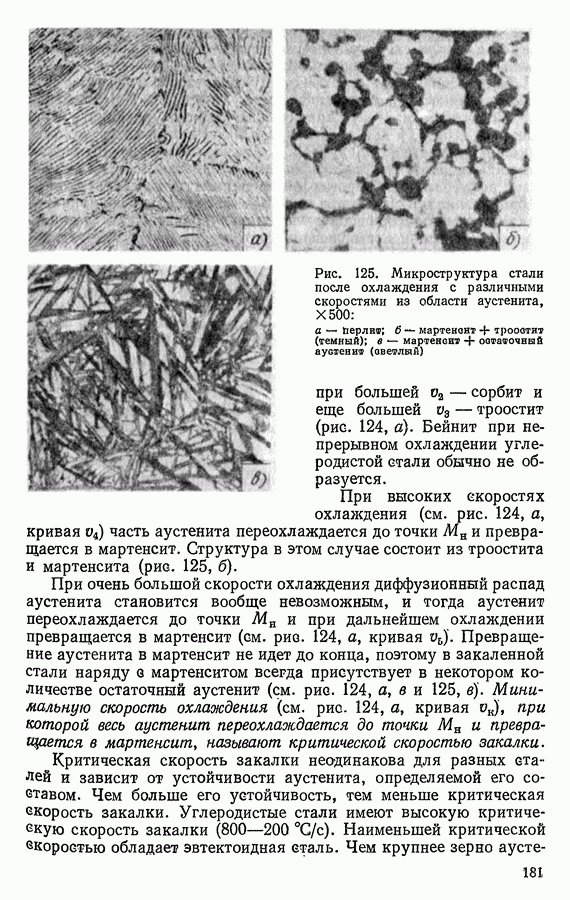
- 8. ПРЕВРАЩЕНИЕ АУСТЕНИТА ПРИ НЕПРЕРЫВНОМ ОХЛАЖДЕНИИ
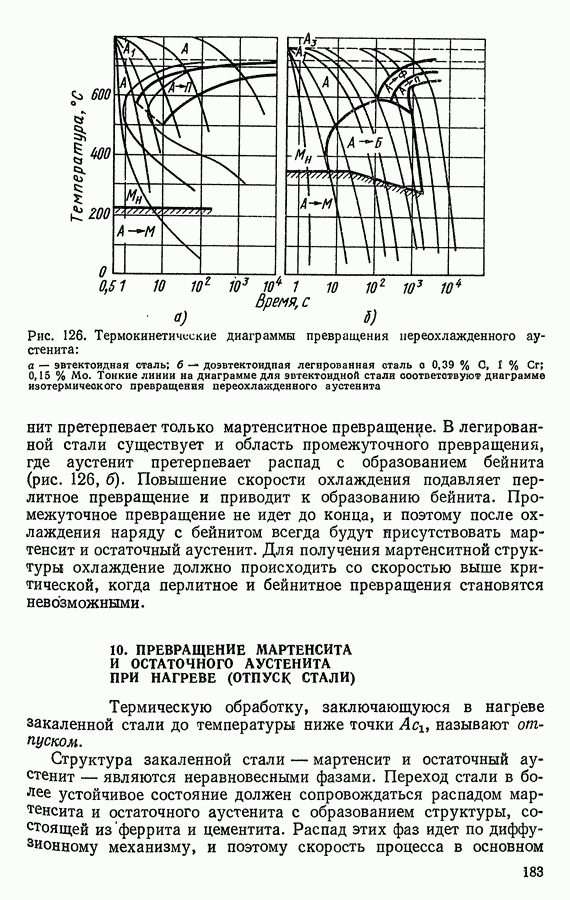
- 9. ТЕРМОКИНЕТИЧЕСКИЕ ДИАГРАММЫ ПРЕВРАЩЕНИЯ ПЕРЕОХЛАЖДЕННОГО АУСТЕНИТА
- 10. ПРЕВРАЩЕНИЕ МАРТЕНСИТА И ОСТАТОЧНОГО АУСТЕНИТА ПРИ НАГРЕВЕ (ОТПУСК СТАЛИ)
- 11. ТЕРМИЧЕСКОЕ И ДЕФОРМАЦИОННОЕ СТАРЕНИЕ УГЛЕРОДИСТОЙ СТАЛИ
- ГЛАВА XI. ТЕХНОЛОГИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ
- 2. ОТЖИГ II РОДА (ФАЗОВАЯ ПЕРЕКРИСТАЛЛИЗАЦИЯ)
- 3. ЗАКАЛКА
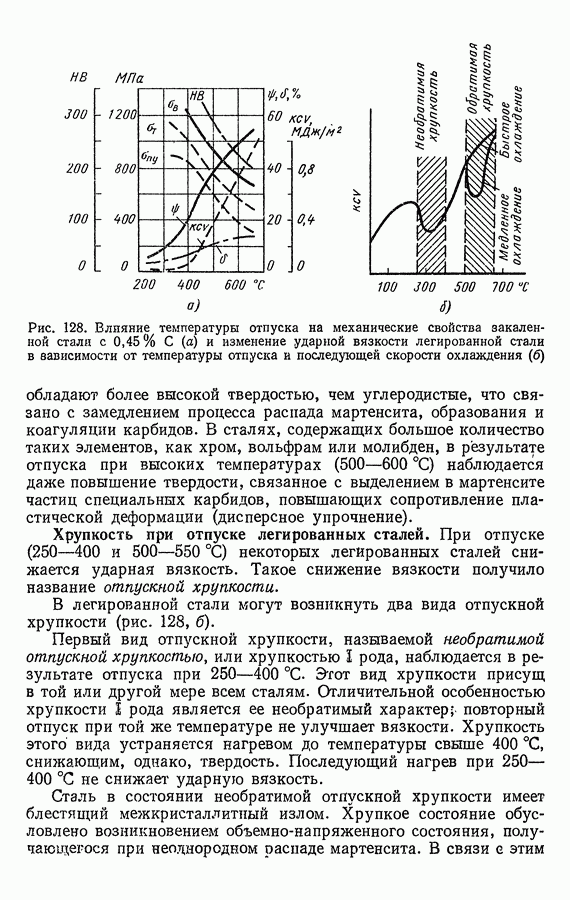
- 4. ОТПУСК
- 5. ТЕРМОМЕХАНИЧЕСКАЯ ОБРАБОТКА (ТМО)
- 6. ДЕФЕКТЫ, ВОЗНИКАЮЩИЕ ПРИ ТЕРМИЧЕСКОЙ ОБРАБОТКЕ СТАЛИ
- 7. ПОВЕРХНОСТНАЯ ЗАКАЛКА
- ГЛАВА XII. ХИМИКО-ТЕРМИЧЕСКАЯ ОБРАБОТКА СТАЛИ
- 1. ЦЕМЕНТАЦИЯ
- 2. НИТРОЦЕМЕНТАЦИЯ
- 3. АЗОТИРОВАНИЕ
- 4. ЦИАНИРОВАНИЕ
- 5. БОРИРОВАНИЕ
- 6. СИЛИЦИРОВАНИЕ
- 7. ДИФФУЗИОННОЕ НАСЫЩЕНИЕ МЕТАЛЛАМИ
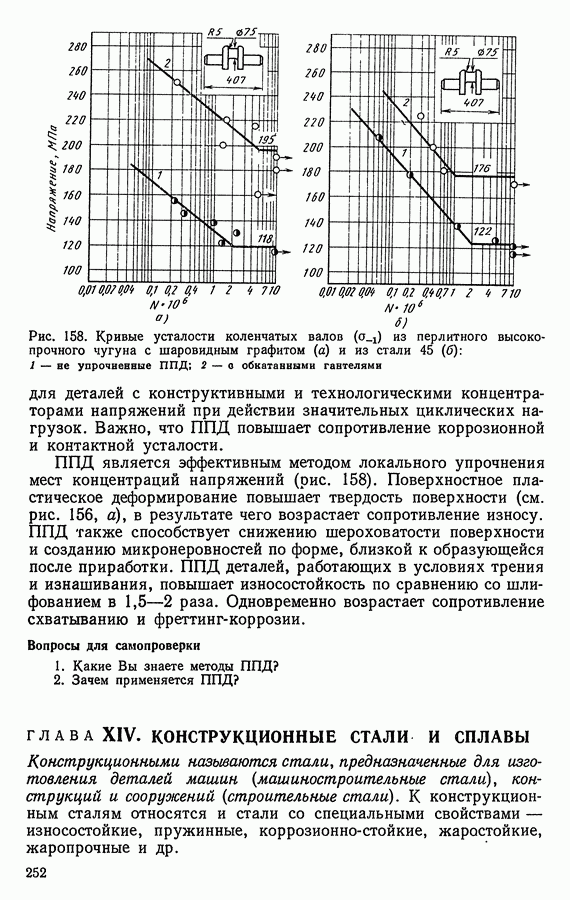
- ГЛАВА XIII. ПОВЕРХНОСТНАЯ ПЛАСТИЧЕСКАЯ ДЕФОРМАЦИЯ
- ГЛАВА XIV. КОНСТРУКЦИОННЫЕ СТАЛИ И СПЛАВЫ
- 1. УГЛЕРОДИСТЫЕ КОНСТРУКЦИОННЫЕ СТАЛИ
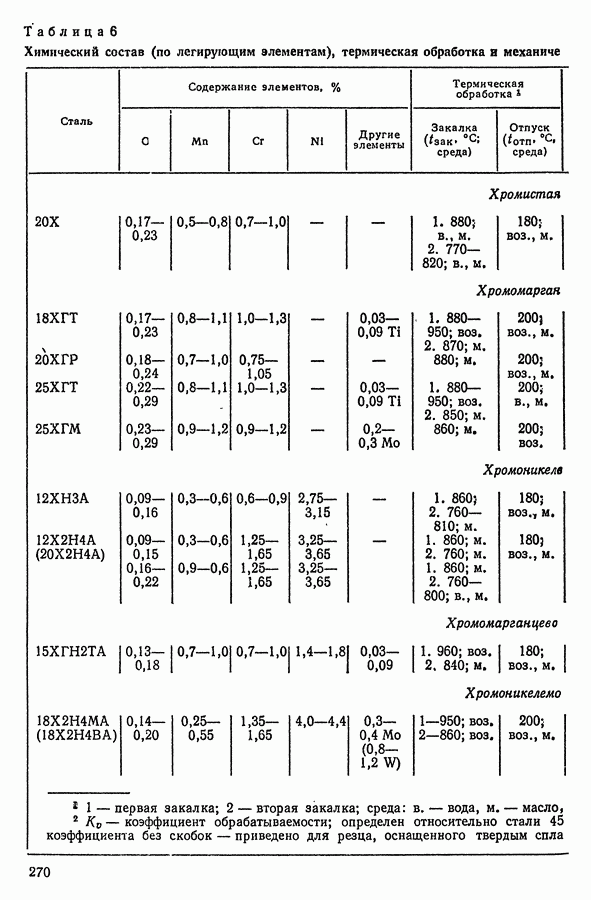
- 2. ЛЕГИРОВАННЫЕ КОНСТРУКЦИОННЫЕ СТАЛИ
- 3. СТРОИТЕЛЬНЫЕ НИЗКОЛЕГИРОВАННЫЕ СТАЛИ
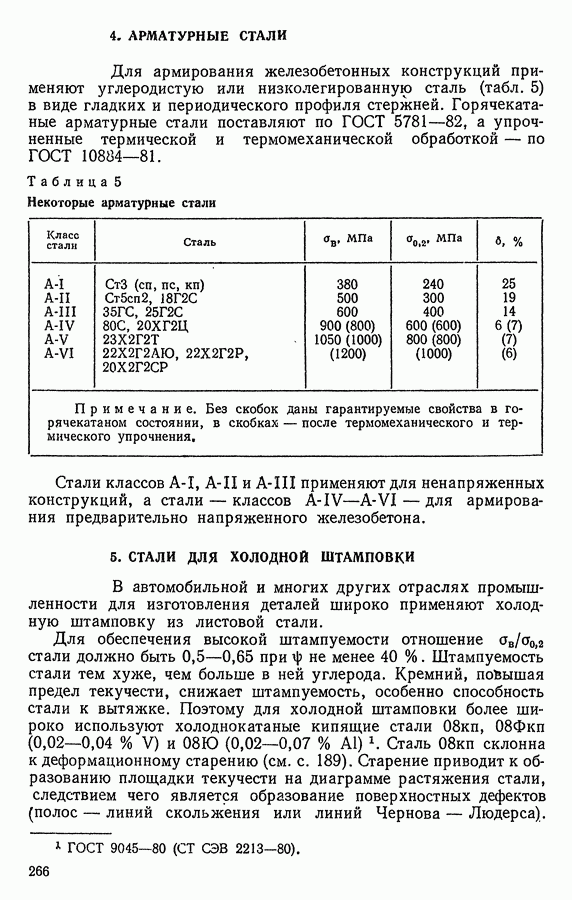
- 4. АРМАТУРНЫЕ СТАЛИ
- 5. СТАЛИ ДЛЯ ХОЛОДНОЙ ШТАМПОВКИ
- 6. КОНСТРУКЦИОННЫЕ (МАШИНОСТРОИТЕЛЬНЫЕ) ЦЕМЕНТУЕМЫЕ (НИТРОЦЕМЕНТУЕМЫЕ) ЛЕГИРОВАННЫЕ СТАЛИ
- 7. КОНСТРУКЦИОННЫЕ (МАШИНОСТРОИТЕЛЬНЫЕ) УЛУЧШАЕМЫЕ ЛЕГИРОВАННЫЕ СТАЛИ
- 8. СТАЛИ С ПОВЫШЕННОЙ ОБРАБАТЫВАЕМОСТЬЮ РЕЗАНИЕМ
- 9. МАРТЕНСИТНО-СТАРЕЮЩИЕ ВЫСОКОПРОЧНЫЕ СТАЛИ
- 10. ВЫСОКОПРОЧНЫЕ СТАЛИ С ВЫСОКОЙ ПЛАСТИЧНОСТЬЮ (ТРИП-ИЛИ ПИП-СТАЛИ)
- 11. РЕССОРНО-ПРУЖИННЫЕ СТАЛИ ОБЩЕГО НАЗНАЧЕНИЯ
- 12. ШАРИКОПОДШИПНИКОВЫЕ СТАЛИ
- 13. ИЗНОСОСТОЙКИЕ СТАЛИ
- 14. КОРРОЗИОННО-СТОЙКИЕ И ЖАРОСТОЙКИЕ СТАЛИ И СПЛАВЫ
- 15. КРИОГЕННЫЕ СТАЛИ
- 16. ЖАРОПРОЧНЫЕ СТАЛИ И СПЛАВЫ
- ГЛАВА XV. ОСНОВЫ РАЦИОНАЛЬНОГО ВЫБОРА СТАЛИ (ЧУГУНА) И МЕТОДОВ УПРОЧНЕНИЯ ДЕТАЛЕЙ МАШИН
- 2. ПРИМЕРЫ ТЕРМИЧЕСКОЙ И ХИМИКО-ТЕРМИЧЕСКОЙ ОБРАБОТКИ ДЕТАЛЕЙ МАШИН
- 3. УПРОЧНЕНИЕ ПОВЕРХНОСТНЫМ ПЛАСТИЧЕСКИМ ДЕФОРМИРОВАНИЕМ
- 4. ИЗНОСОСТОЙКИЕ И КОРРОЗИОННО-СТОЙКИЕ ПОКРЫТИЯ
- ГЛАВА XVI. ИНСТРУМЕНТАЛЬНЫЕ СТАЛИ И ТВЕРДЫЕ СПЛАВЫ
- 1. СТАЛИ ДЛЯ РЕЖУЩЕГО ИНСТРУМЕНТА
- 2. СТАЛИ ДЛЯ ИЗМЕРИТЕЛЬНОГО ИНСТРУМЕНТА
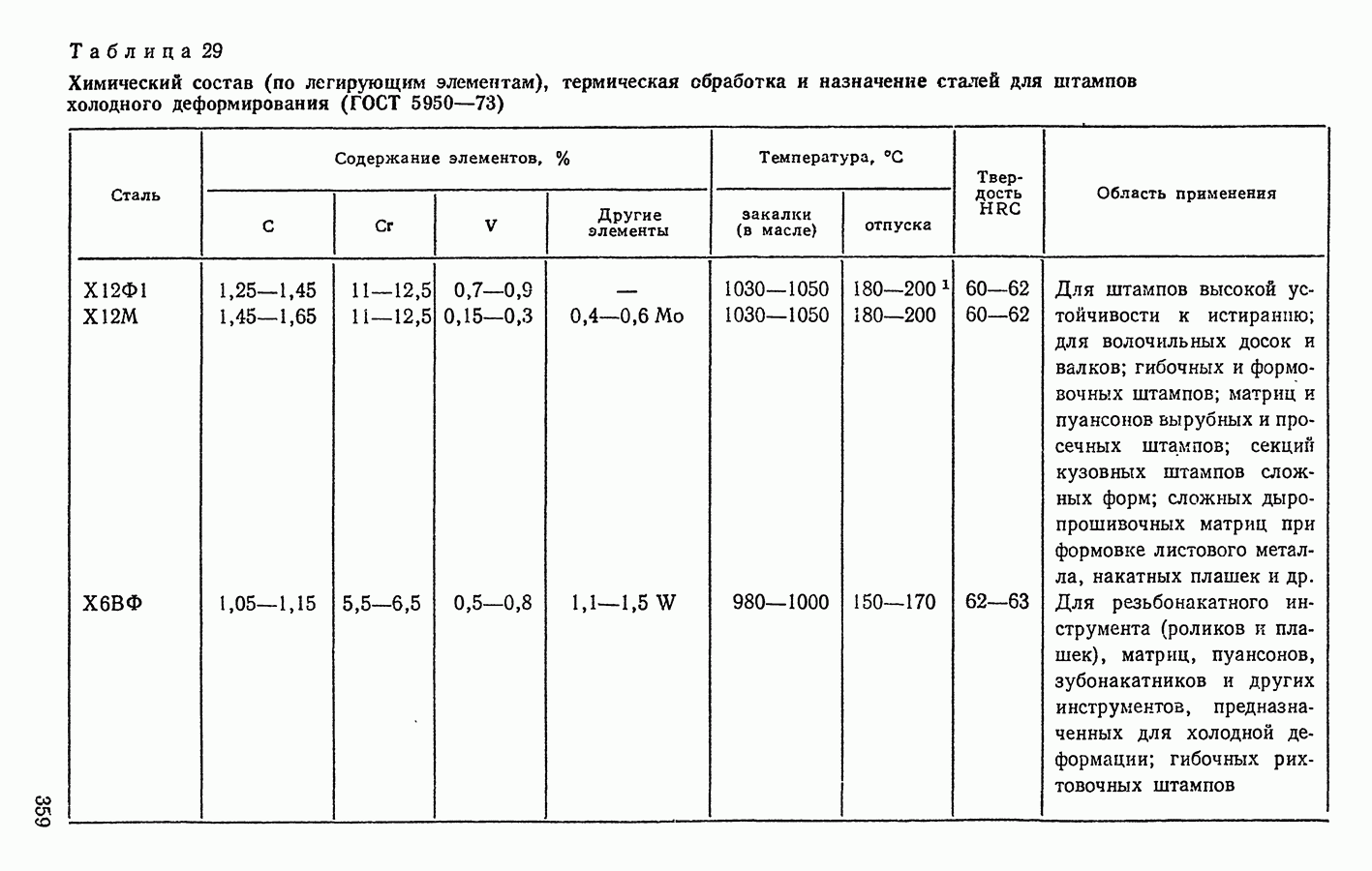
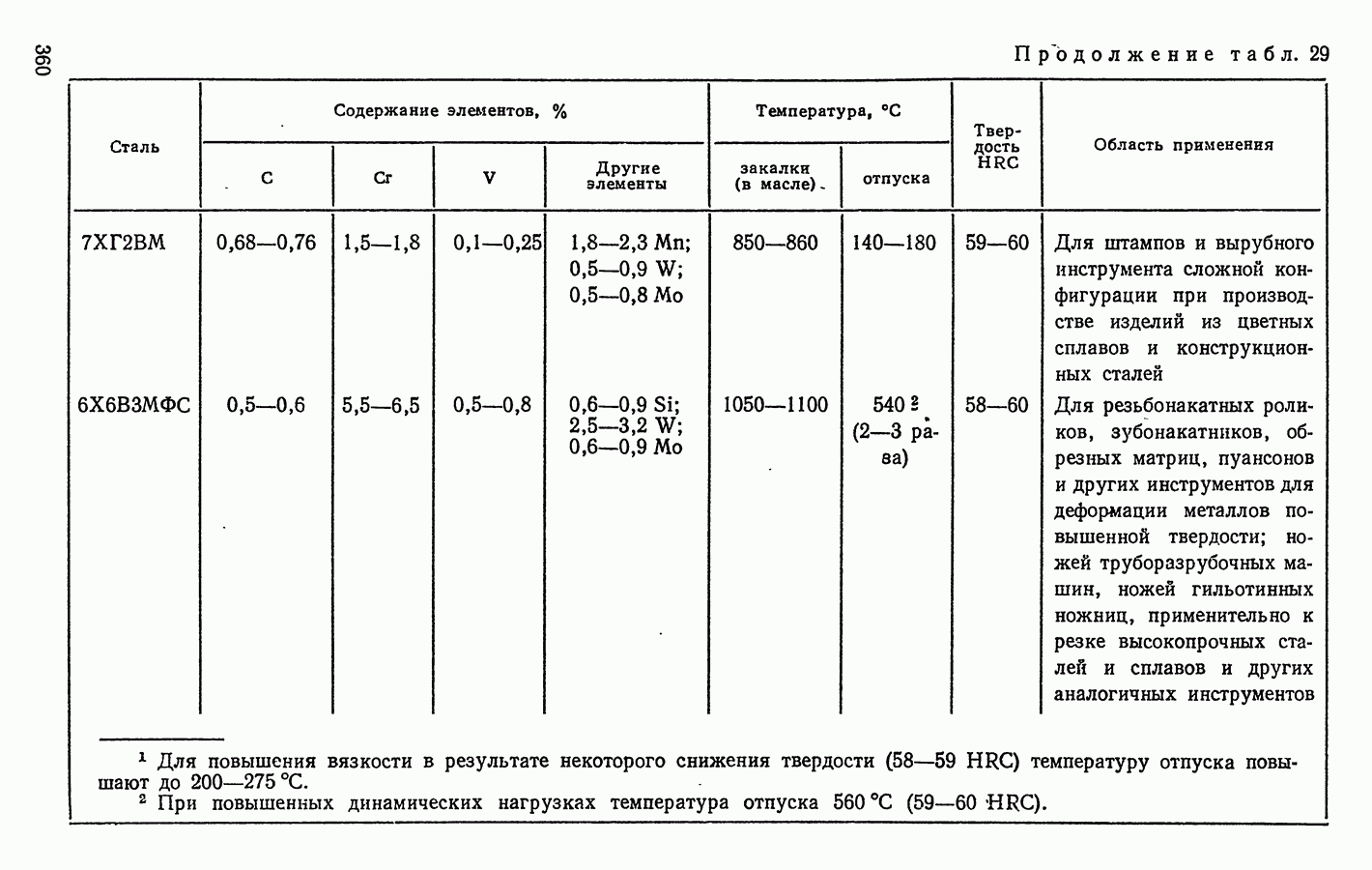
- 3. СТАЛИ ДЛЯ ШТАМПОВ ХОЛОДНОГО ДЕФОРМИРОВАНИЯ
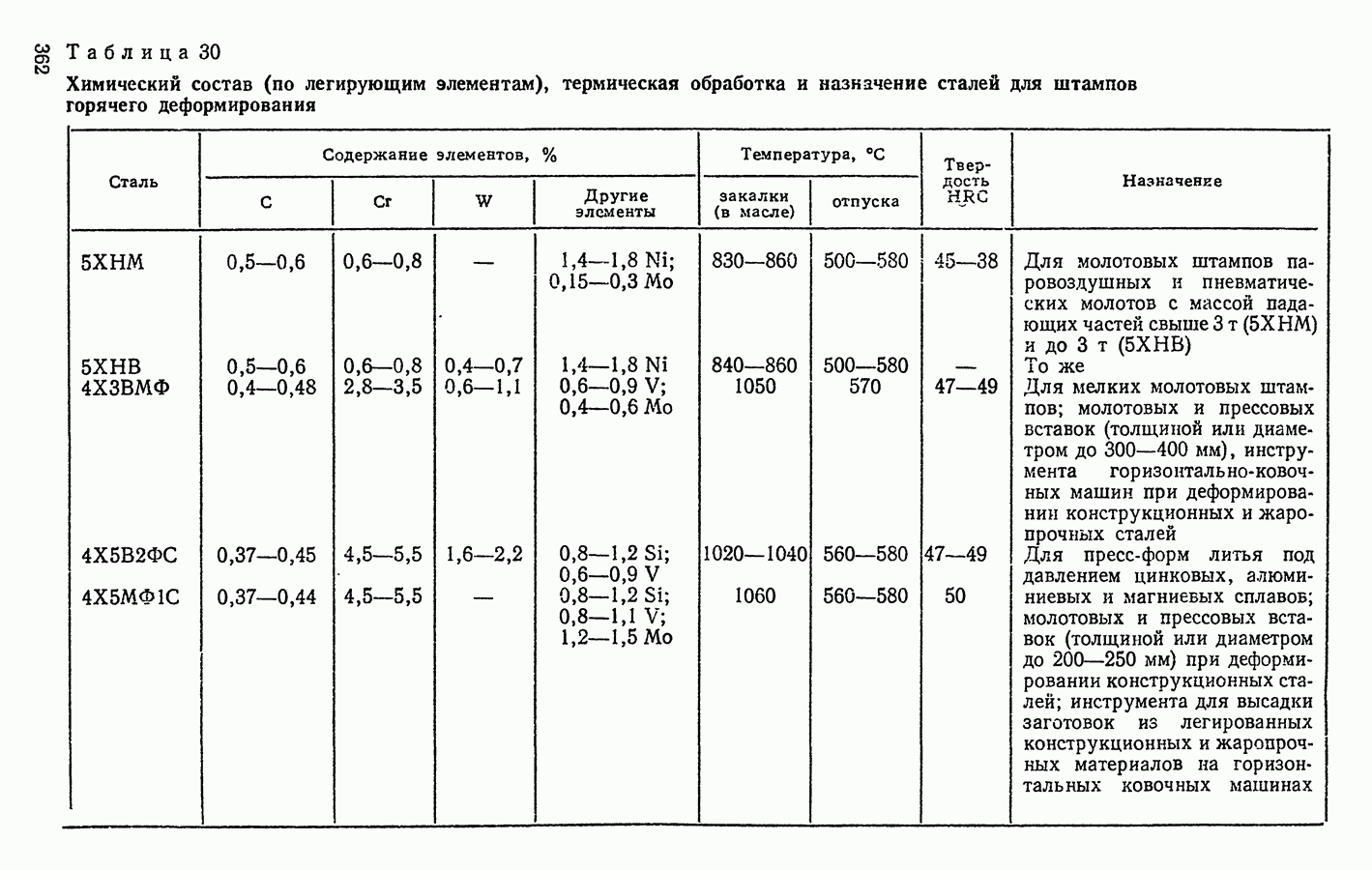
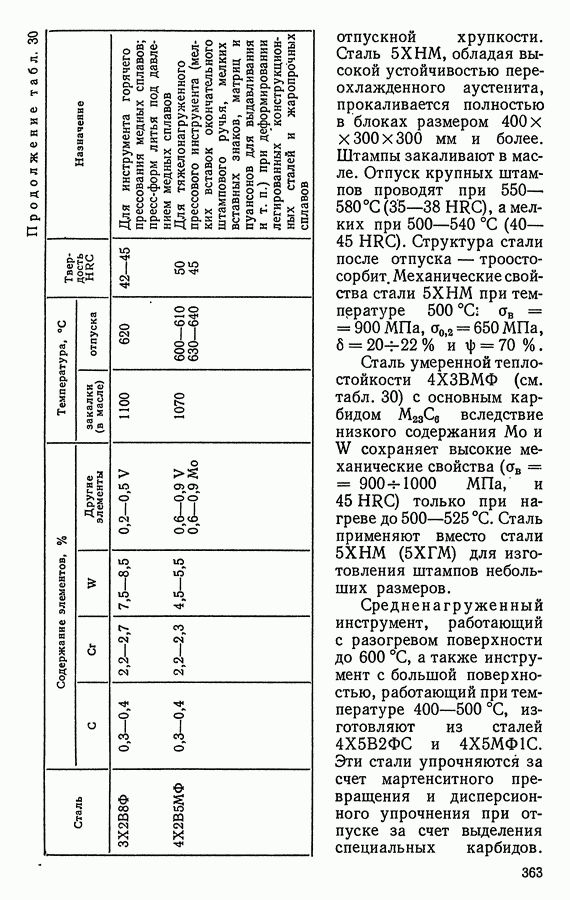
- 4. СТАЛИ ДЛЯ ШТАМПОВ ГОРЯЧЕГО ДЕФОРМИРОВАНИЯ
- 5. ТВЕРДЫЕ СПЛАВЫ
- ГЛАВА XVII. СТАЛИ И СПЛАВЫ С ОСОБЫМИ ФИЗИЧЕСКИМИ СВОЙСТВАМИ
- 2. МЕТАЛЛИЧЕСКИЕ СТЕКЛА (АМОРФНЫЕ СПЛАВЫ)
- 3. СТАЛИ И СПЛАВЫ С ВЫСОКИМ ЭЛЕКТРИЧЕСКИМ СОПРОТИВЛЕНИЕМ ДЛЯ НАГРЕВАТЕЛЬНЫХ ЭЛЕМЕНТОВ
- 4. СПЛАВЫ С ЗАДАННЫМ ТЕМПЕРАТУРНЫМ КОЭФФИЦИЕНТОМ ЛИНЕЙНОГО РАСШИРЕНИЯ
- 5. СПЛАВЫ С ЭФФЕКТОМ «ПАМЯТИ ФОРМЫ»
- ГЛАВА XVIII. ТУГОПЛАВКИЕ МЕТАЛЛЫ И ИХ СПЛАВЫ
- ГЛАВА XIX. ТИТАН И СПЛАВЫ НА ЕГО ОСНОВЕ
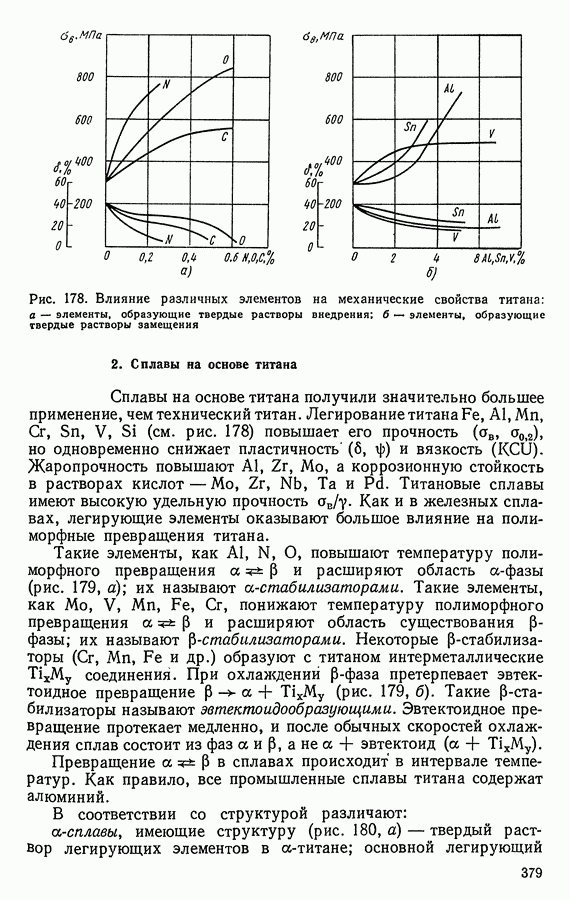
- 2. Сплавы на основе титана
- ГЛАВА XX. АЛЮМИНИЙ И СПЛАВЫ НА ЕГО ОСНОВЕ
- 2. КЛАССИФИКАЦИЯ АЛЮМИНИЕВЫХ СПЛАВОВ
- 3. ТЕРМИЧЕСКАЯ ОБРАБОТКА АЛЮМИНИЕВЫХ СПЛАВОВ
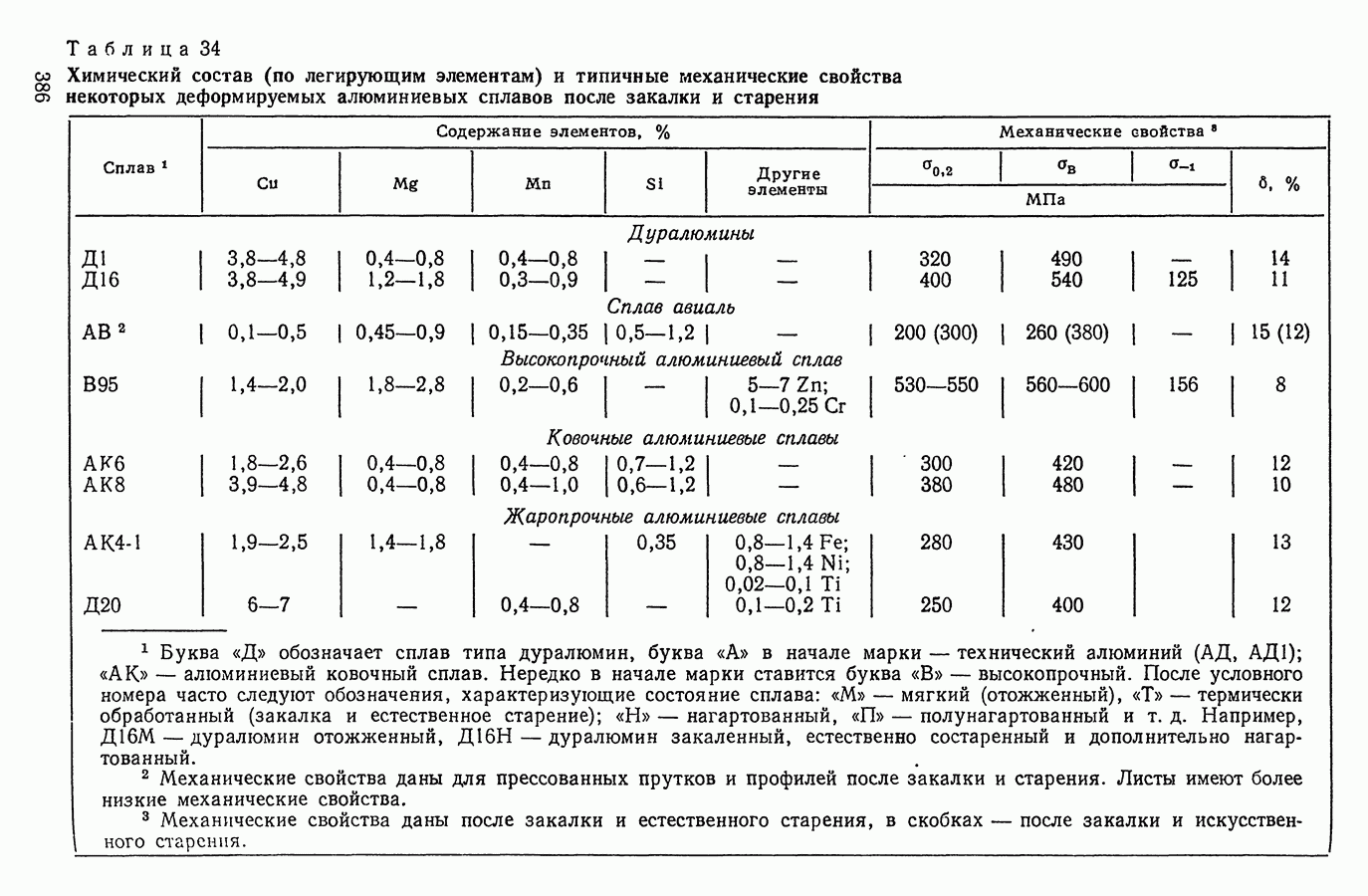
- 4. ДЕФОРМИРУЕМЫЕ АЛЮМИНИЕВЫЕ СПЛАВЫ, УПРОЧНЯЕМЫЕ ТЕРМИЧЕСКОЙ ОБРАБОТКОЙ
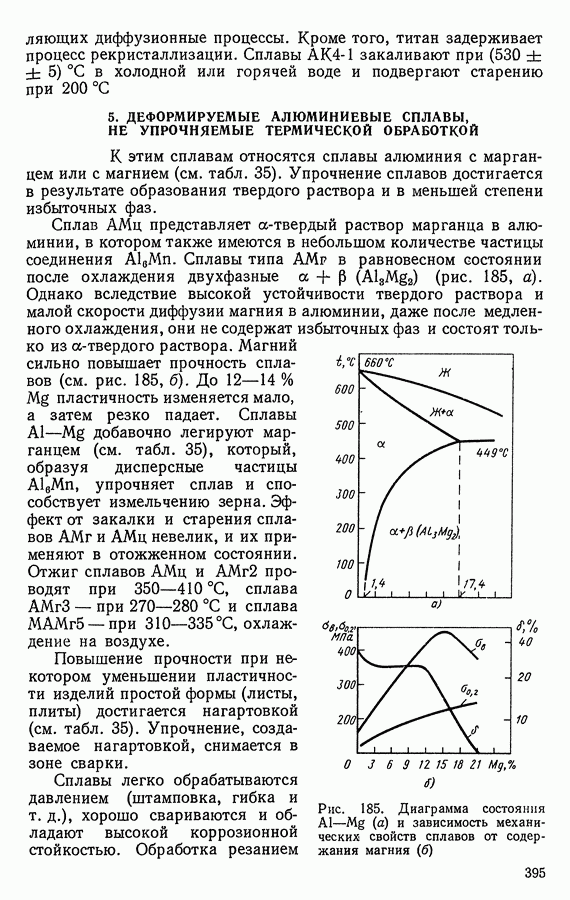
- 5. ДЕФОРМИРУЕМЫЕ АЛЮМИНИЕВЫЕ СПЛАВЫ, НЕ УПРОЧНЯЕМЫЕ ТЕРМИЧЕСКОЙ ОБРАБОТКОЙ
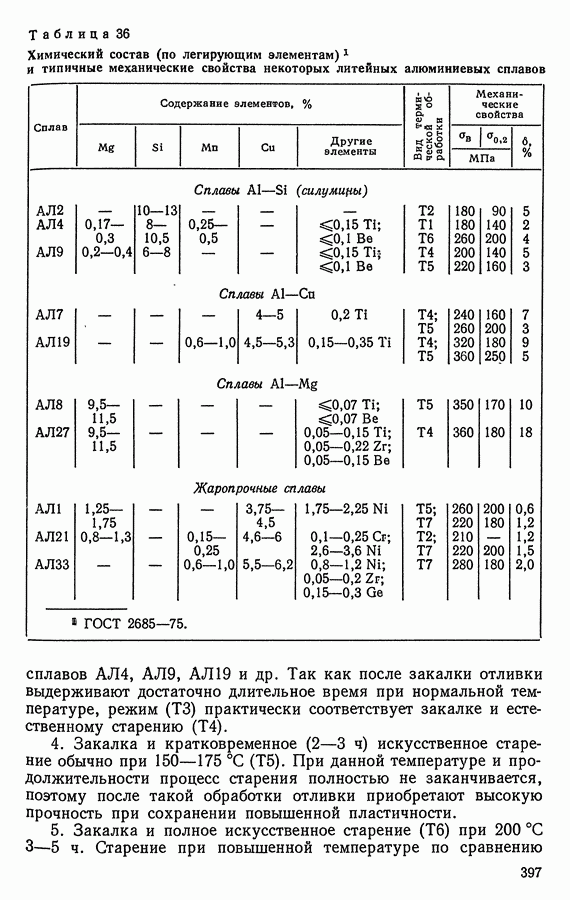
- 6. ЛИТЕЙНЫЕ АЛЮМИНИЕВЫЕ СПЛАВЫ
- ГЛАВА XXI. МАГНИЙ И СПЛАВЫ НА ЕГО ОСНОВЕ
- ГЛАВА XXII. МЕДЬ И СПЛАВЫ НА ЕЕ ОСНОВЕ
- 2. СПЛАВЫ НА ОСНОВЕ МЕДИ
- ГЛАВА XXIII. АНТИФРИКЦИОННЫЕ (ПОДШИПНИКОВЫЕ) СПЛАВЫ НА ОЛОВЯННОЙ, СВИНЦОВОЙ, ЦИНКОВЫЙ И АЛЮМИНИЕВОЙ ОСНОВАХ
- ГЛАВА XXIV. КОМПОЗИЦИОННЫЕ МАТЕРИАЛЫ С МЕТАЛЛИЧЕСКОЙ МАТРИЦЕЙ
- ГЛАВА XXV. КОНСТРУКЦИОННЫЕ ПОРОШКОВЫЕ МАТЕРИАЛЫ
- ЧАСТЬ II. НЕМЕТАЛЛИЧЕСКИЕ МАТЕРИАЛЫ
- ГЛАВА XXVI. ОБЩИЕ СВЕДЕНИЯ О НЕМЕТАЛЛИЧЕСКИХ МАТЕРИАЛАХ
- 2. ОСОБЕННОСТИ СВОЙСТВ ПОЛИМЕРНЫХ МАТЕРИАЛОВ
- ГЛАВА XXVII. ПЛАСТИЧЕСКИЕ МАССЫ
- 1. СОСТАВ, КЛАССИФИКАЦИЯ И СВОЙСТВА ПЛАСТМАСС
- 2. ТЕРМОПЛАСТИЧНЫЕ ПЛАСТМАССЫ
- 3. ТЕРМОРЕАКТИВНЫЕ ПЛАСТМАССЫ
- 4. ГАЗОНАПОЛНЕННЫЕ ПЛАСТМАССЫ
- 5. ЭКОНОМИЧЕСКАЯ ЭФФЕКТИВНОСТЬ ПРИМЕНЕНИЯ ПЛАСТМАСС
- ГЛАВА XXVIII. КОМПОЗИЦИОННЫЕ МАТЕРИАЛЫ С НЕМЕТАЛЛИЧЕСКОЙ МАТРИЦЕЙ
- 1. ОБЩИЕ СВЕДЕНИЯ, СОСТАВ И КЛАССИФИКАЦИЯ
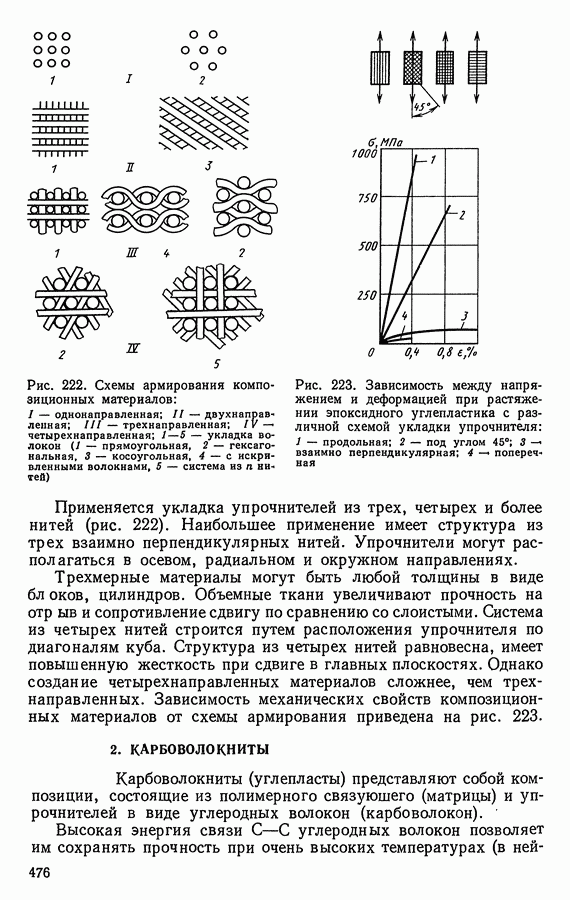
- 2. КАРБОВОЛОКНИТЫ
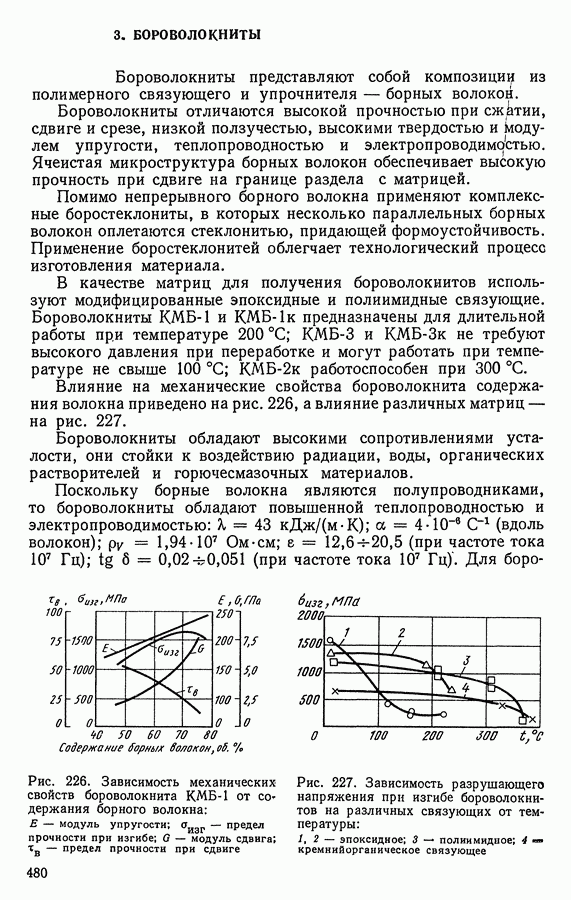
- 3. БОРОВОЛОКНИТЫ
- 4. ОРГАНОВОЛОКНИТЫ
- ГЛАВА XXIX. РЕЗИНОВЫЕ МАТЕРИАЛЫ
- 2. РЕЗИНЫ ОБЩЕГО НАЗНАЧЕНИЯ
- 3. РЕЗИНЫ СПЕЦИАЛЬНОГО НАЗНАЧЕНИЯ
- 4. ВЛИЯНИЕ ФАКТОРОВ ЭКСПЛУАТАЦИИ НА СВОЙСТВА РЕЗИН
- ГЛАВА XXX. КЛЕЯЩИЕ МАТЕРИАЛЫ И ГЕРМЕТИКИ
- 1. ОБЩИЕ СВЕДЕНИЯ, СОСТАВ И КЛАССИФИКАЦИЯ ПЛЕНКООБРАЗУЮЩИХ МАТЕРИАЛОВ
- 2. КОНСТРУКЦИОННЫЕ СМОЛЯНЫЕ И РЕЗИНОВЫЕ КЛЕИ
- 3. НЕОРГАНИЧЕСКИЕ КЛЕИ
- 4. СВОЙСТВА КЛЕЕВЫХ СОЕДИНЕНИЙ
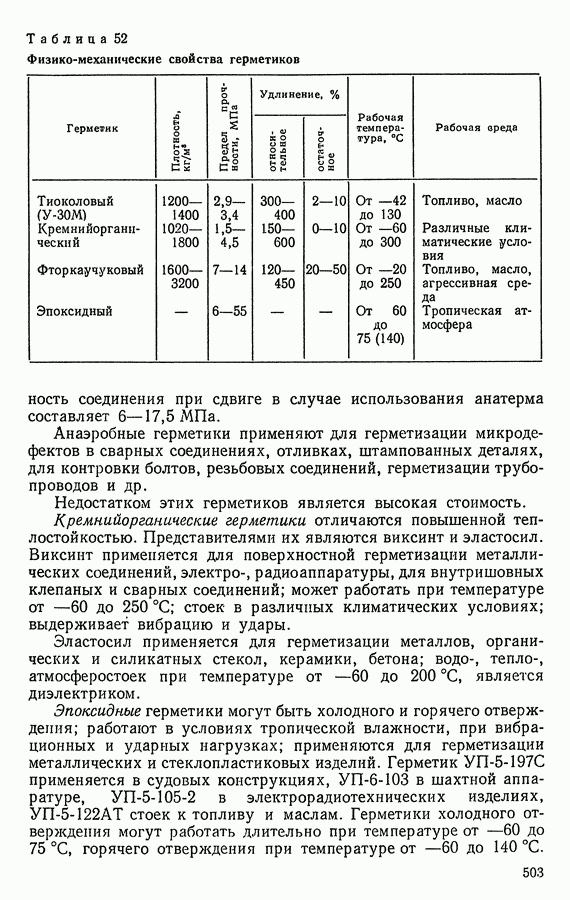
- 5. ГЕРМЕТИКИ
- ГЛАВА XXXI. НЕОРГАНИЧЕСКИЕ МАТЕРИАЛЫ
- 2. НЕОРГАНИЧЕСКОЕ СТЕКЛО
- 3. СИТАЛЛЫ (СТЕКЛОКРИСТАЛЛИЧЕСКИЕ МАТЕРИАЛЫ)
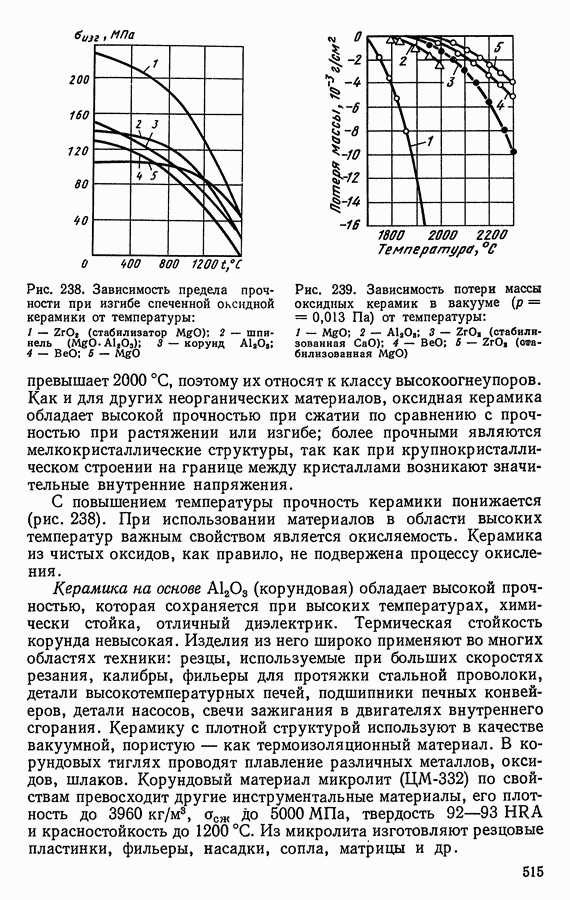
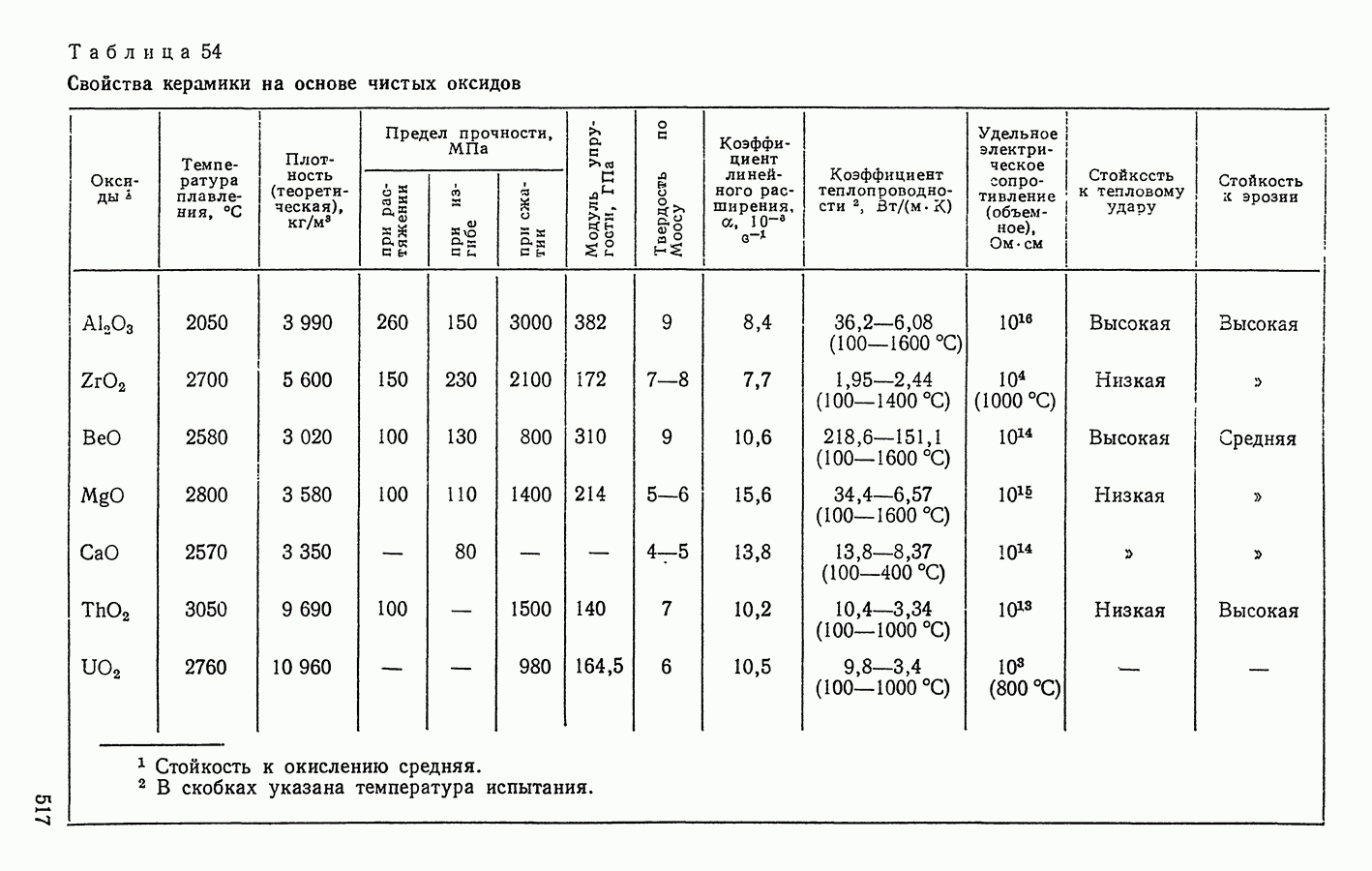
- 4. КЕРАМИЧЕСКИЕ МАТЕРИАЛЫ