| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
3. ДИАГРАММА СОСТОЯНИЯ СПЛАВОВ, ОБРАЗУЮЩИХ НЕОГРАНИЧЕННЫЕ ТВЕРДЫЕ РАСТВОРЫ
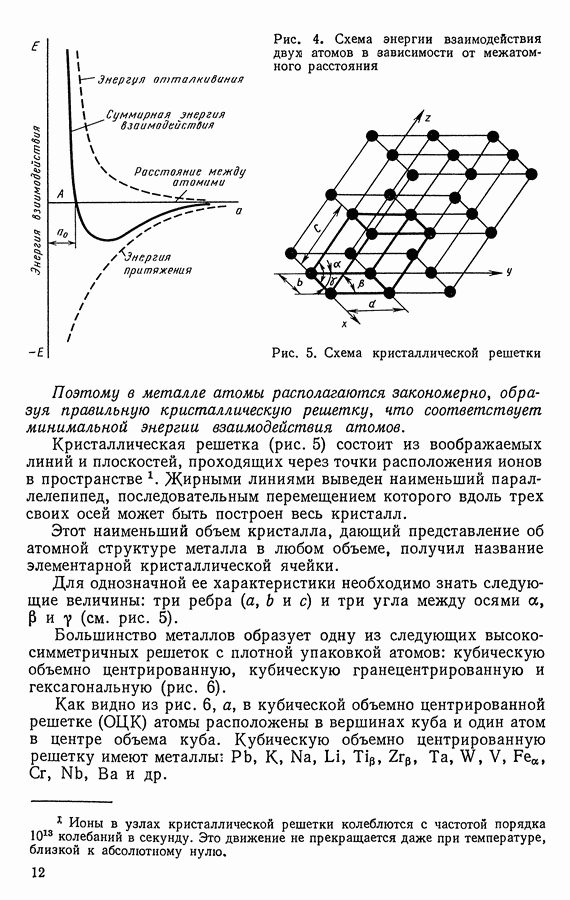
Диаграмма состояния для случая полной взаимной растворимости компонентов А и В в жидком и твердом состояниях и изменение энергии Гиббса в зависимости от концентрации и температуры даны на рис. 35.
При температуре выше линии  называемой линией ликвидус, существует только жидкая фаза
называемой линией ликвидус, существует только жидкая фаза  В этой области (рис. 35, б) энергия Гиббса жидкой фазы
В этой области (рис. 35, б) энергия Гиббса жидкой фазы  меньше энергии Гиббса твердого раствора
меньше энергии Гиббса твердого раствора  состоящего из компонентов А и В.
состоящего из компонентов А и В.
В области ниже линии  называемой линией солидус, устойчив
называемой линией солидус, устойчив  -твердый раствор, так как его энергия Гиббса
-твердый раствор, так как его энергия Гиббса  меньше, чем энергия Гиббса жидкой фазы
меньше, чем энергия Гиббса жидкой фазы  (рис. 35, г).
(рис. 35, г).
Между линиями ликвидус и солидус в равновесии находятся жидкая фаза и  -твердый раствор. При температуре
-твердый раствор. При температуре  (рис. 35, а, в) энергия Гиббса меняется с изменением состава по линии
(рис. 35, а, в) энергия Гиббса меняется с изменением состава по линии  . В интервале
. В интервале  (см рис. 35, а) устойчив жидкий раствор, а в интервале
(см рис. 35, а) устойчив жидкий раствор, а в интервале  -твердый раствор. В интервале
-твердый раствор. В интервале  равновесным является двухфазное состояние: жидкость состава точки а
равновесным является двухфазное состояние: жидкость состава точки а  и кристаллы а состава точки
и кристаллы а состава точки  . Энергия Гиббса этих сплавов определяется прямой
. Энергия Гиббса этих сплавов определяется прямой  являющейся отрезком общей касательной
являющейся отрезком общей касательной

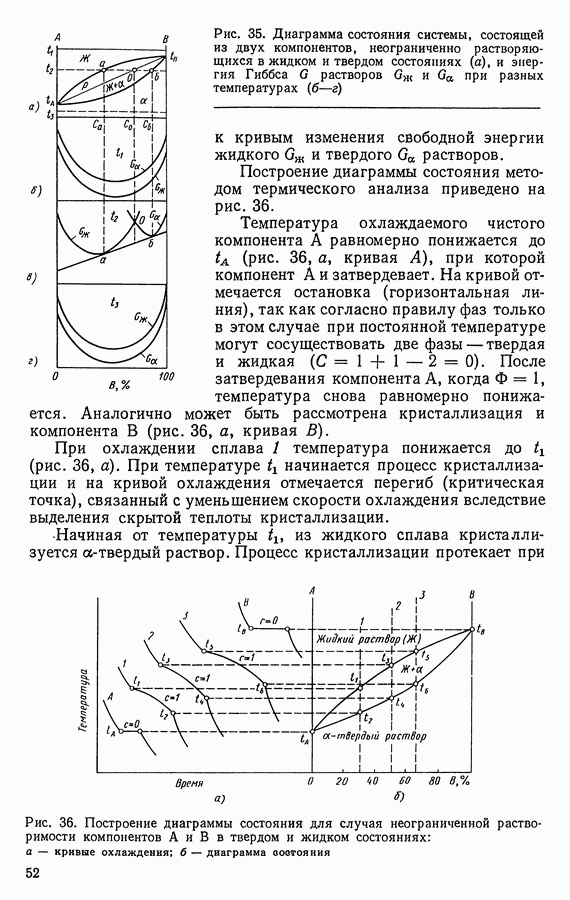
Рис. 35. Диаграмма состояния системы, состоящей из двух компонентов, неограниченно растворяющихся в жидком и твердом состояниях (а), и энергия Гиббса  растворов
растворов  при разных температурах (б-г)
при разных температурах (б-г)
к кривым изменения свободной энергии жидкого  и твердого
и твердого  растворов.
растворов.
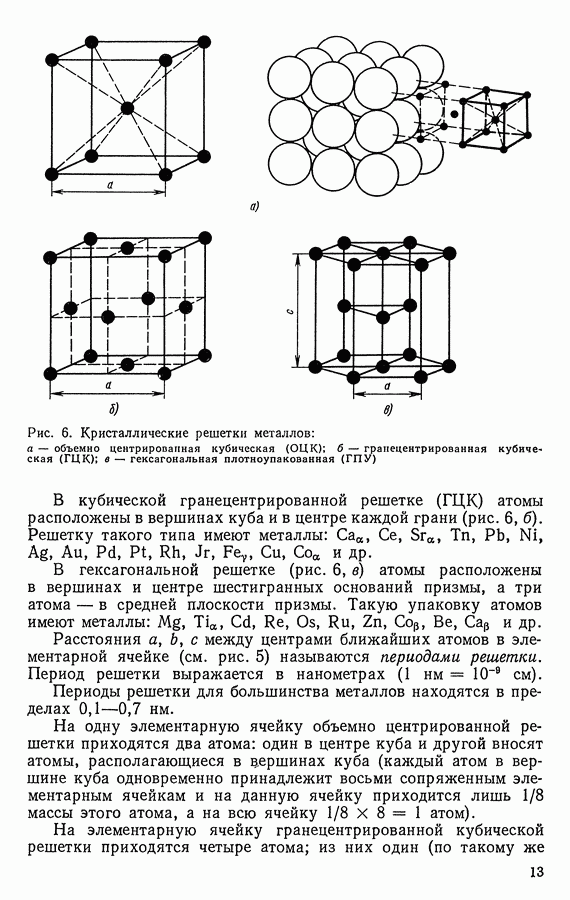
Построение диаграммы состояния методом термического анализа приведено на рис. 36.
Температура охлаждаемого чистого компонента А равномерно понижается до  (рис. 36, а, кривая А), при которой компонент А и затвердевает. На кривой отмечается остановка (горизонтальная линия), так как согласно правилу фаз только в этом случае при постоянной температуре могут сосуществовать две фазы — твердая и жидкая
(рис. 36, а, кривая А), при которой компонент А и затвердевает. На кривой отмечается остановка (горизонтальная линия), так как согласно правилу фаз только в этом случае при постоянной температуре могут сосуществовать две фазы — твердая и жидкая  После затвердевания компонента А, когда
После затвердевания компонента А, когда  температура снова равномерно понижается. Аналогично может быть рассмотрена кристаллизация и компонента В (рис. 36, а, кривая В).
температура снова равномерно понижается. Аналогично может быть рассмотрена кристаллизация и компонента В (рис. 36, а, кривая В).
При охлаждении сплава 1 температура понижается до  (рис. 36, а). При температуре
(рис. 36, а). При температуре  начинается процесс кристаллизации и на кривой охлаждения отмечается перегиб (критическая точка), связанный с уменьшением скорости охлаждения вследствие выделения скрытой теплоты кристаллизации.
начинается процесс кристаллизации и на кривой охлаждения отмечается перегиб (критическая точка), связанный с уменьшением скорости охлаждения вследствие выделения скрытой теплоты кристаллизации.
Начиная от температуры  из жидкого сплава кристаллизуется
из жидкого сплава кристаллизуется  -твердый раствор. Процесс кристаллизации протекает при
-твердый раствор. Процесс кристаллизации протекает при

Рис. 36. Построение диаграммы состояния для случая неограниченной растворимости компонентов А и В в твердом и жидком состояниях: а — кривые охлаждения;  — диаграмма состояния
— диаграмма состояния

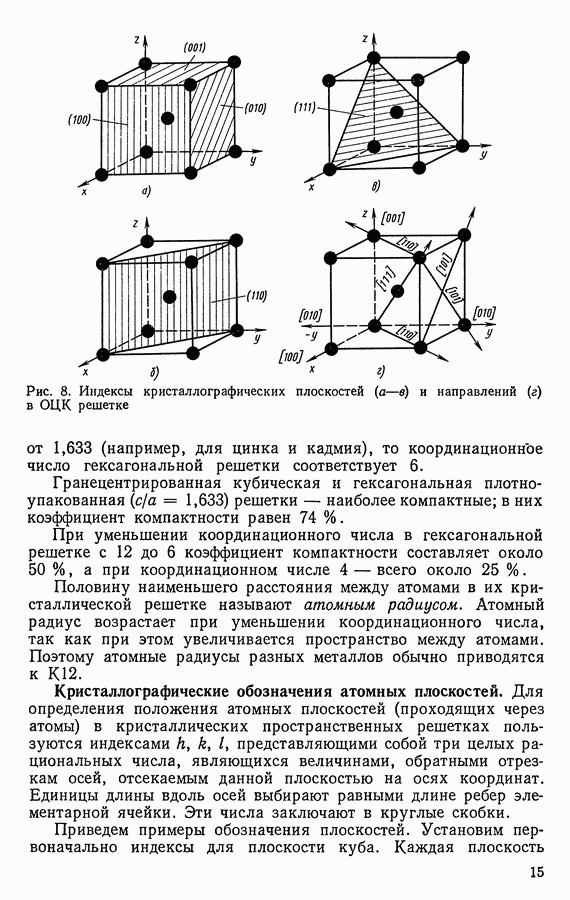
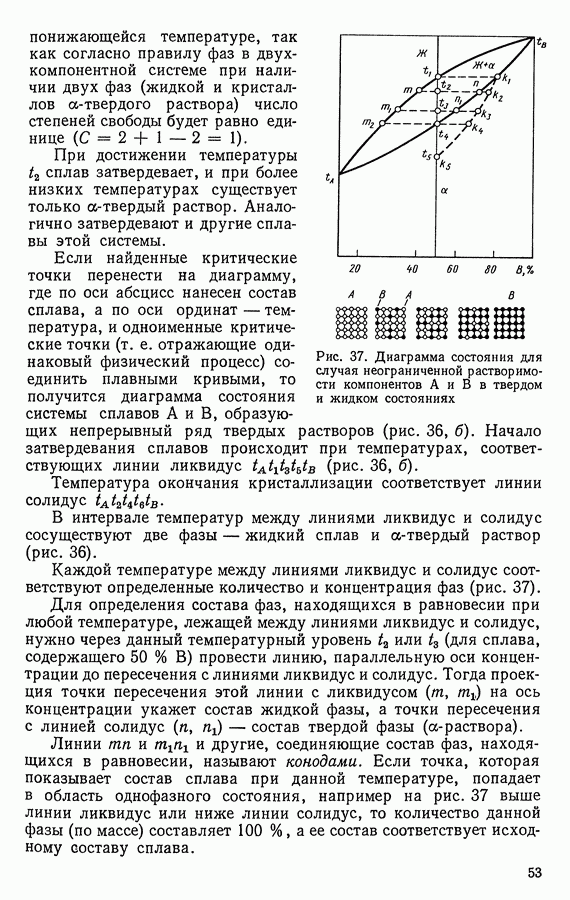
Рис. 37. Диаграмма состояния для случая неограниченной растворимости компонентов А и В в твердом и жидком состояниях
понижающейся температуре, так как согласно правилу фаз в двухкомпонентной системе при наличии двух фаз (жидкой и кристаллов  -твердого раствора) число степеней свободы будет равно единице
-твердого раствора) число степеней свободы будет равно единице 
При достижении температуры  сплав затвердевает, и при более низких температурах существует только а-твердый раствор. Аналогично затвердевают и другие сплавы этой системы.
сплав затвердевает, и при более низких температурах существует только а-твердый раствор. Аналогично затвердевают и другие сплавы этой системы.
Если найденные критические точки перенести на диаграмму, где по оси абсцисс нанесен состав сплава, а по оси ординат — температура, и одноименные критические точки (т. е. отражающие одинаковый физический процесс) соединить плавными кривыми, то получится диаграмма состояния системы сплавов А и В, образующих непрерывный ряд твердых растворов (рис. 36, б). Начало затвердевания сплавов происходит при температурах, соответствующих линии ликвидус  (рис. 36, б).
(рис. 36, б).
Температура окончания кристаллизации соответствует линии солидус 
В интервале температур между линиями ликвидус и солидус сосуществуют две фазы — жидкий сплав и  -твердый раствор (рис. 36).
-твердый раствор (рис. 36).
Каждой температуре между линиями ликвидус и солидус соответствуют определенные количество и концентрация фаз (рис. 37).
Для определения состава фаз, находящихся в равновесии при любой температуре, лежащей между линиями ликвидус и солидус, нужно через данный температурный уровень  или
или  (для сплава, содержащего
(для сплава, содержащего  провести линию, параллельную оси концентрации до пересечения с линиями ликвидус и солидус. Тогда проекция точки пересечения этой линии с ликвидусом
провести линию, параллельную оси концентрации до пересечения с линиями ликвидус и солидус. Тогда проекция точки пересечения этой линии с ликвидусом  на ось концентрации укажет состав жидкой фазы, а точки пересечения с линией солидус
на ось концентрации укажет состав жидкой фазы, а точки пересечения с линией солидус  — состав твердой фазы (
— состав твердой фазы ( -раствор а).
-раствор а).
Линии  и
и  и другие, соединяющие состав фаз, находящихся в равновесии, называют конодами. Если точка, которая показывает состав сплава при данной температуре, попадает в область однофазного состояния, например на рис. 37 выше линии ликвидус или ниже линии солидус, то количество данной фазы (по массе) составляет
и другие, соединяющие состав фаз, находящихся в равновесии, называют конодами. Если точка, которая показывает состав сплава при данной температуре, попадает в область однофазного состояния, например на рис. 37 выше линии ликвидус или ниже линии солидус, то количество данной фазы (по массе) составляет  а ее состав соответствует исходному составу сплава.
а ее состав соответствует исходному составу сплава.
В процессе кристаллизации изменяется не только состав фаз, но и количественное соотношение между ними. Для определения количественного соотношения фаз, находящихся в равновесии при данной температуре, пользуются правилом отрезков (рычага). Согласно этому правилу, например, для определения массового или объемного количества твердой фазы необходимо вычислить отношение длины отрезка, примыкающего к составу жидкой фазы, к длине всей коноды; для определения количества жидкой фазы — отношение длины отрезка, примыкающего к составу твердой фазы, к длине коноды. Следовательно, количество твердой фазы а (в процентах) при температуре определяется отношением отрезка  к длине коноды
к длине коноды  а масса или объем жидкой фазы
а масса или объем жидкой фазы  .
.
Выделяющиеся кристаллы твердого раствора имеют переменный состав, зависящий от температуры. Однако при медленном охлаждении процессы диффузии в жидкой и твердой фазах (объемная диффузия), а также процессы взаимной диффузии между ними (межфазная диффузия) успевают за процессом кристаллизации, поэтому состав кристаллов выравнивается. В этих условиях сплав после затвердевания будет состоять из однородных кристаллических зерен твердого раствора (см. рис. 31, а), а их состав будет соответствовать исходному составу сплава.
Неравновесная кристаллизация. Процесс диффузии протекает медленно, поэтому в реальных условиях охлаждения состав в пределах каждого кристалла и разных кристаллов не успевает выравниваться и будет неодинаковым.
Неоднородные по составу кристаллы твердого раствора можно характеризовать средней концентрацией, которая на рис. 37 лежит справа от линии солидус.
Рассмотрим сплав, содержащий 50 % компонента В, начинающий затвердевать при температуре  при которой образуются кристаллы а; состав их соответствует точке
при которой образуются кристаллы а; состав их соответствует точке 
При температуре  состав жидкой фазы будет соответствовать точке
состав жидкой фазы будет соответствовать точке  , а а-фазы — точке
, а а-фазы — точке  Но отдельные части кристаллов
Но отдельные части кристаллов  -фазы, которые образовались при температурах, превышающих температуру
-фазы, которые образовались при температурах, превышающих температуру  не изменили своего начального состава, и средний состав кристаллов будет соответствовать точке
не изменили своего начального состава, и средний состав кристаллов будет соответствовать точке  При понижении температуры средний состав кристаллов
При понижении температуры средний состав кристаллов  -твердого раствора все более отклоняется от равновесного. При температуре
-твердого раствора все более отклоняется от равновесного. При температуре  он будет соответствовать не точке
он будет соответствовать не точке  , а точке
, а точке  Если через точки
Если через точки  провести кривую, она будет характеризовать средний состав кристаллов
провести кривую, она будет характеризовать средний состав кристаллов  -фазы при данной скорости охлаждения. При температуре в условиях равновесия фаз выбранный сплав должен затвердеть. В неравновесных условиях этого не произойдет,
-фазы при данной скорости охлаждения. При температуре в условиях равновесия фаз выбранный сплав должен затвердеть. В неравновесных условиях этого не произойдет,

Рис. 38. Микроструктура твердого раствора  : а — после литья; б - после деформации и гомогенизации
: а — после литья; б - после деформации и гомогенизации
так как в сплаве останется жидкая фаза, количество которой определяется из соотношения 100. Сплав окончательно затвердевает тогда, когда средний состав  -фазы будет соответствовать составу взятого сплава. Это произойдет при температуре
-фазы будет соответствовать составу взятого сплава. Это произойдет при температуре  (точка
(точка  при которой периферийные зоны кристаллов будут иметь состав, отвечающий 50 % компонента В (рис. 37). Следовательно, в неравновесных условиях сплав затвердевает ниже равновесной температуры затвердевания. Линию
при которой периферийные зоны кристаллов будут иметь состав, отвечающий 50 % компонента В (рис. 37). Следовательно, в неравновесных условиях сплав затвердевает ниже равновесной температуры затвердевания. Линию  называют неравновесный солидус. Каждый сплав при заданной скорости охлаждения характеризуется своим неравновесным солидусом.
называют неравновесный солидус. Каждый сплав при заданной скорости охлаждения характеризуется своим неравновесным солидусом.
Дендритная (внутрикристаллитная) ликвация. В результате неравновесной кристаллизации химический состав образующихся кристаллов а-твердого раствора по сечению оказывается переменным.
В процессе кристаллизации обычно образуются кристаллы твердого раствора дендритного типа, поэтому оси первого порядка, возникающие в начальный момент кристаллизации, обогащены более тугоплавким компонентом В. Периферийные слои кристалла и межосные пространства, кристаллизующиеся в последнюю очередь, будут обогащены компонентом А, понижающим температуру плавления сплава, и их состав близок к концентрации, соответствующей исходной концентрации сплава. Такую неоднородность состава сплава внутри отдельных кристаллов называют внутрикристаллитной, или дендритной, ликвацией. Чем больше разность температур между солидусом и ликвидусом, тем больше дифференциация по составу между жидкой и твердойфазами и тем сильнее проявляется этот вид ликвации. Быстрое охлаждение способствует развитию дендритной ликвации. Вследствие разной травимости участков твердого раствора, имеющих неодинаковый состав,
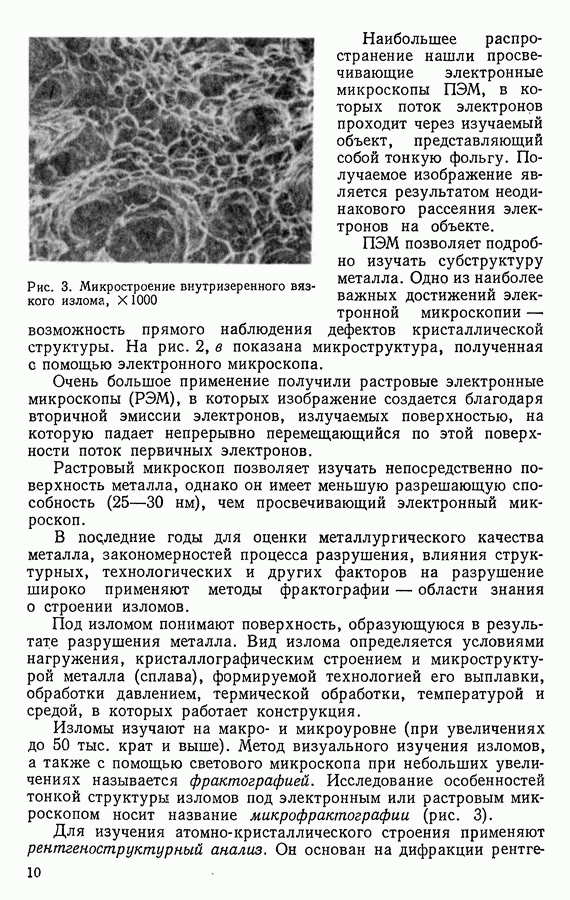
неоднородность внутри каждого кристалла может быть легко выявлена при микроанализе (рис. 38, а). Дендритная ликвация ухудшает технологические и механические свойства сплавов.
Дендритная ликвация может быть ослаблена продолжительным нагревом затвердевшего сплава при температурах, обеспечивающих достаточную скорость диффузии (несколько ниже солидуса). После такого нагрева, называемого диффузионным отжигом, или гомогенизацией, дендритная структура литого сплава уже не выявляется и сплав состоит из однородных кристаллов твердого раствора (рис. 38, б).
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ЧАСТЬ I. МЕТАЛЛОВЕДЕНИЕ И ТЕРМИЧЕСКАЯ ОБРАБОТКА
- ГЛАВА 1. КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ
- 2. АТОМНО-КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА МЕТАЛЛОВ
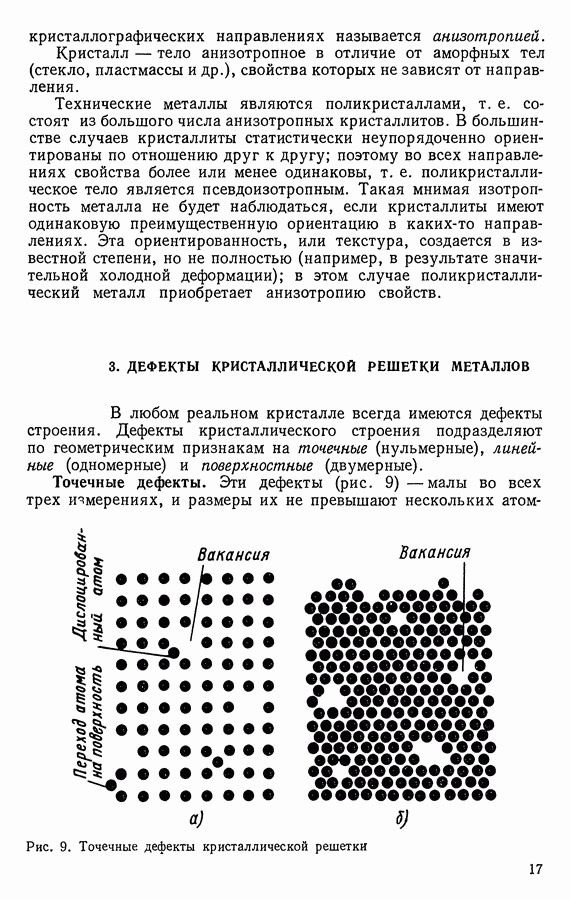
- 3. ДЕФЕКТЫ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ МЕТАЛЛОВ
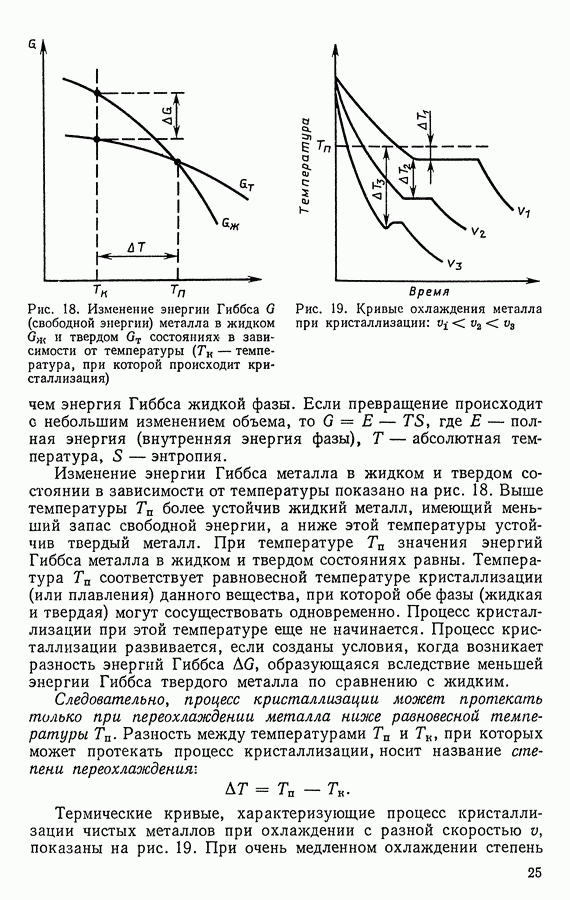
- ГЛАВА II. ФОРМИРОВАНИЕ СТРУКТУРЫ МЕТАЛЛА ПРИ КРИСТАЛЛИЗАЦИИ
- 2. ГЕТЕРОГЕННОЕ ОБРАЗОВАНИЕ ЗАРОДЫШЕЙ
- 3. СТРОЕНИЕ МЕТАЛЛИЧЕСКОГО СЛИТКА
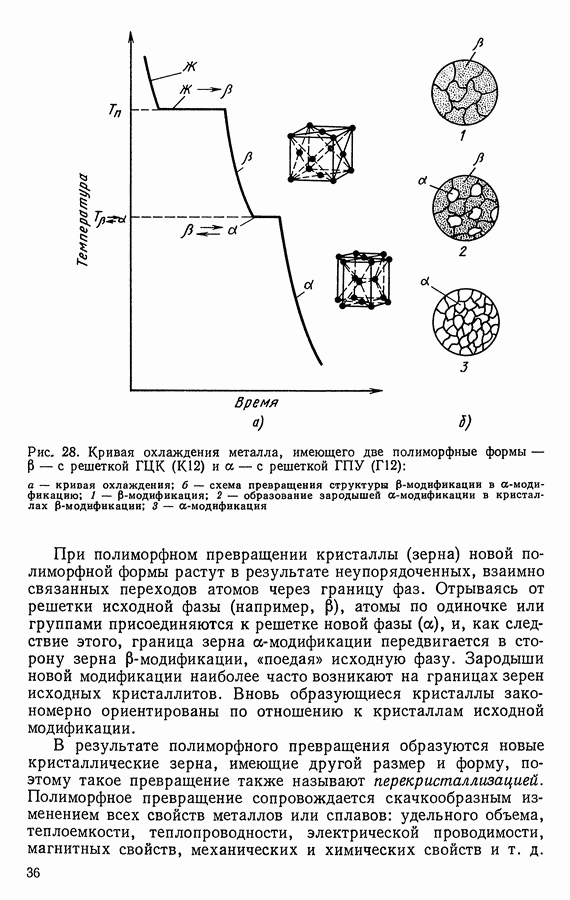
- 4. ПОЛИМОРФНЫЕ ПРЕВРАЩЕНИЯ
- ГЛАВА III. ФАЗЫ И СТРУКТУРА В МЕТАЛЛИЧЕСКИХ СПЛАВАХ
- 2. ХИМИЧЕСКИЕ СОЕДИНЕНИЯ
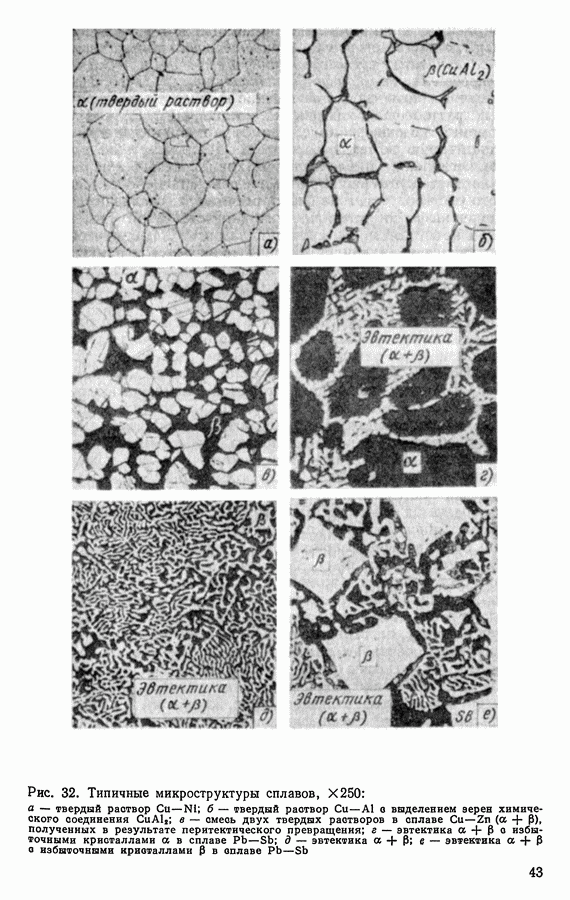
- 3. СТРУКТУРА СПЛАВОВ
- ГЛАВА IV. ФОРМИРОВАНИЕ СТРУКТУРЫ СПЛАВОВ ПРИ КРИСТАЛЛИЗАЦИИ
- 2. ДИАГРАММЫ ФАЗОВОГО РАВНОВЕСИЯ
- 3. ДИАГРАММА СОСТОЯНИЯ СПЛАВОВ, ОБРАЗУЮЩИХ НЕОГРАНИЧЕННЫЕ ТВЕРДЫЕ РАСТВОРЫ
- 4. ДИАГРАММЫ СОСТОЯНИЯ СПЛАВОВ, ОБРАЗУЮЩИХ ОГРАНИЧЕННЫЕ ТВЕРДЫЕ РАСТВОРЫ
- 5. ДИАГРАММЫ СОСТОЯНИЯ СПЛАВОВ, КОМПОНЕНТЫ КОТОРЫХ ИМЕЮТ ПОЛИМОРФНЫЕ ПРЕВРАЩЕНИЯ
- 6. ПОНЯТИЕ О ДИАГРАММАХ СОСТОЯНИЯ ТРОЙНЫХ СПЛАВОВ
- ГЛАВА V. ДЕФОРМАЦИЯ И РАЗРУШЕНИЕ МЕТАЛЛОВ
- 2. УПРУГАЯ И ПЛАСТИЧЕСКАЯ ДЕФОРМАЦИИ МЕТАЛЛОВ
- 3. СВЕРХПЛАСТИЧНОСТЬ МЕТАЛЛОВ И СПЛАВОВ
- 4. РАЗРУШЕНИЕ МЕТАЛЛОВ
- ГЛАВА VI. ВЛИЯНИЕ НАГРЕВА НА СТРУКТУРУ И СВОЙСТВА ДЕФОРМИРОВАННОГО МЕТАЛЛА
- 2. РЕКРИСТАЛЛИЗАЦИЯ
- 3. ХОЛОДНАЯ И ГОРЯЧАЯ ДЕФОРМАЦИИ
- ГЛАВА VII. МЕХАНИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ
- 2. МЕХАНИЧЕСКИЕ СВОЙСТВА, ОПРЕДЕЛЯЕМЫЕ ПРИ СТАТИЧЕСКИХ ИСПЫТАНИЯХ
- 3. ТВЕРДОСТЬ МЕТАЛЛОВ
- 4. МЕХАНИЧЕСКИЕ СВОЙСТВА, ОПРЕДЕЛЯЕМЫЕ ПРИ ДИНАМИЧЕСКИХ ИСПЫТАНИЯХ
- 5. МЕХАНИЧЕСКИЕ СВОЙСТВА ПРИ ПЕРЕМЕННЫХ (ЦИКЛИЧЕСКИХ) НАГРУЗКАХ
- 6. ИЗНАШИВАНИЕ МЕТАЛЛОВ
- 7. ПУТИ ПОВЫШЕНИЯ ПРОЧНОСТИ МЕТАЛЛОВ
- ГЛАВА VIII. ЖЕЛЕЗО И СПЛАВЫ НА ЕГО ОСНОВЕ
- 2. ДИАГРАММА СОСТОЯНИЯ ЖЕЛЕЗО — ЦЕМЕНТИТ (МЕТАСТАБИЛЬНОЕ РАВНОВЕСИЕ)
- 3. ДИАГРАММА СОСТОЯНИЯ ЖЕЛЕЗО — ГРАФИТ (СТАБИЛЬНОЕ РАВНОВЕСИЕ)
- 4. ВЛИЯНИЕ УГЛЕРОДА И ПОСТОЯННЫХ (ТЕХНОЛОГИЧЕСКИХ) ПРИМЕСЕЙ НА СВОЙСТВА СТАЛИ
- 5. ЛЕГИРУЮЩИЕ ЭЛЕМЕНТЫ В СТАЛИ
- 6. СТРУКТУРНЫЕ КЛАССЫ ЛЕГИРОВАННЫХ СТАЛЕЙ
- ГЛАВА IX. ЧУГУН
- 1. СЕРЫЙ И БЕЛЫЙ ЧУГУНЫ
- 2. ВЫСОКОПРОЧНЫЙ ЧУГУН С ШАРОВИДНЫМ ГРАФИТОМ
- 3. КОВКИЙ ЧУГУН
- 4. СПЕЦИАЛЬНЫЕ ЧУГУНЫ
- ГЛАВА X. ФАЗОВЫЕ ПРЕВРАЩЕНИЯ В СПЛАВАХ ЖЕЛЕЗА (ТЕОРИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ)
- 2. РОСТ ЗЕРНА АУСТЕНИТА ПРИ НАГРЕВЕ
- 3. ОБЩАЯ ХАРАКТЕРИСТИКА ПРЕВРАЩЕНИЯ ПЕРЕОХЛАЖДЕННОГО АУСТЕНИТА (ДИАГРАММА ИЗОТЕРМИЧЕСКОГО ПРЕВРАЩЕНИЯ АУСТЕНИТА)
- 4. ПЕРЛИТНОЕ ПРЕВРАЩЕНИЕ
- 5. МАРТЕНСИТНОЕ ПРЕВРАЩЕНИЕ В СТАЛИ
- 6. ПРОМЕЖУТОЧНОЕ (БЕЙНИТНОЕ) ПРЕВРАЩЕНИЕ
- 7. ИЗОТЕРМИЧЕСКОЕ ПРЕВРАЩЕНИЕ АУСТЕНИТА В ЛЕГИРОВАННЫХ СТАЛЯХ
- 8. ПРЕВРАЩЕНИЕ АУСТЕНИТА ПРИ НЕПРЕРЫВНОМ ОХЛАЖДЕНИИ
- 9. ТЕРМОКИНЕТИЧЕСКИЕ ДИАГРАММЫ ПРЕВРАЩЕНИЯ ПЕРЕОХЛАЖДЕННОГО АУСТЕНИТА
- 10. ПРЕВРАЩЕНИЕ МАРТЕНСИТА И ОСТАТОЧНОГО АУСТЕНИТА ПРИ НАГРЕВЕ (ОТПУСК СТАЛИ)
- 11. ТЕРМИЧЕСКОЕ И ДЕФОРМАЦИОННОЕ СТАРЕНИЕ УГЛЕРОДИСТОЙ СТАЛИ
- ГЛАВА XI. ТЕХНОЛОГИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ
- 2. ОТЖИГ II РОДА (ФАЗОВАЯ ПЕРЕКРИСТАЛЛИЗАЦИЯ)
- 3. ЗАКАЛКА
- 4. ОТПУСК
- 5. ТЕРМОМЕХАНИЧЕСКАЯ ОБРАБОТКА (ТМО)
- 6. ДЕФЕКТЫ, ВОЗНИКАЮЩИЕ ПРИ ТЕРМИЧЕСКОЙ ОБРАБОТКЕ СТАЛИ
- 7. ПОВЕРХНОСТНАЯ ЗАКАЛКА
- ГЛАВА XII. ХИМИКО-ТЕРМИЧЕСКАЯ ОБРАБОТКА СТАЛИ
- 1. ЦЕМЕНТАЦИЯ
- 2. НИТРОЦЕМЕНТАЦИЯ
- 3. АЗОТИРОВАНИЕ
- 4. ЦИАНИРОВАНИЕ
- 5. БОРИРОВАНИЕ
- 6. СИЛИЦИРОВАНИЕ
- 7. ДИФФУЗИОННОЕ НАСЫЩЕНИЕ МЕТАЛЛАМИ
- ГЛАВА XIII. ПОВЕРХНОСТНАЯ ПЛАСТИЧЕСКАЯ ДЕФОРМАЦИЯ
- ГЛАВА XIV. КОНСТРУКЦИОННЫЕ СТАЛИ И СПЛАВЫ
- 1. УГЛЕРОДИСТЫЕ КОНСТРУКЦИОННЫЕ СТАЛИ
- 2. ЛЕГИРОВАННЫЕ КОНСТРУКЦИОННЫЕ СТАЛИ
- 3. СТРОИТЕЛЬНЫЕ НИЗКОЛЕГИРОВАННЫЕ СТАЛИ
- 4. АРМАТУРНЫЕ СТАЛИ
- 5. СТАЛИ ДЛЯ ХОЛОДНОЙ ШТАМПОВКИ
- 6. КОНСТРУКЦИОННЫЕ (МАШИНОСТРОИТЕЛЬНЫЕ) ЦЕМЕНТУЕМЫЕ (НИТРОЦЕМЕНТУЕМЫЕ) ЛЕГИРОВАННЫЕ СТАЛИ
- 7. КОНСТРУКЦИОННЫЕ (МАШИНОСТРОИТЕЛЬНЫЕ) УЛУЧШАЕМЫЕ ЛЕГИРОВАННЫЕ СТАЛИ
- 8. СТАЛИ С ПОВЫШЕННОЙ ОБРАБАТЫВАЕМОСТЬЮ РЕЗАНИЕМ
- 9. МАРТЕНСИТНО-СТАРЕЮЩИЕ ВЫСОКОПРОЧНЫЕ СТАЛИ
- 10. ВЫСОКОПРОЧНЫЕ СТАЛИ С ВЫСОКОЙ ПЛАСТИЧНОСТЬЮ (ТРИП-ИЛИ ПИП-СТАЛИ)
- 11. РЕССОРНО-ПРУЖИННЫЕ СТАЛИ ОБЩЕГО НАЗНАЧЕНИЯ
- 12. ШАРИКОПОДШИПНИКОВЫЕ СТАЛИ
- 13. ИЗНОСОСТОЙКИЕ СТАЛИ
- 14. КОРРОЗИОННО-СТОЙКИЕ И ЖАРОСТОЙКИЕ СТАЛИ И СПЛАВЫ
- 15. КРИОГЕННЫЕ СТАЛИ
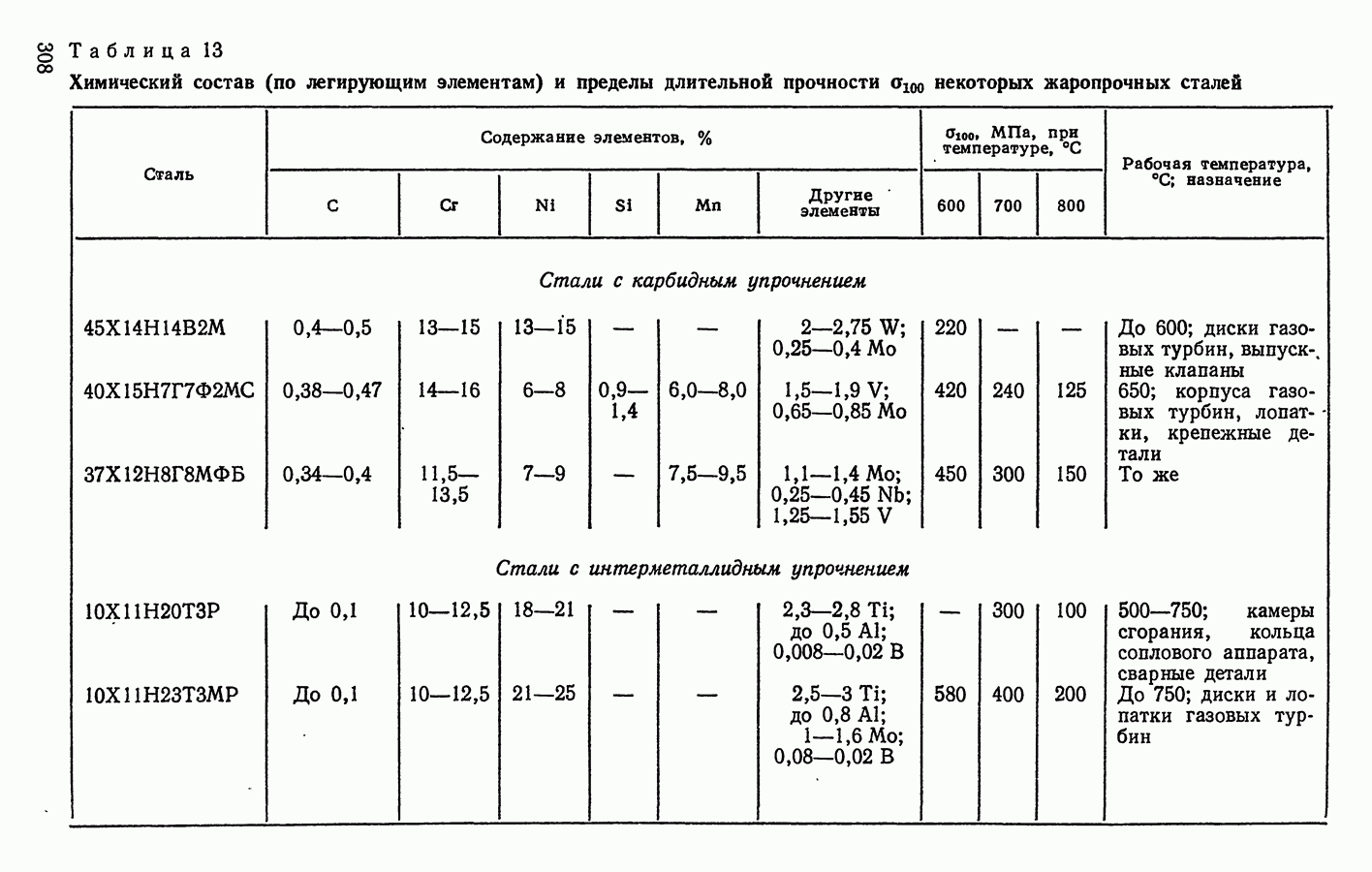
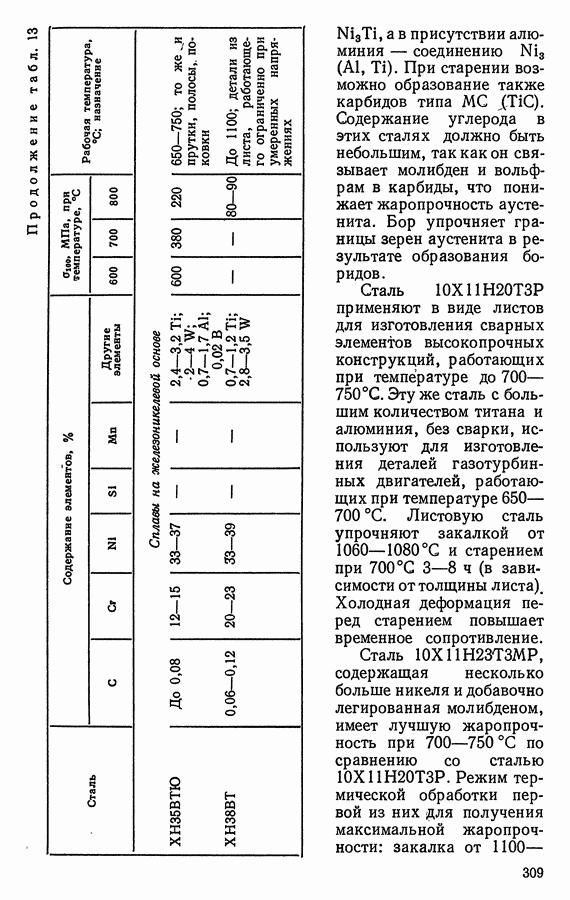
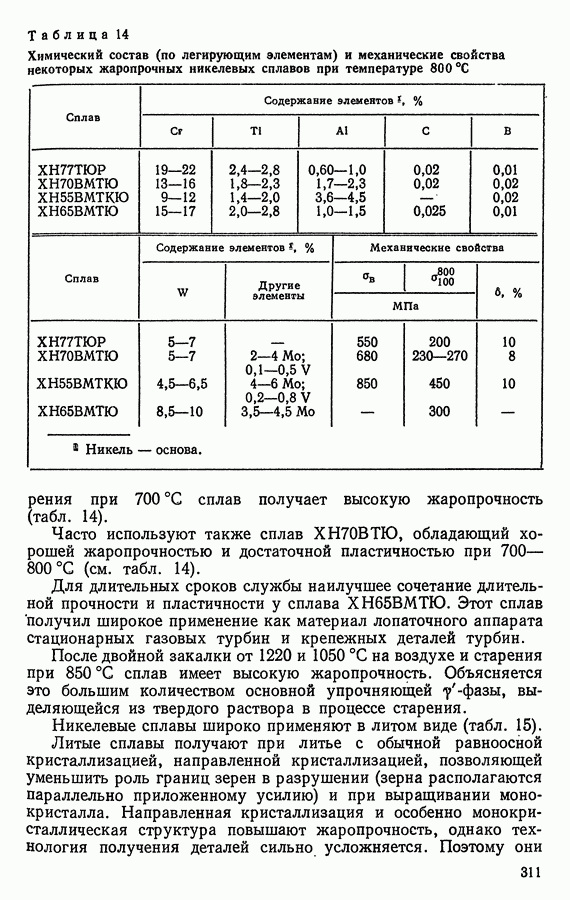
- 16. ЖАРОПРОЧНЫЕ СТАЛИ И СПЛАВЫ
- ГЛАВА XV. ОСНОВЫ РАЦИОНАЛЬНОГО ВЫБОРА СТАЛИ (ЧУГУНА) И МЕТОДОВ УПРОЧНЕНИЯ ДЕТАЛЕЙ МАШИН
- 2. ПРИМЕРЫ ТЕРМИЧЕСКОЙ И ХИМИКО-ТЕРМИЧЕСКОЙ ОБРАБОТКИ ДЕТАЛЕЙ МАШИН
- 3. УПРОЧНЕНИЕ ПОВЕРХНОСТНЫМ ПЛАСТИЧЕСКИМ ДЕФОРМИРОВАНИЕМ
- 4. ИЗНОСОСТОЙКИЕ И КОРРОЗИОННО-СТОЙКИЕ ПОКРЫТИЯ
- ГЛАВА XVI. ИНСТРУМЕНТАЛЬНЫЕ СТАЛИ И ТВЕРДЫЕ СПЛАВЫ
- 1. СТАЛИ ДЛЯ РЕЖУЩЕГО ИНСТРУМЕНТА
- 2. СТАЛИ ДЛЯ ИЗМЕРИТЕЛЬНОГО ИНСТРУМЕНТА
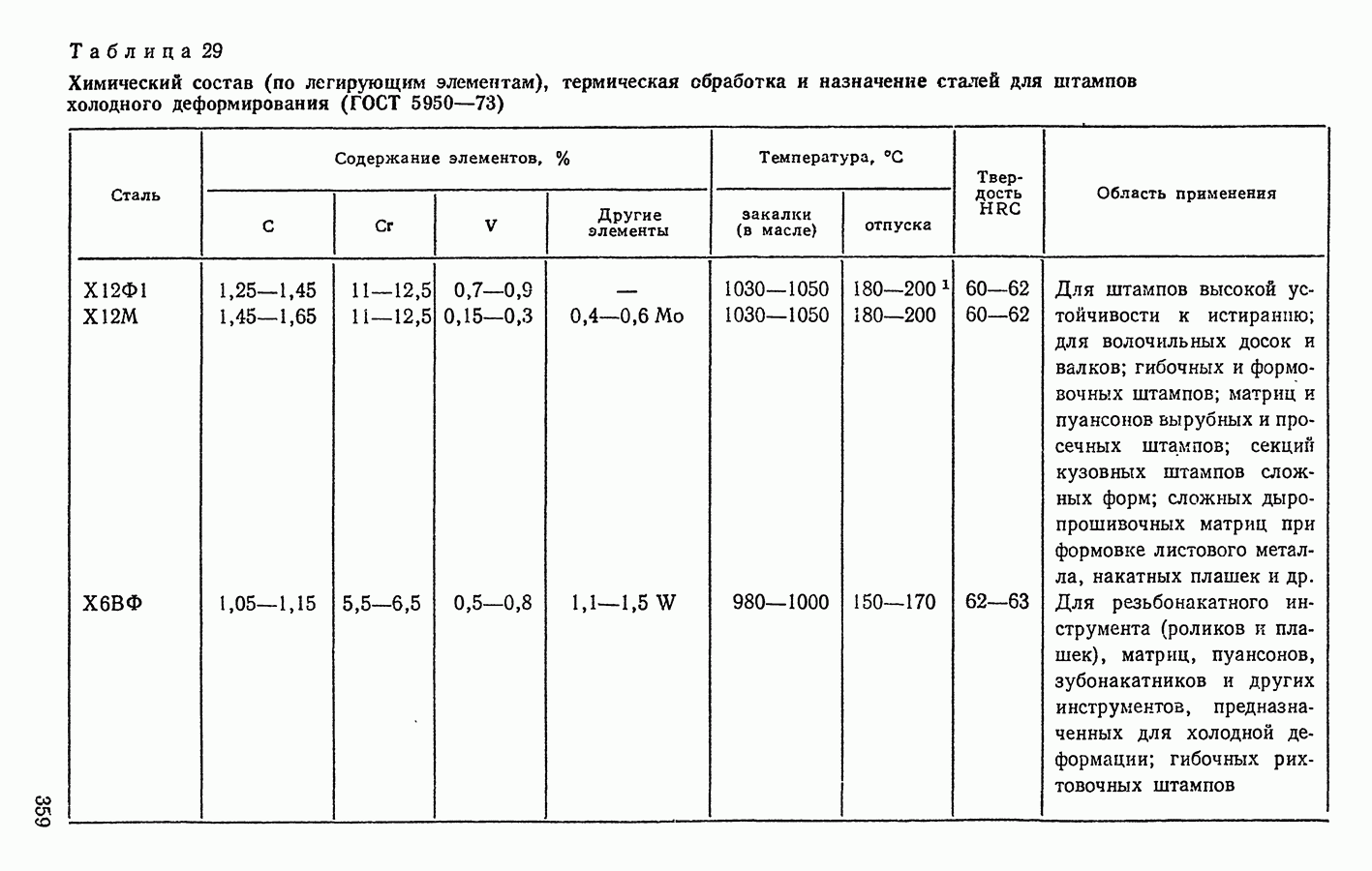
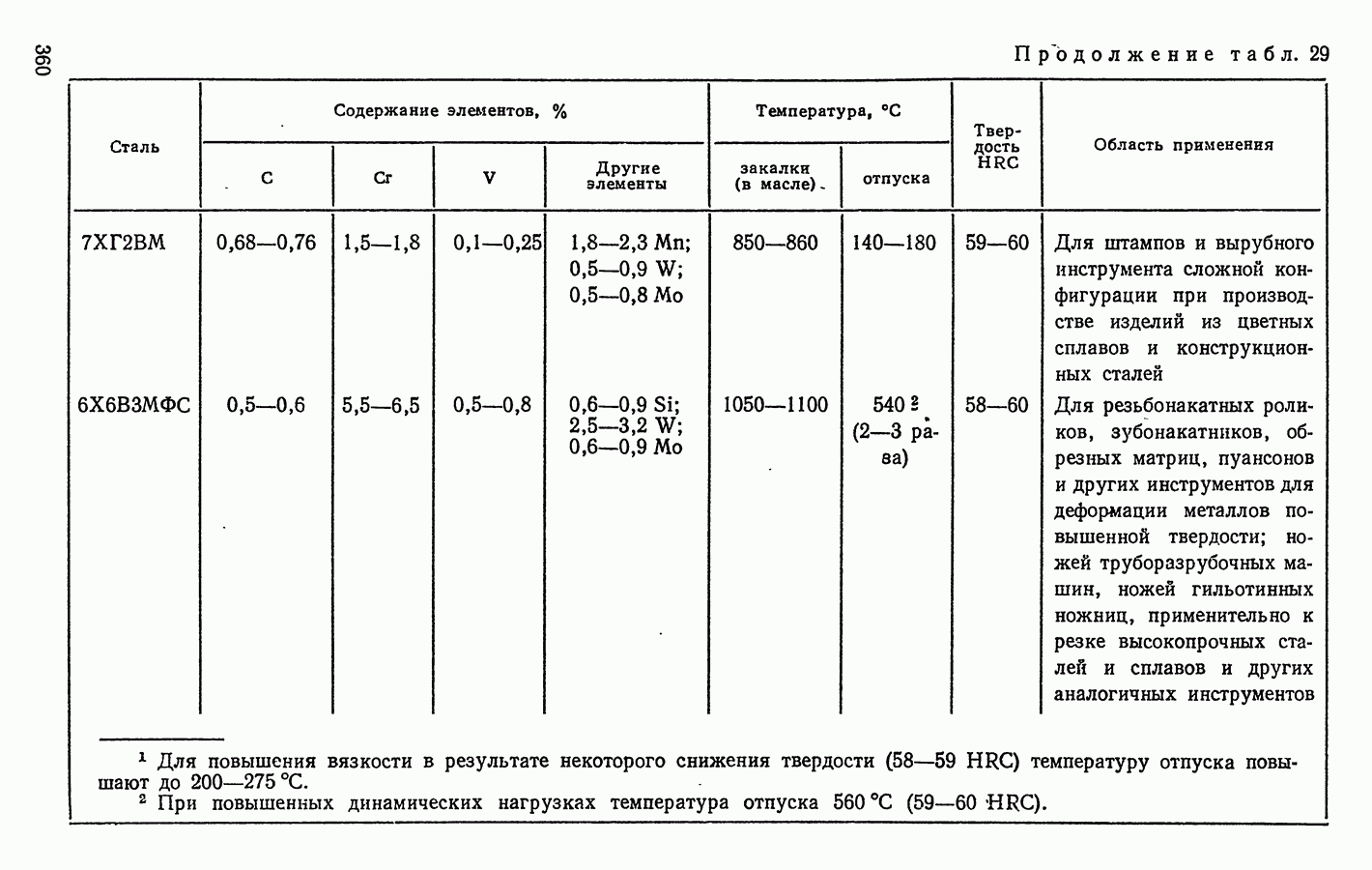
- 3. СТАЛИ ДЛЯ ШТАМПОВ ХОЛОДНОГО ДЕФОРМИРОВАНИЯ
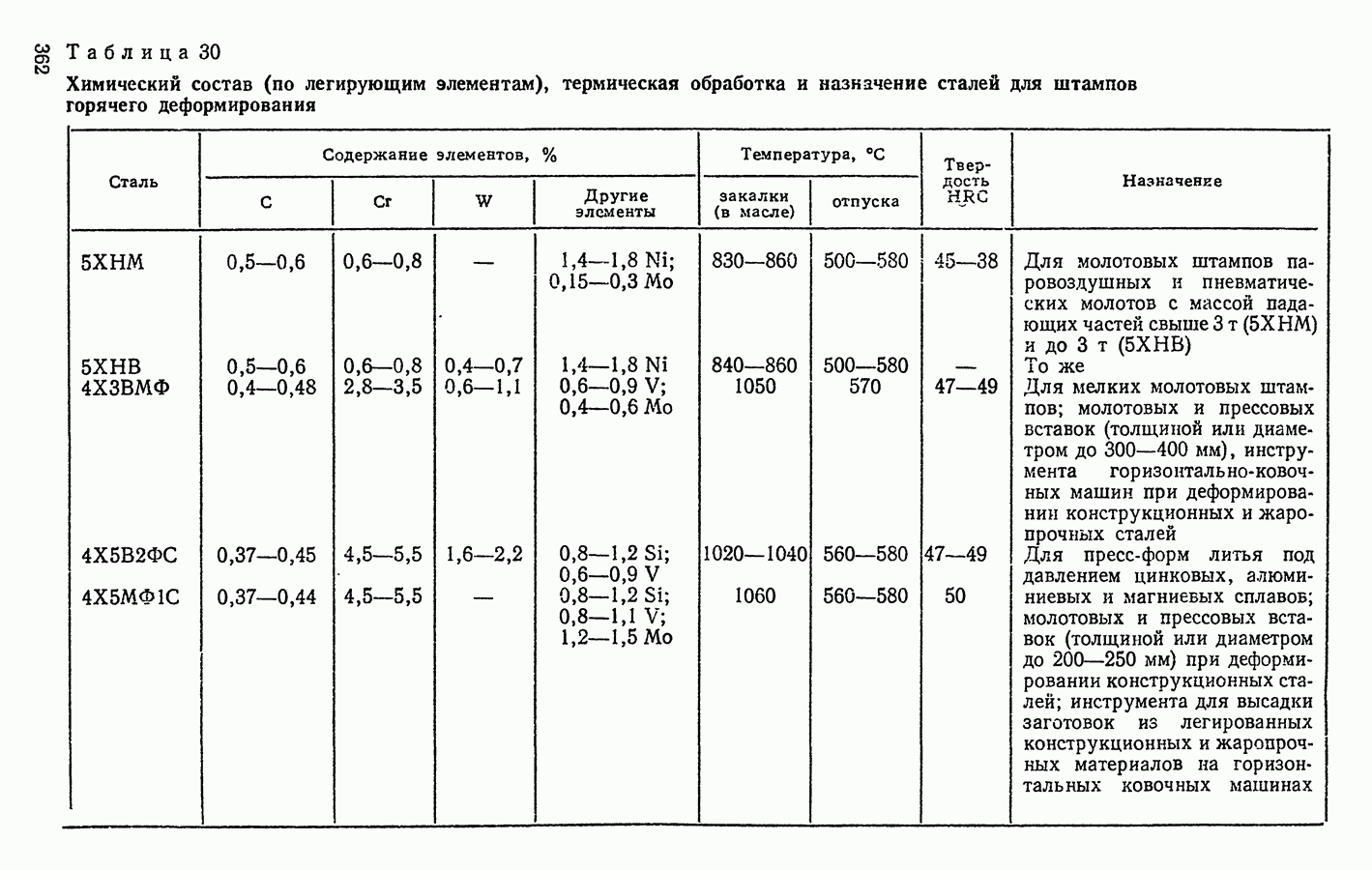
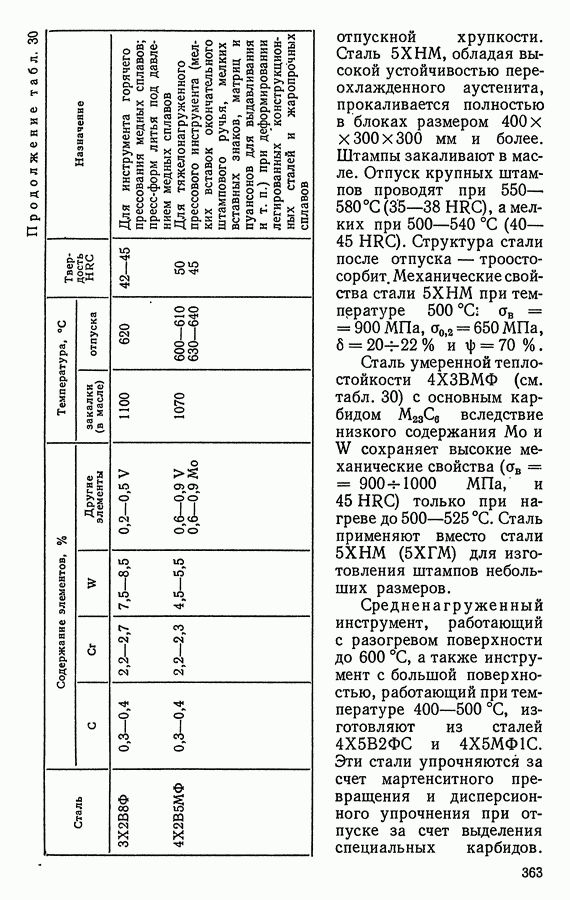
- 4. СТАЛИ ДЛЯ ШТАМПОВ ГОРЯЧЕГО ДЕФОРМИРОВАНИЯ
- 5. ТВЕРДЫЕ СПЛАВЫ
- ГЛАВА XVII. СТАЛИ И СПЛАВЫ С ОСОБЫМИ ФИЗИЧЕСКИМИ СВОЙСТВАМИ
- 2. МЕТАЛЛИЧЕСКИЕ СТЕКЛА (АМОРФНЫЕ СПЛАВЫ)
- 3. СТАЛИ И СПЛАВЫ С ВЫСОКИМ ЭЛЕКТРИЧЕСКИМ СОПРОТИВЛЕНИЕМ ДЛЯ НАГРЕВАТЕЛЬНЫХ ЭЛЕМЕНТОВ
- 4. СПЛАВЫ С ЗАДАННЫМ ТЕМПЕРАТУРНЫМ КОЭФФИЦИЕНТОМ ЛИНЕЙНОГО РАСШИРЕНИЯ
- 5. СПЛАВЫ С ЭФФЕКТОМ «ПАМЯТИ ФОРМЫ»
- ГЛАВА XVIII. ТУГОПЛАВКИЕ МЕТАЛЛЫ И ИХ СПЛАВЫ
- ГЛАВА XIX. ТИТАН И СПЛАВЫ НА ЕГО ОСНОВЕ
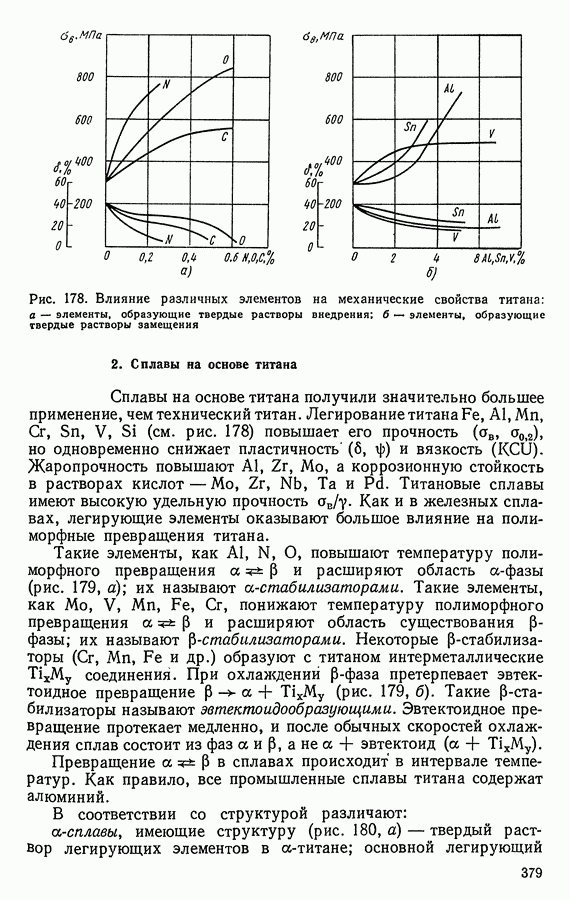
- 2. Сплавы на основе титана
- ГЛАВА XX. АЛЮМИНИЙ И СПЛАВЫ НА ЕГО ОСНОВЕ
- 2. КЛАССИФИКАЦИЯ АЛЮМИНИЕВЫХ СПЛАВОВ
- 3. ТЕРМИЧЕСКАЯ ОБРАБОТКА АЛЮМИНИЕВЫХ СПЛАВОВ
- 4. ДЕФОРМИРУЕМЫЕ АЛЮМИНИЕВЫЕ СПЛАВЫ, УПРОЧНЯЕМЫЕ ТЕРМИЧЕСКОЙ ОБРАБОТКОЙ
- 5. ДЕФОРМИРУЕМЫЕ АЛЮМИНИЕВЫЕ СПЛАВЫ, НЕ УПРОЧНЯЕМЫЕ ТЕРМИЧЕСКОЙ ОБРАБОТКОЙ
- 6. ЛИТЕЙНЫЕ АЛЮМИНИЕВЫЕ СПЛАВЫ
- ГЛАВА XXI. МАГНИЙ И СПЛАВЫ НА ЕГО ОСНОВЕ
- ГЛАВА XXII. МЕДЬ И СПЛАВЫ НА ЕЕ ОСНОВЕ
- 2. СПЛАВЫ НА ОСНОВЕ МЕДИ
- ГЛАВА XXIII. АНТИФРИКЦИОННЫЕ (ПОДШИПНИКОВЫЕ) СПЛАВЫ НА ОЛОВЯННОЙ, СВИНЦОВОЙ, ЦИНКОВЫЙ И АЛЮМИНИЕВОЙ ОСНОВАХ
- ГЛАВА XXIV. КОМПОЗИЦИОННЫЕ МАТЕРИАЛЫ С МЕТАЛЛИЧЕСКОЙ МАТРИЦЕЙ
- ГЛАВА XXV. КОНСТРУКЦИОННЫЕ ПОРОШКОВЫЕ МАТЕРИАЛЫ
- ЧАСТЬ II. НЕМЕТАЛЛИЧЕСКИЕ МАТЕРИАЛЫ
- ГЛАВА XXVI. ОБЩИЕ СВЕДЕНИЯ О НЕМЕТАЛЛИЧЕСКИХ МАТЕРИАЛАХ
- 2. ОСОБЕННОСТИ СВОЙСТВ ПОЛИМЕРНЫХ МАТЕРИАЛОВ
- ГЛАВА XXVII. ПЛАСТИЧЕСКИЕ МАССЫ
- 1. СОСТАВ, КЛАССИФИКАЦИЯ И СВОЙСТВА ПЛАСТМАСС
- 2. ТЕРМОПЛАСТИЧНЫЕ ПЛАСТМАССЫ
- 3. ТЕРМОРЕАКТИВНЫЕ ПЛАСТМАССЫ
- 4. ГАЗОНАПОЛНЕННЫЕ ПЛАСТМАССЫ
- 5. ЭКОНОМИЧЕСКАЯ ЭФФЕКТИВНОСТЬ ПРИМЕНЕНИЯ ПЛАСТМАСС
- ГЛАВА XXVIII. КОМПОЗИЦИОННЫЕ МАТЕРИАЛЫ С НЕМЕТАЛЛИЧЕСКОЙ МАТРИЦЕЙ
- 1. ОБЩИЕ СВЕДЕНИЯ, СОСТАВ И КЛАССИФИКАЦИЯ
- 2. КАРБОВОЛОКНИТЫ
- 3. БОРОВОЛОКНИТЫ
- 4. ОРГАНОВОЛОКНИТЫ
- ГЛАВА XXIX. РЕЗИНОВЫЕ МАТЕРИАЛЫ
- 2. РЕЗИНЫ ОБЩЕГО НАЗНАЧЕНИЯ
- 3. РЕЗИНЫ СПЕЦИАЛЬНОГО НАЗНАЧЕНИЯ
- 4. ВЛИЯНИЕ ФАКТОРОВ ЭКСПЛУАТАЦИИ НА СВОЙСТВА РЕЗИН
- ГЛАВА XXX. КЛЕЯЩИЕ МАТЕРИАЛЫ И ГЕРМЕТИКИ
- 1. ОБЩИЕ СВЕДЕНИЯ, СОСТАВ И КЛАССИФИКАЦИЯ ПЛЕНКООБРАЗУЮЩИХ МАТЕРИАЛОВ
- 2. КОНСТРУКЦИОННЫЕ СМОЛЯНЫЕ И РЕЗИНОВЫЕ КЛЕИ
- 3. НЕОРГАНИЧЕСКИЕ КЛЕИ
- 4. СВОЙСТВА КЛЕЕВЫХ СОЕДИНЕНИЙ
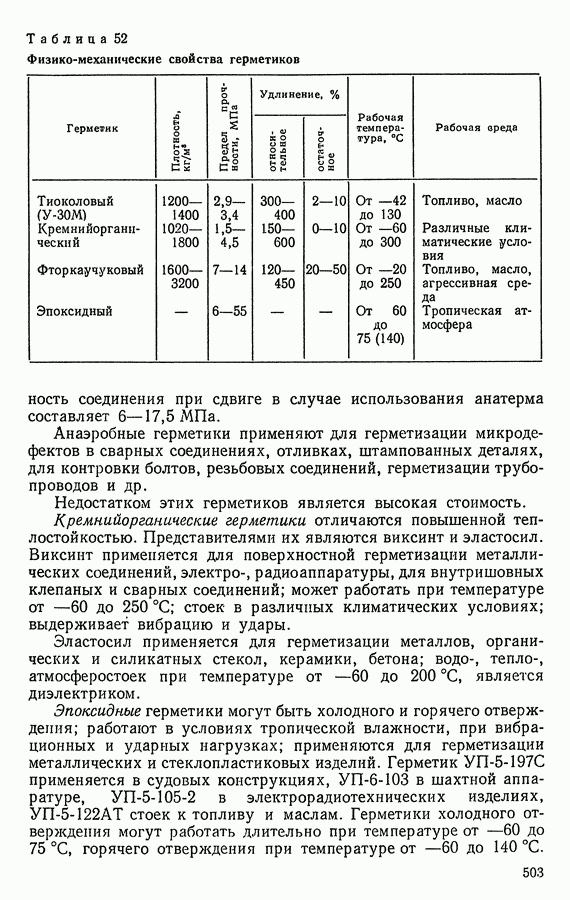
- 5. ГЕРМЕТИКИ
- ГЛАВА XXXI. НЕОРГАНИЧЕСКИЕ МАТЕРИАЛЫ
- 2. НЕОРГАНИЧЕСКОЕ СТЕКЛО
- 3. СИТАЛЛЫ (СТЕКЛОКРИСТАЛЛИЧЕСКИЕ МАТЕРИАЛЫ)
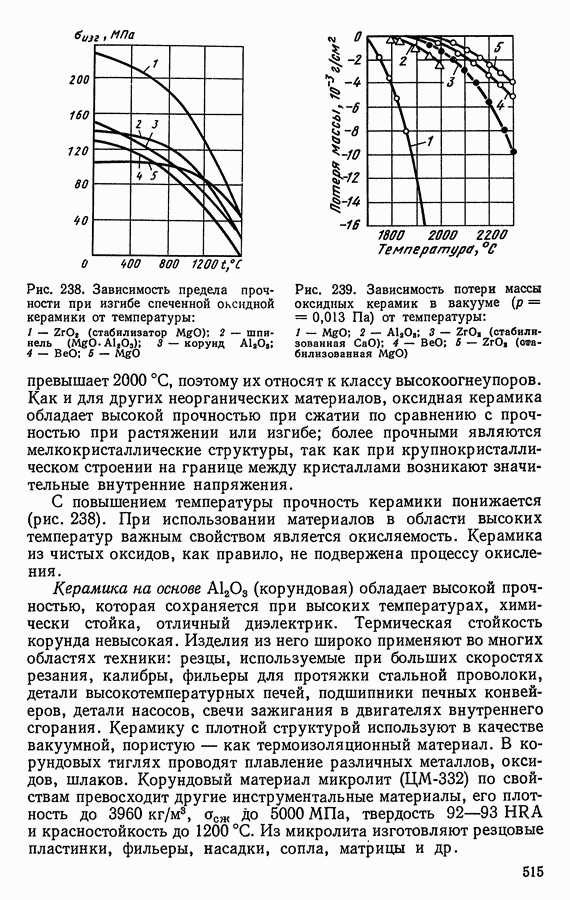
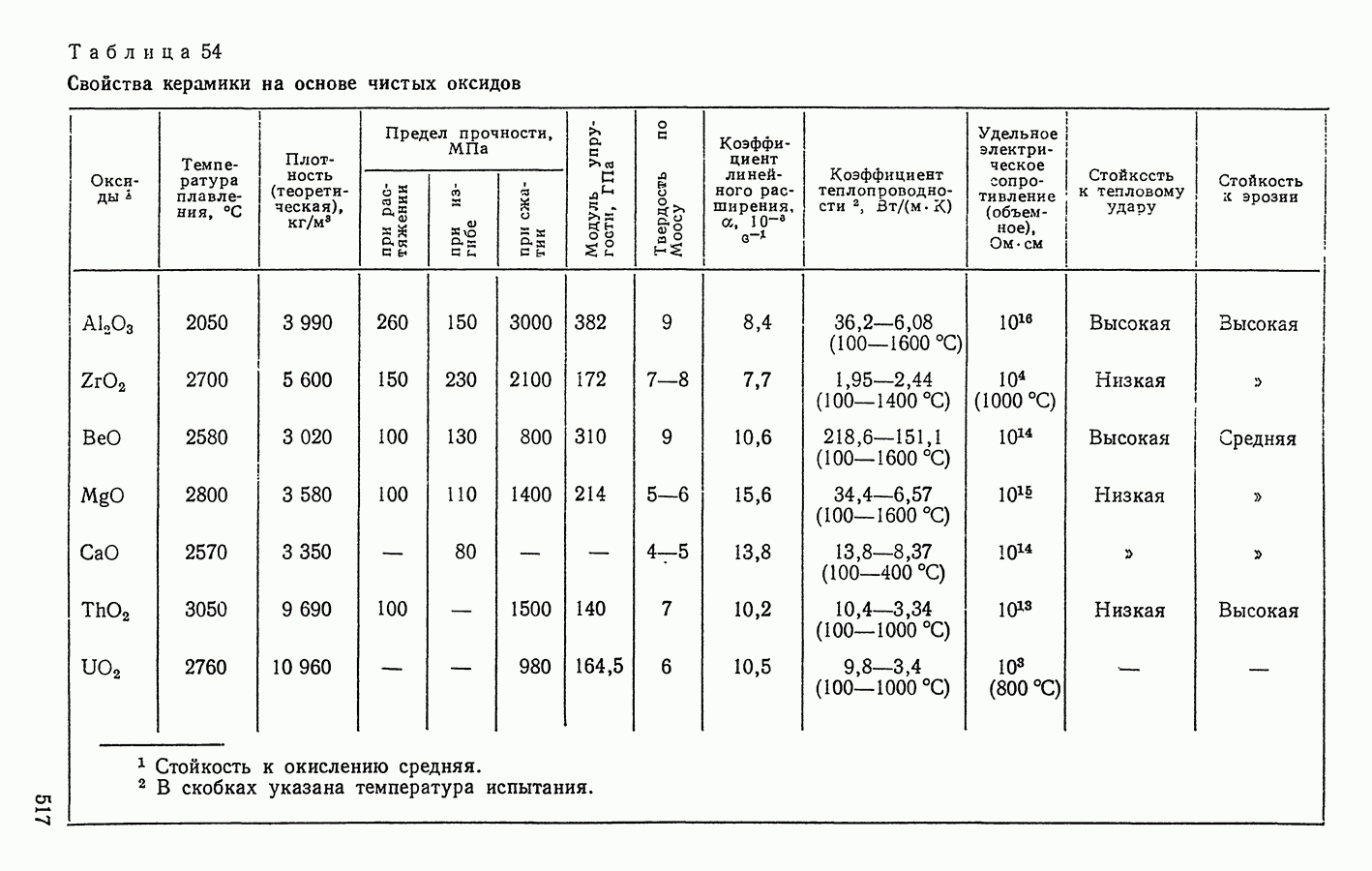
- 4. КЕРАМИЧЕСКИЕ МАТЕРИАЛЫ