| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДИСКРЕТНЫЕ СПЕКТРАЛЬНЫЕ ЛИНИИ
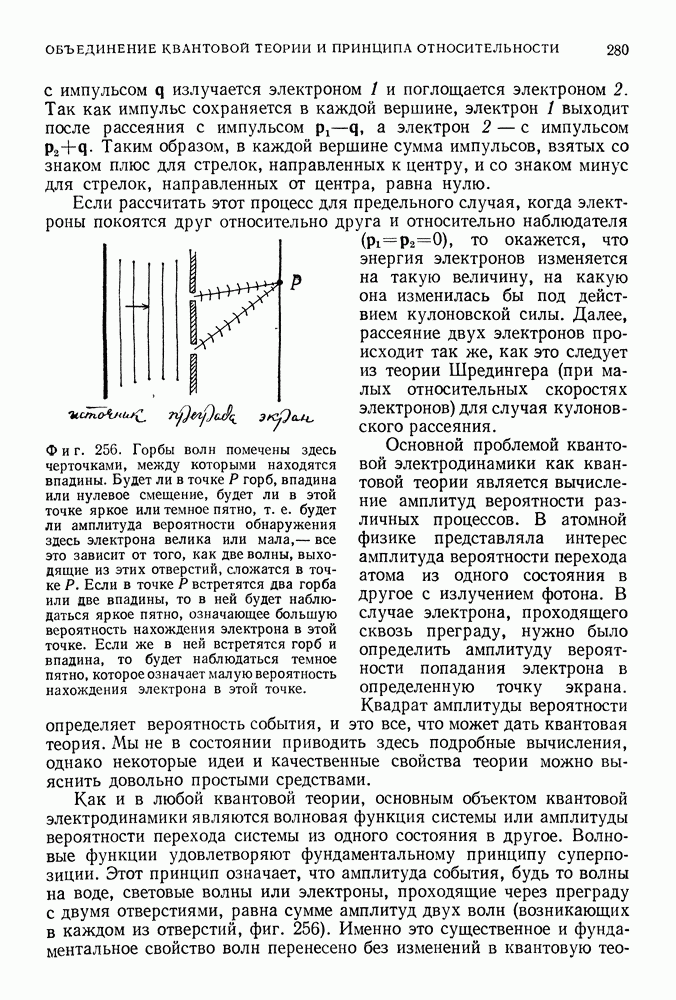
Чтобы «произвести опыты над знаменитым явлением цветов» [1], Ньютон затемнил свою комнату, проделал небольшую дыру в оконных ставнях, поместил призму там, где входил свет, и наблюдал «зрелище живых и ярких красок, получавшихся при этом» [2]. Было это в 1666 г. В 1802 г. Волластон обнаружил «среди живых и ярких красок, получившихся при этом», темные линии. В 1814 г. Фраунгофер скомбинировал призму со зрительной трубой и наблюдал свет, пропущенный через удаленную узкую щель. Этот прибор называется теперь спектроскопом (фото 1). Рассматривая солнечный спектр через свой инструмент, Фраунгофер
«...обнаружил не одну линию, а чрезвычайно большое количество вертикальных линий, резких и слабых, которые, однако, оказались темнее остальной части спектра, а некоторые из них казались почти совершенно черными» [3].
Публикуя в 1817 г. свои результаты, он добавил:
«С помощью многочисленных экспериментов и разнообразных методов я убедился, что эти линии и полосы обязаны своим происхождением природе солнечного света, а не дифракции, обману зрения и т. д.».
Темные линии расположены между различными цветными полосами, а поскольку каждому цвету соответствует определенная длина волны, то и каждой темной полосе можно тоже приписать определенное значение длины волны. Фраунгофер, оказав предпочтение латинскому алфавиту перед греческим, обозначил эти линии буквами А, Б, С, D,... (фото 2). Изучая две близкие линии в желтой части спектра, обозначенные Фраунгофером буквой D, Густав Кирхгоф и Роберт Бунзен (широко известный благодаря горелке, названной его именем) пришли
в 1859 г. к объяснению происхождения темных линий в спектре. Кирхгоф пишет:
«Занимаясь совместно с Бунзеном исследованием спектров цветного пламени, с помощью которого удалось установить качественный состав сложных смесей по виду их спектров в пламени горелки, я провел несколько наблюдений, приведших к неожиданному объяснению происхождения линий Фраунгофера,и позволивших сделать выводы о составе солнечной атмосферы и, возможно, также о составе ярких неподвижных звезд» [41.
Он продолжает:
«Фраунгофер обнаружил, что в спектре пламени свечи имеются две светлые линии, совпадающие с двумя темными линиями солнечного спектра. Мы получили те же самые светлые линии, но гораздо более интенсивные, в спектре пламени, в которое была введена обычная поваренная соль. Наблюдая солнечный спектр, я пропустил солнечные лучи, прежде чем они попадали в щель, через пламя, в которое было введено достаточно много соли. Когда солнечный свет был существенно ослаблен, на месте двух темных линий D появились две светлые линии...» [51.
И далее:
«Можно предположить, что светлые линии, отвечающие линиям D в спектре пламени, появляются всегда при наличии натрия; присутствие темных линий D в солнечном спектре свидетельствует, по нашему мнению, о том, что в солнечной атмосфере имеется натрий» [6].
Вскоре после этого Кирхгоф сформулировал два так называемых основных закона спектроскопии: 1) каждое химическое вещество обладает своим специфическим спектром и 2) каждое вещество способно поглощать такое излучение, какое оно может само излучить. Если ввести в пламя горелки Бунзена натрий, то оно станет ярко-желтым (фото 3). (Наличие соли во многих веществах объясняет желтый цвет большинства пламен.) Если проанализировать этот желтый цвет, то мы увидим, что он определяется двумя светлыми D-линиями спектра. Однако если раскаленный натрий излучает две светлые линии D, то холодные пары натрия поглощают их. В результате, если яркий луч света, содержащего все цвета, проходит через холодные пары натрия, две линии D будут выглядеть темными на ярком фоне цветного спектра.
Далее Кирхгоф предположил, что наличие темных линий в солнечном спектре объясняется присутствием относительно холодных паров натрия и других элементов во внешней солнечной атмосфере. Непрерывный спектр света, испущенного внутренними областями Солнца и прошедшего затем через относительно холодные пары, теряет характерные линии различных элементов. Таким образом, изучая темные линии солнечного спектра или спектр какой-нибудь звезды, мы можем
узнать, какие элементы имеются во внешних атмосферах этих звезд (фото 4). Этот результат мог бы удивить французского позитивиста Огюста Конта, который в 1825 г. привел химический состав звезд в качестве примера принципиально непознаваемой вещи.
Суть открытий Фраунгофера, Бунзена и Кирхгофа состоит вкратце в следующем. Если нагреть чистый элемент до достаточно высокой температуры, помещая его, например, в относительно бесцветное пламя горелки Бунзена, то этот элемент начнет светиться определенным цветом, характерным для каждого элемента: натрий излучает желтый свет, стронций — красный свет и т. д. Если разложить этот свет, пропуская его через спектроскоп, на отдельные длины волн, то мы обнаружим, что каждому элементу соответствует свой характерный набор линий, всегда один и тот же для данного элемента. Неизвестно ни одной пары различных элементов, обладающих одинаковыми наборами линий.
Этот результат позволяет определять химический состав сложных соединений. Достаточно поместить исследуемое вещество в пламя и сравнить полученный спектр со спектрами различных элементов, чтобы узнать, из каких элементов состоит данное химическое соединение. Более того, по интенсивности различных линий можно даже определить относительное содержание каждого элемента. Таким образом Кирхгофу и Бунзену «... удалось установить качественный состав различных смесей по виду спектров этих смесей» [7], решив тем самым древнюю проблему определения химического состава заданного вещества.
Однако то, что каждый отдельный элемент обладал своим характерным спектром, состоящим из четких линий, т. е. каждый атом имел как бы свою роспись, для физиков было крайне неожиданным и загадочным. Вскоре было обнаружено, что некоторые линии являются невидимыми и лежат в ультрафиолетовой или инфракрасной областях спектра. Для изучения этих линий потребовалась новая специальная аппаратура, так как в обычном спектрометре их не было видно. Наиболее простым спектром обладал водород, самый легкий из элементов; поэтому его спектр был подвергнут анализу в первую очередь.
В 1885 г. Иоганн Бальмер получил формулу, описывающую четыре основные линии водородного спектра; сравнение этой формулы с другими линиями, открытыми немного позднее, показало, что она очень точно соответствует почти всему спектру водорода. Весь последующий спектральный анализ различных элементов основывался на этой формуле. Бальмер получил ее не из каких-то теоретических предположений, а просто подбирая несложное алгебраическое выражение, удовлетворяющее наблюдаемым фактам.
«Длины волн первых четырех водородных линий получаются умножением основного числа  последовательно на множители 9/5, 4/3, 25/21 и 9/8. На первый взгляд эти множители не образуют регулярной последовательности; но если умножить второе
последовательно на множители 9/5, 4/3, 25/21 и 9/8. На первый взгляд эти множители не образуют регулярной последовательности; но если умножить второе
и четвертое числа на 4, то получим регулярную последовательность: числители этих множителей равны 32, 42, 52, 62 , а знаменатели меньше соответствующих числителей на 4» [4].
Бальмер, однако, не добавил, что элементы поют: в этом отразился прогресс науки со времен Пифагора.
Формулу Бальмера можно представить в виде

где  — численная постоянная, о которой говорит Бальмер, равная 3645,6, если длина волны спектральной линии X измеряется в ангстремах [1 ангстрем (пишется
— численная постоянная, о которой говорит Бальмер, равная 3645,6, если длина волны спектральной линии X измеряется в ангстремах [1 ангстрем (пишется  , а
, а  целое число, принимающее значения 3, 4, 5, 6, каждому из которых соответствует определенная длина волны X, наблюдаемая в спектре водорода.
целое число, принимающее значения 3, 4, 5, 6, каждому из которых соответствует определенная длина волны X, наблюдаемая в спектре водорода.
Что это? Игра чисел? Астрология? Или черная магия? Возможно, что и то, и другое, и третье вместе. Тем не менее, и это было главным, каждому значению X, полученному по формуле

точно соответствовала наблюдаемая спектральная линия. Эта формула позволила систематизировать известные до этого данные и явилась тем алгебраическим выражением, которое должно вытекать из будущей теории (такими выражениями были в свое время формулы Кеплера для последовавшей затем теории Ньютона).
Пример. Проверим, что красной линии в спектре водорода соответствует значение 

Эта длина волны относится к красному участку спектра.
| << Предыдущий параграф | Следующий параграф >> |
- 28. АБСОЛЮТНОЕ ДВИЖЕНИЕ, АБСОЛЮТНЫЙ ПОКОЙ
- СИСТЕМЫ ОТСЧЕТА
- СВЕТОНОСНЫЙ ЭФИР
- 29. ОПЫТ МАЙКЕЛЬСОНА-МОРЛИ
- ИНТЕРФЕРОМЕТР
- РЕЗУЛЬТАТЫ
- 30. ПРИНЦИП ОТНОСИТЕЛЬНОСТИ
- ЗАГОВОР
- СКОРОСТЬ СВЕТА
- TEMPS PERDU
- О ПРОСТРАНСТВЕННЫХ И ВРЕМЕННЫХ ПРОМЕЖУТКАХ, ОПРЕДЕЛЯЕМЫХ В СИСТЕМАХ ОТСЧЕТА, РАВНОМЕРНО ДВИЖУЩИХСЯ ДРУГ ОТНОСИТЕЛЬНО ДРУГА
- ЗАМЕДЛЕНИЕ ВРЕМЕНИ
- СЛОЖЕНИЕ СКОРОСТЕЙ
- ДЕДУШКИНЫ ЧАСЫ ВО ВНЕШНЕМ ПРОСТРАНСТВЕ
- 31. ОБЪЕДИНЕНИЕ ЗАКОНОВ НЬЮТОНА И ПРИНЦИПА ОТНОСИТЕЛЬНОСТИ
- РЕЛЯТИВИСТСКОЕ СООТНОШЕНИЕ МЕЖДУ ЭНЕРГИЕЙ И ИМПУЛЬСОМ
- О ДВИЖЕНИИ РЕЛЯТИВИСТСКИХ ЭЛЕКТРОНОВ
- 32. ПАРАДОКС БЛИЗНЕЦОВ
- 33. ОБЩАЯ ТЕОРИЯ ОТНОСИТЕЛЬНОСТИ (ТЕОРИЯ ТЯГОТЕНИЯ ЭЙНШТЕЙНА)
- ПРИНЦИП ЭКВИВАЛЕНТНОСТИ
- СТРОЕНИЕ АТОМА
- 34. СЕРЕБРЯНЫЕ НИТИ
- ДИСКРЕТНЫЕ СПЕКТРАЛЬНЫЕ ЛИНИИ
- ИКС-ЛУЧИ
- РАДИОАКТИВНОСТЬ
- 35. ОТКРЫТИЕ ЭЛЕКТРОНА
- ЭЛЕКТРИЧЕСКОЕ СТРОЕНИЕ МАТЕРИИ
- АТОМ ТОМСОНА
- 36. АТОМ РЕЗЕРФОРДА
- 37. ИСТОКИ КВАНТОВОЙ ТЕОРИИ
- КВАНТ ДЕЙСТВИЯ МАКСА ПЛАНКА
- ФОТОН АЛЬБЕРТА ЭЙНШТЕЙНА
- ВОДОРОДНЫЙ АТОМ БОРА
- КВАНТОВАЯ ТЕОРИЯ
- 38. ЭЛЕКТРОН КАК ВОЛНА
- ОПЫТ ДЭВИССОНА — ДЖЕРМЕРА
- 39. УРАВНЕНИЕ ШРЕДИНГЕРА — ЗАКОН ДВИЖЕНИЯ ДЛЯ КВАНТОВЫХ СИСТЕМ
- СВОБОДНЫЕ РЕШЕНИЯ
- СВЯЗАННЫЕ РЕШЕНИЯ
- 40. ЧТО ТАКОЕ ВОЛНА ДЕ БРОЙЛЯ
- ИНТЕРПРЕТАЦИЯ ШРЕДИНГЕРА: ПЛОТНОСТЬ ВЕЩЕСТВА
- ВЕРОЯТНОСТНАЯ ИНТЕРПРЕТАЦИЯ
- ДРУГИЕ ВОЗМОЖНЫЕ ИНТЕРПРЕТАЦИИ
- 41. О ВНУТРЕННЕЙ СОГЛАСОВАННОСТИ КВАНТОВОМЕХАНИЧЕСКОЙ ТОЧКИ ЗРЕНИЯ
- ПРИНЦИП НЕОПРЕДЕЛЕННОСТИ ГЕЙЗЕНБЕРГА
- МЫСЛЕННЫЕ ЭКСПЕРИМЕНТЫ ГЕЙЗЕНБЕРГА
- О РОЛИ НЕНАБЛЮДАЕМЫХ ВЕЛИЧИН В ФИЗИЧЕСКОЙ ТЕОРИИ
- ДУАЛИЗМ ВОЛНА — ЧАСТИЦА
- 42. ПЕРЕХОД ОТ КВАНТОВОЙ ТОЧКИ ЗРЕНИЯ К КЛАССИЧЕСКОЙ
- МИР КВАНТОВ
- 43. АТОМ ВОДОРОДА
- О ПРИРОДЕ ВЫРОЖДЕНИЯ ЭНЕРГЕТИЧЕСКИХ УРОВНЕЙ КВАНТОВЫХ СИСТЕМ
- СФЕРИЧЕСКАЯ СИММЕТРИЯ КУЛОНОВСКОЙ СИЛЫ. АЗИМУТАЛЬНЫЕ КВАНТОВЫЕ ЧИСЛА
- УРОВНИ ЭНЕРГИИ АТОМА ВОДОРОДА
- ВЛИЯНИЕ МАГНИТНОГО ПОЛЯ
- СПИН ЭЛЕКТРОНА
- 44. ВЗАИМОДЕЙСТВИЕ ЧАСТИЦ И ФОТОНОВ С АТОМНЫМИ СИСТЕМАМИ
- СВЕТ
- ВЕРОЯТНОСТИ ПЕРЕХОДОВ
- 45. КВАНТОВЫЕ СИСТЕМЫ МНОГИХ ЧАСТИЦ
- СИММЕТРИЯ ВОЛНОВОЙ ФУНКЦИИ ОТНОСИТЕЛЬНО ПЕРЕСТАНОВКИ ТОЖДЕСТВЕННЫХ ЧАСТИЦ
- НЕВЗАИМОДЕЙСТВУЮЩИЕ ЭЛЕКТРОНЫ, ЗАКЛЮЧЕННЫЕ В СОСУДЕ, — ПРОСТЕЙШАЯ МОДЕЛЬ МЕТАЛЛА
- ПЕРИОДИЧЕСКАЯ ТАБЛИЦА ЭЛЕМЕНТОВ
- 46. АТОМНОЕ ЯДРО
- КАК ЯДЕРНЫЕ ЧАСТИЦЫ УДЕРЖИВАЮТСЯ ВМЕСТЕ?
- ЯДЕРНЫЕ СИЛЫ И МОДЕЛИ ЯДЕР
- ЯДЕРНЫЕ ПРОЦЕССЫ И УСТОЙЧИВОСТЬ
- ОГОНЬ ЗВЕЗД
- ОБЪЕДИНЕНИЕ КВАНТОВОЙ ТЕОРИИ И ПРИНЦИПА ОТНОСИТЕЛЬНОСТИ
- 47. ЭЛЕКТРОН КАК РЕЛЯТИВИСТСКАЯ ВОЛНА
- ЭЛЕКТРОН ДИРАКА
- ВАКУУМ ДИРАКА
- АНТИВЕЩЕСТВО
- 48. ВЗАИМОДЕЙСТВИЕ ЭЛЕКТРОНОВ И ФОТОНОВ
- ПРОСТРАНСТВЕННО-ВРЕМЕННЫЕ ДИАГРАММЫ
- КВАНТОВАЯ ЭЛЕКТРОДИНАМИКА
- РАДИАЦИОННЫЕ ПОПРАВКИ И МЕТОД ПЕРЕНОРМИРОВОК
- ПЕРВОМАТЕРИЯ
- 49. ЧТО ТАКОЕ ЭЛЕМЕНТАРНАЯ ЧАСТИЦА
- 50. КАК НАБЛЮДАЮТ ЭЛЕМЕНТАРНЫЕ ЧАСТИЦЫ
- 51. КАК СОЗДАЮТ ЭЛЕМЕНТАРНЫЕ ЧАСТИЦЫ
- 52. ЧТО УДЕРЖИВАЕТ ЧАСТИЦЫ ЯДРА ВМЕСТЕ
- 53. СТРАННЫЕ ЧАСТИЦЫ
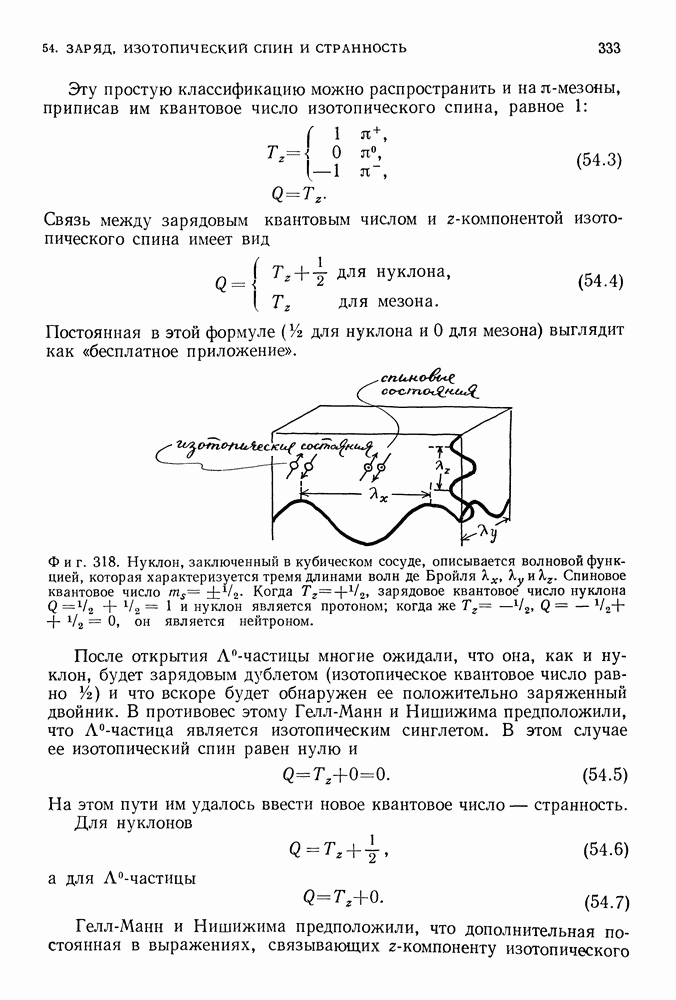
- 54. ЗАРЯД, ИЗОТОПИЧЕСКИЙ СПИН И СТРАННОСТЬ
- 55. СИММЕТРИЯ: ОТ ПИФАГОРА ДО ПАУЛИ
- 56. ПЕРВОМАТЕРИЯ
- ВОПРОСЫ И ЗАДАЧИ
- ОТВЕТЫ НА НЕКОТОРЫЕ ЗАДАЧИ
- ЛИТЕРАТУРА