| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
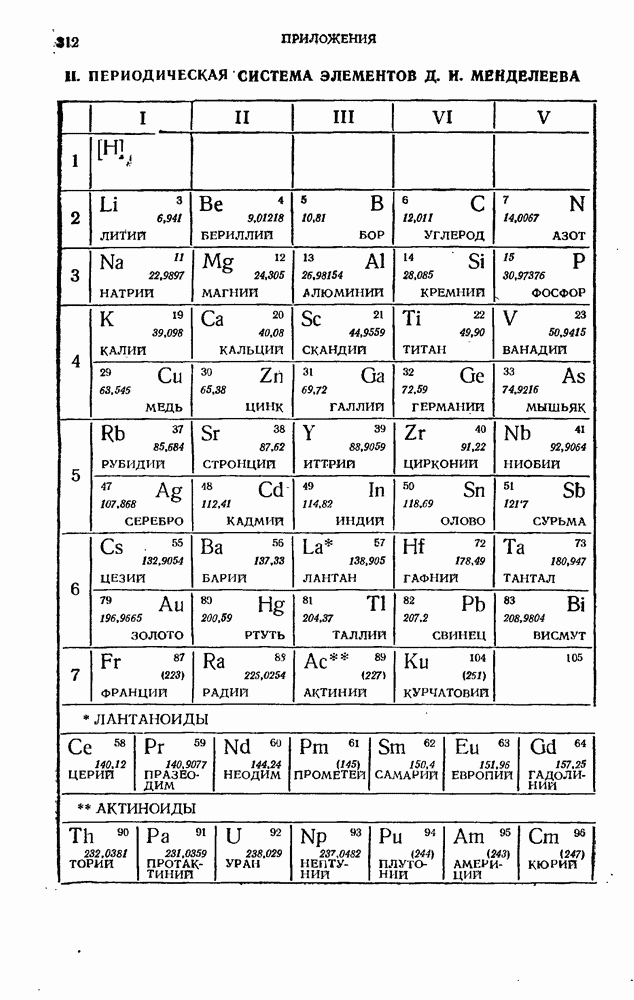
§ 37. Периодическая система элементов Менделеева
Принцип Паули дает объяснение периодической повторяемости свойств атомов. Проследим построение периодической системы элементов Д. И. Менделеева.
Начнем с атома водорода, имеющего один электрон. Каждый последующий атом будем получать, увеличивай заряд ядра предыдущего атома на единицу и добавляя один электрон, который мы будем помещать в доступное ему согласно принципу Паули состояние с наименьшей энергией.
В атоме водорода имеется в основном состоянии один  -электрон с произвольной ориентацией спина. Квантовые числа атома имеют значения:
-электрон с произвольной ориентацией спина. Квантовые числа атома имеют значения:  . Соответственно основной терм водородного атома имеет вид
. Соответственно основной терм водородного атома имеет вид 
Если заряд ядра атома водорода увеличить на единицу и добавить еще один электрон, получится атом гелия. Оба электрона в этом атоме могут находиться в  -оболочке, но с антипараллельной ориентацией спинов. Так называемая электронная конфигурация атома может быть записана как
-оболочке, но с антипараллельной ориентацией спинов. Так называемая электронная конфигурация атома может быть записана как  (два
(два  -электрона). Основным термом будет
-электрона). Основным термом будет  .
.
На атоме гелия заканчивается заполнение  -оболочки. Третий электрон атома лития может занять лишь уровень
-оболочки. Третий электрон атома лития может занять лишь уровень  (рис. 37.1). Получается электронная конфигурация
(рис. 37.1). Получается электронная конфигурация  . Основное состояние характеризуется квантовыми числами
. Основное состояние характеризуется квантовыми числами  . Поэтому основным термом, как и у водорода, будет
. Поэтому основным термом, как и у водорода, будет  . Третий электрон атома лития, занимая более высокий энергетический уровень, чем остальные два электрона, оказывается слабее, чем они, связанным с ядром атома. В результате он определяет оптические и химические свойства атома.
. Третий электрон атома лития, занимая более высокий энергетический уровень, чем остальные два электрона, оказывается слабее, чем они, связанным с ядром атома. В результате он определяет оптические и химические свойства атома.

Рис. 37.1.
У четвертого элемента, бериллия, полностью заполняется подоболочка  . У последующих шести элементов (В, С, N, О, F и Ne) происходит заполнение электронами подоболочки
. У последующих шести элементов (В, С, N, О, F и Ne) происходит заполнение электронами подоболочки  в результате чего неон имеет полностью заполненные оболочки К (двумя электронами) и L (восемью электронами), образующие устойчивую систему, подобную системе гелия, чем обусловливаются специфические свойства инертных газов.
в результате чего неон имеет полностью заполненные оболочки К (двумя электронами) и L (восемью электронами), образующие устойчивую систему, подобную системе гелия, чем обусловливаются специфические свойства инертных газов.
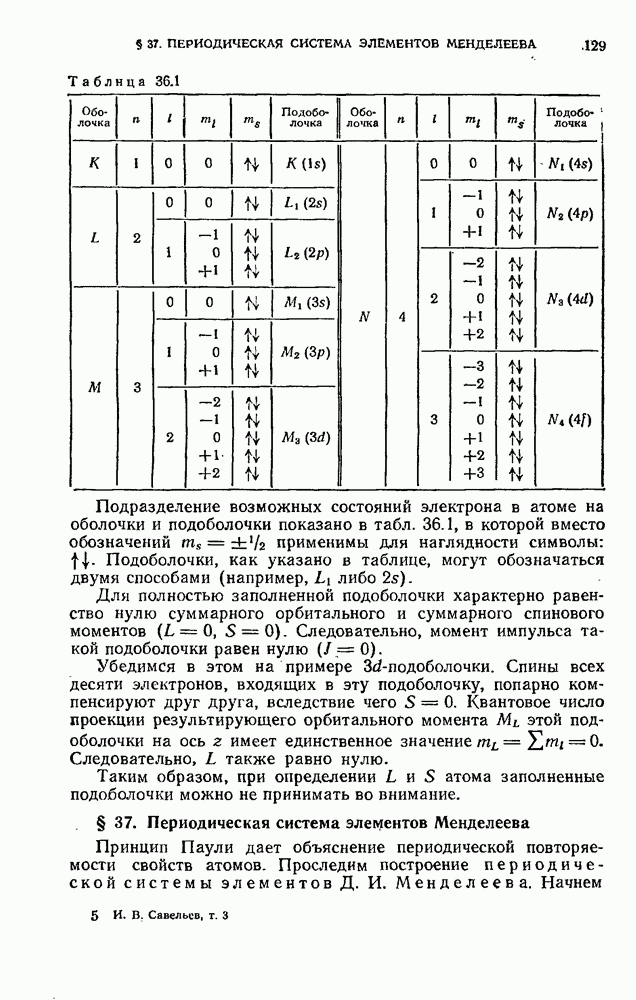
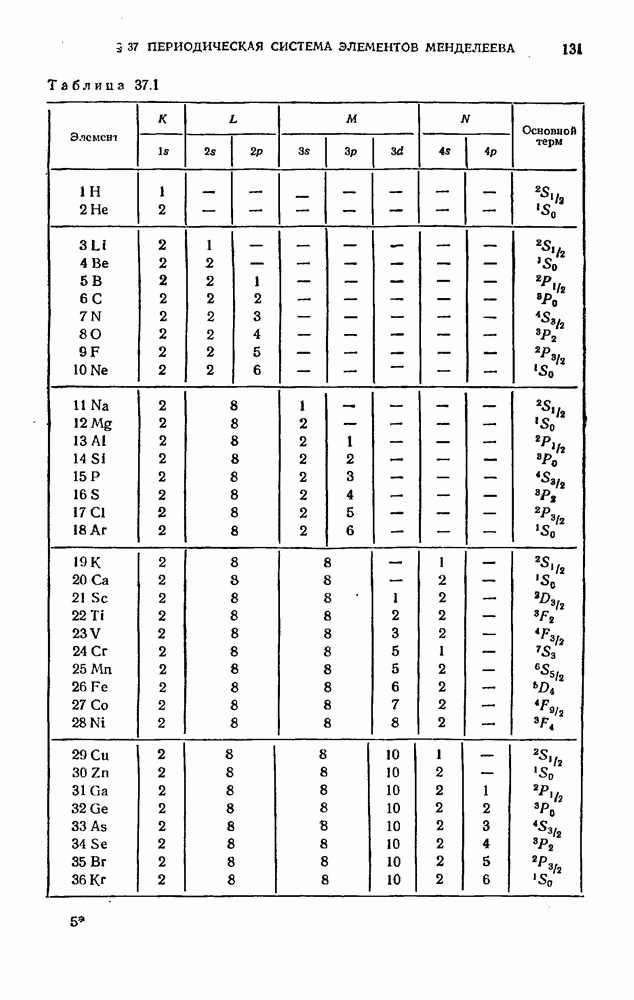
Процесс застройки электронных оболочек первых 36 элементов периодической системы представлен в табл. 37.1. Одиннадцатый элемент, натрий, имеет, кроме заполненных оболочек К и L, один электрон в подоболочке  Электронная конфигурация имеет вид:
Электронная конфигурация имеет вид:  Основным термом будет
Основным термом будет  Электрон
Электрон  связан с ядром слабее других и является валентным или оптическим электроном. В связи с этим химические и оптические свойства натрия подобны свойствам лития. Основное состояние оптического электрона в атоме натрия характеризуется значением
связан с ядром слабее других и является валентным или оптическим электроном. В связи с этим химические и оптические свойства натрия подобны свойствам лития. Основное состояние оптического электрона в атоме натрия характеризуется значением 
Таблица 37.1

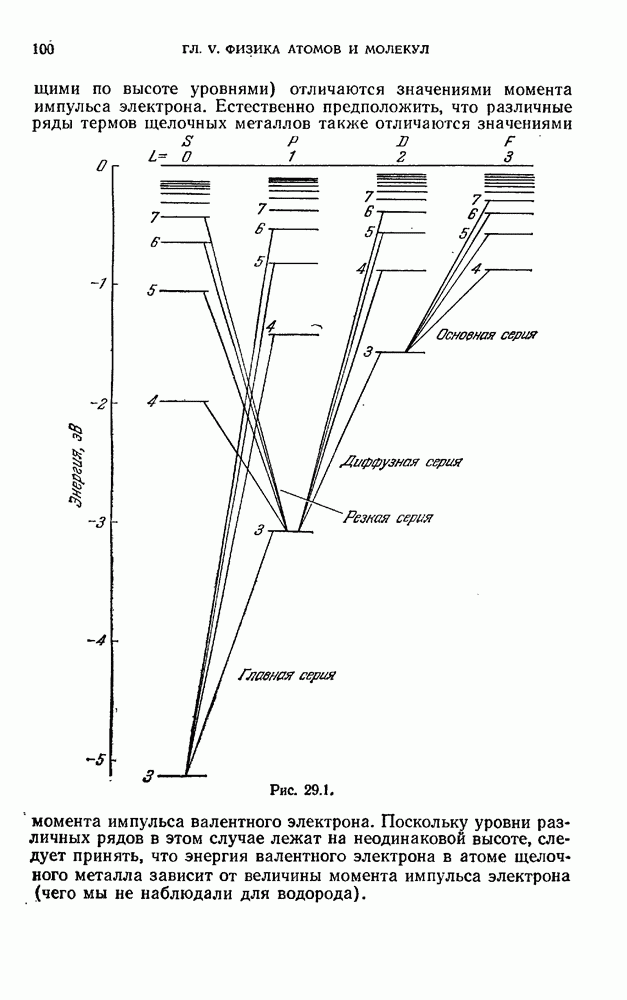
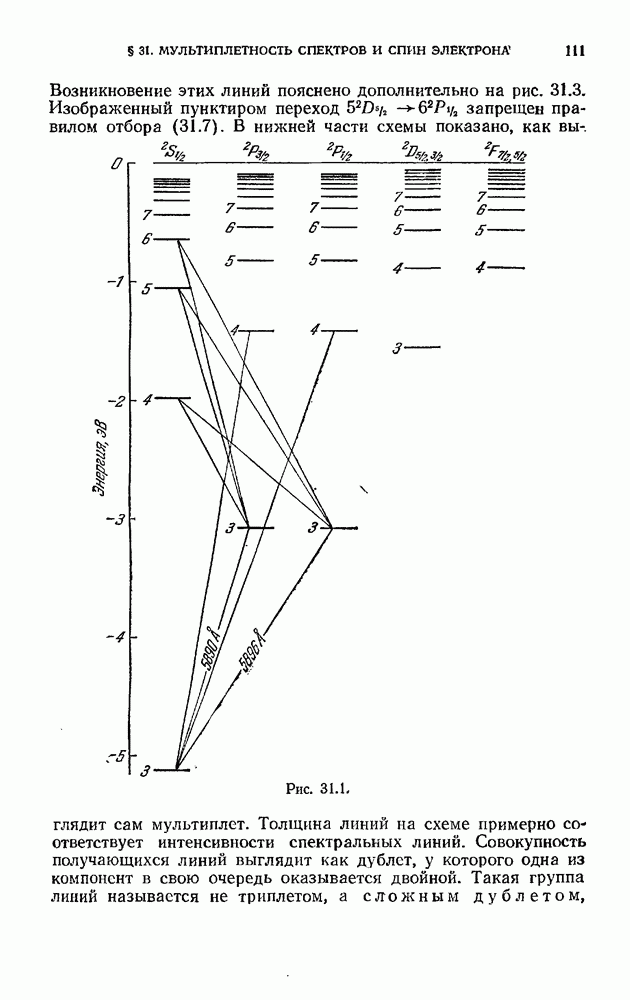
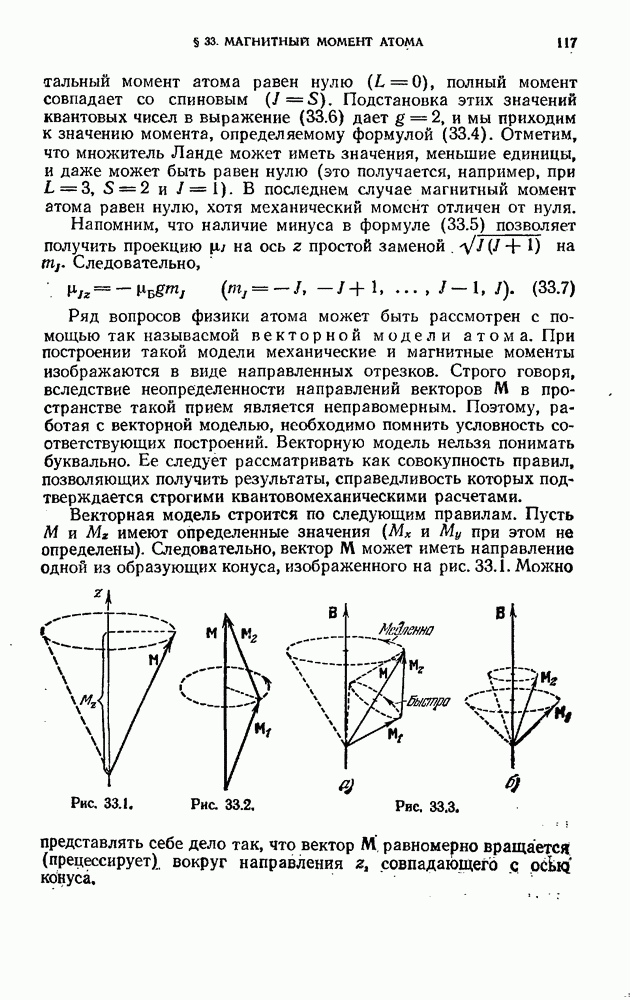
Этим и объясняется то обстоятельство, что на схеме уровней атома натрия (см. рис. 31.1) основной уровень помечен цифрой 3. Попутно отметим, что атом цезия имеет  основном состоянии электронную конфигурацию
основном состоянии электронную конфигурацию

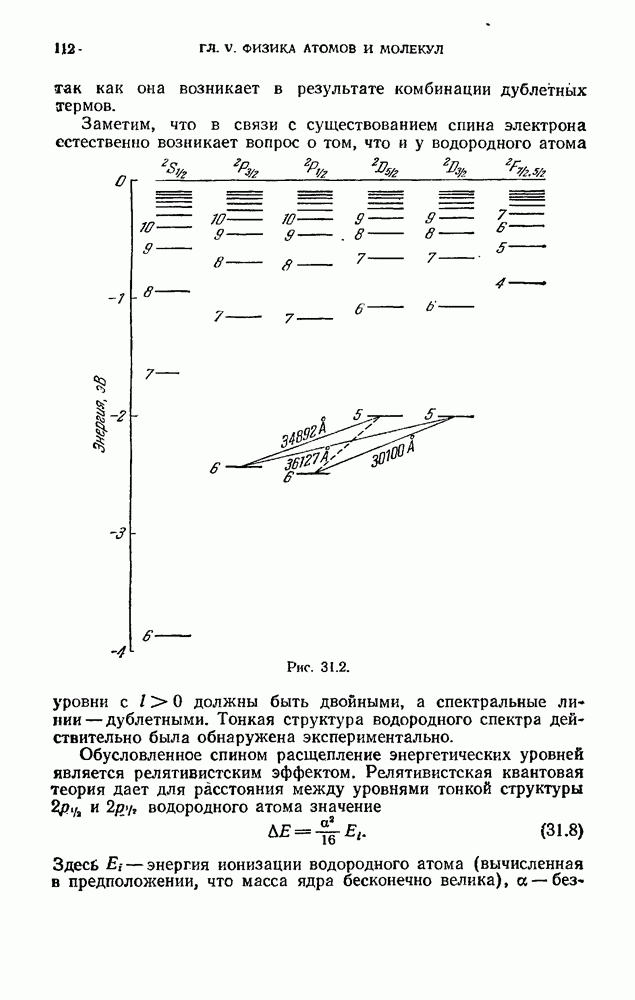
Следовательно, его оптический электрон имеет в основном состоянии  . В соответствии с этим помечены уровни на рис. 31.2.
. В соответствии с этим помечены уровни на рис. 31.2.
У следующих за натрием элементов нормально заполняются подоболочки  Подоболочка
Подоболочка  при данной общей конфигурации оказывается энергетически выше подоболочки
при данной общей конфигурации оказывается энергетически выше подоболочки  в связи с чем при незавершенном в целом заполнении оболочки М начинается заполнение оболочки N. Подоболочка
в связи с чем при незавершенном в целом заполнении оболочки М начинается заполнение оболочки N. Подоболочка  лежит уже выше, чем
лежит уже выше, чем  так что после
так что после  заполняется подоболочка
заполняется подоболочка 
С аналогичными отступлениями от обычной последовательности, повторяющимися время от времени, осуществляется застройка электронных уровней всех атомов. При этом периоди» чески повторяются сходные электронные конфигурации (например,  и т. д.) сверх полностью заполненных подоболочек, чем обусловливается периодическая повторяемость химических и оптических свойств атомов.
и т. д.) сверх полностью заполненных подоболочек, чем обусловливается периодическая повторяемость химических и оптических свойств атомов.
При установлении вида термов, возможных при заданной электронной конфигурации, нужно иметь в виду, что принцип Паули разрешает не все сочетания значений L и S, которые вытекают из конфигурации. Так, например, при конфигурации  (два электрона с главным квантовым числом
(два электрона с главным квантовым числом  ) возможными значениями L будут 0, 1, 2, a S может иметь значения 0 и 1. В соответствии с этим, казалось бы, возможны термы
) возможными значениями L будут 0, 1, 2, a S может иметь значения 0 и 1. В соответствии с этим, казалось бы, возможны термы

Однако согласно принципу Паули разрешены лишь такие термы, для которых значения хотя бы одного из квантовых чисел  эквивалентных электронов (т. е. электронов с одинаковыми
эквивалентных электронов (т. е. электронов с одинаковыми  ) не совпадают. Этому требованию не удовлетворяет, например, терм
) не совпадают. Этому требованию не удовлетворяет, например, терм  Действительно,
Действительно,  означает, что орбитальные моменты электронов «параллельны», следовательно, значения
означает, что орбитальные моменты электронов «параллельны», следовательно, значения  у этих электронов будут совпадать. Аналогично
у этих электронов будут совпадать. Аналогично  означает, что спины электронов также «параллельны», вследствие чего совпадают и значения
означает, что спины электронов также «параллельны», вследствие чего совпадают и значения  . В итоге все четыре квантовых числа
. В итоге все четыре квантовых числа  у обоих электронов оказываются одинаковыми, что противоречит принципу Паули. Таким образом, терм
у обоих электронов оказываются одинаковыми, что противоречит принципу Паули. Таким образом, терм  в системе из двух эквивалентных электронов реализоваться не может.
в системе из двух эквивалентных электронов реализоваться не может.
Чтобы установить разрешенные принципом Паули термы эквивалентных электронов, используют следующий прием: в столб  таблицы, помеченных значениями
таблицы, помеченных значениями  отдельно взятого электрона, проставляют в виде стрелок значения
отдельно взятого электрона, проставляют в виде стрелок значения  (стрелка вверх означает
(стрелка вверх означает  стрелка вниз —
стрелка вниз —  ) (см. табл. 37.2, составленную для двух эквивалентных
) (см. табл. 37.2, составленную для двух эквивалентных  -электронов).
-электронов).
Таблица 37.2.

В таблице содержатся все допустимые принципом Паули сочетания значений  обоих электронов. В тех случаях, когда обе стрелки попадают в один столбец (это означает, что
обоих электронов. В тех случаях, когда обе стрелки попадают в один столбец (это означает, что  обоих электронов одинаково), они направлены в противоположные стороны
обоих электронов одинаково), они направлены в противоположные стороны  должны быть разными). В следующих столбцах таблицы проставлены соответствующие данному сочетанию значения квантовых чисел
должны быть разными). В следующих столбцах таблицы проставлены соответствующие данному сочетанию значения квантовых чисел  равные алгебраической сумме чисел
равные алгебраической сумме чисел  Совокупность допустимых значений
Совокупность допустимых значений  позволяет установить допустимые сочетания значений L и S. Одна из таких совокупностей, помеченная буквой А в последнем столбце таблицы, соответствует сочетанию
позволяет установить допустимые сочетания значений L и S. Одна из таких совокупностей, помеченная буквой А в последнем столбце таблицы, соответствует сочетанию  т. е. терму
т. е. терму  вторая совокупность, помеченная буквой В, соответствует
вторая совокупность, помеченная буквой В, соответствует  , т. е. терму
, т. е. терму  и, наконец, совокупность, помеченная буквой С, соответствует
и, наконец, совокупность, помеченная буквой С, соответствует  , т. е. терму S. Таким образом, из указанных в (37.1) шести формально возможных термов не противоречат принципу Паули только три:
, т. е. терму S. Таким образом, из указанных в (37.1) шести формально возможных термов не противоречат принципу Паули только три:  причем терм
причем терм  является триплетом — он подразделяется на компоненты:
является триплетом — он подразделяется на компоненты: 
Теперь возникает вопрос, какой из термов

соответствует основному состоянию, т. е. состоянию с наименьшей энергией. Ответ на этот вопрос дают два эмпирических правила Хунда:
1. Из термов, принадлежащих данной электронной конфигурации, наименьшей энергией обладает терм с наибольшим возможным значением S и с наибольшим возможным при таком S значением 
2. Мультиплеты, образованные эквивалентными электронами, являются правильными (это значит, что с увеличением  возрастает энергия состояния), если заполнено не более половины подоболочки, и обращенными (с увеличением
возрастает энергия состояния), если заполнено не более половины подоболочки, и обращенными (с увеличением  энергия убывает), если заполнено больше половины подоболочки.
энергия убывает), если заполнено больше половины подоболочки.
Из второго правила Хунда следует, что в случае, когда заполнено не более половины подоболочки, наименьшей энергией обладает компонента мультиплета с  в противном случае — компонента с
в противном случае — компонента с 
Согласно первому правилу Хунда из числа термов (37.2) наименьшей энергией должен обладать один из Р-термов (у этих термов наибольшее S). При конфигурации  подоболочка
подоболочка  заполнена только на
заполнена только на  т. е. меньше чем наполовину. Следовательно, согласно второму правилу Хунда наименьшей энергией обладает терм с наименьшим значением
т. е. меньше чем наполовину. Следовательно, согласно второму правилу Хунда наименьшей энергией обладает терм с наименьшим значением  т. е. терм
т. е. терм  Этот терм и является основным для конфигурации
Этот терм и является основным для конфигурации  (см.
(см.  в табл. 37.1).
в табл. 37.1).
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
- ЧАСТЬ 1. КВАНТОВАЯ ОПТИКА
- § 1. Тепловое излучение и люминесценция
- § 2. Закон Кирхгофа
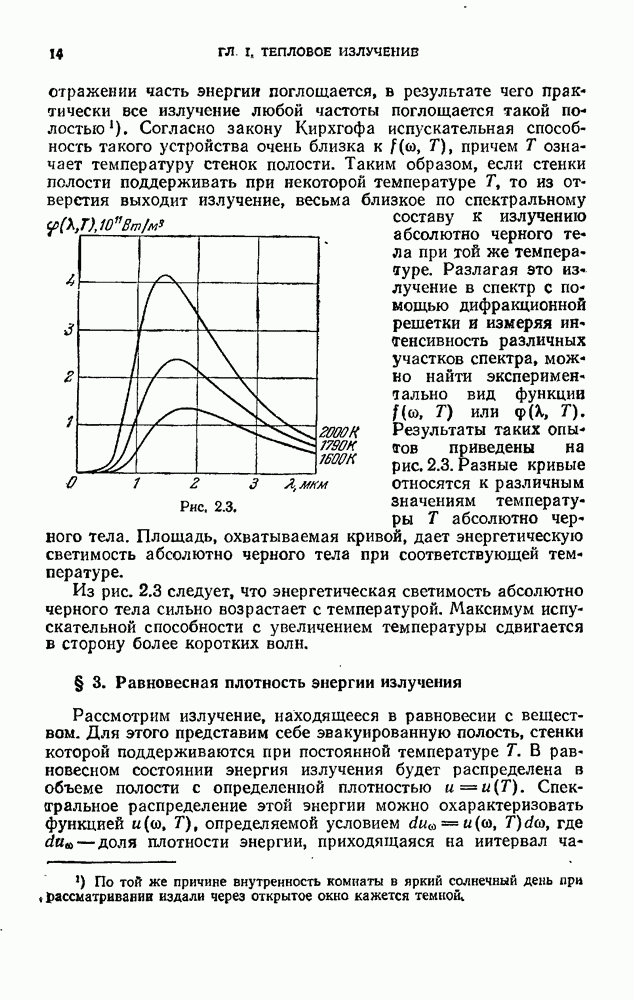
- § 3. Равновесная плотность энергии излучения
- § 4. Закон Стефана — Больцмана и закон Вина
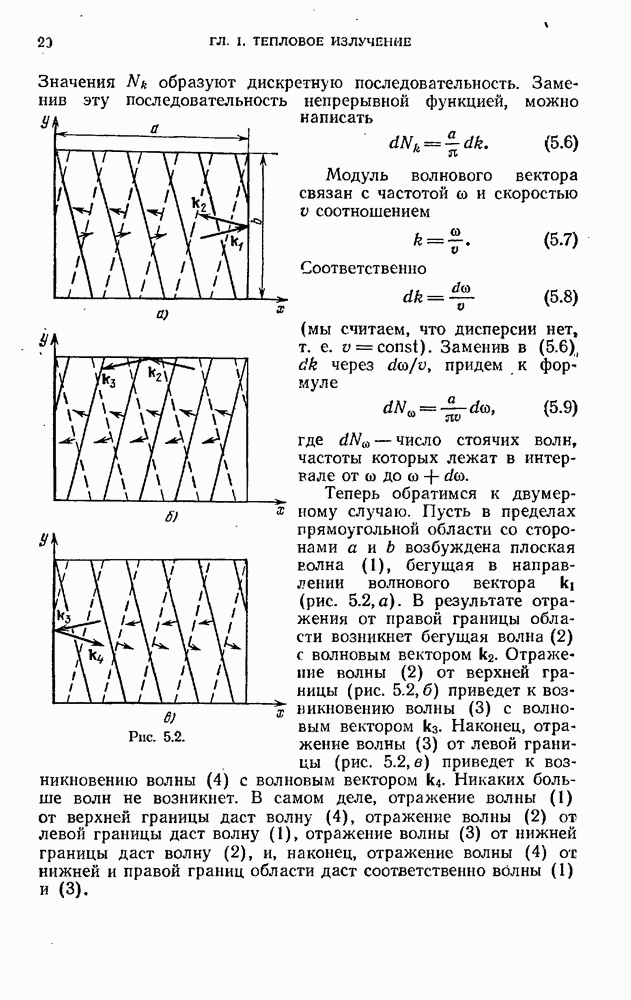
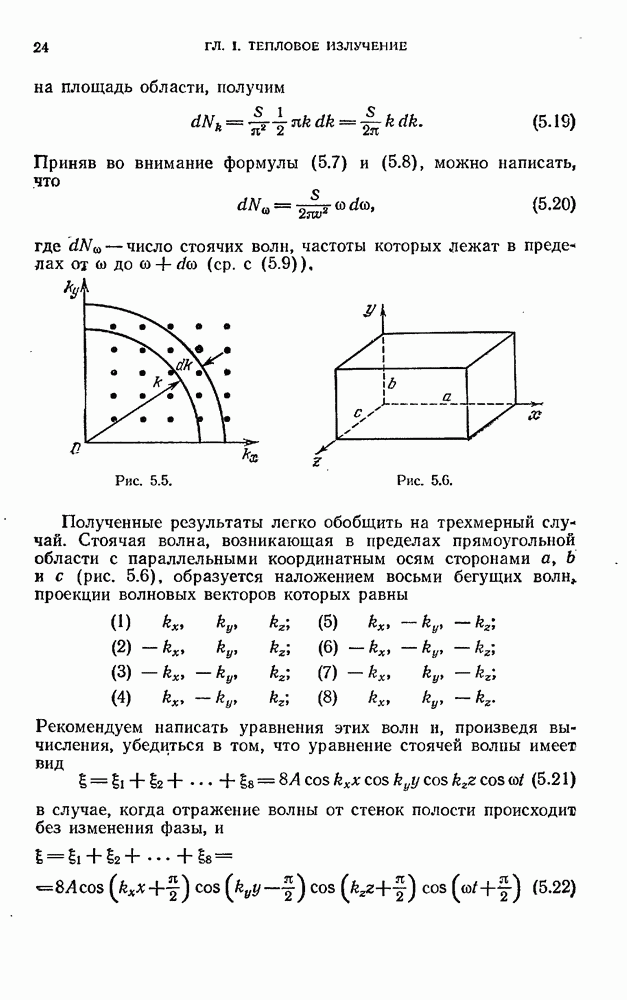
- § 5. Стоячие волны в пространстве трех измерений
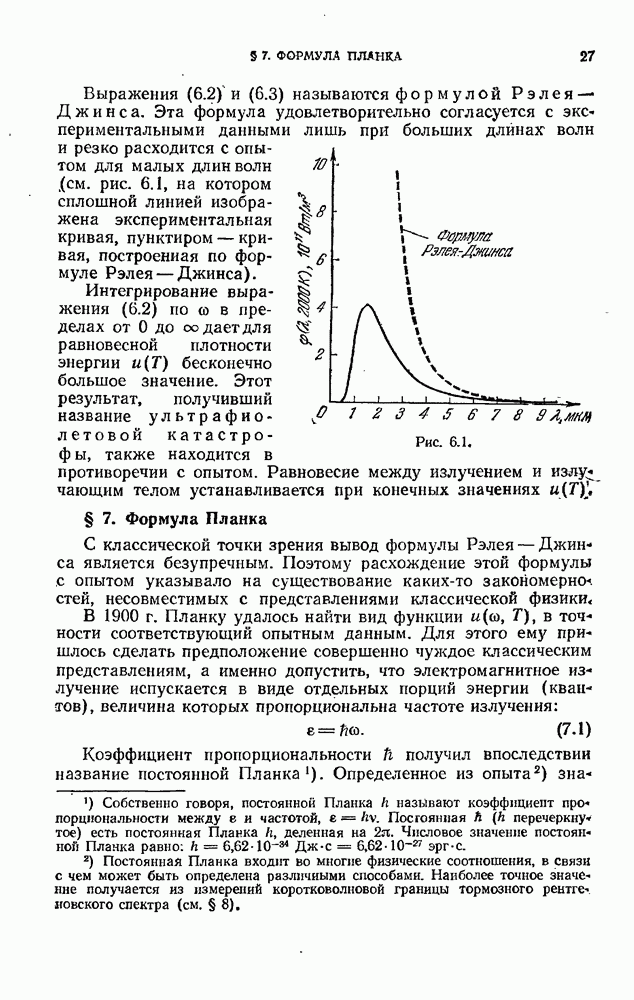
- § 6. Формула Рэлея — Джинса
- § 7. Формула Планка
- ГЛАВА II. ФОТОНЫ
- § 8. Тормозное рентгеновское излучение
- § 9. Фотоэффект
- § 10. Опыт Боте. Фотоны
- § 11. Эффект Комптона
- ЧАСТЬ 2. АТОМНАЯ ФИЗИКА
- § 12. Закономерности в атомных спектрах
- § 13. Модель атома Томсона
- § 14. Опыты по рассеянию а-частиц. Ядерная модель атома
- § 15. Постулаты Бора. Опыт Франка и Герца
- § 16. Правило квантования круговых орбит
- § 17. Элементарная боровская теория водородного атома
- ГЛАВА IV. ЭЛЕМЕНТЫ КВАНТОВОЙ МЕХАНИКИ
- § 18. Гипотеза де-Бройля. Волновые свойства вещества
- § 19. Необычные свойства микрочастиц
- § 20. Принцип неопределенности
- § 21. Уравнение Шрёдингера
- § 22. Смысл пси-функции
- § 23. Квантование энергии
- § 24. Квантование момента импульса
- § 25. Принцип суперпозиции
- § 26. Прохождение частиц через потенциальный барьер
- § 27. Гармонический осциллятор
- ГЛАВА V. ФИЗИКА АТОМОВ И МОЛЕКУЛ
- § 28. Атом водорода
- § 29. Спектры щелочных металлов
- § 30. Ширина спектральных линий
- § 31. Мультиплетность спектров и спин электрона
- § 32. Результирующий механический момент многоэлектронного атома
- § 33. Магнитный момент атома
- § 34. Эффект Зеемана
- § 35. Электронный парамагнитный резонанс
- § 36. Принцип Паули. Распределение электронов по энергетическим уровням атома
- § 37. Периодическая система элементов Менделеева
- § 38. Рентгеновские спектры
- § 39. Энергия молекулы
- § 40. Молекулярные спектры
- § 41. Комбинационное рассеяние света
- § 42. Вынужденное излучение
- § 43. Лазеры
- § 44. Нелинейная оптика
- ЧАСТЬ 3. ФИЗИКА ТВЕРДОГО ТЕЛА
- § 45. Кристаллическая решетка. Индексы Миллера
- § 46. Теплоемкость кристаллов. Теория Эйнштейна
- § 47. Колебания систем с большим числом степеней свободы
- § 48. Теория Дебая
- § 49. Фононы
- § 50. Эффект Мёссбауэра
- ГЛАВА VII. ЗОННАЯ ТЕОРИЯ ТВЕРДЫХ ТЕЛ
- § 51. Квантовая теория свободных электронов в металле
- § 52. Распределение Ферми — Дирака
- § 53. Энергетические зоны в кристаллах
- § 54. Динамика электронов в кристаллической решетке
- ГЛАВА VIII. ЭЛЕКТРОПРОВОДНОСТЬ МЕТАЛЛОВ И ПОЛУПРОВОДНИКОВ
- § 55. Электропроводность металлов
- § 56. Сверхпроводимость
- § 57. Полупроводники
- § 58. Собственная проводимость полупроводников
- § 59. Примесная проводимость полупроводников
- ГЛАВА IX. КОНТАКТНЫЕ И ТЕРМОЭЛЕКТРИЧЕСКИЕ ЯВЛЕНИЯ
- § 60. Работа выхода
- § 61. Термоэлектронная эмиссия. Электронные лампы
- § 62. Контактная разность потенциалов
- § 63. Термоэлектрические явления
- § 64. Полупроводниковые диоды и триоды
- § 65. Внутренний фотоэффект
- ЧАСТЬ 4. ФИЗИКА АТОМНОГО ЯДРА И ЭЛЕМЕНТАРНЫХ ЧАСТИЦ
- § 66. Состав и характеристики атомного ядра
- § 67. Масса и энергия связи ядра
- § 68. Модели атомного ядра
- § 69. Ядерные силы
- § 70. Радиоактивность
- § 71. Ядерные реакции
- § 72. Деление ядер
- § 73. Термоядерные реакции
- ГЛАВА XI. ЭЛЕМЕНТАРНЫЕ ЧАСТИЦЫ
- § 74. Виды взаимодействий и классы элементарных частиц
- § 75. Методы регистрации элементарных частиц
- § 76. Космические лучи
- § 77. Частицы и античастицы
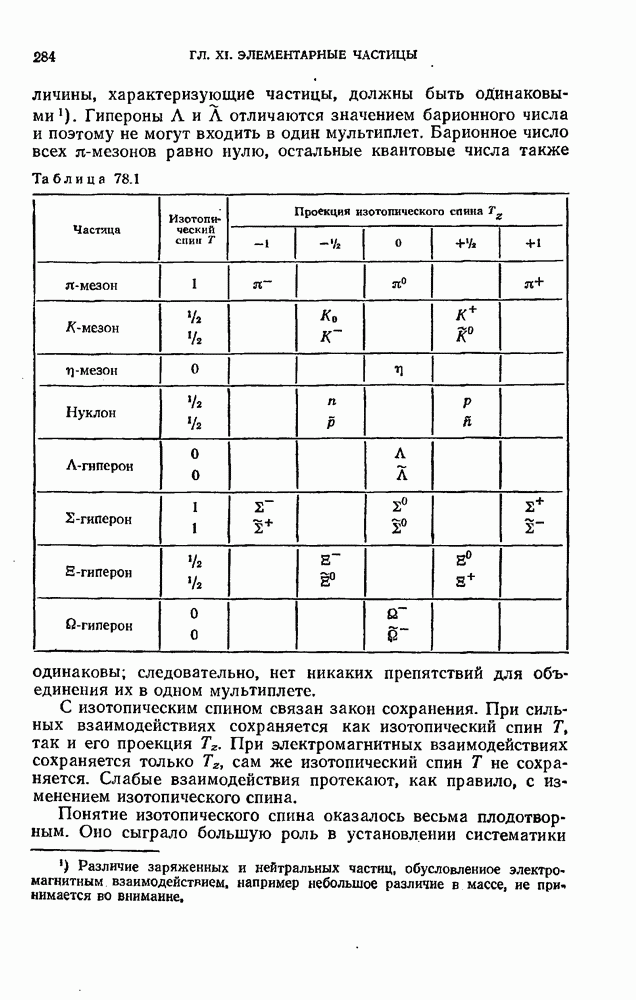
- § 78. Изотопический спин
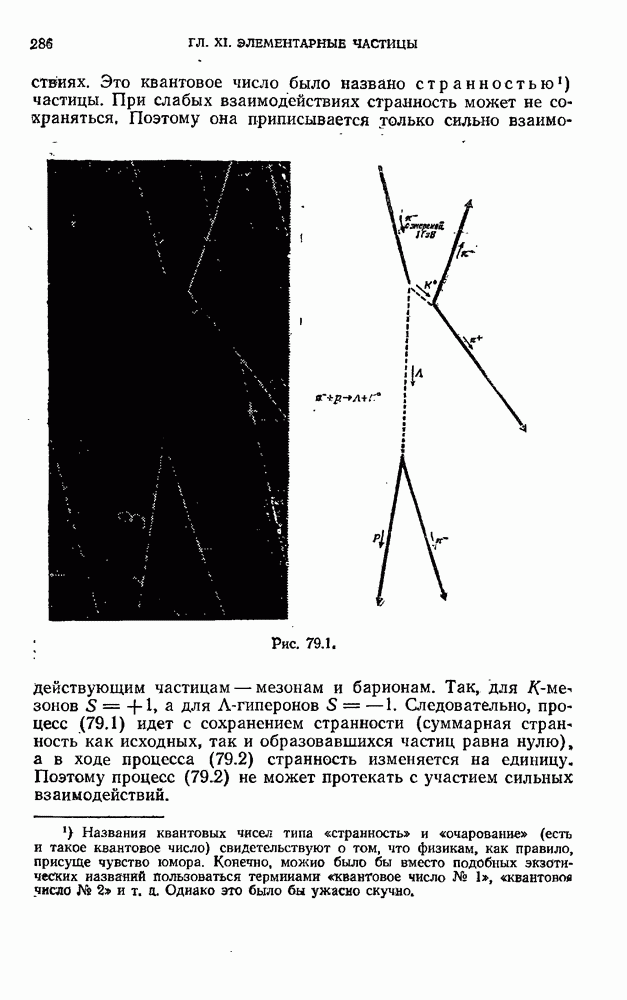
- § 79. Странные частицы
- § 80. Несохранение четности в слабых взаимодействиях
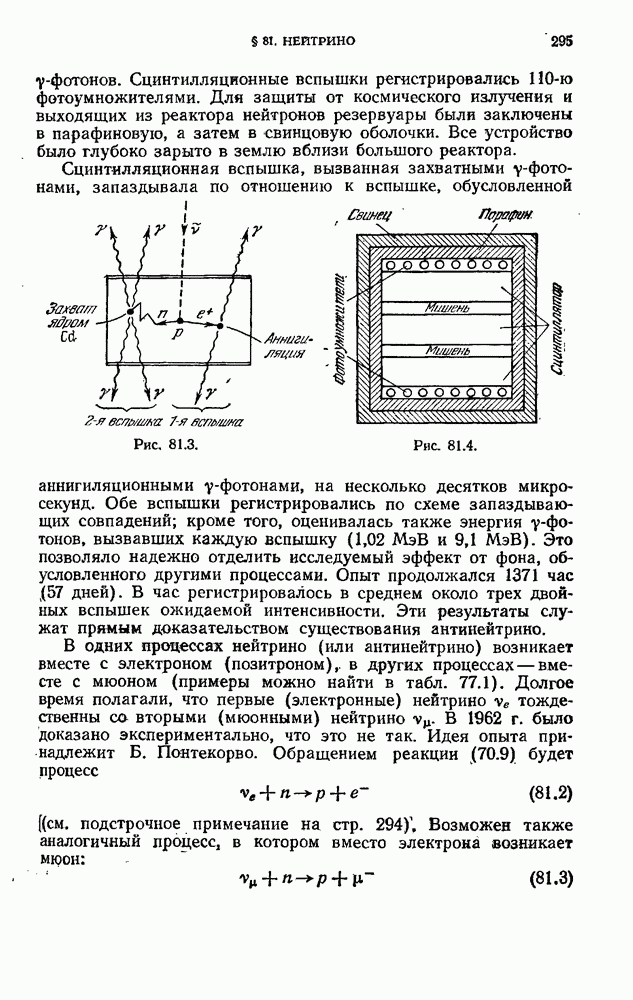
- § 81. Нейтрино
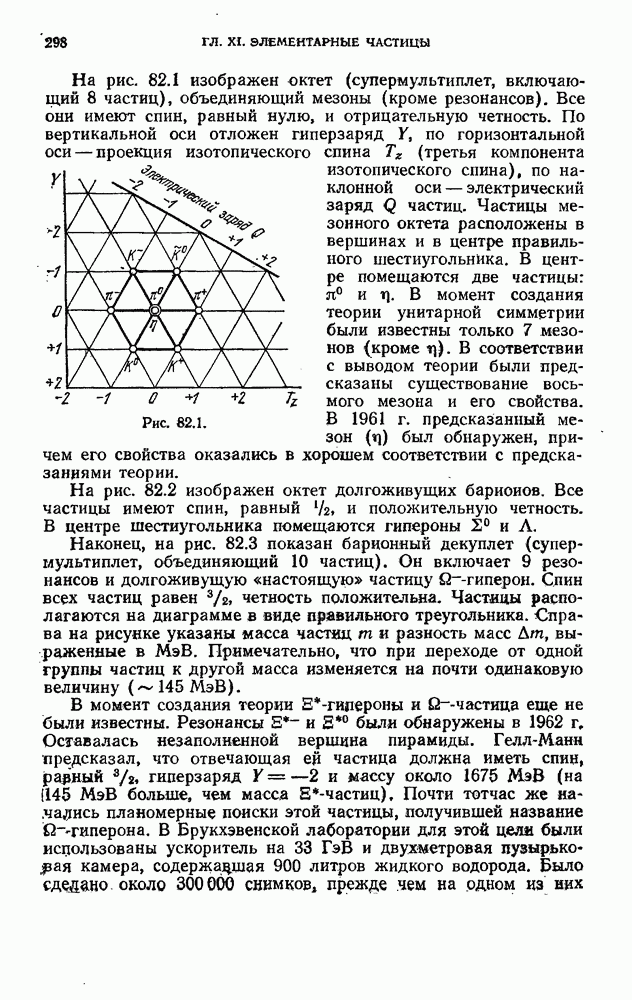
- § 82. Систематика элементарных частиц
- § 83. Кварки
- § 84. Великое объединение
- ПРИЛОЖЕНИЯ
- I. ГРАВИТАЦИОННОЕ ВЗАИМОДЕЙСТВИЕ