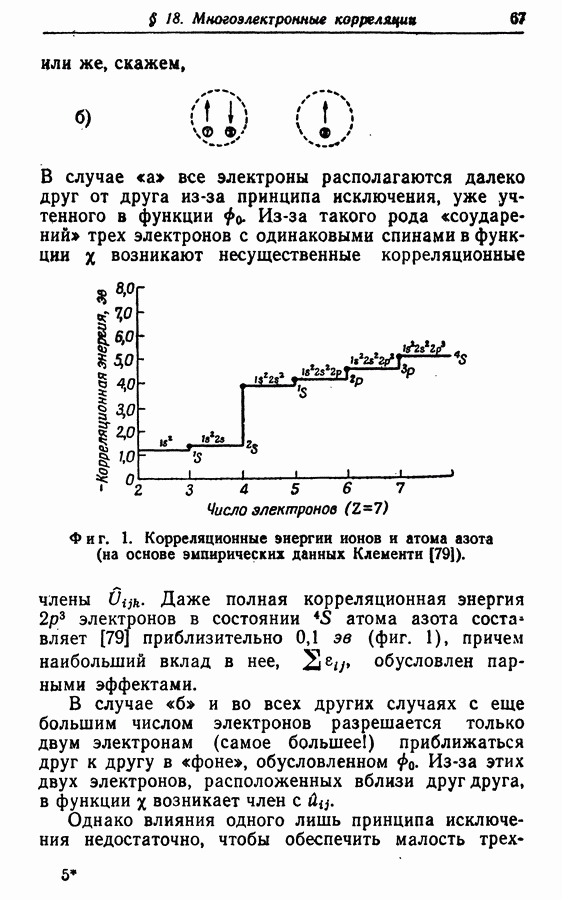
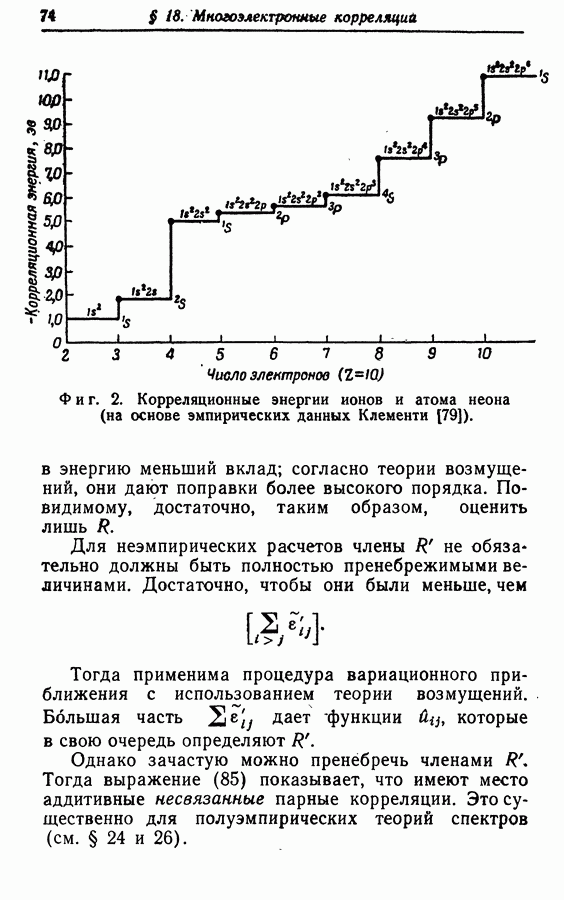
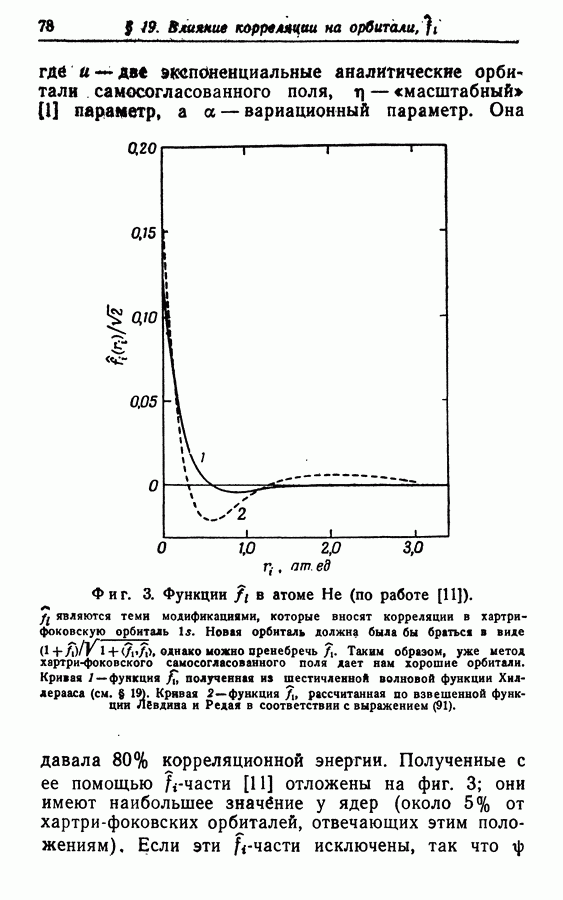
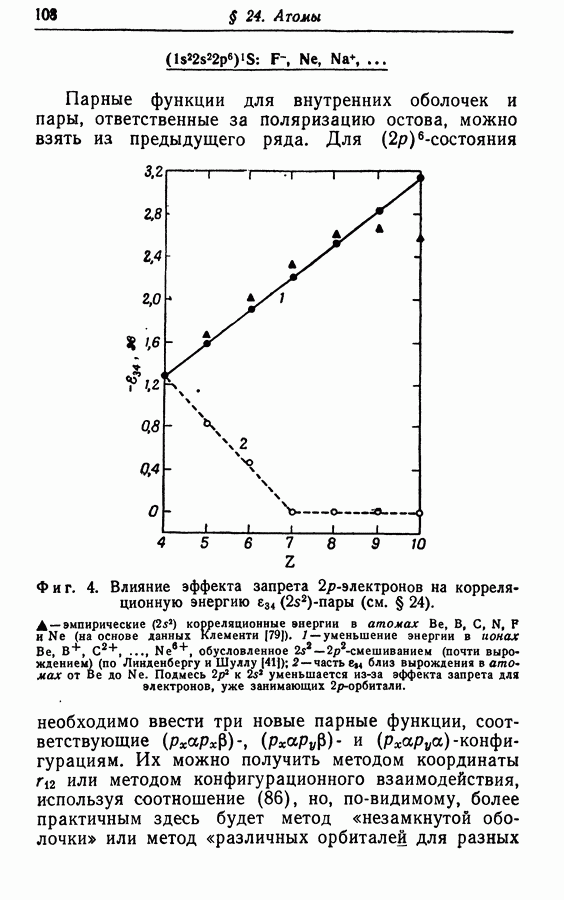
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 10. ОРТОГОНАЛЬНОСТЬ ОРБИТАЛЕЙ
Выражения (24) фактически заключают в себе два различных эффекта [8]: каждая функция  является ортогональной
является ортогональной
а) к своим собственным орбиталям 
б) ко всем другим орбиталям  занятым в
занятым в 
Эффект  связан с тем, что в (24) выделяются корреляции меньшего числа электронов, чем в
связан с тем, что в (24) выделяются корреляции меньшего числа электронов, чем в  [как и в уравнениях (32) и (35)]. Это особенно существенно в
[как и в уравнениях (32) и (35)]. Это особенно существенно в  когда выделены
когда выделены  Одноэлектронные члены
Одноэлектронные члены  описывают влияние корреляций на орбитали (см. также § 19).
описывают влияние корреляций на орбитали (см. также § 19).
Чтобы разъяснить этот вопрос, рассмотрим атом гелия. В этом случае

есть хартри-фоковский детерминант  -состояния. Для
-состояния. Для  точной волновой функции
точной волновой функции  -терма —
-терма —
имеем

где

[из соотношения (18)]. Применяя выражения  получаем
получаем

Например,

и

На языке метода конфигурационного взаимодействия функции  являются суммами отдельных возбуждений, а функции
являются суммами отдельных возбуждений, а функции  только двойных возбуждений [3, 8]. С помощью полного базисного набора
только двойных возбуждений [3, 8]. С помощью полного базисного набора  ряд в методе конфигурационного взаимодействия записываем [1, 3] в виде
ряд в методе конфигурационного взаимодействия записываем [1, 3] в виде

Умножая это выражение на  и интегрируя, получаем
и интегрируя, получаем

следовательно,

и

Эти соотношения поясняют, каким образом выражения (20) и (24) можно проверить, применяя метод конфигурационного взаимодействия.
Из этого примера видно, что эффект  упомянутый выше, не имеет места в атоме гелия и оказывается возможным лишь в многоэлектронной системе. Пусть мы имеем
упомянутый выше, не имеет места в атоме гелия и оказывается возможным лишь в многоэлектронной системе. Пусть мы имеем

Это означает, что когда электроны  коррелируют, т. е. «сталкиваются» друг с другом, то из-за принципа исключения Паули они не могут оказаться в состоянии
коррелируют, т. е. «сталкиваются» друг с другом, то из-за принципа исключения Паули они не могут оказаться в состоянии  уже занятом в
уже занятом в  отсюда — термин «эффект запрета» [3, 8]. В методе конфигурационного взаимодействия это означает, что для случая более чем двух электронов последняя сумма из выражения (43) начинается с номеров, больших
отсюда — термин «эффект запрета» [3, 8]. В методе конфигурационного взаимодействия это означает, что для случая более чем двух электронов последняя сумма из выражения (43) начинается с номеров, больших 

| << Предыдущий параграф | Следующий параграф >> |
- ОТ РЕДАКТОРА ПЕРЕВОДА
- § 1. ВВЕДЕНИЕ
- § 2. НЕОБХОДИМОСТЬ «МНОГОЭЛЕКТРОННОЙ ТЕОРИИ»
- § 3. ПОЛУЭМПИРИЧЕСКИЕ ТЕОРИИ
- § 4. НЕЭМПИРИЧЕСКИЕ ТЕОРИИ
- § 5. СХЕМА ПОСТРОЕНИЯ «МНОГОЭЛЕКТРОННОЙ ТЕОРИИ»
- § 6. ОРБИТАЛИ
- § 7. АНТИСИММЕТРИЯ И ОТНОСИТЕЛЬНЫЕ ЭЛЕКТРОННЫЕ РАСПРЕДЕЛЕНИЯ
- § 8. УРАВНЕНИЯ ХАРТРИ — ФОКА
- § 9. ТОЧНАЯ МНОГОЭЛЕКТРОННАЯ ВОЛНОВАЯ ФУНКЦИЯ
- § 10. ОРТОГОНАЛЬНОСТЬ ОРБИТАЛЕЙ
- § 11. НЕСВЯЗАННЫЕ КОМПЛЕКСЫ
- § 12. ВАРИАЦИОННЫЙ ПРИНЦИП И ТОЧНАЯ ЭНЕРГИЯ
- § 13. РАЗЛИЧНЫЕ КОРРЕЛЯЦИОННЫЕ ЭФФЕКТЫ В ТОЧНОЙ ВОЛНОВОЙ ФУНКЦИИ И ЭНЕРГИИ
- § 14. ВАРИАЦИОННЫЙ ПОДХОД, ИСПОЛЬЗУЮЩИЙ ТЕОРИЮ ВОЗМУЩЕНИЙ
- § 15. РАЗЛИЧНЫЕ ТЕОРИИ МНОГИХ ЧАСТИЦ
- § 16. ВОЛНОВАЯ ФУНКЦИЯ «МНОГОЭЛЕКТРОННОЙ ТЕОРИИ»
- § 17. ВАРИАЦИОННАЯ ЭНЕРГИЯ «МНОГОЭЛЕКТРОННОЙ ТЕОРИИ»
- § 18. МНОГОЭЛЕКТРОННЫЕ КОРРЕЛЯЦИИ
- § 19. ВЛИЯНИЕ КОРРЕЛЯЦИИ НА ОРБИТАЛИ
- § 20. НЕЗАМКНУТЫЕ ОБОЛОЧКИ
- § 21. ПОЧТИ ВЫРОЖДЕННЫЕ СОСТОЯНИЯ
- § 22. ПАРНЫЕ КОРРЕЛЯЦИИ
- § 23. СВОЙСТВА СИММЕТРИИ
- § 24. АТОМЫ
- § 25. МАЛЫЕ МОЛЕКУЛЫ
- § 26. «пи»-ЭЛЕКТРОННЫЕ СИСТЕМЫ
- § 27. СВЯЗИ-ЛОКАЛИЗАЦИЯ, ОТДЕЛЬНЫЕ ПАРЫ, ИОННЫЕ ОСТОВЫ
- § 28. ВАНДЕРВААЛЬСОВЫ ПРИТЯЖЕНИЯ
- § 29. РЕЛЯТИВИСТСКИЕ ЭФФЕКТЫ
- § 30. ЗАКЛЮЧЕНИЕ
- ДОПОЛНЕНИЕ АВТОРА