| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ЗАДАЧИ И УПРАЖНЕНИЯ
Уровень 1
165. Приведите пример термохимического уравнения.
166. Что называют теплотой: а) образования; б) разложения; в) сгорания вещества? В каких единицах ее выражают?
167. При стандартных условиях теплота полного сгорания белого фосфора равна 760,1 кДж/моль, а теплота полного сгорания черного фосфора равна 722,1 кДж/моль. Чему равна теплота превращения черного фосфора в белый при стандартных условиях?
168. Как формулируется основное положение химической кинетики? Каков физический смысл константы скорости химической реакции?
169. От каких факторов зависит скорость: а) гомогенной; б) гетерогенной химической реакции?
170. Приведите пример кинетического уравнения.
171. В результате некоторой реакции в единице объема в единицу времени образовалось 3,4 г аммиака, а в результате другой реакции в тех же условиях — 3,4 г фосфина.
Одинаковы ли скорости этих реакций? Ответ поясните.
172. Как изменится скорость образования оксида азота (IV) в соответствии с реакцией:  если давление в системе увеличить в 3 раза, а температуру оставить неизменной?
если давление в системе увеличить в 3 раза, а температуру оставить неизменной?
173. Скорость некоторой реакции увеличивается в 2,5 раза при повышении температуры на каждые  в интервале от 0 до
в интервале от 0 до  . Во сколько раз увеличится скорость при повышении температуры от 20 до
. Во сколько раз увеличится скорость при повышении температуры от 20 до 
174. Как действует катализатор на химическое равновесие?
175. Как будет влиять увеличение температуры на состояние равновесия в следующих реакциях: 
176. Как будет влиять увеличение давления на состояние равновесия в следующих реакциях: 
177. Какие факторы способствуют смещению равновесия в сторону образования продуктов в реакциях:

178. Какие условия способствуют смещению равновесия в реакции гидролиза жира в сторону образования продуктов?
179. Рассчитайте константу равновесия при некоторой заданной температуре для обратимой реакции  учитывая, что в состоянии равновесия концентрации участвующих в реакции веществ были равны:
учитывая, что в состоянии равновесия концентрации участвующих в реакции веществ были равны:  .
.
Уровень 2
180. При сгорании 2 моль этилена в кислороде выделилось 2822 кДж теплоты. Определите теплоту образования этилена, если стандартные теплоты образования  равны
равны  соответственно.
соответственно.
181. При сгорании 2 молей фосфористого водорода (фосфи-на)  образуются оксид фосфора
образуются оксид фосфора  и вода и выделяется 2440 кДж. Определите теплоту образования фосфина, если при образовании оксида фосфора (V) и воды выделяется, соответственно,
и вода и выделяется 2440 кДж. Определите теплоту образования фосфина, если при образовании оксида фосфора (V) и воды выделяется, соответственно, 
182. Растворение образца цинка в соляной кислоте при 20 °С заканчивается через 27 минут, а при 40 °С такой же образец металла растворяется за 3 минуты. За какое время данный образец цинка растворится при 55 °С?
183. При увеличении температуры от 0 °С до 13 °С скорость некоторой реакции возросла в 2,97 раза. Чему равна энергия активации этой реакции?
184. В каком из двух случаев скорость реакции увеличится в большее число раз: при нагревании от 0 °С до 11 °С или при нагревании от 11 °С до 22 °С? Ответ обоснуйте с помощью уравнения Аррениуса.
185. Для каких из указанных реакций уменьшение объема сосуда приведет к смещению равновесия в том же направлении, что и понижение температуры:

186. Равновесие реакции  устанавливается при следующих концентрациях участвующих в них веществ:
устанавливается при следующих концентрациях участвующих в них веществ:  Вычислите константу равновесия и исходные концентрации азота и водорода.
Вычислите константу равновесия и исходные концентрации азота и водорода.
187. В 0,2 М растворе фосфористой кислоты  концентрация ионов
концентрация ионов  равна 0,05 М. Вычислите константу диссоциации
равна 0,05 М. Вычислите константу диссоциации  предполагая, что второй протон не отщепляется.
предполагая, что второй протон не отщепляется.
188. Обратимая реакция описывается уравнением:  Смешали по одному молю всех веществ. После установления равновесия в смеси обнаружено 1,5 моля вещества С. Найти константу равновесия.
Смешали по одному молю всех веществ. После установления равновесия в смеси обнаружено 1,5 моля вещества С. Найти константу равновесия.
Уровень 3
189. Даны три уравнения химических реакций:

Определите тепловой эффект реакции  .
.
190. Как известно, высокотемпературное пламя ацетилено-кислородных горелок широко используется для сварки и резки металлов. Можно ли для аналогичных целей использовать пламя метано-кислородной горелки? Рассчитайте, в какой из двух указанных типов горелок и во сколько раз выделится больше теплоты при сгорании одинаковых объемов ацетилена и метана. Теплоты образования  равны
равны  соответственно.
соответственно.
191. Тонкоизмельченную смесь алюминия и железной окалины  часто называемую термитом, применяют для сварки металлических изделий, поскольку при поджигании термита выделяется большое количество теплоты и развивается высокая температура. Рассчитайте минимальную массу термитной смеси, которую необходимо взять для того, чтобы выделилось 665,26 кДж теплоты в процессе алюмотермии, если теплоты образования
часто называемую термитом, применяют для сварки металлических изделий, поскольку при поджигании термита выделяется большое количество теплоты и развивается высокая температура. Рассчитайте минимальную массу термитной смеси, которую необходимо взять для того, чтобы выделилось 665,26 кДж теплоты в процессе алюмотермии, если теплоты образования  равны
равны  соответственно.
соответственно.
192. При сжигании паров этанола в кислороде выделилось 494,2 кДж теплоты и осталось  непрореагировавшего кислорода (измерено при давлении 101,3 кПа и температуре
непрореагировавшего кислорода (измерено при давлении 101,3 кПа и температуре  .
.
Рассчитайте массовые доли компонентов в исходной смеси, если известно, что теплоты образования оксида углерода (IV), паров воды и паров этанола составляют  соответственно.
соответственно.
193. 48 г минерала, содержащего 46,7% железа и 53,3% серы по массе, сожгли в избытке кислорода, а твердый продукт сгорания прокалили с 18,1 г алюминия. Какое количество теплоты выделилось в результате каждого из этих процессов, если известно, что реакции проводились при постоянной температуре, а теплоты образования при данной температуре равны: сульфид железа  оксид железа (III)
оксид железа (III)  оксид серы (IV)
оксид серы (IV)  оксид алюминия
оксид алюминия 
194. Кинетические измерения показали, что скорость реакции  описывается уравнением:
описывается уравнением:  Определите, в каком молярном отношении надо ввести
Определите, в каком молярном отношении надо ввести  в реакцию, чтобы скорость реакции была максимальной.
в реакцию, чтобы скорость реакции была максимальной.
195. Рассчитайте равновесные концентрации веществ, участвующих в реакции  если исходные концентрации веществ равны:
если исходные концентрации веществ равны:  а константа равновесия при данной температуре равна 1.
а константа равновесия при данной температуре равна 1.
196. Концентрация аммиака в замкнутом сосуде при  равна
равна  При нагревании сосуда до
При нагревании сосуда до  давление внутри увеличилось в 3,3 раза. Определите константу равновесия для реакции разложения аммиака при
давление внутри увеличилось в 3,3 раза. Определите константу равновесия для реакции разложения аммиака при 
197. Как изменится массовая доля хлорида калия в насыщенном водном растворе» находящемся в равновесии с кристаллами соли, при: а) повышении температуры; б) повышении давления; в) введении в раствор твердого нитрата калия, если при 10 °С массовая доля соли в насыщенном растворе равна 23,8% плотности насыщенного раствора, кристаллов соли и воды равны, соответственно, 1,16, 1,99 и 0,999 г/см3, а образование  насыщенного раствора из кристаллов и воды сопровождается поглощением 1,6 кДж теплоты?
насыщенного раствора из кристаллов и воды сопровождается поглощением 1,6 кДж теплоты?
198. При нагревании до некоторой температуры 36 г уксусной кислоты и 7,36 г 100%-ного этанола в присутствии серной кислоты получена равновесная смесь. Эта смесь при действии избытка раствора хлорида бария образует 4,66 г осадка, а при действии избытка раствора гидрокарбоната калия выделяет  оксида углерода (IV) (при норм, усл.). Найдите количество сложного эфира (в молях) в равновесной смеси, которая образуется при нагревании до той же температуры 150 г уксусной кислоты и 200 мл 90%-ного этанола (плотность
оксида углерода (IV) (при норм, усл.). Найдите количество сложного эфира (в молях) в равновесной смеси, которая образуется при нагревании до той же температуры 150 г уксусной кислоты и 200 мл 90%-ного этанола (плотность  ) в присутствии серной кислоты в качестве катализатора.
) в присутствии серной кислоты в качестве катализатора.
| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- Глава I. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ
- § 1. Предмет химии. Важнейшие понятия и законы химии
- Основные стехиометрические законы химии
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 2. Строение атома
- Электронные конфигурации атомов
- Ядро атома и радиоактивные превращения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 3. Строение молекул. Химическая связь. Валентность элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 4. Агрегатные состояния вещества
- Характерные свойства газов, жидкостей и твердых тел
- Газообразное состояние. Газовые законы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 5. Закономерности протекания химических реакций
- Химическая кинетика
- Химическое равновесие
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 6. Растворы. Электролитическая диссоциация. Гидролиз солей
- Электролиты и электролитическая диссоциация
- Гидролиз солей
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 7. Классификация химических реакций. Окислительно-восстановительные процессы. Электролиз
- Окислительно-восстановительные реакции
- Электролиз
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
- § 8. Номенклатура, классификация неорганических веществ. Свойства и способы получения
- Оксиды
- Основания (гидроксиды металлов)
- Кислоты
- Соли
- § 9. Водород. Галогены и их соединения
- Галогены и их соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 10. Подгруппа кислорода
- Сера и ее соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 11. Подгруппа азота
- Фосфор и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 12. Подгруппа углерода
- Углерод и его соединения
- Кремний и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 13. Свойства s-элементов (щелочных и щелочноземельных металлов) и их соединений
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 14. Алюминий — типичный р-металл
- Соединения алюминия и их свойства
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 15. Главные переходные металлы (d-элементы) и их соединения
- Химические свойства d-элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 16. Задачи для повторения по неорганической химии
- Глава III. ОРГАНИЧЕСКАЯ ХИМИЯ
- § 17. Основные понятия и закономерности в органической химии. Предмет органической химии
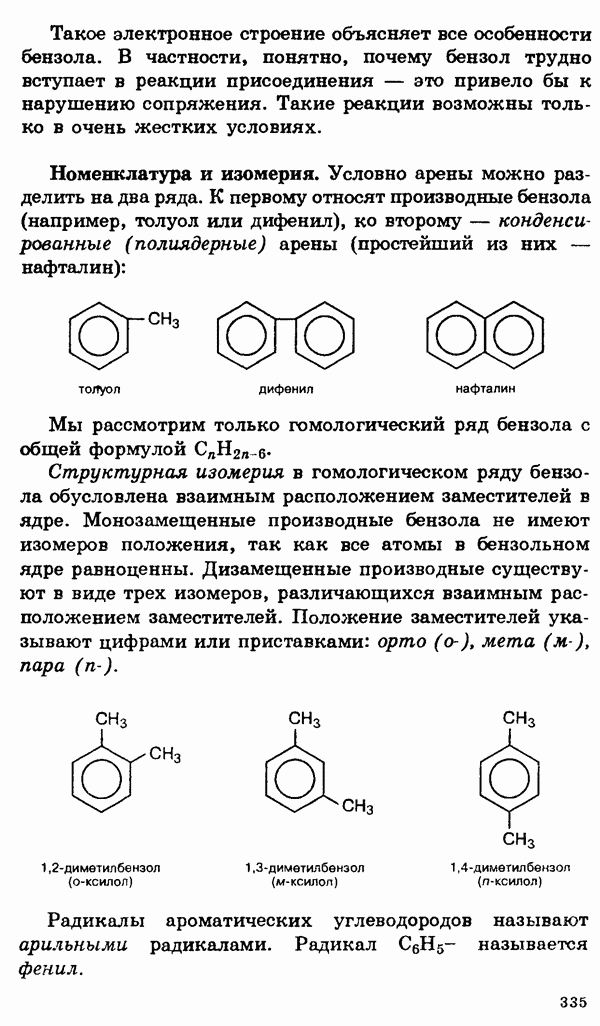
- Классификация и номенклатура органических соединений
- Изомерия органических соединений
- Взаимное влияние атомов в молекуле и реакционная способность органических соединений
- Общая характеристика органических реакций
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 18. Предельные (насыщенные) углеводороды
- Циклоалканы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 19. Алкены. Диеновые углеводороды
- Диеновые углеводороды (алкадиены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 20. Алкины
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 21. Ароматические углеводороды (арены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 22. Спирты и фенолы
- Многоатомные спирты
- Фенолы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 23. Карбонильные соединения — альдегиды и кетоны
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 24. Карбоновые кислоты. Сложные эфиры. Жиры
- Сложные эфиры. Жиры
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава 4. ОСНОВНЫЕ ПРИЕМЫ РЕШЕНИЯ ЗАДАЧ
- Определение молекулярной формулы веществ
- Определение состава и разделение смесей
- Задачи на газовые законы
- Способы выражения концентрации растворов
- Ионные реакции в растворах
- Задачи на окислительно-восстановительные реакции
- Разные задачи
- ПРОГРАММА ПО ХИМИИ ДЛЯ ПОСТУПАЮЩИХ В УНИВЕРСИТЕТЫ
- ОТВЕТЫ
- Рекомендуемая литература