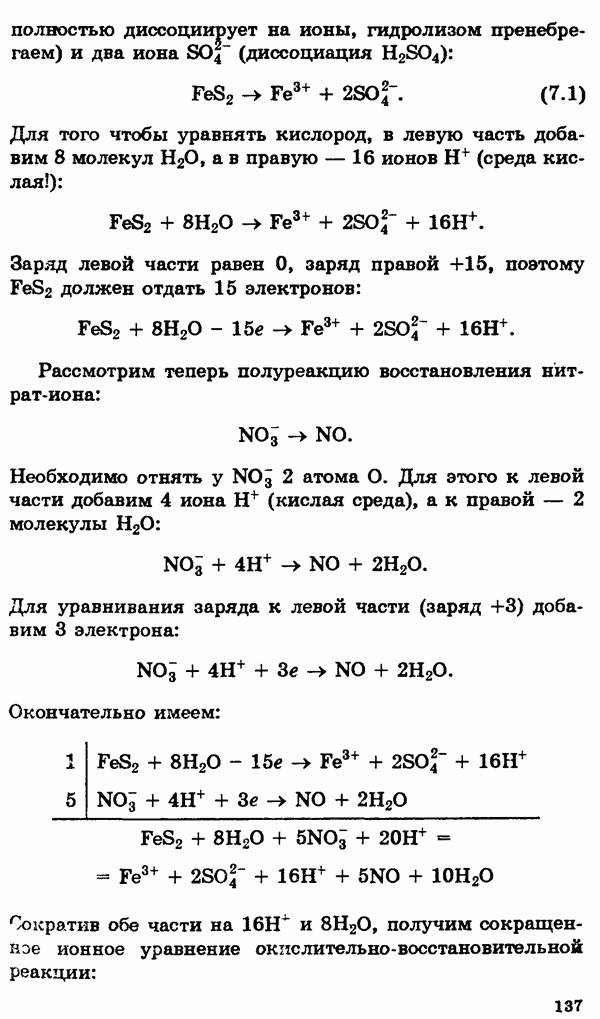| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
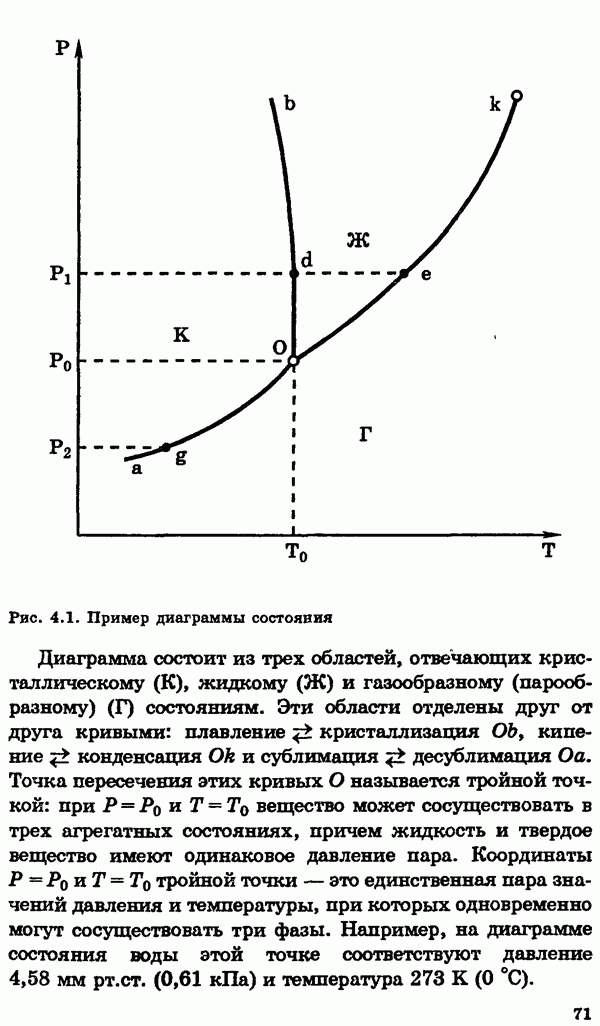
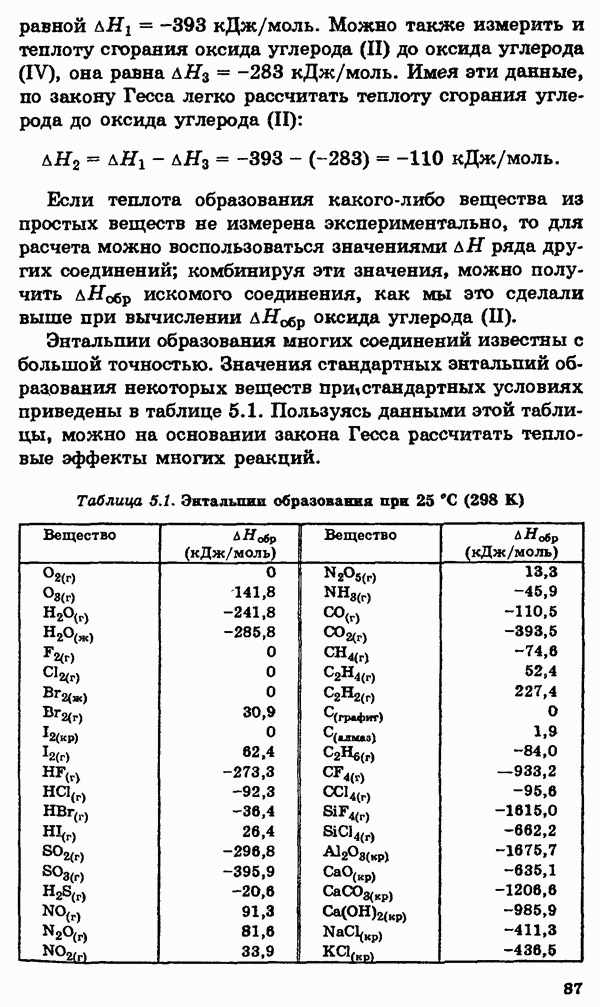
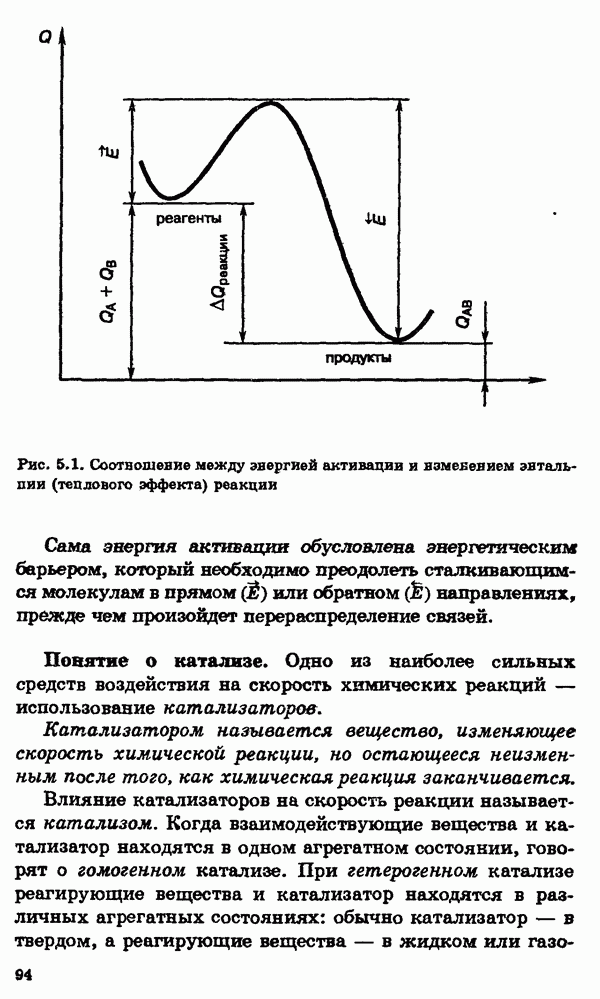
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
§ 14. Алюминий — типичный р-металл
Алюминий — основной представитель металлов главной подгруппы III группы периодической системы. Свойства его аналогов — галлия, индия и таллия — во многом напоминают свойства алюминия, поскольку все эти элементы имеют одинаковую электронную конфигурацию внешнего уровня  и поэтому все они проявляют степень окисления
и поэтому все они проявляют степень окисления  . Ниже мы рассмотрим свойства только одного элемента — алюминия.
. Ниже мы рассмотрим свойства только одного элемента — алюминия.
Бор, также представляющий p-элементы III группы, — типичный неметалл, по своим физическим и химическим свойствам он скорее похож на углерод и кремний.
Алюминий — серебристо-белый металл, обладающий высокой тепло- и электропроводностью. Поверхность металла покрыта тонкой, но очень прочной пленкой оксида алюминия  .
.
Алюминий весьма активен, если нет защитной пленки  . Эта пленка препятствует взаимодействию алюминия с водой. Если удалить защитную пленку химическим способом (например, раствором щелочи), то металл начинает энергично взаимодействовать с водой с выделением водорода:
. Эта пленка препятствует взаимодействию алюминия с водой. Если удалить защитную пленку химическим способом (например, раствором щелочи), то металл начинает энергично взаимодействовать с водой с выделением водорода:

Алюминий в виде стружки или порошка ярко горит на воздухе, выделяя большое количество энергии:

Эта особенность алюминия широко используется для получения различных металлов из их оксидов путем восстановления алюминием. Метод получил название алюмотермии. Алюмотермией можно получить только те металлы, у которых теплоты образования оксидов меньше теплоты образования  , например:
, например:

При нагревании алюминий реагирует с галогенами, серой, азотом и углеродом, образуя при этом соответственно галогениды

Сульфид и карбид алюминия полностью гидролизуются с образованием гидроксида алюминия и соответственно сероводорода и метана.
Алюминий легко растворяется в соляной кислоте любой концентрации:

Концентрированные серная и азотная кислоты на холоде не действуют на алюминий. При нагревании алюминий способен восстанавливать эти кислоты без выделения водорода:

В разбавленной серной кислоте алюминий растворяется с выделением водорода:

В разбавленной азотной кислоте реакция идет с выделением оксида азота (II):

Алюминий растворяется в растворах щелочей и карбонатов щелочных металлов с образованием тетрагидрок-соалюминатов:

| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ВВЕДЕНИЕ
- Глава I. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ
- § 1. Предмет химии. Важнейшие понятия и законы химии
- Основные стехиометрические законы химии
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 2. Строение атома
- Электронные конфигурации атомов
- Ядро атома и радиоактивные превращения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 3. Строение молекул. Химическая связь. Валентность элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 4. Агрегатные состояния вещества
- Характерные свойства газов, жидкостей и твердых тел
- Газообразное состояние. Газовые законы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 5. Закономерности протекания химических реакций
- Химическая кинетика
- Химическое равновесие
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 6. Растворы. Электролитическая диссоциация. Гидролиз солей
- Электролиты и электролитическая диссоциация
- Гидролиз солей
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 7. Классификация химических реакций. Окислительно-восстановительные процессы. Электролиз
- Окислительно-восстановительные реакции
- Электролиз
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
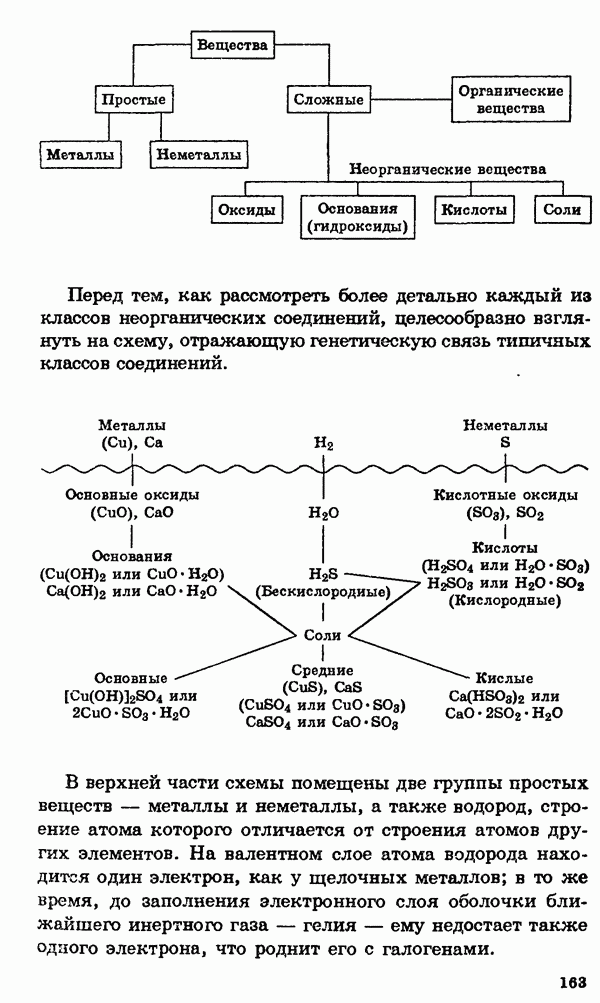
- § 8. Номенклатура, классификация неорганических веществ. Свойства и способы получения
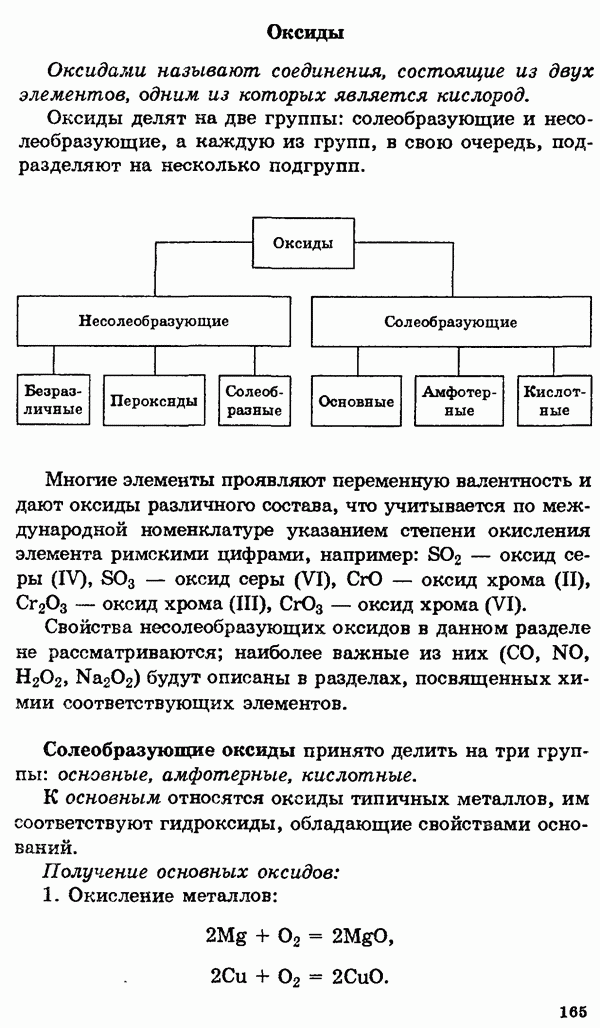
- Оксиды
- Основания (гидроксиды металлов)
- Кислоты
- Соли
- § 9. Водород. Галогены и их соединения
- Галогены и их соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 10. Подгруппа кислорода
- Сера и ее соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 11. Подгруппа азота
- Фосфор и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 12. Подгруппа углерода
- Углерод и его соединения
- Кремний и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 13. Свойства s-элементов (щелочных и щелочноземельных металлов) и их соединений
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 14. Алюминий — типичный р-металл
- Соединения алюминия и их свойства
- ЗАДАЧИ И УПРАЖНЕНИЯ
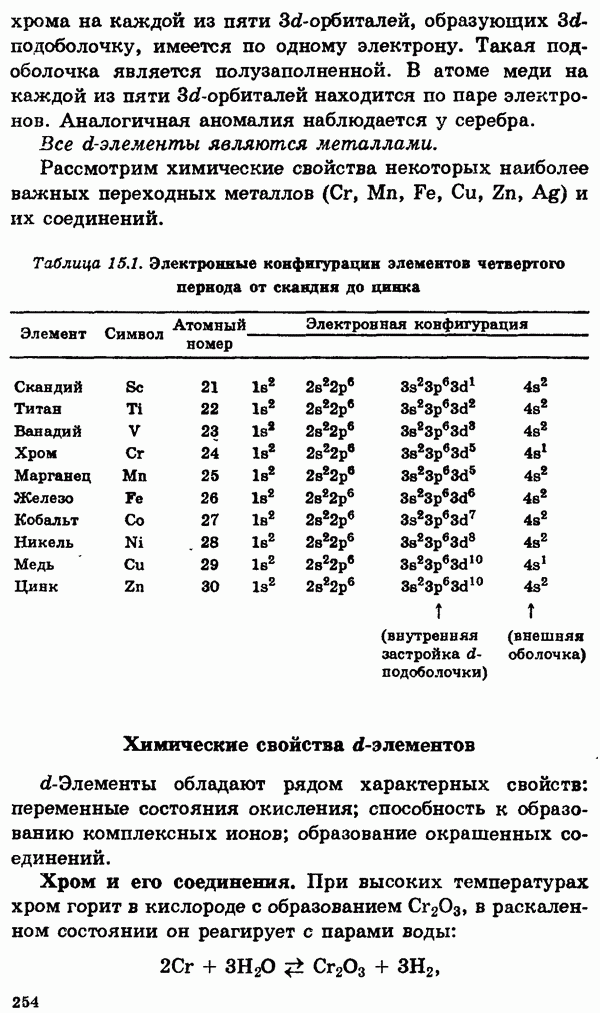
- § 15. Главные переходные металлы (d-элементы) и их соединения
- Химические свойства d-элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 16. Задачи для повторения по неорганической химии
- Глава III. ОРГАНИЧЕСКАЯ ХИМИЯ
- § 17. Основные понятия и закономерности в органической химии. Предмет органической химии
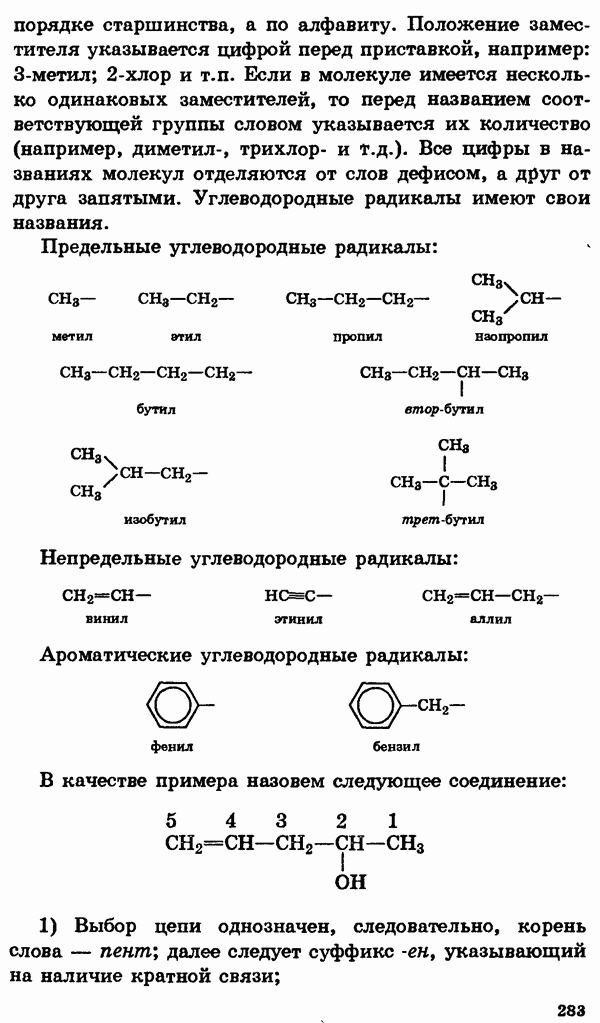
- Классификация и номенклатура органических соединений
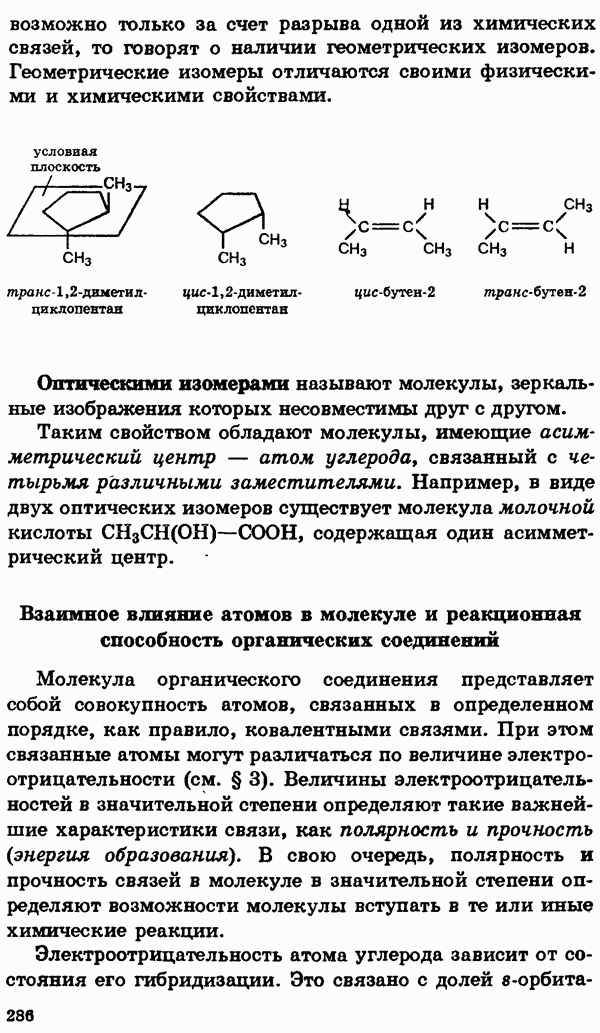
- Изомерия органических соединений
- Взаимное влияние атомов в молекуле и реакционная способность органических соединений
- Общая характеристика органических реакций
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 18. Предельные (насыщенные) углеводороды
- Циклоалканы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 19. Алкены. Диеновые углеводороды
- Диеновые углеводороды (алкадиены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 20. Алкины
- ЗАДАЧИ И УПРАЖНЕНИЯ
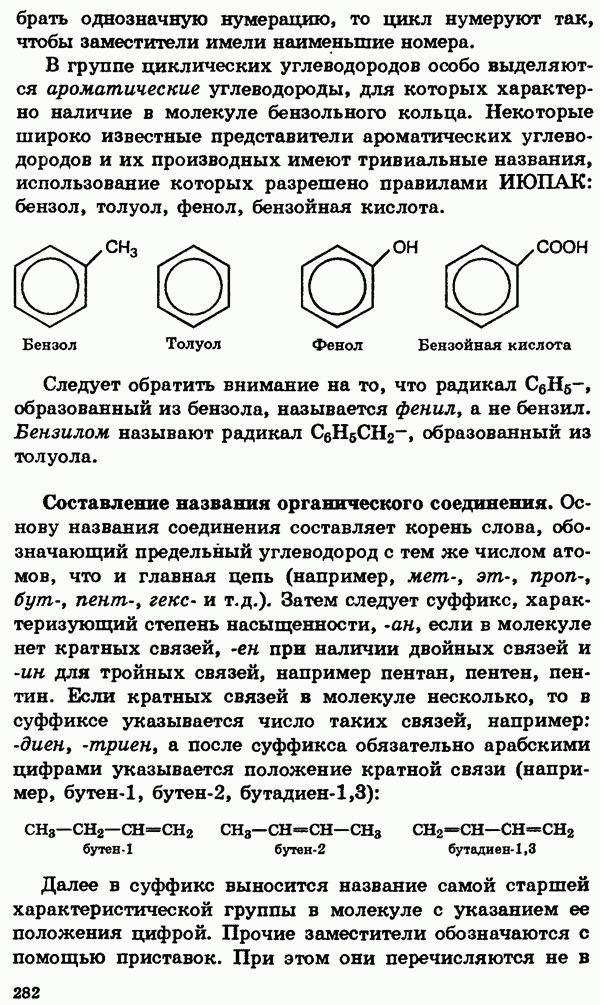
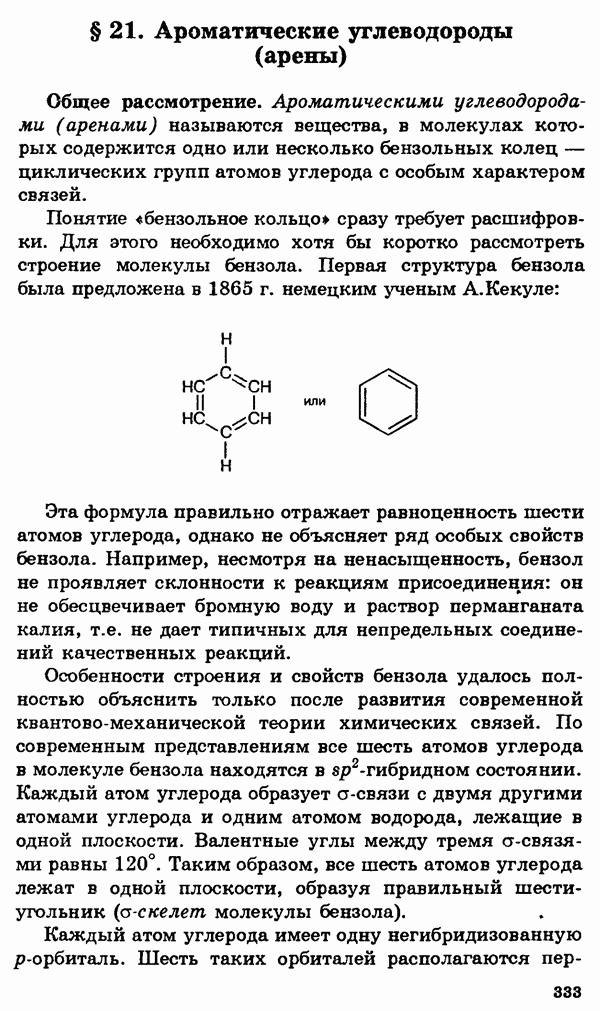
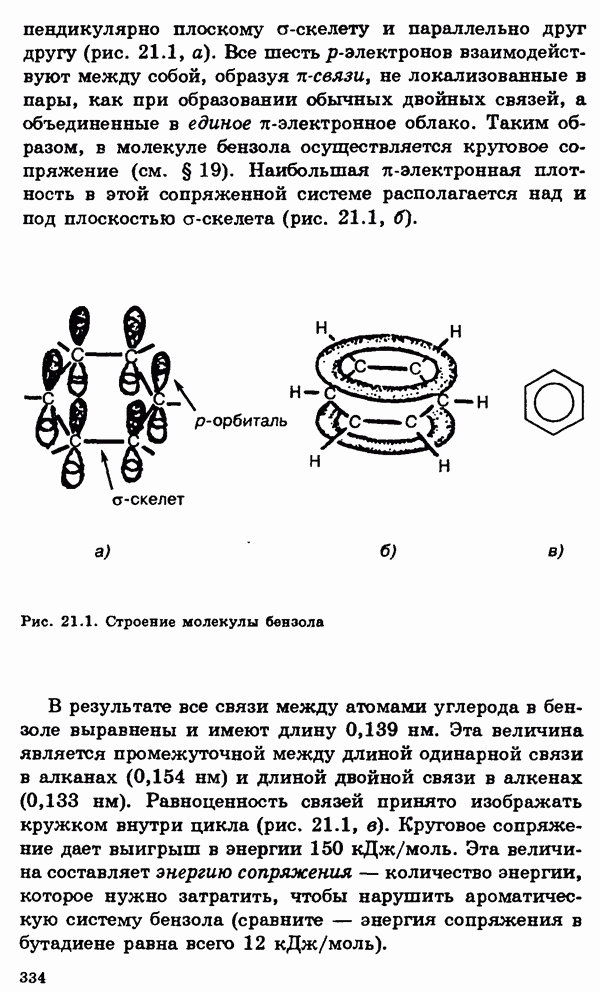
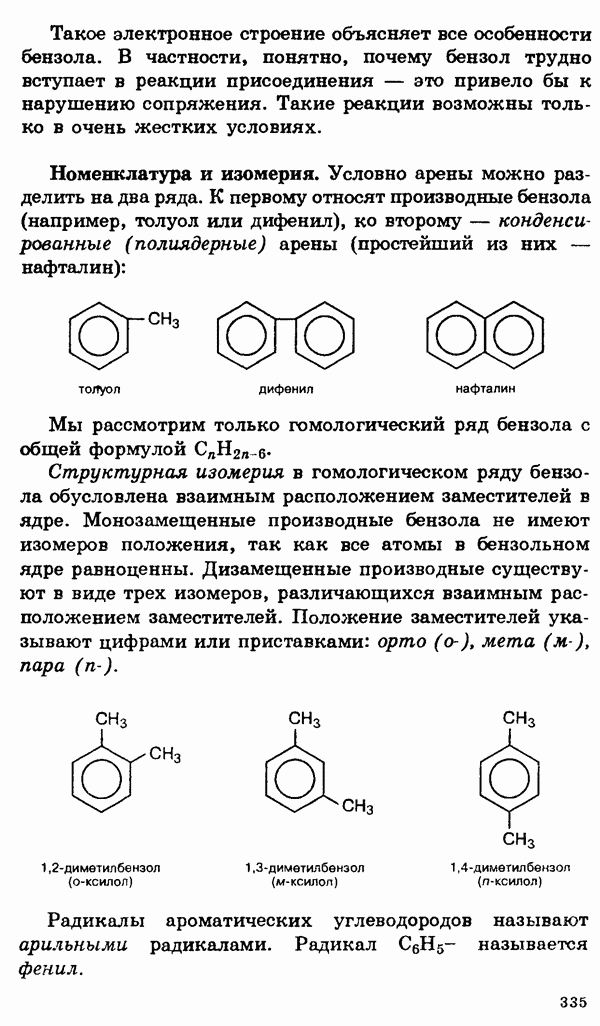
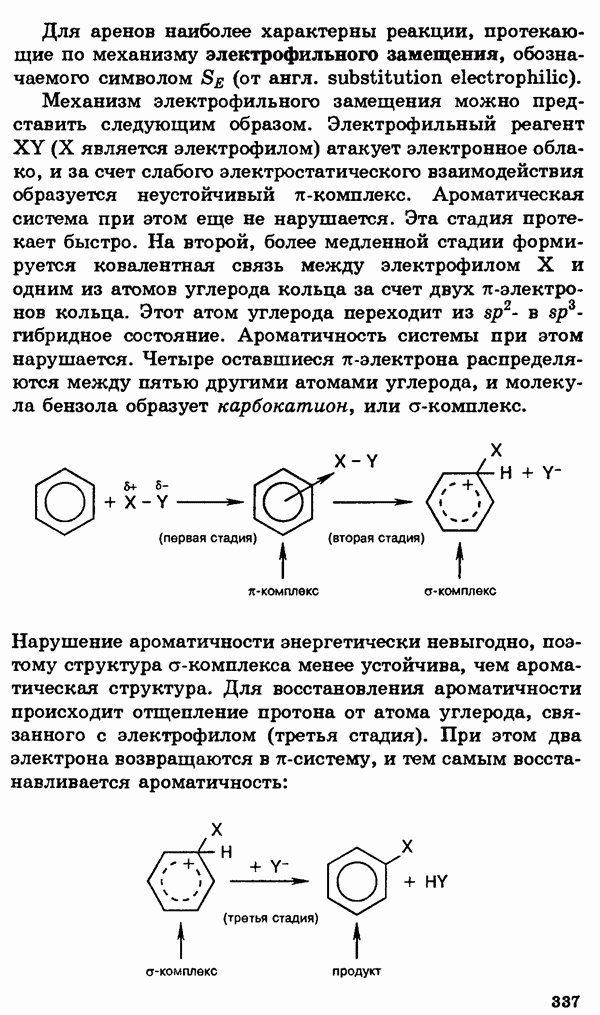
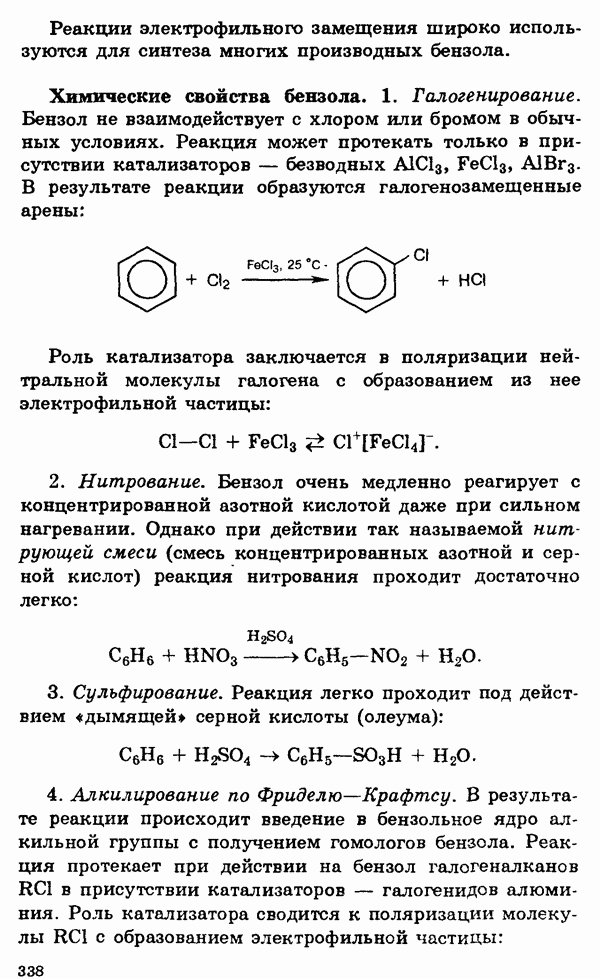
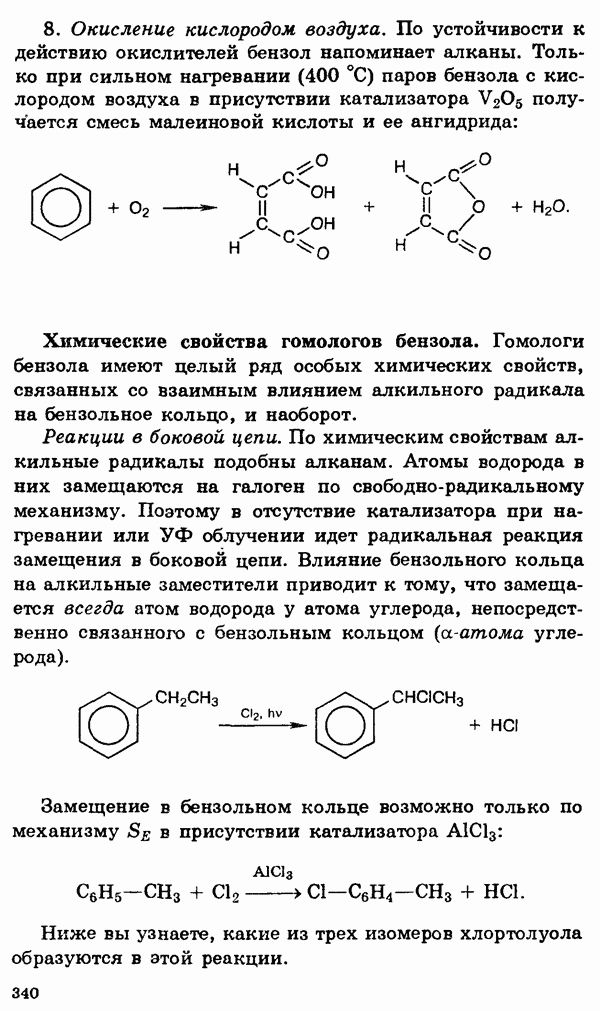
- § 21. Ароматические углеводороды (арены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 22. Спирты и фенолы
- Многоатомные спирты
- Фенолы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 23. Карбонильные соединения — альдегиды и кетоны
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 24. Карбоновые кислоты. Сложные эфиры. Жиры
- Сложные эфиры. Жиры
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава 4. ОСНОВНЫЕ ПРИЕМЫ РЕШЕНИЯ ЗАДАЧ
- Определение молекулярной формулы веществ
- Определение состава и разделение смесей
- Задачи на газовые законы
- Способы выражения концентрации растворов
- Ионные реакции в растворах
- Задачи на окислительно-восстановительные реакции
- Разные задачи
- ПРОГРАММА ПО ХИМИИ ДЛЯ ПОСТУПАЮЩИХ В УНИВЕРСИТЕТЫ
- ОТВЕТЫ
- Рекомендуемая литература