| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Гидролиз солей
Выше мы выяснили, что реакция чистой воды является нейтральной  Водные растворы кислот и оснований имеют, соответственно, кислую
Водные растворы кислот и оснований имеют, соответственно, кислую  и щелочную
и щелочную  реакцию. Практика, однако, показывает, что не только кислоты и основания, но и соли могут иметь щелочную или кислую реакцию — причиной этого является гидролиз солей.
реакцию. Практика, однако, показывает, что не только кислоты и основания, но и соли могут иметь щелочную или кислую реакцию — причиной этого является гидролиз солей.
Взаимодействие солей с водой, в результате которого образуются кислота (или кислая соль) и основание (или основная соль), называется гидролизом солей.
Причиной гидролиза является электролитическая диссоциация соответствующих солей и воды. Вода незначительно диссоциирует на ионы  но в процессе гидролиза один или оба из этих ионов могут связываться ионами, образующимися при диссоциации соли, в малодиссоциированные, летучие или труднорастворимые вещества.
но в процессе гидролиза один или оба из этих ионов могут связываться ионами, образующимися при диссоциации соли, в малодиссоциированные, летучие или труднорастворимые вещества.
Рассмотрим гидролиз солей следующих основных типов:
1. Соли сильного основания и сильной кислоты при растворении в воде (например,  ) не гидролизуются, и раствор соли имеет нейтральную реакцию.
) не гидролизуются, и раствор соли имеет нейтральную реакцию.
2. Соли сильного основания и слабой кислоты, например 
Запишем уравнение гидролиза ацетата натрия:

В результате реакции образовался слабый электролит — уксусная кислота. В ионном виде этот процесс можно записать так:

Следовательно, раствор  будет проявлять щелочную реакцию.
будет проявлять щелочную реакцию.
При растворении солей многоосновных кислот гидролиз протекает ступенчато, например:

или в ионной форме

Процесс (6.17) отражает гидролиз  по первой ступени. Чтобы гидролиз прошел полностью, как правило, увеличивают температуру процесса:
по первой ступени. Чтобы гидролиз прошел полностью, как правило, увеличивают температуру процесса:

Таким образом, при растворении в воде соли сильного основания и слабой кислоты раствор приобретает щелочную реакцию вследствие гидролиза.
3. Соли слабого основания и сильной кислоты, например  .
.
Рассмотрим гидролиз хлорида железа (II):

В ионном виде этот процесс можно записать так:

По второй ступени гидролиз протекает следующим образом:

Из реакций  ясно, что в результате гидролиза солей слабого основания и сильной кислоты раствор приобретает кислую реакцию.
ясно, что в результате гидролиза солей слабого основания и сильной кислоты раствор приобретает кислую реакцию.
4. Соли слабого основания и слабой кислоты, например  При растворении в воде таких солей образуются малодиссоциирующие кислота и основание:
При растворении в воде таких солей образуются малодиссоциирующие кислота и основание:

или в ионном виде:

Реакция среды в растворах подобных солей зависит от относительной силы кислоты и основания. Другими словами, водные растворы таких солей могут иметь нейтральную, кислую или щелочную реакцию в зависимости от констант диссоциации образующихся кислот и оснований.
Так, при гидролизе  реакция раствора будет слабощелочной, поскольку константа диссоциации гидроксида аммония
реакция раствора будет слабощелочной, поскольку константа диссоциации гидроксида аммония  больше константы диссоциации уксусной кислоты
больше константы диссоциации уксусной кислоты  .
.
Рекомендуемая литература: [Кузьменко, 1977, гл. 6, 7], [Третьяков, § 22—25], [Фримантл, т. 1, гл. 8], [Хомченко, 1993, гл. 5].
| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- Глава I. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ
- § 1. Предмет химии. Важнейшие понятия и законы химии
- Основные стехиометрические законы химии
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 2. Строение атома
- Электронные конфигурации атомов
- Ядро атома и радиоактивные превращения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 3. Строение молекул. Химическая связь. Валентность элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 4. Агрегатные состояния вещества
- Характерные свойства газов, жидкостей и твердых тел
- Газообразное состояние. Газовые законы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 5. Закономерности протекания химических реакций
- Химическая кинетика
- Химическое равновесие
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 6. Растворы. Электролитическая диссоциация. Гидролиз солей
- Электролиты и электролитическая диссоциация
- Гидролиз солей
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 7. Классификация химических реакций. Окислительно-восстановительные процессы. Электролиз
- Окислительно-восстановительные реакции
- Электролиз
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
- § 8. Номенклатура, классификация неорганических веществ. Свойства и способы получения
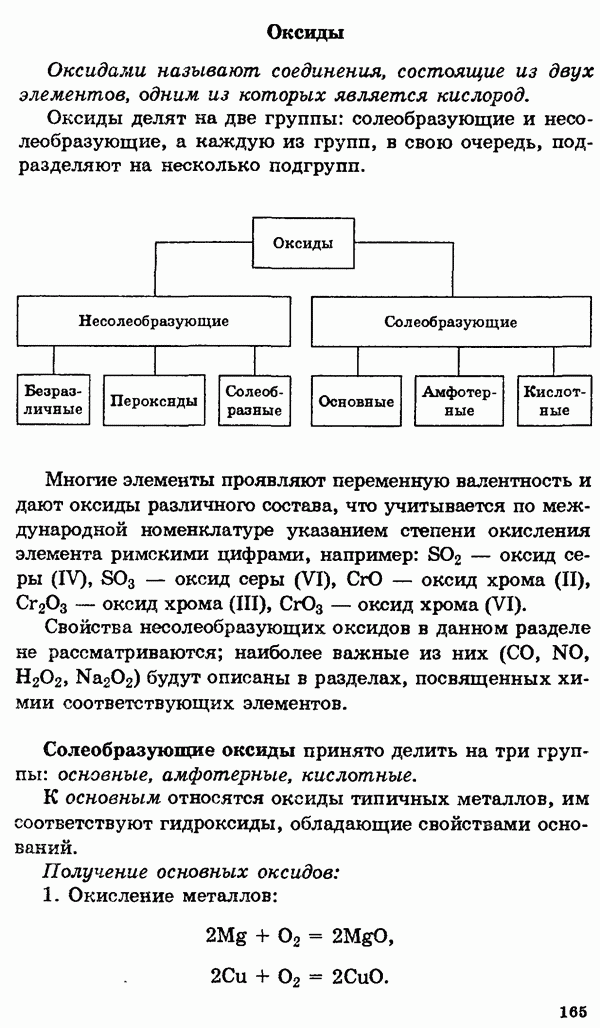
- Оксиды
- Основания (гидроксиды металлов)
- Кислоты
- Соли
- § 9. Водород. Галогены и их соединения
- Галогены и их соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 10. Подгруппа кислорода
- Сера и ее соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 11. Подгруппа азота
- Фосфор и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 12. Подгруппа углерода
- Углерод и его соединения
- Кремний и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 13. Свойства s-элементов (щелочных и щелочноземельных металлов) и их соединений
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 14. Алюминий — типичный р-металл
- Соединения алюминия и их свойства
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 15. Главные переходные металлы (d-элементы) и их соединения
- Химические свойства d-элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 16. Задачи для повторения по неорганической химии
- Глава III. ОРГАНИЧЕСКАЯ ХИМИЯ
- § 17. Основные понятия и закономерности в органической химии. Предмет органической химии
- Классификация и номенклатура органических соединений
- Изомерия органических соединений
- Взаимное влияние атомов в молекуле и реакционная способность органических соединений
- Общая характеристика органических реакций
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 18. Предельные (насыщенные) углеводороды
- Циклоалканы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 19. Алкены. Диеновые углеводороды
- Диеновые углеводороды (алкадиены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 20. Алкины
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 21. Ароматические углеводороды (арены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 22. Спирты и фенолы
- Многоатомные спирты
- Фенолы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 23. Карбонильные соединения — альдегиды и кетоны
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 24. Карбоновые кислоты. Сложные эфиры. Жиры
- Сложные эфиры. Жиры
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава 4. ОСНОВНЫЕ ПРИЕМЫ РЕШЕНИЯ ЗАДАЧ
- Определение молекулярной формулы веществ
- Определение состава и разделение смесей
- Задачи на газовые законы
- Способы выражения концентрации растворов
- Ионные реакции в растворах
- Задачи на окислительно-восстановительные реакции
- Разные задачи
- ПРОГРАММА ПО ХИМИИ ДЛЯ ПОСТУПАЮЩИХ В УНИВЕРСИТЕТЫ
- ОТВЕТЫ
- Рекомендуемая литература