| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 22. Спирты и фенолы
Спиртами называют соединения, содержащие одну или несколько гидроксильных групп, непосредственно связанных с углеводородным радикалом.
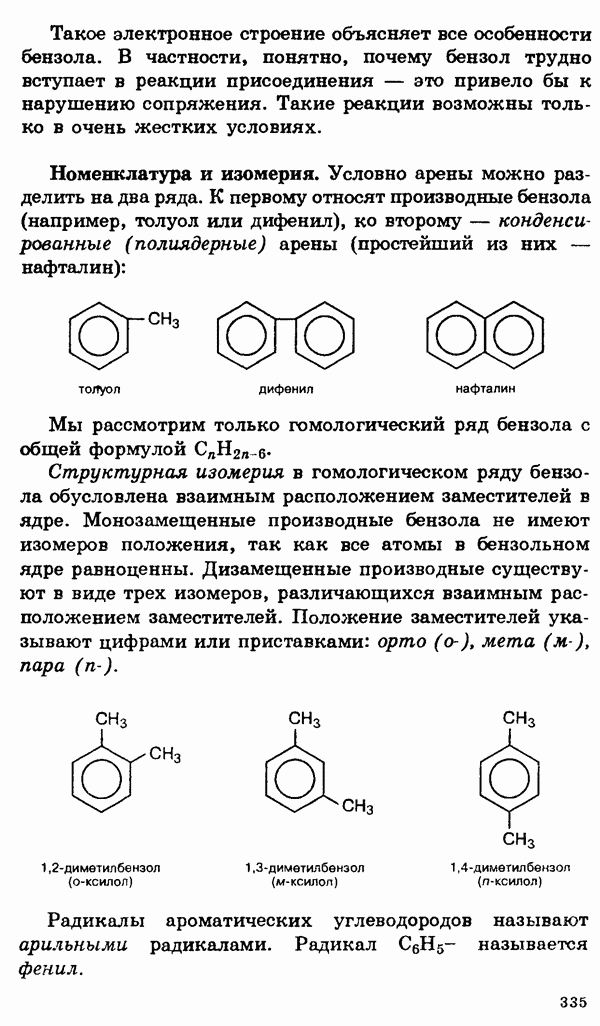
В зависимости от характера углеводородного радикала, спирты делятся на алифатические, алициклические и ароматические, причем у последних гидроксильная группа не связана с атомом углерода бензольного кольца. Спирты, у которых гидроксильная группа связана с ароматическим кольцом, называются фенолами.
В зависимости от числа гидроксильных групп, спирты подразделяют на одно-, двух- и трехатомные. Двухатомные спирты часто называют гликолями. Спирты, содержащие несколько групп —ОН, объединяют общим названием многоатомные спирты.
В зависимости от того, при каком углеродном атоме находится гидроксильная группа, различают спирты первичные  вторичные
вторичные  и третичные
и третичные 
Мы рассмотрим только алифатические спирты (далее — просто спирты) и фенолы.
Спирты
Структурная изомерия предельных одноатомных спиртов определяется строением углеродной цепи и положением гидроксильной группы в цепи. Изомерия двух- и трехатомных спиртов, кроме того, определяется взаимным расположением гидроксильных групп.
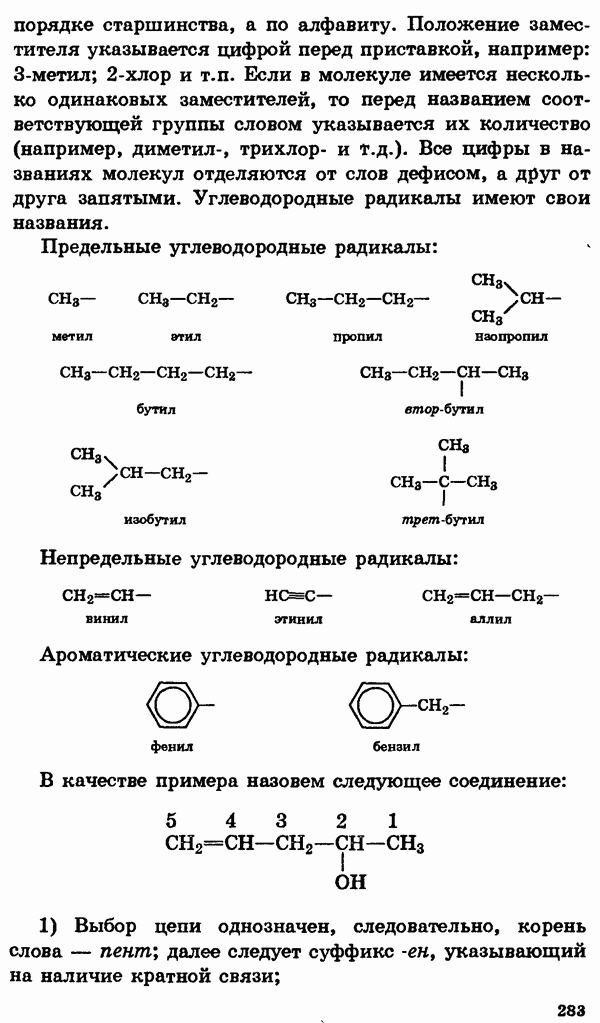
По систематической номенклатуре названия спиртов образуют, добавляя суффикс -ол к названию углеводорода с самой длинной углеродной цепью, включающей гидроксильную группу.
Нумерацию цепи начинают с того края, ближе к которому расположена гидроксильная группа.
Физические свойства
спиртов зависят от строения углеводородного радикала, количества гидроксильных групп и их положения. Первые представители гомологического ряда спиртов — жидкости, высшие — твердые вещества. Метанол и этанол смешиваются с водой в любых соотношениях. С ростом молекулярной массы растворимость спиртов в воде падает. Высшие спирты практически не растворимы в воде. Спирты обладают аномально высокими температурами кипения по сравнению с углеводородами, что объясняется сильной ассоциацией молекул спирта в жидком состоянии за счет образования достаточно прочных водородных связей.
Способы получения.
1. Получение из алкенов. Гидратация алкенов протекает по механизму электрофильного присоединения по правилу Марковникова (см. § 19). Это один из наиболее важных промышленных способов получения спиртов.
2. Получение из галогенпроизводных. Галогеналканы гидролизуются под действием водных растворов щелочей. Реакция протекает по механизму нуклеофильного замещения:

3. Восстановление карбонильных соединений. При восстановлении альдегидов образуются первичные спирты, при восстановлении кетонов — вторичные:

4. Действие реактивов Гриньяра на карбонильные соединения (см. § 23).
Химические свойства.
Различают два основных типа реакций спиртов с участием функциональной группы —ОН:
1) реакции с разрывом связи  взаимодействие спиртов с щелочными и щелочноземельными металлами с образованием алкоксидов;
взаимодействие спиртов с щелочными и щелочноземельными металлами с образованием алкоксидов;
б) реакции спиртов с органическими и минеральными кислотами с образованием сложных эфиров; в) окисление спиртов под действием дихромата или перманганата калия до карбонильных соединений. Скорость реакций, при которых разрывается связь  , уменьшается в ряду: первичные спирты
, уменьшается в ряду: первичные спирты  вторичные
вторичные  третичные.
третичные.
2) Реакции, сопровождающиеся разрывом связи С-О: а) каталитическая дегидратация с образованием алкенов (внутримолекулярная дегидратация) или простых эфиров (межмолекулярная дегидратация); б) замещение группы —ОН галогеном, например при действии галогеноводородов с образованием алкилгалогенидов. Скорость реакций, при которых разрывается связь  уменьшается в ряду: третичные спирты
уменьшается в ряду: третичные спирты  вторичные
вторичные  первичные.
первичные.
Спирты являются амфотерными соединениями.
1. Кислотные свойства спиртов выражены очень слабо. Низшие спирты бурно реагируют с щелочными металлами:

С увеличением длины углеводородного радикала скорость этой реакции замедляется.
В присутствии следов влаги образующиеся алкоголяты разлагаются до исходных спиртов:

Это доказывает, что спирты — более слабые кислоты, чем вода.
2. Слабые основные свойства спиртов обусловлены наличием неподеленной электронной пары на атоме кислорода и проявляются в обратимых реакциях с галогеноводородами:

Положение равновесия зависит от соотношения реагентов.
3. Образование сложных эфиров протекает по механизму нуклеофильного присоединения - отщепления:

В качестве нуклеофила выступает молекула спирта, атакующая атом углерода карбоксильной группы, несущий частичный положительный заряд. Отличительной особенностью этой реакции является то, что замещение протекает у атома углерода, находящегося в состоянии  -гибридизации.
-гибридизации.
4. Межмолекулярная дегидратация спиртов. При нагревании спирта в присутствии каталитических количеств сильной кислоты происходит отщепление молекулы воды от двух молекул спирта и образуется простой эфир.

5. Реакция элиминирования, или внутримолекулярной дегидратации была рассмотрена в разделе «Получение алкенов» (§ 19). Конкурентная реакции 4) реакция 5) становится преобладающей при использовании больших количеств кислоты:

6. Реакции окисления. Первичные спирты окисляются в альдегиды, которые, в свою очередь, могут окисляться в карбоновые кислоты:

Вторичные спирты окисляются в кетоны:

Третичные спирты более устойчивы к окислению. При действии на них сильных окислителей может происходить расщепление углеродного скелета молекулы третичного спирта с образованием карбоновых кислот и кетонов с меньшим числом углеродных атомов, чем в молекуле исходного третичного спирта. Окисление обычно проводят дихроматом или перманганатом калия с серной кислотой.
| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- Глава I. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ
- § 1. Предмет химии. Важнейшие понятия и законы химии
- Основные стехиометрические законы химии
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 2. Строение атома
- Электронные конфигурации атомов
- Ядро атома и радиоактивные превращения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 3. Строение молекул. Химическая связь. Валентность элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 4. Агрегатные состояния вещества
- Характерные свойства газов, жидкостей и твердых тел
- Газообразное состояние. Газовые законы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 5. Закономерности протекания химических реакций
- Химическая кинетика
- Химическое равновесие
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 6. Растворы. Электролитическая диссоциация. Гидролиз солей
- Электролиты и электролитическая диссоциация
- Гидролиз солей
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 7. Классификация химических реакций. Окислительно-восстановительные процессы. Электролиз
- Окислительно-восстановительные реакции
- Электролиз
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
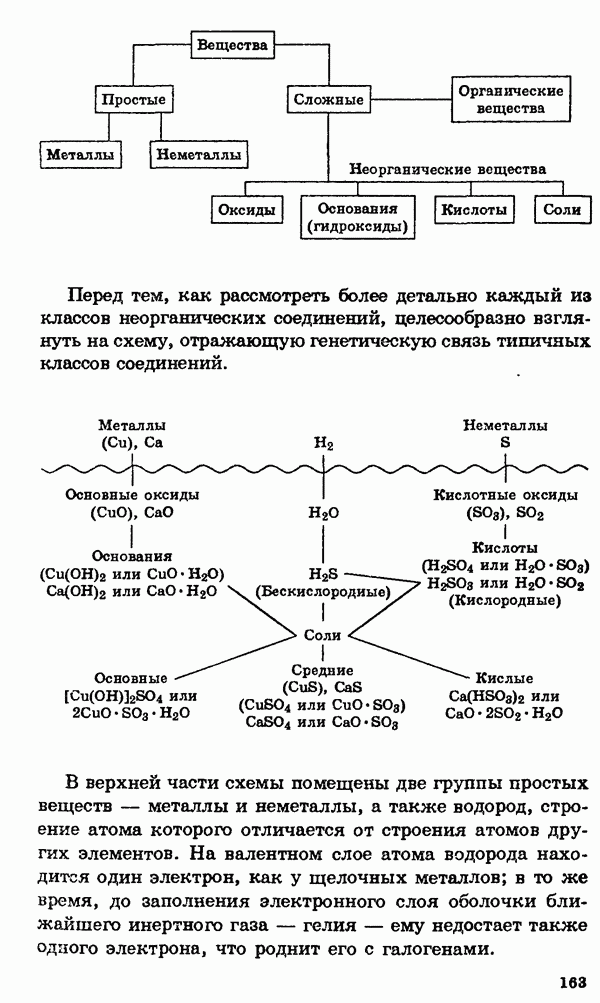
- § 8. Номенклатура, классификация неорганических веществ. Свойства и способы получения
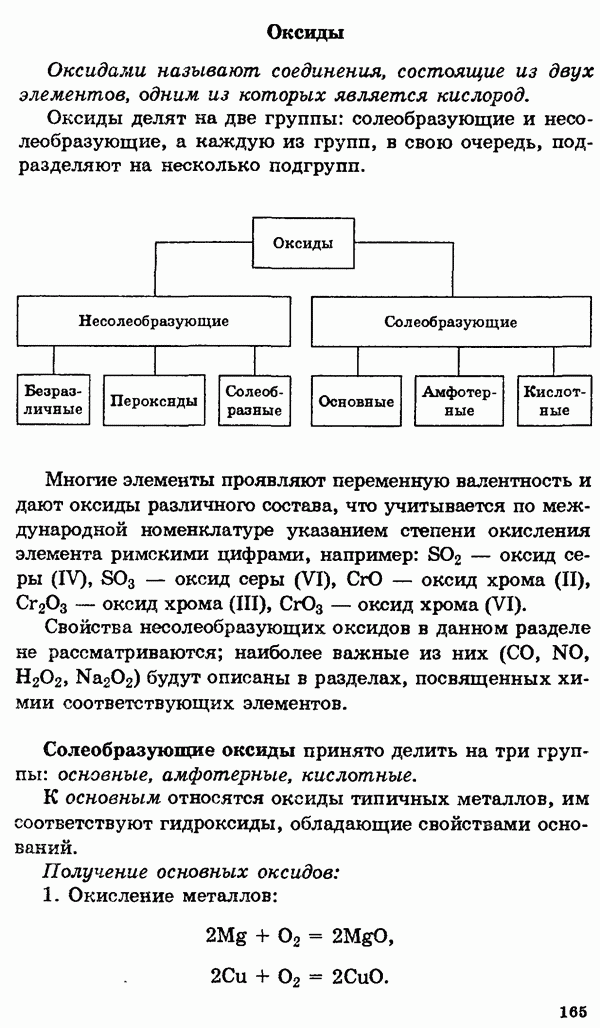
- Оксиды
- Основания (гидроксиды металлов)
- Кислоты
- Соли
- § 9. Водород. Галогены и их соединения
- Галогены и их соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 10. Подгруппа кислорода
- Сера и ее соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 11. Подгруппа азота
- Фосфор и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 12. Подгруппа углерода
- Углерод и его соединения
- Кремний и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 13. Свойства s-элементов (щелочных и щелочноземельных металлов) и их соединений
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 14. Алюминий — типичный р-металл
- Соединения алюминия и их свойства
- ЗАДАЧИ И УПРАЖНЕНИЯ
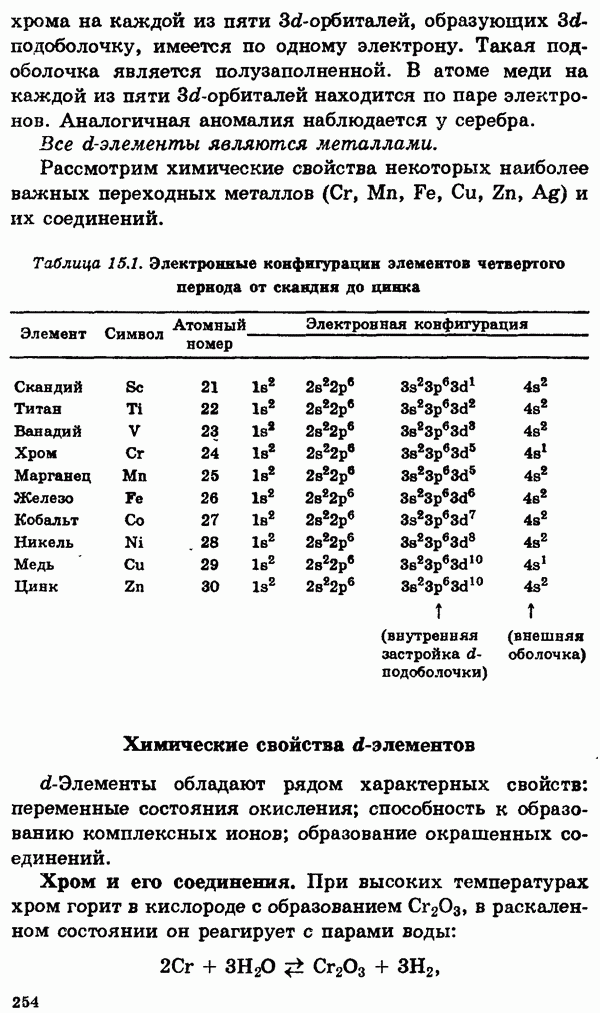
- § 15. Главные переходные металлы (d-элементы) и их соединения
- Химические свойства d-элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 16. Задачи для повторения по неорганической химии
- Глава III. ОРГАНИЧЕСКАЯ ХИМИЯ
- § 17. Основные понятия и закономерности в органической химии. Предмет органической химии
- Классификация и номенклатура органических соединений
- Изомерия органических соединений
- Взаимное влияние атомов в молекуле и реакционная способность органических соединений
- Общая характеристика органических реакций
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 18. Предельные (насыщенные) углеводороды
- Циклоалканы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 19. Алкены. Диеновые углеводороды
- Диеновые углеводороды (алкадиены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 20. Алкины
- ЗАДАЧИ И УПРАЖНЕНИЯ
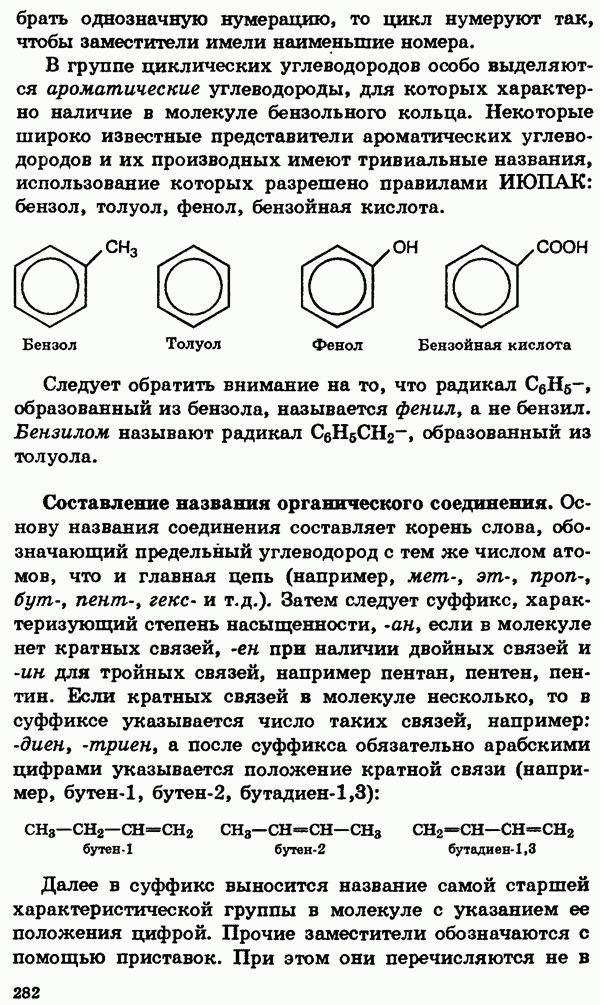
- § 21. Ароматические углеводороды (арены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 22. Спирты и фенолы
- Многоатомные спирты
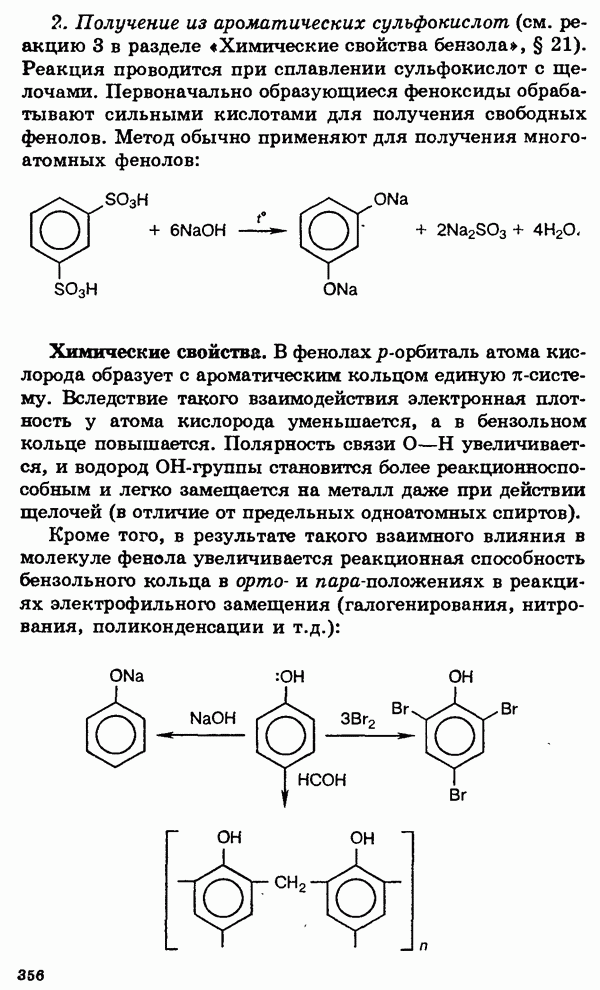
- Фенолы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 23. Карбонильные соединения — альдегиды и кетоны
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 24. Карбоновые кислоты. Сложные эфиры. Жиры
- Сложные эфиры. Жиры
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава 4. ОСНОВНЫЕ ПРИЕМЫ РЕШЕНИЯ ЗАДАЧ
- Определение молекулярной формулы веществ
- Определение состава и разделение смесей
- Задачи на газовые законы
- Способы выражения концентрации растворов
- Ионные реакции в растворах
- Задачи на окислительно-восстановительные реакции
- Разные задачи
- ПРОГРАММА ПО ХИМИИ ДЛЯ ПОСТУПАЮЩИХ В УНИВЕРСИТЕТЫ
- ОТВЕТЫ
- Рекомендуемая литература