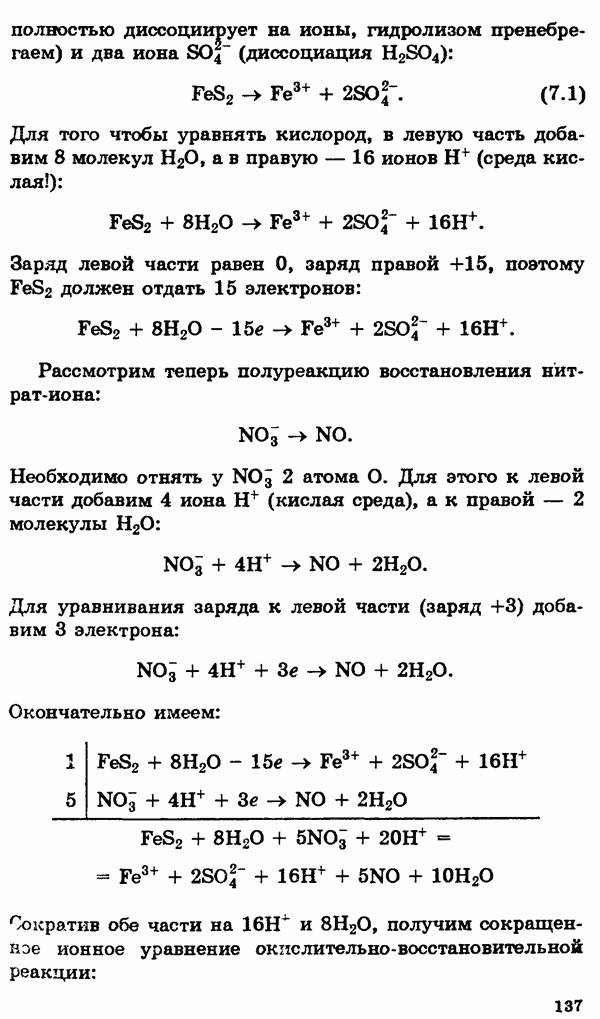| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
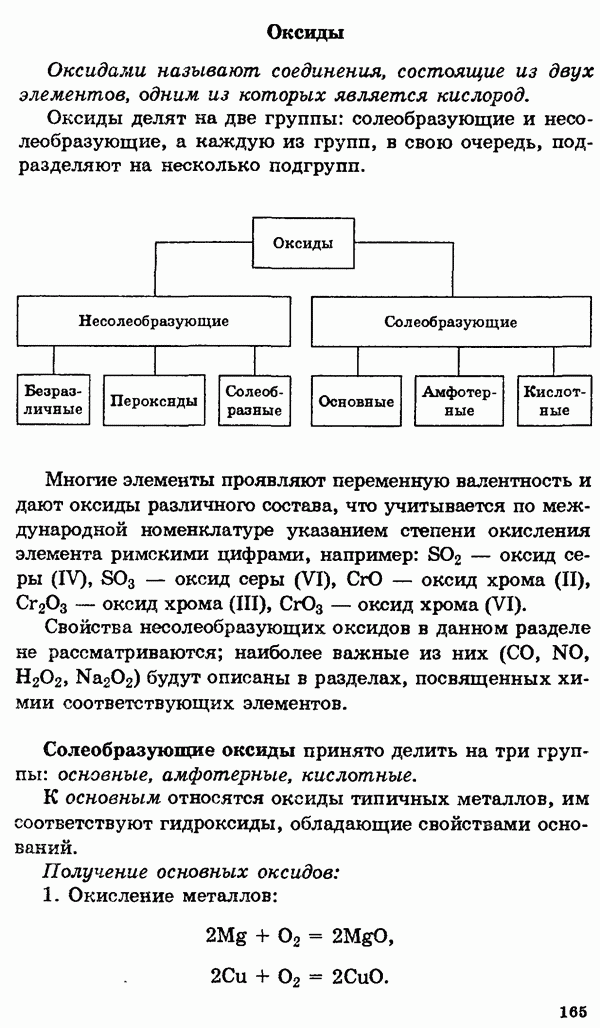
§ 9. Водород. Галогены и их соединения
Водород
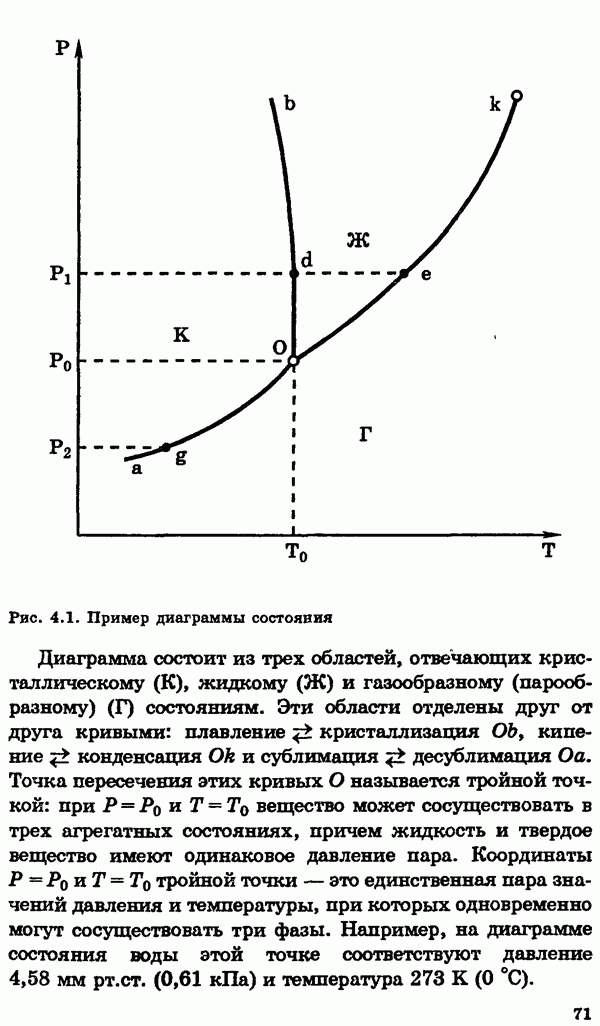
Место водорода в периодической системе.
Атом водорода состоит из одного протона и одного электрона. Этот простейший атом не имеет аналогов в периодической системе. Он способен терять электрон, превращаясь в катион  и в этом отношении сходен с щелочными металлами, которые также проявляют степень окисления
и в этом отношении сходен с щелочными металлами, которые также проявляют степень окисления  Атом водорода может также присоединять электрон, образуя при этом анион
Атом водорода может также присоединять электрон, образуя при этом анион  электронная конфигурация которого такая же, как у атома гелия. В этом отношении водород сходен с галогенами, анионы которых имеют электронные конфигурации соседних благородных газов.
электронная конфигурация которого такая же, как у атома гелия. В этом отношении водород сходен с галогенами, анионы которых имеют электронные конфигурации соседних благородных газов.
Таким образом, водород имеет двойственную природу, проявляя как окислительную, так и восстановительную способность. По этой причине в одних случаях водород помещают в подгруппу щелочных металлов, в других — в подгруппу галогенов.
Химические свойства.
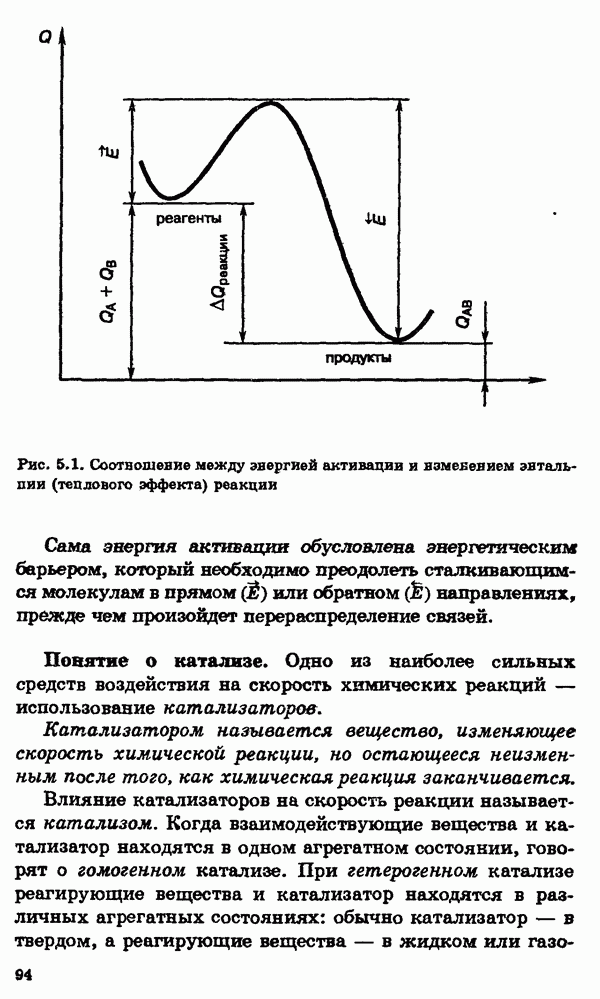
Энергия связи в молекуле водорода  составляет 436 кДж/моль. Большая величина энергии связи объясняет сравнительно малую активность молекулярного водорода при обычных условиях. Так, при комнатной температуре водород реагирует лишь с фтором
составляет 436 кДж/моль. Большая величина энергии связи объясняет сравнительно малую активность молекулярного водорода при обычных условиях. Так, при комнатной температуре водород реагирует лишь с фтором

и с хлором при ультрафиолетовом облучении (см. ниже).
При повышенной температуре водород реагирует со многими веществами, например он сгорает в атмосфере кислорода с образованием воды и выделением большого количества теплоты (см. § 5):

При нагревании водород обратимо реагирует также с бромом, иодом, серой и азотом, причем с последним только в присутствии катализатора и при высоком давлении (см. § 11).
Водород при нагревании способен реагировать не только с простыми, но и со сложными веществами:

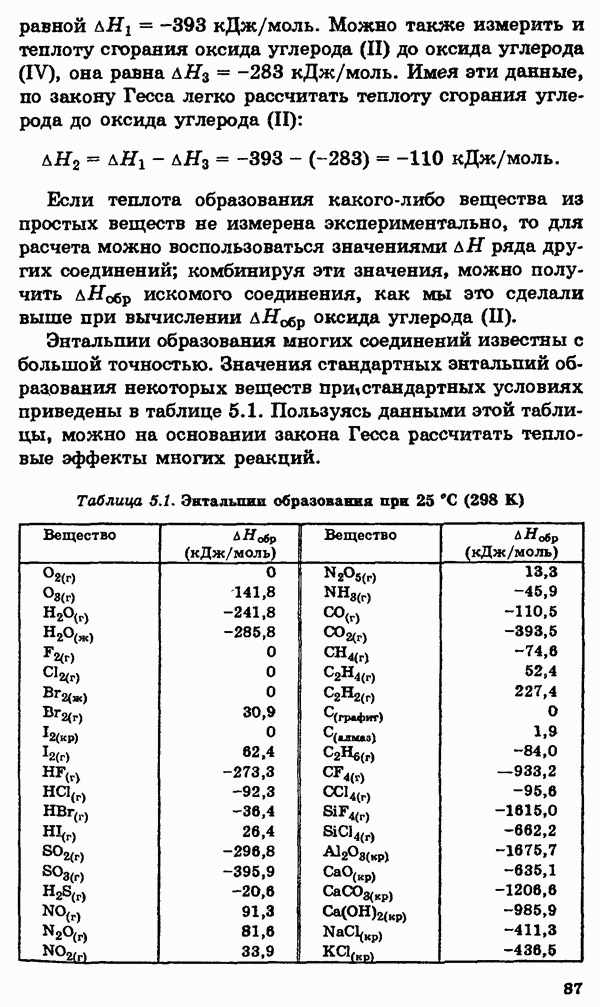
Во всех рассматриваемых реакциях водород является восстановителем, образуя соединения, где его степень окисления равна 
Со многими металлами водород вступает в реакции при повышенных температуре и давлении с образованием гидридов  , где его степень окисления равна 1-:
, где его степень окисления равна 1-:

Гидрид натрия — белое кристаллическое соединение, по физическим свойствам напоминающее хлорид натрия. Однако химические свойства  сильно различаются. Так, хлорид натрия растворяется в воде и диссоциирует в растворе на ионы. Гидрид натрия водой разлагается с образованием щелочи и водорода:
сильно различаются. Так, хлорид натрия растворяется в воде и диссоциирует в растворе на ионы. Гидрид натрия водой разлагается с образованием щелочи и водорода:

Получение водорода.
Для промышленного получения водорода используют следующие способы:
1. Электролиз водных растворов хлоридов (§ 7).
2. Пропускание паров воды над раскаленным углем при температуре 1000 °С:

3. Конверсия метана при высоких температурах:

4. Крекинг углеводородов (§ 18).
Для лабораторного получения водорода используют следующие способы:
1. Взаимодействие металлов с кислотами, например:

2. Взаимодействие щелочноземельных металлов с водой:

3. Взаимодействие алюминия или кремния с водными растворами щелочей:

4. Взаимодействие гидридов с водой (см. выше).
| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- Глава I. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ
- § 1. Предмет химии. Важнейшие понятия и законы химии
- Основные стехиометрические законы химии
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 2. Строение атома
- Электронные конфигурации атомов
- Ядро атома и радиоактивные превращения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 3. Строение молекул. Химическая связь. Валентность элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 4. Агрегатные состояния вещества
- Характерные свойства газов, жидкостей и твердых тел
- Газообразное состояние. Газовые законы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 5. Закономерности протекания химических реакций
- Химическая кинетика
- Химическое равновесие
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 6. Растворы. Электролитическая диссоциация. Гидролиз солей
- Электролиты и электролитическая диссоциация
- Гидролиз солей
- ЗАДАЧИ И УПРАЖНЕНИЯ
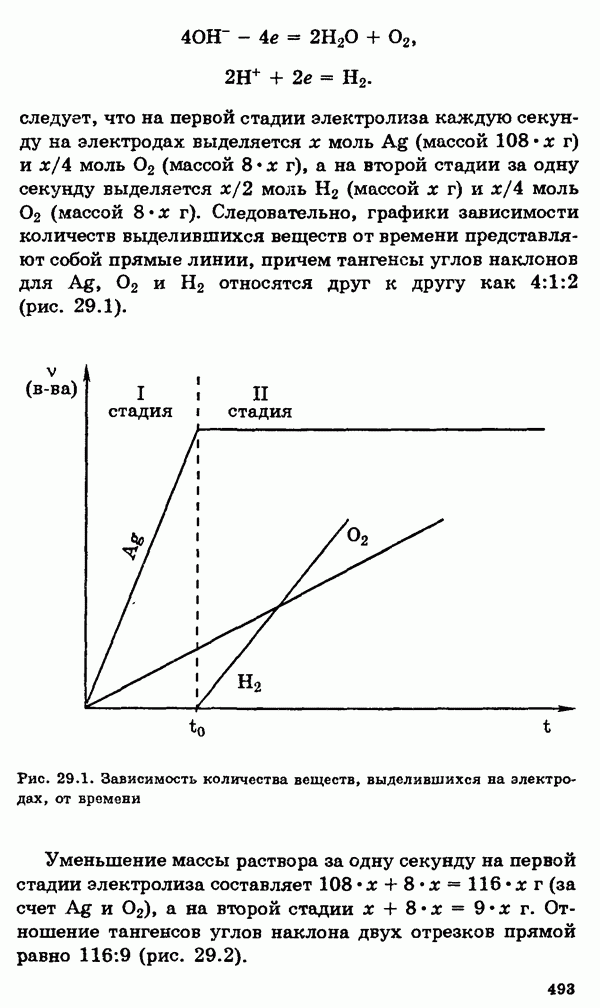
- § 7. Классификация химических реакций. Окислительно-восстановительные процессы. Электролиз
- Окислительно-восстановительные реакции
- Электролиз
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
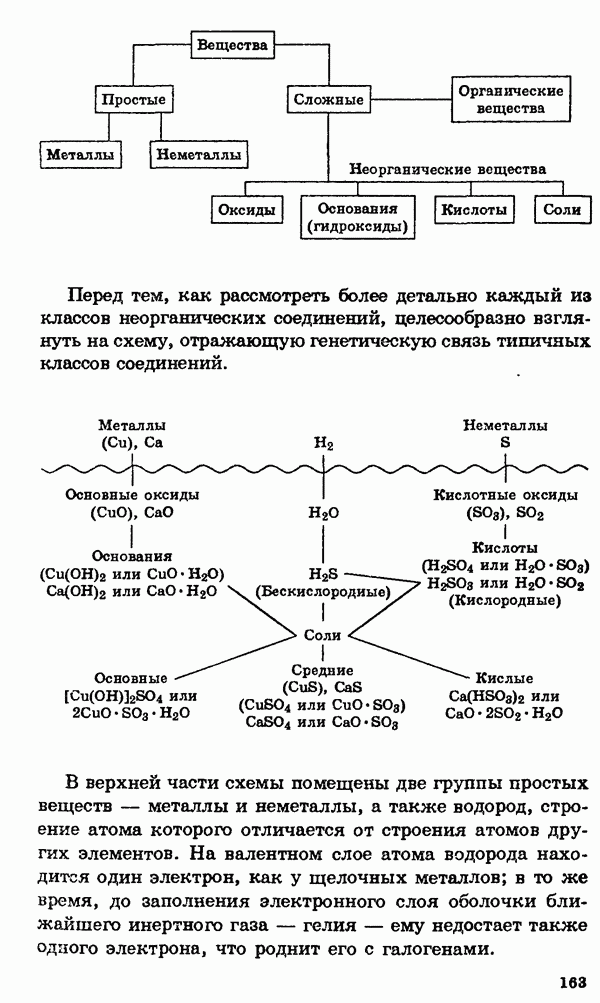
- § 8. Номенклатура, классификация неорганических веществ. Свойства и способы получения
- Оксиды
- Основания (гидроксиды металлов)
- Кислоты
- Соли
- § 9. Водород. Галогены и их соединения
- Галогены и их соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 10. Подгруппа кислорода
- Сера и ее соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 11. Подгруппа азота
- Фосфор и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 12. Подгруппа углерода
- Углерод и его соединения
- Кремний и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 13. Свойства s-элементов (щелочных и щелочноземельных металлов) и их соединений
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 14. Алюминий — типичный р-металл
- Соединения алюминия и их свойства
- ЗАДАЧИ И УПРАЖНЕНИЯ
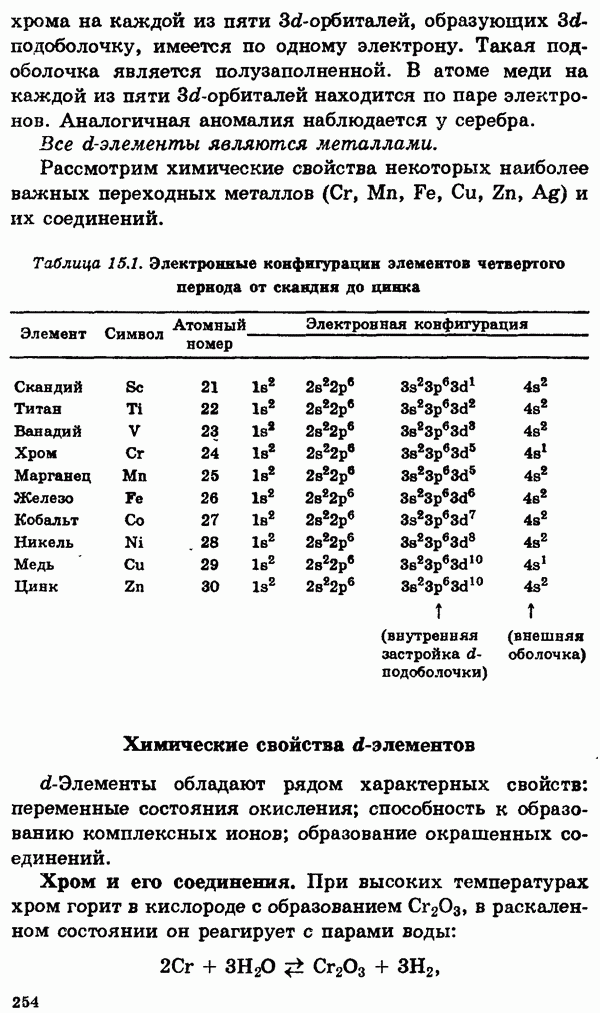
- § 15. Главные переходные металлы (d-элементы) и их соединения
- Химические свойства d-элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 16. Задачи для повторения по неорганической химии
- Глава III. ОРГАНИЧЕСКАЯ ХИМИЯ
- § 17. Основные понятия и закономерности в органической химии. Предмет органической химии
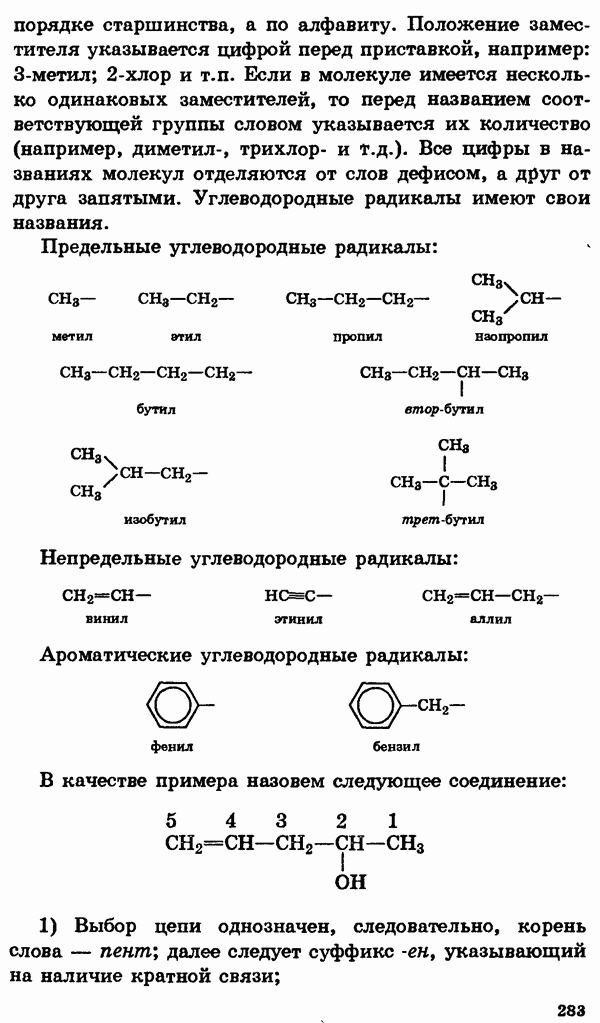
- Классификация и номенклатура органических соединений
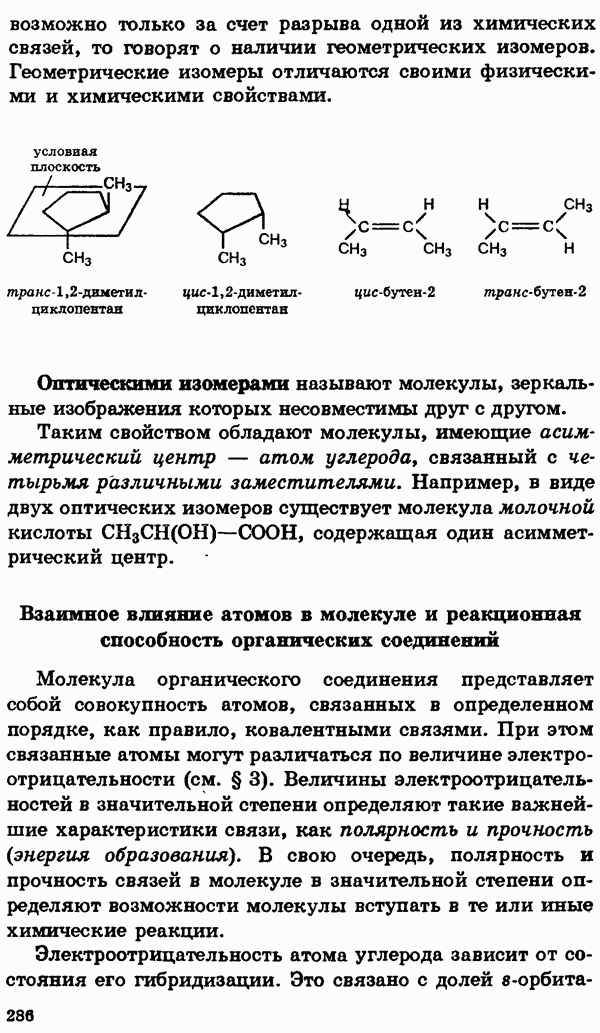
- Изомерия органических соединений
- Взаимное влияние атомов в молекуле и реакционная способность органических соединений
- Общая характеристика органических реакций
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 18. Предельные (насыщенные) углеводороды
- Циклоалканы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 19. Алкены. Диеновые углеводороды
- Диеновые углеводороды (алкадиены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 20. Алкины
- ЗАДАЧИ И УПРАЖНЕНИЯ
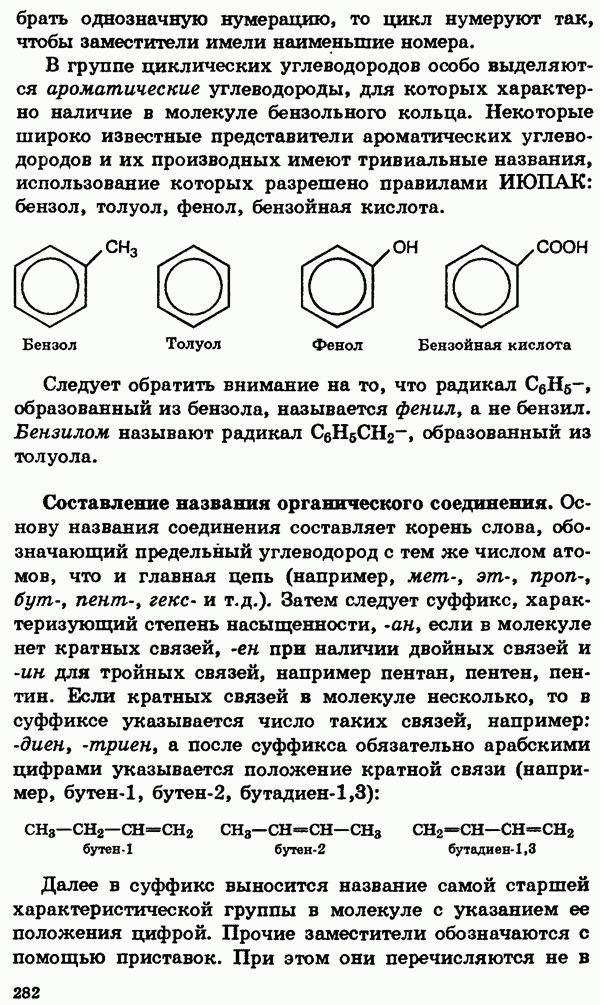
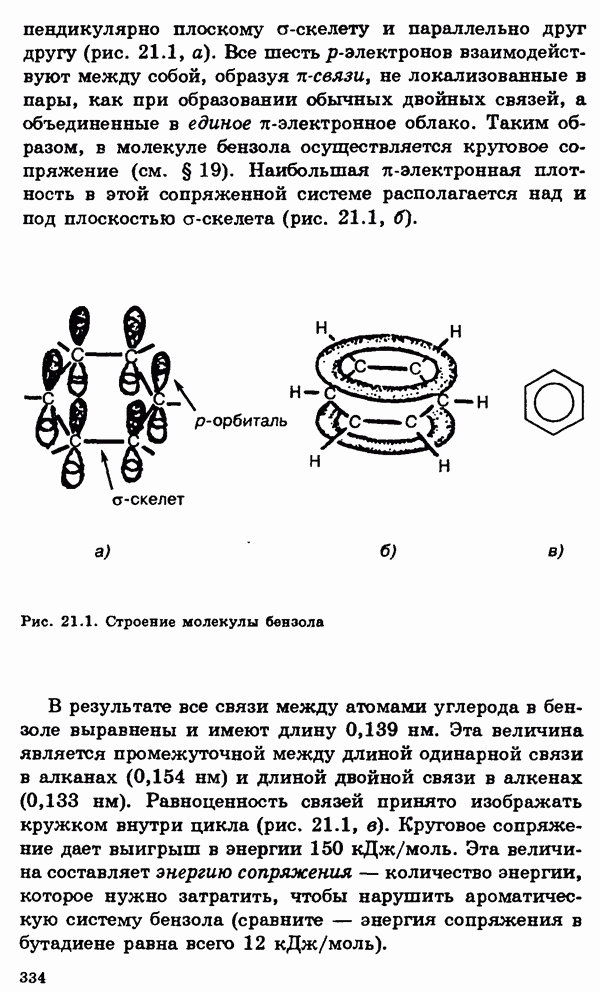
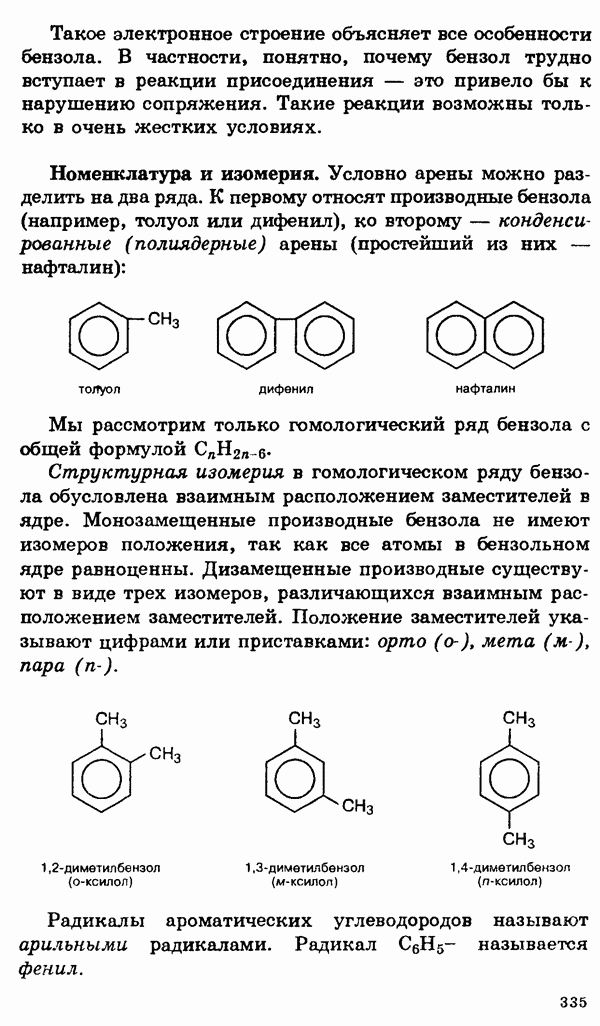
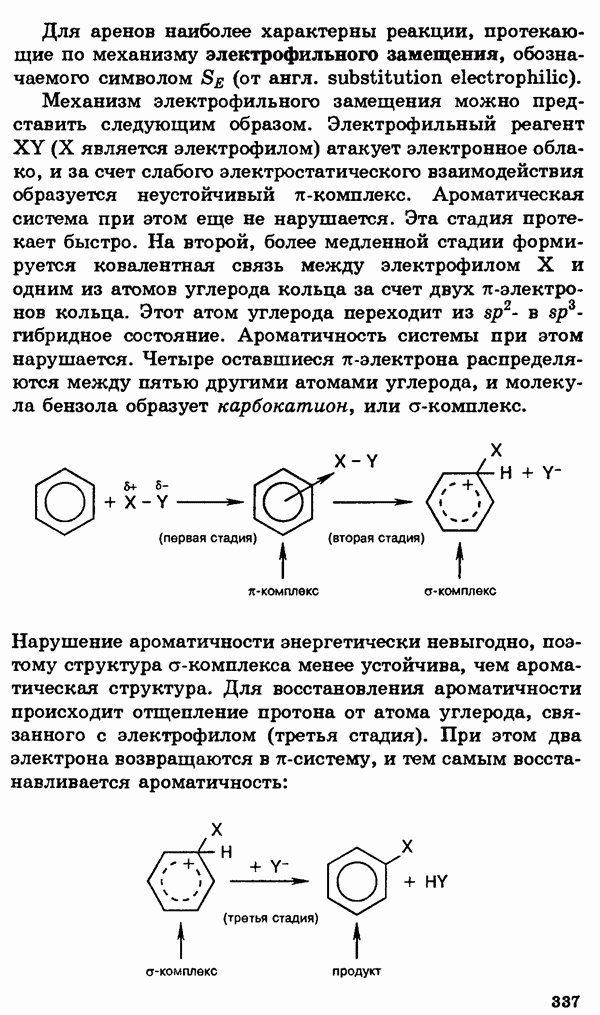
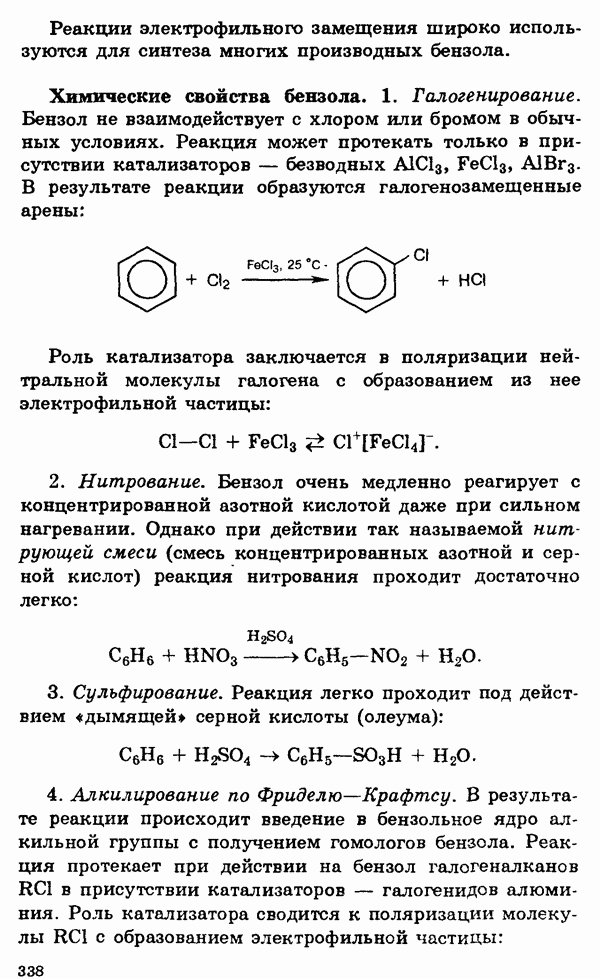
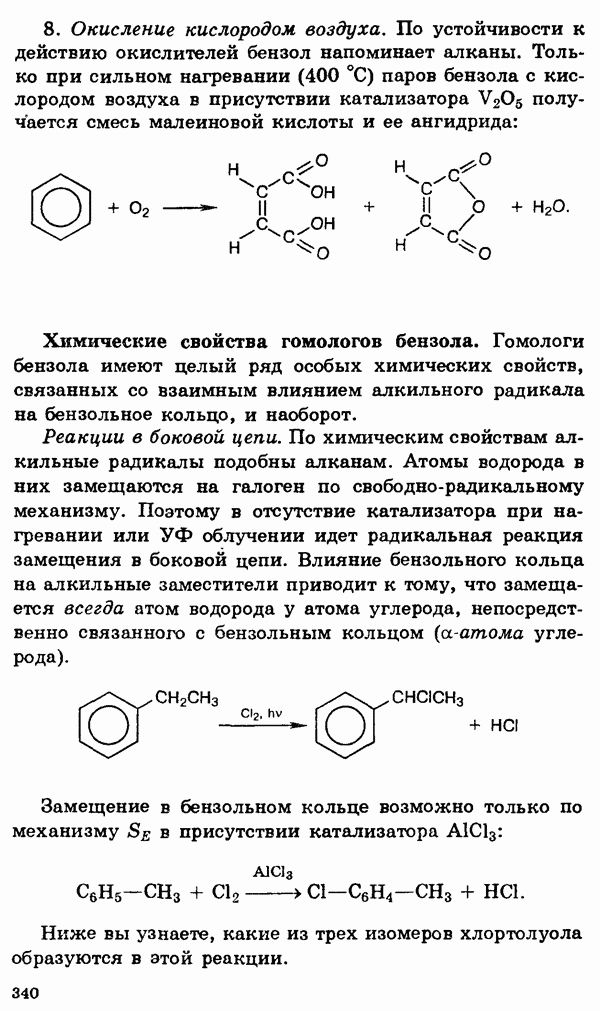
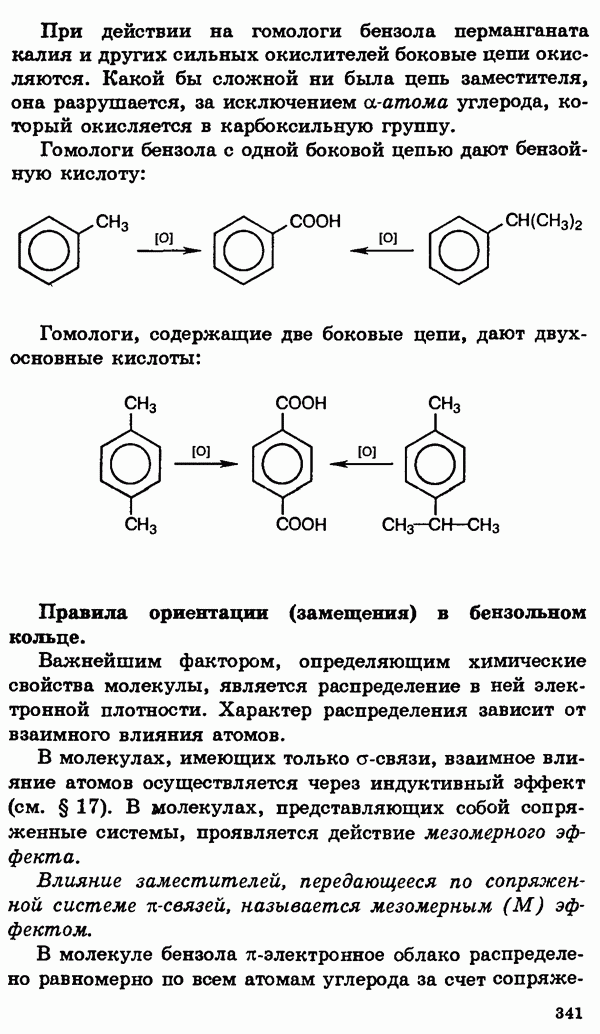
- § 21. Ароматические углеводороды (арены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 22. Спирты и фенолы
- Многоатомные спирты
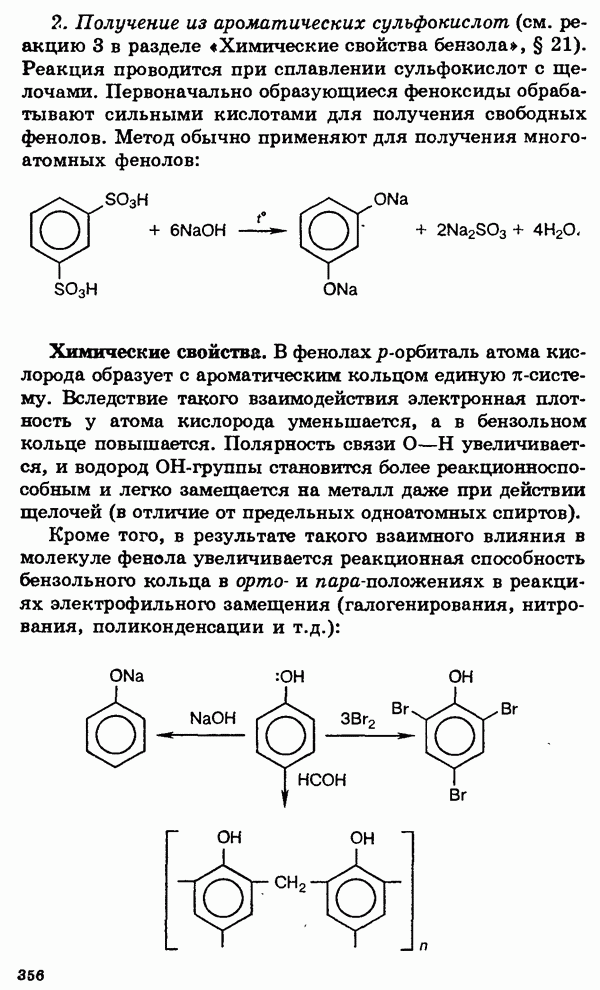
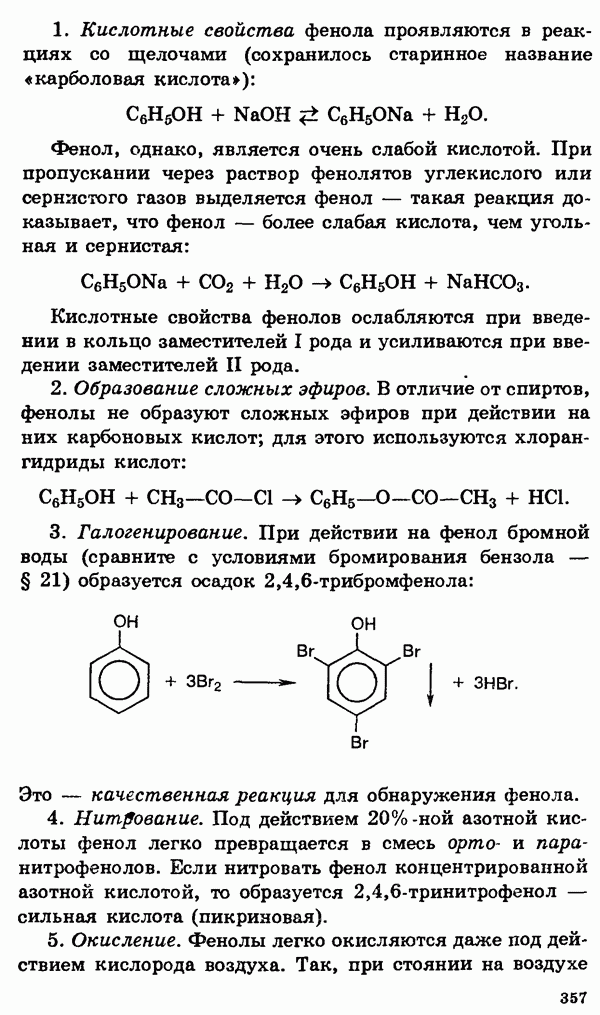
- Фенолы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 23. Карбонильные соединения — альдегиды и кетоны
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 24. Карбоновые кислоты. Сложные эфиры. Жиры
- Сложные эфиры. Жиры
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава 4. ОСНОВНЫЕ ПРИЕМЫ РЕШЕНИЯ ЗАДАЧ
- Определение молекулярной формулы веществ
- Определение состава и разделение смесей
- Задачи на газовые законы
- Способы выражения концентрации растворов
- Ионные реакции в растворах
- Задачи на окислительно-восстановительные реакции
- Разные задачи
- ПРОГРАММА ПО ХИМИИ ДЛЯ ПОСТУПАЮЩИХ В УНИВЕРСИТЕТЫ
- ОТВЕТЫ
- Рекомендуемая литература