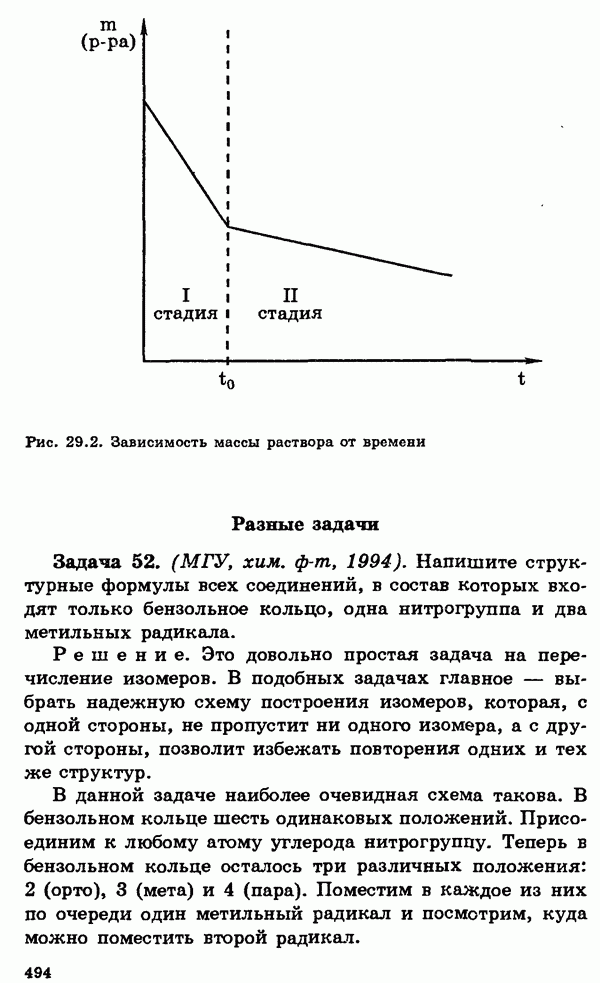
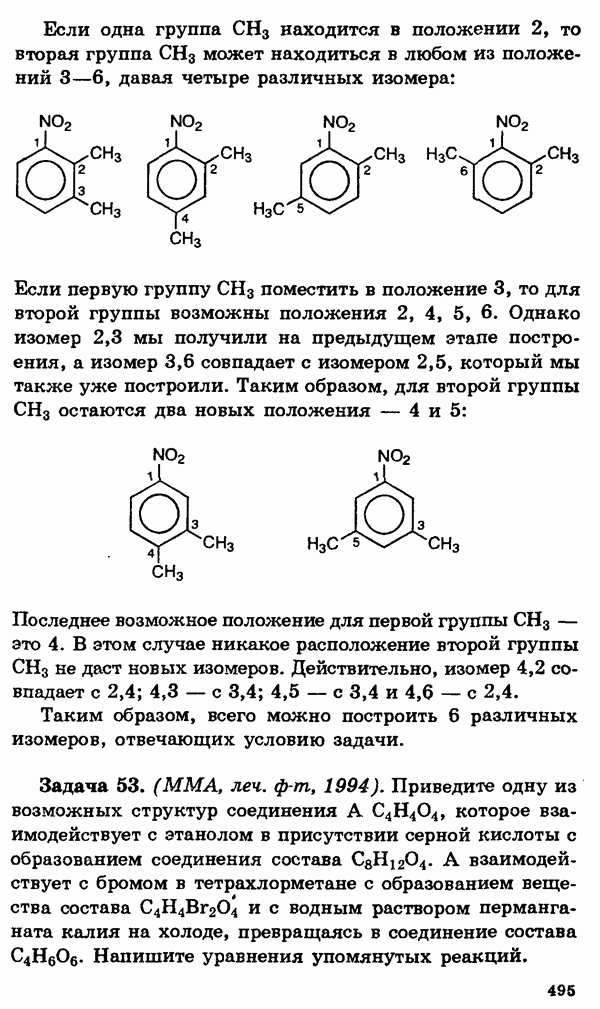
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Глава III. ОРГАНИЧЕСКАЯ ХИМИЯ
§ 17. Основные понятия и закономерности в органической химии. Предмет органической химии
Углерод выделяется среди всех элементов тем, что его атомы могут связываться друг с другом в длинные цепи или циклы. Именно это свойство позволяет углероду образовывать миллионы соединений, изучению которых посвящена целая область — органическая химия.
Несколько причин обусловили проявление углеродом выше отмеченных свойств. Доказано, что энергия связи (прочность связи)  сопоставима с прочностью связей
сопоставима с прочностью связей  . Для сравнения укажем, что связь
. Для сравнения укажем, что связь  намного прочнее связи Si—Si. Углерод обладает возможностью проявлять не одну, а целых три разновидности гибридизации орбиталей: в случае
намного прочнее связи Si—Si. Углерод обладает возможностью проявлять не одну, а целых три разновидности гибридизации орбиталей: в случае  -гибридизации образуются четыре гибридных орбитали, имеющие тетраэдрическую ориентацию; с их помощью образуются простые ковалентные связи; в случае
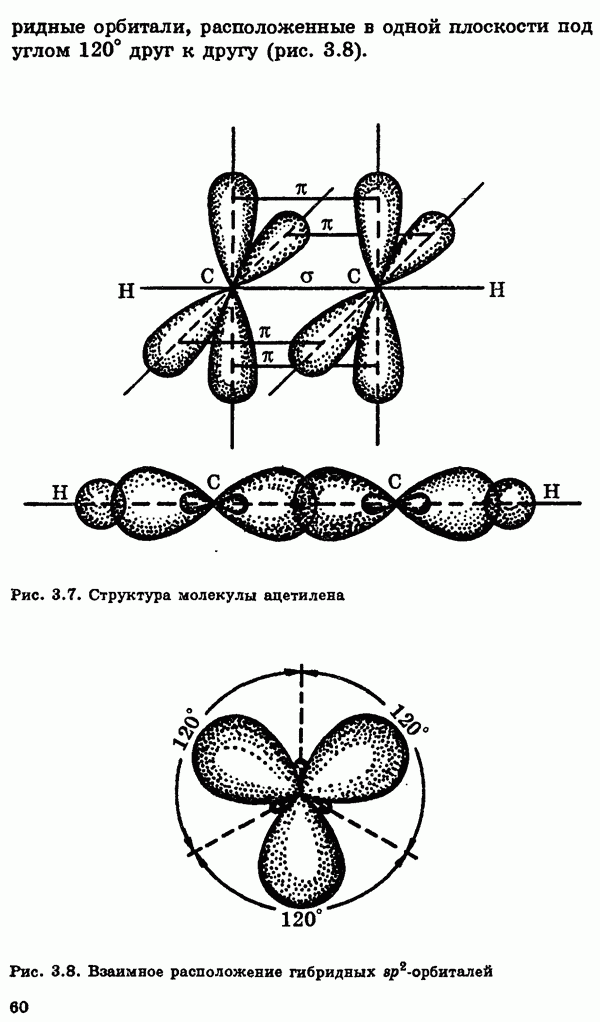
-гибридизации образуются четыре гибридных орбитали, имеющие тетраэдрическую ориентацию; с их помощью образуются простые ковалентные связи; в случае  -гибридизации образуются три гибридные орбитали, ориентированные в одной плоскости, и с их помощью образуются двойные кратные связи; наконец, с помощью двух
-гибридизации образуются три гибридные орбитали, ориентированные в одной плоскости, и с их помощью образуются двойные кратные связи; наконец, с помощью двух  -гибридизованных орбиталей, имеющих линейную ориентацию, между атомами углерода возникают тройные кратные связи. Сейчас хорошо известно, что атомы углерода способны образовывать простые, двойные и тройные связи не только друг с другом, но также и с другими элементами. Таким образом, современная теория строения молекул (ее основы см. в § 3) объясняет и огромное число органических соединений, и зависимость свойств этих соединений от их химического строения.
-гибридизованных орбиталей, имеющих линейную ориентацию, между атомами углерода возникают тройные кратные связи. Сейчас хорошо известно, что атомы углерода способны образовывать простые, двойные и тройные связи не только друг с другом, но также и с другими элементами. Таким образом, современная теория строения молекул (ее основы см. в § 3) объясняет и огромное число органических соединений, и зависимость свойств этих соединений от их химического строения.
Она же полностью подтверждает основные принципы теории химического строения, разработанные выдающимся русским ученым А. М. Бутлеровым и изложенные им в докладе «О теории химического строения» на Международном съезде естествоиспытателей в 1861 г.
Основные положения этой теории (иногда ее называют структурной) сводятся к следующему:
1) атомы в молекулах соединены между собой в определенном порядке химическими связями согласно их валентности;
2) свойства вещества определяются не только качественным составом, но и его строением, взаимным влиянием атомов, как связанных между собой химическими связями, так и непосредственно не связанных;
3) строение молекул может быть установлено на осцове изучения их химических свойств.
Важным следствием теории строения был вывод о том, что каждое органическое соединение должно иметь одну химическую формулу, отражающую ее строение. Такой вывод теоретически обосновывал хорошо известное уже тогда явление изомерии, открытое в 1830 г., — существование веществ с одинаковым молекулярным составом, но обладающих различными свойствами.
Существование изомеров потребовало использования не только простых молекулярных формул, но и структурных формул, отражающих порядок связи атомов в молекуле каждого изомера.
Структурная формула — изображение химических связей между атомами в молекуле с учетом их валентности (см. § 3).
| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- Глава I. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ
- § 1. Предмет химии. Важнейшие понятия и законы химии
- Основные стехиометрические законы химии
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 2. Строение атома
- Электронные конфигурации атомов
- Ядро атома и радиоактивные превращения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 3. Строение молекул. Химическая связь. Валентность элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 4. Агрегатные состояния вещества
- Характерные свойства газов, жидкостей и твердых тел
- Газообразное состояние. Газовые законы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 5. Закономерности протекания химических реакций
- Химическая кинетика
- Химическое равновесие
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 6. Растворы. Электролитическая диссоциация. Гидролиз солей
- Электролиты и электролитическая диссоциация
- Гидролиз солей
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 7. Классификация химических реакций. Окислительно-восстановительные процессы. Электролиз
- Окислительно-восстановительные реакции
- Электролиз
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
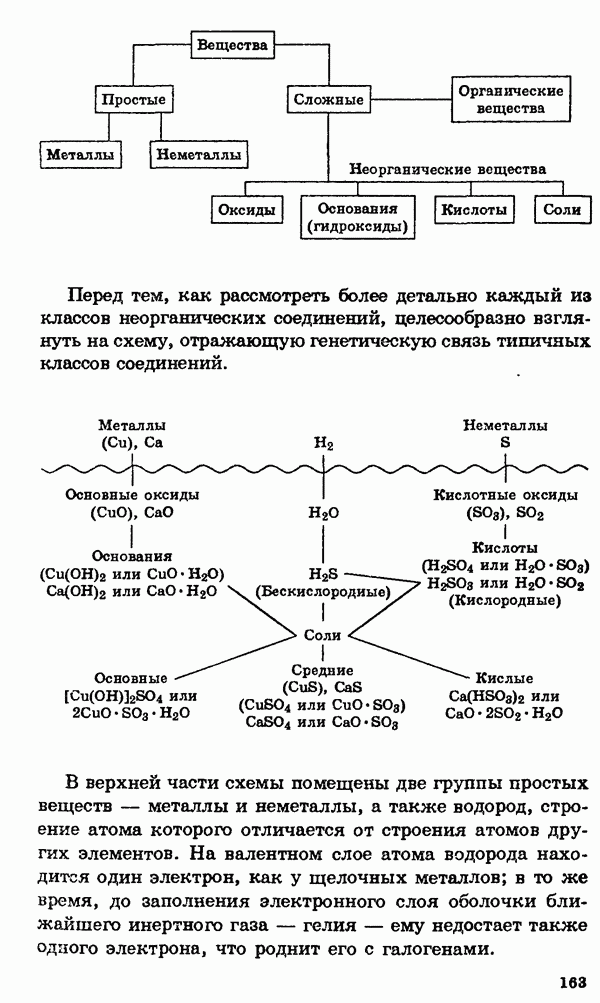
- § 8. Номенклатура, классификация неорганических веществ. Свойства и способы получения
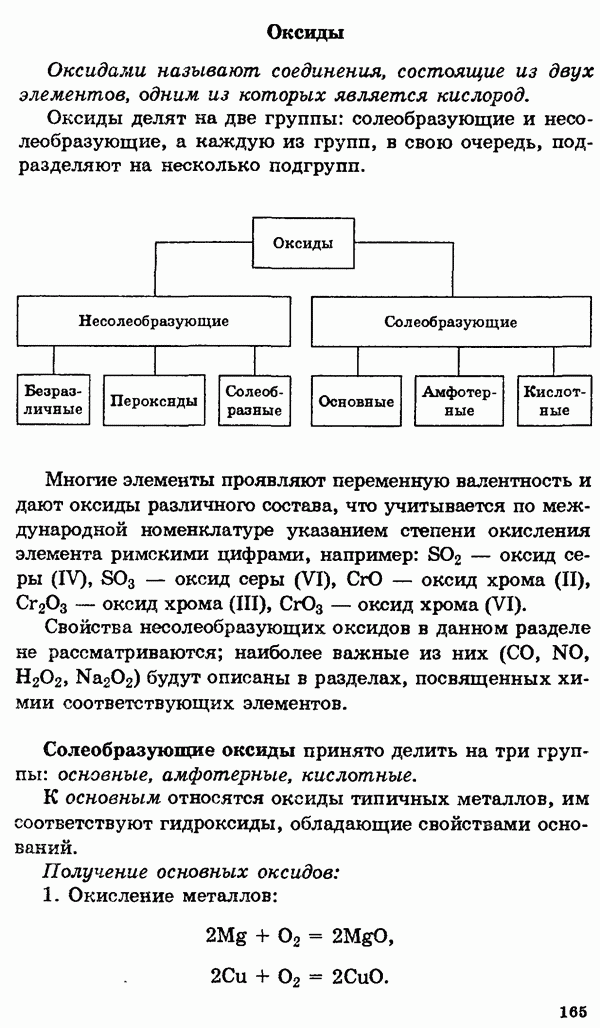
- Оксиды
- Основания (гидроксиды металлов)
- Кислоты
- Соли
- § 9. Водород. Галогены и их соединения
- Галогены и их соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 10. Подгруппа кислорода
- Сера и ее соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 11. Подгруппа азота
- Фосфор и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 12. Подгруппа углерода
- Углерод и его соединения
- Кремний и его соединения
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 13. Свойства s-элементов (щелочных и щелочноземельных металлов) и их соединений
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 14. Алюминий — типичный р-металл
- Соединения алюминия и их свойства
- ЗАДАЧИ И УПРАЖНЕНИЯ
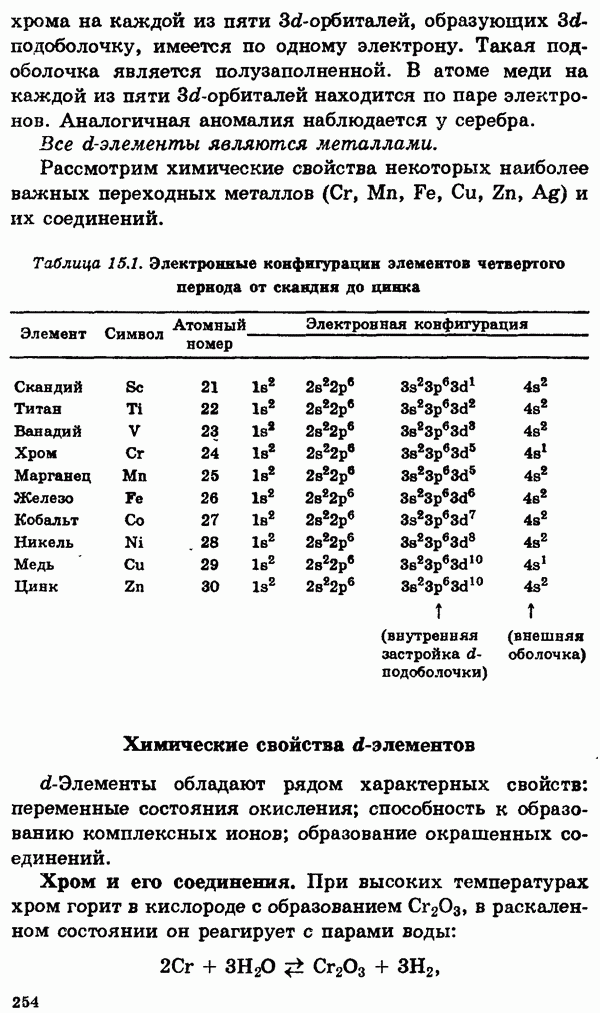
- § 15. Главные переходные металлы (d-элементы) и их соединения
- Химические свойства d-элементов
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 16. Задачи для повторения по неорганической химии
- Глава III. ОРГАНИЧЕСКАЯ ХИМИЯ
- § 17. Основные понятия и закономерности в органической химии. Предмет органической химии
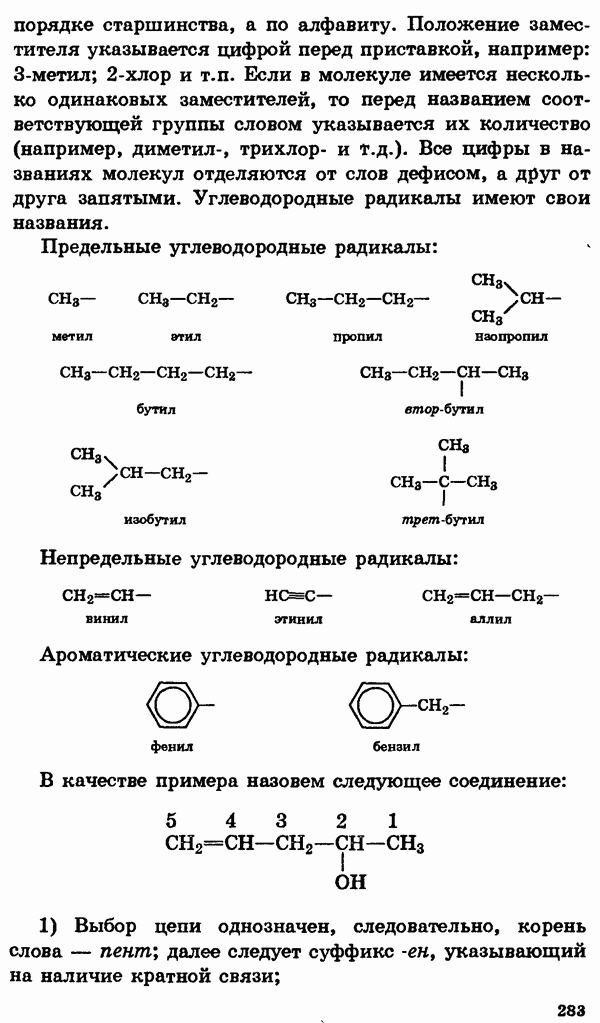
- Классификация и номенклатура органических соединений
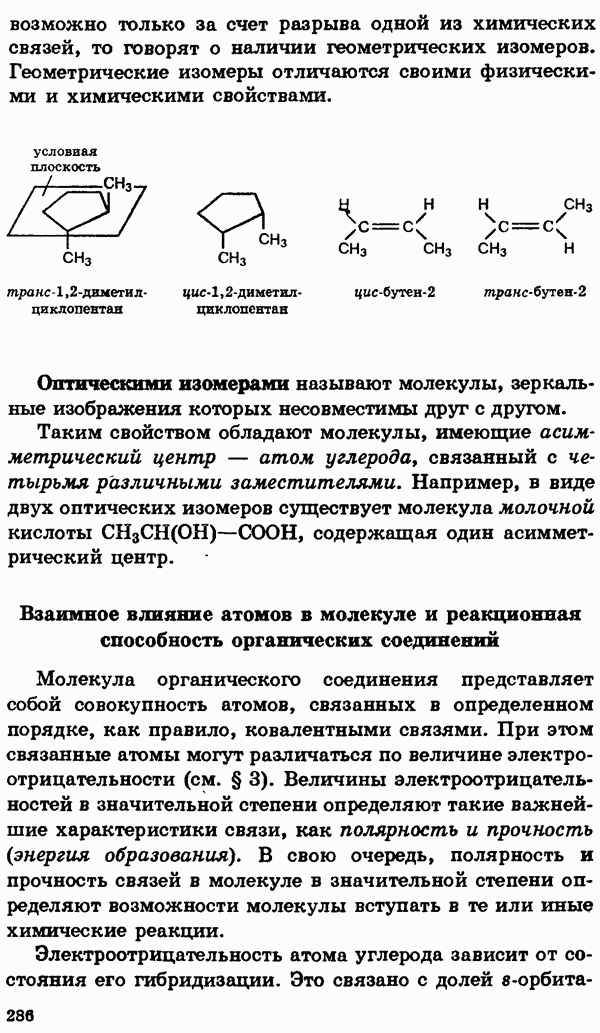
- Изомерия органических соединений
- Взаимное влияние атомов в молекуле и реакционная способность органических соединений
- Общая характеристика органических реакций
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 18. Предельные (насыщенные) углеводороды
- Циклоалканы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 19. Алкены. Диеновые углеводороды
- Диеновые углеводороды (алкадиены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 20. Алкины
- ЗАДАЧИ И УПРАЖНЕНИЯ
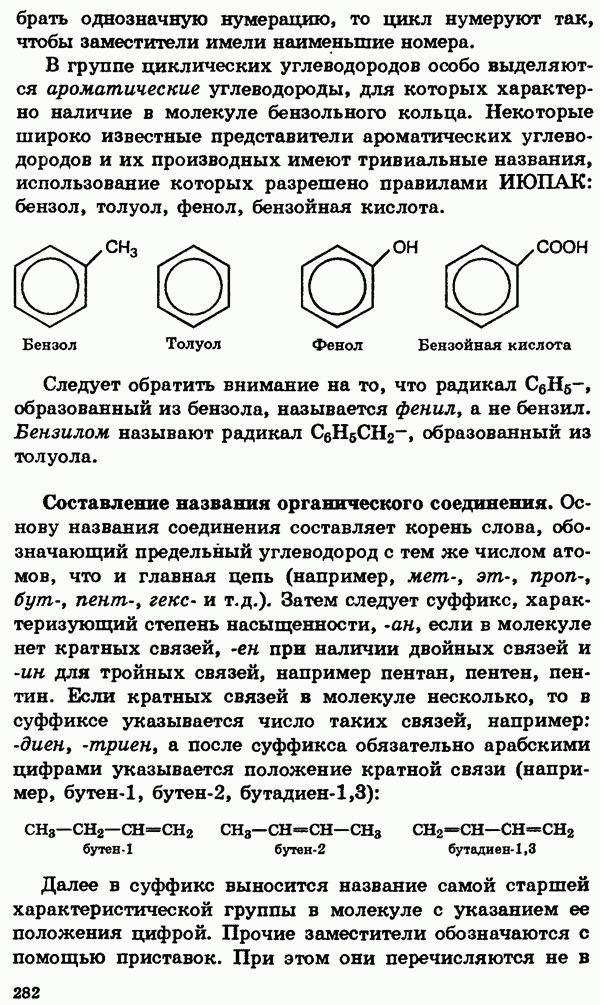
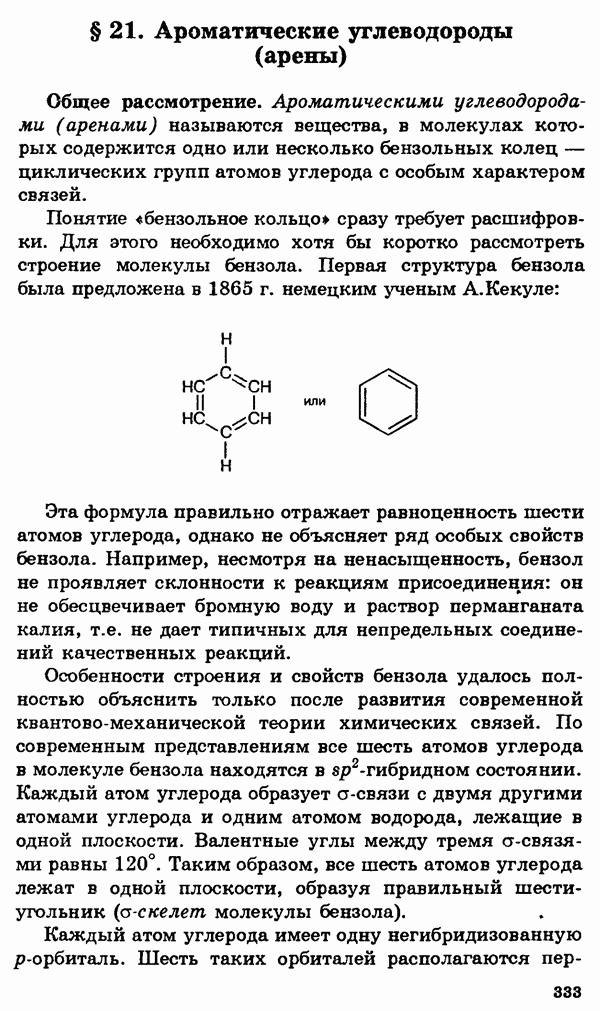
- § 21. Ароматические углеводороды (арены)
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 22. Спирты и фенолы
- Многоатомные спирты
- Фенолы
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 23. Карбонильные соединения — альдегиды и кетоны
- ЗАДАЧИ И УПРАЖНЕНИЯ
- § 24. Карбоновые кислоты. Сложные эфиры. Жиры
- Сложные эфиры. Жиры
- ЗАДАЧИ И УПРАЖНЕНИЯ
- Глава 4. ОСНОВНЫЕ ПРИЕМЫ РЕШЕНИЯ ЗАДАЧ
- Определение молекулярной формулы веществ
- Определение состава и разделение смесей
- Задачи на газовые законы
- Способы выражения концентрации растворов
- Ионные реакции в растворах
- Задачи на окислительно-восстановительные реакции
- Разные задачи
- ПРОГРАММА ПО ХИМИИ ДЛЯ ПОСТУПАЮЩИХ В УНИВЕРСИТЕТЫ
- ОТВЕТЫ
- Рекомендуемая литература