| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
22. ЯЩИК ВАНТ-ГОФФА
Равновесие химических реакций в газах можно описать термодинамически, предполагая, что существует идеальная полупроницаемая перегородка, наделенная следующими двумя свойствами:
1) перегородка, полупроницаемая для газа А, полностью непроницаема для других газов;
2) когда перегородка, полупроницаемая для газа А, разделяет два объема, каждый из которых содержит смесь газа  с каким-либо другим газом, то газ А проходит через перегородку из той смеси, где его парциальное давление выше, в смесь с более низким парциальным давлением. Равновесие достигается, когда парциальные давления газа А с обеих сторон перепонки становятся равными.
с каким-либо другим газом, то газ А проходит через перегородку из той смеси, где его парциальное давление выше, в смесь с более низким парциальным давлением. Равновесие достигается, когда парциальные давления газа А с обеих сторон перепонки становятся равными.
Отметим, что газ может течь самопроизвольно из области с более низким общим давлением в область с более высоким общим давлением если парциальное давление газа, который проходит через перегородку, выше в той области, где общее давление ниже, и ниже в области более высокого общего давления. Таким образом, если перегородка, полупроницаемая для водорода, разделяет ящик, содержащий водород под давлением в одну атмосферу, от ящика, содержащего кислород при двух атмосферах, то водород будет течь через перепонку, несмотря на то, что общее давление с другой стороны вдвое больше.
Следовало бы сказать, что в действительности не существует идеальных полупроницаемых перегородок. Для водорода наилучшим приближением к такой перегородке является горячая палладиевая фольга.
Чтобы вывести условия равновесия химических реакций (135), опишем сначала процесс, при котором реакция может быть
выполнена изотермически и обратимо. Это можно сделать при помощи так называемого ящика Вант-Гоффа.
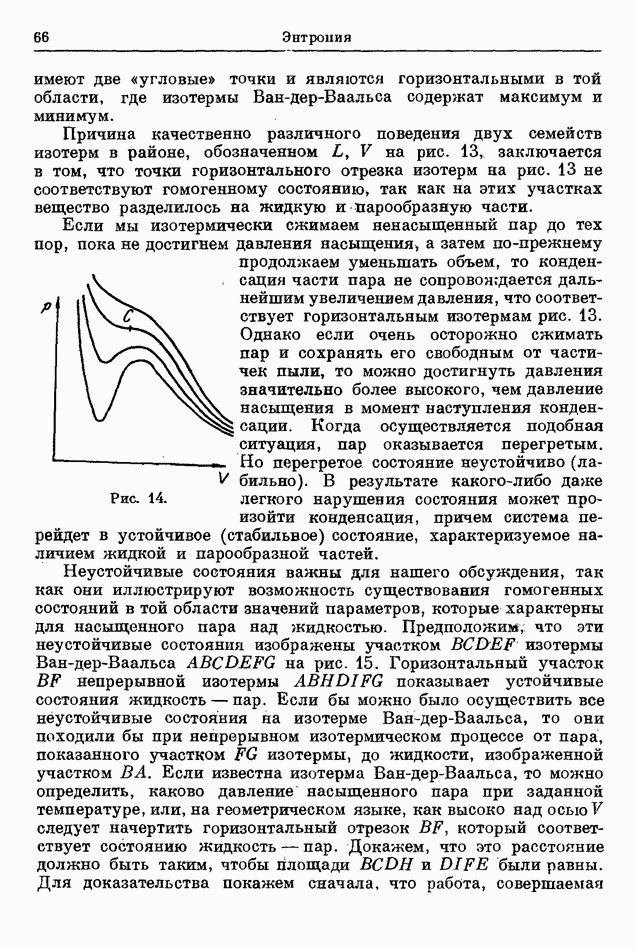
Ящик представляет собой огромный резервуар, в котором находится большое количество газов  в химическом равновесии при температуре
в химическом равновесии при температуре  С одной стороны ящика (на рис. 17 слева) расположено
С одной стороны ящика (на рис. 17 слева) расположено  окон, причем
окон, причем  (мы считаем сверху вниз) полупроницаемо для газа
(мы считаем сверху вниз) полупроницаемо для газа  а с другой стороны (на рис. 17 справа, на котором мы полагаем
а с другой стороны (на рис. 17 справа, на котором мы полагаем  имеется
имеется  окон, полупроницаемых для некоторых других газов
окон, полупроницаемых для некоторых других газов  Снаружи к окнам присоединены цилиндры с подвижными поршнями, как показано на рисунке.
Снаружи к окнам присоединены цилиндры с подвижными поршнями, как показано на рисунке.

Рис. 17.
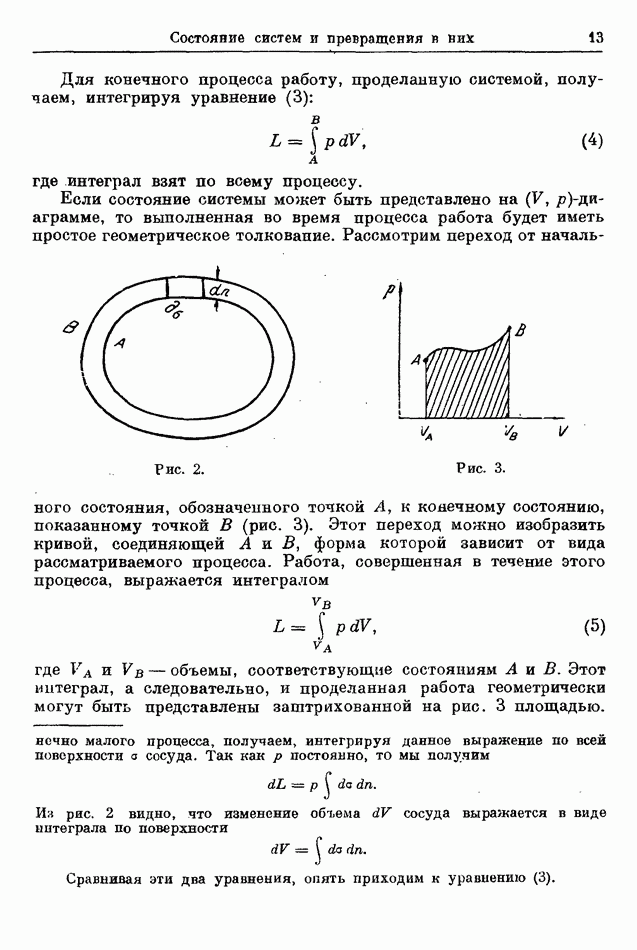
Теперь опишем обратимое изотермическое превращение нашей системы и подсчитаем непосредственно работу  проделанную системой во время этого превращения. Однако, согласно результату § 17, работа
проделанную системой во время этого превращения. Однако, согласно результату § 17, работа  при превращении должна равняться свободной энергии начального состояния минус свободная энергия конечного состояния. Сравнивая эти два выражения для
при превращении должна равняться свободной энергии начального состояния минус свободная энергия конечного состояния. Сравнивая эти два выражения для  получим выведенный ранее результат.
получим выведенный ранее результат.

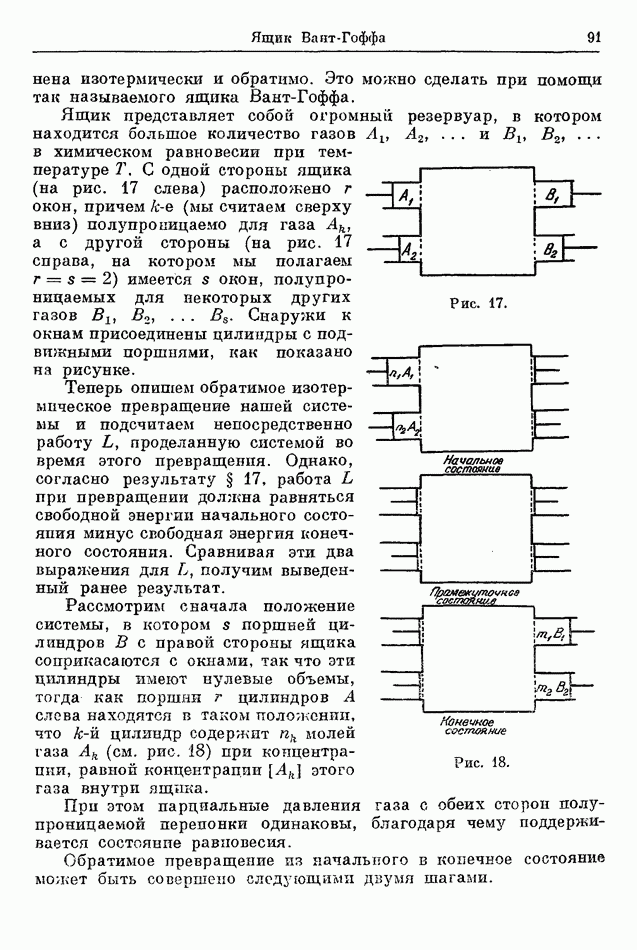
Рис. 18.
Рассмотрим сначала положение системы, в котором  поршней цилиндров В с правой стороны ящика соприкасаются с окнами, так что эти цилиндры имеют нулевые объемы, тогда как поршни
поршней цилиндров В с правой стороны ящика соприкасаются с окнами, так что эти цилиндры имеют нулевые объемы, тогда как поршни  цилиндров А слева находятся в таком положении, что
цилиндров А слева находятся в таком положении, что  цилиндр содержит
цилиндр содержит  молей газа
молей газа  (см. рис. 18) при концентрации, равной концентрации
(см. рис. 18) при концентрации, равной концентрации  этого газа внутри ящика.
этого газа внутри ящика.
При этом парциальные давления газа с обеих сторон полупроницаемой перепонки одинаковы, благодаря чему поддерживается состояние равновесия.
Обратимое превращение из начального в конечное состояние может быть совершено следующими двумя шагами.
1-й шаг. Начиная с первоначального положения (рис. 18), медленно перемещаем внутрь поршни в цилиндрах — с левой стороны ящика — до тех пор, пока газы, содержащиеся в этих цилиндрах, пройдут через полупроницаемую перепонку в большой ящик. В конце процесса система будет находиться в промежуточном состоянии, которое изображено на рис. 18. Мы предполагаем, что объем большого ящика столь велик, что относительное изменение концентрации в результате такого отекания газа пренебрежимо мало. Поэтому концентрации газов А во время процесса практически постоянны и равны 
Совершенная системой во время этого процесса работа  очевидно, является отрицательной, так как она проделана поршнями в направлении, противоположном давлению газов. В первом цилиндре давление остается постоянным и равным парциальному давлению
очевидно, является отрицательной, так как она проделана поршнями в направлении, противоположном давлению газов. В первом цилиндре давление остается постоянным и равным парциальному давлению  газа
газа  виутри ящика, тогда как объем цилиндра изменяется от начального объема
виутри ящика, тогда как объем цилиндра изменяется от начального объема  до конечного объема, равного нулю. Работа равна произведению постоянного давления
до конечного объема, равного нулю. Работа равна произведению постоянного давления  на изменение объема, т. е.
на изменение объема, т. е.

Так как цилиндр первоначально содержал  молей, то из уравнения состояния имеем
молей, то из уравнения состояния имеем  Работа, таким образом, равна
Работа, таким образом, равна  Суммируя по всем цилиндрам слева, получаем
Суммируя по всем цилиндрам слева, получаем

2-й шаг. Начиная с промежуточного состояния, очень медленно переместим наружу поршни в  цилиндрах с правой стороны ящика (первоначально они соприкасались с окнами). Так как дно
цилиндрах с правой стороны ящика (первоначально они соприкасались с окнами). Так как дно  цилиндра, считая сверху вниз, полупроницаемо для газа
цилиндра, считая сверху вниз, полупроницаемо для газа  то этот цилиндр поглощает во время процесса газ
то этот цилиндр поглощает во время процесса газ  и его концентрация в цилиндре будет равна концентрации в большом ящике, т. е. равна
и его концентрация в цилиндре будет равна концентрации в большом ящике, т. е. равна  Перемещаем поршни в цилиндрах сверху вниз до тех пор, пока не достигнем
Перемещаем поршни в цилиндрах сверху вниз до тех пор, пока не достигнем  молей газов
молей газов 
Таким образом, мы придем к конечному состоянию, показанному на рис. 18 справа. У цилиндров А поршни касаются окон, вследствие чего их объемы равны нулю, тогда как все поршни в цилиндрах В расположены так, что  цилиндр, считая сверху вниз, содеряшт
цилиндр, считая сверху вниз, содеряшт  молей газа
молей газа  при концентрации, равной концентрации
при концентрации, равной концентрации  этого газа внутри ящика. Следовательно, газы
этого газа внутри ящика. Следовательно, газы  в цилиндрах и ящике находятся в равновесии благодаря полупроницаемости днищ цилиндров. Работа
в цилиндрах и ящике находятся в равновесии благодаря полупроницаемости днищ цилиндров. Работа  проделанная системой во время второго шага, будет, очевидно,
проделанная системой во время второго шага, будет, очевидно,
положительной. Она может быть подсчитана так же, как и раньше. Находим

Общая работа, выполненная во время всего превращения — сумма  т. е.
т. е.

Эта работа равна разности между свободными энергиями начального и конечного состояний. Чтобы найти эту разность, отметим, что в начальном и конечном состояниях содержимое большого ящика одно и то же. Действительно, при переходе из одного состояния в другое мы сначала ввели внутрь большого ящика  молей
молей  молей
молей  молей
молей  (1-й шаг), а затем извлекли
(1-й шаг), а затем извлекли  молей
молей  молей
молей  молей
молей  Но, согласно уравнению реакции (135), вещества, введенные в большой ящик, эквивалентны изъятым. Поэтому надо учесть только разность между свободной энергией газов А, содержащихся в цилиндрах А вначале, и свободной энергией газов В, содержащихся в цилиндрах В в конце.
Но, согласно уравнению реакции (135), вещества, введенные в большой ящик, эквивалентны изъятым. Поэтому надо учесть только разность между свободной энергией газов А, содержащихся в цилиндрах А вначале, и свободной энергией газов В, содержащихся в цилиндрах В в конце.
Свободная энергия  молей
молей  в первом цилиндре (начальное состояние) может быть вычислена следующим образом. Объем, занимаемый одним молем газа, очевидно, равен обратной величине концентрации
в первом цилиндре (начальное состояние) может быть вычислена следующим образом. Объем, занимаемый одним молем газа, очевидно, равен обратной величине концентрации  Свободная энергия одного моля
Свободная энергия одного моля  получается тогда из уравнения (119) подстановкой в него
получается тогда из уравнения (119) подстановкой в него  для объема одного моля. Так как мы имеем
для объема одного моля. Так как мы имеем  молей
молей  то свободная энергия этого газа составляет
то свободная энергия этого газа составляет

где  и — молярные теплоемкость, энергия и энтропийная постоянная газа
и — молярные теплоемкость, энергия и энтропийная постоянная газа  Используя подобные обозначения для газов
Используя подобные обозначения для газов  получаем для свободной энергии газов А, находящихся первоначально в цилиндрах А, следующее выражение:
получаем для свободной энергии газов А, находящихся первоначально в цилиндрах А, следующее выражение:

Подобно этому свободную энергию газов В в цилиндрах В в конце процесса представим в виде

где  ) — молярные теплоемкость, энергия и энтропийная постоянная газа
) — молярные теплоемкость, энергия и энтропийная постоянная газа 
Разность между этими двумя выражениями должна быть равна работе  приведенной в (137). Следовательно, имеем
приведенной в (137). Следовательно, имеем

Разделив на  и потенцируя, приводим уравнение (138) к следующему виду:
и потенцируя, приводим уравнение (138) к следующему виду:

Правая часть уравнения (139) является функцией только температуры. Таким образом, это уравнение не только доказывает закон действующих масс (136), но и показывает вид функции 
Мы обсудим уравнение (139) в § 24; в следующем параграфе дадим еще одно доказательство той же формулы.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ВВЕДЕНИЕ
- ГЛАВА I. ТЕРМОДИНАМИЧЕСКИЕ СИСТЕМЫ
- 2. ИДЕАЛЬНЫЕ ГАЗЫ
- ГЛАВА II. ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 3. ФОРМУЛИРОВКА ПЕРВОГО ЗАКОНА ТЕРМОДИНАМИКИ
- 4. ПРИМЕНЕНИЕ ПЕРВОГО ЗАКОНА К СИСТЕМАМ, СОСТОЯНИЕ КОТОРЫХ МОЖЕТ БЫТЬ ИЗОБРАЖЕНО НА ДИАГРАММЕ (V, p)
- 5. ПРИМЕНЕНИЕ ПЕРВОГО ЗАКОНА К ГАЗАМ
- 6. АДИАБАТИЧЕСКИЕ ПРОЦЕССЫ В ГАЗАХ
- ГЛАВА III. ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ
- 7. ФОРМУЛИРОВКА ВТОРОГО ЗАКОНА ТЕРМОДИНАМИКИ
- 8. ЦИКЛ КАРНО
- 9. АБСОЛЮТНАЯ ТЕРМОДИНАМИЧЕСКАЯ ТЕМПЕРАТУРА
- 10. ТЕПЛОВЫЕ МАШИНЫ
- ГЛАВА IV. ЭНТРОПИЯ
- 11. НЕКОТОРЫЕ СВОЙСТВА ЦИКЛОВ
- 12. ЭНТРОПИЯ
- 18. НЕКОТОРЫЕ ДАЛЬНЕЙШИЕ СВОЙСТВА ЭНТРОПИИ
- 14. ЭНТРОПИЯ СИСТЕМЫ, СОСТОЯНИЕ КОТОРОЙ МОЖЕТ БЫТЬ ИЗОБРАЖЕНО НА ДИАГРАММЕ (V, p)
- 15. УРАВНЕНИЕ КЛАПЕЙРОНА
- 16. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- ГЛАВА V. ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ
- 18. ТЕРМОДИНАМИЧЕСКИЙ ПОТЕНЦИАЛ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- 19. ПРАВИЛО ФАЗ
- 20. ТЕРМОДИНАМИКА ОБРАТИМОГО ГАЛЬВАНИЧЕСКОГО ЭЛЕМЕНТА
- ГЛАВА VI. РЕАКЦИИ В ГАЗОВОЙ ФАЗЕ
- 21. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В ГАЗАХ
- 22. ЯЩИК ВАНТ-ГОФФА
- 23. ДРУГОЕ ДОКАЗАТЕЛЬСТВО УРАВНЕНИЯ ГАЗОВОГО РАВНОВЕСИЯ
- 24. ОБСУЖДЕНИЕ УРАВНЕНИЯ ГАЗОВОГО РАВНОВЕСИЯ. ПРИНЦИП ЛЕ ШАТЕЛЬЕ
- ГЛАВА VII. ТЕРМОДИНАМИКА СЛАБЫХ РАСТВОРОВ
- 28. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ
- 27. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- 28. РАСПРЕДЕЛЕНИЕ РАСТВОРЕННОГО ВЕЩЕСТВА МЕЖДУ ДВУМЯ ФАЗАМИ
- 29. ДАВЛЕНИЕ ПАРА, ТОЧКА КИПЕНИЯ И ТОЧКА ЗАМЕРЗАНИЯ РАСТВОРА
- ГЛАВА VIII. ПОСТОЯННАЯ В ЗАВИСИМОСТИ ЭНТРОПИИ ОТ ТЕМПЕРАТУРЫ
- 30. ТЕОРЕМА НЕРНСТА
- 31. ПРИМЕНЕНИЕ ТЕОРЕМЫ НЕРНСТА К ТВЕРДЫМ ТЕЛАМ
- 32. ЭНТРОПИЙНАЯ КОНСТАНТА ГАЗОВ
- 33. ТЕРМИЧЕСКАЯ ИОНИЗАЦИЯ ГАЗА. ТЕРМОИОННЫЙ ЭФФЕКТ