| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
31. ПРИМЕНЕНИЕ ТЕОРЕМЫ НЕРНСТА К ТВЕРДЫМ ТЕЛАМ
Рассмотрим твердое тело, которое нагревается (например, при постоянном давлении) до тех пор, пока его температура не возрастет от абсолютного нуля до некоторой определенной величины  Пусть
Пусть  теплоемкость тела (при постоянном давлении) при температуре
теплоемкость тела (при постоянном давлении) при температуре  Тогда при изменении температуры на величину
Тогда при изменении температуры на величину  тело поглощает количество теплоты
тело поглощает количество теплоты  Поэтому энтропия тела при температуре
Поэтому энтропия тела при температуре  может быть представлена (см. уравнение (192)) в следующем виде:
может быть представлена (см. уравнение (192)) в следующем виде:


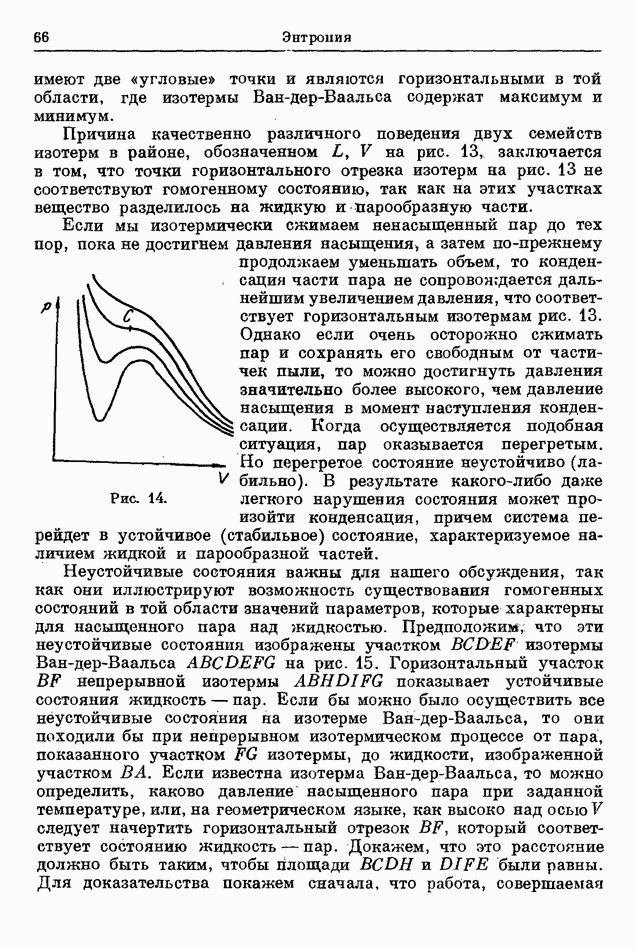
Рис. 22.
Из уравнения (193) можно получить первое следствие теоремы Нернста: видно, что если бы теплоемкость при абсолютном нуле  отличалась от нуля, то интеграл (193) расходился бы на нижнем пределе. Поэтому должно быть
отличалась от нуля, то интеграл (193) расходился бы на нижнем пределе. Поэтому должно быть

Этот результат находится в согласии с опытными данными для теплоемкости твердых тел.
Для простоты ограничимся рассмотрением твердых химических элементов и выполним вычисления для одного грамм-атома. Рисунок 22 является качественным графическим изображением изменения атомной теплоемкости от температуры согласно эксперименту. Из рисунка видно, что атомная теплоемкость действительно обращается в нуль в абсолютном нуле. При более высоких температурах  приближается к предельной величине, которая мало отличается для различных элементов и лежит очень близко к величине
приближается к предельной величине, которая мало отличается для различных элементов и лежит очень близко к величине  Предельное значение достигается при комнатной температуре. Этот результат является выражением хорошо известного закона Дюлонга и Пти, который может быть сформулирован следующим образом: все твердые элементы при комнатной температуре имеют одинаковую атомную теплоемкость, которая равна
Предельное значение достигается при комнатной температуре. Этот результат является выражением хорошо известного закона Дюлонга и Пти, который может быть сформулирован следующим образом: все твердые элементы при комнатной температуре имеют одинаковую атомную теплоемкость, которая равна  Другими словами, произведение удельной теплоемкости и атомного веса одинаково для всех твердых элементов и равно
Другими словами, произведение удельной теплоемкости и атомного веса одинаково для всех твердых элементов и равно 
Теоретическая формула для удельной теплоемкости твердых элементов, которая хорошо согласуется с опытом, была выведена
Дебаем на основе квантовой теории. Выражение Дебая можно записать в виде

где  характеристическая константа вещества, которая имеет размерность температуры; она называется температурой Дебая;
характеристическая константа вещества, которая имеет размерность температуры; она называется температурой Дебая;  представляет собой следующую функцию:
представляет собой следующую функцию:

Поскольку для больших значений  функция
функция  стремится к единице, то из (195) следует, что атомная теплоемкость при ятлеоких температурах стремится к пределу, равному
стремится к единице, то из (195) следует, что атомная теплоемкость при ятлеоких температурах стремится к пределу, равному  как и требуется по закону Дюлонга и Пти.
как и требуется по закону Дюлонга и Пти.
При малых значениях  верхний предел интеграла (196) можно заменить бесконечностью и опустить второе слагаемое выражения, потому что оно очень быстро стремится к нулю при
верхний предел интеграла (196) можно заменить бесконечностью и опустить второе слагаемое выражения, потому что оно очень быстро стремится к нулю при  Поэтому для
Поэтому для  запишем
запишем

Из этого асимптотического выражения для  получим следующее выражение для атомной теплоемкости в области низких температур:
получим следующее выражение для атомной теплоемкости в области низких температур:

из которого видно, что при низких температурах атомная теплоемкость пропорциональна кубу температуры. Этот вывод из теории Дебая хорошо согласуется с опытом.
Используя формулу Дебая, можно вычислить энтропию грамм-атома твердого тела, подставляя (195) в (193). Проделав это, находим

Заменяя  в (199) его точным выражением, получим
в (199) его точным выражением, получим

Последняя формула справедлива для  т. е. в области температур, для которых применим закон Дюлонга и Пти.
т. е. в области температур, для которых применим закон Дюлонга и Пти.
При помощи теоремы Нернста обсудим теперь превращение твердого тела из одной кристаллической формы в другую. В качестве примера рассмотрим превращение олова из серого в белое. Серое олово является устойчивой формой при низких температурах, а белое устойчиво при высоких температурах. Температура перехода  равна
равна  или
или 
Превращение олова из одной аллотропической модификации в другую во многих отношениях аналогично плавлению твердого тела. Например, оловом поглощается некоторое количество теплоты при переходе от серой к белой модификации. Эта теплота превращения  равна 535 калориям на грамм-атом при температуре перехода.
равна 535 калориям на грамм-атом при температуре перехода.
Устойчивой модификацией ниже температуры перехода является серое олово. При низких температурах может, однако,
существовать и белое олово — в неустойчивом метастабильном состоянии. Поэтому можно измерить удельную теплоемкость как серого, так и белого олова от низких температур вплоть до температуры перехода. Атомные теплоемкости этих двух модификаций не равны: при одной и той же температуре атомная теплоемкость серого олова меньше, чем белого.
Превращение олова из серого в белое является необратимым при температурах ниже температуры перехода (так как серое олово устойчиво ниже температуры перехода, то самопроизвольный переход может произойти только от белой к серой модификации). Однако при температуре перехода превращение между двумя модификациями обратимо.
Пусть и  энтропии при температурах перехода одного грамм-атома соответственно серого и белого олова. Применяя соотношение (69) к обратимому изотермическому превращению серого олова в белое, получаем:
энтропии при температурах перехода одного грамм-атома соответственно серого и белого олова. Применяя соотношение (69) к обратимому изотермическому превращению серого олова в белое, получаем:
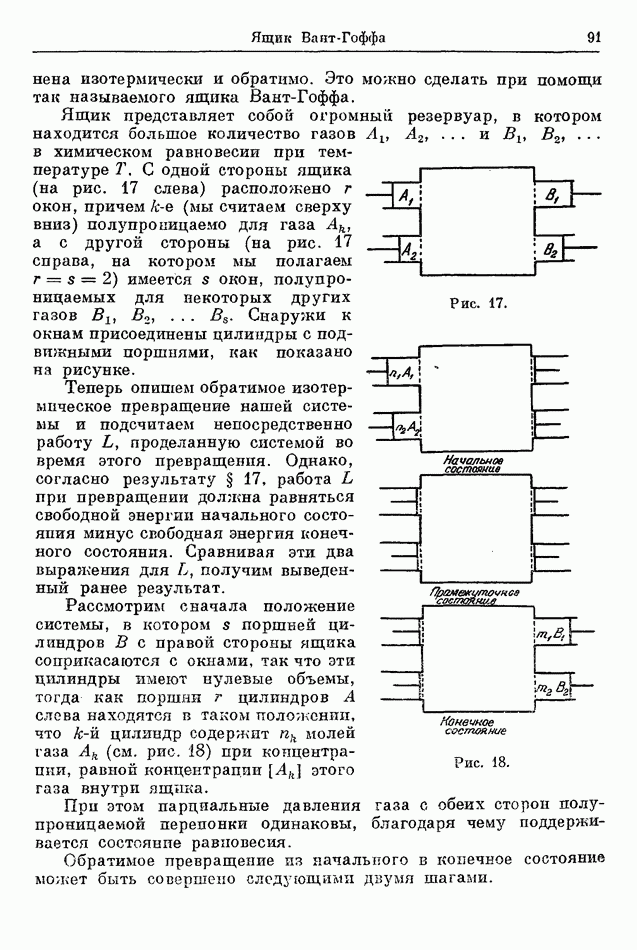
Оелое

серое
Обозначив атомную теплоемкость серого и белого олова соответственно через  можно выразить
можно выразить  при помощи уравнения (193) следующим образом:
при помощи уравнения (193) следующим образом:

Таким образом, из (201) находим уравнение

которое выражает теплоту превращения  процесса через температуру перехода
процесса через температуру перехода  и атомную теплоемкость двух форм олова. Чтобы проверить справедливость уравнения (203), выполним интегрирование. В результате численного интегрирования получим
и атомную теплоемкость двух форм олова. Чтобы проверить справедливость уравнения (203), выполним интегрирование. В результате численного интегрирования получим

Так как  то из (203) мы получаем
то из (203) мы получаем

Хорошее согласие между этой величиной и экспериментальной величиной  кал можно рассматривать как серьезное подтверждение теоремы Нернста. Небольшую разницу между этими величинами можно объяснить ошибками опыта.
кал можно рассматривать как серьезное подтверждение теоремы Нернста. Небольшую разницу между этими величинами можно объяснить ошибками опыта.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ВВЕДЕНИЕ
- ГЛАВА I. ТЕРМОДИНАМИЧЕСКИЕ СИСТЕМЫ
- 2. ИДЕАЛЬНЫЕ ГАЗЫ
- ГЛАВА II. ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 3. ФОРМУЛИРОВКА ПЕРВОГО ЗАКОНА ТЕРМОДИНАМИКИ
- 4. ПРИМЕНЕНИЕ ПЕРВОГО ЗАКОНА К СИСТЕМАМ, СОСТОЯНИЕ КОТОРЫХ МОЖЕТ БЫТЬ ИЗОБРАЖЕНО НА ДИАГРАММЕ (V, p)
- 5. ПРИМЕНЕНИЕ ПЕРВОГО ЗАКОНА К ГАЗАМ
- 6. АДИАБАТИЧЕСКИЕ ПРОЦЕССЫ В ГАЗАХ
- ГЛАВА III. ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ
- 7. ФОРМУЛИРОВКА ВТОРОГО ЗАКОНА ТЕРМОДИНАМИКИ
- 8. ЦИКЛ КАРНО
- 9. АБСОЛЮТНАЯ ТЕРМОДИНАМИЧЕСКАЯ ТЕМПЕРАТУРА
- 10. ТЕПЛОВЫЕ МАШИНЫ
- ГЛАВА IV. ЭНТРОПИЯ
- 11. НЕКОТОРЫЕ СВОЙСТВА ЦИКЛОВ
- 12. ЭНТРОПИЯ
- 18. НЕКОТОРЫЕ ДАЛЬНЕЙШИЕ СВОЙСТВА ЭНТРОПИИ
- 14. ЭНТРОПИЯ СИСТЕМЫ, СОСТОЯНИЕ КОТОРОЙ МОЖЕТ БЫТЬ ИЗОБРАЖЕНО НА ДИАГРАММЕ (V, p)
- 15. УРАВНЕНИЕ КЛАПЕЙРОНА
- 16. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- ГЛАВА V. ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ
- 18. ТЕРМОДИНАМИЧЕСКИЙ ПОТЕНЦИАЛ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- 19. ПРАВИЛО ФАЗ
- 20. ТЕРМОДИНАМИКА ОБРАТИМОГО ГАЛЬВАНИЧЕСКОГО ЭЛЕМЕНТА
- ГЛАВА VI. РЕАКЦИИ В ГАЗОВОЙ ФАЗЕ
- 21. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В ГАЗАХ
- 22. ЯЩИК ВАНТ-ГОФФА
- 23. ДРУГОЕ ДОКАЗАТЕЛЬСТВО УРАВНЕНИЯ ГАЗОВОГО РАВНОВЕСИЯ
- 24. ОБСУЖДЕНИЕ УРАВНЕНИЯ ГАЗОВОГО РАВНОВЕСИЯ. ПРИНЦИП ЛЕ ШАТЕЛЬЕ
- ГЛАВА VII. ТЕРМОДИНАМИКА СЛАБЫХ РАСТВОРОВ
- 28. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ
- 27. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- 28. РАСПРЕДЕЛЕНИЕ РАСТВОРЕННОГО ВЕЩЕСТВА МЕЖДУ ДВУМЯ ФАЗАМИ
- 29. ДАВЛЕНИЕ ПАРА, ТОЧКА КИПЕНИЯ И ТОЧКА ЗАМЕРЗАНИЯ РАСТВОРА
- ГЛАВА VIII. ПОСТОЯННАЯ В ЗАВИСИМОСТИ ЭНТРОПИИ ОТ ТЕМПЕРАТУРЫ
- 30. ТЕОРЕМА НЕРНСТА
- 31. ПРИМЕНЕНИЕ ТЕОРЕМЫ НЕРНСТА К ТВЕРДЫМ ТЕЛАМ
- 32. ЭНТРОПИЙНАЯ КОНСТАНТА ГАЗОВ
- 33. ТЕРМИЧЕСКАЯ ИОНИЗАЦИЯ ГАЗА. ТЕРМОИОННЫЙ ЭФФЕКТ