| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
29. ДАВЛЕНИЕ ПАРА, ТОЧКА КИПЕНИЯ И ТОЧКА ЗАМЕРЗАНИЯ РАСТВОРА
Давление пара, точка кипения и точка замерзания раствора не такие, как для чистого растворителя. Этот факт очень важен с практической точки зрения, потому что, как будет показано ниже, изменения в точках кипения и замерзания, по крайней мере для разбавленных растворов, пропорциональны молярным концентрациям растворенных веществ. Измерение зтих изменений дает очень удобный метод определения молярной концентрации раствора.
Предположим, что раствор не летучий. В таком случае пар над раствором будет содержать только чистый испарившийся растворитель. Допустим далее, что когда раствор замерзает, то твердеет чистый растворитель, а все растворенные вещества остаются в растворе.
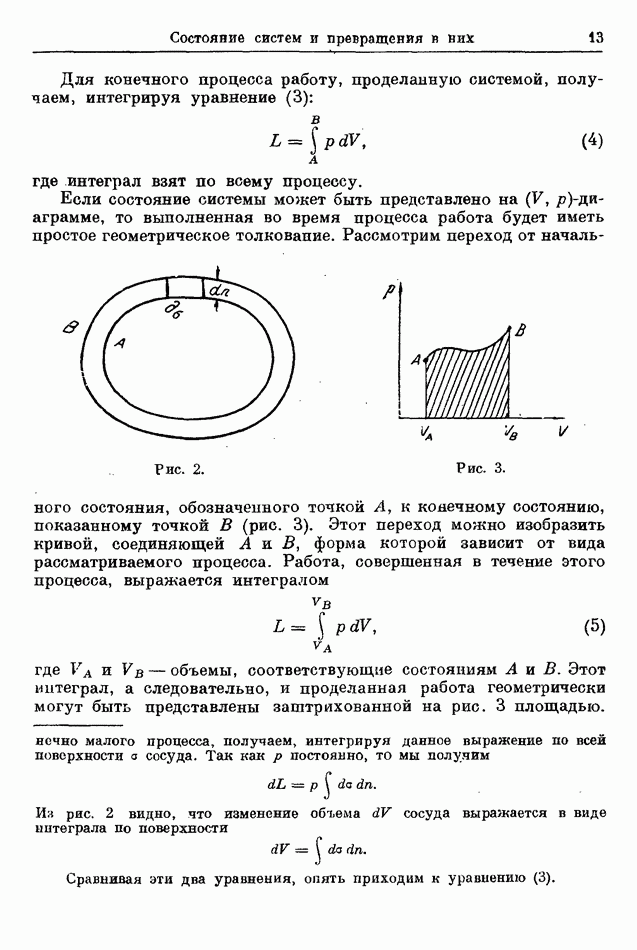
Теперь можно легко показать, что давление пара над раствором при данной температуре ниже, чем над чистым растворителем при той же температуре. Рассмотрим аппарат, показанный на рис. 21. Он состоит из трубки прямоугольной формы, в которой чистый растворитель и раствор отделены один от другого в нижней части (у точки В) полупроницаемой перепонкой. Вследствие
осмотического давления уровни  соответственно чистого растворителя и раствора не будут находиться на одной высоте. Уровень С раствора будет выше. Так как растворенное вещество неулетучивающееся, то область в трубке над
соответственно чистого растворителя и раствора не будут находиться на одной высоте. Уровень С раствора будет выше. Так как растворенное вещество неулетучивающееся, то область в трубке над  будет заполнена парами только чистого растворителя.
будет заполнена парами только чистого растворителя.
Подождем, пока установится равновесие. Давление пара в непосредственной близости мениска А будет равно давлению насыщенного пара в равновесии со своей жидкой фазой, а давление пара у С будет таковым для насыщенного пара в равновесии с раствором. Очевидно, что давления  С не равны, так как
С не равны, так как  находятся на различных уровнях.
находятся на различных уровнях.

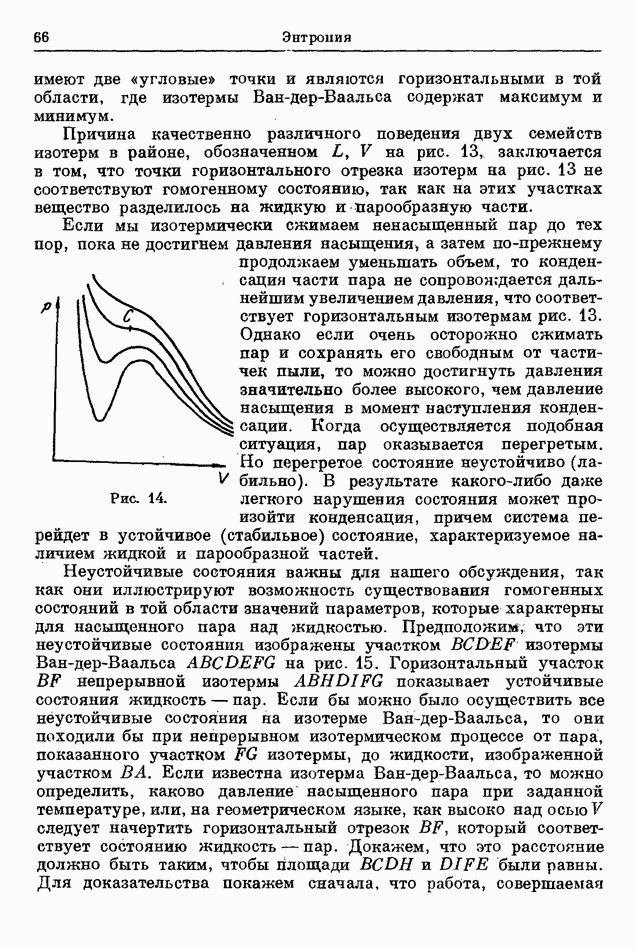
Рис. 21.
Поскольку С лежит выше, чем А, то давление пара у точки С ниже, чем у точки А, т. е. давление пара над раствором ниже, чем давление пара над чистым растворителем.
Чтобы количественно определить эту разность давлений  отметим, что она равна давлению, оказываемому столбом пара высотой
отметим, что она равна давлению, оказываемому столбом пара высотой  Если
Если  плотность пара,
плотность пара,  ускорение силы тяжести, то
ускорение силы тяжести, то

С другой стороны, давление, оказываемое жидким столбом  равно осмотическому давлению
равно осмотическому давлению  раствора. Если
раствора. Если  плотность чистого растворителя, то для осмотического давления, пренебрегая разницей между плотностью раствора и плотностью чистого растворителя, а также плотностью пара, по сравнению с плотностью жидкости, получим
плотность чистого растворителя, то для осмотического давления, пренебрегая разницей между плотностью раствора и плотностью чистого растворителя, а также плотностью пара, по сравнению с плотностью жидкости, получим

Разделив первое уравнение на второе, запишем

или

где и  объемы, занятые одним молем чистого растворителя соответственно в жидкой и газообразной фазах
объемы, занятые одним молем чистого растворителя соответственно в жидкой и газообразной фазах  обратно пропорциональны
обратно пропорциональны  Подставляя в последнее выражение осмотическое давление
Подставляя в последнее выражение осмотическое давление  согласно формуле (165), и полагая для простоты, что в растворе находится только одно растворенное вещество, получим
согласно формуле (165), и полагая для простоты, что в растворе находится только одно растворенное вещество, получим

что представляет разность между давлением пара раствора и давлением пара чистого растворителя.
Тот факт, что давление пара для раствора ниже, чем для чистого растворителя, непосредственно связан с тем, что точка кипения раствора выше, чем чистого растворителя, так как точка кипения является температурой, при которой давление пара равно одной атмосфере. Рассмотрим чистый растворитель в точке кипения; давление его пара равно одной атмосфере. Если растворить некоторое количество вещества в этом растворителе, поддерживая температуру постоянной, то давление пара упадет ниже одной атмосферы. Следовательно, чтобы вернуть давление вновь к его первоначальной величине в одну атмосферу, мы должны повысить температуру раствора. При помощи уравнения  уравнения Клапейрона легко можно вывести выражение для изменения температуры кипения раствора. Вместо этого подсчитаем прямым методом и уменьшение давления пара, и повышение температуры кипения.
уравнения Клапейрона легко можно вывести выражение для изменения температуры кипения раствора. Вместо этого подсчитаем прямым методом и уменьшение давления пара, и повышение температуры кипения.
Рассмотрим слабый раствор, состоящий из  молей растворителя и
молей растворителя и  молей растворенного вещества в равновесии с паром чистого растворителя.
молей растворенного вещества в равновесии с паром чистого растворителя.
Пусть  число молей растворителя, содержащееся в парообразной фазе. Из (148), (149), (155) и (121) для термодинамического потенциала Фраств получаем
число молей растворителя, содержащееся в парообразной фазе. Из (148), (149), (155) и (121) для термодинамического потенциала Фраств получаем

где

Пусть  термодинамический потенциал одного моля пара растворителя. Тогда термодинамический потенциал
термодинамический потенциал одного моля пара растворителя. Тогда термодинамический потенциал  молей парообразной фазы составляет
молей парообразной фазы составляет

а термодинамический потенциал всей системы

Условием равновесия является минимум  при постоянной температуре и постоянном давлении. Поэтому для бесконечно малого изотермического и изобарического процесса должно быть
при постоянной температуре и постоянном давлении. Поэтому для бесконечно малого изотермического и изобарического процесса должно быть  Если
Если  молей растворителя в результате такого превращения перешло из газообразной фазы в раствор, т. е. если
молей растворителя в результате такого превращения перешло из газообразной фазы в раствор, т. е. если  изменяются соответственно на
изменяются соответственно на  то
то

или

Заменяя производные в этом уравнении их выражениями, вычисленными из (183), получаем

или

Уравнение (184) выражает соотношение между температурой и давлением пара над раствором.
Пусть  давление насыщенного пара чистого растворителя при температуре
давление насыщенного пара чистого растворителя при температуре  Величины
Величины  будут удовлетворять уравнению (184), если положить
будут удовлетворять уравнению (184), если положить  потому что в этом случае растворенное вещество отсутствует. Таким образом,
потому что в этом случае растворенное вещество отсутствует. Таким образом,

Когда в растворителе находится молей растворенного вещества, то давление  пара равно
пара равно

где  малая величина. Разлагая левую часть (184) по степеням
малая величина. Разлагая левую часть (184) по степеням  и используя члены первого порядка, находим:
и используя члены первого порядка, находим:

Так как  является термодинамическим потенциалом одного моля нашего растворителя, то из (123) имеем
является термодинамическим потенциалом одного моля нашего растворителя, то из (123) имеем

где  объем одного моля растворителя, и подобно этому
объем одного моля растворителя, и подобно этому

где  объем одного моля пара чистого растворителя. Подставляя последнее выражение в (186), имеем
объем одного моля пара чистого растворителя. Подставляя последнее выражение в (186), имеем

Так как объем  одного моля пара больше, чем объем
одного моля пара больше, чем объем  одного моля жидкого растворителя, то
одного моля жидкого растворителя, то  отрицательно.
отрицательно.
Следовательно, давление пара над раствором ниже, чем давление над чистым растворителем. Если величиной  можно пренебречь по сравнению с
можно пренебречь по сравнению с  как мы предполагали при выводе уравнения (182), то можно считать, что уравнение (187) совпадает с уравнением (182) (знак минус означает, что давление пара над раствором меньше, чем давление пара над чистым растворителем).
как мы предполагали при выводе уравнения (182), то можно считать, что уравнение (187) совпадает с уравнением (182) (знак минус означает, что давление пара над раствором меньше, чем давление пара над чистым растворителем).
Таким образом, из уравнения (184) мы вывели выражение для уменьшения давления пара. При помощи этого же уравнения и методом, аналогичным только что использованному, можно вычислить также изменение температуры кипения раствора.
Рассмотрим раствор, температура которого такова, что давление  его пара равно одной атмосфере. Пусть
его пара равно одной атмосфере. Пусть  точка кипения чистого растворителя, а
точка кипения чистого растворителя, а  точка кипения раствора. Так как давление пара при кипении равно атмосферному давлению
точка кипения раствора. Так как давление пара при кипении равно атмосферному давлению  то давление пара чистого растворителя при температуре
то давление пара чистого растворителя при температуре  равно
равно  Поскольку для чистого растворителя
Поскольку для чистого растворителя  то при помощи уравнения (184) находим, что
то при помощи уравнения (184) находим, что

Применяя уравнение (184) к раствору, получаем

Разлагая левую часть предыдущего уравнения по степеням  и опуская все члены выше первой степени, запишем, используя 188), следующее
и опуская все члены выше первой степени, запишем, используя 188), следующее  авнение:
авнение:

Из (124) имеем

где  энтропия одного моля растворителя соответственно в жидкой
энтропия одного моля растворителя соответственно в жидкой  в парообразной фазах.
в парообразной фазах.
Из двух предыдущих уравнений находим

Пусть  теплота испарения одного моля растворителя. Если дать возможность одному молю растворителя испариться в точке кипения
теплота испарения одного моля растворителя. Если дать возможность одному молю растворителя испариться в точке кипения  то количество поглощенной теплоты составит А, а
то количество поглощенной теплоты составит А, а  представит изменение энтропии. Следовательно,
представит изменение энтропии. Следовательно,

Подставляя это выражение в уравнение (189), получаем

Полученное выражение — формула для разности между температурой кипения раствора и температурой кипения чистого растворителя. Поскольку  то точка кипения раствора выше, чем точка кипения чистого растворителя. Из уравнения (190) видно также, что изменение точки кипения пропорционально молярной концентрации раствора.
то точка кипения раствора выше, чем точка кипения чистого растворителя. Из уравнения (190) видно также, что изменение точки кипения пропорционально молярной концентрации раствора.
В качестве примера применим полученное уравнение к нормальному раствору некоторого вещества в воде. Для такого раствора имеем:

(Можно выражать и  и
и  в калориях, потому что их отношение, очевидно, безразмерно).
в калориях, потому что их отношение, очевидно, безразмерно).
Подставляя эти величины в (190), находим, что

Ту же формулу  можно также использовать для того, чтобы определить изменение точки замерзания раствора. Разница заключается лишь в том, что вместо парообразной фазы мы имеем здесь твердую фазу. Величина
можно также использовать для того, чтобы определить изменение точки замерзания раствора. Разница заключается лишь в том, что вместо парообразной фазы мы имеем здесь твердую фазу. Величина  в данном случае представляет теплоту, поглощенную одним молем растворителя при изотермическом переходе через точку замерзания из жидкого состояния в твердое. Эта теплота отрицательна и равна —А, где
в данном случае представляет теплоту, поглощенную одним молем растворителя при изотермическом переходе через точку замерзания из жидкого состояния в твердое. Эта теплота отрицательна и равна —А, где  теплота плавления одного моля растворителя. В случае замерзания уравнение
теплота плавления одного моля растворителя. В случае замерзания уравнение  удобно записать так:
удобно записать так:

Из этого уравнения видно, что точка замерзания для раствора ниже, чем для чистого растворителя, причем понижение пропорционально молярной концентрации раствора.
В случае нормального раствора в воде, для которой

Находим, что

Следовало бы отметить, что во всех этих формулах  представляет действительное число молей вещества, содержащегося в растворе. Однако для электролитических растворов каждый ион может рассматриваться как независимая молекула. Таким образом, для очень сильных электролитов (имеющих высокую степень диссоциации) значение
представляет действительное число молей вещества, содержащегося в растворе. Однако для электролитических растворов каждый ион может рассматриваться как независимая молекула. Таким образом, для очень сильных электролитов (имеющих высокую степень диссоциации) значение  находим, умножая число молей растворенного вещества на число ионов, на которое распадается находящаяся в растворе одна молекула растворенного вещества.
находим, умножая число молей растворенного вещества на число ионов, на которое распадается находящаяся в растворе одна молекула растворенного вещества.
Задачи
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ВВЕДЕНИЕ
- ГЛАВА I. ТЕРМОДИНАМИЧЕСКИЕ СИСТЕМЫ
- 2. ИДЕАЛЬНЫЕ ГАЗЫ
- ГЛАВА II. ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 3. ФОРМУЛИРОВКА ПЕРВОГО ЗАКОНА ТЕРМОДИНАМИКИ
- 4. ПРИМЕНЕНИЕ ПЕРВОГО ЗАКОНА К СИСТЕМАМ, СОСТОЯНИЕ КОТОРЫХ МОЖЕТ БЫТЬ ИЗОБРАЖЕНО НА ДИАГРАММЕ (V, p)
- 5. ПРИМЕНЕНИЕ ПЕРВОГО ЗАКОНА К ГАЗАМ
- 6. АДИАБАТИЧЕСКИЕ ПРОЦЕССЫ В ГАЗАХ
- ГЛАВА III. ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ
- 7. ФОРМУЛИРОВКА ВТОРОГО ЗАКОНА ТЕРМОДИНАМИКИ
- 8. ЦИКЛ КАРНО
- 9. АБСОЛЮТНАЯ ТЕРМОДИНАМИЧЕСКАЯ ТЕМПЕРАТУРА
- 10. ТЕПЛОВЫЕ МАШИНЫ
- ГЛАВА IV. ЭНТРОПИЯ
- 11. НЕКОТОРЫЕ СВОЙСТВА ЦИКЛОВ
- 12. ЭНТРОПИЯ
- 18. НЕКОТОРЫЕ ДАЛЬНЕЙШИЕ СВОЙСТВА ЭНТРОПИИ
- 14. ЭНТРОПИЯ СИСТЕМЫ, СОСТОЯНИЕ КОТОРОЙ МОЖЕТ БЫТЬ ИЗОБРАЖЕНО НА ДИАГРАММЕ (V, p)
- 15. УРАВНЕНИЕ КЛАПЕЙРОНА
- 16. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- ГЛАВА V. ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ
- 18. ТЕРМОДИНАМИЧЕСКИЙ ПОТЕНЦИАЛ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- 19. ПРАВИЛО ФАЗ
- 20. ТЕРМОДИНАМИКА ОБРАТИМОГО ГАЛЬВАНИЧЕСКОГО ЭЛЕМЕНТА
- ГЛАВА VI. РЕАКЦИИ В ГАЗОВОЙ ФАЗЕ
- 21. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В ГАЗАХ
- 22. ЯЩИК ВАНТ-ГОФФА
- 23. ДРУГОЕ ДОКАЗАТЕЛЬСТВО УРАВНЕНИЯ ГАЗОВОГО РАВНОВЕСИЯ
- 24. ОБСУЖДЕНИЕ УРАВНЕНИЯ ГАЗОВОГО РАВНОВЕСИЯ. ПРИНЦИП ЛЕ ШАТЕЛЬЕ
- ГЛАВА VII. ТЕРМОДИНАМИКА СЛАБЫХ РАСТВОРОВ
- 28. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ
- 27. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- 28. РАСПРЕДЕЛЕНИЕ РАСТВОРЕННОГО ВЕЩЕСТВА МЕЖДУ ДВУМЯ ФАЗАМИ
- 29. ДАВЛЕНИЕ ПАРА, ТОЧКА КИПЕНИЯ И ТОЧКА ЗАМЕРЗАНИЯ РАСТВОРА
- ГЛАВА VIII. ПОСТОЯННАЯ В ЗАВИСИМОСТИ ЭНТРОПИИ ОТ ТЕМПЕРАТУРЫ
- 30. ТЕОРЕМА НЕРНСТА
- 31. ПРИМЕНЕНИЕ ТЕОРЕМЫ НЕРНСТА К ТВЕРДЫМ ТЕЛАМ
- 32. ЭНТРОПИЙНАЯ КОНСТАНТА ГАЗОВ
- 33. ТЕРМИЧЕСКАЯ ИОНИЗАЦИЯ ГАЗА. ТЕРМОИОННЫЙ ЭФФЕКТ