| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
2.7.1.5. Изучение карбокатионов: методы и результаты
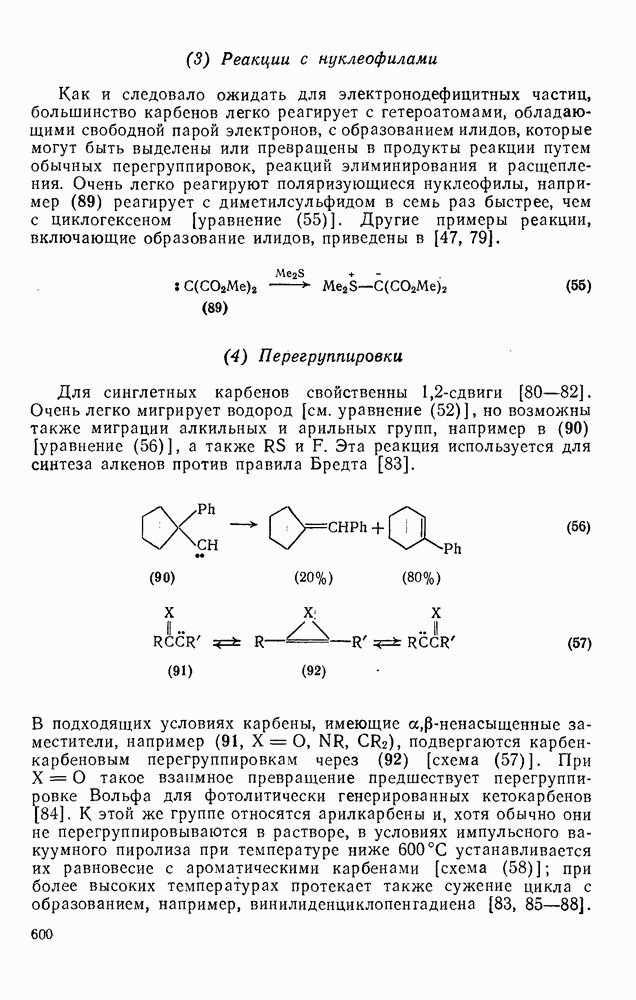
Как отмечено в разд. 2.7.1.3, карбокатионы можно генерировать как в газовой фазе, так и в растворе; известны также твердые соли карбокатионов. Для изучения карбокатионов используют различные методы; выбор метода обусловлен физическим состоянием иона, временем его жизни, природой требуемой информации (простое детектирование иона как неустойчивого интермедиата, или количественные данные о структуре и устойчивости карбокатиона).
Обычно наряду с катионами присутствуют противоионы, что часто изменяет поведение карбокатиона.
(1) Теоретические методы
Среди многочисленных квантово-химических (квантово-механических) методов, которые были использованы для расчетов карбокатионов, в данном разделе будут рассмотрены только методы молекулярных орбиталей Хюккеля (МОХ) для сопряженных систем,  initio, и возмущения МО. Эти методы применялись только для расчета карбокатионов в газовой фазе.
initio, и возмущения МО. Эти методы применялись только для расчета карбокатионов в газовой фазе.
Метод МОХ как первый простой метод сыграл, возможно, наибольшую роль в создании теоретического фундамента для качественного и полуколичественного анализа сопряженных карбениевых ионов. По этому методу  -электронную систему рассматривают отдельно от
-электронную систему рассматривают отдельно от  -остова органической молекулы и энергии
-остова органической молекулы и энергии  -орбиталей, построенных по методу
-орбиталей, построенных по методу  , оценивают, используя константу Кулона и резонансные интегралы (
, оценивают, используя константу Кулона и резонансные интегралы ( и
и  соответственно). Полное пренебрежение взаимодействием электронов и использование несамосогласованного поля в карбениевых ионах приводит к неудовлетворительным количественным результатам. Однако вводя соответствующие параметры, можно достаточно хорошо предсказать, например, положение максимумов поглощения в электронных спектрах [22]. Одним из ценных предсказаний теории МОХ является то, что сопряженные нечетные альтернантные углеводороды (карбениевые ионы, карбанионы и свободные радикалы) обладают несвязывающей молекулярной орбиталью (вакантной у карбениевых ионов), которая является линейной комбинацией
соответственно). Полное пренебрежение взаимодействием электронов и использование несамосогласованного поля в карбениевых ионах приводит к неудовлетворительным количественным результатам. Однако вводя соответствующие параметры, можно достаточно хорошо предсказать, например, положение максимумов поглощения в электронных спектрах [22]. Одним из ценных предсказаний теории МОХ является то, что сопряженные нечетные альтернантные углеводороды (карбениевые ионы, карбанионы и свободные радикалы) обладают несвязывающей молекулярной орбиталью (вакантной у карбениевых ионов), которая является линейной комбинацией  -атомных орбиталей углерода только на атомах, помеченных звездочкой. Отсюда следует, что в этом приближении ионный заряд сосредоточен именно на атомах, помеченных звездочкой, и можно очень просто предсказать его распределение. Вероятно, наибольшим успехом метода МОХ явилось предсказание (задолго до получения экспериментальных данных) особой устойчивости моноциклических карбениевых ионов ароматического типа, обладающих
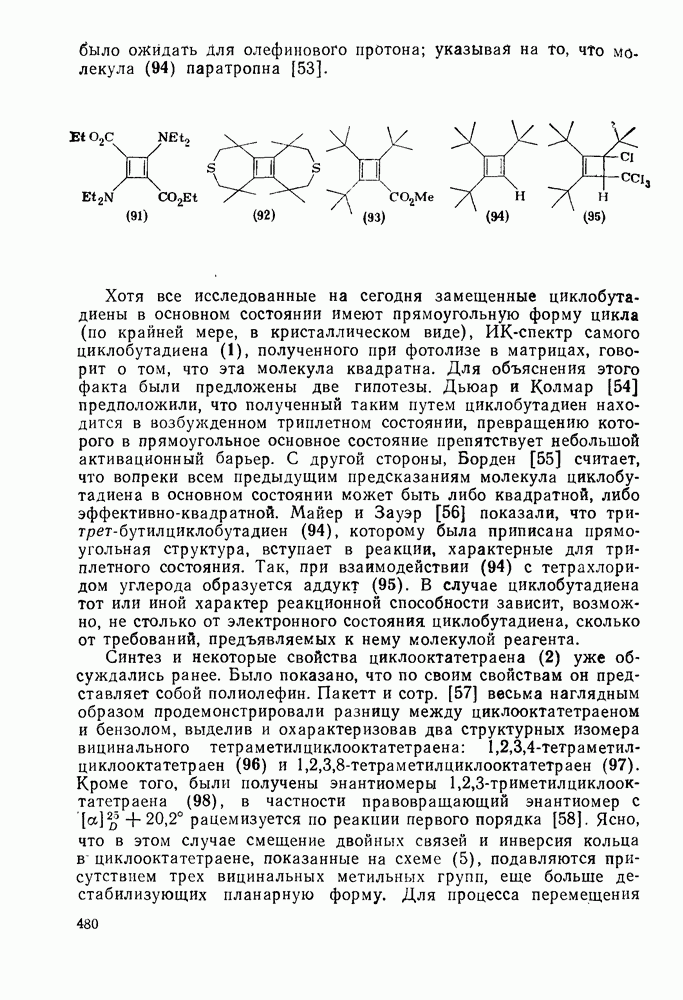
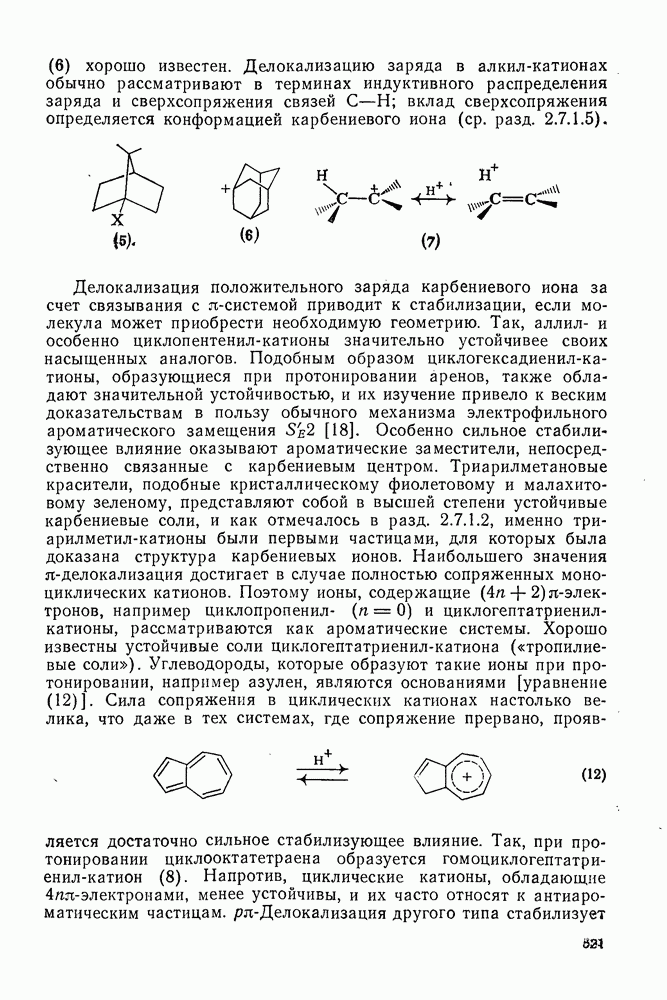
-атомных орбиталей углерода только на атомах, помеченных звездочкой. Отсюда следует, что в этом приближении ионный заряд сосредоточен именно на атомах, помеченных звездочкой, и можно очень просто предсказать его распределение. Вероятно, наибольшим успехом метода МОХ явилось предсказание (задолго до получения экспериментальных данных) особой устойчивости моноциклических карбениевых ионов ароматического типа, обладающих  -элек-ронами, в частности циклопропенил- и циклогептатриенил-катионов, циклобутадиенил-дикатиона [24], а также триплетного основного состояния циклопентадиенил-катиона [25].
-элек-ронами, в частности циклопропенил- и циклогептатриенил-катионов, циклобутадиенил-дикатиона [24], а также триплетного основного состояния циклопентадиенил-катиона [25].
Помимо метода МОХ был разработан также ряд более сложных методов, включая метод самосогласованного поля (ССП), однако для достижения количественных результатов все эти методы нуждаются в параметризации [26]. В наиболее современных работах, однако, используют метод ССП  initio, для которого не требуется экспериментальных данных [27]. Осуществляя минимизацию энергии карбокатионов в соответствии с геометрическими параметрами, удается предсказать структуру, и эти предсказания обычно хорошо согласуются с экспериментальными результатами.
initio, для которого не требуется экспериментальных данных [27]. Осуществляя минимизацию энергии карбокатионов в соответствии с геометрическими параметрами, удается предсказать структуру, и эти предсказания обычно хорошо согласуются с экспериментальными результатами.
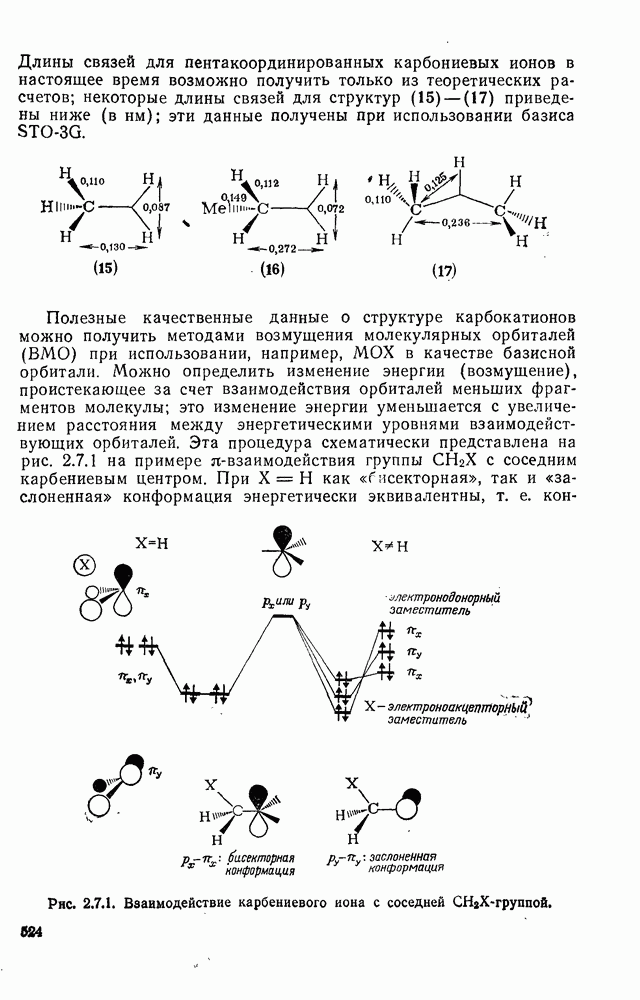
Длины связей для пентакоординированных карбониевых ионов в настоящее время возможно получить только из теоретических расчетов; некоторые длины связей для структур (15) — (17) приведены ниже (в нм); эти данные получены при использовании базиса  .
.

Полезные качественные данные о структуре карбокатионов можно получить методами возмущения молекулярных орбиталей (ВМО) при использовании, например, МОХ в качестве базисной орбитали. Можно определить изменение энергии (возмущение), проистекающее за счет взаимодействия орбиталей меньших фрагментов молекулы; это изменение энергии уменьшается с увеличением расстояния между энергетическими уровнями взаимодействующих орбиталей. Эта процедура схематически представлена на рис. 2.7.1 на примере  -взаимодействия группы
-взаимодействия группы  с соседним карбениевым центром. При
с соседним карбениевым центром. При  как «бисекторная», так и «заслоненная» конформация энергетически эквивалентны, т. е. конформационная предпочтительность отсутствует.
как «бисекторная», так и «заслоненная» конформация энергетически эквивалентны, т. е. конформационная предпочтительность отсутствует.

Рис. 2.7.1. Взаимодействие карбениевого иона с соседней  -группой.
-группой.
Однако если X — электроноакцепторный заместитель, бисекторная конформация становится менее выгодной, чем заслоненная, в случае электродонорного заместителя справедливо обратное соотношение.
(2) Газофазные методы
Масс-спектрометрические методы позволяют определить отношение массы к заряду, на основании которого можно судить о составе ионов, генерируемых, например, при использовании метода электронного удара или фотоионизации. Наряду с составом ионов можно определить энергии (потенциалы появления), которые требуются для образования ионов. Масс-спектрометрические методы не дают прямой информации о структуре ионов, однако она может быть выведена на основании последующей фрагментации ионов в масс-спектрометре [28] или при использовании двойного резонанса в случае ион-циклотрон-резонансной спектроскопии [29].
Если не учитывать избыток энергии образующихся фрагментов, то потенциал появления А карбениевого иона  , который образуется в реакции
, который образуется в реакции  , выражается уравнением
, выражается уравнением  , где
, где  ионизации радикала, а
ионизации радикала, а  — энергия диссоциации связи. Величины потенциалов ионизации
— энергия диссоциации связи. Величины потенциалов ионизации  можно определить непосредственно. Зная потенциал ионизации
можно определить непосредственно. Зная потенциал ионизации  и теплоту образования радикала
и теплоту образования радикала  , можно установить теплоту образования карбокатионов
, можно установить теплоту образования карбокатионов  . В табл. 2.7.5 приведены эти величины для некоторых карбениевых ионов.
. В табл. 2.7.5 приведены эти величины для некоторых карбениевых ионов.
Работая при больших давлениях газа, чем обычно используются в аналитической масс-спектрометрии, можно изучать разнообразные ион-молекулярные реакции. Можно, например, генерировать карбениевые ионы и пентакоординированные карбониевые ионы соответственно протонированием олефинов или насыщенных углеводородов и изучать энергетические закономерности этих процессов. Подобные основности в газовой фазе выражают обычно как —АН протонирования и называют эту величину сродством к протону; ряд этих значений приведен в табл. 2.7.6.
Таблица 2.7.5. Потенциалы ионизации радикалов  и теплоты образования соответствующих карбениевых ионов
и теплоты образования соответствующих карбениевых ионов  [29а]
[29а]

Таблица 2.7.6. Сродство к протону некоторых углеводородов [296]

(3) Твердые соли
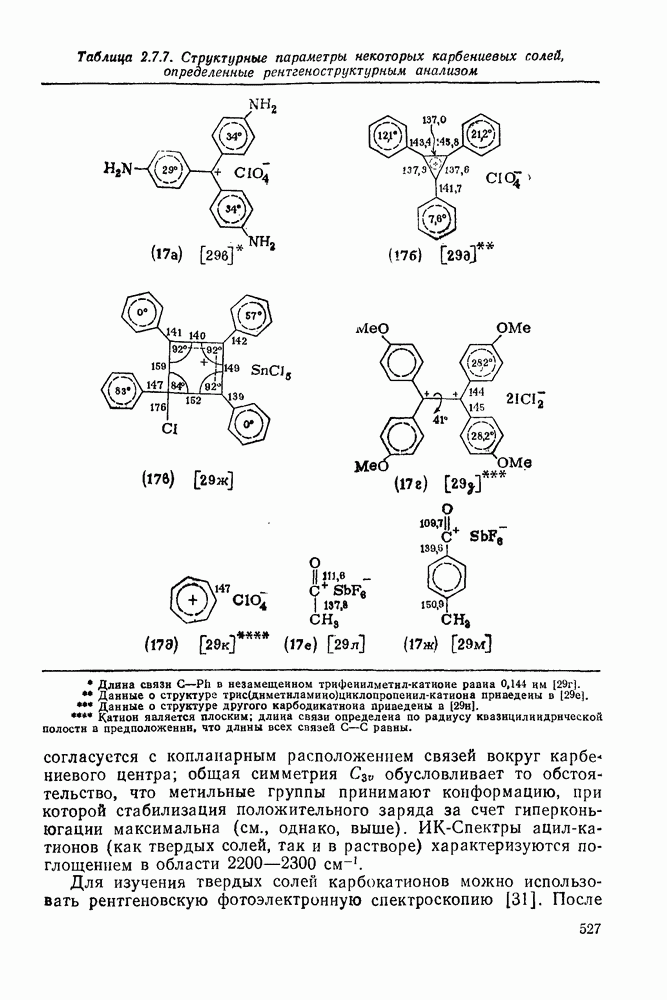
Наиболее прямые и подробные структурные данные дает метод рентгеноструктурного анализа, однако этим методом исследовано лишь относительно небольшое число карбокатионов. Некоторые из полученных данных приведены в табл. 2.7.7. В основном карбениевые ионы являются плоскими в области карбениевого центра, адил-катионы—линейными. Как и ожидалось, «ароматический» катион (17в) имеет плоское центральное кольцо. Пространственные взаимодействия между стабилизующими арильными заместителями в карбениевых ионах  ведут к повороту плоскости ароматических колец на некоторый угол относительно плоскости карбениевого центра (величины этих углов на табл. 2.7.7 вписаны в кольца). Вращение вокруг центральной связи в дикатионе (17г) приводит к тому, что каждый из полных положительных зарядов сосредоточен в области, ограниченной половиной структуры. Во всех случаях сопряжение и делокализация положительного заряда приводит к уменьшению длины связи между заместителями и карбениевым центром.
ведут к повороту плоскости ароматических колец на некоторый угол относительно плоскости карбениевого центра (величины этих углов на табл. 2.7.7 вписаны в кольца). Вращение вокруг центральной связи в дикатионе (17г) приводит к тому, что каждый из полных положительных зарядов сосредоточен в области, ограниченной половиной структуры. Во всех случаях сопряжение и делокализация положительного заряда приводит к уменьшению длины связи между заместителями и карбениевым центром.
Для изучения структуры твердых солей, а также растворов можно использовать колебательную (инфракрасную и Раман (комбинационного рассеяния) спектроскопию) [30]. Эти методы позволяют получать данные о симметрии молекул и определять силовые постоянные различных типов колебаний. Так, простота инфракрасного спектра циклогептатриенилбромида, трихлорцикло-пропенилтетрахлоралюмината и трифенилметильных солей свидетельствует, что эти соединения обладают очень симметричными структурами (соответственно  и
и  Силовые постоянные, определенные для двух «ароматических» ионов, образуют ряды, согласующиеся с рядом для бензола, и коррелируют с кристаллографическими длинами связей
Силовые постоянные, определенные для двух «ароматических» ионов, образуют ряды, согласующиеся с рядом для бензола, и коррелируют с кристаллографическими длинами связей  . Карбениевые ионы обычно характеризуются поглощением в области
. Карбениевые ионы обычно характеризуются поглощением в области  (табл. 2.7.8), достаточно интенсивным за счет больших изменений дипольного момента при возбуждении. Сравнение И К- и Раман-спектров ряда третичных алкил-катионов позволяет провести полное отнесение полос поглощения.
(табл. 2.7.8), достаточно интенсивным за счет больших изменений дипольного момента при возбуждении. Сравнение И К- и Раман-спектров ряда третичных алкил-катионов позволяет провести полное отнесение полос поглощения.
Таблица 2.7.7. Структурные параметры некоторых карбениевых солей, определенные рентгеноструктурным анализом

В частности, спектр трет-бутил-катиона аналогичен спектру изоэлектронного ему триметилбора и согласуется с копланарным расположением связей вокруг карбениевого центра; общая симметрия  обусловливает то обстоятельство, что метальные группы принимают конформацию, при которой стабилизация положительного заряда за счет гиперконьюгации максимальна (см., однако, выше). ИК-Спектры ацил-катионов (как твердых солей, так и в растворе) характеризуются поглощением в области
обусловливает то обстоятельство, что метальные группы принимают конформацию, при которой стабилизация положительного заряда за счет гиперконьюгации максимальна (см., однако, выше). ИК-Спектры ацил-катионов (как твердых солей, так и в растворе) характеризуются поглощением в области  .
.
Для изучения твердых солей карбокатионов можно использовать рентгеновскую фотоэлектронную спектроскопию [31].
Таблица 2.7.8. Предполагаемая корреляция структуры карбениевого иона и поглощения в ИК-области [30а]

Таблица 2.7.9.  -Энергия связывания углерода
-Энергия связывания углерода  для карбениевых ионов [31а]
для карбениевых ионов [31а]
Точность измерений  эВ, воспроизводимость результатов
эВ, воспроизводимость результатов  эВ.
эВ.

После определения кинетической энергии электронов  , генерируемых облучением соли рентгеновскими лучами (обычно с энергией 1485,6 эВ) при температуре жидкого азота, вычисляют
, генерируемых облучением соли рентгеновскими лучами (обычно с энергией 1485,6 эВ) при температуре жидкого азота, вычисляют  -энергию связывания
-энергию связывания  атомов углерода по уравнению:
атомов углерода по уравнению:  , где
, где  — рабочая функция спектрометра (обычно 4,6 эВ). Значение
— рабочая функция спектрометра (обычно 4,6 эВ). Значение  с возрастанием положительного заряда на углероде должно расти, что позволяет получить информацию о распределении заряда. Этот метод, однако, позволяет различать лишь большие разности в энергиях связывания, поскольку ширина линий составляет 1—2 эВ. В табл. 2.7.9 приведены некоторые из полученных результатов для карбениевых ионов и их неионных предшественников. Видно, что только в трет-бутил-катионе имеются углеродные атомы, энергии связывания которых могут быть разрешены спектрометрически; экспериментально найденная разность энергии составляет 3,4 эВ, что примерно на 1 эВ ниже предсказываемой на основании расчетов
с возрастанием положительного заряда на углероде должно расти, что позволяет получить информацию о распределении заряда. Этот метод, однако, позволяет различать лишь большие разности в энергиях связывания, поскольку ширина линий составляет 1—2 эВ. В табл. 2.7.9 приведены некоторые из полученных результатов для карбениевых ионов и их неионных предшественников. Видно, что только в трет-бутил-катионе имеются углеродные атомы, энергии связывания которых могут быть разрешены спектрометрически; экспериментально найденная разность энергии составляет 3,4 эВ, что примерно на 1 эВ ниже предсказываемой на основании расчетов  initio. Результаты, полученные для других солей, согласуются с представлением о значительной делокализации положительного заряда в этих ионах.
initio. Результаты, полученные для других солей, согласуются с представлением о значительной делокализации положительного заряда в этих ионах.
(4) Спектроскопия растворов
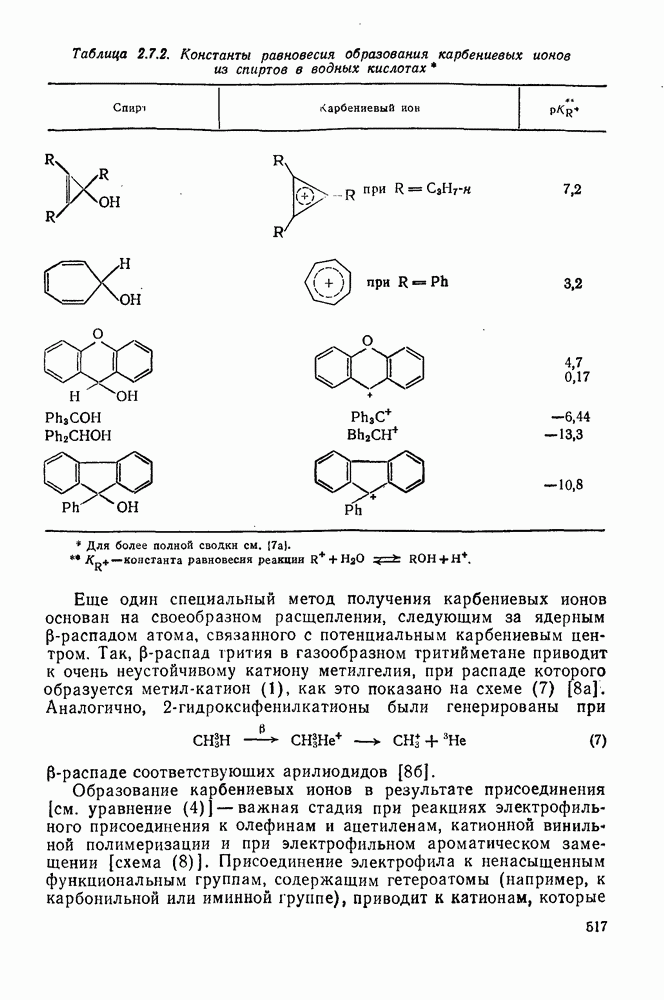
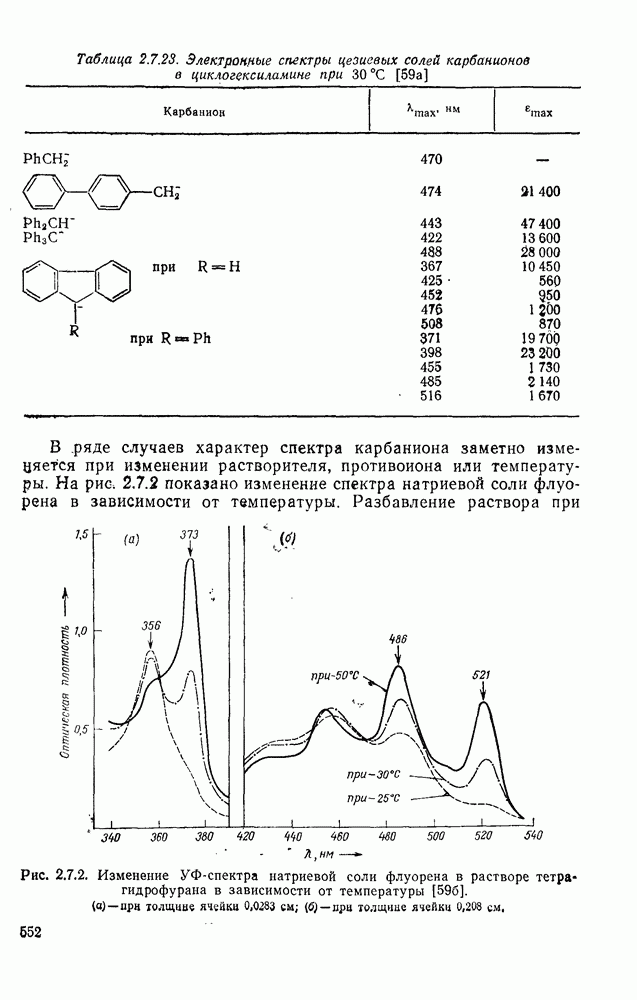
Наличие у карбениевых ионов окраски было впервые обнаружено на примере трифенилметил-катиона, и это свойство послужило основой для обнаружения карбениевых ионов. И до сих пор электронная спектроскопия продолжает оставаться ценным методом, в особенности для количественного изучения равновесия образования карбениевых ионов [22].
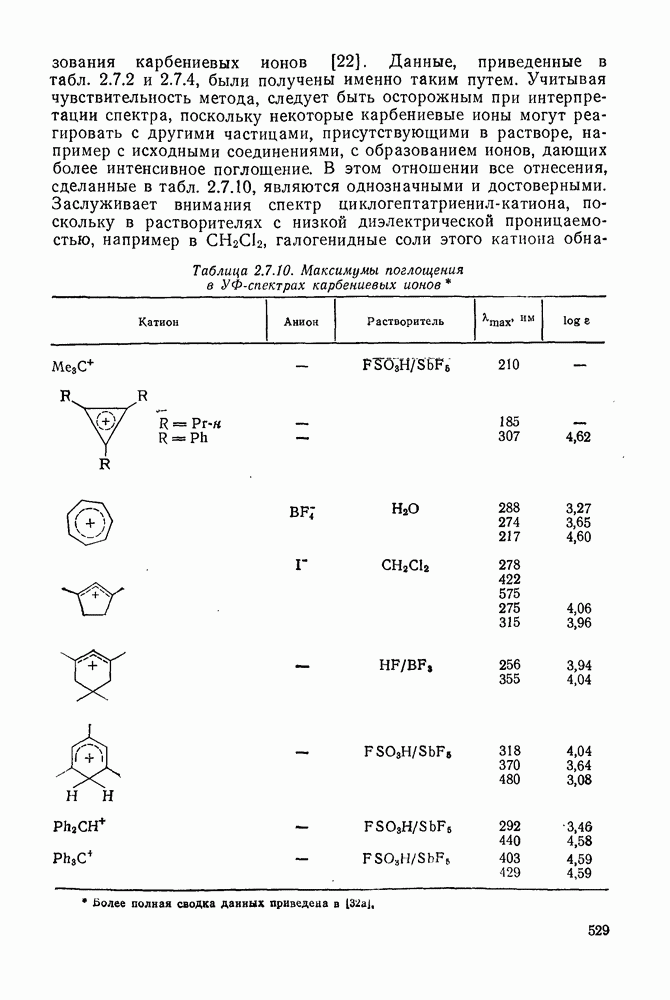
Данные, приведенные в табл. 2.7.2 и 2.7.4, были получены именно таким путем. Учитывая чувствительность метода, следует быть осторожным при интерпретации спектра, поскольку некоторые карбениевые ионы могут реагировать с другими частицами, присутствующими в растворе, например с исходными соединениями, с образованием ионов, дающих более интенсивное поглощение. В этом отношении все отнесения, сделанные в табл. 2.7.10, являются однозначными и достоверными. Заслуживает внимания спектр циклогептатриенил-катиона, поскольку в растворителях с низкой диэлектрической проницаемостью, например в  , галогенидные соли этого катиона обнаруживают поглощение, характерное для частиц с внутримолекулярным переносом заряда, длина волны которого изменяется в зависимости от способности растворителя сольватировать ионы и поэтому может быть использована как мера полярности растворителя [32].
, галогенидные соли этого катиона обнаруживают поглощение, характерное для частиц с внутримолекулярным переносом заряда, длина волны которого изменяется в зависимости от способности растворителя сольватировать ионы и поэтому может быть использована как мера полярности растворителя [32].
Таблица 2.7.10. Максимумы поглощения в УФ-спектрах карбениевых ионов 

Однако в большинстве случаев ассоциация ионов, по-видимому, не вызывает количественных изменений в спектрах карбеииевых ионов.
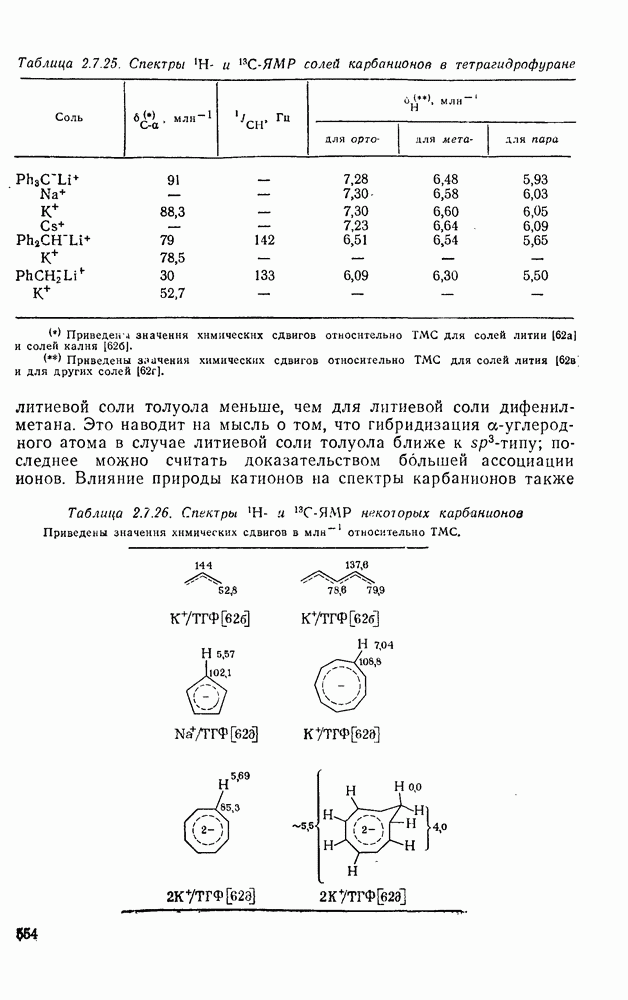
Наиболее мощным методом для исследования структур карбениевых ионов в растворах является спектроскопия ядерного магнитного резонанса (ЯМР) на ядрах  и в меньшей степени на
и в меньшей степени на  [33]. Для снятия спектра обычно приготовляют растворы карбениевого иона в суперкислой среде и при возможно более низкой температуре с тем, чтобы максимально уменьшить возможность протекания каких-либо реакций с образующимся ионом, особенно его перегруппировок.
[33]. Для снятия спектра обычно приготовляют растворы карбениевого иона в суперкислой среде и при возможно более низкой температуре с тем, чтобы максимально уменьшить возможность протекания каких-либо реакций с образующимся ионом, особенно его перегруппировок.
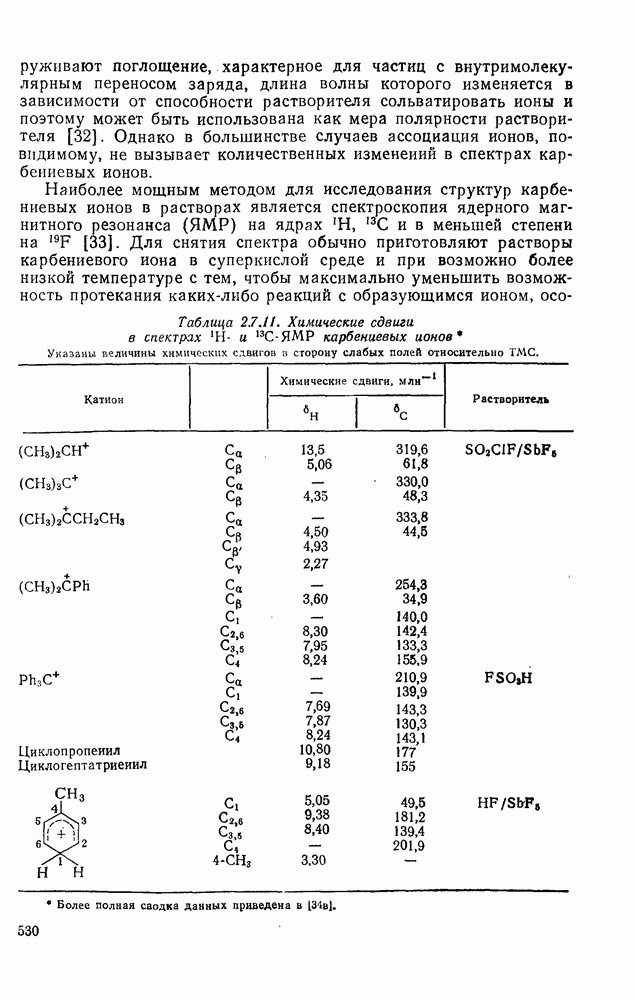
Таблица 27.11. Химические сдвиги в спектрах  и
и  -ЯМР карбениевых ионов
-ЯМР карбениевых ионов
Указаны величины химических сдвигов в сторону слабых полей относительно ТМС.

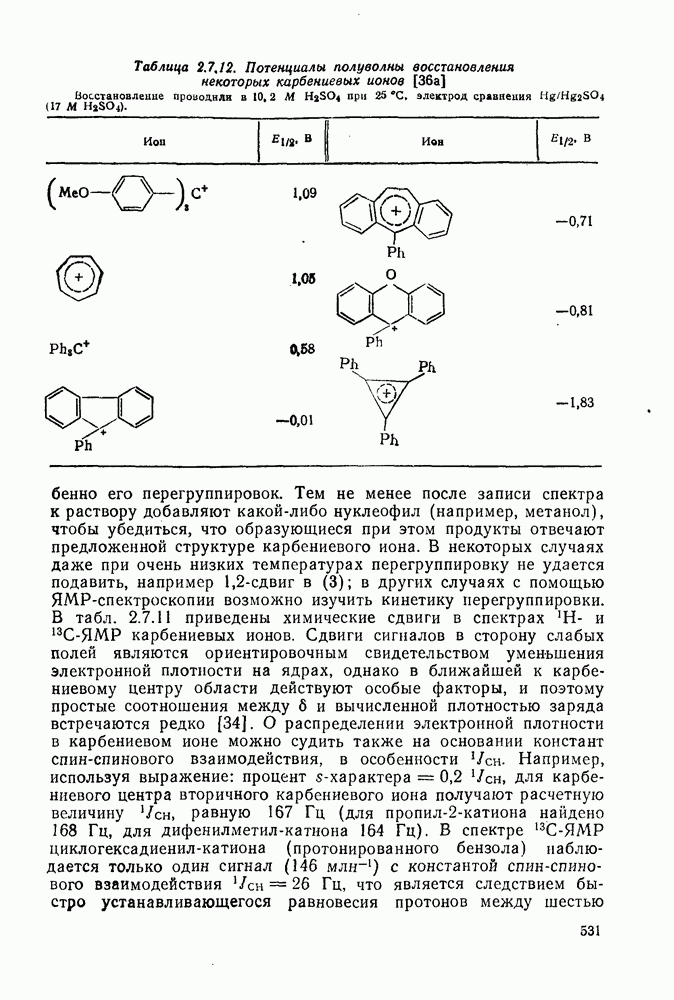
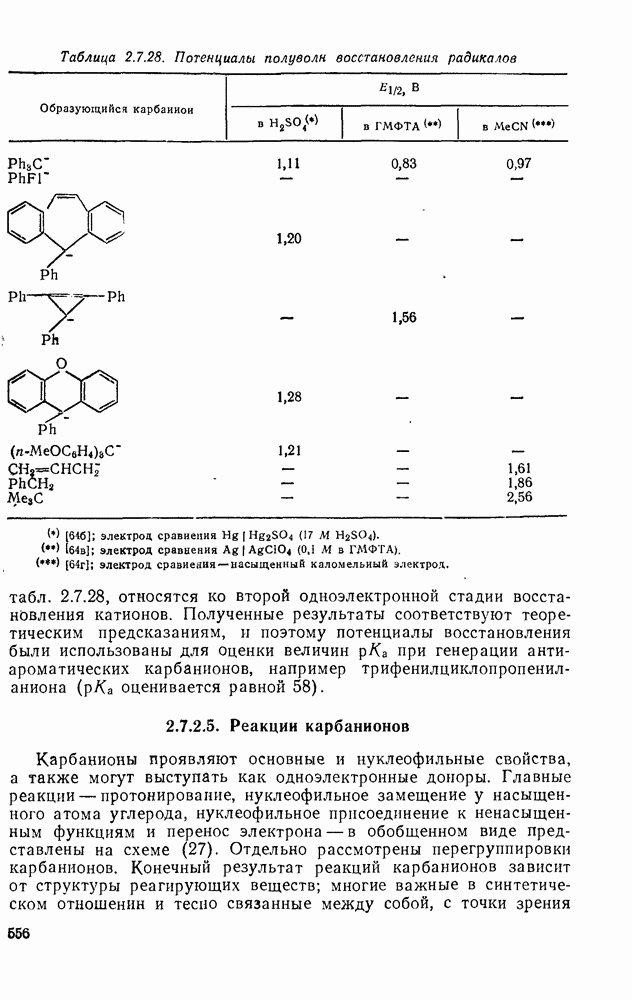
Таблица 2.7.12. Потенциалы полуволны восстановления некоторых карбениевых ионов [36а]
Восстановление проводили в 10,2 М  при
при  , электрод сравнения
, электрод сравнения  .
.

Тем не менее после записи спектра к раствору добавляют какой-либо нуклеофил (например, метанол), чтобы убедиться, что образующиеся при этом продукты отвечают предложенной структуре карбениевого иона. В некоторых случаях даже при очень низких температурах перегруппировку не удается подавить, например  -сдвиг в (3); в других случаях с помощью ЯМР-спектроскопии возможно изучить кинетику перегруппировки. В табл. 2.7.11 приведены химические сдвиги в спектрах
-сдвиг в (3); в других случаях с помощью ЯМР-спектроскопии возможно изучить кинетику перегруппировки. В табл. 2.7.11 приведены химические сдвиги в спектрах  и
и  -ЯМР карбениевых ионов. Сдвиги сигналов в сторону слабых полей являются ориентировочным свидетельством уменьшения электронной плотности на ядрах, однако в ближайшей к карбениевому центру области действуют особые факторы, и поэтому простые соотношения между б и вычисленной плотностью заряда встречаются редко [34]. О распределении электронной плотности в карбениевом ионе можно судить также на основании констант спин-спинового взаимодействия, в особенности
-ЯМР карбениевых ионов. Сдвиги сигналов в сторону слабых полей являются ориентировочным свидетельством уменьшения электронной плотности на ядрах, однако в ближайшей к карбениевому центру области действуют особые факторы, и поэтому простые соотношения между б и вычисленной плотностью заряда встречаются редко [34]. О распределении электронной плотности в карбениевом ионе можно судить также на основании констант спин-спинового взаимодействия, в особенности  . Например, используя выражение: процент
. Например, используя выражение: процент  -характера
-характера  , для карбениевого центра вторичного карбениевого иона получают расчетную величину
, для карбениевого центра вторичного карбениевого иона получают расчетную величину  , равную 167 Гц (для
, равную 167 Гц (для  найдено 168 Гц, для дифенилметил-катиона 164 Гц). В спектре
найдено 168 Гц, для дифенилметил-катиона 164 Гц). В спектре  -ЯМР циклогексадиенил-катиона (протонированного бензола) наблюдается только один сигнал
-ЯМР циклогексадиенил-катиона (протонированного бензола) наблюдается только один сигнал  ) с константой спин-спинового взаимодействия
) с константой спин-спинового взаимодействия  Гц, что является следствием быстро устанавливающегося равновесия протонов между шестью эквивалентными атомами углерода цикла.
Гц, что является следствием быстро устанавливающегося равновесия протонов между шестью эквивалентными атомами углерода цикла.
В этом случае вычисление усредненного значения константы спин-спинового взаимодействия для двух взаимодействий  и пяти
и пяти  среди шести положений приводит к величине
среди шести положений приводит к величине  Гц. Несовпадение данных по усредненным процессам, подобным вышеприведенным химическим сдвигам, является доказательством наличия мостиковых структур, например типа (36), а не двух находящихся в равновесии карбениевых структур (За) [2].
Гц. Несовпадение данных по усредненным процессам, подобным вышеприведенным химическим сдвигам, является доказательством наличия мостиковых структур, например типа (36), а не двух находящихся в равновесии карбениевых структур (За) [2].
(5) Электрические свойства
Электропроводность солей карбокатионов изучена относительно мало. Полученные результаты трудны в интерпретации из-за неполноты диссоциации солей [35]. Для изучения равновесия типа:  и оценки различий в свободной энергии между карбениевыми ионами была сконструирована обратимая электрохимическая ячейка [36]. Однако эта ячейка, по-видимому, использовалась только для изучения триарилметил-катионов. В табл. 2.7.12 приведены потенциалы полуволны полярографического восстановления карбениевых ионов в соответствующие радикалы.
и оценки различий в свободной энергии между карбениевыми ионами была сконструирована обратимая электрохимическая ячейка [36]. Однако эта ячейка, по-видимому, использовалась только для изучения триарилметил-катионов. В табл. 2.7.12 приведены потенциалы полуволны полярографического восстановления карбениевых ионов в соответствующие радикалы.
(6) Изучение промежуточно образующихся карбениевых ионов в растворе
Одним из важнейших доказательств промежуточного образования в ходе определенных химических реакций реакционноспособных карбениевых ионов является исследование соответствующих продуктов реакций, в особенности их структуры, стереохимии и соотношения, в которых они образуются. Наиболее информативным и достаточно веским доказательством является обнаружение продуктов реакции с перегруппированным скелетом. Простой пример приведен в уравнении (13).

Достаточно строгим доказательством в пользу появления таких реакционноспособных интермедиатов является образование аналогичных смесей продуктов из нескольких различных реагентов (RX), которые способны генерировать один и тот же карбениевый ион  . Чаще, однако, соотношение между возможными конкурентными направлениями реакции карбокатионов, например между замещением и элиминированием, изменяется за счет ассоциации промежуточного образующегося карбениевого иона с уходящей группой. Это в особенности справедливо при проведении реакций в растворителях с низкой полярностью. Так, сольволиз трет-бутил-бромида и трет-бутилдиметилсульфонийперхлората в воде (при
. Чаще, однако, соотношение между возможными конкурентными направлениями реакции карбокатионов, например между замещением и элиминированием, изменяется за счет ассоциации промежуточного образующегося карбениевого иона с уходящей группой. Это в особенности справедливо при проведении реакций в растворителях с низкой полярностью. Так, сольволиз трет-бутил-бромида и трет-бутилдиметилсульфонийперхлората в воде (при  ) приводит к примерно одинаковому соотношению продуктов замещения и элиминирования
) приводит к примерно одинаковому соотношению продуктов замещения и элиминирования  , в то время как в уксусной кислоте (при
, в то время как в уксусной кислоте (при  ) эти соотношения равны соответственно 0,44 и 7,5 [35].
) эти соотношения равны соответственно 0,44 и 7,5 [35].
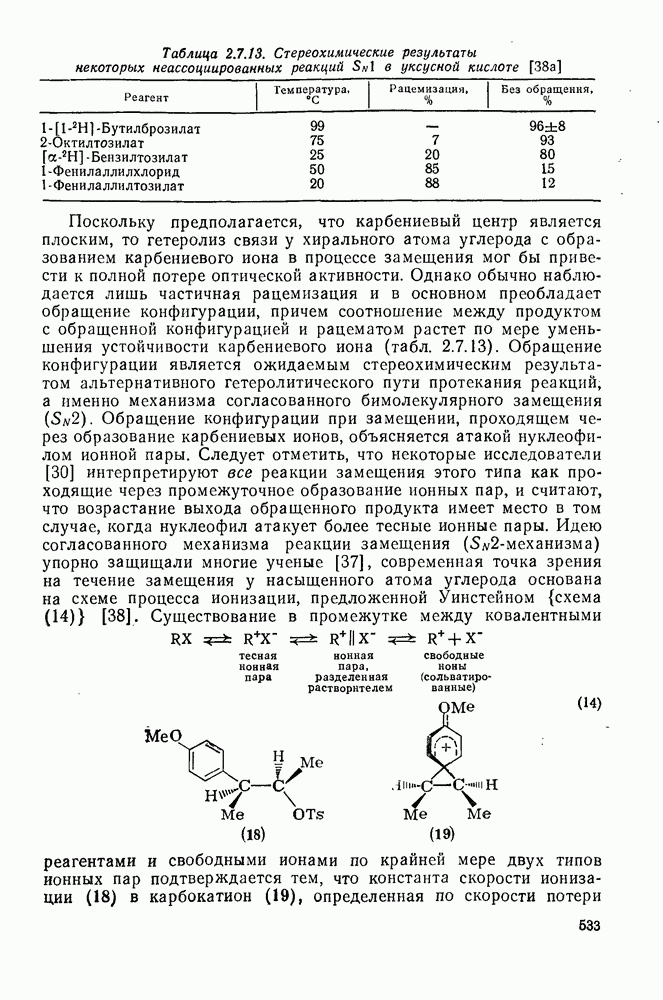
Таблица 2.7.13. Стереохимические результаты некоторых неассоциированных реакций  в уксусной кислоте [38а]
в уксусной кислоте [38а]

Поскольку предполагается, что карбениевый центр является плоским, то гетеролиз связи у хирального атома углерода с образованием карбениевого иона в процессе замещения мог бы привести к полной потере оптической активности. Однако обычно наблюдается лишь частичная рацемизация и в основном преобладает обращение конфигурации, причем соотношение между продуктом с обращенной конфигурацией и рацематом растет по мере уменьшения устойчивости карбениевого иона (табл. 2.7.13). Обращение конфигурации является ожидаемым стереохимическим результатом альтернативного гетеролитического пути протекания реакций, а именно механизма согласованного бимолекулярного замещения  . Обращение конфигурации при замещении, проходящем через образование карбениевых ионов, объясняется атакой нуклеофилом ионной пары. Следует отметить, что некоторые исследователи [30] интерпретируют все реакции замещения этого типа как проходящие через промежуточное образование ионных пар, и считают, что возрастание выхода обращенного продукта имеет место в том случае, когда нуклеофил атакует более тесные ионные пары. Идею согласованного механизма реакции замещения
. Обращение конфигурации при замещении, проходящем через образование карбениевых ионов, объясняется атакой нуклеофилом ионной пары. Следует отметить, что некоторые исследователи [30] интерпретируют все реакции замещения этого типа как проходящие через промежуточное образование ионных пар, и считают, что возрастание выхода обращенного продукта имеет место в том случае, когда нуклеофил атакует более тесные ионные пары. Идею согласованного механизма реакции замещения  упорно защищали многие ученые [37], современная точка зрения на течение замещения у насыщенного атома углерода основана на схеме процесса ионизации, предложенной Уинстейном (схема 14) [38]. Существование в промежутке между ковалентными
упорно защищали многие ученые [37], современная точка зрения на течение замещения у насыщенного атома углерода основана на схеме процесса ионизации, предложенной Уинстейном (схема 14) [38]. Существование в промежутке между ковалентными

реагентами и свободными ионами по крайней мере двух типов ионных пар подтверждается тем, что константа скорости ионизации (18) в карбокатион (19), определенная по скорости потери оптической активности  , больше, чем константа, полученная из скорости образования титруемой кислоты
, больше, чем константа, полученная из скорости образования титруемой кислоты  , даже в отсутствие рекомбинации кинетически свободных ионов, генерируемых при гетеролитическом расщеплении.
, даже в отсутствие рекомбинации кинетически свободных ионов, генерируемых при гетеролитическом расщеплении.
Добавки небольших количеств перхлората лития приводят к более быстрому возрастанию  по сравнению с
по сравнению с  , однако даже при очень высоких концентрациях перхлората лития отношение
, однако даже при очень высоких концентрациях перхлората лития отношение  не становится равным 1. Этот так называемый специфический солевой эффект указывает, что перхлорат способен перехватывать некоторые, но не все ионные пары. Ионные пары, перехватываемые перхлорат-ионом, относят к более слабо ассоциированным, разделенным растворителем ионным парам.
не становится равным 1. Этот так называемый специфический солевой эффект указывает, что перхлорат способен перехватывать некоторые, но не все ионные пары. Ионные пары, перехватываемые перхлорат-ионом, относят к более слабо ассоциированным, разделенным растворителем ионным парам.
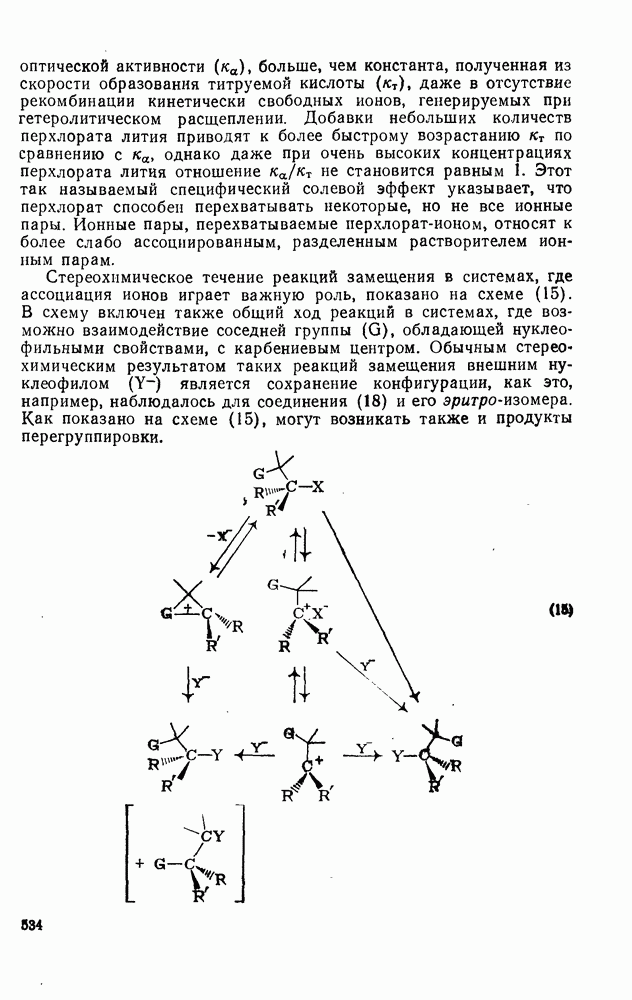
Стереохимическое течение реакций замещения в системах, где ассоциация ионов играет важную роль, показано на схеме (15). В схему включен также общий ход реакций в системах, где возможно взаимодействие соседней группы (G), обладающей нуклеофильными свойствами, с карбениевым центром. Обычным стерео-химическим результатом таких реакций замещения внешним нуклеофилом  является сохранение конфигурации, как это, например, наблюдалось для соединения (18) и его эритро-изомера. Как показано на схеме (15), могут возникать также и продукты перегруппировки.
является сохранение конфигурации, как это, например, наблюдалось для соединения (18) и его эритро-изомера. Как показано на схеме (15), могут возникать также и продукты перегруппировки.

Для того чтобы констатировать промежуточное образование карбениевых ионов и получить данные об их относительной устойчивости по сравнению с их предшественниками, возможно использовать кинетические методы изучения нуклеофильного замещения. Если допустить, что промежуточно образующиеся роны являются кинетически независимыми частицами, то кинетическое уравнение нуклеофильного замещения по механизму  [см. схему (2)] будет иметь вид:
[см. схему (2)] будет иметь вид:

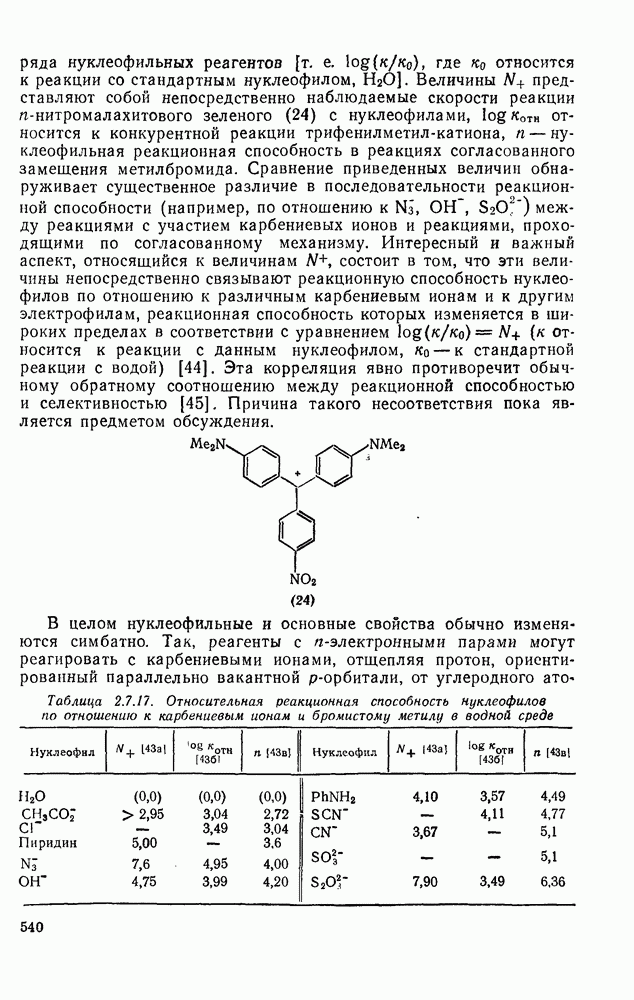
В частном случае, когда в роли нуклеофила  выступает молекула растворителя
выступает молекула растворителя  и наблюдаемая константа скорости
и наблюдаемая константа скорости  представляет собой константу скорости ионизации. При этих условиях скорость реакции не зависит от концентрации нуклеофилов в системе, хотя они и влияют на соотношение образующихся продуктов. Вид кинетического уравнения, однако, не позволяет различить механизмы
представляет собой константу скорости ионизации. При этих условиях скорость реакции не зависит от концентрации нуклеофилов в системе, хотя они и влияют на соотношение образующихся продуктов. Вид кинетического уравнения, однако, не позволяет различить механизмы  и
и  в реакциях сольволиза. Добавление к реакционной смеси общего иона
в реакциях сольволиза. Добавление к реакционной смеси общего иона  обычно замедляет реакции
обычно замедляет реакции  , однако такое поведение наблюдается только в случае реагентов, образующих достаточно устойчивые промежуточные карбениевые ионы, например в случае
, однако такое поведение наблюдается только в случае реагентов, образующих достаточно устойчивые промежуточные карбениевые ионы, например в случае  и
и  , но не
, но не  .
.
Даже если отвлечься от проблемы сольволиза, кинетическая характеристика реакций замещения не позволяет сделать однозначного заключения об образовании карбениевых ионов, если промежуточно образующиеся ионы не становятся кинетически независимыми. В этом случае кинетическая характеристика как  , так и
, так и  -механизмов одинакова и для констатации стадии ионизации следует использовать менее прямые доказательства, например влияние растворителей на скорость реакции и корреляционный анализ с использованием уравнения
-механизмов одинакова и для констатации стадии ионизации следует использовать менее прямые доказательства, например влияние растворителей на скорость реакции и корреляционный анализ с использованием уравнения  , где значения
, где значения  взяты из табл. 2.7.1, а
взяты из табл. 2.7.1, а  равно примерно 1 в случае мономолекулярного замещения в отсутствие эффекта содействия. Можно использовать также стереохимические изменения в подходящих системах или перераспределение изотопной метки в таких реагентах, как, например,
равно примерно 1 в случае мономолекулярного замещения в отсутствие эффекта содействия. Можно использовать также стереохимические изменения в подходящих системах или перераспределение изотопной метки в таких реагентах, как, например,  и
и  .
.
В тех случаях, когда  константа скорости ионизации часто используется для оценки устойчивости, а следовательно, и структуры помежуточно образующегося карбениевого иона. При этом подразумевают, что 1) переходное состояние стадии ионизации имеет структуру, близкую к структуре промежуточно образующегося иона, что, вероятно, справедливо только для сильно эндотермичных процессов (постулат Хэммонда); 2) устойчивость иона оценивается относительно устойчивости реагента. Большая часть результатов, особенно по реакциям сольволиза, нуждается в очень тщательной проверке, поскольку данные по относительным скоростям могут быть искажены за счет нуклеофильного содействия растворителя отрыву уходящей группы (что зависит как от структуры реагента, так и от природы растворителя) и «внутреннего превращения» ионной пары в исходный реагент, которое иногда очень трудно отличить от тесных ионных пар [39].
константа скорости ионизации часто используется для оценки устойчивости, а следовательно, и структуры помежуточно образующегося карбениевого иона. При этом подразумевают, что 1) переходное состояние стадии ионизации имеет структуру, близкую к структуре промежуточно образующегося иона, что, вероятно, справедливо только для сильно эндотермичных процессов (постулат Хэммонда); 2) устойчивость иона оценивается относительно устойчивости реагента. Большая часть результатов, особенно по реакциям сольволиза, нуждается в очень тщательной проверке, поскольку данные по относительным скоростям могут быть искажены за счет нуклеофильного содействия растворителя отрыву уходящей группы (что зависит как от структуры реагента, так и от природы растворителя) и «внутреннего превращения» ионной пары в исходный реагент, которое иногда очень трудно отличить от тесных ионных пар [39].
Таблица 2.7.14. Относительные скорости сольволиза алкил- и циклоалкилпроизводных [39а, б]
Оценка по данным тнтрометрни или кондуктометрни

В табл. 2.7.14 приведены некоторые кинетические данные по сольволизу алкил-и циклоалкилпроизводных. Наименее нуклеофильным из приведенных растворителей является трифторуксусная кислота, и поэтому при ее использовании относительные скорости сольволиза наиболее точно отражают устойчивость промежуточно образующихся карбениевых ионов. Муравьиная кислота является более нуклеофильным растворителем, и это приводит к тому, что скорость сольволиза алкилпроизводных, которые могут образовывать очень неустойчивые карбениевые ионы, возрастает за счет нуклеофильного содействия растворителя. Это становится еще более очевидным при проведении сольволиза в этаноле. Адамантил- является особенно подходящим стандартом для определения относительных скоростей, поскольку в каркасных структурах механизм
является особенно подходящим стандартом для определения относительных скоростей, поскольку в каркасных структурах механизм  очень затруднен и, как полагают, сольволиз проходит
очень затруднен и, как полагают, сольволиз проходит

исключительно по ионному механизму. Как и ожидалось, сольволиз алкилхлоридов, несущих группы, которые способны к  -делокализации карбениевого заряда, значительно ускоряется, как это видно из следующих данных по сольволизу аллил- и арилалкил-хлоридов
-делокализации карбениевого заряда, значительно ускоряется, как это видно из следующих данных по сольволизу аллил- и арилалкил-хлоридов  в
в  -ном водном этаноле при
-ном водном этаноле при  [39а]:
[39а]:
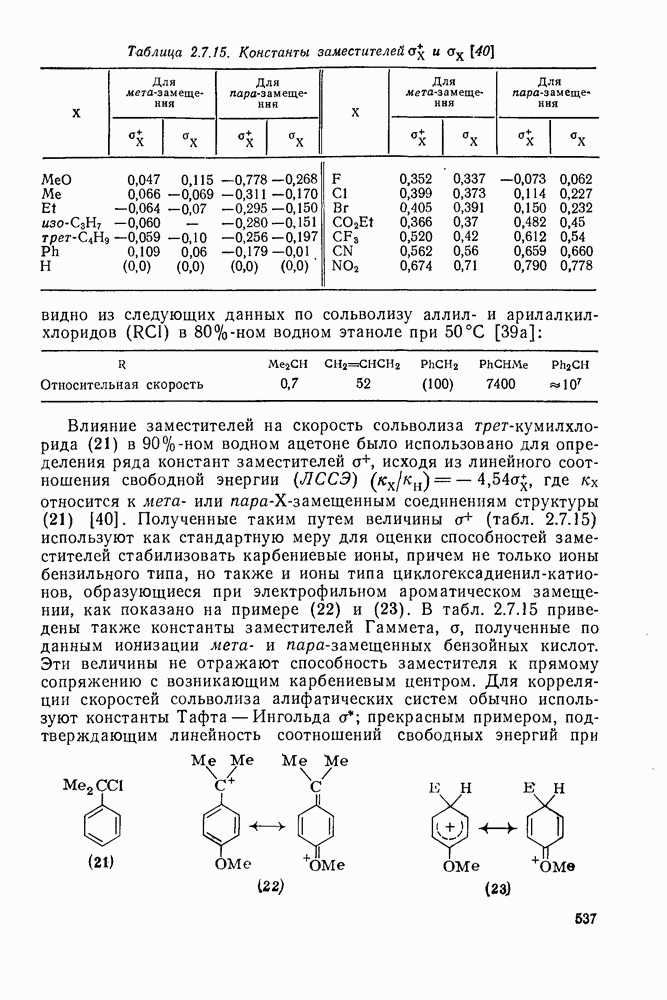
Таблица 2.7.15. Константы заместителей  и
и  [40]
[40]


Влияние заместителей на скорость сольволиза трет-кумилхло-рида (21) в  -ном водном ацетоне было использовано для определения ряда констант заместителей
-ном водном ацетоне было использовано для определения ряда констант заместителей  , исходя из линейного соотношения свободной энергии (ЛССЭ)
, исходя из линейного соотношения свободной энергии (ЛССЭ)  , где
, где  относится к мета- или пара-Х-замещенным соединениям структуры (21) [40]. Полученные таким путем величины
относится к мета- или пара-Х-замещенным соединениям структуры (21) [40]. Полученные таким путем величины  (табл. 2.7.15) используют как стандартную меру для оценки способностей заместителей стабилизовать карбениевые ионы, причем не только ионы бензильного типа, но также и ионы типа циклогексадиенил-катионов, образующиеся при электрофильном ароматическом замещении, как показано на примере (22) и (23). В табл. 2.7.15 приведены также константы заместителей Гаммета, а, полученные по данным ионизации мета- и пара-замещенных бензойных кислот. Эти величины не отражают способность заместителя к прямому сопряжению с возникающим карбениевым центром. Для корреляции скоростей сольволиза алифатических систем обычно используют константы Тафта — Ингольда
(табл. 2.7.15) используют как стандартную меру для оценки способностей заместителей стабилизовать карбениевые ионы, причем не только ионы бензильного типа, но также и ионы типа циклогексадиенил-катионов, образующиеся при электрофильном ароматическом замещении, как показано на примере (22) и (23). В табл. 2.7.15 приведены также константы заместителей Гаммета, а, полученные по данным ионизации мета- и пара-замещенных бензойных кислот. Эти величины не отражают способность заместителя к прямому сопряжению с возникающим карбениевым центром. Для корреляции скоростей сольволиза алифатических систем обычно используют константы Тафта — Ингольда  прекрасным примером, подтверждающим линейность соотношений свободных энергий при использовании таких констант, служит сольволиз трет-алкилхлоридов [41].
прекрасным примером, подтверждающим линейность соотношений свободных энергий при использовании таких констант, служит сольволиз трет-алкилхлоридов [41].

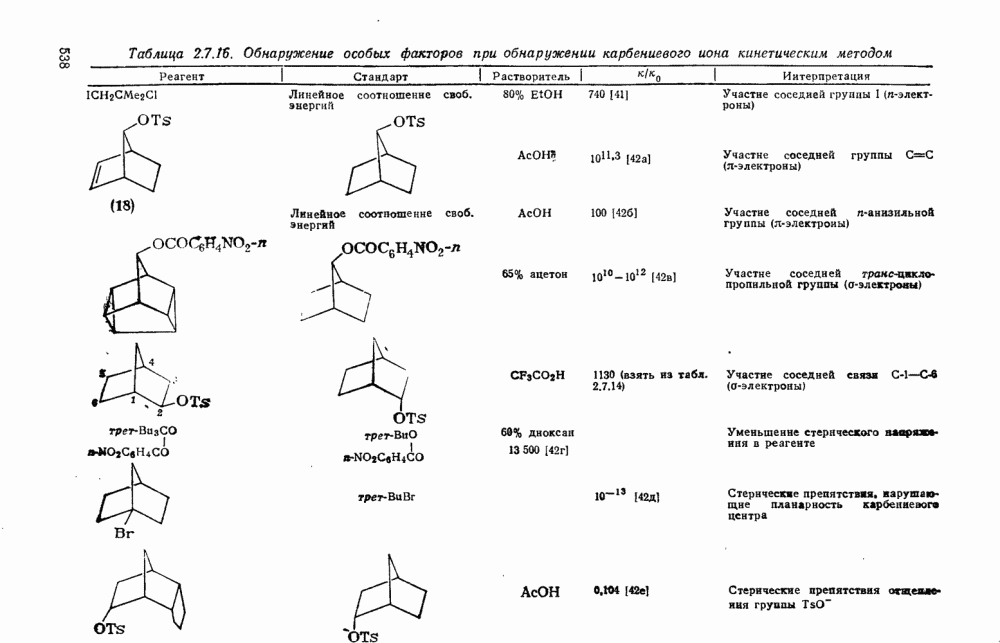
Таблица 2.7.16. Обнаружение особых факторов при обнаружении карбениевого иона кинетическим методом

Отклонения от таких корреляций указывают, по-видимому, на участие особых факторов, ускоряющих или замедляющих реакцию, таких как участие соседней группы, стерическое ускорение или пространственное затруднение ионизации. Некоторые примеры приведены в табл. 2.7.16, включающей случаи, когда особые факторы были обнаружены сравнением экспериментальной константы скорости реакции с константой скорости реакции модельного соединения или с константой скорости реакции, рассчитанной по уравнению, предложенному Футом и Шлейером [42].
В тех случаях, когда обнаружено участие соседней группы, в формуле промежуточно образующегося карбокатиона обычно отражают участие этой группы в делокализации положительного заряда. Если соучаствующая группа является насыщенной алкильной группой, то карбокатион следует изображать как пентакоордини-рованный карбониевый ион.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- ИЗ ПРЕДИСЛОВИЯ К ТОМУ 1 АНГЛИЙСКОГО ИЗДАНИЯ
- ЧАСТЬ I. НОМЕНКЛАТУРА И СТЕРЕОХИМИЯ
- 1.1. ВВЕДЕНИЕ И СТЕРЕОХИМИЯ
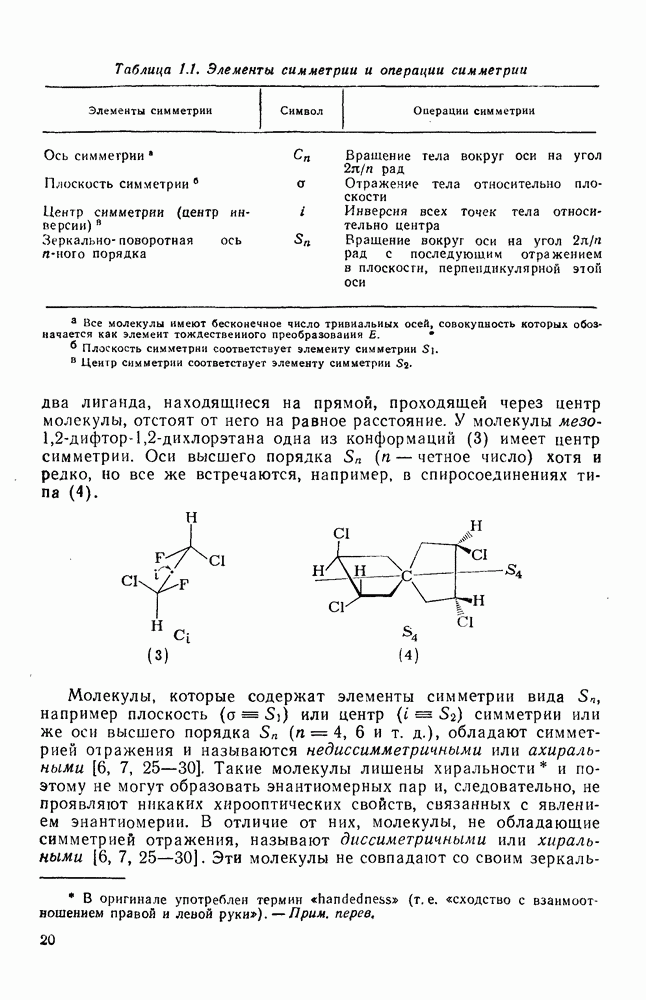
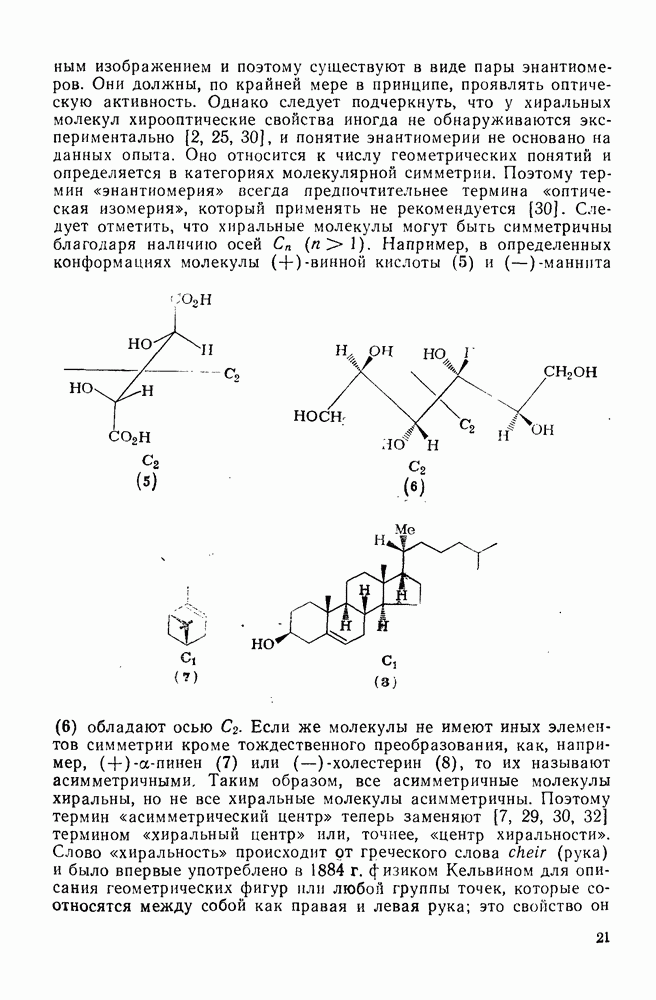
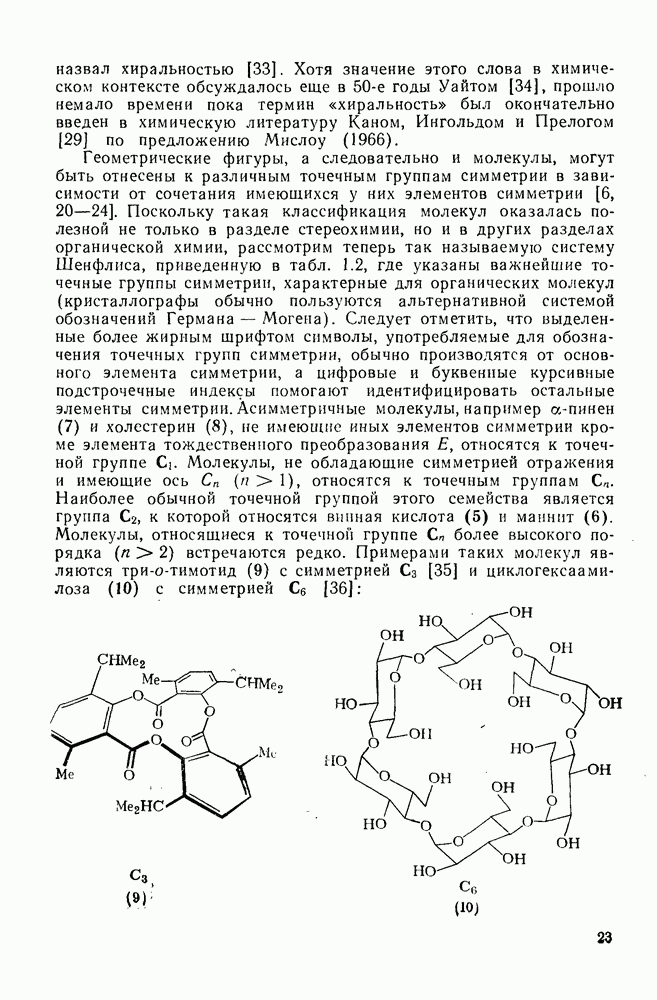
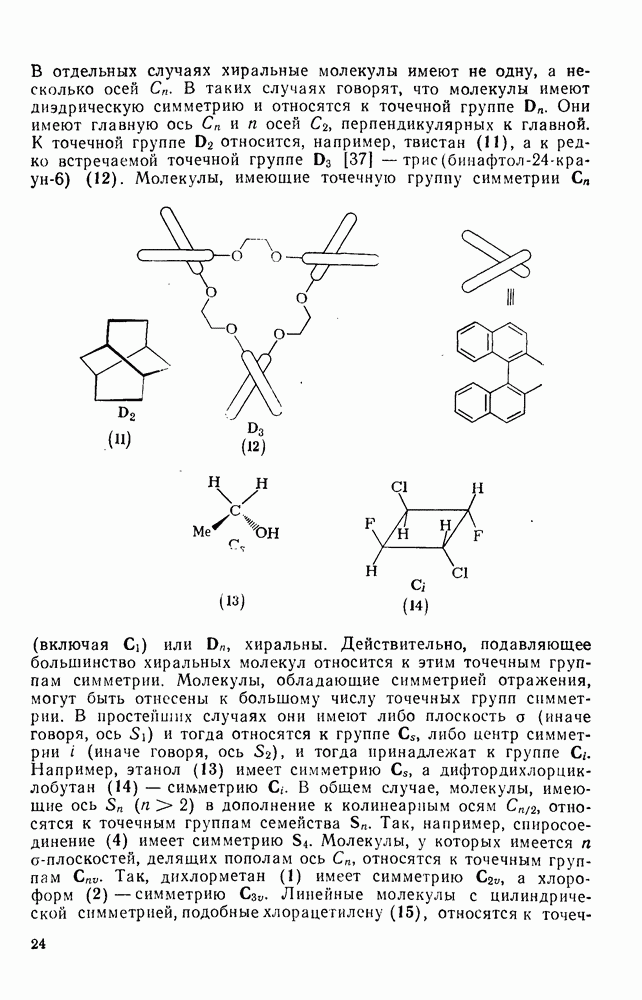
- 1.1.2. СИММЕТРИЯ И ХИРАЛЬНОСТЬ
- 1.1.3. ХИМИЧЕСКАЯ ТОПОЛОГИЯ
- 1.1.4. ИЗОМЕРИЯ
- 1.1.4.2. Строение
- 1.1.4.3. Абсолютная конфигурация
- 1.1.4.4. Относительная конфигурация
- 1.1.4.5. Конформация
- 1.1.4.6. Концепция изомерии
- 1.1.5. ТОПИЗМ
- 1.1.5.2. Прохиральность
- 1.1.5.3. Псевдоасимметрия (псевдохиральность)
- 1.1.6. ТОПОМЕРИЯ
- 1.1.7. ДИНАМИЧЕСКАЯ СТЕРЕОХИМИЯ. КРАТКИЕ СВЕДЕНИЯ
- ЧАСТЬ 2. УГЛЕВОДОРОДЫ
- 2.1. НАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- 2.1.2. Строение и номенклатура
- 2.1.2.1. Номенклатура IUPAC
- 2.1.2.2. Алициклические алканы
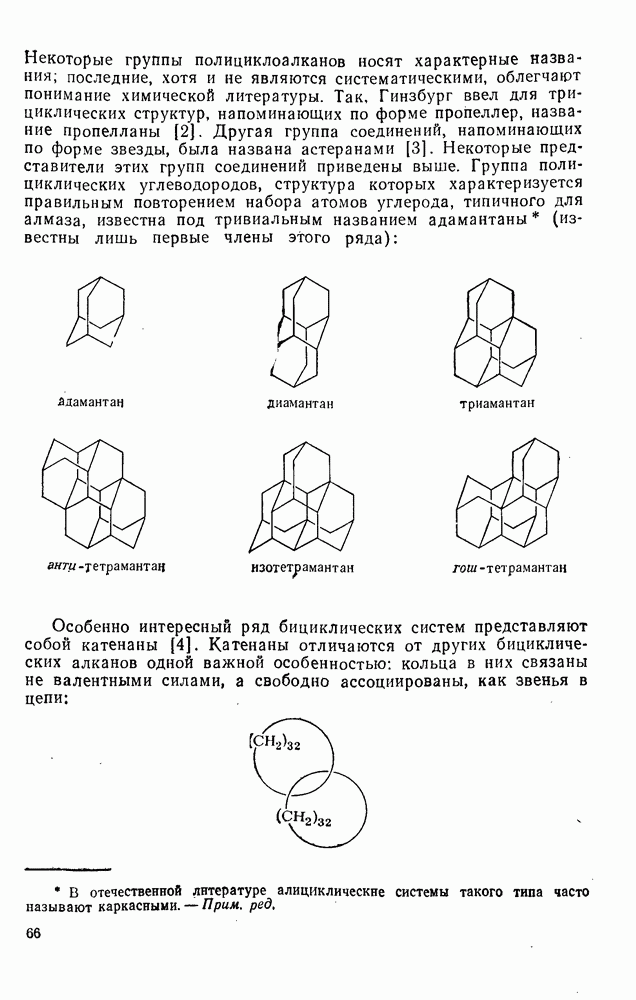
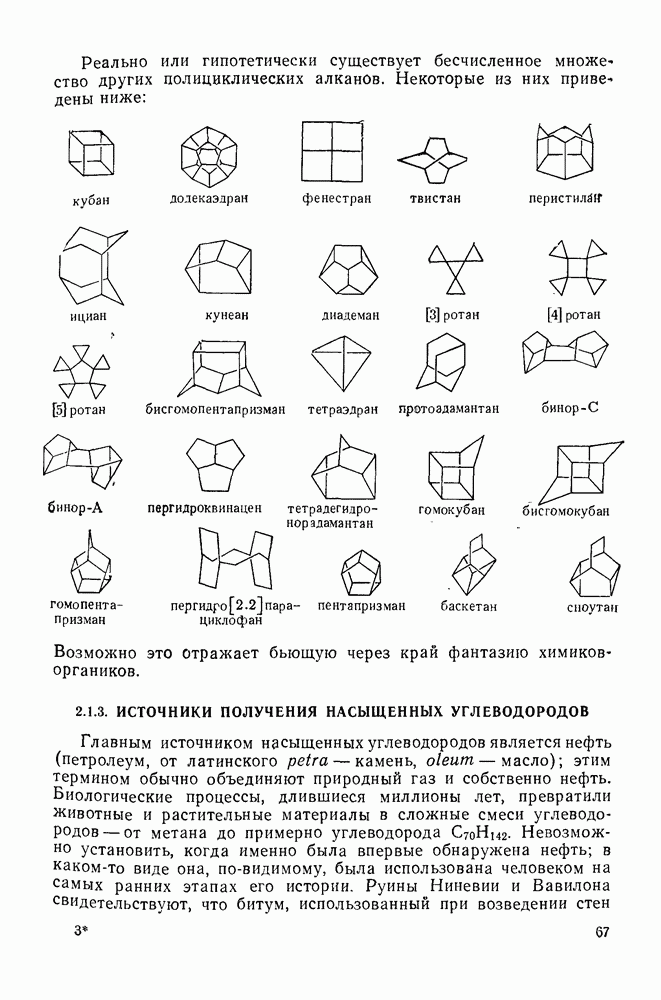
- 2.1.2.3. Полициклоалканы
- 2.1.3. ИСТОЧНИКИ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ УГЛЕВОДОРОДОВ
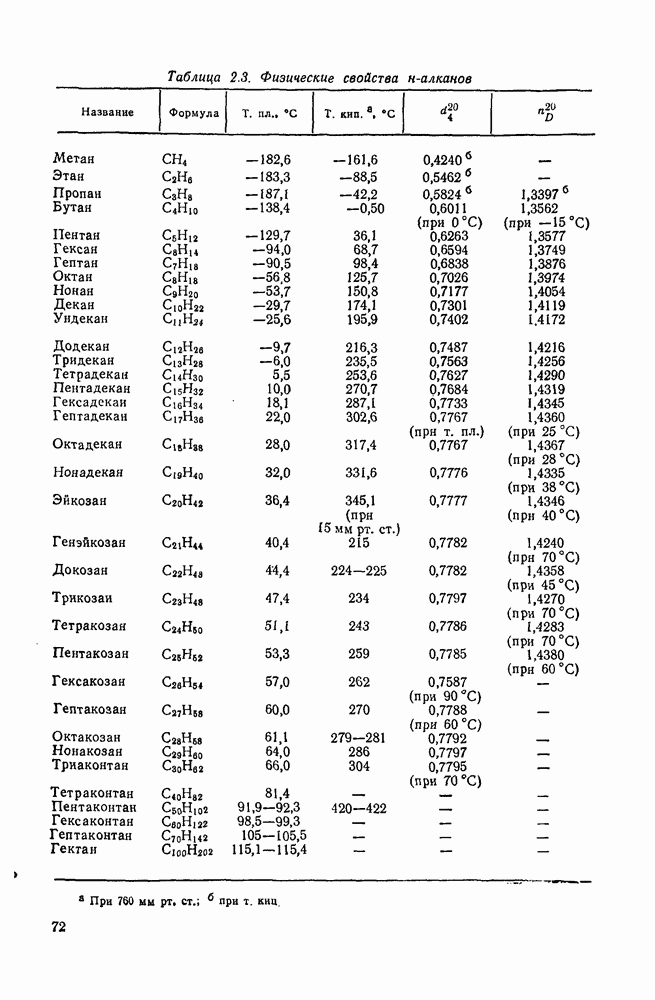
- 2.1.4. ФИЗИЧЕСКИЕ СВОЙСТВА
- 2.1.4.1. Ациклические алканы
- 2.1.4.2. Моно- и полициклоалканы
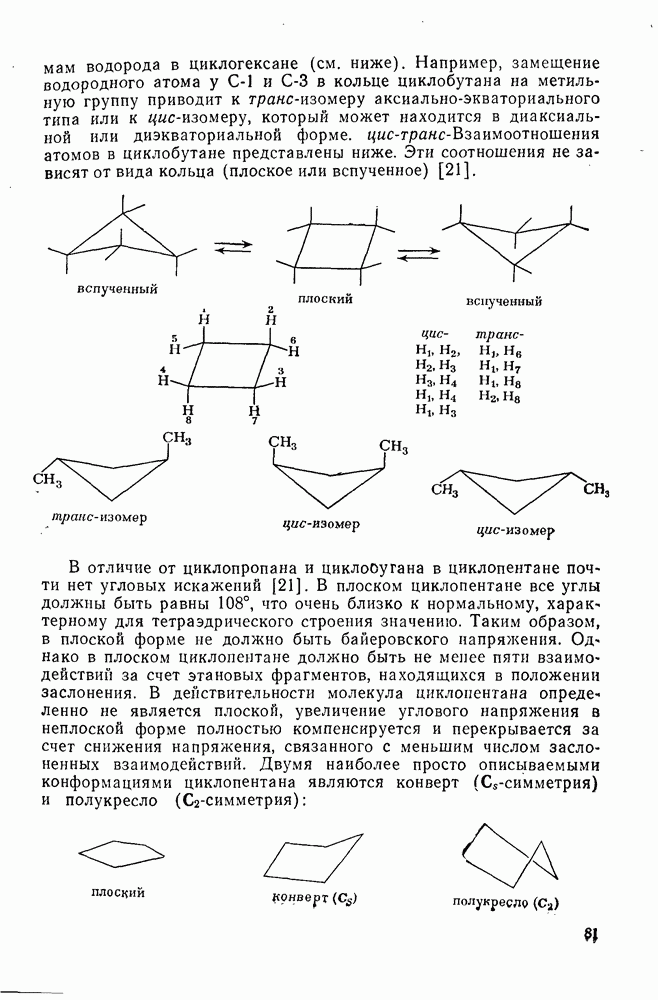
- 2.1.5. СТЕРЕОХИМИЯ И КОНФОРМАЦИОННЫЙ АНАЛИЗ
- 2.1.5.1. Углы и длины связей
- 2.1.5.2. Алкил- и полиалкилциклогексаны
- 2.1.5.3. Конформация карбоциклических колец, больших, чем циклогексан
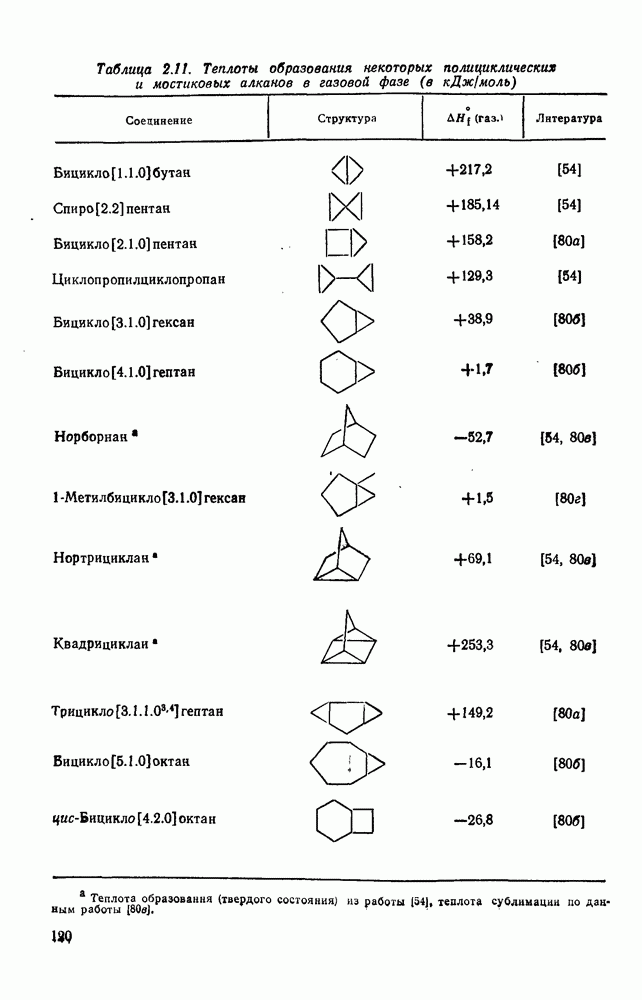
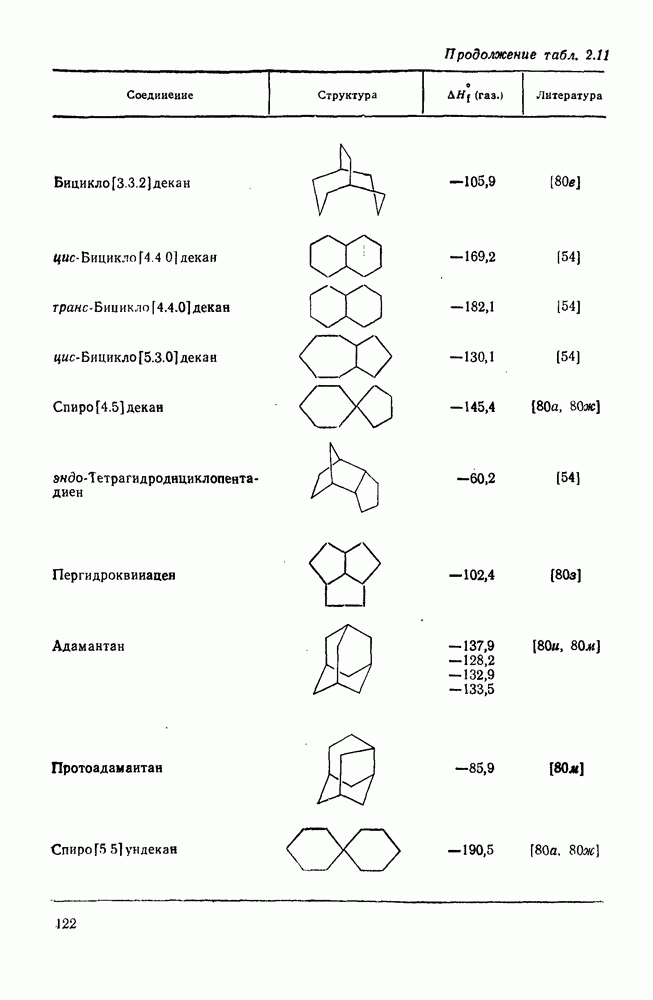
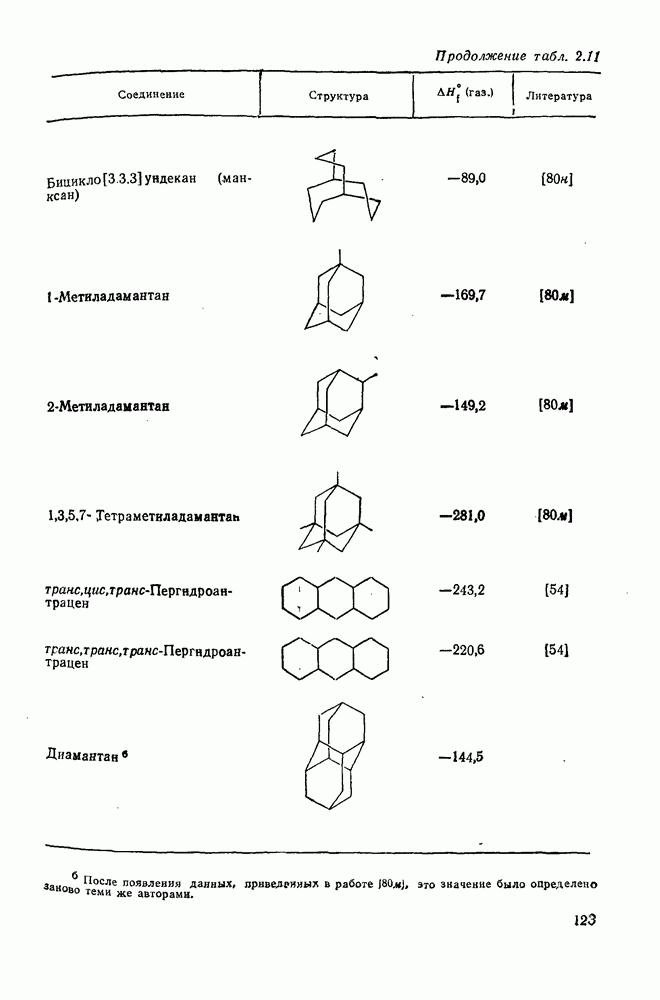
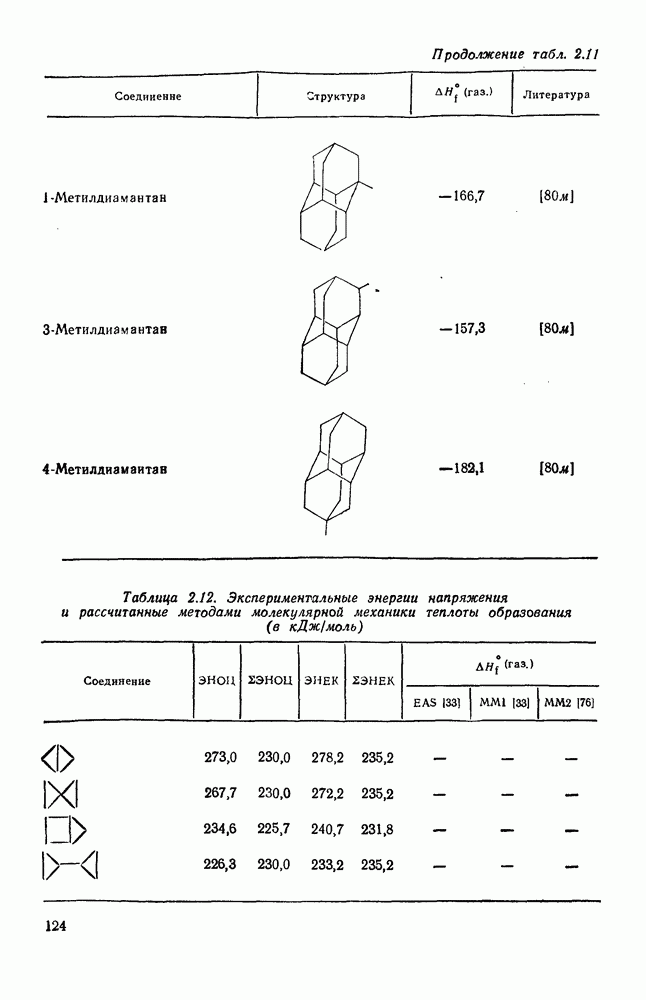
- 2.1.6. ТЕРМОХИМИЧЕСКИЕ СВОЙСТВА
- 2.1.6.1. Горение. Алканы и циклоалканы как топливо
- 2.1.6.2. Определение теплот сгорания и термохимические свойства
- 2.1.6.3. Эмпирические методы оценки теплот образования алканов
- 2.1.6.4. Оценка теплот образования алканов на основе энергии связей
- 2.1.6.5. Оценка теплот образования алканов на основе инкрементов групп
- 2.1.6.6. Оценка теплот образования циклических, полициклических и мостиковых алканов на основе инкрементов «скошенных разобщенных» групп и «единственных» наиболее устойчивых конформаций
- 2.1.6.7. Молекулярно-механические расчеты теплот образования и энергии напряжения
- 2.1.6.8. Моно- и полициклоалкаиы
- 2.1.7. ПОЛУЧЕНИЕ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.7.1. Получение алканов восстановлением олефинов
- 2.1.7.2. Получение алканов из альдегидов и кетонов
- 2.1.7.3. Получение алканов из спиртов и алкилгалогенидов
- 2.1.7.4. Получение алканов из карбоновых кислот
- 2.1.8. СИНТЕЗ МОНО- И ПОЛИЦИКЛОАЛКАНОВ
- 2.1.9. РЕАКЦИИ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.9.1. Галогенирование
- 2.1.9.2. Нитрование
- 2.1.9.3. Окисление
- 2.1.9.4. Каталитическая изомеризация алканов
- 2.1.9.5. Каталитическое алкилирование алканов
- 2.1.9.6. Реакции крекинга алканов
- 2.1.9.7. Термический крекинг
- 2.1.9.8. Каталитический крекинг
- 2.1.9.9. Каталитический риформинг и дегидроциклизация алканов
- 2.1.10. РЕАКЦИИ ЦИКЛОАЛКАНОВ И ПОЛИЦИКЛОАЛКАНОВ
- 2.2. ОЛЕФИНОВЫЕ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.2.2. ПОЛУЧЕНИЕ ОЛЕФИНОВ
- 2.2.2.1. Элиминирование в системах
- 2.2.2.2. Элиминирование из систем
- 2.2.2.3. Циклоэлиминирование
- 2.2.2.4. Частичное восстановление
- 2.2.2.5. Элиминирование сульфонилгидразонов
- 2.2.2.6. Реакция Виттига и родственные ей реакции
- 2.2.2.7. Различные реакции конденсации
- 2.2.2.8. Электроциклические реакции
- 2.2.2.9. Циклоолигомеризация
- 2.2.2.11. Реакции винильных производных
- 2.2.3. РЕАКЦИИ ОЛЕФИНОВ
- 2.2.3.1. Электрофильное присоединение
- 2.2.3.2. Нуклеофильное присоединение
- 2.2.3.3. Радикальное присоединение
- 2.2.3.4. Циклоприсоединение и родственные реакции
- 2.2.3.5. Окисление
- 2.2.3.6. Восстановление
- 2.2.3.7. Перегруппировки
- 2.2.3.8. Фотохимические реакции
- 2.2.3.9. Прочие реакции
- 2.3. ДИЕНЫ, ПОЛНЕНЫ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.3.1. СОПРЯЖЕННЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.1.2. Получение сопряженных диенов
- 2.3.2. РЕАКЦИИ СОПРЯЖЕННЫХ ДИЕНОВ
- 2.3.2.2. Восстановление
- 2.3.2.3. Гидроборирование
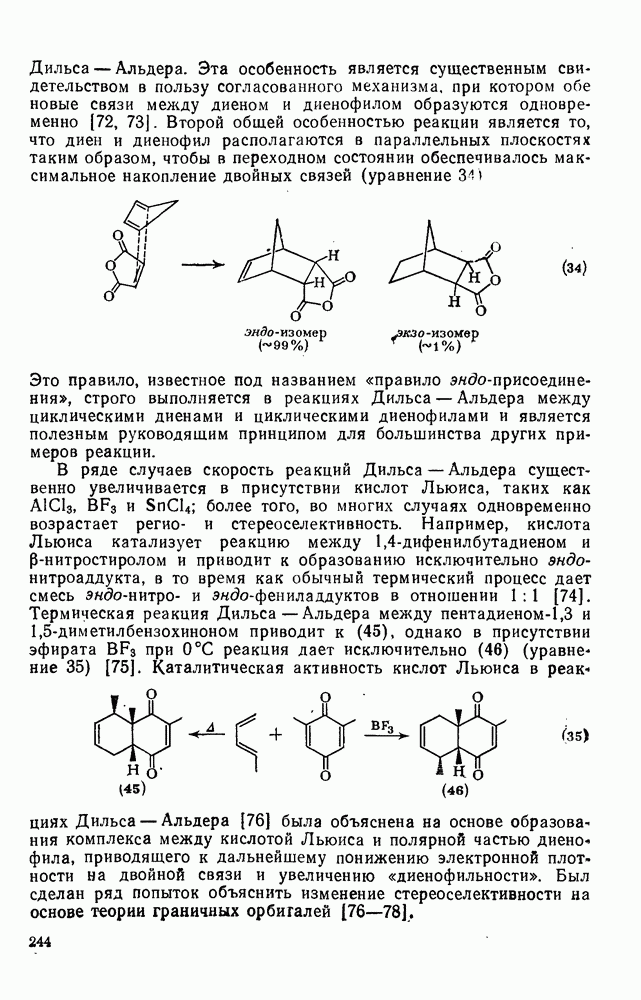
- 2.3.2.4. Реакция Дильса — Альдера
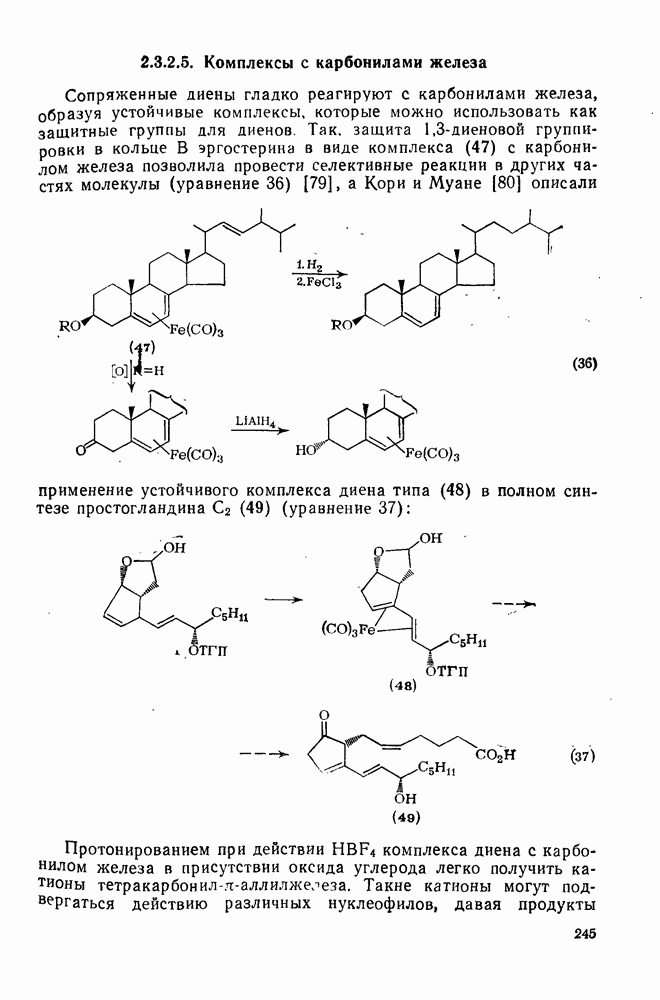
- 2.3.2.5. Комплексы с карбонилами железа
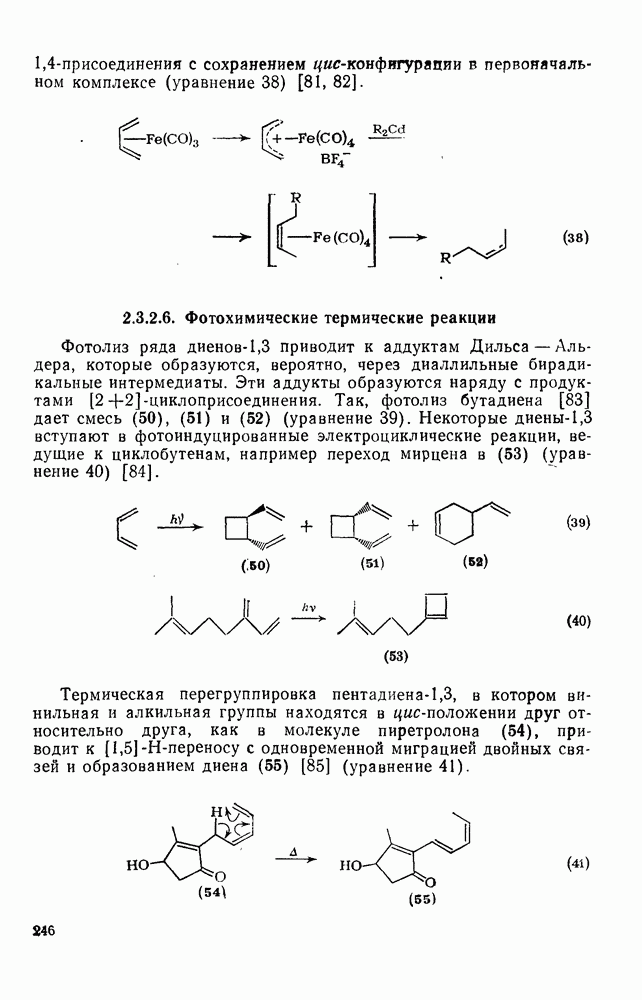
- 2.3.2.6. Фотохимические термические реакции
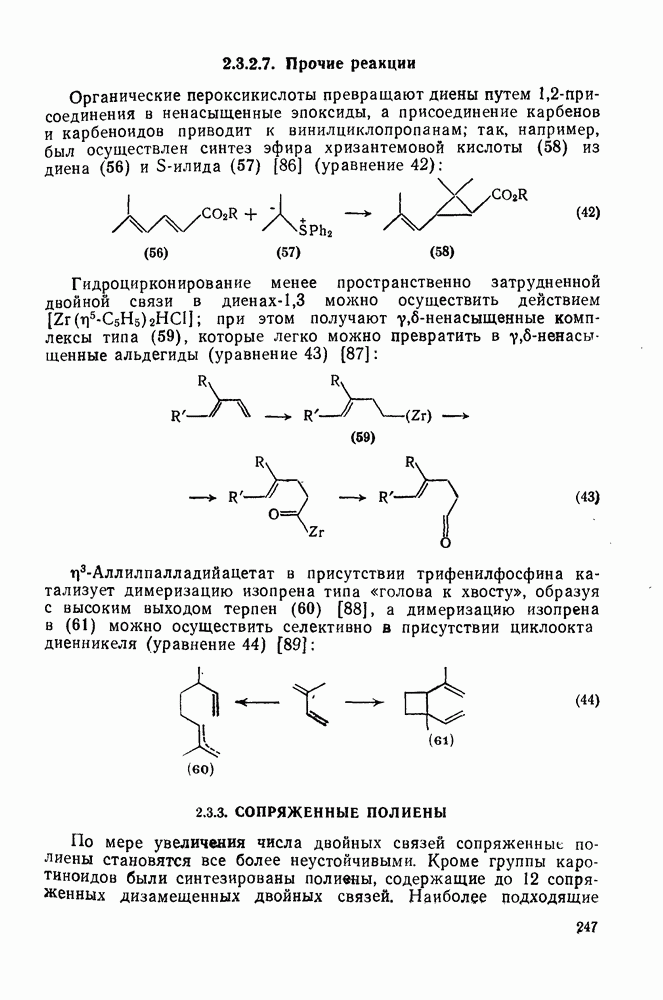
- 2.3.2.7. Прочие реакции
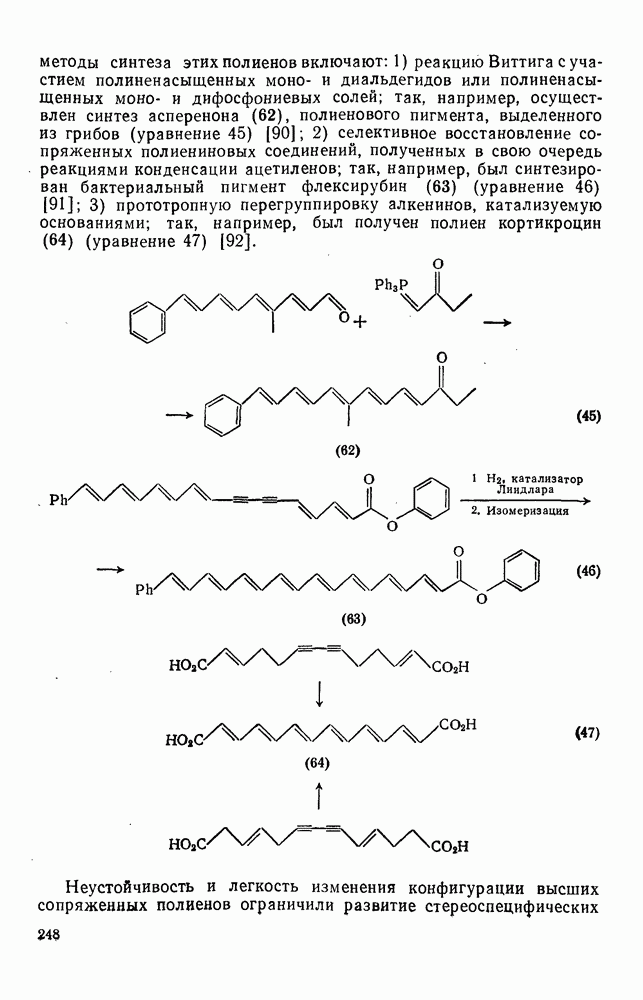
- 2.3.3. СОПРЯЖЕННЫЕ ПОЛИЕНЫ
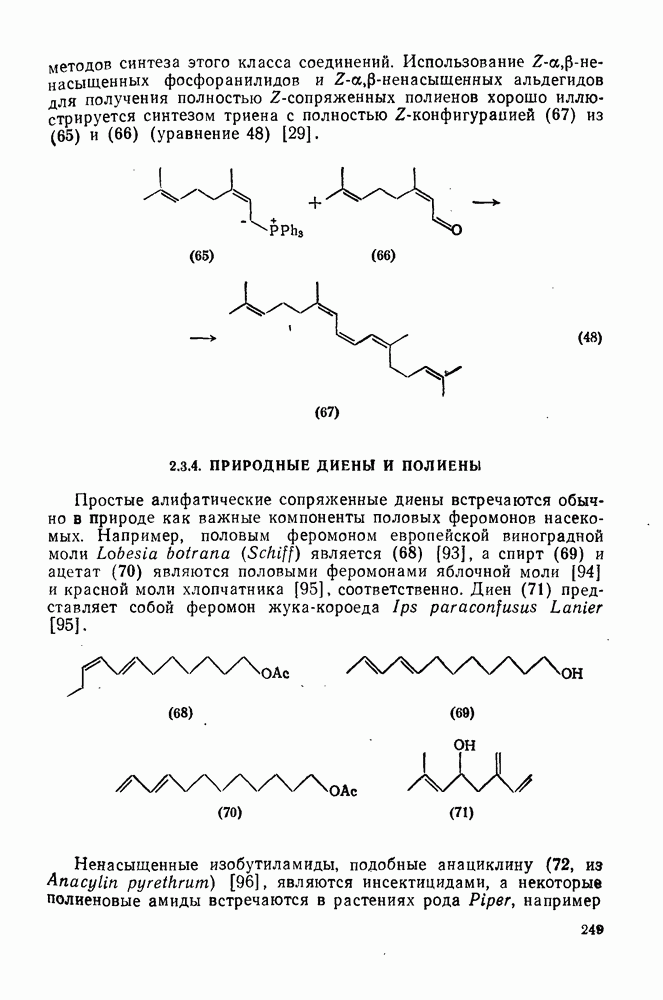
- 2.3.4. ПРИРОДНЫЕ ДИЕНЫ И ПОЛНЕНЫ
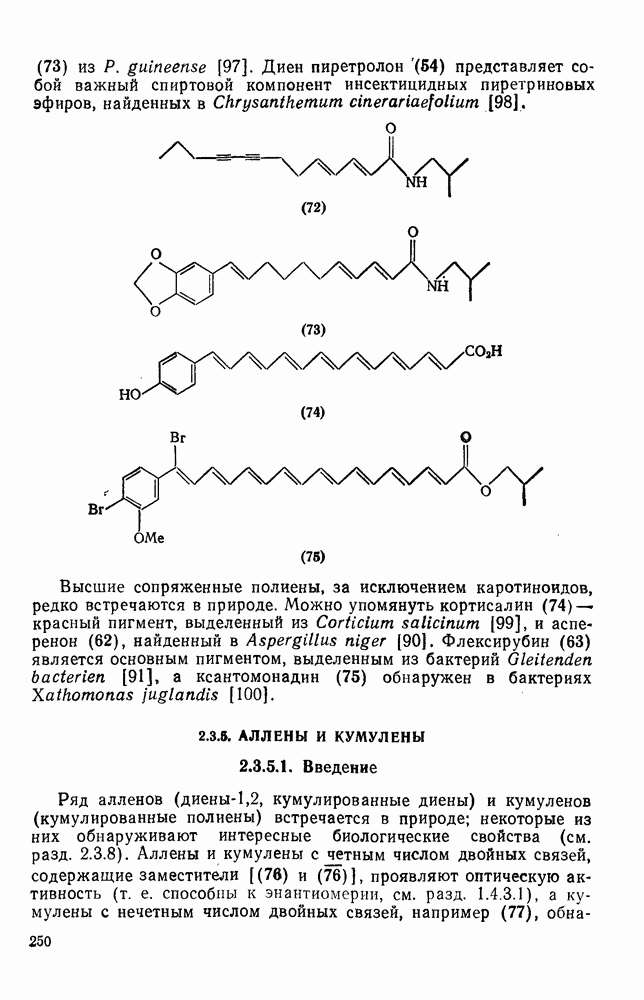
- 2.3.5. АЛЛЕНЫ И КУМУЛЕНЫ
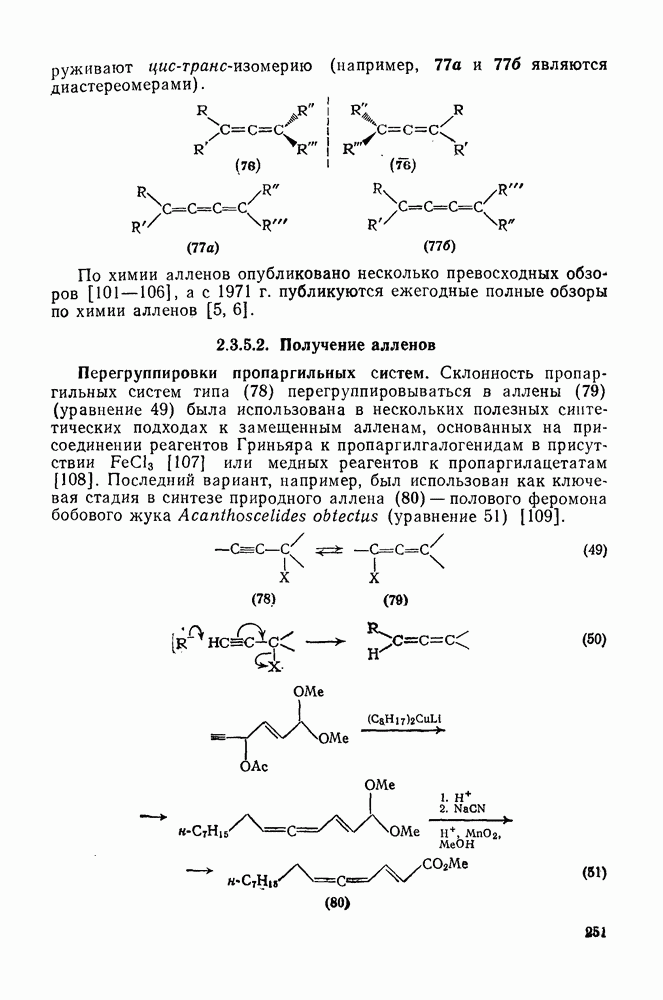
- 2.3.5.2. Получение алленов
- 2.3.6. РЕАКЦИИ АЛЛЕНОВ
- 2.3.6.2. Гидрирование
- 2.3.6.3. Реакции алленов в присутствии комплексов металлов
- 2.3.7. КУМУЛЕНЫ
- 2.3.8. ПРИРОДНЫЕ АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.9. АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.9.2. Получение ацетиленов
- 2.3.10. РЕАКЦИИ АЦЕТИЛЕНОВ
- 2.3.10.2. Изомеризация
- 2.3.10.3. Пропаргильные перегруппировки
- 2.3.10.4. Реакции присоединения
- 2.3.10.5. Гидроборирование и гидроалюминирование
- 2.3.10.6. Реакции замещения
- 2.3.10.7. Восстановление
- 2.3.10.8. Окисление
- 2.3.10.9. Циклоприсоединение
- 2.3.10.10. Реакции катализуемые металлами
- 2.3.11. ПОЛИАЦЕТИЛЕНЫ
- 2.3.12. ПРИРОДНЫЕ АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.13. СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.3.13.1. Получение сопряженных енинов
- 2.3.14. РЕАКЦИИ СОПРЯЖЕННЫХ ЕНИНОВ
- 2.3.15. ПРИРОДНЫЕ СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.4. АРОМАТИЧНОСТЬ
- 2.4.2. ЭЛЕКТРОННЫЕ ТЕОРИИ СТРОЕНИЯ БЕНЗОЛА
- 2.4.3. КРИТЕРИИ АРОМАТИЧНОСТИ
- 2.4.3.1. Термодинамические свойства
- 2.4.3.2. Структурные особенности
- 2.4.3.3. Магнитные свойства
- 2.4.3.4. Прочие критерии
- 2.4.4. АНТИАРОМАТИЧНОСТЬ
- 2.4.4.1. Термодинамические свойства
- 2.4.4.2. Структурные особенности
- 2.4.4.3. Магнитные свойства
- 2.4.4.4. Прочие свойства
- 2.4.5. ТЕОРЕТИЧЕСКИЕ ОПРЕДЕЛЕНИЯ АРОМАТИЧНОСТИ
- 2.4.5.1. Полуэмпирические расчеты и дьюаровская резонансная энергия
- 2.4.5.2. Расчеты по методу валентных пар и применение резонансного метода
- 2.4.5.3. Локализация связей
- 2.4.5.4. Связь энергетических критериев с критериями локализации связей
- 2.4.6. АРОМАТИЧЕСКИЕ ПЕРЕХОДНЫЕ СОСТОЯНИЯ
- 2.5. АРЕНЫ И ИХ РЕАКЦИИ
- 2.5.2. НОМЕНКЛАТУРА
- 2.5.3. ФИЗИЧЕСКИЕ СВОЙСТВА АРЕНОВ
- 2.5.4. ПРОМЫШЛЕННОЕ ПРОИЗВОДСТВО АРЕНОВ
- 2.5.5. ЦИКЛОТРИМЕРИЗАЦИЯ АЦЕТИЛЕНОВ
- 2.5.6. РЕАКЦИИ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ АРЕНОВ
- 2.5.6.1. Механизм ароматического нитрования [15]
- 2.5.6.2. Кинетические изотопные эффекты [21]
- 2.5.6.3. Реакции, включающие ипсо-протонирование
- 2.5.6.4. Металлирование
- 2.5.6.5. Электрофилы IV группы
- 2.5.6.6. Электрофилы V группы
- 2.5.6.7. Электрофилы VI группы [18, 56]
- 2.5.6.8. Электрофилы VII группы [18, 25а, 56]
- 2.5.7. ОРИЕНТАЦИЯ В РЕАКЦИЯХ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ
- 2.5.8. РАДИКАЛЬНОЕ ГАЛОГЕНИРОВАНИЕ АРЕНОВ В БОКОВУЮ ЦЕПЬ [96]
- 2.5.9. РЕАКЦИИ ПРИСОЕДИНЕНИЯ К АРЕНАМ
- 2.5.9.1. Восстановление аренов
- 2.5.9.2. Термическое циклоприсоединение к аренам
- 2.5.9.3. Фотоциклоприсоединение к моноциклическим аренам [126]
- 2.5.9.4. Фотохимические реакции полициклических аренов
- 2.6.10. ФОТОИЗОМЕРИЗАЦИЯ АРЕНОВ [126б]
- 2.5.11. ОКИСЛЕНИЕ АРЕНОВ [153]
- 2.5.12. РЕАКЦИИ АРЕНОВ С СИНГЛЕТНЫМ КИСЛОРОДОМ [162]
- 2.5.13. ПРИГОТОВЛЕНИЕ БИ- И ПОЛИАРИЛОВ
- 2.5.14. ВНУТРИМОЛЕКУЛЯРНАЯ ФОТОЦИКЛИЗАЦИЯ, ПРИВОДЯЩАЯ К ПОЛИЦИКЛИЧЕСКИМ АРЕНАМ
- 2.5.15. ВНУТРИМОЛЕКУЛЯРНАЯ ЦИКЛИЗАЦИЯ ДИЗАМЕЩЕННЫХ АРЕНОВ
- 2.5.16. ЦИКЛОФАНЫ
- 2.5.17. КОНФОРМАЦИЯ И ХИРАЛЬНОСТЬ АРЕНОВ
- 2.5.18. АЗУЛЕНЫ И НЕБЕНЗОИДНЫЕ АРЕНЫ
- 2.6. АННУЛЕНЫ И РОДСТВЕННЫЕ СИСТЕМЫ
- 2.6.2. МЕТОДЫ СИНТЕЗА
- 2.6.2.1. Окислительное сочетание терминальных ацетиленов (метод Зондхеймера)
- 2.6.2.2. Фотооблучение полициклических валентных таутомеров
- 2.6.2.3. Валентная таутомерия типа норкарадиен — циклогептатриен (метод Фогеля)
- 2.6.2.4. Прочие методы
- 2.6.3. СВОЙСТВА АННУЛЕНОВ
- 2.6.4. СВОЙСТВА 4n-АННУЛЕНОВ
- 2.6.5. ДЕГИДРОАННУЛЕНЫ
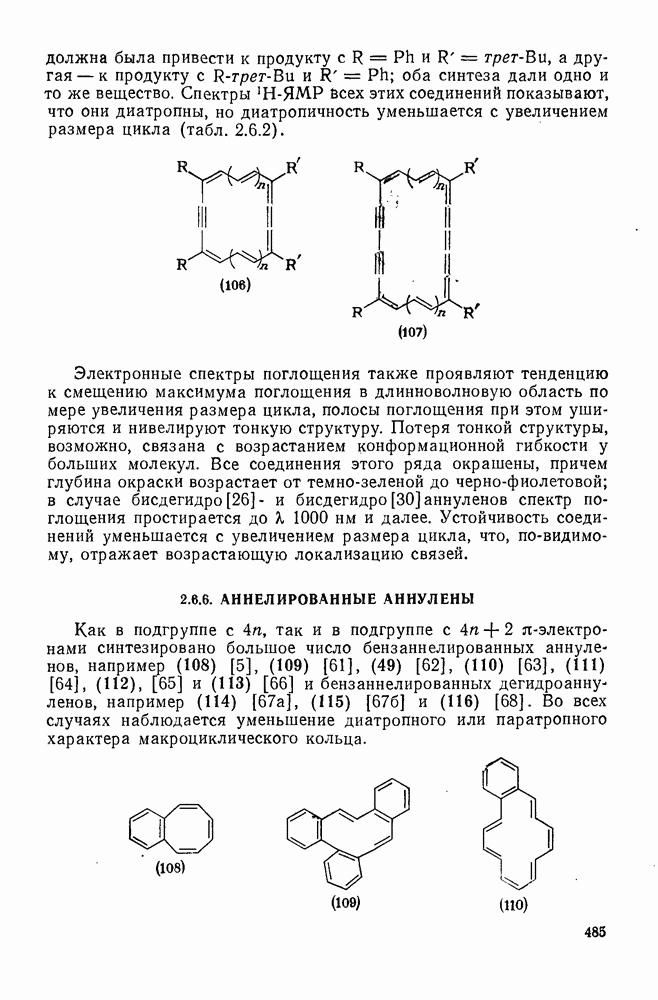
- 2.6.6. АННЕЛИРОВАННЫЕ АННУЛЕНЫ
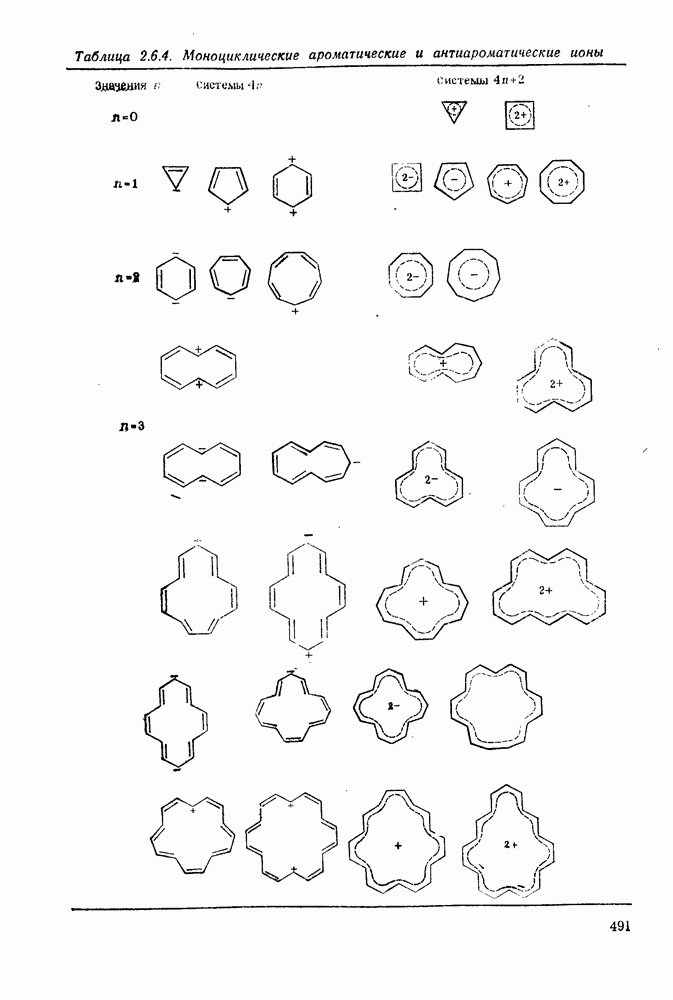
- 2.6.7. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ МОНОЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.8. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ ПОЛИЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.9. ГОМОАРОМАТИЧЕСКИЕ СИСТЕМЫ
- 2.7. КАРБОКАТИОНЫ И КАРБАНИОНЫ
- 2.7.1.2. Краткий исторический очерк развития химии карбокатионов
- 2.7.1.3. Методы генерации карбокатионов
- 2.7.1.4. Типы карбокатионов
- 2.7.1.5. Изучение карбокатионов: методы и результаты
- 2.7.1.6. Реакции карбокатионов
- 2.7.2. КАРБАНИОНЫ
- 2.7.2.2. Методы генерации карбанионов
- 2.7.2.3. Типы карбанионов
- 2.7.2.4. Физические свойства карбанионов
- 2.7.5.2. Реакции карбанионов
- 2.8. РАДИКАЛЫ, КАРБЕНЫ, АРИНЫ
- 2.8.1. РАДИКАЛЫ
- 2.8.1.1. Структура, устойчивость и реакционная способность радикалов
- 2.8.1.2. Методы генерации и реакции радикалов
- 2.8.2. КАРБЕНЫ
- 2.8.2.1. Методы генерации карбенов и карбеноидов
- 2.8.2.2. Реакции карбенов
- 2.8.3. АРИНЫ
- 2.8.3.1. Структура и спектры аринов
- 2.8.3.2. Методы генерации аринов
- 2.8.3.3. Реакции аринов
- ЧАСТЬ 3. ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- 3.2. МЕТОДЫ ГАЛОГЕНИРОВАНИЯ
- 3.2.1. Гомолитическое замещение водорода
- 3.2.1.2. Использование галогенпроизводных в качестве реагентов
- 3.2.2. Гомолитическое замещение функциональных групп
- 3.2.3. Гомолитическое присоединение к ненасыщенным системам
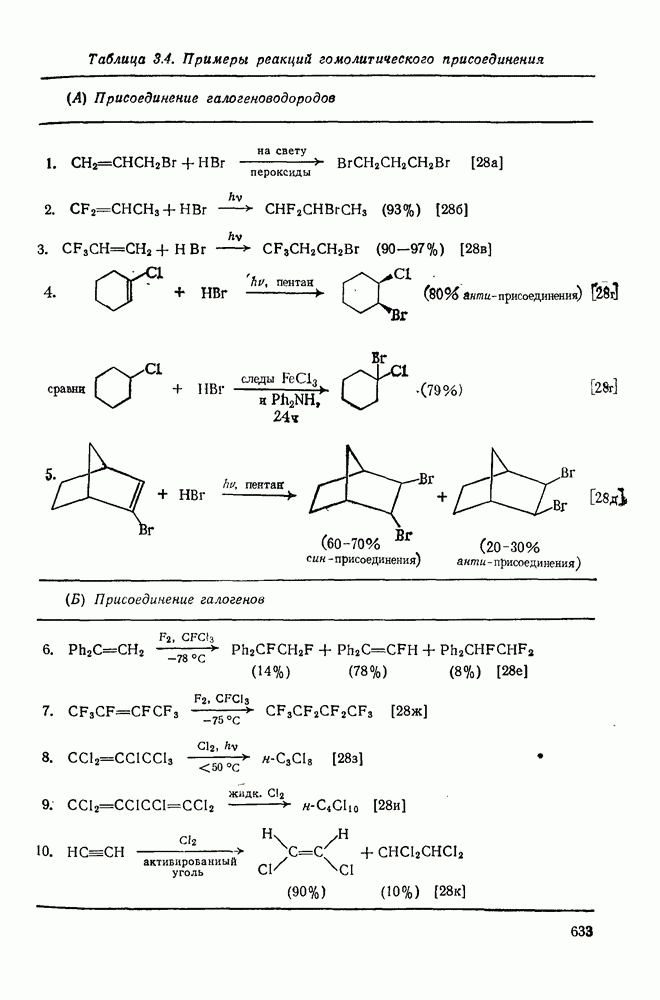
- 3.2.3.1. Присоединение галогеноводородов
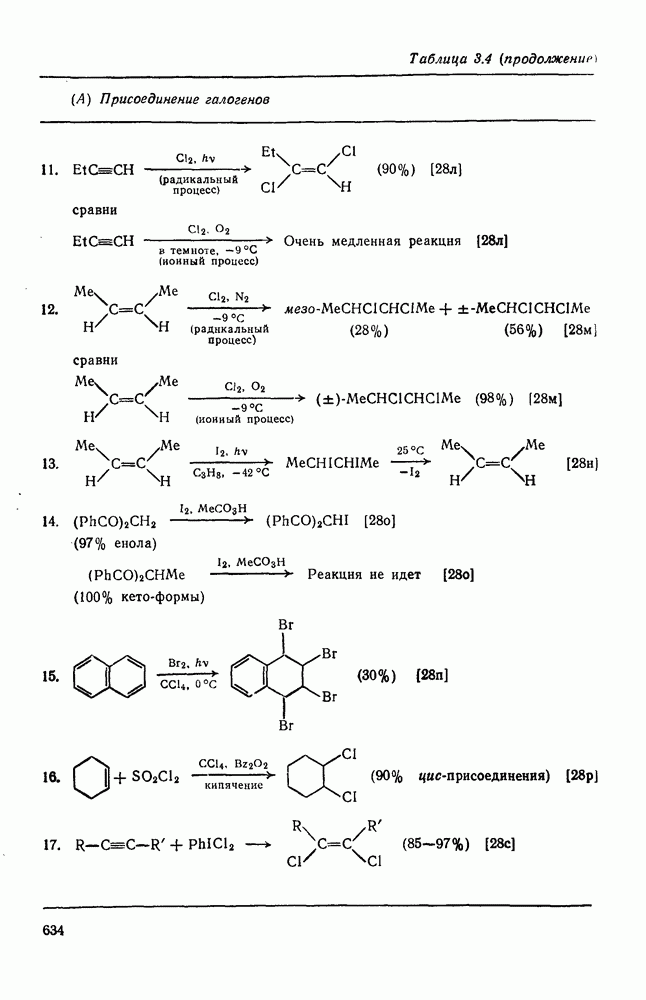
- 3.2.3.2. Присоединение галогенов
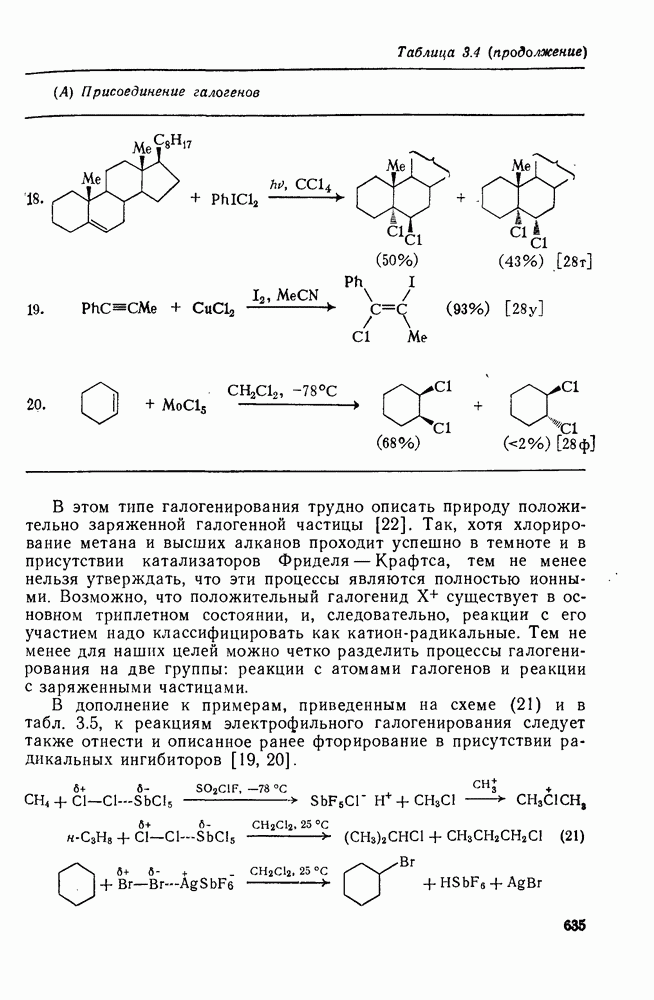
- 3.2.4. Электрофильное галогенирование
- 3.2.4.1. Замещение у насыщенной связи С-Н
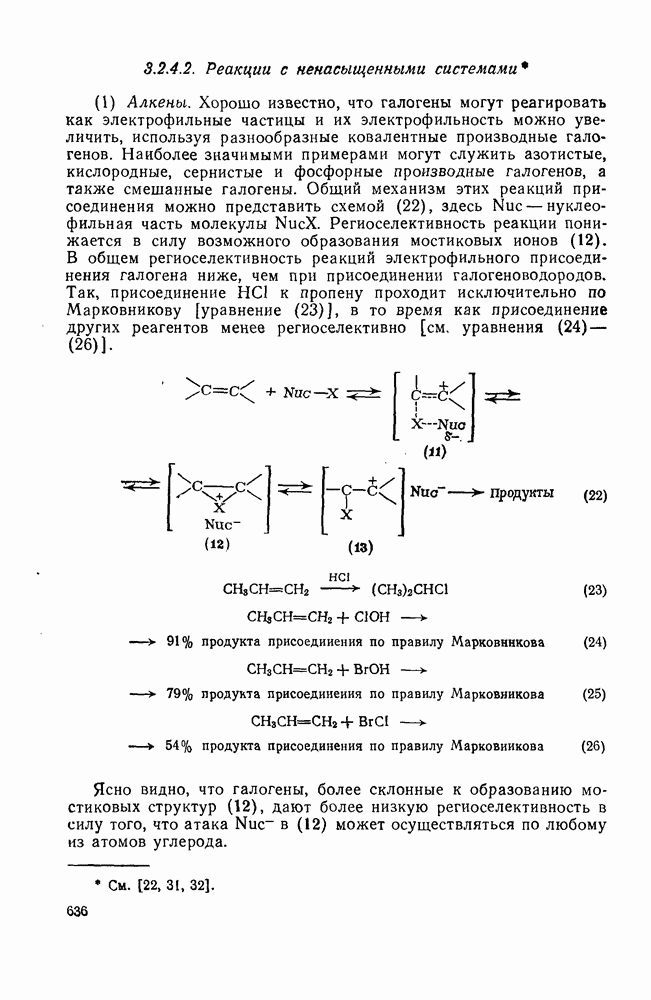
- 3.2.4.2. Реакции с ненасыщенными системами
- 3.2.4.3. Реакции с карбанионами
- 3.2.5. Нуклеофильное галогенирование
- 3.2.5.1. Галогенирование с замещением функциональной группы
- 3.2.5.2. Галогенирование в ароматических системах
- 3.2.5.3. Галогенирование путем обмена галогенов
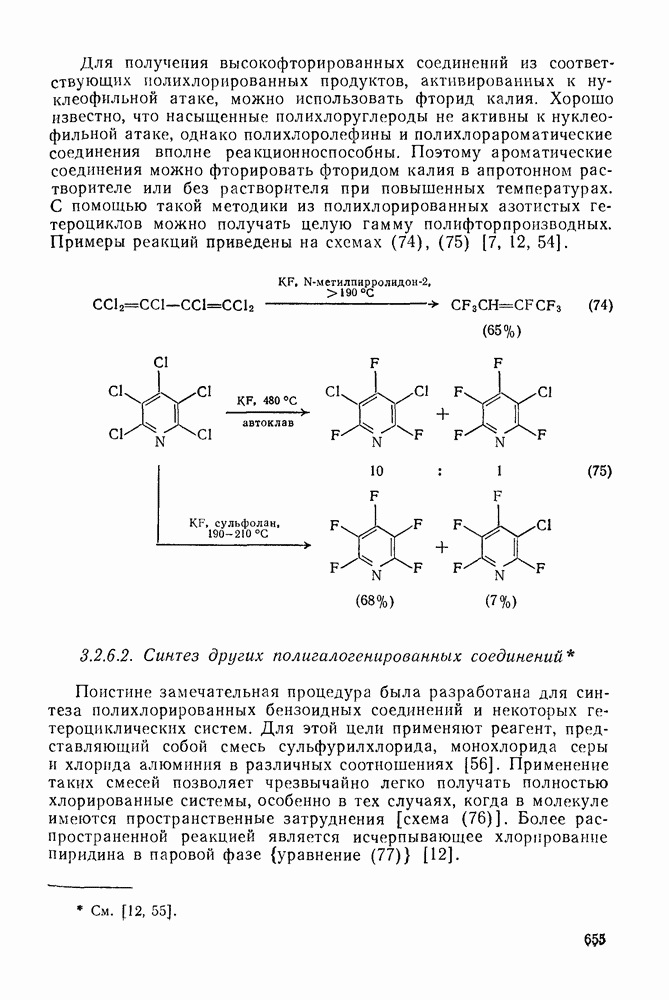
- 3.2.6. Синтез полигалогенированных соединений
- 3.2.6.1. Синтез полифторированных соединений
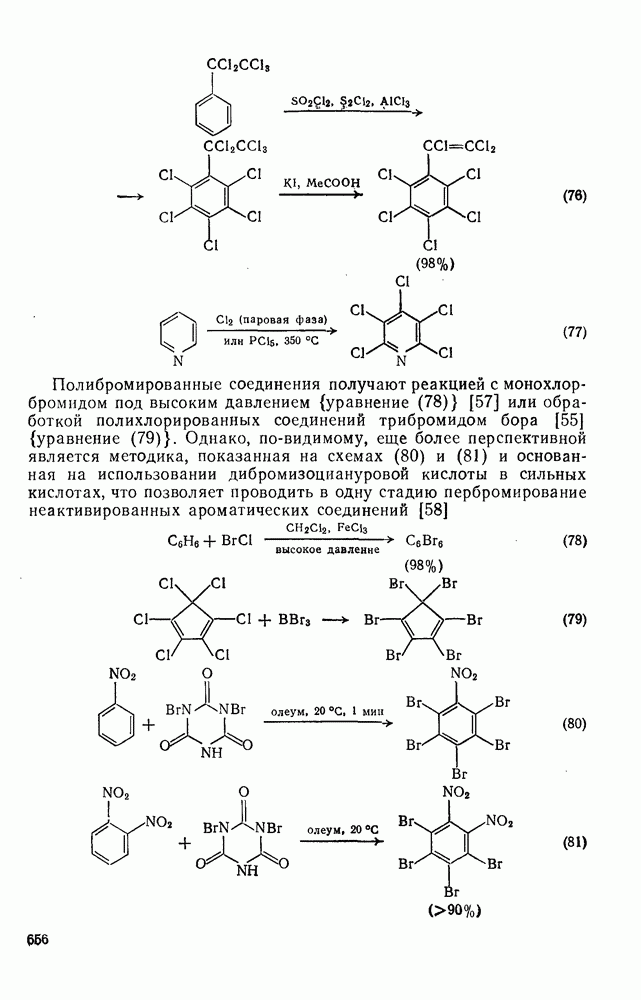
- 3.2.6.2. Синтез других полигалогенированных соединений
- 3.3. ГАЛОГЕНАЛКАНЫ
- 3.3.1. Характеристика связей углерод-галоген
- 3.3.2. Промышленное применение
- 3.3.3. Нуклеофильное замещение галогена
- 3.3.3.1. Реакции SN2 и родственные процессы
- 3.3.3.2. Соучастие соседних групп
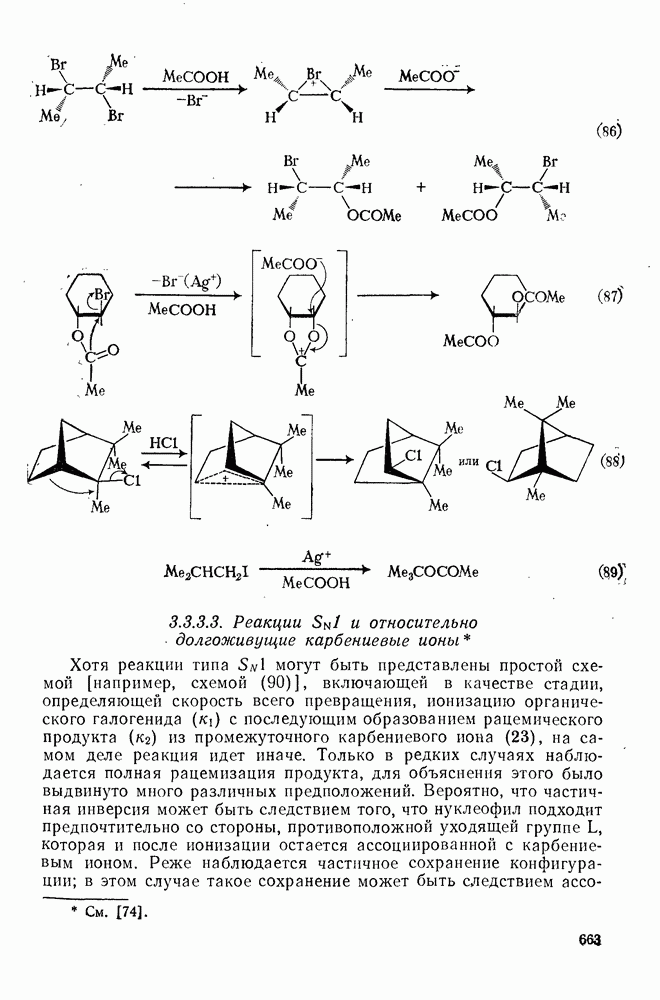
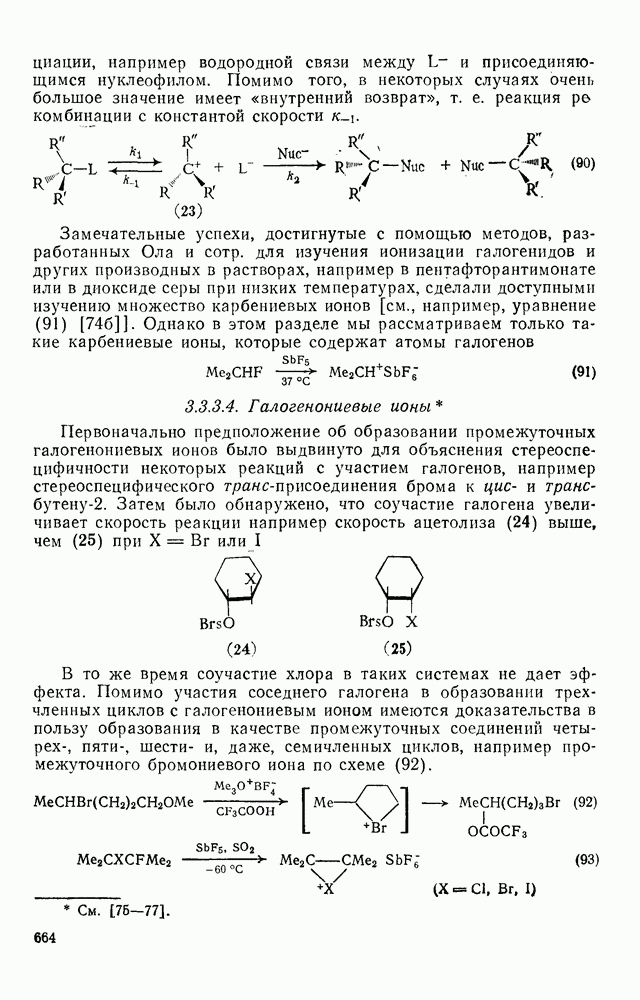
- 3.3.3.3. Реакции SN1 и относительно долгоживущие карбениевые ионы
- 3.3.3.4. Галогенониевые ионы
- 3.3.3.5. Галогенсодержащие карбениевые ионы
- 3.3.3.6. Механизм замещения с переносом электрона
- 3.3.4. Восстановление
- 3.3.5. Замещение на металлы
- 3.3.6. Элиминирование
- 3.3.6.1. b-Элиминирование
- 3.3.6.2. Галогенкарбанионы
- 3.3.6.3. Элиминирование через карбанионы
- 3.3.6.4. b-Элиминирование из металлорганических соединений
- 3.3.6.5. a-Элиминирование (генерирование карбенов)
- 3.4. ГАЛОГЕНАЛКЕНЫ
- 3.4.1. Синтез галогеналкенов
- 3.4.2. Нуклеофильная атака
- 3.4.2.1. Реакции, индуцируемые фторид-ионом
- 3.4.2.2. Другие реакции замещения
- 3.4.3. Радикальное присоединение
- 3.4.4. Электрофильное присоединение
- 3.4.5. Циклоприсоединение
- 3.4.5.1. [2+2]-Циклоприсоединение
- 3.4.5.2. [4+2]-Циклоприсоединение
- 3.5. ГАЛОГЕНАЛКИНЫ
- 3.6. ГАЛОГЕНАРЕНЫ
- 3.6.1. Замещение галогена
- 3.6.1.2. Присоединение-элиминирование
- 3.6.1.3. Нуклеофильная атака на галоген
- 3.6.1.4. Перенос электрона
- 3.6.2. Перегруппировки
- 3.6.2.1. Перегруппировки под действием кислот Льюиса
- 3.6.2.2. Образование валентных изомеров