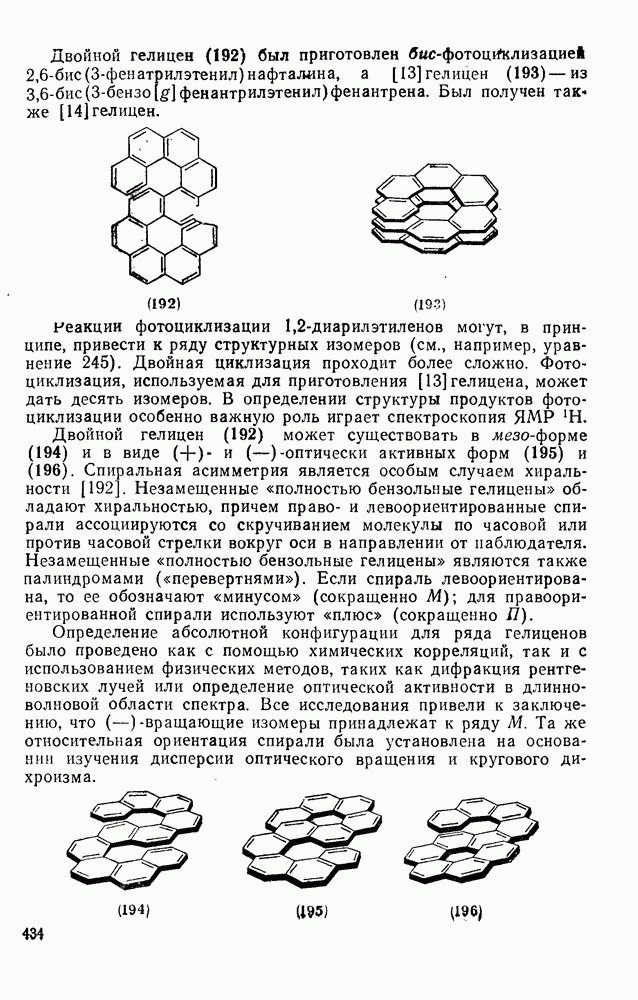
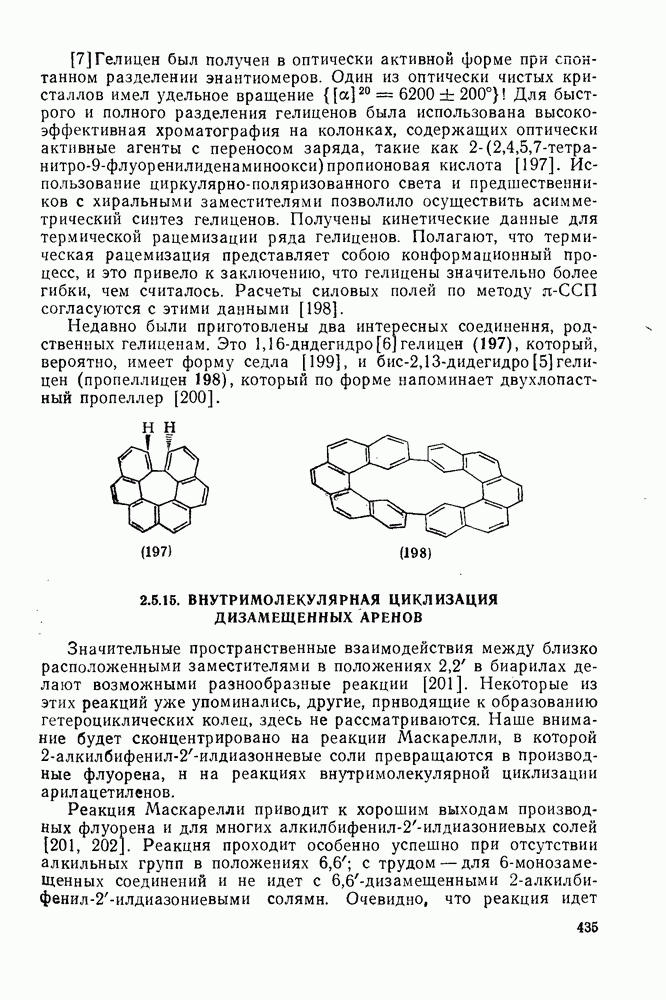
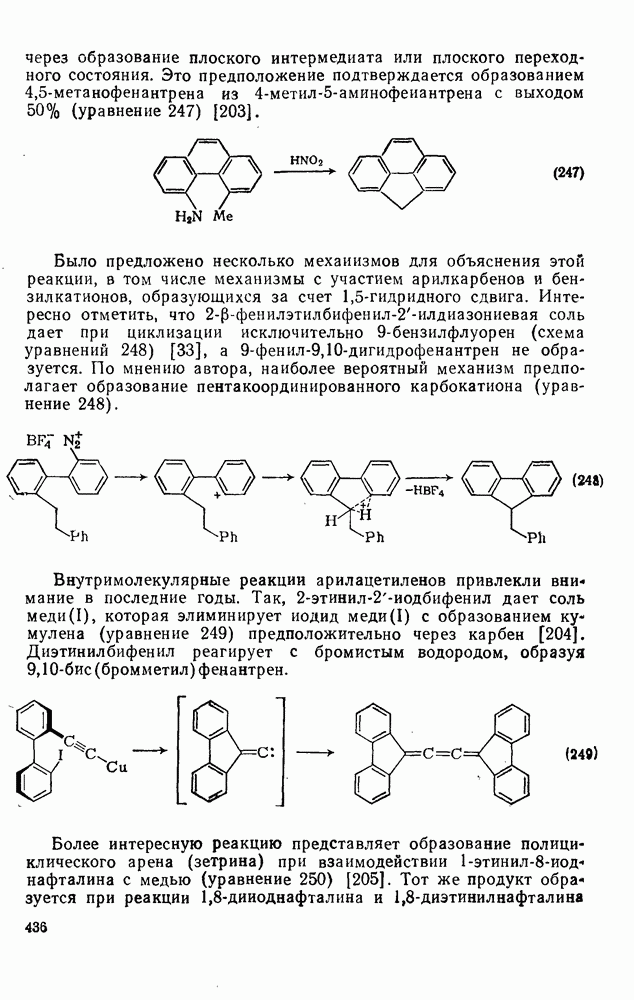
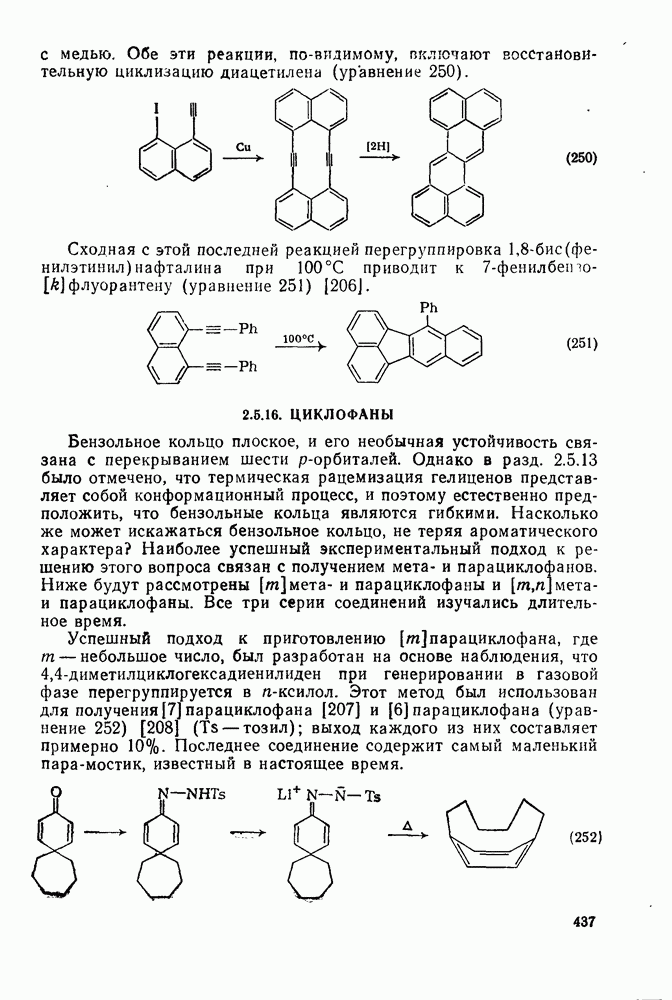
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
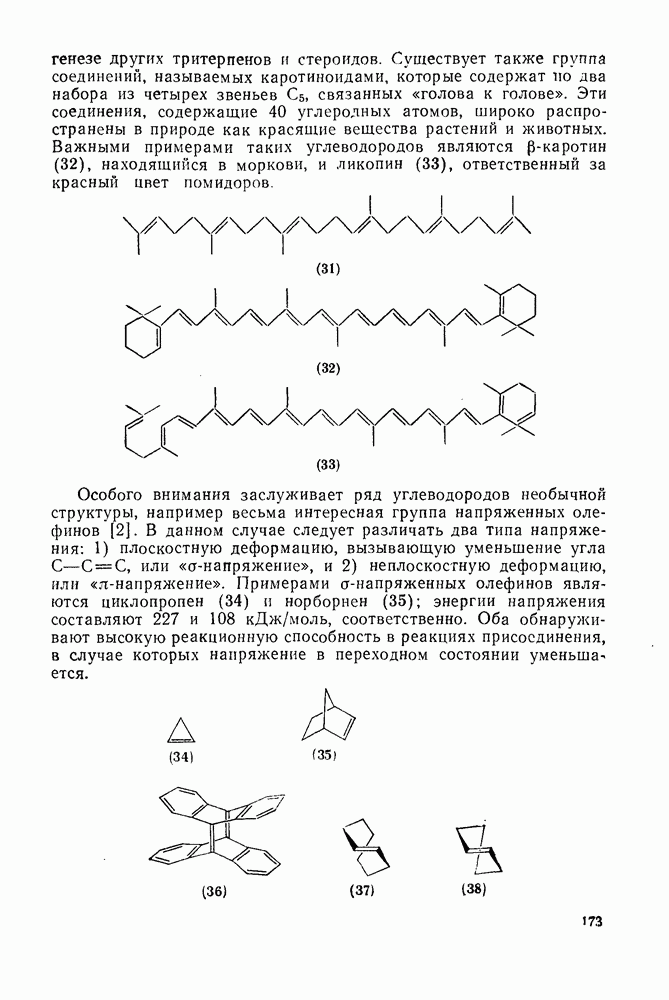
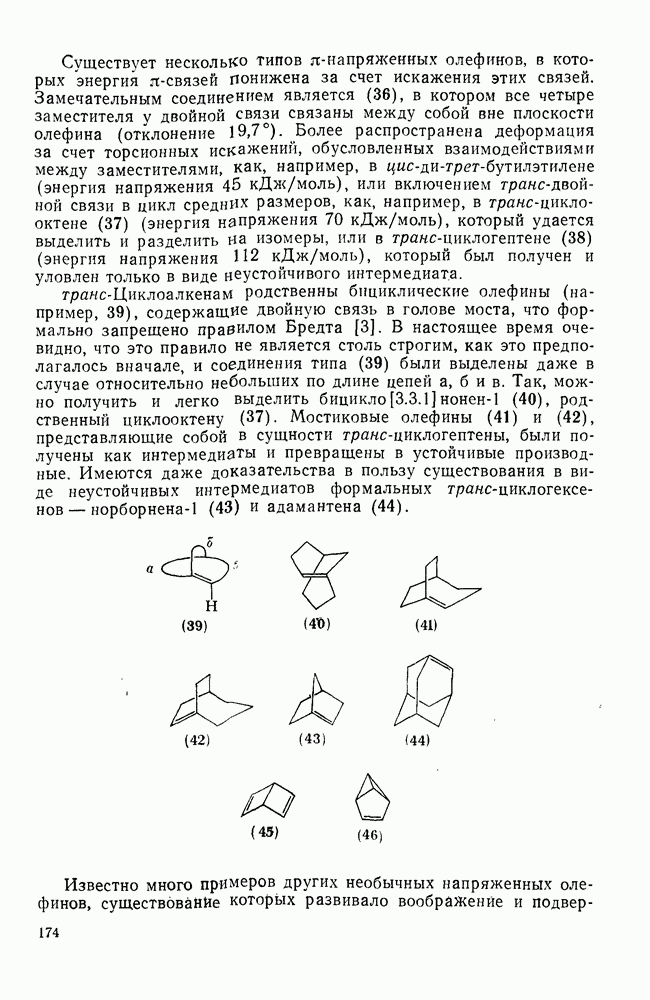
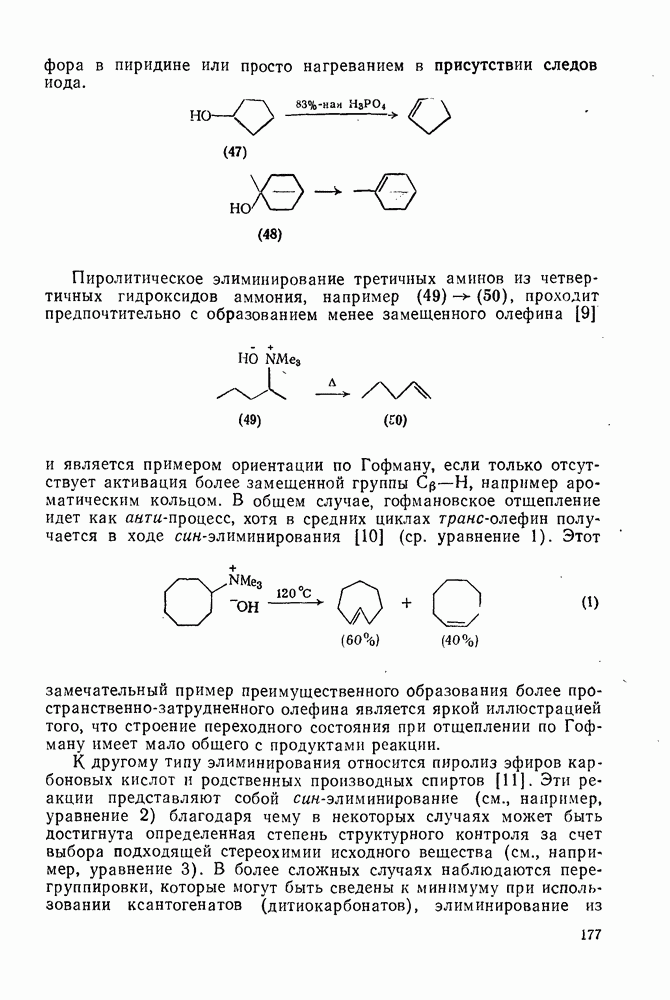
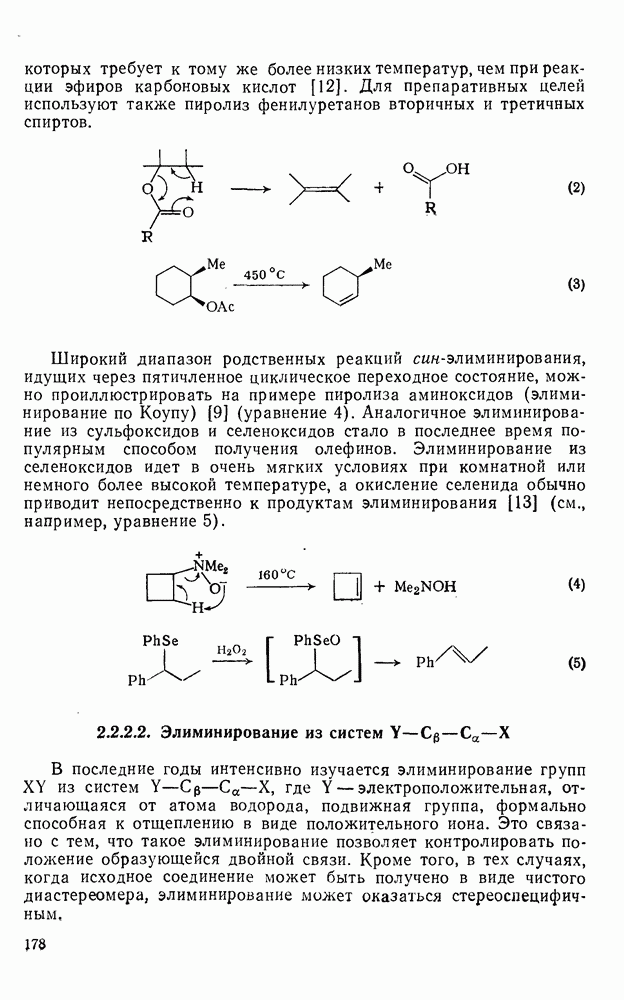
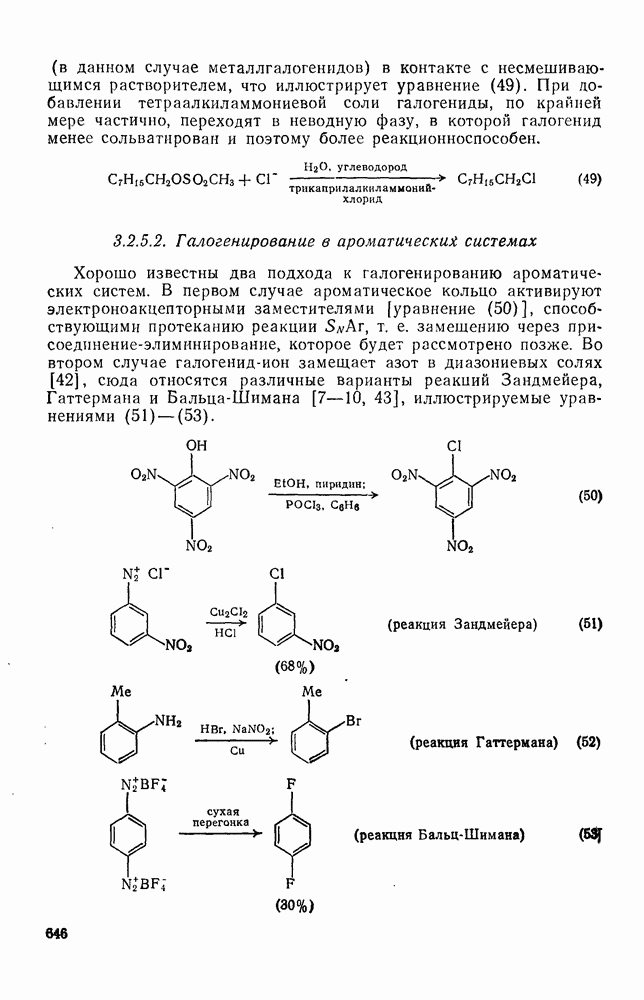
2.1.5.2. Алкил- и полиалкилциклогексаны
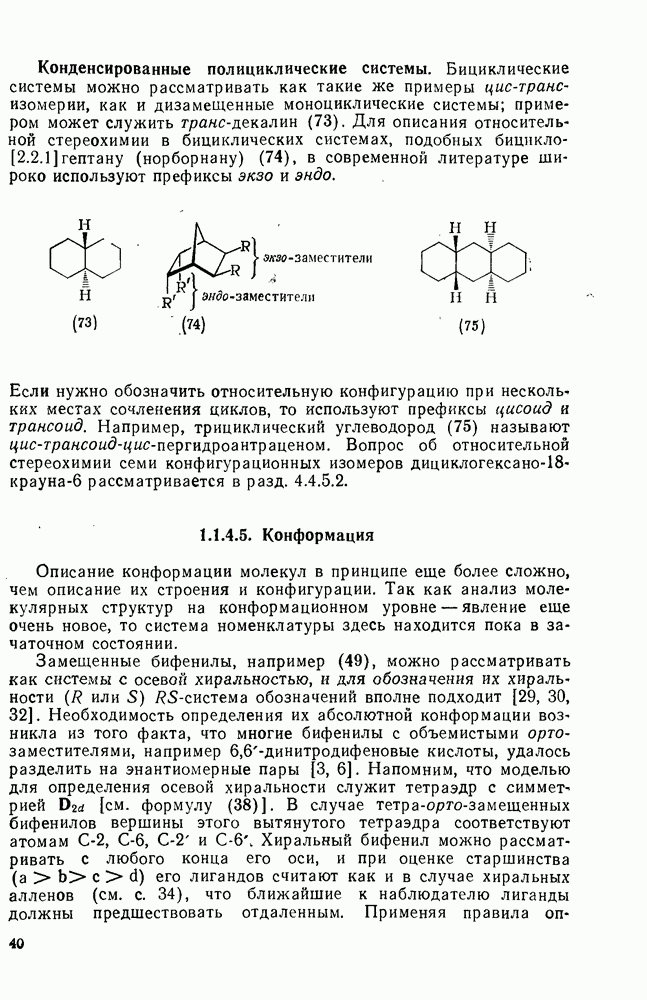
В процессе инверсии кольца циклогексана все экваториальные С—Н-связи становятся аксиальными, а все аксиальные С—Н-связи становятся экваториальными. В исходной системе это изменение вырождено, однако в замещенных циклогексанах оно имеет важные конформационные последствия.
Замещение в циклогексановом кольце не влияет существенно на скорость инверсии конформации, однако оно влияет на распределение в равновесии альтернативных форм кресла, которые не являются больше идентичными. Разницу в энергиях конформаций замещенных циклогексанов, как и кинетику инверсии кольца, можно определить различными физическими методами [21 в]. Как для термодинамических, так и для кинетических исследований особую ценность представляет ЯМР-спектроскопия [36].
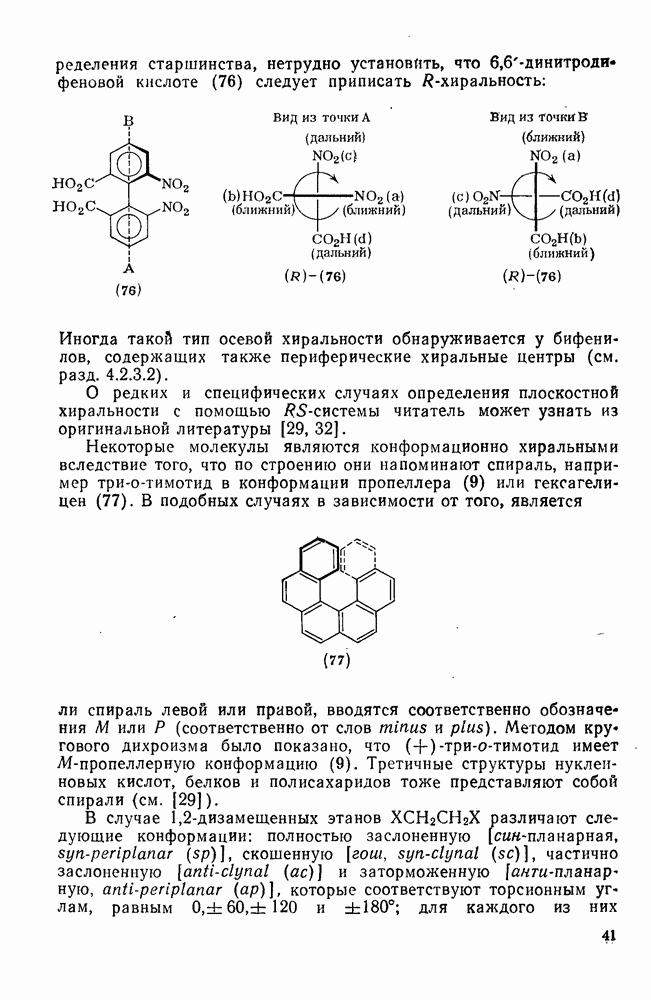
Метилциклогексан может существовать либо в конформации с экваториальным заместителем, либо в конформации с аксиальным заместителем, обе конформации находятся в быстро устанавливающемся равновесии между собой. Константа равновесия соответствует содержанию в смеси  экваториального и
экваториального и  аксиального метилциклогексанов; свободная энергия перехода
аксиального метилциклогексанов; свободная энергия перехода  , равна
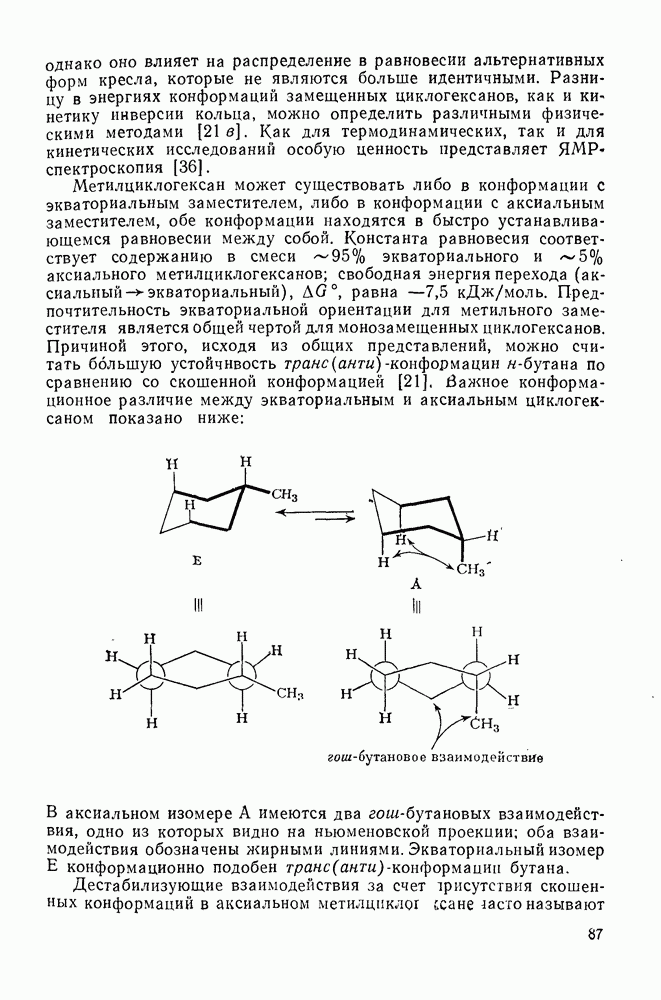
, равна  . Предпочтительность экваториальной ориентации для метильного заместителя является общей чертой для монозамещенных циклогексанов. Причиной этого, исходя из общих представлений, можно считать большую устойчивость транс(анти)-конформации н-бутана по сравнению со скошенной конформацией [21]. Важное конформационное различие между экваториальным и аксиальным циклогексаном показано ниже:
. Предпочтительность экваториальной ориентации для метильного заместителя является общей чертой для монозамещенных циклогексанов. Причиной этого, исходя из общих представлений, можно считать большую устойчивость транс(анти)-конформации н-бутана по сравнению со скошенной конформацией [21]. Важное конформационное различие между экваториальным и аксиальным циклогексаном показано ниже:

В аксиальном изомере А имеются два гош-бутановых взаимодействия, одно из которых видно на ньюменовской проекции; оба взаимодействия обозначены жирными линиями. Экваториальный изомер Е конформационно подобен транс(анти)-конформации бутана.
Дестабилизующие взаимодействия за счет присутствия скошенных конформаций в аксиальном метилциклогексане часто называют  -диаксиальными взаимодействиями или взаимодействиями через кольцо.
-диаксиальными взаимодействиями или взаимодействиями через кольцо.
Более четко эти взаимодействия представлены ниже:

Когда атомы водорода метильной группы находятся в заторможенном положении по отношению к группам у атома углерода, к которому присоединена метильная группа, то один из водородов должен обязательно располагаться над кольцом, сближаясь с син-аксиальными атомами водорода в положениях 3 и 5 на расстояние  . Такие взаимодействия не возникают в экваториальном изомере. Поскольку в аксиальном метилциклогексане имеются два гош-бутановых взаимодействия, разница в энергии аксиального и экваториального изомеров должна быть равна удвоенному значению разницы энергии для гош- и анти-бутанов, т. е. около
. Такие взаимодействия не возникают в экваториальном изомере. Поскольку в аксиальном метилциклогексане имеются два гош-бутановых взаимодействия, разница в энергии аксиального и экваториального изомеров должна быть равна удвоенному значению разницы энергии для гош- и анти-бутанов, т. е. около  . Это хорошо согласуется с большинством экспериментальных данных [21 в]; так, например, эта величина, определенная в работе [37], составляет
. Это хорошо согласуется с большинством экспериментальных данных [21 в]; так, например, эта величина, определенная в работе [37], составляет  . Расчеты, основанные на молекулярной механике и теории молекулярных орбиталей, также приводят примерно к этим значениям [33, 34, 38].
. Расчеты, основанные на молекулярной механике и теории молекулярных орбиталей, также приводят примерно к этим значениям [33, 34, 38].
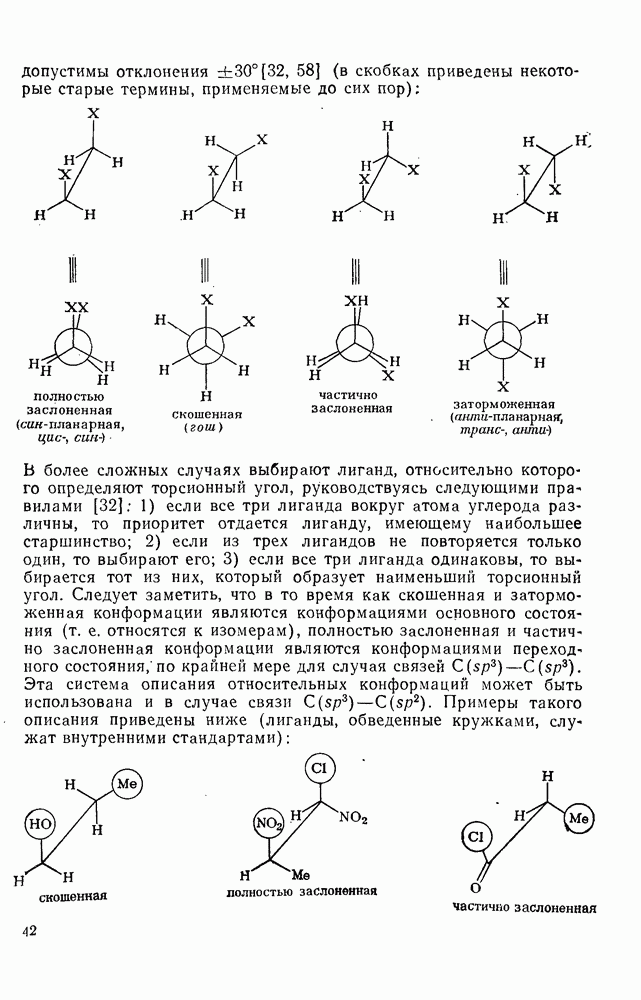
При анализе дестабилизующих взаимодействий в алкилцикло-гексанах обычно значительно проще учитывать  -диаксиальные взаимодействия, чем гош-бутановые взаимодействия; преимущество такого подхода и в том, что при рассмотрении заместителей, иных, чем метил, он позволяет принимать во внимание размеры заместителя, участвующего во взаимодействии. Разница в свободной энергии аксиальной и экваториальной форм ряда алкилциклогексанов указывает на то, что размеры и природа замещающей группы играют важную роль: для этнлциклогексана эта разница почти не отличается от разницы для метилциклогексана; в случае изопропилциклогексана она несколько выше (около 9
-диаксиальные взаимодействия, чем гош-бутановые взаимодействия; преимущество такого подхода и в том, что при рассмотрении заместителей, иных, чем метил, он позволяет принимать во внимание размеры заместителя, участвующего во взаимодействии. Разница в свободной энергии аксиальной и экваториальной форм ряда алкилциклогексанов указывает на то, что размеры и природа замещающей группы играют важную роль: для этнлциклогексана эта разница почти не отличается от разницы для метилциклогексана; в случае изопропилциклогексана она несколько выше (около 9  ), а для трет-бутилциклогексана — не менее
), а для трет-бутилциклогексана — не менее  . Сходство между метильной, этильной и изопропильными группами отражает то обстоятельство, что вращение вокруг связи между заместителем и кольцом позволяет придать молекуле ту конформацию, при которой влияние дополнительных метильных заместителей в этильной и изопропильной группах сводится к минимальному [21 в]. Однако аксиальная трет-бутильная группа вступает в сильное отталкивающее ван-дер-ваальсово взаимодействие с син-аксиальными водородными атомами, которое не может быть уменьшено за счет вращения вокруг связи, соединяющей кольцо с заместителем. Разница в энергиях аксиального и экваториального тре-бутилциклогексана близка к разнице энергий между конформациями кресла и искаженной ванны (твист-конформация) циклогексана, поэтому любые определения равновесия могут осложняться присутствием конформаций, отличных от кресла [39].
. Сходство между метильной, этильной и изопропильными группами отражает то обстоятельство, что вращение вокруг связи между заместителем и кольцом позволяет придать молекуле ту конформацию, при которой влияние дополнительных метильных заместителей в этильной и изопропильной группах сводится к минимальному [21 в]. Однако аксиальная трет-бутильная группа вступает в сильное отталкивающее ван-дер-ваальсово взаимодействие с син-аксиальными водородными атомами, которое не может быть уменьшено за счет вращения вокруг связи, соединяющей кольцо с заместителем. Разница в энергиях аксиального и экваториального тре-бутилциклогексана близка к разнице энергий между конформациями кресла и искаженной ванны (твист-конформация) циклогексана, поэтому любые определения равновесия могут осложняться присутствием конформаций, отличных от кресла [39].
Аллинджер [40] выразил сомнение в том, что  -аксиальные взаимодействия являются главной причиной относительной неустойчивости аксиальных конформаций, и выдвинул другое возможное объяснение, в котором сделан упор на пространственное окружение не аксиальных заместителей, а экваториального агома водорода, связанного с углеродным атомом, несущим заместитель. В сущности это объяснение сводится к тому, что неустойчивость аксиальной конформации обусловлена пространственными затруднениями между экваториальным третичным атомом водорода и ближайшими заместителями. Шлейер с сотр. [31] рассмотрели эту возможность с учетом структурных данных и молекулярно-механических расчетов и пришли к выводу, что такое объяснение неверно.
-аксиальные взаимодействия являются главной причиной относительной неустойчивости аксиальных конформаций, и выдвинул другое возможное объяснение, в котором сделан упор на пространственное окружение не аксиальных заместителей, а экваториального агома водорода, связанного с углеродным атомом, несущим заместитель. В сущности это объяснение сводится к тому, что неустойчивость аксиальной конформации обусловлена пространственными затруднениями между экваториальным третичным атомом водорода и ближайшими заместителями. Шлейер с сотр. [31] рассмотрели эту возможность с учетом структурных данных и молекулярно-механических расчетов и пришли к выводу, что такое объяснение неверно.
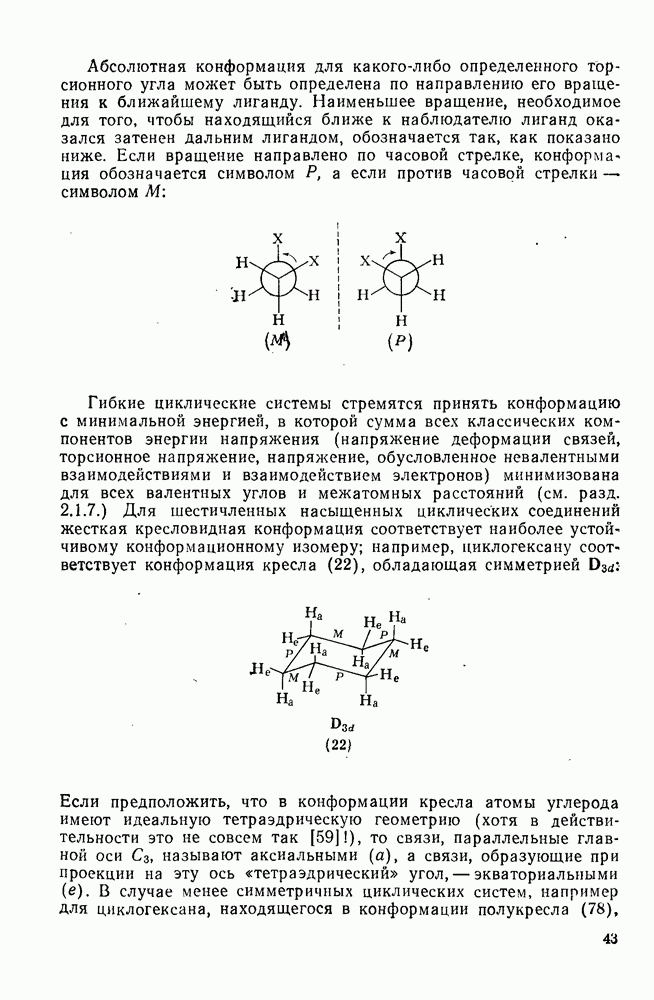
Конформационный анализ циклогексановых колец, несущих два и более алкильных заместителей, аналогичен описанному выше, за исключением того, что, когда заместители присоединены к различным углеродным атомам в кольце, следует рассматривать и конфигурационные взаимоотношения [21]. Если два неодинаковых заместителя связаны с одним и тем же атомом углерода, то при инверсии кольца аксиальные и экваториальные заместители меняются местами, и молекула стремится принять конформацию, в которой более крупный заместитель занимает экваториальное положение.
В системах, в которых заместители связаны с различными углеродными атомами, можно установить ряд стереохимических зависимостей, которые рассмотрены в настоящем разделе только на примере диметилциклогексанов в конформациях кресла;  , 1,3- и
, 1,3- и  -диметилциклогексаны могут существовать в цис- и транс-формах (т. е. как диастереомеры). Каждый из диастереомеров может существовать в двух конформациях кресла и соотношение между этими конформациями определяется расположением заместителей. транс-
-диметилциклогексаны могут существовать в цис- и транс-формах (т. е. как диастереомеры). Каждый из диастереомеров может существовать в двух конформациях кресла и соотношение между этими конформациями определяется расположением заместителей. транс-  -Диметилциклогексан может быть либо диэкваториальным (е, е), либо диаксиальным (а, а). В а, а-форме возможны четыре гош-бутановых взаимодействия, в то время как в е, е-форме — только одно.
-Диметилциклогексан может быть либо диэкваториальным (е, е), либо диаксиальным (а, а). В а, а-форме возможны четыре гош-бутановых взаимодействия, в то время как в е, е-форме — только одно.

В соответствии с этим разница в свободной энергии между а, а- и е, е-формами соствляет  , т. е.
, т. е.  , и в равновесии е, е-форма будет преобладать над а, а-формой. Обе конформации транс-
, и в равновесии е, е-форма будет преобладать над а, а-формой. Обе конформации транс- хиральны, и для каждой из них существует несовмещающее зеркальное изображение. Поэтому молекула существует в виде (
хиральны, и для каждой из них существует несовмещающее зеркальное изображение. Поэтому молекула существует в виде ( -пары, т. е. в рацемической модификации. В цис-
-пары, т. е. в рацемической модификации. В цис- в конформации кресла имеются один аксиальный и один экваториальный заместители (а, е). Инверсия кольца приводит к энергетически эквивалентному конформеру
в конформации кресла имеются один аксиальный и один экваториальный заместители (а, е). Инверсия кольца приводит к энергетически эквивалентному конформеру  . Молекула не обладает элементами симметрии. Хотя обе конформации кресла являются несовмещающимися зеркальными изображениями, молекула не проявляет оптической активности; дело в том, что потенциальный барьер конверсии кресло — кресло настолько низок, что в этом случае мы имеем дело с быстро инвертирующейся неразделимой (
. Молекула не обладает элементами симметрии. Хотя обе конформации кресла являются несовмещающимися зеркальными изображениями, молекула не проявляет оптической активности; дело в том, что потенциальный барьер конверсии кресло — кресло настолько низок, что в этом случае мы имеем дело с быстро инвертирующейся неразделимой ( -парой. В цис-
-парой. В цис- имеются три гош-бутановых взаимодействия. В соответствии с этим разница в энергиях цис- и транс-форм, равная энергии двух гош-бутановых взаимодействий, должна быть в пользу транс-формы. Экспериментально определенное изменение свободной энергии перехода цис-транс оказалось равным
имеются три гош-бутановых взаимодействия. В соответствии с этим разница в энергиях цис- и транс-форм, равная энергии двух гош-бутановых взаимодействий, должна быть в пользу транс-формы. Экспериментально определенное изменение свободной энергии перехода цис-транс оказалось равным  .
.
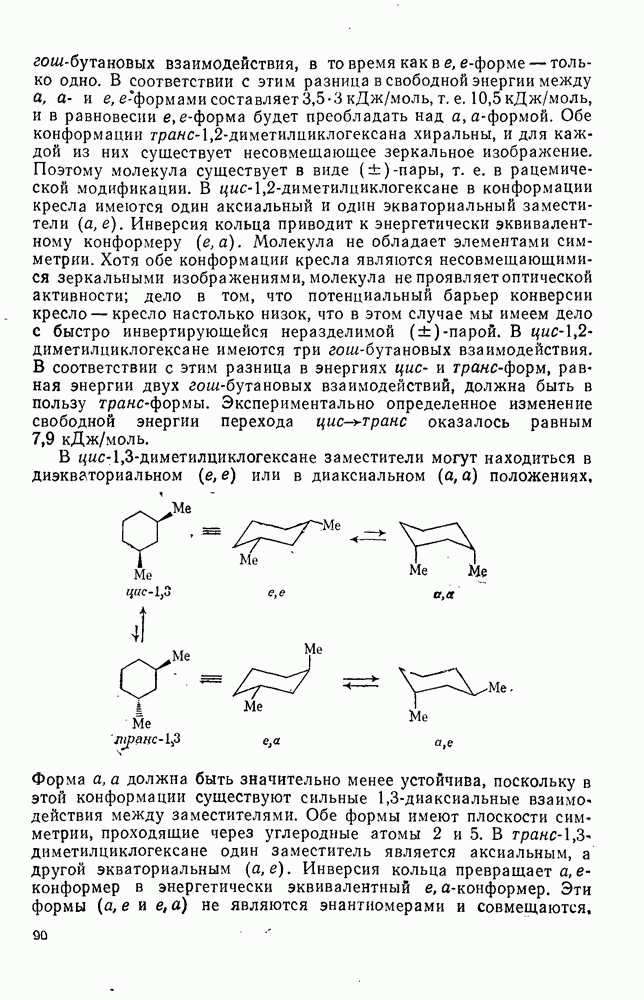
В цис- заместители могут находиться в диэкваториальном (е, е) или в диаксиальном (а, а) положениях,
заместители могут находиться в диэкваториальном (е, е) или в диаксиальном (а, а) положениях,

Форма а, а должна быть значительно менее устойчива, поскольку в этой конформации существуют сильные  -диаксиальные взаимодействия между заместителями. Обе формы имеют плоскости симметрии, проходящие через углеродные атомы 2 и 5. В транс-
-диаксиальные взаимодействия между заместителями. Обе формы имеют плоскости симметрии, проходящие через углеродные атомы 2 и 5. В транс- один заместитель является аксиальным, а другой экваториальным (а, е). Инверсия кольца превращает а, е-конформер в энергетически эквивалентный е, а-конформер. Эти формы (
один заместитель является аксиальным, а другой экваториальным (а, е). Инверсия кольца превращает а, е-конформер в энергетически эквивалентный е, а-конформер. Эти формы ( и
и  ) не являются энантиомерами и совмещаются.
) не являются энантиомерами и совмещаются.
Молекула не имеет плоскости симметрии, и  и (
и ( -формы способны к существованию. Поскольку в транс-
-формы способны к существованию. Поскольку в транс- имеются два гош-бутановых взаимодействия, а в цис-изомере в е, е-конформации такие взаимодействия отсутствуют, энергетическая разница должна составлять
имеются два гош-бутановых взаимодействия, а в цис-изомере в е, е-конформации такие взаимодействия отсутствуют, энергетическая разница должна составлять  экспериментально найденное значение
экспериментально найденное значение  для перехода цис-стране равно
для перехода цис-стране равно  .
.
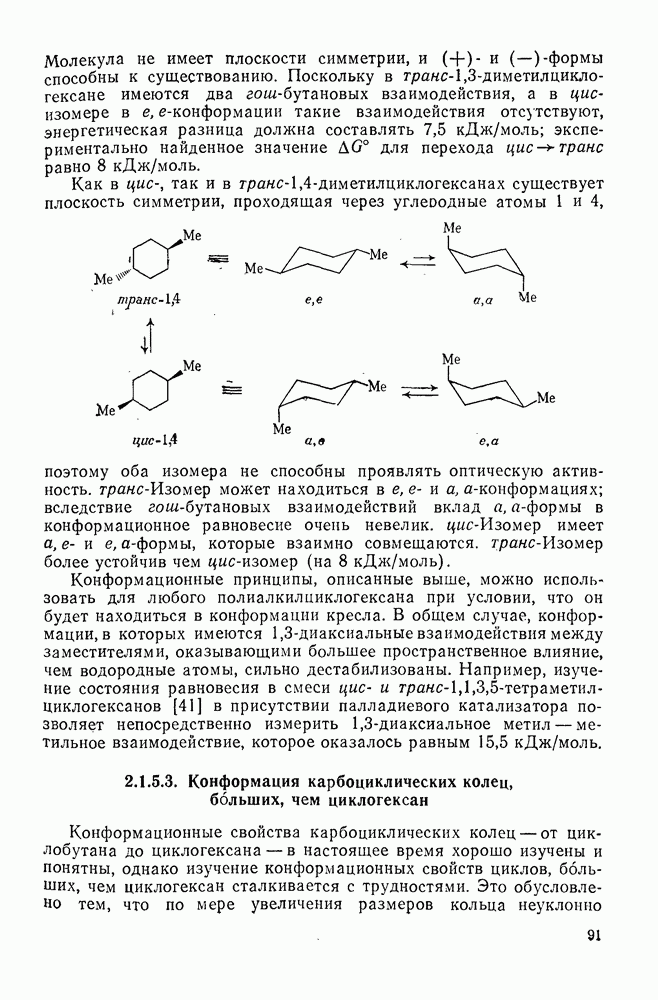
Как в  , так и в транс-
, так и в транс- существует плоскость симметрии, проходящая через углеродные атомы 1 и 4,
существует плоскость симметрии, проходящая через углеродные атомы 1 и 4,

поэтому оба изомера не способны проявлять оптическую активность. Транс-Изомер может находиться в е, е- и а, а-конформациях; вследствие гош-бутановых взаимодействий вклад а, а-формы в конформационное равновесие очень невелик. Цис-Изомер имеет а, е- и е, а-формы, которые взаимно совмещаются, транс-Изомер более устойчив чем цис-изомер (на 8  ).
).
Конформационные принципы, описанные выше, можно использовать для любого полиалкилциклогексана при условии, что он будет находиться в конформации кресла. В общем случае, конформации, в которых имеются  -диаксиальные взаимодействия между заместителями, оказывающими большее пространственное влияние, чем водородные атомы, сильно дестабилизованы. Например, изучение состояния равновесия в смеси цис- и транс-
-диаксиальные взаимодействия между заместителями, оказывающими большее пространственное влияние, чем водородные атомы, сильно дестабилизованы. Например, изучение состояния равновесия в смеси цис- и транс- в присутствии палладиевого катализатора позволяет непосредственно измерить
в присутствии палладиевого катализатора позволяет непосредственно измерить  -диаксиальное метил — метальное взаимодействие, которое оказалось равным
-диаксиальное метил — метальное взаимодействие, которое оказалось равным  .
.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- ИЗ ПРЕДИСЛОВИЯ К ТОМУ 1 АНГЛИЙСКОГО ИЗДАНИЯ
- ЧАСТЬ I. НОМЕНКЛАТУРА И СТЕРЕОХИМИЯ
- 1.1. ВВЕДЕНИЕ И СТЕРЕОХИМИЯ
- 1.1.2. СИММЕТРИЯ И ХИРАЛЬНОСТЬ
- 1.1.3. ХИМИЧЕСКАЯ ТОПОЛОГИЯ
- 1.1.4. ИЗОМЕРИЯ
- 1.1.4.2. Строение
- 1.1.4.3. Абсолютная конфигурация
- 1.1.4.4. Относительная конфигурация
- 1.1.4.5. Конформация
- 1.1.4.6. Концепция изомерии
- 1.1.5. ТОПИЗМ
- 1.1.5.2. Прохиральность
- 1.1.5.3. Псевдоасимметрия (псевдохиральность)
- 1.1.6. ТОПОМЕРИЯ
- 1.1.7. ДИНАМИЧЕСКАЯ СТЕРЕОХИМИЯ. КРАТКИЕ СВЕДЕНИЯ
- ЧАСТЬ 2. УГЛЕВОДОРОДЫ
- 2.1. НАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- 2.1.2. Строение и номенклатура
- 2.1.2.1. Номенклатура IUPAC
- 2.1.2.2. Алициклические алканы
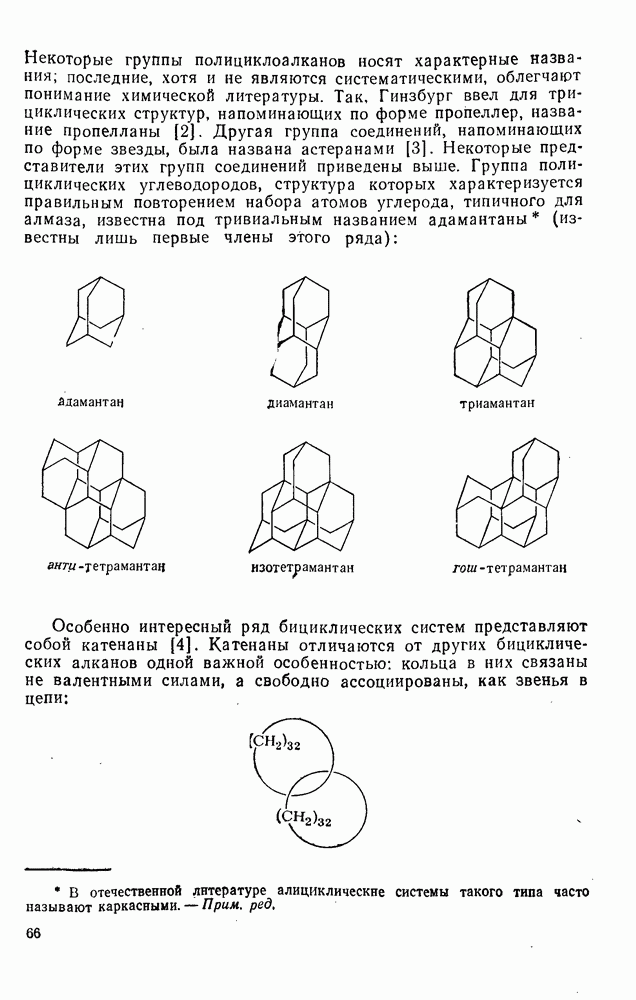
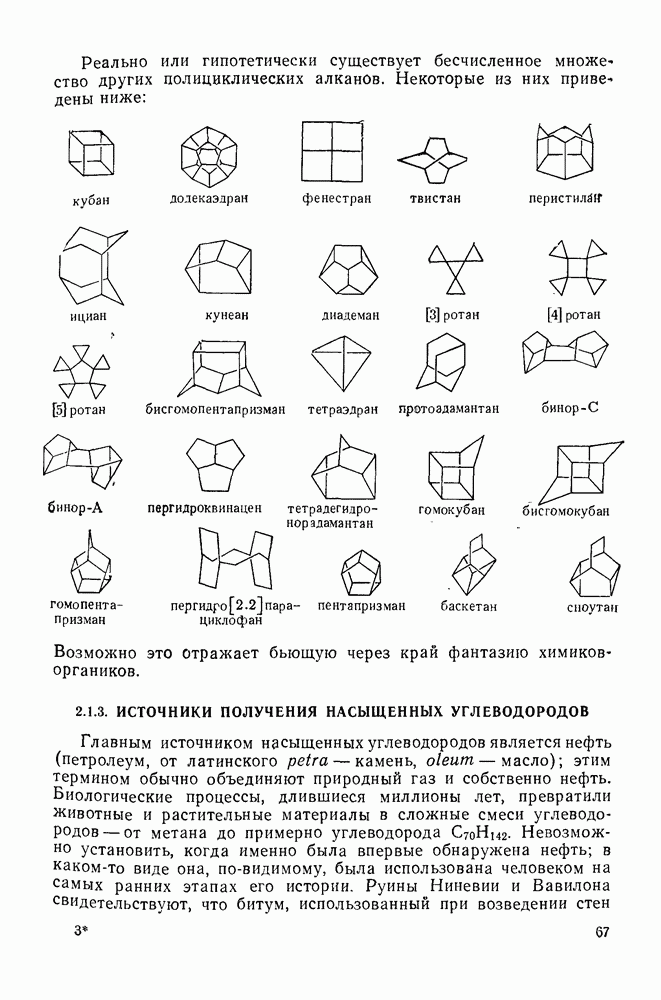
- 2.1.2.3. Полициклоалканы
- 2.1.3. ИСТОЧНИКИ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ УГЛЕВОДОРОДОВ
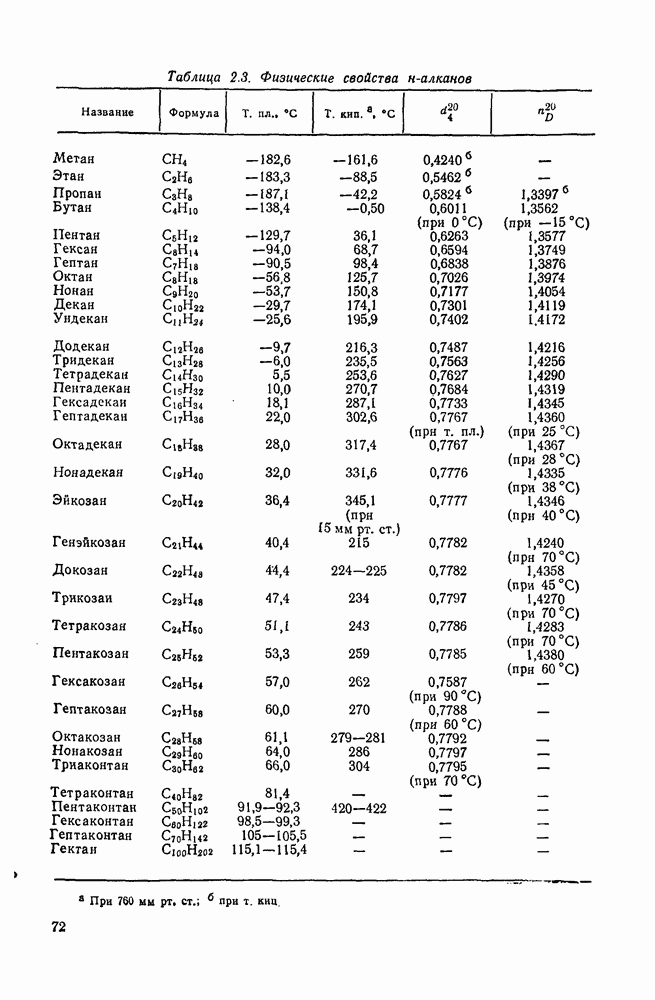
- 2.1.4. ФИЗИЧЕСКИЕ СВОЙСТВА
- 2.1.4.1. Ациклические алканы
- 2.1.4.2. Моно- и полициклоалканы
- 2.1.5. СТЕРЕОХИМИЯ И КОНФОРМАЦИОННЫЙ АНАЛИЗ
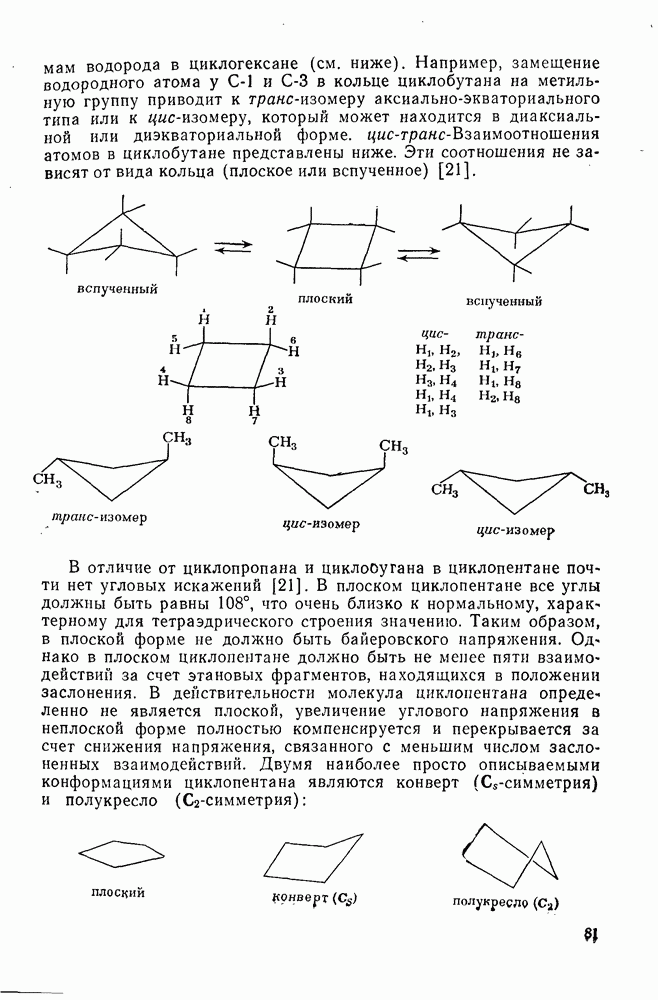
- 2.1.5.1. Углы и длины связей
- 2.1.5.2. Алкил- и полиалкилциклогексаны
- 2.1.5.3. Конформация карбоциклических колец, больших, чем циклогексан
- 2.1.6. ТЕРМОХИМИЧЕСКИЕ СВОЙСТВА
- 2.1.6.1. Горение. Алканы и циклоалканы как топливо
- 2.1.6.2. Определение теплот сгорания и термохимические свойства
- 2.1.6.3. Эмпирические методы оценки теплот образования алканов
- 2.1.6.4. Оценка теплот образования алканов на основе энергии связей
- 2.1.6.5. Оценка теплот образования алканов на основе инкрементов групп
- 2.1.6.6. Оценка теплот образования циклических, полициклических и мостиковых алканов на основе инкрементов «скошенных разобщенных» групп и «единственных» наиболее устойчивых конформаций
- 2.1.6.7. Молекулярно-механические расчеты теплот образования и энергии напряжения
- 2.1.6.8. Моно- и полициклоалкаиы
- 2.1.7. ПОЛУЧЕНИЕ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.7.1. Получение алканов восстановлением олефинов
- 2.1.7.2. Получение алканов из альдегидов и кетонов
- 2.1.7.3. Получение алканов из спиртов и алкилгалогенидов
- 2.1.7.4. Получение алканов из карбоновых кислот
- 2.1.8. СИНТЕЗ МОНО- И ПОЛИЦИКЛОАЛКАНОВ
- 2.1.9. РЕАКЦИИ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.9.1. Галогенирование
- 2.1.9.2. Нитрование
- 2.1.9.3. Окисление
- 2.1.9.4. Каталитическая изомеризация алканов
- 2.1.9.5. Каталитическое алкилирование алканов
- 2.1.9.6. Реакции крекинга алканов
- 2.1.9.7. Термический крекинг
- 2.1.9.8. Каталитический крекинг
- 2.1.9.9. Каталитический риформинг и дегидроциклизация алканов
- 2.1.10. РЕАКЦИИ ЦИКЛОАЛКАНОВ И ПОЛИЦИКЛОАЛКАНОВ
- 2.2. ОЛЕФИНОВЫЕ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.2.2. ПОЛУЧЕНИЕ ОЛЕФИНОВ
- 2.2.2.1. Элиминирование в системах
- 2.2.2.2. Элиминирование из систем
- 2.2.2.3. Циклоэлиминирование
- 2.2.2.4. Частичное восстановление
- 2.2.2.5. Элиминирование сульфонилгидразонов
- 2.2.2.6. Реакция Виттига и родственные ей реакции
- 2.2.2.7. Различные реакции конденсации
- 2.2.2.8. Электроциклические реакции
- 2.2.2.9. Циклоолигомеризация
- 2.2.2.11. Реакции винильных производных
- 2.2.3. РЕАКЦИИ ОЛЕФИНОВ
- 2.2.3.1. Электрофильное присоединение
- 2.2.3.2. Нуклеофильное присоединение
- 2.2.3.3. Радикальное присоединение
- 2.2.3.4. Циклоприсоединение и родственные реакции
- 2.2.3.5. Окисление
- 2.2.3.6. Восстановление
- 2.2.3.7. Перегруппировки
- 2.2.3.8. Фотохимические реакции
- 2.2.3.9. Прочие реакции
- 2.3. ДИЕНЫ, ПОЛНЕНЫ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.3.1. СОПРЯЖЕННЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.1.2. Получение сопряженных диенов
- 2.3.2. РЕАКЦИИ СОПРЯЖЕННЫХ ДИЕНОВ
- 2.3.2.2. Восстановление
- 2.3.2.3. Гидроборирование
- 2.3.2.4. Реакция Дильса — Альдера
- 2.3.2.5. Комплексы с карбонилами железа
- 2.3.2.6. Фотохимические термические реакции
- 2.3.2.7. Прочие реакции
- 2.3.3. СОПРЯЖЕННЫЕ ПОЛИЕНЫ
- 2.3.4. ПРИРОДНЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.5. АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.5.2. Получение алленов
- 2.3.6. РЕАКЦИИ АЛЛЕНОВ
- 2.3.6.2. Гидрирование
- 2.3.6.3. Реакции алленов в присутствии комплексов металлов
- 2.3.7. КУМУЛЕНЫ
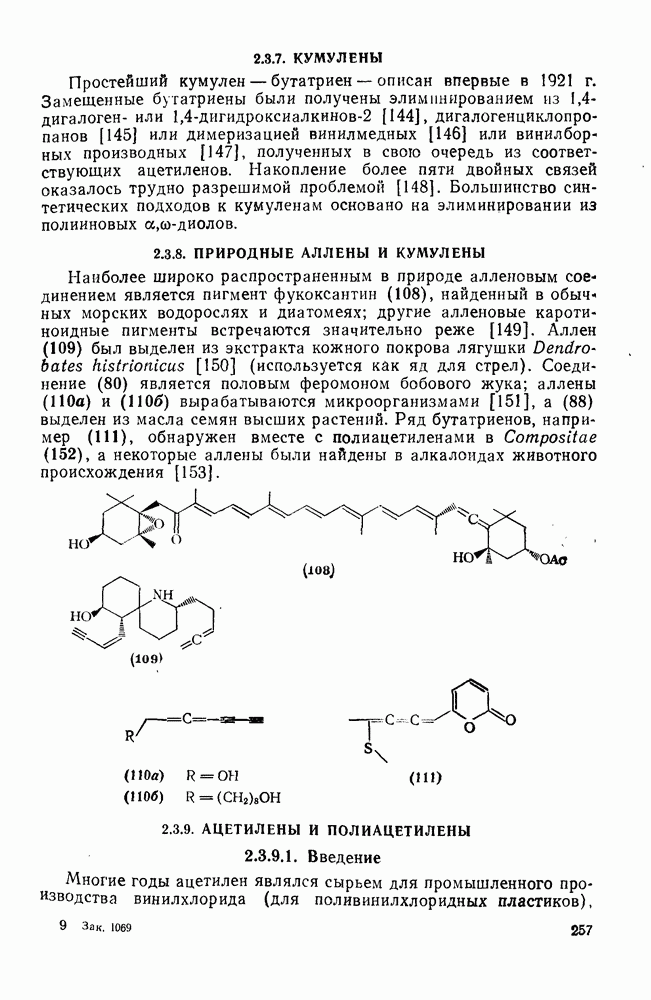
- 2.3.8. ПРИРОДНЫЕ АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.9. АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.9.2. Получение ацетиленов
- 2.3.10. РЕАКЦИИ АЦЕТИЛЕНОВ
- 2.3.10.2. Изомеризация
- 2.3.10.3. Пропаргильные перегруппировки
- 2.3.10.4. Реакции присоединения
- 2.3.10.5. Гидроборирование и гидроалюминирование
- 2.3.10.6. Реакции замещения
- 2.3.10.7. Восстановление
- 2.3.10.8. Окисление
- 2.3.10.9. Циклоприсоединение
- 2.3.10.10. Реакции катализуемые металлами
- 2.3.11. ПОЛИАЦЕТИЛЕНЫ
- 2.3.12. ПРИРОДНЫЕ АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.13. СОПРЯЖЕННЫЕ ЕНИНЫ
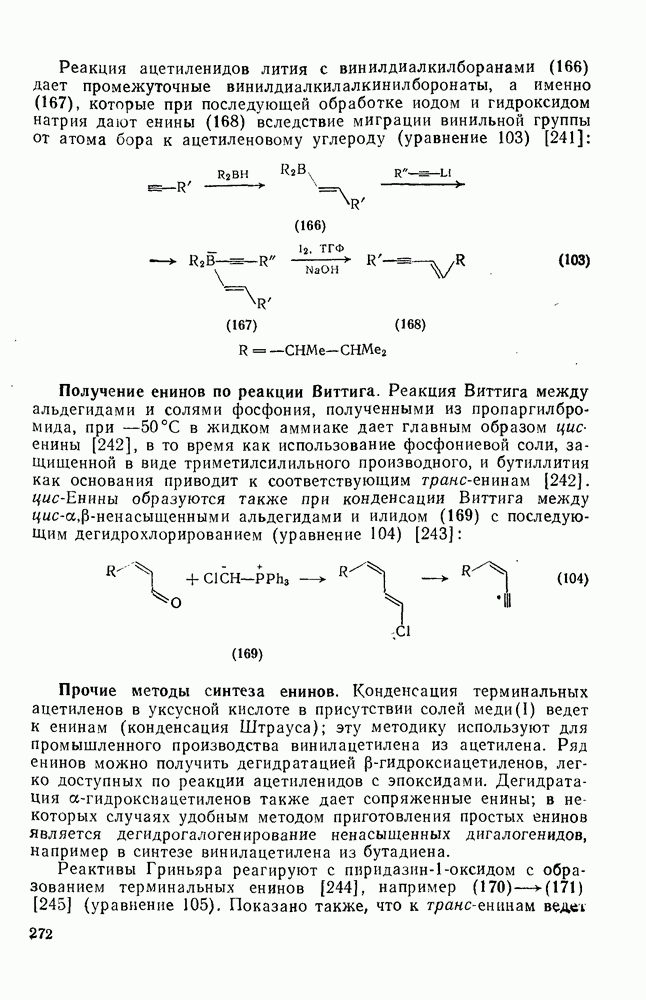
- 2.3.13.1. Получение сопряженных енинов
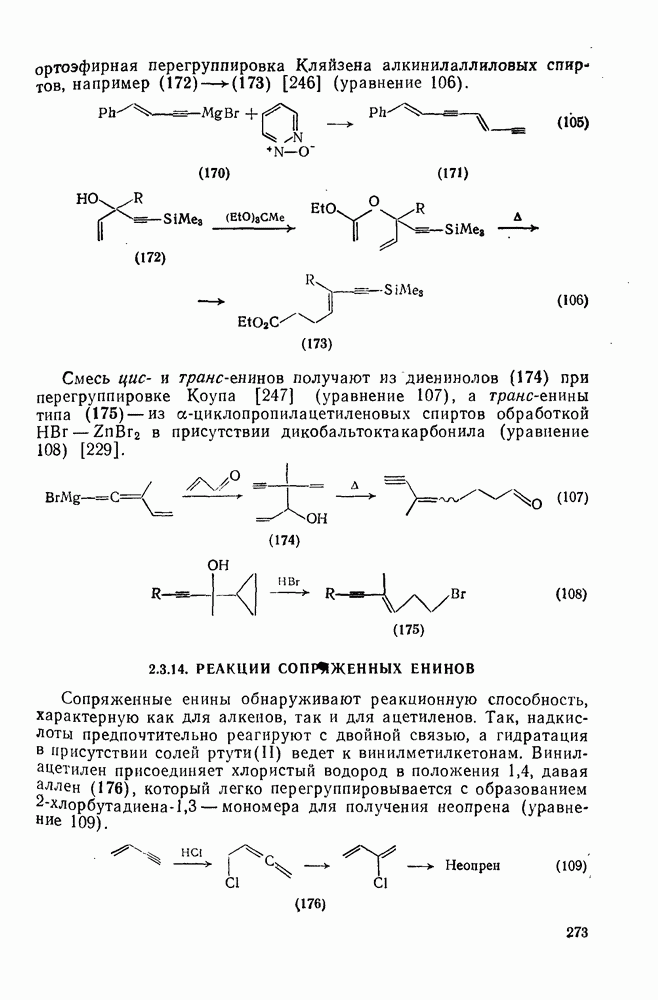
- 2.3.14. РЕАКЦИИ СОПРЯЖЕННЫХ ЕНИНОВ
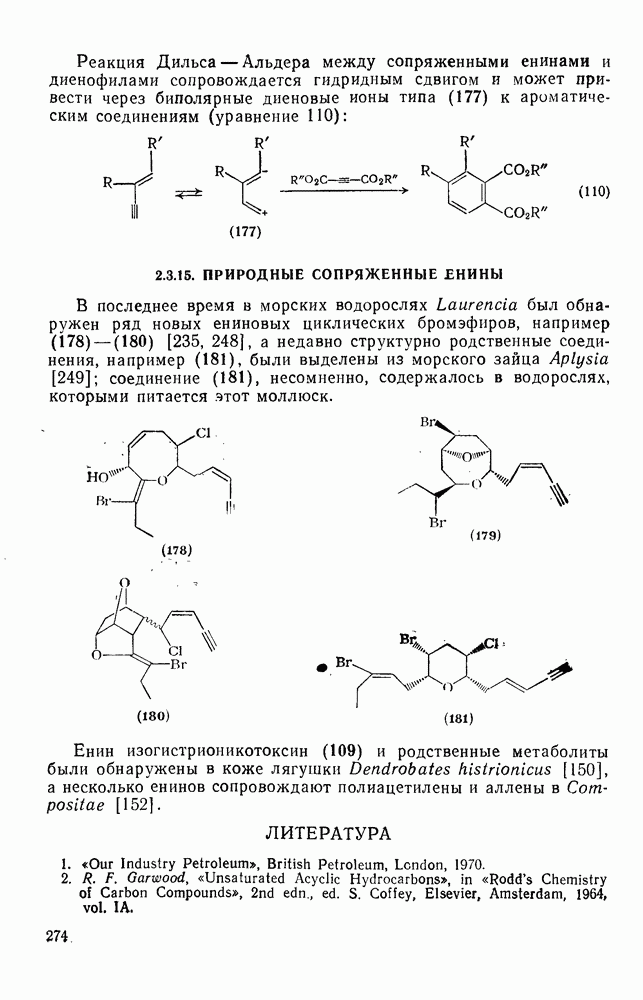
- 2.3.15. ПРИРОДНЫЕ СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.4. АРОМАТИЧНОСТЬ
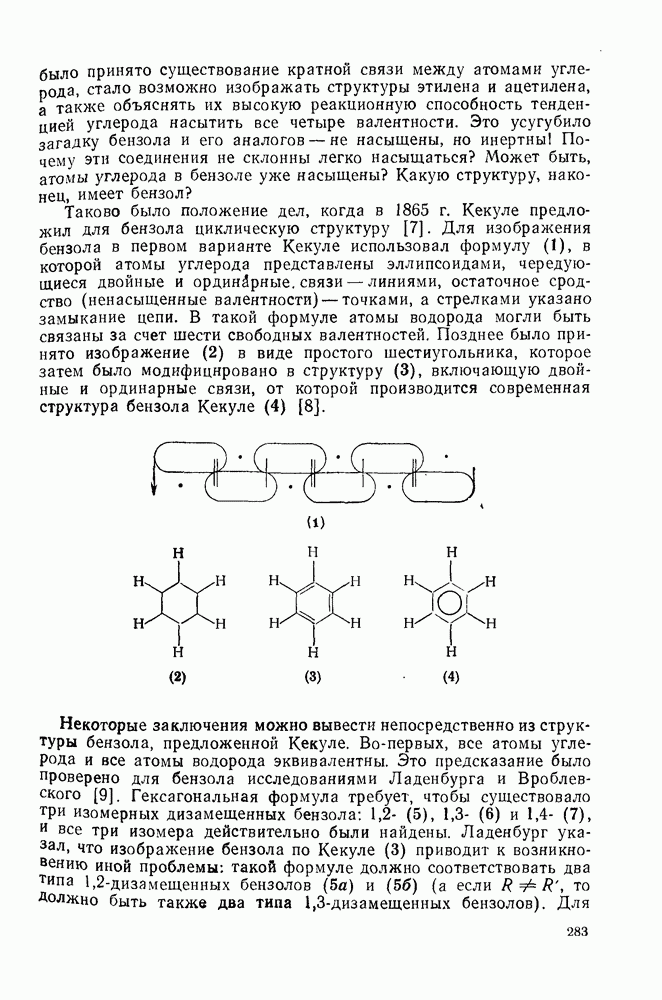
- 2.4.2. ЭЛЕКТРОННЫЕ ТЕОРИИ СТРОЕНИЯ БЕНЗОЛА
- 2.4.3. КРИТЕРИИ АРОМАТИЧНОСТИ
- 2.4.3.1. Термодинамические свойства
- 2.4.3.2. Структурные особенности
- 2.4.3.3. Магнитные свойства
- 2.4.3.4. Прочие критерии
- 2.4.4. АНТИАРОМАТИЧНОСТЬ
- 2.4.4.1. Термодинамические свойства
- 2.4.4.2. Структурные особенности
- 2.4.4.3. Магнитные свойства
- 2.4.4.4. Прочие свойства
- 2.4.5. ТЕОРЕТИЧЕСКИЕ ОПРЕДЕЛЕНИЯ АРОМАТИЧНОСТИ
- 2.4.5.1. Полуэмпирические расчеты и дьюаровская резонансная энергия
- 2.4.5.2. Расчеты по методу валентных пар и применение резонансного метода
- 2.4.5.3. Локализация связей
- 2.4.5.4. Связь энергетических критериев с критериями локализации связей
- 2.4.6. АРОМАТИЧЕСКИЕ ПЕРЕХОДНЫЕ СОСТОЯНИЯ
- 2.5. АРЕНЫ И ИХ РЕАКЦИИ
- 2.5.2. НОМЕНКЛАТУРА
- 2.5.3. ФИЗИЧЕСКИЕ СВОЙСТВА АРЕНОВ
- 2.5.4. ПРОМЫШЛЕННОЕ ПРОИЗВОДСТВО АРЕНОВ
- 2.5.5. ЦИКЛОТРИМЕРИЗАЦИЯ АЦЕТИЛЕНОВ
- 2.5.6. РЕАКЦИИ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ АРЕНОВ
- 2.5.6.1. Механизм ароматического нитрования [15]
- 2.5.6.2. Кинетические изотопные эффекты [21]
- 2.5.6.3. Реакции, включающие ипсо-протонирование
- 2.5.6.4. Металлирование
- 2.5.6.5. Электрофилы IV группы
- 2.5.6.6. Электрофилы V группы
- 2.5.6.7. Электрофилы VI группы [18, 56]
- 2.5.6.8. Электрофилы VII группы [18, 25а, 56]
- 2.5.7. ОРИЕНТАЦИЯ В РЕАКЦИЯХ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ
- 2.5.8. РАДИКАЛЬНОЕ ГАЛОГЕНИРОВАНИЕ АРЕНОВ В БОКОВУЮ ЦЕПЬ [96]
- 2.5.9. РЕАКЦИИ ПРИСОЕДИНЕНИЯ К АРЕНАМ
- 2.5.9.1. Восстановление аренов
- 2.5.9.2. Термическое циклоприсоединение к аренам
- 2.5.9.3. Фотоциклоприсоединение к моноциклическим аренам [126]
- 2.5.9.4. Фотохимические реакции полициклических аренов
- 2.6.10. ФОТОИЗОМЕРИЗАЦИЯ АРЕНОВ [126б]
- 2.5.11. ОКИСЛЕНИЕ АРЕНОВ [153]
- 2.5.12. РЕАКЦИИ АРЕНОВ С СИНГЛЕТНЫМ КИСЛОРОДОМ [162]
- 2.5.13. ПРИГОТОВЛЕНИЕ БИ- И ПОЛИАРИЛОВ
- 2.5.14. ВНУТРИМОЛЕКУЛЯРНАЯ ФОТОЦИКЛИЗАЦИЯ, ПРИВОДЯЩАЯ К ПОЛИЦИКЛИЧЕСКИМ АРЕНАМ
- 2.5.15. ВНУТРИМОЛЕКУЛЯРНАЯ ЦИКЛИЗАЦИЯ ДИЗАМЕЩЕННЫХ АРЕНОВ
- 2.5.16. ЦИКЛОФАНЫ
- 2.5.17. КОНФОРМАЦИЯ И ХИРАЛЬНОСТЬ АРЕНОВ
- 2.5.18. АЗУЛЕНЫ И НЕБЕНЗОИДНЫЕ АРЕНЫ
- 2.6. АННУЛЕНЫ И РОДСТВЕННЫЕ СИСТЕМЫ
- 2.6.2. МЕТОДЫ СИНТЕЗА
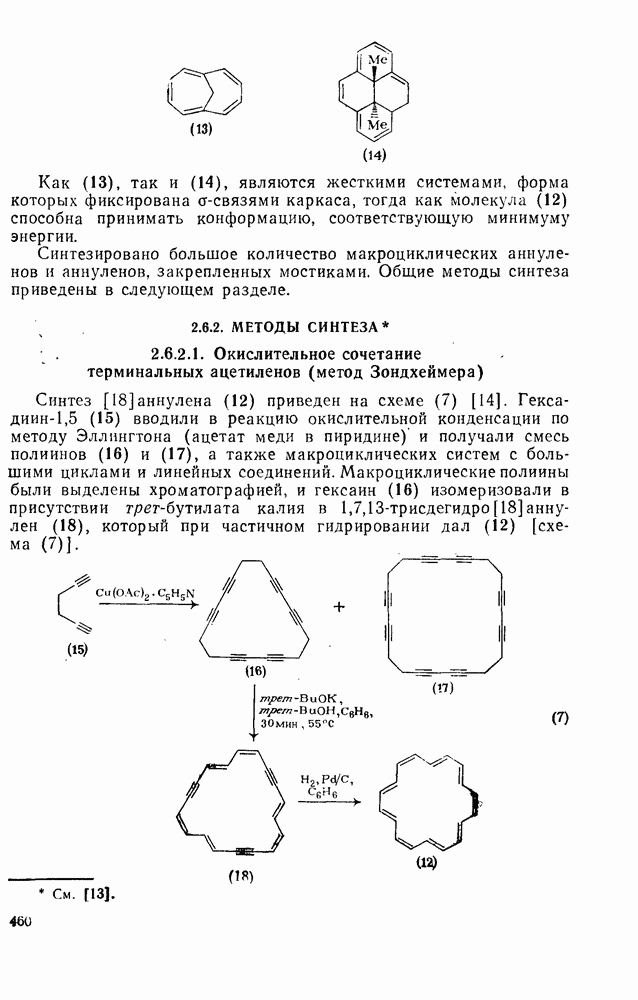
- 2.6.2.1. Окислительное сочетание терминальных ацетиленов (метод Зондхеймера)
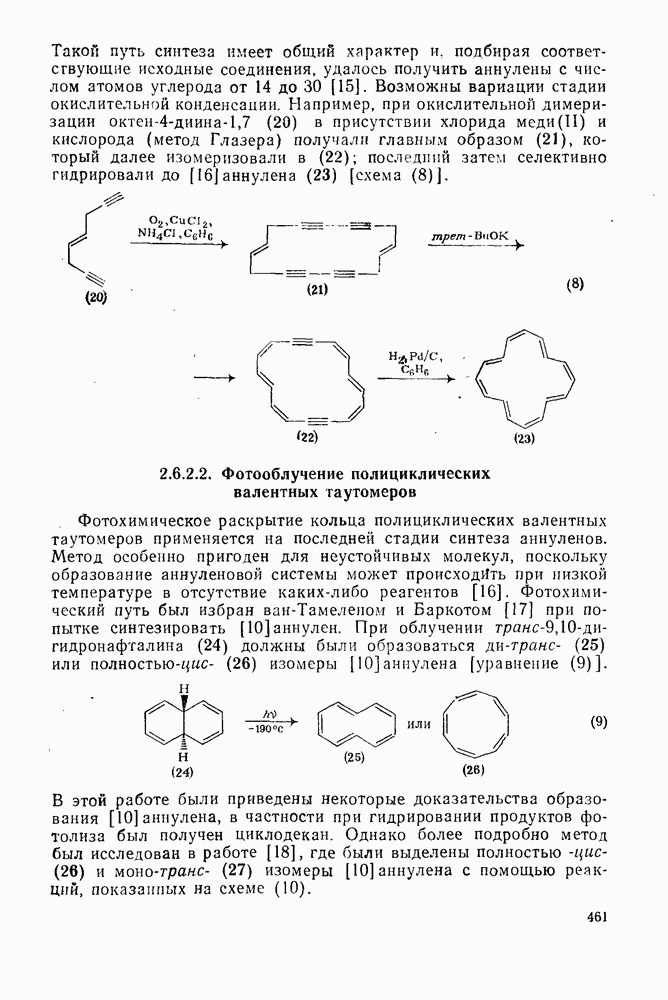
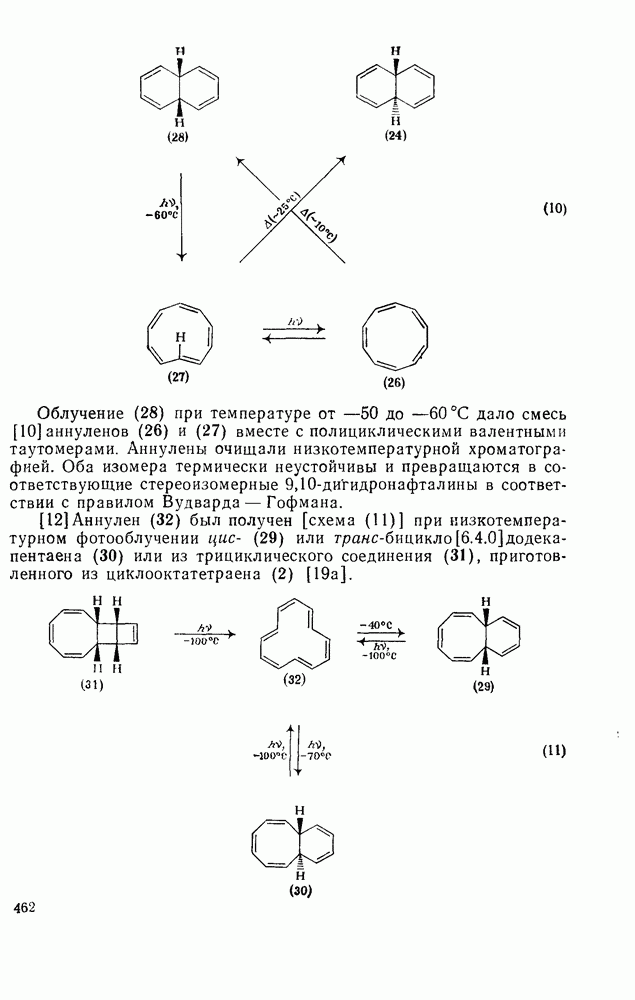
- 2.6.2.2. Фотооблучение полициклических валентных таутомеров
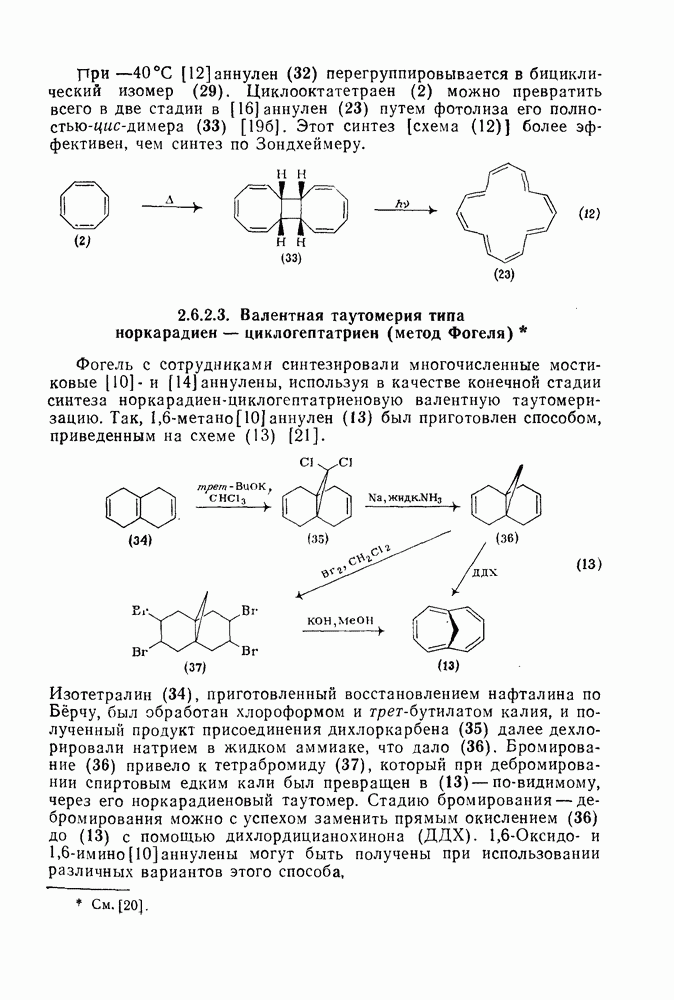
- 2.6.2.3. Валентная таутомерия типа норкарадиен — циклогептатриен (метод Фогеля)
- 2.6.2.4. Прочие методы
- 2.6.3. СВОЙСТВА АННУЛЕНОВ
- 2.6.4. СВОЙСТВА 4n-АННУЛЕНОВ
- 2.6.5. ДЕГИДРОАННУЛЕНЫ
- 2.6.6. АННЕЛИРОВАННЫЕ АННУЛЕНЫ
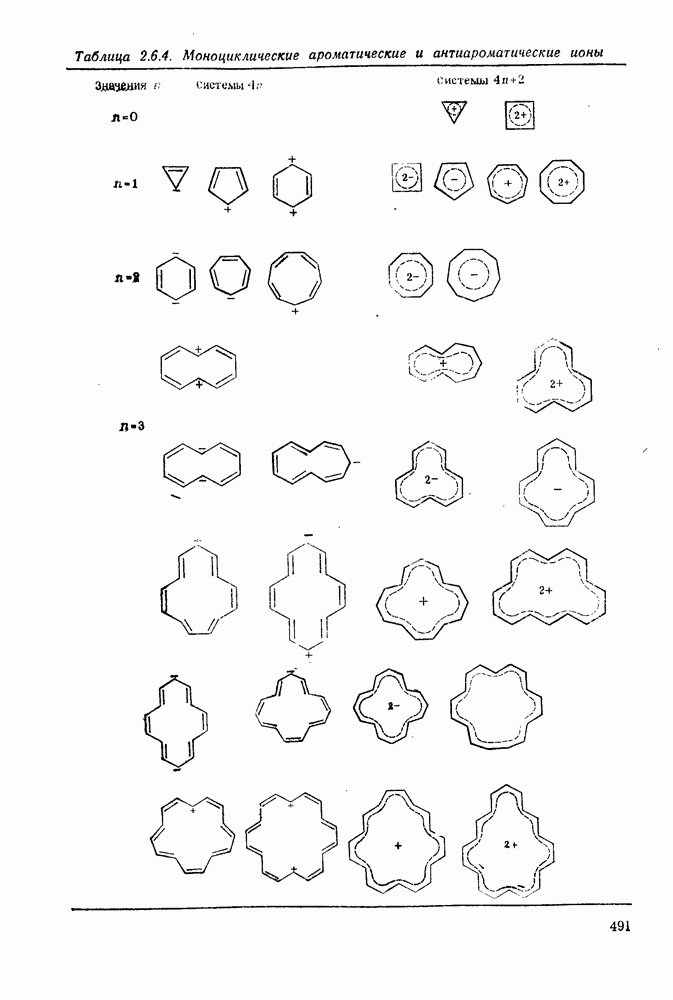
- 2.6.7. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ МОНОЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.8. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ ПОЛИЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.9. ГОМОАРОМАТИЧЕСКИЕ СИСТЕМЫ
- 2.7. КАРБОКАТИОНЫ И КАРБАНИОНЫ
- 2.7.1.2. Краткий исторический очерк развития химии карбокатионов
- 2.7.1.3. Методы генерации карбокатионов
- 2.7.1.4. Типы карбокатионов
- 2.7.1.5. Изучение карбокатионов: методы и результаты
- 2.7.1.6. Реакции карбокатионов
- 2.7.2. КАРБАНИОНЫ
- 2.7.2.2. Методы генерации карбанионов
- 2.7.2.3. Типы карбанионов
- 2.7.2.4. Физические свойства карбанионов
- 2.7.5.2. Реакции карбанионов
- 2.8. РАДИКАЛЫ, КАРБЕНЫ, АРИНЫ
- 2.8.1. РАДИКАЛЫ
- 2.8.1.1. Структура, устойчивость и реакционная способность радикалов
- 2.8.1.2. Методы генерации и реакции радикалов
- 2.8.2. КАРБЕНЫ
- 2.8.2.1. Методы генерации карбенов и карбеноидов
- 2.8.2.2. Реакции карбенов
- 2.8.3. АРИНЫ
- 2.8.3.1. Структура и спектры аринов
- 2.8.3.2. Методы генерации аринов
- 2.8.3.3. Реакции аринов
- ЧАСТЬ 3. ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- 3.2. МЕТОДЫ ГАЛОГЕНИРОВАНИЯ
- 3.2.1. Гомолитическое замещение водорода
- 3.2.1.2. Использование галогенпроизводных в качестве реагентов
- 3.2.2. Гомолитическое замещение функциональных групп
- 3.2.3. Гомолитическое присоединение к ненасыщенным системам
- 3.2.3.1. Присоединение галогеноводородов
- 3.2.3.2. Присоединение галогенов
- 3.2.4. Электрофильное галогенирование
- 3.2.4.1. Замещение у насыщенной связи С-Н
- 3.2.4.2. Реакции с ненасыщенными системами
- 3.2.4.3. Реакции с карбанионами
- 3.2.5. Нуклеофильное галогенирование
- 3.2.5.1. Галогенирование с замещением функциональной группы
- 3.2.5.2. Галогенирование в ароматических системах
- 3.2.5.3. Галогенирование путем обмена галогенов
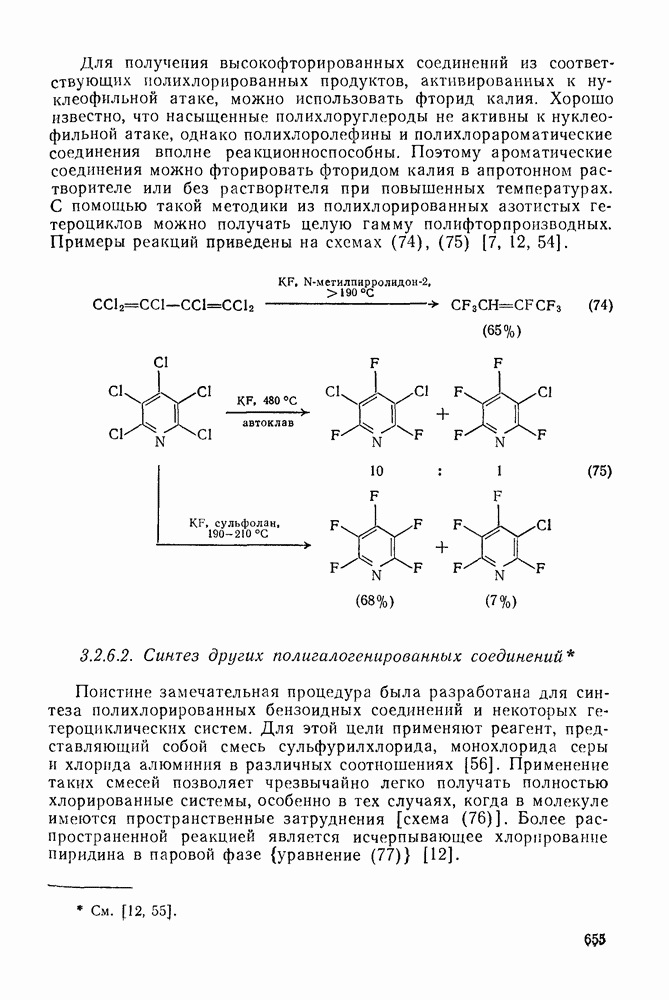
- 3.2.6. Синтез полигалогенированных соединений
- 3.2.6.1. Синтез полифторированных соединений
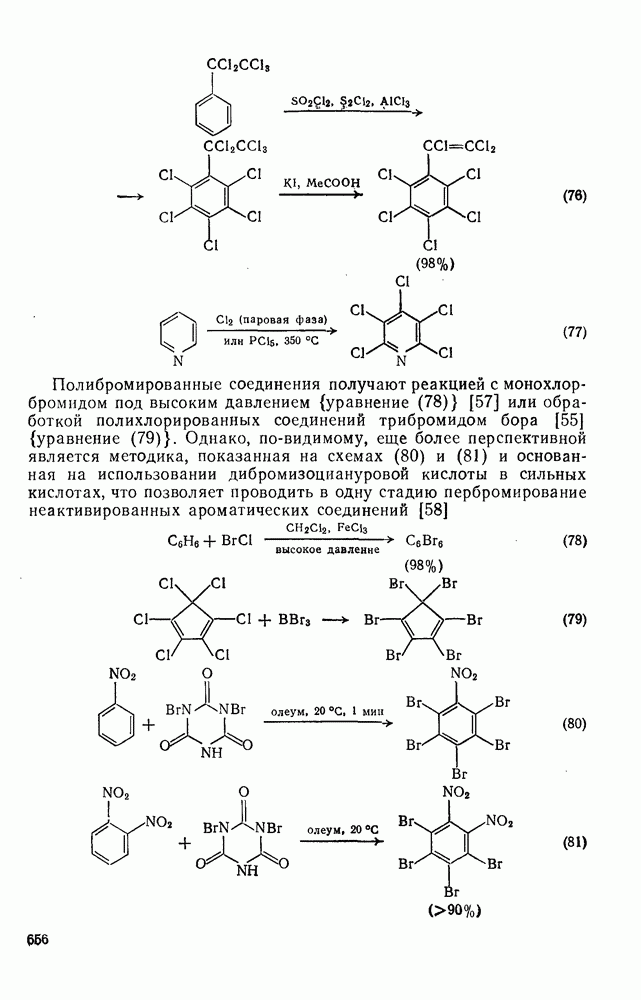
- 3.2.6.2. Синтез других полигалогенированных соединений
- 3.3. ГАЛОГЕНАЛКАНЫ
- 3.3.1. Характеристика связей углерод-галоген
- 3.3.2. Промышленное применение
- 3.3.3. Нуклеофильное замещение галогена
- 3.3.3.1. Реакции SN2 и родственные процессы
- 3.3.3.2. Соучастие соседних групп
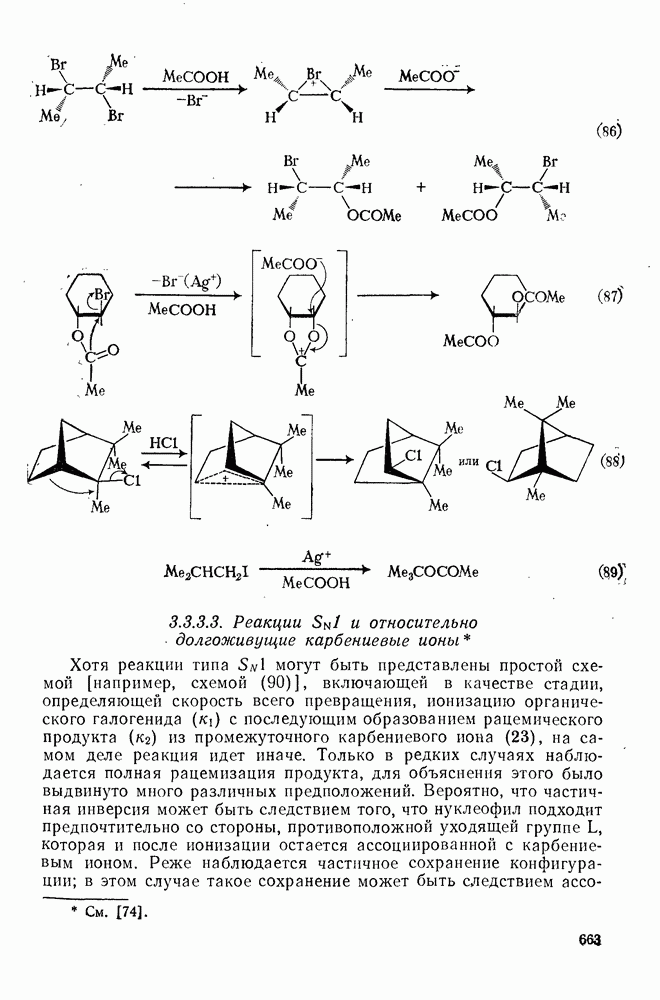
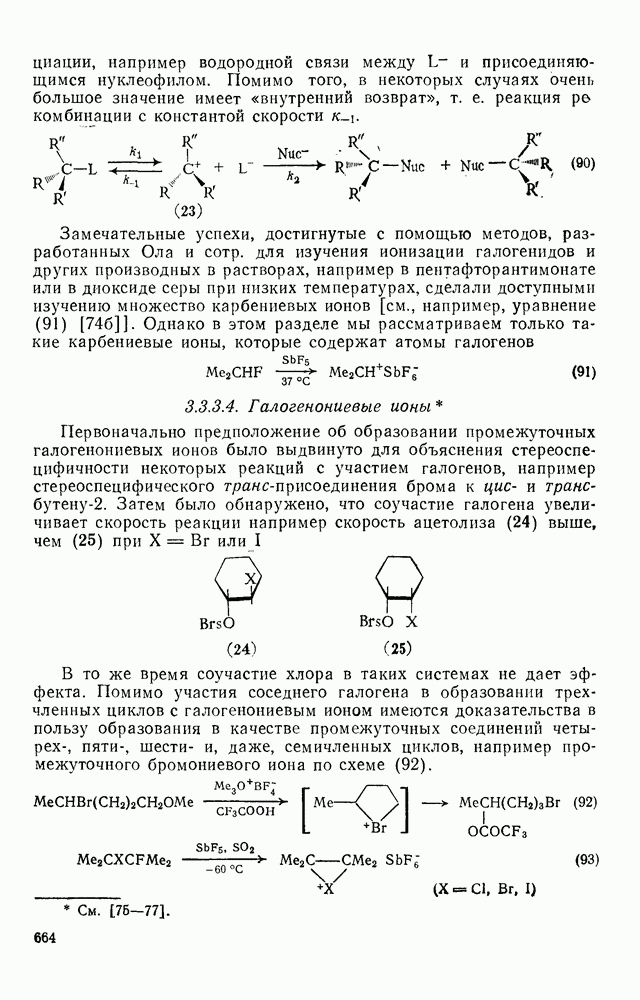
- 3.3.3.3. Реакции SN1 и относительно долгоживущие карбениевые ионы
- 3.3.3.4. Галогенониевые ионы
- 3.3.3.5. Галогенсодержащие карбениевые ионы
- 3.3.3.6. Механизм замещения с переносом электрона
- 3.3.4. Восстановление
- 3.3.5. Замещение на металлы
- 3.3.6. Элиминирование
- 3.3.6.1. b-Элиминирование
- 3.3.6.2. Галогенкарбанионы
- 3.3.6.3. Элиминирование через карбанионы
- 3.3.6.4. b-Элиминирование из металлорганических соединений
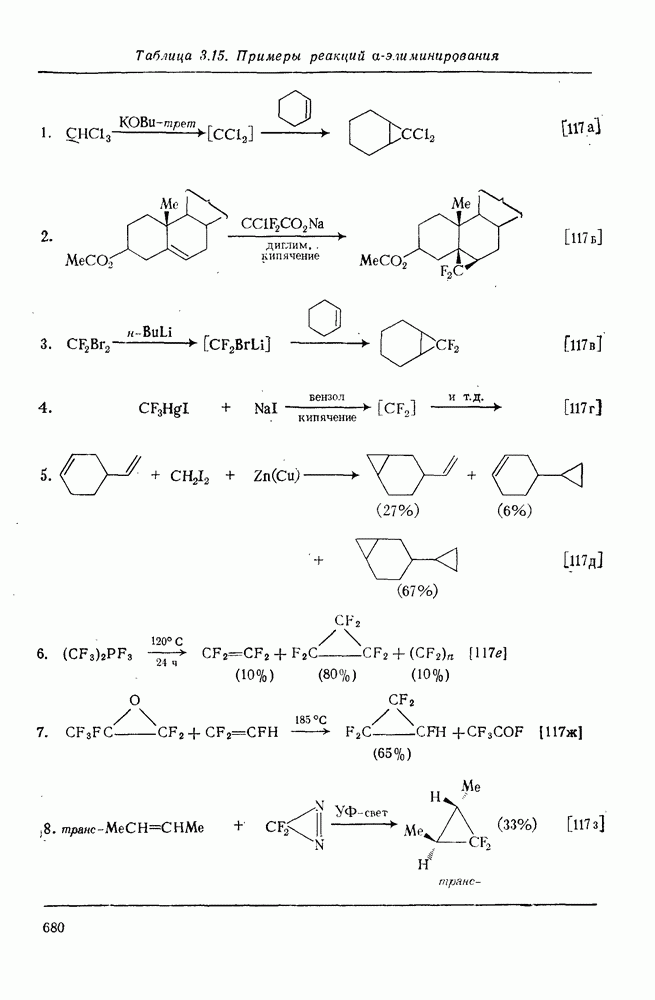
- 3.3.6.5. a-Элиминирование (генерирование карбенов)
- 3.4. ГАЛОГЕНАЛКЕНЫ
- 3.4.1. Синтез галогеналкенов
- 3.4.2. Нуклеофильная атака
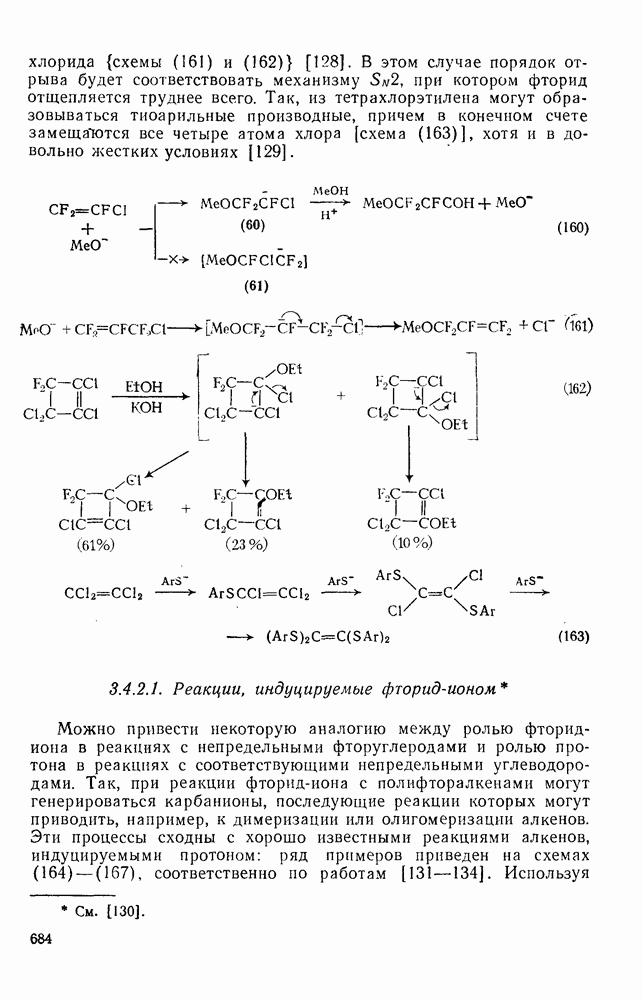
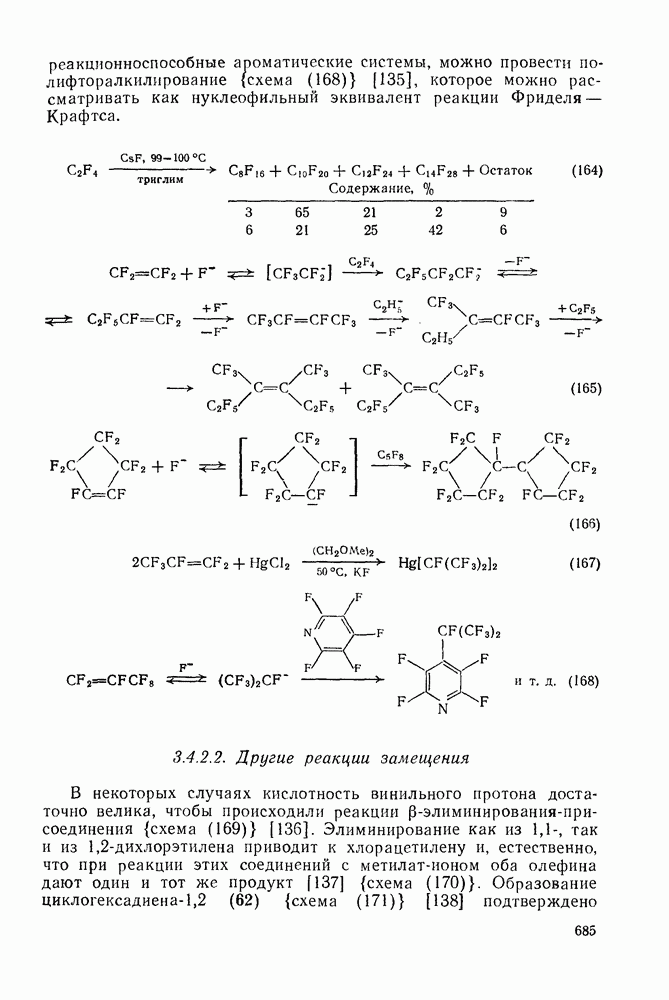
- 3.4.2.1. Реакции, индуцируемые фторид-ионом
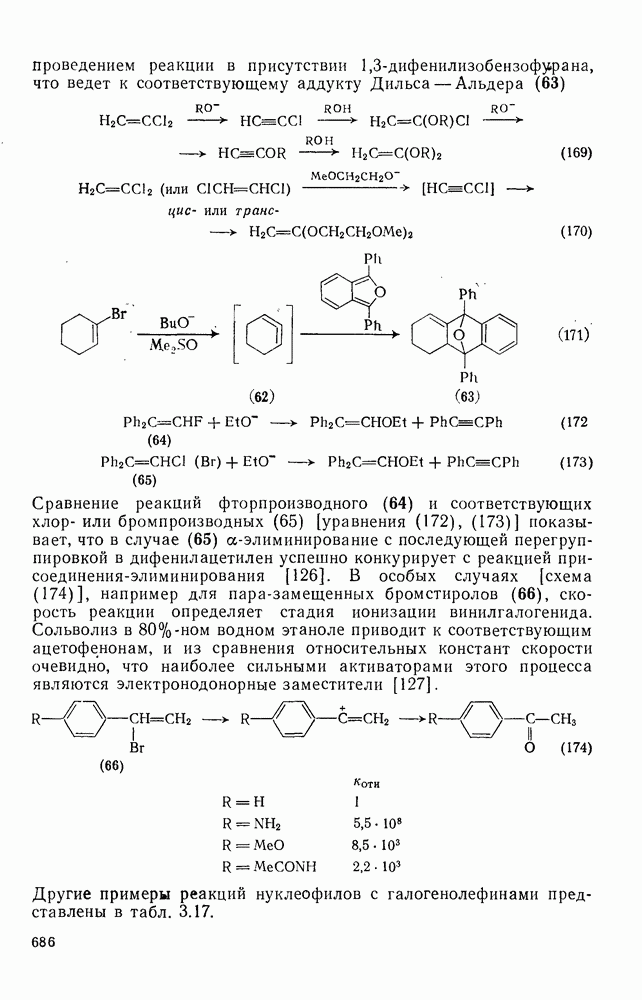
- 3.4.2.2. Другие реакции замещения
- 3.4.3. Радикальное присоединение
- 3.4.4. Электрофильное присоединение
- 3.4.5. Циклоприсоединение
- 3.4.5.1. [2+2]-Циклоприсоединение
- 3.4.5.2. [4+2]-Циклоприсоединение
- 3.5. ГАЛОГЕНАЛКИНЫ
- 3.6. ГАЛОГЕНАРЕНЫ
- 3.6.1. Замещение галогена
- 3.6.1.2. Присоединение-элиминирование
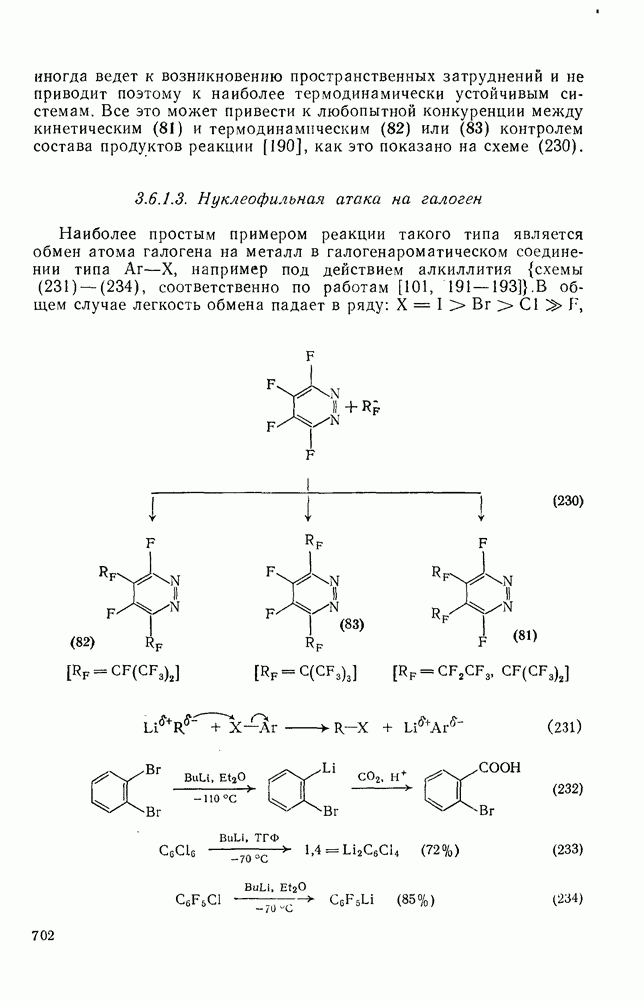
- 3.6.1.3. Нуклеофильная атака на галоген
- 3.6.1.4. Перенос электрона
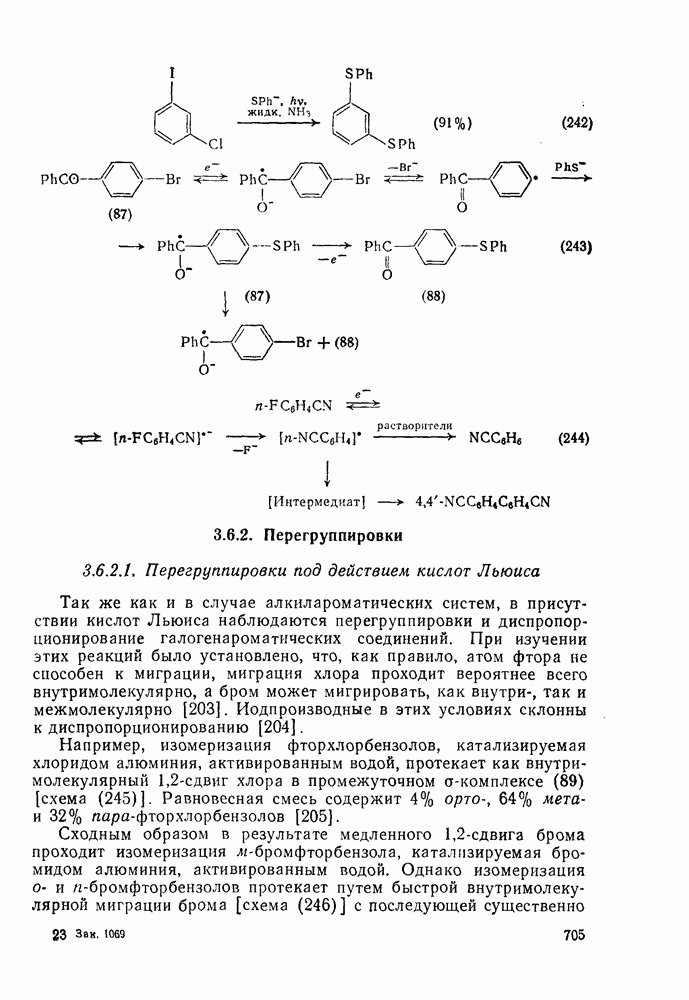
- 3.6.2. Перегруппировки
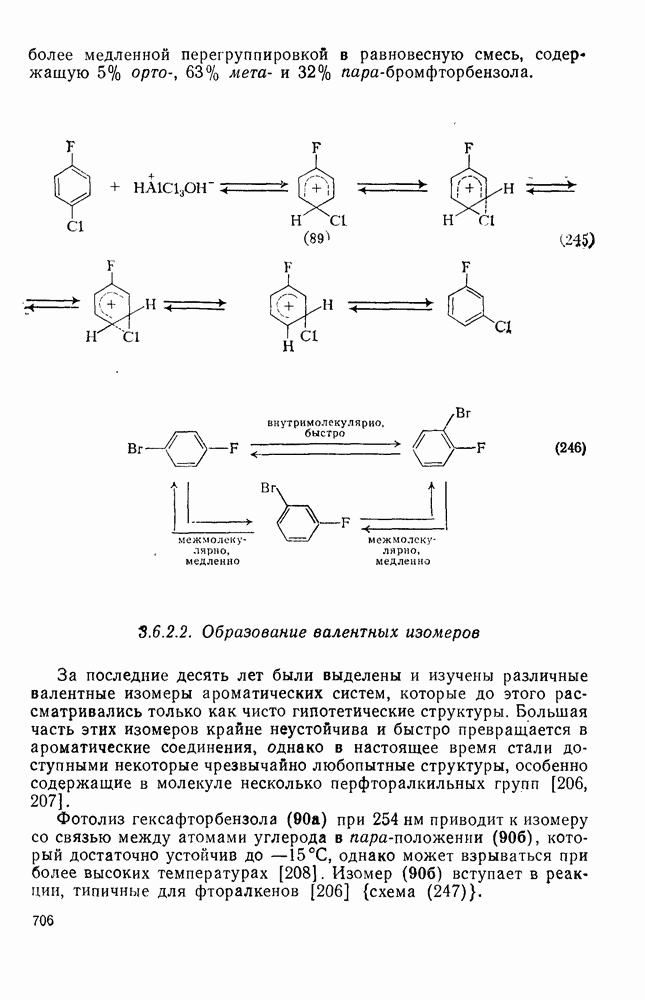
- 3.6.2.1. Перегруппировки под действием кислот Льюиса
- 3.6.2.2. Образование валентных изомеров