| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
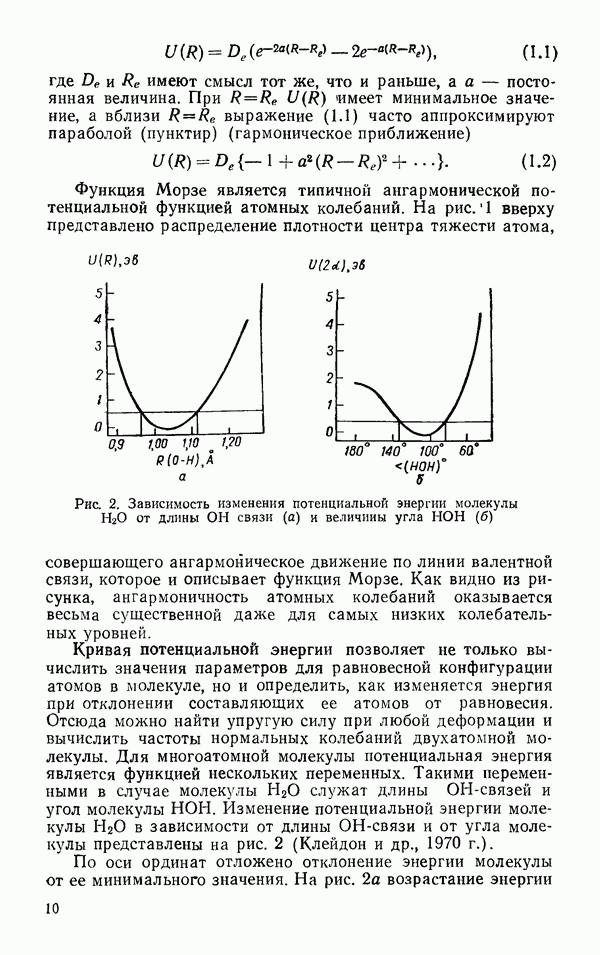
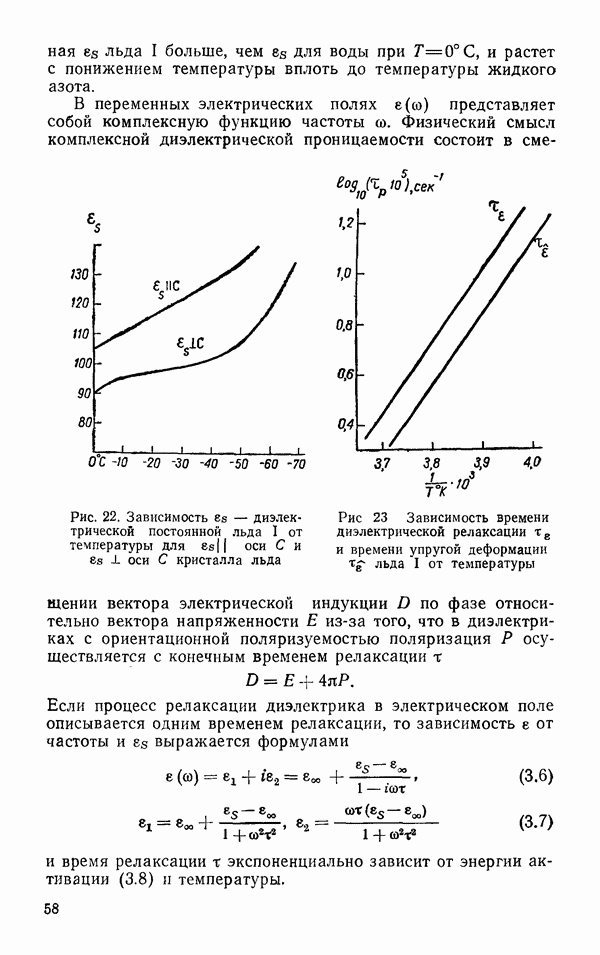
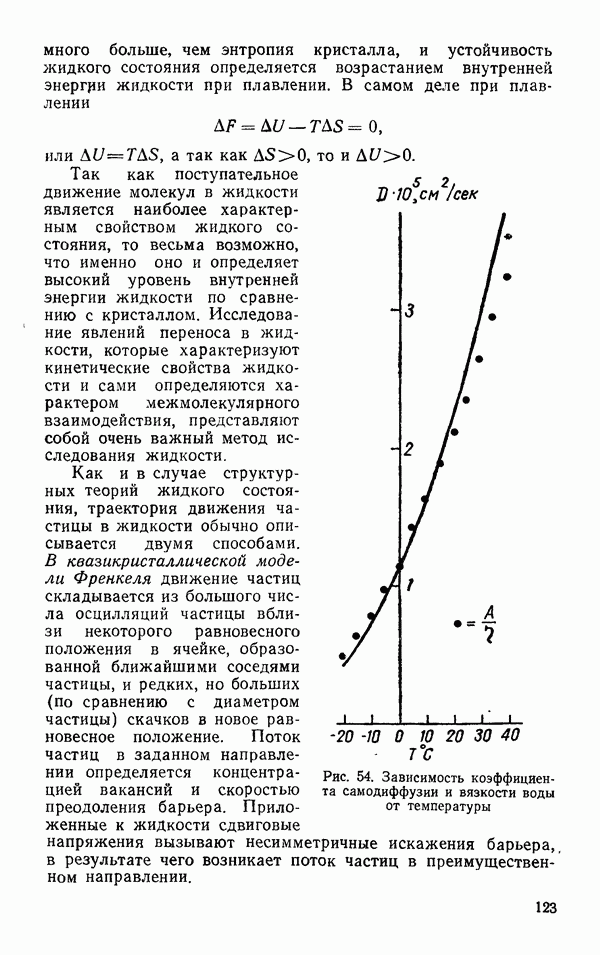
§ 2. СВОЙСТВА АТОМОВ, ОБРАЗУЮЩИХ ВОДОРОДНУЮ СВЯЗЬ
Известно несколько причин, по которой водород способен к образованию особого специфического вида связи с электроотрицательными атомами. Одна из них, по-видимому, состоит в том, что система  характеризуется минимальным электронным отталкиванием. Обладая единственным электроном, осуществляющим связь
характеризуется минимальным электронным отталкиванием. Обладая единственным электроном, осуществляющим связь  водород допускает максимальное приближение атома
водород допускает максимальное приближение атома  Сумма радиуса Ван-дер-Ваальса свободных атомов
Сумма радиуса Ван-дер-Ваальса свободных атомов  составляет 2,6 А, в то время как расстояние между атомами
составляет 2,6 А, в то время как расстояние между атомами  связанными водородной связью, составляет
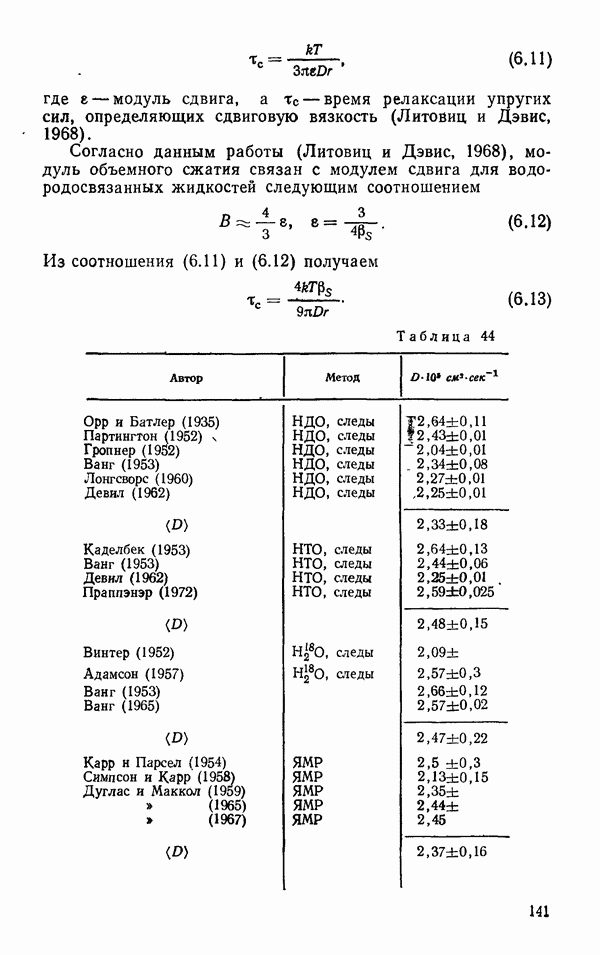
связанными водородной связью, составляет  . В табл. 30 представлены расстояния между атсгмами участниками водородной связи, рассчитанные на основании данных о радиусах Ван-дер-Ваальса и измеренные экспериментально. Как видно, наблюдаемые расстояния между тяжелыми атомами 0,3 А короче, тем сумма их радиусов Ван-дер-Ваальса. Расстояние между -атомами
. В табл. 30 представлены расстояния между атсгмами участниками водородной связи, рассчитанные на основании данных о радиусах Ван-дер-Ваальса и измеренные экспериментально. Как видно, наблюдаемые расстояния между тяжелыми атомами 0,3 А короче, тем сумма их радиусов Ван-дер-Ваальса. Расстояние между -атомами  в водородной связи короче расстояния между этими атомами, полученными суммированием радиусов Ван-дер-Ваальса на
в водородной связи короче расстояния между этими атомами, полученными суммированием радиусов Ван-дер-Ваальса на  , и больше для сильных связей и
, и больше для сильных связей и  для самых слабых связей.
для самых слабых связей.
Другая состоит в том, что в водородной связи принимают участие тяжелые атомы, характеризующиеся большой величиной электроотрицательности. Первая количественная шкала электроотрицательности, которая до сих пор широко используется, была введена в химию Полингом. При помощи числа, характеризующего электроотрицательность элемента, выражается доля ионного характера связи. Ниже приведены
Таблица 30 Расстояние между атомами, связанными водородной связью, как сумма радиусов Ван-дер-Ваальса (расчетное) и наблюдаемые значения тех же расстояний

значения электроотрицательности для ряда интересующих наг атомов по Полингу:

Шкала Полинга — экспериментальная шкала, она построена при предположении, что ионность в ковалентной связи делает связь более прочной. Так, мало и одинаково электроотрицательные  образуют почти чисто ковалентную связь. Для них разница в теплоте образования
образуют почти чисто ковалентную связь. Для них разница в теплоте образования  связи и полусуммы теплот образования
связи и полусуммы теплот образования  и
и  связей ничтожно мала
связей ничтожно мала

В то время, как теплота образования молекулы  существенно больше
существенно больше  ккал/моль.
ккал/моль.
На этом основании по Полингу для одинарной ковалентной связи теплота ее образования связана с электроотрицательностью двух атомов  образующих связь следующим образом:
образующих связь следующим образом:

где  электроотрицательности атомов по Полингу (табл. 31).
электроотрицательности атомов по Полингу (табл. 31).
Распределение зарядов по атомам в водородной связи можно описать схемой

где  — атом донор,
— атом донор,  атом акцептор. Увеличение электроотрицательности — ионности связи — определяет и процесс диссоциации молекул в растворах с большой диэлектрической постоянной. Атом донор X оттягивает электроны от атома водорода, определяя тем самым величину положительного заряда на атоме водорода (кислотность водорода).
атом акцептор. Увеличение электроотрицательности — ионности связи — определяет и процесс диссоциации молекул в растворах с большой диэлектрической постоянной. Атом донор X оттягивает электроны от атома водорода, определяя тем самым величину положительного заряда на атоме водорода (кислотность водорода).

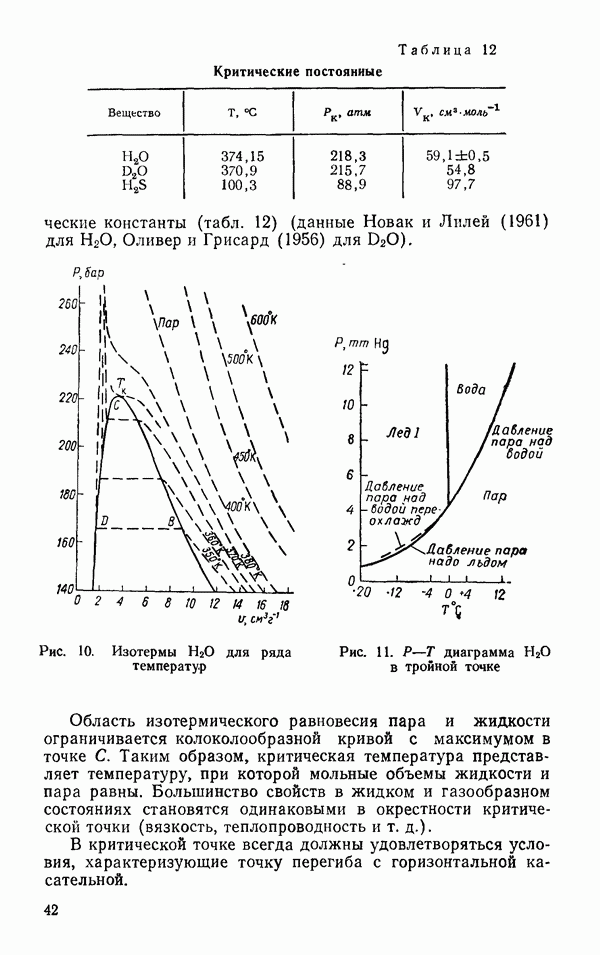
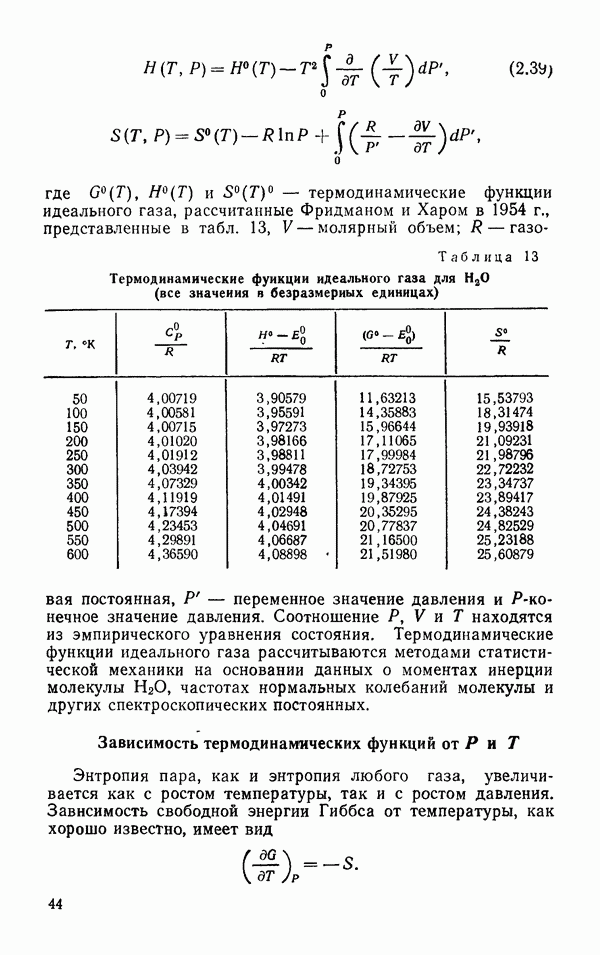
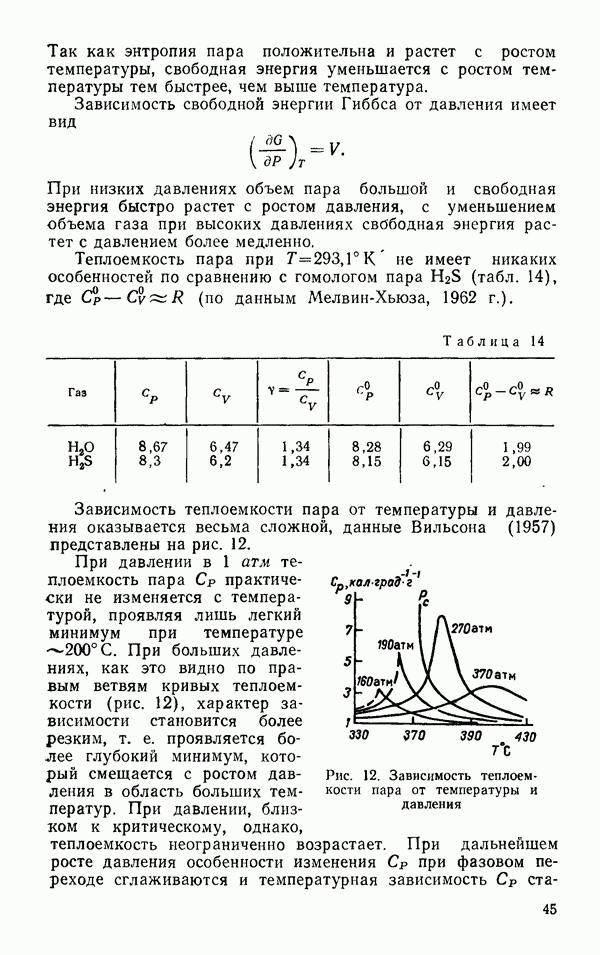
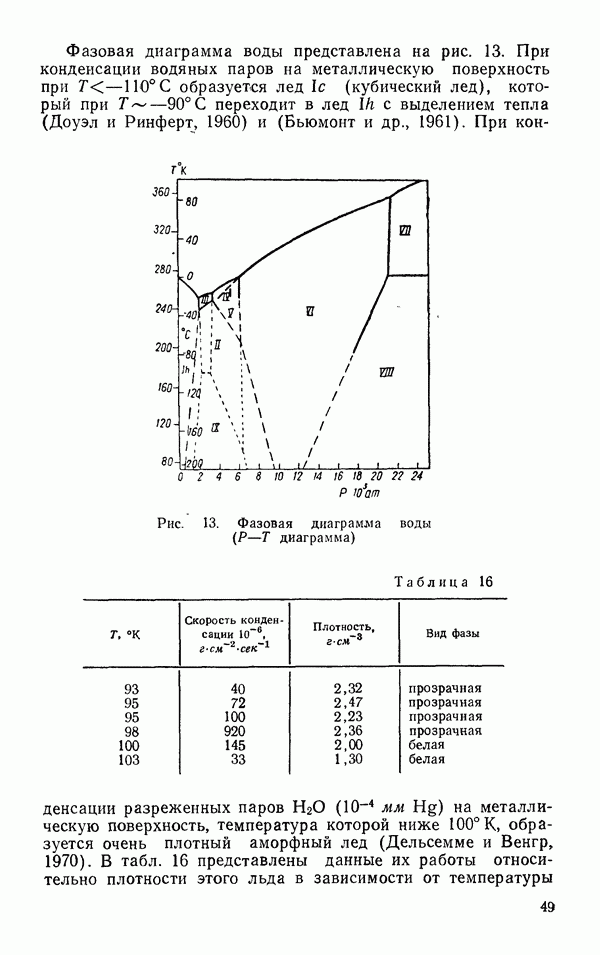
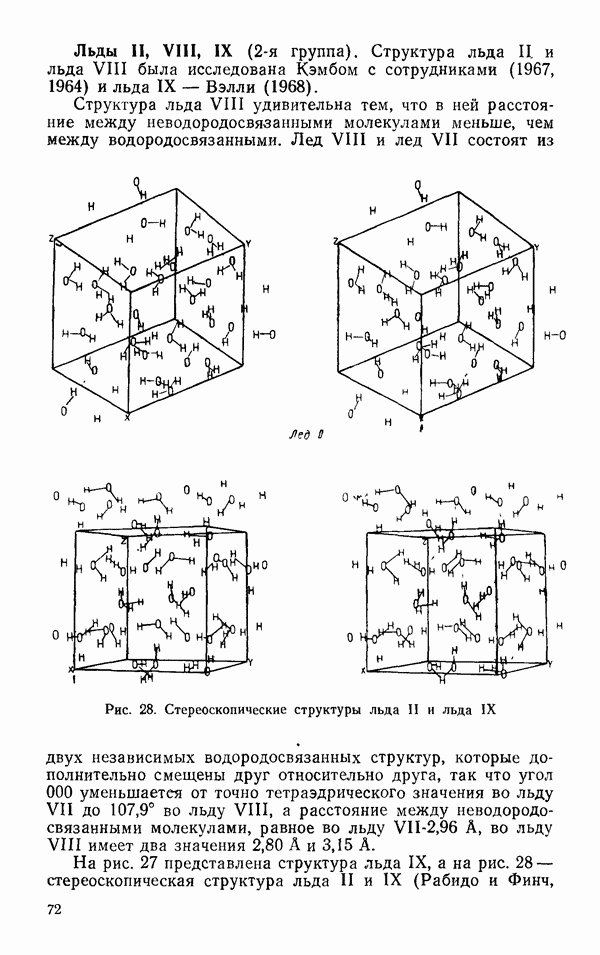
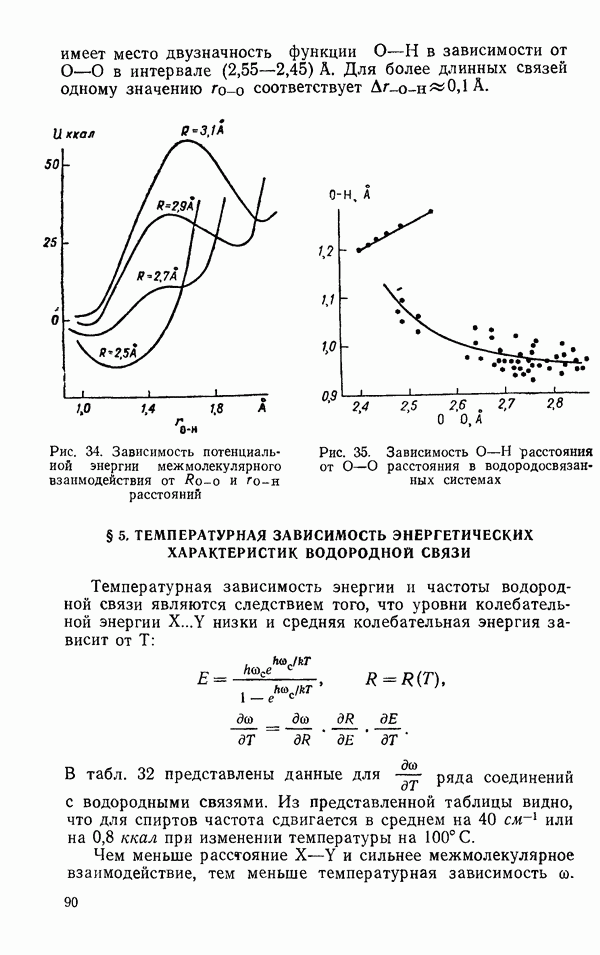
Рис. 33. Расстояния между атомами, участниками водородной связи
Кокрэн из данных по рассеянию рентгеновских лучей определил интегральную плотность электронов (число электронов, непосредственно связанных с водородным атомом) для ряда соединений и получил, что она составляет 0,8 для Н, связанного с С, и только 0,4 для Н, связанного с О, который является более электроотрицательным атомом, чем атом С.
Таблица 31 Функциональные группы, играющие роль доноров и акцепторов в водородной связи

Атом-акцептор должен обладать районами высокой отрицательной плотности, способными к взаимодействию с  Идеальными акцепторами являются неподеленные пары электронов атомов второго периода периодической системы элементов
Идеальными акцепторами являются неподеленные пары электронов атомов второго периода периодической системы элементов  Функциональные группы, наиболее часто играющие роль донора и акцептора протона в водородной связи, представлены в табл. 31.
Функциональные группы, наиболее часто играющие роль донора и акцептора протона в водородной связи, представлены в табл. 31.
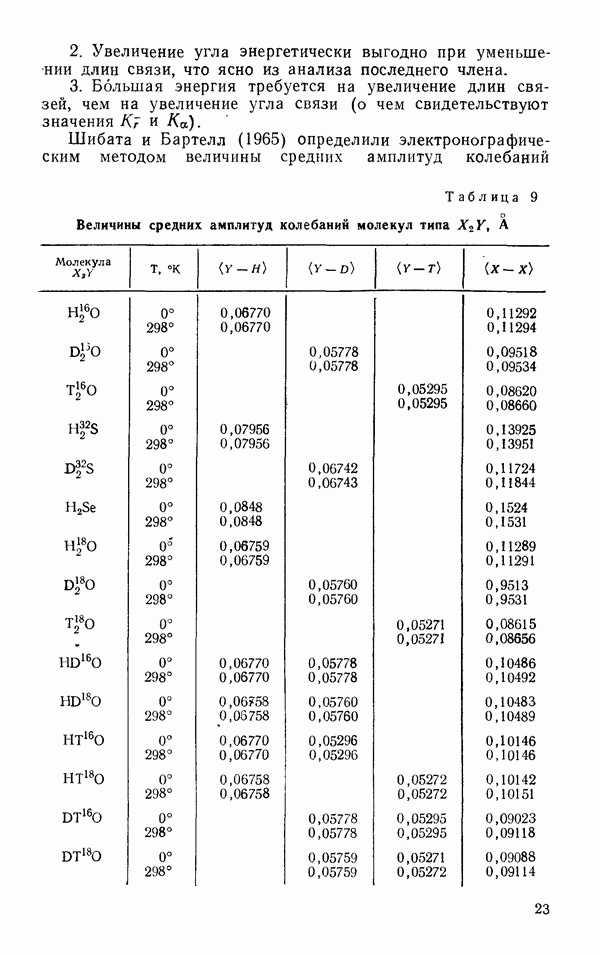
Третья причина состоит в том, что атом водорода является самым легким элементом и амплитуды его атомных колебаний в молекулах велики.
| << Предыдущий параграф | Следующий параграф >> |
- Введение
- Глава 1. МОЛЕКУЛА H2O
- Энергия образования молекулы
- Полная энергия молекулы
- § 3. РАЗМЕРЫ И ФОРМА
- § 4. ЭЛЕКТРИЧЕСКИЕ СВОЙСТВА
- § 5. КОЛЕБАТЕЛЬНЫЕ ЧАСТОТЫ МОЛЕКУЛЫ
- ЗАКЛЮЧЕНИЕ
- Глава 2. СВОЙСТВА ПАРА
- Исследования межмолекулярных сил отталкивания
- § 2. УРАВНЕНИЯ СОСТОЯНИЯ РЕАЛЬНОГО ГАЗА
- Вириальная форма уравнения состояния
- Эмпирическое уравнение состояния
- § 3. ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА
- Термодинамические функции
- Зависимость термодинамических функций от P и T
- § 4. ВЯЗКОСТЬ
- Глава 3. СВОЙСТВА ЛЬДОВ
- § 1. ЛЕД
- Пластическая деформация монокристалла льда I
- Диэлектрические свойства льда 1
- Электропроводность льда
- Самодиффузия
- Спектральные свойства льда I
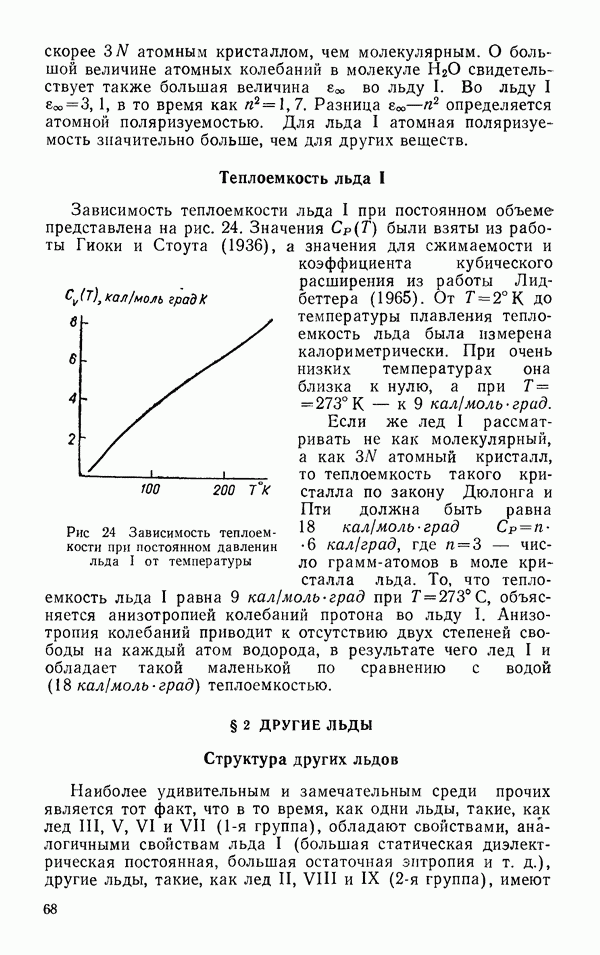
- Теплоемкость льда I
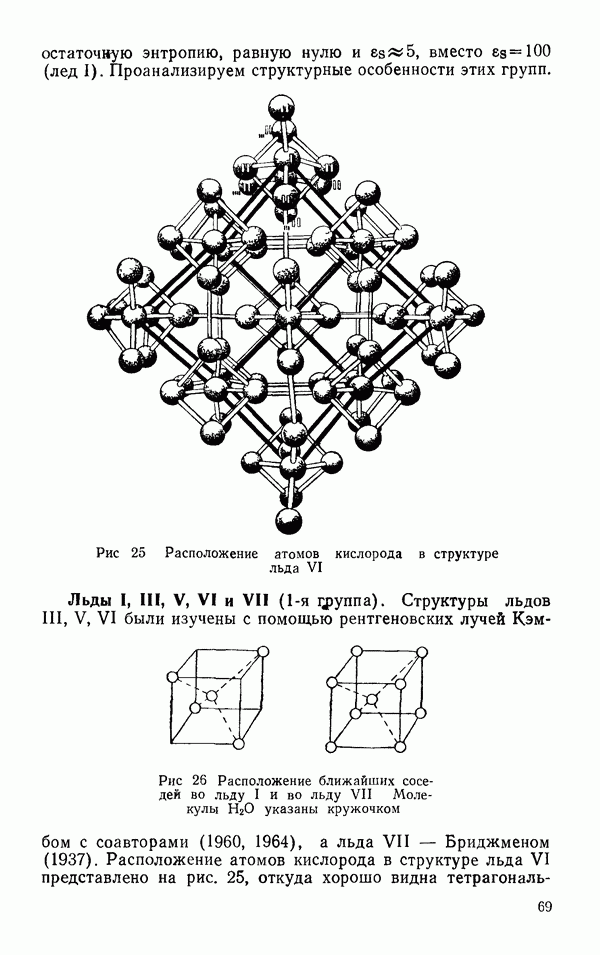
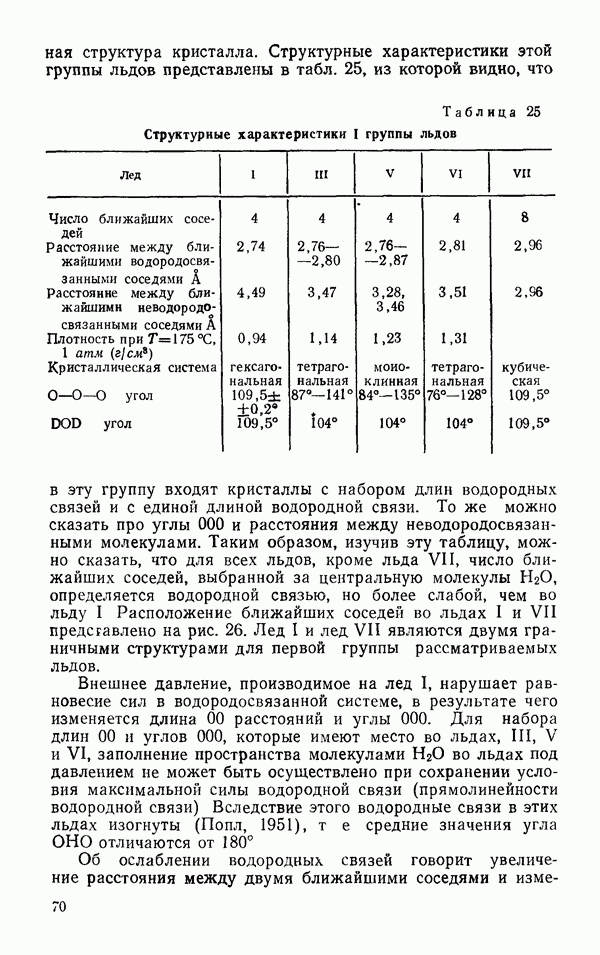
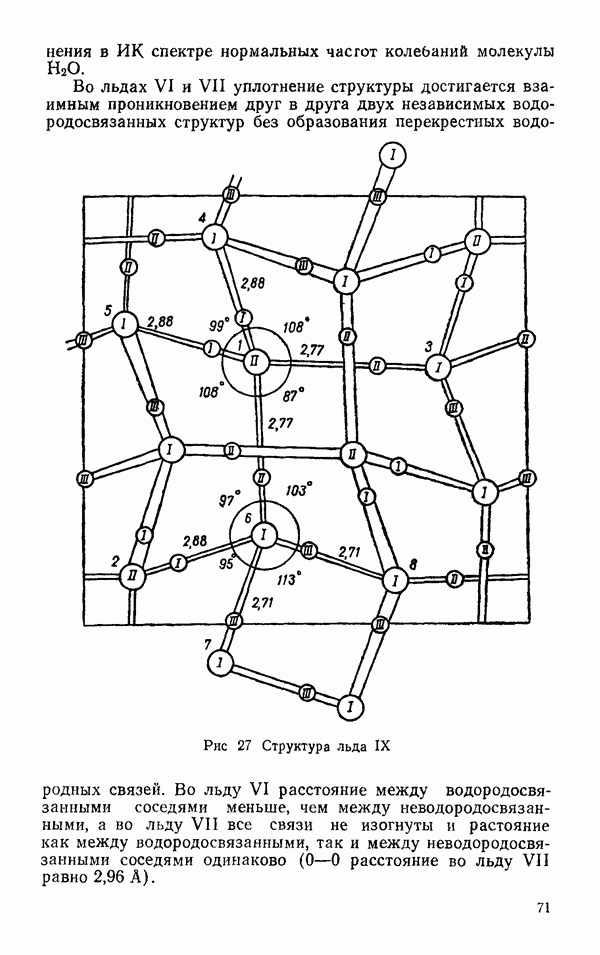
- § 2 ДРУГИЕ ЛЬДЫ
- Термодинамические свойства льдов
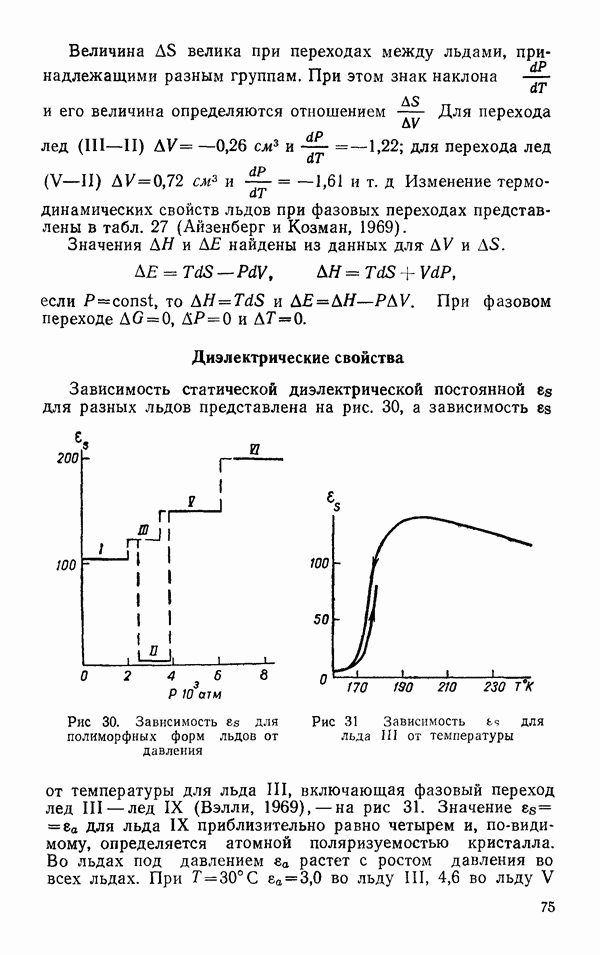
- Диэлектрические свойства
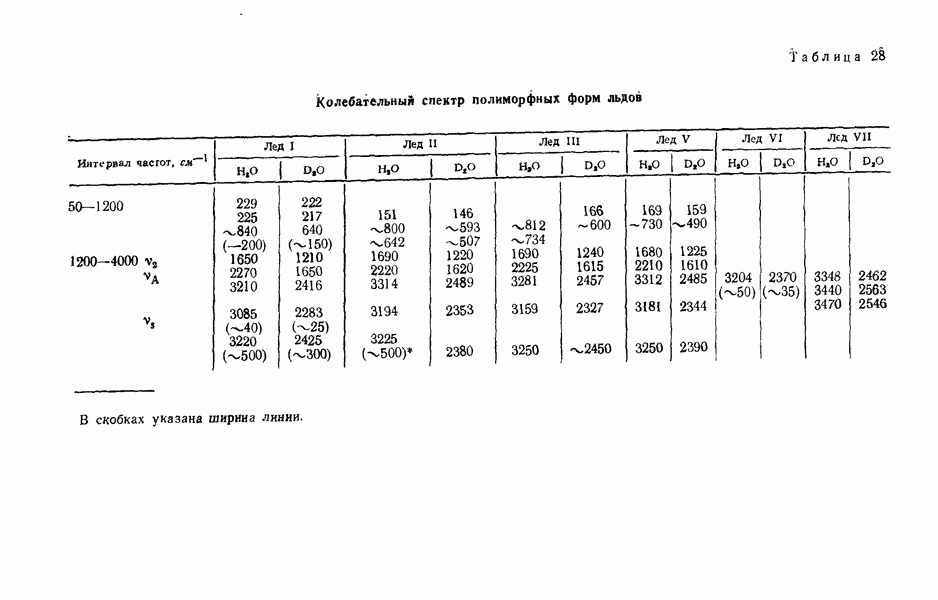
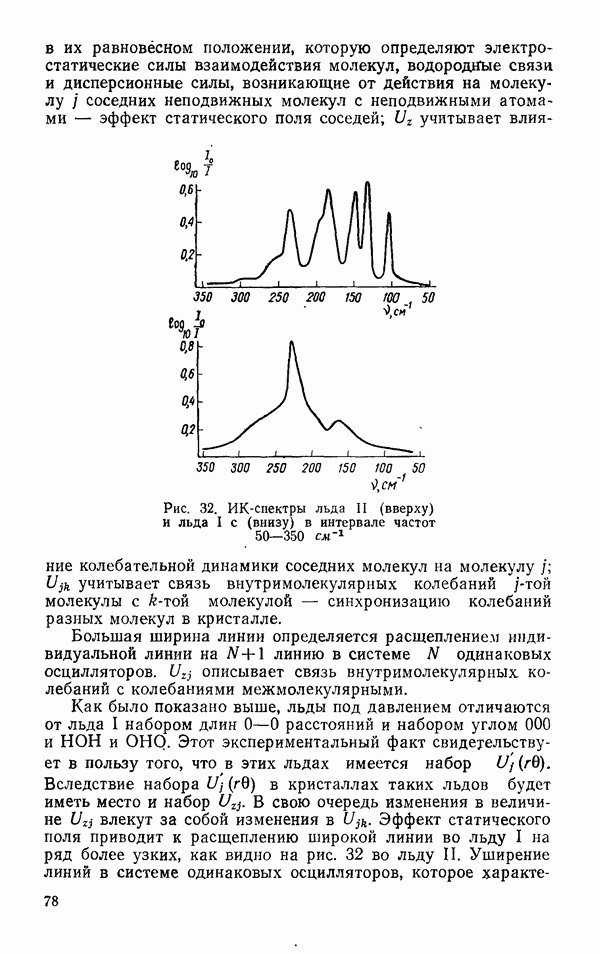
- Спектральные свойства
- ЗАКЛЮЧЕНИЕ
- Глава 4. ВОДОРОДНАЯ СВЯЗЬ
- § 2. СВОЙСТВА АТОМОВ, ОБРАЗУЮЩИХ ВОДОРОДНУЮ СВЯЗЬ
- § 3. МЕТОДЫ ВЫЧИСЛЕНИЯ ЭНЕРГИИ
- § 4. ПОЛУЭМПИРИЧЕСКИЕ ПОТЕНЦИАЛЬНЫЕ ФУНКЦИИ
- § 5. ТЕМПЕРАТУРНАЯ ЗАВИСИМОСТЬ ЭНЕРГЕТИЧЕСКИХ ХАРАКТЕРИСТИК ВОДОРОДНОЙ СВЯЗИ
- ЗАКЛЮЧЕНИЕ
- Глава 5. ЖИДКОЕ СОСТОЯНИЕ
- § 1. РАЗЛИЧНЫЕ ПОДХОДЫ К РЕШЕНИЮ ПРОБЛЕМЫ ЖИДКОГО СОСТОЯНИЯ
- § 2. СТРУКТУРА ЖИДКОСТИ
- § 3. ПЛАВЛЕНИЕ
- Глава 6. СВОЙСТВА ЖИДКОЙ ВОДЫ
- § 2. СПЕКТРАЛЬНЫЕ ДАННЫЕ
- § 3. ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА
- Теплоемкость
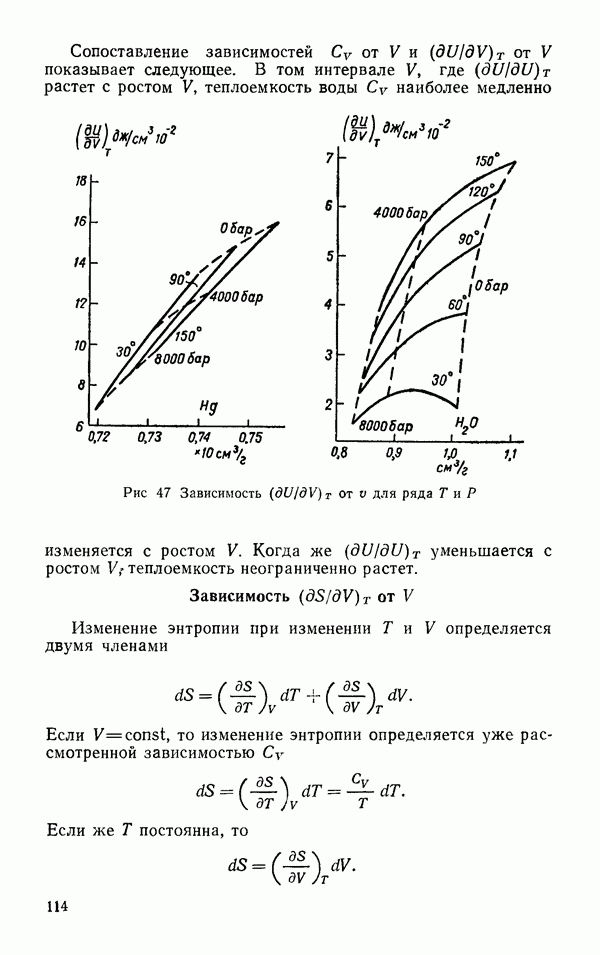
- Зависимость … от V (молекулярный объем)
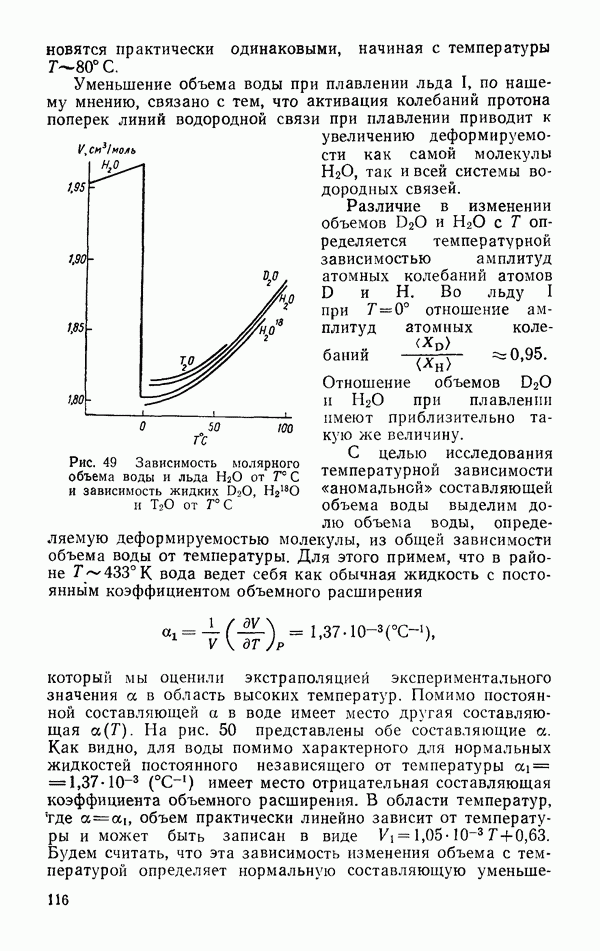
- Зависимость объема и его производных от температуры
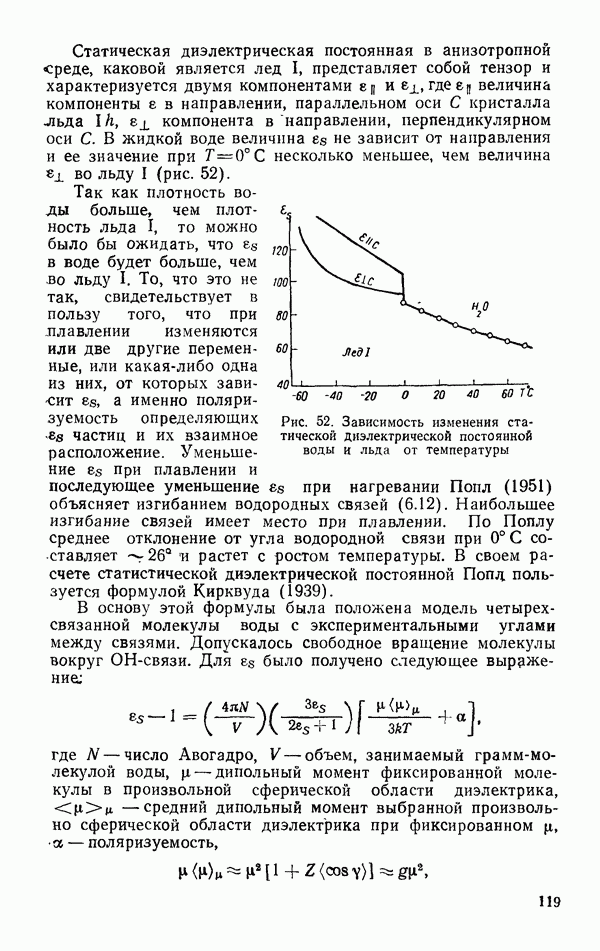
- § 4. СТАТИСТИЧЕСКАЯ ДИЭЛЕКТРИЧЕСКАЯ ПОСТОЯННАЯ
- § 5. ЯВЛЕНИЕ ПЕРЕНОСА
- Вязкость
- Теплопроводность
- Самодиффузия
- § 6. НЕКОТОРЫЕ ЭКСПЕРИМЕНТАЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ПРОЦЕССОВ МОЛЕКУЛЯРНОГО ВЗАИМОДЕЙСТВИЯ
- Молекулярное рассеяние света
- Вода как самодиссоциирующая среда
- § 7. ВОДА D2O
- ЗАКЛЮЧЕНИЕ
- ЛИТЕРАТУРА