| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ЗАКЛЮЧЕНИЕ
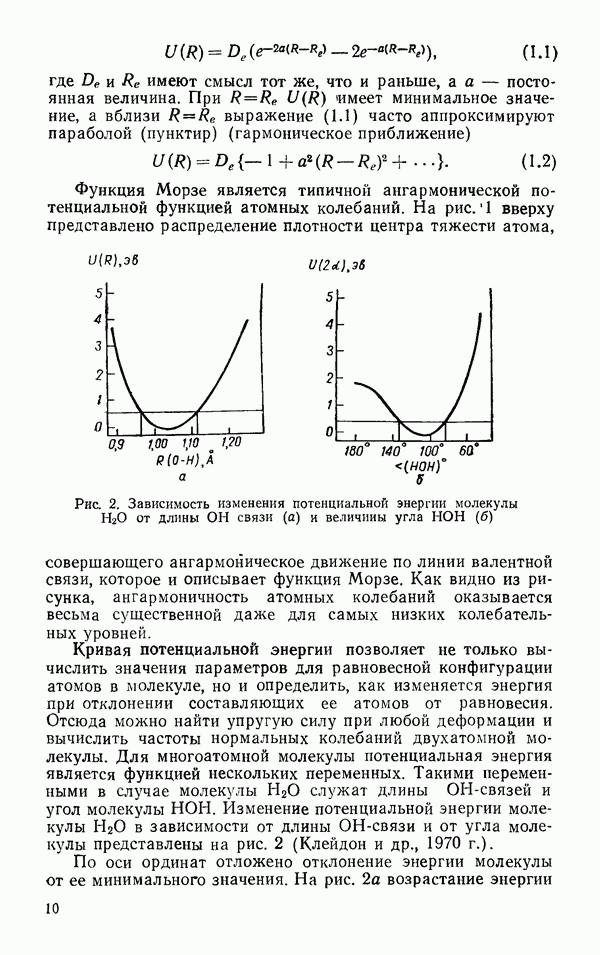
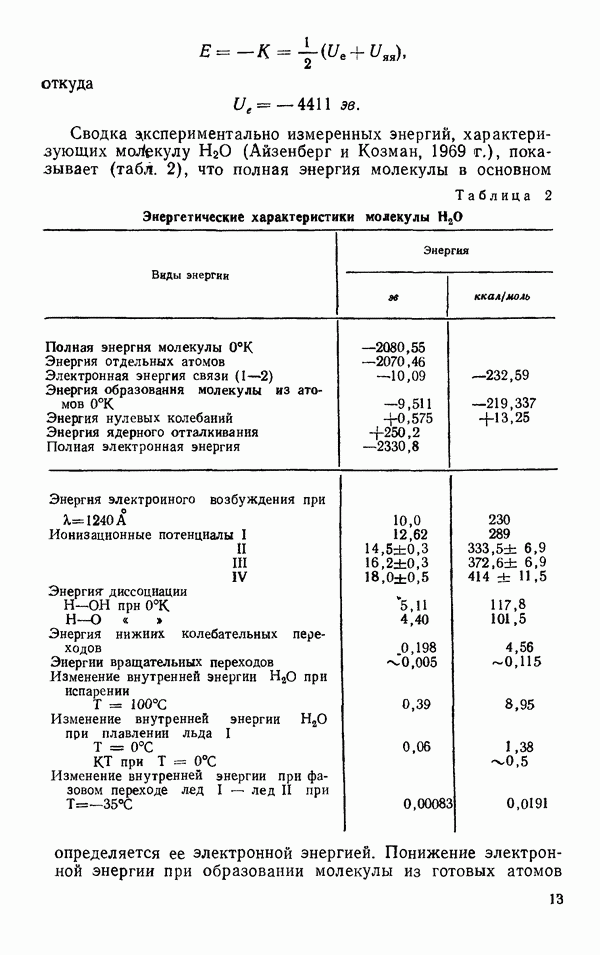
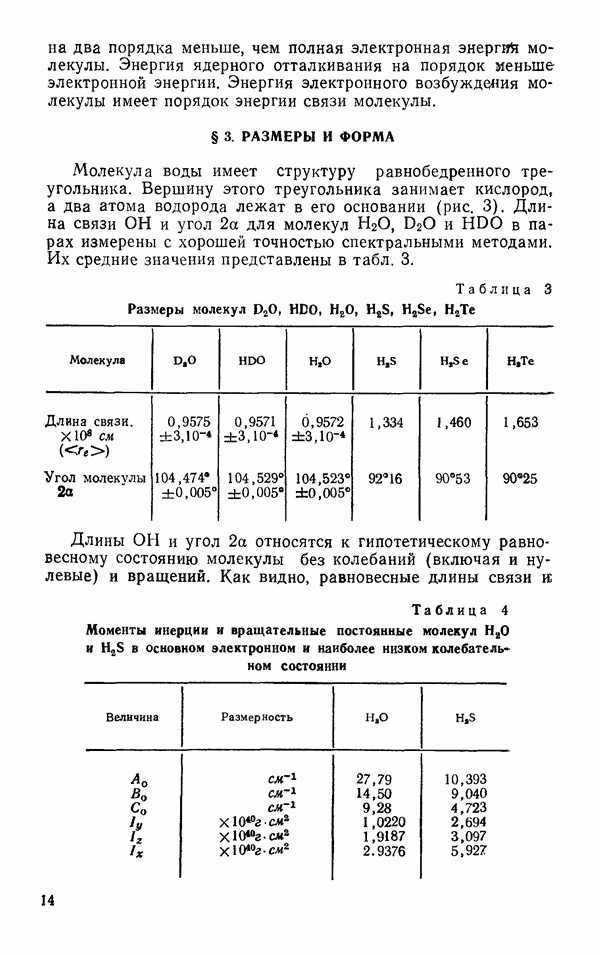
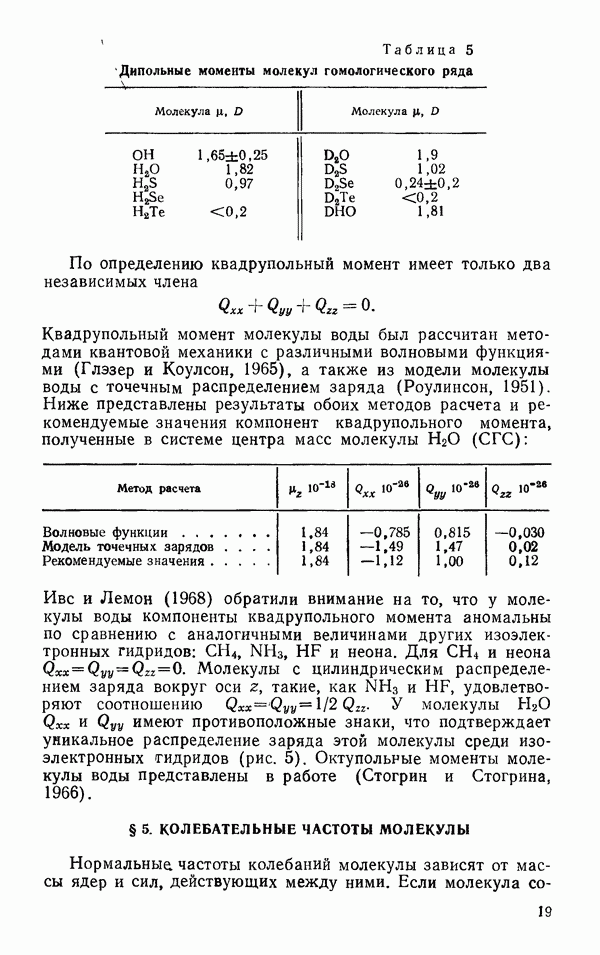
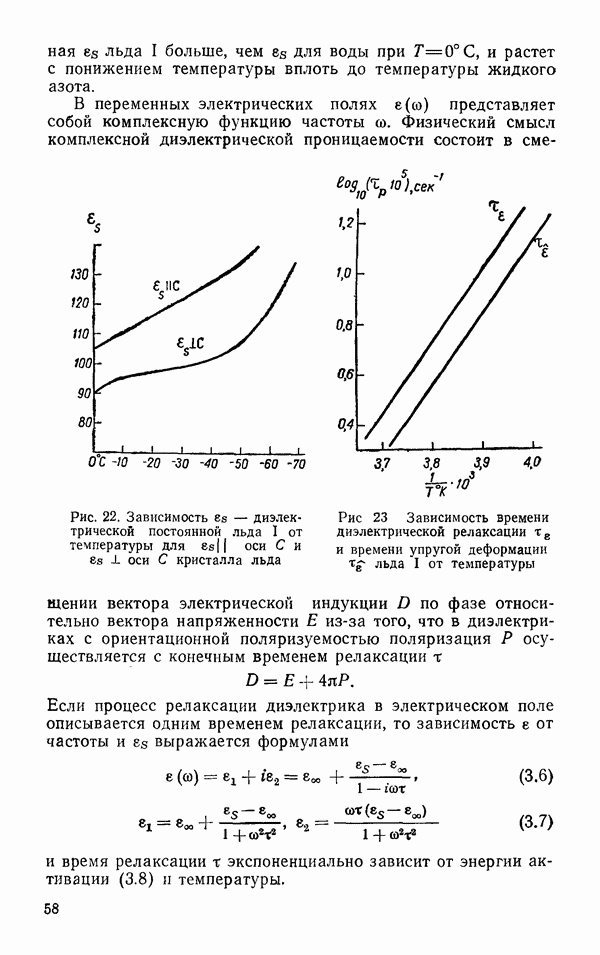
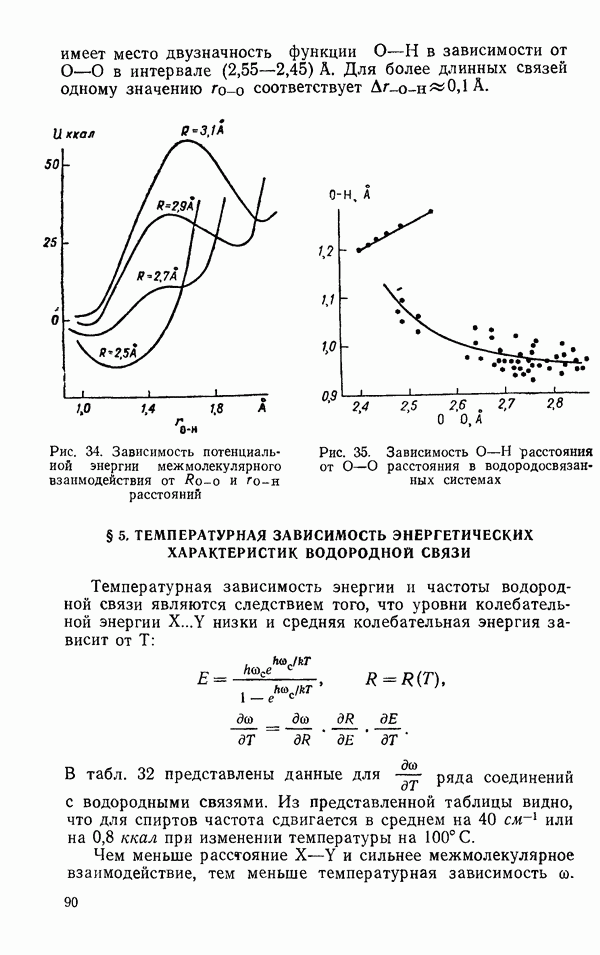
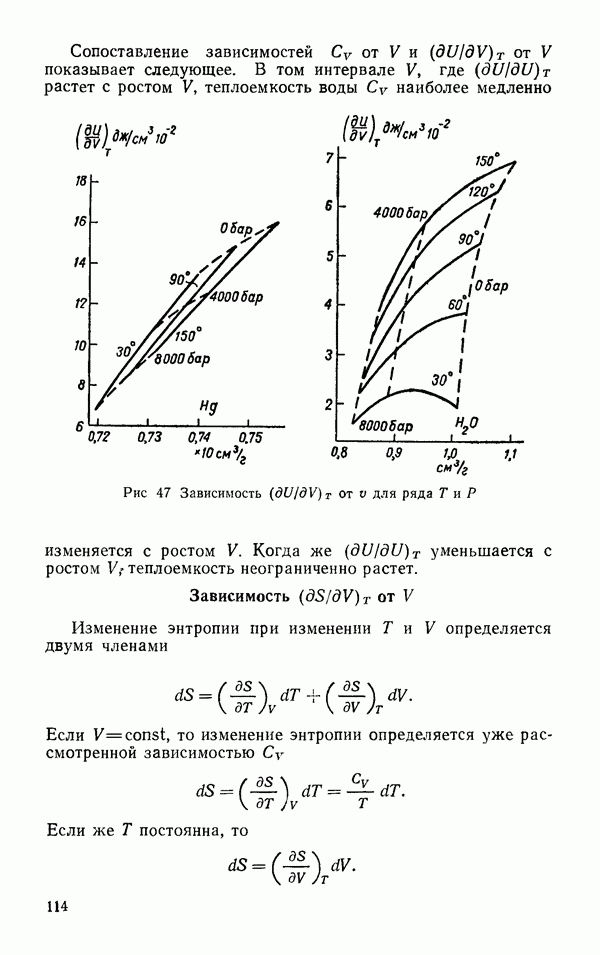
Сложный вид экспериментальной зависимости  от
от  (рис. 35) показывает, что энергия водородной связи не может быть однозначно определена при помощи парного потенциала взаимодействия, в связи с чем важны поиски новых подходов к проблеме водородной связи. К этому же выводу приводит и анализ свойств льдов. Энергия и равновесная структура кристаллов
(рис. 35) показывает, что энергия водородной связи не может быть однозначно определена при помощи парного потенциала взаимодействия, в связи с чем важны поиски новых подходов к проблеме водородной связи. К этому же выводу приводит и анализ свойств льдов. Энергия и равновесная структура кристаллов  существенно определяются объемом конденсированной фазы. Зависимость энергии межмолекулярного взаимодействия и структуры кристалла от объема показывает, что особенно существенными в этом случае оказываются коллективные взаимодействия молекул (дальнодействие).
существенно определяются объемом конденсированной фазы. Зависимость энергии межмолекулярного взаимодействия и структуры кристалла от объема показывает, что особенно существенными в этом случае оказываются коллективные взаимодействия молекул (дальнодействие).
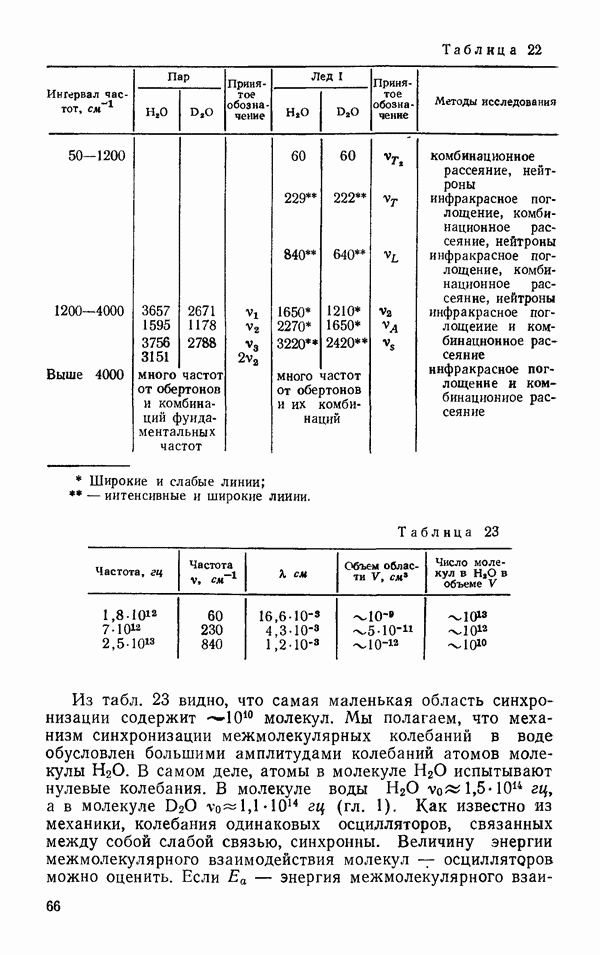
Дальнодействие описывается колебаниями решетки кристалла. В самом деле, существование длинноволновых колебаний решетки обусловлено синхронными колебаниями большой области кристалла, включающей 1011—1012 молекул, по крайней мере (гл. 3, табл. 23).
На основании рассмотренных свойств льдов можно сказать, что дальнодействующее взаимодействие во льдах не определяется переходами протонов по линии водородной связи от молекулы к молекуле (протонным беспорядком). Этот вывод следует из того факта, что средние частоты решеточных колебаний кристаллов с дефектами и кристаллов без дефектов близки.
Структура молекулы  с четырьмя локализованными в пространстве областями зарядов обусловливает тот факт, что как колебания протонов по линии
с четырьмя локализованными в пространстве областями зарядов обусловливает тот факт, что как колебания протонов по линии  связи, так и колебания протонов, перпендикулярные направлению этой связи, сопровождаются изменениями величины атомной поляризуемости молекулы
связи, так и колебания протонов, перпендикулярные направлению этой связи, сопровождаются изменениями величины атомной поляризуемости молекулы  с той же частотой (колебаниями величины диполеного момента молекулы). В связи с этим любой из двух типов атомных колебаний, представленных на рис. 36, или их комбинация будет приводить к дисперсионному взаимодействию осциллирующих диполей типа Лондона. Однако
с той же частотой (колебаниями величины диполеного момента молекулы). В связи с этим любой из двух типов атомных колебаний, представленных на рис. 36, или их комбинация будет приводить к дисперсионному взаимодействию осциллирующих диполей типа Лондона. Однако
в отличие от мгновенных атомных диполей молекулярные диполи во льдах колеблются по строго фиксированным направлениям, что приводит к тому, что их резонансное взаимодействие оказывается существенно более дальнодействующим, так как оно зависит от третьей, а не от шестой степени межмолекулярного расстояния.
Энергия такого дисперсионного взаимодействия велика из-за большой величины амплитуд атомных колебаний и сравнительно высоких частот колебаний атомов молекулы  т. е. определяется структурой молекулы
т. е. определяется структурой молекулы 

Рис. 36. Ангармонические колебания атома водорода вдоль линии  связи (а) и поперек линии
связи (а) и поперек линии  связи (б)
связи (б)
Введение чужих молекул в любые жидкости должно сопровождаться нарушением синхронизации колебаний электронов в атомах, определяющих дисперсионное взаимодействие Лондона. Однако радиус действия сил Лондона определяется величиной обратно пропорциональной шестой степени межмолекулярного расстояния и сравнительно невелик. В связи с этим существенные нарушения структуры растворителя будут иметь место, когда средние расстояния между молекулами растворяемого вещества будут порядка радиуса действия сил Ван-дер-Ваальса. При этих расстояниях, однако, сами растворенные молекулы уже начинают взаимодействовать друг с другом, так как радиусы Ван-дер-Ваальса для разных неполярных молекул мало отличаются друг от друга по порядку величины. Таким образом, в таких растворах нарушение дисперсионного взаимодействия растворителя растворенными молекулами и установление дисперсионого взаимодействия растворенных молекул между собой через растворитель как среду осуществляются приблизительно при одних и тех же концентрациях молекул.
Вода отличается от рассмотренных неполярных растворителей тем, что взаимодействие молекул в ней определяется не силами Ван-дер-Ваальса, а водородными связями, которые зависят от межмолекулярного расстояния обратно пропорционально третьей степеним расстояния. Таким образом, силы, синхронизирующие межмолекулярные взаимодействия в воде, оказываются существенно более дальнодействующими. В связи с этим введение чужих молекул в воду приводит к нарушению синхронизации взаимодействия одинаковых молекул
при существенно меньших значениях концентрации растворенного вещества, чем в других растворителях. Кроме того, в воде область концентраций установления контакта растворенная молекула — растворенная молекула и область концентраций, определяющих нарушение синхронизации межмолекулярных колебаний  не совпадают друг с другом. Поэтому в водных растворах неэлектролитов имеет место область концентраций растворенного вещества, в которой велики флуктуации плотности и сжимаемости растворителя
не совпадают друг с другом. Поэтому в водных растворах неэлектролитов имеет место область концентраций растворенного вещества, в которой велики флуктуации плотности и сжимаемости растворителя  (нарушена синхронизация в воде и не установлена связь между молекулами растворенного вещества).
(нарушена синхронизация в воде и не установлена связь между молекулами растворенного вещества).
| << Предыдущий параграф | Следующий параграф >> |
- Введение
- Глава 1. МОЛЕКУЛА H2O
- Энергия образования молекулы
- Полная энергия молекулы
- § 3. РАЗМЕРЫ И ФОРМА
- § 4. ЭЛЕКТРИЧЕСКИЕ СВОЙСТВА
- § 5. КОЛЕБАТЕЛЬНЫЕ ЧАСТОТЫ МОЛЕКУЛЫ
- ЗАКЛЮЧЕНИЕ
- Глава 2. СВОЙСТВА ПАРА
- Исследования межмолекулярных сил отталкивания
- § 2. УРАВНЕНИЯ СОСТОЯНИЯ РЕАЛЬНОГО ГАЗА
- Вириальная форма уравнения состояния
- Эмпирическое уравнение состояния
- § 3. ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА
- Термодинамические функции
- Зависимость термодинамических функций от P и T
- § 4. ВЯЗКОСТЬ
- Глава 3. СВОЙСТВА ЛЬДОВ
- § 1. ЛЕД
- Пластическая деформация монокристалла льда I
- Диэлектрические свойства льда 1
- Электропроводность льда
- Самодиффузия
- Спектральные свойства льда I
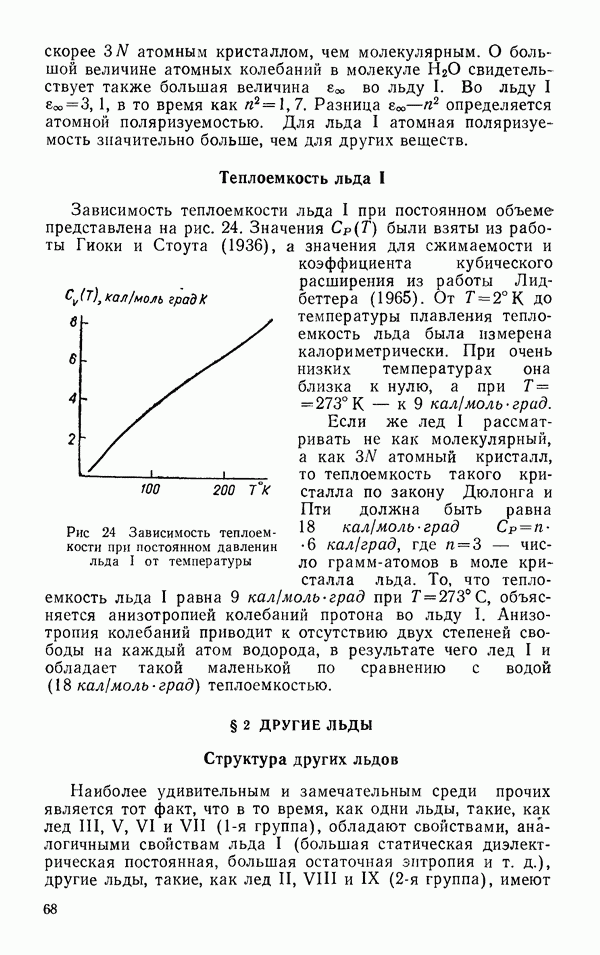
- Теплоемкость льда I
- § 2 ДРУГИЕ ЛЬДЫ
- Термодинамические свойства льдов
- Диэлектрические свойства
- Спектральные свойства
- ЗАКЛЮЧЕНИЕ
- Глава 4. ВОДОРОДНАЯ СВЯЗЬ
- § 2. СВОЙСТВА АТОМОВ, ОБРАЗУЮЩИХ ВОДОРОДНУЮ СВЯЗЬ
- § 3. МЕТОДЫ ВЫЧИСЛЕНИЯ ЭНЕРГИИ
- § 4. ПОЛУЭМПИРИЧЕСКИЕ ПОТЕНЦИАЛЬНЫЕ ФУНКЦИИ
- § 5. ТЕМПЕРАТУРНАЯ ЗАВИСИМОСТЬ ЭНЕРГЕТИЧЕСКИХ ХАРАКТЕРИСТИК ВОДОРОДНОЙ СВЯЗИ
- ЗАКЛЮЧЕНИЕ
- Глава 5. ЖИДКОЕ СОСТОЯНИЕ
- § 1. РАЗЛИЧНЫЕ ПОДХОДЫ К РЕШЕНИЮ ПРОБЛЕМЫ ЖИДКОГО СОСТОЯНИЯ
- § 2. СТРУКТУРА ЖИДКОСТИ
- § 3. ПЛАВЛЕНИЕ
- Глава 6. СВОЙСТВА ЖИДКОЙ ВОДЫ
- § 2. СПЕКТРАЛЬНЫЕ ДАННЫЕ
- § 3. ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА
- Теплоемкость
- Зависимость … от V (молекулярный объем)
- Зависимость объема и его производных от температуры
- § 4. СТАТИСТИЧЕСКАЯ ДИЭЛЕКТРИЧЕСКАЯ ПОСТОЯННАЯ
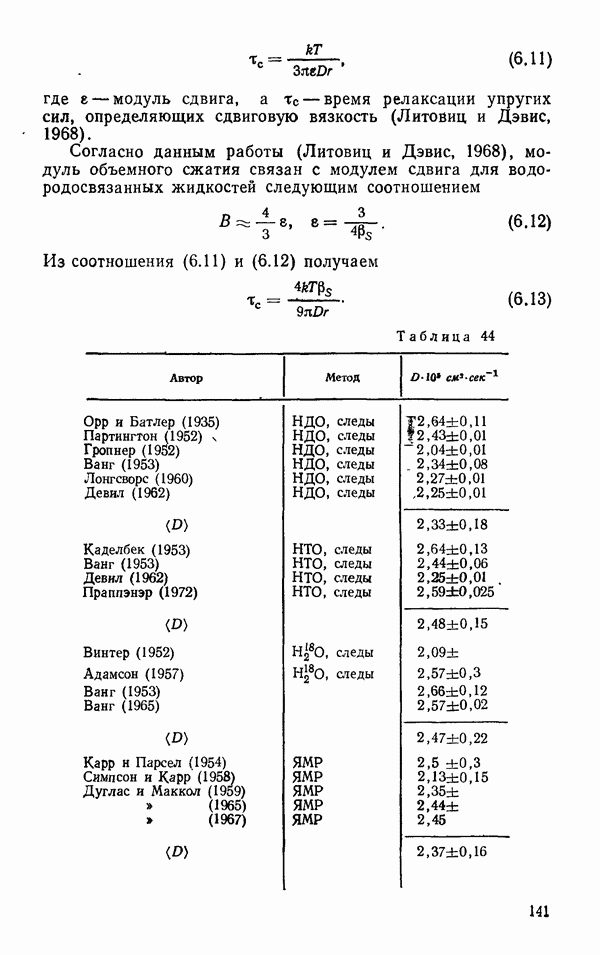
- § 5. ЯВЛЕНИЕ ПЕРЕНОСА
- Вязкость
- Теплопроводность
- Самодиффузия
- § 6. НЕКОТОРЫЕ ЭКСПЕРИМЕНТАЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ПРОЦЕССОВ МОЛЕКУЛЯРНОГО ВЗАИМОДЕЙСТВИЯ
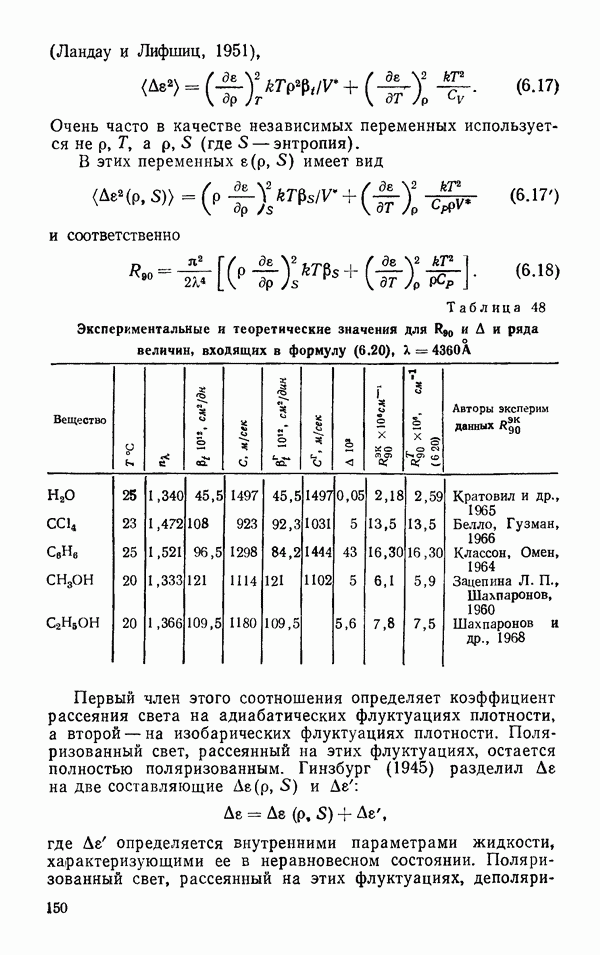
- Молекулярное рассеяние света
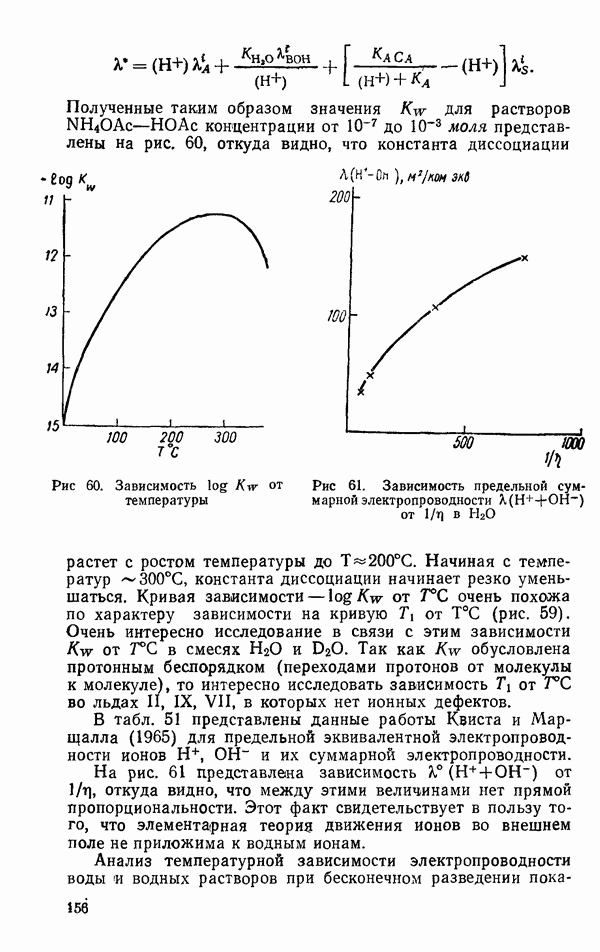
- Вода как самодиссоциирующая среда
- § 7. ВОДА D2O
- ЗАКЛЮЧЕНИЕ
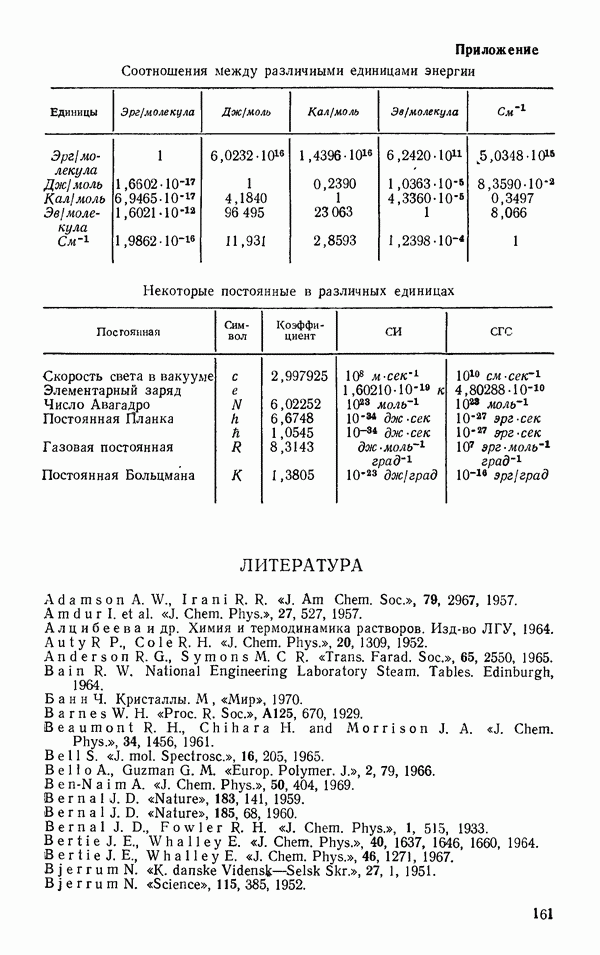
- ЛИТЕРАТУРА