| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
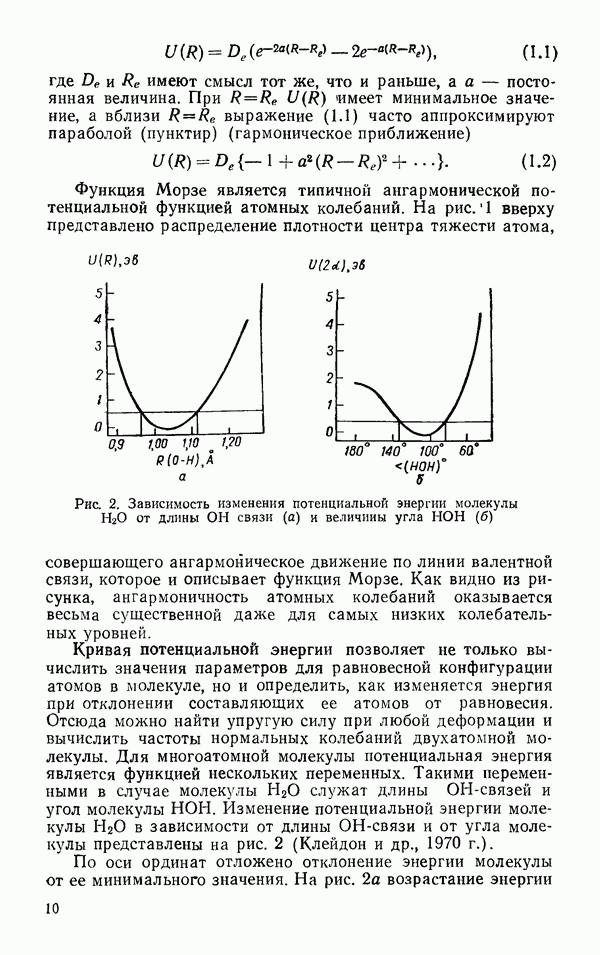
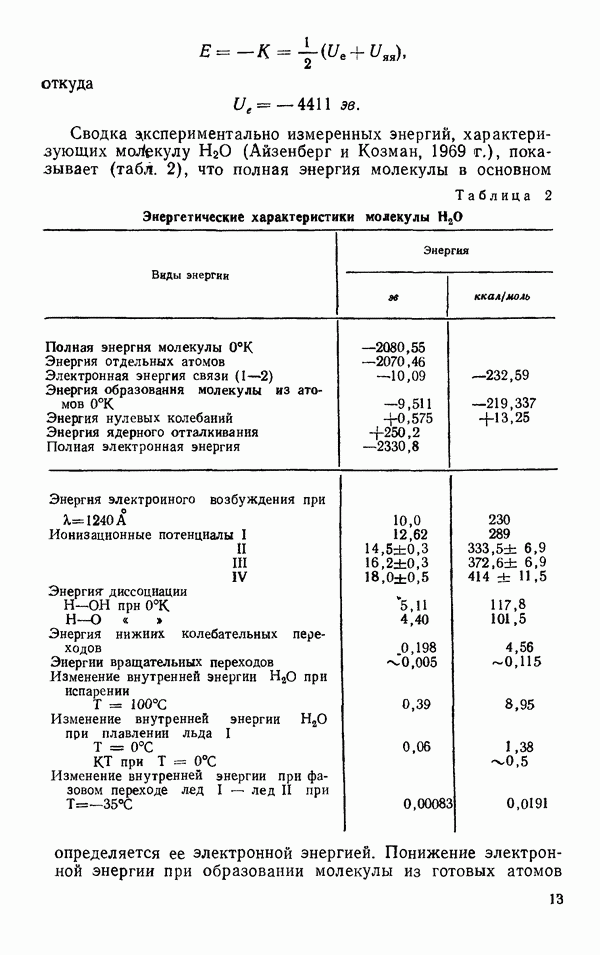
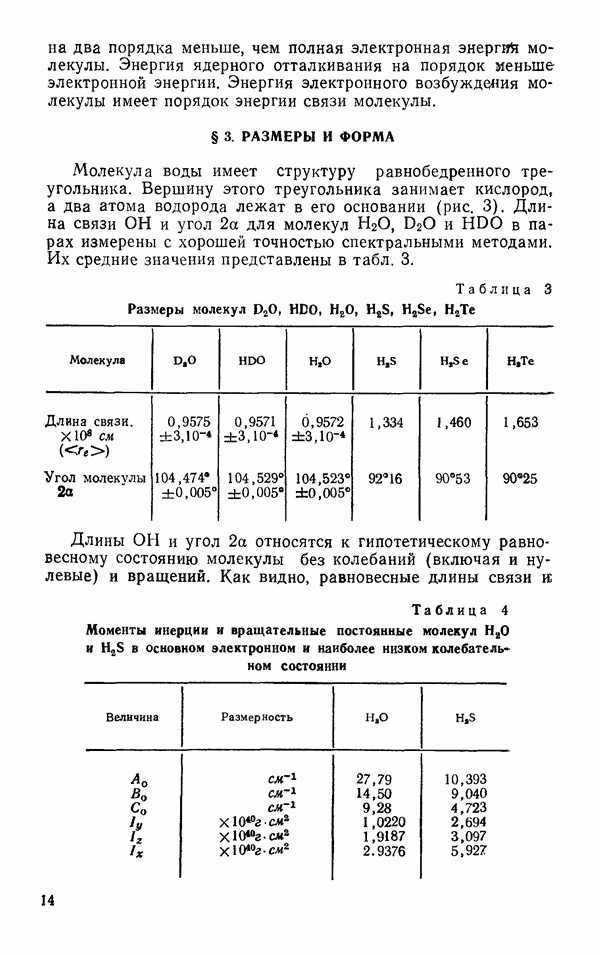
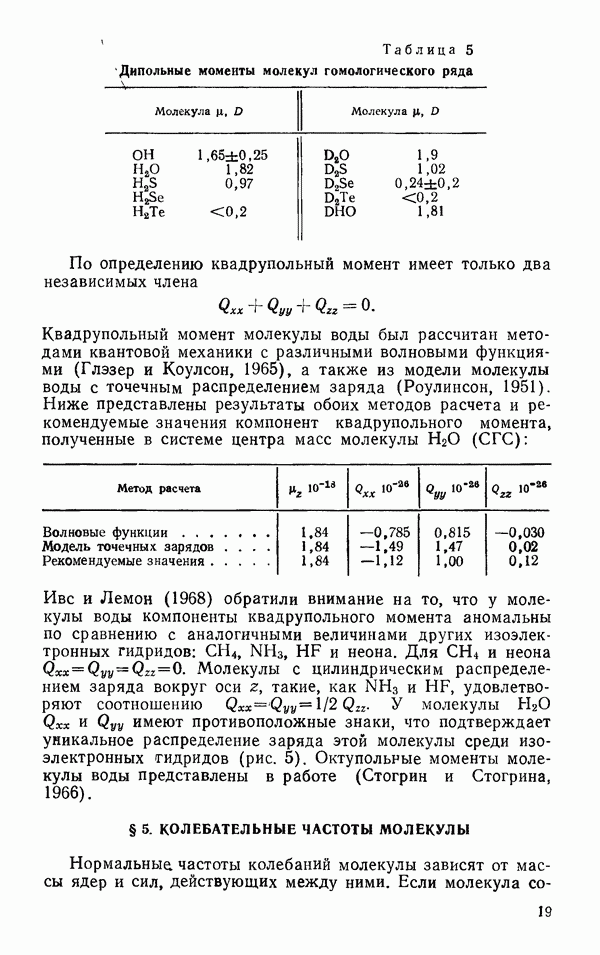
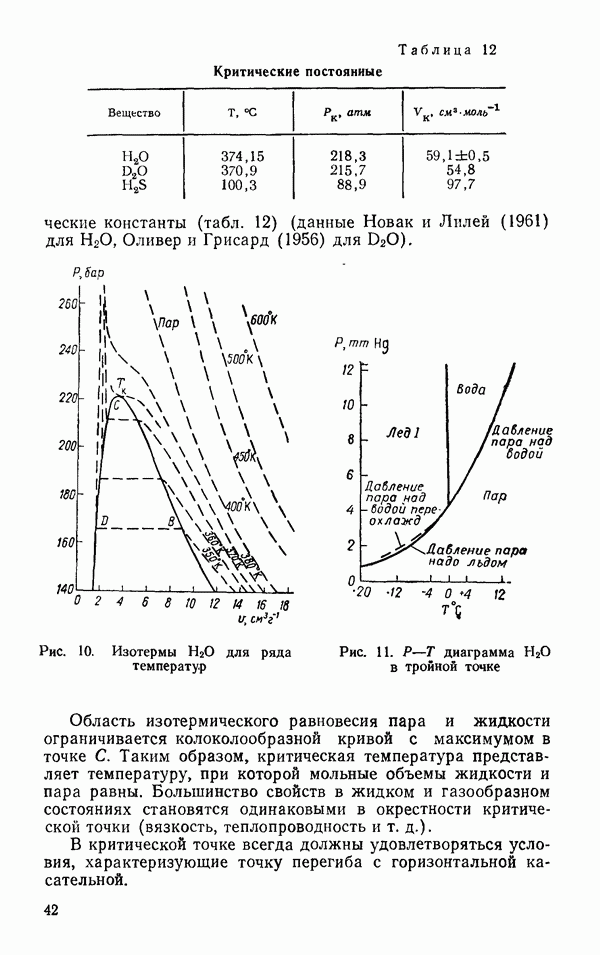
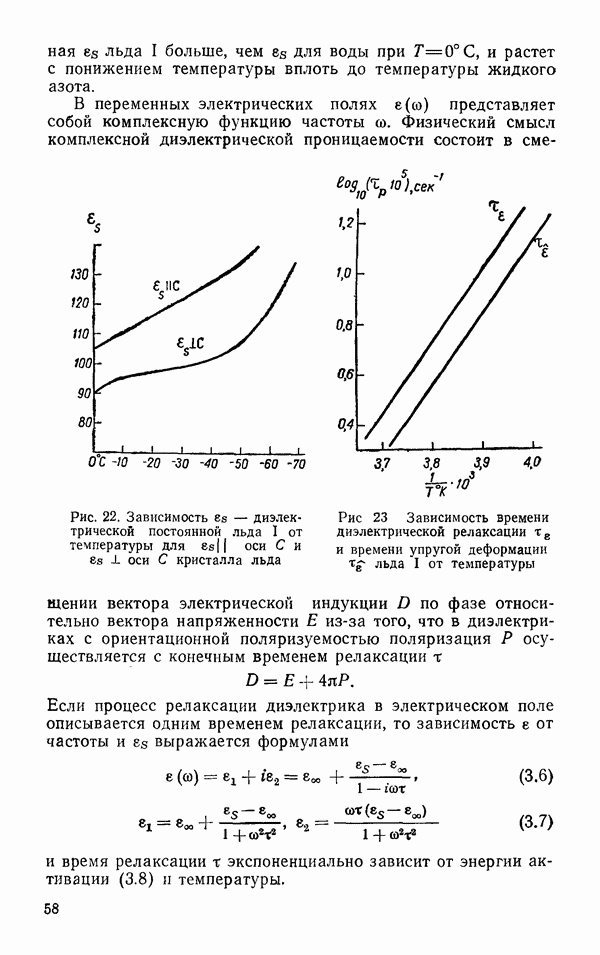
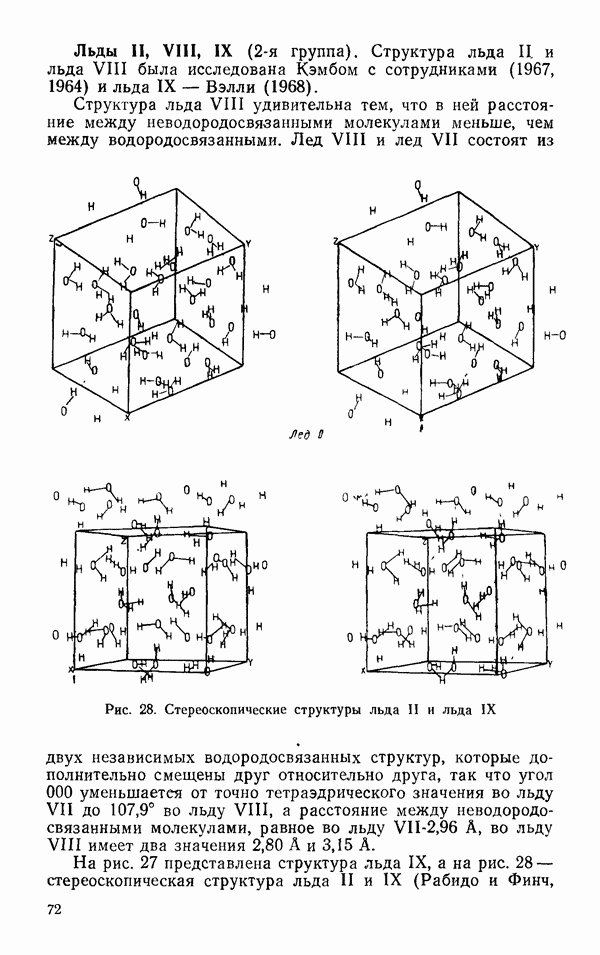
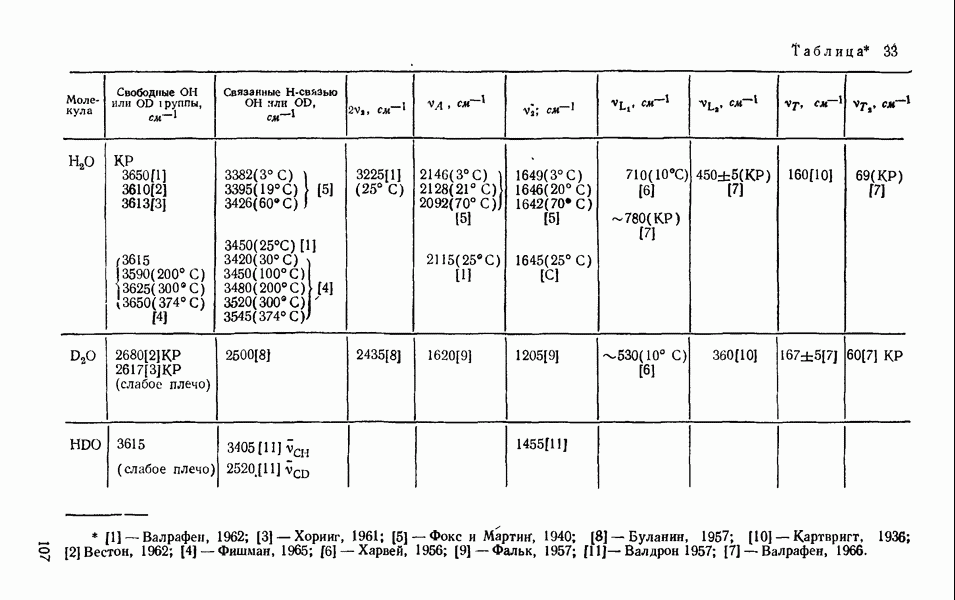
Глава 6. СВОЙСТВА ЖИДКОЙ ВОДЫ
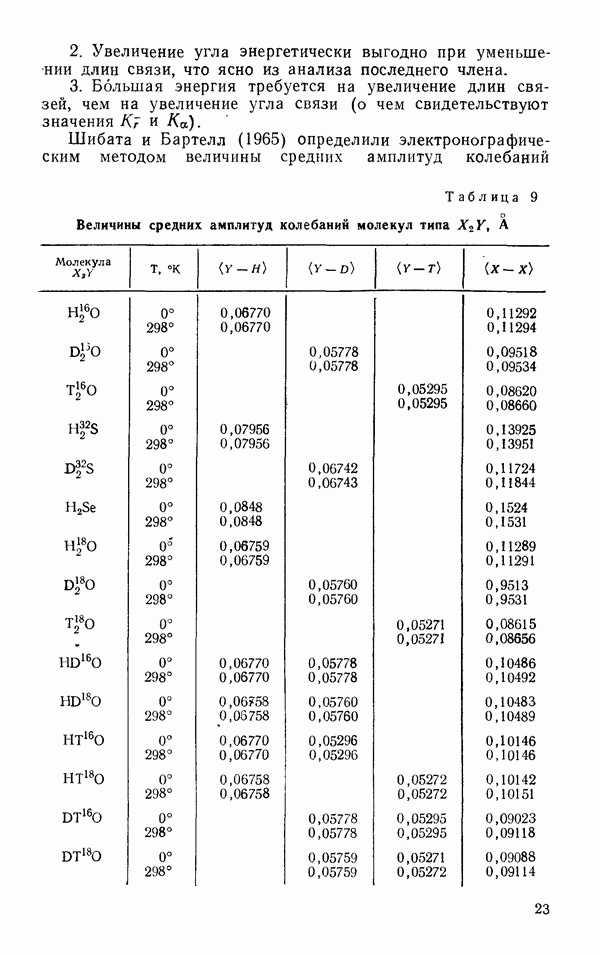
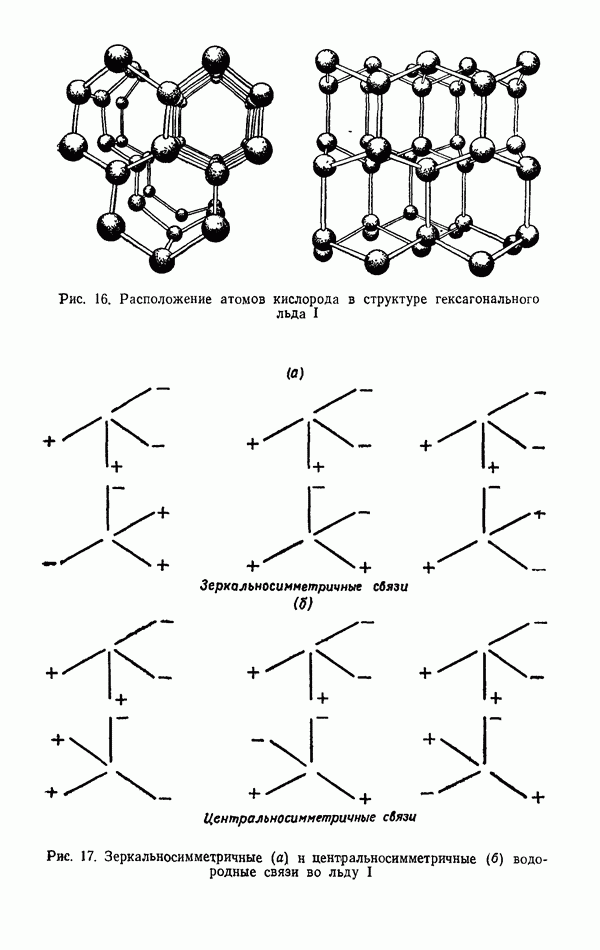
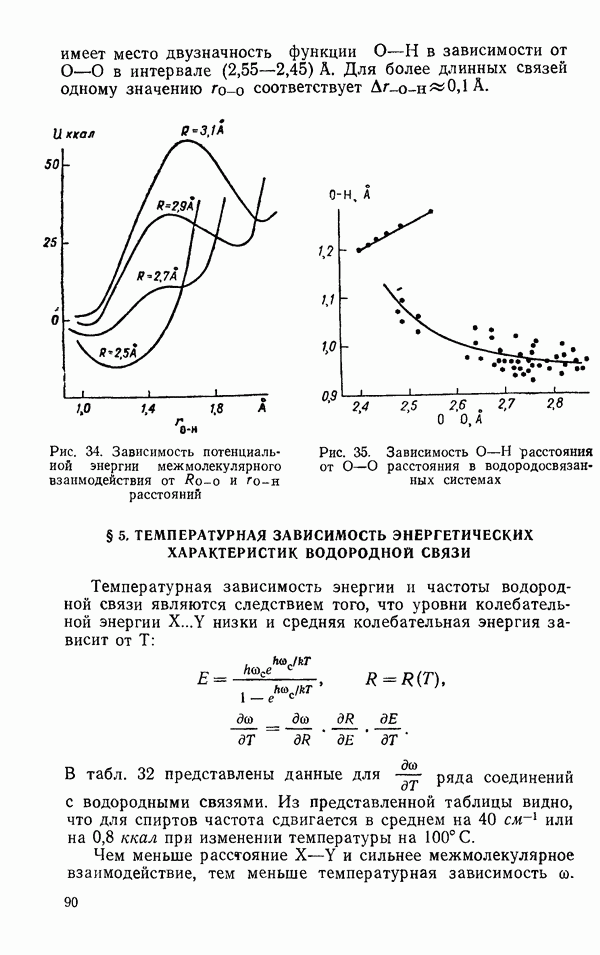
Жидкая вода при  плотнее, чем лед I приблизительно на 10%. Это свидетельствует о том, что структурный беспорядок в жидкой воде обладает своими преимуществами в смысле упаковки молекул. Каждая молекула воды в воде, как и во льдах, имеет четырех соседей, и межмолекулярное взаимодействие в воде определяется водородными связями. Отсюда следует, что водородные связи в жидкой воде обладают особенностями, допускающими более плотную упаковку молекул, чем во льду. Чтобы понять, в чем эти особенности, рассмотрим сначала те экспериментальные факты, которые характеризуют энергетику водородных связей в воде. К ним относятся данные о длине водородной связи
плотнее, чем лед I приблизительно на 10%. Это свидетельствует о том, что структурный беспорядок в жидкой воде обладает своими преимуществами в смысле упаковки молекул. Каждая молекула воды в воде, как и во льдах, имеет четырех соседей, и межмолекулярное взаимодействие в воде определяется водородными связями. Отсюда следует, что водородные связи в жидкой воде обладают особенностями, допускающими более плотную упаковку молекул, чем во льду. Чтобы понять, в чем эти особенности, рассмотрим сначала те экспериментальные факты, которые характеризуют энергетику водородных связей в воде. К ним относятся данные о длине водородной связи  о длине
о длине  -связи, частотах
-связи, частотах  и ОН-колебаний, а также данные относительно межмолекулярных колебаний и об амплитудах колебаний отдельных атомов молекулы
и ОН-колебаний, а также данные относительно межмолекулярных колебаний и об амплитудах колебаний отдельных атомов молекулы  в воде. После этого рассмотрим явления переноса, которые наиболее ярко характеризуют жидкое состояние.
в воде. После этого рассмотрим явления переноса, которые наиболее ярко характеризуют жидкое состояние.
§ 1. РАДИАЛЬНАЯ ФУНКЦИЯ РАСПРЕДЕЛЕНИЯ МОЛЕКУЛ
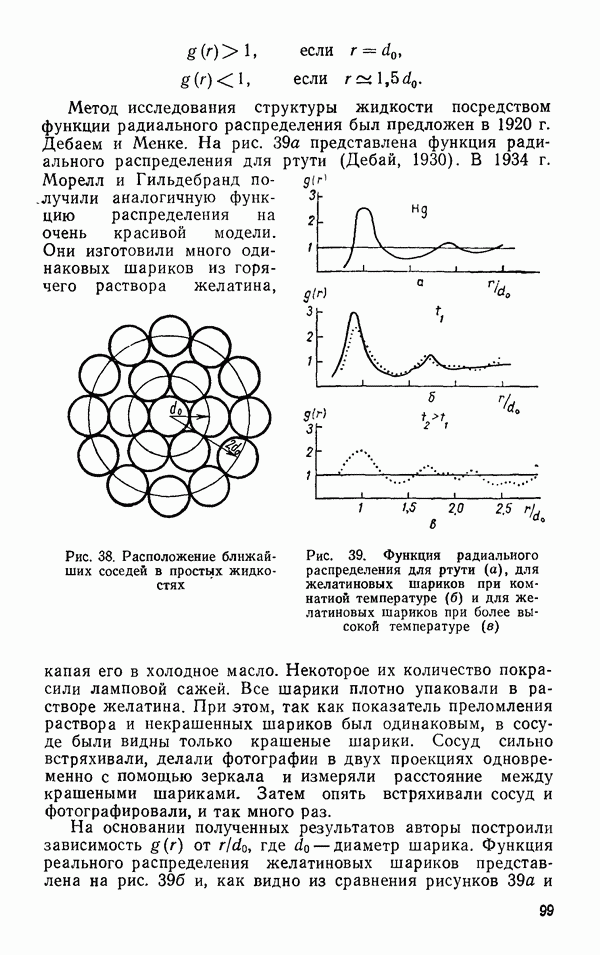
На рис. 42 представлена радиальная функция распределения молекул  в воде при
в воде при  полученная с помощью дифракции рентгеновских лучей от образца жидкой воды (Денфорд и Леви, 1962). Первый максимум кривой радиального распределения находится на расстоянии 2,9 А, которое на 6% больше, чем расстояние
полученная с помощью дифракции рентгеновских лучей от образца жидкой воды (Денфорд и Леви, 1962). Первый максимум кривой радиального распределения находится на расстоянии 2,9 А, которое на 6% больше, чем расстояние  (лед I). Площадь под кривой согласуется с предположением четырех соседей около каждой молекулы
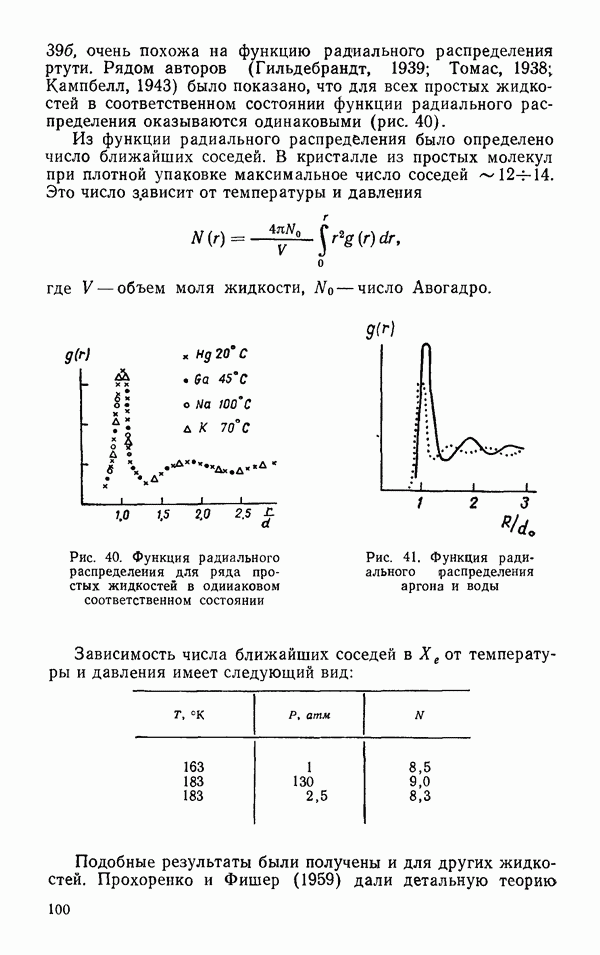
(лед I). Площадь под кривой согласуется с предположением четырех соседей около каждой молекулы  Число следующих соседей, однако, оказывается большим, чем во льду
Число следующих соседей, однако, оказывается большим, чем во льду  расстояние до них оказывается большим, чем во льду I, а именно: вместо 4,7 А во льду I, 4,9 А в воде.
расстояние до них оказывается большим, чем во льду I, а именно: вместо 4,7 А во льду I, 4,9 А в воде.
Имеется два различных объяснения этому экспериментальному факту. Первое основывается на предположении, что вода представляет собой смесь льда и пара. Согласно этой модели, уплотнение структуры связано с тем, что пар заполняет пустоты льда (Самойлов, 1946; Денфорд и Леви, 1962).
Вторая гипотеза состоит в том, что характер водородных связей изменяется при плавлении. Водородные связи в воде изогнуты, в то время как во льду I они линейны (Попл, 1951; Зацепина, 1970).
Против первой гипотезы свидетельствует тот факт, что во льдах ни при каком давлении повышение плотности не сопровождается заполнением пустот структуры льда 
Во многих льдах под давлением уплотнение структуры сопровождается не просто увеличением  -расстояний между ближайшими соседями, а переходом от единого расстояния между
-расстояний между ближайшими соседями, а переходом от единого расстояния между  во льду I к набору расстояний во льдах под давлением.
во льду I к набору расстояний во льдах под давлением.

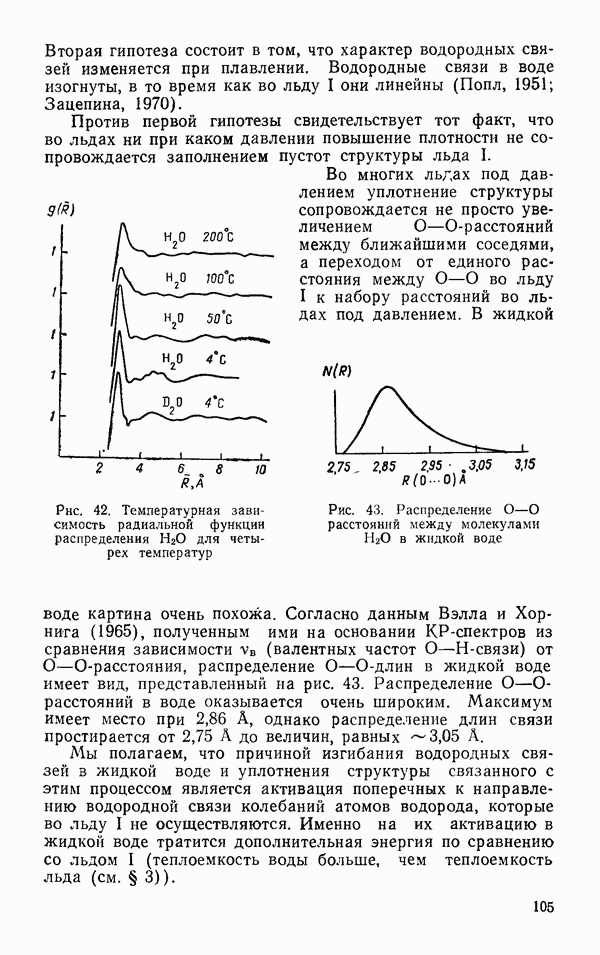
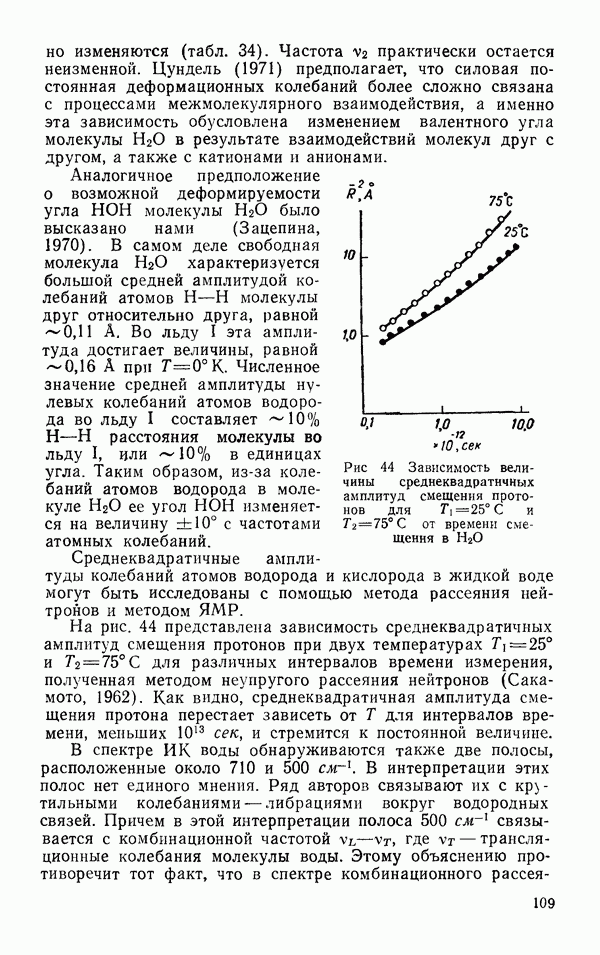
Рис. 42. Температурная зависимость радиальной функции распределения  для четырех температур воде картина очень похожа.
для четырех температур воде картина очень похожа.

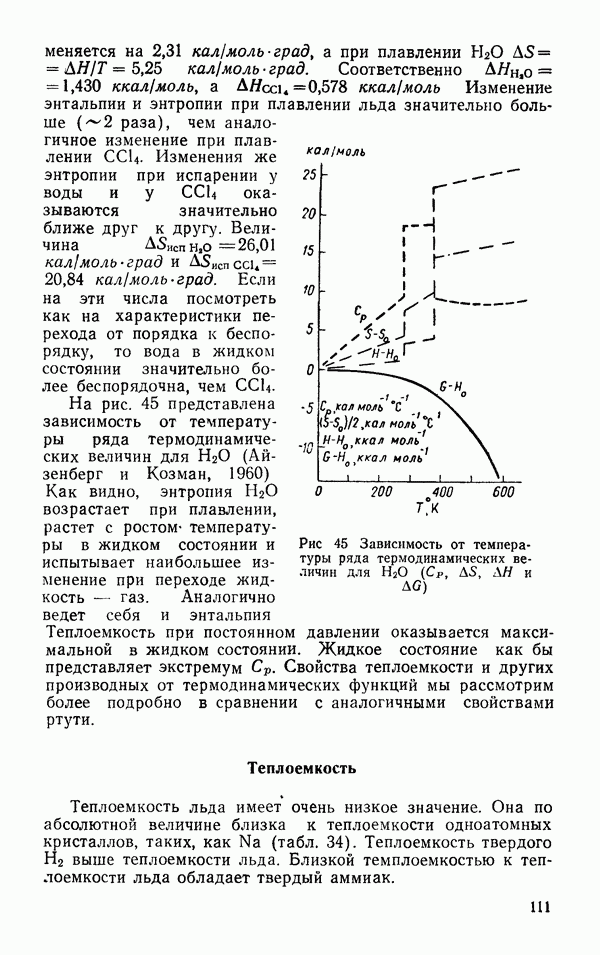
Рис. 43. Распределение  расстояний между молекулами
расстояний между молекулами  в жидкой воде
в жидкой воде
В жидкой воде картина очень похожа. Согласно данным Вэлла и Хорнига (1965), полученным ими на основании КР-спектров из сравнения зависимости  (валентных частот
(валентных частот  -связи) от
-связи) от  -расстояния, распределение
-расстояния, распределение  -длин в жидкой воде имеет вид, представленный на рис. 43. Распределение
-длин в жидкой воде имеет вид, представленный на рис. 43. Распределение  -расстояний в воде оказывается очень широким. Максимум имеет место при 2,86 А, однако распределение длин связи простирается от 2,75 А до величин, равных
-расстояний в воде оказывается очень широким. Максимум имеет место при 2,86 А, однако распределение длин связи простирается от 2,75 А до величин, равных  .
.
Мы полагаем, что причиной изгибания водородных связей в жидкой воде и уплотнения структуры связанного с этим процессом является активация поперечных к направлению водородной связи колебаний атомов водорода, которые во льду I не осуществляются. Именно на их активацию в жидкой воде тратится дополнительная энергия по сравнению со льдом I (теплоемкость воды больше, чем теплоемкость льда (см. § 3)).
| << Предыдущий параграф | Следующий параграф >> |
- Введение
- Глава 1. МОЛЕКУЛА H2O
- Энергия образования молекулы
- Полная энергия молекулы
- § 3. РАЗМЕРЫ И ФОРМА
- § 4. ЭЛЕКТРИЧЕСКИЕ СВОЙСТВА
- § 5. КОЛЕБАТЕЛЬНЫЕ ЧАСТОТЫ МОЛЕКУЛЫ
- ЗАКЛЮЧЕНИЕ
- Глава 2. СВОЙСТВА ПАРА
- Исследования межмолекулярных сил отталкивания
- § 2. УРАВНЕНИЯ СОСТОЯНИЯ РЕАЛЬНОГО ГАЗА
- Вириальная форма уравнения состояния
- Эмпирическое уравнение состояния
- § 3. ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА
- Термодинамические функции
- Зависимость термодинамических функций от P и T
- § 4. ВЯЗКОСТЬ
- Глава 3. СВОЙСТВА ЛЬДОВ
- § 1. ЛЕД
- Пластическая деформация монокристалла льда I
- Диэлектрические свойства льда 1
- Электропроводность льда
- Самодиффузия
- Спектральные свойства льда I
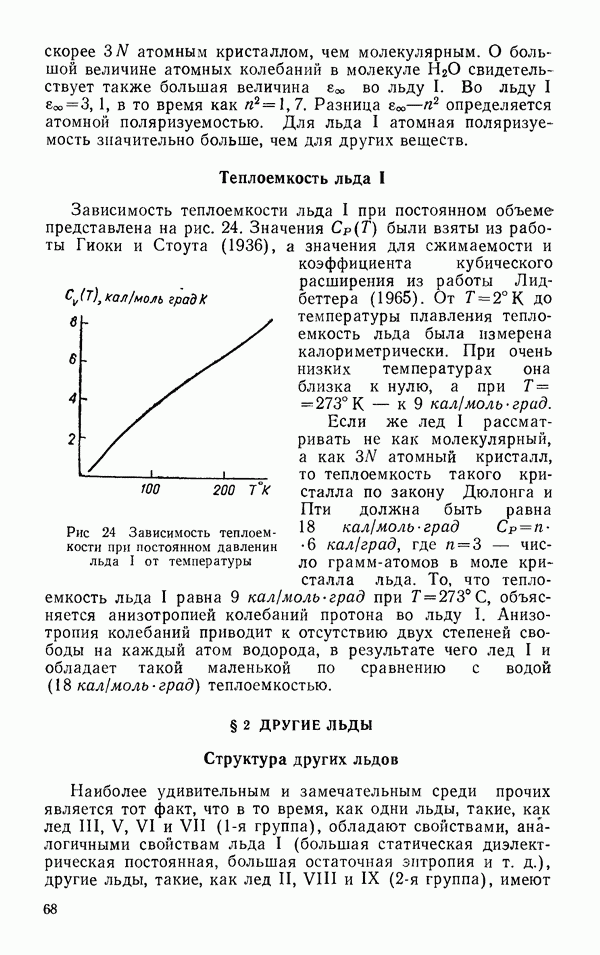
- Теплоемкость льда I
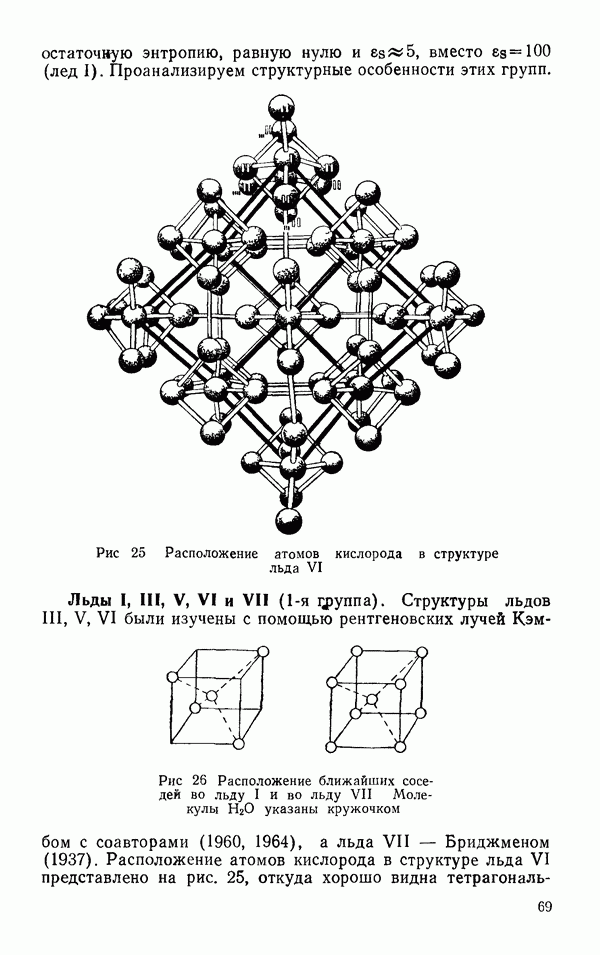
- § 2 ДРУГИЕ ЛЬДЫ
- Термодинамические свойства льдов
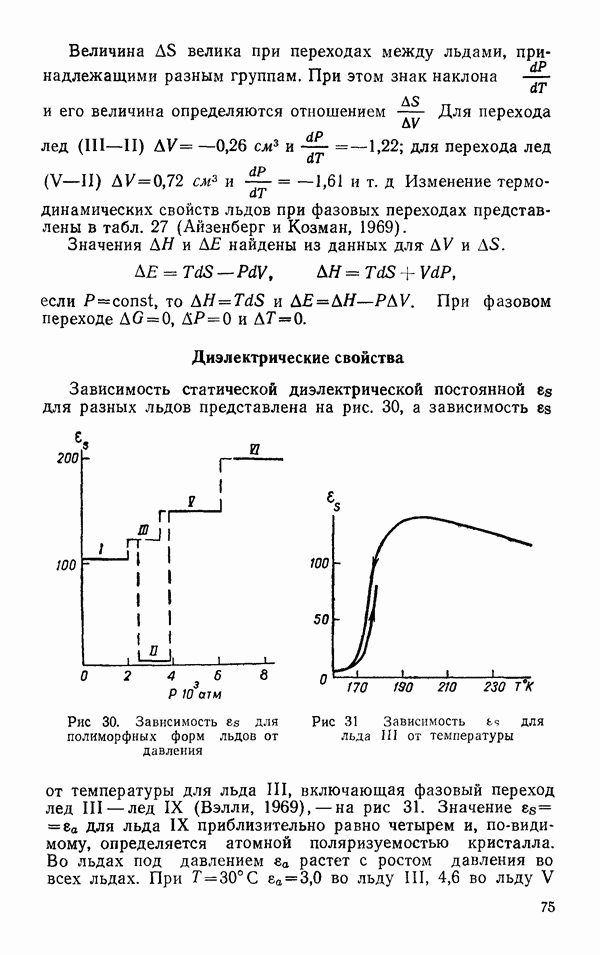
- Диэлектрические свойства
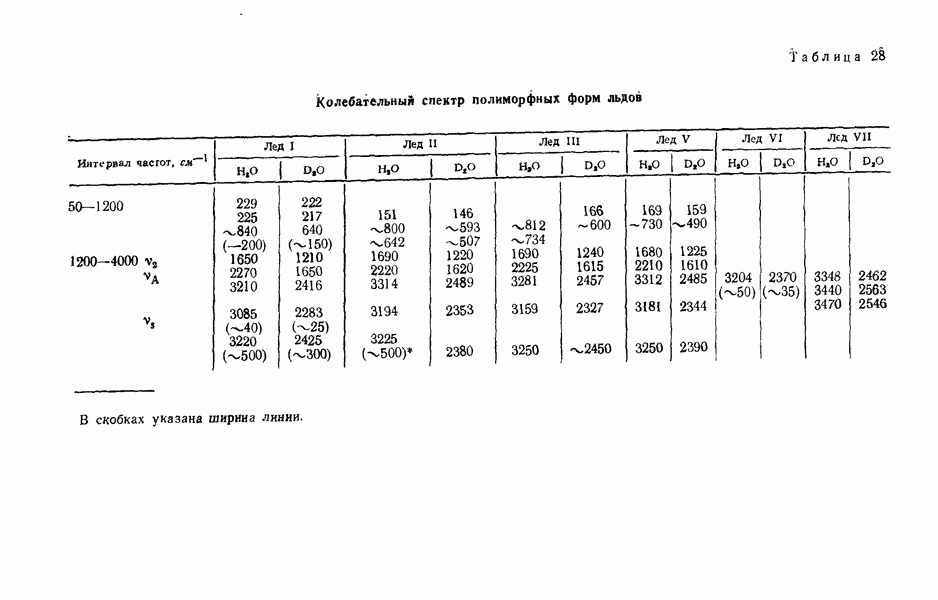
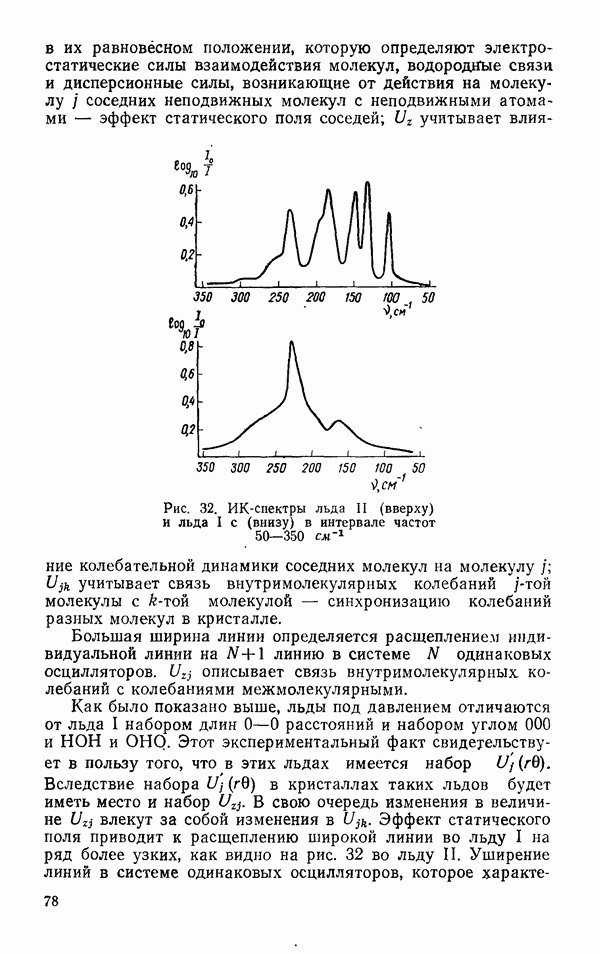
- Спектральные свойства
- ЗАКЛЮЧЕНИЕ
- Глава 4. ВОДОРОДНАЯ СВЯЗЬ
- § 2. СВОЙСТВА АТОМОВ, ОБРАЗУЮЩИХ ВОДОРОДНУЮ СВЯЗЬ
- § 3. МЕТОДЫ ВЫЧИСЛЕНИЯ ЭНЕРГИИ
- § 4. ПОЛУЭМПИРИЧЕСКИЕ ПОТЕНЦИАЛЬНЫЕ ФУНКЦИИ
- § 5. ТЕМПЕРАТУРНАЯ ЗАВИСИМОСТЬ ЭНЕРГЕТИЧЕСКИХ ХАРАКТЕРИСТИК ВОДОРОДНОЙ СВЯЗИ
- ЗАКЛЮЧЕНИЕ
- Глава 5. ЖИДКОЕ СОСТОЯНИЕ
- § 1. РАЗЛИЧНЫЕ ПОДХОДЫ К РЕШЕНИЮ ПРОБЛЕМЫ ЖИДКОГО СОСТОЯНИЯ
- § 2. СТРУКТУРА ЖИДКОСТИ
- § 3. ПЛАВЛЕНИЕ
- Глава 6. СВОЙСТВА ЖИДКОЙ ВОДЫ
- § 2. СПЕКТРАЛЬНЫЕ ДАННЫЕ
- § 3. ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА
- Теплоемкость
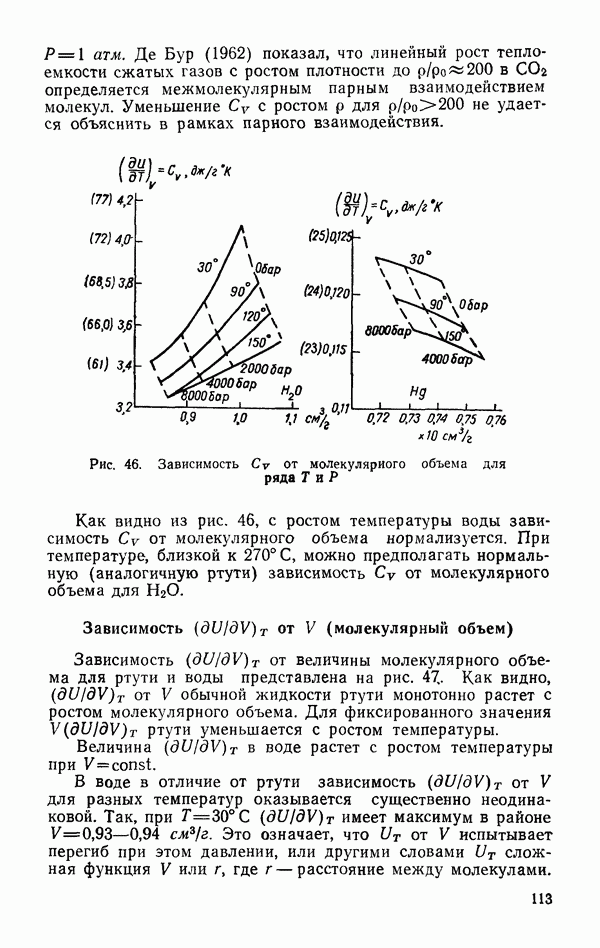
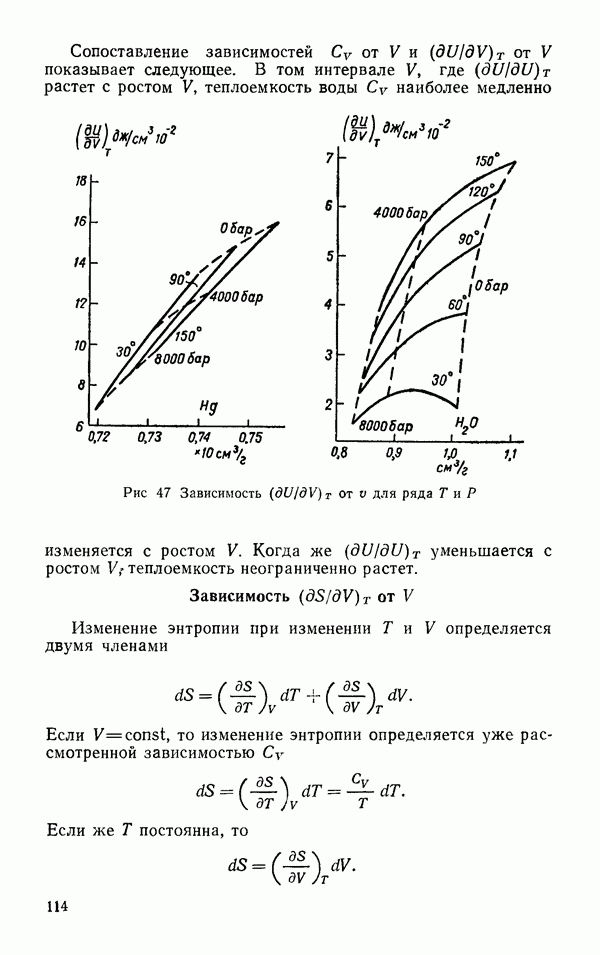
- Зависимость … от V (молекулярный объем)
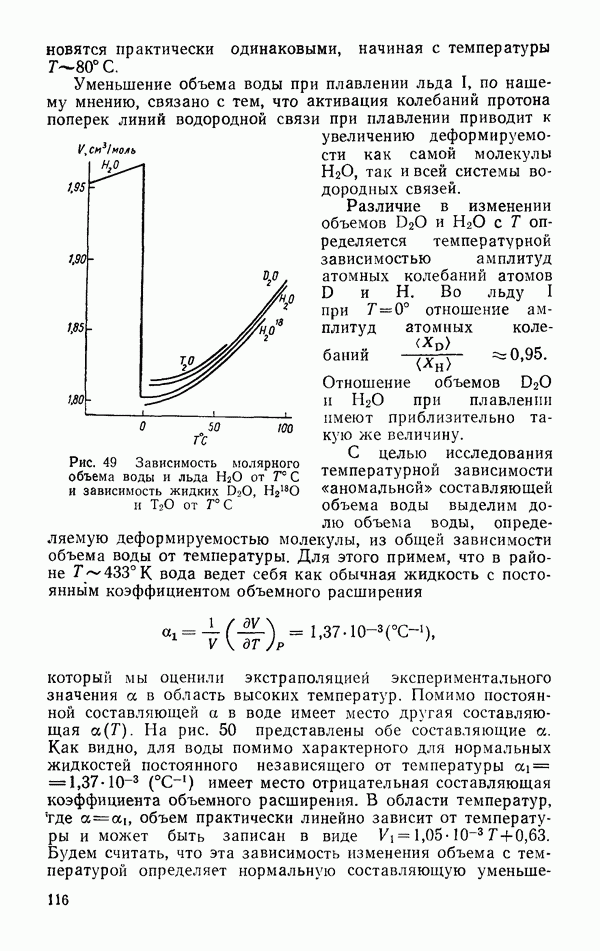
- Зависимость объема и его производных от температуры
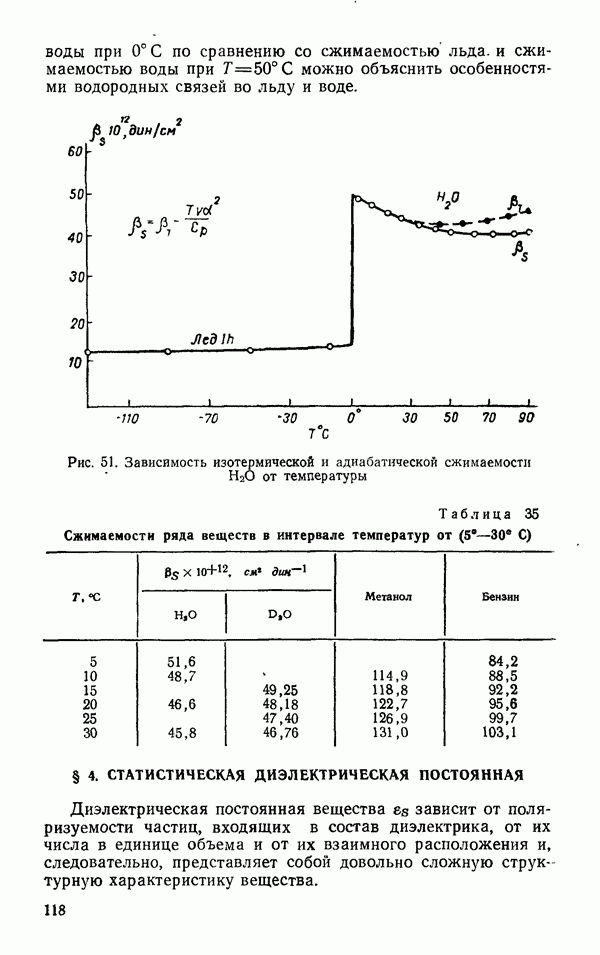
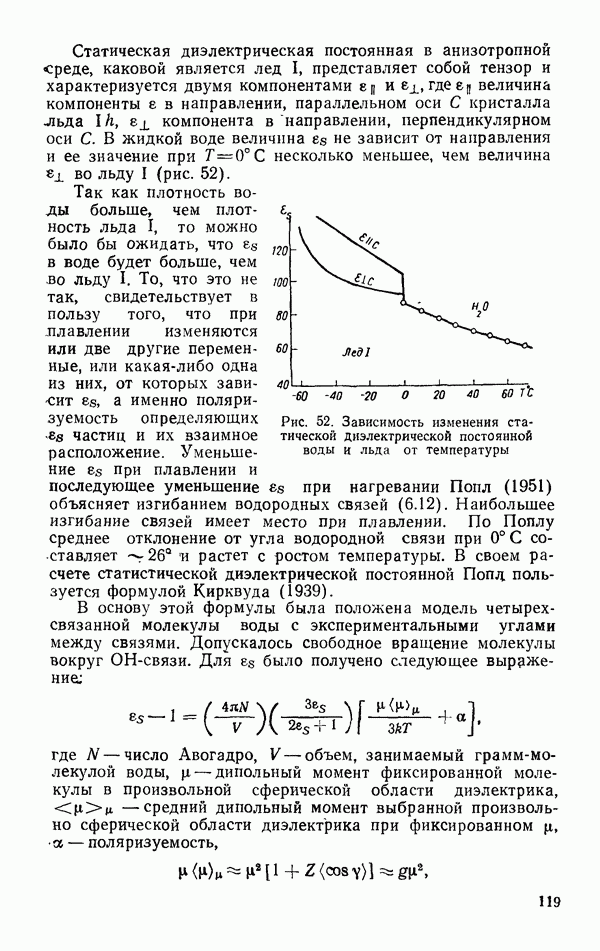
- § 4. СТАТИСТИЧЕСКАЯ ДИЭЛЕКТРИЧЕСКАЯ ПОСТОЯННАЯ
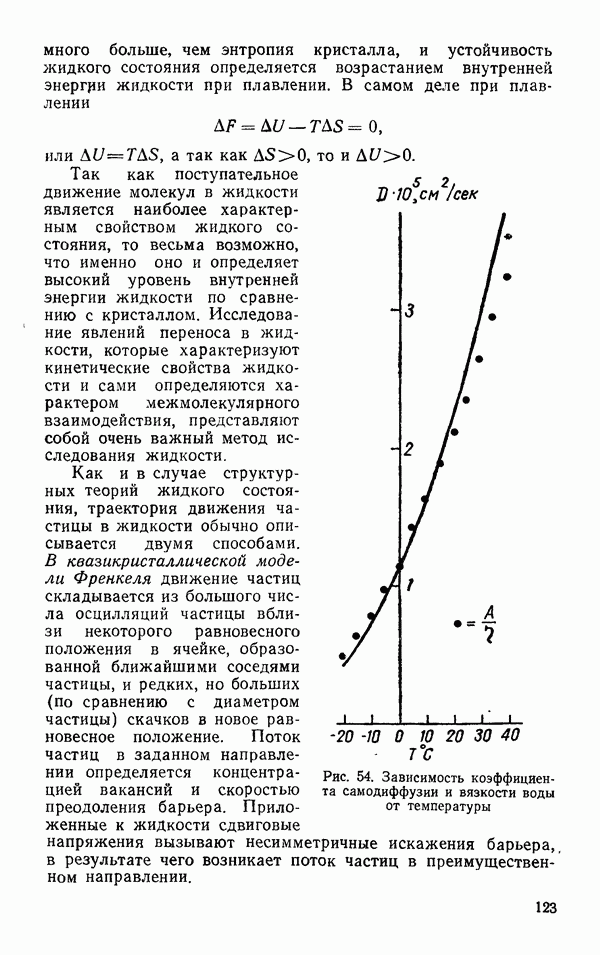
- § 5. ЯВЛЕНИЕ ПЕРЕНОСА
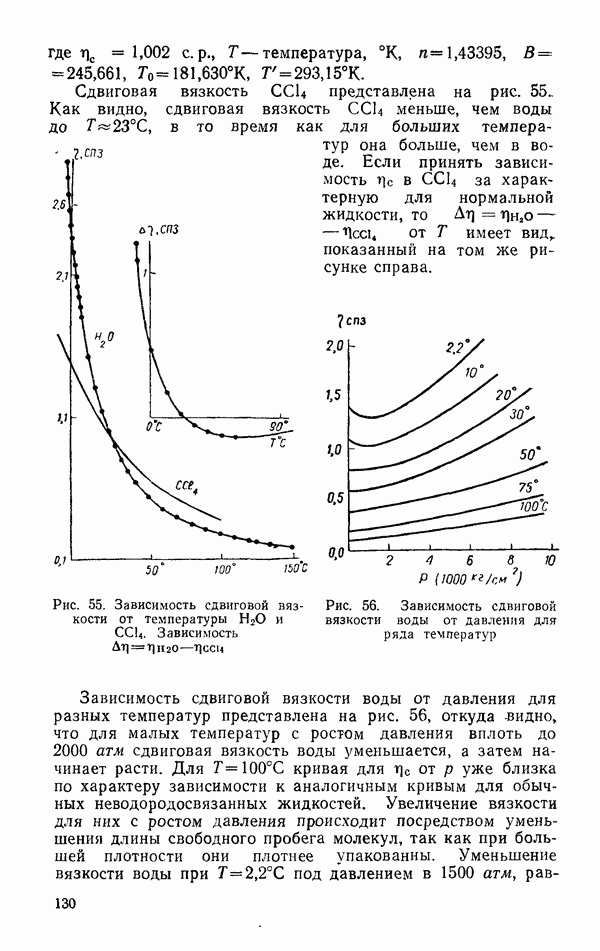
- Вязкость
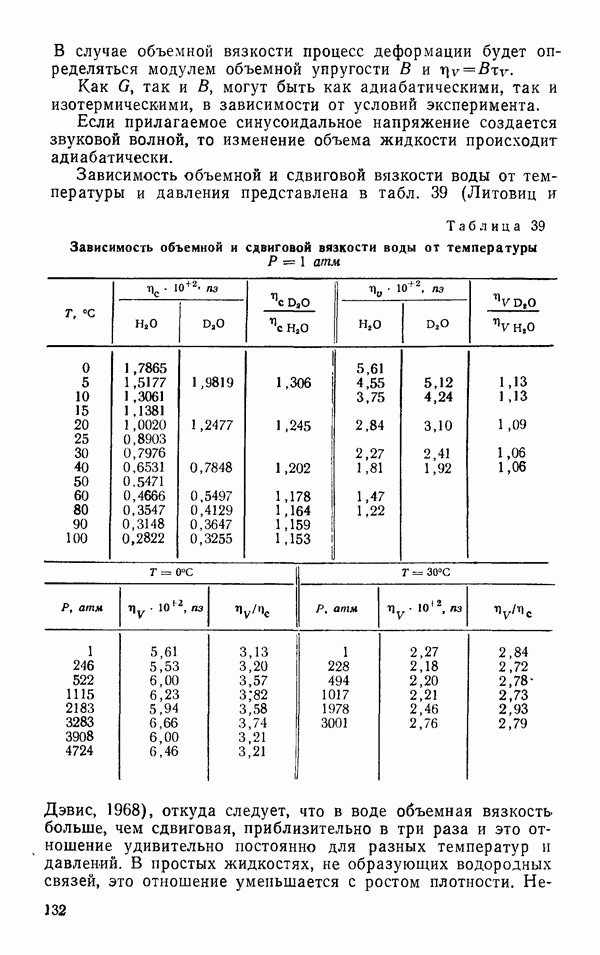
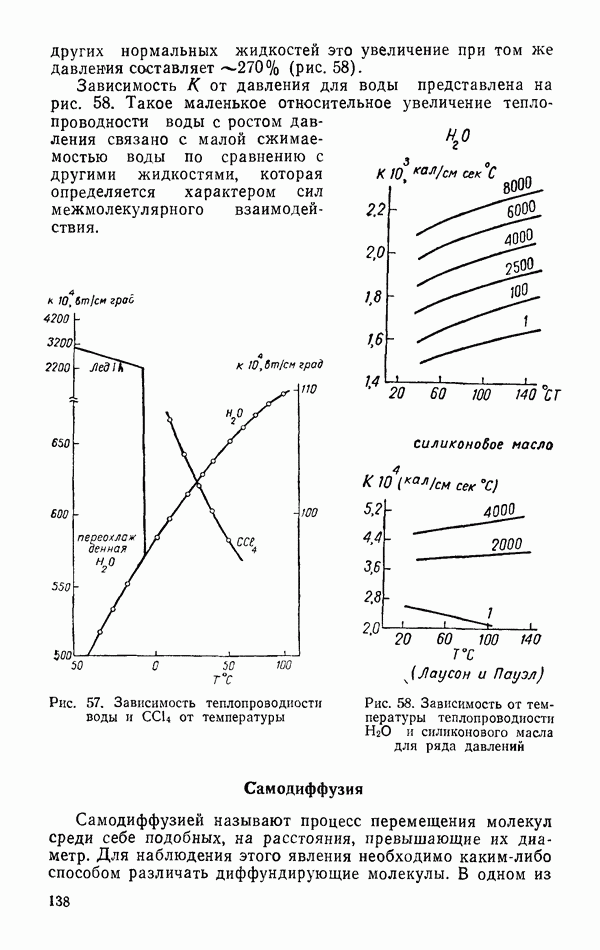
- Теплопроводность
- Самодиффузия
- § 6. НЕКОТОРЫЕ ЭКСПЕРИМЕНТАЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ПРОЦЕССОВ МОЛЕКУЛЯРНОГО ВЗАИМОДЕЙСТВИЯ
- Молекулярное рассеяние света
- Вода как самодиссоциирующая среда
- § 7. ВОДА D2O
- ЗАКЛЮЧЕНИЕ
- ЛИТЕРАТУРА