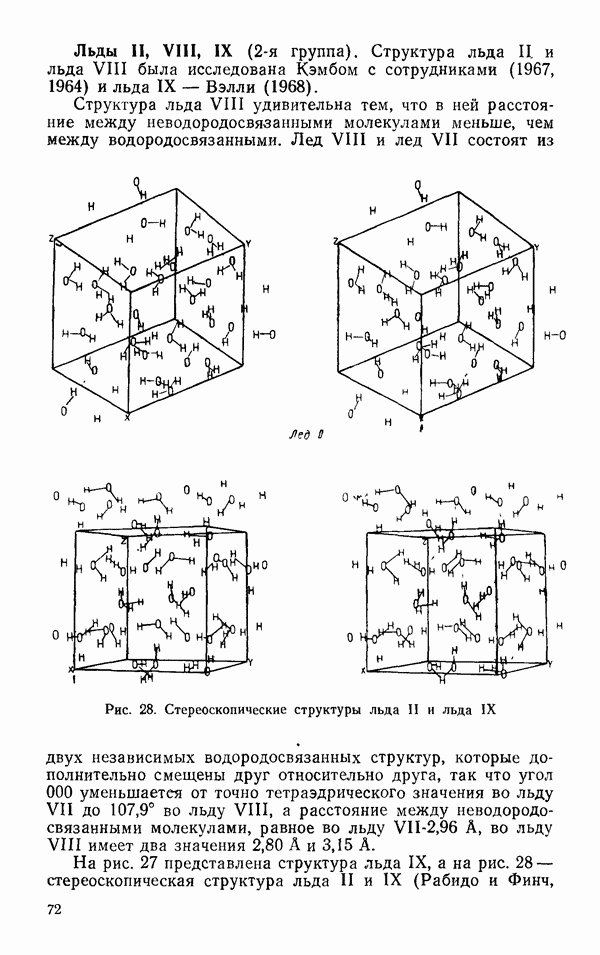
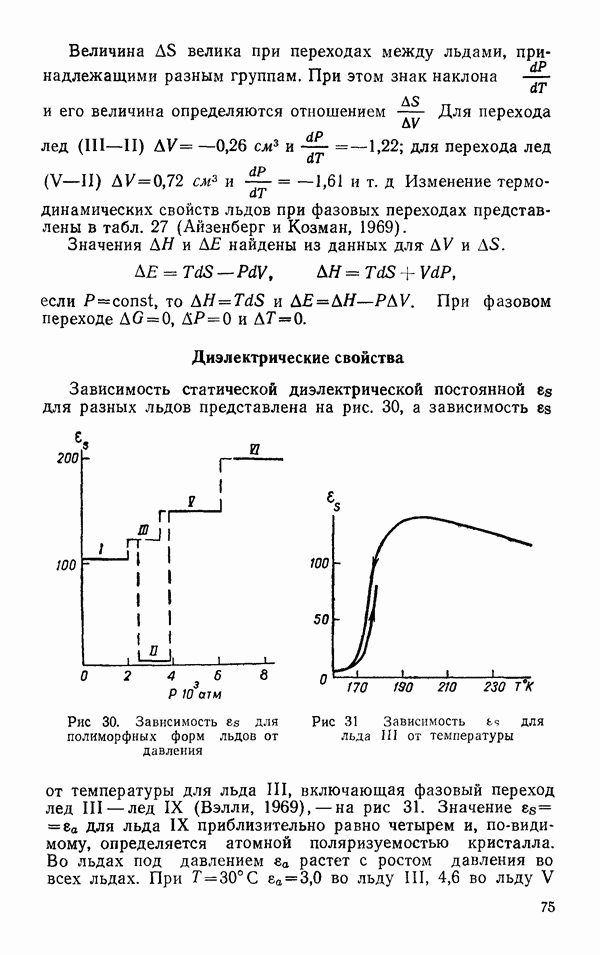
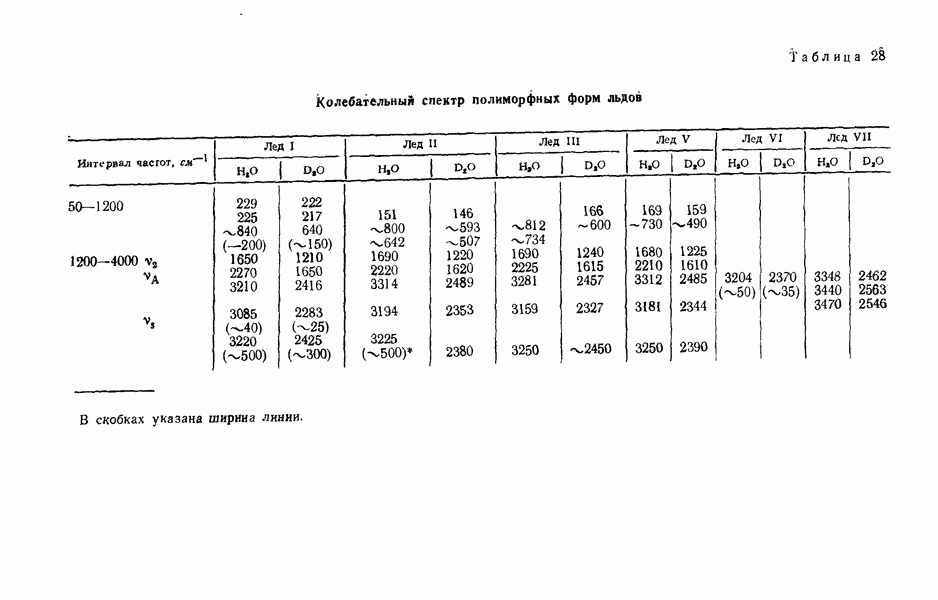
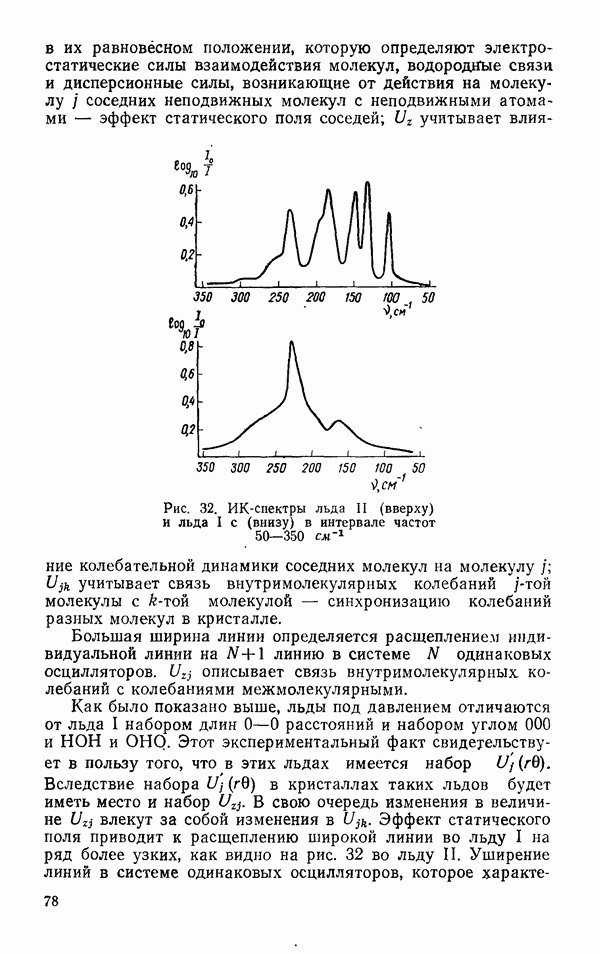
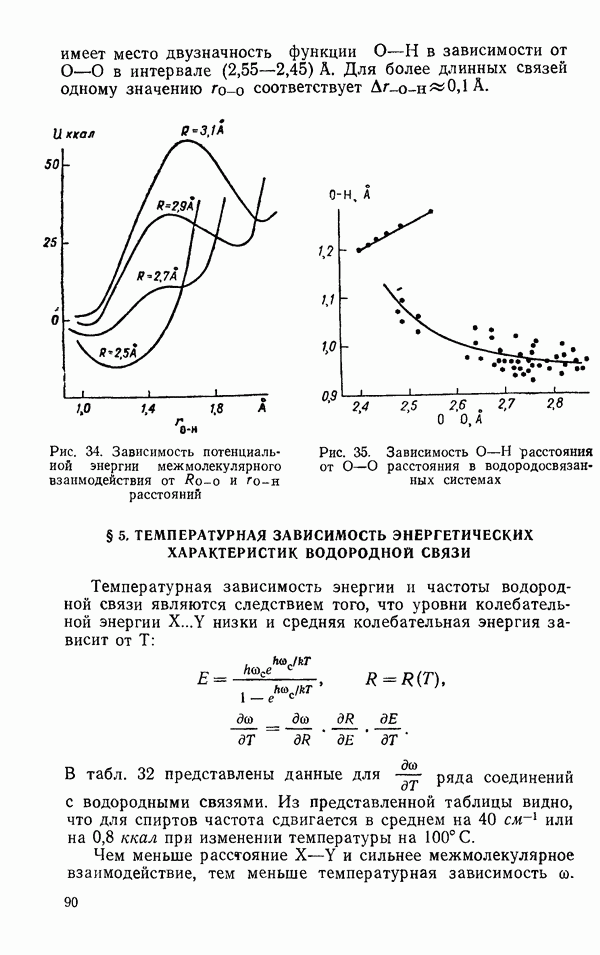
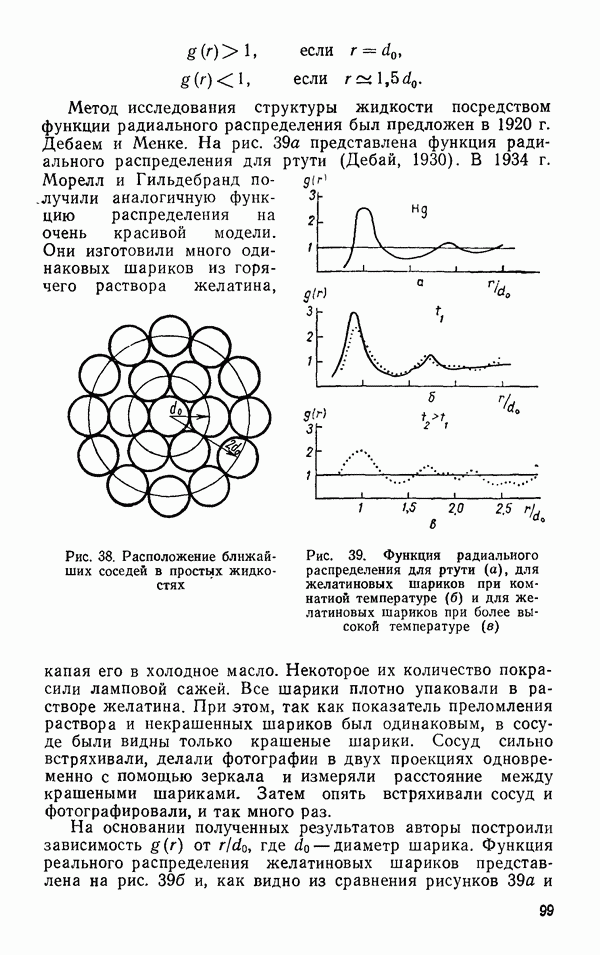
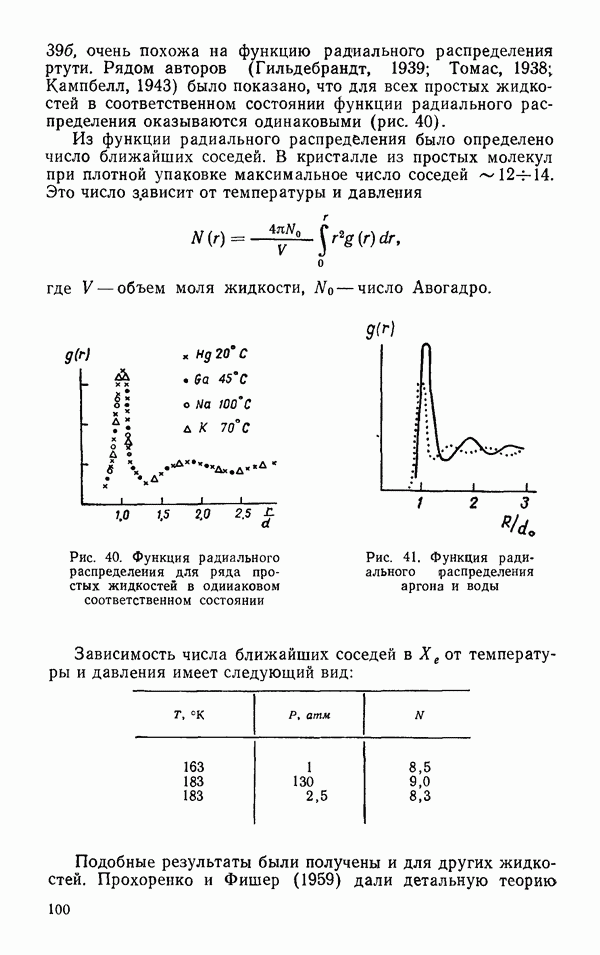
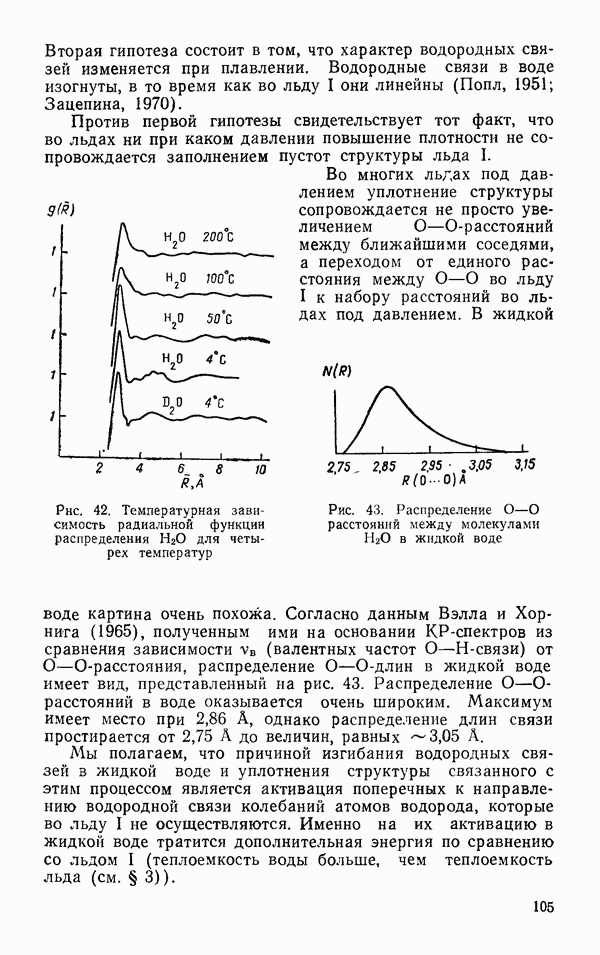
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
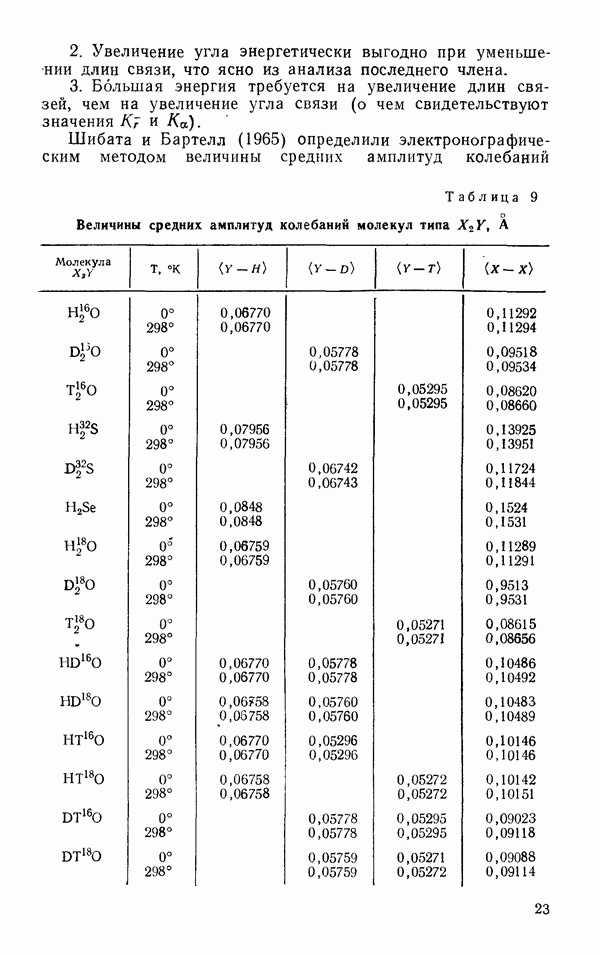
§ 3. ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА
Критические явления
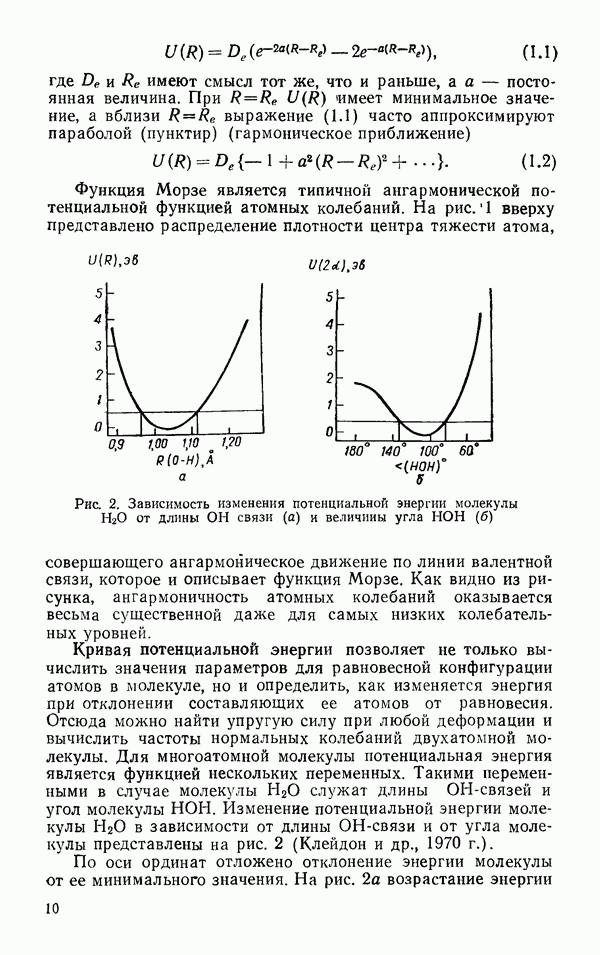
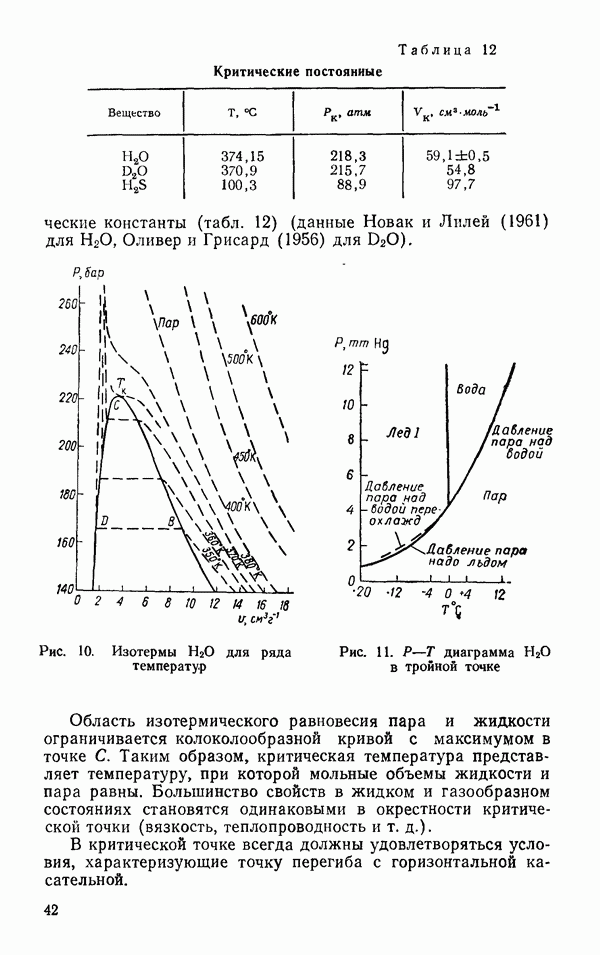
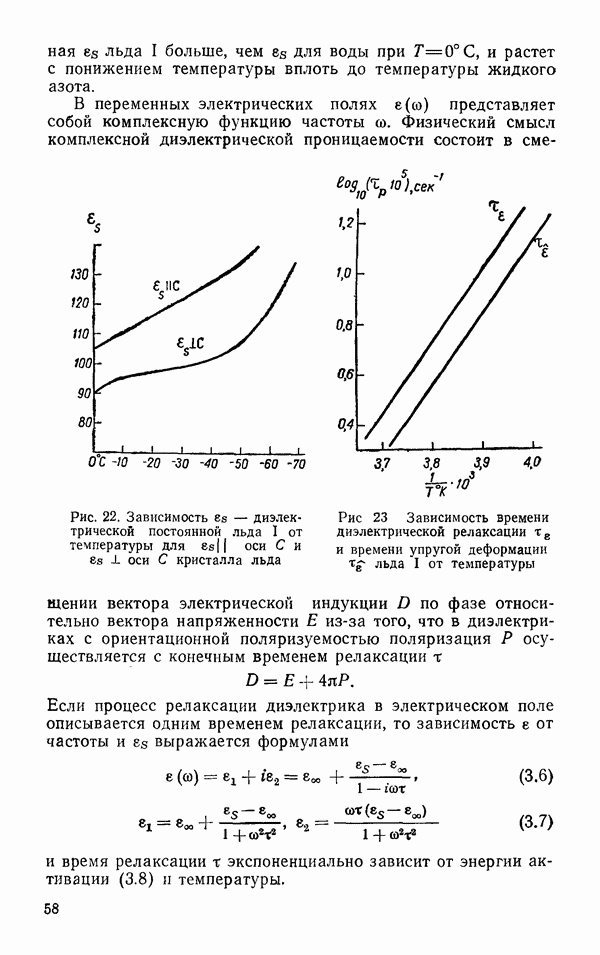
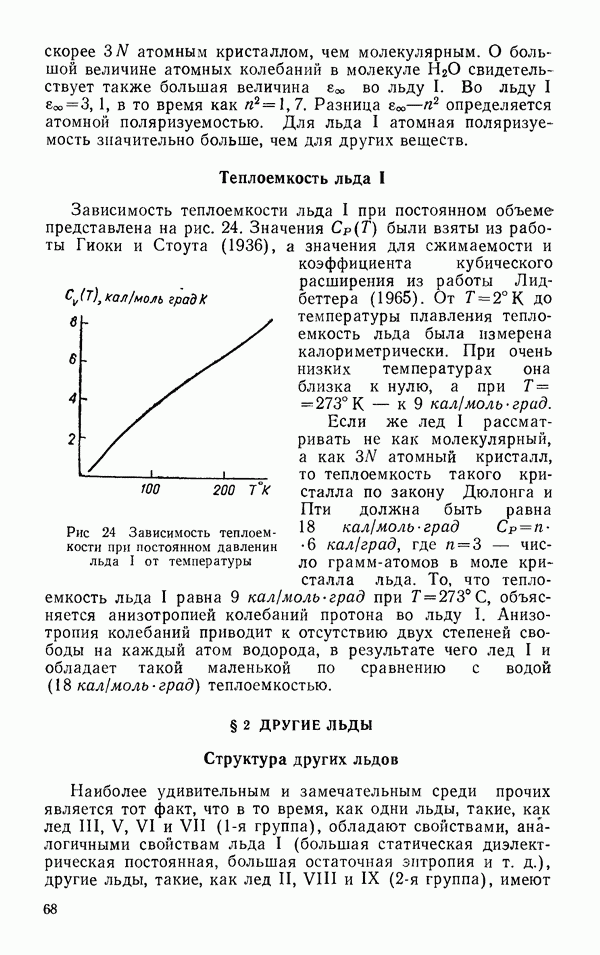
На рис. 10 приведены изотермы  для ряда температур (Бэйн, 1964 и Новак, 1961). Вместо ряда коаксиальных прямоугольных гипербол, которые следовало бы ожидать в случае действия законов идеальных газов, изотермы представляют кривые, каждая из которых ниже критической точки имеет два разрыва. На участке кривой от
для ряда температур (Бэйн, 1964 и Новак, 1961). Вместо ряда коаксиальных прямоугольных гипербол, которые следовало бы ожидать в случае действия законов идеальных газов, изотермы представляют кривые, каждая из которых ниже критической точки имеет два разрыва. На участке кривой от  до В увеличение давления сопровождается слишком сильным уменьшением объема, так что
до В увеличение давления сопровождается слишком сильным уменьшением объема, так что  не остается постоянным, а уменьшается; в точке В появляется жидкая фаза. В интервале от В до
не остается постоянным, а уменьшается; в точке В появляется жидкая фаза. В интервале от В до  при постоянном дэвлении изменяется соотношение между количеством жидкости и пара. Следы пара исчезают в точке
при постоянном дэвлении изменяется соотношение между количеством жидкости и пара. Следы пара исчезают в точке  и кривая
и кривая  показывает сжимаемость чистой жидкости. В точке С образование жидкости прекращается, поэтому эта точка называется критической. Давление, объем и температура в этой точке представляют
показывает сжимаемость чистой жидкости. В точке С образование жидкости прекращается, поэтому эта точка называется критической. Давление, объем и температура в этой точке представляют
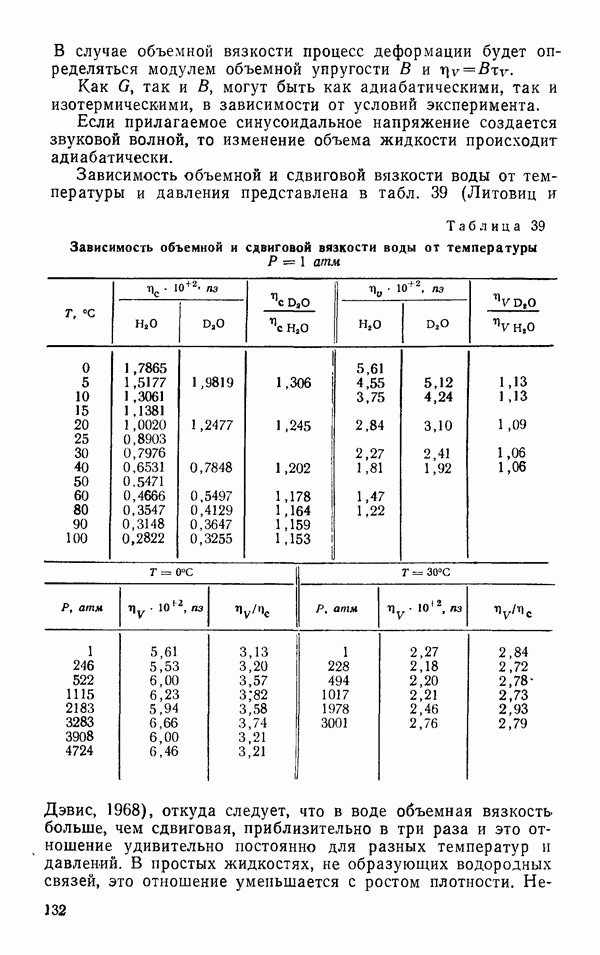
Таблица 12 Критические постоянные

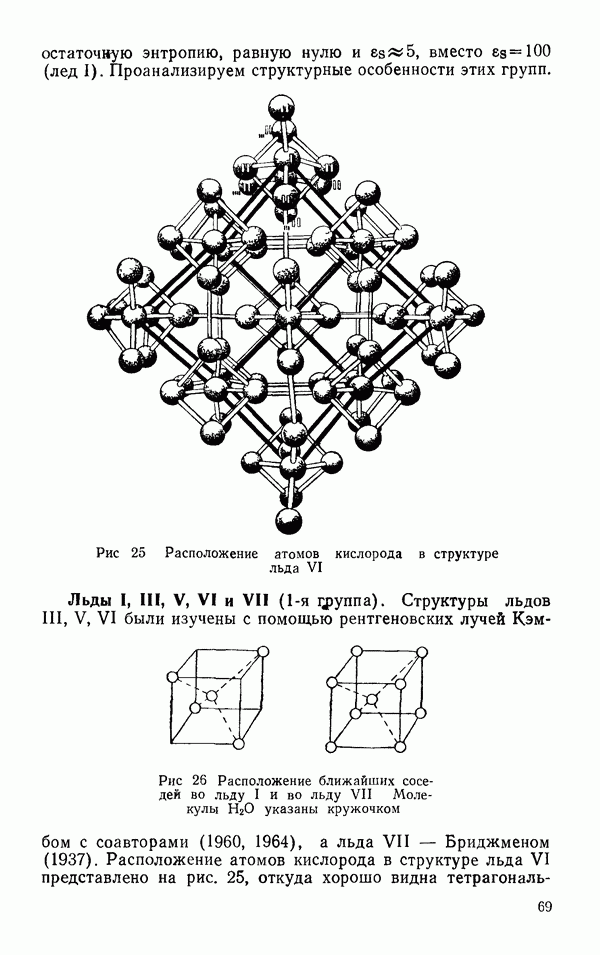
критические константы (табл. 12) (данные Новак и Лилей (1961) для  Оливер и Грисард (1956) для
Оливер и Грисард (1956) для 

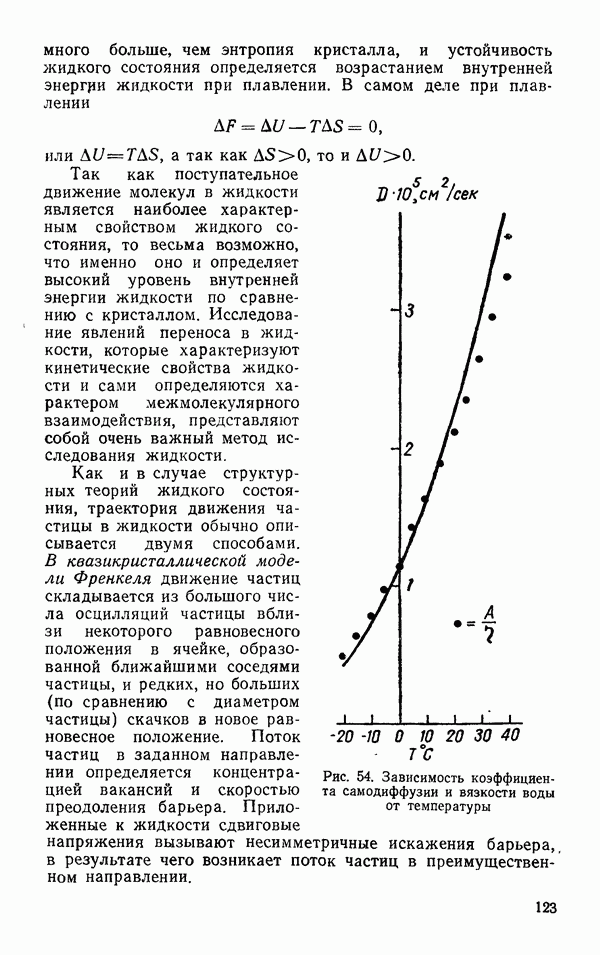
Рис. 10. Изотермы  для ряда температур
для ряда температур

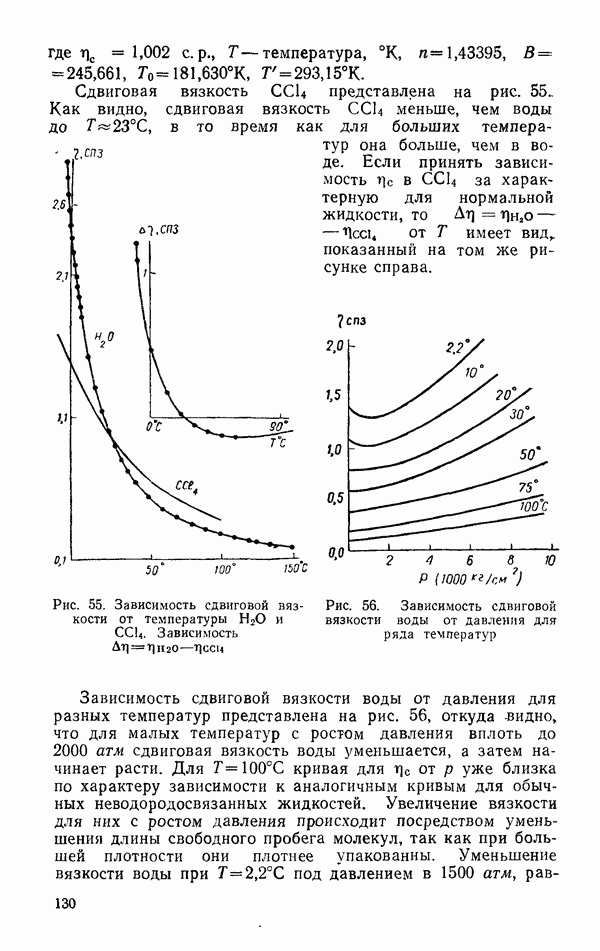
Рис. 11.  диаграмма
диаграмма  в тройной точке
в тройной точке
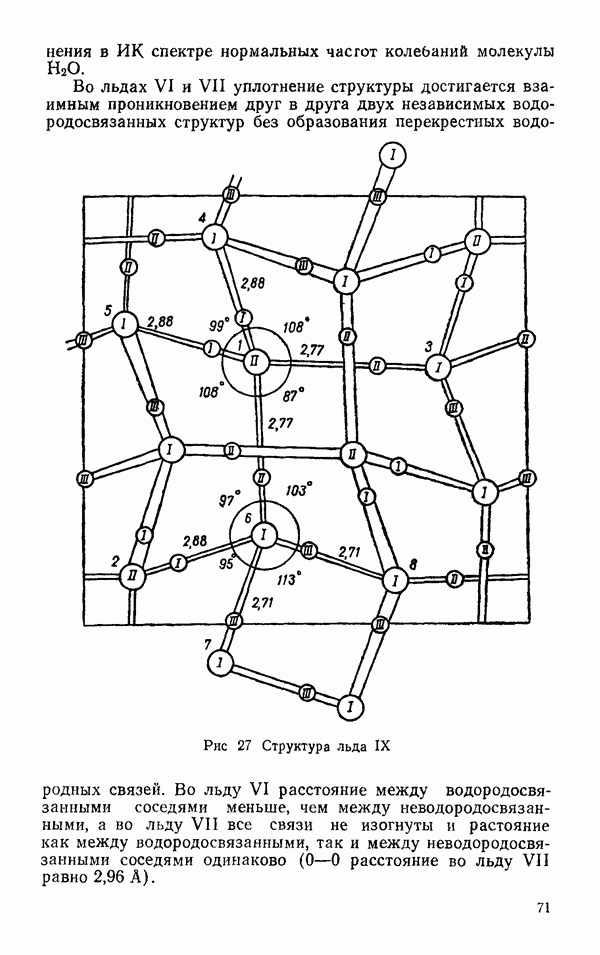
Область изотермического равновесия пара и жидкости ограничивается колоколообразной кривой с максимумом в точке С. Таким образом, критическая температура представляет температуру, при которой мольные объемы жидкости и пара равны. Большинство свойств в жидком и газообразном состояниях становятся одинаковыми в окрестности критической точки (вязкость, теплопроводность и т. д.).
В критической точке всегда должны удовлетворяться условия, характеризующие точку перегиба с горизонтальной касательной.

Зависимость объема от давления для  в интервале температур от 5 °С до
в интервале температур от 5 °С до  хорошо передается формулой Осборна и Майер (Дорсей, 1940):
хорошо передается формулой Осборна и Майер (Дорсей, 1940):

где Р — давление пара в атмосферах,

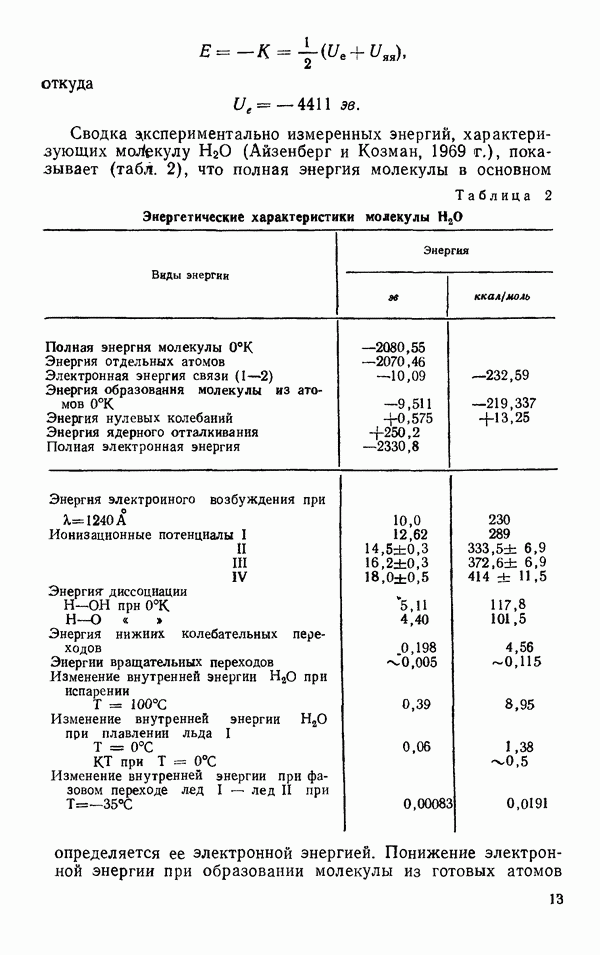
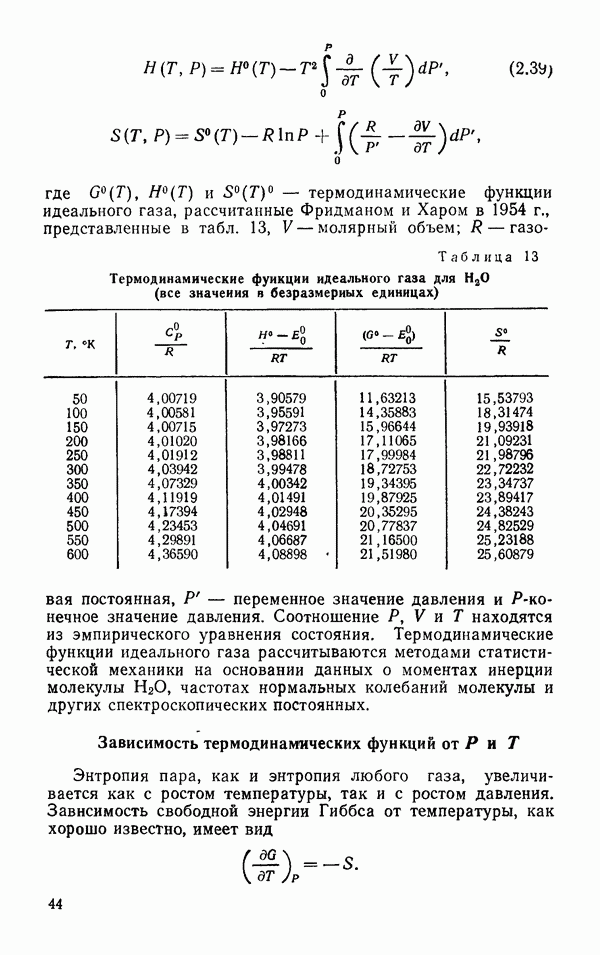
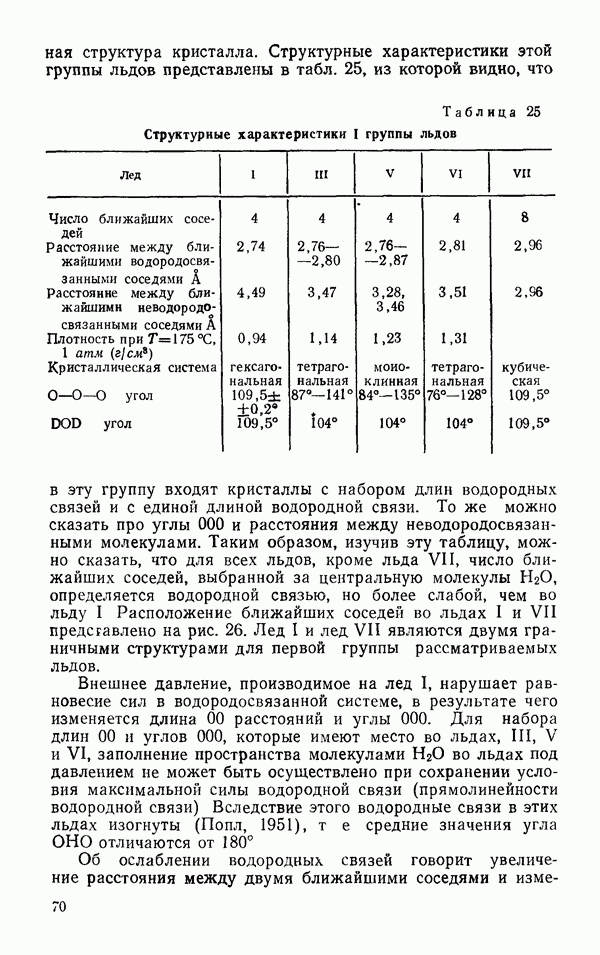
На рис. 11 представлена  -диаграмма для
-диаграмма для  в тройной точке. Согласно Васбурну (Дорсей, 1940) давление пара над льдом 1 описывается соотношением
в тройной точке. Согласно Васбурну (Дорсей, 1940) давление пара над льдом 1 описывается соотношением

где  давление пара над льдом I при
давление пара над льдом I при 

Давление пара над переохлажденной водой несколько выше, чем над льдом I (см. рис. 11).
| << Предыдущий параграф | Следующий параграф >> |
- Введение
- Глава 1. МОЛЕКУЛА H2O
- Энергия образования молекулы
- Полная энергия молекулы
- § 3. РАЗМЕРЫ И ФОРМА
- § 4. ЭЛЕКТРИЧЕСКИЕ СВОЙСТВА
- § 5. КОЛЕБАТЕЛЬНЫЕ ЧАСТОТЫ МОЛЕКУЛЫ
- ЗАКЛЮЧЕНИЕ
- Глава 2. СВОЙСТВА ПАРА
- Исследования межмолекулярных сил отталкивания
- § 2. УРАВНЕНИЯ СОСТОЯНИЯ РЕАЛЬНОГО ГАЗА
- Вириальная форма уравнения состояния
- Эмпирическое уравнение состояния
- § 3. ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА
- Термодинамические функции
- Зависимость термодинамических функций от P и T
- § 4. ВЯЗКОСТЬ
- Глава 3. СВОЙСТВА ЛЬДОВ
- § 1. ЛЕД
- Пластическая деформация монокристалла льда I
- Диэлектрические свойства льда 1
- Электропроводность льда
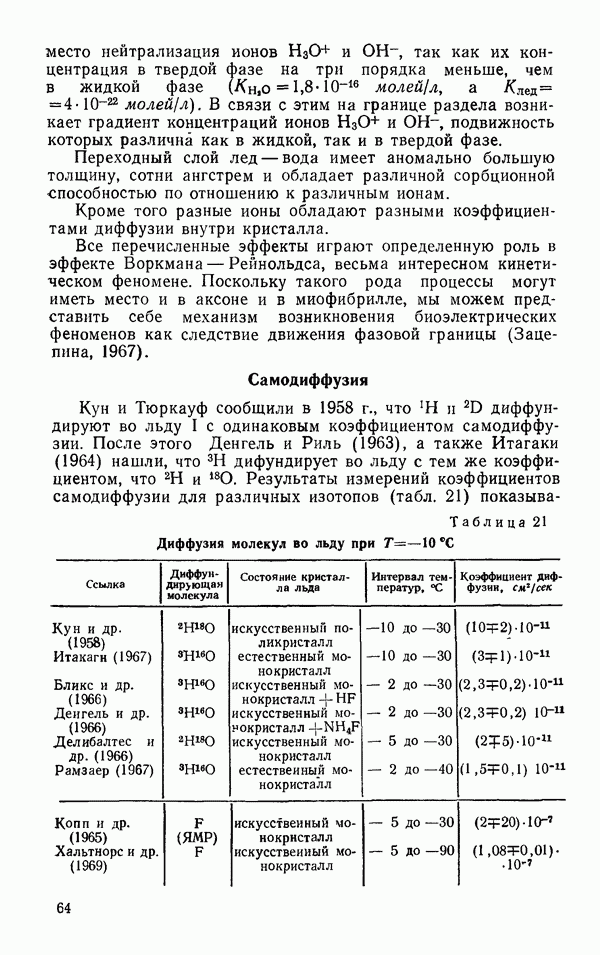
- Самодиффузия
- Спектральные свойства льда I
- Теплоемкость льда I
- § 2 ДРУГИЕ ЛЬДЫ
- Термодинамические свойства льдов
- Диэлектрические свойства
- Спектральные свойства
- ЗАКЛЮЧЕНИЕ
- Глава 4. ВОДОРОДНАЯ СВЯЗЬ
- § 2. СВОЙСТВА АТОМОВ, ОБРАЗУЮЩИХ ВОДОРОДНУЮ СВЯЗЬ
- § 3. МЕТОДЫ ВЫЧИСЛЕНИЯ ЭНЕРГИИ
- § 4. ПОЛУЭМПИРИЧЕСКИЕ ПОТЕНЦИАЛЬНЫЕ ФУНКЦИИ
- § 5. ТЕМПЕРАТУРНАЯ ЗАВИСИМОСТЬ ЭНЕРГЕТИЧЕСКИХ ХАРАКТЕРИСТИК ВОДОРОДНОЙ СВЯЗИ
- ЗАКЛЮЧЕНИЕ
- Глава 5. ЖИДКОЕ СОСТОЯНИЕ
- § 1. РАЗЛИЧНЫЕ ПОДХОДЫ К РЕШЕНИЮ ПРОБЛЕМЫ ЖИДКОГО СОСТОЯНИЯ
- § 2. СТРУКТУРА ЖИДКОСТИ
- § 3. ПЛАВЛЕНИЕ
- Глава 6. СВОЙСТВА ЖИДКОЙ ВОДЫ
- § 2. СПЕКТРАЛЬНЫЕ ДАННЫЕ
- § 3. ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА
- Теплоемкость
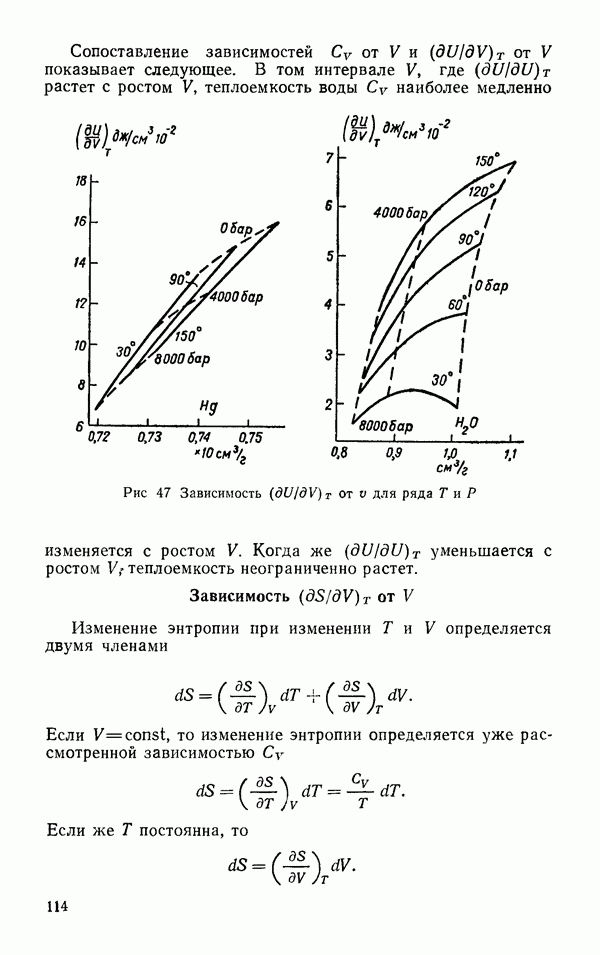
- Зависимость … от V (молекулярный объем)
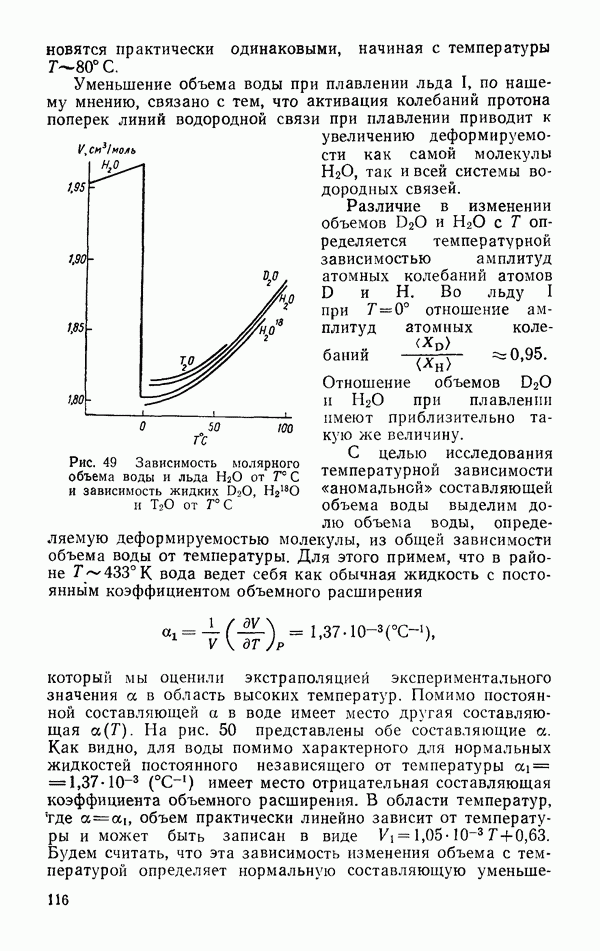
- Зависимость объема и его производных от температуры
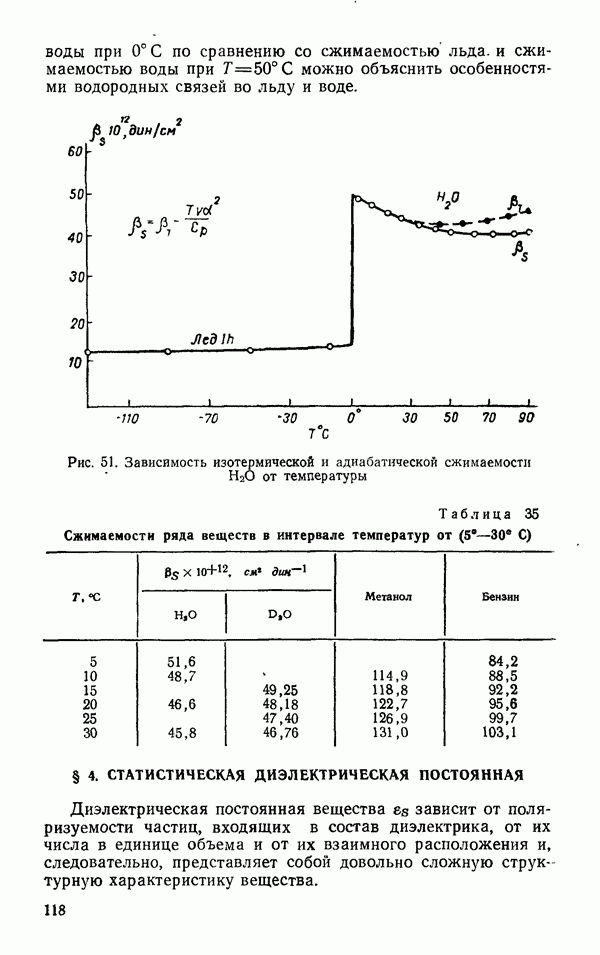
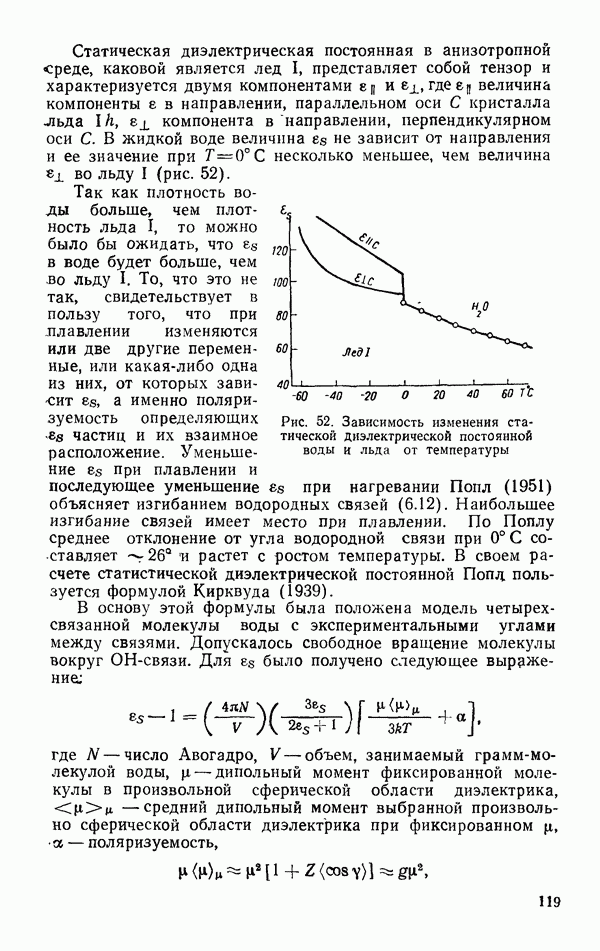
- § 4. СТАТИСТИЧЕСКАЯ ДИЭЛЕКТРИЧЕСКАЯ ПОСТОЯННАЯ
- § 5. ЯВЛЕНИЕ ПЕРЕНОСА
- Вязкость
- Теплопроводность
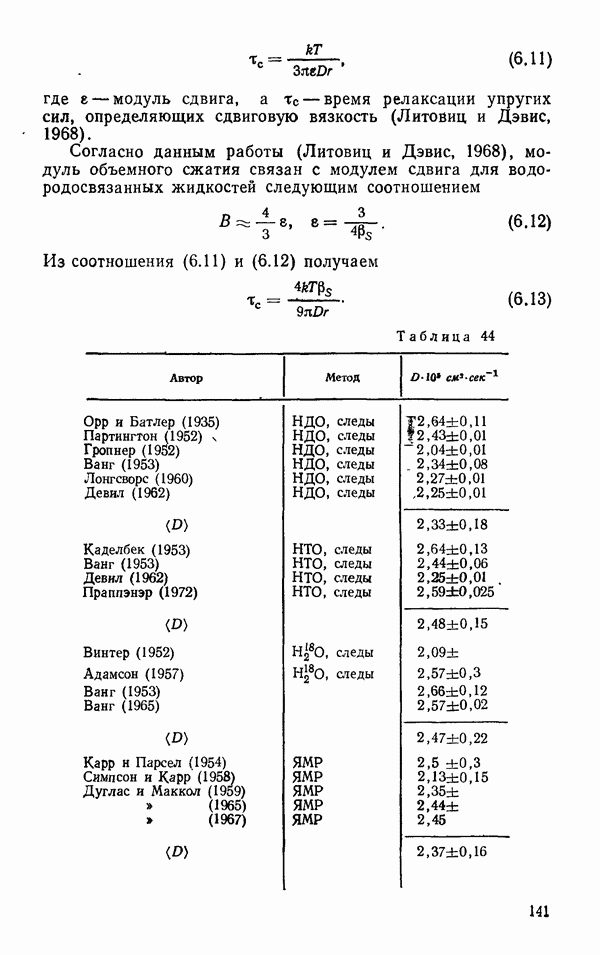
- Самодиффузия
- § 6. НЕКОТОРЫЕ ЭКСПЕРИМЕНТАЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ПРОЦЕССОВ МОЛЕКУЛЯРНОГО ВЗАИМОДЕЙСТВИЯ
- Молекулярное рассеяние света
- Вода как самодиссоциирующая среда
- § 7. ВОДА D2O
- ЗАКЛЮЧЕНИЕ
- ЛИТЕРАТУРА