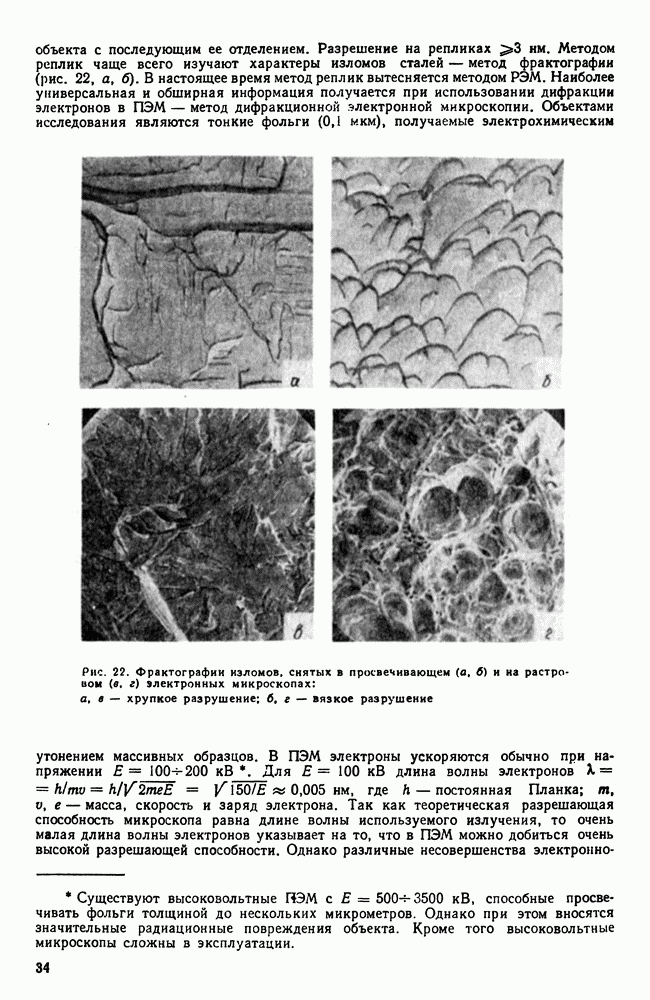
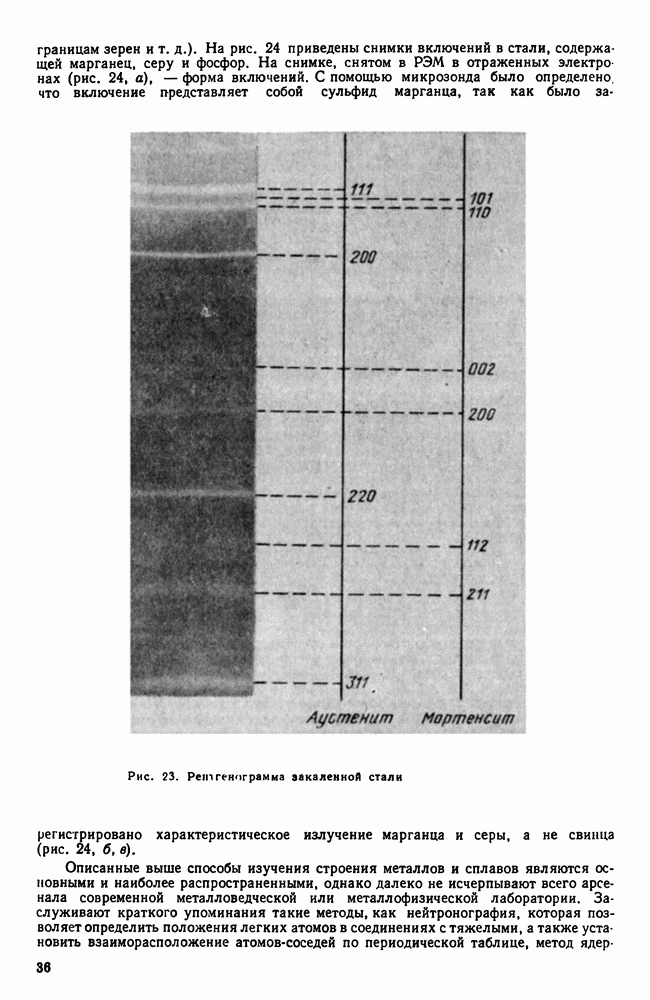
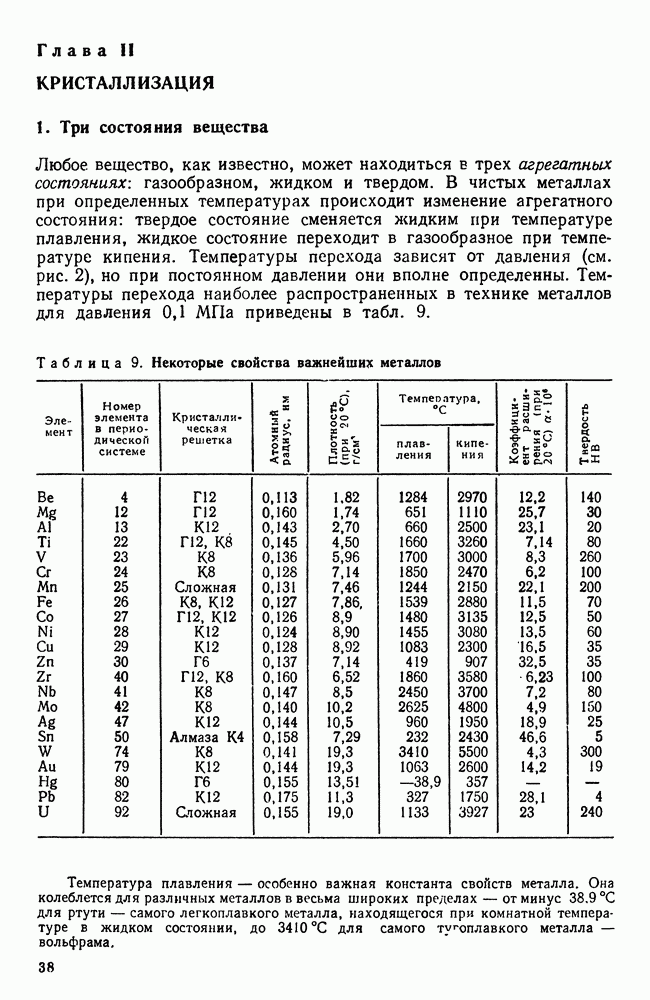
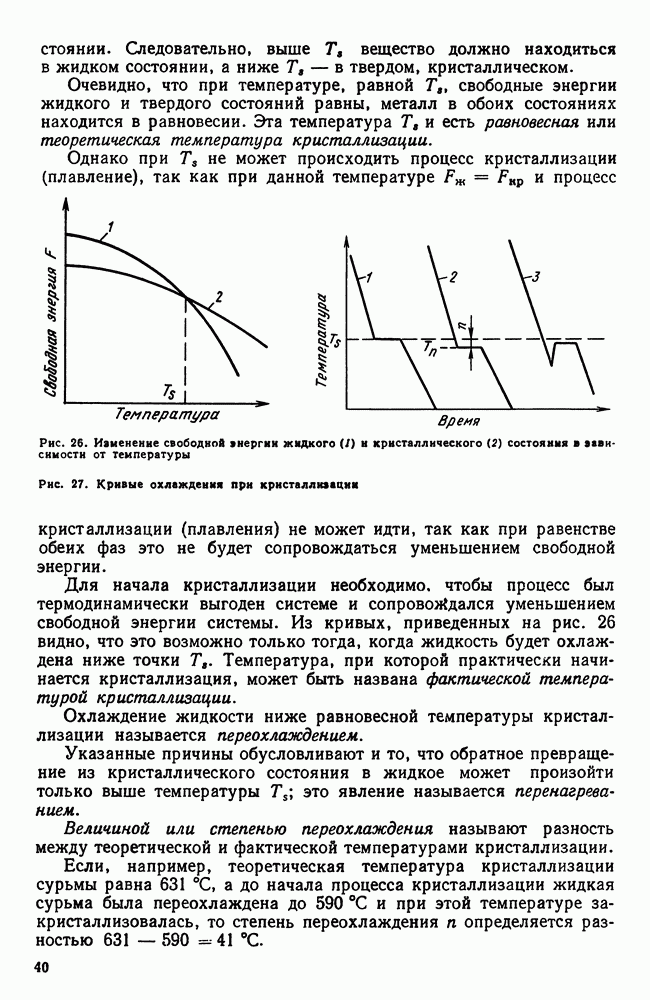
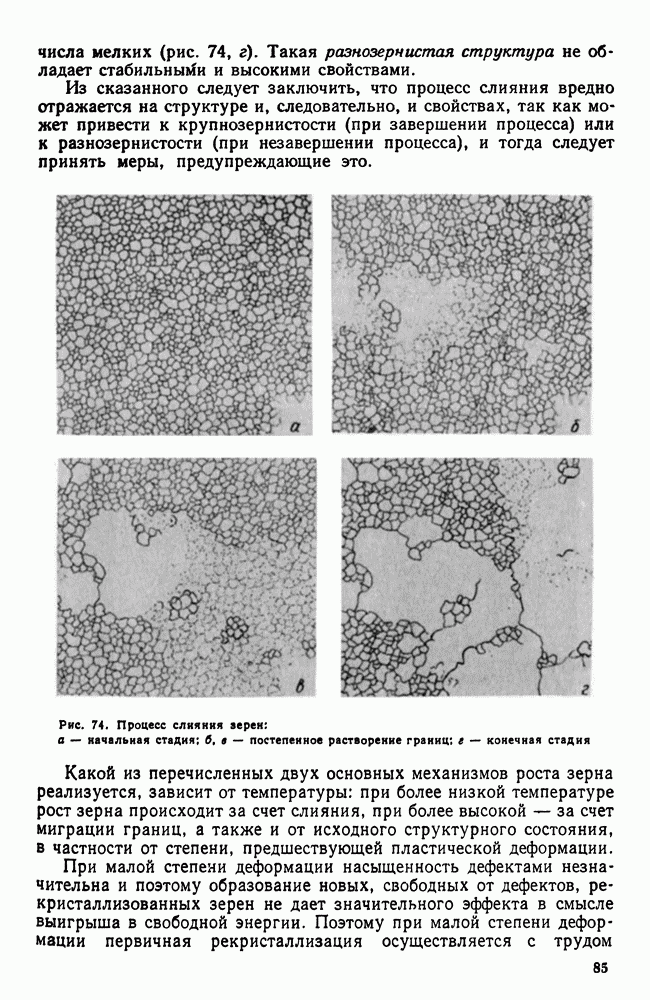
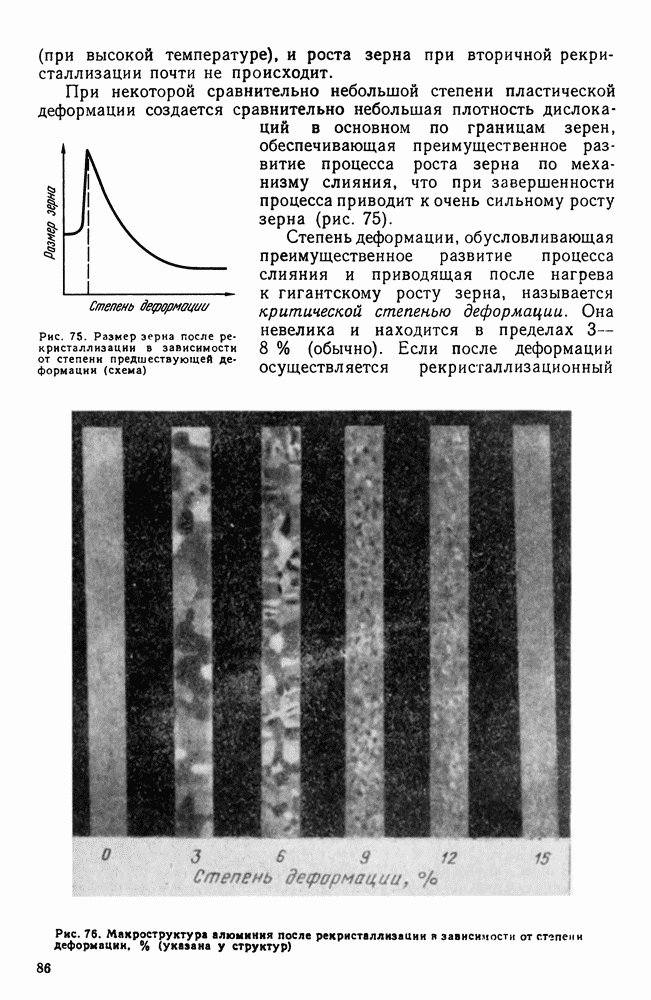
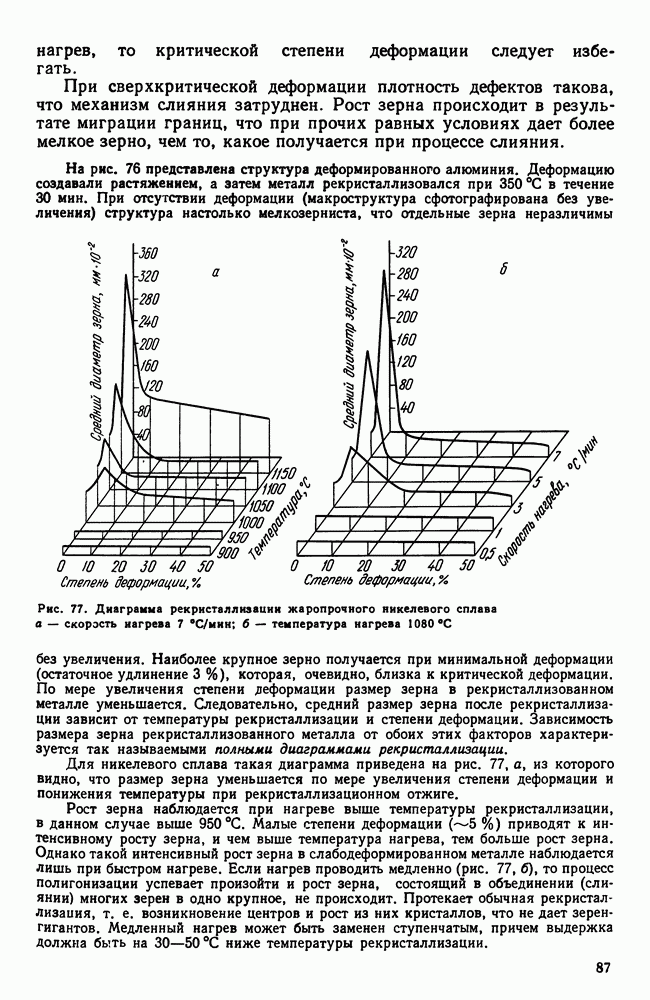
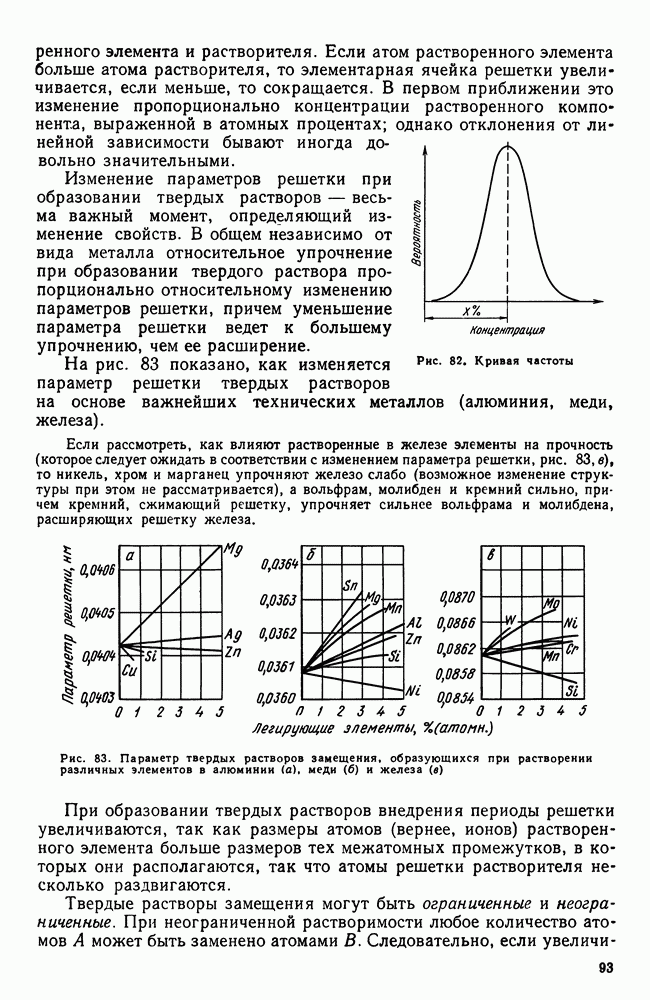
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
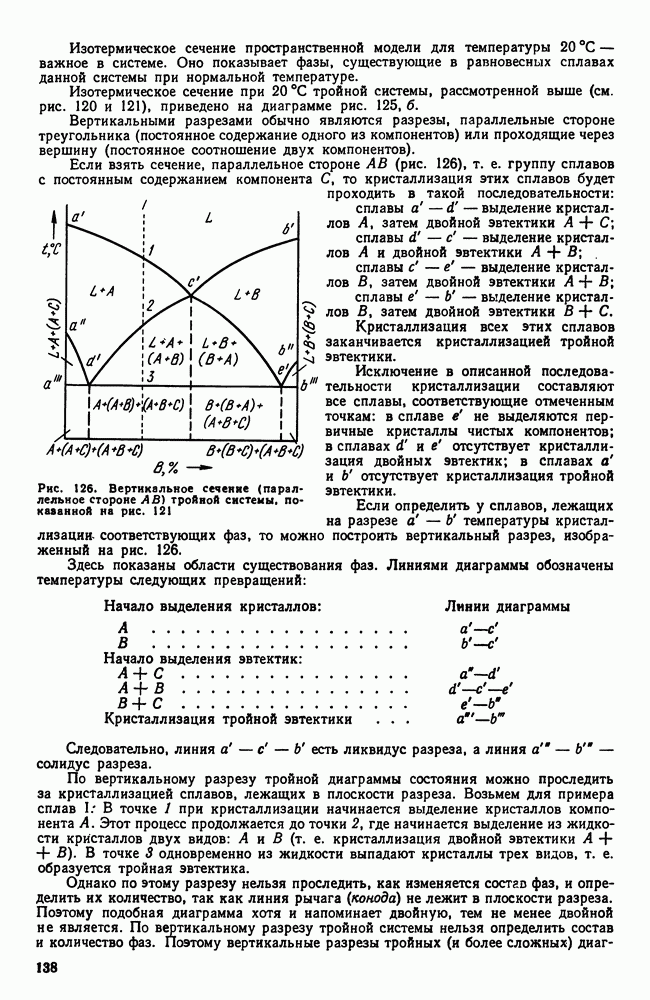
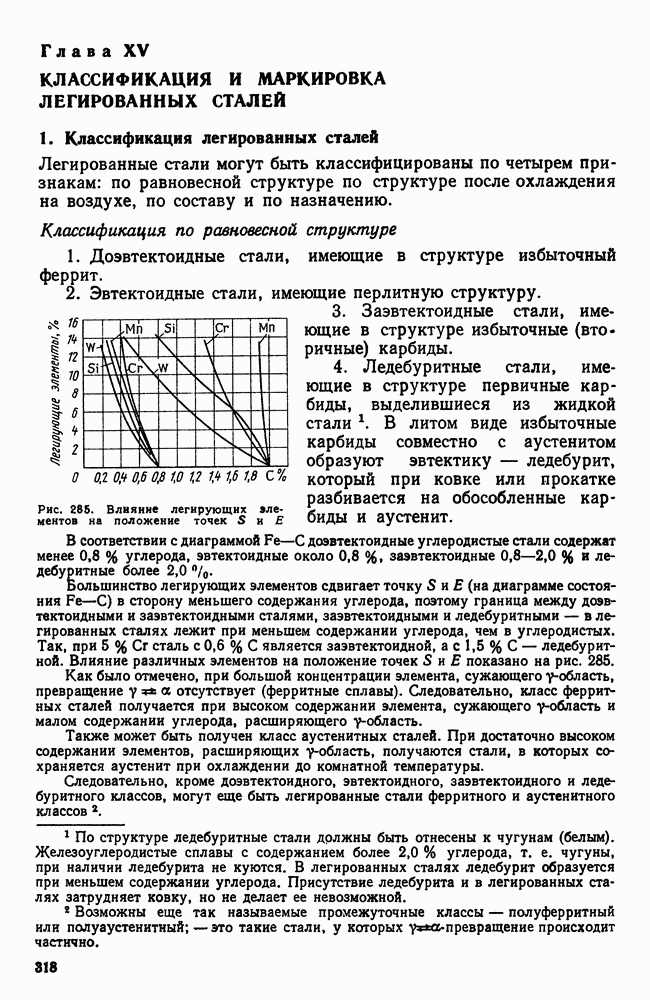
3. Экспериментальное построение диаграмм
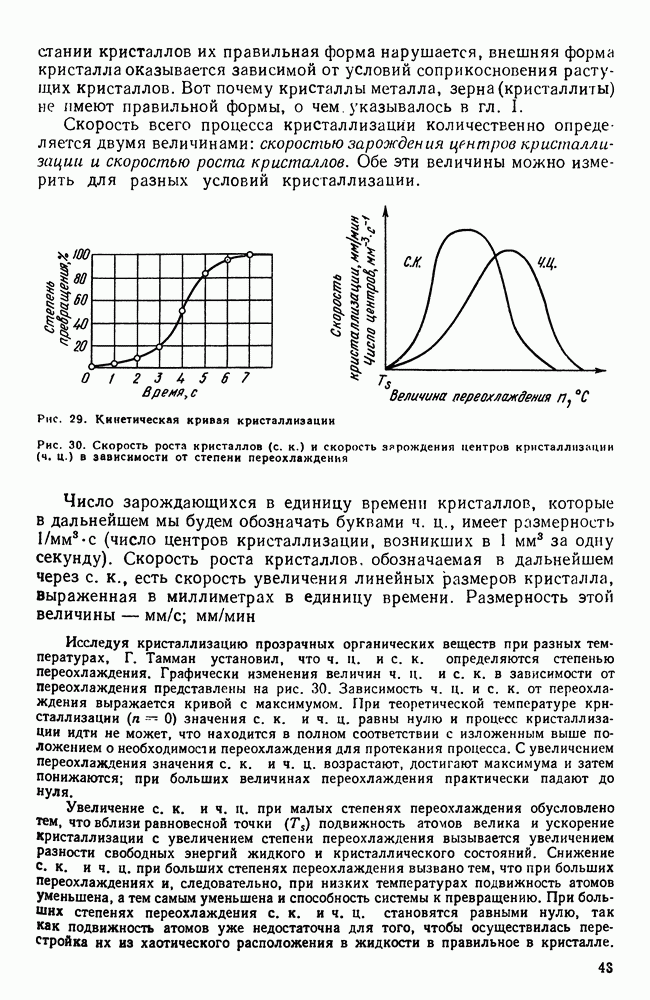
Обычно для построения диаграмм состояния пользуются результатами термического анализа, т. е. строят кривые охлаждения и по остановкам и перегибам на этих кривых, вызванным тепловым эффектом превращений, определяют температуры превращения.
Температуру металлов измеряют обычно при помощи термопары. Принцип измерения температуры термопарой см. ниже стр. 470.
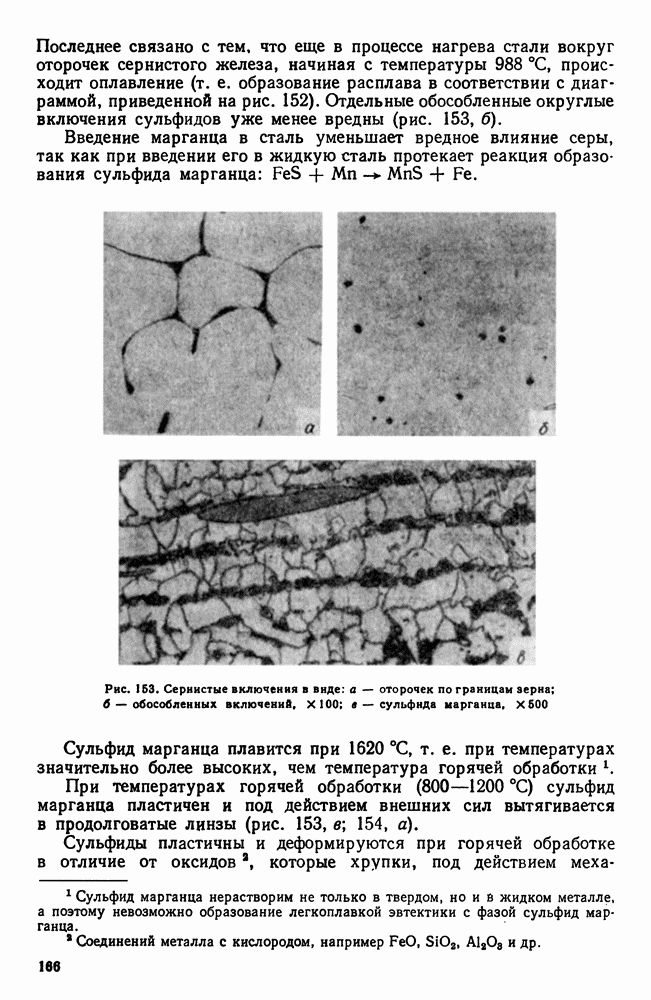
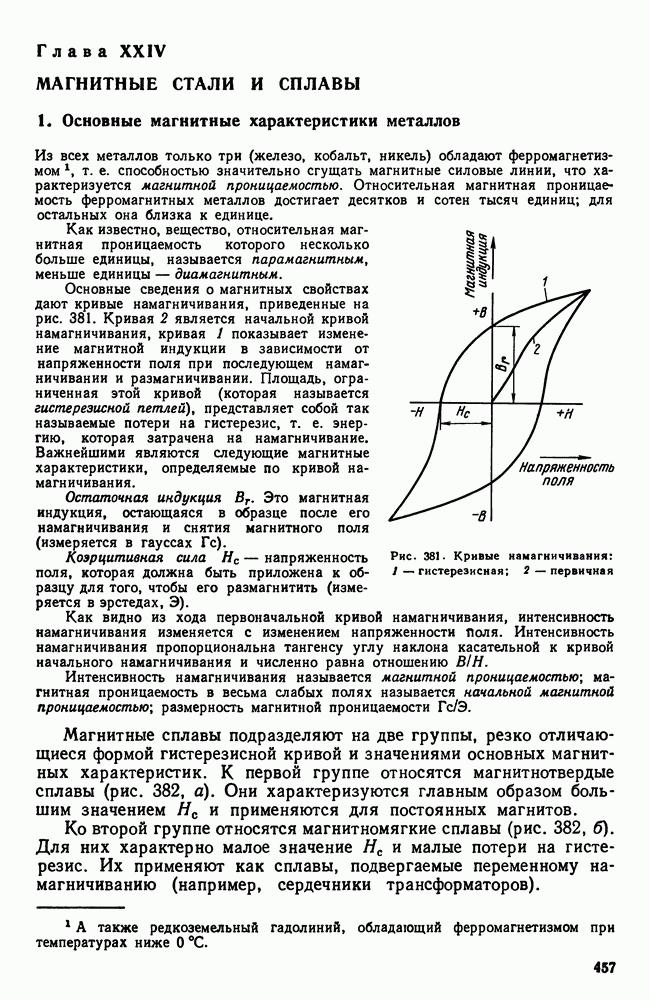
Температура кристаллизации определяется следующим образом. В печь 1 (рис. 89) помещают тигелек 2, в котором расплавляют исследуемый сплав 3. Затем в расплав погружают горячий спай 4 термопары 5 (защищенной фарфоровым или кварцевым колпачком 6) и выключают печь. Начинается охлаждение и температуру отмечают через определенные промежутки времени. Появление изменений в агрегатном состоянии в связй с выделением скрытой теплоты превращения отражается на кривой температура — время.

Рис. 89. Схема установки для изучения процесса кристаллизации термическим методом: 1 — печь; 2 — тигель; 3 — расплавленный металл; 4 — горячий спай; 5 — термопара; 6 — колпачок; 7 — холодный спай; 8 — гальванометр
Имея достаточное количество сплавов и определив в каждом сплаве температуры превращений, можно построить диаграмму состояния.
Для более точного построения диаграммы состояния в дополнение к термическому методу изучают с помощью микроскопа и рентгеновских лучей структуру сплавов разного состава и по-разному обработанных термически, измеряют разнообразнейшие физические свойства сплавов и т. д.
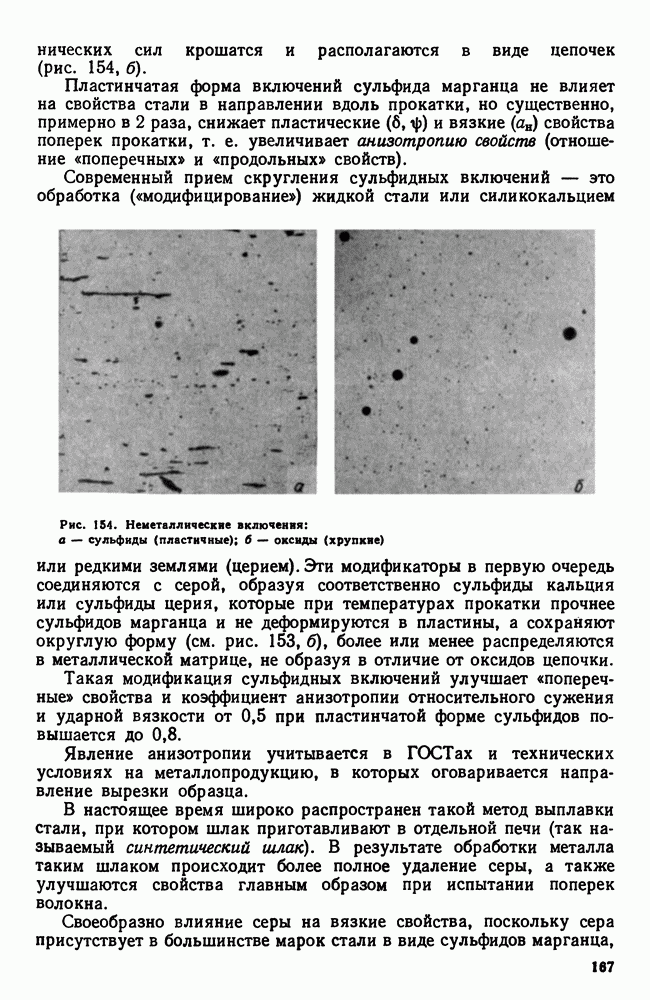
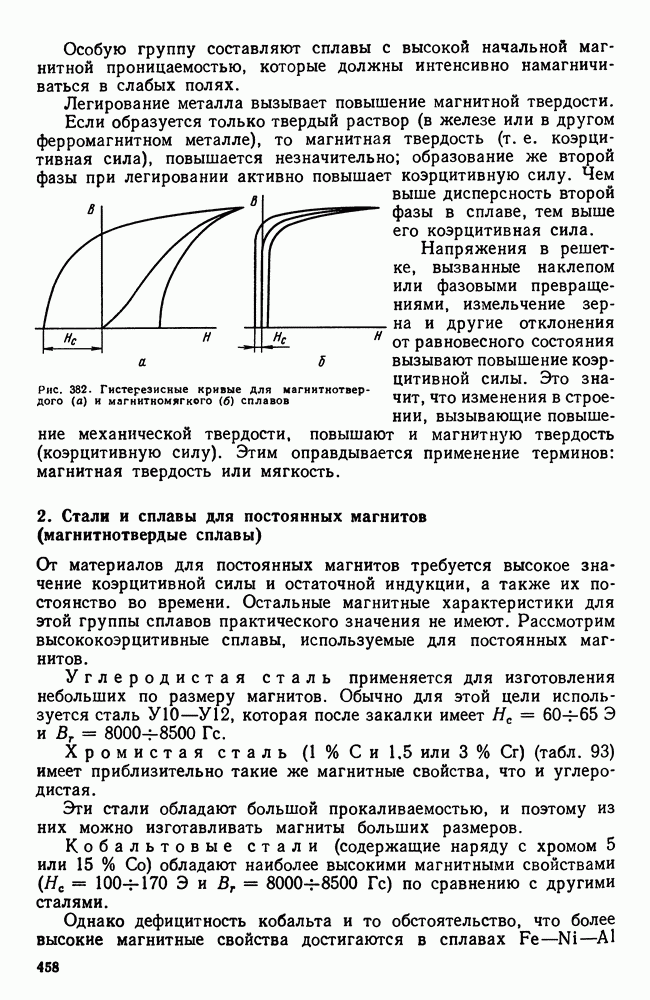
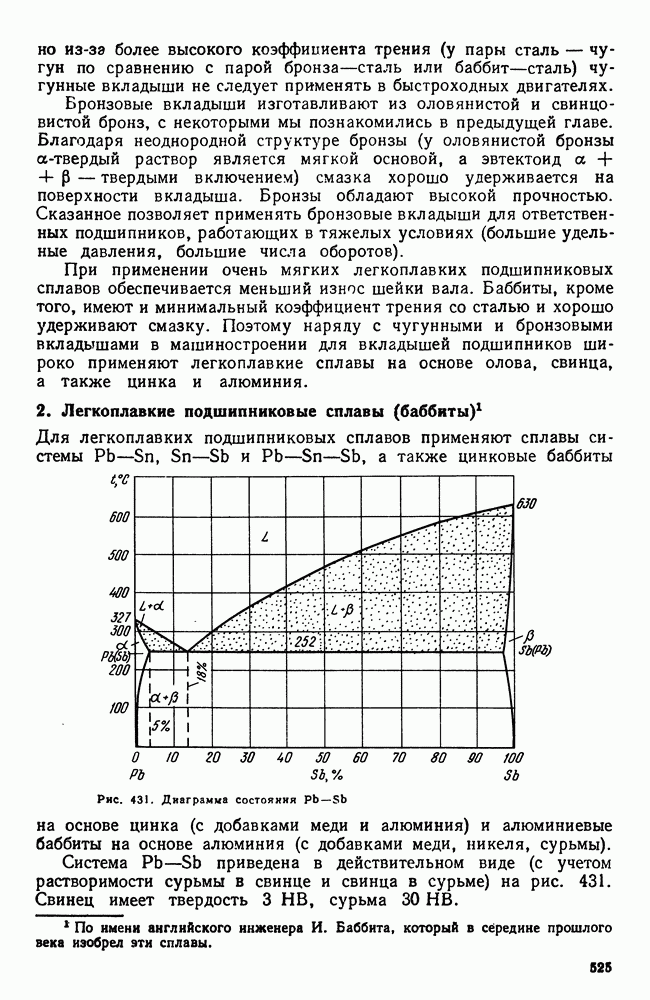
Обратимся к реальному примеру. Предположим, что мы имеем систему из двух компонентов, взаимно нерастворимых в твердом состоянии и не образующих друг с другом химических соединений, но неограниченно растворимых в жидком состоянии. Можно принять с некоторым приближением, что такой системой является например, система свинец — сурьма (фактически эти металлы ограниченно растворимы в твердом состоянии). Предположим далее, что имеется серия сплавов этих двух металлов: за процессом кристаллизации этих сплавов наблюдают по кривым охлаждения (рис. 90).
Кривая (рис. 90, а) относится к чистому свинцу. При температуре выше  свинец находится в жидком состоянии. При
свинец находится в жидком состоянии. При  происходит кристаллизация свинца и ниже
происходит кристаллизация свинца и ниже  свинец находится в кристаллическом состоянии.
свинец находится в кристаллическом состоянии.
тельно, на кривой охлаждения свинца отрезок  соответствует охлаждению жидкости, отрезок
соответствует охлаждению жидкости, отрезок  кристаллизации и
кристаллизации и  охлаждению твердого тела.
охлаждению твердого тела.
Кривая на рис.  относится к сплаву с
относится к сплаву с  и
и  Кристаллизация начинается при температуре ниже
Кристаллизация начинается при температуре ниже  (точка
(точка  и протекает при переменной температуре (от точки 1 до точки 2), а затем при
и протекает при переменной температуре (от точки 1 до точки 2), а затем при  оставшаяся часть жидкости кристаллизуется при постоянной температуре (отрезок на кривой охлаждения
оставшаяся часть жидкости кристаллизуется при постоянной температуре (отрезок на кривой охлаждения  На отрезке 1—2, т. е. при переменной температуре, из жидкости выделяются кристаллы свинца. Это согласуется с правилом фаз, так как число степеней в этом случае равняется единице. В данном случае компонентов два, число фаз равняется двум (жидкость и кристаллы свинца) и, следовательно:
На отрезке 1—2, т. е. при переменной температуре, из жидкости выделяются кристаллы свинца. Это согласуется с правилом фаз, так как число степеней в этом случае равняется единице. В данном случае компонентов два, число фаз равняется двум (жидкость и кристаллы свинца) и, следовательно:

Одновременная кристаллизация сурьмы и свинца должна протекать при постоянной температуре (отрезок 2—2), так как в данном случае при этой температуре имеются три фазы (жидкость, кристаллы сурьмы, кристаллы свинца) и число степеней свободы равно нулю 

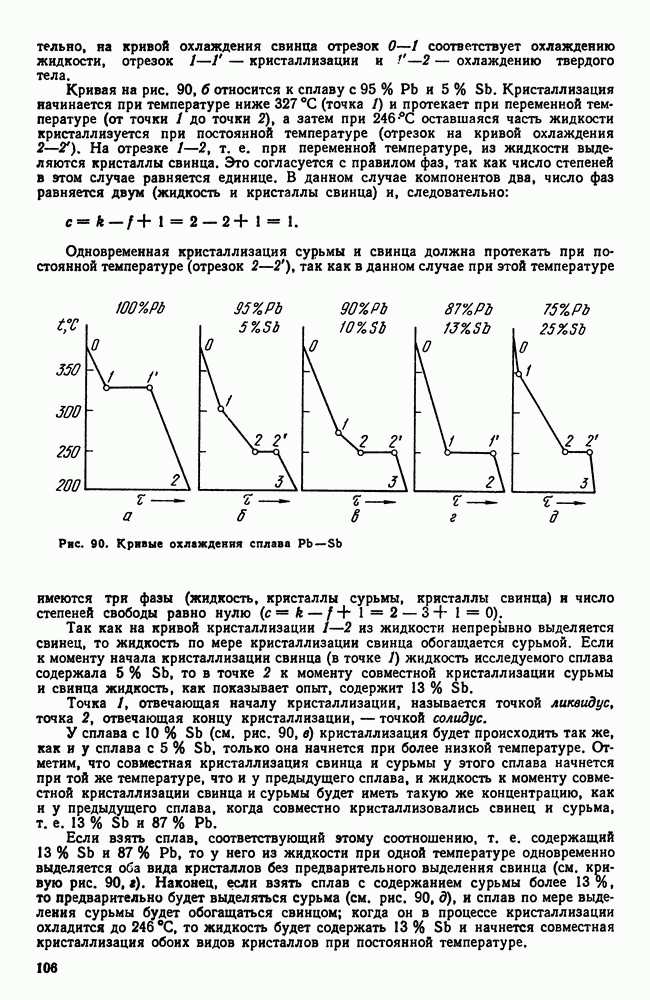
Рис. 90. Кривые охлаждения сплава 
Так как на кривой кристаллизации 1—2 из жидкости непрерывно выделяется свинец, то жидкость по мере кристаллизации свинца обогащается сурьмой. Если к моменту начала кристаллизации свинца (в точке 1) жидкость исследуемого сплава содержала  то в точке 2 к моменту совместной кристаллизации сурьмы и свинца жидкость, как показывает опыт, содержит
то в точке 2 к моменту совместной кристаллизации сурьмы и свинца жидкость, как показывает опыт, содержит 
Точка  отвечающая началу кристаллизации, называется точкой ликвидус, точка 2, отвечающая концу кристаллизации, — точкой солидус.
отвечающая началу кристаллизации, называется точкой ликвидус, точка 2, отвечающая концу кристаллизации, — точкой солидус.
У сплава с  (см. рис. 90, в) кристаллизация будет происходить так же, как и у сплава с
(см. рис. 90, в) кристаллизация будет происходить так же, как и у сплава с  только она начнется при более низкой температуре. Отметим, что совместная кристаллизация свинца и сурьмы у этого сплава начнется при той же температуре, что и у предыдущего сплава, и жидкость к моменту совместной кристаллизации свинца и сурьмы будет иметь такую же концентрацию, как и у предыдущего сплава, когда совместно кристаллизовались свинец и сурьма, т. е.
только она начнется при более низкой температуре. Отметим, что совместная кристаллизация свинца и сурьмы у этого сплава начнется при той же температуре, что и у предыдущего сплава, и жидкость к моменту совместной кристаллизации свинца и сурьмы будет иметь такую же концентрацию, как и у предыдущего сплава, когда совместно кристаллизовались свинец и сурьма, т. е. 
Если взять сплав, соответствующий этому соотношению, т. е. содержащий  то у него из жидкости при одной температуре одновременно выделяется оба вида кристаллов без предварительного выделения свинца (см. кривую рис.
то у него из жидкости при одной температуре одновременно выделяется оба вида кристаллов без предварительного выделения свинца (см. кривую рис.  Наконец, если взять сплав с содержанием сурьмы более 13%, то предварительно будет выделяться сурьма (см. рис. 90, д), и сплав по мере выделения сурьмы будет обогащаться свинцом; когда он в процессе кристаллизации охладится до
Наконец, если взять сплав с содержанием сурьмы более 13%, то предварительно будет выделяться сурьма (см. рис. 90, д), и сплав по мере выделения сурьмы будет обогащаться свинцом; когда он в процессе кристаллизации охладится до  то жидкость будет содержать
то жидкость будет содержать  и начнется совместная кристаллизация обоих видов кристаллов при постоянной температуре.
и начнется совместная кристаллизация обоих видов кристаллов при постоянной температуре.
У рассмотренных пяти сплавов точки начала  и конца
и конца  кристаллизации будут находиться при следующих температурах:
кристаллизации будут находиться при следующих температурах:

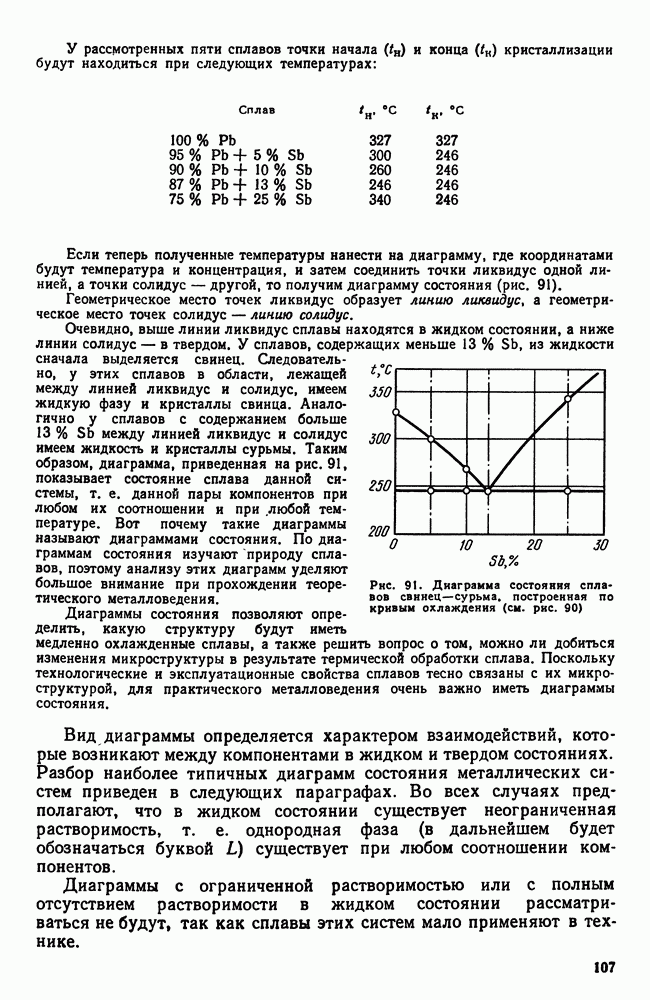
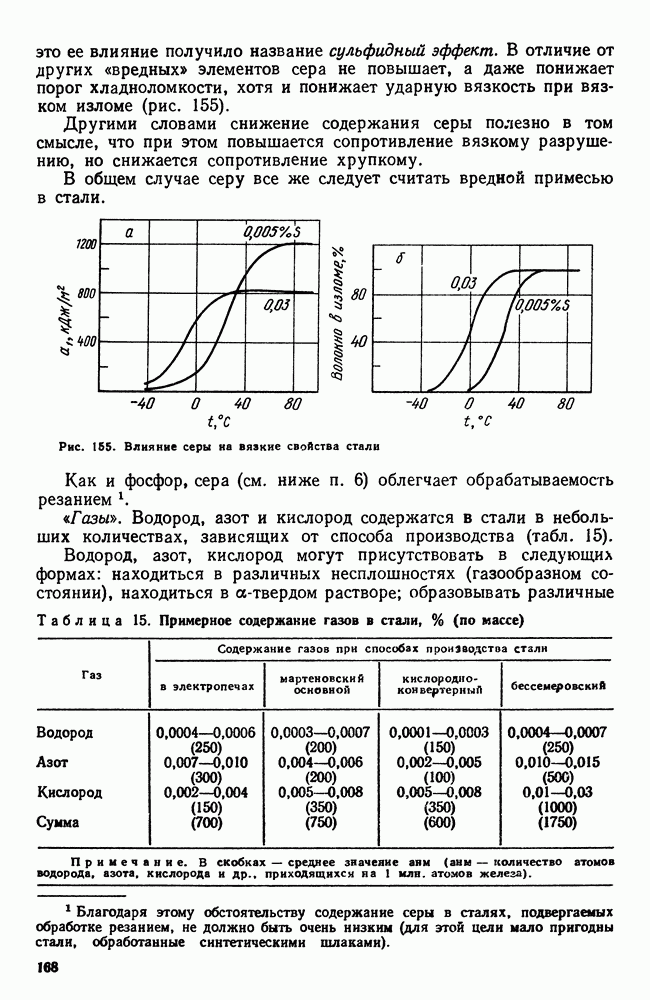
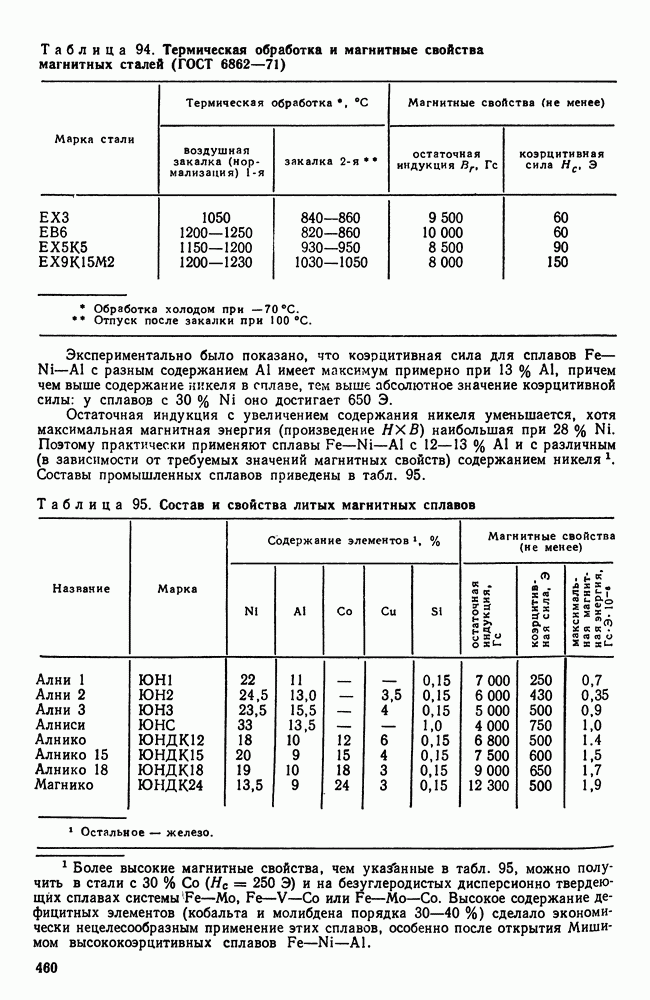
Если теперь полученные температуры нанести на диаграмму, где координатами будут температура и концентрация, и затем соединить точки ликвидус одной линией, а точки солидус — другой, то получим диаграмму состояния (рис. 91).
Геометрическое место точек ликвидус образует линию ликвидус, а геометрическое место точек солидус — линию солидус.
Очевидно, выше линии ликвидус сплавы находятся в жидком состоянии, а ниже линии солидус — в твердом. У сплавов, содержащих меньше  из жидкости сначала выделяется свинец. Следовательно, у этих сплавов в области, лежащей между линией ликвидус и солидус, имеем жидкую фазу и кристаллы свинца. Аналогично у сплавов с содержанием больше
из жидкости сначала выделяется свинец. Следовательно, у этих сплавов в области, лежащей между линией ликвидус и солидус, имеем жидкую фазу и кристаллы свинца. Аналогично у сплавов с содержанием больше  между линией ликвидус и солидус имеем жидкость и кристаллы сурьмы. Таким образом, диаграмма, приведенная на рис. 91, показывает состояние сплава данной системы, т. е. данной пары компонентов при любом их соотношении и при любой температуре. Вот почему такие диаграммы называют диаграммами состояния. По диаграммам состояния изучают природу сплавов, поэтому анализу этих диаграмм уделяют большое внимание при прохождении теоретического металловедения.
между линией ликвидус и солидус имеем жидкость и кристаллы сурьмы. Таким образом, диаграмма, приведенная на рис. 91, показывает состояние сплава данной системы, т. е. данной пары компонентов при любом их соотношении и при любой температуре. Вот почему такие диаграммы называют диаграммами состояния. По диаграммам состояния изучают природу сплавов, поэтому анализу этих диаграмм уделяют большое внимание при прохождении теоретического металловедения.

Рис. 91. Диаграмма состояния сплавов свинец—сурьма, построенная по кривым охлаждения (см. рис. 90)
Диаграммы состояния позволяют определить, какую структуру будут иметь медленно охлажденные сплавы, а также решить вопрос о том, можно ли добиться изменения микроструктуры в результате термической обработки сплава. Поскольку технологические и эксплуатационные свойства сплавов тесно связаны с их микроструктурой, для практического металловедения очень важно иметь диаграммы состояния.
Вид диаграммы определяется характером взаимодействий, которые возникают между компонентами в жидком и твердом состояниях. Разбор наиболее типичных диаграмм состояния металлических систем приведен в следующих параграфах. Во всех случаях предполагают, что в жидком состоянии существует неограниченная растворимость, т. е. однородная фаза (в дальнейшем будет обозначаться буквой  существует при любом соотношении компонентов.
существует при любом соотношении компонентов.
Диаграммы с ограниченной растворимостью или с полным отсутствием растворимости в жидком состоянии рассматриваться не будут, так как сплавы этих систем мало применяют в технике.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Часть первая. ТЕОРИЯ СПЛАВОВ
- Глава I. КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ
- 2. Классификация металлов
- 3. Кристаллическое строение металлов
- 4. Кристаллические решетки металлов
- 5. Реальное строение металлических кристаллов
- 6. Анизотропия свойств кристаллов
- 7. Методы изучения строения металлов
- Глава II. КРИСТАЛЛИЗАЦИЯ
- 1. Три состояния вещества
- 2. Энергетические условия процесса кристаллизации
- 3. Механизм процесса кристаллизации
- 4. Форма кристаллических образований
- 5. Строение слитка
- 6. Превращения в твердом состояние. Полиморфизм
- 7. Магнитные превращения
- 8. Закалка из жидкого состояния. Аморфное состояние
- Глава III. МЕХАНИЧЕСКИЕ СВОЙСТВА. НАКЛЕП И РЕКРИСТАЛЛИЗАЦИЯ
- 2. Упругая и пластическая деформация. Несовершенства решетки и прочность металлов
- 3. Сверхпластичность
- 4. Разрушение
- 5. Методы определения механических свойств
- 6. Наклеп
- 7. Влияние нагрева на строение и свойства деформированного металла (рекристаллизационные процессы)
- Глава IV. СТРОЕНИЕ СПЛАВОВ
- 2. Химическое соединение
- 3. Твердый раствор на основе одного из компонентов сплава
- 4. Твердый раствор на основе химического соединения
- 5. Упорядоченные твердые растворы
- 6. Электронные соединения (фазы Юм-Розери)
- 7. Фазы Лавеса
- 8. Фазы внедрения
- Глава V. ДИАГРАММА СОСТОЯНИЯ
- 2. Общие замечания о построении диаграмм состояния
- 3. Экспериментальное построение диаграмм
- 4. Диаграмма состояния для сплавов, образующих механические смеси из чистых компонентов (I рода)
- 5. Правило отрезков
- 6. Диаграмма состояния для сплавов с неограниченной растворимостью в твердом состоянии (II рода)
- 7. Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии (III рода)
- 8. Диаграмма состояния для сплавов, образующих химические соединения (IV рода)
- 9. Диаграмма состояния для сплавов, испытывающих полиморфные превращения
- 10. Кристаллизация сплавов в неравновесных условиях
- 11. Системы с тремя компонентами
- 12. Упрощенные методы изучения многокомпонентных систем
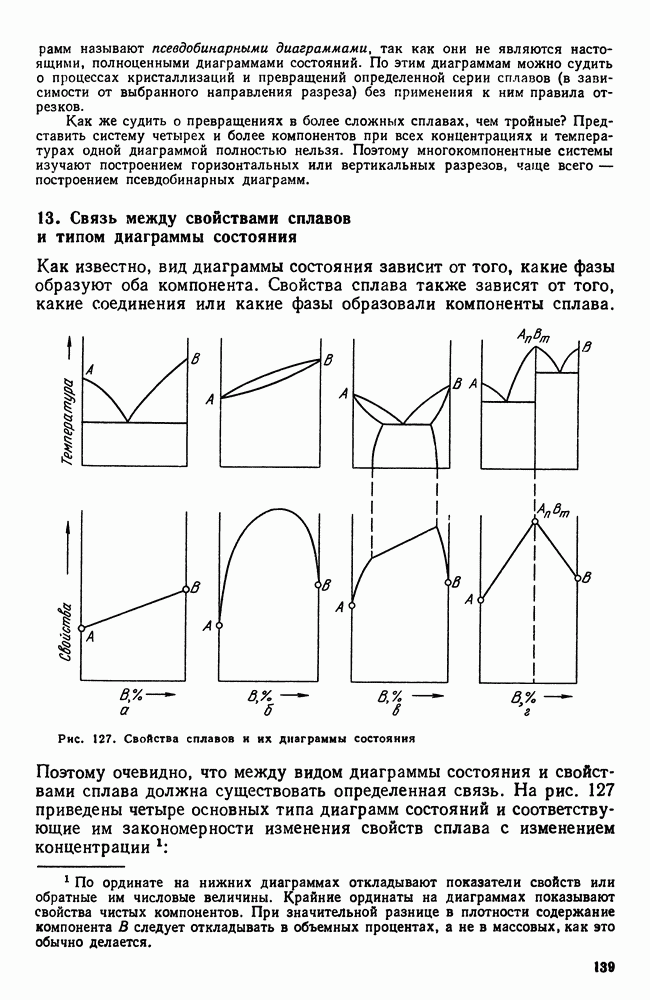
- 13. Связь между свойствами сплавов и типом диаграммы состояния
- Часть вторая. ЖЕЛЕЗОУГЛЕРОДИСТЫЕ СПЛАВЫ
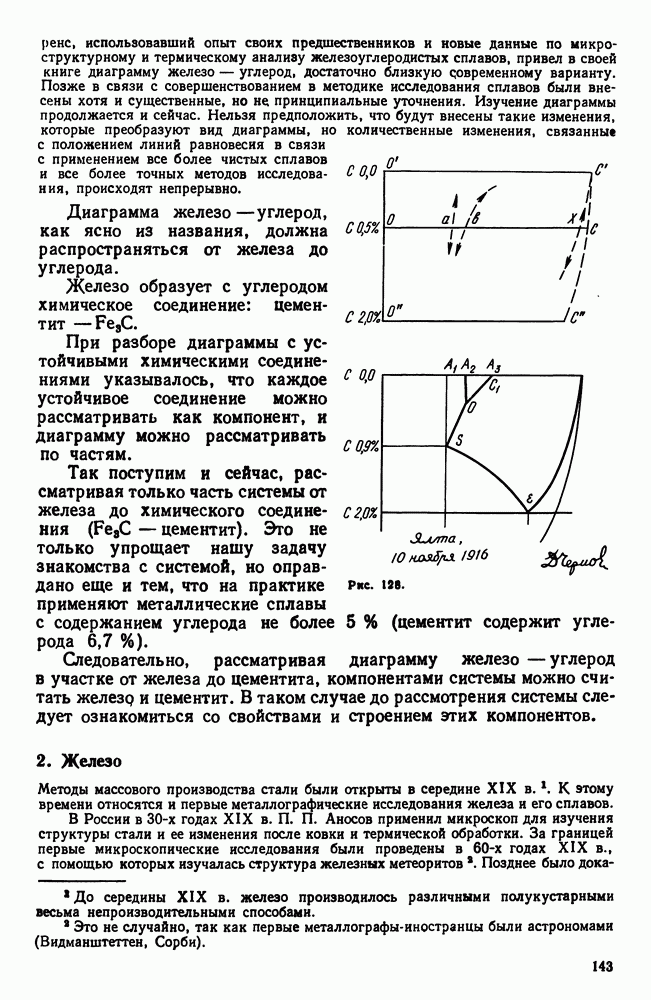
- Глава VI. ДИАГРАММА ЖЕЛЕЗО—УГЛЕРОД
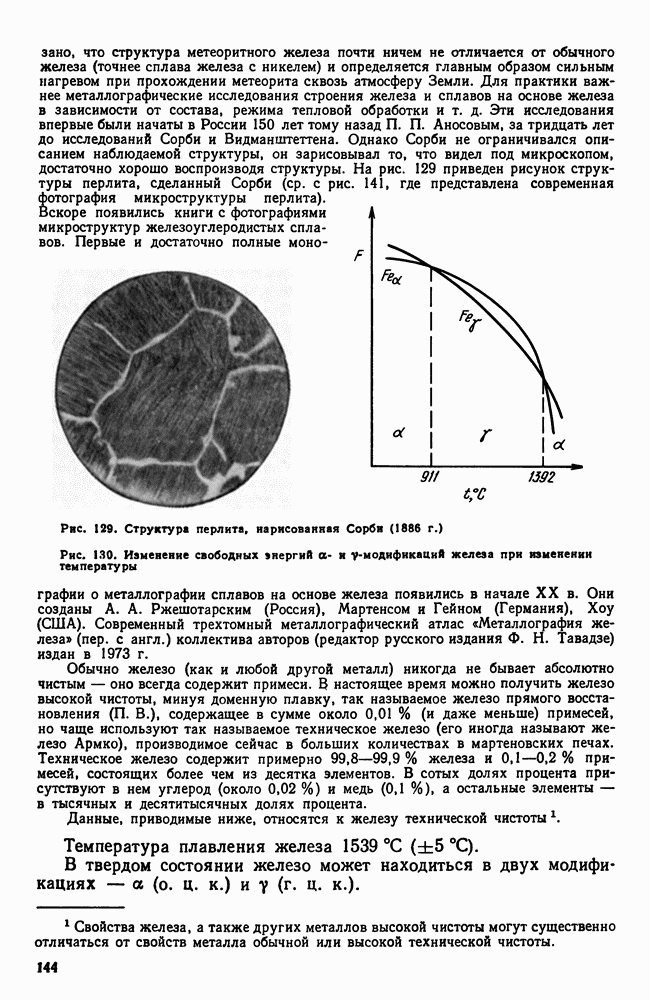
- 2. Железо
- 3. Цементит
- 4. Диаграмма состояния
- Глава VII. УГЛЕРОДИСТЫЕ СТАЛИ
- 1. Влияние углерода на свойства стали
- 2. Влияние постоянных примесей на свойства стали
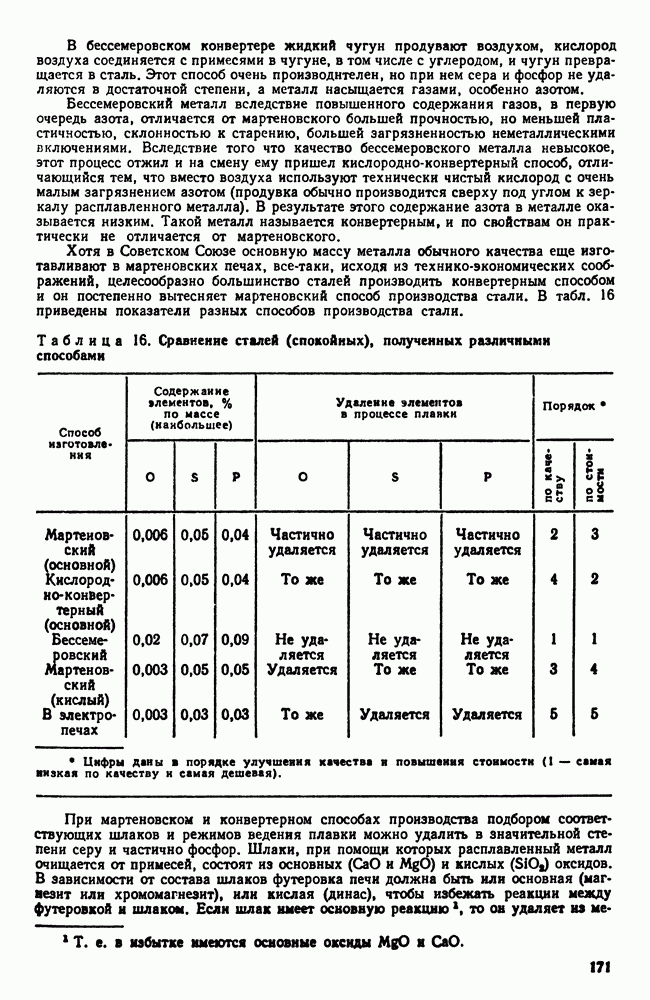
- 3. Сталь различных способов производства. Чистая сталь
- 4. Углеродистая сталь общего назначения
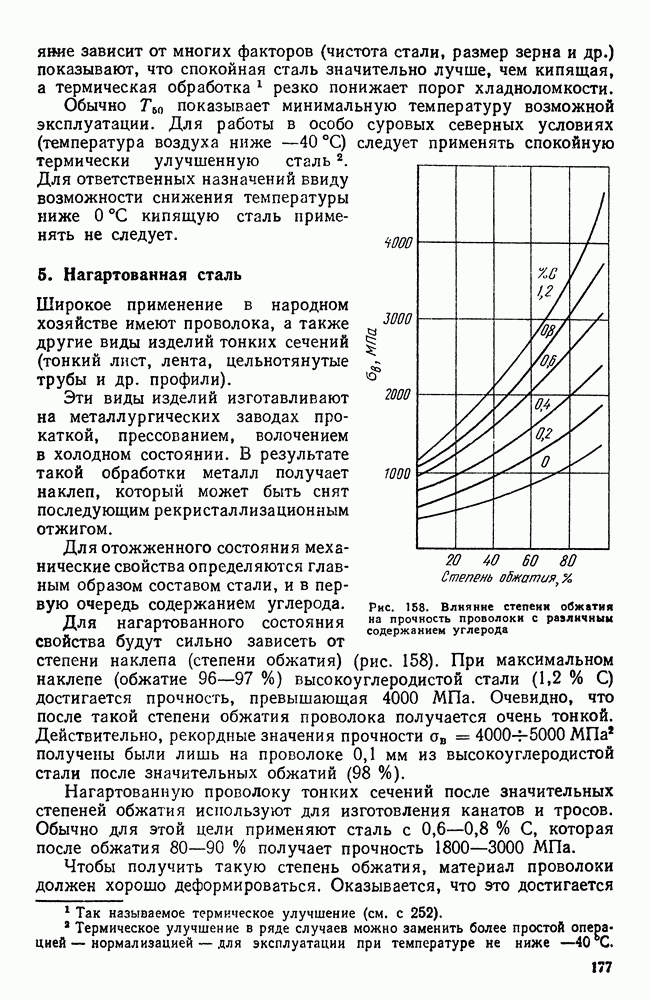
- 5. Нагартованная сталь
- 6. Листовая сталь для холодной штамповки
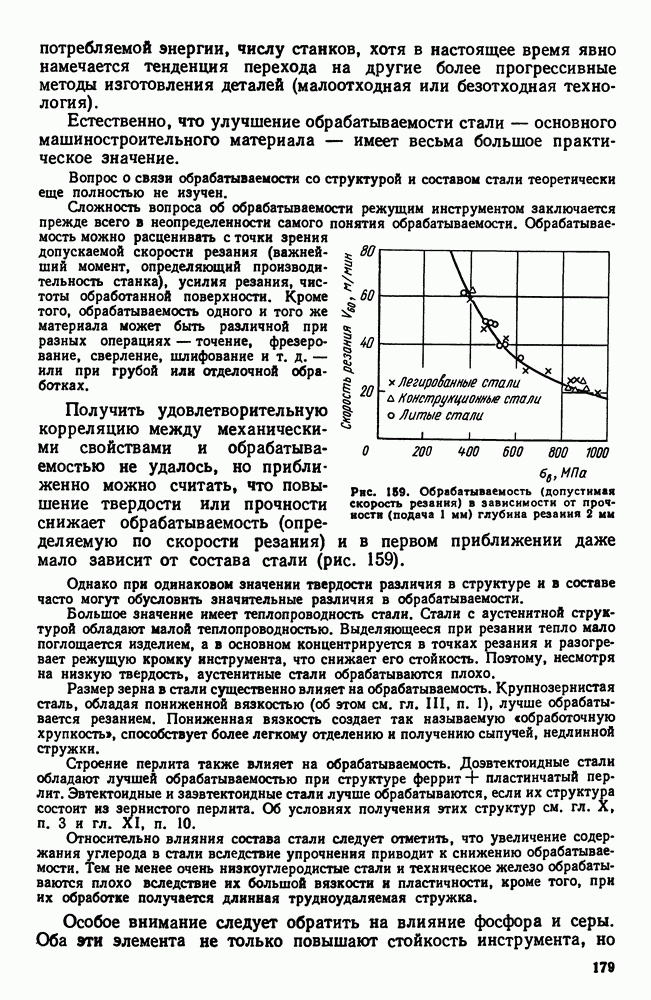
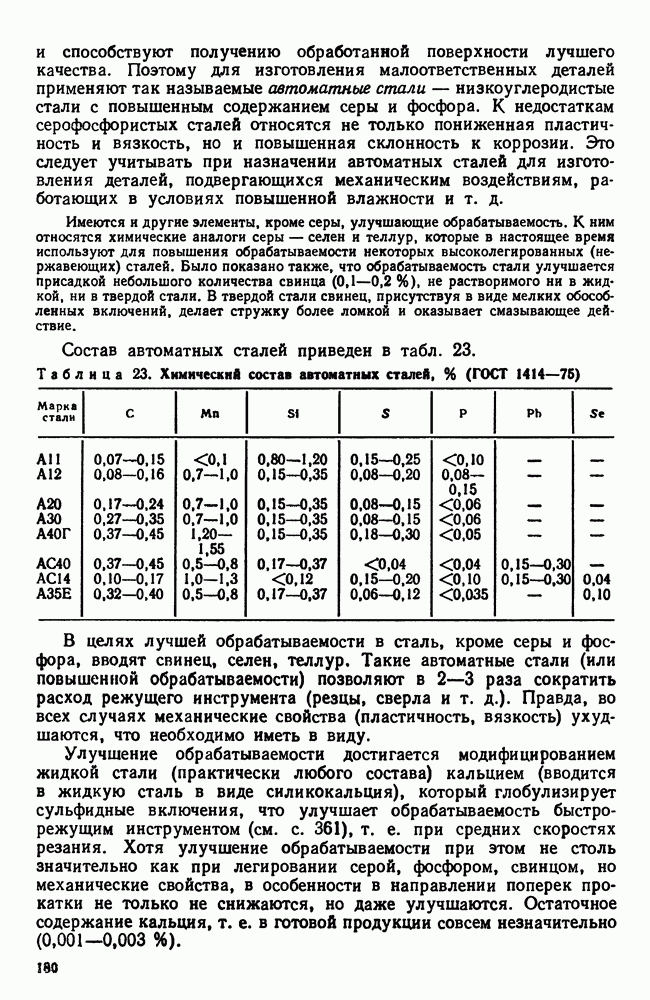
- 7. Обрабатываемость резанием. Автоматные стали
- Глава VIII. ЧУГУН
- 2. Структура чугуна. Формы графита
- 3. Структура и свойства чугуна
- 4. Примеси в чугуне
- 5. Марки серых и высокопрочных чугунов
- 6. Ковкий чугун
- Часть третья. ТЕРМИЧЕСКАЯ ОБРАБОТКА
- Глава IX. ОБЩИЕ ПОЛОЖЕНИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ
- 2. Классификация видов термической обработки
- 3. Термическая обработка и диаграмма состояния
- 4 Основные виды термической обработки стали
- 5. Четыре основных превращения в стали
- Глава X. ТЕОРИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ
- 2. Рост аустенитного зерна
- 3. Распад аустенита
- 4. Мартенситное превращение
- 5. Бейнитное превращение
- 6. Превращения при отпуске
- 7. Влияние термической обработки на свойства стали
- 8. Термомеханическая обработка
- Глава XI. ПРАКТИКА ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ
- 2. Время нагрева
- 3. Химическое воздействие нагревающей среды
- 4. Закалочные среды
- 5. Прокаливаемость
- 6. Внутренние напряжения
- 7. Способы закалки
- 8. Обработка стали холодом
- 9. Дефекты, возникающие при закалке
- 10. Отжиг и нормализация
- Глава XII. ПОВЕРХНОСТНАЯ ЗАКАЛКА СТАЛИ
- 2. Высокочастотная закалка
- Глава XIII. ХИМИКО-ТЕРМИЧЕСКАЯ ОБРАБОТКА СТАЛИ
- 2. Цементация стали
- 3. Азотирование стали
- 4. Цианирование стали
- 5. Диффузионная металлизация
- Часть четвертая. ЛЕГИРОВАННЫЕ СТАЛИ И СПЛАВЫ
- Глава XIV. ВЛИЯНИЕ ЛЕГИРУЮЩИХ ЭЛЕМЕНТОВ
- 2. Влияние элементов на полиморфизм железа
- 3. Распределение легирующих элементов в стали
- 4. Влияние легирующих элементов на феррит
- 5. Карбидная фаза в легированных сталях
- 6. Влияние легирующих элементов на превращения в стали
- Глава XV. КЛАССИФИКАЦИЯ И МАРКИРОВКА ЛЕГИРОВАННЫХ СТАЛЕЙ
- 2. Маркировка легированных сталей
- Глава XVI. КОНСТРУКЦИОННЫЕ СТАЛИ
- 1. Механические свойства стали, влияние структуры и легирующих элементов
- 2. Термическая обработка конструкционных сталей
- 3. Цементуемые (низкоуглеродистые) стали
- 4. Улучшаемые (среднеуглеродистые) стали
- 5. Высокопрочные стали
- 6. Свариваемость стали
- 7. Строительная сталь
- 8. Арматурная сталь
- 9. Пружинная сталь
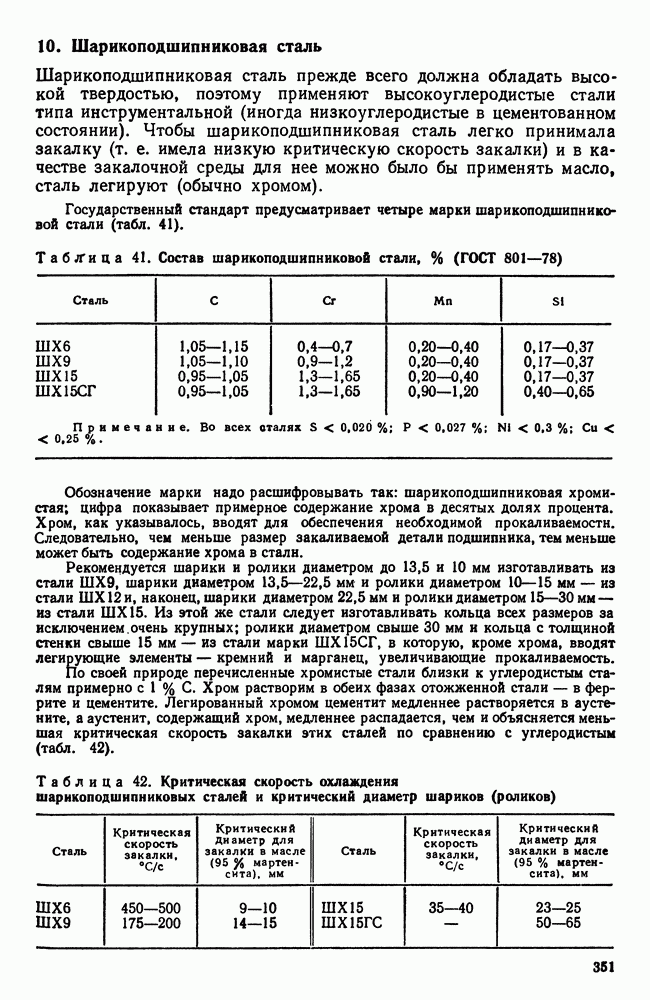
- 10. Шарикоподшипниковая сталь
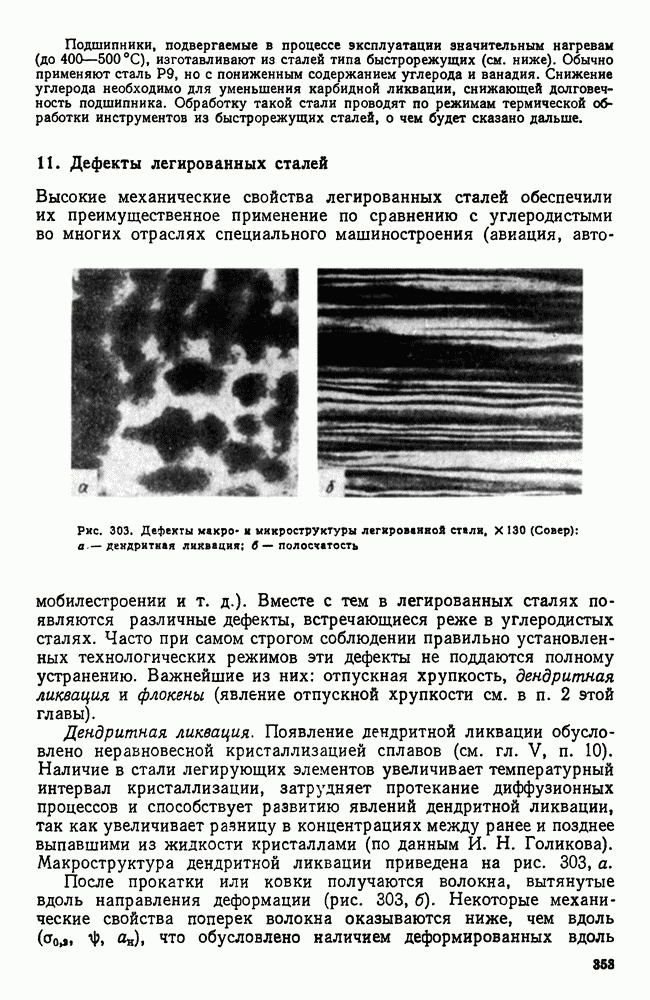
- 11. Дефекты легированных сталей
- Глава XVII. ИНСТРУМЕНТАЛЬНЫЕ СТАЛИ
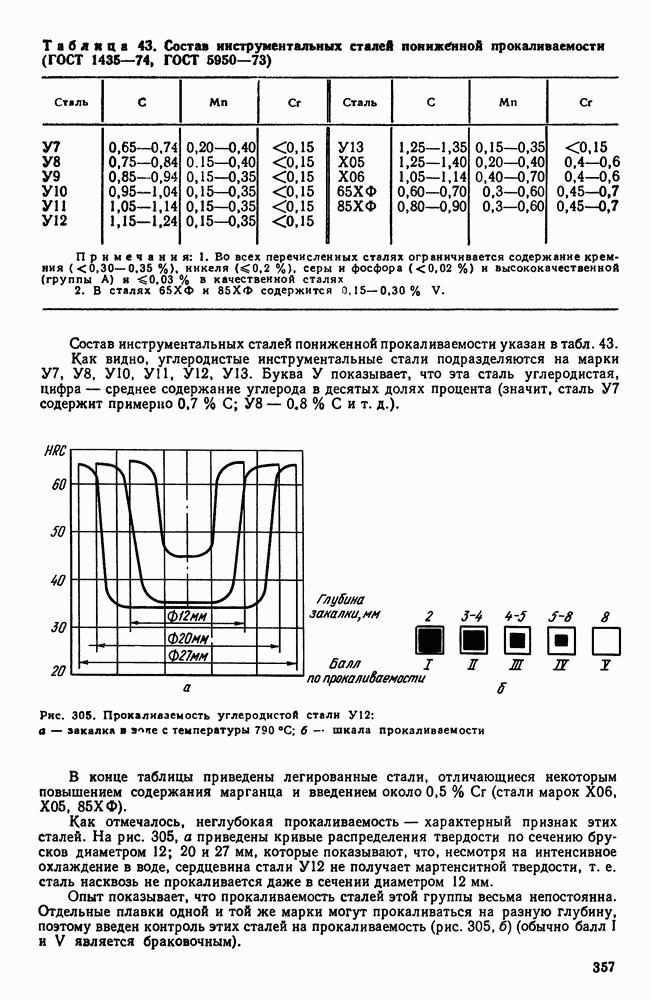
- 2. Инструментальные стали пониженной прокаливаемости
- 3. Инструментальные стали повышенной прокаливаемости (легированные инструментальные стали)
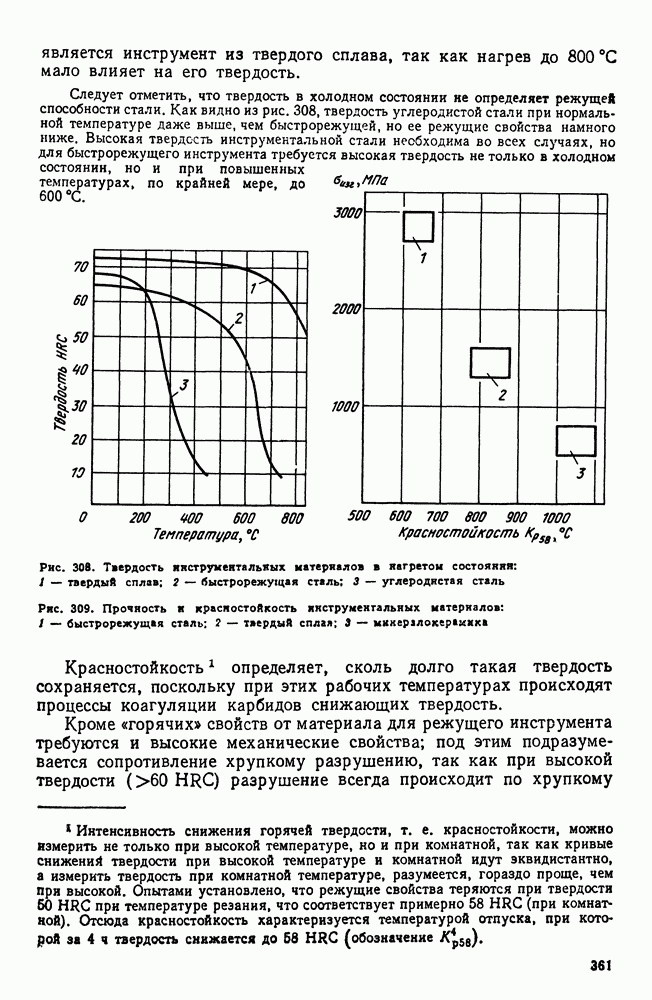
- 4. Быстрорежущие стали
- 5. Штамповые стали
- 6. Твердые сплавы
- Глава XVIII. ЖАРОСТОЙКИЕ И ЖАРОПРОЧНЫЕ СТАЛИ И СПЛАВЫ
- 2. Жаропрочность
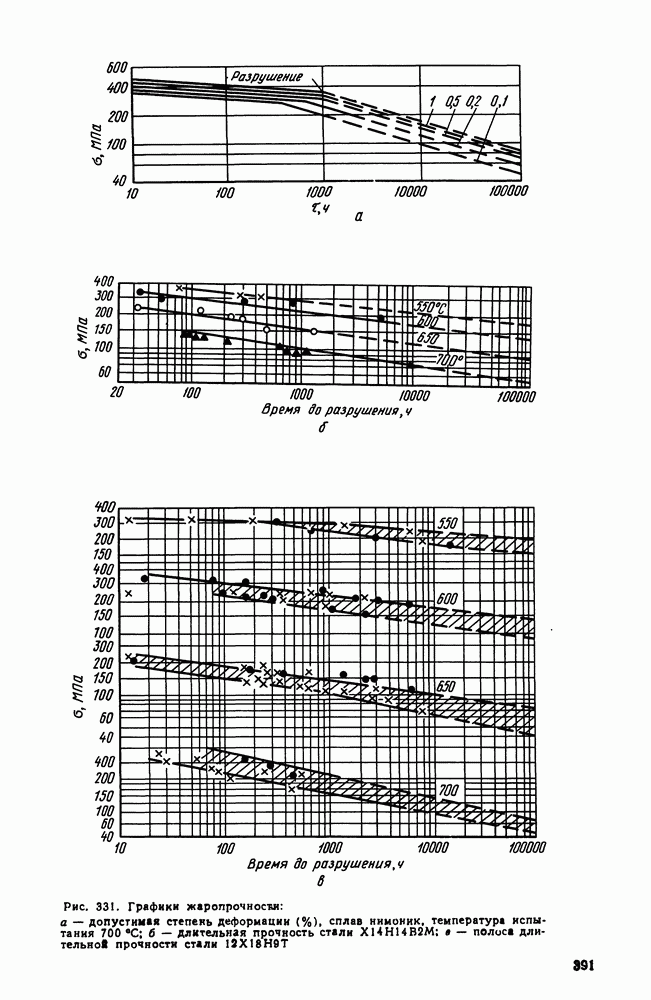
- 3. Оценка жаропрочных свойств
- 4. Влияние структуры и состава на жаропрочность
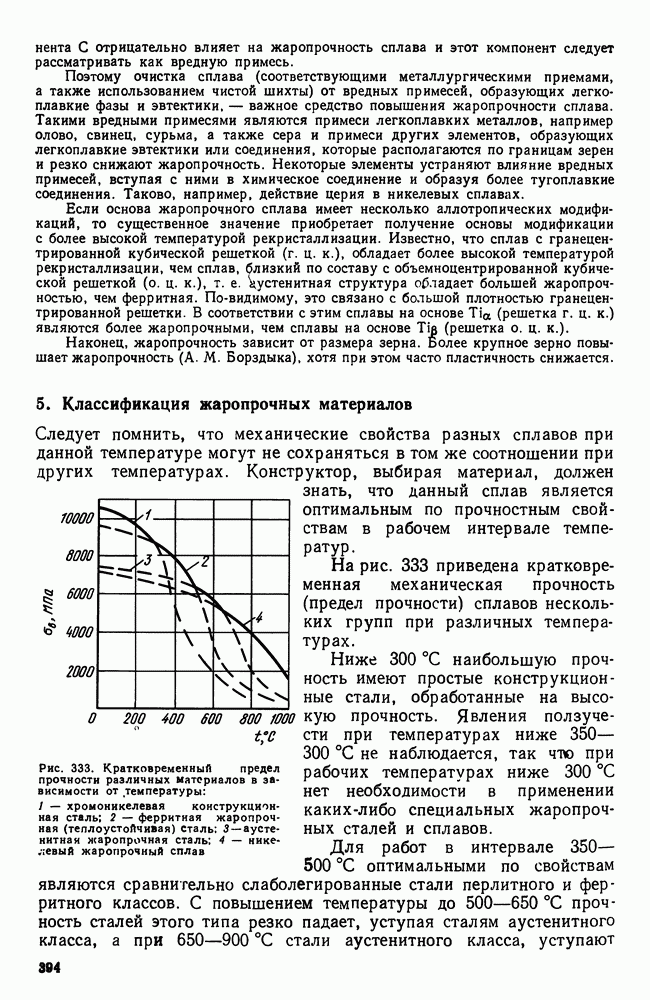
- 5. Классификация жаропрочных материалов
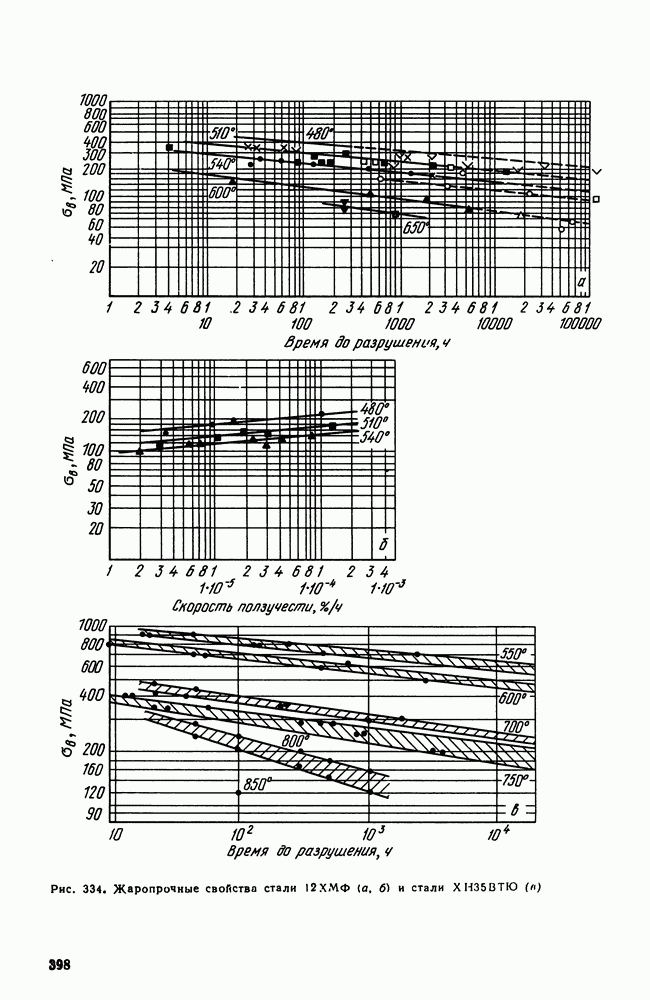
- 6. Перлитные и мартенситные жаропрочные стали
- 7. Аустенитные жаропрочные стали
- 8. Никелевые и кобальтовые жаропрочные сплавы
- Глава XIX. КОРРОЗИОННОСТОЙКИЕ (НЕРЖАВЕЮЩИЕ) СТАЛИ И СПЛАВЫ
- 2. Хромоникелевые нержавеющие стали
- 3. Кислотостойкие стали и сплавы
- 4. Криогенные стали и сплавы
- Глава XX. ИЗНОСОСТОЙКИЕ СТАЛИ И СПЛАВЫ
- 2. Графитизированная сталь
- 3. Высокомарганцовистая сталь
- 4. Наплавочные материалы
- Глава XXI. ТИТАН И ЕГО СПЛАВЫ
- 2. Легирование титана
- 3. Фазовые превращения в титановых сплавах
- 5. Термическая обработка титановых сплавов
- 6. Примеси в титановых сплавах
- 7. Коррозионная стойкость титана
- Глава XXII. ТУГОПЛАВКИЕ МЕТАЛЛЫ
- 2. Взаимодействие тугоплавких металлов с другими элементами и между собой
- 3. Механические свойства и жаропрочность
- 4. Хладноломкость тугоплавких металлов
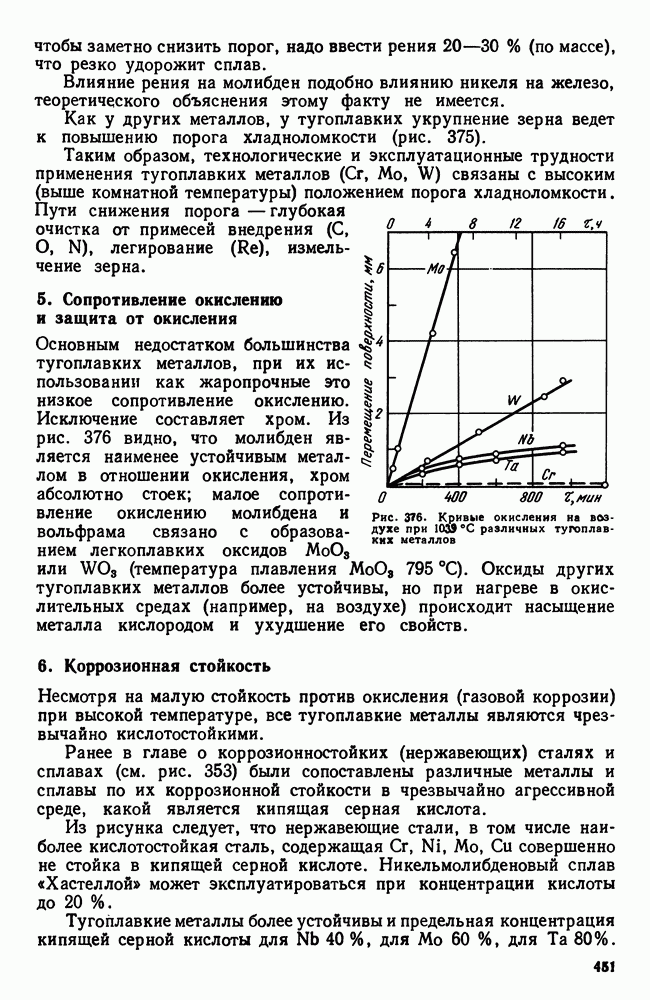
- 5. Сопротивление окислению и защита от окисления
- 6. Коррозионная стойкость
- Глава XXIII. СПЛАВЫ С ОСОБЫМИ ТЕПЛОВЫМИ И УПРУГИМИ СВОЙСТВАМИ
- 2. Сплавы с постоянным модулем упругости
- Глава XXIV. МАГНИТНЫЕ СТАЛИ И СПЛАВЫ
- 2. Стали и сплавы для постоянных магнитов (магнитнотвердые сплавы)
- 3. Магнитномягкие сплавы
- 4. Немагнитные стали
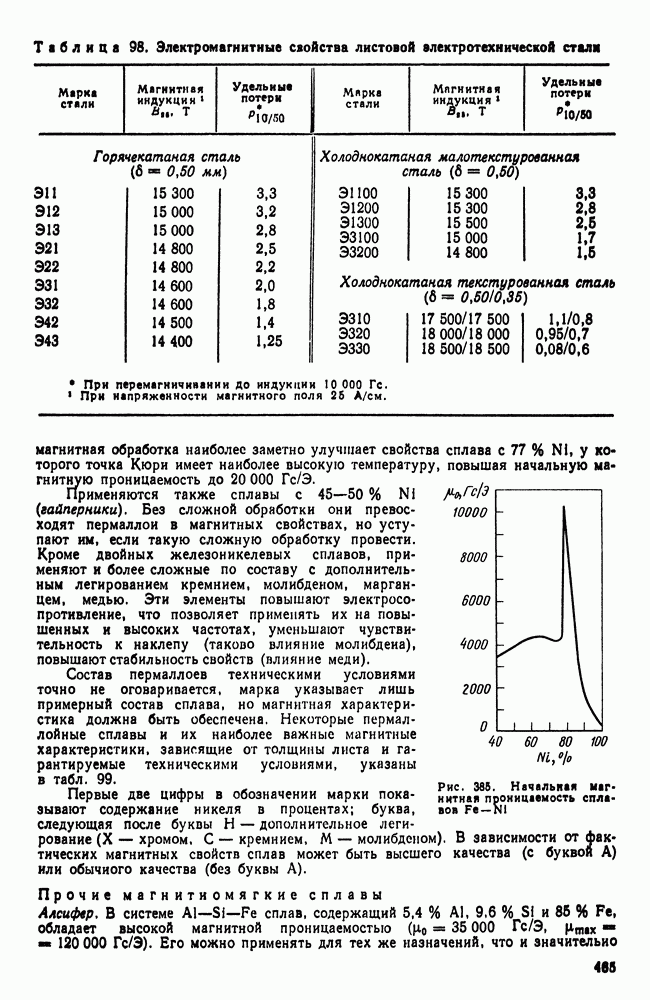
- 5. Электротехнические сплавы
- Глава XXV. СПЛАВЫ АТОМНОЙ ЭНЕРГЕТИКИ
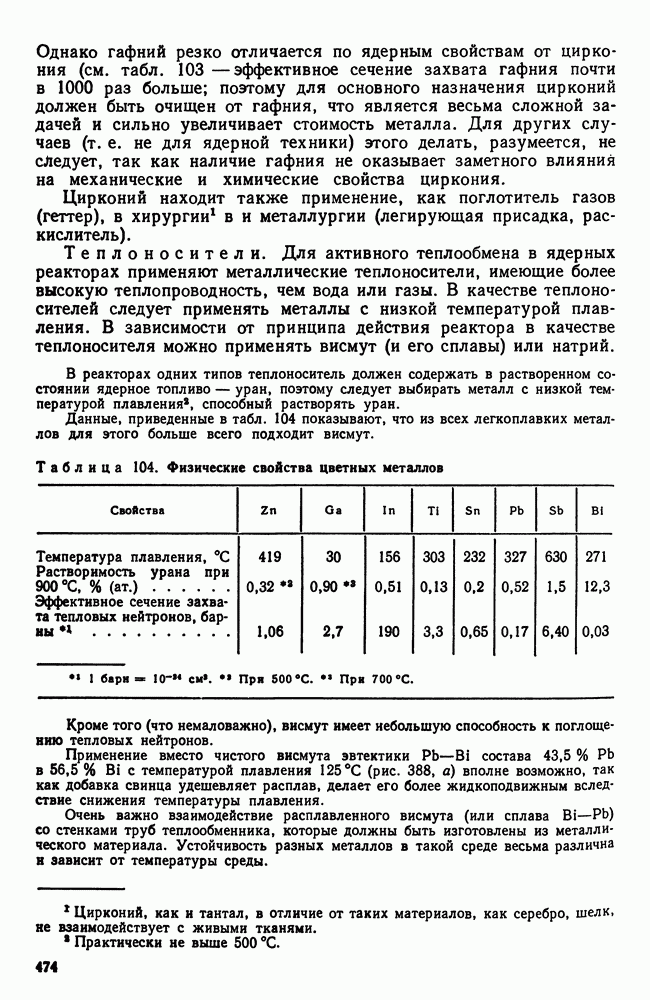
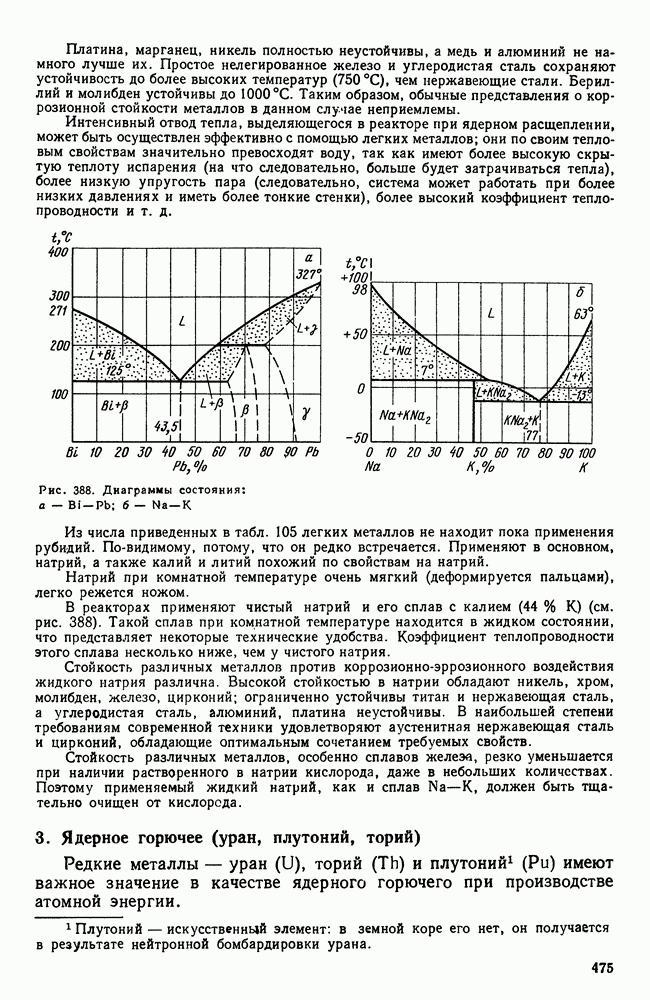
- 2. Конструкционные материалы. Теплоносители
- 3. Ядерное горючее (уран, плутоний, торий)
- Часть пятая. Цветные металлы и сплавы
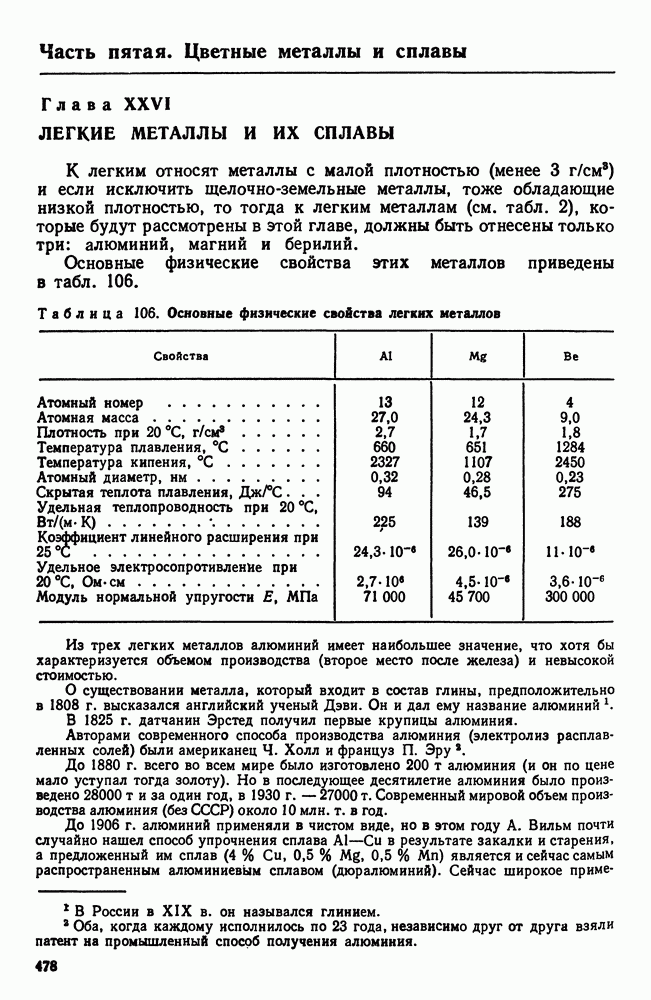
- Глава XXVI. ЛЕГКИЕ МЕТАЛЛЫ И ИХ СПЛАВЫ
- 1. Свойства алюминия
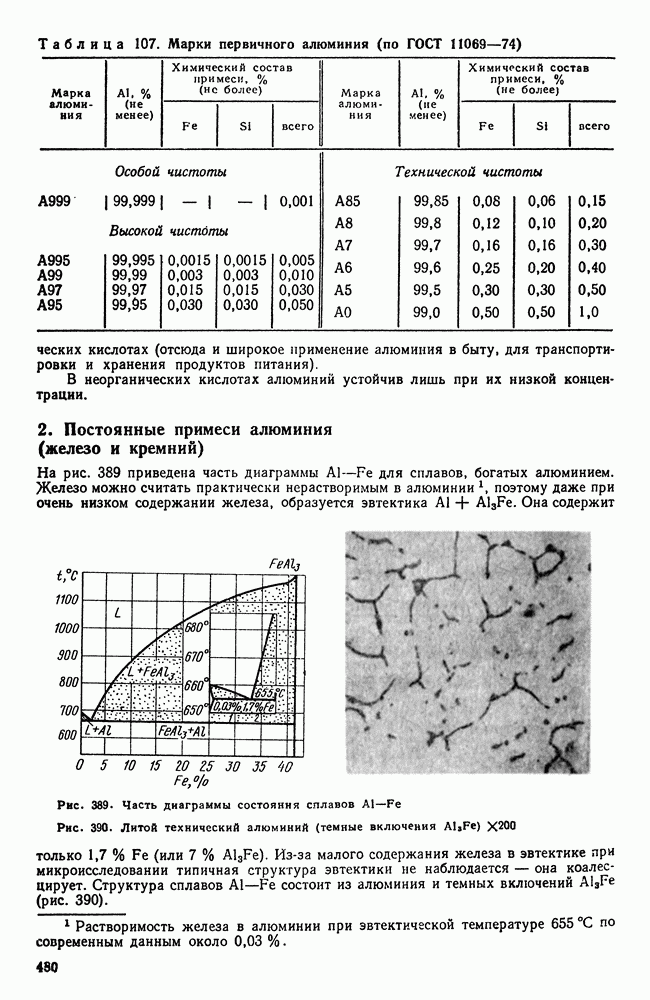
- 2. Постоянные примеси алюминия (железо и кремний)
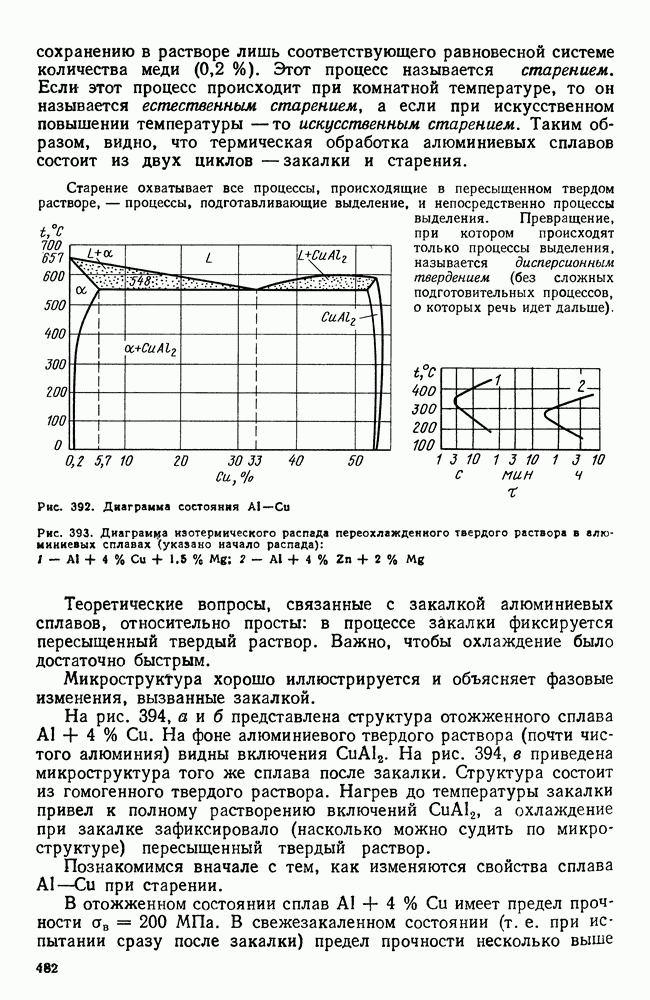
- 3. Термическая обработка сплавов Al-Cu
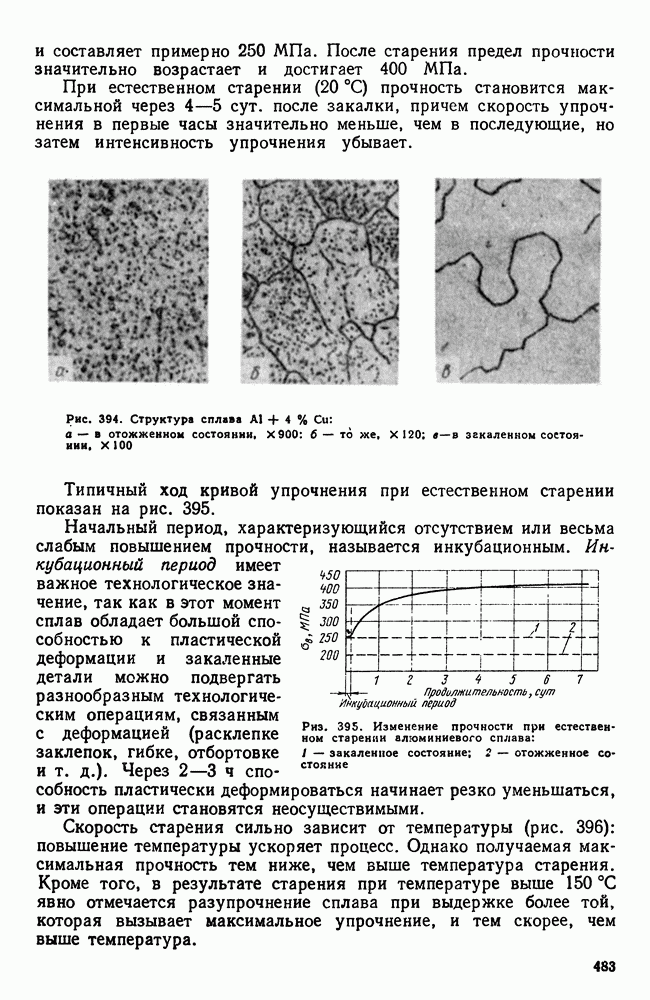
- 4. Влияние состава алюминиевых сплавов на процессы, происходящие при термической обработке
- 5. Классификация алюминиевых сплавов
- 6. Деформируемые сплавы, не упрочняемые термической обработкой
- 7. Дюралюминий и другие деформируемые сплавы, упрочняемые термической обработкой
- 8. Алюминиевые сплавы для поковок и штамповок
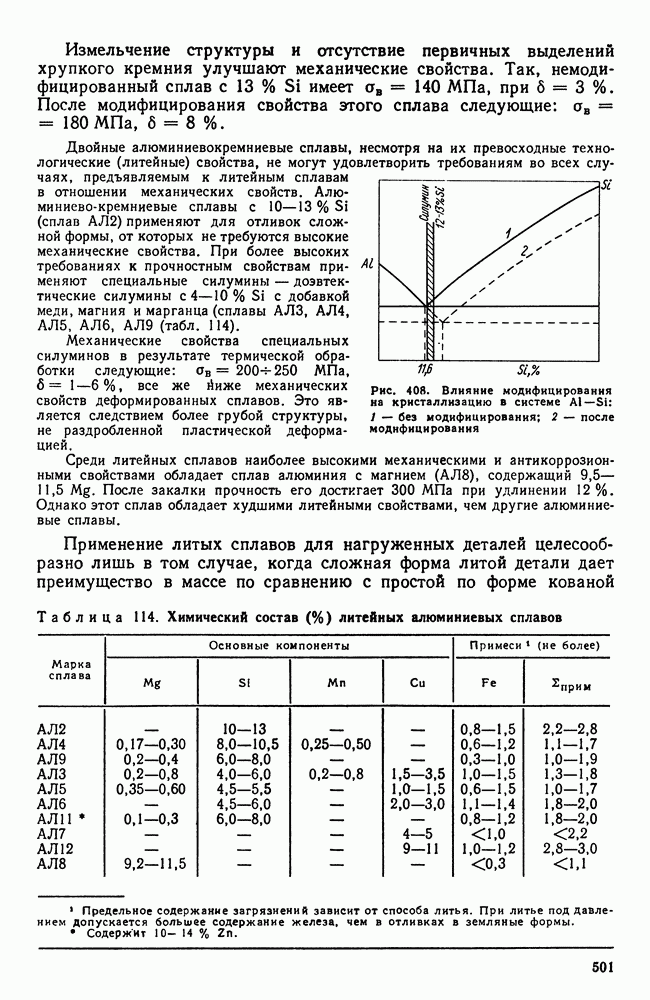
- 9. Силумины и другие алюминиевые сплавы для фасонного литья
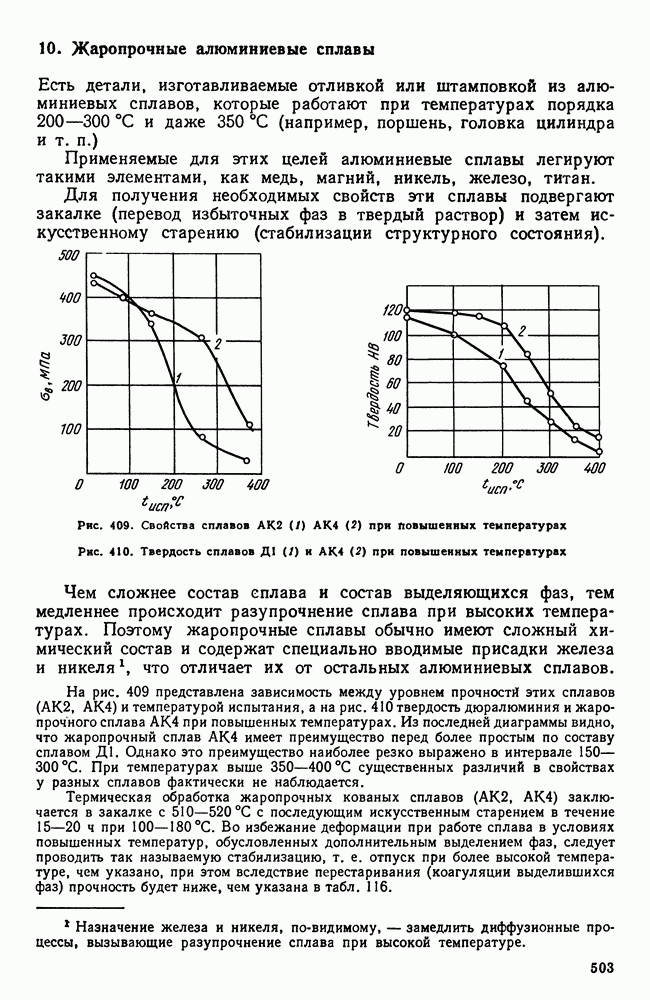
- 10. Жаропрочные алюминиевые сплавы
- 11. Магний
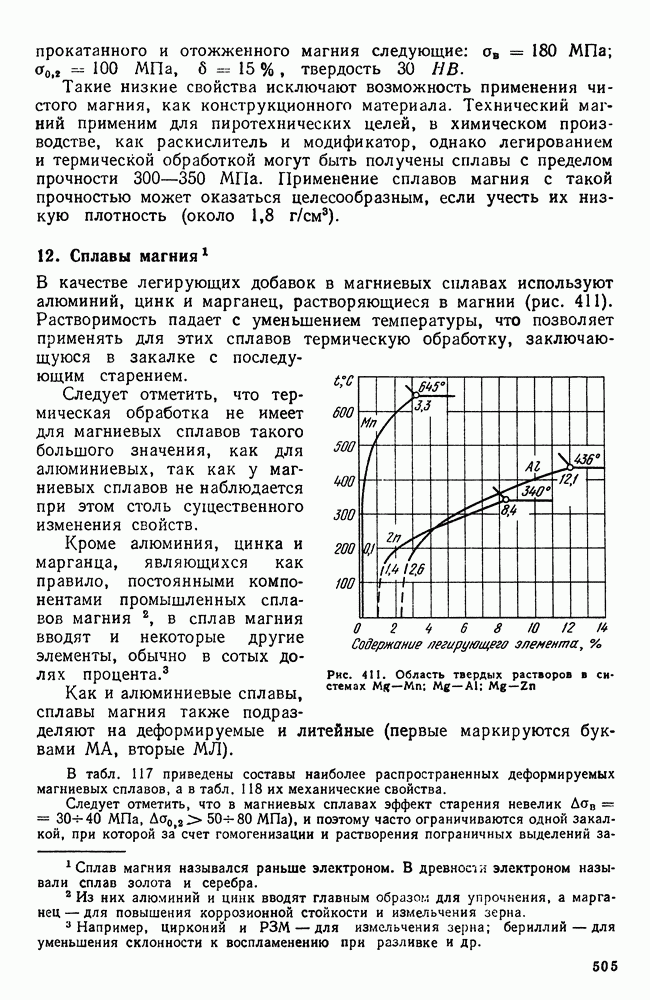
- 12. Сплавы магния
- 13. Бериллий
- 14. Сплавы бериллия
- Глава XXVII. МЕДЬ И ЕЕ СПЛАВЫ
- 2. Сплавы меди с цинком (латуни)
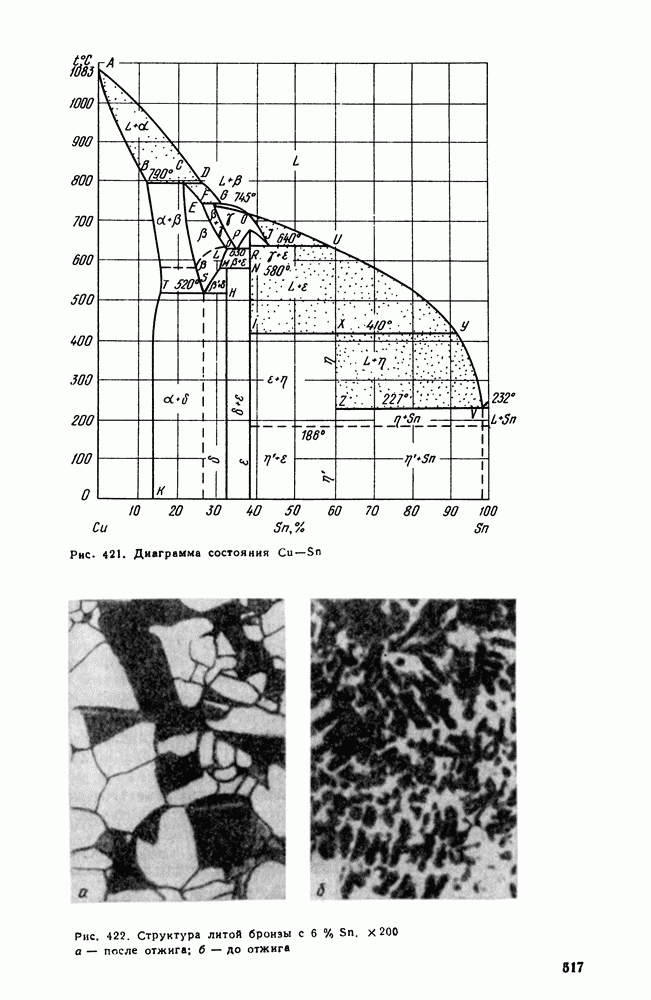
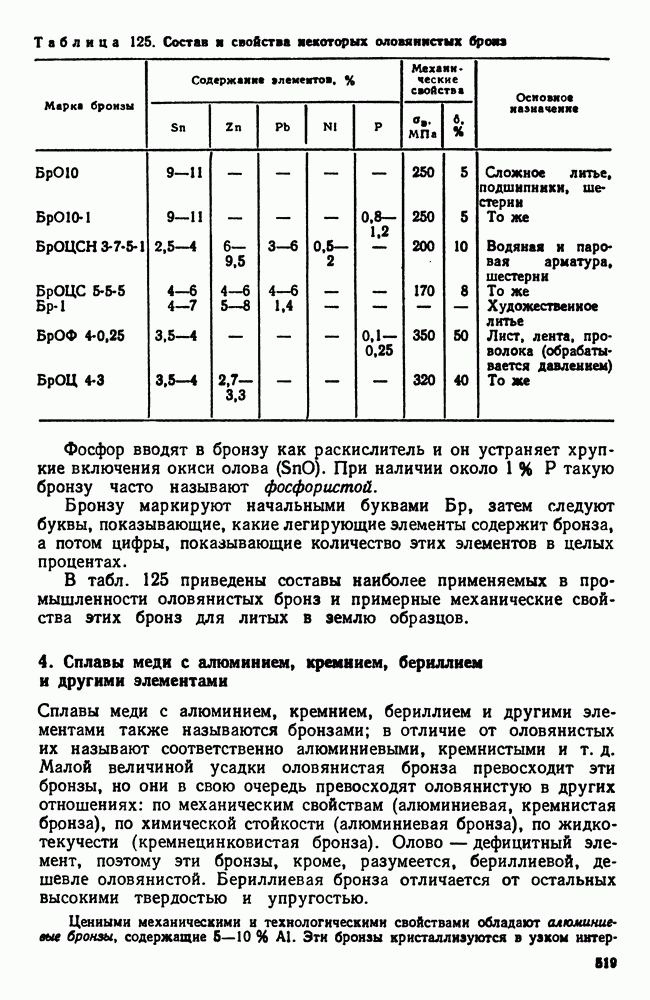
- 3. Сплавы меди с оловом (оловянистые бронзы)
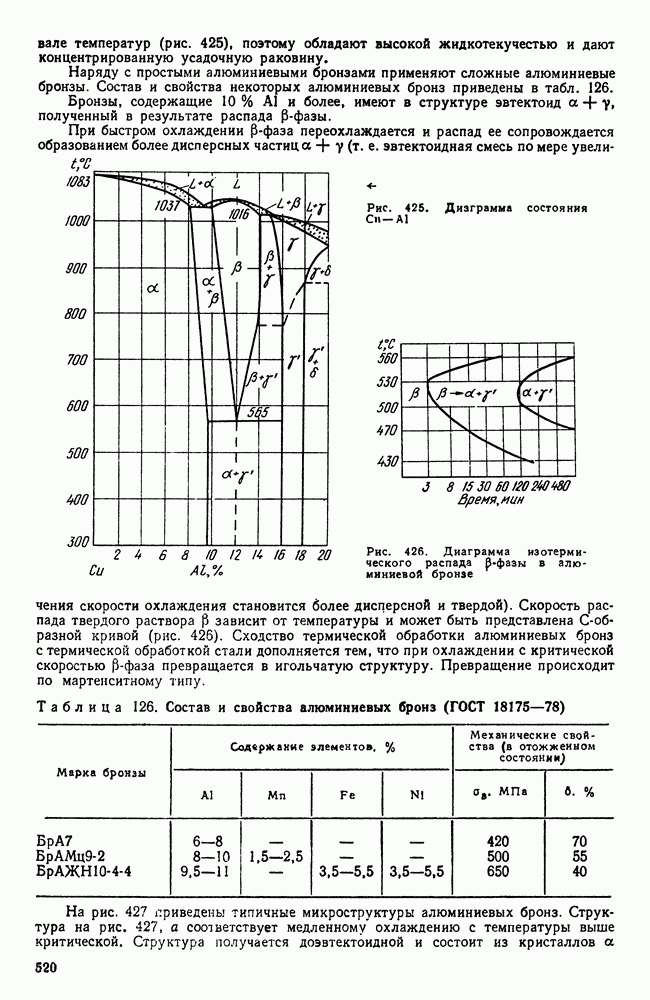
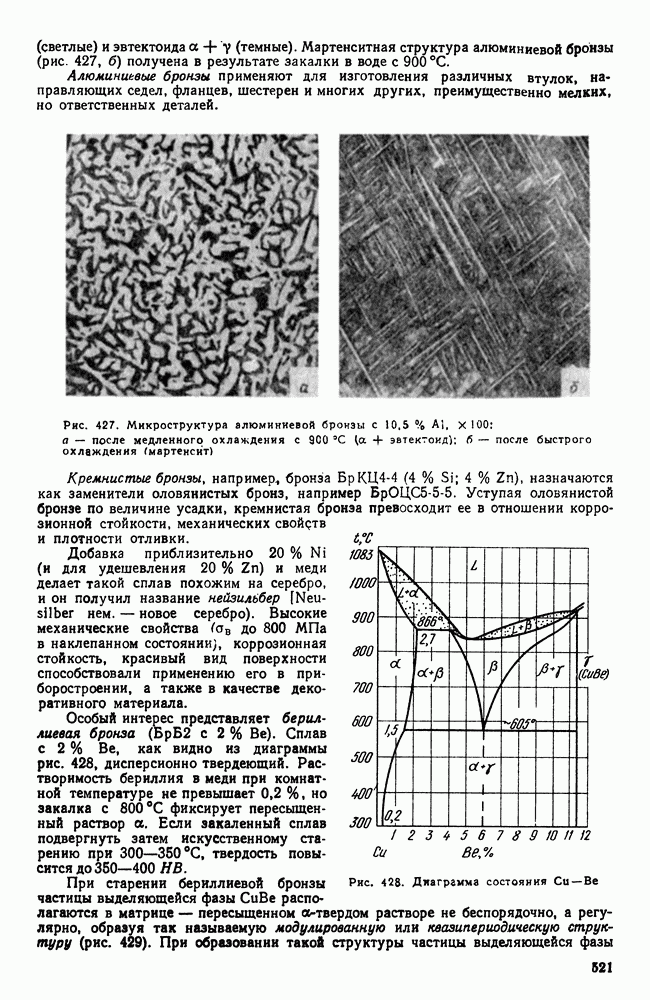
- 4. Сплавы меди с алюминием, кремнием, бериллием и другими элементами
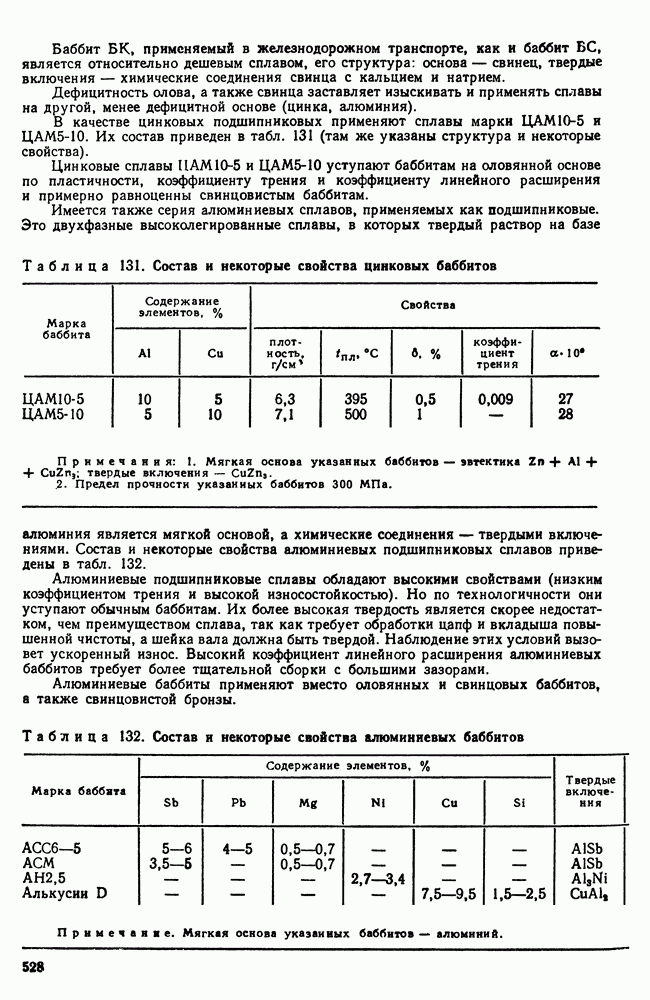
- ГЛАВА XXVIII. ПОДШИПНИКОВЫЕ СПЛАВЫ И ПРИПОИ
- 2. Легкоплавкие подшипниковые сплавы (баббиты)
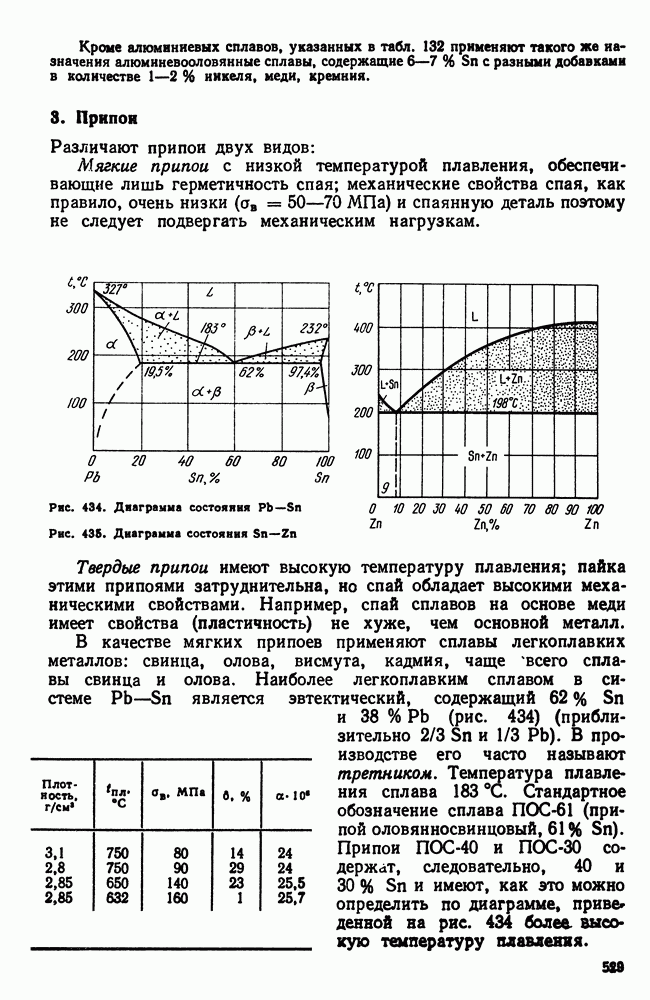
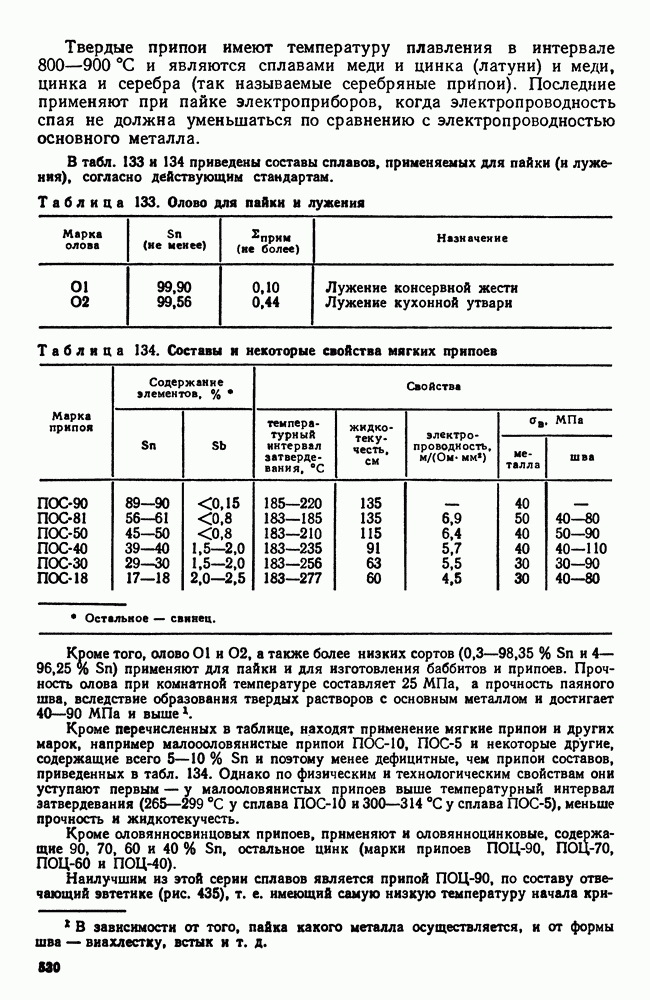
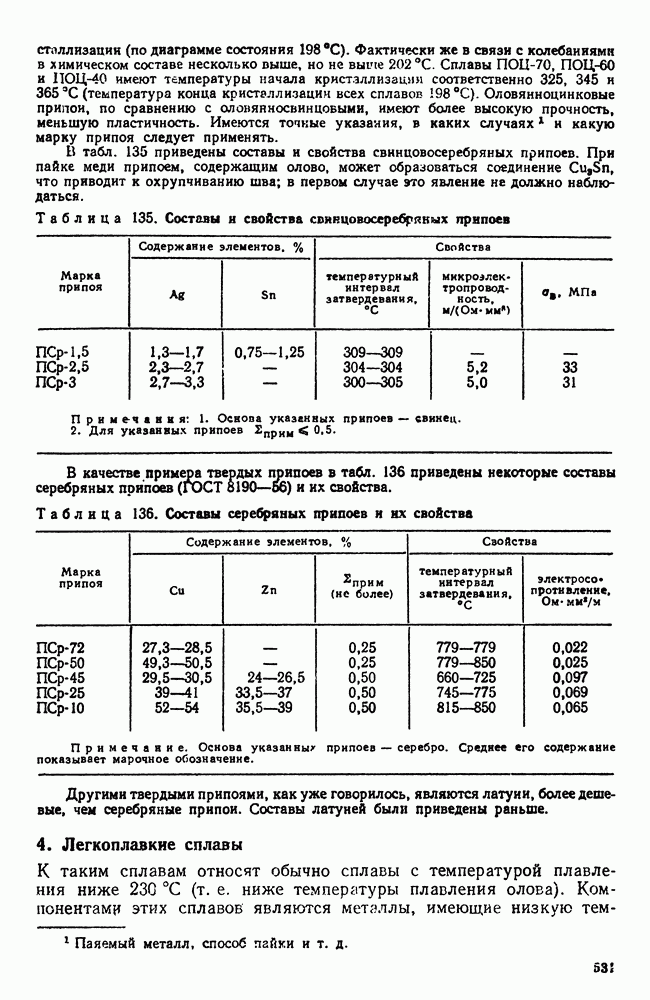
- 3. Припои
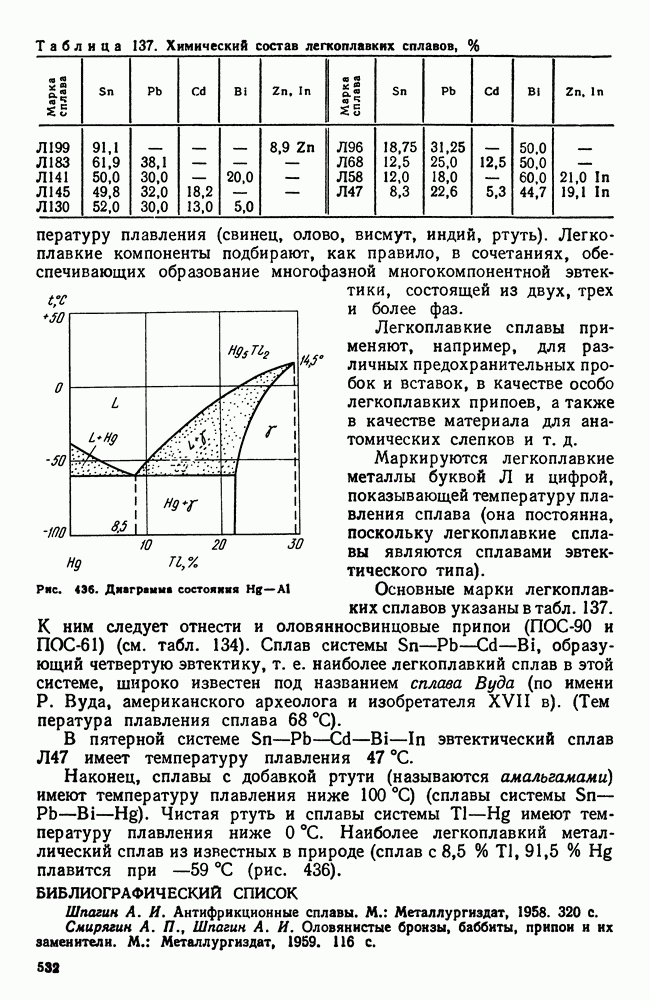
- 4. Легкоплавкие сплавы
- Глава XXIX. НЕКОТОРЫЕ СПЛАВЫ ЦВЕТНЫХ МЕТАЛЛОВ
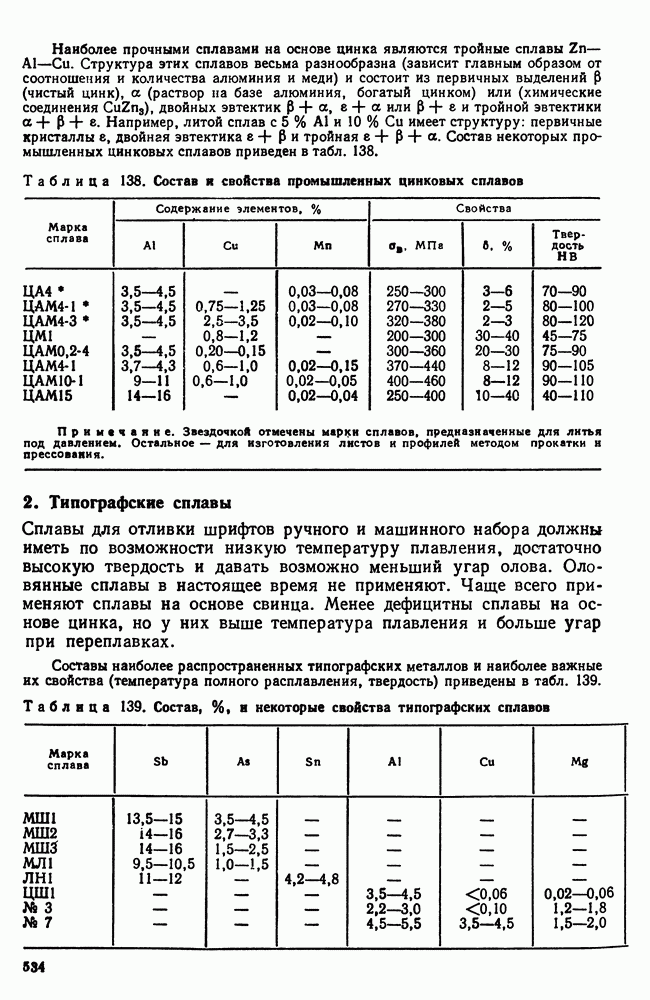
- 2. Типографские сплавы
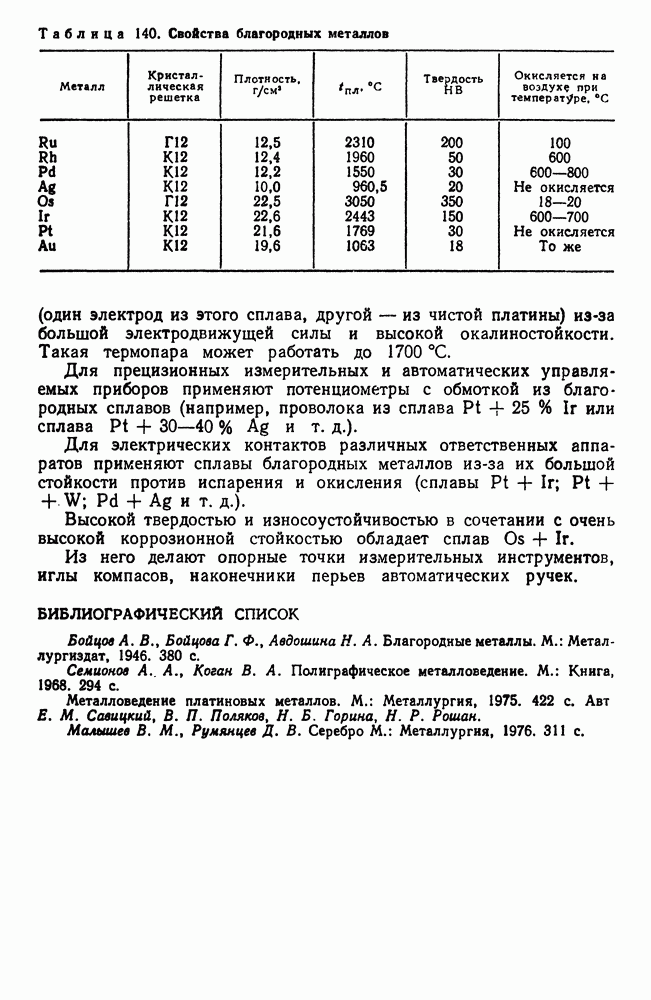
- 3. Благородные металлы