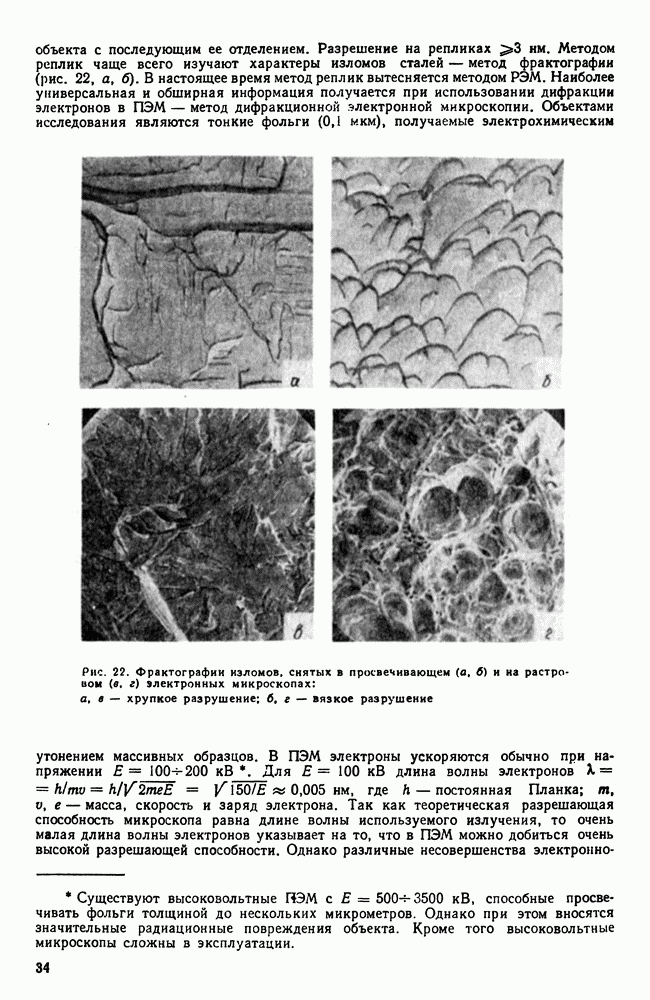
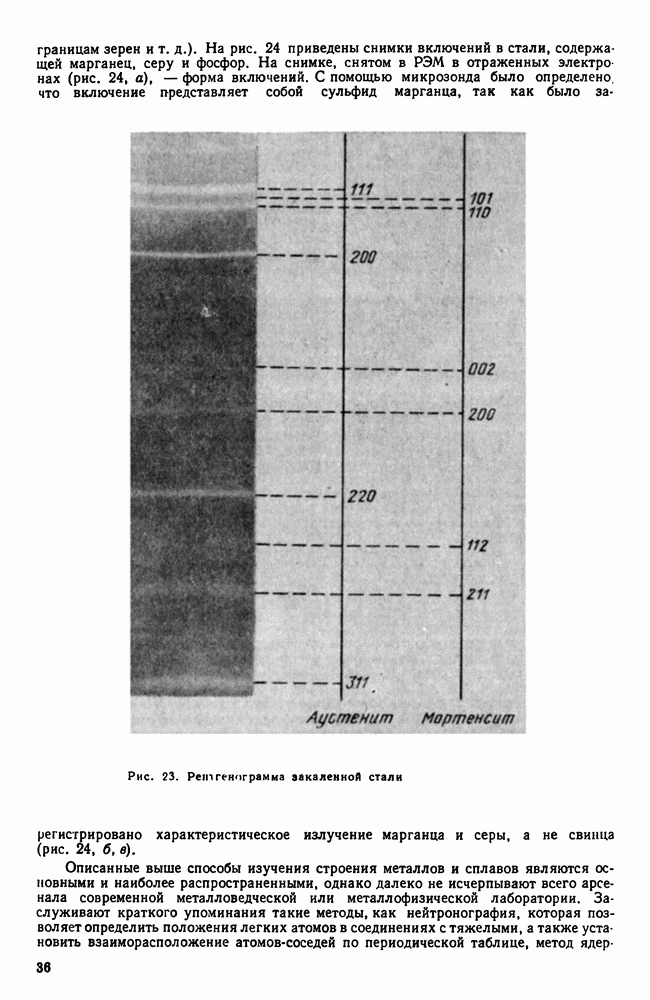
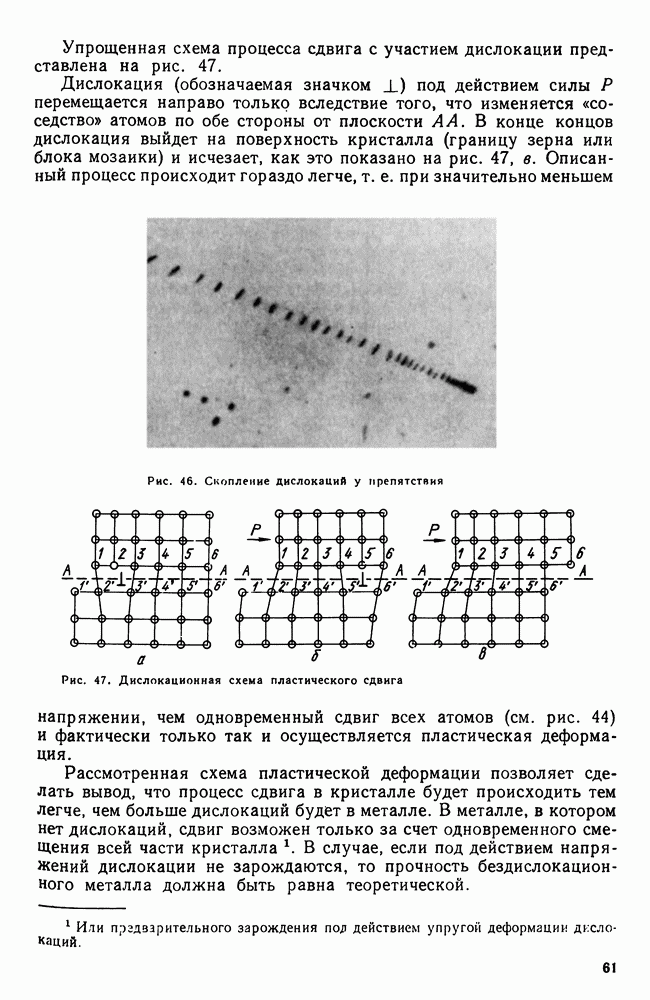
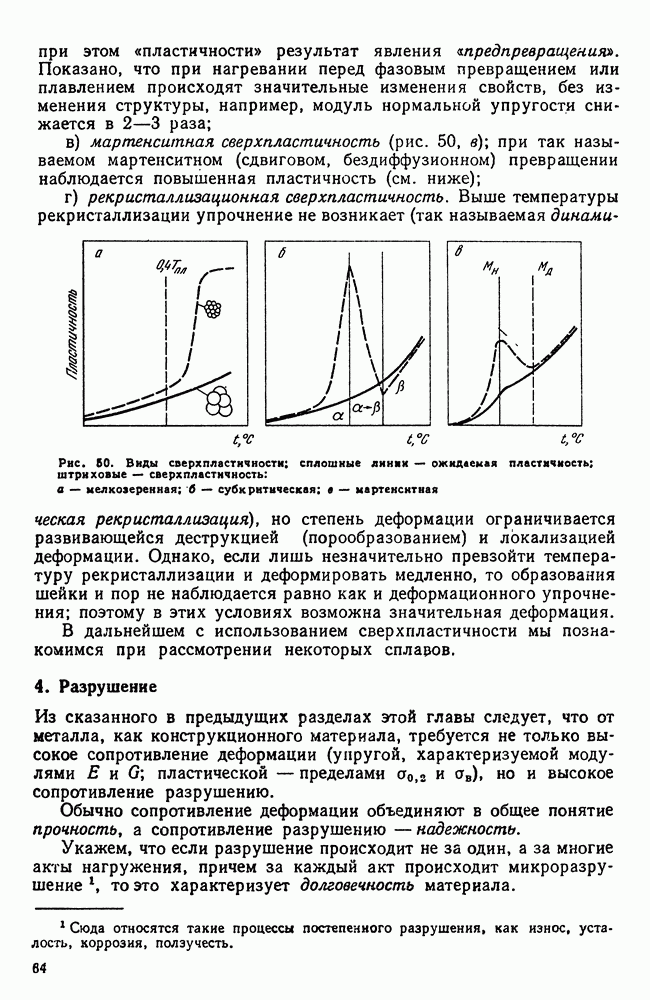
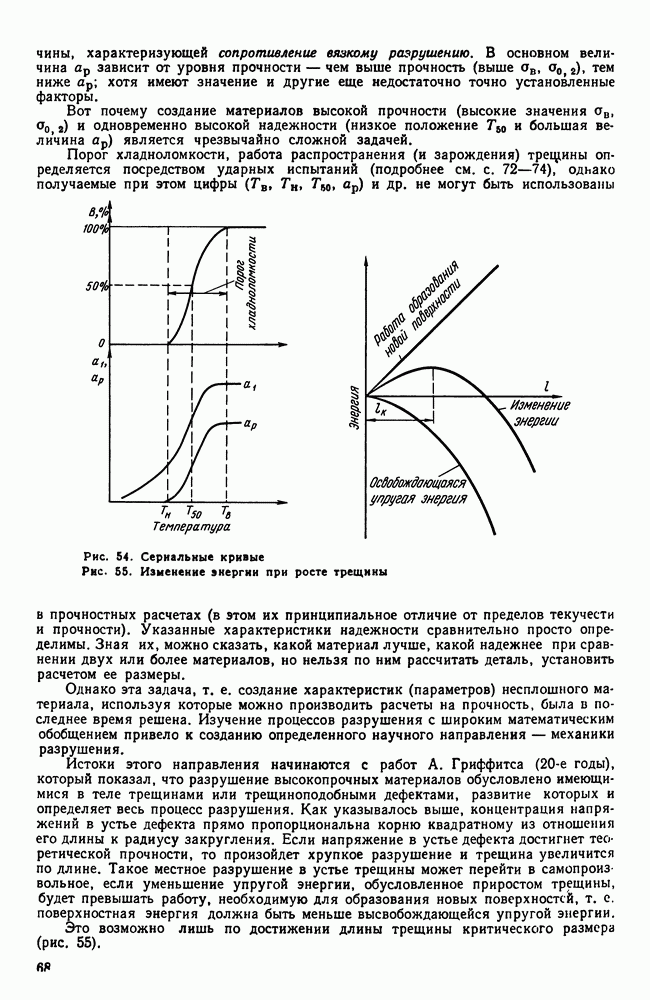
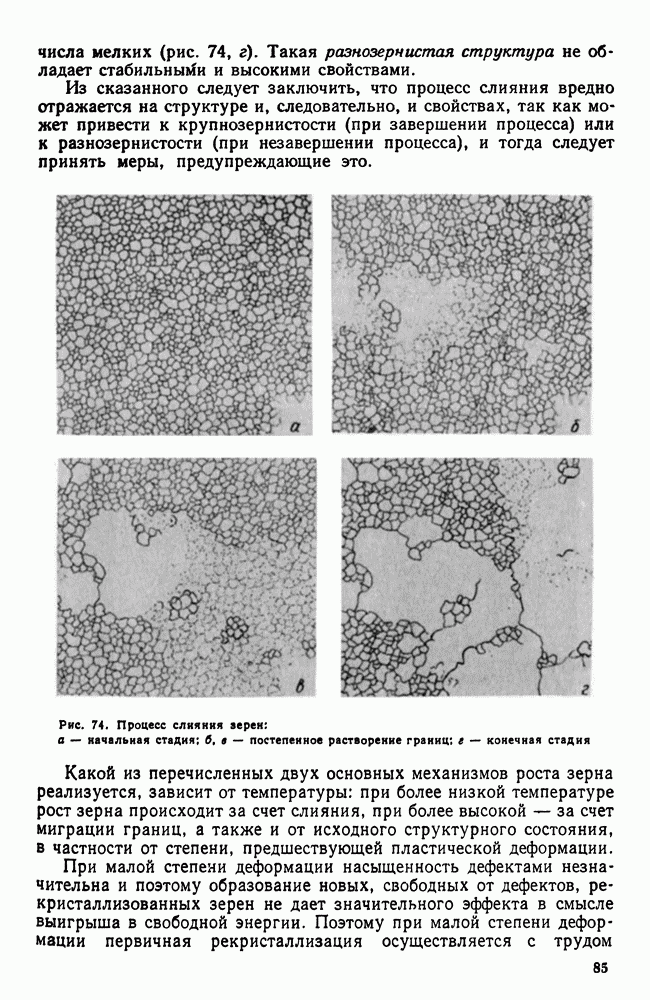
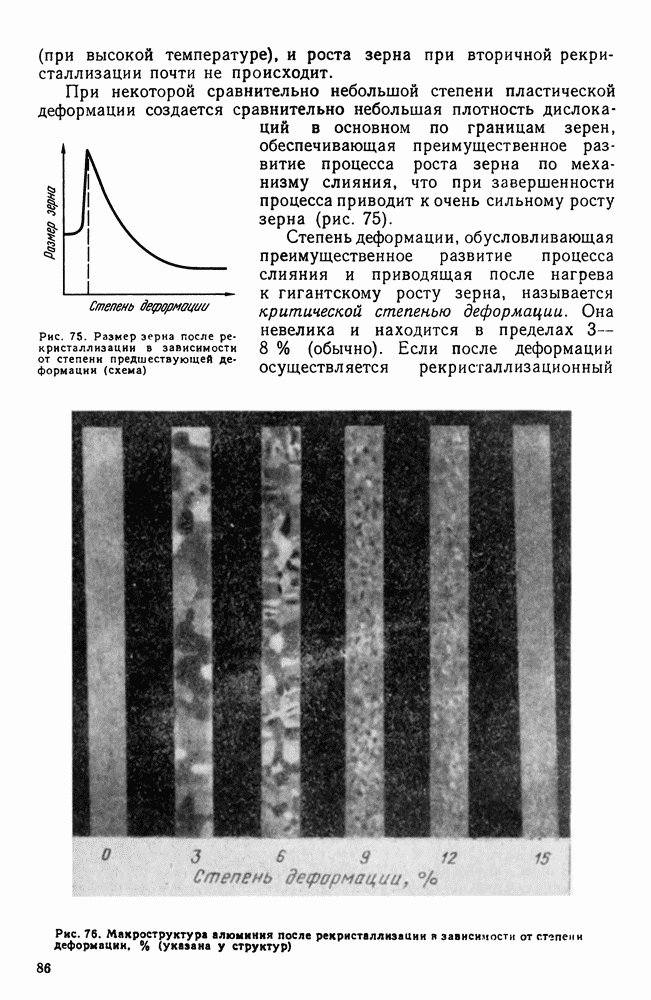
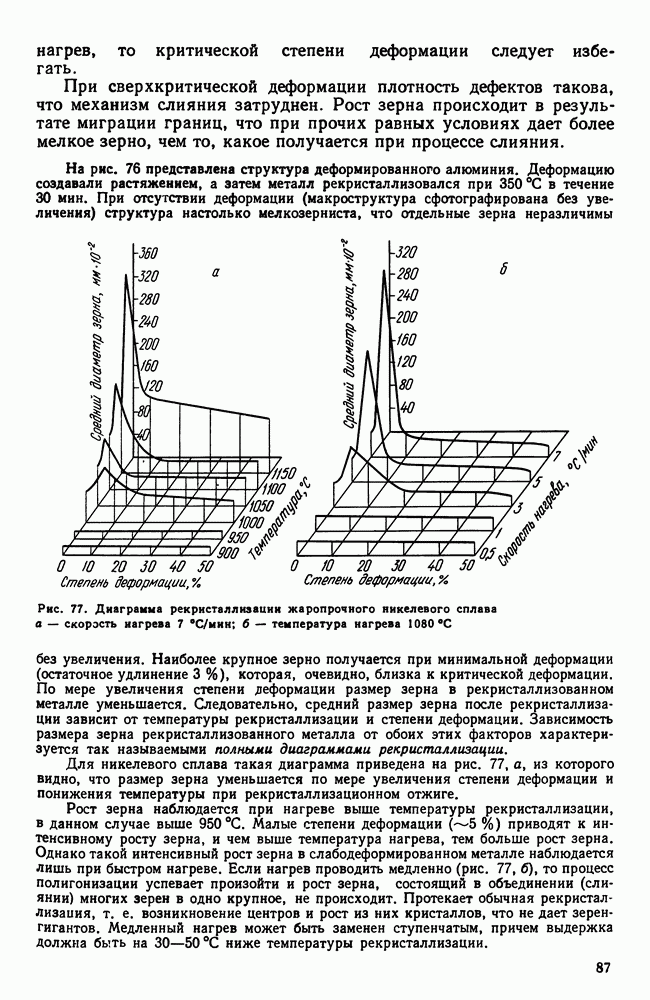
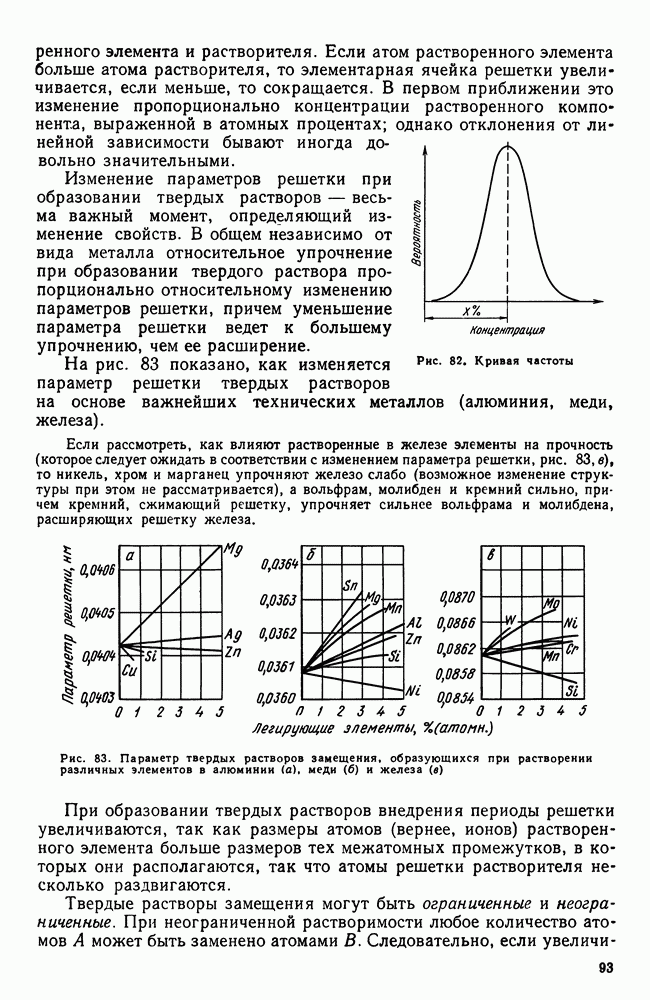
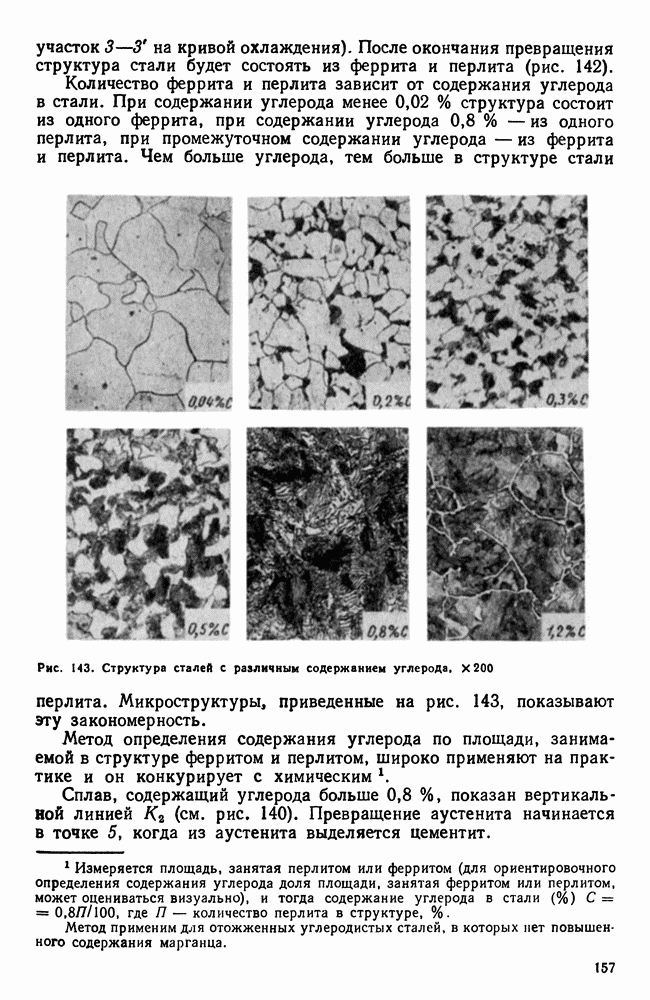
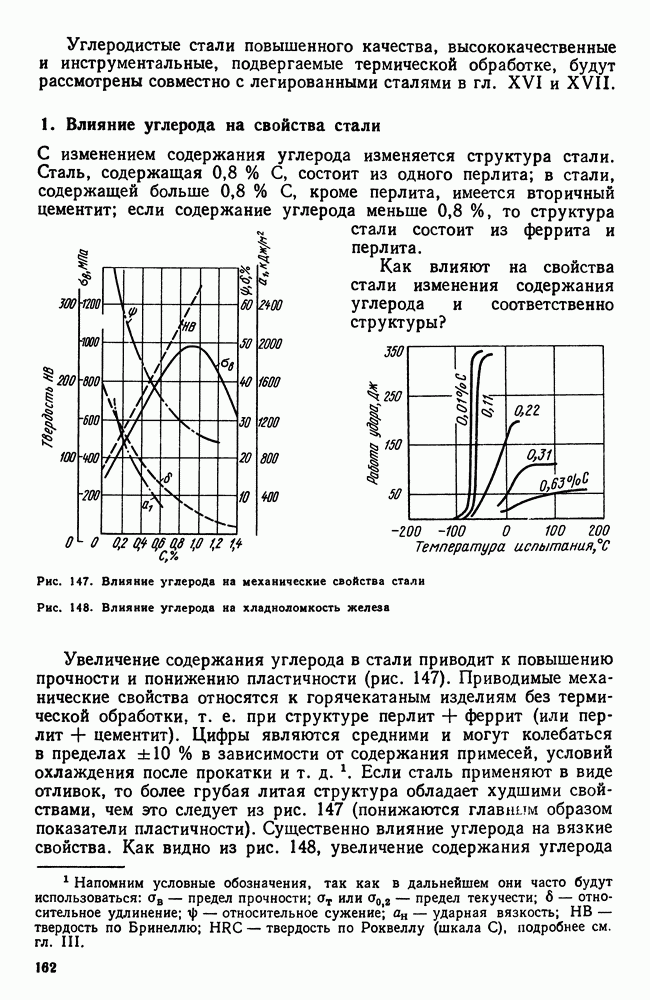
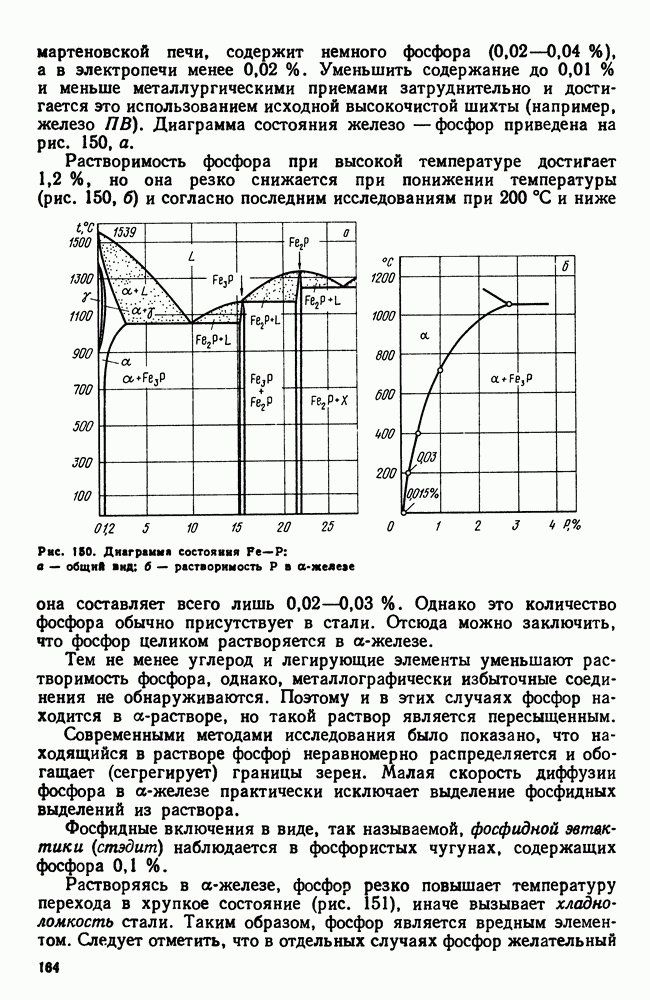
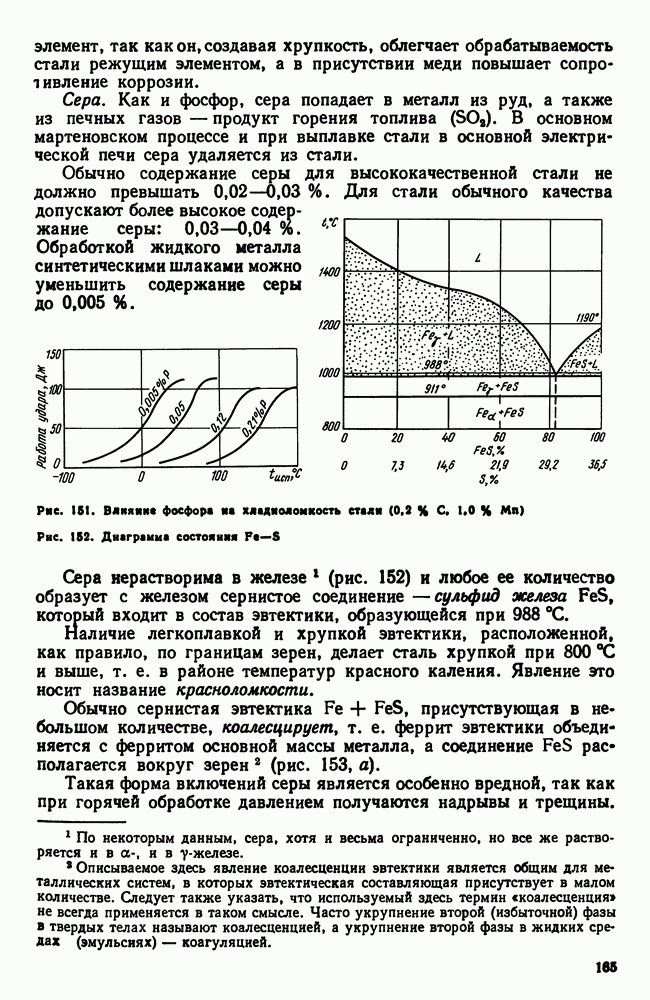
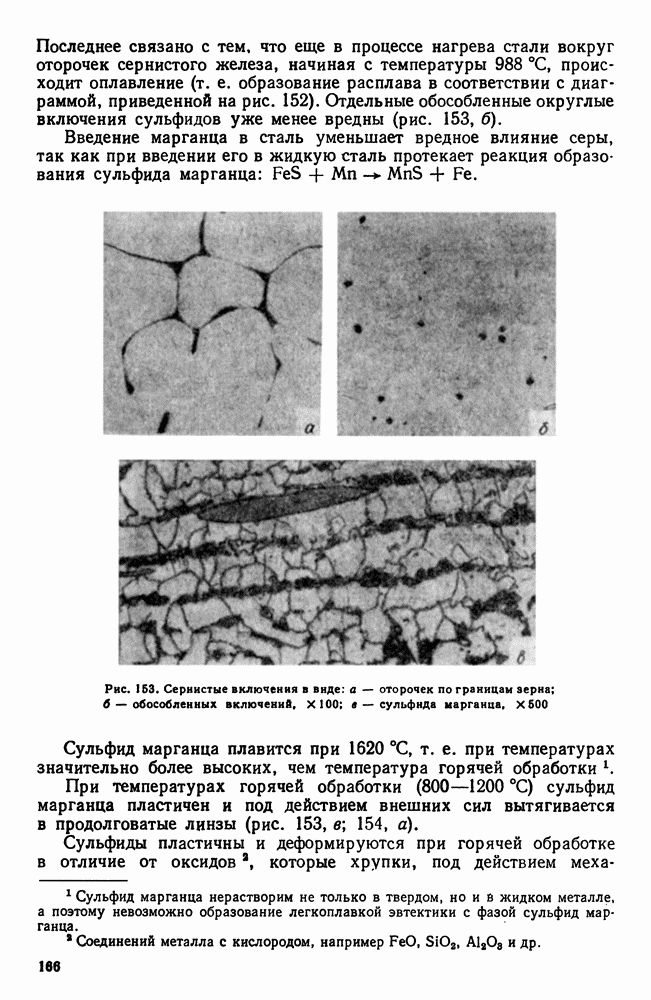
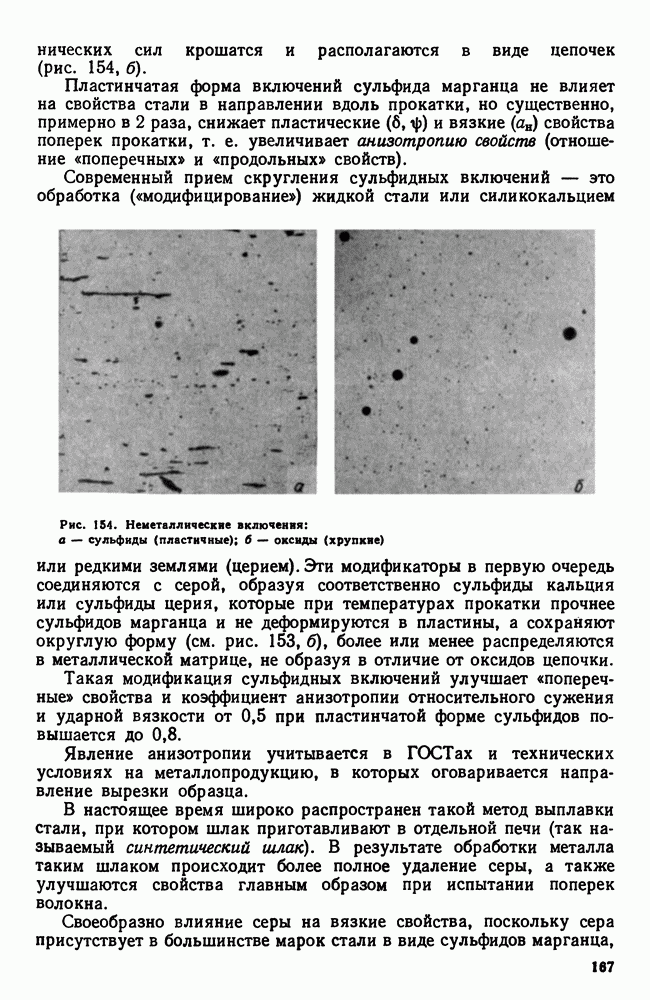
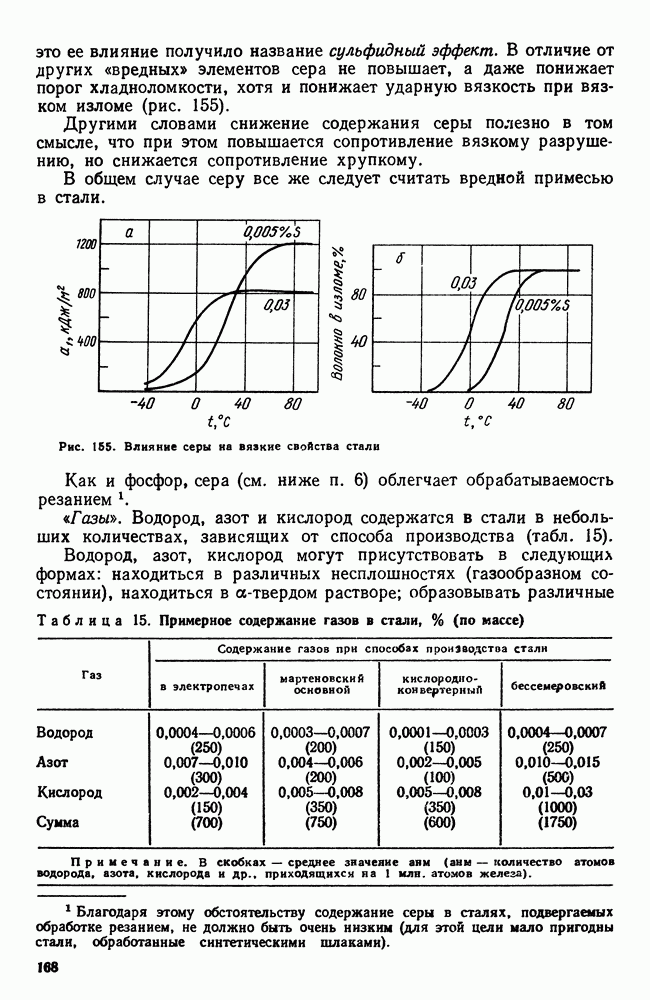
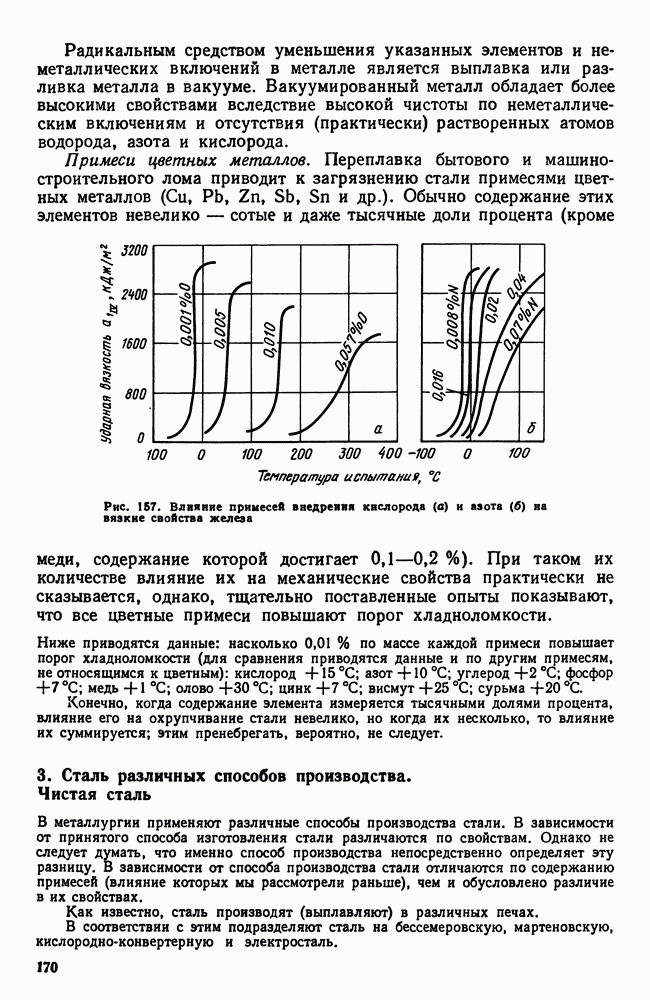
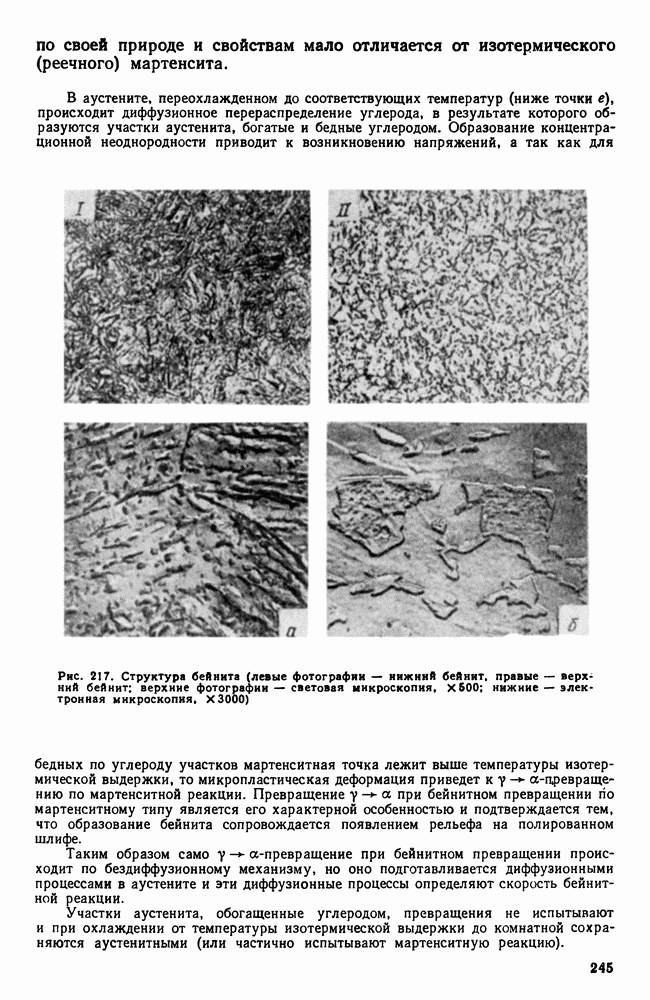
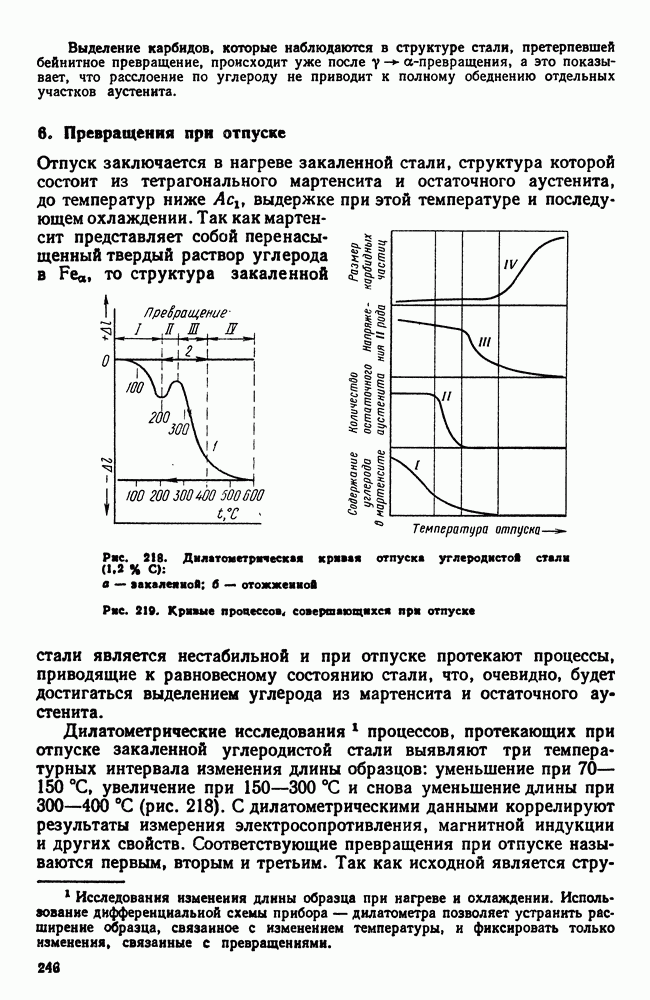
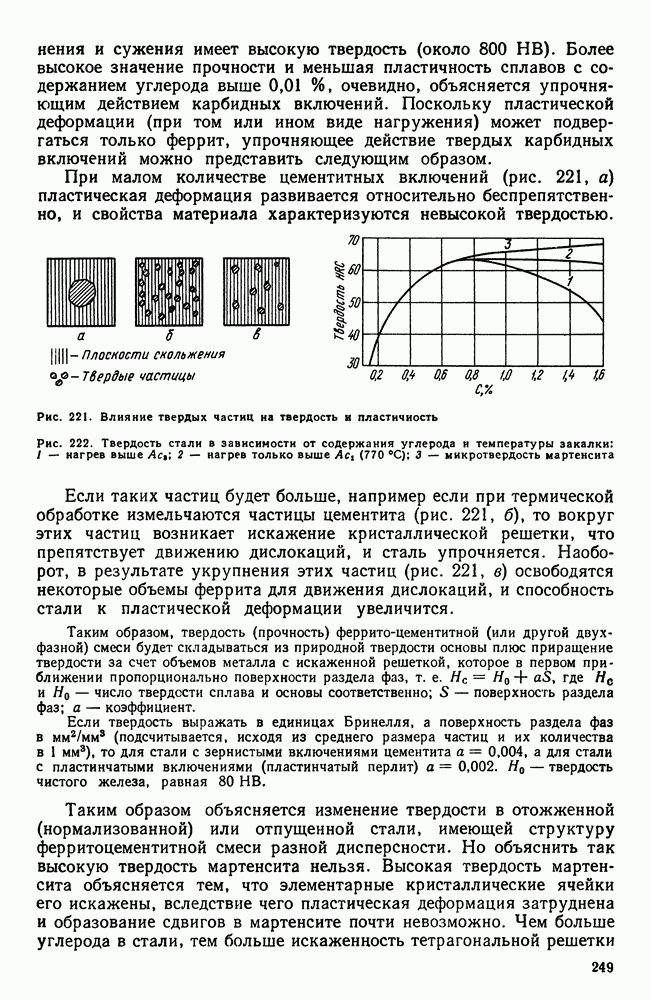
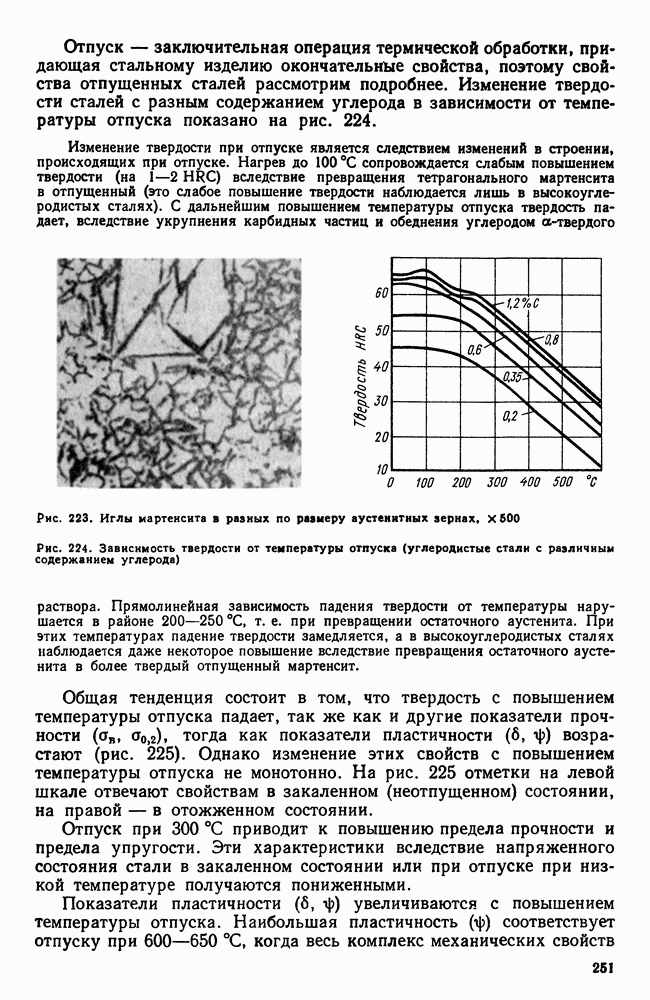
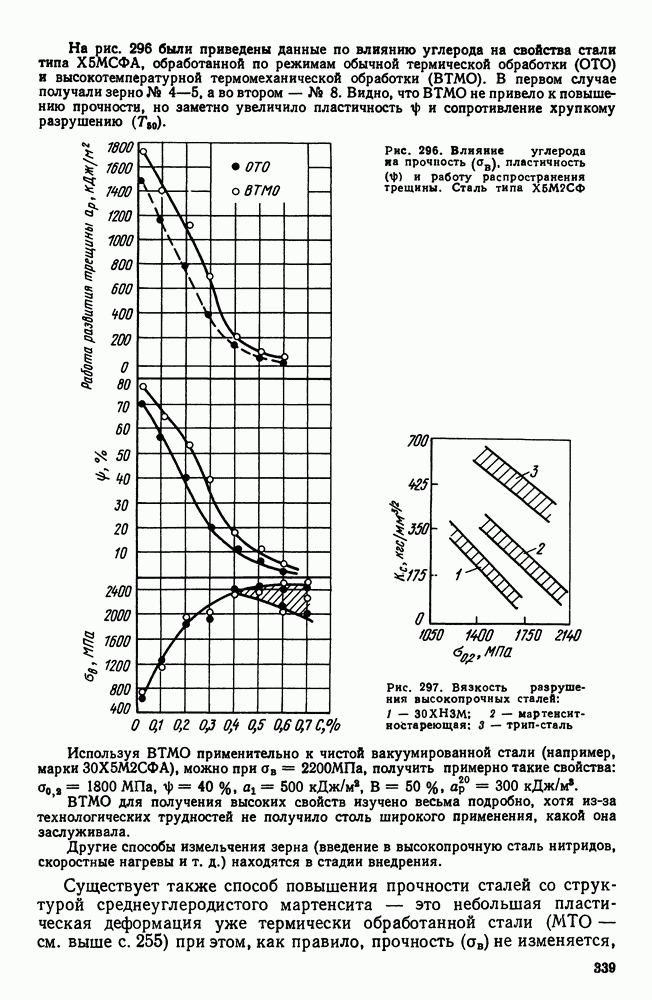
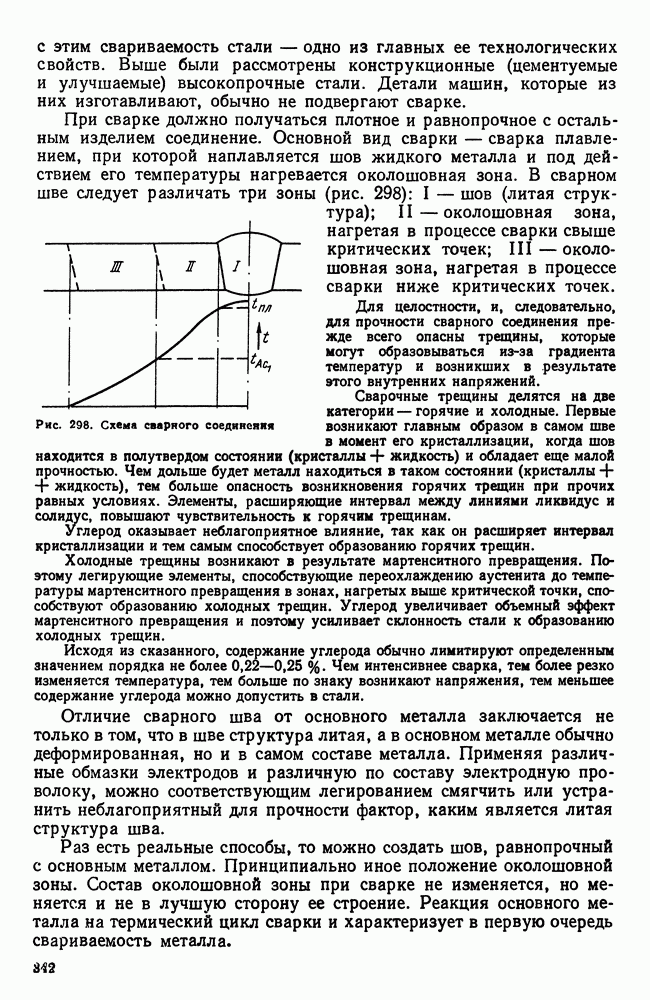
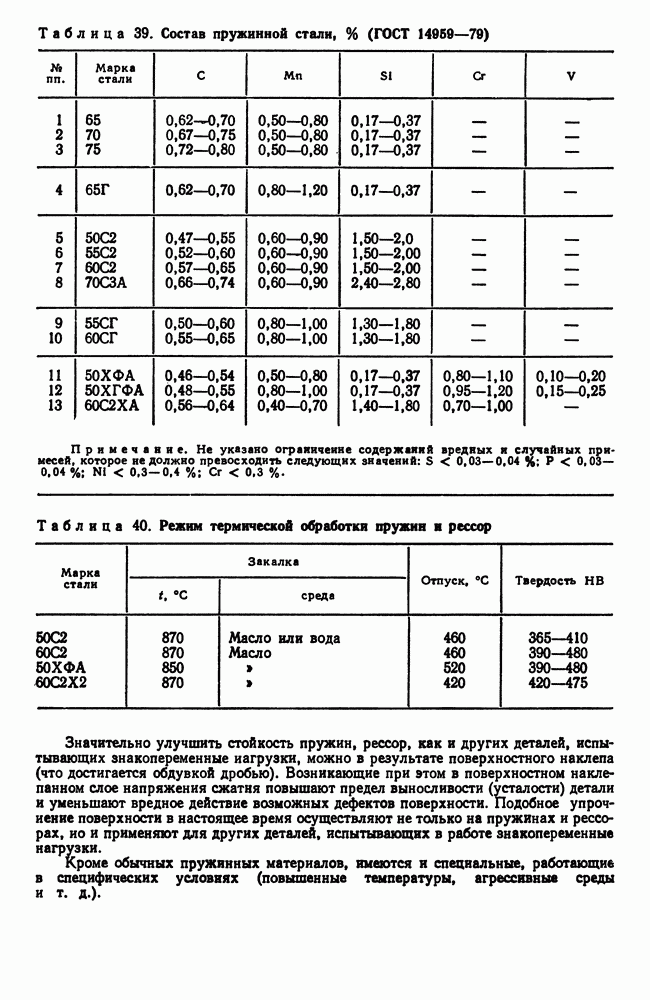
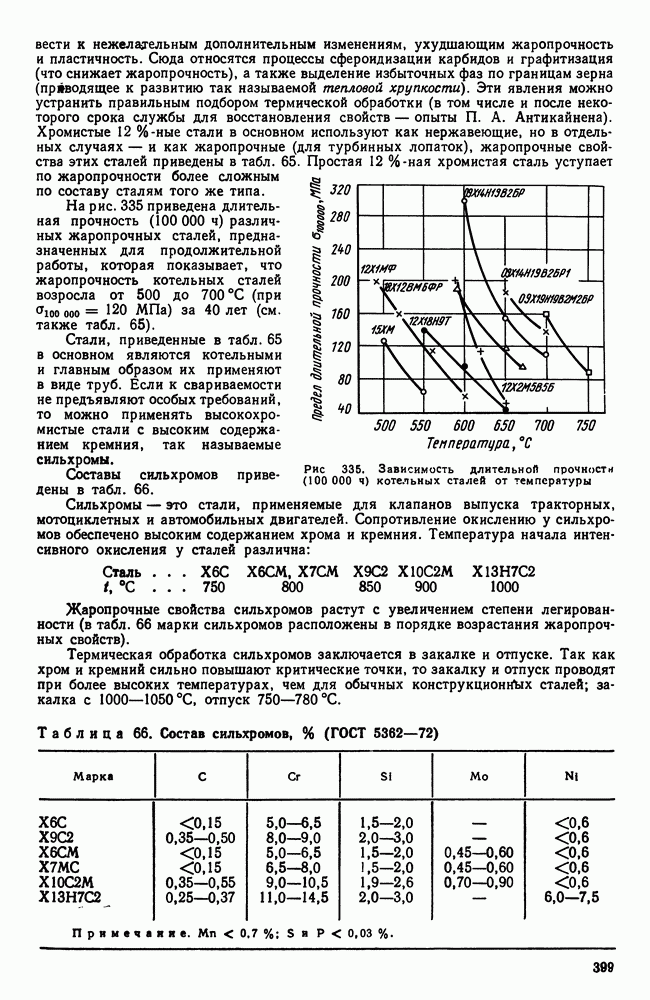
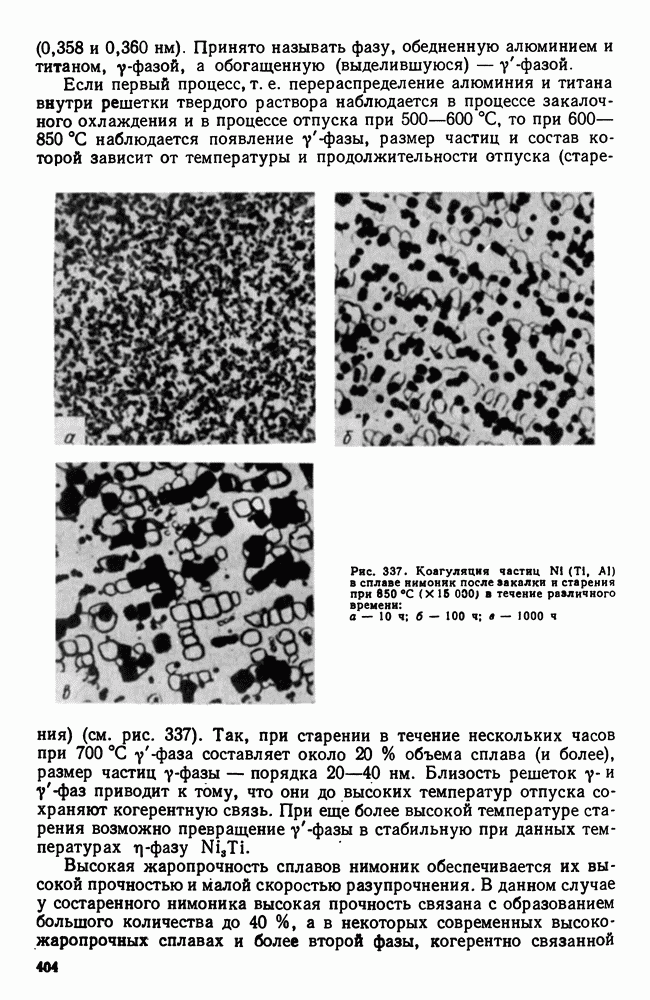
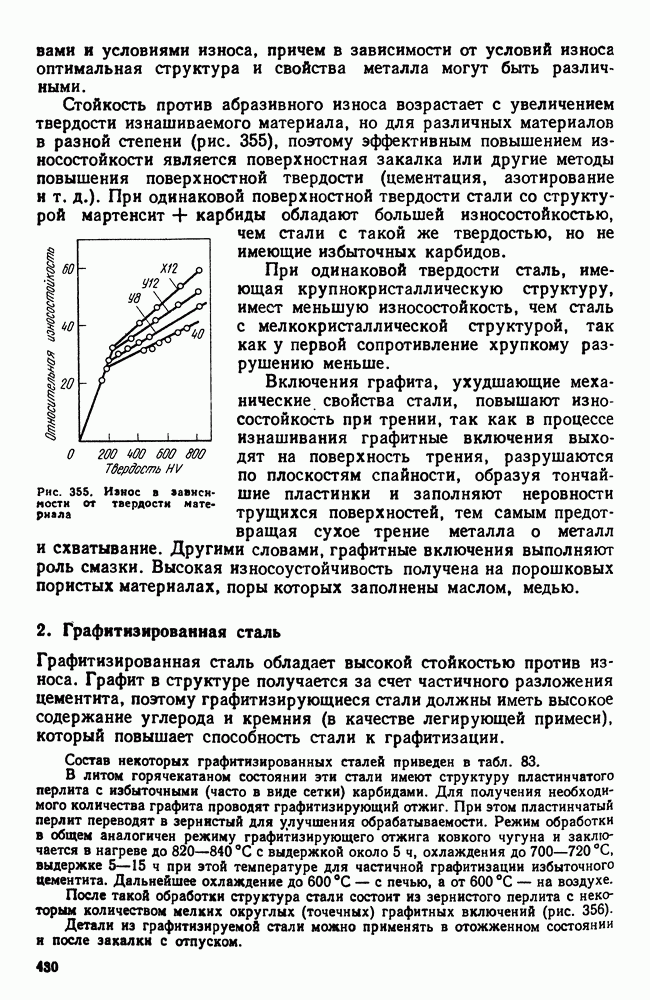
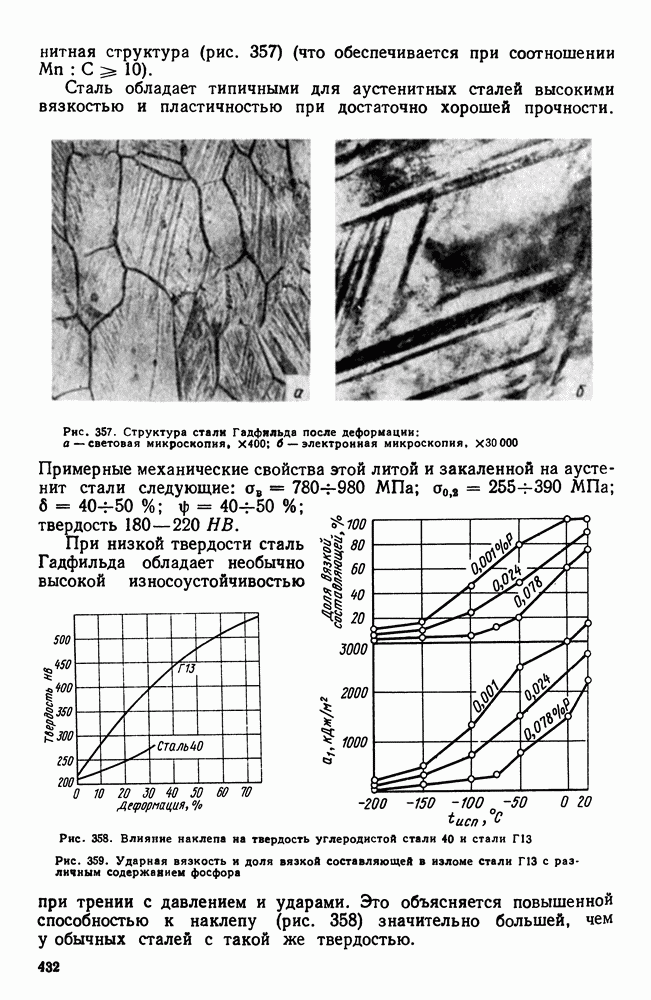
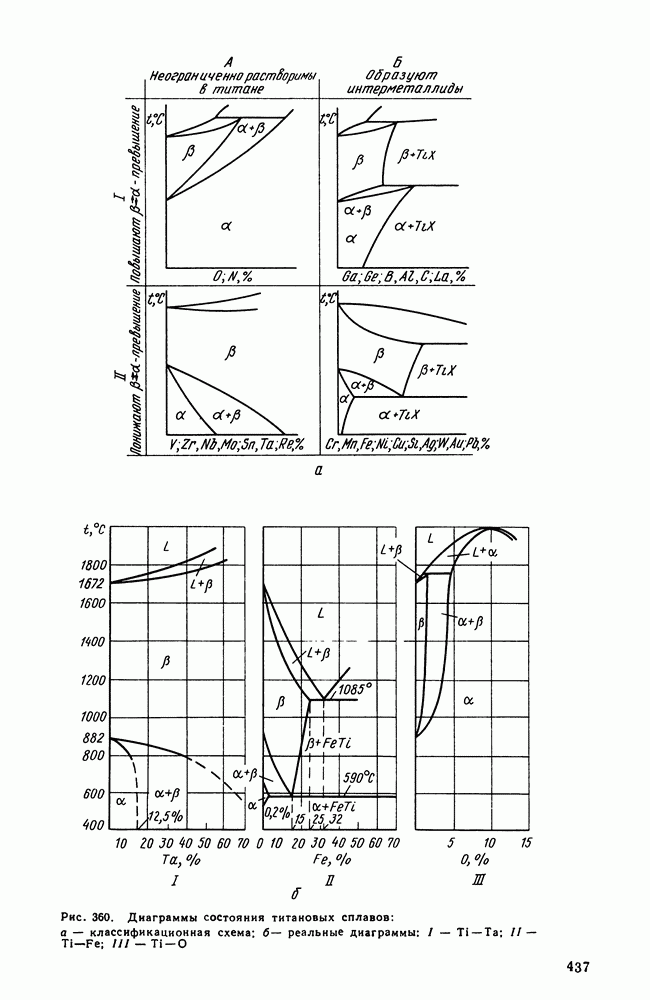
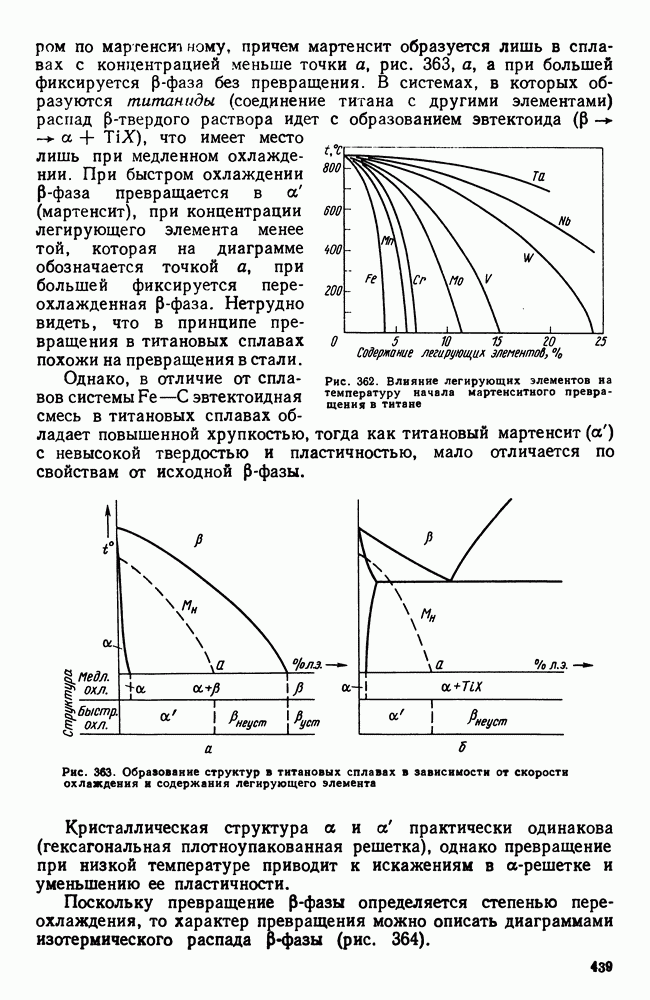
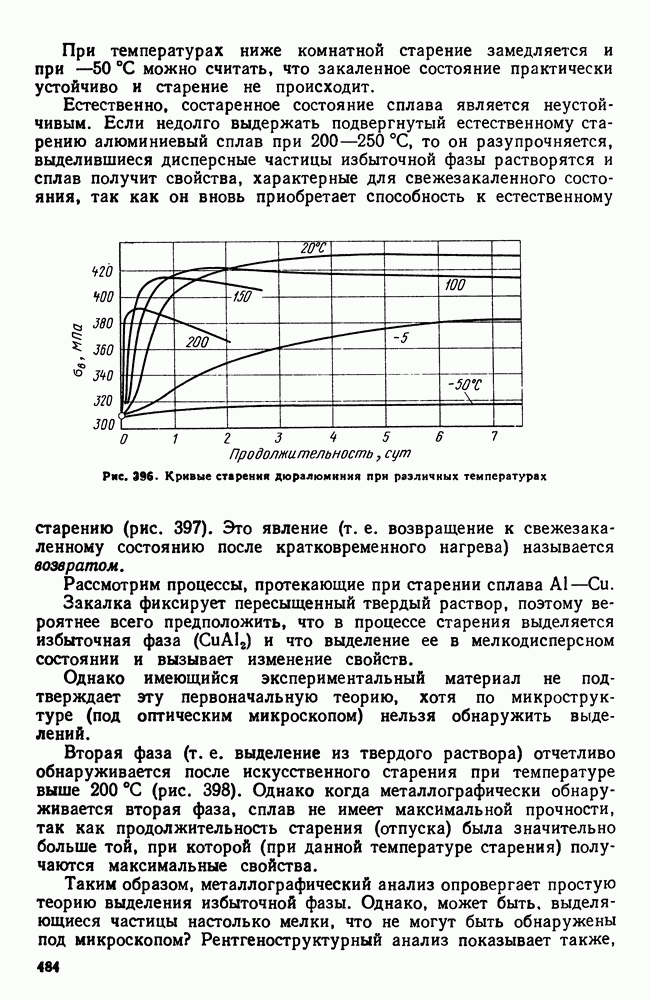
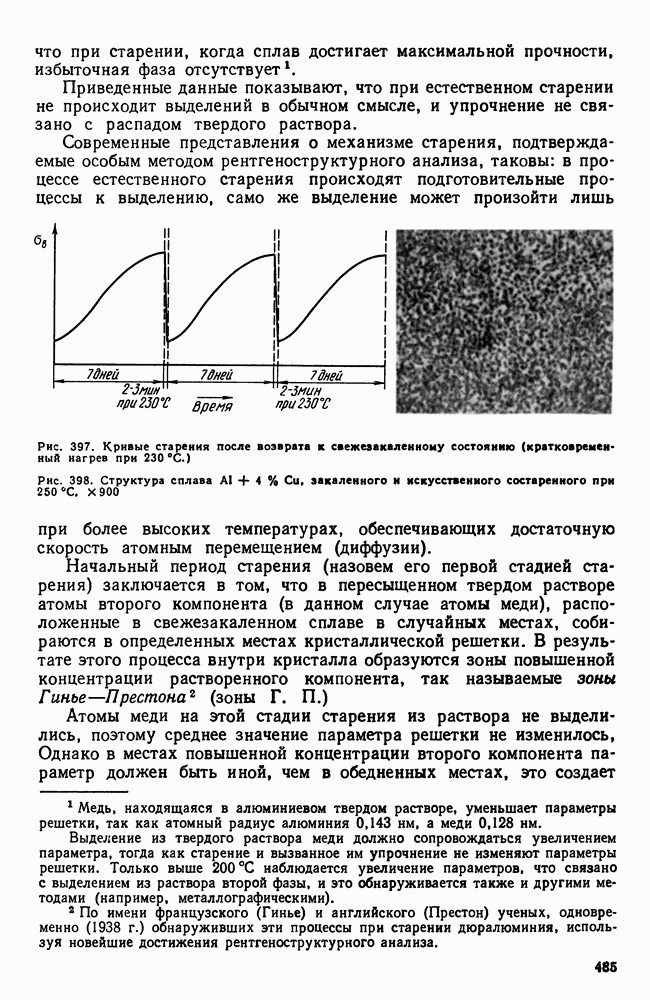
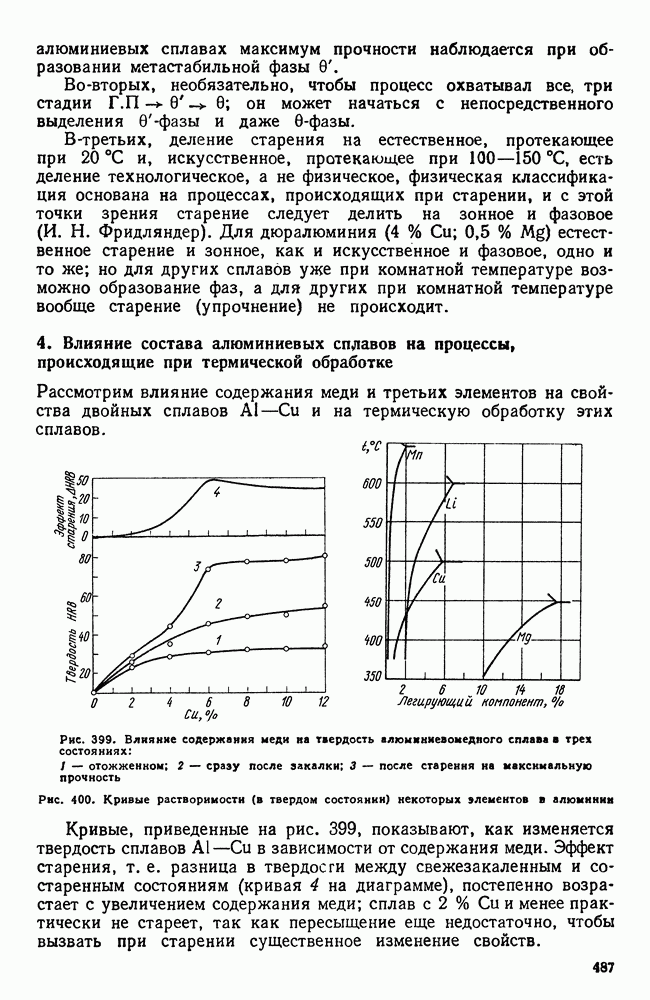
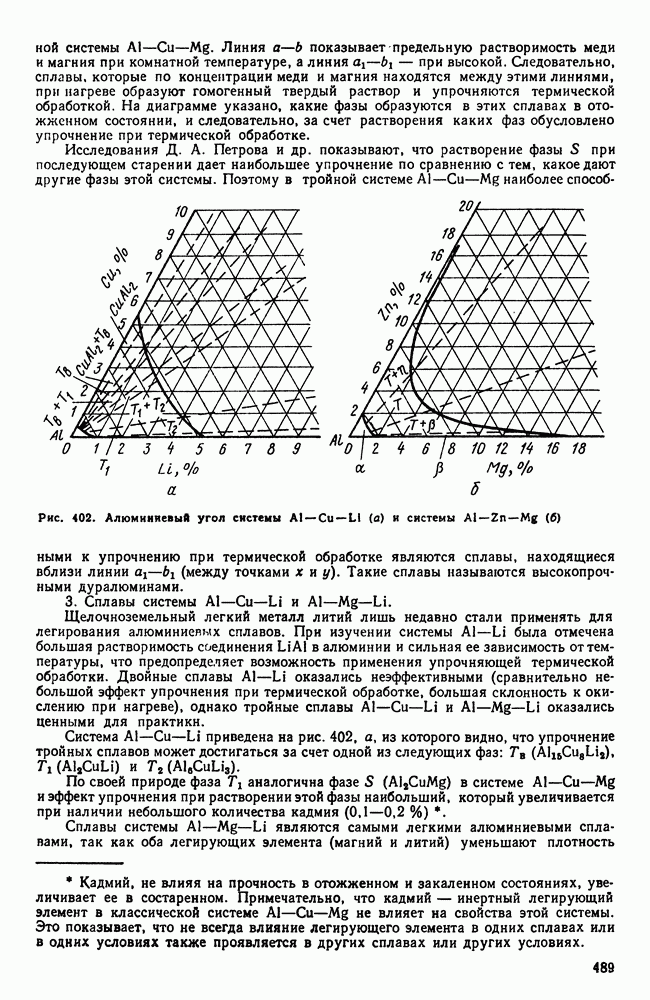
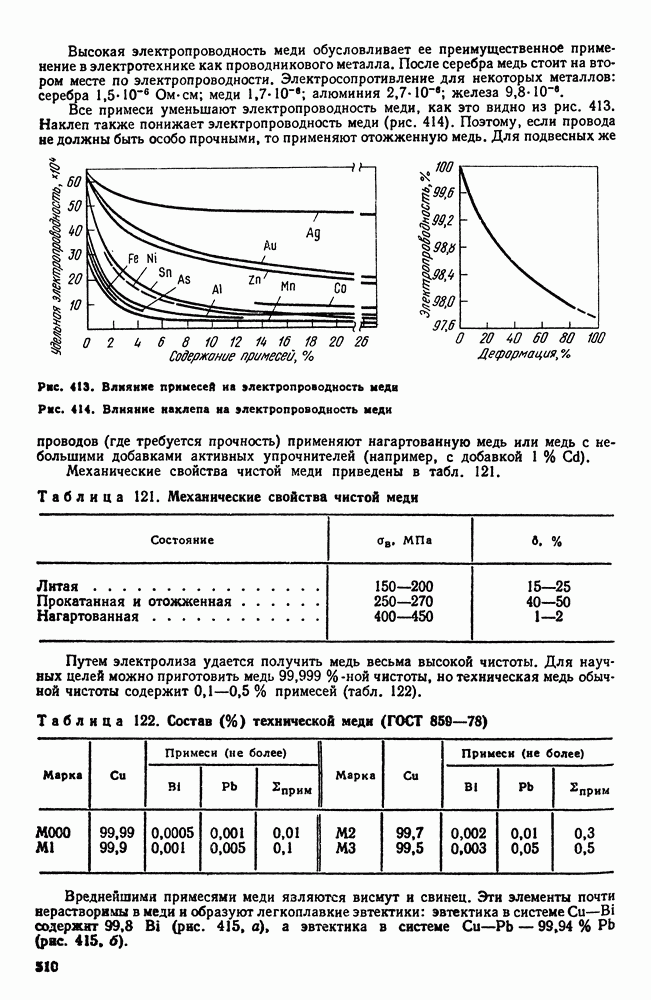
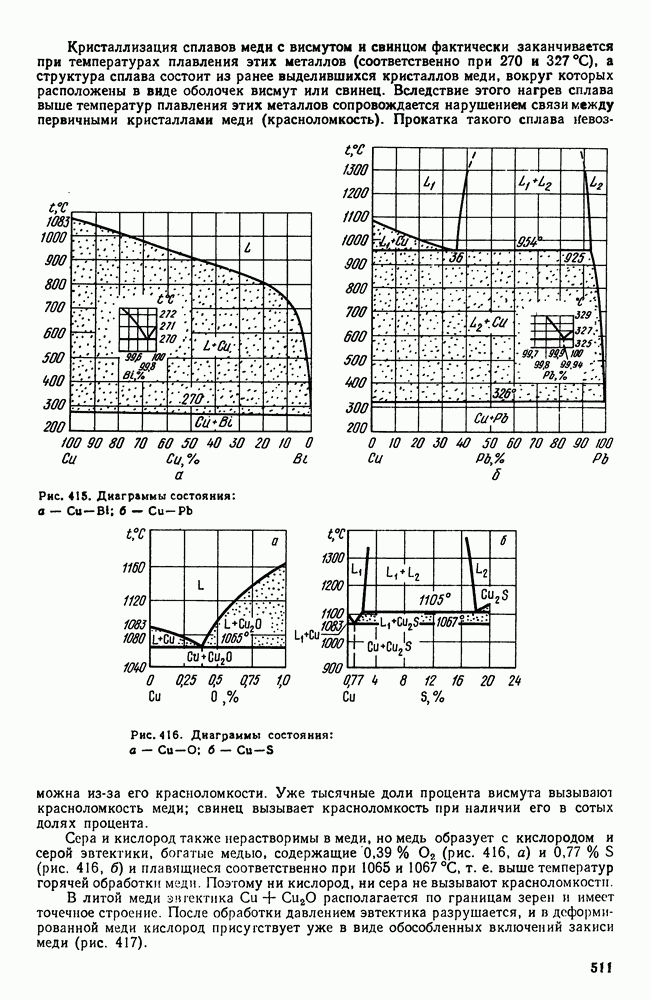
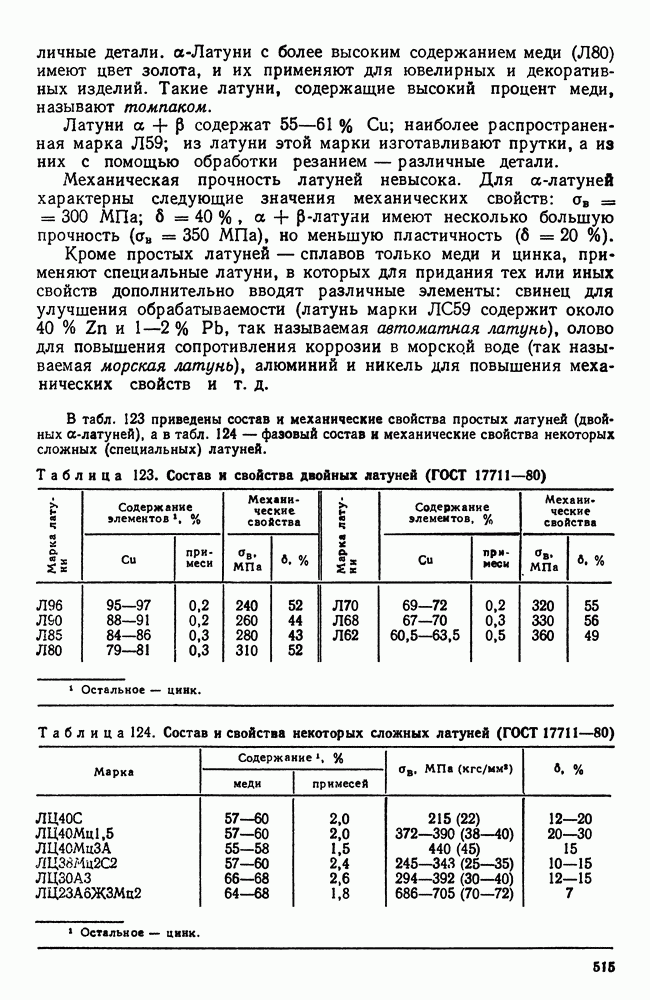
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
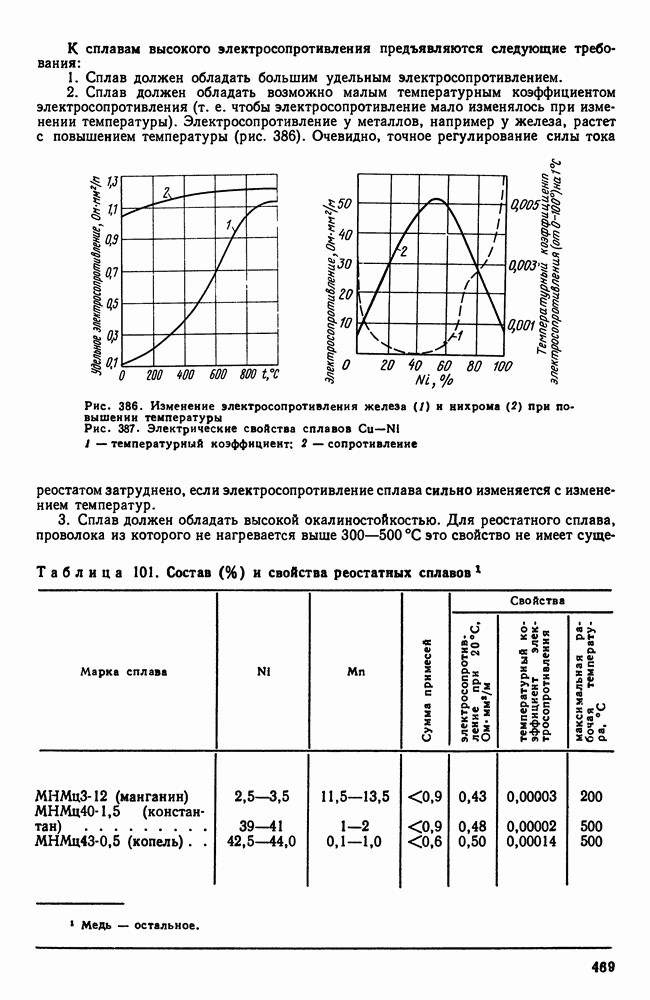
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
10. Кристаллизация сплавов в неравновесных условиях
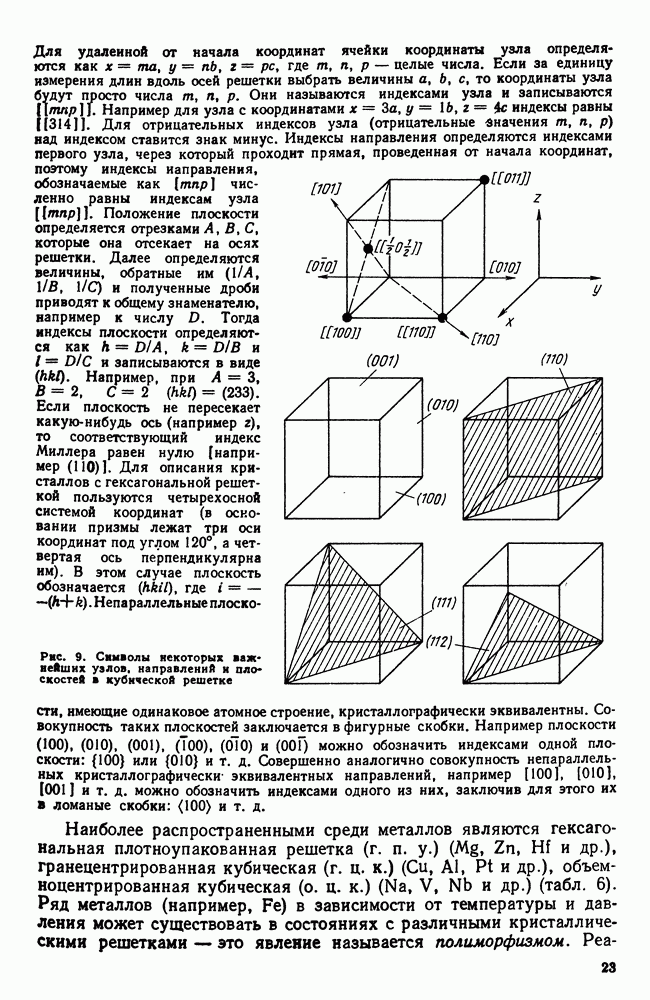
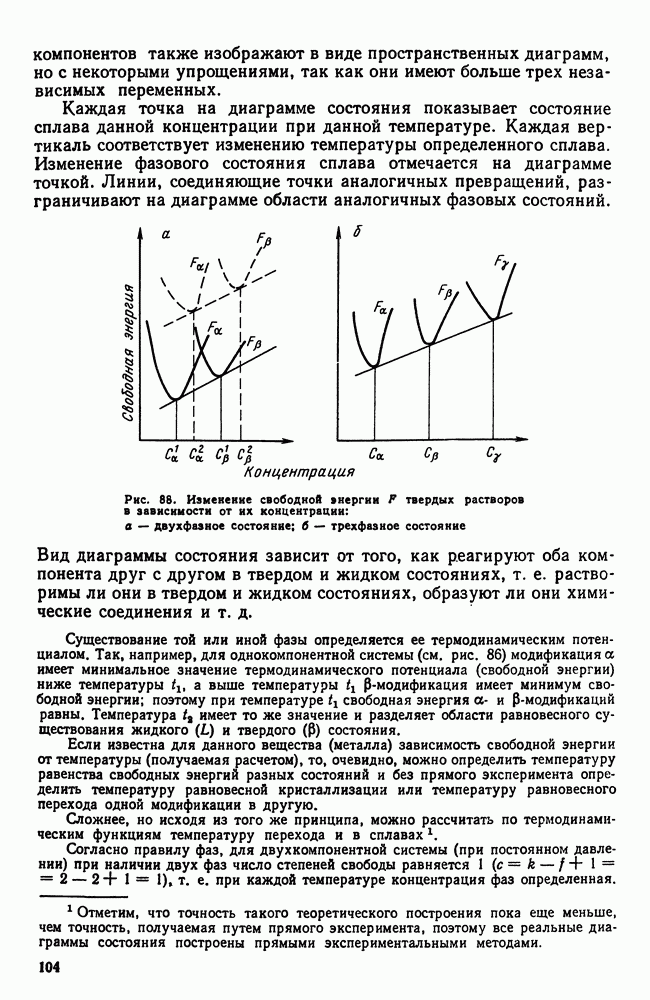
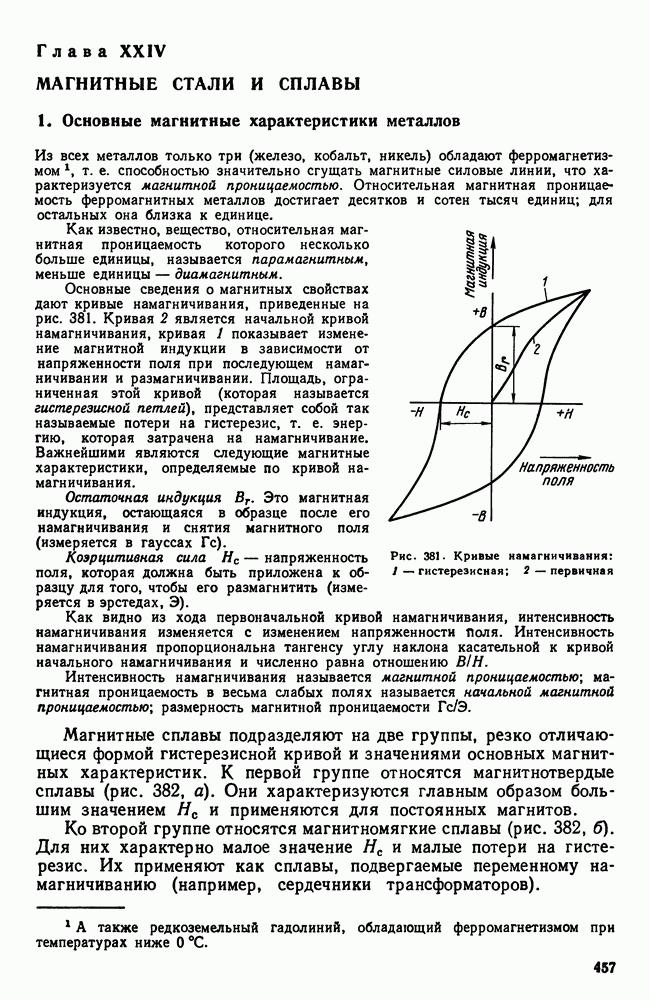
В начале этой главы говорилось, что диаграмма состояния характеризует равновесное состояние сплава, а линии на диаграмме показывают температурно-концентрационные условия превращения в в равновесных условиях, когда свободные энергии старой и образующихся фаз равны.
Вместе с тем отмечалось (см. также гл. II), что превращение при температуре фазового равновесия невозможно, так как в этом случае нет стимула для превращения, нет выигрыша в запасе свободной энергии. Поэтому равновесную диаграмму состояния следует рассматривать как тот предельный случай, когда при бесконечно малых скоростях нагрева или охлаждения достигается бесконечно малая разность уровней свободных энергий сосуществующих фаз и когда, следовательно, превращение совершается с бесконечно малой скоростью.

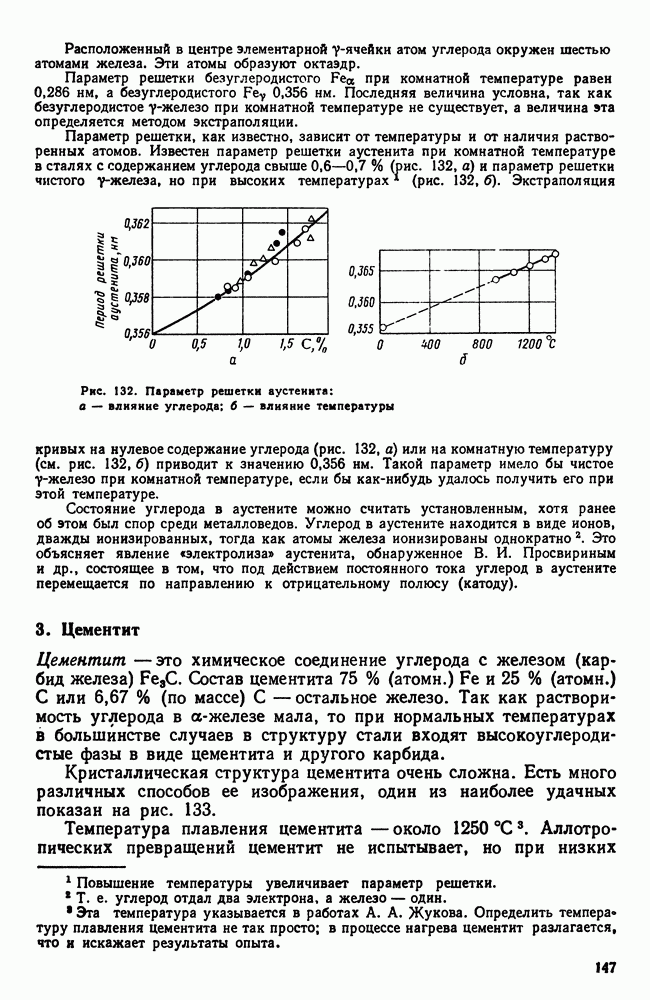
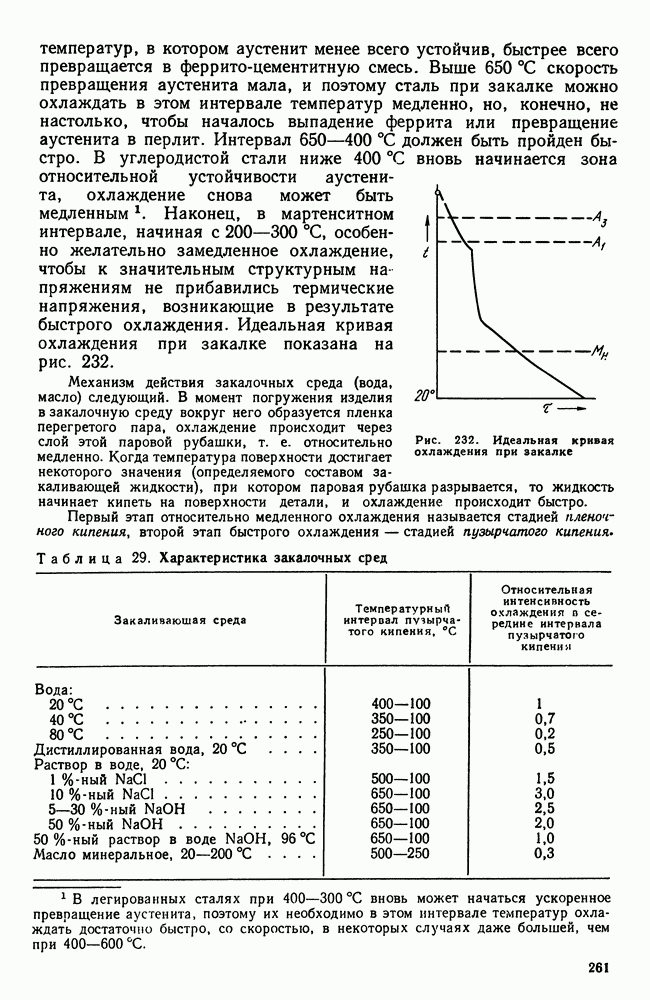
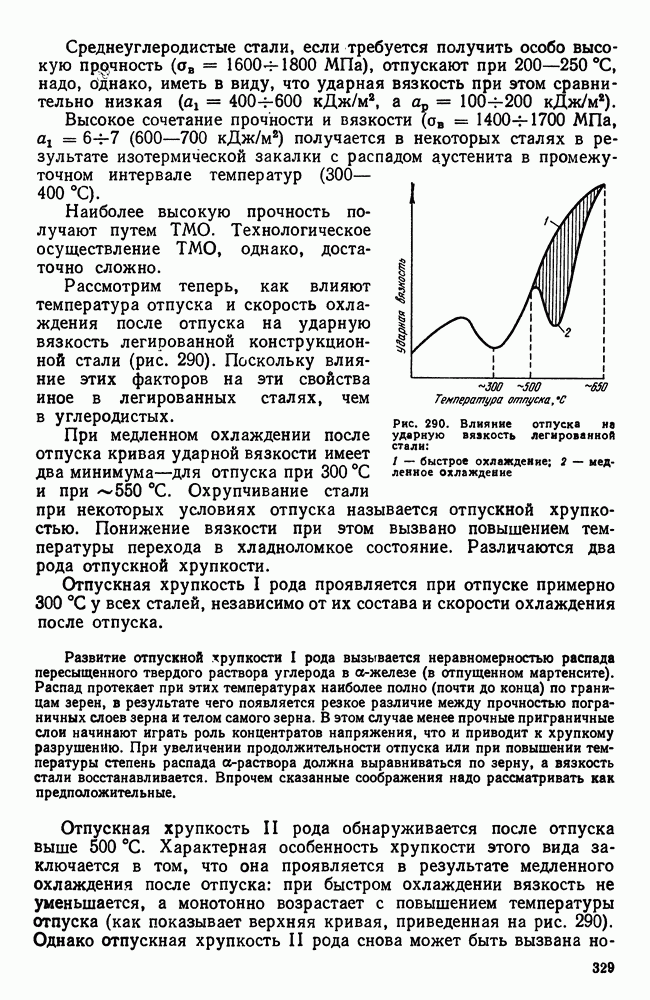
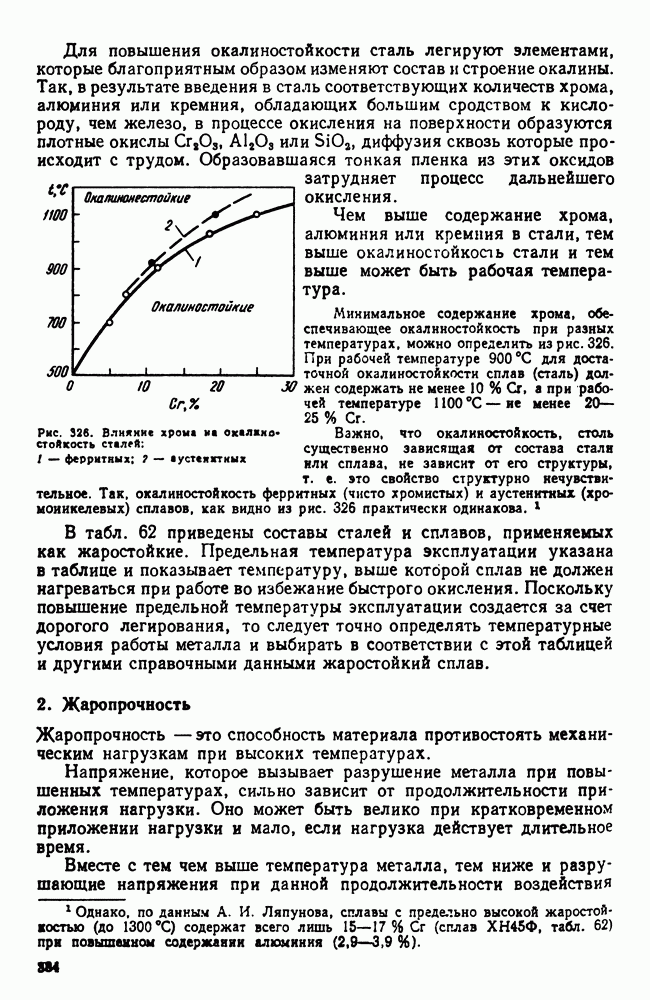
Рис. 106. Влияние скорости нагрева или охлаждения на температуры превращения: а — для систем с нулевой степенью свободы; б — для систем с одной или более степенями свободы
Реально же обнаруживаемые температуры превращения при нагреве, который производится с какой-то конечной скоростью, лежат всегда выше равновесных, а для случая охлаждения всегда ниже, что и показано схематически на рис. 106.
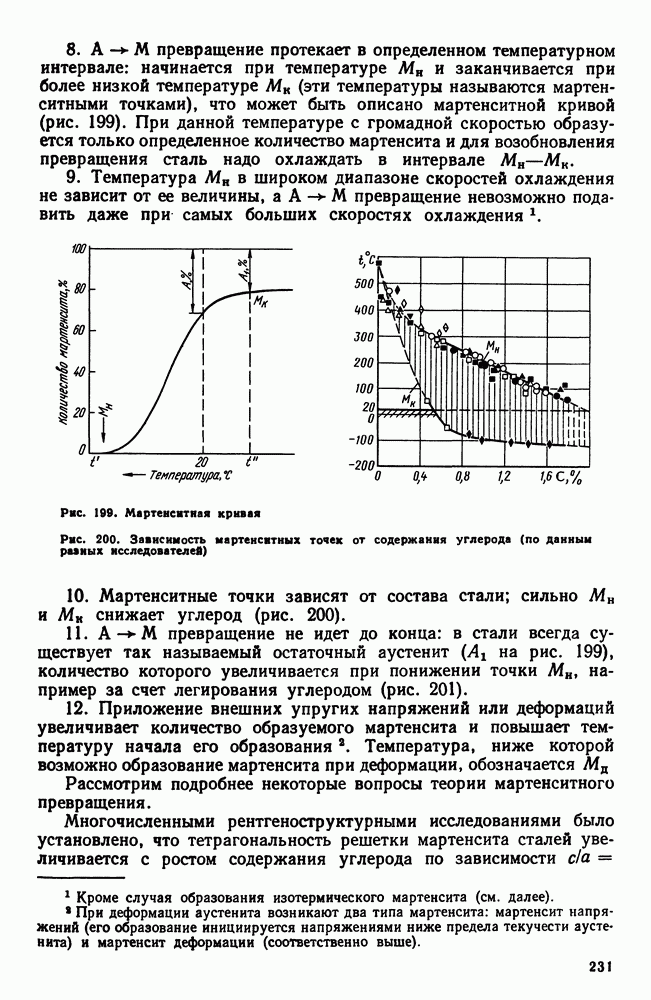
На этой схеме полиморфному превращению  при бесконечно малой скорости охлаждения (или нагревания) отвечают теоретические температуры равновесия:
при бесконечно малой скорости охлаждения (или нагревания) отвечают теоретические температуры равновесия:  — для нонвариантных систем (например, полиморфное превращение в чистых металлах) или интервал
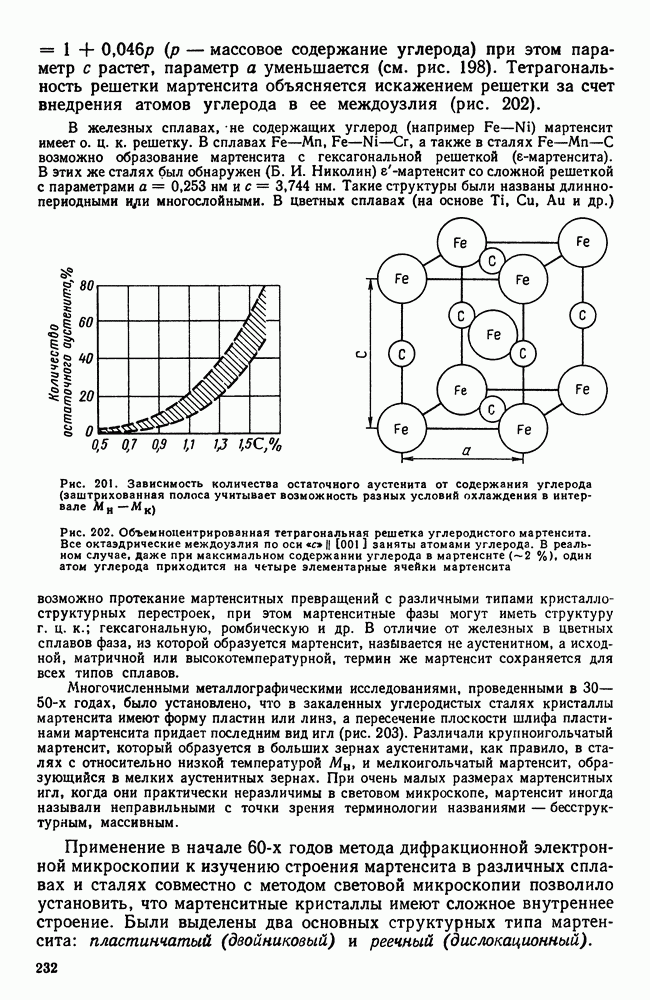
— для нонвариантных систем (например, полиморфное превращение в чистых металлах) или интервал  для систем с одной или более степенями свободы (например, превращение твердых растворов). В условиях же конечных скоростей нагрева или охлаждения начинается и заканчивается выше или ниже равновесных температур. Кроме того, здесь отражено еще два других существенылх обстоятельства:
для систем с одной или более степенями свободы (например, превращение твердых растворов). В условиях же конечных скоростей нагрева или охлаждения начинается и заканчивается выше или ниже равновесных температур. Кроме того, здесь отражено еще два других существенылх обстоятельства:
1. Перегрев или переохлаждение системы тем больше, чем больше скорость нагрева или скорость охлаждения, причем склонность к переохлаждению больше, чем к перегреву.
2. В реальных условиях превращение для всех систем протекает в интервале температур. Этот интервал тем больше, чем больше скорость нагрева или охлаждения.
Таким образом, описываемые диаграммой состояния превращения представляют собой некоторую абстракцию, поскольку необходимость переохлаждения (перегрева) для протекания превращения в ней не учитывается. Но эта абстракция необходима для изучения реальных условий кристаллизации.
Еслис корость изменения температур невелика, т. е. если превращения проходят в условиях малых переохлаждений (перенагрев же обычно бывает невелик), то в этих случаях можно пренебречь этой небольшой степенью переохлаждения и рассматривать превращения как совершающиеся при температурах и в последовательности, указанной на диаграмме состояния.
В дальнейшем будем широко пользоваться диаграммами состояний при анализе так называемых равновесных структур и превращений, совершающихся при медленных охлаждениях (нагревах).
В условиях же быстрых изменений температур изменяется не только температура превращения, но и условия превращения, так как не успевают (для переохлажденных систем) произойти диффузионные процессы, необходимые для осуществления превращений по типу равновесных. Для этих случаев равновесия диаграмма уже недействительна.
Непрерывная кристаллизация жидкого раствора
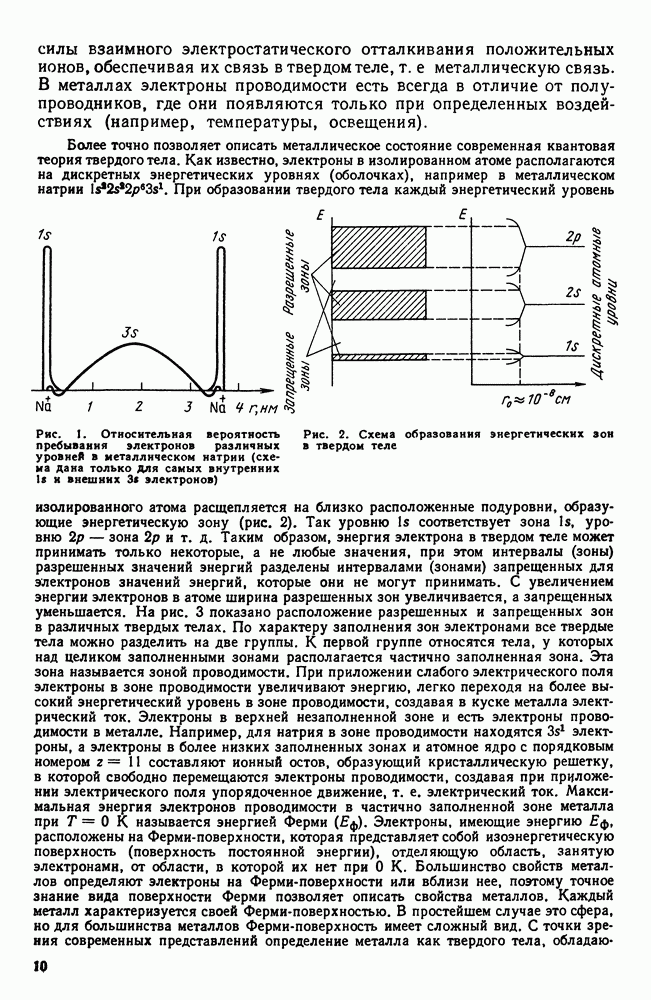
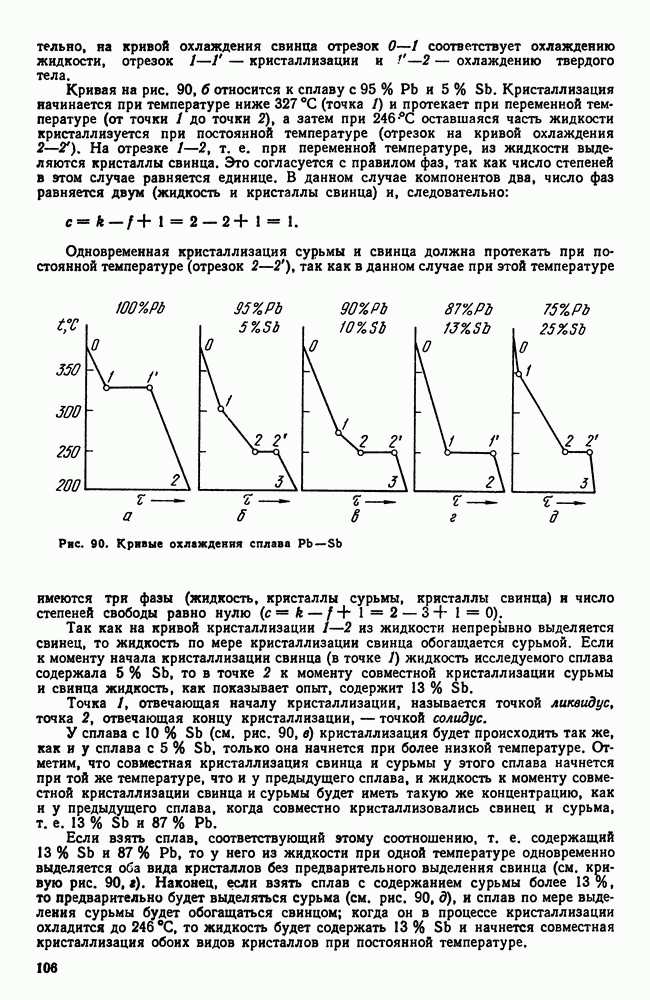
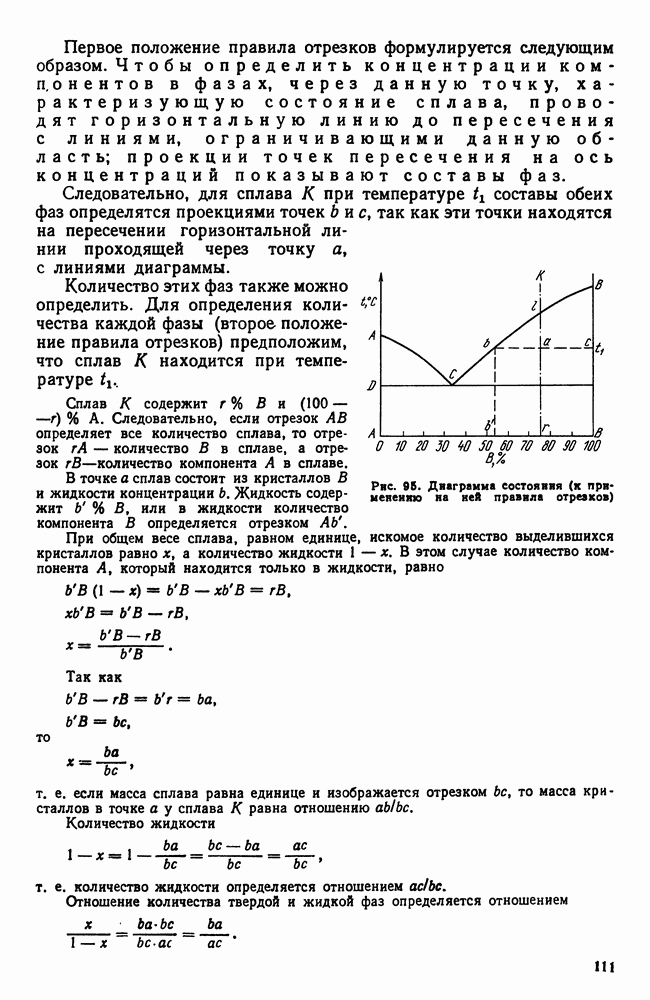
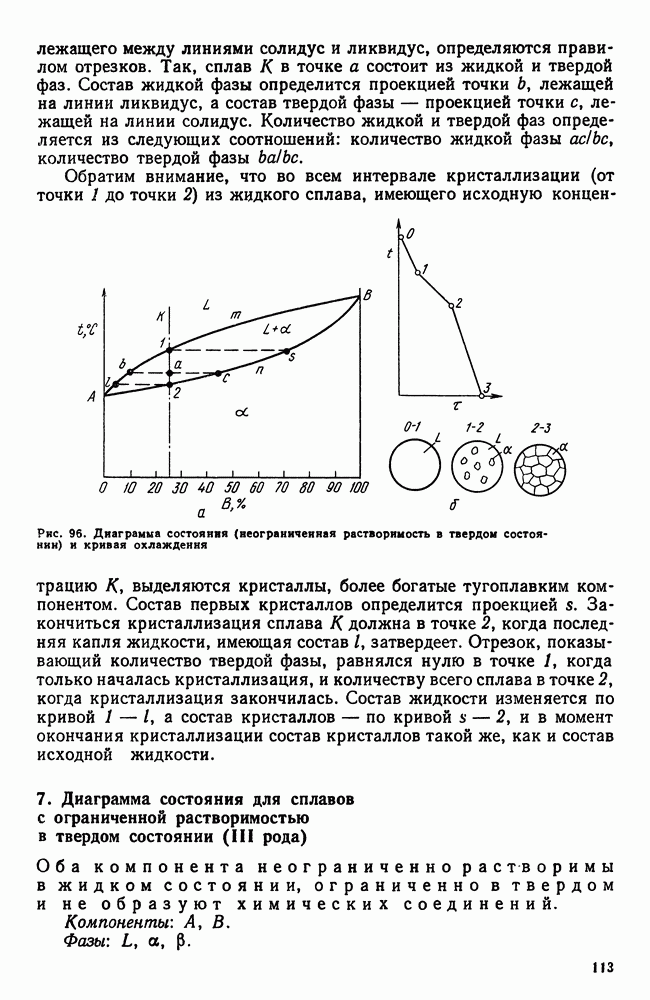
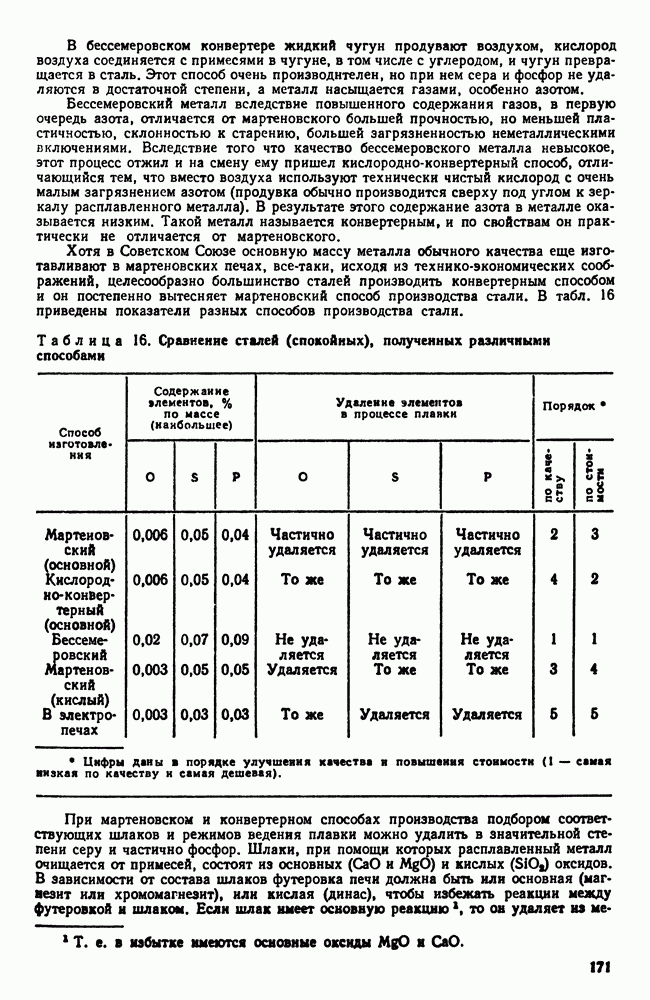
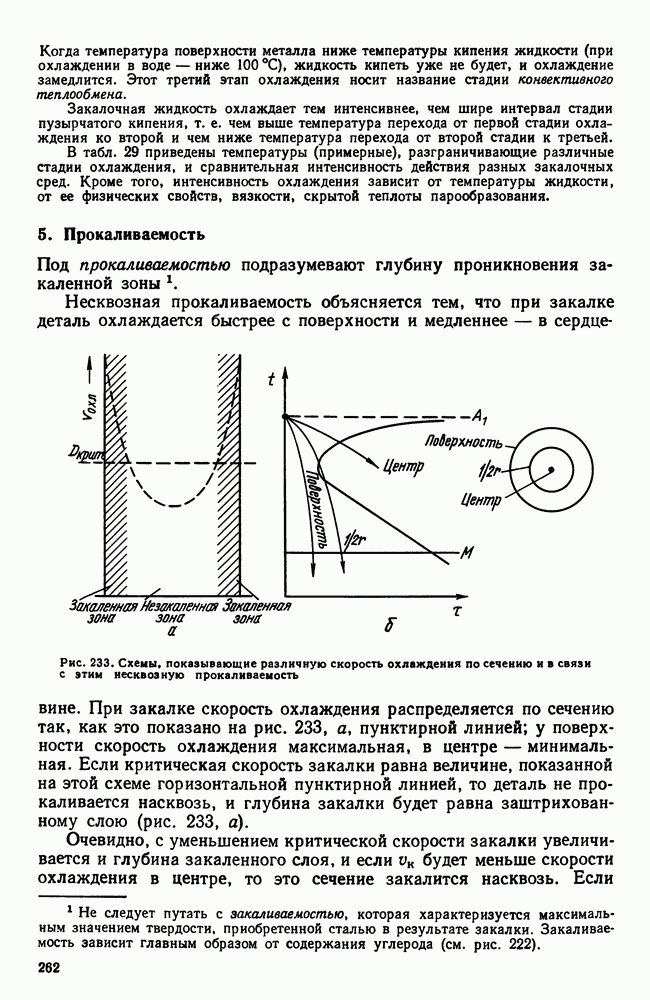
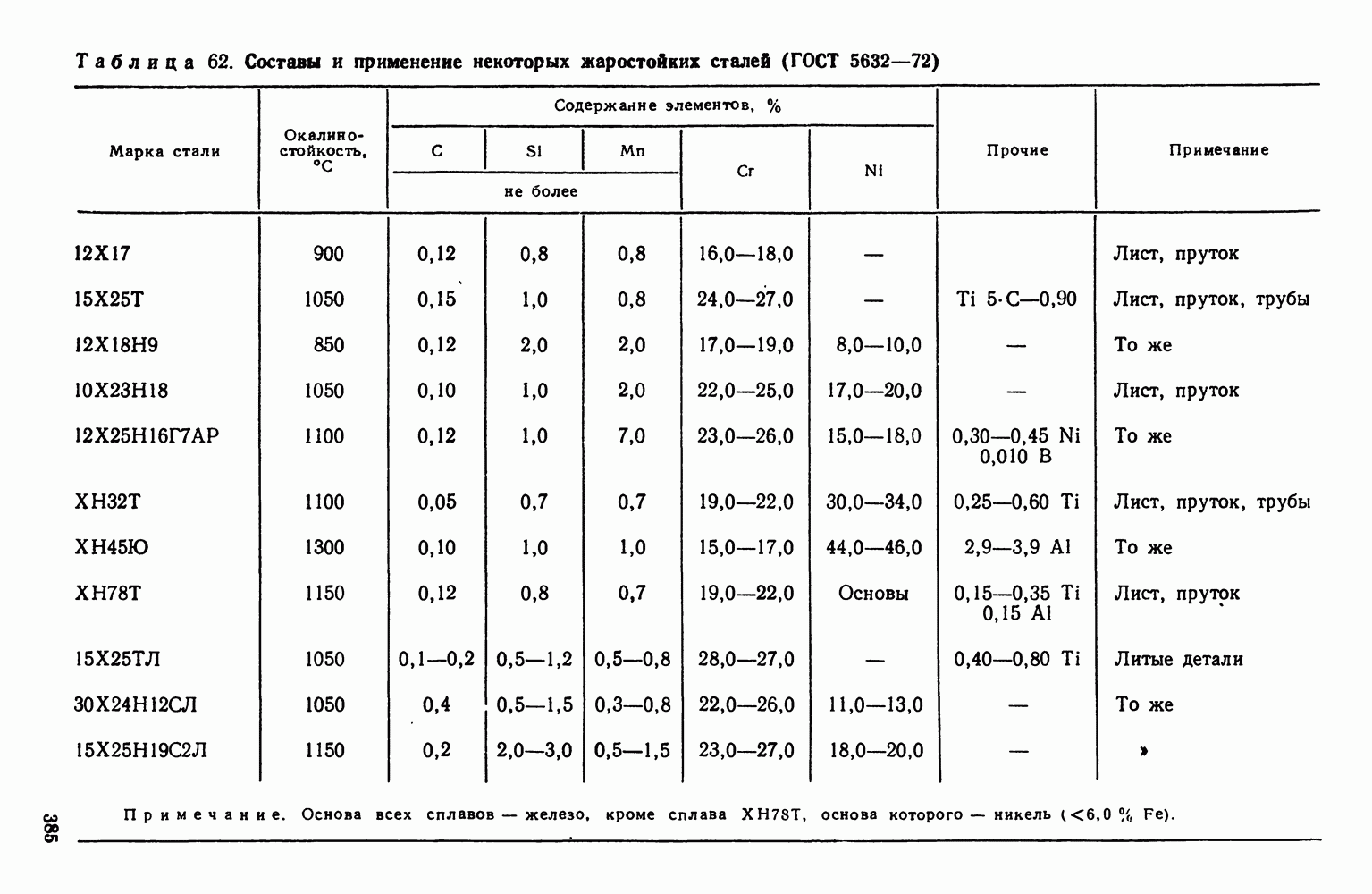
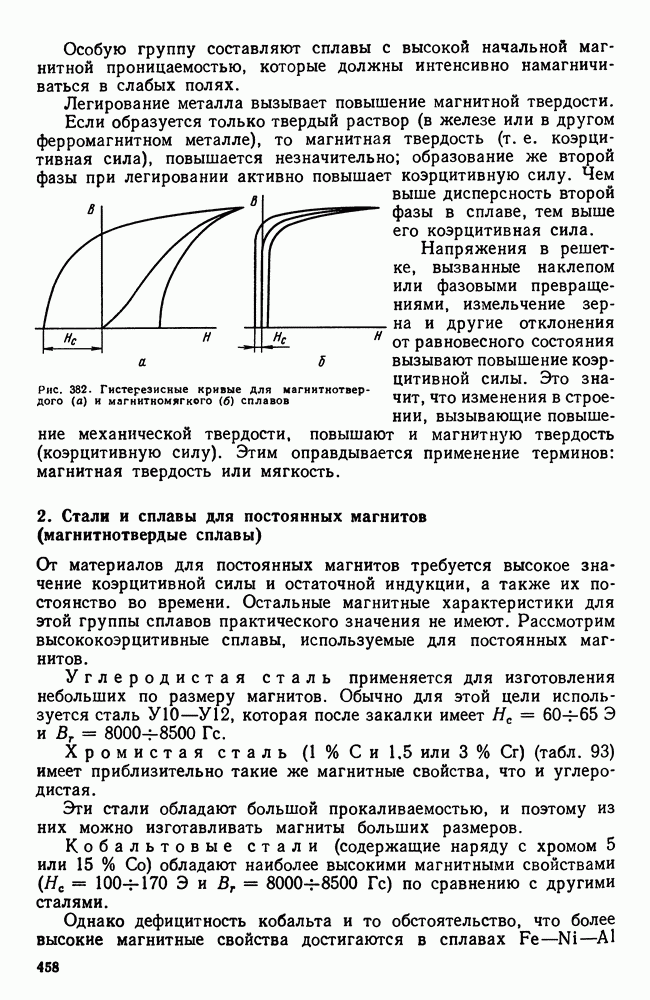
При равновесной кристаллизации (см. рис. 96) состав жидкости и выпавших кристаллов непрерывно меняется в соответствии с линиями ликвидус и солидус. Состав остающейся жидкости удаляется от среднего (исходного) состава, а состав кристаллов приближается к среднему и достигает его к моменту окончания кристаллизации жидкого раствора в однородный твердый. Для осуществления этого процесса должна происходить диффузия как в жидкой, так и в твердой фазе, чтобы выравнить состав.

Рис. 107. Изменение среднего состава кристаллов при неравновесной кристаллизации
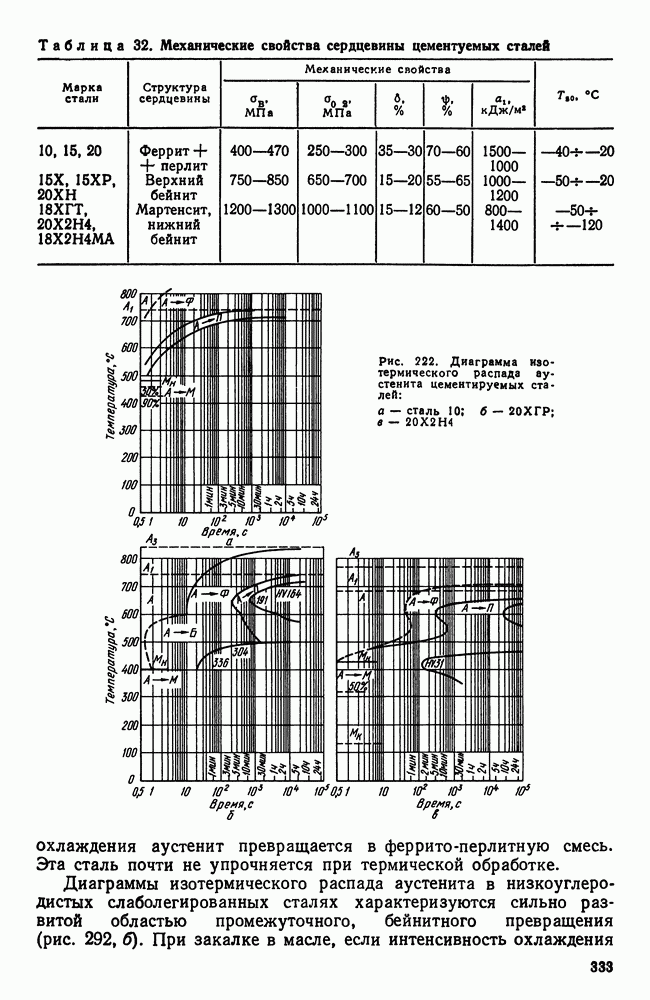
Однако в реальных условиях кристаллизации диффузия в твердой фазе запаздывает. У сплава  (рис. 107) при кристаллизации состав выделяющихся кристаллов меняется в соответствии с положением линии солидуса
(рис. 107) при кристаллизации состав выделяющихся кристаллов меняется в соответствии с положением линии солидуса  но не успевает произойти диффузия, выравнивающая состав твердой фазы и средний состав кристаллов изобразится штриховой линией
но не успевает произойти диффузия, выравнивающая состав твердой фазы и средний состав кристаллов изобразится штриховой линией  . А поэтому когда теоретически должна закончиться кристаллизация (при температуре
. А поэтому когда теоретически должна закончиться кристаллизация (при температуре  еще остается
еще остается
какое-то количество жидкости  характеризуется отрезком
характеризуется отрезком  , а жидкость состава
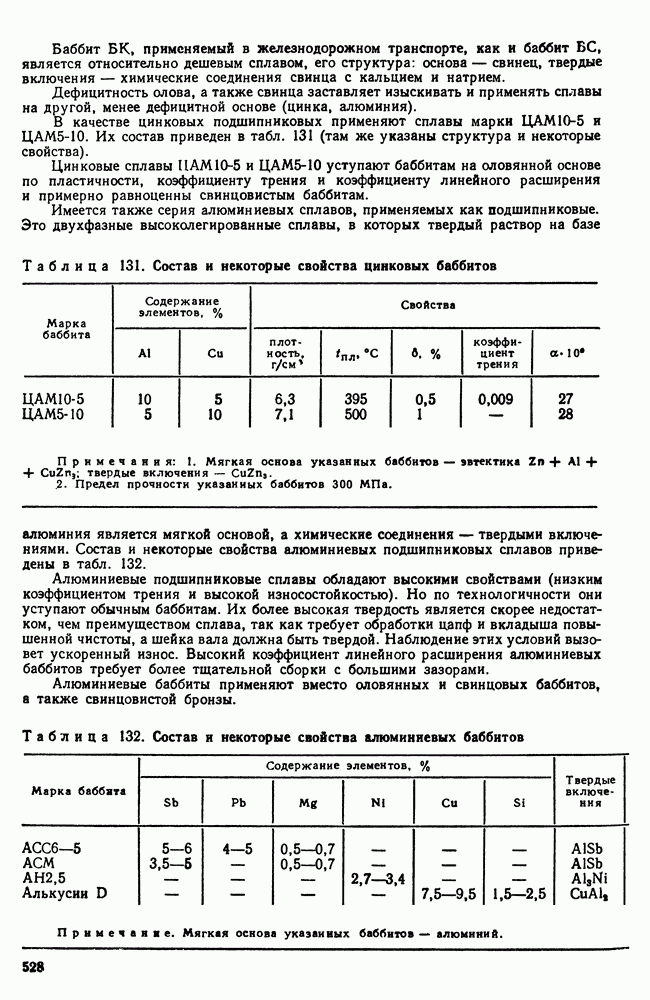
, а жидкость состава  может, обогащаясь компонентом В, продолжать охлаждаться и когда сплав охладится до эвтектической температуры
может, обогащаясь компонентом В, продолжать охлаждаться и когда сплав охладится до эвтектической температуры  жидкость примет состав точки
жидкость примет состав точки  кристаллы не будут однородны и их средний состав будет не
кристаллы не будут однородны и их средний состав будет не  , следовательно, остается какое-то количество жидкости (характеризуемое отрезком
, следовательно, остается какое-то количество жидкости (характеризуемое отрезком  которое затвердеет и даст эвтектику. Таким образом, реальная структура литого сплава I—I в результате описанной схемы кристаллизации будет сильно отличаться от равновесной, описываемой диаграммой состояния.
которое затвердеет и даст эвтектику. Таким образом, реальная структура литого сплава I—I в результате описанной схемы кристаллизации будет сильно отличаться от равновесной, описываемой диаграммой состояния.

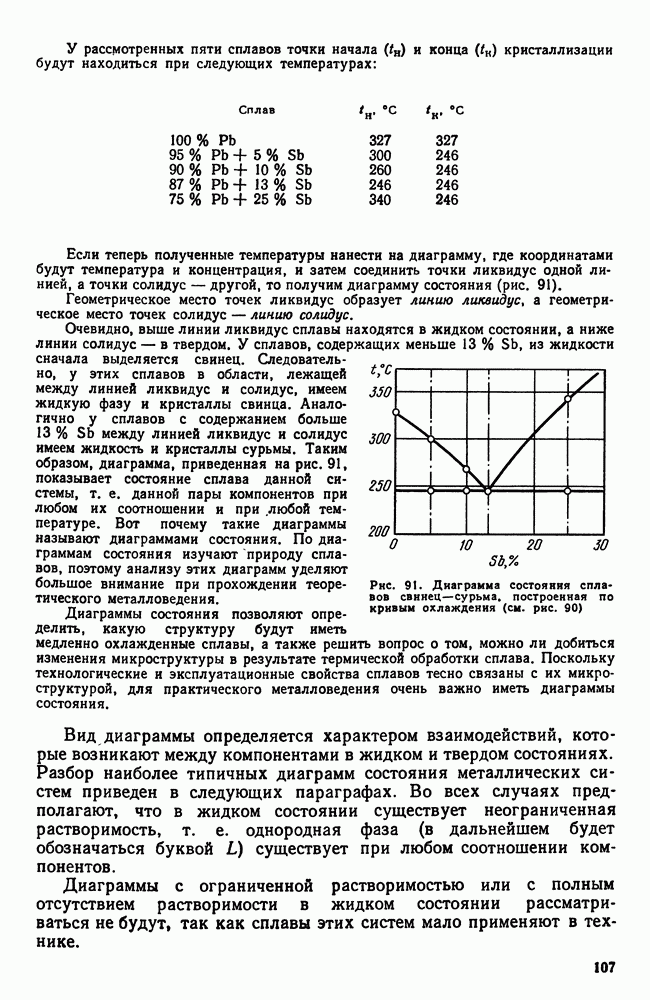
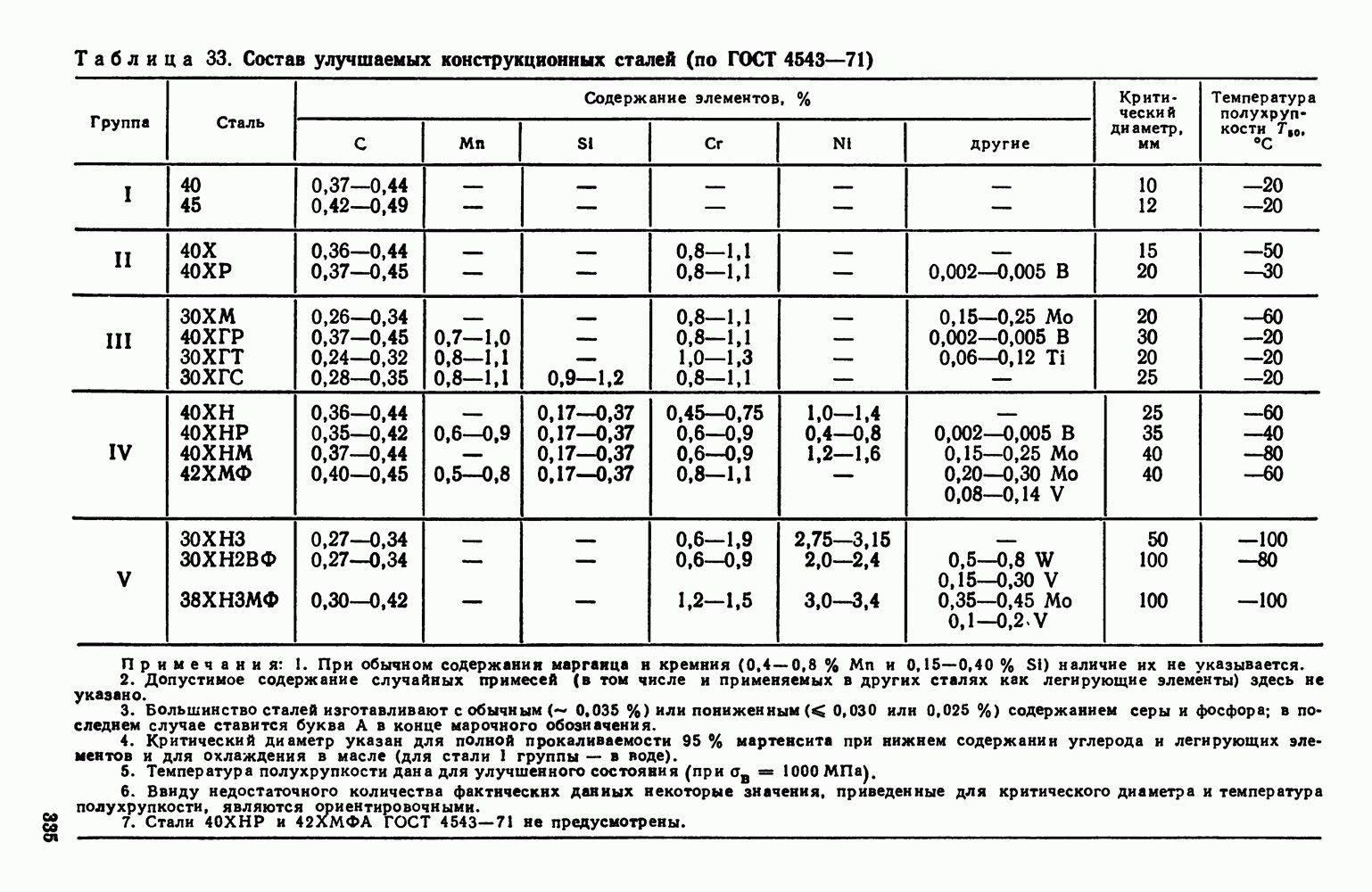
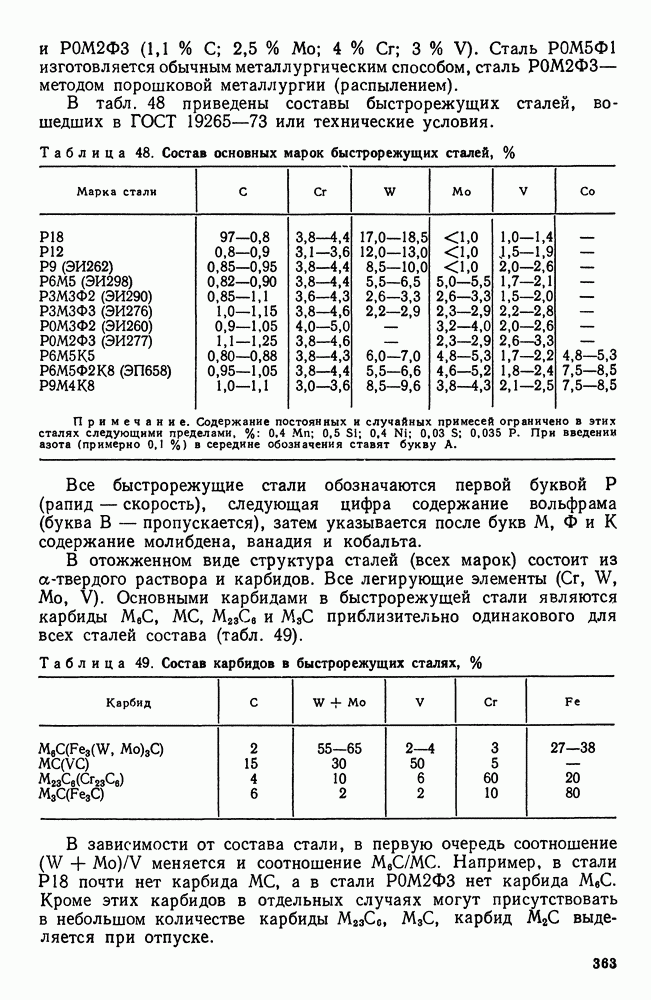
Рис. 108. Структура сплава нейзильбер (твердый раствор цинка и никеля в меди; А. А. Бочвар, X 100: а - в литом состоянии; б — после диффузионного отжига
Вместо однородного твердого раствора получается структура неоднородного твердого раствора  эвтектика. Если точка
эвтектика. Если точка  совпадет с точкой
совпадет с точкой  точнее в процессе кристаллизации достигнет вертикали
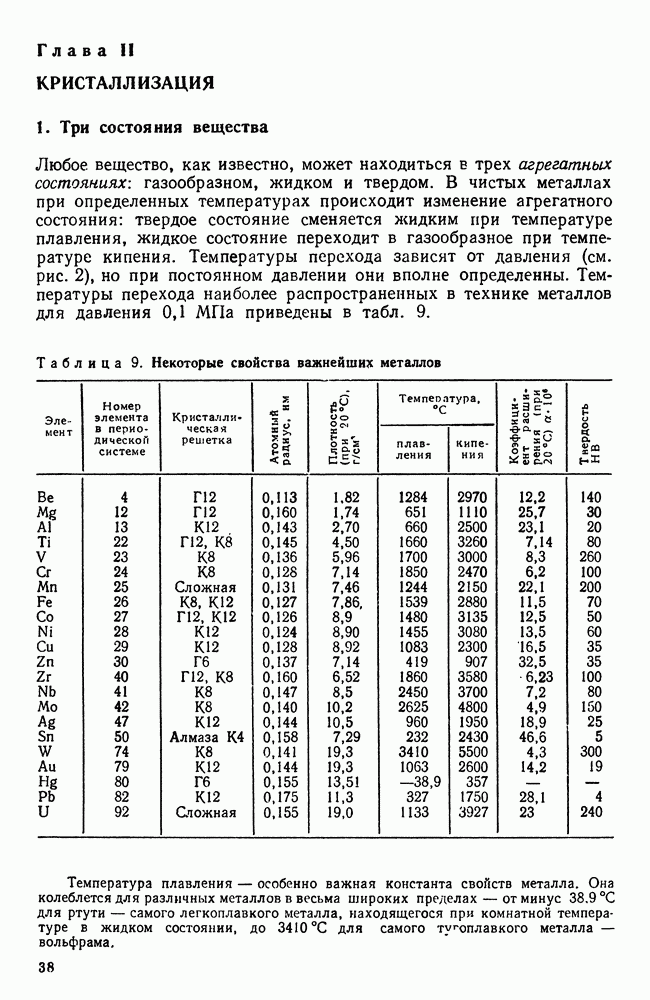
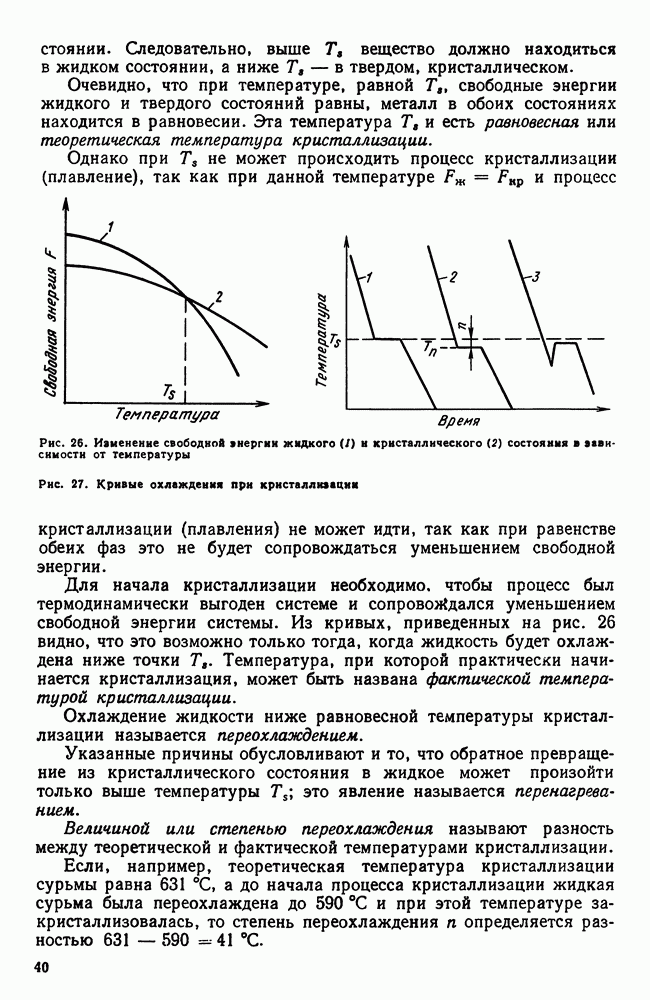
точнее в процессе кристаллизации достигнет вертикали  эвтектики не будет. Отсюда следует, что наличие эвтектики не обязательно в структуре литого сплава, но неоднородный твердый раствор — типичная характеристика литой структуры.
эвтектики не будет. Отсюда следует, что наличие эвтектики не обязательно в структуре литого сплава, но неоднородный твердый раствор — типичная характеристика литой структуры.
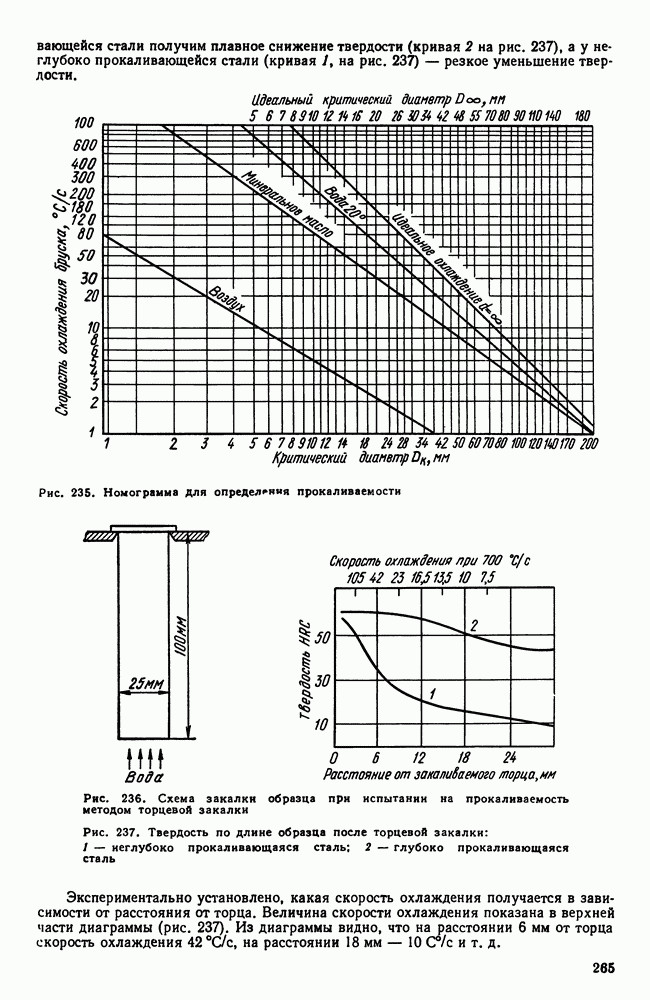
Известно, что в жидкой стали образуются древовидные кристаллы — дендриты (см. с. 46).
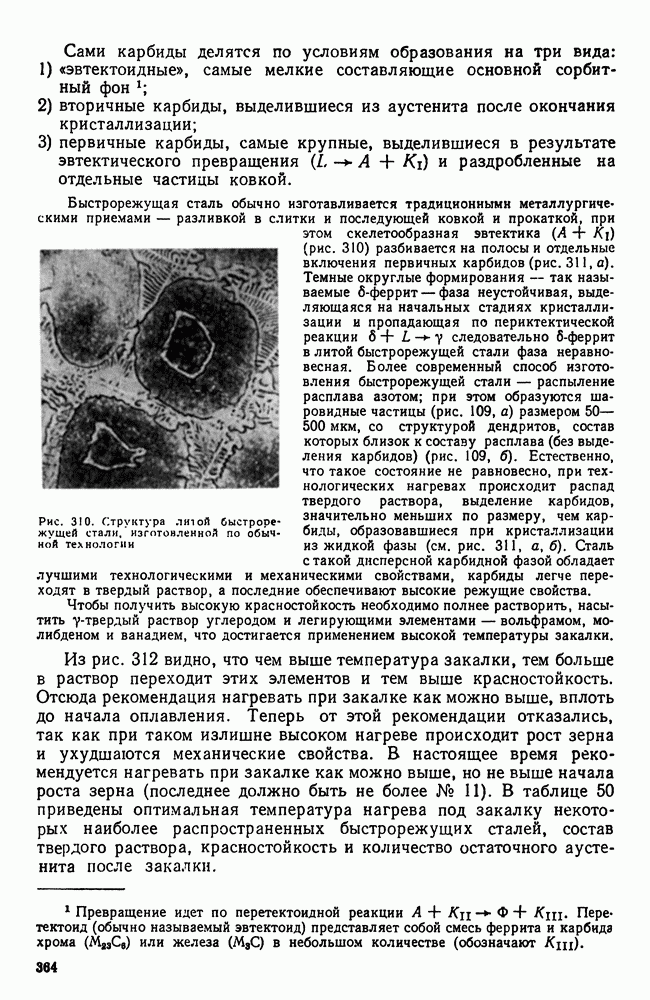
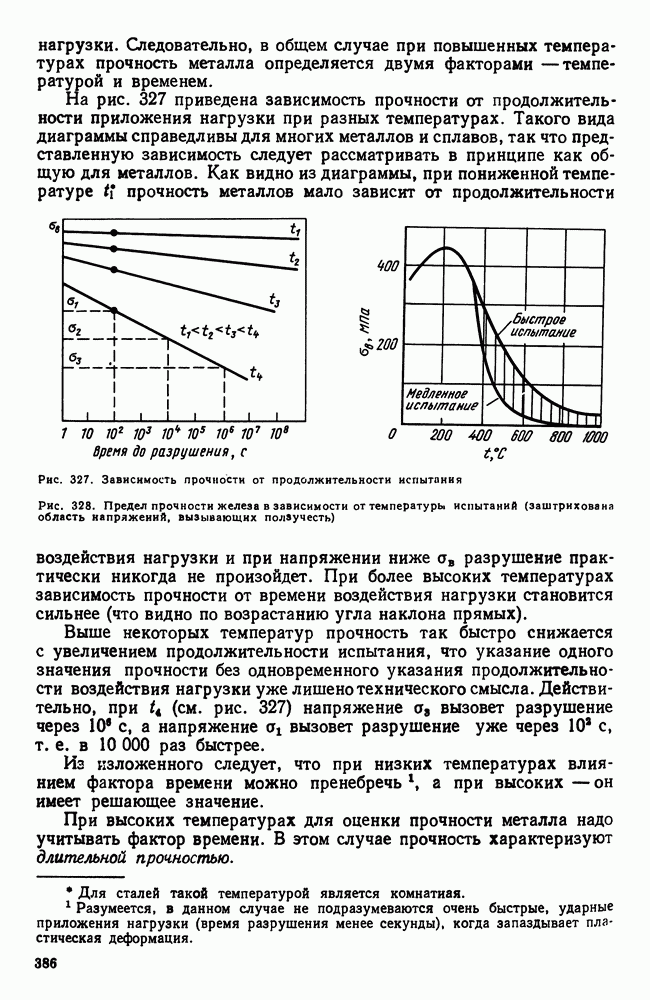
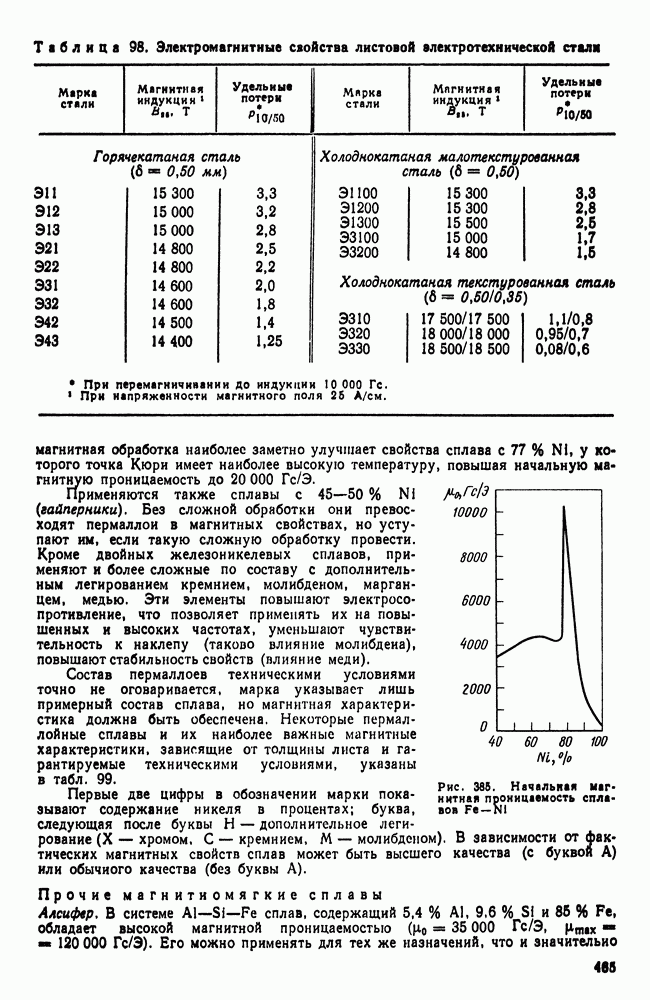
Обычно при кристаллизации твердых растворов первые кристаллы имеют более высокую концентрацию тугоплавкого компонента, чем последующие. Вследствие этого ось первого порядка дендрита содержит больше тугоплавкого компонента, чем ось второго порядка, и и т. д. Междендритные пространства, кристаллизовавшиеся последними, содержат наибольшее количество легкоплавкого компонента, и поэтому они самые легкоплавкие. Описанное явление носит название дендритной ликвации. Состояние дендритной ликвации является неравновесным, неоднородный раствор имеет более высокий уровень свободной энергии, чем однородный. При длительном нагреве сплава дендритная ликвация может быть в большей или меньшей степени устранена диффузией, которая выравнивает концентрацию во всех кристаллах (рис. 108).
Рассмотренная выше схема (рис. 107) предусматривает не очень высокие скорости охлаждения  обычная скорость охлаждения не очень больших слитков); в начале кристаллизации сплав не сильно переохлаждается, но значительно переохлаждается в конце кристаллизации из-за запаздывания диффузии в твердой фазе.
обычная скорость охлаждения не очень больших слитков); в начале кристаллизации сплав не сильно переохлаждается, но значительно переохлаждается в конце кристаллизации из-за запаздывания диффузии в твердой фазе.
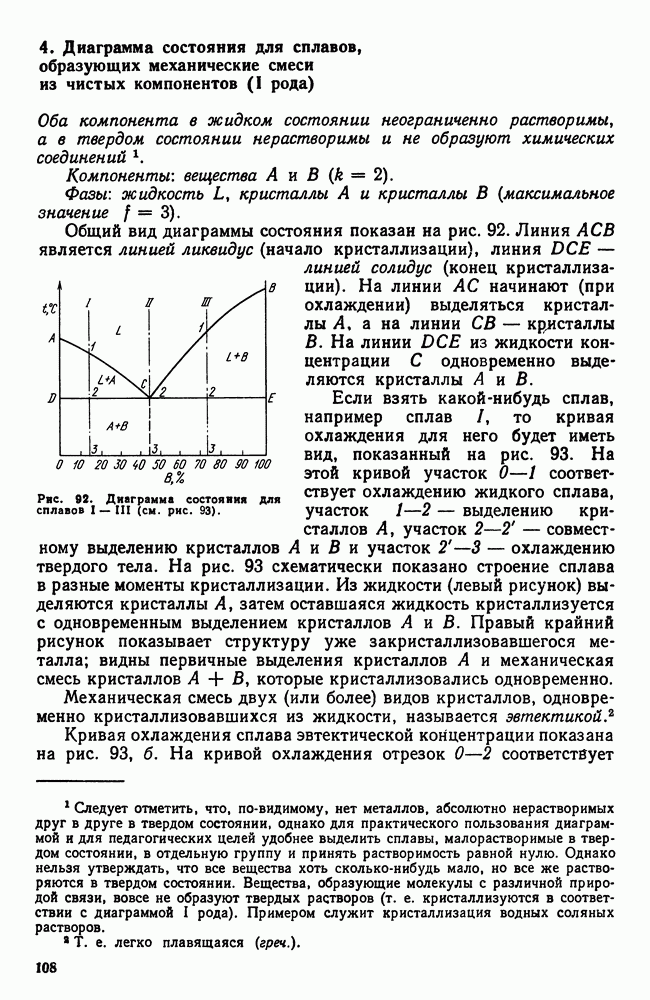
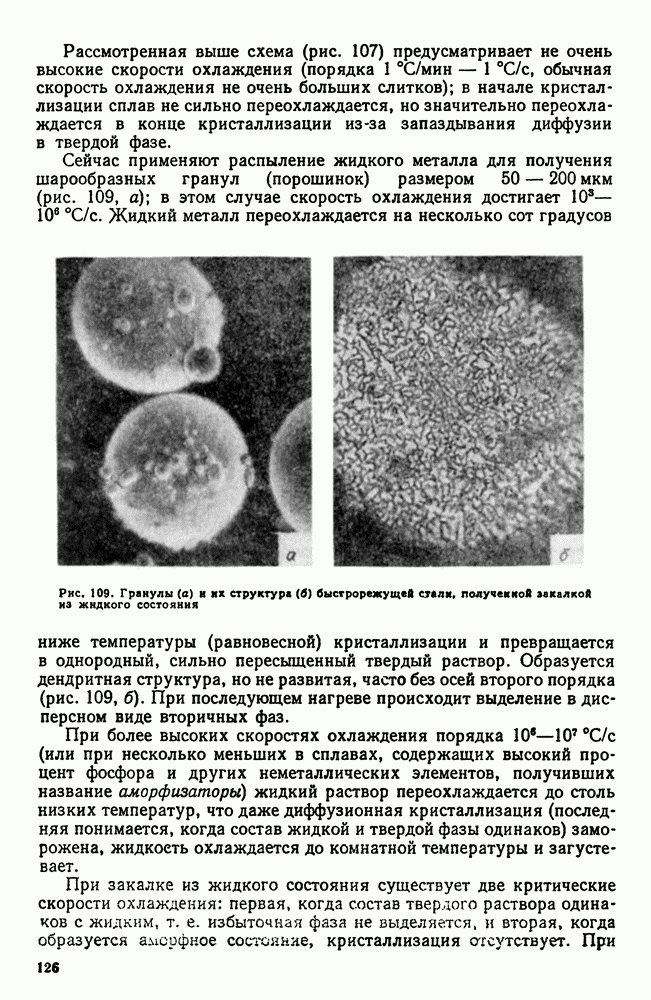
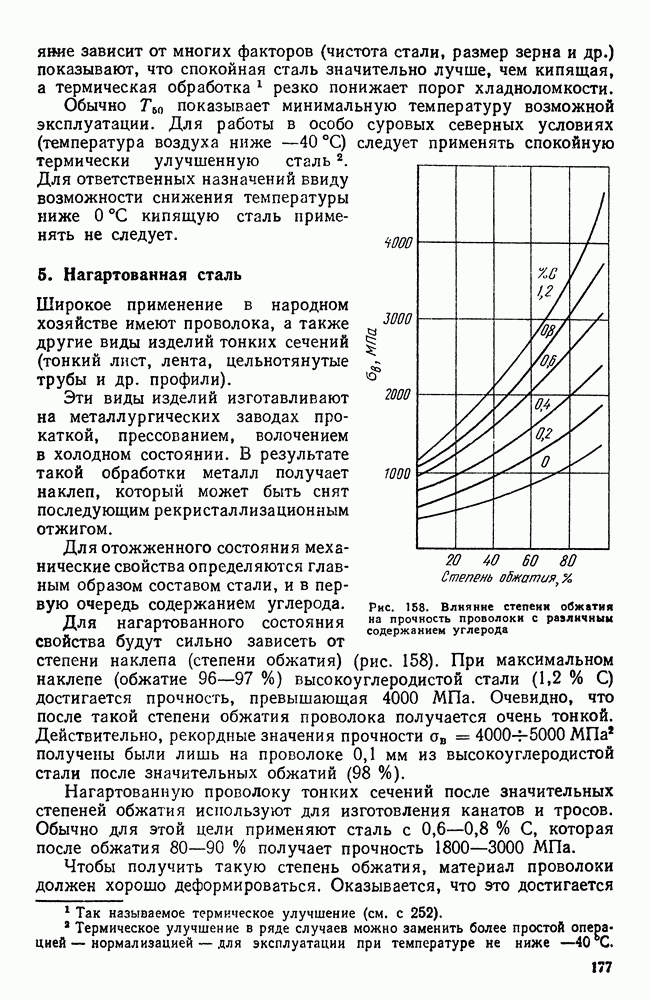
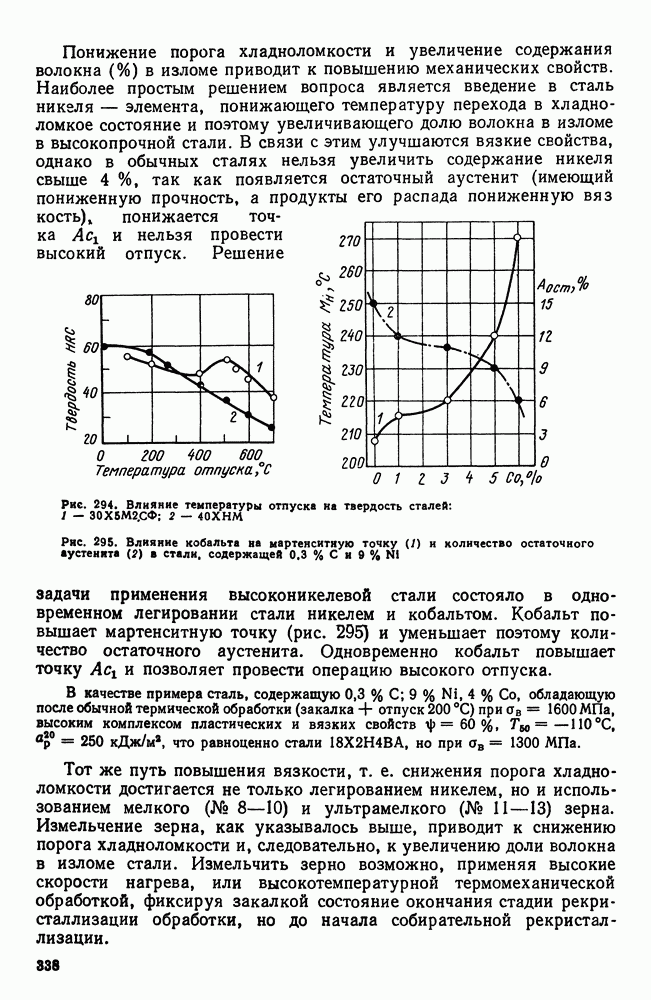
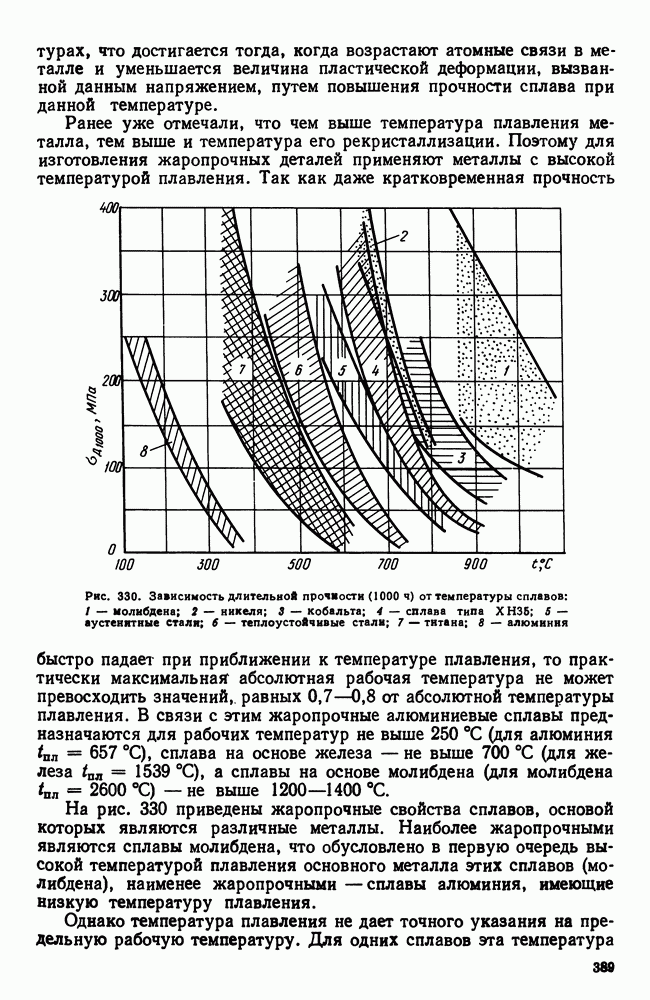
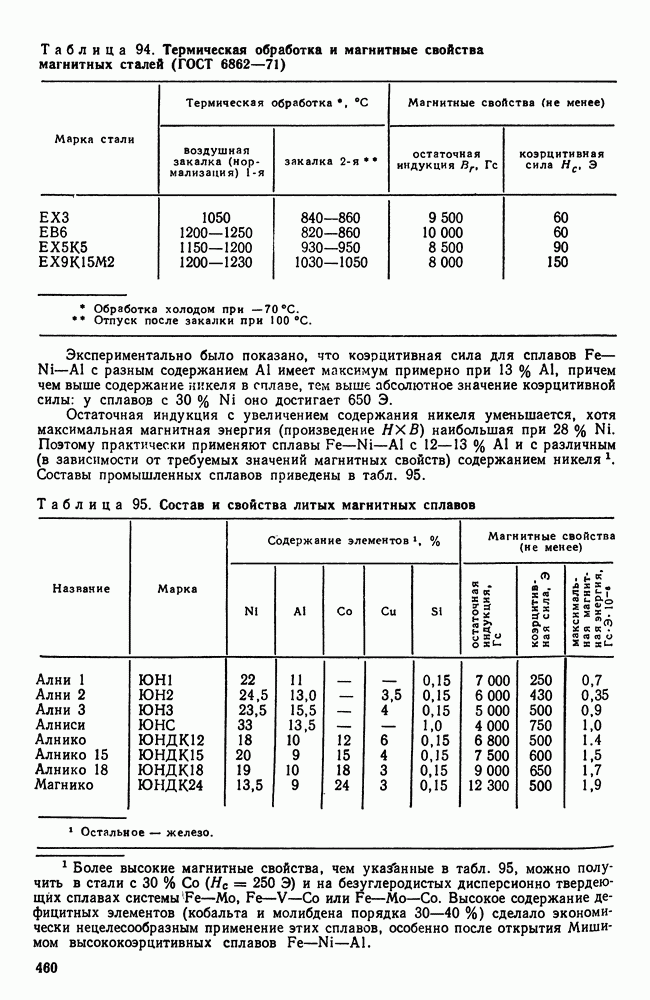
Сейчас применяют распыление жидкого металла для получения шарообразных гранул (порошинок) размером 50 — 200 мкм (рис. 109, а); в этом случае скорость охлаждения достигает  Жидкий металл переохлаждается на несколько сот градусов ниже температуры (равновесной) кристаллизации и превращается в однородный, сильно пересыщенный твердый раствор.
Жидкий металл переохлаждается на несколько сот градусов ниже температуры (равновесной) кристаллизации и превращается в однородный, сильно пересыщенный твердый раствор.

Рис. 109. Гранулы (а) и их структура (б) быстрорежущей сталь, получек кой закалкой из жидкого состояния
Образуется дендритная структура, но не развитая, часто без осей второго порядка (рис. 109, б). При последующем нагреве происходит выделение в дисперсном виде вторичных фаз.
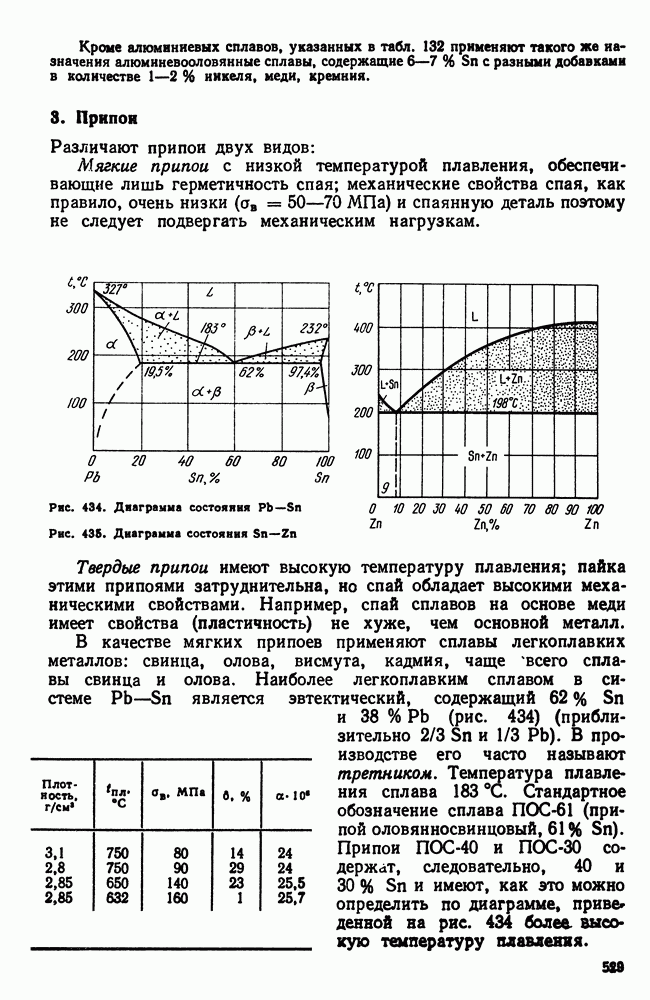
При более высоких скоростях охлаждения порядка  (или при несколько меньших в сплавах, содержащих высокий процент фосфора и других неметаллических элементов, получивших название аморфизаторы) жидкий раствор переохлаждается до столь низких температур, что даже диффузионная кристаллизация (последняя понимается, когда состав жидкой и твердой фазы одинаков) заморожена, жидкость охлаждается до комнатной температуры и загустевает.
(или при несколько меньших в сплавах, содержащих высокий процент фосфора и других неметаллических элементов, получивших название аморфизаторы) жидкий раствор переохлаждается до столь низких температур, что даже диффузионная кристаллизация (последняя понимается, когда состав жидкой и твердой фазы одинаков) заморожена, жидкость охлаждается до комнатной температуры и загустевает.
При закалке из жидкого состояния существует две критические скорости охлаждения: первая, когда состав твердого раствора одинаков с жидким, т. е. избыточная фаза не выделяется, и вторая, когда образуется аморфное состояние, кристаллизация отсутствует. При
большой скорости охлаждения, но меньшей чем первая критическая скорость, избыточная фаза частично или полностью успеет выделиться, но в дисперсном виде. Получается большое разнообразие структур, что, естественно, обусловливает и большое разнообразие свойств. Использование этого нового способа термической обработки — закалка из жидкого состояния, делает первые шаги в направлении ее использования в практических целях.
Неравновесная кристаллизация твердого раствора
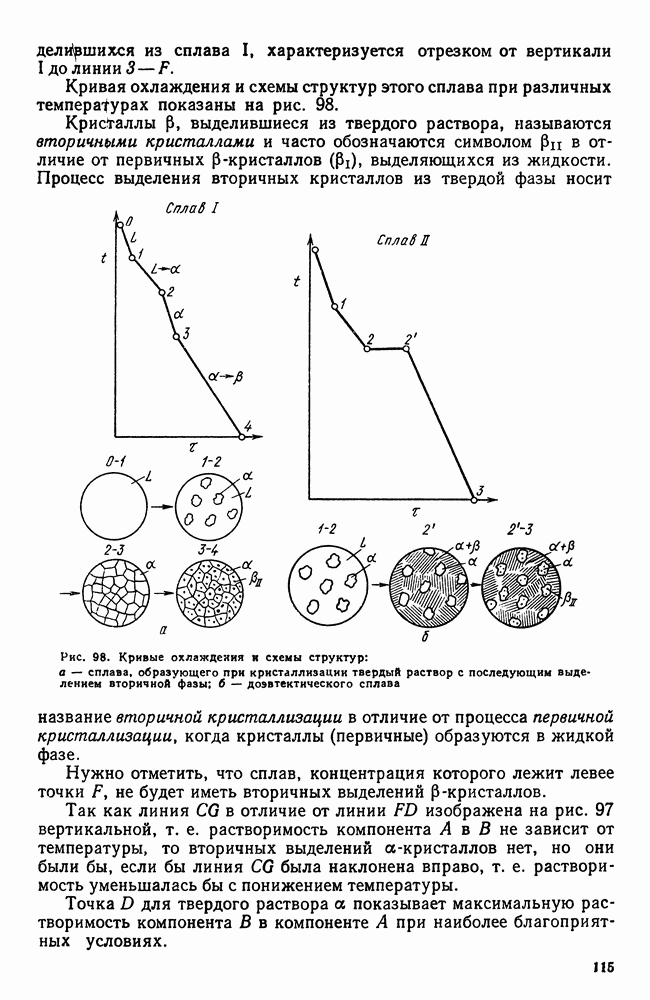
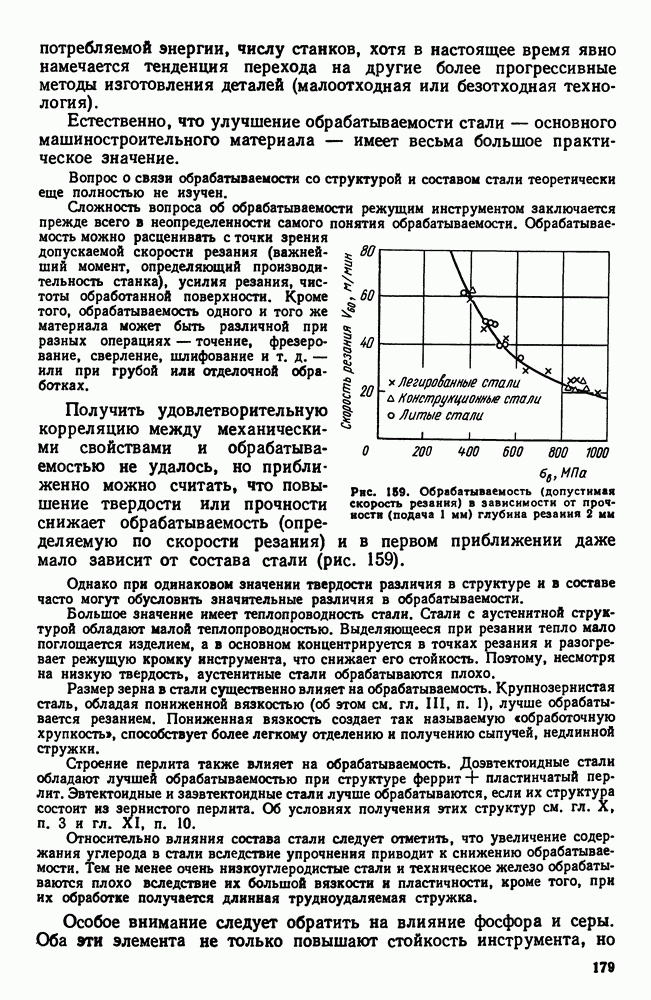
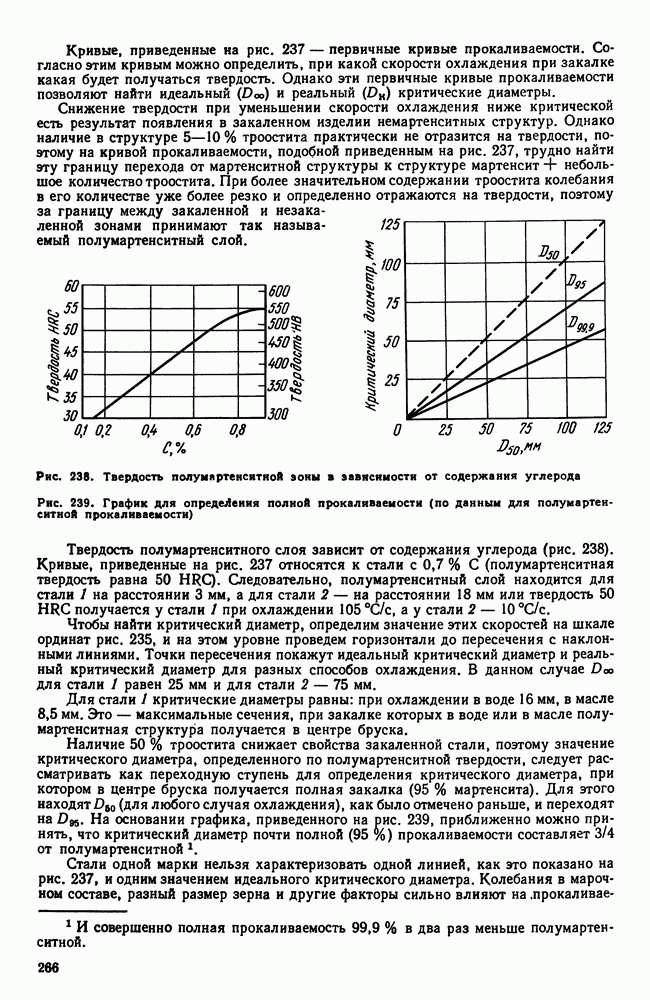
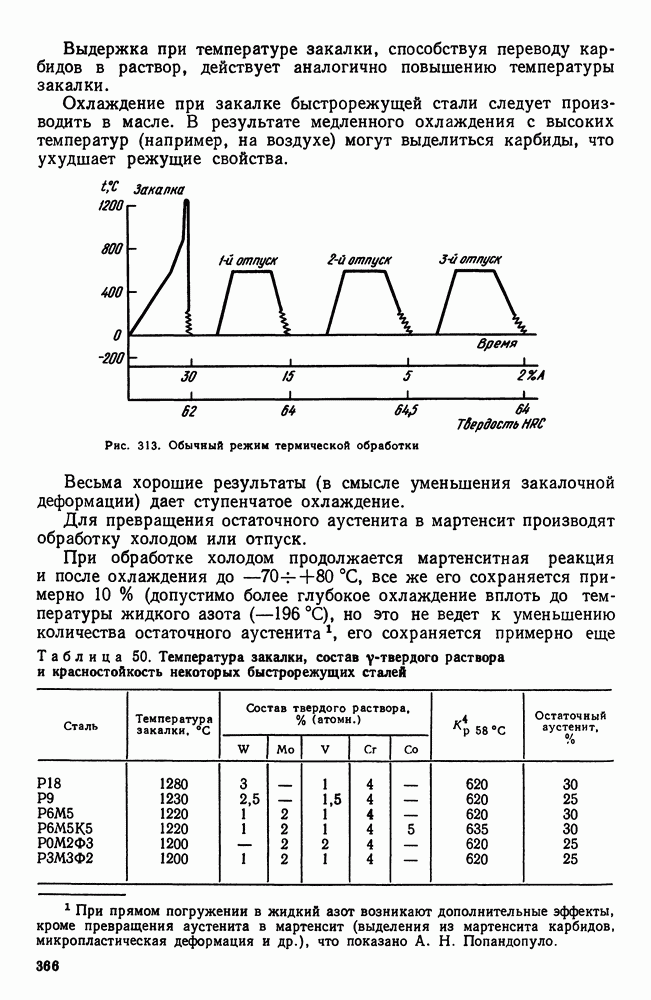
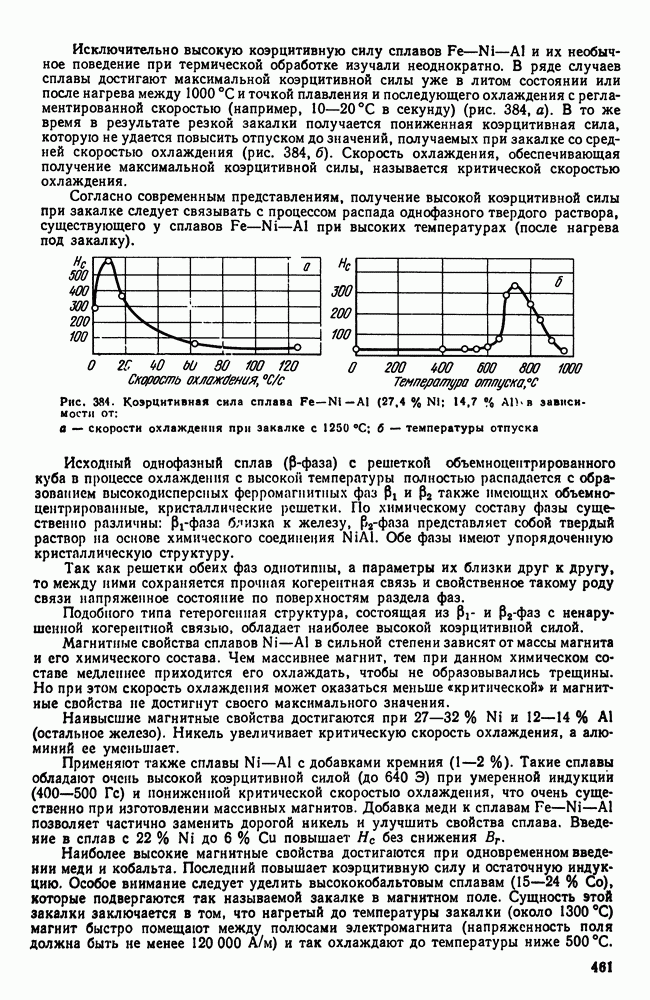
Если в процессе охлаждения возможен распад твердого раствора, то диаграмма состояния показывает начало этого процесса при самом медленном охлаждении — для сплава  точка 1 (рис. 110). С увеличением скорости охлаждения температура начала выделения избыточной фазы
точка 1 (рис. 110). С увеличением скорости охлаждения температура начала выделения избыточной фазы  снижается (точки
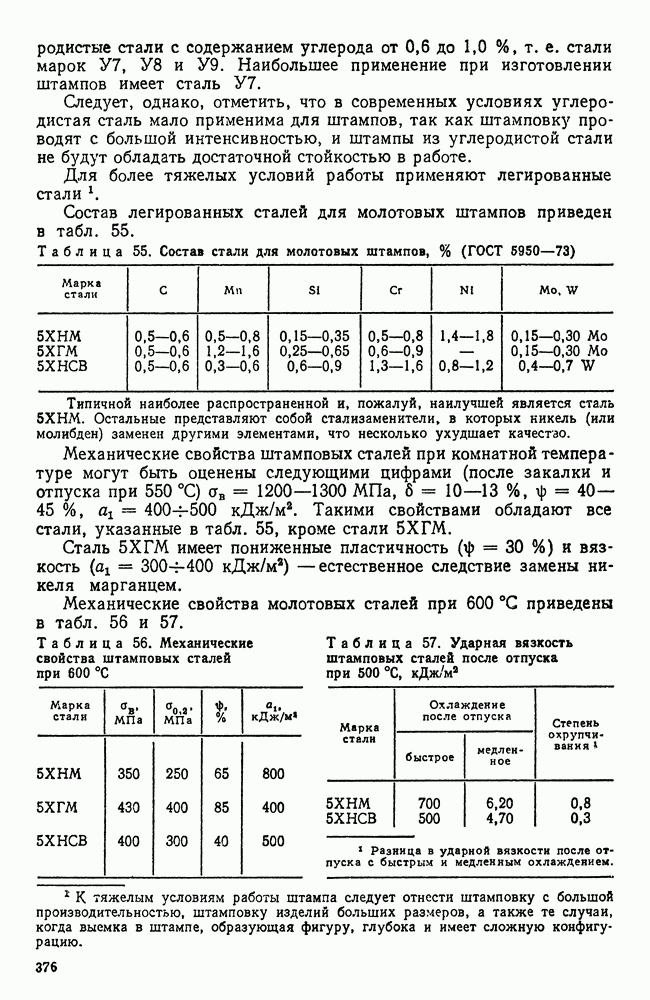
снижается (точки  количество выделившейся фазы уменьшается (отрезок от Г или
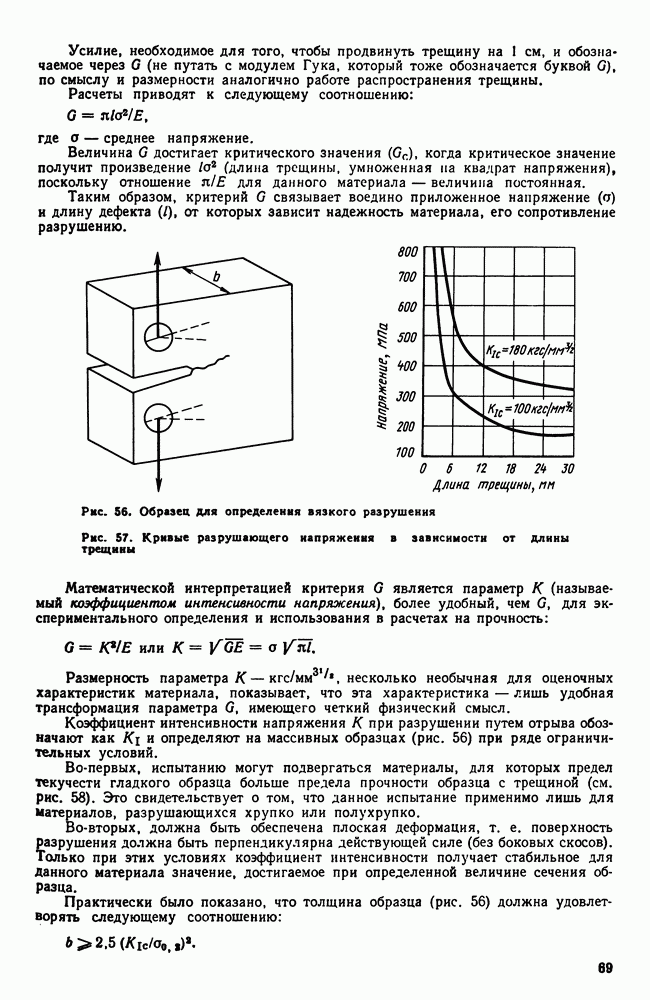
количество выделившейся фазы уменьшается (отрезок от Г или  до
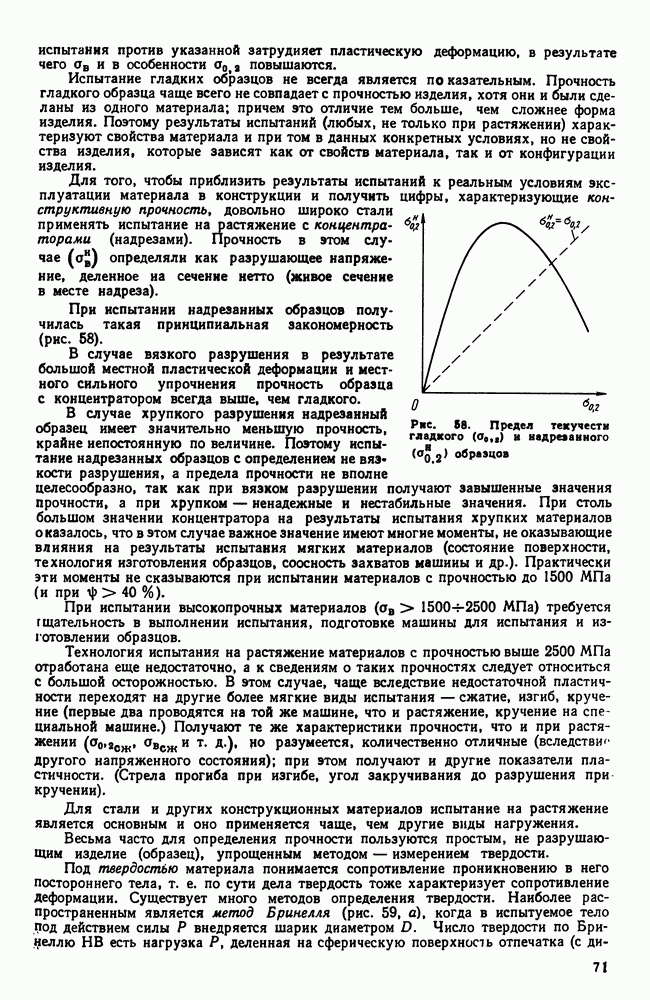
до  и наконец при определенной, еще большей, скорости охлаждения твердый раствор без выделений полностью переохлаждается до комнатной температуры.
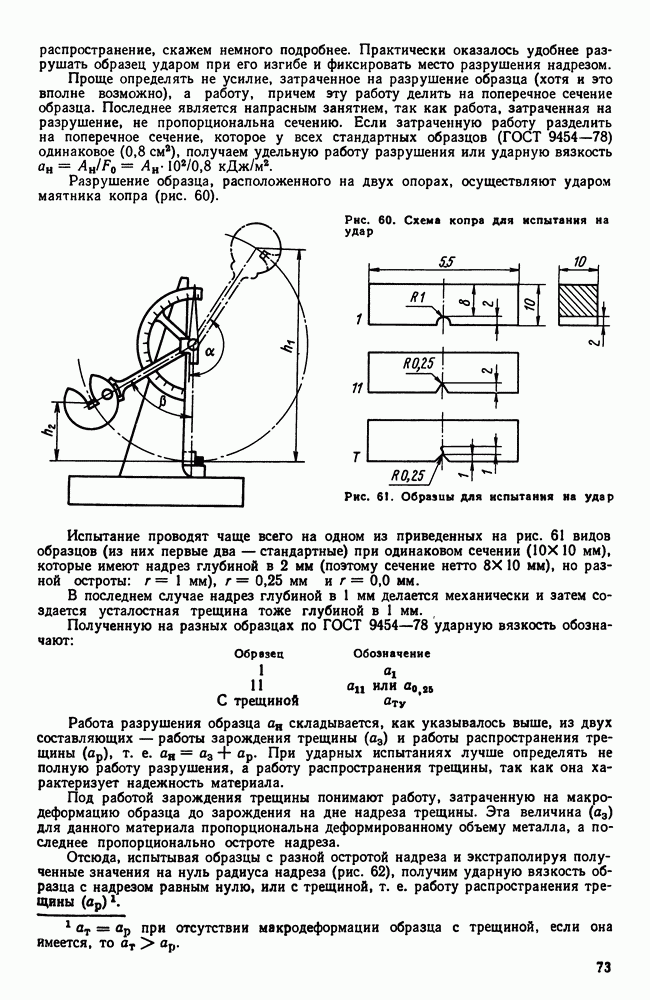
и наконец при определенной, еще большей, скорости охлаждения твердый раствор без выделений полностью переохлаждается до комнатной температуры.

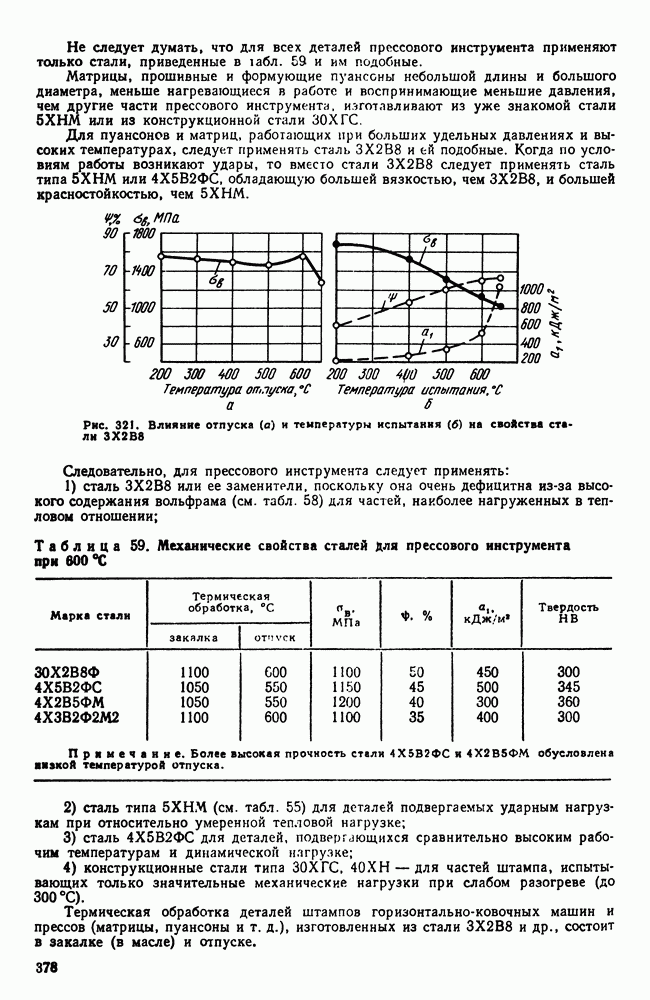
Рис. 110. Кристаллизация из твердого раствора в условиях переохлаждения
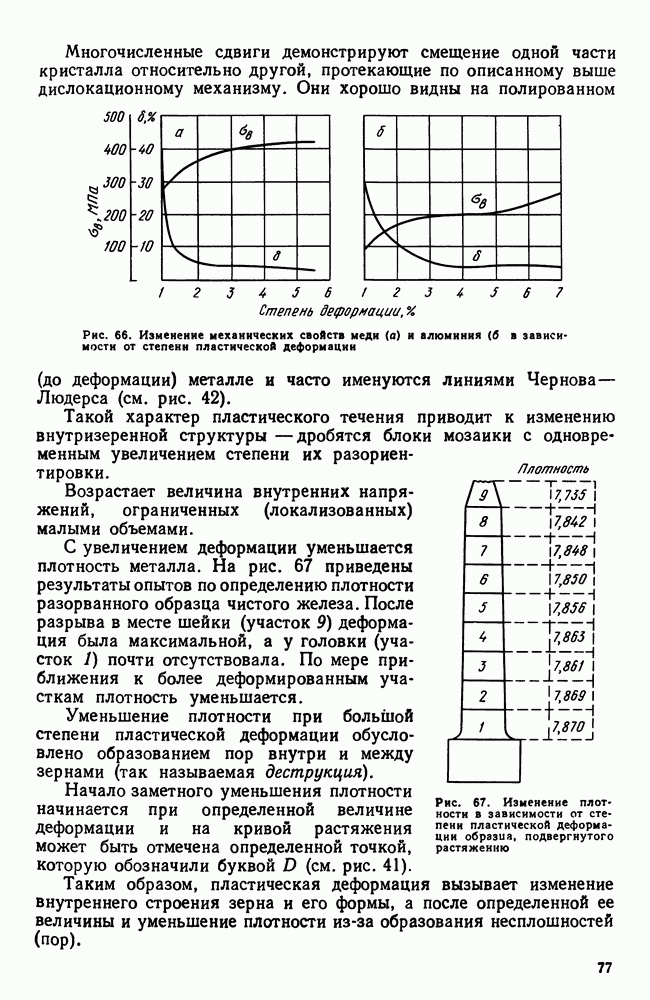
Таким образом, регулируя скорость охлаждения, можно добиться разной степени распада — вплоть до полного его подавления. Такие пересыщенные растворы неустойчивы. Если, однако, тепловая подвижность атомов переохлажденного раствора недостаточна, то состояние пересыщения может сохраняться неопределенно долгое время. В противном случае с течением времени будет происходить постепенный распад пересыщенного раствора с выделением избыточной фазы. Этот процесс будет ускоряться при повышении температуры.
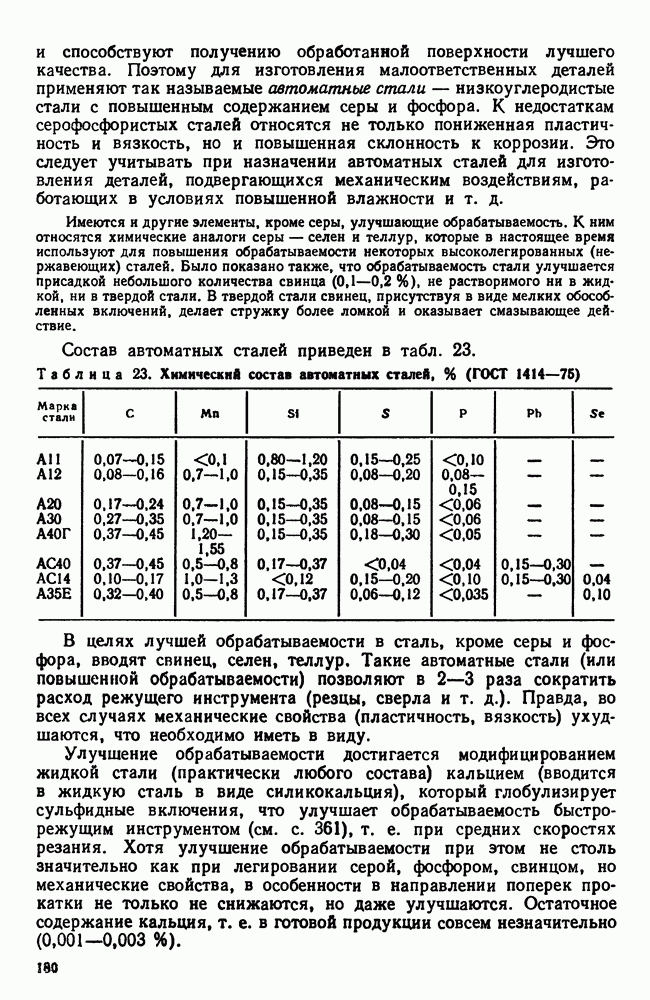
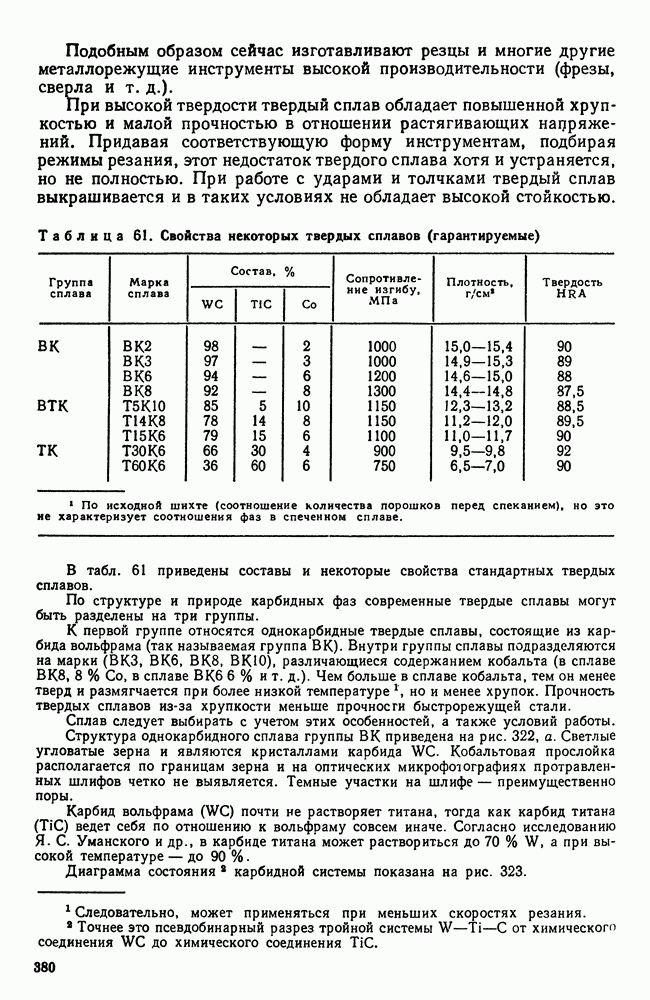
Образующиеся при высокой температуре вторичные фазы при медленном охлаждении твердого раствора или высоком вторичном нагреве закаленного (пересыщенного) твердого раствора не только крупнее по размерам, но ориентационно не связаны с маточной фазой. Слой атомов, принадлежащий старой фазе, соседствует со слоем атомов, принадлежащим решетке новой фазы, как показано на рис. 111 у а.
Для случая выделения при низкой температуре новая  -фаза (она по составу обычно не отвечает составу стабильной
-фаза (она по составу обычно не отвечает составу стабильной  -фазы указанной на равновесной диаграмме) определенным образом ориентирована относительно исходной, так что пограничный слой атомов в равной степени принадлежит обеим решеткам (рис. 111, б). Подобное сочленение кристаллических решеток называется когерентным. На границе раздела при когерентной связи возникают и сохраняются напряжения тем большие, чем больше отличие в строении (в плоскости раздела) сопряженных решеток.
-фазы указанной на равновесной диаграмме) определенным образом ориентирована относительно исходной, так что пограничный слой атомов в равной степени принадлежит обеим решеткам (рис. 111, б). Подобное сочленение кристаллических решеток называется когерентным. На границе раздела при когерентной связи возникают и сохраняются напряжения тем большие, чем больше отличие в строении (в плоскости раздела) сопряженных решеток.
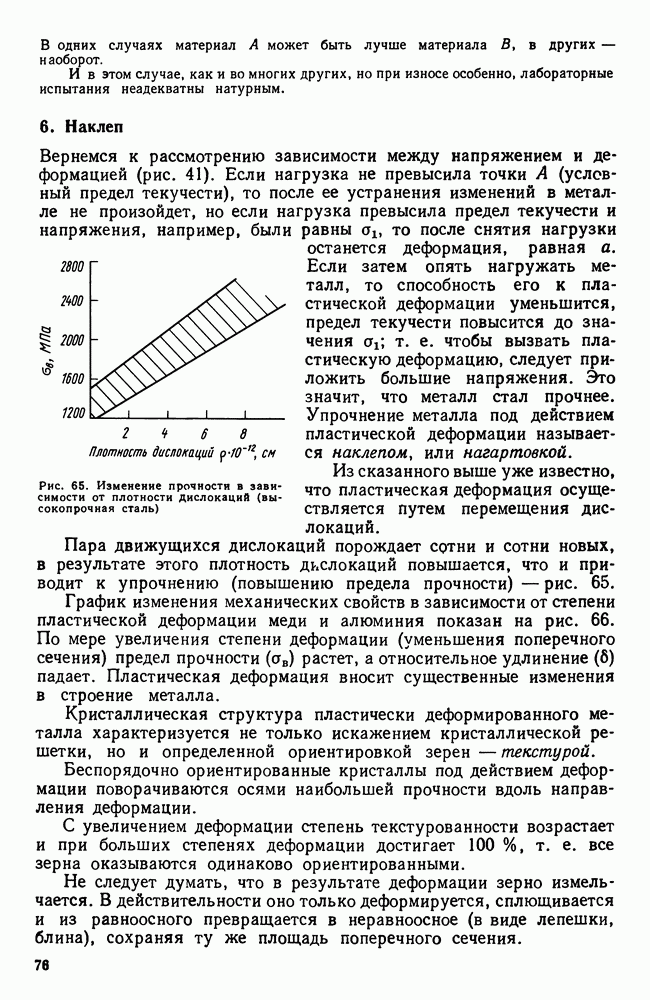
Если температуру сплава повышать, то вследствие увеличения тепловой подвижности атомов и наличия напряжений на границах раздела фаз. Когерентная связь разрывается (явление срыва когерентности), метастабильные фазы переходят в устойчивую  -фазу, пластинчатые кристаллики
-фазу, пластинчатые кристаллики  -фазы растут, стремясь принять округлую форму. Когда описанные процессы пройдут полностью, структура и фазовый состав станут такими же, как и в случае медленного охлаждения.
-фазы растут, стремясь принять округлую форму. Когда описанные процессы пройдут полностью, структура и фазовый состав станут такими же, как и в случае медленного охлаждения.
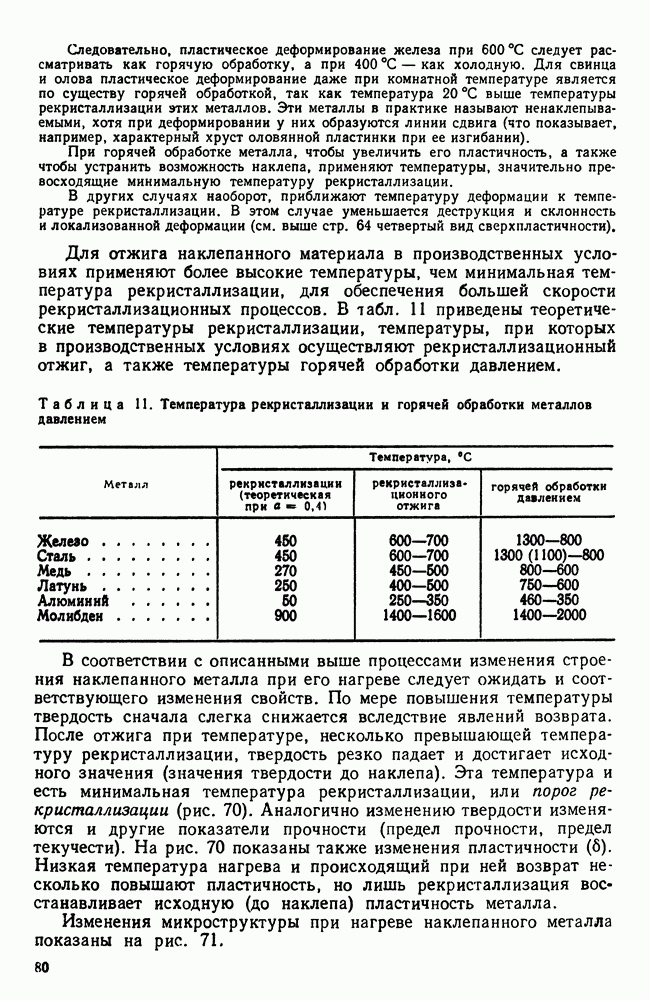
Описанный выше процесс фиксирования быстрым охлаждением неустойчивого состояния носит название закалки, а последующий процесс постепенного приближения к равновесному состоянию  нагрева или длительной выдержки) называется отпуском и старением.
нагрева или длительной выдержки) называется отпуском и старением.

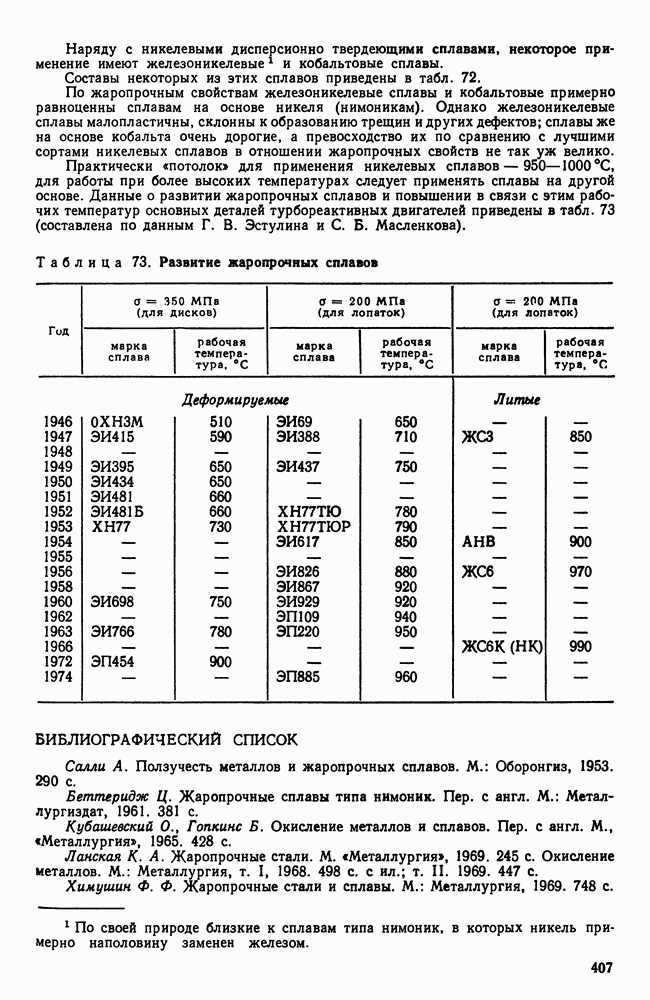
Рис. 111. Схемы сочленения кристаллических решеток: а — несвязанная; б — связанная (когерентная)
Столь разнообразное изменение структуры, достигаемое разной степенью приближения сплава к равновесному состоянию, приводит к разнообразному изменению свойств, чем и обусловлено широкое применение термической обработки, в основе которой заложены процессы неравновесной кристаллизации, в общих чертах описанные выше.
Существо происходящих процессов, а также и получаемые при этом свойства будут более конкретно рассмотрены дальше.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Часть первая. ТЕОРИЯ СПЛАВОВ
- Глава I. КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ
- 2. Классификация металлов
- 3. Кристаллическое строение металлов
- 4. Кристаллические решетки металлов
- 5. Реальное строение металлических кристаллов
- 6. Анизотропия свойств кристаллов
- 7. Методы изучения строения металлов
- Глава II. КРИСТАЛЛИЗАЦИЯ
- 1. Три состояния вещества
- 2. Энергетические условия процесса кристаллизации
- 3. Механизм процесса кристаллизации
- 4. Форма кристаллических образований
- 5. Строение слитка
- 6. Превращения в твердом состояние. Полиморфизм
- 7. Магнитные превращения
- 8. Закалка из жидкого состояния. Аморфное состояние
- Глава III. МЕХАНИЧЕСКИЕ СВОЙСТВА. НАКЛЕП И РЕКРИСТАЛЛИЗАЦИЯ
- 2. Упругая и пластическая деформация. Несовершенства решетки и прочность металлов
- 3. Сверхпластичность
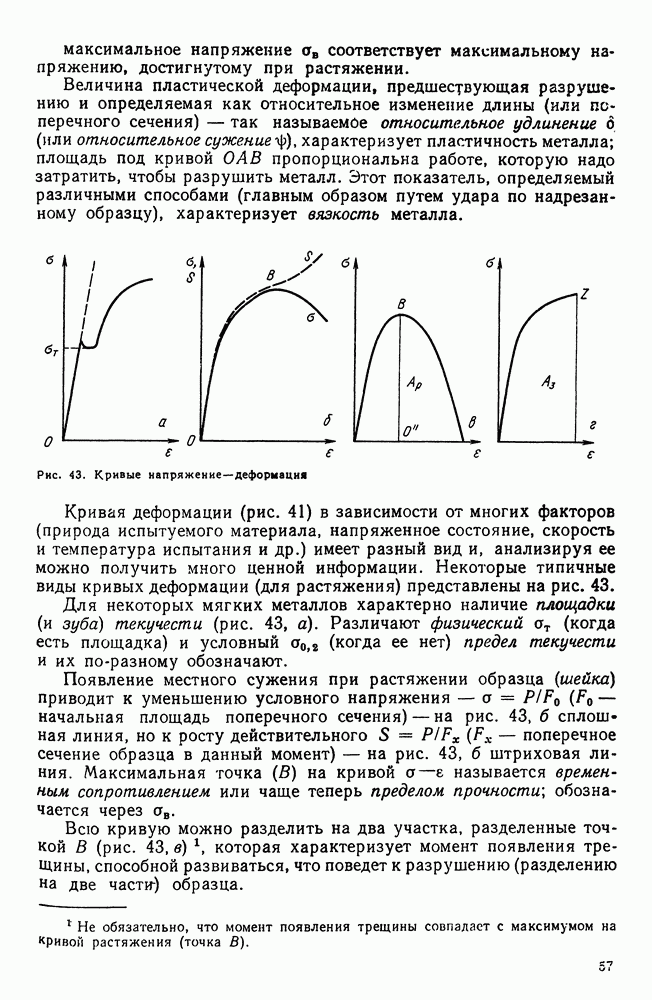
- 4. Разрушение
- 5. Методы определения механических свойств
- 6. Наклеп
- 7. Влияние нагрева на строение и свойства деформированного металла (рекристаллизационные процессы)
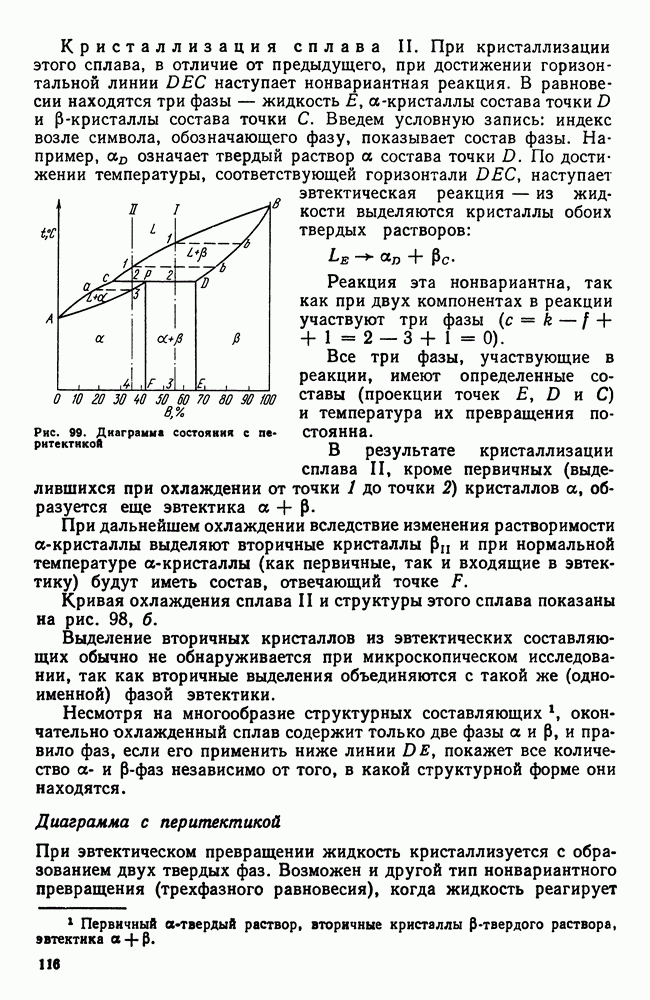
- Глава IV. СТРОЕНИЕ СПЛАВОВ
- 2. Химическое соединение
- 3. Твердый раствор на основе одного из компонентов сплава
- 4. Твердый раствор на основе химического соединения
- 5. Упорядоченные твердые растворы
- 6. Электронные соединения (фазы Юм-Розери)
- 7. Фазы Лавеса
- 8. Фазы внедрения
- Глава V. ДИАГРАММА СОСТОЯНИЯ
- 2. Общие замечания о построении диаграмм состояния
- 3. Экспериментальное построение диаграмм
- 4. Диаграмма состояния для сплавов, образующих механические смеси из чистых компонентов (I рода)
- 5. Правило отрезков
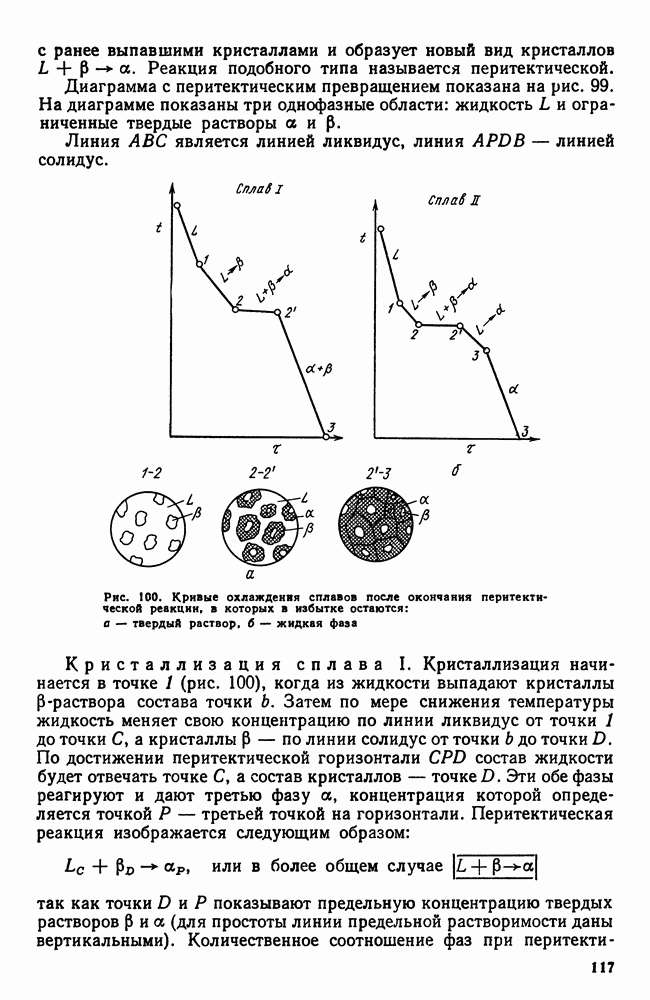
- 6. Диаграмма состояния для сплавов с неограниченной растворимостью в твердом состоянии (II рода)
- 7. Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии (III рода)
- 8. Диаграмма состояния для сплавов, образующих химические соединения (IV рода)
- 9. Диаграмма состояния для сплавов, испытывающих полиморфные превращения
- 10. Кристаллизация сплавов в неравновесных условиях
- 11. Системы с тремя компонентами
- 12. Упрощенные методы изучения многокомпонентных систем
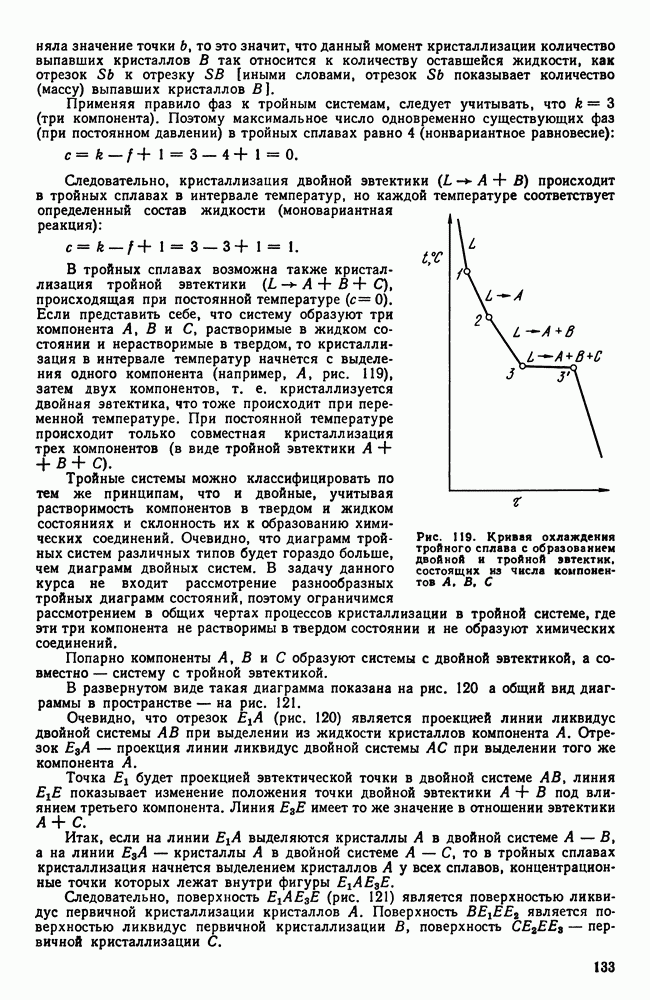
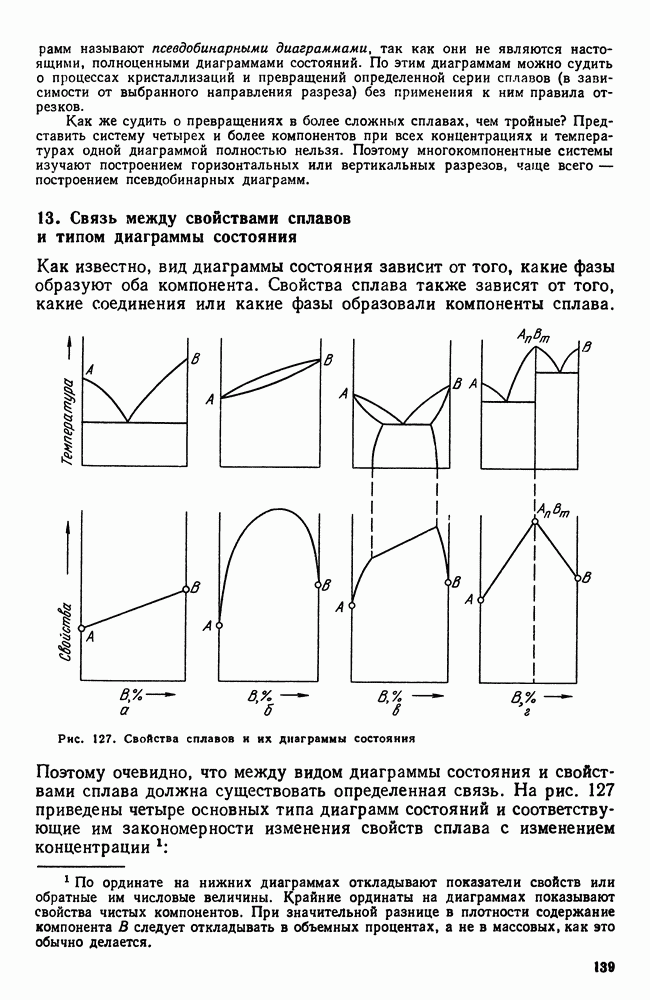
- 13. Связь между свойствами сплавов и типом диаграммы состояния
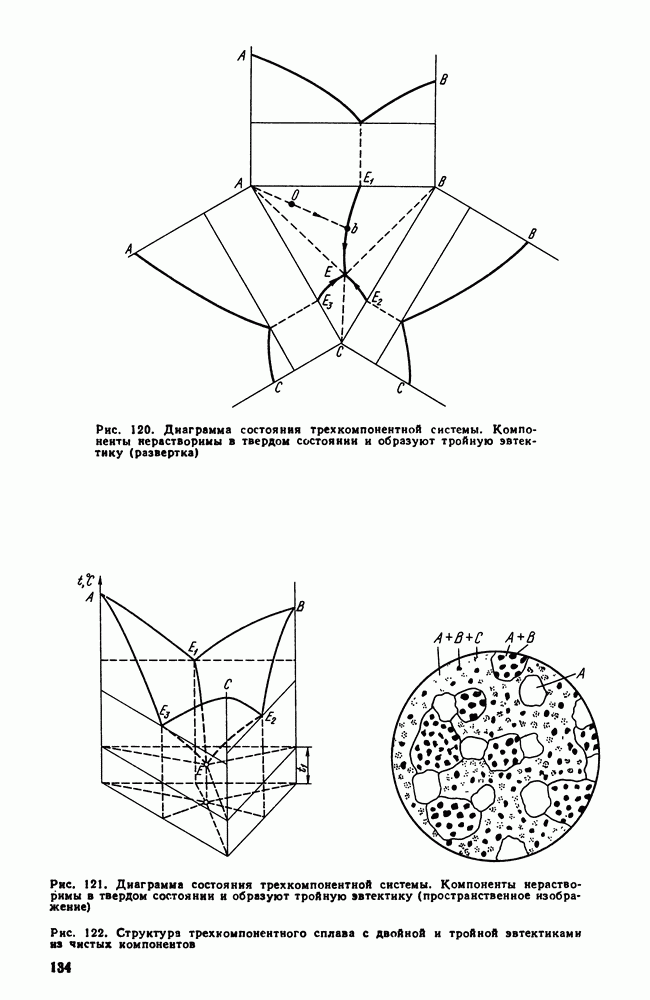
- Часть вторая. ЖЕЛЕЗОУГЛЕРОДИСТЫЕ СПЛАВЫ
- Глава VI. ДИАГРАММА ЖЕЛЕЗО—УГЛЕРОД
- 2. Железо
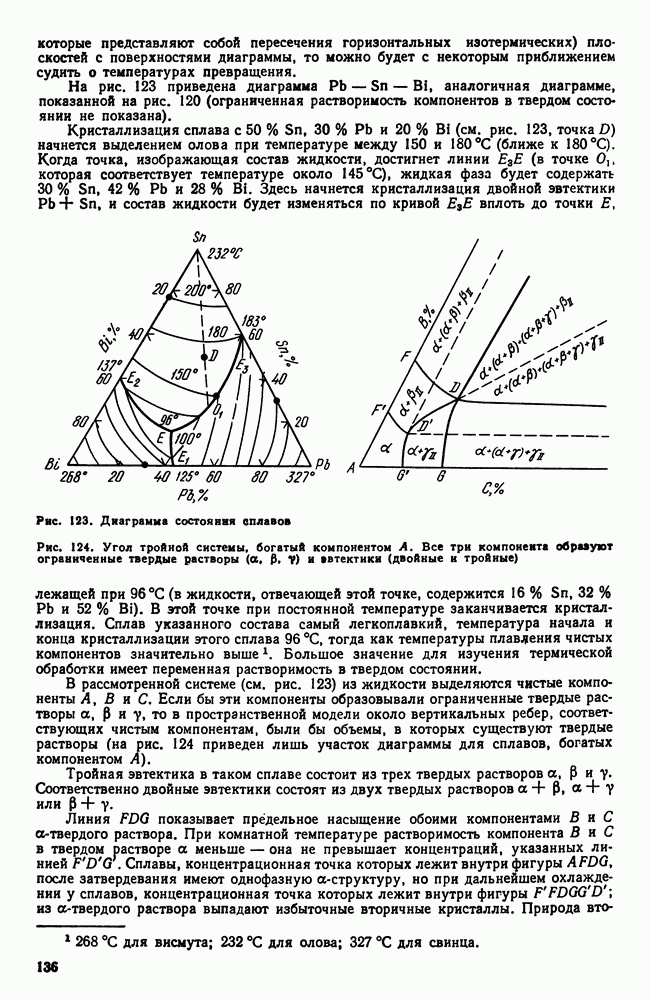
- 3. Цементит
- 4. Диаграмма состояния
- Глава VII. УГЛЕРОДИСТЫЕ СТАЛИ
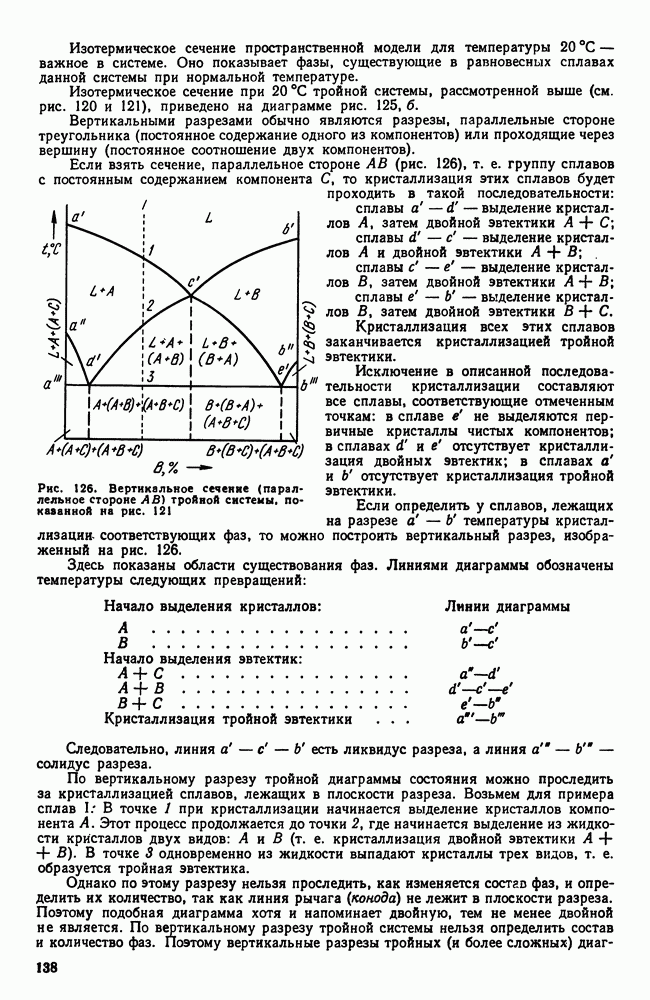
- 1. Влияние углерода на свойства стали
- 2. Влияние постоянных примесей на свойства стали
- 3. Сталь различных способов производства. Чистая сталь
- 4. Углеродистая сталь общего назначения
- 5. Нагартованная сталь
- 6. Листовая сталь для холодной штамповки
- 7. Обрабатываемость резанием. Автоматные стали
- Глава VIII. ЧУГУН
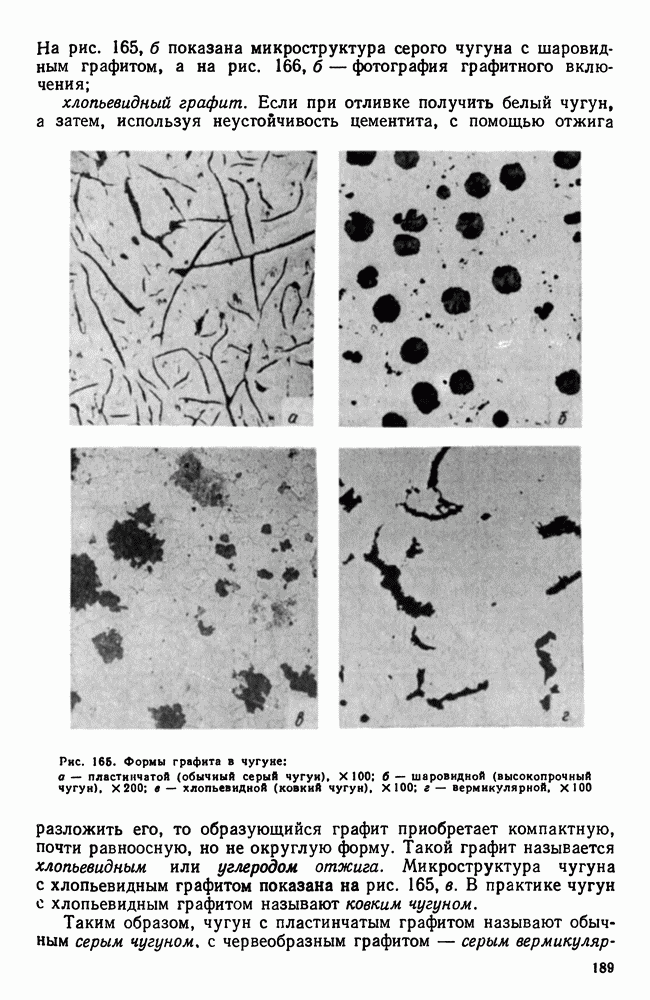
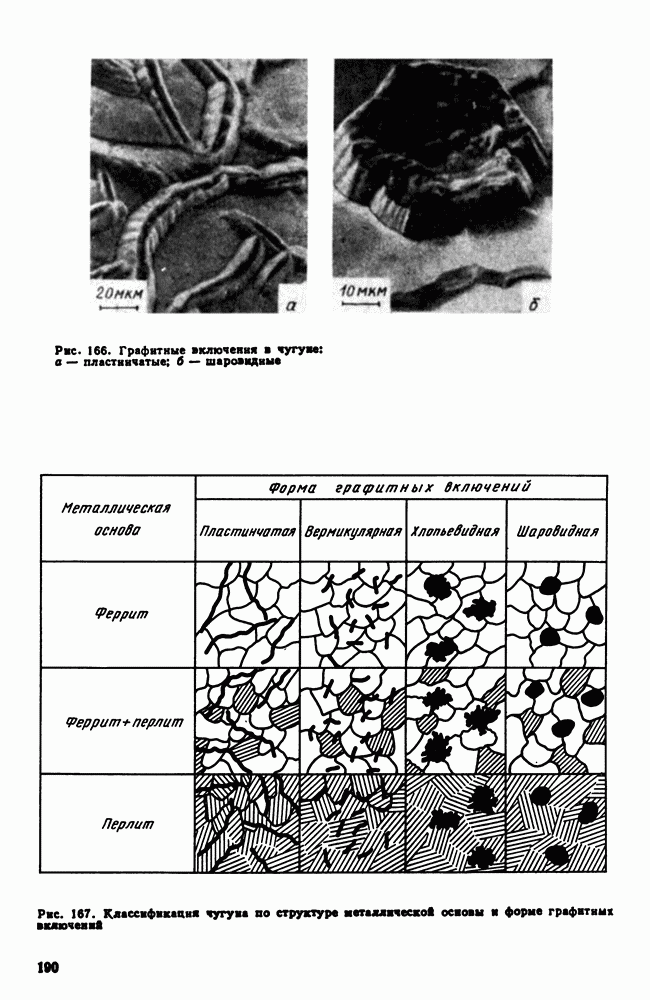
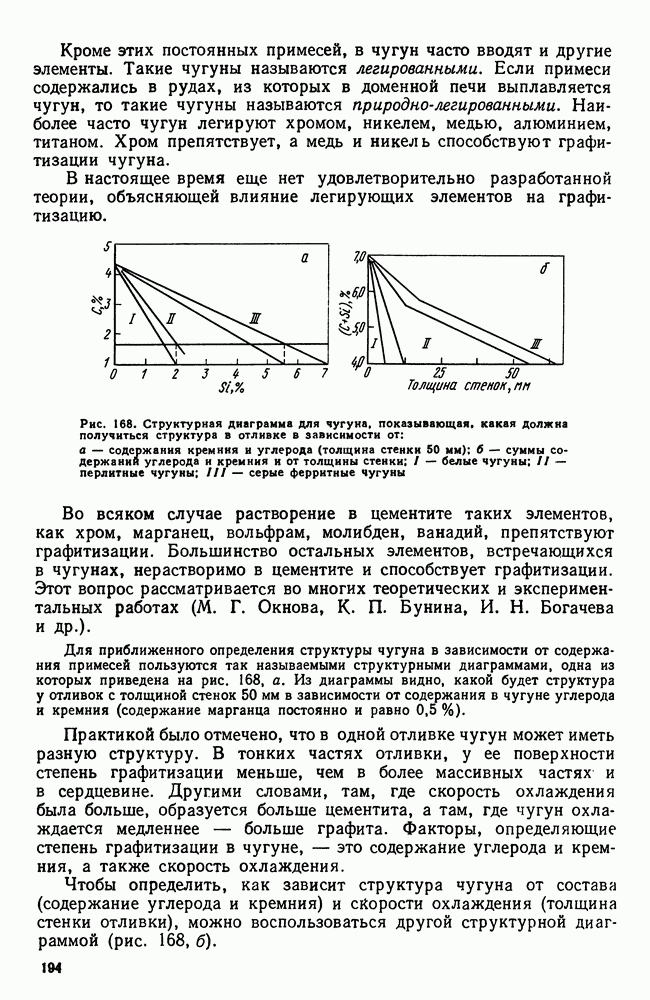
- 2. Структура чугуна. Формы графита
- 3. Структура и свойства чугуна
- 4. Примеси в чугуне
- 5. Марки серых и высокопрочных чугунов
- 6. Ковкий чугун
- Часть третья. ТЕРМИЧЕСКАЯ ОБРАБОТКА
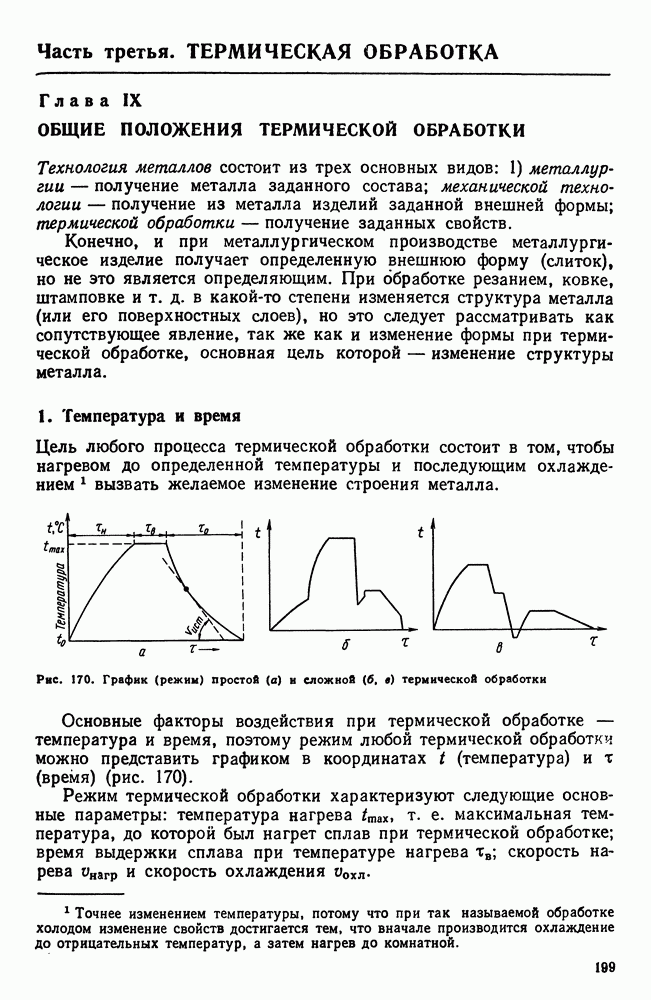
- Глава IX. ОБЩИЕ ПОЛОЖЕНИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ
- 2. Классификация видов термической обработки
- 3. Термическая обработка и диаграмма состояния
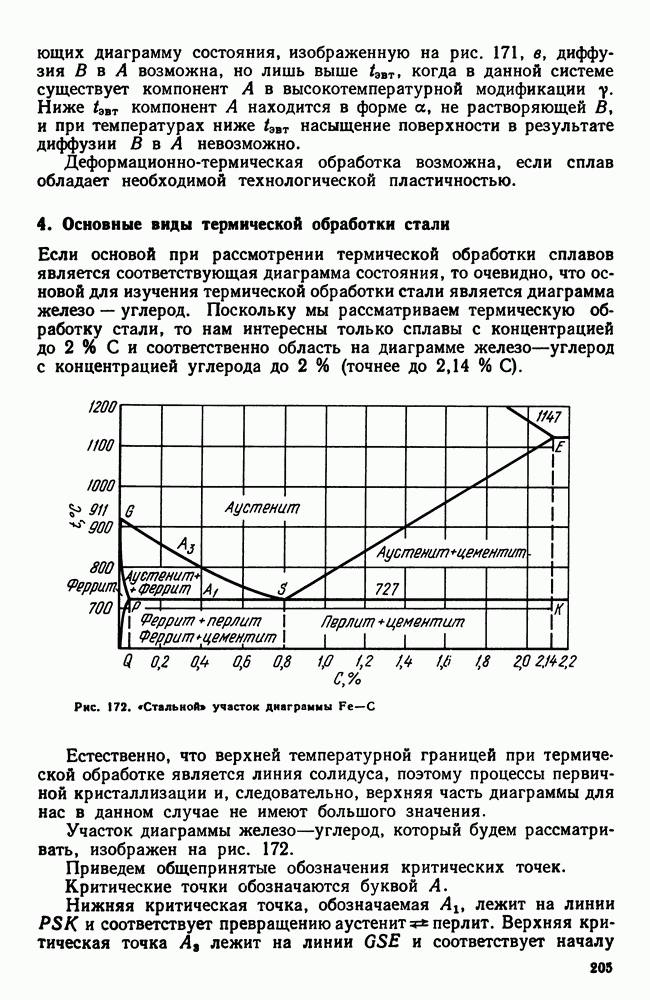
- 4 Основные виды термической обработки стали
- 5. Четыре основных превращения в стали
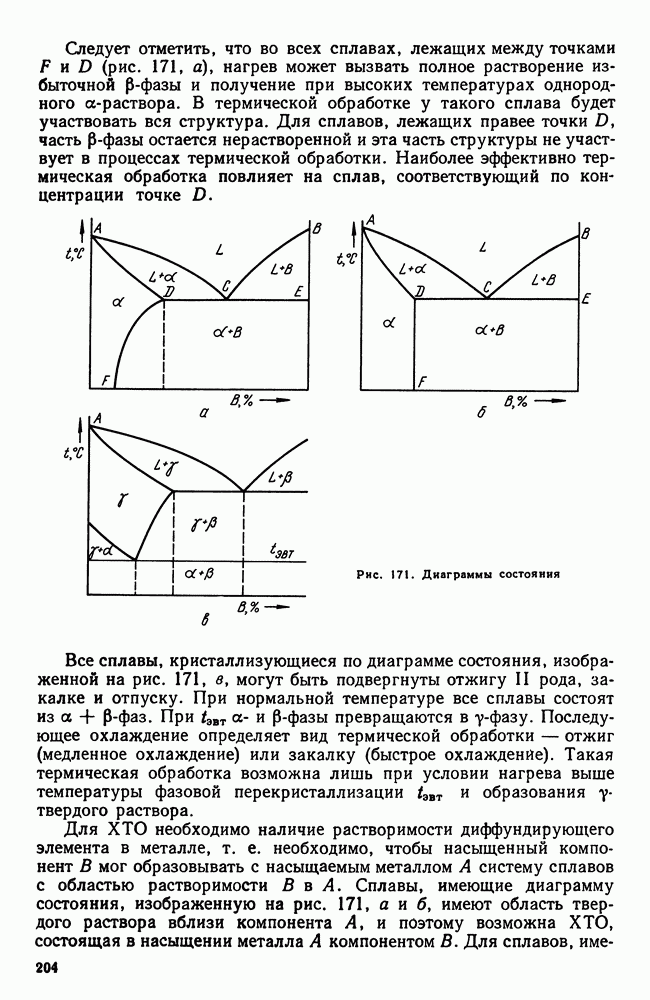
- Глава X. ТЕОРИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ
- 2. Рост аустенитного зерна
- 3. Распад аустенита
- 4. Мартенситное превращение
- 5. Бейнитное превращение
- 6. Превращения при отпуске
- 7. Влияние термической обработки на свойства стали
- 8. Термомеханическая обработка
- Глава XI. ПРАКТИКА ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ
- 2. Время нагрева
- 3. Химическое воздействие нагревающей среды
- 4. Закалочные среды
- 5. Прокаливаемость
- 6. Внутренние напряжения
- 7. Способы закалки
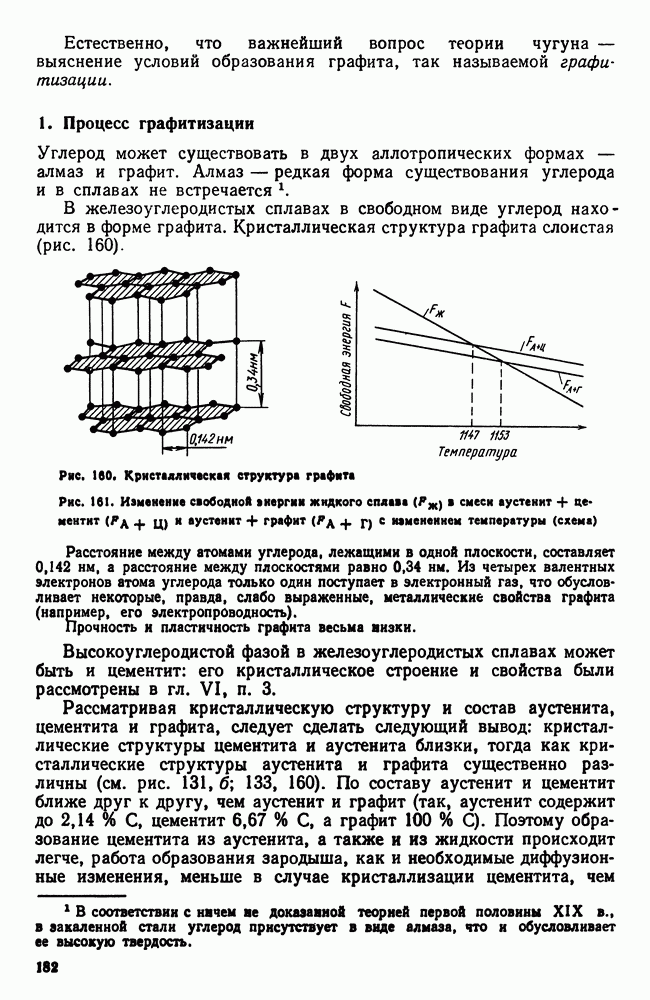
- 8. Обработка стали холодом
- 9. Дефекты, возникающие при закалке
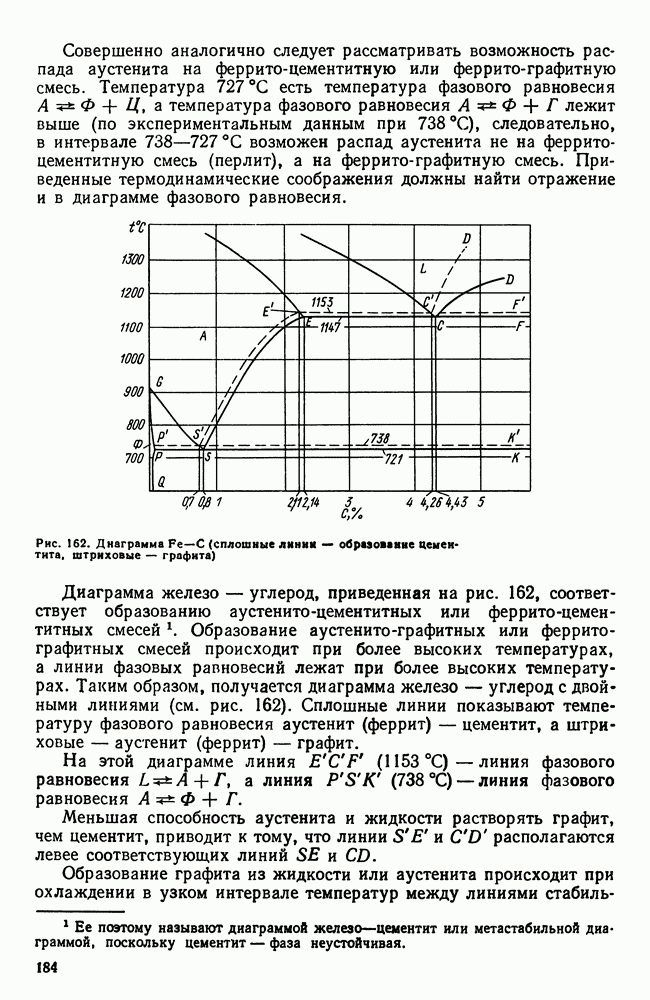
- 10. Отжиг и нормализация
- Глава XII. ПОВЕРХНОСТНАЯ ЗАКАЛКА СТАЛИ
- 2. Высокочастотная закалка
- Глава XIII. ХИМИКО-ТЕРМИЧЕСКАЯ ОБРАБОТКА СТАЛИ
- 2. Цементация стали
- 3. Азотирование стали
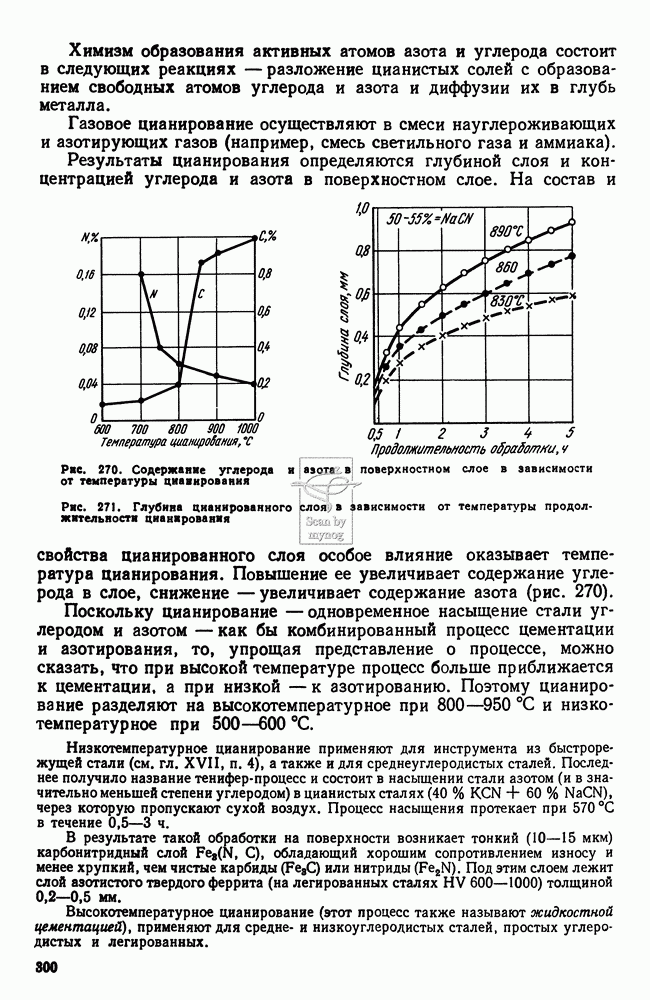
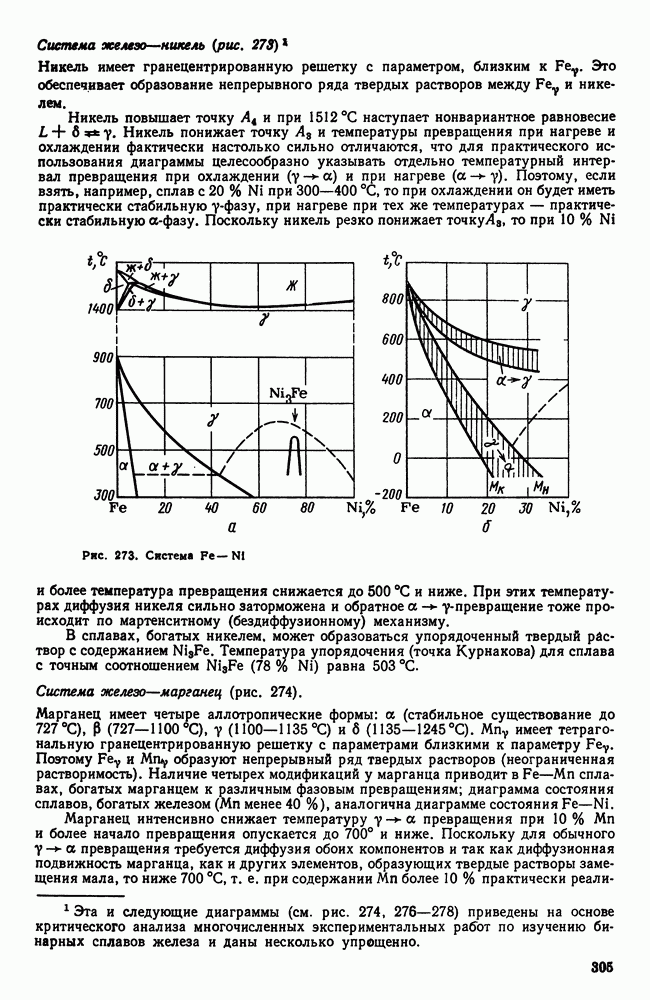
- 4. Цианирование стали
- 5. Диффузионная металлизация
- Часть четвертая. ЛЕГИРОВАННЫЕ СТАЛИ И СПЛАВЫ
- Глава XIV. ВЛИЯНИЕ ЛЕГИРУЮЩИХ ЭЛЕМЕНТОВ
- 2. Влияние элементов на полиморфизм железа
- 3. Распределение легирующих элементов в стали
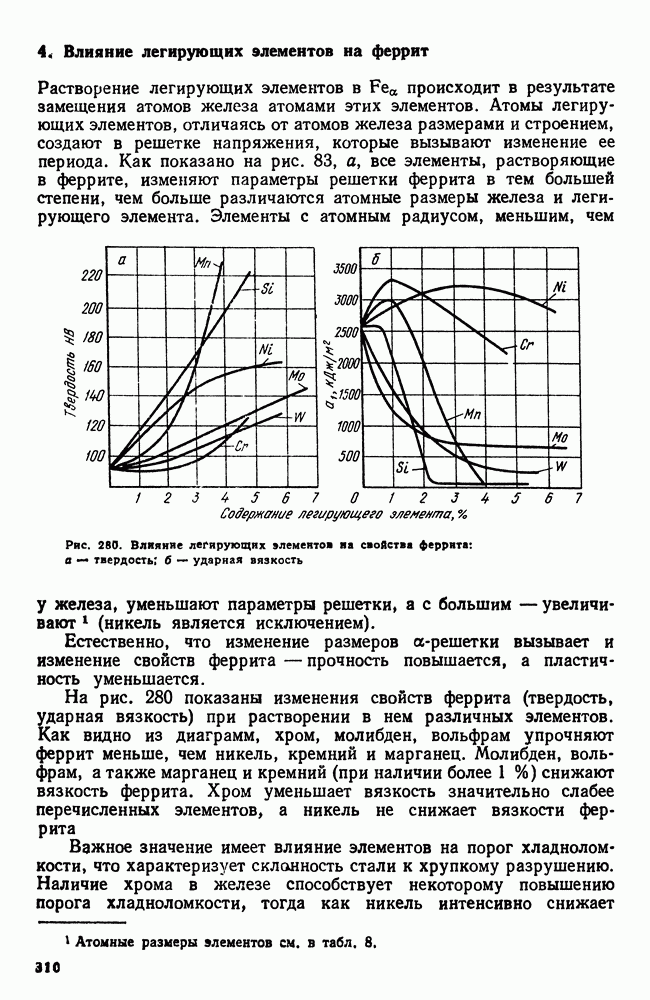
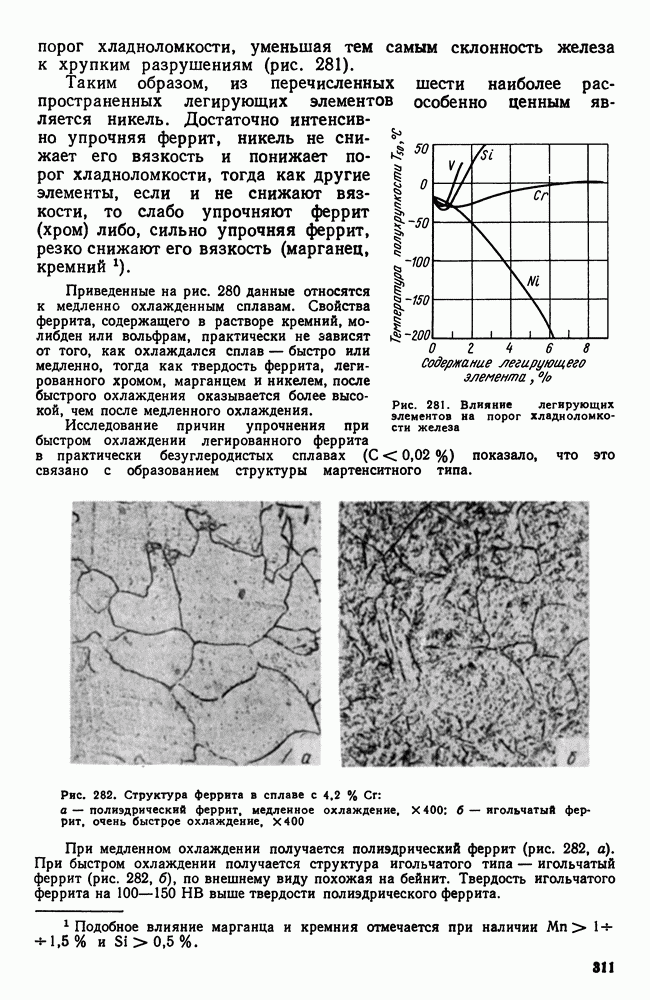
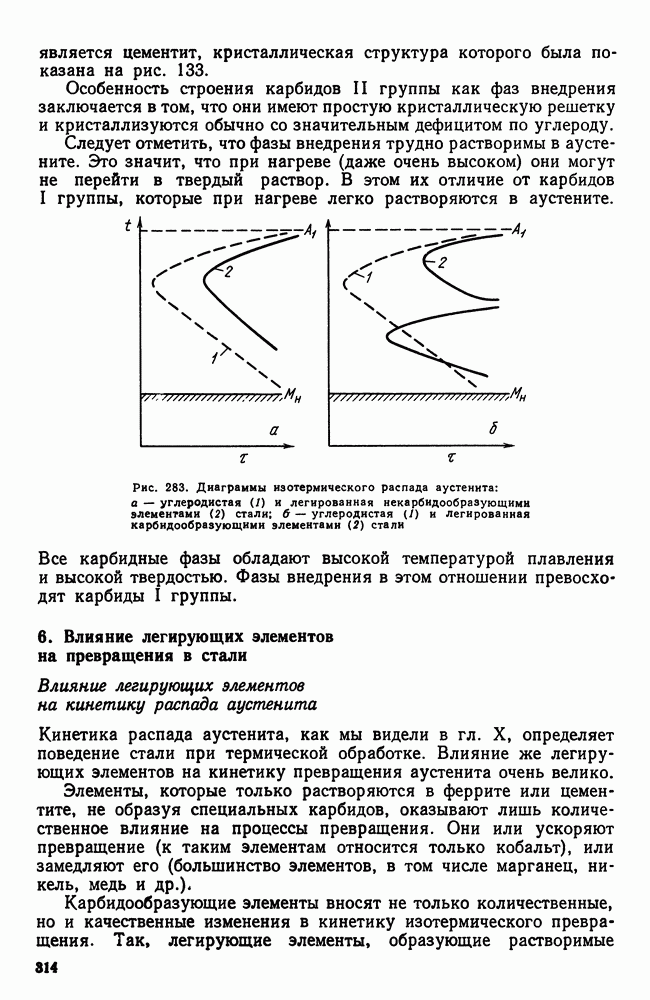
- 4. Влияние легирующих элементов на феррит
- 5. Карбидная фаза в легированных сталях
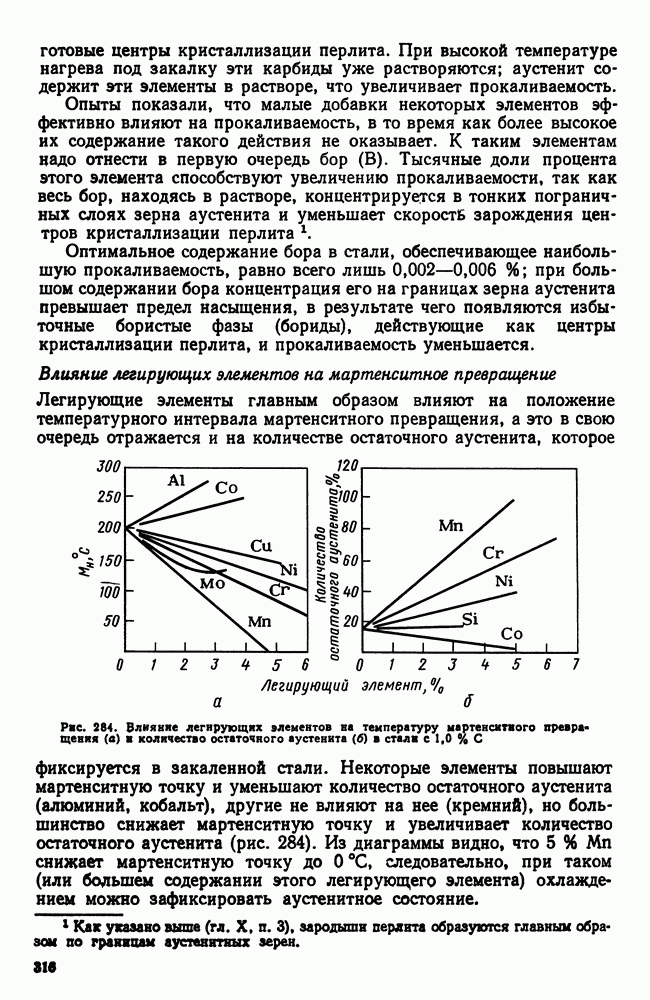
- 6. Влияние легирующих элементов на превращения в стали
- Глава XV. КЛАССИФИКАЦИЯ И МАРКИРОВКА ЛЕГИРОВАННЫХ СТАЛЕЙ
- 2. Маркировка легированных сталей
- Глава XVI. КОНСТРУКЦИОННЫЕ СТАЛИ
- 1. Механические свойства стали, влияние структуры и легирующих элементов
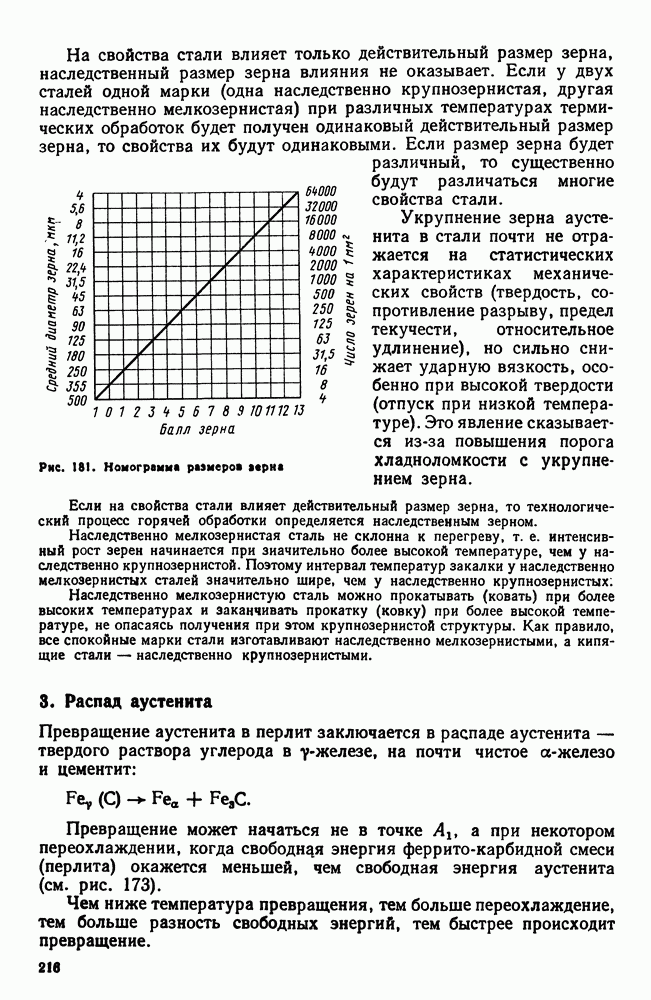
- 2. Термическая обработка конструкционных сталей
- 3. Цементуемые (низкоуглеродистые) стали
- 4. Улучшаемые (среднеуглеродистые) стали
- 5. Высокопрочные стали
- 6. Свариваемость стали
- 7. Строительная сталь
- 8. Арматурная сталь
- 9. Пружинная сталь
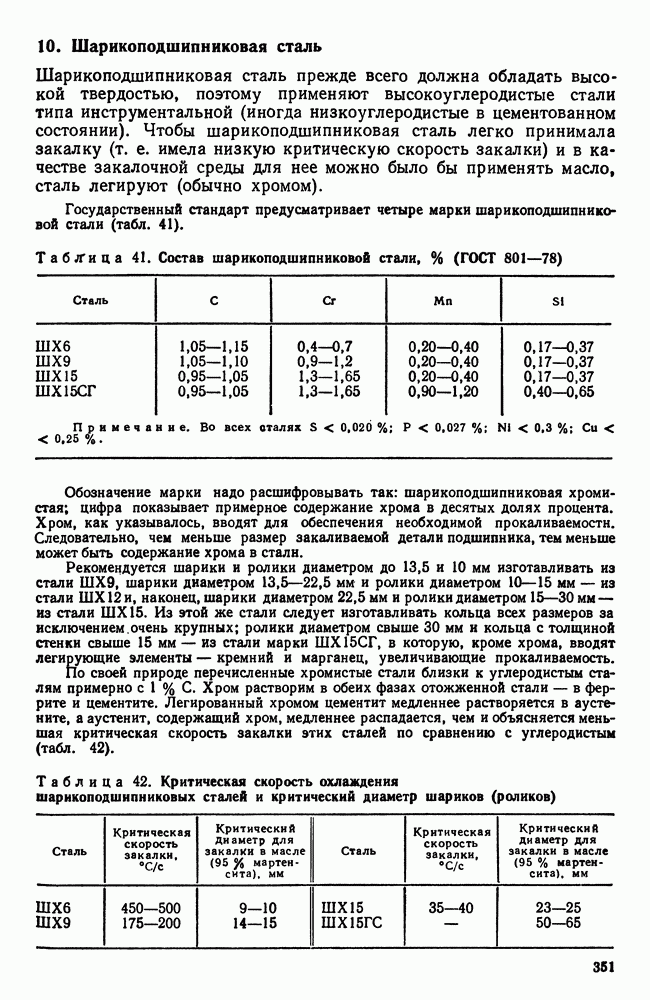
- 10. Шарикоподшипниковая сталь
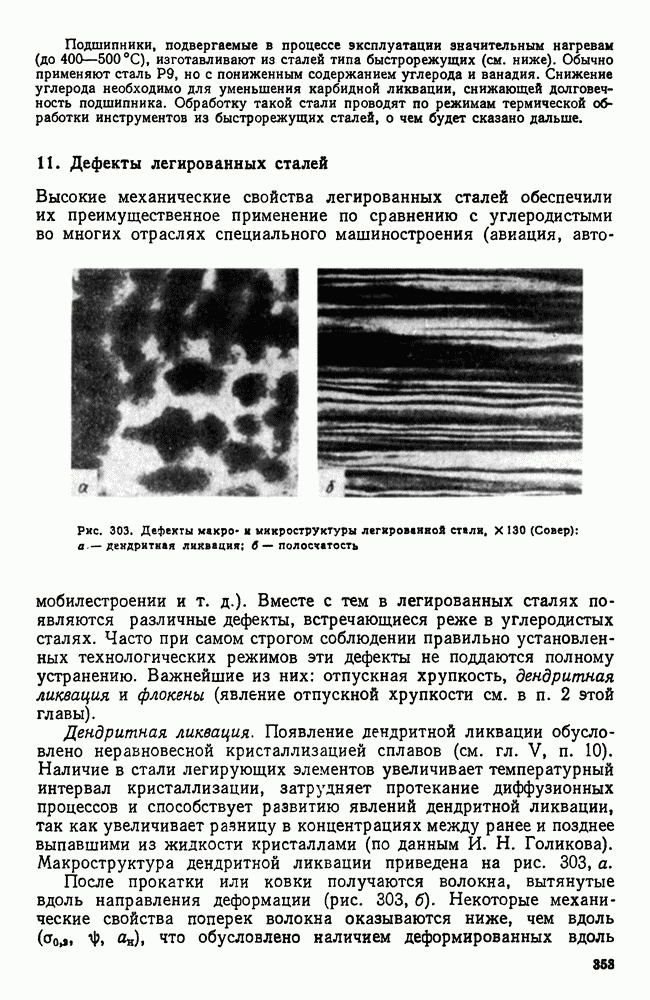
- 11. Дефекты легированных сталей
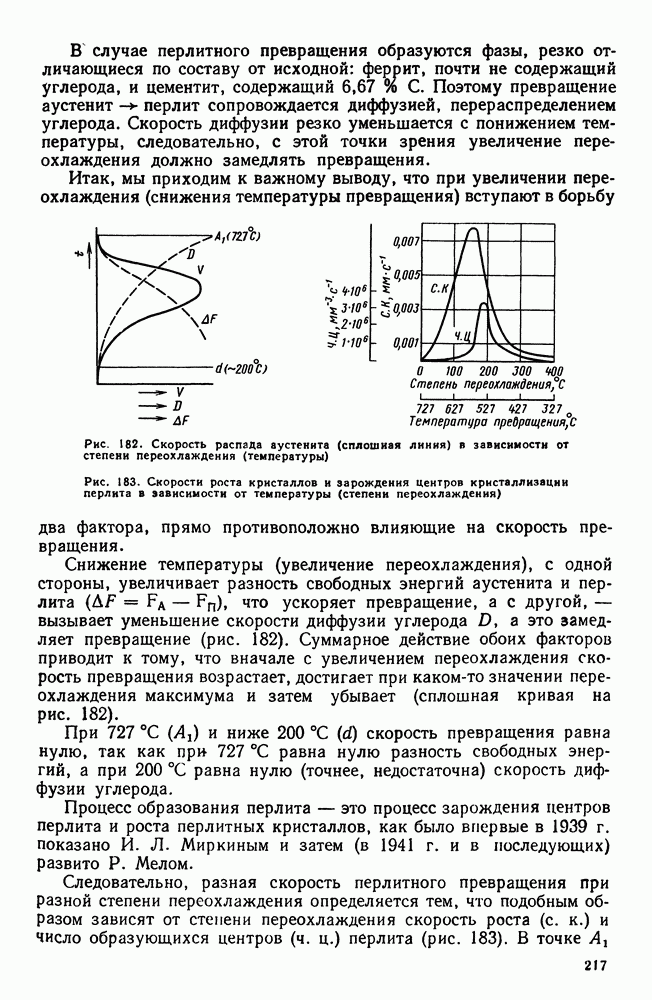
- Глава XVII. ИНСТРУМЕНТАЛЬНЫЕ СТАЛИ
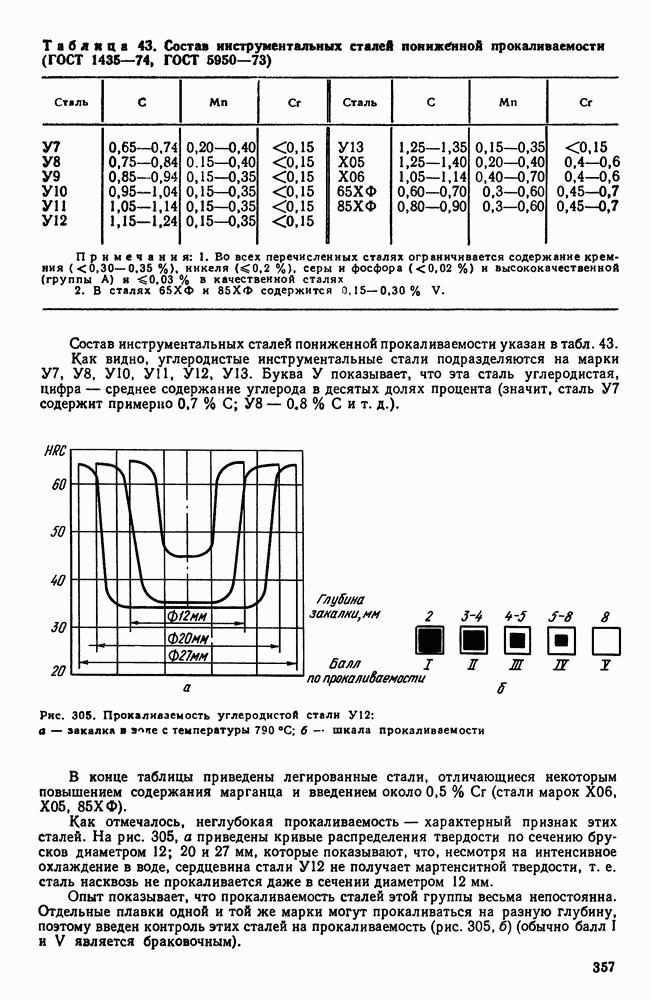
- 2. Инструментальные стали пониженной прокаливаемости
- 3. Инструментальные стали повышенной прокаливаемости (легированные инструментальные стали)
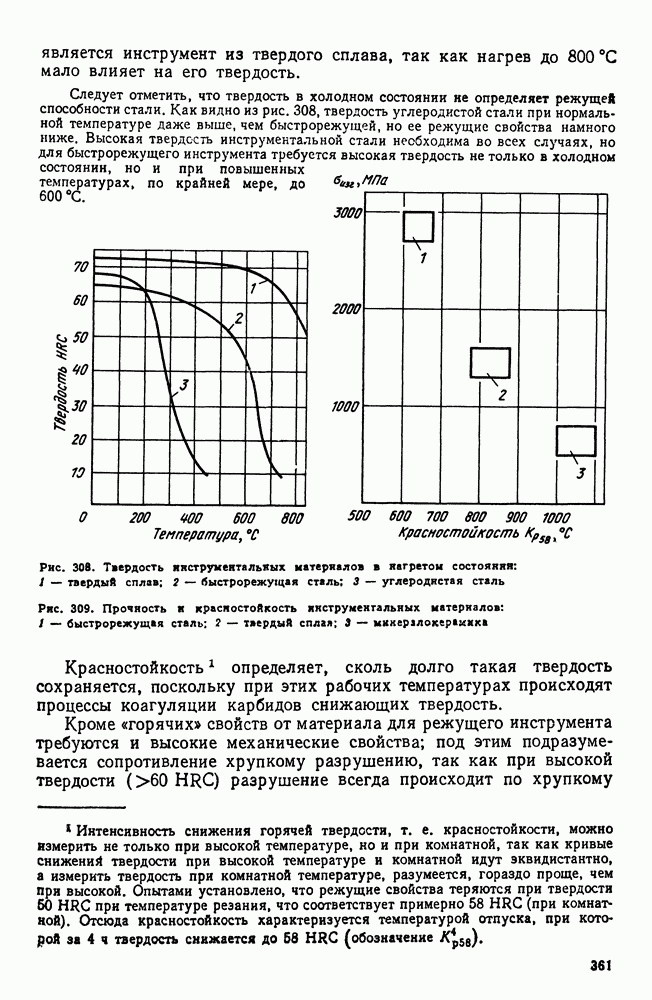
- 4. Быстрорежущие стали
- 5. Штамповые стали
- 6. Твердые сплавы
- Глава XVIII. ЖАРОСТОЙКИЕ И ЖАРОПРОЧНЫЕ СТАЛИ И СПЛАВЫ
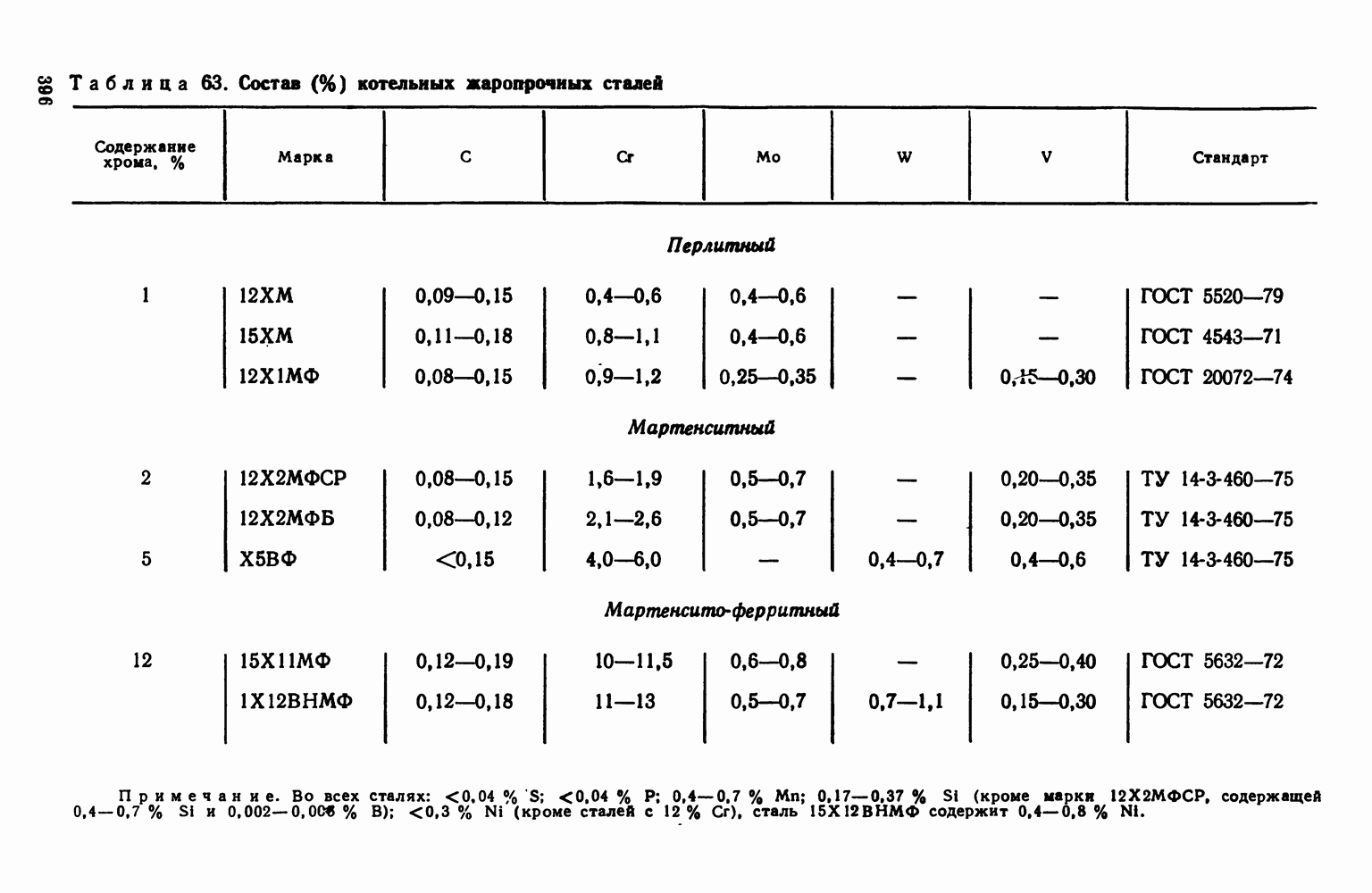
- 2. Жаропрочность
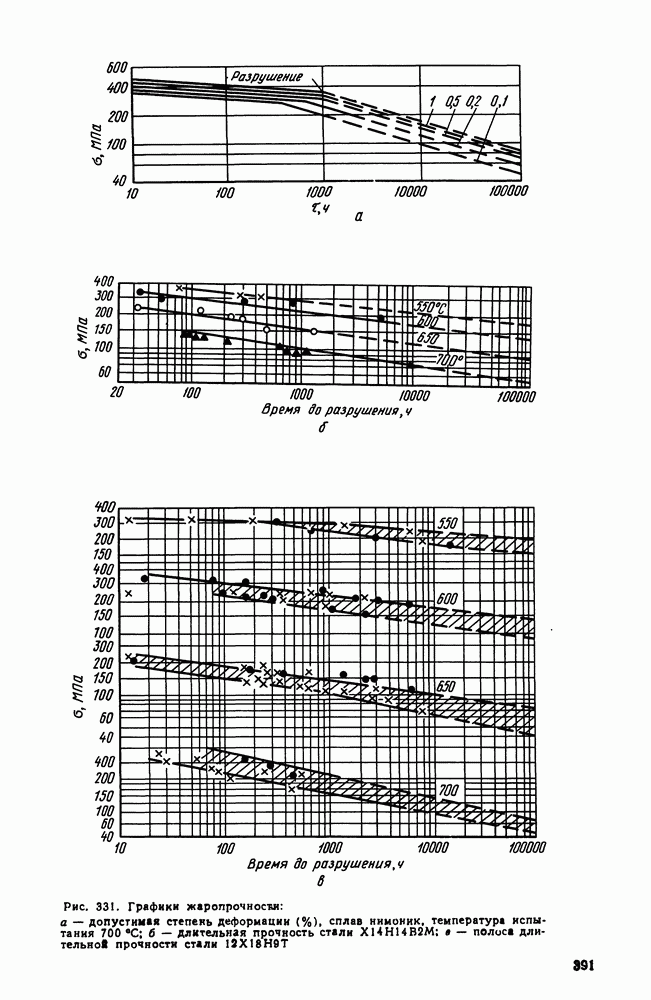
- 3. Оценка жаропрочных свойств
- 4. Влияние структуры и состава на жаропрочность
- 5. Классификация жаропрочных материалов
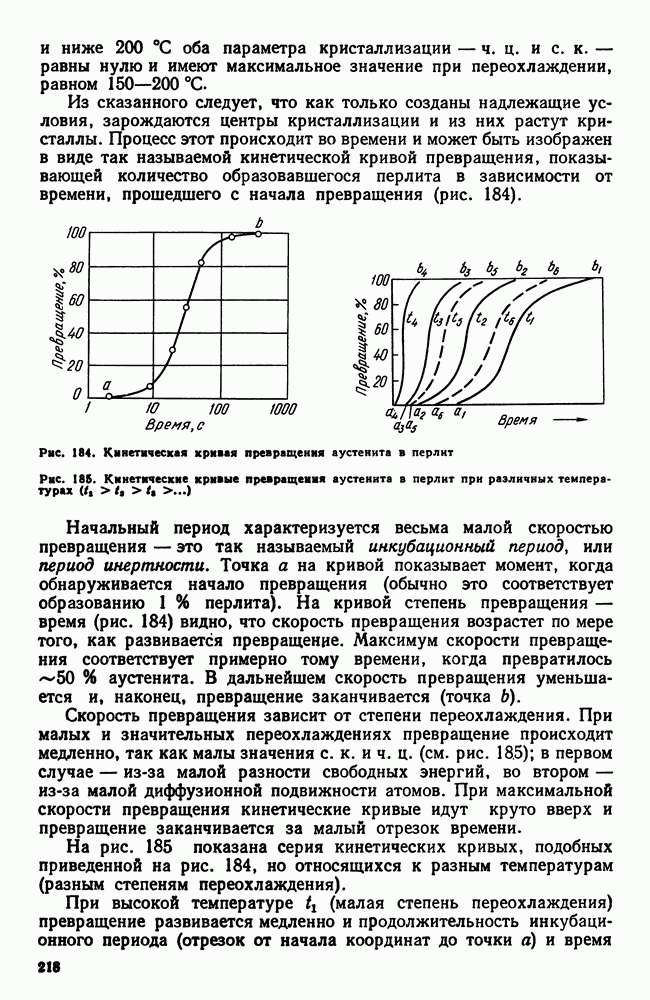
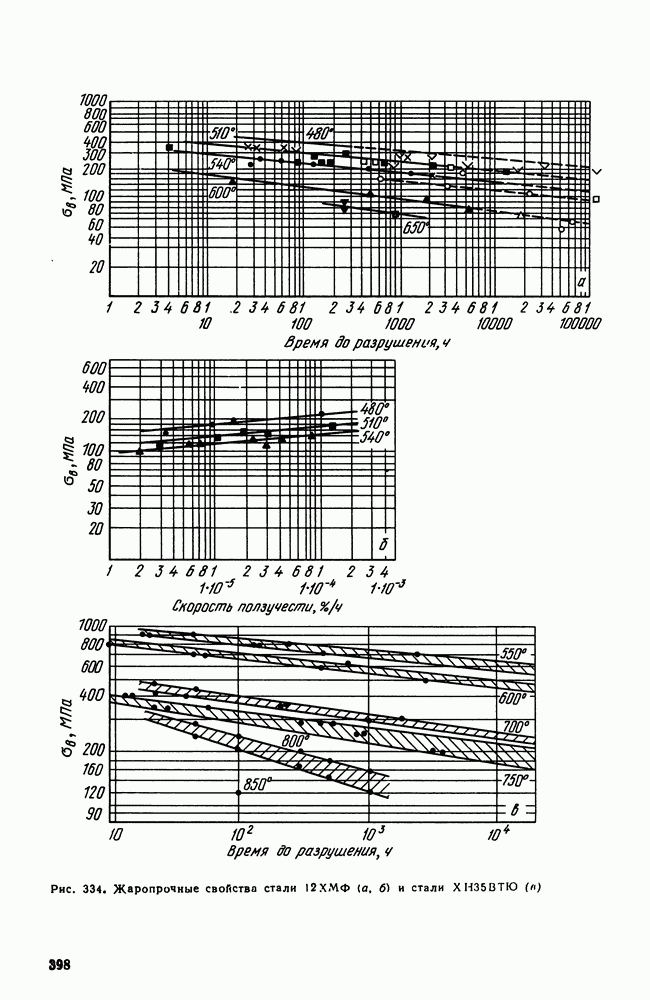
- 6. Перлитные и мартенситные жаропрочные стали
- 7. Аустенитные жаропрочные стали
- 8. Никелевые и кобальтовые жаропрочные сплавы
- Глава XIX. КОРРОЗИОННОСТОЙКИЕ (НЕРЖАВЕЮЩИЕ) СТАЛИ И СПЛАВЫ
- 2. Хромоникелевые нержавеющие стали
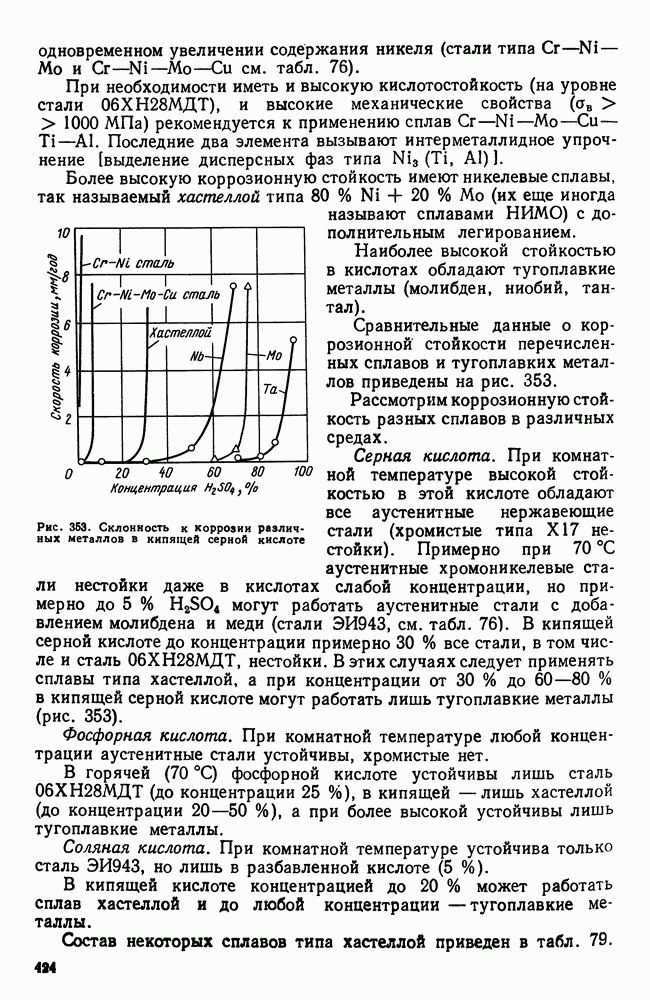
- 3. Кислотостойкие стали и сплавы
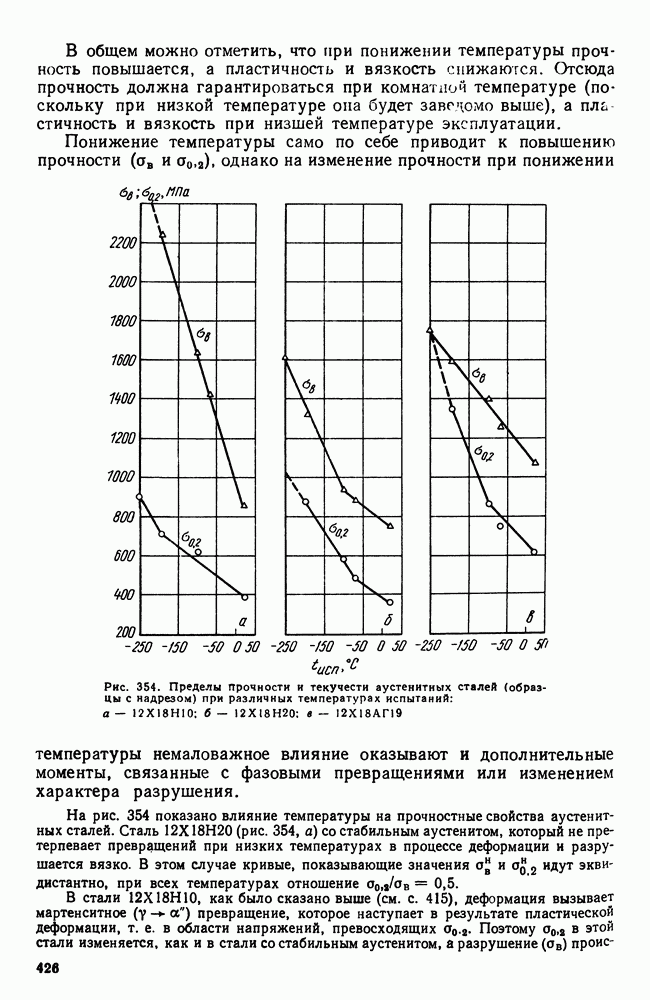
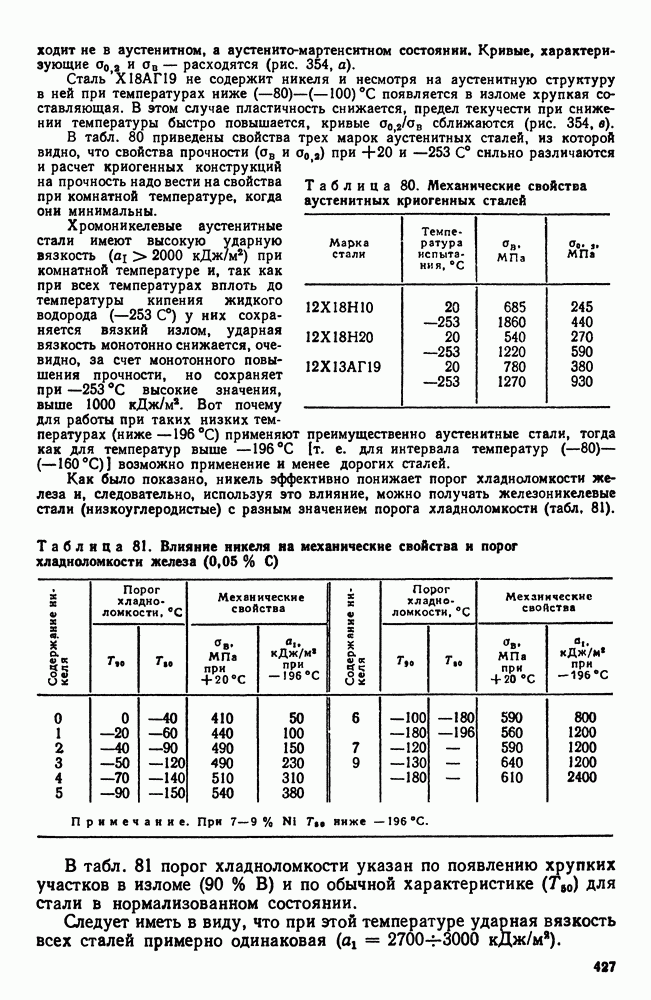
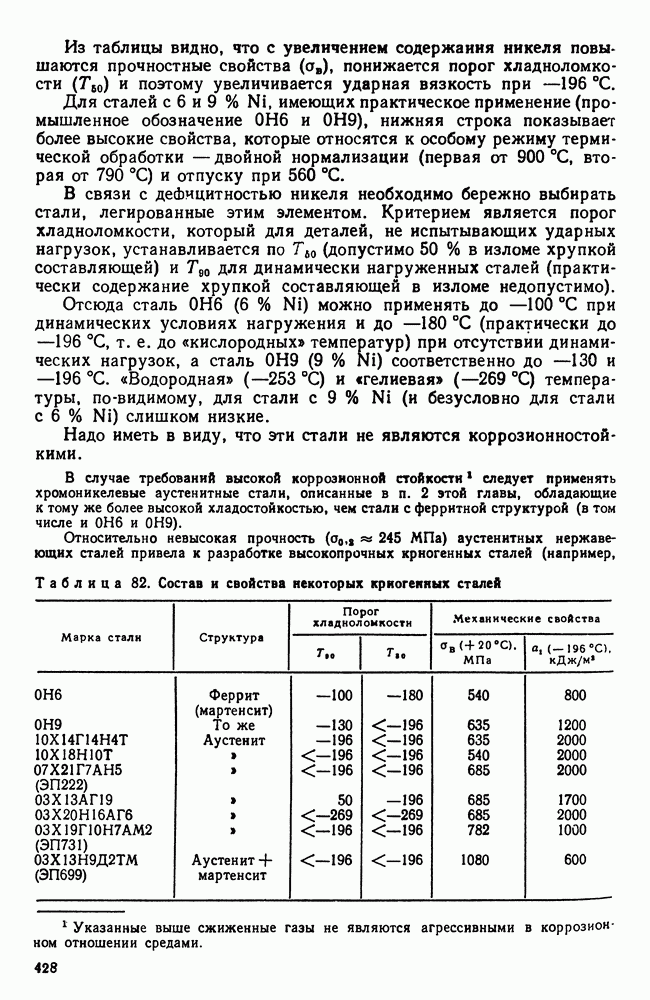
- 4. Криогенные стали и сплавы
- Глава XX. ИЗНОСОСТОЙКИЕ СТАЛИ И СПЛАВЫ
- 2. Графитизированная сталь
- 3. Высокомарганцовистая сталь
- 4. Наплавочные материалы
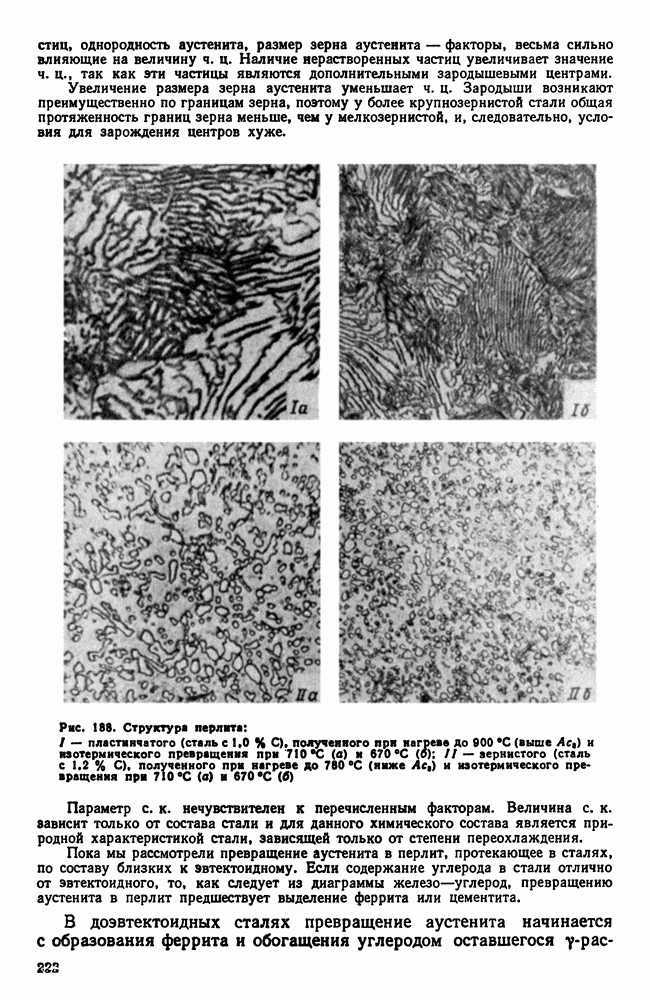
- Глава XXI. ТИТАН И ЕГО СПЛАВЫ
- 2. Легирование титана
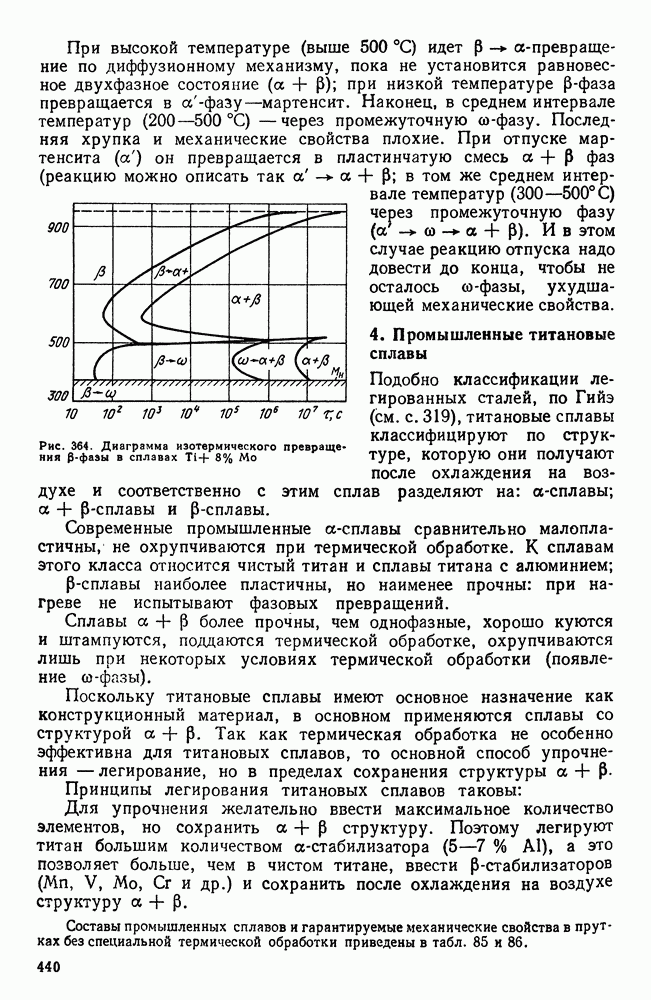
- 3. Фазовые превращения в титановых сплавах
- 5. Термическая обработка титановых сплавов
- 6. Примеси в титановых сплавах
- 7. Коррозионная стойкость титана
- Глава XXII. ТУГОПЛАВКИЕ МЕТАЛЛЫ
- 2. Взаимодействие тугоплавких металлов с другими элементами и между собой
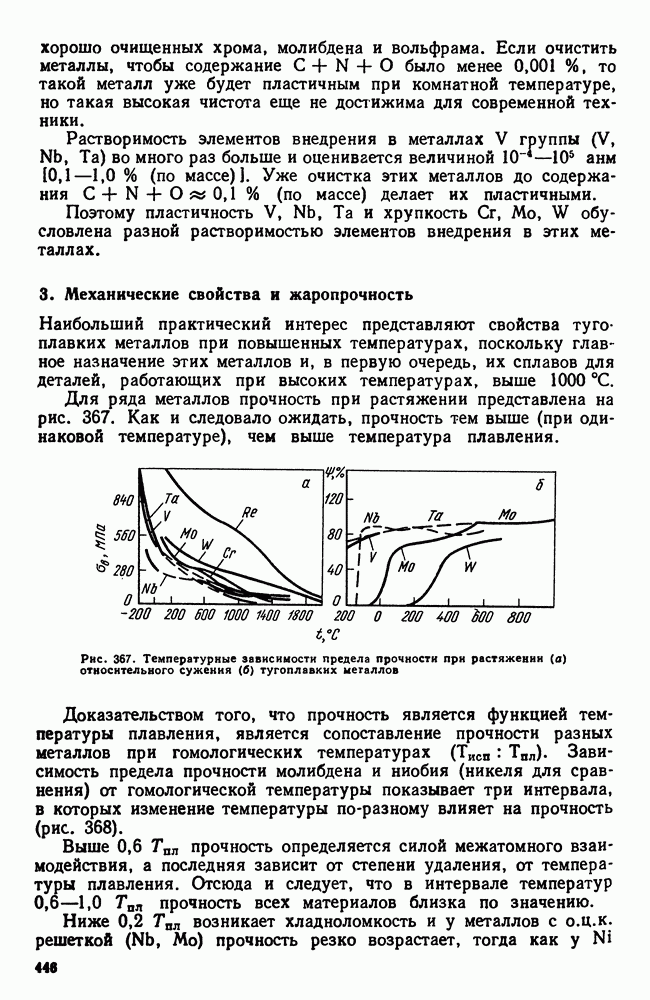
- 3. Механические свойства и жаропрочность
- 4. Хладноломкость тугоплавких металлов
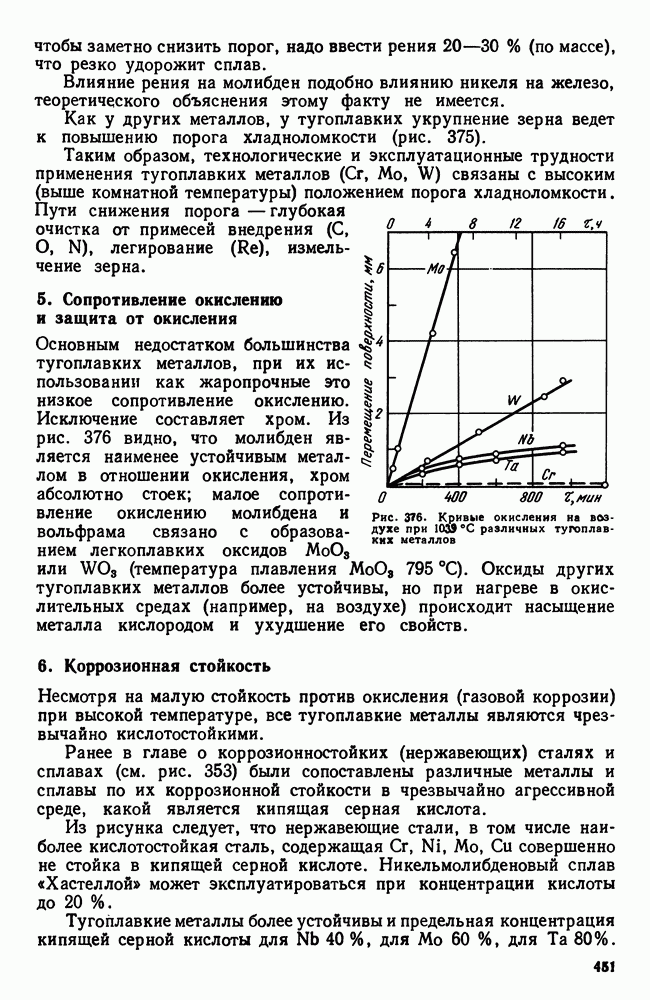
- 5. Сопротивление окислению и защита от окисления
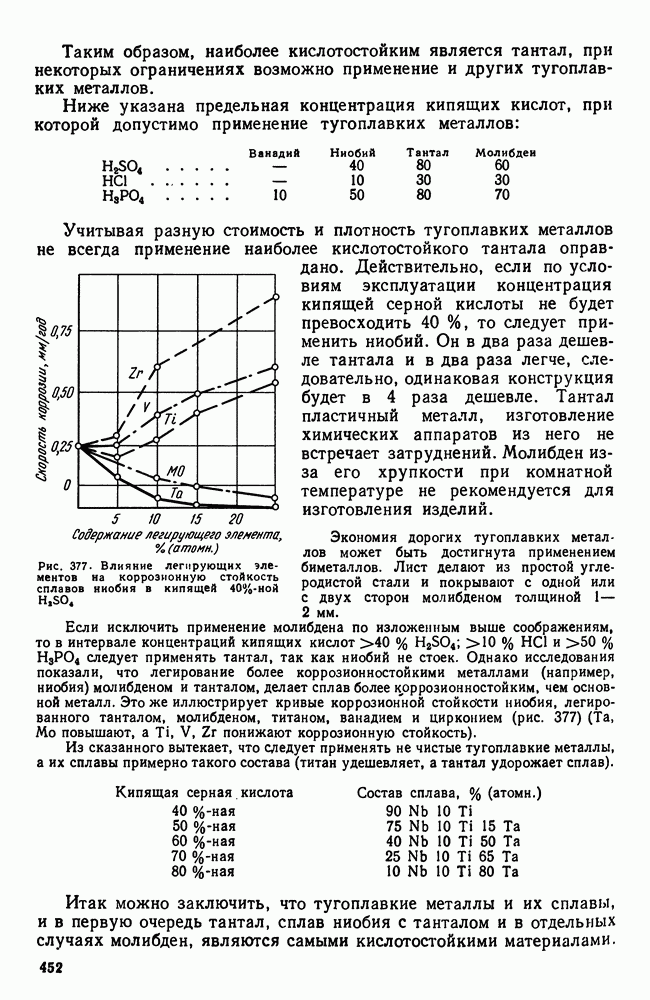
- 6. Коррозионная стойкость
- Глава XXIII. СПЛАВЫ С ОСОБЫМИ ТЕПЛОВЫМИ И УПРУГИМИ СВОЙСТВАМИ
- 2. Сплавы с постоянным модулем упругости
- Глава XXIV. МАГНИТНЫЕ СТАЛИ И СПЛАВЫ
- 2. Стали и сплавы для постоянных магнитов (магнитнотвердые сплавы)
- 3. Магнитномягкие сплавы
- 4. Немагнитные стали
- 5. Электротехнические сплавы
- Глава XXV. СПЛАВЫ АТОМНОЙ ЭНЕРГЕТИКИ
- 2. Конструкционные материалы. Теплоносители
- 3. Ядерное горючее (уран, плутоний, торий)
- Часть пятая. Цветные металлы и сплавы
- Глава XXVI. ЛЕГКИЕ МЕТАЛЛЫ И ИХ СПЛАВЫ
- 1. Свойства алюминия
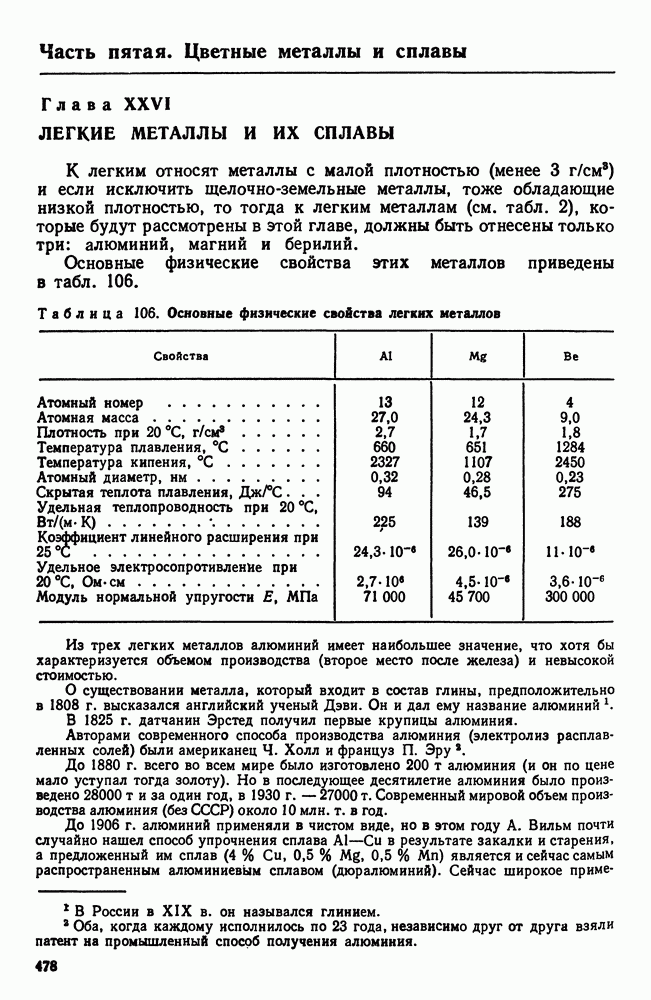
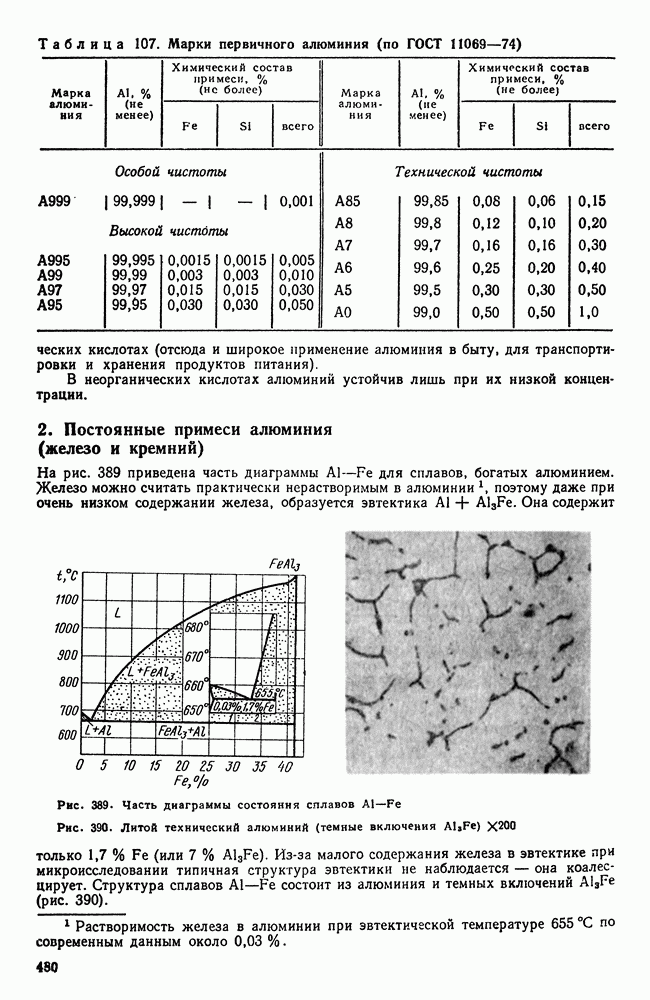
- 2. Постоянные примеси алюминия (железо и кремний)
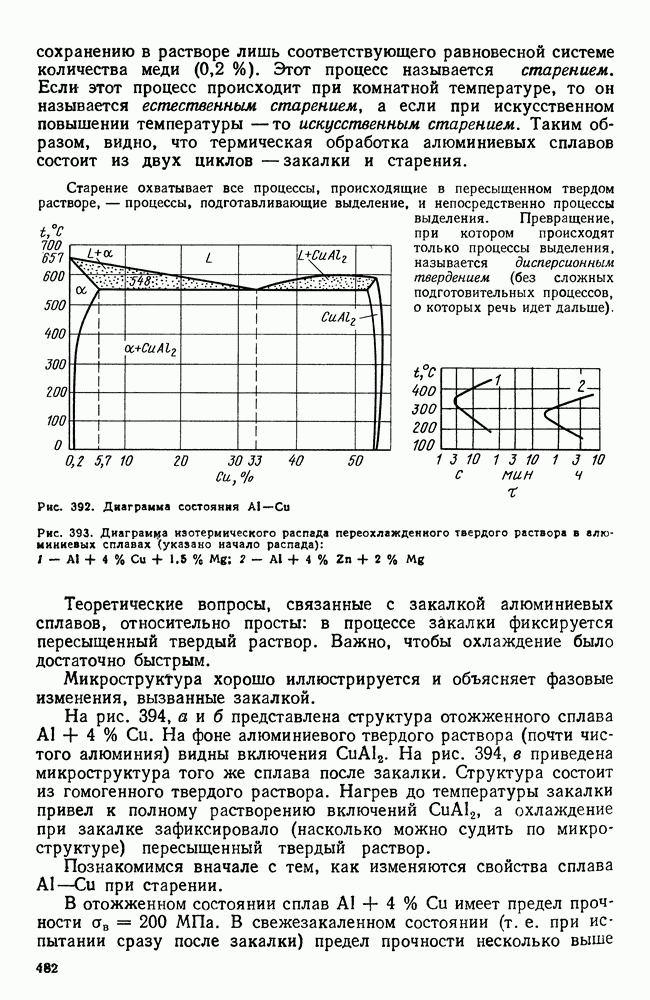
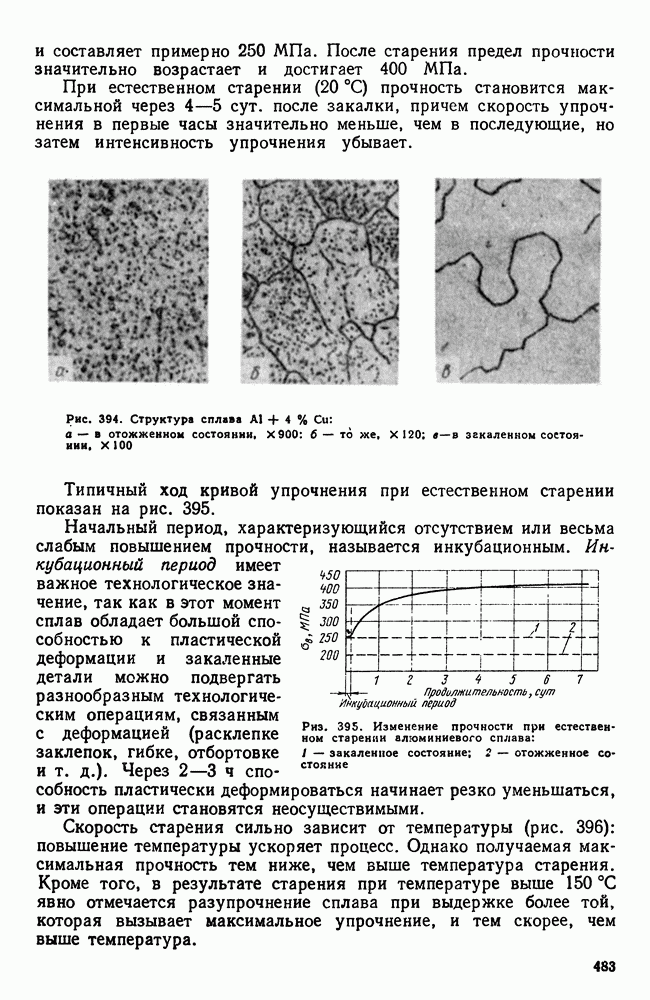
- 3. Термическая обработка сплавов Al-Cu
- 4. Влияние состава алюминиевых сплавов на процессы, происходящие при термической обработке
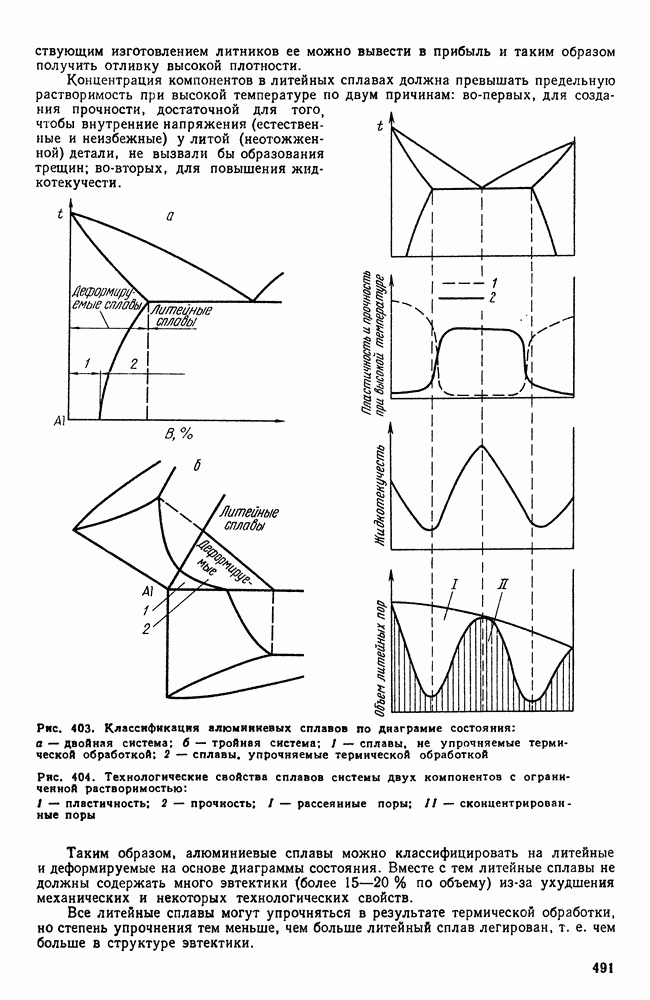
- 5. Классификация алюминиевых сплавов
- 6. Деформируемые сплавы, не упрочняемые термической обработкой
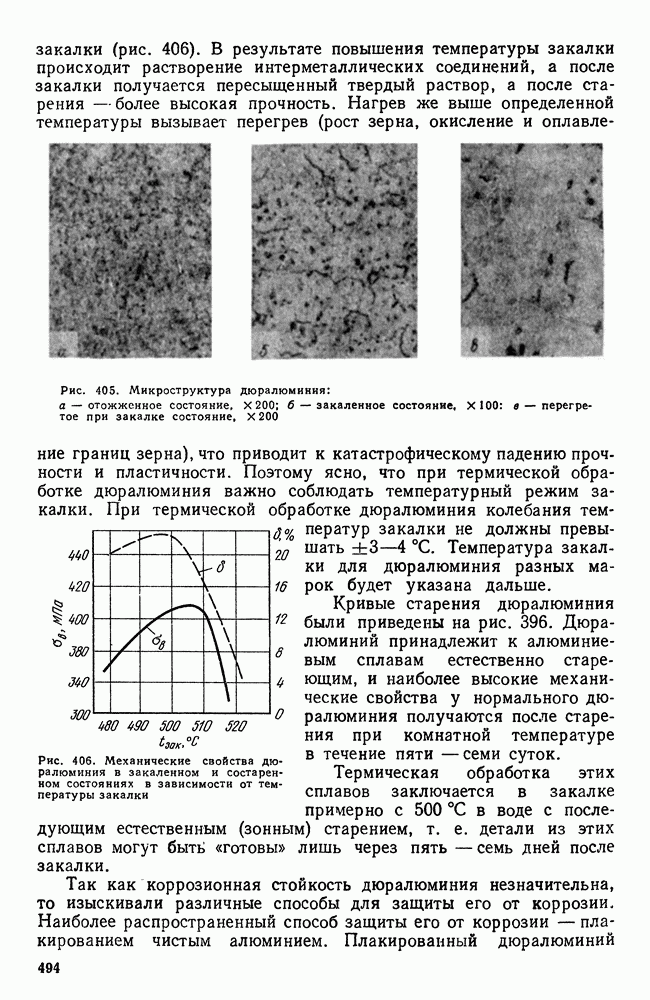
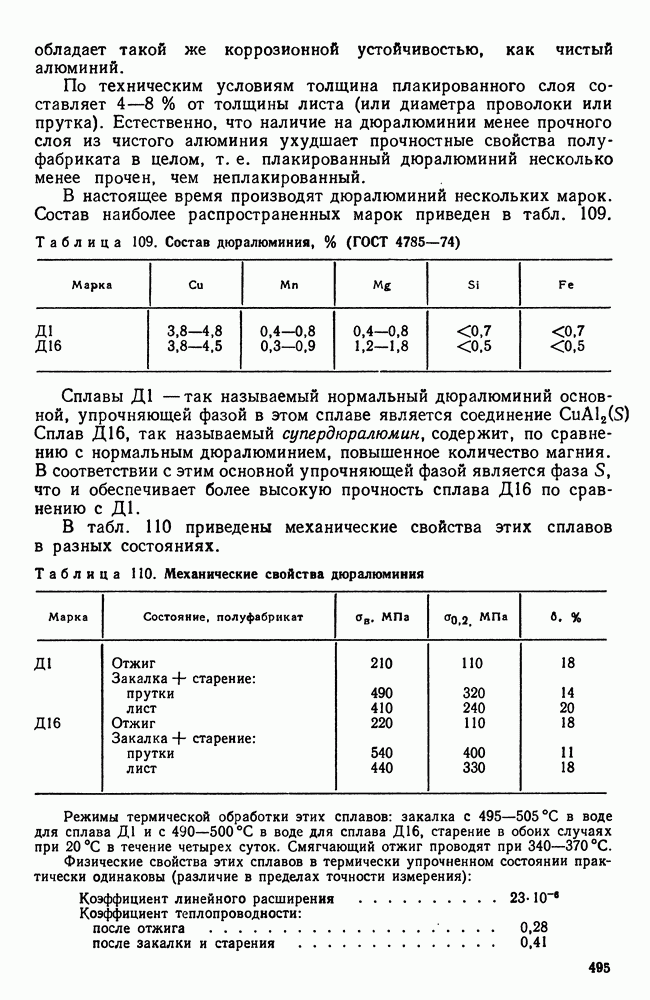
- 7. Дюралюминий и другие деформируемые сплавы, упрочняемые термической обработкой
- 8. Алюминиевые сплавы для поковок и штамповок
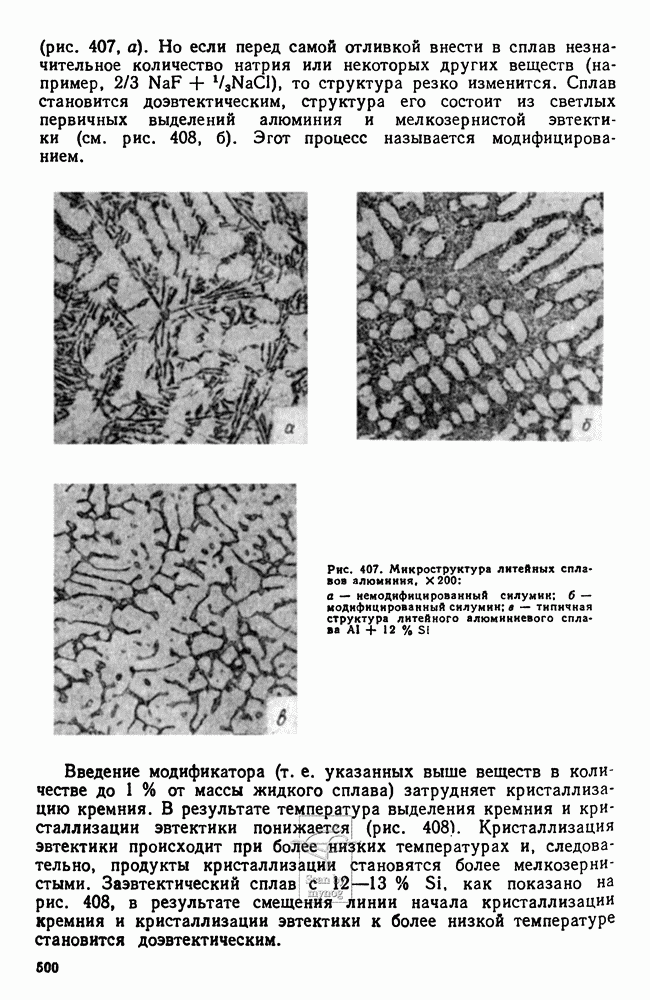
- 9. Силумины и другие алюминиевые сплавы для фасонного литья
- 10. Жаропрочные алюминиевые сплавы
- 11. Магний
- 12. Сплавы магния
- 13. Бериллий
- 14. Сплавы бериллия
- Глава XXVII. МЕДЬ И ЕЕ СПЛАВЫ
- 2. Сплавы меди с цинком (латуни)
- 3. Сплавы меди с оловом (оловянистые бронзы)
- 4. Сплавы меди с алюминием, кремнием, бериллием и другими элементами
- ГЛАВА XXVIII. ПОДШИПНИКОВЫЕ СПЛАВЫ И ПРИПОИ
- 2. Легкоплавкие подшипниковые сплавы (баббиты)
- 3. Припои
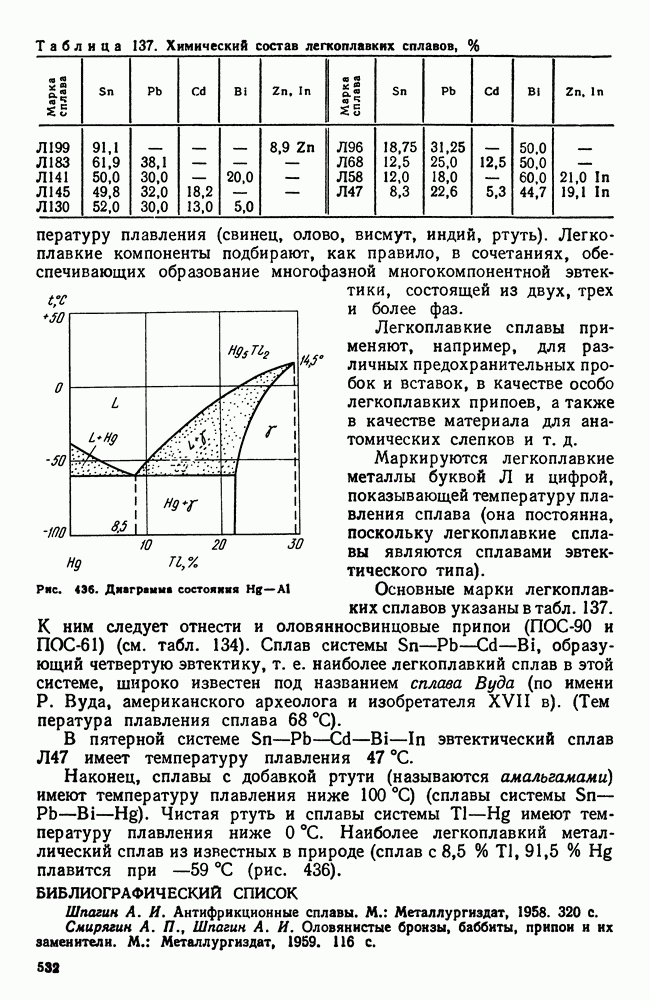
- 4. Легкоплавкие сплавы
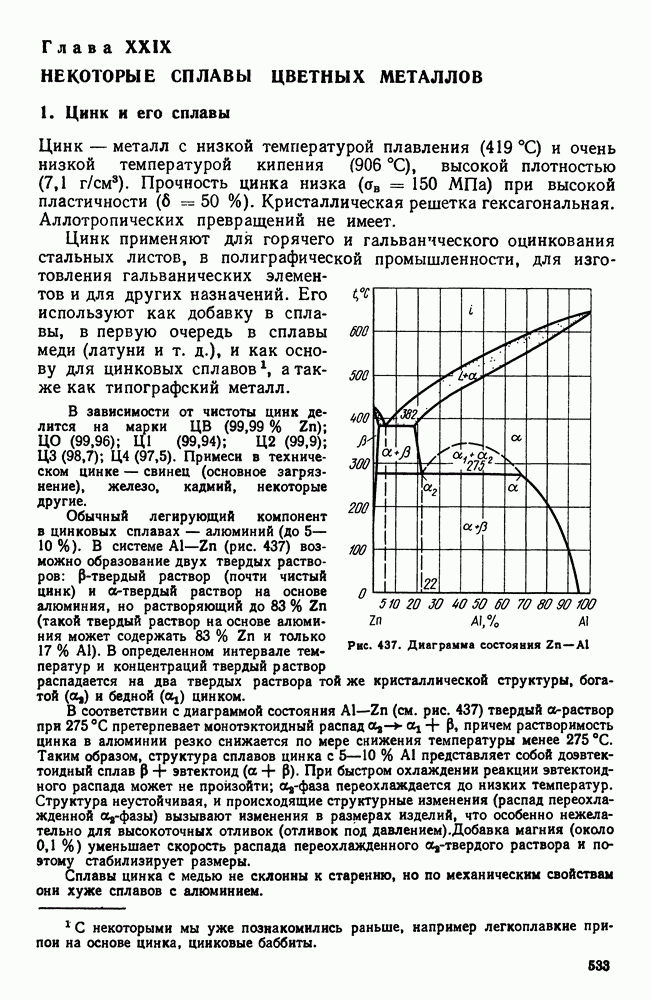
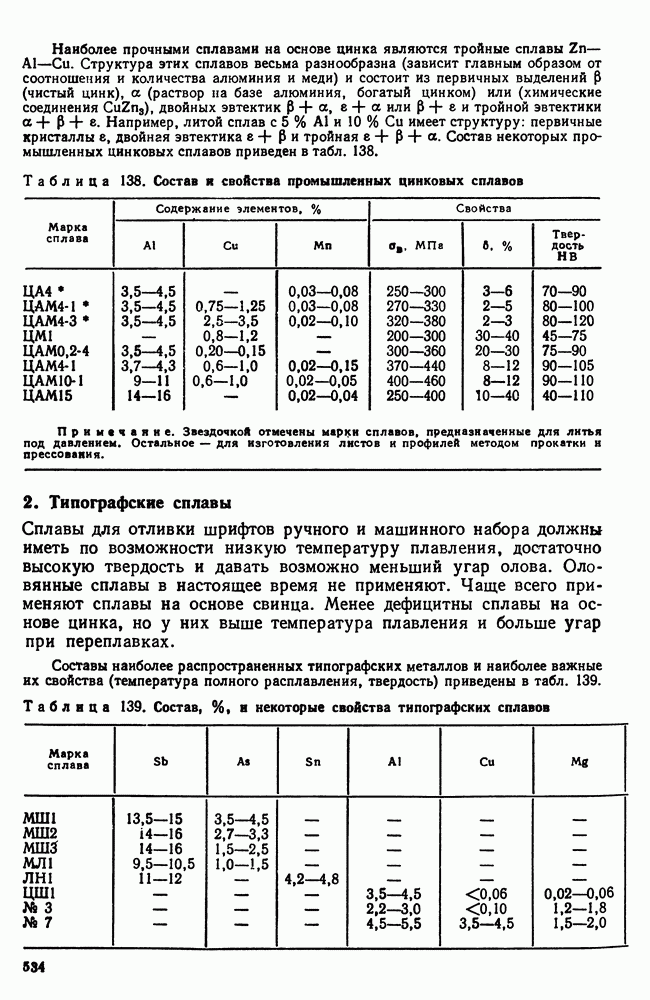
- Глава XXIX. НЕКОТОРЫЕ СПЛАВЫ ЦВЕТНЫХ МЕТАЛЛОВ
- 2. Типографские сплавы
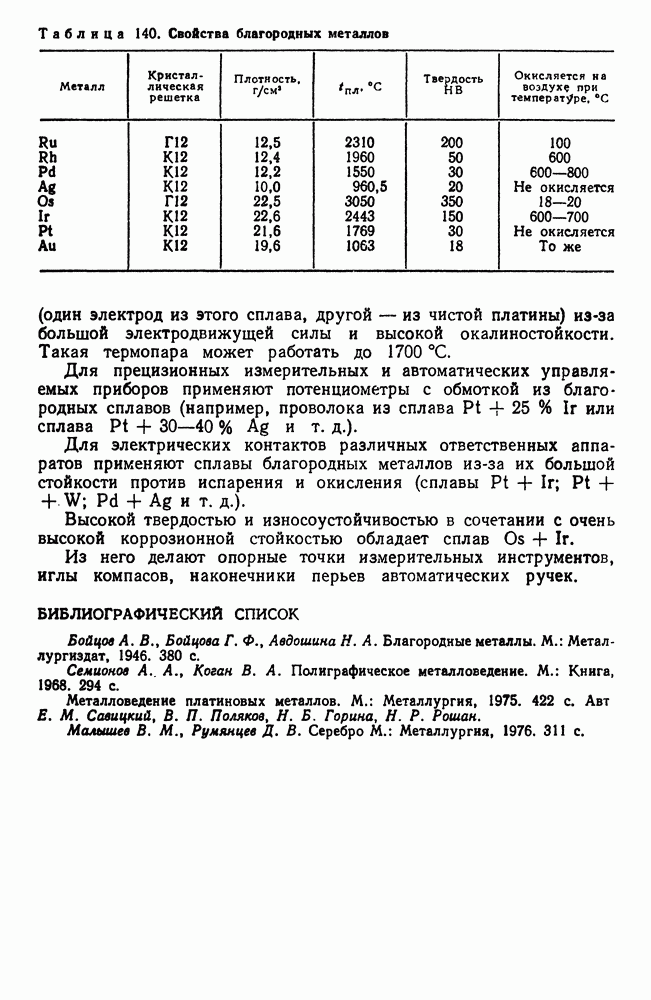
- 3. Благородные металлы