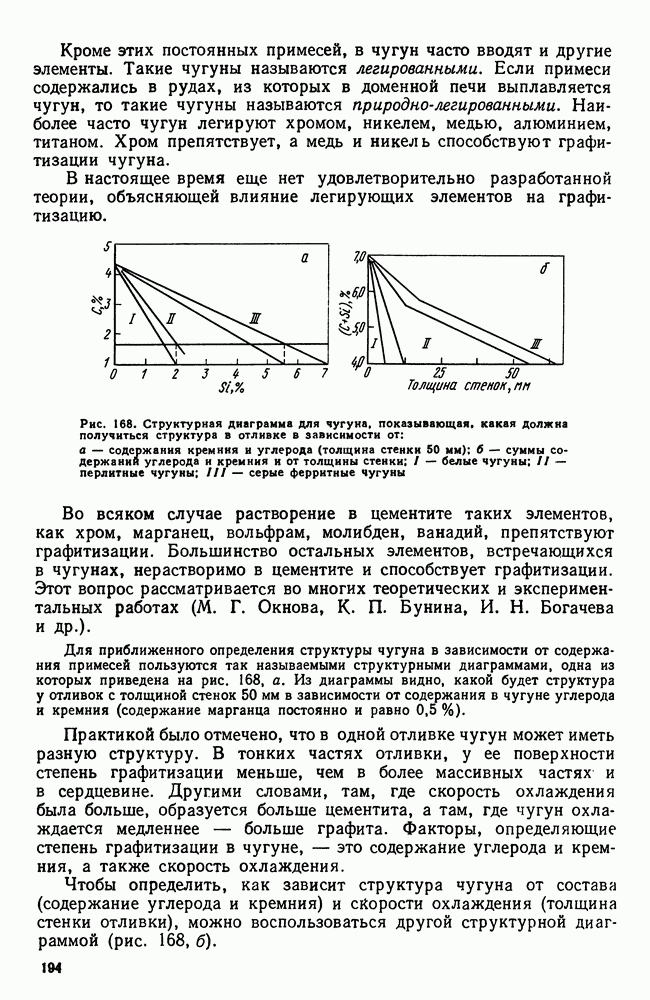
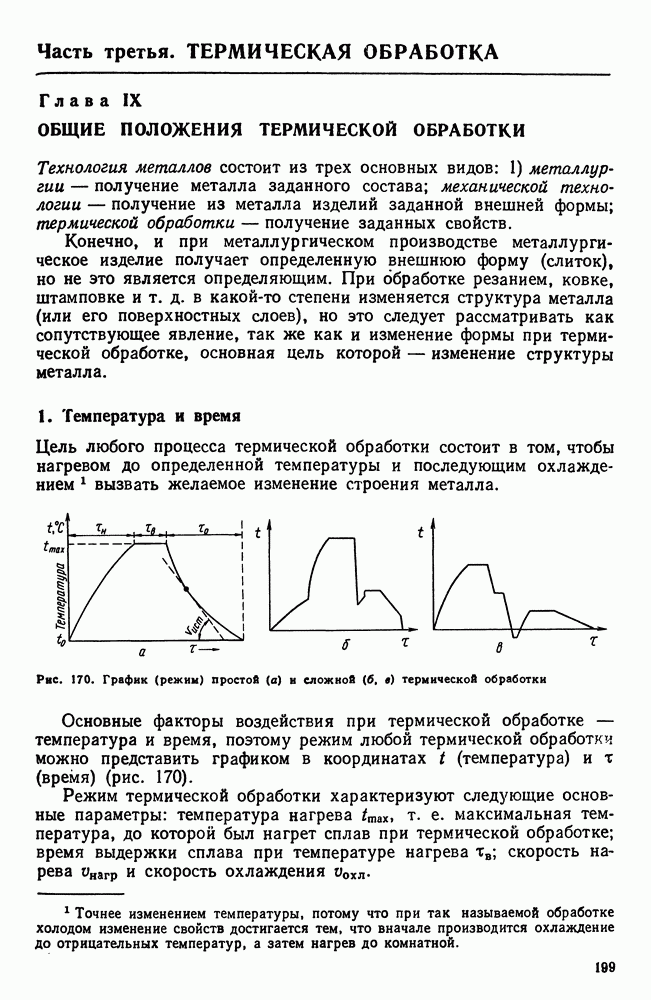
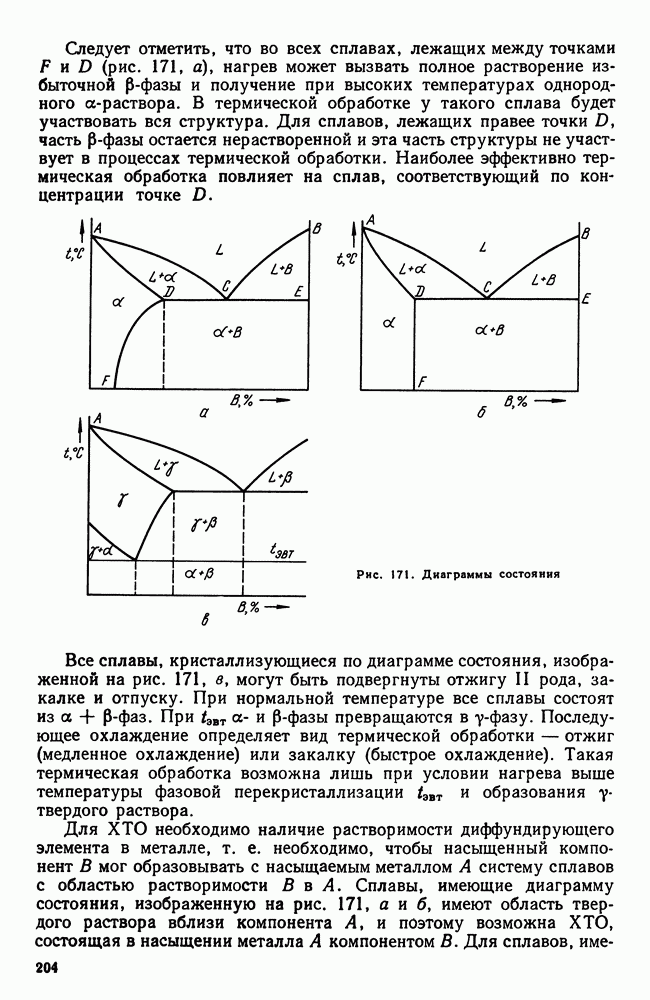
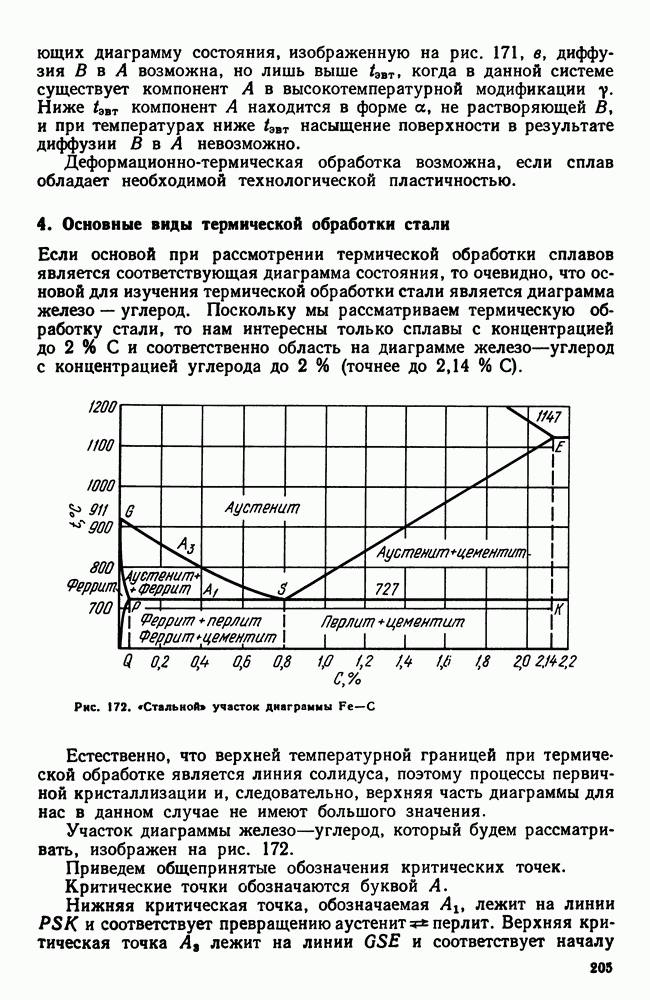
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
4. Кристаллические решетки металлов
Как отмечалось в предыдущем параграфе, атомы в кристаллическом твердом теле располагаются в пространстве закономерно, периодически повторяясь в трех измерениях через строго определенные расстояния, т. е. образуют кристаллическую решетку. Кристаллическую решетку можно «построить», выбрав для этого определенный «строительный блок» (аналогично постройке стены из кирпичей) и многократно смещая этот блок по трем непараллельным направлениям. Такая «строительная» единица кристаллической решетки имеет форму параллелепипеда и называется элементарной ячейкой. Все элементарные ячейки, составляющие кристаллическую решетку, имеют одинаковую форму и объемы. Атомы могут располагаться как в вершинах элементарной ячейки, так и в других ее точках (в узлах кристаллической решетки). В первом случае элементарные ячейки называются простыми (примитивными), во втором — сложными. Если форма элементарной ячейки определена и известно расположение всех атомов внутри нее, то имеется полное геометрическое описание кристалла, т. е. известна его атомно-кристаллическая структура.
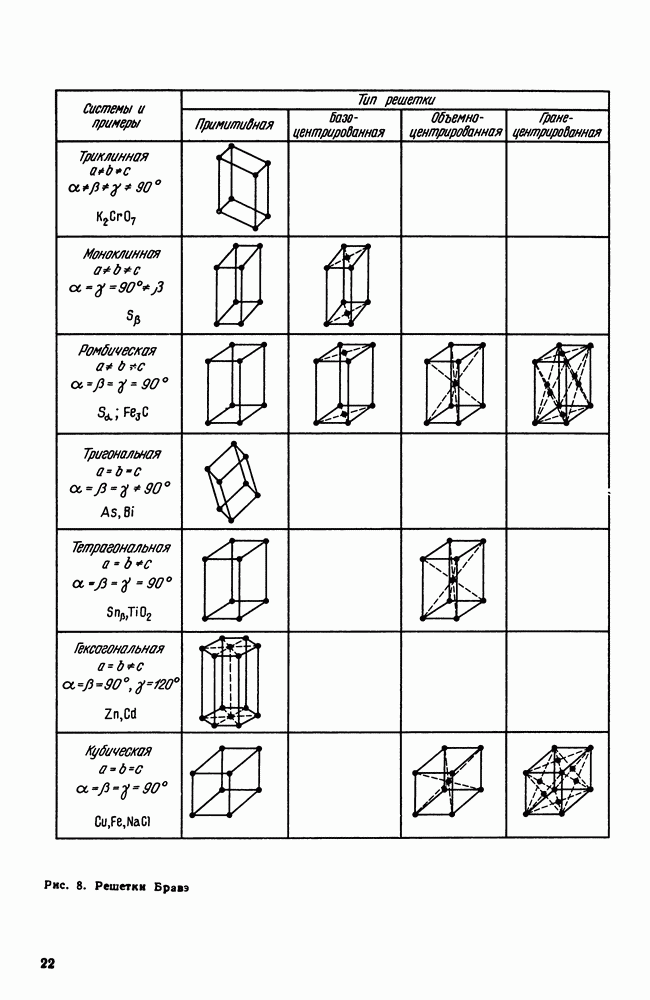
В кристаллографии рассматривают 14 типов элементарных ячеек. Их называют пространственными решетками Бравэ. Для характеристики элементарной ячейки задают шесть величин: три ребра ячейки  и три угла между ними
и три угла между ними  (см. рис. 6). Эти величины называются параметрами элементарной ячейки (кристаллической решетки). Все 14 решеток Бравэ распределены по семи кристаллическим системам (сингониям) в соответствии с ориентацией и относительными величинами параметров решетки (рис. 8). Каждая кристаллическая система включает одну или несколько типов пространственных кристаллических решеток. В простой решетке атомы располагаются только по вершинам решетки, в объемноцентрированной еще один атом в центре решетки, в гранецентрированной еще по одному атому в центре каждой грани, и в базоцентрированной еще по одному атому в центрах пары параллельных граней.
(см. рис. 6). Эти величины называются параметрами элементарной ячейки (кристаллической решетки). Все 14 решеток Бравэ распределены по семи кристаллическим системам (сингониям) в соответствии с ориентацией и относительными величинами параметров решетки (рис. 8). Каждая кристаллическая система включает одну или несколько типов пространственных кристаллических решеток. В простой решетке атомы располагаются только по вершинам решетки, в объемноцентрированной еще один атом в центре решетки, в гранецентрированной еще по одному атому в центре каждой грани, и в базоцентрированной еще по одному атому в центрах пары параллельных граней.
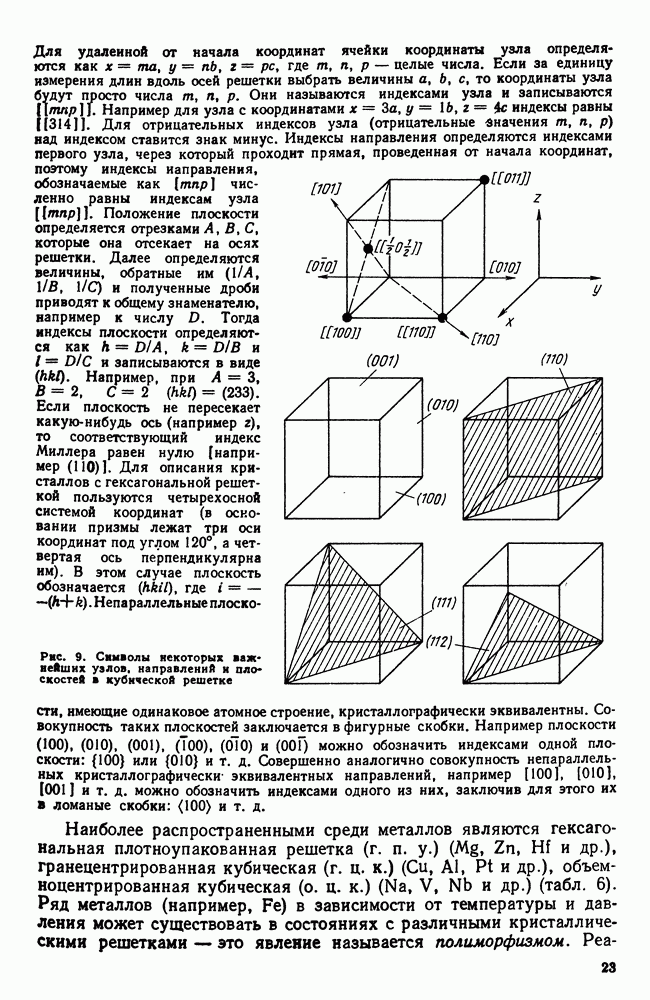
Узлы (положения атомов), направления в плоскости и пространстве обозначаются с помощью так называемых индексов Миллера (рис. 9). Положение любого узла кристаллической решетки относительно произвольно выбранного начала координат определяют заданием координат  Для одной элементарной ячейки очевидно эти координаты равны параметрам решетки
Для одной элементарной ячейки очевидно эти координаты равны параметрам решетки  с соответственно.
с соответственно.

(кликните для просмотра скана)
Для удаленной от начала координат ячейки координаты узла определяются как  где
где  целые числа. Если за единицу измерения длин вдоль осей решетки выбрать величины
целые числа. Если за единицу измерения длин вдоль осей решетки выбрать величины  , то координаты узла будут просто числа
, то координаты узла будут просто числа  Они называются индексами узла и записываются
Они называются индексами узла и записываются  Например для узла с координатами х
Например для узла с координатами х  индексы равны
индексы равны  Для отрицательных индексов узла (отрицательные значения
Для отрицательных индексов узла (отрицательные значения  над индексом ставится знак минус. Индексы направления определяются индексами первого узла, через который проходит прямая, проведенная от начала координат, поэтому индексы направления, обозначаемые как
над индексом ставится знак минус. Индексы направления определяются индексами первого узла, через который проходит прямая, проведенная от начала координат, поэтому индексы направления, обозначаемые как  численно равны индексам узла
численно равны индексам узла  Положение плоскости определяется отрезками
Положение плоскости определяется отрезками  , которые она отсекает на осях решетки. Далее определяются величины, обратные им
, которые она отсекает на осях решетки. Далее определяются величины, обратные им  и полученные дроби приводят к общему знаменателю, например к числу
и полученные дроби приводят к общему знаменателю, например к числу  Тогда индексы плоскости определяются как
Тогда индексы плоскости определяются как  и записываются в виде
и записываются в виде  Например, при
Например, при 
Если плоскость не пересекает какую-нибудь ось (например  ), то соответствующий индекс Миллера равен нулю [например (110)]. Для описания кристаллов с гексагональной решеткой пользуются четырехосной системой координат (в основании призмы лежат три оси координат под углом 120°, а четвертая ось перпендикулярна им). В этом случае плоскость обозначается
), то соответствующий индекс Миллера равен нулю [например (110)]. Для описания кристаллов с гексагональной решеткой пользуются четырехосной системой координат (в основании призмы лежат три оси координат под углом 120°, а четвертая ось перпендикулярна им). В этом случае плоскость обозначается  , где
, где 

Рис. 9. Символы некоторых важнейших узлов, направлений и плоскостей в кубической решетке
Непараллельные плоскоти, имеющие одинаковое атомное строение, кристаллографически эквивалентны. Совокупность таких плоскостей заключается в фигурные скобки. Например плоскости (100), (010), (001), (100), (010) и (001) можно обозначить индексами одной плоскости:  или (010) и т. д. Совершенно аналогично совокупность непараллельных кристаллографически эквивалентных направлений, например [100], [010], [001] и т. д. можно обозначить индексами одного из них, заключив для этого их
или (010) и т. д. Совершенно аналогично совокупность непараллельных кристаллографически эквивалентных направлений, например [100], [010], [001] и т. д. можно обозначить индексами одного из них, заключив для этого их  ломаные скобки: (100) и т. д.
ломаные скобки: (100) и т. д.
Наиболее распространенными среди металлов являются гексагональная плотноупакованная решетка  , гранецентрированная кубическая (г. ц. к.)
, гранецентрированная кубическая (г. ц. к.)  , объем ноцентрированная кубическая
, объем ноцентрированная кубическая  (табл. 6). Ряд металлов (например,
(табл. 6). Ряд металлов (например,  в зависимости от температуры и давления может существовать в состояниях с различными кристаллическими решетками — это явление называется полиморфизмом.
в зависимости от температуры и давления может существовать в состояниях с различными кристаллическими решетками — это явление называется полиморфизмом.
Реализация в металлах отмеченных структур является следствием их высокой компактности, т. е. отношение объема, занимаемого атомами в элементарной ячейке к объему ячейки. Компактность структуры является одним из факторов, уменьшающим свободную энергию твердого тела, т. е. обеспечивающим его равновесное состояние и следствием особенностей электронной структуры металлов и характером их межатомного взаимодействия.
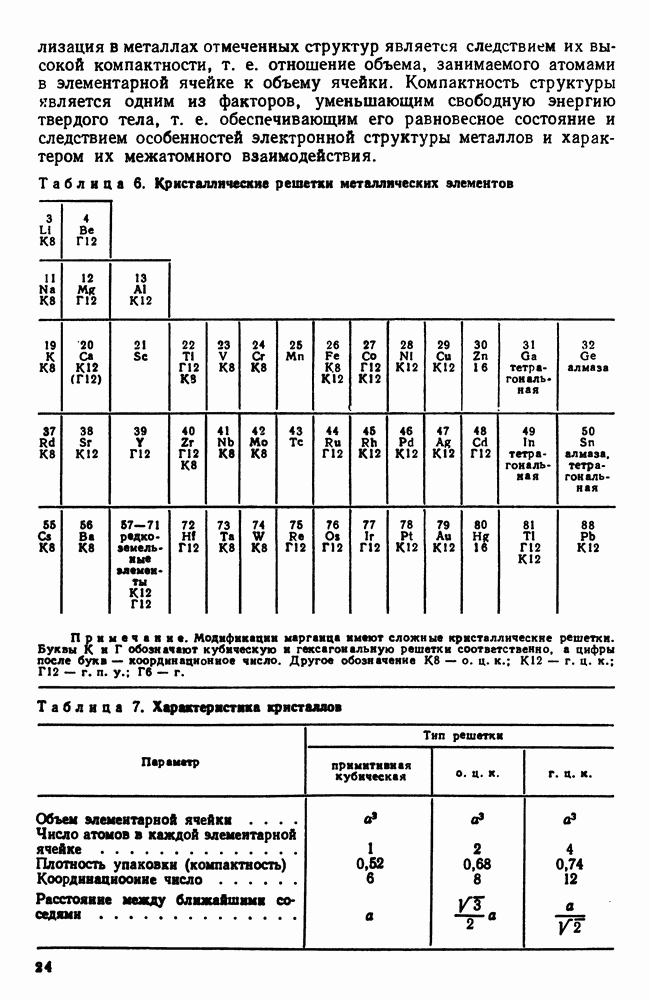
Таблица 6. (см. скан) Кристаллические решетки металлических элементов
Таблица 7. (см. скан) Характеристика кристаллов
Приведем (табл. 7) наиболее важные характеристики кристаллов с кубической решеткой. За координационное число принято число ближайших соседей данного атома.
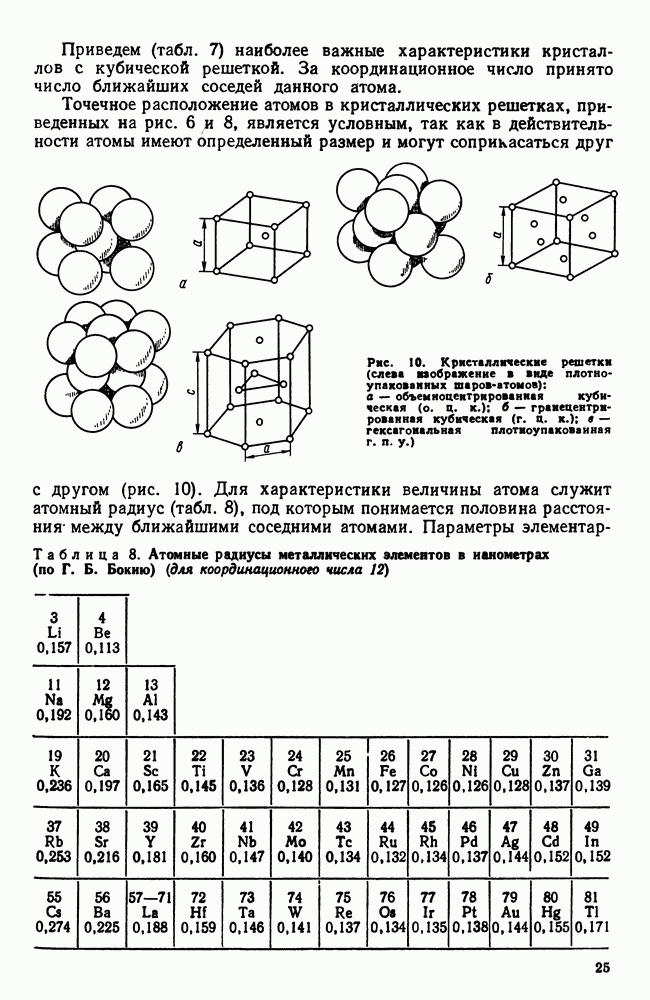
Точечное расположение атомов в кристаллических решетках, приведенных на рис. 6 и 8, является условным, так как в действительности атомы имеют определенный размер и могут соприкасаться друг с другом (рис. 10).
Рис. 10. (см. скан) Кристаллические решетки (слева изображение в виде плотно-упакованных шаров атомов): а — объемиоцеитрированиая кубическая (о. ц. к.); б — гранецентрированная кубическая (г. ц. к.); в — гексагональная плотноупакованная г. п. у.)
Для характеристики величины атома служит атомный радиус (табл. 8), под которым понимается половина расстояния между ближайшими соседними атомами. Параметры
Таблица 8. (см. скан) Атомные радиусы металлических элементов в нанометрах (по Г. Б. Бокию) (для координационною числа 12)
элементарной ячейки  и атомные радиусы измеряются в ангстремах
и атомные радиусы измеряются в ангстремах  или в нанометрах
или в нанометрах  . Параметры решетки металлов (их также называют периодами решетки) находятся в пределах 0,2-0,7 нм и определяются методом рентгеноструктурного анализа с точностью до третьего, а при необходимости и до четвертого или даже пятого знака после запятой.
. Параметры решетки металлов (их также называют периодами решетки) находятся в пределах 0,2-0,7 нм и определяются методом рентгеноструктурного анализа с точностью до третьего, а при необходимости и до четвертого или даже пятого знака после запятой.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Часть первая. ТЕОРИЯ СПЛАВОВ
- Глава I. КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ
- 2. Классификация металлов
- 3. Кристаллическое строение металлов
- 4. Кристаллические решетки металлов
- 5. Реальное строение металлических кристаллов
- 6. Анизотропия свойств кристаллов
- 7. Методы изучения строения металлов
- Глава II. КРИСТАЛЛИЗАЦИЯ
- 1. Три состояния вещества
- 2. Энергетические условия процесса кристаллизации
- 3. Механизм процесса кристаллизации
- 4. Форма кристаллических образований
- 5. Строение слитка
- 6. Превращения в твердом состояние. Полиморфизм
- 7. Магнитные превращения
- 8. Закалка из жидкого состояния. Аморфное состояние
- Глава III. МЕХАНИЧЕСКИЕ СВОЙСТВА. НАКЛЕП И РЕКРИСТАЛЛИЗАЦИЯ
- 2. Упругая и пластическая деформация. Несовершенства решетки и прочность металлов
- 3. Сверхпластичность
- 4. Разрушение
- 5. Методы определения механических свойств
- 6. Наклеп
- 7. Влияние нагрева на строение и свойства деформированного металла (рекристаллизационные процессы)
- Глава IV. СТРОЕНИЕ СПЛАВОВ
- 2. Химическое соединение
- 3. Твердый раствор на основе одного из компонентов сплава
- 4. Твердый раствор на основе химического соединения
- 5. Упорядоченные твердые растворы
- 6. Электронные соединения (фазы Юм-Розери)
- 7. Фазы Лавеса
- 8. Фазы внедрения
- Глава V. ДИАГРАММА СОСТОЯНИЯ
- 2. Общие замечания о построении диаграмм состояния
- 3. Экспериментальное построение диаграмм
- 4. Диаграмма состояния для сплавов, образующих механические смеси из чистых компонентов (I рода)
- 5. Правило отрезков
- 6. Диаграмма состояния для сплавов с неограниченной растворимостью в твердом состоянии (II рода)
- 7. Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии (III рода)
- 8. Диаграмма состояния для сплавов, образующих химические соединения (IV рода)
- 9. Диаграмма состояния для сплавов, испытывающих полиморфные превращения
- 10. Кристаллизация сплавов в неравновесных условиях
- 11. Системы с тремя компонентами
- 12. Упрощенные методы изучения многокомпонентных систем
- 13. Связь между свойствами сплавов и типом диаграммы состояния
- Часть вторая. ЖЕЛЕЗОУГЛЕРОДИСТЫЕ СПЛАВЫ
- Глава VI. ДИАГРАММА ЖЕЛЕЗО—УГЛЕРОД
- 2. Железо
- 3. Цементит
- 4. Диаграмма состояния
- Глава VII. УГЛЕРОДИСТЫЕ СТАЛИ
- 1. Влияние углерода на свойства стали
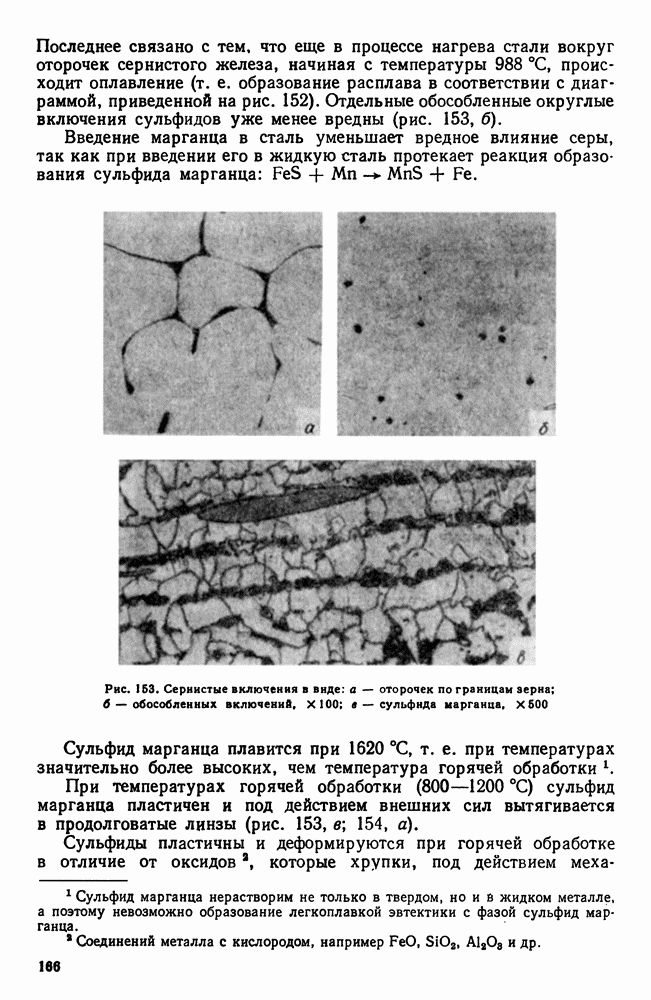
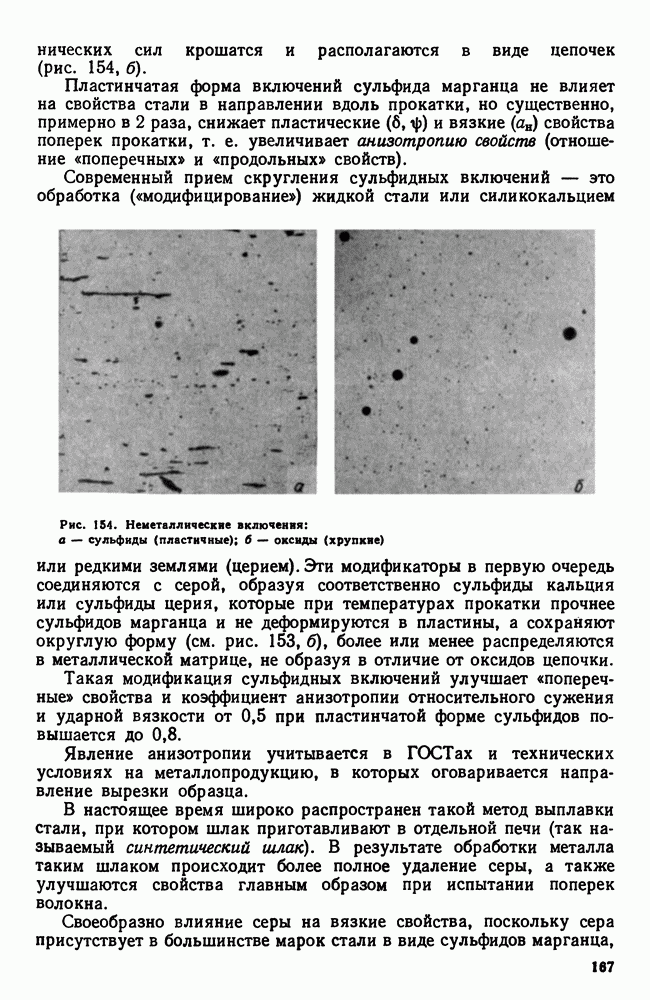
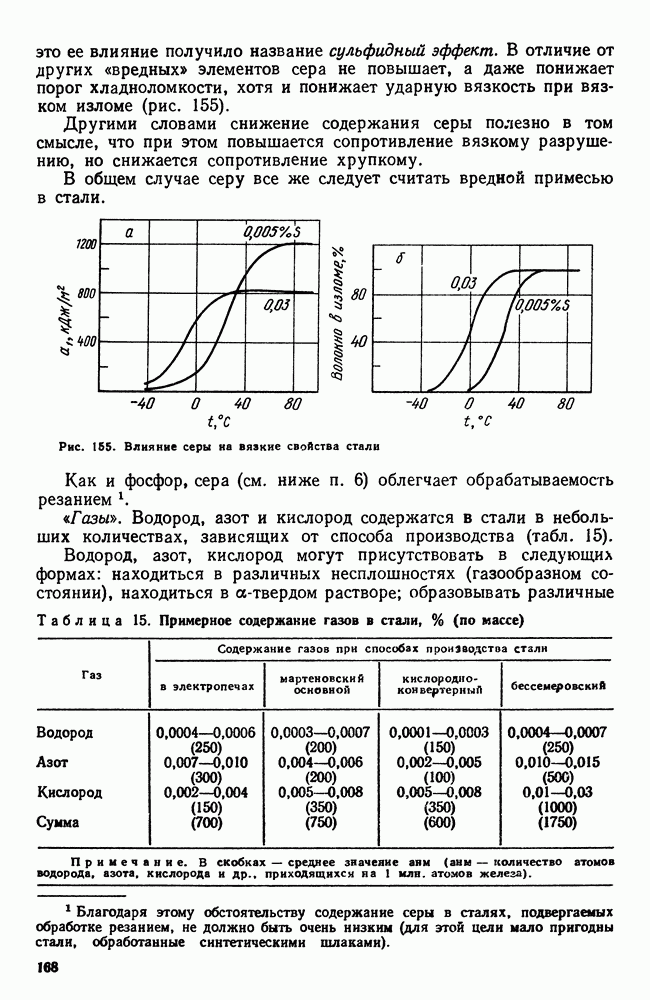
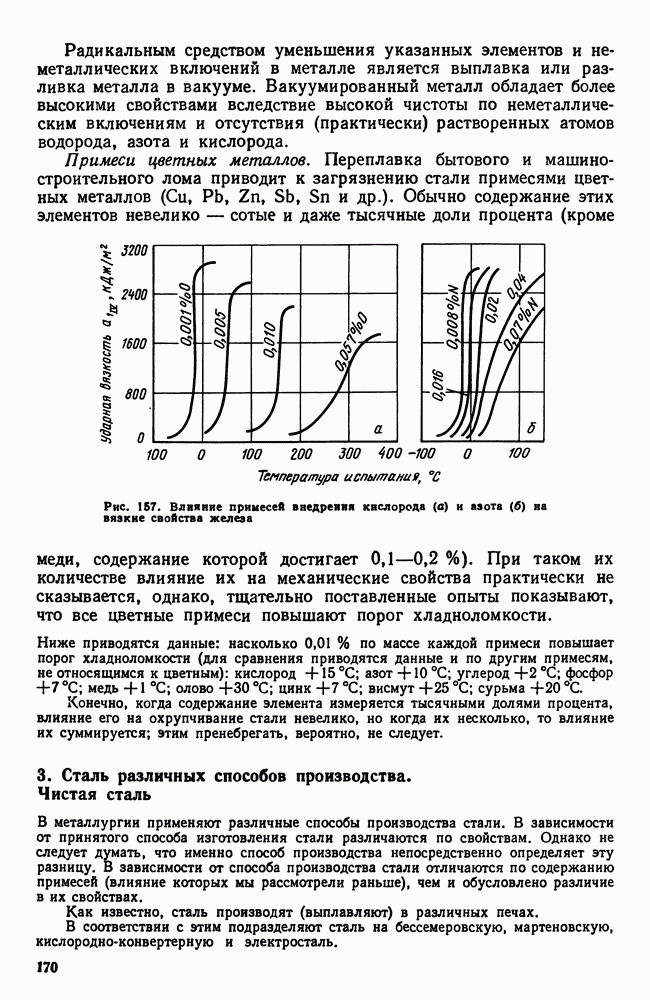
- 2. Влияние постоянных примесей на свойства стали
- 3. Сталь различных способов производства. Чистая сталь
- 4. Углеродистая сталь общего назначения
- 5. Нагартованная сталь
- 6. Листовая сталь для холодной штамповки
- 7. Обрабатываемость резанием. Автоматные стали
- Глава VIII. ЧУГУН
- 2. Структура чугуна. Формы графита
- 3. Структура и свойства чугуна
- 4. Примеси в чугуне
- 5. Марки серых и высокопрочных чугунов
- 6. Ковкий чугун
- Часть третья. ТЕРМИЧЕСКАЯ ОБРАБОТКА
- Глава IX. ОБЩИЕ ПОЛОЖЕНИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ
- 2. Классификация видов термической обработки
- 3. Термическая обработка и диаграмма состояния
- 4 Основные виды термической обработки стали
- 5. Четыре основных превращения в стали
- Глава X. ТЕОРИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ
- 2. Рост аустенитного зерна
- 3. Распад аустенита
- 4. Мартенситное превращение
- 5. Бейнитное превращение
- 6. Превращения при отпуске
- 7. Влияние термической обработки на свойства стали
- 8. Термомеханическая обработка
- Глава XI. ПРАКТИКА ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ
- 2. Время нагрева
- 3. Химическое воздействие нагревающей среды
- 4. Закалочные среды
- 5. Прокаливаемость
- 6. Внутренние напряжения
- 7. Способы закалки
- 8. Обработка стали холодом
- 9. Дефекты, возникающие при закалке
- 10. Отжиг и нормализация
- Глава XII. ПОВЕРХНОСТНАЯ ЗАКАЛКА СТАЛИ
- 2. Высокочастотная закалка
- Глава XIII. ХИМИКО-ТЕРМИЧЕСКАЯ ОБРАБОТКА СТАЛИ
- 2. Цементация стали
- 3. Азотирование стали
- 4. Цианирование стали
- 5. Диффузионная металлизация
- Часть четвертая. ЛЕГИРОВАННЫЕ СТАЛИ И СПЛАВЫ
- Глава XIV. ВЛИЯНИЕ ЛЕГИРУЮЩИХ ЭЛЕМЕНТОВ
- 2. Влияние элементов на полиморфизм железа
- 3. Распределение легирующих элементов в стали
- 4. Влияние легирующих элементов на феррит
- 5. Карбидная фаза в легированных сталях
- 6. Влияние легирующих элементов на превращения в стали
- Глава XV. КЛАССИФИКАЦИЯ И МАРКИРОВКА ЛЕГИРОВАННЫХ СТАЛЕЙ
- 2. Маркировка легированных сталей
- Глава XVI. КОНСТРУКЦИОННЫЕ СТАЛИ
- 1. Механические свойства стали, влияние структуры и легирующих элементов
- 2. Термическая обработка конструкционных сталей
- 3. Цементуемые (низкоуглеродистые) стали
- 4. Улучшаемые (среднеуглеродистые) стали
- 5. Высокопрочные стали
- 6. Свариваемость стали
- 7. Строительная сталь
- 8. Арматурная сталь
- 9. Пружинная сталь
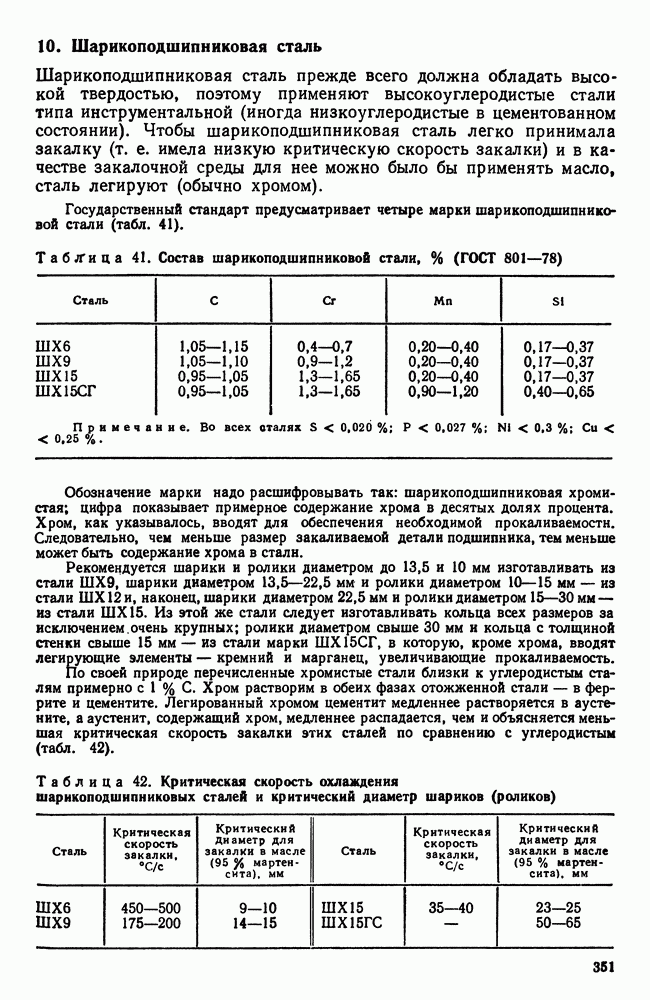
- 10. Шарикоподшипниковая сталь
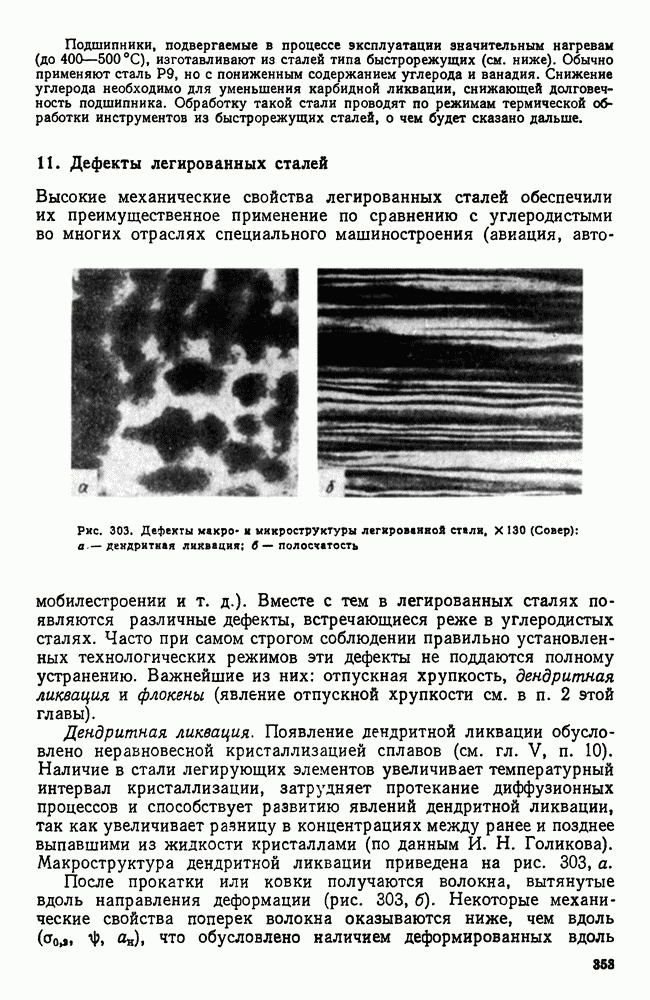
- 11. Дефекты легированных сталей
- Глава XVII. ИНСТРУМЕНТАЛЬНЫЕ СТАЛИ
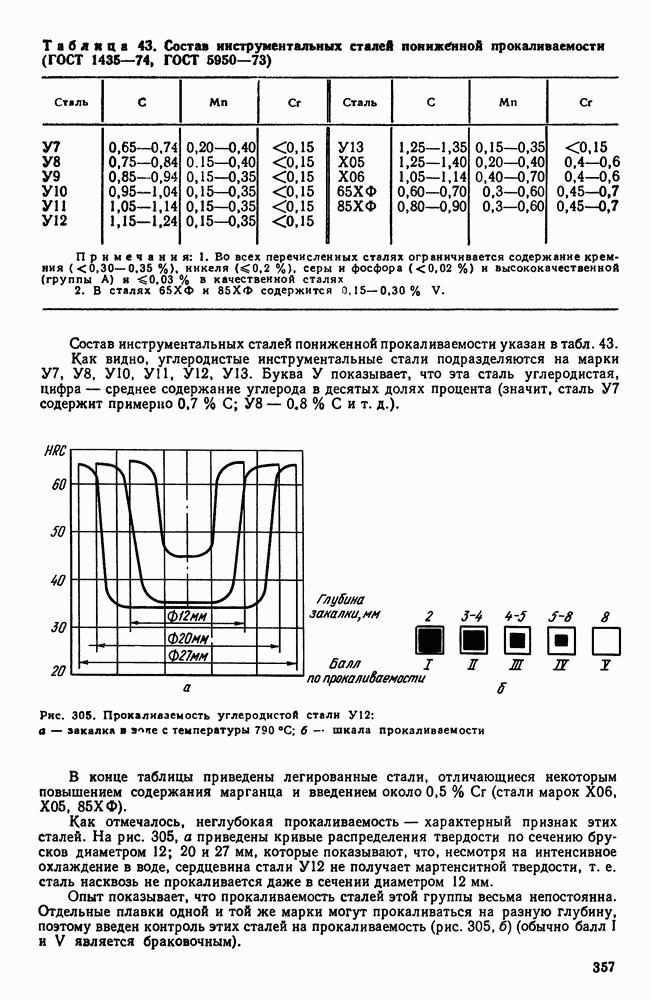
- 2. Инструментальные стали пониженной прокаливаемости
- 3. Инструментальные стали повышенной прокаливаемости (легированные инструментальные стали)
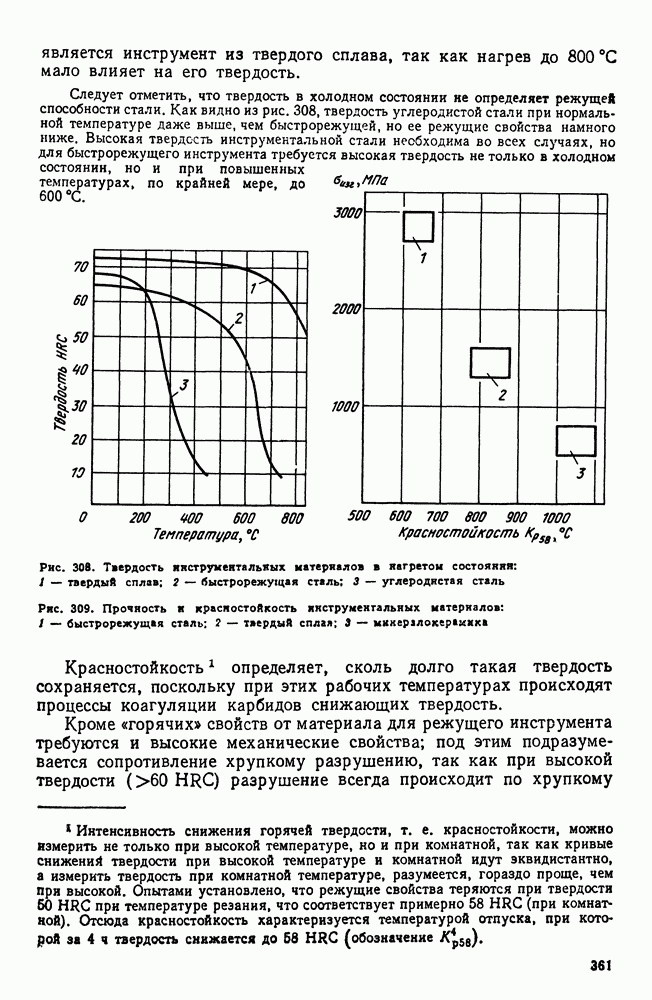
- 4. Быстрорежущие стали
- 5. Штамповые стали
- 6. Твердые сплавы
- Глава XVIII. ЖАРОСТОЙКИЕ И ЖАРОПРОЧНЫЕ СТАЛИ И СПЛАВЫ
- 2. Жаропрочность
- 3. Оценка жаропрочных свойств
- 4. Влияние структуры и состава на жаропрочность
- 5. Классификация жаропрочных материалов
- 6. Перлитные и мартенситные жаропрочные стали
- 7. Аустенитные жаропрочные стали
- 8. Никелевые и кобальтовые жаропрочные сплавы
- Глава XIX. КОРРОЗИОННОСТОЙКИЕ (НЕРЖАВЕЮЩИЕ) СТАЛИ И СПЛАВЫ
- 2. Хромоникелевые нержавеющие стали
- 3. Кислотостойкие стали и сплавы
- 4. Криогенные стали и сплавы
- Глава XX. ИЗНОСОСТОЙКИЕ СТАЛИ И СПЛАВЫ
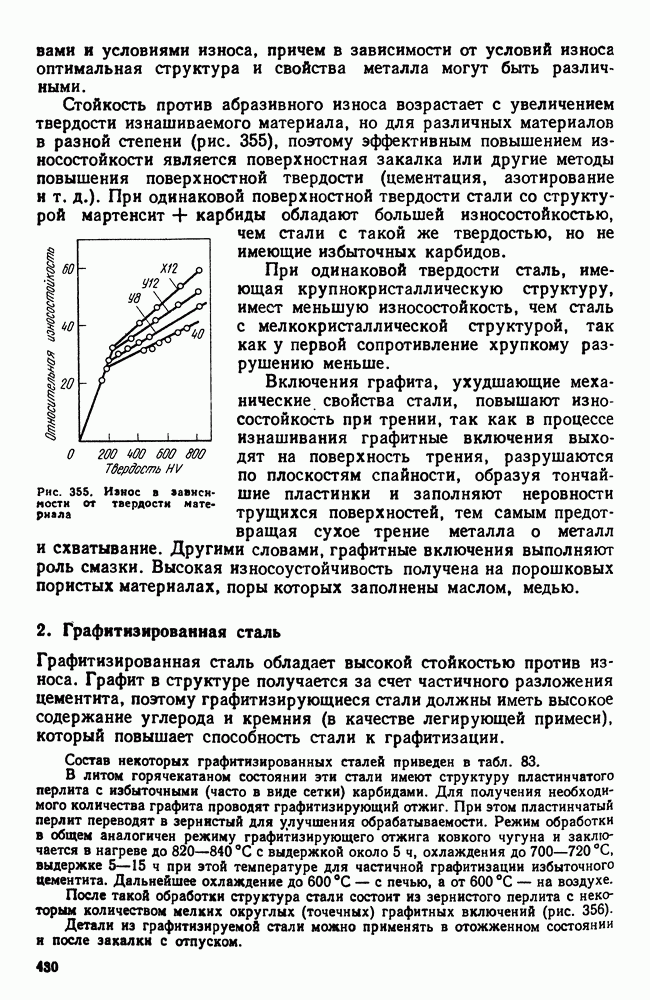
- 2. Графитизированная сталь
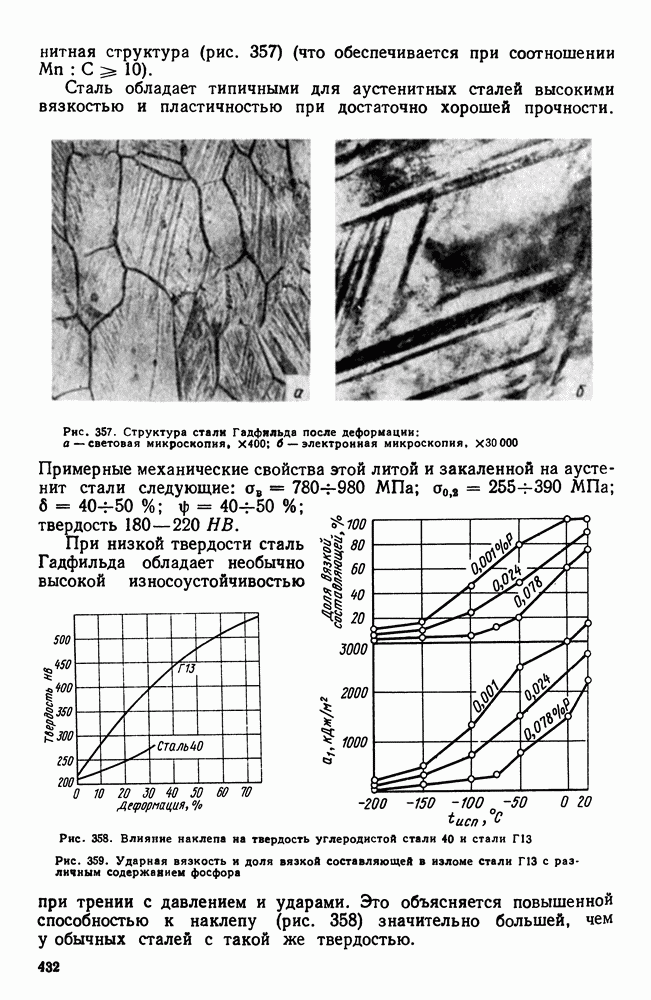
- 3. Высокомарганцовистая сталь
- 4. Наплавочные материалы
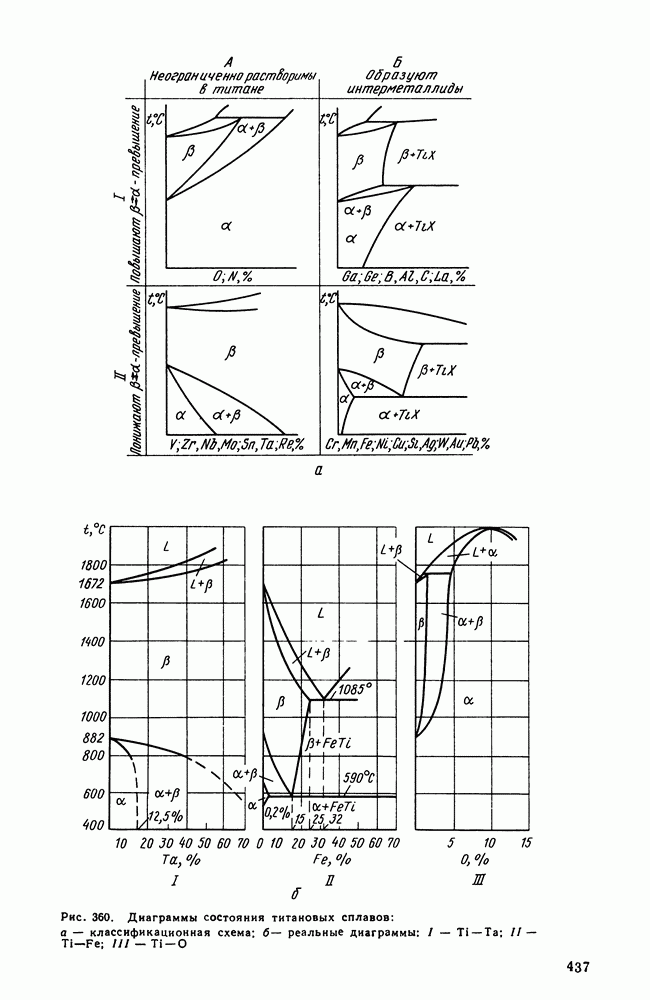
- Глава XXI. ТИТАН И ЕГО СПЛАВЫ
- 2. Легирование титана
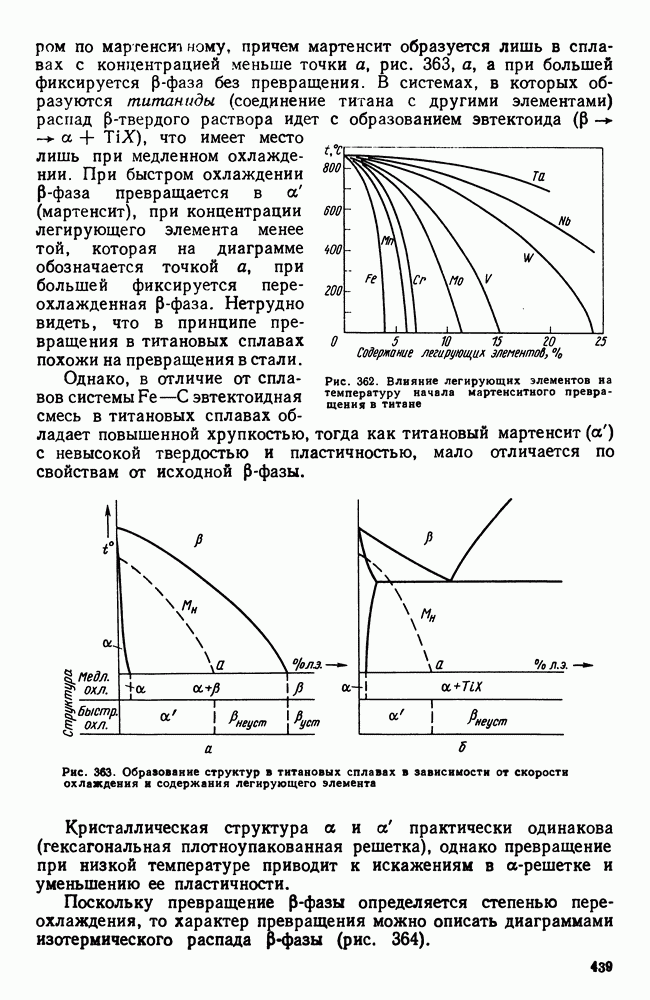
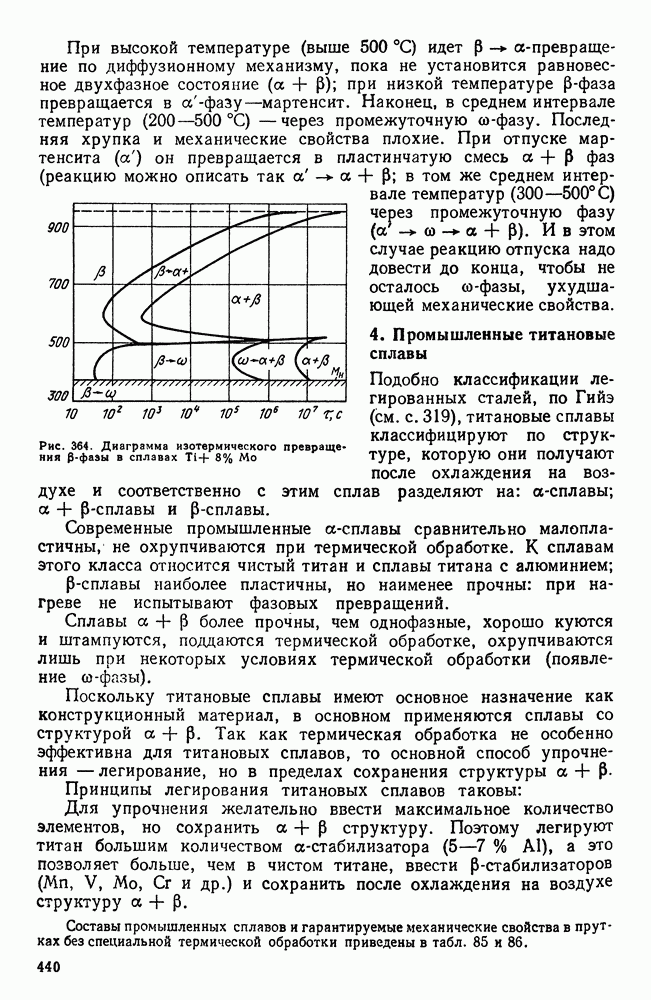
- 3. Фазовые превращения в титановых сплавах
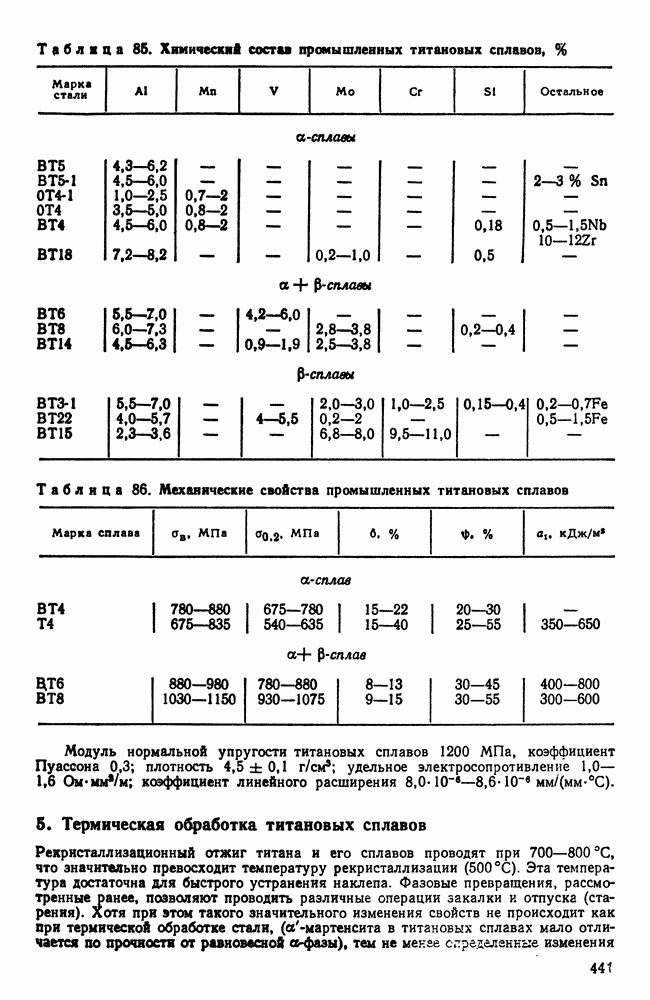
- 5. Термическая обработка титановых сплавов
- 6. Примеси в титановых сплавах
- 7. Коррозионная стойкость титана
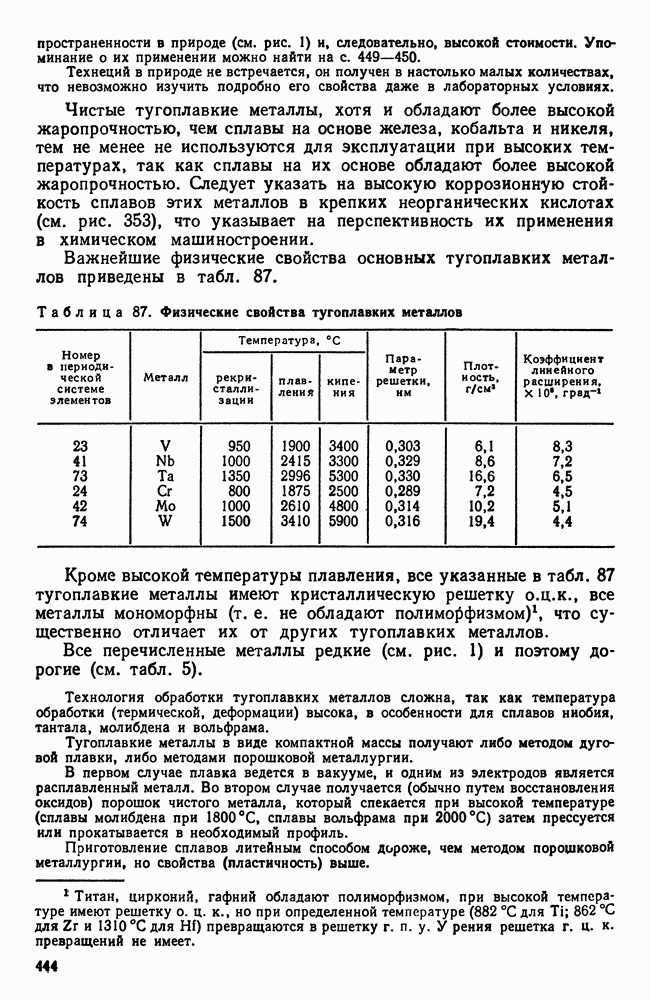
- Глава XXII. ТУГОПЛАВКИЕ МЕТАЛЛЫ
- 2. Взаимодействие тугоплавких металлов с другими элементами и между собой
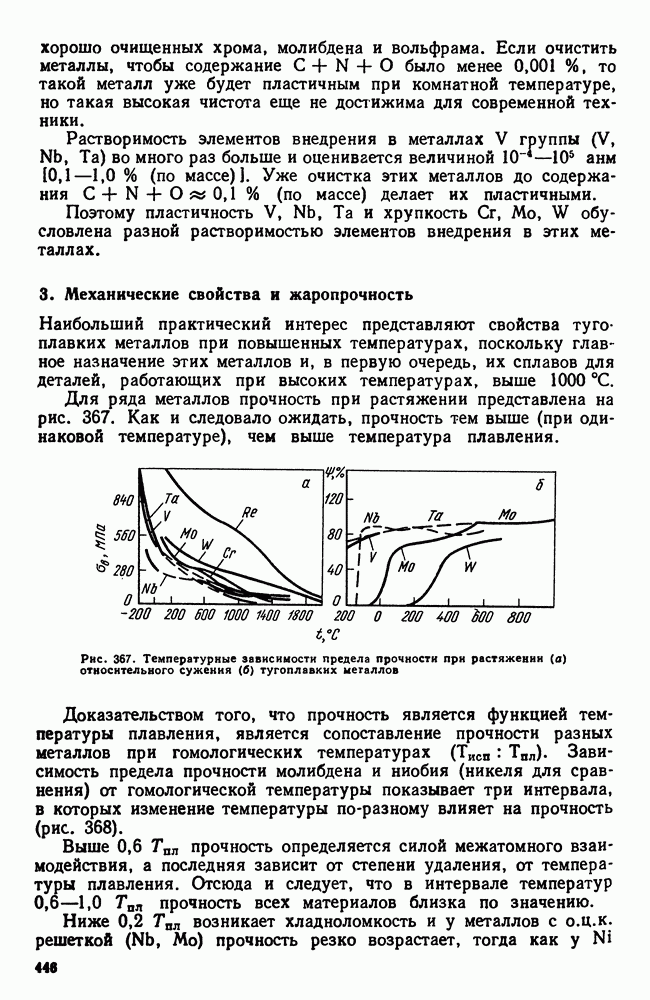
- 3. Механические свойства и жаропрочность
- 4. Хладноломкость тугоплавких металлов
- 5. Сопротивление окислению и защита от окисления
- 6. Коррозионная стойкость
- Глава XXIII. СПЛАВЫ С ОСОБЫМИ ТЕПЛОВЫМИ И УПРУГИМИ СВОЙСТВАМИ
- 2. Сплавы с постоянным модулем упругости
- Глава XXIV. МАГНИТНЫЕ СТАЛИ И СПЛАВЫ
- 2. Стали и сплавы для постоянных магнитов (магнитнотвердые сплавы)
- 3. Магнитномягкие сплавы
- 4. Немагнитные стали
- 5. Электротехнические сплавы
- Глава XXV. СПЛАВЫ АТОМНОЙ ЭНЕРГЕТИКИ
- 2. Конструкционные материалы. Теплоносители
- 3. Ядерное горючее (уран, плутоний, торий)
- Часть пятая. Цветные металлы и сплавы
- Глава XXVI. ЛЕГКИЕ МЕТАЛЛЫ И ИХ СПЛАВЫ
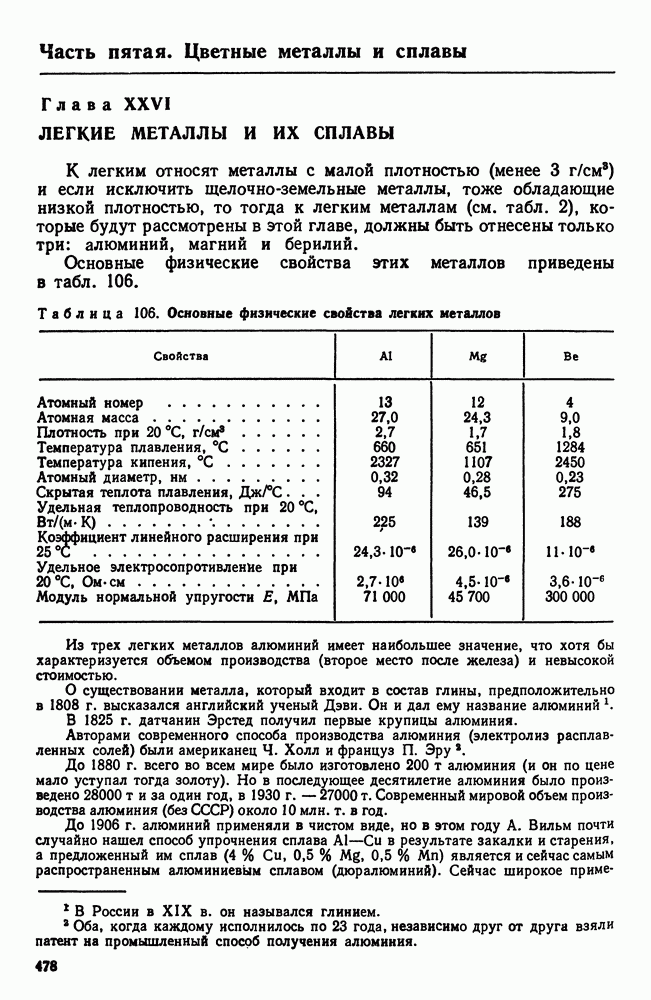
- 1. Свойства алюминия
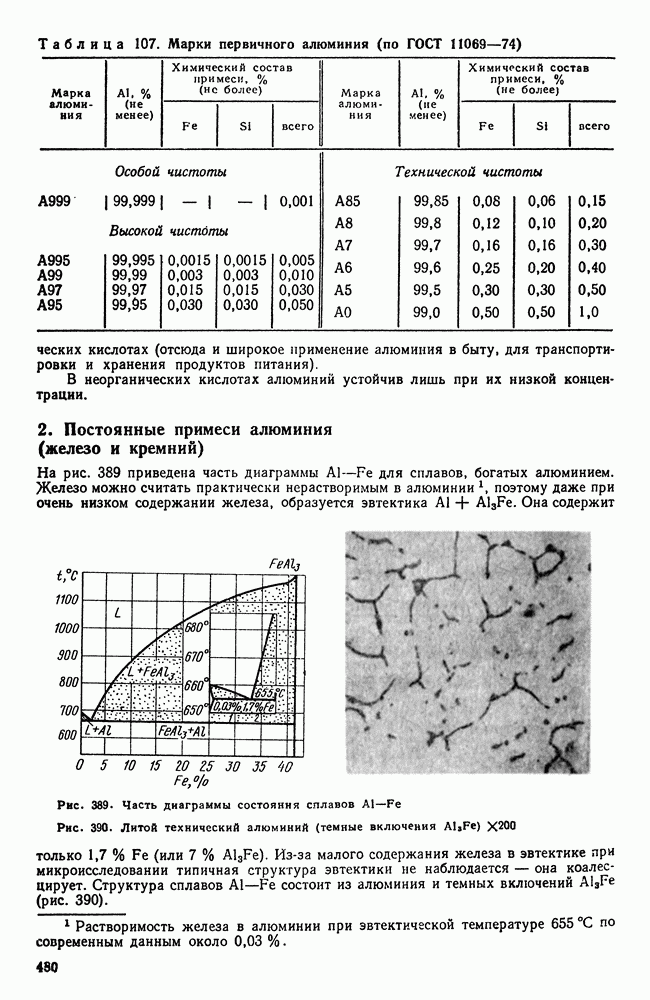
- 2. Постоянные примеси алюминия (железо и кремний)
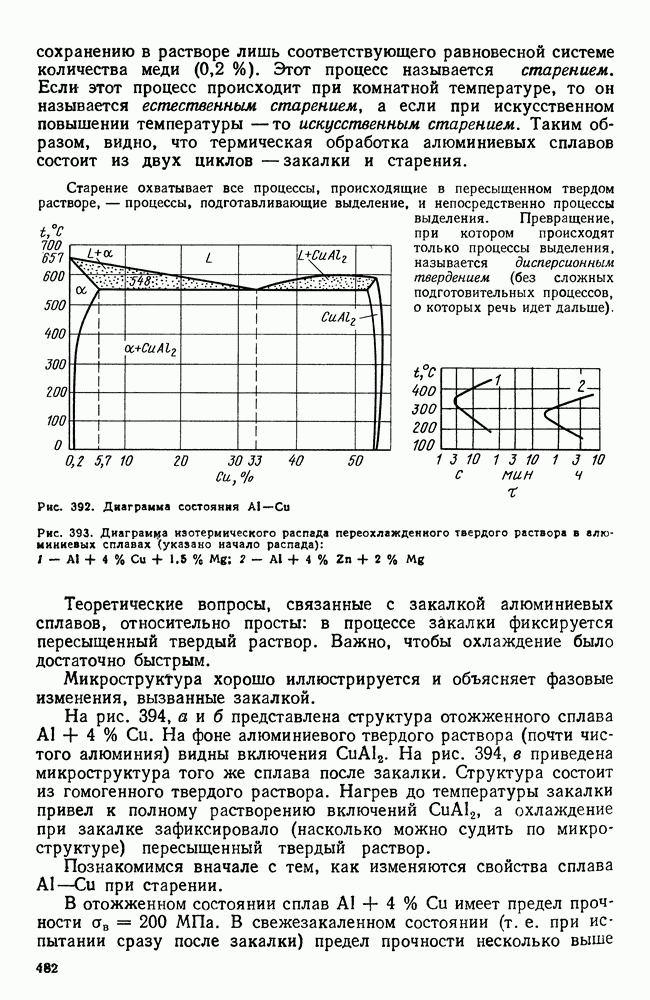
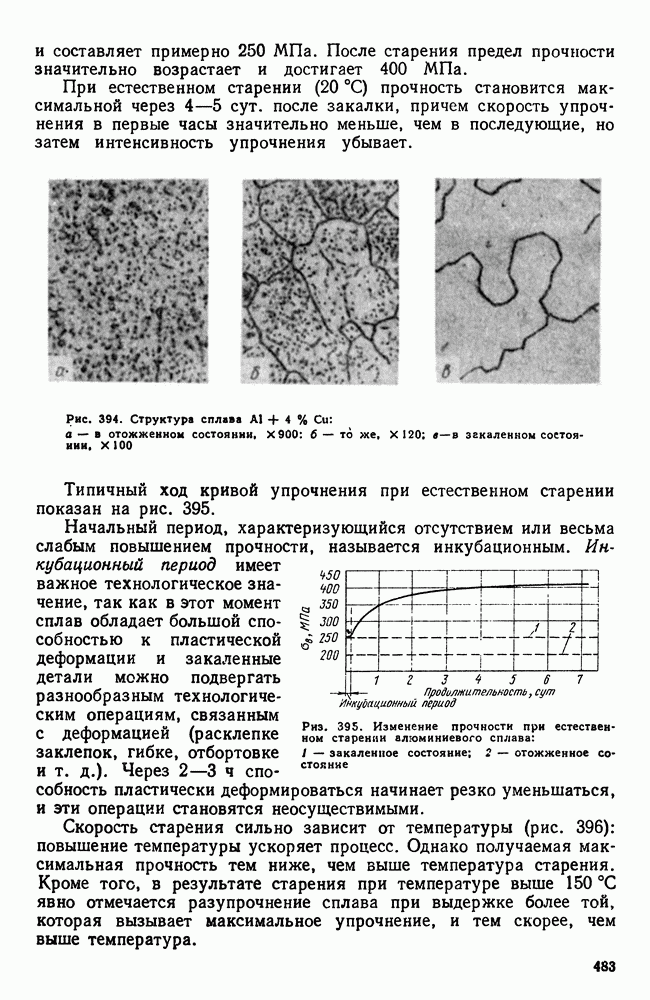
- 3. Термическая обработка сплавов Al-Cu
- 4. Влияние состава алюминиевых сплавов на процессы, происходящие при термической обработке
- 5. Классификация алюминиевых сплавов
- 6. Деформируемые сплавы, не упрочняемые термической обработкой
- 7. Дюралюминий и другие деформируемые сплавы, упрочняемые термической обработкой
- 8. Алюминиевые сплавы для поковок и штамповок
- 9. Силумины и другие алюминиевые сплавы для фасонного литья
- 10. Жаропрочные алюминиевые сплавы
- 11. Магний
- 12. Сплавы магния
- 13. Бериллий
- 14. Сплавы бериллия
- Глава XXVII. МЕДЬ И ЕЕ СПЛАВЫ
- 2. Сплавы меди с цинком (латуни)
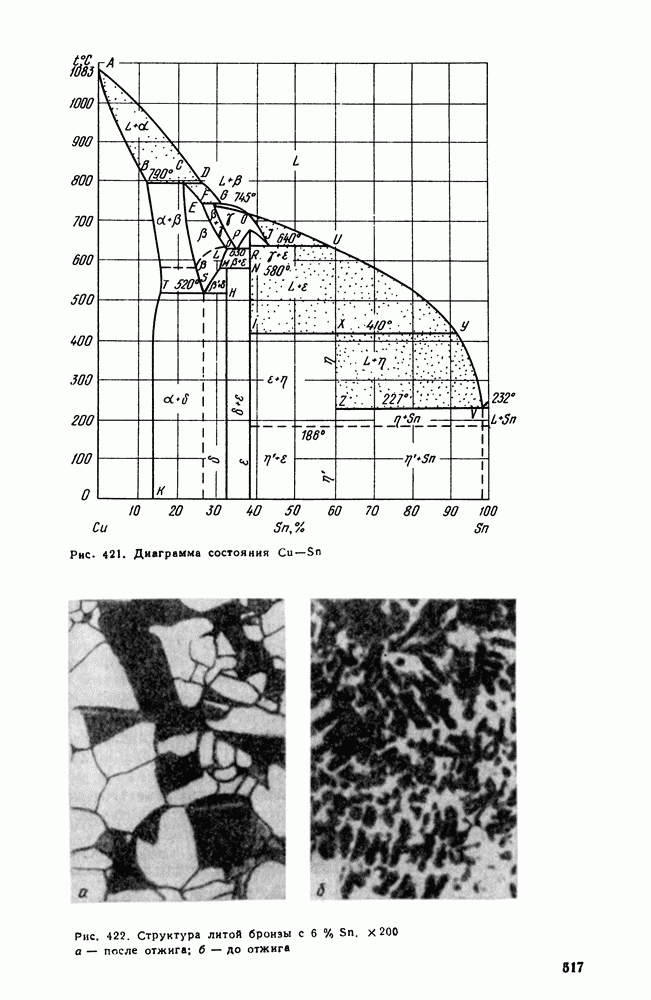
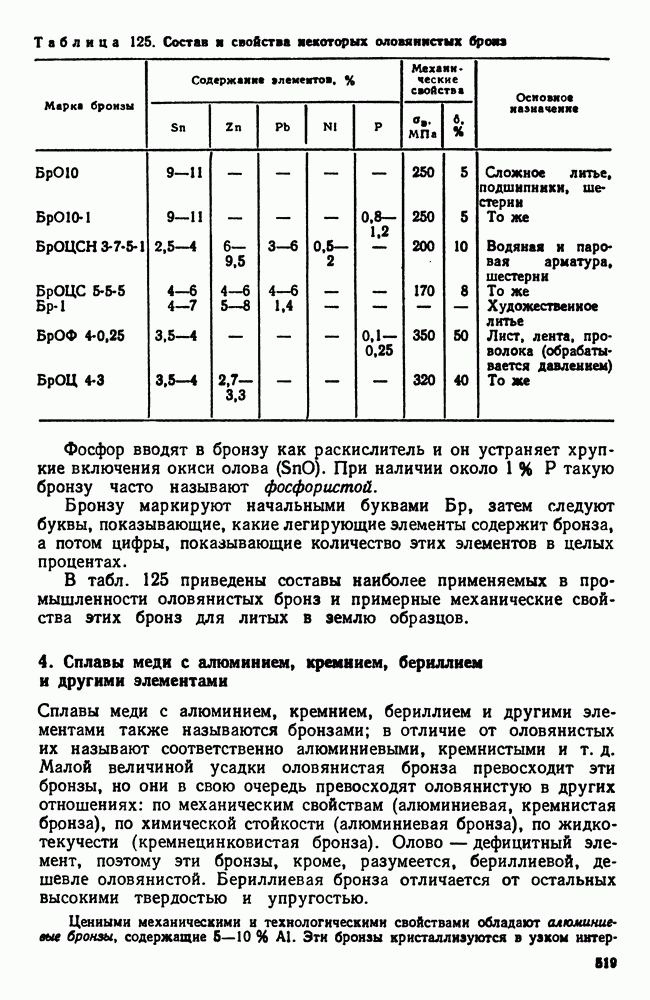
- 3. Сплавы меди с оловом (оловянистые бронзы)
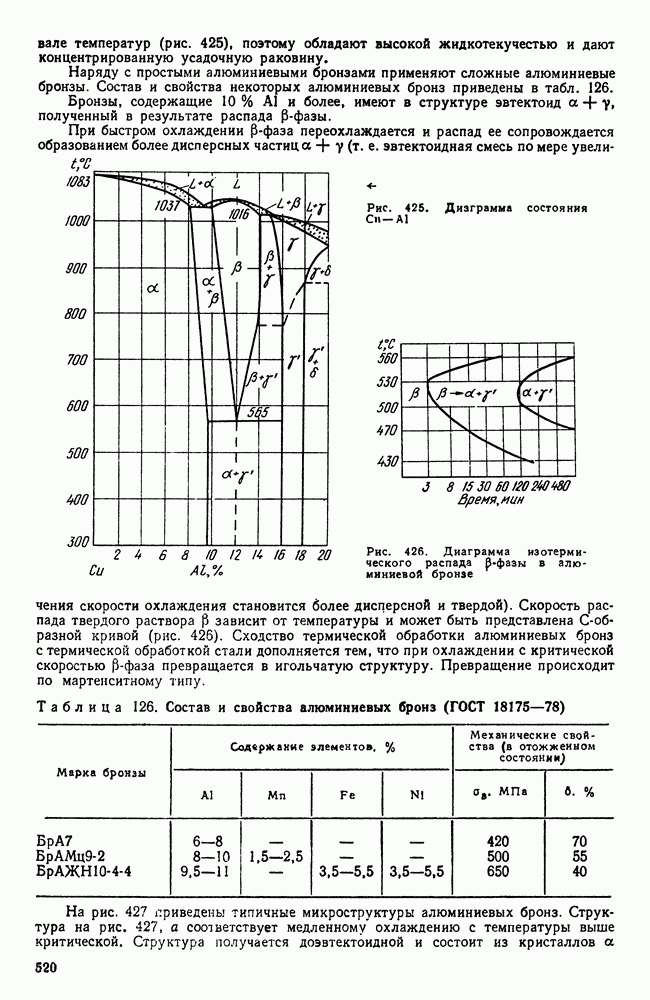
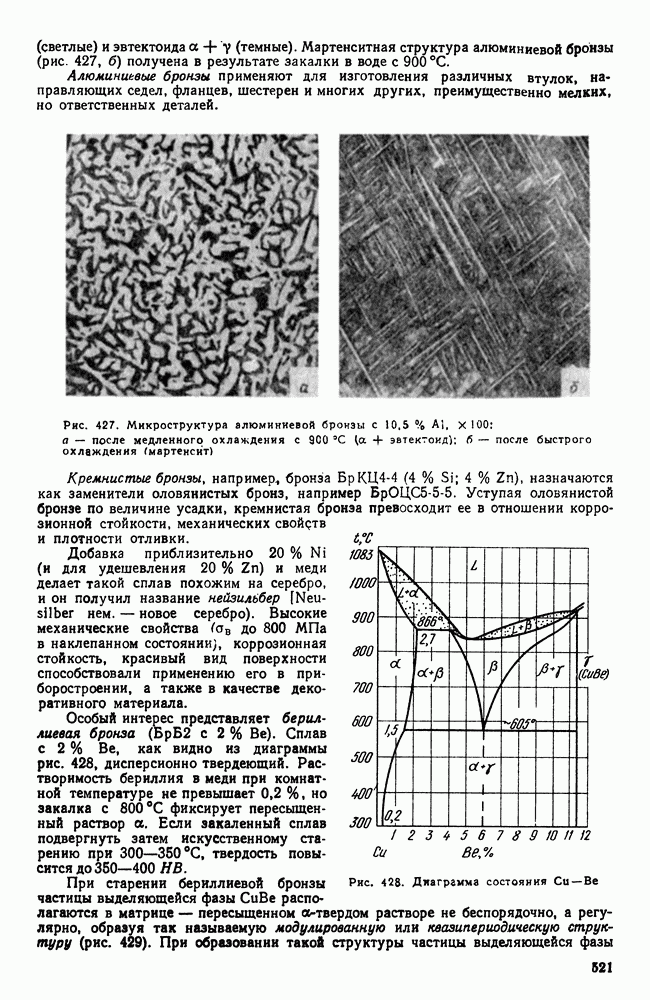
- 4. Сплавы меди с алюминием, кремнием, бериллием и другими элементами
- ГЛАВА XXVIII. ПОДШИПНИКОВЫЕ СПЛАВЫ И ПРИПОИ
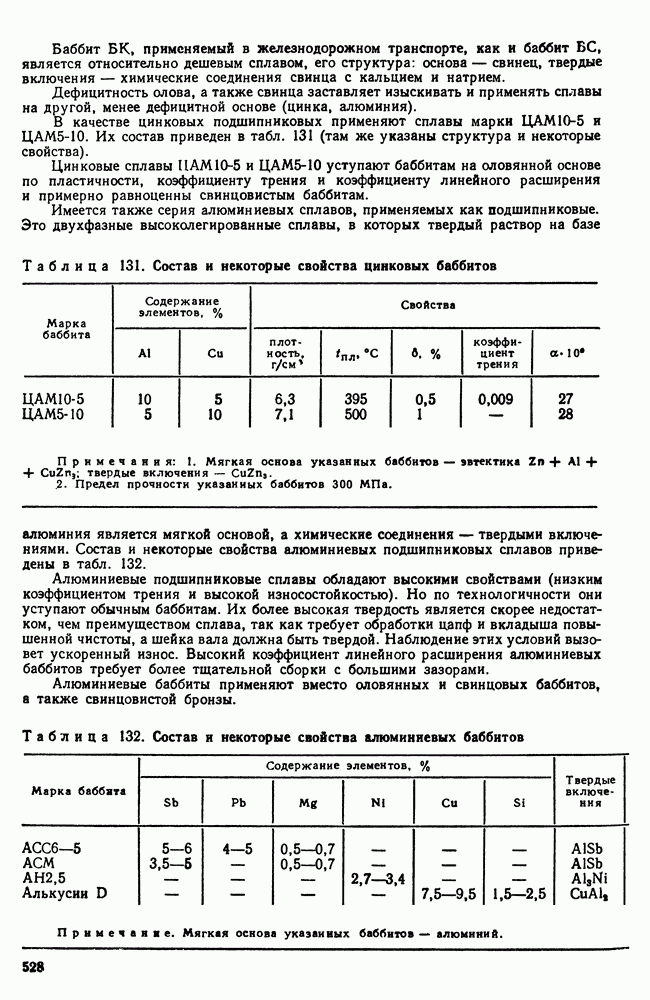
- 2. Легкоплавкие подшипниковые сплавы (баббиты)
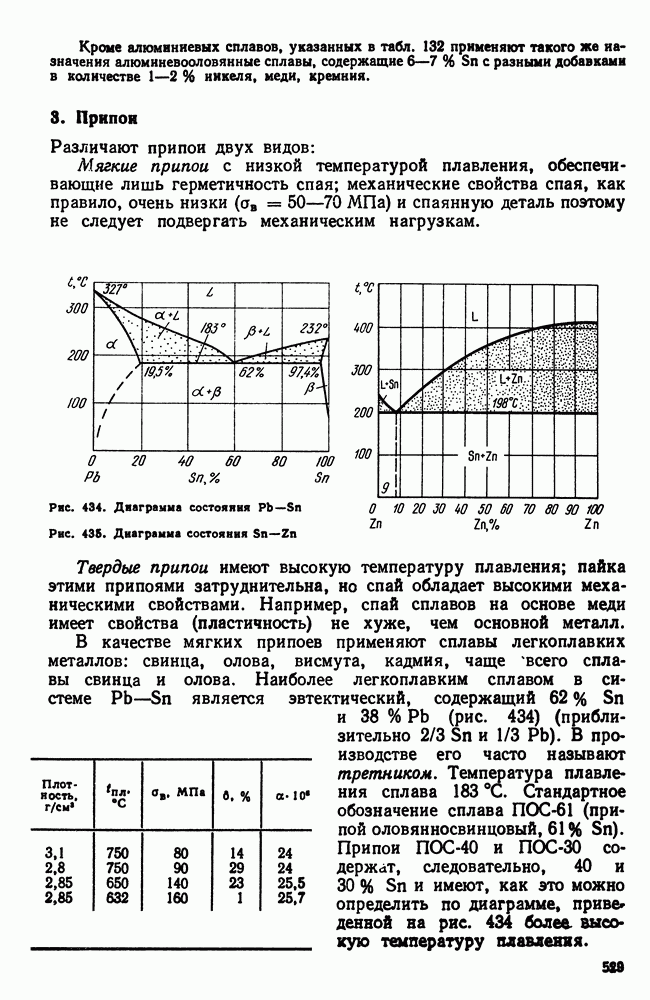
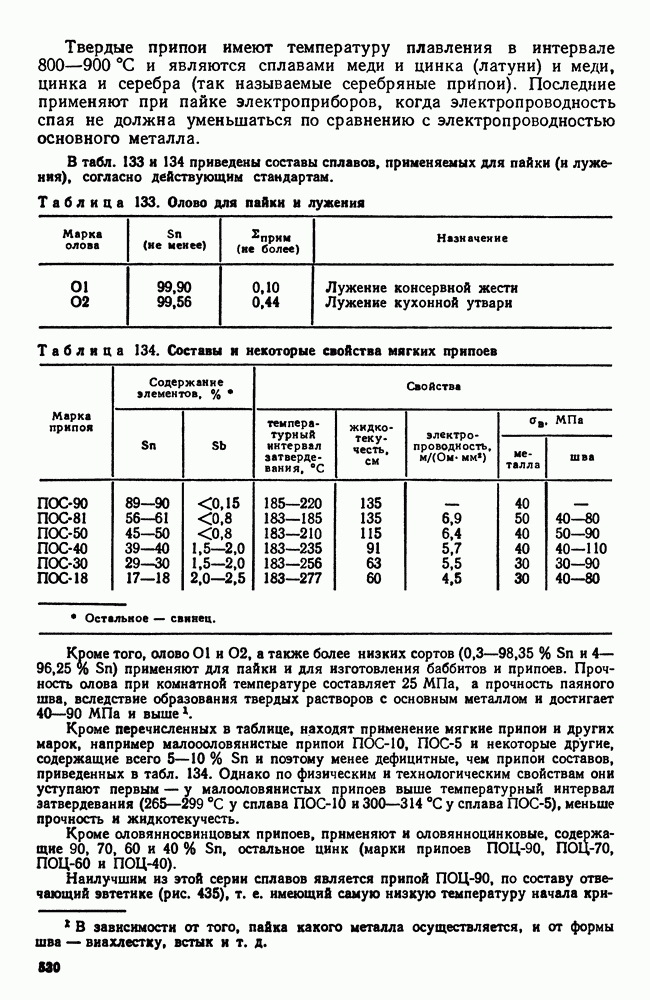
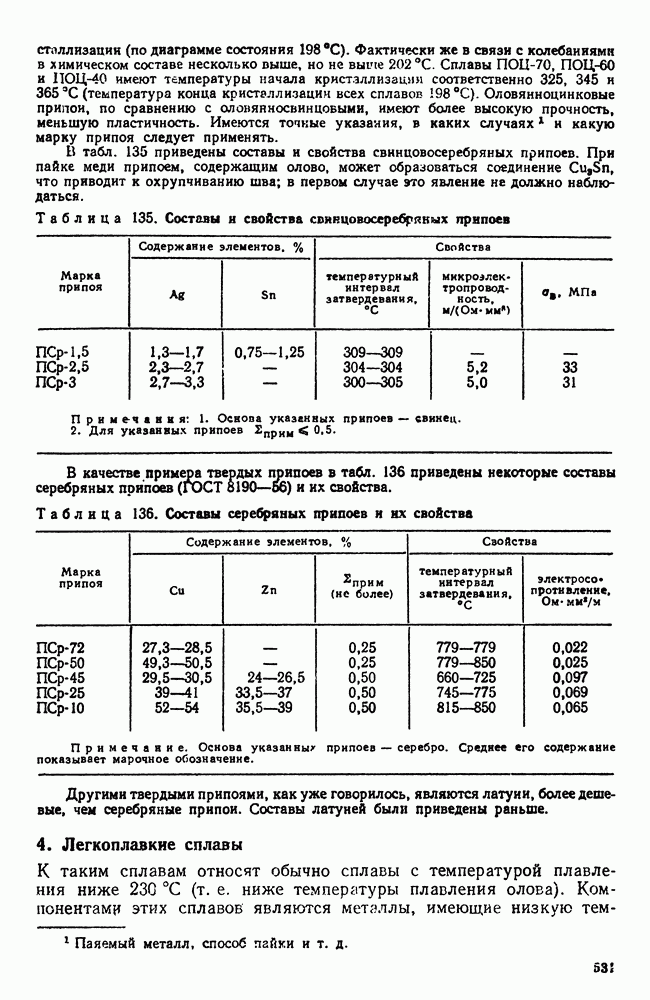
- 3. Припои
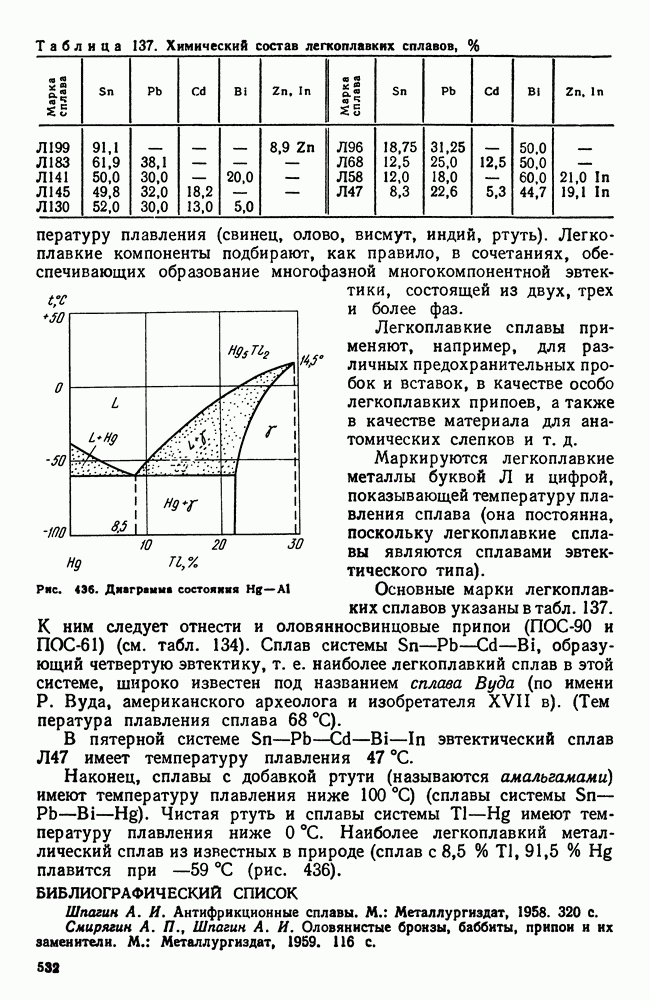
- 4. Легкоплавкие сплавы
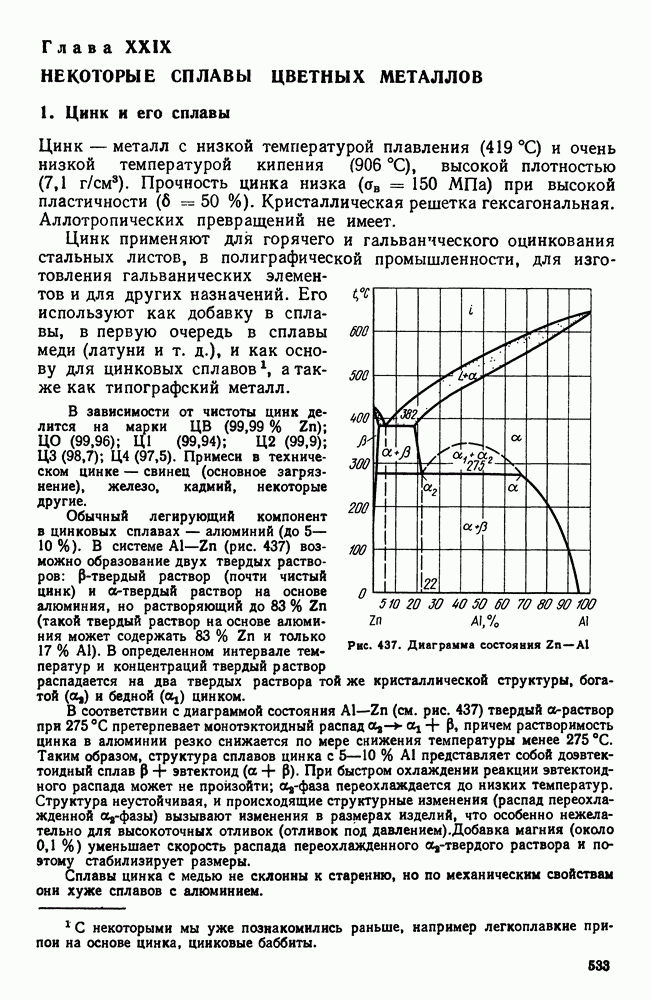
- Глава XXIX. НЕКОТОРЫЕ СПЛАВЫ ЦВЕТНЫХ МЕТАЛЛОВ
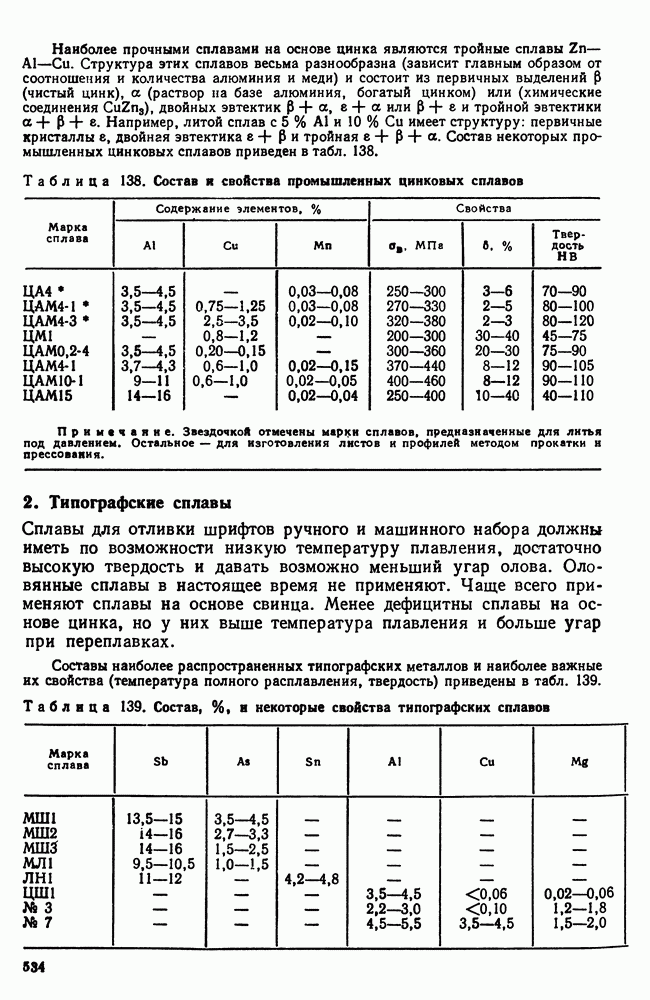
- 2. Типографские сплавы
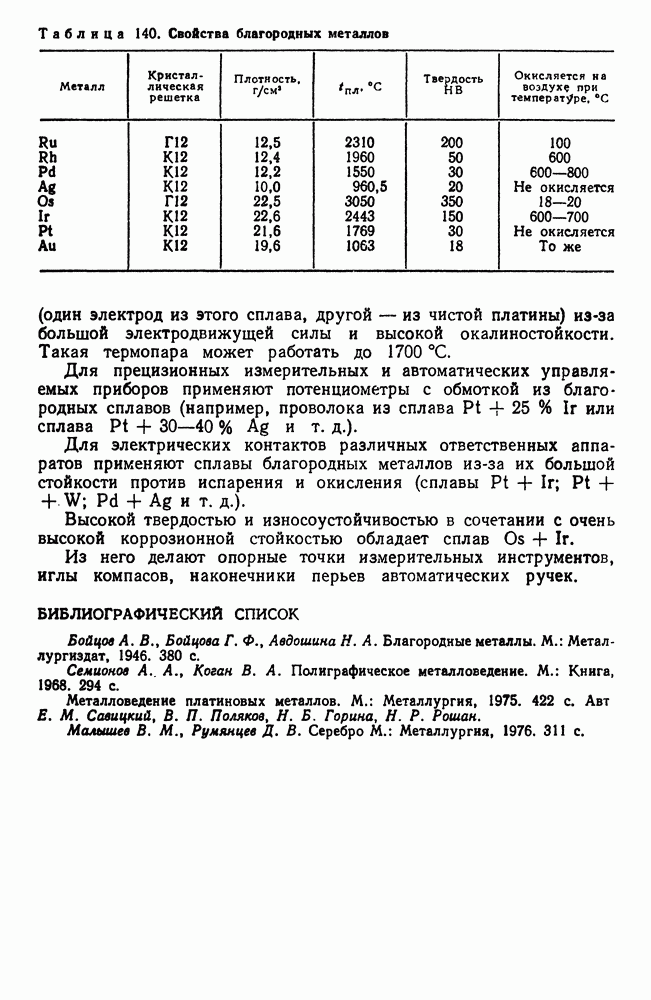
- 3. Благородные металлы